WO2012060185A1 - エステルの製法 - Google Patents
エステルの製法 Download PDFInfo
- Publication number
- WO2012060185A1 WO2012060185A1 PCT/JP2011/073340 JP2011073340W WO2012060185A1 WO 2012060185 A1 WO2012060185 A1 WO 2012060185A1 JP 2011073340 W JP2011073340 W JP 2011073340W WO 2012060185 A1 WO2012060185 A1 WO 2012060185A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- reaction
- nmr
- mhz
- cdcl
- catalyst
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D313/00—Heterocyclic compounds containing rings of more than six members having one oxygen atom as the only ring hetero atom
- C07D313/02—Seven-membered rings
- C07D313/04—Seven-membered rings not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B33/00—Oxidation in general
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/50—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by reactions decreasing the number of carbon atoms
- C07C37/56—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring by reactions decreasing the number of carbon atoms by replacing a carboxyl or aldehyde group by a hydroxy group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/39—Preparation of carboxylic acid esters by oxidation of groups which are precursors for the acid moiety of the ester
- C07C67/42—Preparation of carboxylic acid esters by oxidation of groups which are precursors for the acid moiety of the ester by oxidation of secondary alcohols or ketones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/26—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D307/30—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D307/32—Oxygen atoms
- C07D307/33—Oxygen atoms in position 2, the oxygen atom being in its keto or unsubstituted enol form
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
- C07D307/79—Benzo [b] furans; Hydrogenated benzo [b] furans with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
- C07D307/82—Benzo [b] furans; Hydrogenated benzo [b] furans with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to carbon atoms of the hetero ring
- C07D307/83—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/87—Benzo [c] furans; Hydrogenated benzo [c] furans
- C07D307/88—Benzo [c] furans; Hydrogenated benzo [c] furans with one oxygen atom directly attached in position 1 or 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/93—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems condensed with a ring other than six-membered
- C07D307/935—Not further condensed cyclopenta [b] furans or hydrogenated cyclopenta [b] furans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/16—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D309/28—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D309/30—Oxygen atoms, e.g. delta-lactones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D323/00—Heterocyclic compounds containing more than two oxygen atoms as the only ring hetero atoms
- C07D323/04—Six-membered rings
Abstract
Description
以下の実施例及び比較例で触媒として使用したボレート塩について説明する。NaB(3,5-CF3C6H3)4,LiB(C6F5)4とPh3CB(C6F5)4は市販品をそのまま反応に用いた。LiB(3,5-CF3C6H3)4とKB(3,5-CF3C6H3)4は文献(Organomet., 1992, vol.11, p3920)に記載された方法に従って合成した。
白色粉末。1H NMR (CD3CN, 400 MHz)δ 7.65-7.70 (m, 12H); 13C NMR (CD3CN, 100 MHz) δ118.7, 125.5 (q, JC-F = 270 Hz), 129.9 (q, JC-F = 31.5 Hz), 135.7, 162.6 (q, JB-C = 49.6 Hz); 19F NMR (CD3CN) δ-63.1. Anal. Calcd. for C32H20BF24LiO4: C, 40.79; H, 2.14. Found: C, 41.00; H, 1.88.
白色粉末。 1H NMR (CD3CN, 400 MHz)δ 7.65-7.70 (m, 12H); 13C NMR (CD3CN, 100 MHz) δ118.7, 125.5 (q, JC-F = 271 Hz), 130.0 (q, JC-F = 32.4 Hz), 135.7, 162.7 (q, JB-C = 49.6 Hz); 19F NMR (CD3CN) δ-63.1. Anal. Calcd. for C32H16BF24LiO2: C, 40.96; H, 1.72. Found: C, 41.01; H, 1.70.
白色粉末。 1H NMR (CD3CN, 400 MHz)δ7.65-7.70 (m, 24H); 13C NMR (CD3CN, 100 MHz) δ118.7, 125.5 (q, JC-F = 271 Hz), 129.9 (q, JC-F = 31.5 Hz), 135.7, 162.7 (q, JB-C = 49.6 Hz); 19F NMR (CD3CN) δ-63.1. Anal. Calcd. For C64H44BF48O10Sr: C, 38.55; H, 2.22. Found: C, 38.56; H, 2.13.
白色粉末。1H NMR (CD3CN, 400 MHz)δ7.65-7.70 (m, 24H); 13C NMR (CD3CN, 100 MHz) δ118.6, 125.4 (q, JC-F = 271 Hz), 129.9 (q, JC-F = 31.5 Hz), 135.6, 162.6 (q, JB-C = 48.6 Hz); 19F NMR (CD3CN) δ-63.1. Anal. Calcd. for C64H40BCaF48O8: C,40.23; H, 2.11. Found: C, 40.23; H, 2.30.
淡茶色粉末。1H NMR (CD3CN, 400 MHz)δ77.65-7.70 (m, 24H); 19F NMR (CD3CN) δ-63.1. Anal. Calcd. For C64H38BBaF24O7: C, 38.63; H, 1.92. Found: C, 38.65; H, 2.08.
白色粉末。 19F NMR (CD3CN) δ-168.3, -163.8 (t, J = 24.6 Hz), -133.7.
表1に示すように、実施例1~11では、各種のボレート塩を触媒とし、バイヤー・ビリガー酸化反応により過酸化水素を用いて市販のシクロヘキサノンからε-カプロラクトンを製造した。比較例1,2では、それぞれTsOH及びSc(OTf)3を触媒とし、同様にしてε-カプロラクトンを製造した。各実施例、各比較例で用いた触媒及び反応条件の詳細は表1に示したとおりである。また、この反応では、ε-カプロラクトンのほか、このラクトンが加水分解したヒドロキシカルボン酸やバイヤー・ビリガー酸化反応の反応中間体であるCriegee中間体(表1の欄外の※4参照)が二量化したスピロビスペルオキシドが生成した。表1には、シクロヘキサノンから反応生成物への転換率及び各反応生成物の収率を示した。なお、表1のシクロヘキサノンの転換率や各生成物の収率は、反応溶液から少量をサンプリングし、1H NMR解析により算出した。
無色液体。 TLC, Rf = 0.11 (hexane-EtOAc = 4:1); 1H NMR (CDCl3, 400 MHz) δ1.76-1.87 (m, 6H), 2.63-2.66 (m, 2H), 4.23-4.26 (m, 2H).
無色固体。1H NMR (CDCl3, 400 MHz) δ1.41 (m, 2H), 1.63 (m, 4H), 2.36 (t, J= 7.4 Hz, 2H), 3.65 (t, J= 6.5 Hz, 2H); 13C NMR (CDCl3, 100 MHz) δ24.4, 25.1, 31.9,33.9, 62.3, 178.8.
白色固体。TLC, Rf = 0.67 (hexane-EtOAc = 4:1); 1H NMR (CDCl3, 400 MHz) δ1.47 (bs, 4H), 1.57 (bs, 12H), 2.28 (bs, 4H).
表2に示すように、実施例12~23では、各種のボレート塩を触媒とし、バイヤー・ビリガー酸化反応により過酸化水素を用いて市販の4-tert-ブチルシクロヘキサノンから対応するε-カプロラクトンを製造した。比較例3では無触媒、比較例4~6ではそれぞれNaBF4、NaBPh4、LiNTf2を触媒とし、同様のε-カプロラクトンを製造した。各実施例、各比較例では、表2に示した触媒及び反応条件を採用し、上述した実施例4に準じて反応を行った。また、この反応では、ε-カプロラクトンのほか、スピロビスペルオキシドが生成した。表2には、シクロヘキサノンから反応生成物への転換率及び各反応生成物の収率を示した。なお、表2の転換率や各生成物の収率は、反応溶液から少量をサンプリングし、1H NMR解析により算出した。
無色固体。TLC, Rf = 0.35 (hexane-EtOAc = 4:1); 1H NMR (CDCl3, 400 MHz) δ 0.89(s, 9H), 1.25-1.40 (m 2H), 1.48-1.55 (m, 1H), 2.0-2.1 (m, 2H), 2.53-2.59 (m, 1H), 2.69-2.74 (m, 1H), 4.11-4.18 (m, 1H), 4.34 (ddd, J = 1.9, 5.9, 12.8 Hz, 1H); 13C NMR (CDCl3, 100 MHz) δ23.6, 27.3, 30.1, 32.3, 33.3, 50.6, 69.0, 177.8.
白色固体。TLC, Rf = 0.75 (hexane-EtOAc = 4:1); 1H NMR (CDCl3, 400 MHz) δ 0.86(bs, 18H), 1.05-1.12 (m, 2H), 1.20-1.32 (m, 4H), 1.41-1.51 (m, 4H), 1.74 (bs, 6H), 3.17 (bs, 2H); 13C NMR (CDCl3, 100 MHz) δ 22.8, 23.1, 27.6, 29.7, 32.0, 32.3, 47.4, 47.5, 108.1.
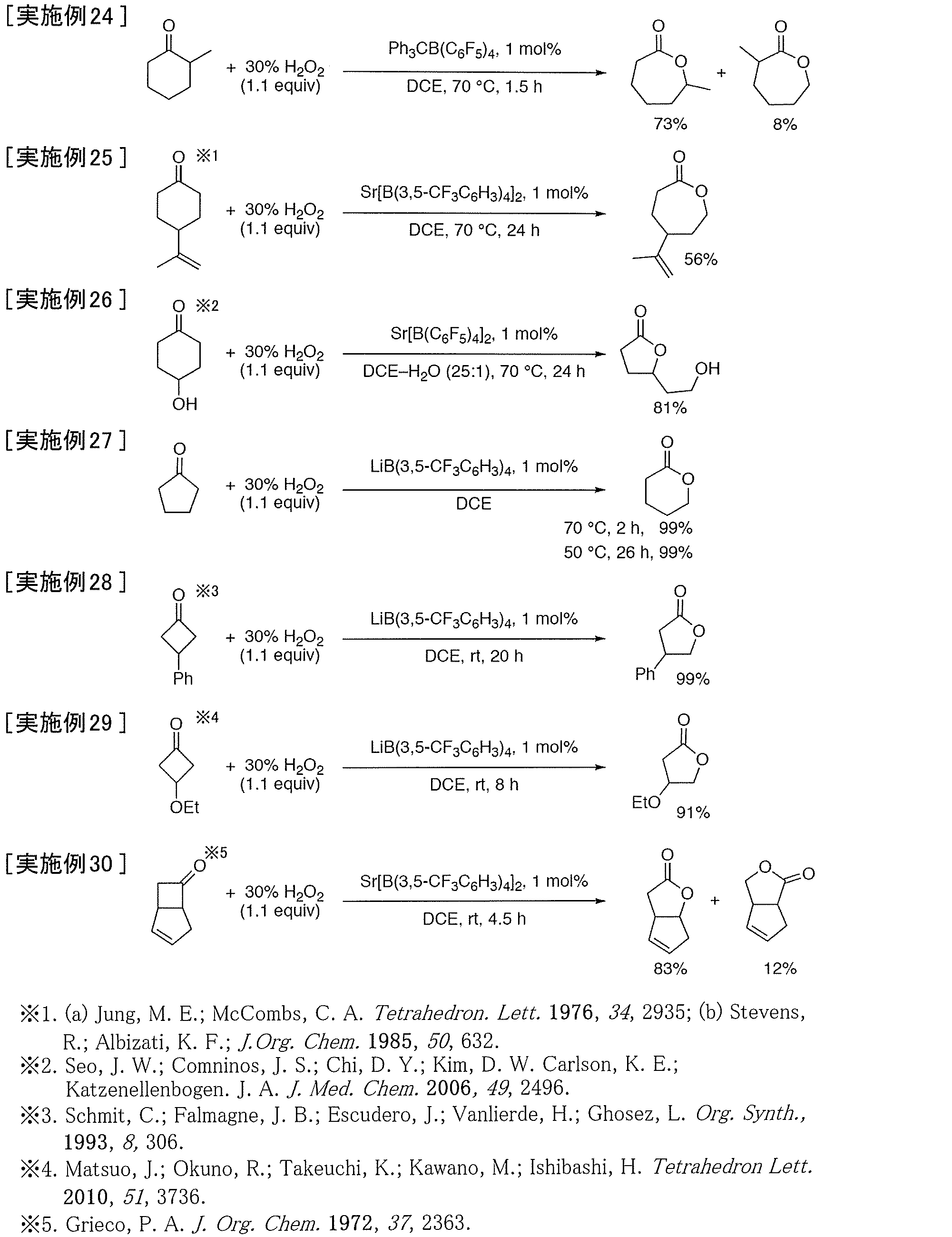
実施例24~30では、化1に示すように、バイヤー・ビリガー酸化反応により過酸化水素を用いて種々の環状ケトンからラクトンを合成した。実施例24では、非対称の環状ケトンである2-メチルシクロヘキサノンを用いたところ、高収率で対応するε-カプロラクトンが通常の位置選択性でもって得られた。実施例25では、オレフィン結合を持つ置換基を有する環状ケトンである4-イソプロペニルシクロヘキサノンを用いたところ、対応するε-カプロラクトンが収率56%で得られ、オレフィンのエポキシ化は見られなかった。実施例26では、4-ヒドロキシシクロヘキサノンを用いたところ、ヒドロキシエチル基を有する5員環ラクトンが得られた。このラクトンは、一旦、対応するε-カプロラクトンが生成したあと、環の歪みの少ない5員環に巻き直したものと考えられる。実施例27~29では、5員環ケトンや4員環ケトンを用いたところ、対応する6員環ラクトンや5員環ラクトンが高収率で得られた。実施例30では、環内にオレフィン結合を有する縮合環ケトンを用いたところ、対応する縮合環ラクトンが通常の位置選択性でもって高収率で得られ、オレフィンのエポキシ化は見られなかった。
表3に示すように、実施例31では、ボレート塩触媒のみを用いてバイヤー・ビリガー酸化反応によりシクロペンタノンからδ-バレロラクトンを合成した。また、実施例32~56では、ボレート塩触媒とブレンステッド酸助触媒とを用いてバイヤー・ビリガー酸化反応によりシクロペンタノンからδ-バレロラクトンを合成した。実施例で使用した助触媒の構造式を表4に示す。
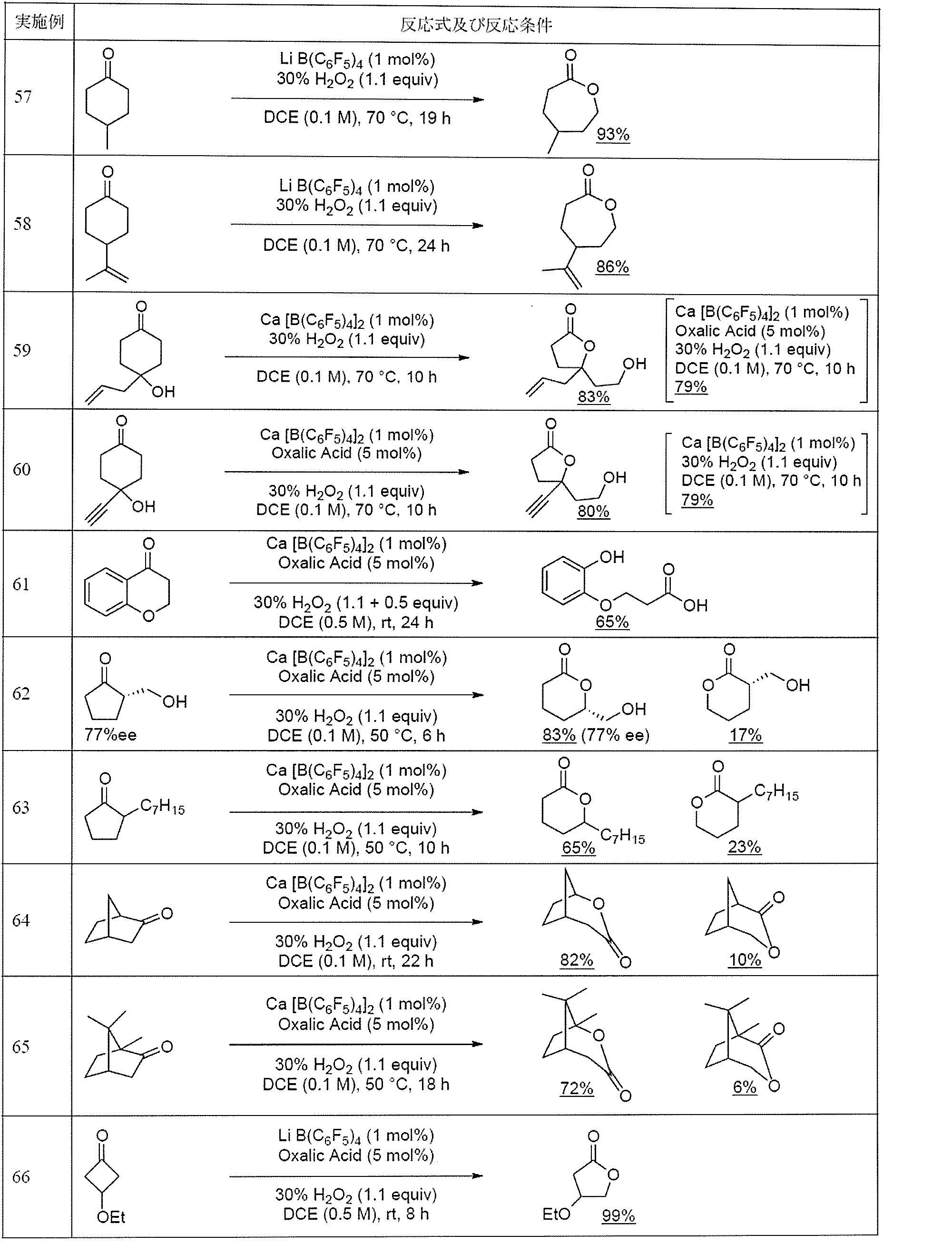
表5及び表6に示すように、様々な反応基質のバイヤービリガー酸化反応を検討した。触媒としては、Li又はCaのボレート塩を用いた。一般的に、触媒活性はCaのボレート塩の方が高いが、Liのボレート塩は市販品であり、分子量が小さいため絶対的な使用量が少ないことから、まずLiのボレート塩を使用した(実施例57,58,66-71,73)。しかし、反応基質によってはLiのボレート塩では不十分で、生成物の化学収率が低い場合には、Caのボレート塩を触媒として用いた(実施例59-65,72,74-76)。
Claims (9)
- バイヤー・ビリガー酸化反応により過酸化水素を用いて反応基質であるケトン又はアルデヒドからエステルを製造する方法であって、
触媒として、ボレート塩であるM(BAr4)n(Mはアルカリ金属、アルカリ土類金属又はトリアリールメチルであり、4つのArは電子吸引性基を有するアリールであって4つとも同じであっても異なっていてもよく、nはMの価数と同じ数である)を用いる、
エステルの製法。 - 前記ボレート塩のArは、ペンタフルオロフェニル又は3,5-ビストリフルオロメチルフェニルである、
請求項1に記載のエステルの製法。 - 前記触媒は、前記反応基質に対して0.1~5mol%使用する、
請求項1又は2に記載のエステルの製法。 - 前記反応基質は、炭素-炭素二重結合、炭素-炭素三重結合、ハロゲン基、ヒドロキシル基、シリル基又はシロキシ基を有している、
請求項1~3のいずれか1項に記載のエステルの製法。 - 前記反応基質は、環状ケトン、鎖状ケトン、クロマノン類又は芳香族アルデヒド類である、
請求項1~4のいずれか1項に記載のエステルの製法。 - 助触媒として、ブレンステッド酸を用いる、
請求項1~5のいずれか1項に記載のエステルの製法。 - 前記助触媒は、芳香環上に1以上のOH基を持つフェノール類、カルボン酸、オキソカーボン酸、リン酸モノエステル又はリン酸ジエステルである、
請求項6に記載のエステルの製法。 - 前記助触媒は、テトラフルオロカテコール又はシュウ酸である、
請求項6又は7に記載のエステルの製法。 - 前記助触媒は、前記触媒に対して1~5倍モル使用する、
請求項6~8のいずれか1項に記載のエステルの製法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11837836.3A EP2636665B1 (en) | 2010-11-02 | 2011-10-11 | Method for producing ester |
| JP2012541793A JP5920889B2 (ja) | 2010-11-02 | 2011-10-11 | エステルの製法 |
| US13/881,544 US8853426B2 (en) | 2010-11-02 | 2011-10-11 | Method for manufacturing ester |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010245944 | 2010-11-02 | ||
| JP2010-245944 | 2010-11-02 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012060185A1 true WO2012060185A1 (ja) | 2012-05-10 |
Family
ID=46024304
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/073340 WO2012060185A1 (ja) | 2010-11-02 | 2011-10-11 | エステルの製法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8853426B2 (ja) |
| EP (1) | EP2636665B1 (ja) |
| JP (1) | JP5920889B2 (ja) |
| WO (1) | WO2012060185A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102942548A (zh) * | 2012-11-20 | 2013-02-27 | 南京理工大学 | 一种δ-十二内酯的合成方法 |
| WO2015074162A1 (es) | 2013-11-22 | 2015-05-28 | Pontificia Universidad Catolica De Chile | Variantes de enzima fenilacetona monooxigenasa (pamo) capaces de catalizar conversión de ciclohexanona a caprolactona. |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11208394B2 (en) * | 2018-09-17 | 2021-12-28 | Regents Of The University Of Minnesota | Chemical process to manufacture branched-caprolactone |
| JP7336541B2 (ja) | 2019-06-12 | 2023-08-31 | ヌーリオン ケミカルズ インターナショナル ベスローテン フェノーツハップ | 過酸化ジアシルを生成するためのプロセス |
| BR112021024870A2 (pt) * | 2019-06-12 | 2022-01-18 | Nouryon Chemicals Int Bv | Método para isolar ácido carboxílico de uma corrente lateral aquosa de um processo de produção de peróxido orgânico |
| US11976034B2 (en) | 2019-06-12 | 2024-05-07 | Nouryon Chemicals International B.V. | Process for the production of diacyl peroxides |
| CN110452212B (zh) * | 2019-07-30 | 2020-08-14 | 浙江大学 | 一种11-十一内酯类化合物和己内酯类化合物的制备方法 |
| CN115057998B (zh) * | 2022-07-07 | 2023-07-25 | 武汉理工大学 | 一种联合生产ε-己内酯与聚丁二酸丁二醇酯的方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09104681A (ja) * | 1995-10-06 | 1997-04-22 | Nippon Peroxide Co Ltd | δ−ラクトン化合物の製造方法 |
| JP2003190804A (ja) | 2001-12-25 | 2003-07-08 | Asahi Kasei Corp | ケトン化合物の酸化触媒 |
| JP2004352636A (ja) * | 2003-05-28 | 2004-12-16 | Takasago Internatl Corp | ラクトン類又はエステル類の製造方法 |
| JP2010245944A (ja) | 2009-04-08 | 2010-10-28 | Mitsubishi Electric Corp | 高周波増幅器 |
-
2011
- 2011-10-11 US US13/881,544 patent/US8853426B2/en not_active Expired - Fee Related
- 2011-10-11 JP JP2012541793A patent/JP5920889B2/ja not_active Expired - Fee Related
- 2011-10-11 EP EP11837836.3A patent/EP2636665B1/en not_active Not-in-force
- 2011-10-11 WO PCT/JP2011/073340 patent/WO2012060185A1/ja active Application Filing
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09104681A (ja) * | 1995-10-06 | 1997-04-22 | Nippon Peroxide Co Ltd | δ−ラクトン化合物の製造方法 |
| JP2003190804A (ja) | 2001-12-25 | 2003-07-08 | Asahi Kasei Corp | ケトン化合物の酸化触媒 |
| JP2004352636A (ja) * | 2003-05-28 | 2004-12-16 | Takasago Internatl Corp | ラクトン類又はエステル類の製造方法 |
| JP2010245944A (ja) | 2009-04-08 | 2010-10-28 | Mitsubishi Electric Corp | 高周波増幅器 |
Non-Patent Citations (19)
| Title |
|---|
| ANGEW. CHEM. INT. ED., vol. 41, 2002, pages 4481 |
| APP. CATAL.B: ENVIRON., vol. 72, 2007, pages 18 |
| CATAL. LETT., vol. 131, 2009, pages 618 |
| DAISUKE NAKAJIMA ET AL.: "Alcali-Alcali Dorui Kinzoku no Kasadakai Borate-en Shokubai to Kasanka Suiso ni yoru Baeyer-Villiger Sanka Hanno", 91ST ANNUAL MEETING OF THE CHEMICAL SOCIETY OF JAPAN, 11 March 2011 (2011-03-11), KOEN YOKOSHU, pages 1221, XP008168374 * |
| DAISUKE NAKAJIMA ET AL.: "Kasanka Suisosui o Sankazai ni Mochiiru Kankyo Chowagata Shokubaiteki Baeyer-Villiger Sanka Hanno", DAI 41 KAI ANNUAL MEETING OF UNION OF CHEMISTRY- RELATED SOCIETIES IN CHUBU AREA, 6 November 2010 (2010-11-06), JAPAN KOEN, pages 199, XP008169387 * |
| FUJIKI K. ET AL.: "Evaluation of Lewis Acidity of "Naked" Lithium Ion through Diels-Alder Reaction Catalyzed by Lithium TFPB in Nonpolar Organic Solvents", CHEMISTRY LETTERS, vol. 29, 2000, pages 62 - 63, XP009097713 * |
| GREEN CHEM., vol. 5, 2003, pages 524 |
| HUDRLIK ET AL., J. AM. CHEM. SOC., vol. 102, 1980, pages 6894 |
| J. MOL. CATAL. A:CHEM., vol. 191, 2003, pages 93 |
| J. ORG. CHEM., vol. 66, 2001, pages 2429 |
| KOTSUKI ET AL., ORG. LETT., vol. 12, 2010, pages 1616 |
| LIAO B.-S. ET AL.: "An Efficient Preparation of Bis(indole)methanes Catalyzed by Tetrakis [3,5-bis(trifluoromethyl)phenyl]borate Salts in Aqueous Medium", SYNTHESIS, no. 20, 2007, pages 3125 - 3128, XP055085511 * |
| NEIMANN K. ET AL.: "Electrophilic Activation of Hydrogen Peroxide: Selective Oxidation Reactions in Perfluorinated Alcohol Solvents", ORGANIC LETTERS, vol. 2, no. 18, 2000, pages 2861 - 2863, XP008116670 * |
| ORGANIC LETTERS, vol. 2, 2000, pages 2861 |
| ORGANOMET., vol. 11, 1992, pages 3920 |
| See also references of EP2636665A4 |
| TETRAHEDRON LETTERS, vol. 42, 2001, pages 2293 |
| TETRAHEDRON LETTERS, vol. 46, 2005, pages 8665 |
| TETRAHEDRON, vol. 63, 2007, pages 1435 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102942548A (zh) * | 2012-11-20 | 2013-02-27 | 南京理工大学 | 一种δ-十二内酯的合成方法 |
| CN102942548B (zh) * | 2012-11-20 | 2015-04-22 | 南京理工大学 | 一种δ-十二内酯的合成方法 |
| WO2015074162A1 (es) | 2013-11-22 | 2015-05-28 | Pontificia Universidad Catolica De Chile | Variantes de enzima fenilacetona monooxigenasa (pamo) capaces de catalizar conversión de ciclohexanona a caprolactona. |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130217898A1 (en) | 2013-08-22 |
| EP2636665B1 (en) | 2016-06-22 |
| JPWO2012060185A1 (ja) | 2014-05-12 |
| US8853426B2 (en) | 2014-10-07 |
| JP5920889B2 (ja) | 2016-05-18 |
| EP2636665A1 (en) | 2013-09-11 |
| EP2636665A4 (en) | 2014-04-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5920889B2 (ja) | エステルの製法 | |
| Ohrai et al. | Effects of solvents and additives in the asymmetric Heck reaction of alkenyl triflates: catalytic asymmetric synthesis of decalin derivatives and determination of the absolute stereochemistry of (+)-vernolepin | |
| Oare et al. | Stereochemistry of the Base‐Promoted Michael Addition Reaction | |
| Hiratake et al. | Irreversible and highly enantioselective acylation of 2-halo-1-arylethanols in organic solvents catalyzed by a lipase from Pseudomonas fluorescens | |
| Caron et al. | An optimized sequential kinetic resolution of trans-1, 2-cyclohexanediol | |
| Thummel et al. | Base-induced rearrangement of epoxides. V. Phenyl-substituted epoxides | |
| Chenal et al. | Carbon monoxide as a building block in organic synthesis: Part II. One-step synthesis of esters by alkoxycarbonylation of naturally occurring allylbenzenes, propenylbenzenes and monoterpenes | |
| JP3251525B2 (ja) | 3−オキソカルボン酸エステルの製造方法 | |
| CN109956850B (zh) | 3,7-二甲基-7-辛烯醇和3,7-二甲基-7-辛烯基羧酸酯化合物的生产方法 | |
| Simpura et al. | Tandem aldol-transfer–Tischtschenko reaction of aldehydes and β-hydroxyketones catalyzed by trimethylaluminum | |
| CN106946705B (zh) | 一种合成(1r,2s)-二氢茉莉酮酸甲酯的方法 | |
| Yadav et al. | InBr3-catalyzed stereoselective synthesis of trans-2, 6-disubstituted 3, 6-dihydro-2H-pyrans | |
| EP0676404A2 (en) | Oxotitanium complexes useful as asymmetric reaction catalysts particularly for producing beta-hydroxy ketones or alpha-hydroxy carboxylic acid esters | |
| Lattanzi et al. | Synthesis of a renewable hydroperoxide from (+)-norcamphor: influence of steric modifications of the bicyclic framework on asymmetric sulfoxidation | |
| EP2948245B1 (en) | Process for the preparation of 4-methylpent-3-en-1-ol derivatives | |
| US3202704A (en) | Ech=che | |
| Yadav et al. | Indium (III) chloride catalyzed allylation of gem-diacetates: a facile synthesis of homoallyl acetates | |
| JP3626520B2 (ja) | 3−置換−3−メチルブタナールの製造方法 | |
| JP2838656B2 (ja) | ヒノキチオール及びその中間生成物の製造方法 | |
| RU2565059C1 (ru) | Способ получения амидов карбоновых кислот | |
| CN114292163B (zh) | 一种香茅醛制备异胡薄荷醇的方法 | |
| Guo | Mild Electrocyclization of Heptatrienyl Anions | |
| Soorukram et al. | Reactions of the vicinal dianion of di-(-)-menthyl succinate with carbonyl compounds and benzyl bromide | |
| SU615056A1 (ru) | Способ получени 1,5-диметилциклооктадиена-1,5 | |
| CN108484554B (zh) | 一种抗锥虫、抗癌天然产物Cryptofolione的合成方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11837836 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2012541793 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13881544 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011837836 Country of ref document: EP |