WO2012008301A1 - siRNA導入による新規hiPSC作製法 - Google Patents
siRNA導入による新規hiPSC作製法 Download PDFInfo
- Publication number
- WO2012008301A1 WO2012008301A1 PCT/JP2011/064846 JP2011064846W WO2012008301A1 WO 2012008301 A1 WO2012008301 A1 WO 2012008301A1 JP 2011064846 W JP2011064846 W JP 2011064846W WO 2012008301 A1 WO2012008301 A1 WO 2012008301A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- base sequence
- stranded
- seq
- pluripotent stem
- polynucleotide
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7105—Natural ribonucleic acids, i.e. containing only riboses attached to adenine, guanine, cytosine or uracil and having 3'-5' phosphodiester links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/713—Double-stranded nucleic acids or oligonucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
- C07H21/02—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids with ribosyl as saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/111—General methods applicable to biologically active non-coding nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0696—Artificially induced pluripotent stem cells, e.g. iPS
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/65—MicroRNA
Definitions
- the present invention relates to a novel small RNA, a pluripotent stem cell inducer, a malignant tumor therapeutic agent, or a pluripotent stem cell.
- Patent Document 1 describes that iPS cells were prepared by introducing four genes (Oct3 / 4, Klf4, Sox2, c-Myc) into cells. Since the development of this technology, the number of reports on research results related to iPS cells has been increasing rapidly.
- Patent Document 2 describes that iPS cells were created by introducing three genes (Oct3 / 4, Klf4, Sox2) and one miRNA (hsa-miR-372 etc.) into the cells. Yes.
- Non-Patent Document 1 describes that the iPS cell production efficiency is increased by deleting the p53 gene of the cells to be iPS-converted when the above four or three genes are introduced.
- Non-Patent Document 2 describes that iPS cells were prepared from cancer cells by introducing pre-miRNA clusters (miR-302a to miR-302d).
- Non-Patent Document 4 it is reported that the expression of hTERT mRNA is related to RGM249 mRNA, and the expression level of hTERT mRNA is decreased by shRNA or siRNA against RGM249 mRNA.
- Patent Document 1 uses the proto-oncogene c-Myc, and therefore has the risk of iPS cells becoming cancerous.
- Patent Document 2 does not use c-Myc, but the process of introducing three genes and one miRNA into a cell is complicated and cannot be said to be an efficient production method.
- non-patent document 1 does not use c-Myc, the p53 gene, which is a tumor suppressor gene, is deficient, and thus has a risk of canceration or destabilization of cells.
- Non-Patent Document 2 uses a cluster of miR-302, and it is reported that miR-302 is a miRNA targeting the tumor suppressor PTEN (phosphatase and tensin homolog deleted on chromosome 10). (Poliseno et al., Sci Signal. 2010 Apr 13; 3 (117): ra29). For this reason, they have a risk of cancerous cells.
- Non-Patent Documents 3 and 4 describe that hTERT mRNA is associated with cancer formation and that shRNA or siRNA against RGM249 mRNA decreases hTERT mRNA, but what substances have a therapeutic effect on cancer? It has not been revealed.
- the present invention has been made in view of the above circumstances, and an object thereof is to provide a novel compound that induces pluripotent stem cells.
- an object of the present invention is to provide an undifferentiated cell marker expression regulator.
- Another object is to provide a p53 expression promoter for pluripotent stem cells.
- Another object is to provide a novel malignant tumor therapeutic agent.
- Another object is to provide a novel pluripotent stem cell.
- a single-stranded or double-stranded polynucleotide comprising one or more nucleotide sequences of SEQ ID NOs: 1, 2, 3, 8, or 44 to 47 is contained, and the cells are pluripotent stem cells.
- An agent for inducing pluripotent stem cells is provided.
- This pluripotent stem cell inducer contains a single-stranded or double-stranded polynucleotide that has been demonstrated to induce cells into pluripotent stem cells in Examples described later. Therefore, using this pluripotent stem cell inducer, cells can be induced into pluripotent stem cells.
- a pluripotency containing a small RNA comprising one or more base sequences of SEQ ID NOs: 1, 2, 3, 8, or 44 to 47 and inducing cells into pluripotent stem cells.
- a stem cell inducer is provided.
- This pluripotent stem cell inducer contains small RNA that has been demonstrated to induce cells into pluripotent stem cells in Examples described later. Therefore, using this pluripotent stem cell inducer, cells can be induced into pluripotent stem cells.
- a single-stranded or double-stranded polynucleotide comprising a base sequence complementary to an RNA strand obtained by treating the RNA strand comprising the base sequence of SEQ ID NO: 7 with Dicer is obtained.
- a pluripotent stem cell inducer is provided which contains and induces cells into pluripotent stem cells.
- This pluripotent stem cell inducer contains a single-stranded or double-stranded polynucleotide that has been demonstrated to induce cells into pluripotent stem cells in Examples described later. Therefore, using this pluripotent stem cell inducer, cells can be induced into pluripotent stem cells.
- an undifferentiated cell comprising a single-stranded or double-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 1, 2, 3, or 8 and regulating the expression of an undifferentiated cell marker.
- a marker expression modulator is provided.
- This undifferentiated cell marker expression regulator contains a single-stranded or double-stranded polynucleotide which has been demonstrated to promote or suppress intracellular undifferentiated cell markers in Examples described later. Therefore, if this undifferentiated cell marker expression regulator is used, the expression level of the undifferentiated cell marker in a cell can be adjusted.
- the present invention also includes a single-stranded or double-stranded polynucleotide comprising one or more base sequences of SEQ ID NOs: 1, 2, 3, 8, or 44 to 47, and is used in pluripotent stem cells.
- a pluripotent stem cell p53 expression promoter that promotes the expression level of p53 is provided.
- This p53 expression promoting agent contains a single-stranded or double-stranded polynucleotide which has been demonstrated to promote the expression level of p53 in pluripotent stem cells in Examples described later. Therefore, if this p53 expression promoter is used, the expression level of p53 in pluripotent stem cells can be promoted.
- the present invention also provides a method for producing pluripotent stem cells, comprising the step of introducing a single-stranded or double-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 1, 2, or 3 into a cell. Is done.
- the present invention also provides a therapeutic agent for malignant tumors comprising a single-stranded or double-stranded polynucleotide comprising one or more base sequences of SEQ ID NOs: 1, 2, 3, 8, or 44 to 47. Is provided.
- This malignant tumor therapeutic agent contains a single-stranded or double-stranded polynucleotide which has been demonstrated to suppress malignant tumors in Examples described later. Therefore, malignant tumor can be treated by using this therapeutic agent for malignant tumor.
- the present invention also provides siRNA containing a single-stranded or double-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1, 2, or 3.
- this siRNA induces cells to pluripotent stem cells, regulates the expression level of undifferentiated cell markers, promotes the expression level of p53 in pluripotent stem cells, or malignant tumors. Contains single-stranded or double-stranded polynucleotides that have been demonstrated to inhibit. Therefore, using this siRNA, cells can be induced into pluripotent stem cells, the expression level of undifferentiated cell markers can be regulated, the expression level of p53 in pluripotent stem cells can be promoted, or malignant tumors can be treated.
- the present invention also provides a vector comprising a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 1.
- a vector comprising a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 2 is provided.
- a vector comprising a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 3 is provided.
- a vector comprising a polynucleotide comprising a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 8 is provided.
- a vector comprising a polynucleotide comprising a polynucleotide comprising a base sequence complementary to one or more base sequences of SEQ ID NOs: 44 to 47 is provided.
- single-stranded or double-stranded polynucleotides containing one or more base sequences of SEQ ID NOs: 1, 2, 3, 8, or 44 to 47 can be expressed. Therefore, by using these vectors, cells can be induced into pluripotent stem cells, the expression level of undifferentiated cell markers can be regulated, the expression level of p53 in pluripotent stem cells can be promoted, or malignant tumors can be treated. .
- a pluripotent composition comprising a single-stranded or double-stranded polynucleotide having an RNAi action on an RNA strand comprising the base sequence of SEQ ID NO: 7, and inducing cells into pluripotent stem cells.
- Sex stem cell inducers are provided.
- This pluripotent stem cell inducer contains a single-stranded or double-stranded polynucleotide that has been demonstrated to induce cells into pluripotent stem cells in Examples described later. Therefore, using this pluripotent stem cell inducer, cells can be induced into pluripotent stem cells.
- the present invention also provides shRNA containing a single-stranded or double-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 8.
- this shRNA induces cells into pluripotent stem cells, regulates the expression level of undifferentiated cell markers, promotes the expression level of p53 in pluripotent stem cells, or malignant tumors. Contains single-stranded or double-stranded polynucleotides that have been demonstrated to inhibit. Therefore, using this shRNA, cells can be induced into pluripotent stem cells, the expression level of undifferentiated cell markers can be regulated, the expression level of p53 in pluripotent stem cells can be promoted, or malignant tumors can be treated.
- kits for pluripotent stem cell induction for undifferentiated cell marker expression regulation, comprising a polynucleotide comprising one or more base sequences of SEQ ID NOs: 1, 2, 3, 8, or 44 to 47.
- inducing cells into pluripotent stem cells, regulating the expression level of undifferentiated cell markers, promoting the expression level of p53 in pluripotent stem cells Alternatively, single-stranded or double-stranded polynucleotides that have been demonstrated to suppress malignant tumors can be used simply. Therefore, using this kit, cells can be induced into pluripotent stem cells, the expression level of undifferentiated cell markers can be regulated, the expression level of p53 in pluripotent stem cells can be promoted, or malignant tumors can be treated.
- pluripotent stem cell inducer undifferentiated cell marker expression regulator, p53 expression promoter, pluripotent stem cell production method, malignant tumor therapeutic agent, siRNA, vector, shRNA, and kit 1 to 3 bases of one or more base sequences of SEQ ID NOs: 1 to 3, 8, or 44 to 47 may be deleted, substituted or added.
- 1 to 5 bases of SEQ ID NOs: 4 to 6 or 9 may be deleted, substituted or added.
- 1 to 4 bases of the base sequence of SEQ ID NO: 7 may be deleted, substituted or added.
- a pluripotent stem cell derived from a mammalian cell, wherein the expression level of endogenous p53 is increased as compared with the HPS0002: 253G1 strain. Since this pluripotent stem cell has a high expression level of p53, malignant tumor formation is unlikely to occur.
- a novel compound that induces pluripotent stem cells can be obtained.
- novel compounds that modulate the expression of undifferentiated cell markers are obtained.
- a p53 expression promoter for pluripotent stem cells is obtained.
- a novel malignant tumor therapeutic agent can be obtained.
- novel pluripotent stem cells can be obtained.
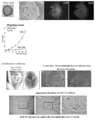
- FIG. 1A is a diagram showing a secondary structure of RGM249.
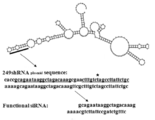
- FIG. 1B is a diagram showing the two-dimensional structure of RGM249 shRNA and RGM249m-1 shRNA.
- FIG. 1C shows the results of investigating changes in tumor volume after subcutaneous injection of RGM24924shRNA.
- FIG. 1D is a result of visual observation of tumor volume when RGM249 shRNA plasmid or the like is injected subcutaneously.
- FIG. 2A shows the results of investigating the expression suppression effect of a gene expressed in a tumor 35 days after subcutaneous injection of RGM249GshRNA plasmid or the like.
- FIG. 3A is a result showing a site corresponding to RGM249 mRNA and three internal miRNAs.
- FIG. 3B is a diagram showing the secondary structure of three miRNAs.
- FIG. 3C shows the result of comparing the sequences of three miRNAs and the antisense strands of three siRNAs.
- FIG. 3D shows the results of investigating the cancer cell growth-inhibiting effect after transfection of three siRNAs into HMV-I.
- FIG. 3A is a result showing a site corresponding to RGM249 mRNA and three internal miRNAs.
- FIG. 3B is a diagram showing the secondary structure of three miRNAs.
- FIG. 3C shows the result of comparing the sequences of three miRNAs and the antisense strands of three siRNAs.
- FIG. 3D shows the results of investigating the cancer cell growth-inhibiting effect after transfection of three siRNAs into HMV-I.
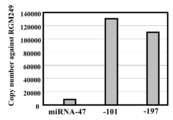
- FIG. 3E shows the results of investigating the expression levels of miR-47, miR-101, and miR-197 by extracting RNA from HMV-I co-transfected with 3 siRNA mixture.
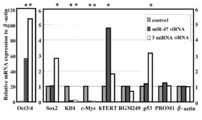
- FIG. 3F shows the results of evaluating transcriptional expression profiling of transformants using a 3 siRNA mixture for genes related to cancer, pluripotency, and stem cell nature.
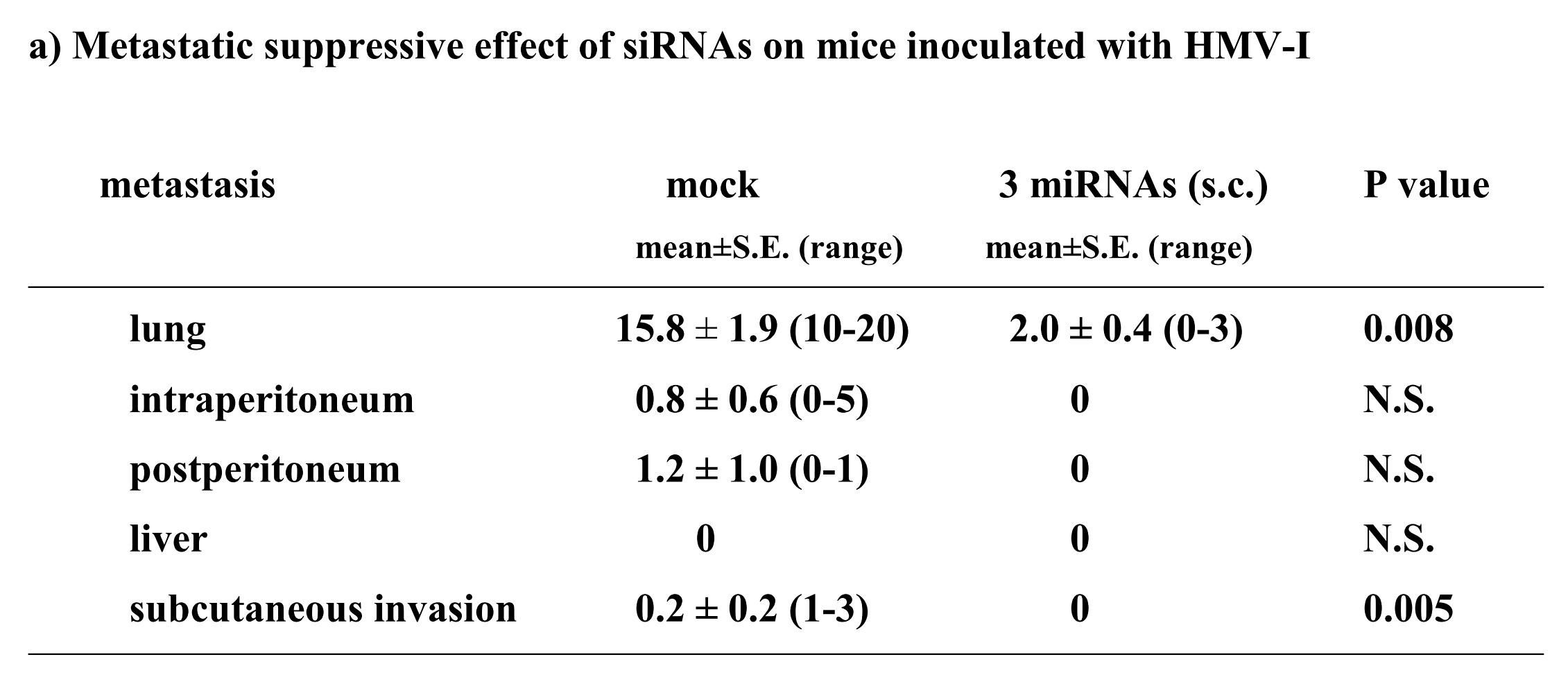
- FIG. 4 shows the results of investigating the suppression of the proliferation of HMV-I cells by subcutaneous administration of 3 siRNA mixture + DDS.
- FIG. 5A is a diagram showing parts with evaluated tumors.
- FIG. 5B shows the results of evaluating the expression suppression effects of miR-47, miR-101, and miR-197 by the 3siRNA mixture.
- FIG. 5C is a photograph of a tumor treated with siRNA observed under a microscope.
- FIG. 5D shows the results of investigating the transcription levels of genes related to tumor, differentiation, and pluripotency when a 3 siRNA mixture was administered.
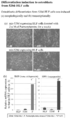
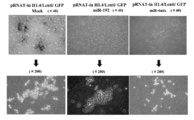
- FIG. 6A is a photograph observed with a microscope after transfection of miR-197 siRNA into 293FT cells.
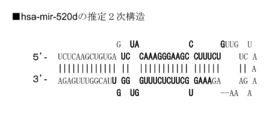
- FIG. 6B shows a secondary structure of hsa-mir-520d.
- FIG. 6C is a photograph of 293FT cells transfected with miR-197 siRNA observed under a microscope by immunohistochemistry.
- FIG. 6D shows the result of observing the expression level of an undifferentiated marker in an immunohistochemical test after infecting hsa-mir-520d in a HT1080 cell with a viral vector and forcibly expressing it.
- FIG. 6E shows the results of observing the expression level of undifferentiated markers in an immunohistochemical test after infecting hsa-mir-520d with T98G cells with a viral vector and forced expression.
- FIG. 6F shows the result of observing the expression level of an undifferentiated marker in an immunohistochemical test after infecting hsa-mir-520d with a viral vector in a PK-45p cell and forcibly expressing it.
- FIG. 7A shows the results of investigating the transcription amounts of various genes in iPS cells prepared using miR-197 siRNA and hsa-mir-520.
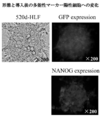
- FIG. 8A shows the results of microscopic evaluation of the floating cell population that emerged after virus introduction of has-mir-520d into 293FT cells.
- FIG. 8B shows the result of confirmation of stem transformation of 520d-293FT based on immunocytochemistry.
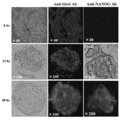
- FIG. 8C shows the results of examining the GFP positive and NANOG positive states of 520d-293FT.
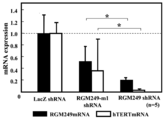
- FIG. 9A shows the results of investigating the expression levels of cells such as p53 and hTERT by RT-PCR.
- FIG. 9B shows the results of examining the expression levels of cells such as p53 and hTERT by Western blot.
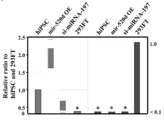
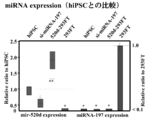
- FIG. 9C shows the results of examining the expression level of miRNA in cells.
- FIG. 9D shows the results of investigating the expression level of miRNA in cells when has-mir-520d is overexpressed.
- FIG. 10A shows the results of cell cycle analysis of 293FT, mock-293FT, and 520d-293FT.
- FIG. 10B shows the results of investigating the expression level ratios of DNMT 1, HDAC, Sin3A, and MBD3 in 293FT, mock-293FT, and 520d-293FT.
- FIG. 11A shows the results of investigating morphological changes of 520d-HLF.
- FIG. 11B shows the results of investigating the expression level ratio of various mRNAs in 520d-HLF.
- FIG. 11C shows the results of investigating the infiltrating properties of mock-HLF and 520d-HLF.
- FIG. 11D shows the results of examining the expression levels of various proteins in HLF, mock-HLF, and 520d-HLF by Western blotting.
- FIG. 12A shows the results of cell cycle analysis of mock-HLF and 520d-HLF.
- FIG. 12B shows the results of investigating expression ratios of various mRNAs in HLF, hiPSC, and 520d-HLF.
- FIG. 13 shows the results of investigating the expression level ratios of DNMT 1, HDAC, Sin3A, and MBD3 in HLF, mock-HLF, and 520d-HLF.
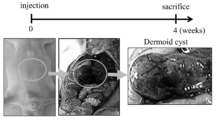
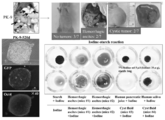
- FIG. 14A is a photograph showing tumor formation.
- FIG. 14B is a photograph showing white nodules.
- FIG. 14C is a photograph showing conversion into normal liver tissue.
- FIG. 14D is a photograph showing adenomatous hyperplasia.
- FIG. 14E is a photograph showing the generated teratoma and liver tissue.
- FIG. 15 shows the results of examining the differentiation of 520d-HLF.
- FIG. 16 shows the results of inducing bone differentiation of 520d-HLF.
- FIG. 15 shows the results of examining the differentiation of 520d-HLF.
- FIG. 16 shows the results of inducing bone differentiation of 520d-HLF.
- FIG. 17 shows the results of investigating morphological changes and the like of Huh7 infected with the has-mir-520d virus.
- FIG. 18 shows the results of investigating morphological changes and the like of T98G infected with the has-mir-520d virus.
- FIG. 19 shows the results of investigating morphological changes and the like of PK-9 infected with the has-mir-520d virus.
- FIG. 20 shows the results of investigating morphological changes and the like of HT1080 infected with the has-mir-520d virus.
- FIG. 21 shows the results of MTT assay performed on HMV-1 after infection with siRNA-producing virus.
- FIG. 22 is a fluorescence micrograph and growth curve of HMV-1 after infection with siRNA-producing virus.
- FIG. 23 shows the results of conducting colony formationHMVassay on HMV-1 after infection with siRNA-producing virus.
- polynucleotide Containing the Base Sequence of SEQ ID NO: 1 One embodiment of the present invention is a single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1. This single- or multiple-stranded polynucleotide has been suggested to induce cells into pluripotent stem cells in the examples described below. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for inducing cells into pluripotent stem cells.
- this single- or multiple-stranded polynucleotide promotes or suppresses the expression of an undifferentiated cell marker in the examples described later, promotes the expression level of p53 in pluripotent stem cells, or malignant tumors. It has been suggested that it is effective for suppression. Therefore, this single- or multiple-stranded polynucleotide can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used for the treatment of malignant tumors.
- pluripotent stem cell inducer that contains a single- or multiple-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 1 and induces cells into pluripotent stem cells.
- the effect of the one- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1 is as described above. Therefore, this pluripotent stem cell inducer can be suitably used for inducing cells into pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for regulating the expression of an undifferentiated cell marker.
- this pluripotent stem cell inducer can be suitably used for promoting the expression level of p53 in pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for the treatment of malignant tumors.
- an undifferentiated cell marker expression regulator, a pluripotent stem cell p53 expression promoter, or a malignant tumor therapeutic agent containing one or more polynucleotides comprising the nucleotide sequence of SEQ ID NO: 1 It is.
- the effect of the one- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1 is as described above. Therefore, the undifferentiated cell marker expression regulator, the pluripotent stem cell p53 expression promoter, or the malignant tumor therapeutic agent can be suitably used for regulating the expression of the undifferentiated cell marker.
- they can be suitably used to induce cells into pluripotent stem cells.
- they can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- the effect of the polynucleotide comprising the base sequence of SEQ ID NO: 1 is the same as the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1 described above. Therefore, this siRNA or miRNA can be suitably used for inducing cells into pluripotent stem cells.
- this siRNA or miRNA can be suitably used to regulate the expression of undifferentiated cell markers.
- this siRNA or miRNA can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- this siRNA or miRNA can be suitably used for the treatment of malignant tumors.
- Another embodiment is a vector containing a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 1.
- This vector can be suitably used for expressing or producing a single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1. Therefore, this vector can be used for the same use (pluripotent stem cell inducer, therapeutic agent, etc.) as the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 1.
- This vector may further contain a base sequence complementary to the base sequence of SEQ ID NO: 4.
- it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to the polynucleotide comprising the nucleotide sequence of SEQ ID NO: 1.
- it can be used suitably for expressing or producing siRNA, miRNA, or shRNA containing a polynucleotide comprising the nucleotide sequence of SEQ ID NO: 1.
- the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 1 may further contain the base sequence of SEQ ID NO: 4.
- the action efficiency of RNAi or miRNA exerted by one or a plurality of polynucleotides containing the base sequence of SEQ ID NO: 1 is increased. This is because it is considered that the base sequence of SEQ ID NO: 1 and the base sequence of SEQ ID NO: 4 are likely to be incorporated into RISC by forming a base pair.
- the structure of shRNA can be taken.
- the base sequence of SEQ ID NO: 4 when the base sequence of SEQ ID NO: 4 is included, it is considered that the one or plural-stranded polynucleotides including the base sequence of SEQ ID NO: 1 are more stabilized. Further, it is considered that the same effect can be obtained even when one or a plurality of polynucleotides containing the base sequence of SEQ ID NO: 1 contain a complementary strand of an RNA strand consisting of the base sequence of SEQ ID NO: 1. .
- the single-stranded or multi-stranded polynucleotides containing the nucleotide sequences of SEQ ID NO: 1, SEQ ID NO: 2, and SEQ ID NO: 3 are miR-47 siRNA, miR-101 siRNA, miR- described in Examples described later. Each may contain a 197 ⁇ siRNA guide strand. These three siRNAs are designed to play RNAi against miRNAs generated from RGM249 mRNA, suggesting that they share a common function in that they block the cascade starting from RGM249 mRNA. . Therefore, if these three siRNAs are introduced into cells, it is considered that a similar effect is exhibited.
- polynucleotide containing the nucleotide sequence of SEQ ID NO: 2 Another embodiment is a single- or multiple-stranded polynucleotide containing the nucleotide sequence of SEQ ID NO: 2.
- This single- or multiple-stranded polynucleotide has been suggested to induce cells into pluripotent stem cells in the examples described below. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for inducing cells into pluripotent stem cells.
- this single- or multiple-stranded polynucleotide promotes or suppresses the expression of an undifferentiated cell marker, promotes the expression level of p53 in pluripotent stem cells, or is used for malignant tumors. It has been suggested that it is effective for suppression. Therefore, this single- or multiple-stranded polynucleotide can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used for the treatment of malignant tumors.
- pluripotent stem cell inducer that contains a single- or multiple-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 2 and induces cells into pluripotent stem cells.
- the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 2 is as described above. Therefore, this pluripotent stem cell inducer can be suitably used for inducing cells into pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for regulating the expression of an undifferentiated cell marker.
- this pluripotent stem cell inducer can be suitably used for promoting the expression level of p53 in pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for the treatment of malignant tumors.
- an agent for regulating expression of an undifferentiated cell marker, a p53 expression promoter for pluripotent stem cells, or a therapeutic agent for malignant tumors comprising one or a plurality of polynucleotides comprising the nucleotide sequence of SEQ ID NO: 2. It is. Here, the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 2 is as described above. Therefore, the undifferentiated cell marker expression regulator, the pluripotent stem cell p53 expression promoter, or the malignant tumor therapeutic agent can be suitably used for regulating the expression of the undifferentiated cell marker. Alternatively, they can be suitably used to induce cells into pluripotent stem cells. Alternatively, they can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, they can be suitably used for the treatment of malignant tumors.
- the effect of the polynucleotide comprising the base sequence of SEQ ID NO: 2 is the same as the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 2 described above. Therefore, this siRNA or miRNA can be suitably used for inducing cells into pluripotent stem cells. Alternatively, this siRNA or miRNA can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this siRNA or miRNA can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this siRNA or miRNA can be suitably used for the treatment of malignant tumors.
- Another embodiment is a vector containing a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 2.
- This vector can be suitably used for expressing or producing a single-stranded polynucleotide comprising the base sequence of SEQ ID NO: 2 described above. Therefore, this vector can be used for the same use (pluripotent stem cell inducer, therapeutic agent, etc.) as the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 2 above.
- This vector may further contain a base sequence complementary to the base sequence of SEQ ID NO: 5.
- it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to the polynucleotide comprising the nucleotide sequence of SEQ ID NO: 2.
- it can be used suitably for expressing or producing siRNA, miRNA, or shRNA containing a polynucleotide comprising the nucleotide sequence of SEQ ID NO: 2.
- the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 2 may further contain the base sequence of SEQ ID NO: 5.
- the action efficiency of RNAi or miRNA exhibited by one or a plurality of polynucleotides containing the base sequence of SEQ ID NO: 2 is increased. This is because it is considered that the base sequence of SEQ ID NO: 2 and the base sequence of SEQ ID NO: 5 form a base pair and are easily incorporated into RISC.
- the structure of shRNA can be taken.
- nucleotide sequence of SEQ ID NO: 5 when the nucleotide sequence of SEQ ID NO: 5 is included, it is considered that the single- or multiple-stranded polynucleotide including the nucleotide sequence of SEQ ID NO: 2 is further stabilized. In addition, it is considered that the same effect can be obtained even when one or a plurality of polynucleotides including the base sequence of SEQ ID NO: 2 includes a complementary strand of an RNA strand consisting of the base sequence of SEQ ID NO: 2. .
- Another embodiment is a single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 3.
- This single- or multiple-stranded polynucleotide has been suggested to induce cells into pluripotent stem cells in the examples described below. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for inducing cells into pluripotent stem cells.
- this single- or multiple-stranded polynucleotide promotes or suppresses the expression of an undifferentiated cell marker in the examples described later, promotes the expression level of p53 in pluripotent stem cells, or malignant tumors. It has been suggested that it is effective for suppression. Therefore, this single- or multiple-stranded polynucleotide can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used for the treatment of malignant tumors.
- Another embodiment is a pluripotent stem cell inducer that contains a single- or multiple-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 3 and induces cells into pluripotent stem cells.
- the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 3 is as described above. Therefore, this pluripotent stem cell inducer can be suitably used for inducing cells into pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for regulating the expression of an undifferentiated cell marker.
- this pluripotent stem cell inducer can be suitably used for promoting the expression level of p53 in pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for the treatment of malignant tumors.
- an undifferentiated cell marker expression regulator, a pluripotent stem cell p53 expression promoter, or a malignant tumor therapeutic agent containing one or more polynucleotides comprising the nucleotide sequence of SEQ ID NO: 3 It is.
- the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 3 is as described above. Therefore, the undifferentiated cell marker expression regulator, the pluripotent stem cell p53 expression promoter, or the malignant tumor therapeutic agent can be suitably used for regulating the expression of the undifferentiated cell marker.
- they can be suitably used to induce cells into pluripotent stem cells.
- they can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- the effect of the polynucleotide comprising the base sequence of SEQ ID NO: 3 is the same as the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 3 described above. Therefore, this siRNA or miRNA can be suitably used for inducing cells into pluripotent stem cells. Alternatively, this siRNA or miRNA can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this siRNA or miRNA can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this siRNA or miRNA can be suitably used for the treatment of malignant tumors.
- Another embodiment is a vector containing a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 3.
- This vector can be suitably used for expressing or producing a single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 3 above. Therefore, this vector can be used for the same use (pluripotent stem cell inducer, therapeutic agent, etc.) as the single- or multi-stranded polynucleotide containing the base sequence of SEQ ID NO: 3 above.
- This vector may further contain a base sequence complementary to the base sequence of SEQ ID NO: 6.
- it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to the polynucleotide comprising the nucleotide sequence of SEQ ID NO: 3.
- it can be used suitably for expressing or producing siRNA, miRNA, or shRNA containing a polynucleotide comprising the nucleotide sequence of SEQ ID NO: 3.
- the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 3 may further contain the base sequence of SEQ ID NO: 6.
- the action efficiency of RNAi or miRNA exerted by one or a plurality of polynucleotides containing the base sequence of SEQ ID NO: 3 is increased. This is because it is considered that the base sequence of SEQ ID NO: 3 and the base sequence of SEQ ID NO: 6 form a base pair and are easily incorporated into RISC.
- the structure of shRNA can be taken.
- the base sequence of SEQ ID NO: 6 when the base sequence of SEQ ID NO: 6 is included, it is considered that the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 3 is more stabilized. In addition, it is considered that the same effect can be obtained even when one or a plurality of polynucleotides including the base sequence of SEQ ID NO: 3 include a complementary strand of an RNA chain consisting of the base sequence of SEQ ID NO: 3. .
- the nucleotide sequence complementary to the RNA strand obtained by treating the RNA strand comprising the nucleotide sequence of SEQ ID NO: 7 with Dicer (
- Dicer treatment it is a single- or multiple-stranded polynucleotide containing “sometimes referred to as a complementary base sequence after Dicer treatment”.
- the complementary base sequence after the dicer treatment includes the base sequence of any of the guide strands of miR-47 siRNA, miR-101 siRNA, and miR-197 siRNA described in the Examples described later.
- the guide strand is a site thought to characterize functions of miR-47 siRNA and the like.
- This miR-47 siRNA induces cells into pluripotent stem cells, promotes or suppresses the expression of undifferentiated cell markers, and promotes the expression level of p53 in pluripotent stem cells in Examples described later. It has been suggested that it is effective in suppressing malignant tumors. Therefore, the single- or multiple-stranded polynucleotide containing a complementary base sequence after Dicer treatment similarly induces cells into pluripotent stem cells, promotes or suppresses the expression of undifferentiated cell markers, It is considered possible to promote the expression level of p53 in pluripotent stem cells or suppress malignant tumors.
- Another embodiment is a pluripotent stem cell inducer that contains a single- or multiple-stranded polynucleotide containing a complementary base sequence after Dicer treatment and induces cells to pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for inducing cells into pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for regulating the expression of an undifferentiated cell marker.
- this pluripotent stem cell inducer can be suitably used for promoting the expression level of p53 in pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for the treatment of malignant tumors.
- an undifferentiated cell marker expression regulator for regulating the expression of the undifferentiated cell marker.
- they can be suitably used to induce cells into pluripotent stem cells.
- they can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- they can be suitably used for the treatment of malignant tumors.
- siRNA or miRNA containing a polynucleotide containing a complementary base sequence after Dicer treatment is the same as the effect which the polynucleotide of 1 or multiple strands containing the complementary base sequence after the said dicer process has. Therefore, this siRNA or miRNA can be suitably used for inducing cells into pluripotent stem cells. Alternatively, this siRNA or miRNA can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this siRNA or miRNA can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this siRNA or miRNA can be suitably used for the treatment of malignant tumors.
- Another embodiment is a vector containing a polynucleotide comprising a base sequence complementary to a complementary base sequence after Dicer treatment.
- This vector can be suitably used for expressing or producing a single- or multiple-stranded polynucleotide containing a complementary base sequence after the above Dicer treatment. Therefore, this vector can be used for the same use (pluripotent stem cell inducer, therapeutic agent, etc.) as the single- or multiple-stranded polynucleotide containing the complementary base sequence after the above Dicer treatment.
- This vector may further contain a complementary base sequence after Dicer treatment.
- a complementary base sequence after Dicer treatment it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to a polynucleotide containing a complementary base sequence after Dicer treatment.
- siRNA, miRNA, or shRNA it can be suitably used for expressing or producing siRNA, miRNA, or shRNA containing a polynucleotide containing a complementary base sequence after Dicer treatment.
- the above-mentioned single- or multiple-stranded polynucleotide containing a complementary base sequence after dicer treatment may further contain a complementary strand of an RNA strand consisting of a complementary base sequence after dicer treatment.
- RNAi or miRNA exhibited by one or a plurality of polynucleotides containing a complementary base sequence after the Dicer treatment is increased. This is because the complementary base sequence after the dicer treatment and the complementary strand of the RNA strand consisting of the complementary base sequence after the dicer treatment form a base pair, so that it can be easily incorporated into RISC. is there.
- the structure of shRNA can be taken.
- a complementary strand of an RNA strand consisting of a complementary base sequence after dicer treatment is included, when one or a plurality of polynucleotides including the complementary base sequence after dicer treatment is further stabilized Conceivable.
- Another embodiment is a single-stranded or double-stranded polynucleotide having RNAi action on an RNA strand comprising one or more base sequences selected from the group consisting of SEQ ID NOs: 11, 12, and 13. . It has been demonstrated that the RNA strand containing one or more base sequences is an RNA strand obtained by treating the RNA strand containing the base sequence of SEQ ID NO: 7 with Dicer in the examples described later. Therefore, it has the same effect as that of a single- or multiple-stranded polynucleotide containing a complementary base sequence after the dicer treatment and can be used for the same purpose.
- polynucleotide Containing the Base Sequence of SEQ ID NO: 8 Another embodiment is a single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 8. It has been suggested that this single- or multiple-stranded polynucleotide induces cells into pluripotent stem cells by inhibiting a cascade starting from RGM249 mRNA in the examples described below. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for inducing cells into pluripotent stem cells. Alternatively, it can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this single- or multiple-stranded polynucleotide can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- this single- or multiple-stranded polynucleotide is effective in suppressing malignant tumors in Examples described later. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for the treatment of malignant tumors.
- pluripotent stem cell inducer that contains a single- or multiple-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 8 and induces cells into pluripotent stem cells.
- the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 8 is as described above. Therefore, this pluripotent stem cell inducer can be suitably used for inducing cells into pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for regulating the expression of an undifferentiated cell marker.
- this pluripotent stem cell inducer can be suitably used for promoting the expression level of p53 in pluripotent stem cells.
- this pluripotent stem cell inducer can be suitably used for the treatment of malignant tumors.
- Another embodiment is an undifferentiated cell marker expression regulator, an undifferentiated cell marker expression regulator, or a therapeutic agent for malignant tumors, comprising one or a plurality of polynucleotides comprising the nucleotide sequence of SEQ ID NO: 8. .
- the effect of the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 8 is as described above. Therefore, the undifferentiated cell marker expression regulator, the undifferentiated cell marker expression regulator, or the malignant tumor therapeutic agent can be suitably used for regulating the expression of the undifferentiated cell marker.
- they can be suitably used to induce cells into pluripotent stem cells.
- they can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- they can be suitably used for the treatment of malignant tumors.
- Another embodiment is an shRNA containing a polynucleotide comprising the base sequence of SEQ ID NO: 8.
- the effect of the polynucleotide containing the base sequence of SEQ ID NO: 8 is the same as the effect of the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 8. Therefore, this shRNA can be suitably used for inducing cells into pluripotent stem cells.
- this shRNA can be suitably used to regulate the expression of undifferentiated cell markers.
- this shRNA can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- this shRNA can be suitably used for the treatment of malignant tumors.
- Another embodiment is a vector containing a polynucleotide comprising a base sequence complementary to the base sequence of SEQ ID NO: 8.
- This vector can be suitably used for expressing or producing a single-stranded polynucleotide comprising the base sequence of SEQ ID NO: 8 above. Therefore, this vector can be used for the same uses (pluripotent stem cell inducer, therapeutic agent, etc.) as the single- or multi-stranded polynucleotide comprising the base sequence of SEQ ID NO: 8 above.
- This vector may further contain a base sequence complementary to the base sequence of SEQ ID NO: 9.
- it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to the polynucleotide comprising the nucleotide sequence of SEQ ID NO: 8.
- it can be suitably used for expressing or producing siRNA, miRNA, shRNA containing a polynucleotide comprising the nucleotide sequence of SEQ ID NO: 8.
- the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 8 may further contain the base sequence of SEQ ID NO: 9.
- the action efficiency of RNAi or miRNA exhibited by one or a plurality of polynucleotides containing the base sequence of SEQ ID NO: 8 is increased. This is because it is considered that the base sequence of SEQ ID NO: 8 and the base sequence of SEQ ID NO: 9 are likely to be incorporated into RISC by forming a base pair.
- the structure of shRNA can be taken.
- the base sequence of SEQ ID NO: 9 when the base sequence of SEQ ID NO: 9 is included, it is considered that the one or plural-stranded polynucleotides including the base sequence of SEQ ID NO: 8 are more stabilized. In addition, it is considered that the same effect can be obtained even when one or a plurality of polynucleotides including the base sequence of SEQ ID NO: 8 include a complementary strand of an RNA strand consisting of the base sequence of SEQ ID NO: 8. .
- the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 8 may be a single-stranded polynucleotide containing the base sequence of SEQ ID NO: 10.
- the RNA strand containing the base sequence of SEQ ID NO: 7 can be suitably used as shRNA having RNAi action.
- Polynucleotide related to the nucleotide sequence of SEQ ID NO: 7 Another embodiment is a single-stranded or double-stranded polynucleotide having RNAi action on an RNA strand comprising the nucleotide sequence of SEQ ID NO: 7. It has been suggested that this single- or multiple-stranded polynucleotide induces cells into pluripotent stem cells by inhibiting a cascade starting from RGM249 mRNA in the examples described below. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for inducing cells into pluripotent stem cells.
- the single- or multiple-stranded polynucleotide can be suitably used for regulating the expression of an undifferentiated cell marker.
- this single- or multiple-stranded polynucleotide can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- this single- or multiple-stranded polynucleotide is effective in suppressing malignant tumors in Examples described later. Therefore, this single- or multiple-stranded polynucleotide can be suitably used for the treatment of malignant tumors.
- RNAi action on an RNA strand comprising the base sequence of SEQ ID NO: 7, and induces cells to pluripotent stem cells.
- a stem cell inducer the effect of the single-stranded or double-stranded polynucleotide having RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7 is as described above. Therefore, this pluripotent stem cell inducer can be suitably used for inducing cells into pluripotent stem cells. Alternatively, this pluripotent stem cell inducer can be suitably used for regulating the expression of an undifferentiated cell marker. Alternatively, this pluripotent stem cell inducer can be suitably used for promoting the expression level of p53 in pluripotent stem cells. Alternatively, this pluripotent stem cell inducer can be suitably used for the treatment of malignant tumors.
- an undifferentiated cell marker expression regulator comprising a single-stranded or double-stranded polynucleotide having RNAi action on an RNA strand comprising the nucleotide sequence of SEQ ID NO: 7 It is a p53 expression promoter or a malignant tumor therapeutic agent.
- the effect of the single-stranded or double-stranded polynucleotide having RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7 is as described above. Therefore, the undifferentiated cell marker expression regulator, the pluripotent stem cell p53 expression promoter, or the malignant tumor therapeutic agent can be suitably used for regulating the expression of the undifferentiated cell marker.
- they can be suitably used to induce cells into pluripotent stem cells.
- they can be suitably used to promote the expression level of p53 in pluripotent stem cells.
- they can be suitably used for the treatment of malignant tumors.
- the effect of the polynucleotide having the RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7 is the single strand having the RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7 or The effect is similar to that of a double-stranded polynucleotide. Therefore, this shRNA can be suitably used for inducing cells into pluripotent stem cells. Alternatively, this shRNA can be suitably used to regulate the expression of undifferentiated cell markers. Alternatively, this shRNA can be suitably used to promote the expression level of p53 in pluripotent stem cells. Alternatively, this shRNA can be suitably used for the treatment of malignant tumors.
- Another embodiment is a vector comprising a base sequence complementary to a base sequence encoding a polynucleotide having RNAi action on an RNA strand comprising the base sequence of SEQ ID NO: 7.
- This vector can be suitably used for expressing or producing a polynucleotide having RNAi action on the RNA strand comprising the base sequence of SEQ ID NO: 7. Therefore, this vector can be used for the same uses (pluripotent stem cell inducer, therapeutic agent, etc.) as the polynucleotide having RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7.
- This vector may further contain a base sequence encoding a polynucleotide having an RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7.
- a base sequence encoding a polynucleotide having an RNAi action on the RNA strand containing the base sequence of SEQ ID NO: 7.
- it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to a polynucleotide having an RNAi action on an RNA strand comprising the nucleotide sequence of SEQ ID NO: 7.
- siRNA, miRNA, and shRNA containing a polynucleotide having RNAi action on an RNA strand comprising the base sequence of SEQ ID NO: 7.
- Polynucleotide related to a base sequence such as SEQ ID NO: 41 Another embodiment is a single- or multiple-stranded polynucleotide comprising SEQ ID NO: 41 or one or more base sequences of 44 to 47.
- This single- or multiple-stranded polynucleotide can exhibit the same effects as those of the single- or multiple-stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 1, 2, 3, or 8 as described above. This is suggested in the examples described later.
- pluripotent stem cell inducer undifferentiated cell marker expression regulator, pluripotent stem cell p53 expression promoter, malignant tumor therapeutic agent, siRNA (or miRNA) or shRNA (or pre-miRNA), or vector Can be used for applications.
- the single- or multiple-stranded polynucleotide comprising the base sequence of SEQ ID NO: 41 may further comprise a complementary strand thereof or a polynucleotide comprising the base sequence of SEQ ID NO: 42.
- the single- or multiple-stranded polynucleotide containing the base sequence of SEQ ID NO: 41 may be a single-stranded polynucleotide containing the base sequence of SEQ ID NO: 43.
- the single- or multiple-stranded polynucleotide comprising the nucleotide sequences of SEQ ID NOs: 44 to 47 may further include a complementary strand thereof or a polynucleotide comprising the nucleotide sequences of SEQ ID NOs: 48 to 51, respectively.
- the single or multiple stranded polynucleotide comprising the nucleotide sequence of SEQ ID NOs: 44 to 47 may be a single or multiple stranded polynucleotide comprising the nucleotide sequence of SEQ ID NO: 52 to 55 or 56 to 59, respectively. Good.
- Another embodiment is a vector containing a polynucleotide comprising a base sequence complementary to one or more base sequences of SEQ ID NO: 41 or 44 to 47.
- This vector can be suitably used for expressing or producing a single- or multiple-stranded polynucleotide comprising one or more base sequences of SEQ ID NO: 41 or 44 to 47 described above. Therefore, this vector can be used for the same use (pluripotent stem cell inducer, therapeutic agent, etc.) as one or multiple-stranded polynucleotides containing one or more base sequences of SEQ ID NO: 41 or 44 to 47.
- This vector may further contain a base sequence complementary to SEQ ID NO: 42 or one or more base sequences of 48 to 51.
- it can be suitably used for expressing or producing a polynucleotide capable of forming a base pair with respect to a polynucleotide comprising one or more base sequences of SEQ ID NO: 41 or 44 to 47.
- siRNA, miRNA, pre-miRNA, or shRNA containing a polynucleotide comprising one or more base sequences of SEQ ID NO: 41 or 44 to 47.
- Cells Introduced with Polynucleotides are cells into which any one or more of the above-described polynucleotides or any of the vectors described above are introduced. Since these cells have induced pluripotency, they can be suitably used as medical materials or research materials for regenerative medicine.
- the expression level of p53 is, for example, 1, 1.2, 1.4, 1.6, 1.8, 2.0, 3.0, 4.0, 5.0, 10, 100, or 1000 times the expression level of p53 in the HPS0002: 253G1 strain of hiPSC. However, it is not limited to them. Moreover, this expression level may be in the range of any two values exemplified here.
- the method for measuring the expression level of p53 is preferably real-time PCR in terms of measurement accuracy and simplicity. For the detailed measurement conditions, the real-time PCR measurement conditions in the examples described later can be used.
- Another embodiment is a method for producing a pluripotent stem cell, comprising the step of introducing any one or more of the above-mentioned polynucleotides into a cell.
- it is a method for producing pluripotent stem cells, which comprises a step of introducing any of the vectors described above into cells. If this method is appropriately used, pluripotent stem cells can be produced.
- the introduction of the polynucleotide or vector into the cell and the culture method can be performed according to methods known in the art.
- ES cells For introduction into cells, for example, calcium phosphate method, lipofection method, electroporation method, method using virus (adenovirus, retrovirus, HIV, etc.), or microinjection can be used [Revised 4th edition New Genetic Engineering Handbook, Yodosha (2003): 152-179. ]. Also, only introduced cells can be selected using drug resistance, cell sorter or the like.
- a medium for primate ES cells Cosmo Bio
- a medium for normal human cells for example, a DMEM or RPMI-based medium
- ES cells are often co-cultured with feeder cells, but the pluripotent stem cells of this embodiment can be established even in the absence of feeder cells.
- Feeder cells can be obtained from, for example, the European Collection of Cell Cultures.
- the pluripotent stem cells of this embodiment are all F-12 HAM [DMEM (15 mM HEPES + 1 mM Sodium Pyruvate + pyridoxine + NaHCO 3 +5 mM L-glutamine)], RPMI-1640 + L-glutamine, DMEM + high glucose + L-glutamine + 0.1 mM NEAA and REPROSTEM (REPROCell): Can be cultured in one or more media selected from the group consisting of bFGF 3-10 ng / ml at 37 ° C., 5% CO 2 , 10% FBS . Therefore, it has succeeded in overcoming the difficulty in culture of so-called iPS cells.
- Another embodiment is a pluripotent stem cell obtained by the above production method.
- it is a pluripotent stem cell in which the expression level of endogenous p53 is increased as compared with the HPS0002: 253G1 strain.
- it is a pluripotent stem cell in which the expression level of any one or more of the above-mentioned polynucleotides is increased. Since these cells express endogenous p53, the risk of malignant tumor formation is low.
- the base sequences of the above SEQ ID NOs: 1 to 10 and 41 to 59 may be mutated to some extent.
- One or more strands of a polynucleotide containing a base sequence having such a mutation are considered to have the same effect as one or more strands of a polynucleotide comprising a wild-type base sequence.
- a polynucleotide containing a mutant base sequence can be artificially prepared, and in that case, it can also be referred to as a polynucleotide containing a modified base sequence.
- the nucleotide sequence variations of SEQ ID NOs: 4-6, 9, 42, 48-51, and 56-59 are SEQ ID NOs: 1-3, 8, 41, 44. Even if it is larger than the mutations of the base sequences of .about.47 and 52.about.55, the function hardly changes. This is because the nucleotide sequences of SEQ ID NOs: 1-3, 8, 41, 44-47, and 52-55 are important sequences that characterize the functions of RNAi, miRNA, etc., while SEQ ID NOs: 4-6, This is because the base sequences of 9, 42, 48 to 51, and 56 to 59 are auxiliary sequences.
- the base sequences of SEQ ID NOs: 1 to 10 and 41 to 59 may be base sequences in which one or several bases of each base sequence are deleted, substituted, or added.
- One or more strands of a polynucleotide containing such a base sequence are considered to have the same effect as one or more strands of a polynucleotide comprising a wild-type base sequence.
- the “one or several” is preferably 10 or less, more preferably 5 or less, more preferably 4 or less, more preferably 3 or less, and more preferably 2 Or less, more preferably one. This is because the smaller the number of “1 or several”, the closer to the wild type.
- the “addition” includes the concept of insertion.
- the base sequences of SEQ ID NOs: 1 to 10 and 41 to 59 may be base sequences having a homology of 80% or more with respect to the respective base sequences.
- One or more strands of a polynucleotide containing such a base sequence are considered to have the same effect as one or more strands of a polynucleotide comprising a wild-type base sequence.
- “80% or more” is preferably 85% or more, more preferably 90% or more, more preferably 95% or more, more preferably 96% or more, more preferably 97% or more. More preferably, it is 98% or more, and most preferably 99% or more. This is because the greater the “80% or more”, the closer to the wild type.
- the base sequences of SEQ ID NOs: 1 to 10 and 41 to 59 are polynucleotides that hybridize under stringent conditions to a polynucleotide consisting of a base sequence complementary to each base sequence. Also good. One or more strands of a polynucleotide containing such a base sequence are considered to have the same effect as one or more strands of a polynucleotide comprising a wild-type base sequence.
- homology is the ratio of the same number of bases in two or more base sequences calculated according to a method known in the art. Before calculating the ratio, the base sequences of the base sequence groups to be compared are aligned, and a gap is introduced into a part of the base sequence if necessary to maximize the same ratio. Also, it means the ratio of the same number of bases to all bases including overlapping bases in an optimally aligned state. Alignment methods, ratio calculation methods, and related computer programs are well known in the art and use common sequence analysis programs (eg GENETYX, GeneChip Sequence Analysis, etc.) Can be measured.
- stringent conditions means, for example, (1) low ionic strength and high temperature for washing, for example, 0.015 M sodium chloride / 0.0015 M sodium citrate / 0.005 at 50 ° C.
- 1% sodium dodecyl sulfate 1% sodium dodecyl sulfate, (2) denaturing agents such as formamide during hybridization, eg 50% (vol / vol) formamide and 0.1% bovine serum albumin / 0.1% ficoll / 42 ° C.
- miR-47 siRNA there are three mismatches between the guide strand and the passenger strand (FIG. 3B).
- miR-101 siRNA there is one mismatch between the guide strand and the passenger strand (FIG. 3B).
- miR-47 siRNA There are three mismatches between the guide strands of miR-47 and miR-47 siRNA (FIG. 3C).
- the “pluripotent stem cell” is a cell that has pluripotency and can differentiate into various cells.
- WO 2007/069666 and literature [Hong et al., Nature. 2009 Aug 27; 460 (7259): 1132-5. Epub 2009 Aug 9.] describe examples of production methods and characteristics. Yes.
- pluripotent stem cells can be recognized by those skilled in the art. For example, as compared with hiPSC (HPS0002 253G1), which is a human induced pluripotent stem cell, any undifferentiated marker is expressed at the same level or higher. Including cells.
- undifferentiated cell marker is a general term for compounds such as DNA strands, RNA strands, or proteins that are specifically expressed in undifferentiated cells. Examples include Klf4, c-Myc, Oct4, Sox2, PROM1, Nanog, SSEA-1, ALP, eRas, Esg1, Ecat1, Fgf4, Gdf3, REX-1. Sometimes referred to as a pluripotent stem cell marker.
- RNAi means that the function of a target gene, mRNA, or the like is suppressed by siRNA (short interfering RNA), shRNA (short hairpin ⁇ RNA), short or long single-stranded RNA, or the like. It is a phenomenon. In general, this repression is sequence specific and is present in various species.
- siRNA short interfering RNA
- shRNA short hairpin ⁇ RNA
- RISC RNA-induced Silencing Complex
- RISC recognizes a target RNA strand having a sequence highly complementary to this single-stranded RNA using the incorporated single-stranded RNA as a guide molecule.
- the target RNA strand is cleaved at the central part of the siRNA by AGO2 in RISC. Thereafter, the cleaved target RNA strand is degraded.
- the above is a typical mechanism, but there are other examples in which miRNA in the living body is targeted as a target [Krutzfeldt et al., Nucleic Acids Res. 2007; 35 (9): 2885-92. Epub 2007 Apr 16 .]It is described in.
- the “molecule having an RNAi action” is a molecule capable of causing an RNAi action, and includes, for example, siRNA, shRNA and the like.
- siRNA is a double-stranded polynucleotide that causes RNAi.
- the duplex of siRNA can be divided into a guide strand and a passenger strand, and the guide strand is incorporated into RISC.
- the guide strand incorporated into the RISC is used to recognize the target RNA.
- artificially prepared materials are mainly used, but those existing endogenously in the living body are also known.
- miRNA is a polynucleotide having a function similar to that of siRNA, and is known to suppress translation and to degrade target RNA strands.
- pre-miRNA is a precursor of miRNA. The difference between miRNA and siRNA generally lies in the production pathway and detailed mechanism.
- a typical production route of miRNA in vivo is as follows. First, it is transcribed as a long pri-RNA (primary miRNA) from the miRNA gene. This pri-miRNA contains a sequence that later becomes miRNA, and the part has a hairpin structure. Drosha cuts the root of this hairpin structure. The excised hairpin is called pre-miRNA.
- This pre-miRNA is transported to the cytoplasm by Exportin-5.
- Dicer cleaves the pre-miRNA in the cytoplasm to form a double-stranded miRNA, which further becomes a single strand to form a RISC.
- This single-stranded RNA acts as a guide molecule, recognizes the target RNA strand, and suppresses cleavage or translation.
- molecule having miRNA action is a molecule capable of causing miRNA action, and includes, for example, miRNA, pre-miRNA, pri-miRNA and the like.
- siRNA is a single-stranded polynucleotide capable of forming a hairpin-like structure (hairpin-like structure), and has a function of inducing RNAi. It has a structure similar to that of pre-miRNA and is normally cleaved by Dicer in the cell, and siRNA is excised. It is known that target RNA is cleaved by this siRNA.
- small RNA refers to a relatively small RNA, and examples thereof include siRNA, miRNA, shRNA, pre-miRNA, and single or multiple-stranded small RNA, but are not limited thereto. Not.
- the number of bases is, for example, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 40, 50, 60, 70, 80, 90, or 100 bases. It is not limited. The number of bases may be within the range of any two values exemplified here.
- Dicer includes an enzyme having a function of cleaving a precursor such as siRNA or miRNA to cut out siRNA or miRNA.
- dsRNA can be led to siRNA, pre-miRNA to miRNA, and shRNA to siRNA.
- Dicer is known to have several functions other than those described above.
- the single or multiple strands described above may be single strands or double strands.
- the mechanism of siRNA, miRNA, shRNA, or antisense RNA can be used.
- any of the above single- or multiple-stranded polynucleotides may be used individually, or two or more may be used in combination. Even in such a case, it can be suitably used as a pluripotent stem cell inducer, an undifferentiated cell marker expression regulator, a p53 expression promoter for pluripotent stem cells, or a malignant tumor therapeutic agent.
- the combination ratio in the case of using 2 or more together is not specifically limited.
- the above single- or multiple-stranded polynucleotide may have an RNAi action.
- the above single- or multiple-stranded polynucleotide may be a small RNA.
- Interferon response is generally known as a phenomenon in which cells enter an antiviral state by sensing double-stranded RNA (dsRNA).
- dsRNA double-stranded RNA
- PSR dsRNA-responsive protein kinase
- the one or more single-stranded polynucleotides described above are, for example, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 40, 50, 60, 70, 80, 90, 100, 200, or 500 nucleotides, but not limited thereto.
- This number may be within the range of any two values illustrated here. If this number is 15 or more, the possibility of being able to bind to the target polynucleotide with high accuracy increases. Moreover, if this number is 100 or less, the risk that disadvantageous phenomena such as interferon response occur will be reduced. This phenomenon is considered less likely to occur as the number of nucleotides decreases.
- the above-mentioned single- or multiple-stranded polynucleotide may be shRNA in the case of a single strand or siRNA in the case of a double strand.
- RNAi Ribonucleic acid
- miRNA may be sufficient.
- the shRNA may be composed of 35 or more nucleotides. If it is 35 or more, the possibility that a hairpin-like structure peculiar to shRNA can be formed with high accuracy is increased.
- the shRNA may be composed of 100 or less nucleotides. If it is 100 or less, the risk that disadvantageous phenomena such as an interferon response occur will be reduced.
- the length of shRNA is not necessarily 100 nucleotides or less. However, it is thought that it can function as shRNA.
- the literature [Lin et al., RNA. 2008; Oct; 14 (10): 2115-24.
- pre-miRNA is able to function even with large molecules artificially linked with four pre-miRNAs.
- this number is not limited as long as it can function as shRNA.
- This number may be within the range of any two values exemplified here.
- pre-miRNA may have the same number of nucleotides as shRNA for the same reason.
- the siRNA or miRNA guide strand may be composed of 15 or more nucleotides. If it is 15 or more, the possibility of being able to bind to the target polynucleotide with high accuracy increases.
- These guide strands may be composed of 40 or less nucleotides. If it is 40 or less, the risk that disadvantageous phenomena such as interferon response occur will be reduced. This number is for example 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, or 40 nucleotides However, it is not limited to them. This number may be within the range of any two values exemplified here.
- the above-mentioned single- or multiple-stranded polynucleotide, shRNA, siRNA, miRNA, and pre-miRNA may contain an overhang consisting of 1 to 5 nucleotides. In this case, it is considered that the efficiency of RNAi increases. This number is, for example, but not limited to 5, 4, 3, 2, or 1 nucleotide. This number may be within the range of any two values exemplified here.
- the vector examples include plasmids derived from E. coli (eg, pBR322, pBR325, pUC12, pUC13), plasmids derived from Bacillus subtilis (eg, pUB110, pTP5, pC194), yeast-derived plasmids (eg, pSH19, pSH15), ⁇ phage
- E. coli eg, pBR322, pBR325, pUC12, pUC13
- Bacillus subtilis eg, pUB110, pTP5, pC194
- yeast-derived plasmids eg, pSH19, pSH15
- ⁇ phage bacteriophage, HIV, adenovirus, retrovirus, vaccinia virus, baculovirus
- vectors derived from viruses pA1-11, pXT1, pRc / CMV, pRc / RSV, pcDNAI
- the pluripotent stem cell inducer may have a function of inducing somatic cells into pluripotent stem cells.
- pluripotent stem cells can be created from somatic cells.
- “somatic cell” refers to other cells excluding germ cells, and includes skin-derived cells, fibroblasts, and the like. Somatic cells usually have limited or disappeared pluripotency.
- the “pluripotent stem cell inducer” refers to a substance having an action of bringing cells close to pluripotent cells such as pluripotent stem cells.
- reprogramming refers to the action of bringing a cell closer to a pluripotent cell such as a pluripotent stem.
- the above pluripotent stem cell inducer may be an inducer that induces malignant tumor cells to pluripotent stem cells.
- pluripotent stem cells can be created from malignant tumor cells.
- malignant tumor includes a disease caused by normal cells undergoing mutation and continuing to grow. Also includes carcinoma and sarcoma. It is known that malignant tumors originate from all organs and tissues throughout the body, and when malignant tumor cells proliferate, they form a mass and invade and destroy surrounding normal tissues.
- Cancer is, for example, lung cancer, esophageal cancer, stomach cancer, liver cancer, pancreatic cancer, kidney cancer, adrenal cancer, biliary tract cancer, breast cancer, colon cancer, small intestine cancer, cervical cancer, endometrial cancer, ovarian cancer, bladder cancer, prostate Cancer, ureteral cancer, renal pelvic cancer, ureteral cancer, penile cancer, testicular cancer, brain tumor, central nervous system cancer, peripheral nervous system cancer, head and neck cancer (oral cancer, pharyngeal cancer, laryngeal cancer, nasal cavity / sinus) Cancer, salivary gland cancer, thyroid cancer, etc.), glioma, glioblastoma multiforme, skin cancer, melanoma, thyroid cancer, salivary gland cancer, blood cancer, or malignant lymphoma.
- the above pluripotent stem cell inducer induces induction of cells of one or more malignant tumors selected from the group consisting of liver cancer, pancreatic cancer, fibrosarcoma, glioblastoma multiforme, and melanoma into pluripotent stem cells.
- An agent may be used.
- pluripotent stem cells can be created from those malignant tumor cells. Induction of malignant tumor cells into pluripotent stem cells has hardly been reported so far, and it can be expected as a new and innovative therapeutic method for malignant tumors.
- the pluripotent stem cell may express endogenous p53.
- p53 In this case, malignant tumor formation is unlikely to occur.
- the expression level of p53 is preferably significantly higher than that of a control sample (for example, p53 knockout cells, normal cells, or samples derived therefrom).
- control sample for example, p53 knockout cells, normal cells, or samples derived therefrom.
- “significantly” means, for example, that a statistically significant difference between a control group and a test group is evaluated using Student's t-test, and p ⁇ 0.05.
- the “control group” refers to a sample placed under conditions different from those of the group to be inspected, and can be represented by a concept within a range normally used in the technical field.
- P53 is a gene generally classified as a malignant tumor suppressor gene, and is known to have a function of being activated when DNA is damaged to induce cell division arrest and damage repair.
- p53 is knocked out or knocked down, the efficiency of iPS cell production is increased (Zhao et al., Cell Stem Cell. 2008 Nov 6; 3 (5): 475-9., Hong et al., Nature. 2009 Aug 27; 460 (7259): 1132-5. Epub 2009 Aug 9.).
- ES cells lacking p53 have been reported to have unstable chromosomes and have resistance to differentiation induction (Lin et al., Nat Cell Biol. 2005 Feb; 7 (2) : 165-71. Epub 2004 Dec 26.). This means that there is a high possibility that undifferentiated cells remain after differentiation induction. Therefore, it is considered that the risk of malignant tumor formation increases when cells lacking p53 are transplanted in regenerative medicine. Therefore, it can be seen from this aspect that p53 is an important molecule for cells.
- endogenous means that the test substance is derived from the internal mechanism of the cell.
- a protein that is constitutively expressed in a cell is endogenously contained only in the expressed protein.
- the undifferentiated cell marker may be one or more undifferentiated cell markers selected from the group consisting of Klf4, c-Myc, Oct4, Sox2, and PROM1.
- Undifferentiated cell markers and various proteins can be detected using a known method such as RT-PCR (Reverse-Transcription-Polymerase-Chain-Reaction).
- RT-PCR is a method in which reverse transcription is performed using an RNA strand as a template, and PCR is performed on the generated cDNA.
- Total RNA can be extracted from cells using the guanidine thiocyanate method, commercially available reagents or kits.
- the cells can be purchased from Invitrogen Corporation, Sanko Junyaku Co., Ltd., Takara Bio Inc. and the like.
- undifferentiated cell markers and various proteins can also be detected in combination with real-time PCR.
- Such a method is called real-time RT-PCR.
- Real-time PCR is a method for monitoring nucleic acids amplified by PCR in real time. For example, it can be performed according to the procedure described in the literature [Real-time PCR experiment guide well understood from the principle, Yodosha, 2007/12]. Examples of the monitoring method include an intercalation method, a hybridization method, and a LUX (Light Upon eXtensyon) method.
- a typical method of intercalation is a method of measuring the amount of nucleic acid using the property that a fluorescent substance such as SYBR (r) Green I enters a double-stranded nucleic acid and emits light when irradiated with excitation light. is there. Since the intensity of fluorescence increases in proportion to the amount of nucleic acid, the amount of nucleic acid amplified can be determined by measuring the fluorescence intensity.
- quantification methods using real-time PCR are roughly divided into two quantification methods, an absolute quantification method and a relative quantification method, which can be used as appropriate.
- expression regulator includes a substance capable of increasing or decreasing the expression level of a target protein or mRNA.
- the amount to increase or decrease has a significant difference compared to the control cells.
- the above-mentioned therapeutic agent for malignant tumor may further contain DDS (Drug Delivery System).
- DDS includes gelatin hydrogel or atelocollagen.
- gelatin hydrogel is a hydrogel made from gelatin as a raw material and can be used as DDS.
- Gelatin hydrogel is excellent in biocompatibility and bioabsorbability.
- Atelocollagen is DDS using atelocollagen as a raw material. Excellent introduction efficiency into cells and safety.
- Atelocollagen is generally a telopeptide contained in collagen that is enzymatically decomposed, and it is difficult to induce an immune reaction.
- the malignant tumor may be one or more malignant tumors selected from the group consisting of liver cancer, lung cancer, pancreatic cancer, fibrosarcoma, glioblastoma multiforme, and melanoma. In this case, it is possible to treat those malignant tumors. In particular, since none of these malignant tumors has an innovative therapeutic method, the above therapeutic agents for malignant tumors are promising therapeutic agents.
- liver cancer includes diseases caused by the continued proliferation of liver cells.
- Hepatocytes capable of causing liver cancer include cells of blood vessels such as bile ducts, portal veins, dendritic cells or hepatocytes. Also included are primary liver cancer and metastatic liver cancer. Many primary liver cancers are known to be hepatocellular carcinoma.
- lung cancer includes malignant tumors that occur in the trachea, bronchi, alveolar epithelial cells, etc., and pathologically classified as adenocarcinoma, squamous cell carcinoma, large cell carcinoma, small cell carcinoma. it can. Adenocarcinoma, squamous cell carcinoma, and large cell carcinoma are also collectively referred to as non-small cell carcinoma because the mode of progression and therapeutic response differ between small cell carcinoma and other cancers. There are also a few tumors that are not included in small and non-small cell carcinomas, such as carcinoids and columnar species.
- pancreatic cancer includes malignant tumors arising from the pancreas.
- the pancreas consists of an acinus that produces pancreatic juice, a pancreatic duct that carries the pancreatic juice, and islets of Langerhans that are endocrine glands. Cancer can arise from any tissue. Examples include invasive pancreatic duct cancer, pancreatic endocrine tumor, intraductal papillary mucinous tumor, mucinous cystic tumor, acinar cell carcinoma, serous cystadenocarcinoma and the like.
- sarcoma includes malignant tumors that develop in connective tissue cells derived from non-epithelial cells such as bone, cartilage, fat, muscle, and blood vessels.
- fibrosarcoma malignant fibrous histiocytoma, cutaneous fibrosarcoma, liposarcoma, rhabdomyosarcoma, leiomyosarcoma, hemangiosarcoma, Kaposi sarcoma, lymphangiosarcoma, synovial sarcoma, alveolar soft tissue sarcoma, extraosseous Chondrosarcoma, extraosseous osteosarcoma, malignant peripheral nerve sheath tumor, osteosarcoma, chondrosarcoma, granulocyte sarcoma, Ewing sarcoma, primary fibrosarcoma, malignant bone giant cell tumor, bone primary liposarcoma, bone primary Examples include angiosarcoma.
- glioma includes malignant tumors that arise from glial cells.
- astroglial tumors oligodendrocyte tumors, ependymal tumors, choroid plexus tumors, glioblastoma multiforme, and the like.
- melanoma includes malignant tumors derived from melanocytes that occur in the skin, intraorbital tissue, oral mucosal epithelium, and the like. Examples include malignant melanoma, superficial enlarged melanoma, nodular melanoma, and terminal melanoma melanoma.
- the “polynucleotide” includes a nucleotide or a base, or an equivalent thereof composed of a plurality of bonded forms.
- Nucleotides and bases include DNA bases or RNA bases.
- the equivalents include, for example, DNA bases or RNA bases that have undergone chemical modification such as methylation, or nucleotide analogs.
- Nucleotide analogs include unnatural nucleotides.
- DNA strand refers to a form in which two or more DNA bases or their equivalents are linked.
- RNA strand refers to a form in which two or more RNA bases or their equivalents are linked.
- the “base sequence” is a sequence of nucleotides constituting the polynucleotide or an equivalent thereof.
- a base sequence can be represented by A (adenine), G (guanine), C (cytosine), and T (thymine).
- T and U can be read each other according to the application.
- A, G, C, and T are used to represent the base sequences of DNA strands and RNA strands in NCBI Reference Sequence, which is a typical database.
- Polynucleotides can be synthesized using a DNA / RNA synthesizer. In addition, it can also be purchased from a DNA base or RNA base synthesis contract company (for example, Invitrogen, Takara Bio, etc.). In addition, synthesis of siRNA, miRNA, shRNA, pre-miRNA, or a vector encoding them can be outsourced to each manufacturer.
- RNAi designer Invitrogen
- siDirect 2.0 Naito et al., BMC Bioinformatics. 2009 2009 Nov 30; 10: 392.
- Etc. can be used.
- Confirmation of RNAi action or miRNA action can be carried out by quantifying the amount of RNA strand expression by real-time RT-PCR. Alternatively, it can also be performed by methods such as analysis of RNA strand expression level by Northern blot, analysis of protein amount by Western blot, and observation of phenotype. In particular, the method using real-time RT-PCR is efficient.
- the “complementary strand” is another polynucleotide having high complementarity capable of hybridizing to one pornucleotide.
- “hybridization” refers to the property of allowing base pairing between a plurality of polynucleotides by hydrogen bonding between bases. Base pairs can occur in Watson-Crick base pairs, Hoogsteen base pairs, or any other sequence specific form. A state in which two single strands are hybridized is called a double strand.
- the term “complementary” includes, for example, a form in which T is associated with A and C is associated with G, and other polynucleotides can hybridize to one polynucleotide.
- treatment refers to the ability to exert a preventive or symptom-improving effect on one or more symptoms associated with a subject's disease or disease.
- subject includes a human or other mammal (eg, mouse, rat, rabbit, cow, monkey, chimpanzee, pig, horse, sheep, goat, dog, cat, guinea pig, hamster, etc.).
- a human or other mammal eg, mouse, rat, rabbit, cow, monkey, chimpanzee, pig, horse, sheep, goat, dog, cat, guinea pig, hamster, etc.
- mouse, rat, monkey, chimpanzee, or human and particularly preferred is human. This is because in the case of humans, the above single- or multiple-stranded polynucleotides can be used for treatment of human diseases, development of human therapeutic agents or diagnostic agents, and the like.
- mice, rats, monkeys, and chimpanzees are widely used as model animals for research all over the world, and many characteristics have been clarified. By investigating the medicinal pharmacology of nucleotides, particularly useful information can be obtained for the development of better therapeutic agents and the like
- the above-mentioned single- or multiple-stranded polynucleotide when used as a therapeutic agent, it can be administered alone, but usually with DDS or one or more pharmaceutically acceptable carriers and Preferably, they are mixed together and provided as pharmaceutical preparations prepared by any method well known in the pharmaceutical arts. Moreover, it is also possible to administer the precursor of the above-mentioned single or multiple-stranded polynucleotide without directly using the single- or multiple-stranded polynucleotide.
- Oral administration or oral, intraoral, intrarectal, subcutaneous Parenteral administration such as intramuscular, intraperitoneal, intraocular or intravenous, can be given and can be administered systemically or locally.
- the administration route is preferably parenteral administration.
- Subcutaneous or intravenous administration may be used as in Examples described later. In this case, the efficiency with which the single- or multiple-stranded polynucleotide reaches the affected area is high.
- compositions include capsules, tablets, granules, syrups, emulsions, injections, suppositories, sprays, ointments, tapes and the like.
- Suitable formulations for oral administration include emulsions, syrups, capsules, tablets, powders, granules and the like.
- Liquid preparations such as emulsions and syrups include sugars such as water, sucrose, sorbitol, fructose, glycols such as polyethylene glycol, propylene glycol, oils such as sesame oil, olive oil, soybean oil, p-hydroxybenzoic acid
- Preservatives such as esters, and flavors such as strawberry flavor and peppermint can be used as additives.
- capsules, tablets, powders, granules, etc. are excipients such as lactose, glucose, sucrose and mannitol, disintegrants such as starch and sodium alginate, lubricants such as magnesium stearate and talc, polyvinyl alcohol , Hydroxypropylcellulose, gelatin and other binders, surfactants such as fatty acid esters, plasticizers such as glycerin and the like can be used as additives.
- excipients such as lactose, glucose, sucrose and mannitol, disintegrants such as starch and sodium alginate, lubricants such as magnesium stearate and talc, polyvinyl alcohol , Hydroxypropylcellulose, gelatin and other binders, surfactants such as fatty acid esters, plasticizers such as glycerin and the like can be used as additives.
- Preparations suitable for parenteral administration include injections, suppositories, sprays and the like.
- Aqueous solutions for injection include, for example, isotonic solutions containing physiological saline, glucose and other adjuvants such as D-sorbitol, D-mannose, D-mannitol and sodium chloride.
- Suitable solubilizers such as Alcohols, specifically ethanol, polyalcohols such as propylene glycol, polyethylene glycol, nonionic surfactants such as polysorbate 80 (TM), HCO-50 may be used in combination.
- Suppositories can be prepared using a carrier such as cacao butter, hydrogenated fat or carboxylic acid.
- the propellant does not irritate any drug containing the above-mentioned single- or multi-stranded polynucleotide, or the recipient's oral cavity or airway mucosa, and contains the single- or multi-stranded polynucleotide.
- It can be prepared using a carrier that disperses any drug as fine particles and facilitates absorption.
- Specific examples of the carrier include lactose and glycerin.
- aerosols, dry powders, and the like it is possible to formulate aerosols, dry powders, and the like.
- the components exemplified as additives for oral preparations can also be added.
- the above therapeutic or prophylactic agents include buffering agents (eg, phosphate buffer, sodium acetate buffer), soothing agents (eg, benzalkonium chloride, procaine hydrochloride, etc.), stabilizers (eg, human Serum albumin, polyethylene glycol, etc.), preservatives (eg, benzyl alcohol, phenol, etc.), antioxidants, etc.
- buffering agents eg, phosphate buffer, sodium acetate buffer
- soothing agents eg, benzalkonium chloride, procaine hydrochloride, etc.
- stabilizers eg, human Serum albumin, polyethylene glycol, etc.
- preservatives eg, benzyl alcohol, phenol, etc.
- the administration method can be appropriately selected depending on the subject's age, symptoms, target organs and the like.
- the dosage of the pharmaceutical composition containing any one of the above-mentioned drugs containing one or more double-stranded polynucleotides can be selected, for example, in the range of 0.0001 mg to 1000 mg per kg body weight. is there. Alternatively, for example, the dose can be selected in the range of 0.001 to 100,000 mg / body per subject, but is not necessarily limited to these values.
- the dose per kg body weight is, for example, 0.0001, 0.01, 1, 50, 100, 250, 500, or 1000 mg. This dose may be within the range of any two values exemplified herein.
- the dose varies depending on the intended therapeutic effect, administration method, treatment period, age, weight, and the like.
- the dose and administration method vary depending on the weight, age, symptoms, etc. of the subject, but those skilled in the art can appropriately select them. It may also be administered in combination with an appropriate chemotherapeutic agent.
- the above single- or multiple-stranded polynucleotide can also be used as an additive for assisting animal growth in livestock through effects such as suppression of malignant cells.
- another embodiment of the present invention is a reagent or a kit containing the above single- or multiple-stranded polynucleotide.
- This reagent or kit can be used as a research reagent or kit, or a medical kit through the effects of the above single- or multiple-stranded polynucleotide.
- it can be used as an additive or auxiliary substance for iPS cell preparation, artificial organ preparation, malignant tumor cell suppression, undifferentiation marker expression regulation, or p53 expression cell preparation.
- the kit may also contain instructions describing how to use or use examples when using the above-mentioned single- or multiple-stranded polynucleotides, texts describing the location of the instructions, or various buffers. .
- Example 1 Administration of RGM249 shRNA to mice and evaluation of anticancer activity>
- (1-1) Creation of RGM249 shRNA The sequence of RGM249 shRNA was designed by Stealth RNAi designer (Invitrogen, CA, USA), and RGM249 shRNA was generated using BLOCK-it Inducible H1 RNAi Entry Vector (Invitrogen, CA, USA). A vector (RGM249 shRNA plasmid) was prepared. This RGM249 shRNA is a small RNA designed to induce RNAi against RGM249 mRNA in vivo.
- RGM249 mRNA nucleotide sequences are 5'-GGAAAACUAAAAUGAGAGAAUGGGUGUCCAAGAGGACAAGUUCAUGCUCACCCGGUGAUGAGAGUUUGAUUGCAGAAUAAGGCUAGACAAAGGGAAGCUGAACAUGACCAAAGCCAUGUGACAUCGUAUGAUCCUCGAAUCUCACAGUAUCUAUGUAUCUAUAAUCAGAUACAUCCCUAGACUUUCCAGGAAUUCUGGUACUUCACGAGGAUGUGAGAAGACUCUGAACAAAAUAAUACACUGCUCGUG-3 '(SEQ ID NO: 7).
- FIG. 1A shows the secondary structure of RGM249 RNA and the target site of RGM249 shRNA.
- the base sequence of RGM249 shRNA is 5′-GCAGAAUAAGGCUAGACAAAGUUCGCUUUGUCUAGCCUUAUUCUGCGGUG-3 ′ (SEQ ID NO: 10). It is thought that a hairpin-like structure is formed after transcription from the plasmid (FIG. 1B). The underlined portion in the figure is a portion capable of forming a hydrogen bond.
- the sequence complementary to a part of RGM249 mRNA is 5'-CUUUGUCUAGCCUUAUUCUGC-3 '(SEQ ID NO: 8).
- This part corresponding to SEQ ID NO: 8 is considered to form a hydrogen pin-like structure by forming a hydrogen bond with 5′-GCAGAAUAAGGCUAGACAAAG-3 ′ (SEQ ID NO: 9) in the base sequence of RGM249 shRNA.
- SEQ ID NO: 9 5′-GCAGAAUAAGGCUAGACAAAG-3 ′
- the part corresponding to SEQ ID NO: 8 is considered to hybridize to RGM249 mRNA.
- UUCG corresponds to the loop portion. GGUG seems to be overhanging.
- RGM249m-1 shRNA plasmid expressing RGM249m-1 shRNA lacking one of the thymines of RGM249 shRNA was prepared.
- the sequence encoding RGM249m-1 shRNA is 5'-CACCGCAGAATAAGGCTAGACAAAGCGAACTTTGTCAGCCTTATTCTGC-3 '(SEQ ID NO: 13).
- the sequence forming a duplex with the top strand is 5′-AAAAGCAGAATAAGGCTGACAAAGTTCGCTTTGTCTAGCCTTATTCTGC-3 ′ (SEQ ID NO: 14).
- LacZhshRNA was used as a control.
- the base sequence of RGM249m-1 shRNA is 5′-GCAGAAUAAGGCUGACAAAGUUCGCUUUGUCUAGCCUUAUUCUGCGGUG-3 ′ (SEQ ID NO: 15).
- the base sequence of SEQ ID NO: 15 differs from the base sequence of SEQ ID NO: 10 in that the 14th A from the 5th end of SEQ ID NO: 10 is deleted.
- the sequence partially complementary to RGM249 mRNA is the same as that of the above RGM249 shRNA.
- FIG. 1D The three photographs in FIG. 1D are the results of visual observation of the tumor volume when the above plasmids were injected subcutaneously. Approximately 28 days after subcutaneous injection, the RGM24924shRNA group showed an average 80% inhibitory effect. The RGM249m-124shRNA group suppressed tumor volume to less than 50% on average.
- DDS includes AteloGene TM (Jo, J., Yamamoto et al., J Nanosci Nanotechnol 6, 2853-2859 (2006)., Takeshita et al., Mol Ther 18, 181-187 (2010).) Was used. Plasmid and DDS were mixed at 100 ⁇ M each according to the manufacturer's protocol.
- RGM249 mRNA affects cancer through some mechanism.
- RGM249m-1 shRNA was slightly inferior to RGM249 shRNA, but had an effect similar to RGM249 shRNA, such as an effect of suppressing cancer.
- the miRNA produced from RGM249G mRNA and the effect of siRNA on the miRNA on cancer were examined.
- Example 2 Inhibition of cancer cell proliferation by three siRNAs and evaluation of influence on undifferentiated markers> (2-1) Constructs of miR-47 siRNA, miR-101 siRNA, miR-197 siRNA RGM249 was ligated to pRNAT-U6.1 / neo vector (GenScript USA, New Jersey, USA). RGM249 mRNA produced by T7 RNA polymerase was digested using the Dicer enzyme (Genlantis, California, USA). miRNA was fractionated by mirVANA miRNA isolation kit (Japan Ambion, Tokyo, Japan) and purified using miRNA isolation kit (Wako Pure Chemical Industries, Tokyo, Japan) using human anti-Ago2 beads .
- FIG. 3A shows RGM249 mRNA, which is a miRNA precursor gene, and sites corresponding to three internal miRNAs.
- the base sequence of miR-47 is 5'-CUCACCCGGUGAUGAGAGUUUGAUU-3 '(SEQ ID NO: 16)
- the base sequence of miR-101 is 5'-AACAUGACCAAAGCCAUGUG-3' (SEQ ID NO: 17)
- the base sequence of miR-197 is 5'- GUACUUCACGAGGAUGUG-3 ′ (SEQ ID NO: 18).
- siRNATin-H1.4 / Lenti When creating a construct (shRNA) that generates siRNA for the above three miRNAs, pRNATin-H1.4 / Lenti was used.
- three siRNAs (miR-47 siRNA, miR-101 siRNA, miR-197 siRNA) were synthesized using siRNA designer manufactured by Invitrogen.
- the predicted secondary structure of each siRNA is shown in FIG. 3B.
- the nucleotide sequence of miR-47 siRNA is 5′-CUCACCCGGUGAUGAGAGUUUGA-3 ′ (SEQ ID NO: 4) for the sense strand and 5′-AAUCAAACUCUCACCGGGUGAG-3 ′ (SEQ ID NO: 1) for the antisense strand.
- the nucleotide sequence of miR-101 siRNA is 5′-AACAUGACCAAAGCCCAUGUGUU-3 ′ (SEQ ID NO: 19) for the sense strand and 5′-CACAUGGCUUUGGUCAUGUU-3 ′ (SEQ ID NO: 2) for the antisense strand.
- thymine protrudes 2 bases at the 3 ′ end.
- the sequence excluding these 2 bases is 5′-AACAUGACCAAAGCCCAUGUG-3 ′ (SEQ ID NO: 5).
- the nucleotide sequence of miR-197 siRNA is 5′-GUACUUCACGAGGAUGUGUU-3 ′ (SEQ ID NO: 20) for the sense strand and 5′-CACAUCCUCGUGAAGUAC-3 ′ (SEQ ID NO: 3) for the antisense strand.
- thymine protrudes 2 bases at the 3 ′ end.
- the sequence excluding these 2 bases is 5′-GUACUUCACGAGGAUGUG-3 ′ (SEQ ID NO: 6).
- FIG. 3C A sequence comparison between the three miRNAs and the antisense strands of the three siRNAs is shown in FIG. 3C.
- c-Myc was down-regulated as with miR-47 siRNA.
- p53 a tumor suppressor gene
- the photograph shown at the bottom is a photograph when 3 siRNA mixture + DDS was injected subcutaneously. * Indicates that there is a significant difference (P ⁇ 0.01) between those not containing RNA and those containing siRNA. Control mice showed multiple nodules in the lung (15.8 ⁇ 1.9 nodules) and intraperitoneally (0.8 ⁇ 0.6 nodules) (Table 2). Several metastatic lesions were observed intraperitoneally and extraperitoneally, and subcutaneous infiltration was also observed.
- Example 4 Administration of 3 siRNA mixture to mouse and evaluation of expression level of undifferentiated marker> (4-1) Evaluation Method of miRNA and mRNA Expression Levels in Tumor Using the tumor treated with siRNA, the expression levels of miR-47, miR-101, and miR-197 were evaluated as follows. The expression level of miRNA was examined using Mir-X TM miRNA qRT-PCR SYBR (R) Kit after miRNA was extracted from cells or tissues using mirVana miRNA Isolation kit. This confirmed the miRNA expression inhibitory effect by siRNA and the change in miRNA expression level.
- Table 4 shows the sequences of the primer sets used for quantifying mRNA.
- Western blotting was performed using an i-Blot gel transfer system.
- Antibodies (anti-hTERT antibody, anti-p53 antibody, anti-c-Myc antibody, anti-Oct4 antibody, anti-PROM1 antibody) were diluted 1: 500 times, and anti- ⁇ -actin antibody was diluted 1: 1000 times.
- a chemiluminescent signal was detected within 1 minute using LAS-4000.
- HMV-I cells (1 ⁇ 10 7 cells) were injected into the tail vein of athymic mice one week before treatment with siRNA mixture (400 ⁇ M) or DDS.
- siRNA mixtures or DDS were administered weekly and tumor volume or metastasis was investigated after 5 weeks. All mice were stored and raised in Japanese Association for Accreditation for Laboratory Animal Care-approved facilities. Animal experiments and handling strictly adhered to the Federal Institutional Animal Care and Use Committee guidelines.
- FIG. 5C shows the results of microscopic investigation (HE (hematoxylin and eosin staining); ⁇ 400) of the tumor obtained in (4-1-2) above.
- the upper part shows a control, and the lower part shows a tumor treated with siRNA.
- Tumors treated with siRNA decreased in HMV-I cells, and necrosis and neovascularization were suppressed with replacement by fibrosis.
- Example 5 Reprogramming of cancer cells and evaluation of iPS cells> (5-1) Inhibition of miRNA-197 and evaluation of upregulation of hsa-mir-520d miR-197 siRNA was transfected into 293FT cells using a FuGene kit (Roche) and then observed under a microscope (FIG. 6A). Further, using a viral vector (pMIRNA1, System Bioscience: manufactured by SBI), hsa-mir-520d (Accession: MI0003164) was infected with human fibroblast cells (TIG-1-20), and then examined under a microscope. Observed.
- pMIRNA1 System Bioscience: manufactured by SBI
- This hsa-mir-520d is a miRNA that is up-regulated by transfection with RGM249 shRNA (A noncoding RNA gene on chromosome 10p15.3 may function upstream of hTERT. Miura et al., BMC Mol Biol. 2009 Feb 2; 10: 5.).
- the base sequence of hsa-mir-520d expressed from the above viral vector is 5′-UCUCAAGCUGUGAGUCUACAAAGGGAAGCCCUUUCUGUUGUCUAAAAGAAAAGAAAGUGCUUCUCUUUGGUUACGGUUUGAGA-3 ′ (SEQ ID NO: 43).
- the estimated secondary structure is shown in FIG. 6B.
- sequence corresponding to the guide strand is 5′-UCUACAAAGGGAAGCCCUUUCUG-3 ′ (SEQ ID NO: 41), and the sequence corresponding to the passenger strand is 5′-AAAGUGCUUCUCUUUGGUGGGU-3 ′ (SEQ ID NO: 42).
- the expression levels of miR-197 siRNA and hsa-mir-520d were evaluated by detecting the GFP protein expressed with each RNA chain.
- the upper part of FIG. 6A is a photograph of cells treated with miR-197 siRNA (magnification: ⁇ 40). After the round cells appeared in the medium, the cells were transferred to a medium for ES cells (ReproCELL) and observed.
- the lower part is a photograph of cells treated with hsa-mir-520d (magnification: ⁇ 100). From the above, the expression of miR-197 siRNA and hsa-mir-520d was confirmed. In this way, miRNA-197 was suppressed or hsa-mir-520d was up-regulated.
- FIG. 6C detects Oct4 and NANOG, which are undifferentiated markers.
- the upper three (0 hr) are photographs of non-transfected 293FT cells observed with a microscope (magnification: x40). The left column is the result of body staining, the middle column is the result of rhodamine staining with anti-Oct4 antibody, and the right column is the result of rhodamine staining with anti-NANOG antibody. Cells were stained for 1 week each.
- the middle three are photographs taken immunohistochemically with a microscope 24 hours after inducing undifferentiated cells with miR-197 siRNA.
- the lower three are photographs that were also observed immunohistochemically under a microscope after 48 hours.
- Oct4 mouse row, magnification factor: ⁇ 100
- NANOG right column, magnification factor: ⁇ 200
- 293FT cells treated with miR-197 siRNA expressed Oct4 or NANOG are reprogrammed and considered to be iPS cells.
- the efficiency was high, and about 20 to 100 iPS cells could be prepared from 10 6 cells.
- the 293FT cells had a cell shape generally found in ES cells and iPS cells.
- the undifferentiated state was maintained after 7 days in the medium.
- iPS cell-converted 293FT cells can be cultured in a culture solution for ES cells, but can be sufficiently cultured in a culture solution for general culture. No feeder cells were required and the culture surface coating could be either collagen or matrigel.
- Hsa-mir-520d was infected with various cancer cells with a viral vector (pMIRNA1, System Bioscience: manufactured by SBI) and forcedly expressed. It was. Thereafter, the expression level of the undifferentiated marker was observed in the same manner as in the above immunohistochemical test. The results are shown in FIGS. 6D, 6E, and 6F.
- the cancer cells used were HT1080 cells (human fibrosarcoma cell line), T98G cells (human glioma cell line), PK-45p cells (human pancreatic cancer-derived cell line), HMV-I cells (human malignant melanoma-derived cell line) ), HLF cells (human liver cancer-derived cell line).
- Oct4 or NANOG which is an undifferentiated marker, was expressed in HMV-I cells and HLF cells.
- the cancer cells treated with hsa-mir-520d were reprogrammed and turned into iPS cells.
- the cancer cells in which hsa-mir-520d was forcibly expressed had a cell shape generally found in ES cells and iPS cells.
- FIG. 7A shows the transcription amounts of various genes in the iPS cells generated as described above. The transcription amounts of various genes in 293FT cells treated with miR-197 siRNA and 293FT cells overexpressing hsa-mir-520d were the same.
- FIG. 7A shows the amount of transcription of the two cells as hiPSC (HPS0002 253G1) ('Generation of mouse-induced pluripotent stem cells with plasmid vectors.' Okita et al., Nat Protoc 5, 418-428 (2010)). It is the result compared with respect to the expression level. Transcription levels were investigated by one-step real-time RT-qPCR.
- the expression level of hiPSC is represented as 0.
- the upper part is the transcription amount 48 hours after transfection or infection of 293FT cells in the medium for 293FT cells.
- the lower part is the amount of transcription when maintained in the medium for ES cells for 2 weeks thereafter.
- the left panel shows the expression level of hsa-mir-520d. From left, 293FT cells overexpressing hiPSC and hsa-mir-520d, 293FT cells and 293FT cells treated with miR-197 siRNA.
- the right panel shows the expression level of miRNA-197. This confirmed miRNA-197 silencing and mir-520d overexpression in the transformants.
- the expression level of hsa-mir-520d in the generated iPS cells is similar to that of hiPSC.
- the expression level of hsa-mir-520d is significantly down-regulated in 293FT cells.
- the generated iPS cells express miRNA-197 as weakly as hiPSC.
- miRNA-197 was expressed 10 times more in 293FT cells than other cells.
- hsa-mir-520d (6-1) Cells
- 293FT a human mesangial cell line
- FBS FBS
- 0.1 mM MEM non-essential amino acid solution 2 mM L-glutamine
- penicillin / streptomycin Cultured in medium.
- HEF Human immature or undifferentiated hepatocyte cell line
- Huh7 well-differentiated hepatoma cell line
- RPMI medium supplemented with 10% FBS and 1% penicillin / streptomycin.
- ReproStem medium ReproCell, Tokyo, Japan
- HPS0001, HPS0002 Human induced pluripotent stem cells
- RGM249miRNA-197 siRNA used as a positive control was designed using Stealth RNAi designer (https://rnaidesigner.invitrogen.com/rnaiexpress/) and FuGENE HD transfection reagent (Roche Diagnostics, Basel , Switzerland) was used to transfect 50 nM synthetic oligonucleotides into 293FT cells.
- 2M purmorphamine was added to normal RPMI1640 medium and the cells were treated for one week.
- RNA containing the small RNA fraction was extracted from cultured cells or homogenized mouse tissue using the mirVana miRNA isolation kit (Ambion, Austin, USA). Quantification of mature miRNAs was performed using the Mir-X TM miRNA qRT-PCR SYBR® kit (Clontech, Mountain View, USA) according to the manufacturer's manual (Clontech). U6 small nuclear RNA was used as an internal control.
- Total RNA (50 ng / ⁇ l) was reverse transcribed and amplified using the OneStep RT-PCR kit (QIAGEN Japan, Tokyo, Japan). PCR analysis and data collection analysis were performed using LineGene (Toyobo, Nagoya, Japan).
- the expression level of the sample was determined using the standard curve method (2- ⁇ method). All data (except for hTERT) was normalized to the internal control ⁇ -actin. hTERT was estimated by copy number according to the quantitative method previously developed by the present inventor.
- the RNA quantification was confirmed with high reproducibility by sequencing. miRNA (25 ng / ⁇ l) was quantified using the Mir-X miRNA qRT-PCR SYBR kit (Takara Bio Inc., Tokyo, Japan). In order to confirm suppression by siRNA, miRNA expression change was evaluated. Table 4 shows primer sequences for mRNA or miRNA quantification. Significant differences were shown as *: P ⁇ 0.05, **: P ⁇ 0.01.
- liver tissue specimens fixed in 4% paraformaldehyde were processed by a conventional method.
- the monoclonal antibodies used in this study are: anti-albumin antibody (Sigma, St. Louis, USA), anti-AFP antibody (Sigma), and anti-GFAP antibody (Sigma).
- anti-albumin antibody Sigma, St. Louis, USA
- anti-AFP antibody Sigma
- anti-GFAP antibody Sigma
- the DNA content was analyzed by a flow cytometer (EPICS ALTRA; Beckman Coulter) equipped with EXPO32 ADC analysis software. DNA content was assessed at approximately 20000 events after transfection with the pMIRNA1-mir-520d / GFP clone. GFP positive cells were sorted (sorted) using a Moflo XDP cell sorter (EPICS ALTRA, Beckman Coulter).
- Tumor volume and metastatic cancer to lung, liver, intraperitoneal and retroperitoneal cavity were examined and measured under a dissecting microscope equipped with bright field imaging function or with the naked eye.
- Tissue samples were fixed overnight in 10% buffered formalin solution, washed with PBS and transferred to 70% ethanol. Thereafter, it was embedded in paraffin, sliced, and stained with hematoxylin and eosin.
- FIG. 8A shows a floating cell population that emerged after virus introduction of has-mir-520d into 293FT cells.
- GFP positive suspension cells FIG. 8A (a)
- FIG. 8A (c) the growth process of transfectants having GFP expression was observed in a time-lapse mode.
- 293FT cells virus-infected with has-mir-520d formed a sheet-like layer within 24 hours. Stemization conversion was confirmed based on immunocytochemistry (FIG. 8B).
- GFP positive cells were strongly stained with anti-Oct4 antibody.
- Transfectant gene expression was assessed by RT-PCR, Western blot, and quantitative miRNA RT-PCR.
- 293FT 520d-293FT
- 293FT 520d-293FT
- p53, RGM249, and Oct4 were more strongly upregulated, whereas hTERT was expressed at the same level (FIG. 9A).
- p53 and Oct4 were more strongly transcriptionally up-regulated in 520d-293FT in a floating state. hTERT was expressed equally.
- has-mir-520d resulted in downregulation of RGM249 miRNA-197 (Fig. 9D).
- 293FT stably expressed mir-520d in either adherent or suspension cells in the medium. Viral infection efficiency was greater than 99.2% as determined using GFP positive cell sorting (data not shown). This also suggests that these are materials that can be adapted for in vivo.
- 520d-293FT increased in G0 phase and decreased in S phase compared to 293FT and mock virus-infected 293FT (mock-293FT) (FIG. 10A).
- HDAC histone deacetylase
- Sin3A histone deacetylase
- MBD3 methyl-CpG binding domain protein 3
- DNMT 1 DNA (cytosine-5-)-methyltransferase) was comparable to that in 293FT or mock-293FT (FIG. 10B).
- FIG. 11A shows the morphological changes. These cells expressed GFP (upper right) and pluripotency markers (lower right). Among them, Oct4 and NANOG were transcriptionally upregulated. In contrast, RGM249, CD44, Alb, and p53 were significantly downregulated (**: P ⁇ 0.01; FIG. 11B). In the invasion assay, most of the pluripotent marker positive cells were unable to migrate through the fibronectin membrane (5 ⁇ g / ml per 6-well plate).
- FIG. 11C Western blot showed upregulation of Oct4 and p53.
- DICER1 was suppressed in has-mir-520d-expressing HLF (520d-HLF) cells (FIG. 11D).
- methylation markers HDAC, Sin3A, and MBD3
- FIG. 11B Cell cycle analysis showed that 520d-HLF cells had increased S phase and decreased G0 phase compared to mock-HLF (FIG. 12A).
- Oct4 and NANOG expression in small round cell populations was more elevated compared to induction with mock vectors.
- 520d-HLF cells were induced into osteoblasts having upregulation of ALP, SPP1, and IBSP by addition of 2 ⁇ M purmorphamine.
- FIG. 13 is a graph for examining the reprogramming level in the case of HLF cells.
- AID and DNMT1 were found, and HDAC, Sin3A, and MBD3 significantly increased expression in 293FT, whereas their expression decreased significantly in HLF.
- mice 520d-HLF cells in 12.5% (1/8) group of mice have (hepatic cell cord, central vein, bile duct (right figure; white arrow), partially with adenoma-like hyperplasia inside ( FIG. 14D) (second diagram from the right)) transformed into normal liver tissue (FIG. 14C, lower panel: HE-stained tissue specimen).
- HLF cells consist of epidermoid cysts with epidermis, sweat glands (left figure; white arrows) ( Figures 14A, 14D, and 14C upper figures; HE-stained tissue specimen), and sebaceous glands ( It was transformed into a teratoma consisting of the second from the left; white arrow).
- the generated teratoma and liver tissue expressed GFP protein (FIG. 14E) (left: HE and right: GFP). It was confirmed by immunohistochemical staining that almost all hepatocytes in the liver tissue strongly expressed human albumin. Glial fibrillary acidic protein (GFAP) and alphafetoprotein (AFP), markers of hepatic stellate cells (HSC) / myofibroblasts (MFs), were weakly expressed. This suggests that within a month, 520d-HLF cells differentiated into immature liver tissue. 50% (4/8) did not form any tumor or specific tissue.
- GFAP Glial fibrillary acidic protein
- AFP alphafetoprotein
- HSC hepatic stellate cells
- MFs myofibroblasts
- FIG. 17 shows the results of evaluation of well-differentiated liver cancer (Huh7) cells. Regardless of the degree of differentiation, hepatic cancer cells were equally able to change to a strong positive pluripotency marker.
- FIG. 18 shows the results of evaluation on glioblastoma multiforme (T98G) cells. Stem induction was also induced in undifferentiated brain tumors, and the tumors did not form in vivo and engrafted in normal tissues.
- FIG. 19 shows the results of evaluation of pancreatic cancer (PK-9) cells. Stem induction was also observed in pancreatic cancer.
- FIG. 20 shows the results of evaluation of fibrosarcoma (HT1080) cells. A sarcoma cell (HT1080), which is a non-epithelial malignant tumor, was also stemmed and differentiated into adipocytes.
- Example 7 Experimental method and results concerning hsa-mir-192 siRNA, etc.> (7-1) Cells HMV-I (human malignant melanoma) T98G (human glioblastoma) HT1080 (human fibroblastoma) Pk-45 (human liver cancer)
- siRNA SiRNA (hsa-mir-192 siRNA, hsa-mir-196a-1 siRNA, hsa-mir-423-3p siRNA, has-mir-222 siRNA) against the miRNAs in Table 5 were obtained from Stealth RNAi designer (Invitrogen). did. The sequence is shown in Table 6. After confirming that these siRNAs have effects such as cell growth inhibition, experiments were conducted to verify whether the above-mentioned shRNA of (7-3) has further effects such as cell growth inhibition. It was.
- Table 7 shows the sequence of the portion complementary to the sequence of the miRNA. This complementary part is considered to be a particularly important part in the action of RNAi or miRNA. Further, the sense strand sequence complementary to that portion is also shown.
- siRNA co-infection Three types of siRNA (has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA) co-infection or four types of siRNA (hsa-mir-192 siRNA / has-mir -196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA) co-infection was carried out at a titer at which one type of virus particle acts effectively.
- RNA miRNA and totalRNA were extracted using mirVana (tm) miRNA Isolation Kit (Ambion, TX, USA).
- Torizol Reagent (Life Technologies Carlabad, CA, USA) was added to the washed cells. After incubation for 3 minutes, 1/5 amount of chloroform (Nippon Gene, Tokyo, Japan) of Torizol Reagent was added. After shaking for 15 seconds, centrifugation was performed at 14,000 rpm for 15 minutes. 1/10 volume of 100% ethanol of the obtained supernatant was added, mixed by inverting several times, put into a spin column, and centrifuged at 10,000 g for 15 seconds.
- FIG. 22 Fluorescence micrograph and growth curve of HMV-1 2 weeks after siRNA-producing Lentivirus infection The introduction by infection with each siRNA-producing virus inhibited miRNA expression. Moreover, the time-dependent change which shows cell growth suppression was shown (FIG. 22).
- the top panel in the figure is a fluorescence micrograph for GFP detection with mock and hsa-mir-196a-1 / hsa-mir-423-3p / hsa-mir-222 after one week.
- the bottom panel in the figure is the growth curve of HMV-1 after virus infection.
- siRNA Compared with control, mock, hsa-mir-192, hsa-mir-196a-1 siRNA, hsa-mir-222 siRNA, there are 3 types of siRNA (has-mir-196a-1 siRNA / has-mir-423- (3p siRNA / has-mir-222 siRNA) Co-infection or 4 types of siRNA (hsa-mir-192 siRNA / has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA) Significant growth inhibition was observed with co-infection, and infected cells reached apoptosis within 3 weeks.
- antagomer small RNA targeting miRNA
- Invitrogen Step 1 RNAi designer (https://rnaidesigner.invitrogen.com/rnaiexpress/)) and GenScript (pRNATin-H1) .4 / Lenti, pRNAT-T6.1 / neo).
- the shRNA-generating vector was prepared according to the protocol using BLOCK-it Inducible H1 RNAi Entry Vector (Invitrogen, CA, USA).
- HLF cell line and HMV-I cell line were purchased from American Type Culture Collection and Tohoku University, respectively, and cultured in RPMI medium supplemented with 10% FBS and 1% penicillin / streptomycin.
- HMV-1 cells were incubated with 50 nM antagomir.
- RNAi HLF or HMV-I cells were transfected with 50 nM siRNA, control oligonucleotide, or empty vector using FuGene HD transfection Reagent (Roche Diagnostic GmbH).
- Dicer enzyme was purchased from Genlantis and used according to the protocol.
- Three miRNAs were obtained by cloning digested with Dicer using miRCAT-microRNA cloning kit (Integrated DNA Technologies).
- Immunodeficient mice were obtained from Charles River from CAnN Cg-Foxn1 BALB / c-nu, SHIMIZU Laboratory Supplies Co., Ltd. Purchased KSN / Slc from
- RNA and small RNA fractions were extracted from cultured cells or homogenized mouse tissues using mirVana miRNA Isolation Kit (Ambion). maturation of miRNA quantitation was performed according to the instructions with reference to Mir-X TM miRNA qRT-PCR SYBR (R) kit (Takara Bio Company). U6 small nuclear RNA was used as an internal control.
- Immunoblotting Western blot analysis was performed using i-Blot gel transcription system (Invitrogen). Each antibody against the target biomarker gene was used at a dilution rate according to the manufacturer's manual. 20 ⁇ g of cell extract was tested.
- antagomir was excreted in the late stage of the metastatic process.
- tumor cells were implanted via the tail vein or subcutaneously in athymic mice.
- antagomir treatment was started at the same dose and frequency as used in the orthotopic experiment. Mice were moribund on day 30 and euthanized by systemic metastases when administered intravenously or by liver or intraperitoneal metastases when given subcutaneously.
- mice were divided into 5 mice per group, and PBS + DDS or 50 ⁇ M antagomer was intravenously administered once a week for 6 times over 4-5 weeks. Body weight was measured once every two weeks. Mice were euthanized 6 days after the last dose and tissues were collected. An aliquot of whole blood was collected in a tube treated with EDTA. Blood cells were removed by centrifugation to obtain plasma. Samples were analyzed using an Olympus Bioanalyzer to determine blood biochemical values. Lung or liver sections were examined for all possible pathological conditions.
- HiPSC Human-induced pluripotent stem cells
- HiPSC HPS0002 253G1
- a human induced pluripotent stem cell is a Riken Bioresource Center Cell Bank ('Generation of induced pluripotent stem cells without Myc from mouse and human fibroblasts.' Nakagawa M et al., Nat Biotechnol 26, 101-106 ( 2008)).
- Pluripotent stem cells prepared by introducing miR-197 siRNA or hsa-mir-520d can be cultured in a culture medium for ES cells, but F-12 HAM [DMEM (15 mM HEPES + 1 mM Sodium Pyruvate + pyridoxine + NaHCO 3 3 +5 mM L-glutamine)], RPMI-1640 + L-glutamine, DMEM + high glucose + L-glutamine + 0.1 mM NEAA and REPROSTEM (REPROCell): one or more selected from the group consisting of bFGF 3-10 ng / ml In the medium of 37 ° C., 5% CO 2 , 10% FBS.
- F-12 HAM DMEM (15 mM HEPES + 1 mM Sodium Pyruvate + pyridoxine + NaHCO 3 3 +5 mM L-glutamine
- RPMI-1640 + L-glutamine DMEM + high glucose + L-glutamine
- Flow cytometry was performed on cells separated and detached by trypsin using 293FT cells transfected with siRNA corresponding to miRNA-197. Single cell suspensions were washed once with chilled PBS. The cell pellet was then loosened by gently shaking the tube and fixed by dropwise addition of cold 70% EtOH in ddH2O. Cells were incubated at ⁇ 20 ° C. for at least overnight. After fixation, the cells were washed twice with chilled PBS to remove EtOH. The cells were then resuspended at 1 ⁇ 10 6 cells / ml in PBS containing 100 U / ml RNAase A and incubated at 37 ° C. for 50 minutes.
- iPS cells were evaluated at approximately 20000 events after siRNA-197 transfection using a flow cytometer equipped with EXPO32 ADC analysis software.
- phosphate buffer (PBS) supplemented with% FCS.
- GFP-positive cells or PE-positive cells were sorted and analyzed using Moflo XDP (Beckman Coulter, California, USA). 1 ⁇ 10 8 cells were analyzed for forward scatter, side scatter, and PE and GFP fluorescence using an argon laser (488 nm, 100 mW). As detectors, FL1 was used for GFP and FL2 for PE, respectively.
- Intracranial injection method An immunodeficient mouse was anesthetized with pentobarbital sodium (50 mg / kg, intraperitoneal injection) and placed in a stereotaxic apparatus. During surgery, the animal's body temperature was maintained at 37 ° C using a heating pad. The skull was exposed and a small craniotomy was made on the left striatum. A 30G needle connected to a 10 ⁇ l Hamilton syringe via a polyethylene tube was used for cell transplantation. Insert the needle into the left striatum stereotaxically (from Bregma A (front) 0.5 mm, L (lateral) 2.0 mm, D (depth) 2.5 mm), and 5 ⁇ l of cell suspension (10 8 Cells / ⁇ l) were pressure injected. After injection, the needle was slowly withdrawn and the skull hole was covered with dental cement. The incision was sutured using 6-0 Prolene. After recovery from surgery, the animals were returned to their original cages.
- pentobarbital sodium 50 mg / kg, intraperi
- RGM249 shRNA has an effect of suppressing the growth of malignant tumors, suppressing the metastasis of malignant tumors, suppressing the amount of intracellular RGM249 mRNA, or suppressing the amount of intracellular hTERT mRNA.
- the three siRNAs also inhibit malignant tumor growth, malignant tumor metastasis, intracellular three miRNA levels, undifferentiated marker up-regulation, p53 up-regulation, or normal or malignant tumor cell re-regulation. It was shown to have a programming effect.
- hsa-mir-520d was shown to have effects such as upregulation of undifferentiated markers, upregulation of p53, or reprogramming of normal cells or malignant tumor cells, growth inhibition of malignant tumors, and the like. Similar effects were also observed for hsa-mir-192 siRNA and the like. The suppression of malignant tumors seen in mice is thought to be due to reprogramming of malignant tumor cells. Moreover, not only undifferentiated but also well differentiated hepatoma cells became Oct4-positive and NANOG-positive cells, and a stemizing effect independent of the differentiated type was observed.
- the RGM249 shRNA and the three siRNAs have a common function in that they block the cascade starting from the RGM249 mRNA, and this function is involved in the effects of the malignant tumor suppression and malignant tumor cell reprogramming. It is thought that there is. It is considered that hsa-mir-520d is up-regulated at this time. Based on the above, it is considered that RGM249 shRNA, three siRNAs, hsa-mir-520d, hsa-mir-192 siRNA and the like can all be suitably used for malignant tumor treatment.
- these small RNAs can be suitably used as an inducer for inducing cells into pluripotent stem cells inside or outside the body, or as a reagent for producing pluripotent stem cells.
- conventional pluripotency in that no oncogene is used, malignant tumor cells can be reprogrammed, single agent can be reprogrammed, p53 up-regulation occurs, or feeder cells are not required during culture. It is believed to have properties superior to those compounds that have been studied to produce stem cells.
- the tumoration of the cells into which the small RNA was introduced occurred when the undifferentiated maintenance environment was maintained after the introduction, and the tumor was unlikely to occur in vivo. Therefore, it is preferable to use for treatment within one week after introduction of small RNA into cells.
- RGM249GshRNA, three siRNAs, and hsa-mir-520d are each composed of a single strand of hairpin-like structure, a single strand of double strand, and a single strand of pre-miRNA-like structure. This suggests that the secondary structure when siRNA or miRNA functions is not necessarily fixed, and a certain range can be tolerated.
- siRNAs hsa-mir-520d, or hsa-mir-192 siRNA are considered to silence the target RNA strand by the action of RNAi or miRNA.
- the three siRNA sense strands SEQ ID NO: 4, SEQ ID NO: 5, or SEQ ID NO: 6) and the antisense strand (SEQ ID NO: 1, SEQ ID NO: 2, or SEQ ID NO: 3) , Hsa-mir-520d (SEQ ID NO: 43), hsa-mir-192 siRNA, etc. (SEQ ID NO: 44, etc.)
- SEQ ID NO: 44 etc.
Abstract
Description
上記文献においてiPS細胞の作成方法が徐々に明らかになってきているが、より効率的に、より高品質のiPS細胞を開発するには、新しい作成方法を明らかにし、iPS細胞に関する情報を蓄積していく必要があった。
本発明の一実施形態は、配列番号1の塩基配列を含む1または複数本鎖のポリヌクレオチドである。この1または複数本鎖のポリヌクレオチドは、後述する実施例で細胞を多能性幹細胞に誘導することが示唆されている。そのため、この1または複数本鎖のポリヌクレオチドは、細胞を多能性幹細胞へ誘導するために好適に使用できる。
他の実施形態は、配列番号2の塩基配列を含む1または複数本鎖のポリヌクレオチドである。この1または複数本鎖のポリヌクレオチドは、後述する実施例で細胞を多能性幹細胞に誘導することが示唆されている。そのため、この1または複数本鎖のポリヌクレオチドは、細胞を多能性幹細胞へ誘導するために好適に使用できる。
他の実施形態は、配列番号3の塩基配列を含む1または複数本鎖のポリヌクレオチドである。この1または複数本鎖のポリヌクレオチドは、後述する実施例で細胞を多能性幹細胞に誘導することが示唆されている。そのため、この1または複数本鎖のポリヌクレオチドは、細胞を多能性幹細胞へ誘導するために好適に使用できる。
他の実施形態は、配列番号7の塩基配列を含むRNA鎖を、ダイサーで処理して得られるRNA鎖に対して相補的な塩基配列(以下、「ダイサー処理後の相補的な塩基配列」と称することもある)を含む、1または複数本鎖のポリヌクレオチドである。上記のダイサー処理後の相補的な塩基配列は、後述する実施例に記載されているmiR-47 siRNA、miR-101 siRNA、miR-197 siRNAのいずれかのガイド鎖の塩基配列を含む。ガイド鎖は、miR-47 siRNA等の機能を特徴付けていると考えられる部位である。
他の実施形態は、配列番号8の塩基配列を含む1または複数本鎖のポリヌクレオチドである。この1または複数本鎖のポリヌクレオチドは、後述する実施例においてRGM249 mRNAから始まるカスケードを阻害することで、細胞を多能性幹細胞に誘導することが示唆されている。そのため、この1または複数本鎖のポリヌクレオチドは、細胞を多能性幹細胞へ誘導するために好適に使用できる。または、未分化細胞マーカーの発現を調節するために好適に使用できる。または、この1または複数本鎖のポリヌクレオチドは、多能性幹細胞のp53の発現量を促進するために好適に使用できる。
他の実施形態は、配列番号7の塩基配列を含むRNA鎖に対してRNAi作用を有する1本鎖または2本鎖のポリヌクレオチドである。この1または複数本鎖のポリヌクレオチドは、後述する実施例においてRGM249 mRNAから始まるカスケードを阻害することで、細胞を多能性幹細胞に誘導することが示唆されている。そのため、この1または複数本鎖のポリヌクレオチドは、細胞を多能性幹細胞へ誘導するために好適に使用できる。または、この1または複数本鎖のポリヌクレオチドは、未分化細胞マーカーの発現を調節するために好適に使用できる。または、この1または複数本鎖のポリヌクレオチドは、多能性幹細胞のp53の発現量を促進するために好適に使用できる。
他の実施形態は、配列番号41、または44~47の1つ以上の塩基配列を含む1または複数本鎖のポリヌクレオチドである。この1または複数本鎖のポリヌクレオチドは、上述したような配列番号1、2、3、または8の塩基配列を含む1または複数本鎖のポリヌクレオチドの有する効果と、同様の効果を発揮しうることが、後述する実施例で示唆されている。そのため、多能性幹細胞誘導剤、未分化細胞マーカー発現調節剤、多能性幹細胞のp53発現促進剤、悪性腫瘍の治療薬、siRNA(またはmiRNA)もしくはshRNA(またはpre-miRNA)、またはベクターの用途に使用できる。なお、配列番号41の塩基配列を含む1または複数本鎖のポリヌクレオチドは、その相補鎖、または配列番号42の塩基配列を含むポリヌクレオチドをさらに含んでいても良い。また、配列番号41の塩基配列を含む1または複数本鎖のポリヌクレオチドは、配列番号43の塩基配列を含む1本鎖のポリヌクレオチドであってもよい。また、配列番号44~47の塩基配列を含む1または複数本鎖のポリヌクレオチドは、その相補鎖、またはそれぞれ配列番号48~51の塩基配列を含むポリヌクレオチドをさらに含んでいても良い。また、配列番号44~47の塩基配列を含む1または複数本鎖のポリヌクレオチドは、それぞれ配列番号52~55もしくはそれぞれ56~59の塩基配列を含む1または複数本鎖のポリヌクレオチドであってもよい。
他の実施形態は、上記のいずれかの1または複数本鎖のポリヌクレオチド、または上記のいずれかのベクターが導入された細胞である。この細胞は多能性が誘導されているため、再生医療等の医療材料や研究材料として好適に使用できる。
他の実施形態は、上記のいずれかの1または複数本鎖のポリヌクレオチドを、細胞に導入する工程を含む、多能性幹細胞の生産方法である。又は、上記のいずれかのベクターを、細胞に導入する工程を含む、多能性幹細胞の生産方法である。この方法を適切に用いれば、多能性幹細胞を生産することができる。なおポリヌクレオチドまたはベクターの細胞への導入、および培養方法は、当該技術分野で公知の方法に従って行うことができる。細胞への導入は、例えば、リン酸カルシウム法、リポフェクション法、エレクトロポレーション法、ウイルス(アデノウイルス、レトロウイルス、HIV等)を用いた方法、またはマイクロインジェクションなどを使用できる[改訂第4版 新 遺伝子工学ハンドブック, 羊土社(2003):152-179.]。また薬剤耐性やセルソーター等を利用して、導入された細胞のみを選択することができる。培地は、例えば、霊長類ES細胞用培地(コスモ・バイオ社)や通常のヒト細胞用の培地(例えば、DMEMやRPMIベースの培地)等を使用できる。一般的にES細胞を樹立する際にはフィーダー細胞と共培養することが多いが、本実施形態の多能性幹細胞はフィーダー細胞の非存在下でも樹立可能である。フィーダー細胞は、例えばEuropean Collection of Cell Culturesより入手できる。さらに、本実施形態の多能性幹細胞は、いずれもF-12 HAM[DMEM(15mM HEPES+1mM Sodium Pyruvate+pyridoxine+NaHCO3+5mML-glutamine)], RPMI-1640+L-glutamine, DMEM+high glucose+L-glutamine+0.1mM NEAA および REPROSTEM(REPROCell社):bFGF 3-10ng/mlからなる群から選ばれる1種以上の培地で37℃、5% CO2、10% FBSの条件で培養可能である。そのため、いわゆるiPS細胞の有する培養上の困難性を克服することにも成功している。
ここで、上記の配列番号1~10、および41~59の塩基配列は、ある程度であれば変異を受けていてもよい。そのような変異を有している塩基配列を含む1または複数本鎖のポリヌクレオチドは、野生型の塩基配列を含む1または複数本鎖のポリヌクレオチドと同様の効果を有すると考えられる。変異型の塩基配列を含むポリヌクレオチドは、人工的に作成することが可能であり、その場合には改変型の塩基配列を含むポリヌクレオチドと呼ぶこともできる。
本明細書において「多能性幹細胞」とは、多能性を有しており、様々な細胞へ分化することができる細胞である。例えば、国際公開第2007/069666号や、文献[Hong et al., Nature. 2009 Aug 27;460(7259):1132-5. Epub 2009 Aug 9.]に生産方法や特性の例が記載されている。また、多能性幹細胞は当業者であれば認識できるが、例えば、ヒト人工多能性幹細胞であるhiPSC(HPS0002 253G1)に比べて、いずれかの未分化マーカーを同程度かそれ以上発現している細胞を含む。
(1-1)RGM249 shRNAの作成
Stealth RNAi designer(Invitrogen, CA, USA)によってRGM249 shRNAの配列をデザインし、BLOCK-it Inducible H1 RNAi Entry Vector (Invitrogen, CA, USA)を用いてRGM249 shRNAを生成するベクター(RGM249 shRNAプラスミド)を作成した。このRGM249 shRNAは、生体内においてRGM249 mRNAに対するRNAiを誘導するように設計されたsmall RNAである。
胸腺欠損マウスの右側腹に、HLF細胞を皮下注射によって播種した。またそのマウスの右側腹に、5日毎にRGM249 shRNAプラスミド+DDS、RGM249m-1 shRNAプラスミド+DDS、またはLacZ shRNAプラスミド+DDSを皮下注射した。この皮下注射は、DDS1mg当たり数μg~数十μgの生理活性物質を混ぜ、マウス20~30gに対して行った。このときの腫瘍ボリュームの変化を調査した(図1C)。その結果、投与から21日後、LacZ shRNAグループと比較してRGM249 shRNAグループによる有意な腫瘍抑制効果が見られた。なお、DDS(Drug Delivery System)としてはカチオン化ゼラチンハイドロゲル(MedGel社製)を使用した。プラスミドとDDSは、メーカーのプロトコールに従い各100nMで混合した。グラフには標準誤差を示してある。データ(n=5)はマン・ホイットニーテストによって分析した(P<0.01)。また、最初の投与から4週間後、RGM249 shRNAグループは、RGM249-m1 shRNAグループとLacZ shRNAグループに比較して、有意に腫瘍抑制効果を示した(P=0.034、P=0.021)。
(1-3-1)皮下投与
また皮下注射から35日後に、腫瘍で発現している遺伝子の発現抑制効果を調査した(図2A)。細胞からmirVana miRNA Isolation kitを用いてmiRNAを抽出した後、Mir-XTM miRNA qRT-PCR SYBR(R) Kitを用いてmiRNAの発現量を調べた。その結果、RGM249 shRNAプラスミド+DDS、またはRGM249m-1 shRNAプラスミド+DDSを投与した場合において、RGM249 mRNAおよびhTERT mRNAの発現レベルが、LacZ shRNAと比較して有意に低下していた(RGM249 mRNAとhTERTmRNAのP値は、それぞれP=0.036、P=0.025)。これらのデータはマン・ホイットニーテストによって分析した。クローズドの四角はRGM249の発現を示し、オープンの四角はhTERT mRNAの発現を示す。
一方で、上記のそれぞれのプラスミドを尾静脈へ静脈注射した場合において、28日後に腫瘍で発現している遺伝子の発現抑制効果を調査した(図2B)。DDSには、アテロコラーゲン(AteloGeneTM)(Jo, J., Yamamoto et al., J Nanosci Nanotechnol 6, 2853-2859 (2006).、Takeshita et al., Mol Ther 18, 181-187 (2010).)を用いた。プラスミドとDDSは、メーカーのプロトコールに従い各100μMで混合した。その結果、RGM249 shRNAプラスミド+DDSを投与した場合において、RGM249 mRNAおよびhTERT mRNAの発現レベルが、LacZ shRNAと比較して有意に低下していた。これらのデータはマン・ホイットニーテストによって分析した(P<0.05)。クローズドの四角はRGM249の発現を示し、オープンの四角はhTERT mRNAの発現を示す。以上のように、RGM249 shRNAグループにおけるRGM249 mRNAとhTERT mRNAの発現は、LacZ shRNAグループと比較して、両方とも有意に抑制された(それぞれP=0.049、0.046)。
また静脈注射から28日後に、肝臓の内外の結節を目視的に観察した。HLF細胞のみのグループ(data not shown)と、LacZ shRNAグループにおいて癌結節が目視的に見られた。また、顕微鏡でみた場合、全てのマウスの肝臓または肺に転移性の病巣が、1匹のマウスで左腎への転移が見られた。
(2-1)miR-47 siRNA、miR-101 siRNA、miR-197 siRNAのコンストラクト
RGM249を、pRNAT-U6.1/neoベクター(GenScript USA社、ニュージャージー、米国)に連結した。T7 RNAポリメラーゼにより生成されたRGM249 mRNAを、Dicer酵素(Genlantis社、カリフォルニア、米国)を使用して消化した。miRNAを、mirVANA miRNA単離キット(日本Ambion社、東京、日本)により分画し、 ヒト抗Ago2ビーズを用いたmiRNA単離キット(和光純薬工業株式会社、東京、日本)を用いて精製した。また、小RNAがAgo2に結合しない可能性があるため抗Ago2を用いずにも精製した。消化したsmall RNAsを、miRCAT-microRNAクローニングキット(Integrated DNA Technologies社、アイオワ、米国)を使用してクローニングし、TOPOベクター(Invitrogen社、カリフォルニア、米国)を使用してシークエンシングした。そして、二次構造を予測した(http://rna.tbi.univie.ac.at/cgi-bin/RNAfold.cgi)。small RNAsの配列相同性を、miRBasを使用して検討した。以上の結果、miR-47、miR-101、miR-197の3つのmiRNAが得られた。miRNA前駆遺伝子であるRGM249 mRNAと、内部の3つのmiRNAに相当する部位を図3Aに示す。
miR-47 siRNA、miR-101 siRNA、miR-197 siRNA、またはそれらの混合物(3siRNA混合物)各50nMを高レベルのRGM249を発現するHMV-Iへトランスフェクションした。トランスフェクションにはFuGeneキット(Roche社製)を使用した。トランスフェクションから24時間経過後の形質転換体を収集した。
上記(2-2)において3siRNA混合物を同時にトランスフェクションしたHMV-IからRNA抽出を行い、miR-47、miR-101、miR-197の発現レベルを調査した(図3E)。
形質転換体の転写発現プロファイリングを、癌(hTERT、c-Myc、p53)、多分化能(Oct4、Sox2、Klf4)、幹細胞性(PROM1)に関連する遺伝子について評価した(図3F)。3siRNA混合物を使用した場合、Oct4、Sox2、hTERT、p53遺伝子は3siRNA混合物による処理に伴いアップレギュレイトし、c-MycとKlf4遺伝子はダウンレギュレイトした。一方でPROM1への影響は見られなかった。またmiR-47 siRNAは、Oct3/4およびhTERT遺伝子をアップレギュレイトし、c-MycおよびKlf4遺伝子をダウンレギュレイトした。図3D中の*は、mRNAの発現をβ-actin mRNAと比較した時に有意差があることを示す。
(3-1)siRNAの皮下投与
3siRNA混合物+DDSの皮下投与は、DDSのみのコントロール投与に比べて、HMV-I細胞の増殖性の抑制を示した(Kruskal-WallisテストにおいてP<0.01、n=5)(図4)。この試験には胸腺欠損マウスを用いた。DDSはアテロコラーゲン(AteloGeneTM)を用いた。3siRNA混合物とDDSは、メーカーのプロトコールに従い各100μMで混合した。図4中の上部に示した写真は、RNAを含まないアテロコラーゲン(mock)を皮下注射したときの写真である。下部に示した写真は、3siRNA混合物+DDSを皮下注射したときの写真である。*はRNAを含まないものとsiRNAを含むものの間に有意差(P<0.01)があることを示す。また、コントロールマウスは肺(15.8±1.9 結節)と腹腔内(0.8±0.6 結節)に複数の結節を示した(表2)。いくつかの転移性の病巣が腹腔内および腹腔外で観察され、皮下浸潤も観察された。
胸腺欠損マウスにHLF細胞を投与した後1週間後から、3siRNA混合物+DDSを毎週静脈注射した。マウス当たりに1×107細胞を含む200 μlをインジェクションした。DDSはアテロコラーゲン(AteloGeneTM)を使用した。3siRNA混合物とDDSは、メーカーのプロトコールに従い各100μMで混合した。28日後にその動物を屠殺し、肝内腫瘍と腹腔内転移の試験を行なった(表3)。この結果、3siRNA混合物+DDSの静脈投与は、HMV-1細胞の抗転移能を有意に誘導した(P<0.05、肺と肝臓それぞれ)。肝臓と肺では転移がほとんど見られず、1匹のマウスのみで腹腔内への転移が見られた。
(4-1)腫瘍におけるmiRNAとmRNAの発現レベルの評価方法
siRNAで処理した腫瘍を用いてmiR-47、miR-101、miR-197の発現レベルの評価を以下の通り行った。miRNAの発現量は、細胞または組織からmirVana miRNA Isolation kit を用いてmiRNAを抽出した後、Mir-XTM miRNA qRT-PCR SYBR(R) Kit を用いて調べた。これにより、siRNAによるmiRNAの発現抑制効果、およびmiRNAの発現量の変化を確認した。
皮下による異種移植によって、3つのmiRNAの抑制効果を実証した。前記異種移植は、1 x 107個のHMV-I細胞を右側腹へ接種することにより確立した。触知できる腫瘍は播種から7日後に確認できた。10匹のマウスをランダムに2グループに分け、3siRNA混合物(100 μM)(n=5)、または等量のDDS(n=5)を投与した。3siRNA混合物をトランスフェクションした細胞は、in vitroで増殖が抑制された。5週間後、腫瘍を分析するためにマウスを屠殺した。腫瘍ボリュームはボリューム = π/6×横幅×縦幅×高さの式によって評価した。
siRNA混合物(400 μM)またはDDSで処理する1週間前に、HMV-I細胞(1×107 細胞)を胸腺欠損マウスの尾静脈にインジェクションした。siRNA混合物またはDDSは毎週投与し、腫瘍ボリュームまたは転移を5週間後に調査した。全てのマウスはJapanese Association for Accreditation for Laboratory Animal Care-approved facilitiesで保管および飼育した。動物実験および取り扱いはfederal Institutional Animal Care and Use Committee guidelinesを厳格に遵守した。
腫瘍内のRNAの定量化、および高い再現性のシークエンシングを行ない、3siRNA混合物による、miR-47、miR-101、miR-197それぞれの発現抑制効果を評価した結果を図5Bに示す。データはクラスカル・ワーリステスト(n=5)を用いて分析した。*はDDS処理した腫瘍に対してmiRNA発現レベルに有意差(P<0.01)があることを示す。3つのmiRNAはの量は、3siRNA混合物を投与することによって減少する傾向が見られた。
上記(4-1-2)で得られた腫瘍について、顕微鏡による調査結果(HE(ヘマトキシリン・エオシン染色); ×400)を図5Cに示す。上部はコントロールを、下部はsiRNAで処理した腫瘍を示す。siRNAで処理した腫瘍はHMV-I細胞で減少し、フィブロシスによる置き換わりに伴って腫瘍は壊死し、新血管新生は抑制された。
上記(4-1-2)で得られた腫瘍について、腫瘍、分化、多能性の関連遺伝子の転写レベルを試験した結果を図5Dに示す(*: P<0.05, **: P<0.01)。Oct4、Klf4、p53、hTERT、PROM1、Sox2は多能性、腫瘍形成、または癌幹細胞性に関与すると考えられる。2-△△法を用いてβ-actin mRNAの発現を比較した。図5D中においてCntlはコントロール(DDSのみ)を表し、3 mixは3siRNA混合物+DDSを表す。この結果、3siRNA混合物はp53およびSox2のmRNAの上昇を誘導した。一方で、hTERT、PROM1、Oct3/4、Klf4は減少した。
(5-1)miRNA-197の抑制と、hsa-mir-520dのアップレギュレーションの評価
FuGeneキット(Roche社製)を用いて、miR-197 siRNAを293FT細胞にトランスフェクションした後、顕微鏡で観察した(図6A)。また、ウイルスベクター(pMIRNA1、System Bioscience:SBI社製)を用いて、hsa-mir-520d(Accession:MI0003164)をヒトの線維芽細胞細胞(TIG-1-20)に感染させた後、顕微鏡で観察した。このhsa-mir-520dは、RGM249 shRNAをトランスフェクションすることによってアップレギュレイトされるmiRNAである(A noncoding RNA gene on chromosome 10p15.3 may function upstream of hTERT. Miura et al., BMC Mol Biol. 2009 Feb 2;10:5.)。上記ウイルスベクターから発現するhsa-mir-520dの塩基配列は5'-UCUCAAGCUGUGAGUCUACAAAGGGAAGCCCUUUCUGUUGUCUAAAAGAAAAGAAAGUGCUUCUCUUUGGUGGGUUACGGUUUGAGA-3'(配列番号43)である。その推定2次構造を図6Bに示す。この配列において、ガイド鎖に相当する配列は5'-UCUACAAAGGGAAGCCCUUUCUG-3'(配列番号41)、パッセンジャー鎖に相当する配列は5'-AAAGUGCUUCUCUUUGGUGGGU-3'(配列番号42)である。
miR-197 siRNAをトランスフェクションした293FT細胞(ヒト胎児腎臓由来細胞株)を、顕微鏡で免疫組織化学的に観察した結果を図6Cに示す。図6Cは未分化マーカーであるOct4とNANOGを検出している。上部(0hr)の3つは、トランスフェクションしていない293FT細胞を顕微鏡(拡大率: ×40)で観察した写真である。左の列は身染色、真ん中の列は抗Oct4抗体によるローダミン染色、右の列は抗NANOG抗体によるローダミン染色を施した結果である。細胞の染色は各1週間行った。
hsa-mir-520dを各種癌細胞にウイルスベクター(pMIRNA1、System Bioscience:SBI社製)で感染させ、強制発現させた。その後、上述の免疫組織科学的試験と同様の方法で未分化マーカーの発現量を観察した。その結果を図6D、図6E、図6Fに示す。使用した癌細胞は、HT1080細胞(ヒト線維肉腫細胞株)、T98G細胞(ヒトグリオーマ細胞株)、PK-45p細胞(ヒト膵臓癌由来細胞株)、HMV-I細胞(ヒト悪性黒色腫由来細胞株)、HLF細胞(ヒト肝癌由来細胞株)である。またHMV-I細胞、およびHLF細胞においては、未分化マーカーであるOct4またはNANOGを発現していた。
上記ようにして生成したiPS細胞における各種遺伝子の転写量を図7Aに示す。miR-197 siRNAで処理した293FT細胞、およびhsa-mir-520dが過剰発現した293FT細胞における各種遺伝子の転写量は同じであった。図7Aは、その2つの細胞の転写量を、hiPSC(HPS0002 253G1)('Generation of mouse-induced pluripotent stem cells with plasmid vectors.' Okita et al., Nat Protoc 5, 418-428 (2010).)の発現量に対して比較した結果である。転写レベルはワンステップリアルタイムRT-qPCRで調査した。図中、hiPSCの発現量を0として表している。上部は、293FT細胞用の培地において293FT細胞にトランスフェクションまたは感染させてから48時間後の転写量である。下部は、その後2週間、ES細胞のための培地で維持したときの転写量である。
(6-1)細胞
in vitroとin vivoにおけるhsa-mir-520d発現の効果を評価するために、複数種類の細胞株とレンチウイルスベクターとを使用した。ヒトメサンギウム細胞株である293FTは、日本Invitrogen社(東京、日本)から提供され、10%FBS、0.1mM MEM非必須アミノ酸溶液、2mM L-グルタミン、および1%ペニシリン/ストレプトマイシンを添加したダルベッコ改変イーグル培地中で培養した。強力なRGM249発現を有するヒト未成熟または未分化肝細胞株(HLF)とRGM249の弱い発現を有する高分化肝癌細胞株(Huh7)を、アメリカ培養細胞系統保存機関(American Type Culture Collection)から購入し、10%FBSおよび1%ペニシリン/ストレプトマイシンを添加したRPMI培地中で培養した。ウイルス処理により形質転換した細胞の未分化状態を維持するため、5ng/mlのbFGF-2を有するReproStem培地(ReproCell社、東京、日本)中で、細胞を培養した。ヒト誘導多能性幹細胞(HPS0001、HPS0002)は、理研バイオリソースセンターの細胞バンク(Riken Bioresource Center Cell Bank)から提供された。
pMIRNA1-mir-520d/GFP(20μg)(System Biosciences社、Mountain View、米国)とモック(mock)ベクターとしてのpCDH(20μg)とを各々、(10cm培養プレートあたり5 x 106細胞の)293FT細胞へトランスフェクトした。 上清中のウイルス粒子を回収するために、4℃、120分間、170000 x gで遠心後、ウイルスペレットを回収し、Lenti-XTM(商標)qRT-PCR滴定キット(Clontech社、カリフォルニア、米国)を使用して力価測定を行った。293FTまたはHLF細胞へのレンチウイルス感染のために、10cm培養プレート当たり100万個のウイルスを使用した。ポジティブコントロールとして使用したRGM249miRNA-197 siRNAを、ステルスRNAiデザイナー(Stealth RNAi designer)(https://rnaidesigner.invitrogen.com/rnaiexpress/)を用いて設計し、FuGENE HDトランスフェクション試薬(Roche Diagnostics社、バーゼル、スイス)を用いて、50nMの合成オリゴヌクレオチドを、293FT細胞へトランスフェクトした。また、520d-HLF細胞が骨芽細胞へと分化誘導することを確認するために、通常のRPMI1640培地中に2Mのpurmorphamineを添加して、その細胞を一週間処理した。
レンチウイルス感染後のHLFを回収し、1マウス当たり5 x 107個のHLF細胞を、各々のマウスの腹腔内および皮下(右側腹)へ接種した。注入体積は、200μlであった。6週齢の免疫不全マウス(KSN/Slc)(清水実験材料株式会社、京都、日本)を、4週間通常給餌した。KSN/Slcマウスを、100 mg/kgのネンブタールを腹腔内注射することにより麻酔し、解剖および組織学的検査のために屠殺した。皮下への異種移植を使用して、hsa-mir-520dの抑制効果を実証した。体積評価は、以下の式を使用して決定した:体積 = π/6 x 幅 x 長さ x 高さ。全ての動物は、日本実験動物管理公認協会承認施設で保管および飼育した。動物の研究と取り扱いについては国際動物実験委員会のガイドラインを厳格に遵守した。
small RNA分画を含んだトータルRNAを、培養細胞またはホモジェナイズしたマウス組織から、mirVana miRNA分離キット(Ambion社、オースチン、米国)を使用して抽出した。Mir-X(商標)miRNA qRT-PCR SYBR(登録商標)キット(Clontech社、Mountain View、米国)を製造元のマニュアル(Clontech)に従って使用することにより、成熟型miRNAsの定量を実施した。U6 small nuclear RNAをインターナルコントロールとして使用した。トータルRNA(50ng/μl)を、OneStep RT-PCRキット(日本QIAGEN社、東京、日本)を用いて逆転写および増幅した。PCR解析とデータ収集解析とは、LineGene(東洋紡、名古屋、日本)を使用して実施した。サンプルの発現レベルを、検量線方法(2-ΔΔ法)を使用して決定した。全てのデータ(hTERTのものを除く)を、インターナルコントロールであるβ-アクチンに対して標準化した。hTERTの推定は、本発明者が以前開発した定量方法に従って、コピー数により行った。そのRNA定量を、シークエンシングによって、高い再現性をもって確認した。miRNA(25ng/μl)を、Mir-X miRNA qRT-PCR SYBRキット(タカラバイオ(株)、東京、日本)を使用して定量した。siRNAによる抑制を確認するために、miRNA発現変化を評価した。mRNAまたはmiRNA定量用のプライマー配列を、表4に示す。有意差を、*: P<0.05、**: P<0.01として示した。
20μg/μlのタンパク質とi-Blotゲル転写システムとを用いてウエスタンブロット解析した。製造元のマニュアルに従って、抗β-アクチン抗体以外の抗体(抗hTERT抗体、抗p53抗体、抗Oct4抗体、抗DICER1抗体、抗AID抗体、抗Alb抗体、および抗GFAP抗体)を1:500倍に希釈し、抗β-アクチン抗体を1:1,000倍に希釈した。LAS-4000(富士フイルム、東京、日本)を使用して、化学発光シグナルを1分以内に検出した。
製造元(R&D Systems社、ミネアポリス、米国)のマニュアルに従って、多能性幹細胞マーカー(抗Oct3/4抗体および抗NANOG抗体)ならびに胚性幹細胞マーカー抗体パネル(Embryonic Stem Cell Marker Antibody Panel)を用いて、免疫組織化学的検査を実施した。293FT細胞およびHLF細胞に、miRNA-197に対するsiRNAもしくはhas-mir-520dを含むレンチウイルス粒子をトランスフェクトまたは感染させた。浮遊するトランスフェクタント(つまり、トランスフェクトされた細胞)を回収し、顕微鏡観察用の新しい培養プレートまたは免疫染色用スライドチャンバーに移した。Huh7においても、293FTとHLFと同一の処理を、免疫細胞化学検査のために行った。
免疫組織化学解析のために、4%パラフォルムアルデヒド中で固定された肝臓組織標本を、常法により処理した。この試験で用いられたモノクローナル抗体は、以下のものである:抗アルブミン抗体(Sigma社、セントルイス、米国)、抗AFP抗体(Sigma社)、および抗GFAP抗体(Sigma社)。ネガティブコントロールとしては、一次抗体を省略して染色工程を実行した。発現の程度は、病理専門家が評価した。
細胞周期解析を実行するために、単一細胞懸濁物を、冷却したPBSで一度洗浄した。細胞ペレットを、その後、穏やかにチューブを振とうすることによりほぐして、ddH2O中の3.7%ホルマリンを滴下して固定した。細胞を、少なくとも一晩、-20℃でインキュベートした。固定後、細胞を冷却したPBSを用いて二回洗浄してEtOHを除去した。その後、細胞を、100U/mlのRNaseA含有PBS中に、1 x 106細胞/mlにて再懸濁し、37℃で50分間インキュベートした。50μg/mlのヨウ化プロピジウムを直接加えて、光を遮蔽して氷上において40分間インキュベートした。DNA含量を、EXPO32 ADC解析ソフトウエアを搭載したフローサイトメーター(EPICS ALTRA; Beckman Coulter社)により解析した。DNA含量は、pMIRNA1-mir-520d/GFPクローンをトランスフェクト後に、約20000イベントで評価した。GFP陽性細胞を、Moflo XDPセルソーター(EPICS ALTRA、Beckman Coulter社)により分取(ソート)した。
腫瘍体積、ならびに肺、肝臓、腹腔内、および後腹膜腔への転移がんを、明視野イメージング機能を備えた解剖顕微鏡下または肉眼で検査および計測した。組織サンプルは、10%緩衝ホルマリン溶液中で一晩固定し、PBSで洗浄し、70%エタノールへ移した。その後、パラフィンに包埋し、薄切し、ヘマトキシリン・エオシンを用いて染色した。
レンチウイルスmir-520d発現ベクターによる感染効率を評価するために、緑色蛍光発現を検出した。
一観察変数を有し、P<0.05を有意なものと見なすMann-Whitney Uテストを用いて、3つの群(コントロール群、モック(mock)群、およびmir-520d群)間で比較した。*: P<0.05、**: P<0.01である。
(6-12-1)293FT細胞へのhas-mir-520dのウイルス感染によるin vitro試験
表現系の変化を、顕微鏡的に評価した。図8Aは、293FT細胞へのhas-mir-520dのウイルス導入後に出現した浮遊細胞集団を示す。GFP陽性浮遊細胞(図8A(a))を、ES細胞用のフィーダー細胞不含有培地中で培養し、GFP発現を有するトランスフェクタントの増殖過程をタイムラプスモードで観察した(図8A(c))。has-mir-520dがウイルス感染した293FT細胞は、24時間以内にシート状の層を形成した。幹性化転換を、免疫細胞化学(図8B)に基づき確認した。GFP陽性細胞は、抗Oct4抗体により強く染色された。3日から1週間後、細胞はより大きなコロニーに生育し、NANOG陽性状態を維持していた(図8C)。トランスフェクタントの遺伝子発現を、RT-PCR、Western blot、および定量的miRNA RT-PCRにより評価した。
has-mir-520d発現ベクターを受容したHLF細胞(以下「520d-HLF」と称することもある)を、10cmプレート当たり20~50個の新規細胞集団へと転換した。図11A(左上図)に形態学的変化を示す。これらの細胞は、GFP(右上)および多能性マーカー(右下)を発現していた。その中で、Oct4およびNANOGは、転写的にアップレギュレートされていた。対照的に、RGM249、CD44、Alb、およびp53は、有意にダウンレギュレートされていた(**: P<0.01;図11B)。浸潤アッセイにおいては、多能性マーカー陽性細胞のほとんどは、フィブロネクチン膜(6穴プレート当たり5μg/ml)を通過して移動することはできなかった。対照的に、mock-HLF細胞は、容易に移動することができた(図11C)。ウエスタンブロットは、Oct4およびp53のアップレギュレーションを示した。has-mir-520d発現HLF(520d-HLF)細胞中で、DICER1が抑制されていた(図11D)。mock-HLF細胞と比較した場合、520d-HLF細胞では、メチル化マーカー(HDAC、Sin3A、およびMBD3)が有意に低いレベルで維持されていた(P<0.01) (図11B)。細胞周期解析によると、mock-HLFと比較して、520d-HLF細胞はS期が増加し、G0期が減少していたことを示した(図12A)。mir-520dを安定的に発現する10クローンのHLF細胞を、ES用培地で一ヶ月間に渡り培養した後には、HLFのものと比べて、520d-HLF細胞中でのhTERTおよびアルブミン(Alb)はダウンレギュレートされていた。520d-HLF細胞中での、Oct4およびp53はアップレギュレートされていた。がん幹細胞マーカー(PROM1:CD133)は、HLF、hiPSC、520d-HLF細胞間では有意差はなかった(図12B)。CD44発現は有意に減少していた(P<0.01) (データは示されない)。さらにまた、mir-520dによるHuh7細胞(高分化肝癌細胞株)における多能性誘導を検証した。小さく丸い細胞集団におけるOct4およびNANOG発現は、モックベクターによる誘導と比較して、より上昇していた。また、2μMのpurmorphamine添加により、ALP、SPP1、およびIBSPのアップレギュレーションを有する骨芽細胞へと、520d-HLF細胞を誘導した。
has-mir-520dのレンチウイルス発現ベクターまたはモックベクターにより、HLF細胞を感染したのち、その細胞(5 × 107細胞)を、免疫不全マウス(KSN/Slc)の腹腔内間隙へ注射した。has-mir-520dを発現したHLF細胞を注入したマウス群の75%は、腹腔内または注射針の刺入部分に沿って腫瘍を形成した(図14A)。対照的に、100%のモック感染群は、白色結節(HE染色(x40)にて組織学的に未分化肝癌細胞)を、腹腔内または肝臓に形成した(図14B)。12.5%(1/8)のマウス群中の520d-HLF細胞は、(肝細胞索、中心静脈、胆管(右図;白矢印)を有し、部分的に腺腫様過形成を内部に有する(図14D)(右から2番目の図))正常肝組織へと転換した(図14C、下図:HE染色組織標本)。37.5%(3/8)のHLF細胞は、表皮を有する類皮嚢胞と、汗腺(左図;白矢印)(図14A、図14D、および図14C上図;HE染色組織標本)とおよび皮脂腺(左から2番目;白矢印)とからなる奇形腫に形質転換した。生成した奇形腫と肝組織は、GFPタンパク質を発現していた(図14E)(左図:HEおよび右図:GFP)。肝組織中のほとんど全ての肝細胞がヒトアルブミンを強く発現しているのを免疫組織化学染色により確認した。肝星細胞(HSC)/筋線維芽細胞(MFs)のマーカーである、グリア線維性酸性タンパク質(GFAP)およびアルファフェトプロテイン(AFP)は、弱く発現していた。このことは、一ヶ月間に、520d-HLF細胞が未成熟肝組織へと分化したことを示唆する。50%(4/8)は、全く腫瘍および特定組織を形成しなかった。
また、免疫組織化学的分析により、未分化な肝臓組織のマーカーを用いて肝組織を構成する肝細胞、胆管、静脈、星細胞などの存在を確認できた(図15)。骨分化誘導によりOsteopontin, sialoprotein陽性の骨芽細胞を得たことから、内・中・外胚葉へ分化できる間葉系幹細胞(MSC)に形質転換できた。(図16)。
図17は高分化型肝癌(Huh7)細胞について評価した結果である。肝癌細胞においては分化度に関わらず、同等に多能性マーカー強陽性に変化させることができた。図18は多形性膠芽腫(T98G)細胞について評価した結果である。未分化脳腫瘍においても幹性誘導し、in vivoで腫瘍を形成せずに正常組織に生着した。図19は膵癌(PK-9)細胞について評価した結果である。膵癌においても幹性誘導が見られた。図20は線維肉腫(HT1080)細胞について評価した結果である。非上皮性悪性腫瘍である肉腫細胞(HT1080)をも幹性誘導し、脂肪細胞へ分化させることができた。
(7-1)細胞
HMV-I(ヒト悪性黒色腫)
T98G(ヒト神経膠芽腫)
HT1080(ヒト線維芽肉腫)
Pk-45(ヒト肝臓癌)
表5のmiRNAに対するshRNA(hsa-mir-192 shRNA、hsa-mir-196a-1 shRNA、hsa-mir-423-3p shRNA、has-mir-222 shRNA)をコードするベクターは、GenScript corp.,(NJ, USA)から購入した。このベクターは、pRNATin-H1.4/Lenti (GenScript, corp.,)に上記shRNAをコードする塩基配列が組込まれたものである(以下、「siRNA生成ウイルス)と称することもある)。細胞に導入後、shRNAを発現し、さらにsiRNAを生成することができる。
表5のmiRNAに対するsiRNA(hsa-mir-192 siRNA、hsa-mir-196a-1 siRNA、hsa-mir-423-3p siRNA、has-mir-222 siRNA)は、Stealth RNAi designer(Invitrogen社)によって入手した。配列を表6に示す。これらsiRNAが細胞増殖抑制等の効果を有していることを確認した後、上記(7-3)のshRNAでさらに細胞増殖抑制等の効果がみられるかどうかを検証するという流れで実験を行った。
細胞へのinfectionは、まず、293FTまたは293H細胞へレンチウイルスベクター(pRNATin-H1.4/Lenti)をtransfectionし、上清を回収し、遺伝子実験施設にある超遠心機で、27,000rpm、2時間遠心してウイルスを回収し、ペレットをPBSに溶解し、力価を検討後、-80度で保存した。そのウイルスを用いて、力価に基づき、各50μlずつ細胞に感染させた。また、3種類のsiRNA ( has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA) 共感染または4種類のsiRNA (hsa-mir-192 siRNA / has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA)共感染では、1種類のウイルス粒子が有効に作用する力価で感染させた。
mirVana(tm) miRNA Isolation Kit ( Ambion , TX , USA )を使用してmiRNA , totalRNAを抽出した。washした細胞にTorizol Reagent( Life Technologies Carlabad , CA , USA )を添加し、3分間インキュベート後Torizol Reagentの1/5量のchloroform( ニッポンジーン , Tokyo , Japan )を添加した。15秒間振盪後、14,000rpmで15分間遠心を行った。得られた上清の1/10量の100%エタノールを加え、数回転倒混和しspin columnに入れ、10,000g で15秒遠心した。カラムをwashするためmiRNA Wash Solution 1を700μl加え、10,000g で15秒遠心した。更にWash Solution 2/3を500μl加え、同様に遠心した。この作業を2回繰り返し、あらかじめ、95度に温めておいたRNase , DNase Free Waterを100μl加え、同様に遠心、そして、この過程を2回繰り返した。その後、真空濃縮を40分間し、そのうち2μlを使用し、NanoDrop( バイオメディカルサイエンス, Tokyo, Japan )を用いて濃度を測定した。
RGM249 , hTERT , Sox2 , p53 , c-Myc , Oct4 , PROM1の7種類の発現を調べるためにQIAGEN OneStep RT-PCR Kit ( Qiagen , Tokyo , Japan )を使用した。GAPDH , β-actinをコントロールとした。検討した遺伝子は多能性関連マーカー、未分化マーカー及び分化マーカー、テロメレース関連遺伝子を使用した。
PBS(-)でwashした細胞をtrypsin処理した後、エッペンドルフチューブに回収し、蛋白分解酵素阻害剤 Complete, Mini ( Roche Japan , Tokyo , Japan ) を含むCell Lysis Buffer ( SIGMA , Tokyo , Japan ) 22μlを加え、たんぱく質抽出液を得た。そのうちの2μlをNanoDropを用いて濃度測定に使用した。
iBlottm ドライブロッティングシステム( Invitorogen , Tokyo , Japan )を使用し、電気泳動したゲルをセミドライ状態でメンブレンに転写した。その後WesternBreeze(r)イムノディテクションキット( Invitorogen , Tokyo , Japan )を使用し、ブロッキング30分、リンス5分×2、一次抗体60分、wash 5分×4、二次抗体30分、wash 5分×4、リンス2分×2を行った。そして、ケミルミネッセンス2.5mlをメンブレンに添加し5分後、遺伝子実験施設のLas-1000plus (FUJIFILM , Kanagawa , Japan ) で検出した。
1×106個の細胞をwashした後、trypsin処理し15mlチューブに回収した。その後、95%エタノールを5ml加え、オーバーナイトで固定した。翌日1μg/mlのRNaseを1ml加え、1時間37度でインキュベートした後、PIを5μl加え、30分以上4度、遮光で遺伝子実験施設のEPICS ALTRA ( Beckman coulter , Tokyo Japan ) で解析を行った。
PBS ( - )で washした細胞をtrypsin処理した後、96wallプレートに1×106個の細胞を100μlずつ蒔いた。Promega社のCellTiter96(R) Non-Radioactive Cell Proliferation Assay kitを使用して細胞増殖能を検討した。
soft agerを使用して、形質転換を起こした細胞の足場依存性及び腫瘍形成能を検討した。60mmディッシュにボトムアガロース( 0.5-0.6% )を2-3ml入れ、ある固形化した後、トップアガロース( 0.4% )で重層した。そして、そのディッシュに細胞を播き、1-2週間培養し、その後、細胞をカウントした。
Takara ( Tokyo , Japan ) 社のmir-x miRNA定量kitを用いて定量した。指定されたプロトコールに準じて施行した。
感染効率はレンチウイルスベクターの情報に準じて評価した。感染をGFP発現に関して蛍光顕微鏡で可視化して判定し、neomycinの導入、miRNAの導入を感染細胞の一部よりDNAまたはRNAを抽出し、PCRで増幅後、電気泳動で可視化して評価した。ゲノムへの取り込み部位の検討は施行しなかった。
(7-15-1)siRNA生成Lentivirus感染後のHMV-1におけるMTT assay
各siRNA生成ウイルスを感染させたHMV-1でのMTT assayを3日間施行した(図21)。3種類のsiRNA ( has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA) 共感染または4種類のsiRNA (hsa-mir-192 siRNA / has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA)共感染細胞で有意に増殖抑制を確認した。統計学的有意差を* ( p<0.05 ) で示した ( Mann-Whitney test ) 。
各siRNA生成ウイルス感染による導入はmiRNA発現を阻害した。また、細胞の増殖抑制を示す経時的変化を示した(図22)。図中のトップパネルは、1週間後のmockとhsa-mir-196a-1 / hsa-mir-423-3p / hsa-mir-222でのGFP検出のための蛍光顕微鏡写真である。図中のボトムパネルは、ウイルス感染後の HMV-1の増殖曲線である。コントロール、mock、hsa-mir-192、hsa-mir-196a-1 siRNA、hsa-mir-222 siRNAと比較して、3種類のsiRNA ( has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA) 共感染または4種類のsiRNA (hsa-mir-192 siRNA / has-mir-196a-1 siRNA / has-mir-423-3p siRNA / has-mir-222 siRNA)共感染で顕著な増殖抑制を観察し、感染細胞は3週間以内にアポトーシスに至った。
miRNAに対するsiRNAを生成するウイルスベクターに感染させ、siRNAが導入されたHMV-1において、腫瘍形成能を評価するためにsoft agerを用いて、colony formation assayを行った(図23)。コントロールではコロニーを多数形成しているのに対し、hsa-mir-192単独導入、4種類 (has-mir-192 / -196a-1 / -423-3p / -222 ) のmiRNAの共発現で、顕著にコロニー形成能が抑制された。hsa-mir-192に対するsiRNAでは途中までコロニー形成を認めたが、その後、増殖は止まり、そのまま細胞の断片化を起こしてアポトーシスに至った。また、4 種類 (has-mir-192 / -196a-1 / -423-3p / -222)の共感染ではコロニーを形成することはなかった。
・アンタゴマーの合成
アンタゴマー(miRNAを標的としたsmall RNA)のデザインと合成はInvitrogen社(Stealth RNAi designer (https://rnaidesigner.invitrogen.com/rnaiexpress/))とGenScript社へ委託した(pRNATin-H1.4/Lenti, pRNAT-T6.1/neo)。shRNA-generatingベクターはBLOCK-it Inducible H1 RNAi Entry Vector (Invitrogen, CA, USA)を用いて、プロトコールに沿って作成した。
HLF細胞ラインとHMV-I細胞ラインはAmerican Type Culture CollectionとTohoku Universityからそれぞれ購入し、10% FBSと1% ペニシリン/ストレプトマイシンを添加したRPMI培地で培養した。アンタゴマー処理の場合、HMV-1細胞を50 nMのantagomirとともにインキュベーションした。
FuGene HD transfection Reagent (Roche Diagnostic GmbH)を使用して、HLFまたはHMV-I細胞に、50 nM siRNA、コントロールのオリゴヌクレオチド、または空のベクターをトランスフェクションした。ダイサー(Dicer enzyme)はGenlantisから購入し、プロトコールに沿って使用した。3つのmiRNAは、ダイサーで消化したものをmiRCAT-microRNA cloning kit (Integrated DNA Technologies)でクローニングすることによって得た。免疫不全マウスは、Charles riverからCAnN Cg-Foxn1 BALB/c-nuを、SHIMIZU Laboratory Supplies Co., Ltd.からKSN/Slcを購入した。
トータルRNA、small RNAフラクションは、培養細胞またはホモジナイズしたマウス組織から、mirVana miRNA Isolation Kit (Ambion)を用いて抽出した。miRNAの成熟化の定量は、Mir-XTM miRNA qRT-PCR SYBR(R) kit (Takara Bio Company)を用いて説明書に従って行った。U6 small nuclear RNAをインターナルコントロールとして使用した。
トータルRNAは、OneStep RT-PCR kit (QIAGEN)を用いて逆転写及び増幅させた。PCRとデータ収集分析はLineGene (TOYOBO)を用いて行った。サンプルの発現レベルは、検量線方法(2-ΔΔ法)を使用して決定した。全てのデータ(hTERTおよびRGM249のものを除く)を、インターナルコントロールであるβ-アクチンに対して標準化した。hTERTおよびRGM249の推定は、本発明者が以前開発した定量方法に従って、コピー数により行った。mRNAに関しては50ng/μlで、small RNAに関しては100ng/μlで試験した。
ウエスタンブロット解析をi-Blotゲル転写システム(Invitrogen社)を使用して実行した。目的バイオマーカー遺伝子に対するそれぞれの抗体を、製造元のマニュアルに従った希釈率を用いて使用した。20μgの細胞抽出物を試験した。
取大学動物実験委員会で承認されたプロトコルに基づいて、動物実験を実施した。腫瘍細胞接種、検死、および組織学的解析を、実験方法セクションに記載したように実施した。播種から7日後、ショートサイレンスオリゴヌクレオチドによる処理を、マウスの尾静脈または右側腹の皮下に、siRNAまたはshRNA (100μM)を週一回のペースで4~5週にわたって行なった。腫瘍を摘出して計量した。腫瘍体積、ならびに肺、肝臓、腹腔内、および腹腔外(postperitoneal)転移がんを、明視野イメージング機能を備えた解剖顕微鏡下または肉眼で検査および計測した。組織サンプルは、10%緩衝ホルマリン溶液中で一晩固定し、PBSで洗浄し、70%エタノールへ移した。その後、パラフィンに包埋し、薄切し、ヘマトキシリン・エオシンを用いて染色した。転移プロセスの後期ステージにおけるantagomirの効果を評価するために、胸腺欠損マウスの尾静脈を介するかまたは皮下に腫瘍細胞を移植した。次に、腫瘍細胞移植7日後に、同所性の実験に使用したと同一の用量と頻度でantagomir治療を開始した。静脈内投与の場合は全身性転移によって、または、皮下接種の場合は肝臓転移もしくは腹腔内転移によって、マウスは30日目には瀕死の状態になり、安楽死させた。
胸腺欠損マウスを、1グループにつき5匹に分けて、PBS+DDSまたは50 μMのアンタゴマーを、週一回のペースで4~5週間にわたって6回、静脈投与した。体重は2週に1回のペースで測定した。マウスは最後の投与後6日で安楽死させ、組織を収集した。全血の一定分量をEDTAで処理したチューブに集めた。遠心分離により血球細胞を除去して、血漿を得た。サンプルを、オリンパス社製Bioanalyzerを使用して解析し、血液の生化学的値を測定した。全ての可能な病理状態に関して、肺または肝臓の切片を検査した。
miRNA-47、-101、-197に対するsiRNAをトランスフェクションすることにより、293FT細胞はヒト正常細胞へと誘導された。その後、RT-PCRとウエスタンブロット法を用いて関連遺伝子の発現の変化を評価した。
製造元(R&D Systems、ミネアポリス、米国)のマニュアルに従って、未分化マーカー(抗Oct-4抗体)ならびに胚性幹細胞マーカー抗体パネル(Embryonic Stem Cell Marker Antibody Panel)を用いて、免疫組織化学検査を実施した。細胞に、miRNA-197に対するsiRNAをトランスフェクトまたは感染した。浮遊するトランスフェクタントを回収し、顕微鏡観察用の新しい培養プレートまたは免疫染色用スライドチャンバーに移した。
ヒト人工多能性幹細胞であるhiPSC(HPS0002 253G1)はRiken Bioresource Center Cell Bank('Generation of induced pluripotent stem cells without Myc from mouse and human fibroblasts.' Nakagawa M et al., Nat Biotechnol 26, 101-106 (2008))から提供された。
miR-197 siRNAまたはhsa-mir-520dを導入して作成した多能性幹細胞は、ES細胞用培養液で培養できるが、F-12 HAM[DMEM(15mM HEPES+1mM Sodium Pyruvate+pyridoxine+NaHCO3+5mML-glutamine)], RPMI-1640+L-glutamine, DMEM+high glucose+L-glutamine+0.1mM NEAA およびREPROSTEM(REPROCell社):bFGF 3-10ng/mlからなる群から選ばれる1種以上の培地で37℃、5%CO2、10%FBSの条件で培養可能であった。
miRNA-197に対応するsiRNAをトランスフェクトした293FT細胞を使用して、トリプシンにより分離脱着した細胞上で、フローサイトメトリーを実行した。単一細胞懸濁物を、冷却したPBSで一度洗浄した。細胞ペレットを、その後、穏やかにチューブを振とうすることによりほぐして、ddH2O中の冷却70%EtOHを滴下して固定した。細胞を、少なくとも一晩、-20℃でインキュベートした。固定後、細胞を冷却したPBSを用いて二回洗浄してEtOHを除去した。その後、細胞を、100U/mlのRNAaseA含有PBS中に、1 x 106細胞/mlにて再懸濁し、37℃で50分間インキュベートした。50μg/mlのヨウ化プロピジウムを直接加えて、光を遮蔽して氷上において40分間インキュベートした。DNA含量を、フローサイトメーター(EPICS ALTRA; Beckman Coulter社)により解析した。リプログラムされた細胞の発現を評価するために、EXPO32 ADC解析ソフトウエアを搭載したフローサイトメーターにより、siRNA-197をトランスフェクション後、約20000イベントで、iPS細胞を評価した。GFP発現細胞もしくはPE陽性細胞のフローサイトメトリーを用いた精製に関しては、ウイルストランスダクション過程の完了24時間後に、(未分化状態を維持して2週間培養後の)293FT細胞またはHLF細胞を、5%FCSを添加したリン酸緩衝液(PBS)中に再懸濁した。PE抱合抗アルカリホスファターゼ(ALP)抗体で、細胞を染色後、GFP陽性細胞またはPE陽性細胞を、Moflo XDP(Beckman Coulter社、カリフォルニア、米国)を使用して分取および解析した。1×108細胞を、アルゴンレーザー(488nm、100mW)を用いて、フォワードスキャッター、サイドスキャッター、ならびにPEおよびGFP蛍光に関して解析した。検出器としては、各々、GFPに関してはFL1を、PEに関してはFL2を使用した。
免疫不全マウスをペントバルビタールナトリウム(50mg/kg、腹腔内注射)を用いて麻酔し、定位固定装置中に配置した。外科手術中、動物の体温を、加熱パッドを使用して、37℃に維持した。頭蓋を露出し、左線条体の上に、小規模な開頭を作製した。ポリエチレンの管を介して10μlのハミルトンシリンジに連結された30Gの注射針を、細胞移植用に使用した。注射針を、左線条体に定位的に挿入(ブレグマからA(前方) 0.5mm、L(側方) 2.0mm、D(深さ) 2.5mm)し、5μlの細胞懸濁物(108細胞/μl)を圧力注射した。注射後、その注射針をゆっくりと引き抜いて、頭蓋の孔を、歯科用セメントを用いて被覆した。切開部を、6-0プロレン(Prolene)を用いて縫合した。外科手術から回復後、動物を元の飼育ケージへと戻した。
以上の結果を踏まえて考察する。実施例の結果、RGM249 shRNAは悪性腫瘍の増殖抑制、悪性腫瘍の転移抑制、細胞内RGM249 mRNA量の抑制、または細胞内hTERT mRNA量の抑制の効果を有していることが示された。また、3つのsiRNAは、悪性腫瘍の増殖抑制、悪性腫瘍の転移抑制、細胞内の3つのmiRNA量の抑制、未分化マーカーのアップレギュレイト、p53のアップレギュレイト、または正常細胞もしくは悪性腫瘍細胞のリプログラミングの効果を有していることが示された。hsa-mir-520dは、未分化マーカーのアップレギュレイト、p53のアップレギュレイト、または正常細胞もしくは悪性腫瘍細胞のリプログラミング、悪性腫瘍の増殖抑制等の効果を有していることが示された。また、hsa-mir-192 siRNA等についても類似の効果が見られた。マウスで見られた悪性腫瘍の抑制は、悪性腫瘍細胞のリプログラミングが要因のひとつであると考えられる。また、未分化型だけでなく高分化型肝癌細胞でもOct4陽性かつNANOG陽性細胞になり、分化型によらない幹性化効果が見られた。なお、RGM249 shRNAと3つのsiRNAは、RGM249 mRNAから始まるカスケードを遮断する点で機能が共通しており、この機能が上記の悪性腫瘍の抑制や悪性腫瘍細胞のリプログラミング等の効果に関与していると考えられる。hsa-mir-520dはこのときアップレギュレイトしていると考えられる。以上から、RGM249 shRNA、3つのsiRNA、hsa-mir-520d、hsa-mir-192 siRNA等はいずれも悪性腫瘍治療に好適に使用できると考えられる。
Claims (47)
- a)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
b)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
c)配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有し、細胞を多能性幹細胞へ誘導する、多能性幹細胞誘導剤。 - 前記1本鎖または2本鎖のポリヌクレオチドが、RNAi作用を有する、請求項1に記載の多能性幹細胞誘導剤。
- 前記1本鎖または2本鎖のポリヌクレオチドが、small RNAである、請求項1に記載の多能性幹細胞誘導剤。
- 前記1本鎖または2本鎖のポリヌクレオチドが、1本鎖または2本鎖のRNA鎖である、請求項1に記載の多能性幹細胞誘導剤。
- 前記1本鎖または2本鎖のポリヌクレオチドが、15以上のヌクレオチドからなる、請求項1に記載の多能性幹細胞誘導剤。
- 前記1本鎖または2本鎖のポリヌクレオチドが、100以下のヌクレオチドからなる、請求項5に記載の多能性幹細胞誘導剤。
- 前記1本鎖のポリヌクレオチドがshRNAであり、前記2本鎖のポリヌクレオチドがsiRNAまたはmiRNAである、請求項1に記載の多能性幹細胞誘導剤。
- 前記shRNAが35~100ヌクレオチドからなり、前記siRNAまたはmiRNAのガイド鎖が15~40ヌクレオチドからなる、請求項7に記載の多能性幹細胞誘導剤。
- 前記shRNA、前記siRNA、および前記miRNAが、1~5ヌクレオチドからなるオーバーハングを含む、請求項7に記載の多能性幹細胞誘導剤。
- 請求項1に記載の多能性幹細胞誘導剤であって、
前記a)の1本鎖または2本鎖のポリヌクレオチドが、さらに、配列番号4の塩基配列、またはその塩基配列に対して1~5個の塩基が欠失、置換もしくは付加された塩基配列、を含み、
前記b)の1本鎖または2本鎖のポリヌクレオチドが、さらに、配列番号5の塩基配列、またはその塩基配列に対して1~5個の塩基が欠失、置換もしくは付加された塩基配列、を含み、
前記c)の1本鎖または2本鎖のポリヌクレオチドが、さらに、配列番号6の塩基配列、またはその塩基配列に対して1~5個の塩基が欠失、置換もしくは付加された塩基配列、を含む、
多能性幹細胞誘導剤。 - 前記1本鎖または2本鎖のポリヌクレオチドが、2本鎖のポリヌクレオチドであり、且つsiRNAである、請求項1に記載の多能性幹細胞誘導剤。
- 配列番号7の塩基配列を含むRNA鎖を、ダイサーで処理して得られるRNA鎖に対して相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、
からなる群から選ばれる1種以上の塩基配列を含む、1本鎖または2本鎖のポリヌクレオチドを含有する、多能性幹細胞誘導剤。 - 体細胞を多能性幹細胞へ誘導する、請求項1に記載の多能性幹細胞誘導剤。
- 悪性腫瘍細胞を多能性幹細胞へ誘導する、請求項1に記載の多能性幹細胞誘導剤。
- 前記悪性腫瘍が、肝臓癌、膵臓癌、線維肉腫、多形性膠芽腫、メラノーマからなる群から選ばれる1種以上の悪性腫瘍である、請求項14に記載の多能性幹細胞誘導剤。
- 前記多能性幹細胞が、内在性のp53を発現している、請求項1に記載の多能性幹細胞誘導剤。
- g)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
h)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
i)配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有し、未分化細胞マーカーの発現を調節する、未分化細胞マーカー発現調節剤。 - 請求項17に記載の未分化細胞マーカー発現調節剤であって、
前記未分化細胞マーカーが、Klf4、c-Myc、Oct4、Sox2、PROM1からなる群から選ばれる1種以上の未分化細胞マーカーである、未分化細胞マーカー発現調節剤。 - j)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
k)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
l)配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有し、多能性幹細胞におけるp53の発現量を促進する、多能性幹細胞のp53発現促進剤。 - m)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
n)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
o)配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを、細胞に導入する工程を含む、多能性幹細胞の生産方法。 - 請求項20に記載の生産方法で得られる、多能性幹細胞。
- HPS0002:253G1株に比べて内在性のp53の発現量が増大している、請求項21に記載の多能性幹細胞。
- p)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
q)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
r)配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有する、悪性腫瘍の治療薬。 - 請求項23に記載の悪性腫瘍の治療薬であって、さらにアテロコラーゲンを含む、悪性腫瘍の治療薬。
- 請求項23に記載の悪性腫瘍の治療薬であって、
前記悪性腫瘍が、肝臓癌、肺癌、膵臓癌、線維肉腫、多形性膠芽腫、メラノーマからなる群から選ばれる1種以上の悪性腫瘍である、悪性腫瘍の治療薬。 - 前記悪性腫瘍が肉腫である、請求項23に記載の悪性腫瘍の治療薬。
- s)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
t)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
u)配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
からなる群から選ばれる1種以上のポリヌクレオチドを含む、siRNA。 - v)配列番号1の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
w)配列番号2の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
x)配列番号3の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
からなる群から選ばれる1種以上のベクター。 - 請求項28に記載のベクターを含有し、細胞を多能性幹細胞へ誘導する、多能性幹細胞誘導剤。
- 請求項28に記載のベクターを含む、悪性腫瘍の治療薬。
- 配列番号8の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、
を含む1本鎖または2本鎖のポリヌクレオチドを含有し、細胞を多能性幹細胞へ誘導する、多能性幹細胞誘導剤。 - 前記1本鎖または2本鎖のポリヌクレオチドが、1本鎖のポリヌクレオチドであり、
且つ配列番号10の塩基配列、またはその塩基配列に対して1~4個の塩基が欠失、置換もしくは付加された塩基配列を含む、
請求項31に記載の多能性幹細胞誘導剤。 - 配列番号7の塩基配列を含むRNA鎖に対してRNAi作用を有する1本鎖または2本鎖のポリヌクレオチドを含有し、細胞を多能性幹細胞へ誘導する、多能性幹細胞誘導剤。
- 配列番号8の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、
を含む1本鎖または2本鎖のポリヌクレオチドを含有し、未分化細胞マーカーの発現を調節する、未分化細胞マーカー発現調節剤。 - 配列番号8の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、
を含む1本鎖または2本鎖のポリヌクレオチドを含有し、多能性幹細胞におけるp53の発現量を促進する、多能性幹細胞のp53発現促進剤。 - 配列番号8の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、
を含む1本鎖または2本鎖のポリヌクレオチドを含有する、悪性腫瘍の治療薬。 - 配列番号8の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、shRNA。
- 配列番号8の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~4個の塩基が欠失、置換もしくは付加された塩基配列をコードするポリヌクレオチドを含む、ベクター。
- y)配列番号1の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
z)配列番号2の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
a')配列番号3の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
b')配列番号8の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
c')配列番号44の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
d')配列番号45の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
e')配列番号46の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
f')配列番号47の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含む、ポリヌクレオチド、
からなる群から選ばれる1種以上のポリヌクレオチドを含む、多能性幹細胞誘導用、未分化細胞マーカー発現調節用、多能性幹細胞のp53発現促進用、または悪性腫瘍の治療用のキット。 - g')配列番号44の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
h')配列番号45の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
i')配列番号46の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
j')配列番号47の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有し、細胞を多能性幹細胞へ誘導する、多能性幹細胞誘導剤。 - k')配列番号44の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
l')配列番号45の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
m')配列番号46の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
n')配列番号47の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有し、未分化細胞マーカーの発現を調節する、未分化細胞マーカー発現調節剤。 - o')配列番号44の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
p')配列番号45の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
q')配列番号46の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
r')配列番号47の塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列、を含む、1本鎖または2本鎖のポリヌクレオチド、
からなる群から選ばれる1種以上の1本鎖または2本鎖のポリヌクレオチドを含有する、悪性腫瘍の治療薬。 - s')配列番号44の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
t')配列番号45の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
u')配列番号46の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
v')配列番号47の塩基配列に相補的な塩基配列、またはその塩基配列に対して1~3個の塩基が欠失、置換もしくは付加された塩基配列を含むポリヌクレオチドを含むベクター、
からなる群から選ばれる1種以上のベクター。 - 哺乳動物の細胞由来の多能性幹細胞であって、
HPS0002:253G1株に比べて内在性のp53の発現量が増大している、多能性幹細胞。 - 前記p53の発現量がHPS0002:253G1株に比べて1.5倍以上である、請求項44記載の多能性幹細胞。
- 前記p53の発現量がリアルタイムPCRによって測定された発現量である、請求項45記載の多能性幹細胞。
- フィーダー細胞の非存在下で培養可能である、請求項45に記載の多能性幹細胞。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11806631.5A EP2594643B1 (en) | 2010-07-12 | 2011-06-28 | Method for producing novel hipsc by means of sirna introduction |
| US13/809,880 US9476041B2 (en) | 2010-07-12 | 2011-06-28 | Method for producing novel hipsc by means of siRNA introduction |
| CN201180043814.8A CN103189511B (zh) | 2010-07-12 | 2011-06-28 | 利用siRNA导入的新型hiPSC制作法 |
| JP2011530188A JP5099570B2 (ja) | 2010-07-12 | 2011-06-28 | siRNA導入による新規hiPSC作製法 |
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010-158193 | 2010-07-12 | ||
| JP2010-158192 | 2010-07-12 | ||
| JP2010158194 | 2010-07-12 | ||
| JP2010158192 | 2010-07-12 | ||
| JP2010158193 | 2010-07-12 | ||
| JP2010-158194 | 2010-07-12 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012008301A1 true WO2012008301A1 (ja) | 2012-01-19 |
Family
ID=45469308
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/064846 WO2012008301A1 (ja) | 2010-07-12 | 2011-06-28 | siRNA導入による新規hiPSC作製法 |
| PCT/JP2011/064847 WO2012008302A1 (ja) | 2010-07-12 | 2011-06-28 | miRNA導入による新規hiPSC作製法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/064847 WO2012008302A1 (ja) | 2010-07-12 | 2011-06-28 | miRNA導入による新規hiPSC作製法 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US9790491B2 (ja) |
| EP (2) | EP2594643B1 (ja) |
| JP (5) | JP5099570B2 (ja) |
| CN (2) | CN103097535A (ja) |
| WO (2) | WO2012008301A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015030149A1 (ja) | 2013-08-29 | 2015-03-05 | 国立大学法人鳥取大学 | 細胞のアンチエイジングに関連する生体分子群 |
| US9476041B2 (en) | 2010-07-12 | 2016-10-25 | National University Corporation Tottori University | Method for producing novel hipsc by means of siRNA introduction |
| WO2018203553A1 (ja) * | 2017-05-02 | 2018-11-08 | 株式会社ペジィー・ファーマ | 分化細胞の品質改善方法 |
| EP3401393A1 (en) * | 2012-02-22 | 2018-11-14 | Exostem Biotec Ltd | Micrornas for the generation of astrocytes |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2872636A4 (en) * | 2012-07-13 | 2016-08-17 | Minerva Biotechnologies Corp | METHOD FOR INDUCING A MINIMUM CELL TREATMENT CONDITION |
| US20160289678A1 (en) * | 2013-11-22 | 2016-10-06 | Dcb-Usa Llc | Use of microrna 146-a in the diagnosis, treatment and prevention of picornavirus infection and microrna 146-a antagonists |
| CN104109670B (zh) * | 2014-03-12 | 2018-01-05 | 首都医科大学附属北京安定医院 | 一种双链siRNA分子及其应用 |
| AP2017009670A0 (en) | 2014-06-27 | 2017-01-31 | Rhizen Pharmaceuticals Sa | Substituted chromene derivatives as selective dual inhibitors of PI3 delta and gamma protein kinases |
| EP3286335A4 (en) | 2015-04-24 | 2018-10-17 | The Johns Hopkins University | Compositions and methods related to characterizing proviral reservoirs |
| JP7116463B2 (ja) * | 2015-10-30 | 2022-08-10 | 典正 三浦 | Dna損傷を修復するrna分子 |
| KR102011336B1 (ko) * | 2015-12-31 | 2019-08-16 | 인터올리고 주식회사 | 약물 전달 및 안정화를 위한 복합체 및 그 제조방법 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006112239A1 (ja) * | 2005-04-15 | 2006-10-26 | National University Corporation Tottori University | hTERT発現調節遺伝子 |
| WO2006137514A1 (ja) * | 2005-06-23 | 2006-12-28 | Locomogene, Inc. | シノビオリンの発現もしくは機能阻害物質を有効成分とする癌治療剤、および癌治療剤のスクリーニング方法 |
| WO2009057831A1 (ja) * | 2007-10-31 | 2009-05-07 | Kyoto University | 核初期化方法 |
| WO2010058819A1 (ja) * | 2008-11-19 | 2010-05-27 | 学校法人 慶應義塾 | ヒト癌タンパク質MDM2とヒト癌抑制タンパク質p53との相互作用阻害ペプチド及びその使用 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060281179A1 (en) * | 2001-11-15 | 2006-12-14 | Yoshiki Sasai | Inducer for differentiation of embryo stem cells into ectodermal cells method of obtaining the same and use thereof |
| WO2004024940A2 (en) | 2002-09-16 | 2004-03-25 | University Of Southern California | Rna-mediated gene modulation |
| EP1592791A2 (en) | 2003-02-10 | 2005-11-09 | National Institute of Advanced Industrial Science and Technology | Regulation of gene expression by dna interference |
| US9453219B2 (en) * | 2003-05-15 | 2016-09-27 | Mello Biotech Taiwan Co., Ltd. | Cosmetic designs and products using intronic RNA |
| DK2302055T3 (da) * | 2004-11-12 | 2014-10-13 | Asuragen Inc | Fremgangsmåder og sammensætninger involverende miRNA og miRNA-inhibitormolekyler |
| CA2597219C (en) | 2005-02-04 | 2014-04-15 | Auburn University | Contact drug delivery system |
| ES2564823T3 (es) * | 2005-05-27 | 2016-03-29 | Ospedale San Raffaele S.R.L. | Vector génico que comprende miARN |
| EP2206724A1 (en) | 2005-12-13 | 2010-07-14 | Kyoto University | Nuclear reprogramming factor |
| ES2545118T3 (es) | 2006-01-05 | 2015-09-08 | The Ohio State University Research Foundation | Métodos basados en microARN y composiciones para el diagnóstico y tratamiento de cánceres sólidos |
| EA015570B1 (ru) | 2006-04-03 | 2011-10-31 | Сантарис Фарма А/С | Фармацевтическая композиция |
| CN101980712B (zh) * | 2007-10-29 | 2015-02-18 | 雷古拉斯治疗公司 | 用于肝癌治疗的靶向微小rna |
| JP5558097B2 (ja) | 2007-12-10 | 2014-07-23 | 国立大学法人京都大学 | 効率的な核初期化方法 |
| EP2238251B1 (en) * | 2007-12-27 | 2015-02-11 | Protiva Biotherapeutics Inc. | Silencing of polo-like kinase expression using interfering rna |
| CN101970664B (zh) * | 2008-01-16 | 2013-08-21 | 林希龙 | 使用可诱导的重组核糖核酸因子生成不含肿瘤的类胚胎干细胞的多能性细胞 |
| CN101333524B (zh) * | 2008-06-25 | 2010-06-02 | 中山大学 | 一个小分子非编码RNA基因hsa-miR-101及其抗肿瘤用途 |
| CN101392251B (zh) * | 2008-11-03 | 2015-07-22 | 清华大学深圳研究生院 | 能诱导干细胞向成骨细胞分化的微小rna及其应用 |
| WO2012008301A1 (ja) | 2010-07-12 | 2012-01-19 | 国立大学法人鳥取大学 | siRNA導入による新規hiPSC作製法 |
-
2011
- 2011-06-28 WO PCT/JP2011/064846 patent/WO2012008301A1/ja active Application Filing
- 2011-06-28 JP JP2011530188A patent/JP5099570B2/ja not_active Expired - Fee Related
- 2011-06-28 CN CN201180043810XA patent/CN103097535A/zh active Pending
- 2011-06-28 EP EP11806631.5A patent/EP2594643B1/en not_active Not-in-force
- 2011-06-28 WO PCT/JP2011/064847 patent/WO2012008302A1/ja active Application Filing
- 2011-06-28 JP JP2011530189A patent/JP5099571B2/ja not_active Expired - Fee Related
- 2011-06-28 CN CN201180043814.8A patent/CN103189511B/zh not_active Expired - Fee Related
- 2011-06-28 US US13/809,882 patent/US9790491B2/en not_active Expired - Fee Related
- 2011-06-28 EP EP11806632.3A patent/EP2594644B1/en not_active Not-in-force
- 2011-06-28 US US13/809,880 patent/US9476041B2/en not_active Expired - Fee Related
-
2012
- 2012-09-14 JP JP2012202508A patent/JP2013046616A/ja active Pending
- 2012-09-14 JP JP2012202509A patent/JP2013034479A/ja active Pending
-
2013
- 2013-12-20 JP JP2013264240A patent/JP5845493B2/ja not_active Expired - Fee Related
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006112239A1 (ja) * | 2005-04-15 | 2006-10-26 | National University Corporation Tottori University | hTERT発現調節遺伝子 |
| WO2006137514A1 (ja) * | 2005-06-23 | 2006-12-28 | Locomogene, Inc. | シノビオリンの発現もしくは機能阻害物質を有効成分とする癌治療剤、および癌治療剤のスクリーニング方法 |
| WO2009057831A1 (ja) * | 2007-10-31 | 2009-05-07 | Kyoto University | 核初期化方法 |
| WO2010058819A1 (ja) * | 2008-11-19 | 2010-05-27 | 学校法人 慶應義塾 | ヒト癌タンパク質MDM2とヒト癌抑制タンパク質p53との相互作用阻害ペプチド及びその使用 |
Non-Patent Citations (5)
| Title |
|---|
| KUMIKO TEI ET AL., RNAI JIKKEN NARUHODO Q&A, 1 October 2006 (2006-10-01), pages 88 - 96, XP008169714 * |
| MIKA SHIMIZU ET AL.: "Hatsugan o Seigyo suru Shinki non-coding RNA Idenshi no in vivo ni Okeru Kento", JAPANESE JOURNAL OF CLINICAL PHARMACOLOGY, vol. 38, 15 November 2007 (2007-11-15), pages S295, XP008168536 * |
| See also references of EP2594643A4 * |
| TAKAHASHI K. ET AL.: "Induction of pluripotent stem cells from adult human fibroblasts by defined factors.", CELL, vol. 131, no. 5, 2007, pages 861 - 872, XP008155962 * |
| WAKA SHINODA ET AL.: "Tei Bunka na Gan Saibo no Akusei Keishitsu o Soshitsu saseru miRNA-gun no Iyaku Oyo o Misueta in vitro Kento", JAPANESE JOURNAL OF CLINICAL PHARMACOLOGY, vol. 40, 18 November 2009 (2009-11-18), pages S190, XP008168534 * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9476041B2 (en) | 2010-07-12 | 2016-10-25 | National University Corporation Tottori University | Method for producing novel hipsc by means of siRNA introduction |
| US9790491B2 (en) | 2010-07-12 | 2017-10-17 | National University Corporation Tottori University | Method for producing novel hiPSC by means of miRNA introduction |
| EP3401393A1 (en) * | 2012-02-22 | 2018-11-14 | Exostem Biotec Ltd | Micrornas for the generation of astrocytes |
| WO2015030149A1 (ja) | 2013-08-29 | 2015-03-05 | 国立大学法人鳥取大学 | 細胞のアンチエイジングに関連する生体分子群 |
| US10265347B2 (en) | 2013-08-29 | 2019-04-23 | Norimasa Miura | Biomolecular group related to cell anti-aging |
| WO2018203553A1 (ja) * | 2017-05-02 | 2018-11-08 | 株式会社ペジィー・ファーマ | 分化細胞の品質改善方法 |
| JPWO2018203553A1 (ja) * | 2017-05-02 | 2020-03-19 | 株式会社ペジィー・ファーマ | 分化細胞の品質改善方法 |
| JP7327801B2 (ja) | 2017-05-02 | 2023-08-16 | 株式会社ペジィー・ファーマ | 分化細胞の品質改善方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2012008302A1 (ja) | 2013-09-09 |
| JPWO2012008301A1 (ja) | 2013-09-09 |
| EP2594644A1 (en) | 2013-05-22 |
| US9790491B2 (en) | 2017-10-17 |
| EP2594643B1 (en) | 2017-04-12 |
| JP2014097059A (ja) | 2014-05-29 |
| JP5099571B2 (ja) | 2012-12-19 |
| CN103189511A (zh) | 2013-07-03 |
| JP2013034479A (ja) | 2013-02-21 |
| EP2594643A1 (en) | 2013-05-22 |
| EP2594644B1 (en) | 2016-08-10 |
| US9476041B2 (en) | 2016-10-25 |
| EP2594643A4 (en) | 2014-12-24 |
| CN103189511B (zh) | 2016-10-12 |
| JP2013046616A (ja) | 2013-03-07 |
| CN103097535A (zh) | 2013-05-08 |
| US20130184335A1 (en) | 2013-07-18 |
| WO2012008302A1 (ja) | 2012-01-19 |
| US20130190389A1 (en) | 2013-07-25 |
| EP2594644A4 (en) | 2014-12-24 |
| JP5099570B2 (ja) | 2012-12-19 |
| JP5845493B2 (ja) | 2016-01-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5845493B2 (ja) | miRNA導入による新規hiPSC作製法 | |
| US11578107B2 (en) | Compositions and methods for reprogramming somatic cells into induced vasculogenic cells | |
| EP2077326A1 (en) | Novel nucleic acid | |
| US20210147853A1 (en) | Use of Trinucleotide Repeat RNAs To Treat Cancer | |
| WO2014096418A2 (en) | Micrornas as therapeutics and biomarkers for epilepsy | |
| KR20130132795A (ko) | 짧은 rna 분자 | |
| US20220056456A1 (en) | Means and methods for reducing tumorigenicity of cancer stem cells | |
| Huang et al. | MicroRNA-133b negatively regulates zebrafish single Mauthner-cell axon regeneration through targeting TPPP3 in vivo | |
| WO2014097875A1 (ja) | 新規の脱分化誘導方法を用いた多能性幹細胞化 | |
| EP3040414B1 (en) | Biomolecular group related to cell anti-aging | |
| AU2011256098A1 (en) | Method for reducing expression of downregulated in renal cell carcinoma in malignant gliomas | |
| KR101197627B1 (ko) | Hpv 감염과 관련된 암의 치료용 조성물 | |
| EP3981473A1 (en) | Therapeutic agent for cancer | |
| US9045752B2 (en) | NKX3-1 saRNA and KLF4 saRNA and uses thereof | |
| JP2010068723A (ja) | アレルギー疾患の治療のための核酸医薬 | |
| JPWO2013162027A1 (ja) | 神経分化促進剤 | |
| TW201631157A (zh) | 用以治療癌症之短干擾核糖核酸分子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011530188 Country of ref document: JP |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11806631 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2011806631 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011806631 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13809880 Country of ref document: US |