WO2009018807A1 - Oxazolidinone als faktor xa- inhibitoren, verfahren zu ihrer herstellung und ihre verwendung in der therapie - Google Patents
Oxazolidinone als faktor xa- inhibitoren, verfahren zu ihrer herstellung und ihre verwendung in der therapie Download PDFInfo
- Publication number
- WO2009018807A1 WO2009018807A1 PCT/DE2008/001252 DE2008001252W WO2009018807A1 WO 2009018807 A1 WO2009018807 A1 WO 2009018807A1 DE 2008001252 W DE2008001252 W DE 2008001252W WO 2009018807 A1 WO2009018807 A1 WO 2009018807A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- general formula
- hydrogen
- branched
- unbranched
- compound
- Prior art date
Links
- 0 COc1ccc(*2C(C(*(CC3)Oc4ccc(*(CCCC5)C5=O)cc4)=O)=C3C(C(*)=O)=*2)cc1 Chemical compound COc1ccc(*2C(C(*(CC3)Oc4ccc(*(CCCC5)C5=O)cc4)=O)=C3C(C(*)=O)=*2)cc1 0.000 description 9
- MFCKUCPBAKLQRV-UHFFFAOYSA-N CCC(N(CCO)c(cc1)ccc1ON(CC(CON(C)C(c([s]1)ccc1Cl)=O)O1)C1=O)=O Chemical compound CCC(N(CCO)c(cc1)ccc1ON(CC(CON(C)C(c([s]1)ccc1Cl)=O)O1)C1=O)=O MFCKUCPBAKLQRV-UHFFFAOYSA-N 0.000 description 1
- DISLBUZBRVFQKK-QJOMKUNGSA-N CCN(CC)CCN(Cc(cc1)ccc1-c1ccc(C(F)(F)F)cc1)C(NCOC/C(/CCc(cc1)ccc1F)=N\C(C1=CCCC1)=O)=O Chemical compound CCN(CC)CCN(Cc(cc1)ccc1-c1ccc(C(F)(F)F)cc1)C(NCOC/C(/CCc(cc1)ccc1F)=N\C(C1=CCCC1)=O)=O DISLBUZBRVFQKK-QJOMKUNGSA-N 0.000 description 1
- UUVBIGLRFLHJIY-UHFFFAOYSA-N CCNOC(CNC(C1CCCCC1)C(N(CC1)C1C(NOCc(cc1)ccc1/C(/N)=N/O)=O)=O)=O Chemical compound CCNOC(CNC(C1CCCCC1)C(N(CC1)C1C(NOCc(cc1)ccc1/C(/N)=N/O)=O)=O)=O UUVBIGLRFLHJIY-UHFFFAOYSA-N 0.000 description 1
- LWOZWBDTKXQDBB-UHFFFAOYSA-N CN(C(c1ccc(F)[s]1)=O)OCC(CN1Oc(cc2)ccc2N(CCOC2)C2=O)OC1=O Chemical compound CN(C(c1ccc(F)[s]1)=O)OCC(CN1Oc(cc2)ccc2N(CCOC2)C2=O)OC1=O LWOZWBDTKXQDBB-UHFFFAOYSA-N 0.000 description 1
- VLYJFMAPLOIGSO-UHFFFAOYSA-N COc(cc1)ccc1NC(C(N(CC1)c(cc2)ccc2N(CCCC2)C2=O)=O)=C1C(C(NO)=O)=N Chemical compound COc(cc1)ccc1NC(C(N(CC1)c(cc2)ccc2N(CCCC2)C2=O)=O)=C1C(C(NO)=O)=N VLYJFMAPLOIGSO-UHFFFAOYSA-N 0.000 description 1
- RJSNPRFPMUZYAW-UHFFFAOYSA-N COc(cc1)ccc1NC(C(N(CC1)c(cc2)ccc2ON(CCCC2)C2=O)=O)=C1C(C(N)=O)=N Chemical compound COc(cc1)ccc1NC(C(N(CC1)c(cc2)ccc2ON(CCCC2)C2=O)=O)=C1C(C(N)=O)=N RJSNPRFPMUZYAW-UHFFFAOYSA-N 0.000 description 1
- IRDACFJKQMNXKQ-UHFFFAOYSA-N C[n]1c(NOc(cc2)ccc2C(N)=N)nc2cc(N(CCC(O)=O)c3ncccc3)ccc12 Chemical compound C[n]1c(NOc(cc2)ccc2C(N)=N)nc2cc(N(CCC(O)=O)c3ncccc3)ccc12 IRDACFJKQMNXKQ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
Definitions
- OXAZOLIDINONE AS FACTOR XA INHIBITORS, PROCESS FOR THEIR PREPARATION AND THEIR USE IN THERAPY
- the present patent application relates to new pharmaceuticals, processes for their preparation and their use in therapy, for example in the field of blood clotting.
- An important protective mechanism of the human and animal organism is the blood clotting, which ensures that defects in the vessel wall can be closed quickly and reliably. This avoids blood loss of the organism. Hemostasis following vascular injury occurs through a coagulation system triggered by an enzymatic cascade of plasma proteins that interact in a complex manner. A whole range of blood coagulation factors are involved, each of which, after activation, converts the next precursor from the inactive to the active form. Finally, the cascade converts the soluble fibrinogen into insoluble fibrin, resulting in a blood clot.
- the coagulation factor Xa which is formed from proenzyme factor X, plays a key role, since two coagulation pathways (intrinsic and extrinsic system) are linked.
- the activated serine protease Xa splits prothrombin to thrombin.
- the latter in turn splits fibrinogen to fibrin.
- thrombin is a trigger of platelet aggregation.
- thromboembolic diseases are the most common cause of morbidity and mortality in industrialized countries.
- the anticoagulants known from the prior art i.
- Substances for the inhibition or prevention of blood clotting have various disadvantages, so that the treatment and prophylaxis of thromboembolic diseases proves to be very difficult.
- Known pharmacological treatment methods of thromboembolic diseases are the administration of heparin and vitamin K antagonists. Recently, attempts have been made to inhibit factor Xa described above. Although it has been shown that various compounds are effective as factor Xa inhibitors, but these have a number of disadvantages.
- the object of the present invention is, in particular, to provide such substances which, with increased selectivity, inhibit the blood coagulation factor Xa and in this case should at least partially avoid the problems of the therapy methods for thromboembolic disorders known from the prior art.
- Z 1 , Z 2 , Z 3 , Z 4 are each independently a direct bond or an oxygen or sulfur atom, R 2 is a hydrogen atom or a branched or unbranched C r C 4 alkyl
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 or -OCH 3 ,
- n stands for the integers 0, 1, 2, 3 or 4,
- R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl
- R 2 is hydrogen, methyl or ethyl, very particularly preferably Hydrogen.
- the group R 4 may be -Cl, -F, -Br, -CF 3 , -OCF 3 , -NO 2 or -OCH 3 , with Cl being preferred.
- the groups Z 1 , Z 2 , Z 3 , Z 4 are each independently a direct bond or an oxygen or sulfur atom. Preference is given to compounds in which at least one of Z 1 , Z 2 , Z 3 , Z 4 is an oxygen atom. Particular preference is given to compounds in which exactly one of the radicals Z 1 , Z 2 , Z 3 , Z 4 is an oxygen atom and the other radicals are a direct bond.
- the compounds of the invention may exist as stereoisomers due to the presence of asymmetric centers.
- the present invention relates to all possible stereoisomers both as racemates, as well as in enantiomerically pure form.
- stereoisomers also encompasses all possible diastereomers and regioisomers and tautomers (eg keto-enol tautomers) in which the compounds according to the invention can be present, which are therefore also the subject of the invention.
- This also applies to the compounds of the alternative embodiments II-XII mentioned below. Particularly preferred embodiments of the formula I
- Z, 1 1 Z - 7 2, Z v3 1 Z - 7 4, Z - 7 5 1 Z - 7 6 1 Z - 7 7 each independently for a direct
- Bond or represents an oxygen or a sulfur atom
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 6 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 2 each independently represents a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R 3 represents a hydrogen atom, -NH 2 , -NHR 2 or -N (R 2 J 2 or a branched or unbranched C r C 4 -alkyl radical, in which R 2 has the abovementioned meaning,
- Each X 1 , X 2 is independently a direct bond or a - (CH 2 ) n - chain, where n is a natural number 1, 2, 3 or 4,
- the group R 1 can represent hydrogen, a hydroxy group, a branched or unbranched -C 4 alkyl group, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert "-butyl or a branched or unbranched C 1 -C 4 alkoxy group, for example, methoxy , Ethoxy, propoxy, isopropoxy, butoxy, isobutoxy or tert- butoxy.
- R 1 is hydrogen, hydroxy, methyl or methoxy, most preferably hydrogen.
- R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl.
- R 2 is hydrogen, methyl or ethyl, most preferably hydrogen.
- the groups Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 are each independently a direct bond or an oxygen or sulfur atom. Preference is given to compounds in which at least one of Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 is an oxygen atom. Particular preference is given to compounds in which exactly one of Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 is an oxygen atom and the other radicals are a direct bond.
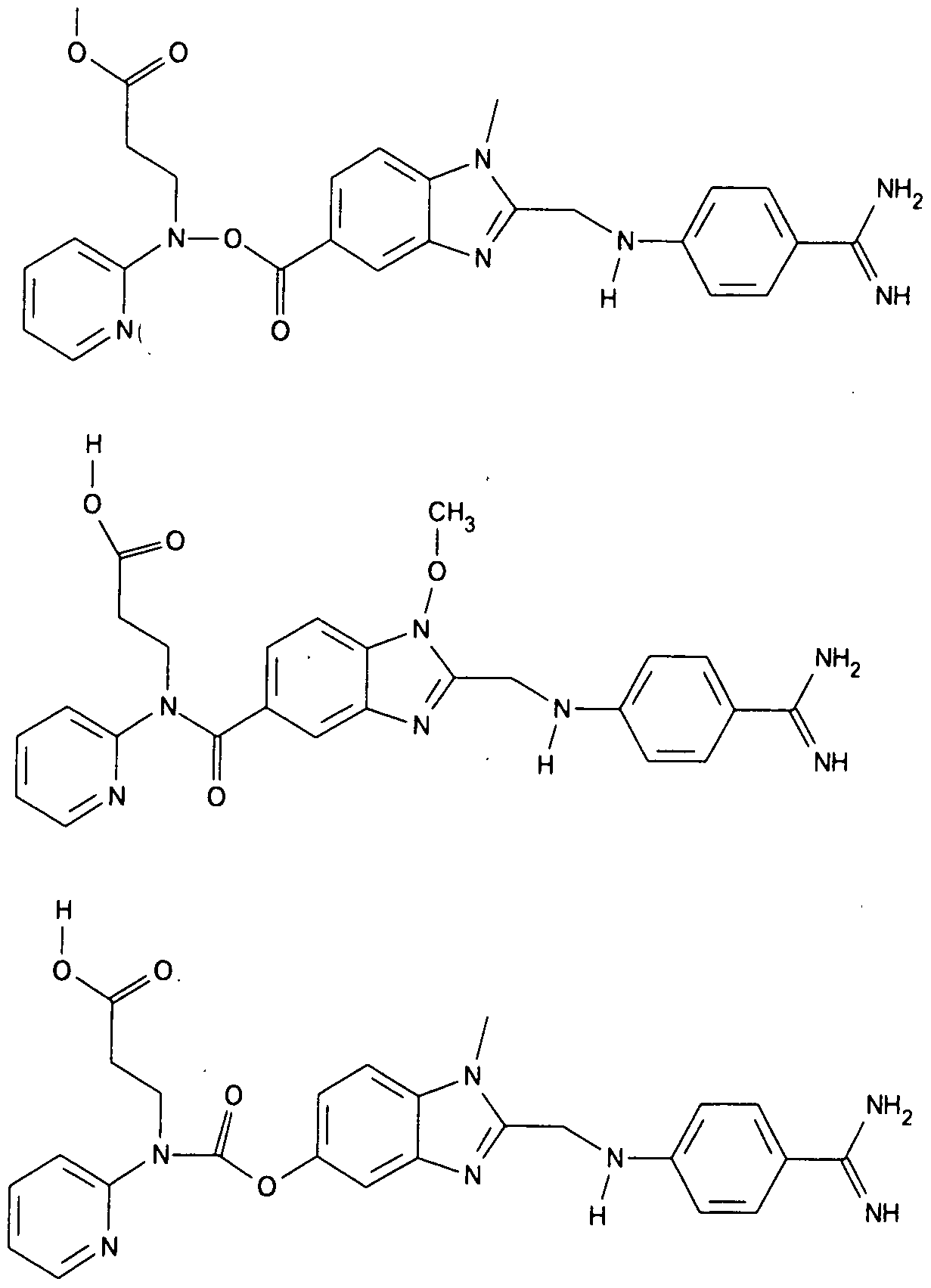
- Particularly preferred compounds of the general formula II are the following:
- Bond or represents an oxygen or a sulfur atom
- R 1 represents a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- Each R 2 is independently a hydrogen atom or a branched or unbranched d-C ⁇ -alkyl radical
- R 5 is a hydrogen atom, -OH, -OR 6 or a group -CO-R 6 , in which R 6 is a branched or unbranched C 1 -C 6 -alkyl radical or a branched or unbranched C 1 -C 8 -alkoxy radical,
- Each X 1 , X 2 is independently a direct bond or a - (Ch 1) n - chain, where n is a natural number 1, 2, 3 or 4,
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched C 1 -C 4 alkyl radical, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched dC 4 alkoxy, for example methoxy , Ethoxy, propoxy, isopropoxy, butoxy, isobutoxy or ter1 " butoxy.
- R 1 is hydrogen, hydroxy, methyl or methoxy, most preferably hydrogen.
- the group R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl, Preferably R 2 is hydrogen, methyl or ethyl, completely especially preferred for hydrogen.
- the group R 5 may be hydrogen, a hydroxy group, a branched or unbranched d-C ⁇ alkyl radical, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert- butyl, "pentyl,” ylexyl, “pteptyl,” octyl, or ' so' octyl or a branched or unbranched C 1 -Ce alkoxy, for example, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, tert -butoxy, 'pentoxy,' ⁇ exoxy, 'heptoxy,' ' octoxy, or / so R 5 preferably represents linear alkoxy groups having 5-8 carbon atoms ("pentoxy,” oxyexoxy, "pteptoxy,” octoxy).
- the groups Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 , Z 7 , Z 8 are each independently a direct bond or an oxygen or sulfur atom. Preference is given to compounds in which at least one of Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 , Z 7 , Z 8 is an oxygen atom. Particular preference is given to compounds in which exactly one of Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 , Z 7 , Z 8 is an oxygen atom and the other radicals are a direct bond.
- Preferred compounds of general formula III are the following:
- Z 1 , Z 2 , Z 3 are each independently a direct bond or an oxygen or sulfur atom
- R 1 is a hydrogen atom, -OH, a branched or unbranched C r C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R ' is a hydrogen atom or a branched or unbranched C r C4-alkyl radical
- R 6 is hydrogen or a branched or unbranched
- Ci-C 4 alkyl group means
- R Ar is a hydrogen atom, -Cl, -F 1 -Br, -CF 3 or -OCF 3 ,
- R N is an optionally one or more times -R Ar or
- L 1 -R Ar is substituted C 5 -C 7 -heterocycloalkyl radical, in which L 1 and R Ar have the abovementioned meanings,
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched C 1 -C 4 alkoxy radical, for example methoxy, ethoxy, Propoxy, isopropoxy, butoxy, isobutoxy or tert- butoxy stand.
- R 1 is hydrogen, hydroxy, methyl or methoxy, most preferably hydrogen.
- R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl
- R 2 is hydrogen, methyl or ethyl, very particularly preferably Hydrogen.
- the groups Z 1 , Z 2 , Z 3 each independently represent a direct bond or an oxygen or a sulfur atom.
- the linkers L 1 , L 2 and L 3 is an ether, ester, amine, amide, carbonyl, carbamate or hydroxamate group.
- R 6 represents a hydrogen atom or a straight-chain or branched alkyl chain, for example a methyl, ethyl, "propyl, ' “ propyl, “butyl,' “ butyl, or (eft ”) butyl group
- R 6 represents a hydrogen atom or a methyl group.
- the group R Ar is preferably a hydrogen atom, -F, -CF 3 or -OCF 3 , -CH 3 or -OCH 3 , -CO-CH 3 .
- the group R N is an optionally mono- or polysubstituted with R Ar or -L 1 -R Ar substituted C 5 -C 7 heterocycloalkyl.
- the C 5 -C 7 -heterocycloalkyl radical may be a cyclopentyl, cyclohexyl or cycloheptyl radical which may contain 1 to 3 nitrogen atoms as ring atoms.
- the C 5 -C 7 heterocycloalkyl radical may be monosubstituted or polysubstituted by R Ar or -L 1 -R Ar , where L 1 and R Ar have the abovementioned meanings.
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched C 1 -C 4 alkyl radical, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched C 1 -C 4 alkoxy radical, for example methoxy, ethoxy , Propoxy, isopropoxy, butoxy, Isobutoxy or tert- butoxy
- R 1 is hydrogen, hydroxy, methyl or methoxy, most preferably hydrogen.
- the group R 2 can be hydrogen or a branched or unbranched C 1 -C 4 -alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl, R 2 being particularly preferably hydrogen, methyl or ethyl preferred for hydrogen.
- the group R 4 may be -Cl, -F, -Br, -CF 3 , -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 , with -OCH 3 being preferred.
- the groups Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 are each independently a direct bond or an oxygen or sulfur atom.
- Preferred compounds of the general formula V are the following:
- Z 2 , Z 3 , Z 4 are each independently of one another a direct bond or an oxygen or a sulfur atom,
- R 1 represents a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- X 1 is a direct bond or a - (CH 2 J n - chain, where n is a natural number 1, 2, 3 or 4,
- R 6 is hydrogen or a branched or unbranched
- C 1 -C 4 -alkyl group means
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched dC 4 alkyl radical, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched C 1 -C 4 alkoxy radical, for example methoxy, ethoxy, Propoxy, isopropoxy, butoxy, isobutoxy or tert- butoxy
- R 1 is hydrogen, hydroxy
- the group R 4 may be -Cl, -F, -Br, -CF 3 , -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 , with -F and -CF 3 being preferred.
- the groups Z 1 , Z 2 , Z 3 , Z 4 are each independently a direct bond or an oxygen or sulfur atom.
- radicals Z 1 , Z 2 , Z 3 , Z 4 represent an oxygen atom.
- radicals Z 1 , Z 2 , Z 3 , Z 4 is an oxygen atom and the other radicals are a direct bond.
- the linker L 1 represents an ether, ester, amine, amide, carbonyl, carbamate or hydroxamate group.
- R 6 represents a hydrogen atom or a straight-chain or branched alkyl chain, for example a methyl, ethyl, "propyl, 'propyl,” ' butyl, ' “ butyl, or' e / Y ' butyl group.
- R 6 is a hydrogen atom or a methyl group.
- Preferred compounds of general formula VI are the following:
- Z 1 , Z 3 , Z 4 , Z 5 are each independently a direct bond or an oxygen or a sulfur atom
- R 1 is a hydrogen atom
- -OH 1 is a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- X 1 , X 2 independently for a direct bond or for a
- the group R 1 can be a hydroxyl group, a branched or unbranched -C 4 alkyl group, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert ⁇ butyl or a branched or unbranched C 1 -C 4 alkoxy, hydrogen, for example, methoxy , Ethoxy, propoxy, isopropoxy, butoxy, isobutoxy or tert -butoxy
- R 1 is hydrogen, hydroxy
- the group R 4 may be -Cl, -F, -Br, -CF 3 , -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 , with -F and -CF 3 being preferred.
- the groups Z 1 , Z 2 , Z 3 , Z 4 , Z 5 are each independently a direct bond or an oxygen or a sulfur atom. Preference is given to compounds in which at least one of Z 1 , Z 2 , Z 3 , Z 4 , Z 5 is an oxygen atom. Particular preference is given to compounds in which exactly one of the radicals Z 1 , Z 2 , Z 3 , Z 4 , Z 5 is an oxygen atom and the other radicals are a direct bond.
- Preferred compounds of the general formula VII are the following:
- Z 1 , Z 2 , Z 3 are each independently a direct bond or an oxygen or sulfur atom
- R 1 represents a hydrogen atom, -OH, a branched or unbranched alkyl radical CRC4 or a branched or unbranched C r C 4 alkoxy
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R 4 is -Cl, -F, -Br 1 -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl,
- Alkoxy for example, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy or tert- butoxy.
- R 1 is hydrogen or hydroxy.
- the group R 2 can be hydrogen or a branched or unbranched C 1 -C 4 -alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl, R 2 being particularly preferably hydrogen, methyl or ethyl preferred for hydrogen.
- the group R 4 may be -Cl, -F 1 -Br, -CF 3 , -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 , with -F and -CF 3 being preferred.
- the groups Z 1 , Z 2 , Z 3 each independently represent a direct bond or an oxygen or a sulfur atom.
- Preferred compounds of the general formula VIII are the following:
- Z 1 1 , Z 72 are each, independently of one another, a direct bond or an oxygen or a sulfur atom, R 2 independently of one another represents a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical,
- the group R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl,
- R 2 is hydrogen, methyl or ethyl, completely R 2 on the carboxyl group particularly preferably stands for hydrogen at all other positions for methyl.
- the groups Z 1 , Z 2 are each independently a direct bond or an oxygen or a sulfur atom.
- radicals Z 1 , Z 2 are an oxygen atom.
- Particularly preferred are compounds in which exactly one of the radicals Z 1 , Z 2 is an oxygen atom and the other radical is a direct bond.
- Preferred compounds of general formula IX are the following:
- each independently of one another represents a direct bond or represents an oxygen or a sulfur atom
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched C 1 -C 4 alkyl radical, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched C 1 -C 4 alkoxy, for example Methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy or tert- butoxy stand.
- a branched or unbranched C 1 -C 4 alkyl radical for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched C 1 -C 4 alkoxy, for example Methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy or tert- butoxy stand.
- R 1 is hydrogen or hydroxy
- R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl.
- R 2 is hydrogen, methyl or ethyl, most preferably hydrogen.
- the group R 4 may be -Cl, -F, -Br, -CF 3 , -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 , with -OCH 3 and -Cl being preferred.
- the groups Z 1 , Z 2 are each independently a direct bond or an oxygen or a sulfur atom.
- radicals Z 1 , Z 2 are an oxygen atom.
- Particularly preferred are compounds in which exactly one of the radicals Z 1 , Z 2 is an oxygen atom and the other radicals are a direct bond.
- Preferred compounds of the general formula X are the following:
- each 72 is independently a direct bond or an oxygen or a sulfur atom
- R 1 represents a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- the group R 1 may be hydrogen, a hydroxy group, a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl or a branched or unbranched C 1 -C 4 alkoxy radical, for example methoxy, ethoxy, Propoxy, isopropoxy, butoxy, isobutoxy or ter1 butoxy
- R 1 is hydrogen or hydroxy
- the group R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert- butyl,
- R 2 is hydrogen, methyl or ethyl, completely especially preferred for hydrogen.
- the group R 4 may be -Cl, -F, -Br, -CF 3 , -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 , with -OCH 3 and -Cl being preferred.
- the groups Z 1 , Z 2 are each independently a direct bond or an oxygen or a sulfur atom.
- radicals Z 1 , Z 2 are an oxygen atom.
- Particularly preferred are compounds in which exactly one of the radicals Z 1 , Z 2 is an oxygen atom and the other radicals are a direct bond.
- Preferred compounds of the general formula XI are the following:
- R 2 each independently represents a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical, where the group also be replaced by a radical R 2 can surprisingly have excellent drug properties. They are particularly suitable for the production of factor Xa inhibitors, for example for influencing blood clotting and for the treatment of acute coronary syndrome.
- the compounds of general formula XII are also suitable as contrast agents in magnetic resonance imaging (MRI).
- MRI magnetic resonance imaging
- the use of the compounds of the general formula XII according to the invention not only alleviates thromboembolic disorders, but also improves the contrast during intraoperative MRI control. This is particularly advantageous because the patient's body does not have to be loaded with additional contrast agent.
- the use of heavy metal-containing (especially gadolinium restroomn) contrast agents is avoided. This is advantageous, especially in patients with impaired renal function.
- the group R 2 may be hydrogen or a branched or unbranched C 1 -C 4 alkyl radical, for example methyl, ethyl, propyl, isopropyl, butyl,
- R 2 is preferably hydrogen, methyl or ethyl, very particularly preferably R 2 is methyl on the carboxyl group and nitrogen is a hydrogen atom on nitrogen.
- novel compounds of general formulas I-XII are useful as pharmaceuticals. They are particularly useful for the preparation of drugs for the inhibition of factor Xa. Thus, they are suitable for the prophylaxis or treatment of diseases that are positively influenced by inhibition of factor Xa.
- the compounds of the general formula I - XI are particularly suitable for the preparation of medicaments for the prophylaxis and / or treatment of thromboembolic disorders, in particular acute coronary syndrome, myocardial infarction, angina pectoris, reocclusions and restenoses (after angioplasty or aortocoronary bypass) stroke, transient ischemic attacks, Peripheral arterial occlusive diseases, pulmonary embolism or deep venous thrombosis. They are also useful in the treatment of atrial fibrillation and arrhythmia, and their benefits are also evident when used in the context of major surgical procedures, such as orthopedic surgery (joint replacement, etc.).
- the compounds of the formula I-XII are also suitable for the treatment of disseminated intravascular coagulation (DIC).
- DIC disseminated intravascular coagulation
- the compounds are also useful in preventing blood coagulation in vitro, particularly in the case of blood conserves or biological samples.
- the compounds of the general formulas I - XII according to the invention are suitable for the treatment of thrombocytopenia. This applies in particular to the compounds of general formula IX.
- the compound of the general formula XII is moreover suitable as an unpaired electron on the N-oxide group
- Contrast agent in magnetic resonance imaging MRI
- thromboembolic diseases such as stenoses, thromboses, etc.
- the use of the compounds of the general formula XII according to the invention not only alleviates the thromboembolic disorders, but also improves the contrast in the intraoperative MRI control.
- the compounds are suitable for acute and chronic diseases.
- the present invention teaches a pharmaceutical composition containing at least one compound of the invention.
- one or more physiologically acceptable excipients and / or carriers may be mixed with the compound and the mixture galenical to local or systemic Gabe, in particular orally, parenterally, for infusion, prepared for injection.
- the choice of additives and / or adjuvants will depend on the chosen dosage form.
- the galenic preparation of the pharmaceutical composition according to the invention is carried out in the usual way.
- Free carboxylic acid groups may also be present in the form of their salts with physiologically acceptable counterions such as Mg ++ , Ca ++ , Na + , K + , Li + or ammonium derivatives such as cyclohexylammonium.
- Amino-containing compounds may also be present in the form of an ammonium salt, for example as chloride, bromide, mesylate, tosylate, oxalate, orotate or tartrate.
- Suitable solid or liquid pharmaceutical preparation forms are, for example, granules, powders, dragees, tablets, microcapsules, suppositories, syrups, juices, suspensions, emulsions, drops or solutions for injection (iV, ip, im, sc) or nebulization (aerosols), forms of preparation for Dry powder inhalation, transdermal systems as well as preparations with sustained-release release, in the production of which conventional auxiliaries such as carriers, blasting agents, binders, coating substances, swelling or lubricants, flavorings, sweeteners and solubilizers are used.
- excipients examples include magnesium carbonate, titanium dioxide, lactose, manidine and other sugars, talc, milk protein, gelatin, starch, cellulose and its derivatives, animal and vegetable oils such as cod liver oil, sunflower, peanut or sesame oil, polyethylene glycols and solvents such as sterile water and monohydric or polyhydric alcohols, for example glycerol.
- a pharmaceutical composition according to the invention can be prepared by mixing at least one substance combination used according to the invention in a defined dose with a pharmaceutically suitable and physiologically acceptable carrier and optionally further suitable active ingredients, additives or excipients with a defined dose and prepared to the desired administration form.
- Suitable diluents are polyglycols, ethanol, water and buffer solutions.
- Suitable buffer substances are, for example, N 1 N-
- the pharmaceutical composition is prepared and administered in dosage units, each unit containing as active ingredient a defined dose of the compound of formula I according to the invention.
- this dose may be from 0.1 to 1000 mg, preferably from 1 to 300 mg, and in the case of injection solutions in the form of ampoules from 0.01 to 1000 mg, preferably from 1 to 100 mg.
- daily doses for the treatment of an adult, patients weighing 50-100 kg, for example 70 kg, daily doses of 0.1-1,000 mg active substance, preferably 1-500 mg, are indicated. However, higher or lower daily doses may be appropriate.
- the administration of the daily dose can be carried out by single administration in the form of a single unit dose or several smaller dosage units as well as by multiple subdivided doses at specific intervals.
- compounds of the invention may be combined with other drugs known per se.
- the compound according to the invention can be mixed with the active substance in the context of a single galenic preparation.
- the pharmaceutical composition consists of two (or more) different galenic preparations, wherein in a first preparation the compound according to the invention and in a second preparation of the active ingredient are contained. In the context of the first preparation, it is also possible to set up a substance which is different from the active ingredient of the second preparation.
- the preparations according to the invention can be prepared, for example, as follows:
- Drageekern contains: • active substance 75,0 mg • Calcium phosphate 93.0 mg
- the active substance is mixed with calcium phosphate, corn starch, polyvinylpyrrolidone, hydroxypropylmethylcellulose and half of the stated amount of magnesium stearate.
- a tableting machine compacts are produced with a diameter of about 13 mm, these are ground on a suitable machine through a sieve with 1, 5 mm mesh size and mixed with the remaining amount of magnesium stearate. This granulate is pressed on a tabletting machine into tablets of the desired shape.
- Core weight 230 mg
- the coated dragee cores are coated with a film consisting essentially of hydroxypropylmethylcellulose.
- the finished film dragees are shined with beeswax. Dragee weight: 245 mg.
- Composition 1 tablet contains:
- 1 tablet contains: • active substance 150.0 mg
- the active substance mixed with milk sugar, corn starch and silicic acid is moistened with a 20% strength aqueous solution of polyvinylpyrrolidone and beaten through a sieve of 1.5 mm mesh size.
- Tablet weight 300 mg hard gelatine capsules (with 150 mg active substance)
- 1 capsule contains:
- the active ingredient is mixed with the excipients, passed through a sieve of 0.75 mm mesh size and mixed homogeneously in a suitable device.
- the final mixture is filled into size 1 hard gelatin capsules. Capsule filling: approx. 320 mg
- 1 suppository contains:
- the active substance After the melting of the suppository mass, the active substance is homogeneously distributed therein and the melt is poured into precooled forms.
- Dest. Water is heated to 70 0 C.
- methyl p-hydroxybenzoate and propyl ester and also glycerol and carboxymethylcellulose sodium salt are dissolved with stirring. It is cooled to room temperature and added with stirring, the active ingredient and dispersed homogeneously. After adding and loosening the Sugar, the sorbitol solution and the aroma, the suspension is evacuated to vent with stirring.
- the active ingredient is dissolved in the required amount of 0.01 N HCl, isotonic with saline, sterile filtered and filled into 10 ml ampoules. production method
- the preparation of the further compounds of the general formula I - XII according to the invention is carried out by the methods of organic chemistry known to the person skilled in the art. Attached to FIGS. 5 and 6 is a general synthesis scheme for the preparation of the compounds according to the invention, which the person skilled in the art can easily modify without having to be inventive.
- the starting compound anilinomorpholinone, which is related in FIG. 1, can be synthesized by the method mentioned in WO 01/47919. There are also other useful procedure notes, as well as in DE 10300111 A1.
- the target compound 5-chloro-N ( ⁇ 5R) -2-oxo [4- (3-oxomorpholin-4-yl) -phenyl] -1,3-oxazolidin-5-yl ⁇ shown in FIG. 5/6 - methoxy) -2-thiophenecarboxamide shows the analytical data according to FIGS. 1-4.
- LG Leaving group
- BOC benzyloxycarbonyl
- compounds which are selective are those compounds of the general formula I - XII in which the IC 50 values for the factor Xa inhibition against the IC 50 values for the inhibition of other serine proteases, in particular thrombin, plasmin and trypsin, to the 100 times, preferably around which are 500 times, in particular 1000 times smaller.
- the compounds of the general formula I - XII according to the invention are selective inhibitors of the blood coagulation factor Xa, which do not (or only in significantly higher constellations) inhibit other serine proteases, such as thrombin, plasmin or trypsin.
- the usual test methods are used, for example those described in WO 01/47919 (Bayer Aktiengesellschaft) in Examples A-1) a.1) and a.2).
- Z 1, Z v2 1 Z 7 3, 7 4 Z is independently a direct bond or represents an oxygen or a sulfur atom
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R 4 is -Cl, -F 1 -Br, -CF 3 or -OCF 3, -NO 2 or -OCH 3,
- n stands for the integers 0, 1, 2, 3 or 4.
- a compound of general formula I according to item 1 characterized in that R 2 is hydrogen, methyl or ethyl, most preferably hydrogen.
- a compound of general formula I according to item 1 characterized in that at least one of Z 1 , Z 2 , Z 3 , Z 4 is an oxygen atom.
- Z 1 Z 2 Z 3 Z 4 Z 5 Z 6 Z 7 each independently represents a direct bond or represents an oxygen or a sulfur atom
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 3 is a hydrogen atom, -NH 2 , -NHR 2 or -N (R 2 J 2 or a branched or unbranched C 1 -C 4 -alkyl radical in which R 2 has the abovementioned meaning,
- X 1 1 , X ⁇ / 2 each independently represent a direct bond or a - (CH 2 ) n - chain, where n stands for a natural number 1, 2, 3 or 4.
- R 1 is hydrogen, hydroxy, methyl or methoxy.
- Oxygen is and the other radicals are a direct bond.
- Z 7 2 z , Z 7 3 J , Z 7 4 ", Z 7 5 ö , Z -76 b , Z 7 7 ', Z -78 ö are each independently of one another for a direct
- Bond or represents an oxygen or a sulfur atom
- R 1 independently of one another represents a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- Each R 2 independently represents a hydrogen atom or a branched or unbranched C r C 4 alkyl radical
- R 5 is a hydrogen atom, -OH, -OR 6 or a group -CO-R 6 , wherein R 6 is a branched or unbranched C 1 -C 6 -alkyl radical or a branched or unbranched C 1 -C 8 -alkoxy radical .
- X 1 , X 2 each independently represent a direct bond or a - (CH 2 ) n - chain, where n stands for a natural number 1, 2, 3 or 4.
- a compound of general formula III, according to item 15, characterized in that X 1 is -CH 2 -CH 2 - (n 2).
- Compounds of the general formula IV in the Z 1 , Z 2 , Z 3 are each independently a direct bond or an oxygen or sulfur atom,
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C r C 4 -alkoxy radical,
- R 2 is a hydrogen atom or a branched or unbranched C r C 4 alkyl
- R 6 is hydrogen or a branched or unbranched
- Ci-C 4 alkyl group means
- R Ar is a hydrogen atom, -Cl 1 -F, -Br 1 -CF 3 or -OCF 3 , -NO 2 , -R 6 , -OR 6 , -CO 2 -R 6 or a group -CO-R 6 in which R 6 has the abovementioned meaning,
- R N is an optionally one or more times -R Ar or
- a compound according to item 24 characterized in that R 1 is hydrogen, hydroxy, methyl or methoxy. 26. A compound according to item 24, characterized in that R 2 is hydrogen, methyl or ethyl.
- a compound according to item 24 characterized in that exactly one of the radicals Z 1 , Z 2 , Z 3 is an oxygen atom.
- R N is selected from the group consisting of:
- Z, 1, Z -, 2, Z 7 3, Z - 74, Z - 7 5, Z - 7 6 are each independently of one another a direct bond or an oxygen or a sulfur atom,
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 6 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 2 is a hydrogen atom or a branched or unbranched C r C4-alkyl radical
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 .
- a compound according to item 32 characterized in that R 1 is hydrogen, hydroxy, methyl or methoxy.
- a compound according to item 32 characterized in that R 4 is -OCH 3 .
- a compound according to item 32 characterized in that exactly one of the radicals Z 1 , Z 2 , Z 3 , Z 4 , Z 5 , Z 6 is an oxygen atom.
- R 1 represents a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 4 is -Cl, -F, -Br, -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- X 1 is a direct bond or a - (CH 2 ) n - chain, where n is a natural number 1, 2, 3 or 4,
- R 6 is hydrogen or a branched or unbranched C 1 -C 4 -alkyl group.
- a compound according to item 38 characterized in that R 1 is hydrogen, hydroxy, methyl or methoxy.
- a compound according to item 38 characterized in that exactly one of the radicals Z ⁇ Z 2 , Z 3 , Z 4 stands for an oxygen atom.
- a compound according to item 43 characterized in that R 6 represents a hydrogen atom or a methyl group.
- Z 1 , Z 3 , Z 4 , Z 5 are each independently a direct bond or an oxygen or a sulfur atom
- R 1 represents a hydrogen atom, -OH, a branched or unbranched C 1 -C -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 4 is -Cl, -F, -Br 1 -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 ,
- X 1 , X 2 independently for a direct bond or for a
- a compound according to item 46 characterized in that R 4 is -F or -CF 3 .
- a compound according to item 46 characterized in that exactly one of the radicals Z 1 , Z 2 , Z 3 , Z 4 , Z 5 is an oxygen atom.
- Z 1 Z 2 Z 3 each independently represents a direct bond or represents an oxygen or a sulfur atom
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 8 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical,
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R 4 is -Cl, -F, -Br 1 -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 .
- a compound according to item 52 characterized in that R 1 is hydrogen, hydroxy, methyl or methoxy.
- a compound according to item 52 characterized in that R 2 is hydrogen, methyl or ethyl.
- a compound according to item 52 characterized in that R 4 is -F or -CF 3 .
- a compound according to item 52 characterized in that exactly one of the radicals Z 1 , Z 2 , Z 3 is an oxygen atom.
- each r is independently a direct bond or an oxygen or a sulfur atom
- R ' is independently a hydrogen atom or a branched or unbranched C r C4-alkyl radical.
- a compound according to item 58 characterized in that R 2 is hydrogen on the carboxyl group and methyl in all other positions.
- a compound according to item 58 characterized in that exactly one of the radicals Z 1 , Z 2 is an oxygen atom.
- Z 1 1 , Z 72 are each, independently of one another, a direct bond or an oxygen or a sulfur atom,
- R 1 represents a hydrogen atom, -OH, a branched or unbranched Ci-Cj-alkyl radical or a branched or unbranched Ci-Cj-alkoxy radical,
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R A is -Cl, -F, -Br 1 -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 .
- a compound according to item 62 characterized in that R 2 is hydrogen, methyl or ethyl.
- Z 1 , Z 2 are each independently a direct bond or an oxygen or sulfur atom
- R 1 is a hydrogen atom, -OH, a branched or unbranched C 1 -C 4 -alkyl radical or a branched or unbranched C 1 -C 4 -alkoxy radical
- R 2 is a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical
- R * is -Cl, -F, -Br 1 -CF 3 or -OCF 3 , -NO 2 , -OCH 3 or -OC 2 H 5 .
- R 2 each independently represents a hydrogen atom or a branched or unbranched C 1 -C 4 -alkyl radical, where can also be replaced by a residue R.
- replacement blade 77 Use of at least one compound of general formulas I-XII according to at least one of items 1-76 for the preparation of medicaments.
- article 77 Use according to article 77 for the preparation of medicaments for the treatment and / or prophylaxis of acute coronary syndrome, myocardial infarction, angina pectoris, reocclusions and restenoses (eg after angioplasty or aortocoronary bypass), stroke, transient ischemic attacks, peripheral arterial occlusive diseases, pulmonary embolisms or deep venous thrombosis, atrial fibrillation or arrhythmias.
- Hal -F, -Cl 1 -Br, -I, (independently of each other)
- n 1
- viral infections in particular RNA viruses, reroviruses, HIV, negative-stranded RNA viruses, multi-drug resistant viruses
- Z 1 bond
- Z 2 and / or Z 3 -O- or -S- and / or ii)
- -HaI -F and / or iii)
- n 1 and / or iv)
- R 2 -CH 3 (preferably all)
- viral infections in particular RNA viruses, reroviruses, HIV, negative-stranded RNA viruses, multi-drug resistant viruses
- Z 1 - Z 11 independently of one another -O-, -S- or bond, at least one of Z 1 - Z 11 no bond
- n 0, 1, 2, 3 or 4
Abstract
Die vorliegende Patentanmeldung betrifft neue Pharmazeutika, Verfahren zu Ihrer Herstellung und ihre Verwendung in der medizinischen Therapie, beispielsweise auf dem Gebiet der Blutgerinnung. Formel (I), in der Z1, Z2, Z3, Z4 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht, R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten C1-C4-Alkylrest steht, R4 für -Cl -F, -Br, -CF3 oder -OCF3, -NO2 oder -OCH3 steht, n für die ganzen Zahlen 0, 1, 2. 3 oder 4 steht.
Description
OXAZOLIDINONE ALS FAKTOR XA-INHIBITOREN, VERFAHREN ZU IHRER HERSTELLUNG UND IHRE VERWENDUNG IN DER THERAPIE
Die vorliegende Patentanmeldung betrifft neue Pharmazeutika, Verfahren zu Ihrer Herstellung und ihre Verwendung in der Therapie, beispielsweise auf dem Gebiet der Blutgerinnung.
Die Anmeldung nimmt folgende Prioritäten in Anspruch: DE 102007037373
{Anmeldetag: 6.8.2007), DE 102008019679 (Anmeldetag: 11.4.2008),
DE 102008033285 {Anmeldetag: 11.7.2008), DE 102008034030 {Arimeldetag:
17.7.2008). Hintergrund und Stand der Technik
Ein wichtiger Schutzmechanismus des menschlichen und tierischen Organismus ist die Blutgerinnung, die dafür sorgt, dass Defekte in der Gefäßwand rasch und zuverlässig geschlossen werden können. So werden Blutverluste des Organismus vermieden. Die Blutstillung nach Gefäßverletzung erfolgt durch ein Gerinnungs- system, ausgelöst durch eine eπzymatische Kaskade von Plasmaproteinen, die in komplexer Weise miteinander reagieren. Eine ganze Reihe von Blutgerinnungs- faktoren sind dabei beteiligt, von denen jeder nach Aktivierung die jeweils nächste Vorstufe von der inaktiven in die aktive Form überführt. Schlussendlich wird durch die Kaskade das lösliche Fibrinogen in unlösliches Fibrin umgewandelt, so dass es zu einem Blutgerinsel kommt.
Dem Blutgerinnungsfaktor Xa, der aus dem Proenzymfaktor X gebildet wird, kommt eine Schlüsselrolle zu, da zwei Gerinnungswege {intrinsisches und extrinsisches System) verbunden werden. Dabei spaltet die aktivierte Serinprotease Xa Prothrombin zu Thrombin. Letzteres spaltet wiederum Fibrinogen zu Fibrin. Weiterhin ist Thrombin ein Auslöser der Thrombozytenaggregation.
Ein komplexer Regulationsmechanismus regelt die Hämostase. Eins ungewollte Aktivierung des Gerinnungssystems kann die Bildung von Thromben oder Embolien bewirken. Dies kann zu Herzinfarkt, Angina pectoris, Reokklusionen und Restenosen, Schlaganfall, transitorisch ischämischen Attacken, peripheren arteriellen Verschlusskrankheiten, Lungenembolien oder tiefen venösen Throm-
bösen führen. Diese Erkrankungen werden nachfolgend auch thromboembolische Erkrankungen bezeichnet.
Diese thromboembolischen Erkrankungen sind die häufigste Ursache von Morbidität und Mortalität in den Industrieländern. Die aus dem Stand der Technik bekannten Antikoagulanzien, d.h. Stoffe zur Hemmung oder Verhinderung der Blutgerinnung weisen verschiedenste Nachteile auf, so dass sich die Behandlung und Prophylaxe von thromboembolischen Erkrankungen als sehr schwierig erweist. Bekannte pharmakologische Behandlungsmethoden von thromboembolischen Erkrankungen sind die Gabe von Heparin sowie von Vitamin K-Antago nisten. In jüngster Zeit wurde versucht, den oben beschriebenen Faktor Xa zu inhibieren. Es konnte dabei zwar gezeigt werden, dass verschiedenste Verbindungen als Faktor Xa Inhibitoren wirksam sind, diese haben aber eine Reihe von Nachteilen.
Es besteht daher weiterhin Bedarf an neuen Faktor Xa Inhibitoren. Aufgabe der vorliegenden Erfindung ist daher die Bereitstellung solcher Substanzen, die eine große therapeutische Bandbreite aufweisen, zur Behandlung von Krankheiten, die die Hemmung oder Verhinderung der Blutgerinnung erfordern. Aufgabe der vorliegenden Erfindung ist insbesondere die Bereitstellung solcher Substanzen, die mit erhöhter Selektivität den Blutgerinnungsfaktor Xa inhibieren und hierbei die Probleme der aus dem Stand der Technik bekannten Therapiemethoden für thromboembolische Erkrankungen zumindestens zum Teil vermeiden sollen.
Beschreibung der Erfindung
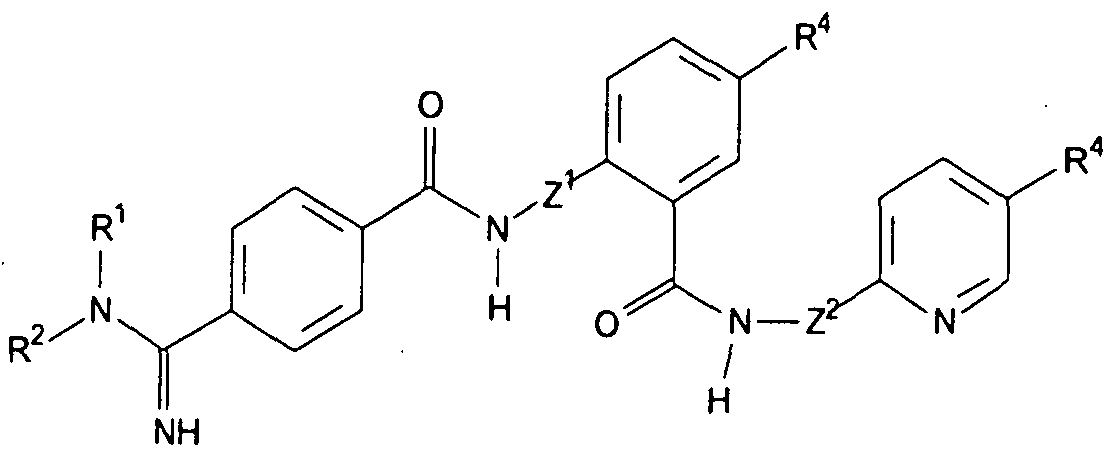
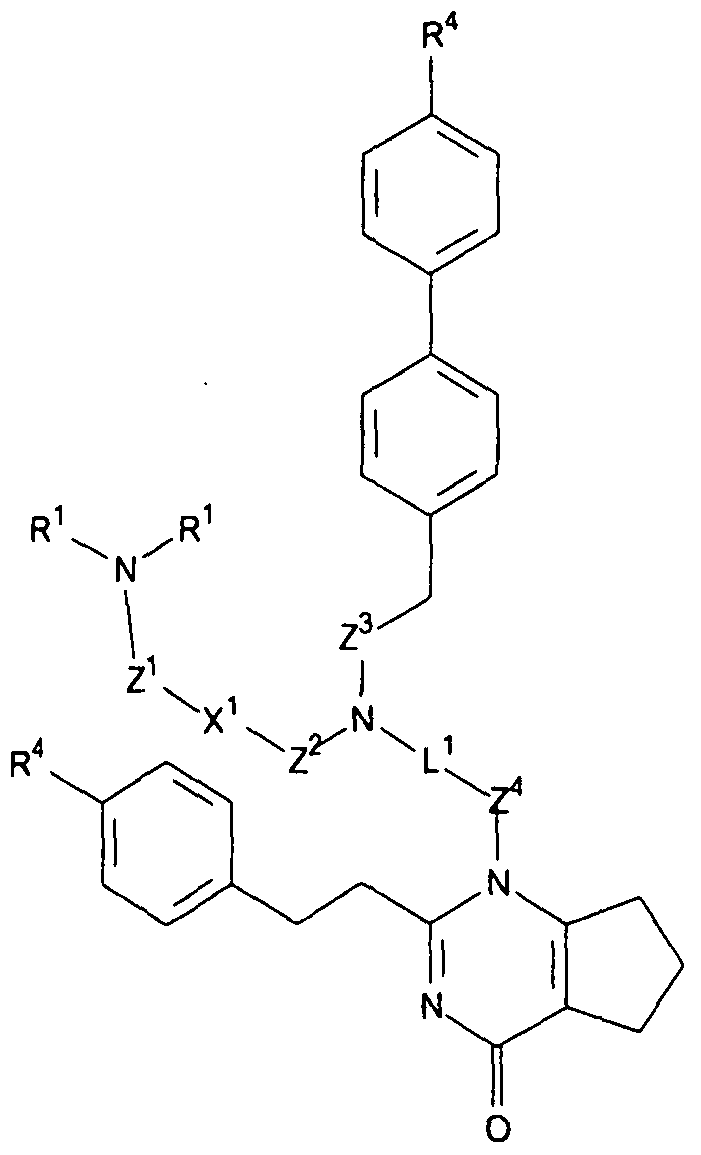
Es wurde gefunden, dass Verbindungen der allgemeinen Formel I
in der
Z1, Z2, Z3, Z4 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2 oder -OCH3 steht,
n für die ganzen Zahlen 0, 1 , 2, 3 oder 4 steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten CrC4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder ter1 "Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R4 kann für -Cl, -F, -Br, -CF3, -OCF3, -NO2 oder -OCH3 stehen, wobei Cl bevorzugt ist.
Die Gruppen Z1, Z2, Z3, Z4 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom. Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3, Z4 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3, Z4 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Die erfindungsgemäßen Verbindungen können durch das Vorhandensein von Asymmetriezentren als Stereoisomere vorliegen. Gegenstand der vorliegenden Erfindung sind alle möglichen Stereoisomere sowohl als Racemate, als auch in enantiomerenreiner Form. Der Begriff Stereoisomere umfaßt auch alle möglichen Diastereomere und Regioisomere und Tautomere (z.B. Keto-Enol-Tautomere), in denen die erfindungsgemäßen Verbindungen vorliegen können, die damit ebenfalls Gegenstand der Erfindung sind. Dies gilt auch für die unten genannten Verbindungen der alternativen Ausführungsformen Il-Xll.
Besonders bevorzugte Ausführungsformen der Formel I
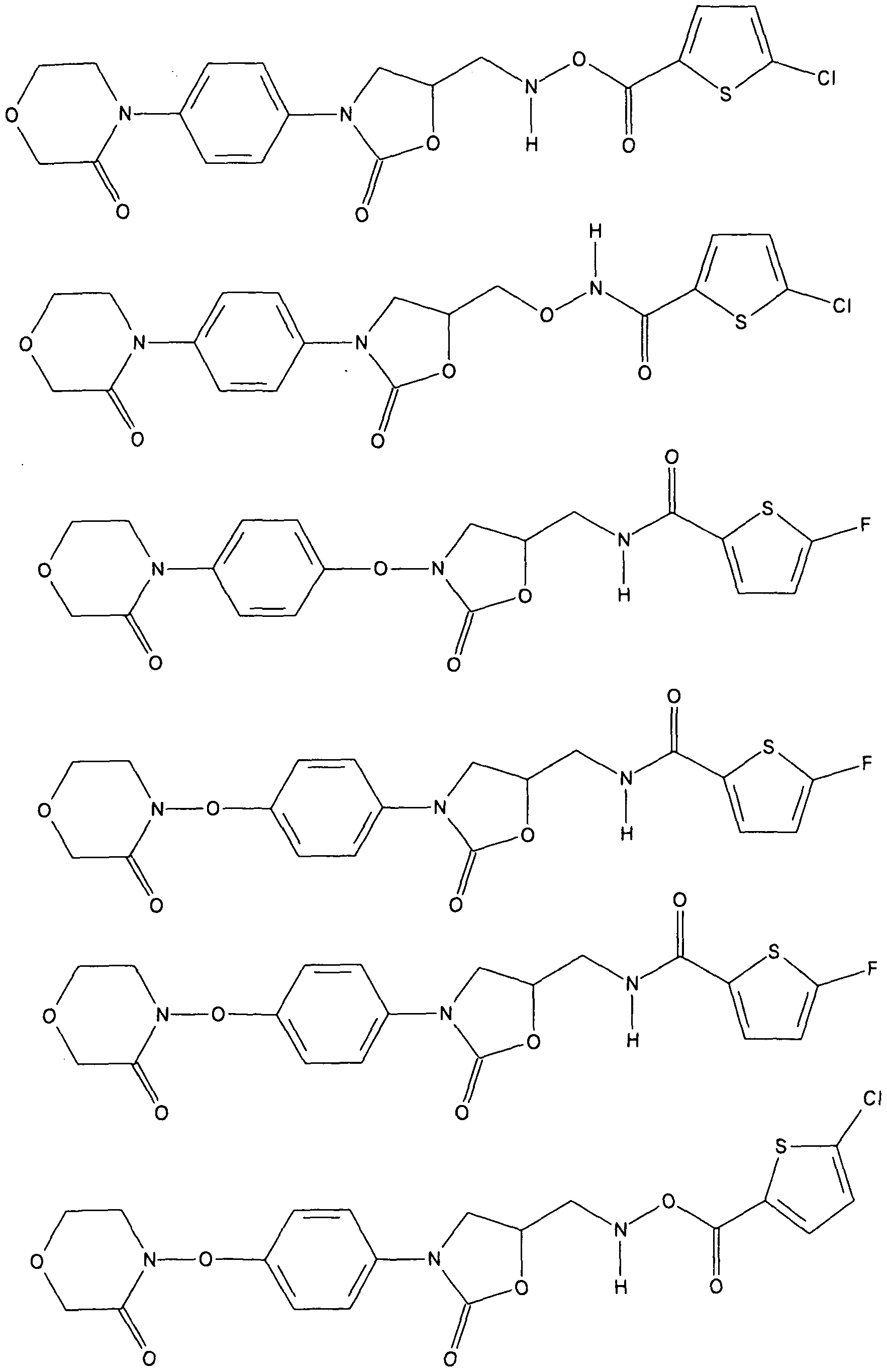
Besonders bevorzugte Ausführungsfomen der Verbindungen der allgemeinen Formel I sind die nachfolgend genannten:
Alternative Ausführungsform der allgemeinen Formel Il
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel Il
in der
Z ,11 Z -72 , Z v31 Z -74 , Z -751 Z -761 Z -77 jeweils unabhängig voneinander für eine direkte
Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten C-i-C-rAlkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 jeweils unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
R3 für ein Wasserstoffatom, -NH2, -NHR2 oder -N(R2J2 oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht, worin R2 die oben genannte Bedeutung hat,
X1, X2 jeweils unabhängig voneinander für eine direkte Bindung oder für eine -(CH2)n- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht,
überaschenderweise ebenfalls hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich gleichfalls insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten CrC4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten C1-C4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder tert "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff, Hydroxy Methyl oder Methoxy, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten C1-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppen Z1, Z2, Z3, Z4, Z5, Z6 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom. Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3, Z4, Z5, Z6 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3, Z4, Z5, Z6 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Die Gruppen X1, X2 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für eine Methylenkette ( -(CH2)n - ) mit 1 bis 4 Kettengliedern, bevorzugt stehen X1 oder X2 Wr -CH2- (n=1 ), besonders bevorzugt stehen X1 und X2fϋr-CH2- (n=1 ).
Besonders bevorzugte Verbindungen der allgemeinen Formel Il sind die nachfolgend abgebildeten:
20
Alternative Ausführungsform der allgemeinen Formel III
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel III
in der
Z »1 , Z -τ2 , Z 73J, Z -741 Z -,5 , Z -76 , Z -»71 Z -78 jeweils unabhängig voneinander für eine direkte
Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten C-i-C-i-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 jeweils unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten d-Cή-Alkylrest steht,
R5 für ein Wasserstoffatom, -OH, -OR6 oder eine Gruppe -CO-R6 steht, worin R6 für einen verzweigten oder unverzweigten CrCβ-Alkylrest oder einen verzweigten oder unverzweigten C-i -C8-Al koxyrest steht,
X1, X2 jeweils unabhängig voneinander für eine direkte Bindung oder für eine -(Ch^)n- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht,
überaschenderweise ebenfalls hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich gleichfalls insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten C1-C4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten d-C4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder ter1 "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff, Hydroxy Methyl oder Methoxy, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten C1-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder ter1 "Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R5 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten d-Cβ Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert "Butyl, " Pentyl, "Ηexyl, "Ηeptyl, "Octyl, oder 'so"Octyl oder einen verzweigten oder unverzweigten C1-Ce Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy, tert "Butoxy, " Pentoxy, "Ηexoxy, " Heptoxy, ""Octoxy, oder /so"Octoxy stehen. Bevorzugt steht R5 für lineare Alkoxygruppen mit 5-8 Kohlenstoffatomen (" Pentoxy, "Ηexoxy, "Ηeptoxy, "Octoxy).
Die Gruppen Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Die Gruppen X1, X2 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für eine Methylenkette ( -(CH2)n- ) mit 1 bis 4 Kettengliedern, bevorzugt stehen X1 oder X2 für -CH2-CH2-Cn=I oder 2), besonders bevorzugt stehen X1 für -CH2-CH2- (n=2) und X2 für -CH2- (n=1).
Bevorzugte Verbindungen der allgemeinen Formel III sind die nachfolgend abgebildeten:
Ganz besonders bevorzugte Verbindungen der allgemeinen Formel III sind die nachfolgend abgebildeten:
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel IV
in der
Z1, Z2, Z3 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoff atom, -OH, einen verzweigten oder unverzweigten CrC4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R' für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
L1 für
-N(R6)-
-O-
-C(=O)-
-O-C(=O)- oder -C(=O)-O-
-N(R6)-C(=O)- oder -C(=O)- N(R6)-, -N(R6)-C(=O)-O- oder -O-C(=O)- N(R6)-, -N(R6)-O- oder -N(R6)-O-,
-O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- worin
R6 Wasserstoff oder eine verzweigte oder unverzweigte
Ci-C4-Alkylgruppe bedeutet,
RAr für ein Wasserstoffatom, -Cl, -F1 -Br, -CF3 oder -OCF3,
-NO2, -R6, -OR6, -CO2-R6 oder eine Gruppe -CO-R6 ' steht, worin R6 die oben genannte Bedeutung hat,
RN für einen gegebenenfalls ein oder mehrfach mit -RAroder
-L1-RAr substituierten C5-C7-Heterocycloalkylrest steht, worin L1 und RAr die oben genannten Bedeutungen haben,
überraschenderweise ebenfalls hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich gleichfalls insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten CrC4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten CrC4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder tert "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff, Hydroxy Methyl oder Methoxy, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten CrC4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppen Z1, Z2, Z3 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Die Linker L1, L2 und L3 steht für eine Ether-, Ester-, Amin-, Amid-, Carbonyl-, Carbamat- oder Hydroxamatgruppe. Bevorzugt steht L für -N(R6)-, -O-, -C(=O)-, -N(R6)-C(=O)- oder -C(=O)- N(R6)-, -O-N(R6)-C(=O)- oder -C(=O)- N(R6J-O-. Ganz besonders bevorzugt steht L für -O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- .
Hierin steht R6 für ein Wasserstoffatom oder eine geradkettige oder verzweigte Alkylkette, zum Beispiel eine Methyl-, Ethyl-, " Propyl-, '"Propyl, " Butyl-, '"Butyl-, oder (eft"Butyl-Gruppe. Bevorzugt steht R6 für ein Wasserstoffatom oder eine Methylgruppe.
Die Gruppe RAr steht für bevorzugt für ein Wasserstoffatom, -F, -CF3 oder -OCF3, -CH3 oder -OCH3, -CO-CH3.
Die Gruppe RN steht für einen gegebenenfalls ein oder mehrfach mit RAr oder -L1-RAr substituierten C5-C7-Heterocycloalkylrest. Der C5-C7-Heterocycloalkylrest kann ein Cyclopentyl-, Cyclohexyl- oder Cycloheptylrest sein, welcher 1 bis 3 Stickstoffatome als Ringatome enthalten kann. Der C5-C7-Heterocycloalkylrest kann ein- oder mehrfach an beliebigen Stellen mit RAr oder -L1-RAr substituiert sein, wobei L1 und RAr die oben genannten Bedeutungen haben.
Bevorzugte Reste RN sind die nachfolgend dargestellten:
OCH,
-N N— OCH, / \ VO— N N-CH I,3 N N \ > 1^ N ™—— O wCv-Fr,3
- N
\
OCH3
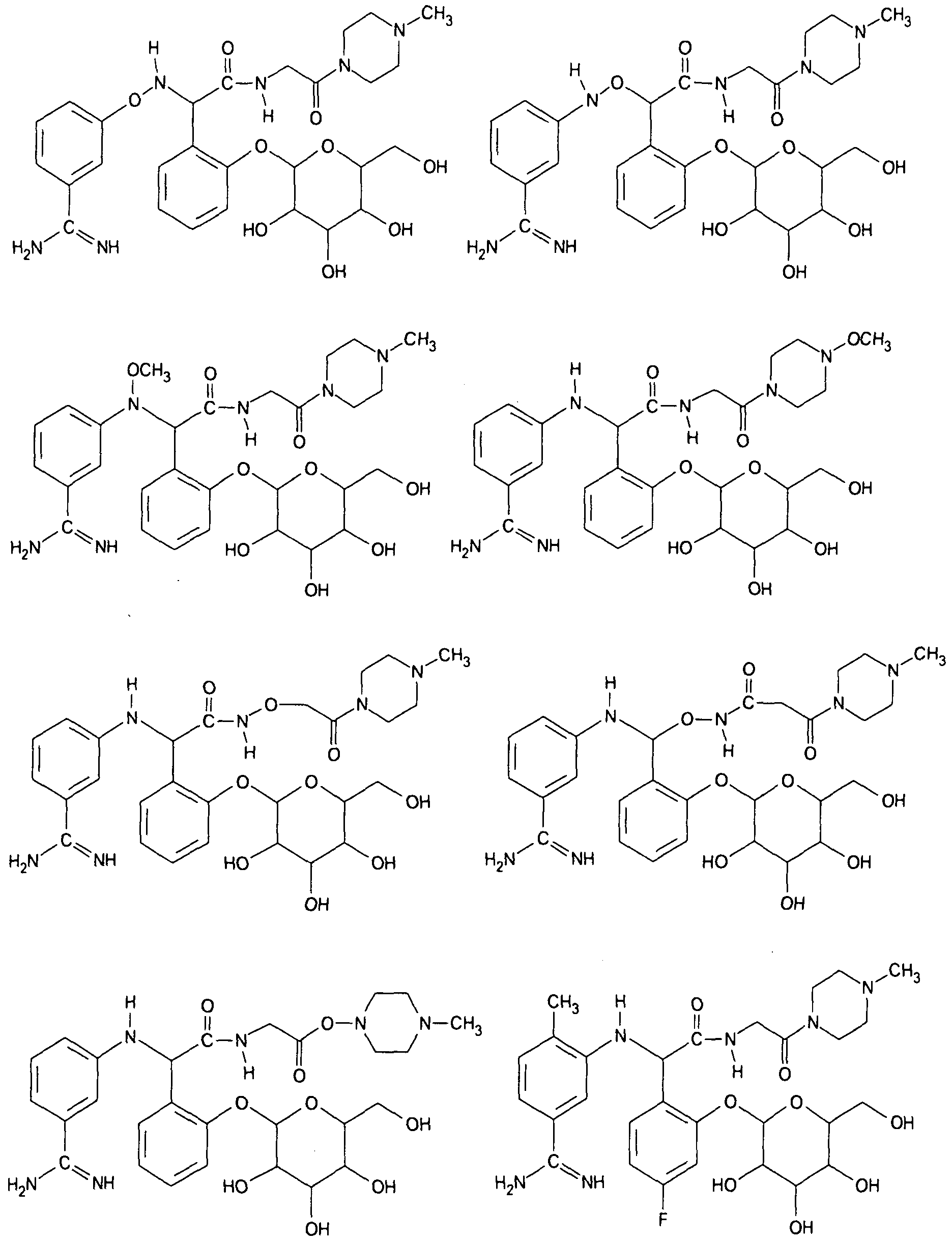
Bevorzugte Verbindungen der allgemeinen Formel IV sind die nachfolgend abgebildeten:
Alternative Ausführungsform der allgemeinen Formel V
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel V
in der
Z r11 Z -Ύ2 , Z -73 , Z -»4 , Z -751 Z -76 j ;eweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten Ci-C4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
R< für -Cl1 -F1 -Br1 -CF3 oder -OCF3, -NO2. -OCH3 oder -OC2H5 steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten C1-C4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten CrC4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy,
Isobutoxy oder tert "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff, Hydroxy Methyl oder Methoxy, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten Ci-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R4 kann für -Cl, -F, -Br, -CF3, -OCF3, -NO2, -OCH3 oder -OC2H5 stehen, wobei -OCH3 bevorzugt ist.
Die Gruppen Z1, Z2, Z3, Z4, Z5, Z6 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3, Z4, Z5, Z6 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3, Z4, Z5, Z6für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Bevorzugte Verbindungen der allgemeinen Formel V sind die nachfolgend abgebildeten:
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel VI
in der
Z1. Z2, Z3, Z4 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC4-Alky!rest oder einen verzweigten oder unverzweigten d-C4-Alkoxyrest steht,
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
X1 für eine direkte Bindung oder für eine -(CH2Jn- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht,
L1 für -N(R6)-
-o-
-C(=O)-
-O-C(=O)- oder -C(=O)-O-
-N(R6)-C(=O)- oder -C(=O)-N(R6)-, -N(R6)-C(=O)-O- oder -O-C(=O)-N(R6)-, -N(R6)-O- oder -N(R6)-O-,
-O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- worin
R6 Wasserstoff oder eine verzweigte oder unverzweigte
CrC4-Alkylgruppe bedeutet,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten d-C4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten CrC4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder tert Butoxy stehen. Bevorzugt steht R1 für Wasserstoff, Hydroxy
Die Gruppe R4 kann für -Cl, -F, -Br, -CF3, -OCF3, -NO2, -OCH3 oder -OC2H5 stehen, wobei -F und -CF3 bevorzugt sind.
Die Gruppen Z1, Z2, Z3, Z4 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3, Z4, für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1 , Z2, Z3, Z4 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Die Gruppe X1 steht für eine direkte Bindung oder für eine Methylenkette (-(CH2)n-) mit 1 bis 4 Kettengliedern, bevorzugt steht X1 für -CH2-CH2- (n=2).
Der Linker L1 steht für eine Ether-, Ester-, Amin-, Amid-, Carbonyl-, Carbamat- oder Hydroxamatgruppe. Bevorzugt steht L1 für -N(R6)-, -O-, -C(=O)-, -N(R6)-C(=O)- oder -C(=O)- N(R6)-,
-O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O-.
Ganz besonders bevorzugt steht L für -O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- .
Hierin steht R6 für ein Wasserstoffatom oder eine geradkettige oder verzweigte Alkylkette, zum Beispiel eine Methyl-, Ethyl-, " Propyl-, ' Propyl, "'Butyl-, '"Butyl-, oder 'e/Y"Butyl-Gruppe. Bevorzugt steht R6 für ein Wasserstoffatom oder eine Methylgruppe.
Bevorzugte Verbindungen der allgemeinen Formel VI sind die nachfolgend abgebildeten:
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel VII
in der
Z\ Z2, Z3, Z4, Z5 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH1 einen verzweigten oder unverzweigten CrC4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
X1, X2 unabhängig voneinander für eine direkte Bindung oder für eine
-(CH2Jn- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten CrC4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert ~Butyl oder einen verzweigten oder unverzweigten C1-C4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder tert "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff, Hydroxy
Die Gruppe R4 kann für -Cl, -F, -Br, -CF3, -OCF3, -NO2, -OCH3 oder -OC2H5 stehen, wobei -F und -CF3 bevorzugt sind.
Die Gruppen Z1, Z2, Z3, Z4, Z5 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom. Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3, Z4, Z5 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3, Z4, Z5 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Die Gruppen X1 und X2 stehen jeweils für eine direkte Bindung oder für eine Methylenkette (-(CH2)n-) mit 1 bis 4 Kettengliedern, bevorzugt steht X1 für -CH2- CH2- (n=2) und X2 für -CH2-CH2- (n=2).
Alternative Ausführungsform der allgemeinen Formel VIII
Z1, Z2, Z3 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten d-C4-Alkylrest steht,
R4 für -Cl, -F, -Br1 -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten CrC4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl,
Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten Ci-C 4
Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder tert "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff oder Hydroxy.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten Ci-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl. Bevorzugt steht R2 für Wasserstoff , Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R4 kann für -Cl, -F1 -Br, -CF3, -OCF3, -NO2, -OCH3 oder -OC2H5 stehen, wobei -F und -CF3 bevorzugt sind.
Die Gruppen Z1, Z2, Z3 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2, Z3 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2, Z3 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Alternative Ausführungsform der allgemeinen Formel IX
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel IX in der
in der
Z 11, Z 72 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R2 unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung, aber auch zur Behandlung der Thrombozytopenie.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten C1-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder ter1 "Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt steht R2 an der Carboxylgruppe für Wasserstoff an allen anderen Positionen für Methyl.
Die Gruppen Z1, Z2 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2 für ein Sauerstoffatom steht und der andere Rest für eine direkte Bindung stehen.
Bevorzugte Verbindungen der allgemeinen Formel IX sind die nachfolgend abgebildeten:
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel X
in der
z -?2 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten d-C4-Alkylrest oder einen verzweigten oder unverzweigten d-C4-Alkoxyrest steht,
für ein Wasserstoffatom oder einen verzweigten oder unverzweigten d-C-i-Alkylrest steht,
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten C1-C4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten C1-C4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder tert "Butoxy stehen. Bevorzugt steht R1 für Wasserstoff oder Hydroxy
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten C1-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R4 kann für -Cl, -F, -Br, -CF3, -OCF3, -NO2, -OCH3 oder -OC2H5 stehen, wobei -OCH3 und -Cl bevorzugt sind.
Die Gruppen Z1, Z2 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Bevorzugte Verbindungen der allgemeinen Formel X sind die nachfolgend abgebildeten:
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel Xl
in der
z 72 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten d-C4-Alkylrest steht,
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung.
Die Gruppe R1 kann für Wasserstoff eine Hydroxygruppe, einen verzweigten oder unverzweigten CrC4 Alkylrest, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl oder einen verzweigten oder unverzweigten CrC4 Alkoxyrest, beispielsweise für Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy oder ter1 Butoxy stehen. Bevorzugt steht R1 für Wasserstoff oder Hydroxy
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten C1-C4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert "Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt für Wasserstoff.
Die Gruppe R4 kann für -Cl, -F, -Br, -CF3, -OCF3, -NO2, -OCH3 oder -OC2H5 stehen, wobei -OCH3 und -Cl bevorzugt sind.
Die Gruppen Z1, Z2 stehen jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom.
Bevorzugt sind Verbindungen, bei denen mindestens einer der Reste Z1, Z2 für ein Sauerstoffatom steht. Besonders bevorzugt sind Verbindungen in denen genau einer der Reste Z1, Z2 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
Bevorzugte Verbindungen der allgemeinen Formel Xl sind die nachfolgend abgebildeten:
Es wurde ferner gefunden, dass Verbindungen der allgemeinen Formel XII
R2 jeweils unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C4-Alkylrest steht, wobei die Gruppe
auch durch einen Rest R2 ersetzt sein kann überraschenderweise hervorragende Arzneimitteleigenschaften aufweisen. Sie eignen sich insbesondere zur Herstellung von Faktor Xa Inhibitoren, beispielsweise zur Beeinflussung der Blutgerinnung und zur Behandlung des akuten Koronarsyndroms. Völlig überraschend eignen sich die Verbindungen der allgemeinen Formel XII darüber hinaus als Kontrastmittel bei der Magnetresonanztomographie (MRT). Bei der chirurgischen Behandlung thromboembolischer Erkrankungen, wie Stenosen, Thrombosen, etc. ist durch den Einsatz der erfindungsgemäßen Verbindungen der allgemeinen Formel XII nicht nur eine Linderung der thromboembolischer Erkrankungen gegeben, sondern auch eine Kontrastverbesserung bei der intraoperativen MRT-Kontrolle. Die is besonders vorteilhaft, weil der Körper des Patienten nicht mit zusätzlichem Kontrastmittel belastet werden muss. Zudem wird die Verwendung von schwermetallhaltigen (insbesondere gadoliniumhaltigen) Kontrastmitteln vermieden. Dies ist vorteilhaft, insbesondere bei Patienten mit eingeschränkter Nierenfunktion.
Die Gruppe R2 kann für Wasserstoff oder einen verzweigten oder unverzweigten CrC4 Alkylrest stehen, beispielsweise für Methyl, Ethyl, Propyl, Isopropyl, Butyl,
Ersatzblatt
IsobutyJ oder tert ~Butyl. Bevorzugt steht R2 für Wasserstoff, Methyl oder Ethyl, ganz besonders bevorzugt steht R2 an der Carboxylgruppe für Methyl, am Stickstoff für ein' Wasserstoffatom .
Die bevorzugte Verbindung der allgemeinen Formel XII ist nachfolgend abgebildet:
Verwendungen
Die neuartigen Verbindungen der allgemeinen Formeln I - XII sind als Arzneimittel verwendbar. Sie sind insbesondere verwendbar zur Herstellung von Arzneimitteln zur Inhibierung von Faktor Xa. Damit eignen sie sich zur Prophylaxe oder zur Behandlung von Erkrankungen, die durch Inhibierung von Faktor Xa positiv beeinflusst werden. Die Verbindungen der allgemeinen Formel I - Xl eignen sich insbesondere zur Herstellung von Arzneimitteln zur Prophylaxe und/oder Behandlung von thromboembolischen Erkrankungen, insbesondere akutes Koronarsyndrom, Herzinfarkt, Angina pectoris, Reokklusionen und Restenosen (nach Angioplastie oder aortokoronaren Bypass) Schlaganfall, transitorisch ischämische Attacken, periphere arterielle Verschlusskrankheiten, Lungenembolien oder tiefe venöse Thrombosen. Ferner eignen sie sich bei der Behandlung von Vorhofflimmern und Arhythmien, Ihre Vorteile kommen auch bei Anwendung im Rahmen größerer chirurgischer Eingriffe zur Geltung, z.B bei orthopädischen Eingriffen (Gelenkersatz o.a.).
Die Verbindungen der Formel I - XII eignen sich darüber hinaus zur Behandlung der disseminierten intravasalen Gerinnung (DIC). Die Verbindungen eignen sich darüber hinaus zur Verhinderung der Blutkoagulation in-vitro, insbesondere bei Blutkonserven oder biologischen Proben.
Ersatzblatt
Ferner eignen sich die erfindungsgemäßen Verbindungen der allgemeinen Formeln I - XII zur Behandlung der Thrombozytopenie. Die gilt insbesondere für die Verbindungen der allgemeinen Formel IX.
Völlig überraschend eignet sich die Verbindung der allgemeinen Formel XII darüber hinaus aufgrund des ungepaarten Elektrons an der N-Oxid Gruppe als
Kontrastmittel bei der Magnetresonanztomographie (MRT). Bei der chirurgischen Behandlung thromboembolischer Erkrankungen, wie Stenosen, Thrombosen, etc. ist durch den Einsatz der erfindungsgemäßen Verbindungen der allgemeinen Formel XII nicht nur eine Linderung der thromboembolischer Erkrankungen gegeben, sondern auch eine Kontrastverbesserung bei der intraoperativen MRT- Kontrolle.
Die Vorteile der Verbindungen der allgemeinen Formeln I - XII sind die nachfolgend genannten:
• Die Verbindungen sind oral verfügbar.
• Die Verbindungen sind im Regelfall nur einmal täglich einzunehmen.
• Es besteht keine Notwendigkeit die Patienten hinsichtlich ihres Gerinnungsstatus zu überwachen.
• Die Verbindungen verfügen über ein breites therapeutisches Fenster.
• Die Verbindungen sind für akute und chronische Erkrankungen geeignet.
• Die Verbindungen sind für klinische, aber auch für ambulante Anwendung geeignet.
• Die Verbindungen zeigen wenig Interaktionen mit anderen Arzneimitteln oder Nahrungsmitteln.
Formulierungen
Die vorliegende Erfindung lehrt eine pharmazeutische Zusammensetzung enthaltend mindestens eine erfindungsgemäße Verbindung. Optional können ein oder mehrere physiologisch verträgliche Hilfsstoffe und/oder Trägersstoffe mit der Verbindung gemischt und die Mischung galenisch zur lokalen oder systemischen
Gabe, insbesondere oral, parenteral, zur Infusion, zur Injektion hergerichtet sein. Die Auswahl der Zusatz- und/oder Hilfsstoffe wird von der gewählten Darreichungsform abhängen. Die galenische Herrichtung der erfindungsgemäßen pharmazeutischen Zusammensetzung erfolgt in fachüblicher Weise. Freie Carbonsäuregruppen können auch in Form ihrer Salze mit physiologisch verträglichen Gegenionen, wie z.B. Mg++, Ca++, Na+, K+, Li+ oder Ammoniumderivaten, wie Cyclohexylammonium vorliegen. Aminogruppenhaltige Verbindungen können auch in Form eines Ammoniumsalzes vorliegen, z.B. als Chlorid, Bromid, Mesylat, Tosylat, Oxalat, Orotat oder als Tartrat. Geeignete feste oder flüssige galenische Zubereitungsformen sind beispielsweise Granulate, Pulver, Dragees, Tabletten, Mikrokapseln, Suppositorien, Sirupe, Säfte, Suspensionen, Emulsionen, Tropfen oder Lösungen zur Injektion (i.V., i.p., i.m., s.c.) oder Vernebelung (Aerosole), Zubereitungsformen zur Trockenpulverinhalation, transdermale Systeme sowie Präparate mit retardierter Wirkstofffreigabe, bei deren Herstellung übliche Hilfsmittel wie Trägerstoffe, Spreng-, Binde-, Überzugs-, Quellungs-, Gleit- oder Schmiermittel, Geschmacksstoffe, Süßungsmittel und Lösungsvermittler Verwendung finden. Als Hilfsstoffe seien beispielsweise Magnesiumkarbonat, Titandioxyd, Laktose, Manid und andere Zucker, Talkum, Milcheiweiß, Gelatine, Stärke, Zellulose und ihre Derivate, tierische und pflanzliche Öle wie Lebertran, Sonnenblumen-, Erdnuss- oder Sesamöl, Polyethylenglykole und Lösungsmittel wie etwa steriles Wasser und ein- oder mehrwertige Alkohole, beispielsweise Glyzerin genannt.
Eine erfindungsgemäße pharmazeutische Zusammensetzung ist dadurch herstellbar, dass mindestens eine erfindungsgemäß verwendete Substanzkombination in definierter Dosis mit einem pharmazeutisch geeigneten und physiologisch verträglichen Träger und ggf. weiteren geeigneten Wirk-, Zusatzoder Hilfsstoffen mit definierter Dosis gemischt und zu der gewünschten Darreichungsform hergerichtet ist.
Als Verdünnungsmittel kommen Polyglykole, Ethanol, Wasser und Pufferlösungen in Frage. Geeignete Puffersubstanzen sind beispielsweise N1N-
Dibenzylethylendiamin, Diethanolamin, Ethylendiamin, N-Methylglukamin, N- Benzylphenethylamin, Diethylamin, Phosphat, Natriumbikarbonat und Natriumkarbonat. Es kann aber auch ohne Verdünnungsmittel gearbeitet werden.
Vorzugsweise wird die pharmazeutische Zusammensetzung in Dosierungseinheiten herstellt und verabreicht, wobei jede Einheit als aktiven Bestandteil eine definierte Dosis der erfindungsgemäßen Verbindung gemäß Formel I enthält. Bei festen Dosierungseinheiten wie Tabletten, Kapseln, Dragees oder Suppositorien kann diese Dosis 0,1 - 1.000 mg, bevorzugt 1 - 300 mg, und bei Injektionslösungen in Ampullenform 0,01 - 1.000 mg, vorzugsweise 1 - 100 mg, betragen.
Für die klinische Anwendung ist die Herstellung von Infusionslösungen eine weitere bevorzugte Ausfϋhrungsform.
Für die Behandlung eines Erwachsenen, 50 - 100 kg schweren, beispielsweise 70 kg schweren, Patienten sind beispielsweise Tagesdosen von 0,1 - 1.000 mg Wirkstoff, vorzugsweise 1 - 500 mg, indiziert. Unter Umständen können jedoch auch höhere oder niedrigere Tagesdosen angebracht sein. Die Verabreichung der Tagesdosis kann sowohl durch Einmalgabe in Form einer einzelnen Dosierungseinheit oder aber mehrerer kleinerer Dosierungseinheiten als auch durch Mehrfachgabe unterteilter Dosen in bestimmten Intervallen erfolgen.
Im Rahmen von pharmazeutischen Zusammensetzungen können erfindungsgemäße Verbindungen mit anderen, per se bekannten Wirkstoffen kombiniert werden. Dabei kann die erfindungsgemäße Verbindung in Rahmen einer einzigen galenischen Herrichtung mit der Wirksubstanz gemischt sein. Es ist aber auch möglich, dass die pharmazeutische Zusammensetzung aus zwei (oder mehr) verschiedenen galenischen Herrichtungen besteht, wobei in einer ersten Herrichtυng die erfindungsgemäße Verbindung und in einer zweiten Herrichtung der Wirkstoff enthalten sind. Dabei kann im Rahmen der ersten Herrichtung auch ein von dem Wirkstoff der zweiten Herrichtung verschiedener Wirkstoff eingerichtet sein.
Die erfindungsgemäßen Zubereitungen können beispielsweise wie folgt hergestellt werden:
Dragees (mit 75 mg Wirksubstanz)
1 Drageekern enthält: • Wirksubstanz 75,0 mg
• Calciumphosphat 93,0 mg
• Maisstärke 35,5 mg
• Polyvinylpyrrolidon 10,0 mg
• Hydroxypropylmethylcellulose 15,0 mg • Magnesiumstearat 1 ,5 mg
Gesamtgewicht: 230,0 mg
Herstellung:
Die Wirksubstanz wird mit Calciumphosphat, Maisstärke, Polyvinylpyrrolidon, Hydroxypropylmethylcellulose und der Hälfte der angegebenen Menge Magnesium stearat gemischt. Auf einer Tablettiermaschine werden Preßlinge mit einem Durchmesser von ca. 13 mm hergestellt, diese werden auf einer geeigneten Maschine durch ein Sieb mit 1 ,5 mm- Maschenweite gerieben und mit der restlichen Menge Magnesiumstearat vermischt. Dieses Granulat wird auf einer Tablettiermaschine zu Tabletten mit der gewünschten Form gepreßt. Kerngewicht: 230 mg
Stempel: 9 mm, gewölbt
Die so hergestellten Drageekerne werden mit einem Film überzogen, der im wesentlichen aus Hydroxypropylmethylcellulose besteht. Die fertigen Filmdragees werden mit Bienenwachs geglänzt. Drageegewicht: 245 mg.
Tabletten (mit 100 mg Wirksubstanz)
Zusammensetzung: 1 Tablette enthält:
• Wirksubstanz 100,0 mg
• Milchzucker 80,0 mg
• Maisstärke 34,0 mg • Polyvinylpyrrolidon 4,0 mg
• Magnesiumstearat 2,0 mg Gesamtgewicht: 220,0 mg
Herstellungverfahren:
Wirkstoff, Milchzucker und Stärke werden gemischt und mit einer wäßrigen Lösung des Polyvinylpyrrolidons gleichmäßig befeuchtet. Nach Siebung der feuchten Masse (2,0 mm-Maschenweite) und Trocknen im Hordentrockenschrank bei 5O0C wird erneut gesiebt (1 ,5 mm-Maschenweite) und das Schmiermittel zugemischt. Die preßfertige Mischung wird zu Tabletten verarbeitet.
Tablettengewicht: 220 mg
Tabletten (mit 150 mg Wirksubstanz)
Zusammensetzung:
1 Tablette enthält: • Wirksubstanz 150,0 mg
• Milchzucker pulv. 89,0 mg
• Maisstärke 40,0 mg
• Kolloide Kieselgelsäure 10,0 mg
• Polyvinylpyrrolidon 10,0 mg • Magnesiumstearat 1 ,0 mg
Gesamtgewicht: 300,0 mg
Herstellung:
Die mit Milchzucker, Maisstärke und Kieselsäure gemischte Wirksubstanz wird mit einer 20%igen wäßrigen Polyvinylpyrrolidonlösung befeuchtet und durch ein Sieb mit 1 ,5 mm-Maschenweite geschlagen.
Das bei 45 0C getrocknete Granulat wird nochmals durch dasselbe Sieb gerieben und mit der angegebenen Menge Magnesiumstearat gemischt. Aus der Mischung werdenTabletten gepreßt.
Tablettengewicht: 300 mg Hartgelatine -Kapseln (mit 150 mg Wirksubstanz)
1 Kapsel enthält:
• Wirkstoff 150,0 mg
• Maisstärke getr. ca. 180,0 mg
• Milchzucker pulv. ca. 87,0 mg • Magnesiumstearat 3,0 mg ca. 420,0 mg
Herstellung:
Der Wirkstoff wird mit den Hilfsstoffen vermengt, durch ein Sieb von 0,75 mm- Maschenweite gegeben und in einem geeigneten Gerät homogen gemischt.
Die Endmischung wird in Hartgelatine-Kapseln der Größe 1 abgefüllt. Kapselfüllung: ca. 320 mg
Suppositorien (mit 150 mg Wirksubstanz)
1 Zäpfchen enthält:
• Wirkstoff 150,0 mg
• Polyethylenglykol 1500 550,0 mg • Polyethylenglykol 6000 460,0 mg
• Polyoxyethylensorbitanmonostearat 840 mg Gesamtgewicht: 2000,0 mg
Herstellung:
Nach dem Aufschmelzen der Sυppositorienmasse wird der Wirkstoff darin homogen verteilt und die Schmelze in vorgekühlte Formen gegossen.
Suspension (mit 50 mg Wirksubstanz)
100 ml Suspension enthalten:
• Wirkstoff 1 ,00 g
• Carboxymethylcellulose-Na-Salz 0,10 g • p-Hydroxybenzoesäuremethylester 0,05 g
• p-Hydroxybenzoesäurepropylester 0,01 g
• Rohrzucker 10,00 g
• Glycerin 5,00 g
• Sorbitlösung 70%ig 20,00 g • Aroma 0,30 g
• Wasser dest. ad 100 ml Herstellung:
Dest. Wasser wird auf 700C erhitzt. Hierin wird unter Rühren p-Hydroxybenzoe- säuremethylester und -propylester sowie Glycerin und Carboxymethylcellυlose- Natriumsalz gelöst. Es wird auf Raumtemperatur abgekühlt und unter Rühren der Wirkstoff zugegeben und homogen dispergiert. Nach Zugabe und Lösen des
Zuckers, der Sorbitlösung und des Aromas wird die Suspension zur Entlüftung unter Rühren evakuiert.
5 ml Suspension enthalten 50 mg Wirkstoff. Ampullen (mit 10 mg Wirksubstanz) Zusammensetzung:
• Wirkstoff 10,0 mg
• 0,01 n Salzsäure s.q.
• Aqua bidest ad 2,0 ml Herstellung: Die Wirksubstanz wird in der erforderlichen Menge 0,01 n HCl gelöst, mit Kochsalz isotonisch gestellt, sterilfiltriert und in 2 ml Ampullen abgefüllt.
Ampullen (mit 50 mg Wirksubstanz)
Zusammensetzung:
• Wirkstoff 50,0 mg • 0,01 n Salzsäure s.q.
• Aqua bidest ad 10,0 ml Herstellung:
Die Wirksubstanz wird in der erforderlichen Menge 0,01 n HCl gelöst, mit Kochsalz isotonisch gestellt, sterilfiltriert und in 10 ml Ampullen abgefüllt. Herstellungsverfahren
Die Herstellung der weiteren erfindungsgemäßen Verbindungen der allgemeinen Formel I - XII erfolgt über die dem Fachmann bekannten Verfahren der organischen Chemie. Als Figur 5 und 6 beigefügt ist ein allgemeines Syntheseschema zur Herstellung der erfindungsgemäßen Verbindungen, welches der Fachmann leicht modifizieren kann ohne erfinderisch tätig werden zu müssen. Die in der Figur 1 verwandte Ausgangsverbindung Anilinomorpholinon kann durch die in WO 01/47919 genannte Methode synthetisiert werden. Dort finden sich auch weitere nützliche Verfahrenshinweise, wie auch in der DE 10300111 A1.
Die in der Figur 5/6 gezeigte Zielverbindung 5-Chloro-N({5R)-2-oxo[4-(3-oxo- morpholin-4-yl)phenyl]-1 ,3-oxazolidin-5-yl}-methoxy)-2-thiophencarboxamide zeigt die analytischen Daten gemäß den Figuren 1-4.
Ausgehend von diesem Schema kann der Fachmann auf dem Gebiet der organischen Chemie die Derivate der allgemeinen Formel I - XII in einfacher Weise herstellen.
Weitere synthetische Möglichkeiten zur Einführung der characteristischen C-O-N Gruppierung sind folgende:
4)
NH,
/
R OH R LG R ONH-BOC R O
5)
LG = Leaving group, BOC = Benzyloxycarbonyl
Zwei weitere Syntheseschemata für Verbindungen der allgemeinen Formel III sind auf den Figuren 7 und 8 ersichtlich.
Der Fachmann auf dem Gebiet der synthetischen organischen Chemie kann, ausgehend von seinem Fachwissen die in diesem Dokument genannten Verbindungen in üblicher Weise herstellen, ohne selbst erfinderisch werden zu müssen.
Assay
Die Verwendbarkeit der erfindungsgemäßen Verbindungen kann wie folgt untersucht werden:
Als „selektiv" werden im Rahmen dieses Dokuments solche Verbindungen der allgemeinen Formel I - XII bezeichnet, bei denen die IC50 Werte für die Faktor Xa Inhibierung gegenüber den IC50 Werten für die Inhibierung anderer Serinproteasen, insbesondere Thrombin, Plasmin und Trypsin, um das 100-fache, vorzugsweise um
das 500-fache, insbesondere um das 1000-fache kleiner sind. Somit sind die erfindungsgemäßen Verbindungen der allgemeinen Formel I - XII selektive Inhibitoren des Blutgerinnungsfaktors Xa, die nicht (oder erst bei deutlich höheren Konstellationen) andere Serinproteasen, wie z.B. Thrombin, Plasmin oder Trypsin hemmen. Zur Bestimmung der IC50 Werte werden die üblichen Testmethoden herangezogen, beispielsweise die in der WO 01/47919 (Bayer Aktiengesellschaft) in den Beispielen A-1) a.1) und a.2).
Gegenstände der Anmeldung:
Gegenstände der vorliegenden Anmeldung sind daher:
1. Verbindungen der allgemeinen Formel
Z ,1 , Z v21 Z 73 , Z 74 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C4-Alkylrest steht
R4 für -Cl, -F1 -Br, -CF3 oder -OCF3, -NO2 oder -OCH3 steht,
n für die ganzen Zahlen 0, 1 , 2, 3 oder 4 steht.
2. Verbindung der allgemeinen Formel I gemäß Gegenstand 1 , dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht, ganz besonders bevorzugt für Wasserstoff.
3. Verbindung der allgemeinen Formel I gemäß Gegenstand 1 , dadurch gekennzeichnet, dass mindestens einer der Reste Z1, Z2, Z3, Z4 für ein Sauerstoffatom steht.
4. Verbindung der allgemeinen Formel I gemäß Gegenstand 1 , dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3, Z4 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
5. Verbindung der allgemeinen Formel I gemäß Gegenstand 1 , dadurch gekennzeichnet, dass R4 für ein Chloratom steht.
6. Verbindung der allgemeinen Formel I gemäß Gegenstand 1 , nämlich
10
7. Verbindungen der allgemeinen Formel Il
in der
Z1 Z2 Z3 Z4 Z5 Z6 Z7 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten d-C4-Alkylrest oder einen verzweigten oder unverzweigten Ci-C4-Alkoxyrest steht,
jeweils unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C-i-Alkylrest steht
R3 für ein Wasserstoffatom, -NH2, -NHR2 oder -N(R2J2 oder einen verzweigten oder unverzweigten d-C4-Alkylrest steht, worin R2 die oben genannte Bedeutung hat,
X 11, X \/2 jeweils unabhängig voneinander für eine direkte Bindung oder für eine -(CH2)n- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht.
8. Verbindung der allgemeinen Formel II, gemäß Gegenstand 7, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy, Methyl oder Methoxy steht.
9. Verbindung der allgemeinen Formel II, gemäß Gegenstand 7, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
10. Verbindung der allgemeinen Formel II, gemäß Gegenstand 7, dadurch gekennzeichnet, dass mindestens einer der Reste Z1, Z2, Z3, Z4, Z5, Z6 für ein Sauerstoffatom steht.
11. Verbindung der allgemeinen Formel II, gemäß Gegenstand 10, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3, Z4, Z5, Z6 für ein
Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
12. Verbindung der allgemeinen Formel II, gemäß Gegenstand 7, dadurch gekennzeichnet, dass X1 oder X2für-CH2- (n=1) stehen.
13. Verbindung der allgemeinen Formel II, gemäß Gegenstand 7, dadurch gekennzeichnet, dass X1 und X2 für -CH2- (n=1 ) stehen.
14. Verbindung der allgemeinen Formel II, gemäß Anspruch 7, nämlich
15. Verbindungen der allgemeinen Formel III
in der
Z 72z, Z 73J, Z 74", Z 75ö, Z -76b, Z 77', Z -78öjeweils unabhängig voneinander für eine direkte
Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 unabhängig voneinander für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 jeweils unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
R5 für ein Wasserstoffatom, -OH, -OR6 oder eine Gruppe -CO-R6 steht, worin R6 für einen verzweigten oder unverzweigten Ci -Ce-Al kylrest oder einen verzweigten oder unverzweigten C1 -C8-Al koxyrest steht,
X1, X2 jeweils unabhängig voneinander für eine direkte Bindung oder für eine -(CH2)n- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht.
16. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy, Methyl oder Methoxy steht.
17. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
18. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass R5 für Wasserstoff, Methyl oder Ethyl steht.
19. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass R5 für -CO-C5Hn, -CO-C6Hi3, -CO-C7H15, oder -CO-C8H17 steht.
20. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
21. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass X1 für -CH2-CH2- (n=2) steht.
22. Verbindung der allgemeinen Formel III, gemäß Gegenstand 15, dadurch gekennzeichnet, dass X2 für -CH2- (n=1 ) steht.
23. Verbindung der aligemeinen Formel III gemäß Gegenstand 15, nämlich
C2H5
24. Verbindungen der allgemeinen Formel IV
in der
Z1, Z2, Z3 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten C1-C4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
L1 für
-N(R6)- -O-
-C(=O)-
-O-C(=O)- oder -C(=O)-O-
-N(R6)-C(=O)- oder -C(=O)-N(R6)-, -N(R6)-C(=O)-O- oder
-O-C(=O)-N(R6)-. -N(R6)-O- oder -N(R6)-O-, -O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- worin
R6 Wasserstoff oder eine verzweigte oder unverzweigte
Ci-C4-Alkylgruppe bedeutet,
RAr für ein Wasserstoffatom, -Cl1 -F, -Br1 -CF3 oder -OCF3, -NO2, -R6, -OR6, -CO2-R6 oder eine Gruppe -CO-R6 steht, worin R6 die oben genannte Bedeutung hat,
RN für einen gegebenenfalls ein oder mehrfach mit -RAroder
-L1-RAr substituierten C5-C7-Heterocycloalkylrest steht, worin L1 und RAr die oben genannten Bedeutungen haben.
25. Verbindung gemäß Gegenstand 24, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy Methyl oder Methoxy steht.
26. Verbindung gemäß Gegenstand 24, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
27. Verbindung gemäß Gegenstand 24, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3 für ein Sauerstoffatom steht.
28. Verbindung gemäß Gegenstand 24, dadurch gekennzeichnet, dass genau einer der Reste L1 oder L2 für O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- steht.
29. Verbindung gemäß Gegenstand 24, dadurch gekennzeichnet, dass RAr für ein Wasserstoffatom, -F, -CF3 oder -OCF3, -CH3 oder -OCH3, -CO-CH3 steht.
30. Verbindung gemäß Gegenstand 24, dadurch gekennzeichnet, dass RN ausgewählt ist aus der Gruppe, bestehend aus:
31. Verbindung gemäß Gegenstand 24, nämlich
in der
Z ,1 , Z -,2 , Z 73 , Z -74 , Z -75 , Z -76 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC/rAlkylrest oder einen verzweigten oder unverzweigten C1 -C4-Al koxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht.
33. Verbindung gemäß Gegenstand 32, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy Methyl oder Methoxy steht.
34. Verbindung gemäß Gegenstand 32, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
35. Verbindung gemäß Gegenstand 32, dadurch gekennzeichnet, dass R4 für -OCH3 steht.
36. Verbindung gemäß Gegenstand 32, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3, Z4, Z5, Z6 für ein Sauerstoffatom steht.
37. Verbindung gemäß Gegenstand 32, nämlich
38. Verbindungen der allgemeinen Formel VI
in der
Z1 , Z2, Z3, Z4 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC4-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
X1 für eine direkte Bindung oder für eine -(CH2)n- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht,
L1 für
-N(R6)-
-O-
-C(=O)-
-O-C(=O)- oder -C(=O)-O- -N(R6)-C(=O)- oder -C(=O)- N(R6)-, -N(R6)-C(=O)-O- oder -O-C(=O)-N(R6)-, -N(R6)-O- oder -N(R6)-O-,
-O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- worin
R6 Wasserstoff oder eine verzweigte oder unverzweigte Ci-C4-Alkylgruppe bedeutet.
39. Verbindung gemäß Gegenstand 38, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy Methyl oder Methoxy steht.
40. Verbindung gemäß Gegenstand 38, dadurch gekennzeichnet, dass R4 für -OCH3 steht.
41. Verbindung gemäß Gegenstand 38, dadurch gekennzeichnet, dass genau einer der Reste Z\ Z2, Z3, Z4 für ein Sauerstoffatom steht.
42. Verbindung gemäß Gegenstand 38, dadurch gekennzeichnet, dass X1 für -CH2-CH2- (n=2) steht.
43. Verbindung gemäß Gegenstand 38, dadurch gekennzeichnet, dass L1 für -O-N(R6)-C(=O)- oder -C(=O)- N(R6)-O- steht.
44. Verbindung gemäß Gegenstand 43, dadurch gekennzeichnet, dass R6 für ein Wasserstoffatom oder eine Methylgruppe steht.
45. Verbindung gemäß Gegenstand 38, nämlich
76
in der
Z\ Z2, Z3, Z4, Z5 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten CrC-i-Alkylrest oder einen verzweigten oder unverzweigten CrC4-Alkoxyrest steht,
R4 für -Cl, -F, -Br1 -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht,
X1, X2 unabhängig voneinander für eine direkte Bindung oder für eine
-(CH2Jn- Kette steht, wobei n für eine natürliche Zahl 1 , 2, 3 oder 4 steht.
47. Verbindung gemäß Gegenstand 46, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy, Methyl oder Methoxy steht.
48. Verbindung gemäß Gegenstand 46, dadurch gekennzeichnet, dass R4 für -F oder -CF3 steht.
49. Verbindung gemäß Gegenstand 46, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3, Z4, Z5 für ein Sauerstoffatom steht.
50. Verbindung gemäß Gegenstand 46, dadurch gekennzeichnet, dass X1 für "CH2-CH2- (n=2) oder dass X2 für -CH2-CH2- (n=2) steht.
51. Verbindung gemäß Gegenstand 46, nämlich
in der
Z1 Z2 Z3 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten Ci-Cή-Alkylrest oder einen verzweigten oder unverzweigten C-ι-C4-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C-,-Alkylrest steht,
R4 für -Cl, -F, -Br1 -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht.
53. Verbindung gemäß Gegenstand 52, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy, Methyl oder Methoxy steht.
54. Verbindung gemäß Gegenstand 52, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
55. Verbindung gemäß Gegenstand 52, dadurch gekennzeichnet, dass R4 für -F oder -CF3 steht.
56. Verbindung gemäß Gegenstand 52, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3 für ein Sauerstoffatom steht.
57. Verbindungen gemäß Gegenstand 52, nämlich
58. Verbindungen der allgemeinen Formel IX
Ersatzblatt
r -?2 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R' unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht.
59. Verbindung gemäß Gegenstand 58, dadurch gekennzeichnet, dass R2 an der Carboxylgruppe für Wasserstoff und an allen anderen Positionen für Methyl steht.
60. Verbindung gemäß Gegenstand 58, dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2 für ein Sauerstoffatom steht.
61. Verbindungen gemäß Gegenstand 58, nämlich
62. Verbindungen der allgemeinen Formel X
in der
Z 11, Z 72 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten Ci-C-j-Alkylrest oder einen verzweigten oder unverzweigten Ci-C-j-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C4-Alkylrest steht,
RA für -Cl, -F, -Br1 -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht.
63. Verbindung gemäß Gegenstand 62, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy, Methyl oder Methoxy steht.
64. Verbindung gemäß Gegenstand 62, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
65. Verbindung gemäß Gegenstand 62, dadurch gekennzeichnet, dass R4 für - Cl oder -OCH3 steht.
66. Verbindung gemäß Gegenstand 62, dadurch gekennzeichnet, dass genau einer der Reste Z\ Z2 für ein Sauerstoffatom steht.
67. Verbindungen gemäß Gegenstand 62, nämlich
68. Verbindungen der allgemeinen Formel Xl
in der
Z1, Z2 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R1 für ein Wasserstoffatom, -OH, einen verzweigten oder unverzweigten d-C4-Alkylrest oder einen verzweigten oder unverzweigten Ci-C4-Alkoxyrest steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten CrC4-Alkylrest steht,
R* für -Cl, -F, -Br1 -CF3 oder -OCF3, -NO2, -OCH3 oder -OC2H5 steht.
69. Verbindung gemäß Gegenstand 68, dadurch gekennzeichnet, dass R1 für Wasserstoff, Hydroxy, Methyl oder Methoxy steht.
70. Verbindung gemäß Gegenstand 68, dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht.
71. Verbindung gemäß Gegenstand 68, dadurch gekennzeichnet, dass R4 für - Cl oder -OCH3 steht.
72. Verbindung gemäß Gegenstand 68, dadurch gekennzeichnet, dass genau einer der Reste Z1 , Z2 für ein Sauerstoffatom steht.
73. Verbindungen gemäß Gegenstand 68, nämlich
74. Verbindungen der allgemeinen Formel XII
in der R2 jeweils unabhängig voneinander für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C4-Alkylrest steht, wo
auch durch einen Rest R ersetzt sein kann.
75. Verbindung gemäß Gegenstand 74, dadurch gekennzeichnet, dass R2 an der Carboxylgruppe für Methyl, am Stickstoff für ein Wasserstoffatom steht.
76. Verbindungen gemäß Gegenstand 74, nämlich
Ersatzblatt
77. Verwendung von mindestens einer Verbindung der allgemeinen Formeln I-Xll gemäß mindestens einem der Gegenstände 1-76 zur Herstellung von Arzneimitteln.
78. Verwendung gemäß Gegenstand 77 zur Herstellung von Arzneimitteln zur Behandlung und/oder Prophylaxe von thromboembolischen Erkrankungen.
79. Verwendung gemäß Gegenstand 77 zur Herstellung von Arzneimitteln zur Behandlung und/oder Prophylaxe von akutem Koronarsyndrom, Herzinfarkt, Angina pectoris, Reokklusionen und Restenosen (z.B. nach Angioplastie oder aortokoronarem Bypass), Schlaganfall, transitorischen ischämischen Attacken, peripheren arteriellen Verschlusskrankheiten, Lungenembolien oder tiefen venösen Thrombosen, Vorhofflimmern oder Arhythmien.
80. Verwendung gemäß Gegenstand 77 zur Herstellung von Arzneimitteln zur Behandlung und/oder Prophylaxe von Blutgerinnungsstörungen im Rahmen größerer chirurgischer Eingriffe.
81. Verwendung gemäß Gegenstand 77 zur Herstellung von Arzneimitteln zur Behandlung der Thrombozytopenie.
82. Verwendung von Verbindungen der allgemeinen Formel XII zur Herstellung von MRT-Kontrastmitteln, insbesondere als intraoperatives Kontrastmittel im Rahmen größerer chirurgischer Eingriffe.
83. Verwendung gemäß Gegenstand 77 zur Herstellung von Arzneimitteln zur Behandlung der disseminierten intravasalen Gerinnung (DIC).
84. Verwendung von mindestens einer Verbindung der allgemeinen Formel I-Xll gemäß mindestens einem der Gegenstände 1 bis 76 zur Verhinderung der Blutkoagulation in-vitro.
85. Pharmazeutische Zusammensetzung, enthaltend mindestens eine Verbindung gemäß mindestens einem der Gegenstände 1 bis 76 in Verbindung mit einem pharmazeutisch geeigneten und physiologisch
verträglichen Träger und ggf. weiteren geeigneten Wirk-, Zusatz- oder Hilfsstoffen.
Weiterer Gegenstand der Anmeldung:
Z1 1:. wie in anderen Gegenständen
HaI = -F, -Cl1 -Br, -I, (unabhängig voneinander)
X1 wie in anderen Gegenständen
Es gelten alle Ausführungen zu anderen Gegenständen analog.
^rsatzblatt
Weitere Gegenstände der Anmeldung:
Z1 Z2 Z3 wie Formel I, zumindest eines keine Bindung n = 0, 1 , 2, 3 oder 4 R2 : wie Formel I, unabhängig voneinander HaI = -F, -Cl, -Br, -I, unabhängig voneinander
Bevorzugt: i) nur eines von Z1, Z2, Z3 -O- oder -S- und/oder ii) -HaI = -F und/oder iii) R2 = -CH3 (bevorzugt alle) und/oder iv) n = 1
Indikationen: virale Infekte, insbesondere RNA-Viren, Reroviren, HIV, negativstrang RNA-Viren, multiresistente Viren
Ersatzh'att
Weitere Gegenstände der Anmeldung:
Z1 Z2 Z3 wie Formel I1 zumindest eines keine Bindung n = 0, 1 , 2, 3 oder 4 R2 : wie Formel I, unabhängig voneinander HaI = -F, -Cl, -Br, -I, unabhängig voneinander
Bevorzugt: i) Z1 = Bindung, Z2 und/oder Z3 = -O- oder -S- und/oder ii) -HaI = -F und/oder iii) n = 1 und/oder iv) R2 = -CH3 (bevorzugt alle)
Indikationen: virale Infekte, insbesondere RNA-Viren, Reroviren, HIV, negativstrang RNA-Viren, multiresistente Viren
Ersätzblatt
Weitere Gegenstände der Anmeldung:
Z1 - Z11 unabhängig voneinander -O-, -S- oder Bindung, zumindest eines von Z1 - Z11 keine Bindung
R2 unabhängig voneinander wie Formel I
n = 0, 1 , 2, 3 oder 4
Indikationen: bakterielle, virale Infektionen
Ersatzblatt
Claims
1. Verbindungen der allgemeinen Formel I
Z1, Z2, Z3, Z4 jeweils unabhängig voneinander für eine direkte Bindung oder für ein Sauerstoff- oder ein Schwefelatom steht,
R2 für ein Wasserstoffatom oder einen verzweigten oder unverzweigten Ci-C4-Alkylrest steht
R4 für -Cl, -F, -Br, -CF3 oder -OCF3, -NO2 oder -OCH3 steht,
n für die ganzen Zahlen 0, 1 , 2, 3 oder 4 steht.
2. Verbindung der allgemeinen Formel I gemäß Anspruch 1 , dadurch gekennzeichnet, dass R2 für Wasserstoff, Methyl oder Ethyl steht, ganz besonders bevorzugt für Wasserstoff.
3. Verbindung der allgemeinen Formel I gemäß Anspruch 1 , dadurch gekennzeichnet, dass mindestens einer der Reste Z1, Z2, Z3, Z4 für ein Sauerstoffatom steht.
4. Verbindung der allgemeinen Formel I gemäß Anspruch 1 , dadurch gekennzeichnet, dass genau einer der Reste Z1, Z2, Z3, Z4 für ein Sauerstoffatom steht und die anderen Reste für eine direkte Bindung stehen.
5. Verbindung der allgemeinen Formel I gemäß Anspruch 1 , dadurch gekennzeichnet, dass R4 für ein Chloratom steht.
6. Verbindung der allgemeinen Formel I gemäß Anspruch 1 , nämlich
7. Verwendung von mindestens einer Verbindung der allgemeinen Formel I gemäß mindestens einem der Ansprüche 1-6 zur Herstellung von Arzneimitteln.
8. Verwendung gemäß Anspruch 7 zur Herstellung von Arzneimitteln zur Behandlung und/oder Prophylaxe von thromboembolischen Erkrankungen.
9. Verwendung gemäß Anspruch 7 zur Herstellung von Arzneimitteln zur Behandlung und/oder Prophylaxe von akutem Koronarsyndrom, Herzinfarkt, Angina pectoris, Reokklusionen und Restenosen (z.B. nach Angioplastie oder aortokoronarem Bypass), Schlaganfall, transitorischen ischämischen Attacken, peripheren arteriellen Verschlusskrankheiten, Lungenembolien oder tiefen venösen Thrombosen, Vorhofflimmern oder Arhythmien.
10. Verwendung gemäß Anspruch 7 zur Herstellung von Arzneimitteln zur Behandlung und/oder Prophylaxe von Blutgerinnungsstörungen im Rahmen größerer chirurgischer Eingriffe.
11. Verwendung gemäß Anspruch 7 zur Herstellung von Arzneimitteln zur Behandlung der Thrombozytopenie.
12. Verwendung gemäß Anspruch 7 zur Herstellung von Arzneimitteln zur Behandlung der disseminierten intravasalen Gerinnung (DIC).
13. Verwendung von mindestens einer Verbindung der allgemeinen Formel I gemäß mindestens einem der Ansprüche 1 bis 6 zur Verhinderung der Blutkoagulation in-vitro.
14. Pharmazeutische Zusammensetzung, enthaltend mindestens eine Verbindung gemäß mindestens einem der Ansprüche 1 bis 6 in Verbindung mit einem pharmazeutisch geeigneten und physiologisch verträglichen Träger und ggf. weiteren geeigneten Wirk-, Zusatz- oder Hilfsstoffen.
Applications Claiming Priority (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102007037373.4 | 2007-08-06 | ||
| DE102007037373A DE102007037373A1 (de) | 2007-08-06 | 2007-08-06 | Neue Pharmazeutika, Verfahren zu ihrer Herstellung und ihre Verwendung in der Therapie |
| DE102008019679.7 | 2008-04-11 | ||
| DE102008019679 | 2008-04-11 | ||
| DE102008033285.2 | 2008-07-11 | ||
| DE102008033285 | 2008-07-11 | ||
| DE102008034030.8 | 2008-07-17 | ||
| DE102008034030 | 2008-07-17 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2009018807A1 true WO2009018807A1 (de) | 2009-02-12 |
| WO2009018807A9 WO2009018807A9 (de) | 2009-11-12 |
Family
ID=40039878
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/DE2008/001252 WO2009018807A1 (de) | 2007-08-06 | 2008-07-31 | Oxazolidinone als faktor xa- inhibitoren, verfahren zu ihrer herstellung und ihre verwendung in der therapie |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2009018807A1 (de) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009019852A1 (de) | 2009-05-06 | 2010-11-11 | Schebo Biotech Ag | Polymere mit neuen Strukturelementen, Verfahren zu ihrer Herstellung und ihre Verwendung |
| CN102796091A (zh) * | 2011-05-24 | 2012-11-28 | 北大方正集团有限公司 | 取代的噁唑烷酮化合物及其制备方法和应用 |
| WO2013024394A1 (en) * | 2011-08-12 | 2013-02-21 | Alembic Pharmaceuticals Limited | Novel reference markers of dabigatran etexilate |
| EP3078378A1 (de) | 2015-04-08 | 2016-10-12 | Vaiomer | Verwendung von faktor-xa-inhibitoren zur regulierung von glykämie |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001047919A1 (de) * | 1999-12-24 | 2001-07-05 | Bayer Aktiengesellschaft | Substituierte oxazolidinone und ihre verwendung im gebiet der blutgerinnung |
| WO2004060887A1 (de) * | 2003-01-07 | 2004-07-22 | Bayer Healthcare Ag | Verfahren zur herstellung von 5-chlor-n-({5s)-2-oxo-3-[4-(3-oxo-4-morpholinyl)-phenyl]-1,3-oxazolidin-5-yl}-methyl)-2-thiophencarboxamid |
| WO2005068456A1 (de) * | 2004-01-15 | 2005-07-28 | Bayer Healthcare Ag | Herstellverfahren |
| DE102005047563A1 (de) * | 2005-10-04 | 2007-04-05 | Bayer Healthcare Ag | Neue polymorphe Form von 5-Chlor-N-{(5S)-2-oxo-3-[4-(3-oxo-4-morpholinyl)-phenyl]-1,3-oxazolidin-5-yl)-methyl)-2-thiophencarboxamid |
| WO2007039134A1 (de) * | 2005-10-04 | 2007-04-12 | Bayer Healthcare Ag | Kombinationstherapie mit substituierten oxazolidinonen zur prophylaxe und behandlung von cerebralen durchblutungsstörungen |
| DE102005048824A1 (de) * | 2005-10-10 | 2007-04-12 | Bayer Healthcare Ag | Behandlung und Prophylaxe von Mikroangiopathien |
| DE102006051625A1 (de) * | 2006-11-02 | 2008-05-08 | Bayer Materialscience Ag | Kombinationstherapie substituierter Oxazolidinone |
-
2008
- 2008-07-31 WO PCT/DE2008/001252 patent/WO2009018807A1/de active Application Filing
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001047919A1 (de) * | 1999-12-24 | 2001-07-05 | Bayer Aktiengesellschaft | Substituierte oxazolidinone und ihre verwendung im gebiet der blutgerinnung |
| WO2004060887A1 (de) * | 2003-01-07 | 2004-07-22 | Bayer Healthcare Ag | Verfahren zur herstellung von 5-chlor-n-({5s)-2-oxo-3-[4-(3-oxo-4-morpholinyl)-phenyl]-1,3-oxazolidin-5-yl}-methyl)-2-thiophencarboxamid |
| WO2005068456A1 (de) * | 2004-01-15 | 2005-07-28 | Bayer Healthcare Ag | Herstellverfahren |
| DE102005047563A1 (de) * | 2005-10-04 | 2007-04-05 | Bayer Healthcare Ag | Neue polymorphe Form von 5-Chlor-N-{(5S)-2-oxo-3-[4-(3-oxo-4-morpholinyl)-phenyl]-1,3-oxazolidin-5-yl)-methyl)-2-thiophencarboxamid |
| WO2007039134A1 (de) * | 2005-10-04 | 2007-04-12 | Bayer Healthcare Ag | Kombinationstherapie mit substituierten oxazolidinonen zur prophylaxe und behandlung von cerebralen durchblutungsstörungen |
| DE102005048824A1 (de) * | 2005-10-10 | 2007-04-12 | Bayer Healthcare Ag | Behandlung und Prophylaxe von Mikroangiopathien |
| DE102006051625A1 (de) * | 2006-11-02 | 2008-05-08 | Bayer Materialscience Ag | Kombinationstherapie substituierter Oxazolidinone |
Non-Patent Citations (1)
| Title |
|---|
| ROEHRIG S ET AL: "Discovery of the Novel Antithrombotic Agent 5-Chloro-N-(((5S)-2-oxo-3 [4-(3-oxomorpholin-4-yl)phenyl]-1,3-oxazolidin-5-yl)methyl)thiophene 2-carboxamide (BAY 59-7939): An Oral, Direct Factor Xa Inhibitor", JOURNAL OF MEDICINAL CHEMISTRY, US AMERICAN CHEMICAL SOCIETY. WASHINGTON, vol. 48, 22 September 2005 (2005-09-22), pages 5900 - 5908, XP002418821, ISSN: 0022-2623 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009019852A1 (de) | 2009-05-06 | 2010-11-11 | Schebo Biotech Ag | Polymere mit neuen Strukturelementen, Verfahren zu ihrer Herstellung und ihre Verwendung |
| CN102796091A (zh) * | 2011-05-24 | 2012-11-28 | 北大方正集团有限公司 | 取代的噁唑烷酮化合物及其制备方法和应用 |
| WO2013024394A1 (en) * | 2011-08-12 | 2013-02-21 | Alembic Pharmaceuticals Limited | Novel reference markers of dabigatran etexilate |
| EP3078378A1 (de) | 2015-04-08 | 2016-10-12 | Vaiomer | Verwendung von faktor-xa-inhibitoren zur regulierung von glykämie |
| WO2016162472A1 (en) | 2015-04-08 | 2016-10-13 | Vaiomer | Use of factor xa inhibitors for regulating glycemia |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009018807A9 (de) | 2009-11-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60118547T2 (de) | Pharmazeutische zusammensetzung zur behandlung von kolorektalem krebs welche thalidomid und irinotecan enthält | |
| DE60123294T2 (de) | Diazepan Derivate als Faktor X Inhibitor | |
| CN104884057B (zh) | 大麻素受体介导的化合物 | |
| EP1113809B1 (de) | Pharmazeutische zubereitung enthaltend ein cyclo-peptide und ein chemotherapeutikum oder einen angiogeneseinhibitor | |
| AT5874U1 (de) | Pharmazeutische zubereitungen enthaltend amlodipinmaleat | |
| EP0128483A2 (de) | Neue galenische Zubereitungsformen von oralen Antidiabetika und Verfahren zu ihrer Herstellung | |
| DE102008028071A1 (de) | Neue Cokristall-Verbindung von Rivaroxaban und Malonsäure | |
| DE69909209T2 (de) | Pyrimidinon-derivate, diese verbindungen enthaltenden pharmazeutische zubereitungen und verfharen zu ihrer herstellung | |
| WO2009018811A1 (de) | Neue pharmazeutika, verfahren zu ihrer herstellung und ihre verwendung in der medizinischen therapie | |
| WO2009018807A1 (de) | Oxazolidinone als faktor xa- inhibitoren, verfahren zu ihrer herstellung und ihre verwendung in der therapie | |
| DE3212736A1 (de) | Verwendung von dihydropyridinen in arzneimitteln mit salidiuretischer wirkung | |
| DE3833393A1 (de) | Verwendung von pteridinen zur verhinderung der primaeren und sekundaeren resistenz bei der chemotherapie und diese verbindungen enthaltende arzneimittel | |
| DE60030654T2 (de) | Verwendung von Lasofoxifen | |
| CN101801461A (zh) | 用于治疗神经组织退化或血液学疾病的[1,10]-菲罗啉衍生物 | |
| WO2001062717A1 (de) | Aminosulfonylbiphenylderivate | |
| DE602004001492T2 (de) | (3-(4-(Pyridin-2-ylamino)-butyryl)-2,3,4,4a,9,9a-hexahydro-1H-3-aza-fluoren-9-yl)-essigsäure Derivate und verwandte tricyclische Indanyle als alphaVbeta3 und alphaVbeta5 Integrin Inhibitoren zur Behandlung von Krebs und instabiler Angina | |
| WO1998016224A1 (de) | Pyrazolinone zur behandlung von potenzstörungen | |
| DE102007037373A1 (de) | Neue Pharmazeutika, Verfahren zu ihrer Herstellung und ihre Verwendung in der Therapie | |
| DE10010423A1 (de) | Substituierte 2,5-Dimethyldihydropyridazinone und ihre Verwendung | |
| WO1995005825A1 (fr) | Traitement symptomatique des troubles circulatoires | |
| DE60123103T2 (de) | Neue verbindungen | |
| WO2001000189A2 (de) | Kombination von mtp-inhibitoren und stoffwechselbeeinflussenden wirkstoffen und ihre verwendung in arzneimitteln | |
| DE3113150A1 (de) | Isophthalsaeurepicolylamidmonohydrat, verfahren zu seiner herstellung und dessen pharmazeutische verwendung | |
| JPWO2002092096A1 (ja) | 抗腫瘍剤 | |
| EP2782574A1 (de) | Salz von (r)-3-(6-amino-pyridin-3-yl)-2-(1-cyclohexyl-1h-imidazol-4-yl)- propionsäureethylester |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 08801090 Country of ref document: EP Kind code of ref document: A1 |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 08801090 Country of ref document: EP Kind code of ref document: A1 |