WO2008084319A2 - 新規核酸 - Google Patents
新規核酸 Download PDFInfo
- Publication number
- WO2008084319A2 WO2008084319A2 PCT/IB2007/004005 IB2007004005W WO2008084319A2 WO 2008084319 A2 WO2008084319 A2 WO 2008084319A2 IB 2007004005 W IB2007004005 W IB 2007004005W WO 2008084319 A2 WO2008084319 A2 WO 2008084319A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- nucleic acid
- acid according
- expression
- microrna
- active ingredient
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2330/00—Production
- C12N2330/10—Production naturally occurring
Definitions
- the present invention relates to a novel nucleic acid, a method for expressing or suppressing the nucleic acid, and a diagnostic or therapeutic agent containing the nucleic acid.
- MicroRNA a kind of nucleic acid, is a small non-coding single-stranded RNA of about 22 nucleotides that is not translated into protein, and has been confirmed to exist in many organisms including humans (non- Patent Documents 1 and 2).
- MicroRNAs are generated from genes that are transcribed into single or clustered microRNA precursors. That is, first, the primary transcription product, primary-microRNA (pri-miRNA), is transcribed, and then the stepwise processing from pri-miRNA to mature microRNA, pri-miRNA Force Approximately 70 base pr ecursor-microRNA (pre-miRNA) having a characteristic hairpin structure is produced. Furthermore, mature microRNA is produced from pre-miRNA by Dicer-mediated processing (Non-patent Document 3). '
- Mature microRNAs are thought to be involved in post-transcriptional regulation of gene expression by binding complementarily to the target mRNA and suppressing translation of the mRNA, or by degrading the mRNA. Les. As of May 2006, the microRNA database miRBase (http: ⁇ microrna.sanger.ac.uk/) contains 455 human and 3685 microRNAs in all living species. Among the microRNAs expressed in mammals, including humans, those that are known for their physiological functions are involved in miR-181 (Non-patent Document 4) involved in blood cell differentiation and insulin secretion. There are only a few such as miR-375 (Non-Patent Document 5), and many of them have unclear physiological activity. However, research capabilities using nematodes and Drosophila flies have also become clear that microRNAs play various important roles in the development and differentiation of organisms. In particular, there are reports that suggest a relationship with cancer (Non-patent Document 6).
- Methods for identifying microRNA include cell-powered low-molecular-weight RNA cloning methods, There is a method of using bioinformatics. In order to be registered as miRNA in miRBase, both information on expression and information on biosynthesis and structure are required, and prediction of structure from genome sequence information alone is not recognized as microRNA. (Non-patent document 7).
- Non-Patent Documents 8 to 10 It is known that mast cells are activated by various stimuli, cause degranulation, and release and produce many inflammatory mediators. For example, when an antigen is recognized by mast cells, histamine and tryptase are rapidly released by degranulation, and chemical mediators such as prostaglandin D2 (PGD2), leukotriene (LT), and platelet activating factor (PAF). It is known that various chemokines such as macrophage inflammatory protein (MIP) -1 ⁇ and various site force-ins such as granulocyte macrophage colony stimulating factor (GM-CSF) are newly synthesized and released. You're being. In addition, regarding the basic basic protein (major basic protein), which was previously thought to be produced by eosinophils, it has recently been clarified that a large amount of mast cells are produced in humans. (Non-Patent Document 11).
- MIP macrophage inflammatory protein
- GM-CSF granulocyte macrophage colony stimulating
- mast cells are thought to play a major role in the pathogenesis of various allergic diseases, it is possible to treat allergic diseases by controlling the function of mast cells. Conceivable.
- Non-patent Document 9 sodium cromoglycate, used as an inhibitor of inflammatory mediator release, remarkably suppresses IgE-dependent release of inflammatory mediators in rat peritoneal mast cells. The effect is not strong (Non-patent Document 12) Azelastine hydrochloride suppresses the release of histamine, PGD2, and LT from human cultured mast cells and the production of GM-CSF and MIP-1a at high concentrations.
- microRNA expressed in mouse bone marrow-derived mast cells has been reported (Non-patent Document 14), but the relationship between microRNA and the function of obesity cells is not known. MicroRNAs expressed in human mast cells have not been reported. Considering the species differences between humans and mice as described above, based on microRNA expression information in mouse mast cells, It is difficult to predict microRNA expression information.
- Mesenchymal stem cells are known as pluripotent stem cells that exist in mammalian bone marrow, adipose tissue, umbilical cord blood, and the like and differentiate into adipocytes, chondrocytes, bone cells, and the like. Because of their pluripotency, mesenchymal stem cells are attracting attention as transplant materials for regenerative medicine of many tissues, including bone, cartilage, tendon, muscle, fat, and periodontal tissue. Non-patent document 15).
- Mesenchymal stem cells can be differentiated into specific cells in vitro by the addition of drugs or cytodynamic ins. For example, it is induced by the action of ⁇ methyl-3-isobutylxanthine, dexamethasone, insulin and indomethacin on fat cells, and by the action of dexamethasone, ⁇ -glycerol phosphate, and ascorbic acid on osteoblasts. Yes (Non-Patent Document 16). However, details regarding the molecular mechanisms of these differentiation processes are unknown. Based on the results of gene expression analysis in gene knockout mice and differentiation stages, adipose cells have PPAR y and C / EBP family capabilities.
- Osteoblasts are involved in gene expression such as Cbfal / Runx2 and Osterix during differentiation. However, it is not possible to explain the differentiation mechanism from mesenchymal stem cells with these genes alone, but artificially control differentiation and proliferation. It ’s so good. Also, microRNAs that act on the differentiation and proliferation of mesenchymal stem cells are not known.
- microRNA Since microRNA is involved in the control of the expression of various genes, abnormalities in microRNA are expected to be involved in various human diseases. Research is progressing especially in cancer, and it has been reported that the expression of microRNAs differs from normal tissues in many cancers, and that cancers can be classified by analyzing the expression profile of microRNAs. Le, Ru (Non-patent Document 18). It is also known that human microRNAs found so far are known to be about half the strength of human cancer, and are present in chromosomal abnormalities or fragile sites of chromosomes. (Non-patent document 19).
- the miR-15a / miR-16 cluster is located on chromosome 13ql4, which is deleted in B-cell chronic lymphocytic leukemia (B-CLL). It is predicted that the deletion will be one of the causes of B-CLL (Non-patent Document 20), and the expression of Let-7, which is one of microRNAs in lung cancer.
- B-CLL B-cell chronic lymphocytic leukemia
- Let-7 which is one of microRNAs in lung cancer.
- Ras which is known as a proto-oncogene (Non-patent documents 21, 22).
- Many microRNAs have reduced expression in cancer cells, but there are also microRNAs that have gene amplification and overexpression in cancer.
- Non-patent Document 25 reports that the external force is microRNA, its precursor, a certain, or its antisense oligonucleotide is administered to increase or decrease the expression of microRNA, thereby suppressing the growth of cancer in animal mode. There are currently no reports.
- Non-Patent Document 1 Science, 294, 853-858 (2001)
- Non-Patent Document 2 Cell, 113, 673-676 (2003)
- Non-Patent Document 3 Nature Reviews Genetics, 5, 522-531 (2004)
- Non-Patent Document 4 Science, 303, 83-86 (2004)
- Non-Patent Document 5 Nature, 432, 226-230 (2004)
- Non-Patent Document 6 Nature Reviews Cancer, 6, 259-269 (2006)
- Non-Patent Document 7 RNA, 9, 277-279 (2003)
- Non-Patent Document 8 Motohiro Kurosawa, “Mast Cell Clinical”, Advanced Medical Institute, pl42 (2001);
- Non-Patent Document 9 Edited by Motohiro Kurosawa, “Mast Cell Clinic”, Advanced Medicine, P559 (2001);
- Non-Patent Document 10 Crit. Rev. Immunol., 22, 115-140 (2002)
- Non-Patent Document 11 Blood, 98, 1127-1134 (2001)
- Non-Patent Document 12 Clin. Exp. Allergy, 28, 1228-1236 (1998)
- Non-Patent Document 13 Blood, 100, 3861-3868 (2002)
- Non-Patent Document 14 Genome Biology, 6, R71 (2005)
- Non-Patent Document 15 “Gene Medicine”, 2000, 4 ⁇ , p. 58-61
- Non-Patent Document 16 Science, 284, 143-147 (1999)
- Non-Patent Document 17 "Experimental Medicine", 2002, 20, vol. 2459-2464
- Non-Patent Document 18 Nature, 435, 839-843 (2005)
- Non-Patent Document 19 Proc.Natl.Acad.Sci.USA, 101, 2999-3004 (2004)
- Non-Patent Document 20 Pnx; .NatLAcad.Sd.USA, 99, 15524-15529 (2002)
- Non-Patent Document 21 Cancer Research, 64, 3753-3756 (2004)
- Non-Patent Document 22 Cell, 120, 635-647 (2005)
- Non-Patent Document 23 Nature, 435, 823-833 (2005)
- Non-Patent Document 24 Prcx; .Natl.Acad.Sci.USA, 102, 3627-3632 (2005)
- Non-Patent Document 25 Cancer Research, 64, 3753-3756 (2004)
- microRNAs that act on mesenchymal stem cells is important for mesenchymal stem cells. It is expected to lead to the elucidation of the functions of differentiation and proliferation, development of a mesenchymal stem cell force differentiation control method for specific cells, and a new therapeutic method using differentiation control. Furthermore, the discovery of microRNAs that cause cancer cell proliferation or suppression not only helps to understand the mechanism of carcinogenesis, but also develops diagnostic and therapeutic agents for human cancer, and uses them to develop new cancers. Expected to lead to diagnostic and therapeutic methods.
- the purpose of the present invention is to obtain a group of microRNAs, and to isolate mast cells ⁇ culture ⁇ differentiation control-degranulation control ⁇ inflammatory mediator 1 production control ⁇ site force in production control ⁇ chemokine production control, and Diagnosis of allergic diseases 'Treatment, regulation of mesenchymal stem cell differentiation and proliferation, regulation of cancer cell differentiation and proliferation, diagnosis of diseases such as cancer' Nucleic acids useful for treatment and use thereof It is in.
- the present invention relates to the following (1) to (64). -
- a nucleic acid comprising a base sequence represented by SEQ ID NOs:!
- nucleic acid comprising a nucleotide sequence having at least 90% identity with the nucleotide sequence of any one of SEQ ID NOs: 1 to 1336.
- nucleic acid that hybridizes under stringent conditions with a complementary strand of nucleic acid having the nucleotide sequence represented by any one of SEQ ID NOs: 1 to 1336.
- a nucleic acid comprising the nucleic acid according to any one of (1) to (3).
- a nucleic acid that hybridizes with a complementary strand of a nucleic acid comprising the base sequence represented by any of SEQ ID NOS: 1337 to 2851 under stringent conditions.
- a core consisting of a base sequence complementary to the nucleic acid described in item 1 above or any one of (1) to (7) acid.
- a double-stranded nucleic acid comprising the nucleic acid according to any one of (1) to (7) and a nucleic acid having a base sequence ability complementary to the base sequence of the nucleic acid.
- a diagnostic or therapeutic agent for a disease caused by an abnormality of obesity cells comprising the nucleic acid according to any one of (1) to (9) as an active ingredient.
- Any one of (1) to (9) A diagnostic or treatment for a disease caused by an abnormality of mast cells, containing as an active ingredient a substance that suppresses expression of the target gene of the nucleic acid according to any one of ⁇ .
- a mast cell degranulation promoter containing a nucleic acid as an active ingredient is a mast cell degranulation promoter containing a nucleic acid as an active ingredient.
- a mast cell degranulation inhibitor comprising, as an active ingredient, a nucleic acid having a base sequence complementary to the nucleic acid according to (21) or (22).
- mast cells comprising as an active ingredient a double-stranded nucleic acid comprising the nucleic acid according to (21) or (22) and a nucleic acid having a nucleotide sequence complementary to the nucleotide sequence of the nucleic acid.
- Granule accelerator or degranulation inhibitor comprising:
- a mast cell degranulation promoter or degranulation inhibitor comprising as an active ingredient a substance that promotes or suppresses the expression or function of the nucleic acid according to (21) or (22).
- a mast cell degranulation promoter or degranulation inhibitor comprising as an active ingredient a substance that suppresses or promotes the expression of the target gene of the nucleic acid according to (21) or (22).
- (31) Having an acid having a base sequence ability complementary to the nucleic acid described in (29) or (30) 3 ⁇ 4
- a mesenchymal system comprising a double-stranded nucleic acid comprising the nucleic acid according to (29) or (30) and a nucleic acid having a base sequence complementary to the base sequence of the nucleic acid as an essential five component
- a diagnostic or therapeutic agent for diseases caused by abnormal proliferation and / or differentiation of stem cells comprising:
- (33) Due to abnormal proliferation and / or differentiation of mesenchymal stem cells containing a substance that promotes or suppresses the expression or function of the nucleic acid according to (29) or (30) as an active ingredient A diagnostic or therapeutic agent for a disease.
- a diagnostic agent for diseases caused by abnormal proliferation and / or differentiation of mesenchymal stem cells using as an index the suppression or promotion of the expression of the target gene of the nucleic acid according to (29) or (30) Or screening methods for therapeutic drugs.
- a mesenchymal stem cell proliferation promoter comprising the nucleic acid according to any one of (5) to (7), wherein SEQ ID NO: 1337 is an active ingredient.
- a mesenchymal stem cell growth inhibitor comprising, as an active ingredient, a nucleic acid having a base sequence complementary to the nucleic acid according to (37) or (38).
- a mesenchymal stem cell growth inhibitor comprising the nucleic acid according to any one of (1) to (4), which is any one of SEQ ID NO: 8, 21, or 36, as an active ingredient.
- a nucleic acid having a base sequence complementary to the nucleic acid described in (37) or (38) is present.
- a force of any one of (37) to (42) A double-stranded nucleic acid comprising the nucleic acid according to item 1 and a nucleic acid having a base sequence complementary to the base sequence of the nucleic acid as an active ingredient A mesenchymal stem cell proliferation promoter or growth inhibitor.
- a growth promoting agent for mesenchymal stem cells comprising a substance that promotes or suppresses the expression or function of the nucleic acid according to item 1 as an active ingredient, Or a growth inhibitor.
- the mesenchymal stem cell proliferation promoter or growth inhibitor comprising a substance that suppresses or promotes the expression of the target gene of the nucleic acid according to item 4 as an active ingredient Agent.
- IJ No. 337, 1339, 1352, 1371, 1372, 1373, 1386 or 1390 A diagnostic or therapeutic agent for diseases caused by abnormal cell proliferation, containing as an active ingredient.
- a diagnostic or therapeutic agent for a disease caused by abnormal cell proliferation comprising as an active ingredient a nucleic acid having a base sequence complementary to the nucleic acid according to (48) or (49).
- (51) Caused by abnormal cell growth, comprising as an active ingredient a double-stranded nucleic acid comprising the nucleic acid according to (48) or (49) and a nucleic acid complementary to the nucleic acid having a base sequence ability.
- a substance that promotes or suppresses the expression or function of the nucleic acid according to (48) or (49) A diagnostic or therapeutic agent for diseases caused by abnormal cell proliferation, containing quality as an active ingredient.
- a screening method for a diagnostic or therapeutic agent for diseases caused by abnormal cell proliferation using as an index the promotion or suppression of the expression or function of the nucleic acid according to (48) or (49) .
- a diagnostic or therapeutic agent for diseases caused by abnormal cell proliferation comprising as an active ingredient a substance that suppresses or promotes the expression of a nucleic acid target gene according to (48) or (49).
- Diseases caused by abnormal cell proliferation include cancer, arteriosclerosis, rheumatoid arthritis, benign prostatic hyperplasia, vascular restenosis after percutaneous transvascular coronary angioplasty, pulmonary fibrosis, glomerulonephritis and self
- a cell growth promoter comprising a nucleic acid comprising a base sequence complementary to the nucleic acid according to (57) or (58) as an active ingredient.
- Cell growth inhibition comprising a double-stranded nucleic acid comprising the nucleic acid according to (57) or (58) and a nucleic acid having a base sequence complementary to the base sequence of the nucleic acid as an active ingredient. Antiproliferative or growth promoter.
- a cell growth inhibitor or growth promoter comprising as an active ingredient a substance that promotes or suppresses the expression or function of the nucleic acid according to (57) or (58).
- (62) Promote or repress the expression or function of the nucleic acid according to (57) or (58). And a method for screening a cell growth inhibitor or growth promoter.
- a novel nucleic acid a vector that expresses the nucleic acid, a method for detecting expression and mutation of the nucleic acid, a method for screening a substance that controls the nucleic acid, and a method for separating a cell that expresses the nucleic acid ,
- diagnostic agents or therapeutic agents for diseases caused by abnormalities such as mast cells or mesenchymal stem cells, diseases such as cancer, and regulators of cell differentiation and proliferation can be provided.
- FIG. 1 shows the secondary structure of the base sequence represented by SEQ ID NO: 1580 of KHK-miR_1194.
- nucleic acid in the present invention examples include the following nucleic acids.
- the nucleic acid is preferably microRNA or a derivative thereof, a microRNA precursor or a derivative thereof, and a double-stranded nucleic acid (hereinafter also referred to as the nucleic acid of the present invention).
- a nucleic acid comprising the base sequence represented by any one of SEQ ID Nos: 1 to 1336.
- nucleic acid comprising a nucleotide sequence having 90% or more identity with the nucleotide sequence represented by any one of SEQ ID NOs: 1 to 336.
- nucleic acid that hybridizes under stringent conditions with a complementary strand of a nucleic acid comprising the base sequence represented by any one of SEQ ID NOs: 1 to 1336.
- a nucleic acid comprising the nucleic acid according to any one of (1) to (3).
- a nucleic acid comprising the base sequence represented by any one of SEQ ID NOs: 1337 to 2851.
- a double-stranded nucleic acid comprising the nucleic acid according to any one of (1) to (7) and a nucleic acid having a base sequence ability complementary to the base sequence of the nucleic acid.
- the microRNA is a single-stranded RNA derived from a cell, and the surrounding genomic sequence including the sequence has a sequence capable of forming a hairpin structure.
- RNA that can be excised from the strand.
- the length of the microRNA is preferably 15 to 28 bases, more preferably 16 to 28 bases, more preferably 16 to 26 bases, and particularly preferably 16 to 24 bases.
- MicroRNAs complementarily bind to their target mRNA, suppress mRNA degradation or translation, and control post-transcriptional gene expression.
- the microRNA of the present invention includes a nucleic acid having a nucleotide sequence represented by any one of SEQ ID NOs: 1 to 1336, 90% or more, preferably 9 with the nucleotide sequence represented by any of SEQ ID NOs: 1 to 1336.
- Examples thereof include nucleic acids having 5% or more identity and having a base sequence ability. Also, it consists of a base sequence represented by SEQ ID NOs: 1 to 1336! Nucleic acids that hybridize under stringent conditions with a complementary strand of acid. Examples of the microRNA of the present invention include nucleic acids containing these nucleic acids.
- the microRNA precursor is a nucleic acid having a length of about 50 to about 200 bases, preferably about 70 to about 100 bases, containing microRNA, and capable of forming a hairpin structure. It is. MicroRNAs are produced through processing by a protein called microcerc precursor power Dicer.
- the microRNA precursor of the present invention includes a nucleic acid consisting of a base sequence represented by SEQ ID NOs: 1337 to 2851, a shift, and a base sequence represented by any one of SEQ ID NOs: 1337 to 2851 and 80% or more.
- a nucleic acid having a nucleotide sequence having preferably 90% or more, more preferably 95% or more identity, and a complementary strand of a nucleic acid having a nucleotide sequence represented by any one of SEQ ID NOs: 1337 to 2851 examples include nucleic acids that hybridize under certain conditions.
- the microRNA precursor includes a microRNA sequence, and the microRNA is generated through microRNA precursor power processing. For example, since it has a function as a precursor, a nucleic acid that has 80% or more homology with the nucleotide sequence represented by any of SEQ ID NOs: 1337 to 2851 is a microRNA precursor. It is thought that it has all functions.
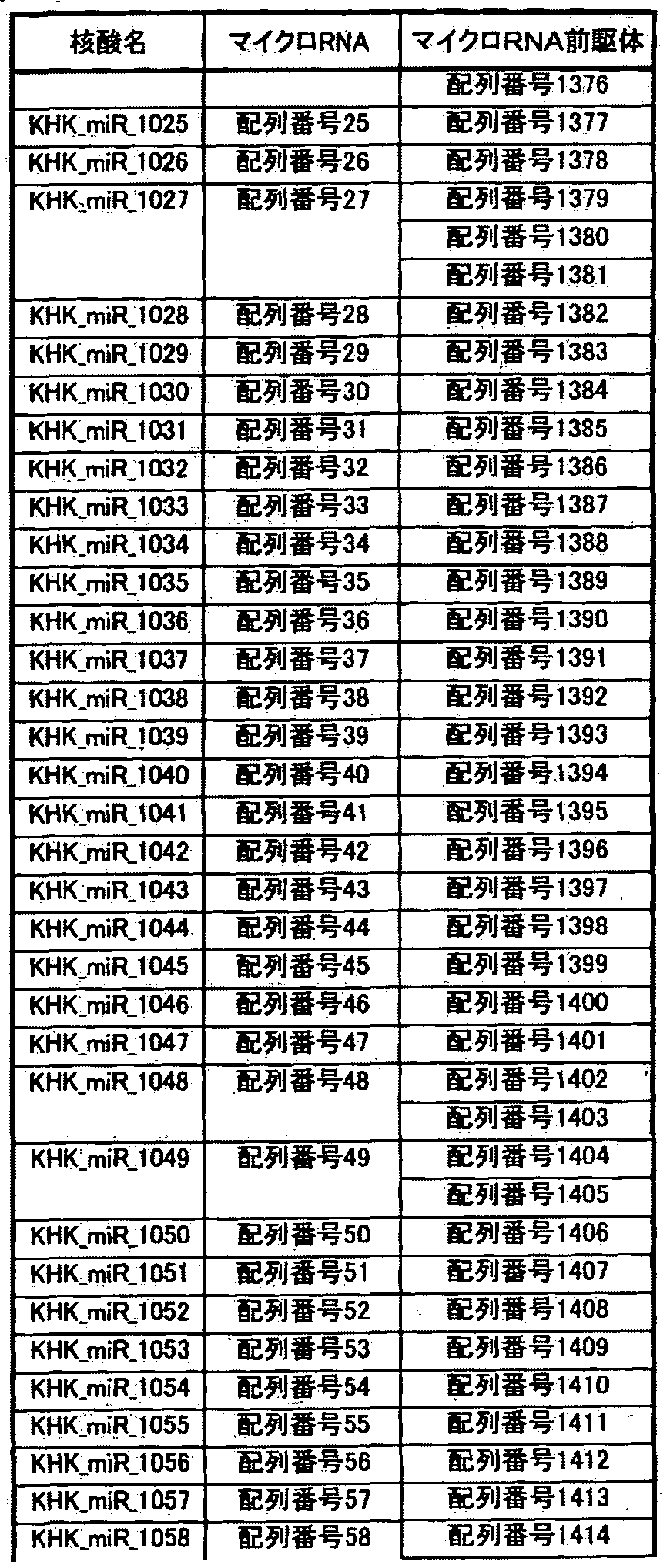
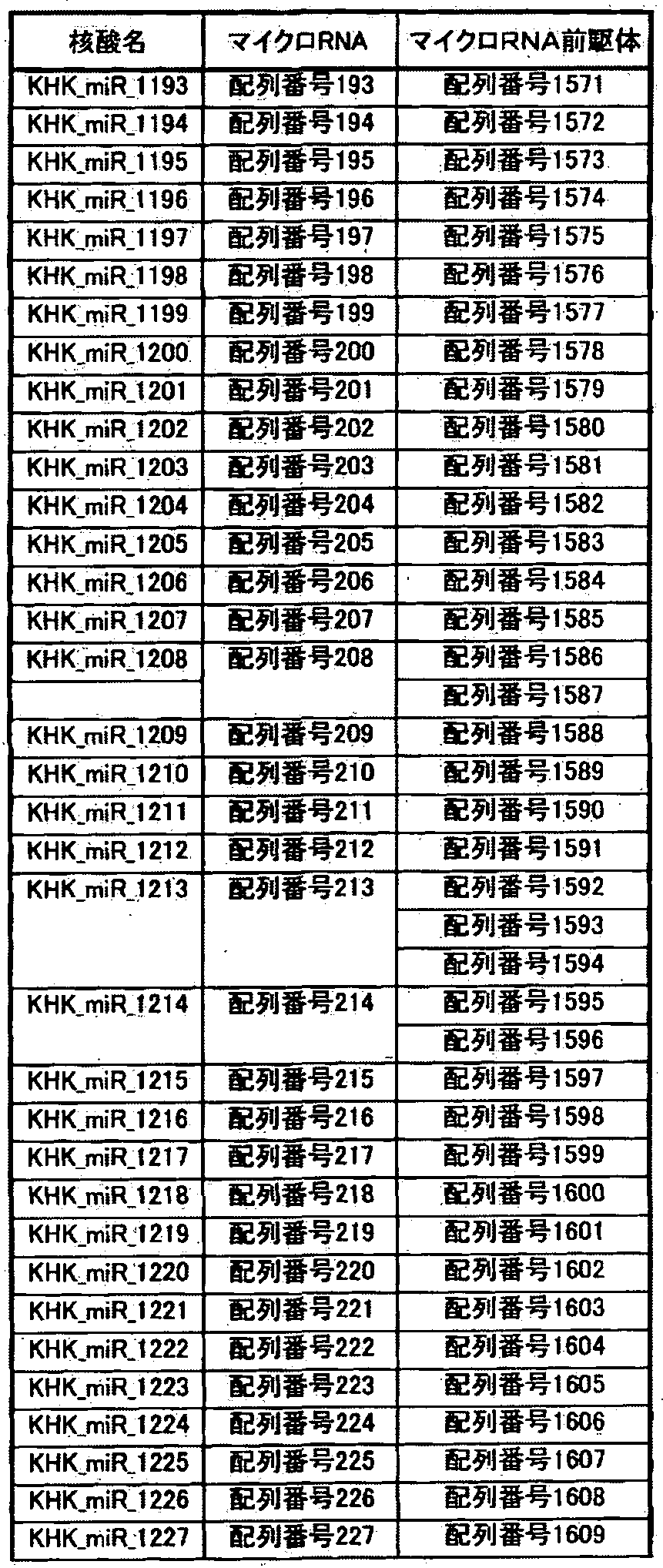
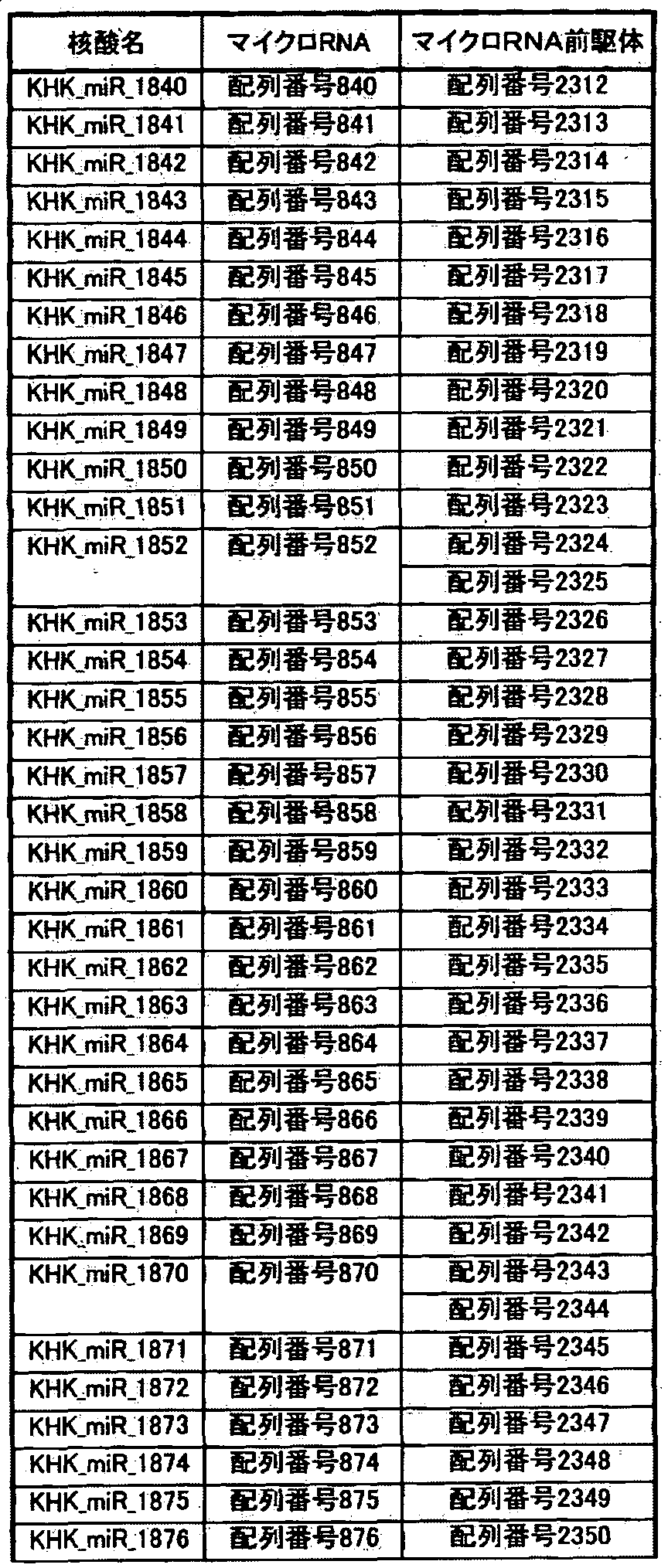
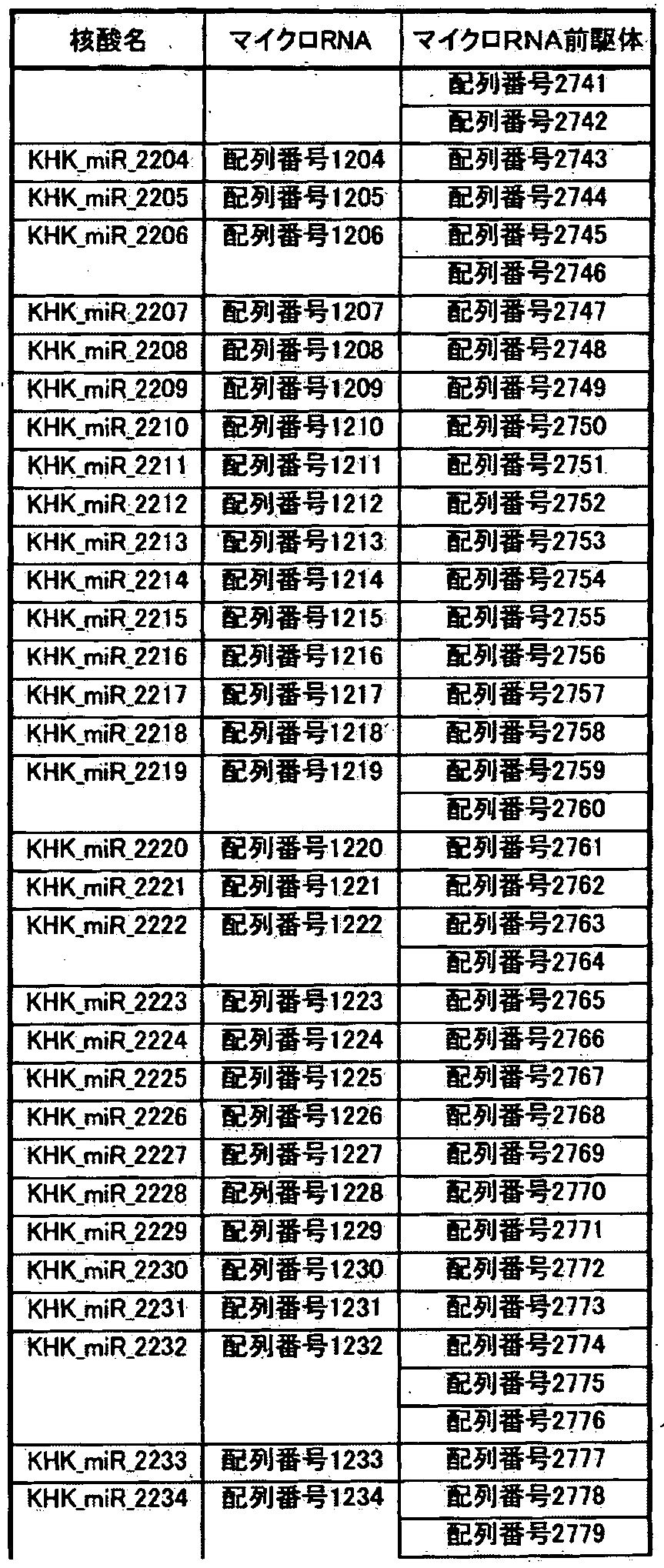
- Tables 1-1 to _40 show the relationship between the base sequences represented by SEQ ID NOs: 1 to 1336 specifically listed as microRNAs and the base sequences of microRNA precursors listed as precursors thereof.
- nucleic acid of the present invention a nucleic acid having a base sequence complementary to the nucleic acid listed above, a nucleic acid listed above, and a nucleic acid having a base sequence complementary to the base sequence of the nucleic acid
- lifted a nucleic acid having a base sequence complementary to the base sequence of the nucleic acid
- a nucleic acid having a base sequence having 90% or more identity with the base sequence represented by any of SEQ ID NOs: 1 to 1336 is BLAST (J. Mol. Biol, 215, 403 (199 0). )] And FASTA [Methods in Enzymology, 183, 63 (1990)], etc., and the number of nucleic acids consisting of the nucleotide sequence represented by any of SEQ ID NOs: 1 to 1336 is small. Meaning that the nucleic acid is at least 90% or more, preferably 91% or more, more preferably 92% or more, further preferably 93% or more, particularly preferably 94% or more, and most preferably 95% or more. To do.
- the nucleic acid consisting of the salt represented by any one of SEQ ID NOS: 1337 to 2851 and the base sequence having 80% or more identity with the base sequence is BLAST [J. Mol. Biol., 215, 403 (1990)) or FASTA [Methods in Enzymology, 183, 63 (1990)], etc., and a nucleic acid consisting of the nucleotide sequence represented by any one of SEQ ID NOs: 1337 to 2851 And at least 80% or more, preferably 85% or more, more preferably 90% or more, even more preferably 92% or more, particularly preferably 95% or more, and most preferably 96% or more.
- nucleic acid that hybridizes under stringent conditions for example, a nucleic acid having the base sequence represented by any one of SEQ ID NOs: 1-2851 or a fragment of a part thereof is used. 20xSSC 7.5 mL, 1M Na HPO (pH 7.2) 0.6 mL
- the nucleic acid may be any molecule in which nucleotides and molecules having functions equivalent to the nucleotides are polymerized.
- RNA which is a polymer of ribonucleotides, and deoxyribonucleotides.
- the polymer include DNA, RNA and a mixture of RNA and nucleotide, and nucleotide polymers including nucleotide analogs, and may be nucleotide polymers including nucleic acid derivatives. It can be a nucleic acid or a double-stranded nucleic acid.
- MicroRNA or a derivative thereof, a microRNA precursor or a derivative thereof are also included in the nucleic acid of the present invention.
- the nucleotide analog is used to improve or stabilize nuclease resistance as compared with RNA or DNA, to increase the affinity with a complementary strand nucleic acid, or to permeate cells.
- Any molecule that modifies ribonucleotides, deoxyribonucleotides, RNA, or DNA to enhance or visualize The molecule may be a naturally occurring molecule or a non-natural molecule, and examples thereof include sugar moiety-modified nucleotide analogs and phosphodiester bond-modified nucleotide analogs.
- the sugar moiety-modified nucleotide analogue may be any substance as long as it is obtained by adding or substituting any chemical structural substance to a part or all of the chemical structure of the sugar of the nucleotide.
- 2 '_0 nucleotide analogs substituted with methyl ribose
- 2 ′ ⁇ 0 nucleotide analogs substituted with propyl ribose
- nucleotide analogues substituted with 2′— ⁇ _fluororibose sugar moiety Bridged Nucleic Acid (BNA), which has two circular structures by introducing a cross-linked structure
- a phosphodiester bond-modified nucleotide analog is a substance that has a chemical structure of a portion of a nucleotide phosphodiester bond, and has any chemical substance added to or added to it.
- nucleotide analogues substituted with phosphorothioate linkages nucleotide analogues substituted with ⁇ 3'- ⁇ 5 'phosphoramidate linkages, etc. [cell engineering, 16, 1463-1473 (1997), RNAi method, anti-sense method, Kodansha (2005)].
- the nucleic acid derivative is used to improve nuclease resistance, stabilize it, increase its affinity with complementary strand nucleic acids, and improve cell permeability compared to nucleic acids.
- the molecule may be any molecule obtained by adding another chemical substance to the nucleic acid for visualization.
- nucleic acid derivative for example, as a modified sugar, an oligonucleotide derivative substituted with 2'-0_propylribose, an oligonucleotide derivative substituted with 2'-methoxyethoxyribose, Oligonucleotide derivatives substituted with 2'-0-methylribose, oligonucleotide derivatives substituted with 2'-0-methoxyethyl ribose, substituted with 2'-0- [2- (guanidinium) ethyl] ribose Oligonucleotide derivatives substituted with 2'-0-fluororibose, etc., and phosphoric acid group modifiers include phosphorothioate-linked phosphate diester bonds in oligonucleotides.
- Transformed oligonucleotide derivative, phosphodiester in oligonucleotide 'linkage is N3'-P5 'phosphoramidate Was converted into engagement oligonucleotide derivative can Oh gel [Cell Technology, 16, 1463-1473 (1997), RNAi method and antisense method, storytelling, Inc. (2005)].
- the microRNA derivative may be any polymer that contains a molecule other than ribonucleotides having the same function as the microRNA.
- deoxyribonucleotides may be used.
- DNA a polymer in which RNA and DNA are mixed, and a nucleotide polymer containing a nucleotide analogue, and a single-stranded chain that may be a nucleotide polymer containing a nucleic acid derivative It may be a nucleic acid or a double-stranded nucleic acid.
- the derivative of the microRNA precursor may be any polymer containing a molecule other than a ribonucleotide having a function equivalent to that of the microRNA precursor.
- the polymer include DNA, RNA and DNA mixed polymers, and nucleotide polymers including nucleotide analogs, and nucleotide polymers including nucleic acid derivatives. It may be a strand nucleic acid or a double-stranded nucleic acid.
- the method for producing the nucleic acid of the present invention is not particularly limited, and the nucleic acid can be produced by a method using a known chemical synthesis method or an enzymatic transcription method.
- Known chemical synthesis methods include phosphoramidite method, phosphorothioate method, phosphotrieste Method, CEM method [Nucleic Acid Research, 35, 3287 (2007)], and the like, for example, can be synthesized by ABI3900 high-throughput nucleic acid synthesizer (manufactured by Applied Biosystems).
- Examples of the enzymatic transcription method include a transcription method using a plasmid or DNA having a desired base sequence and a typical phage RNA polymerase such as T7, ⁇ 3, or SP6 RNA polymerase. Can do.
- any method that can detect a nucleic acid in a sample may be used.
- Northern hybridization (2) Dot blot hybridization, (3) In situ hybridization, (4) Quantitative PCR, (5) Differential 'hybridization, (6) Microarray, (7) Ribonuclease protection assay, etc.
- any method for detecting a mutation in a nucleic acid such as microRNA or a microRNA precursor using the nucleic acid of the present invention any method can be used as long as it can detect a mutation in the base sequence of the nucleic acid in a sample.
- a method for detecting a heteroduplex formed by hybridization of a nucleic acid having a non-mutated base sequence and a nucleic acid having a mutated base sequence, or a base sequence derived from a specimen directly For example, a method of detecting the presence or absence of mutation by sequencing may be mentioned.
- nucleic acids such as microRNAs and microRNA precursors can be obtained from a mixture of various cells. Any method can be used as long as it can separate cells that express the nucleic acid.
- a probe fluorescently labeled with a nucleic acid having a sequence complementary to the base sequence of the nucleic acid of the present invention is introduced into the cell, and
- a method may be used in which only cells that have been cleaved and hybridized with a labeled probe are separated by a flow cytometer having a sorting function.
- the vector expressing the nucleic acid of the present invention refers to a vector designed to biosynthesize the nucleic acid of the present invention by being transcribed in a cell or in a test tube. As long as it has a promoter capable of transcribing the nucleic acid of the present invention, any other vector may be used. Specifically, PCDNA6.2-GW / miR (Invitrogen), pSilencer 4.1-CMV (Ambion), pSINsi-hHl DNA (Takara Bio), pSINsi_hU6 DNA (Takara Bio), P ENTR / U6 (Invitrogen), etc.
- a nucleic acid such as the microRNA of the present invention is used as a target base. Any method may be used as long as it suppresses the expression of the target gene by utilizing the activity of suppressing the expression of mRNA having the sequence.
- to suppress the expression includes the case of suppressing the translation of mRNA and the case of reducing the amount of the protein translated from the mRNA force by cutting or decomposing the mRNA.
- the target base sequence refers to a nucleic acid base sequence of several bases recognized by a nucleic acid such as the microRNA of the present invention. Translation of mRNA having the base sequence is suppressed by a nucleic acid such as the microRNA of the present invention. Translation of mRNA having a base sequence complementary to the 2nd to 8th base sequence and column on the 5 ′ end side of microRNA is suppressed by the microRNA [Current Biology, 15, R458-R460 (2005 Therefore, a base sequence complementary to the second to eighth positions on the 5 ′ end side of a nucleic acid such as the microRNA of the present invention can be mentioned as a target base sequence of the nucleic acid such as the microRNA.
- a target sequence complementary to the 2-8th base sequence on the 5 'end side of microRNA is prepared, and mRNA containing the exact match sequence is compared to the 3' UTR base sequence group of human mRNA. It can be determined by selecting by a method such as character string search.
- the 3'UTR base sequence group of human mRNA is obtained using the ⁇ nom sequence and gene position information that can be protected from ⁇ UCSC Human Genome Browser Gateway (http://genome.ucsc.edu/cgi-bm/hgijateway) ''. Can be produced.
- the gene having the target base sequence of the microRNA represented by SEQ ID NOs: ⁇ to 1336 As a specific example of the gene having the target base sequence of the microRNA represented by SEQ ID NOs: ⁇ to 1336, the US National Biotechnology Company's [National Center for Biotechnology Information (NCBI) EntreGene Table 2—: Names used in the database (http: ⁇ www.ncbi.nlm.nih.gov/Entrez/) and their names (Official Symbol and Gene ID)! The gene described in ⁇ 2-35 can be mentioned. As the gene name, the name as of March 2006 in the EntreGene database was used.
- NCBI National Center for Biotechnology Information
- PRKCZ (5590); TNFRSF14 (8764): TNFRSF9 (360); RCC2 (5592P); NBL1 (4681): LDLRAD2 (4019); CDC42 (998>; E2
- SB (411): SEMA6A (57556); RAD50a01. "> PFD 1 (52013 ⁇ 4WDR55 (54853): N BP3 (23l38); ATXN1 (6 0) f 21 ⁇ 30871>; IER3 (3870); MC) 1 ( ⁇ 01250 ): C6ori 7 (57827 BTBl2 (221527); CREBL1 (138S>; PBX2 (508; BAK1 (578> JHPK3a 17283): CDKN1A (10 6): 2FANb3 (60685); KCNK5 (8e 5>: NFYA (4800): FOXO3A (2i09): SNX8 (29 8 (5476> .CARD4 (10392); WHBA (3624); DKFZp76112123 (83637): ADCY1 (107>: YWHAG (7532): FLJ39237 (375607); LRRC4 (6
- E2F2 870 C) C21 (64793): SDG3 (9672): RBBP4 (5928): KIAA0319U79932; 'orf84 (149469); AGBL4 (8487i): CE
- iKiSF4B (57863): AV1 (89796); PPPim2B (4 ⁇ 60); RPK5 (25778); C1orf95 (375057); YPEL5 (516 6): TEX2ei (1134)
- PCDHi 5097: PDGFRB, 59): NDSTK3340: PLX2 (10814): N4BP3 (2313W : RNF5 (6048); PBX2 (5089) SAK1 (57-8): PACSIN1 (29993): MOCS1 (4337): FOXP ( ⁇ 6''3>: MGC45 91 (221416): TRAM2 (697); PSCD3 (92e5): AQP1 (358); ⁇ 12 ⁇ 883): CASP3 ⁇ 4835): yiP 2;: 7434> C9orf25.
- TPM2 ( 7169): NTR 21 ⁇ 4915) ⁇ 9orf47 (286223): ST6G ALNAC6 (30815); SPOCK2 (9 ⁇ ); SH3PXD2A (9644); VA) O (11023); MTG1 (92n0): SPR (50352): C11orMK747): P 468): MYL6 (4637); GLS2C27l65): CTDSP2 (l010 ⁇ : DDX54 (79039): B4GALN "n (2583); SLC8A3 (6547) J» CNX (22990):
- TNFRSF14 (876): NBL1 (4681): CDC42 (998); LIN28 (79727); KHDRBS1 (10657): J JD2A (9682): GFn (2iB72): CDC14
- AMraO1 (57463); MCL1 (417p); RORC (6097) WEF2D (4209); PEAl5 (8682); UHMKl027933 ADORAl (134):
- PAX3 (5077): HDAC4 (9759); IF1A (547); SRGAP3C99m> .VHLi7428); RBMS3 (27303); AXUD 6 651); ZNF65K92
- EP 3952; FASTK (l0922); TNFRSF10B (8795); TNFRSFlOA (8797): TRlM35 (23037>; CUJ (119l IF13B (23303); DUS
- SPOCK2 (980 ⁇ : NOLC1 (9221): TCF7L2 (6934): C10orf46 (143384); TIAU (7073); LRRC56 (115399); IGF2 (348
- ANKRD9022416 AKT1 (207): KLF13 (51621); TPM1C7168>; GSK (145>, lGnR (3480); CCDC78 (124093; iQTNF8 (
- TSC2 7249
- TRAF7 8 231): TNFRSF12A (51330): £ RN2 (10595; APK3 (53 ⁇ 495); FBXU9 (54S20); CiAPIN
- CMTM4 14e223: TrRADD (87n): l_OC283849 is 838493 ⁇ 4SLC12A (6560): SMPP3 (55512): KIAA0513 (976): C
- NF1 4763: RAB11 F1P4 (8 ⁇ M0); RASIJ0B (91608): NR1D1 (9572): HDAC5 (10014): CRHRKU94); APT (4137):
- NGFR (4804): SPHia (8877): TMCe (11322); SOGS3 (902i); PCYT2 is 833): aDEA (1 M9); CABLES1 (91768): PHLPP (2
- FOSB (2354>, BBC3 ⁇ 27 "3); SLG8A2C65 3); BAX (581>; CD37 (951) SCL2L12 (83596) ⁇ 281 A (5518): YADM
- UB £ 2V1 (7335): CABL £ S2 (8l928); DID01 (11083 ADARBKl04): BCL2L13 (23786); DGCRi4 (8220): SEPT5 (5413);
- MAPK1 (559): SMARCB1 (6598): MN1 (4330); GAS2L1 (10634 UF (3976>: MCM5 (4174); IAA1904 ("4794): CARD10)
- SBF1 (6305); MAPK8IP2 (23542); RS1 (6247): PCTK1 (5127): ELK1 (2002): ZNF81 (3473): SMC1L1 (8243); RP1-112
- ZGPAT (84619): MAPK1 (5594): NF2 (4771); CARD10 (29775); NPTCR (23467XTNRCeB (23112); TOB2 (1076 FIGF (2277); S C1 LI (8243); SEPT6C23157); ECP2 (4204) ,
- CDC2L2 (985); TNFRSn4 (8764): C; HD5 (26038): CDC42C998): E2 iia870); WASF2 (10ie3): RCCK ⁇ 04); KHD BSl (10657); LCK (3932): KIAA0319lX79932): raMS3 ( 9783): CDC20 (991 DKN2C (1031): NOTCH2 (4853): CKS1B0l63>; C1orf21 (81563> PPP1R12B (4660); SYT2O 27833; ADORA1 (i343 ⁇ 4PH3C2BC5287) L10 (3586>: IL24 ("009) 2 (5362): VANGL1 (81839); KiF21 B (23046): RHOB (8): MAPF ⁇ E322924): TGFA (7039>; HK2 (3099); BRRNi (23397); W HBBC3625) f RCC3 (2071)
- TNP 2 (30000.LPHN 1 (22859); SIRT2 (22933> .3SF4GC199731); FOSBC2354.D WD (1762); BBC3 ⁇ 2711 ZR PS" (6205>; PPP2R1A (551 GF3 ⁇ 4LF1 (2909); ZNF343a9n5): C20orf "6 (65992): E2Fl (1869): CEP250 () n90); PPP 1 R16 ⁇ (2 ⁇ 1> ZHX3 (23051): MS (140730); STK4 (6789) : DIDOKl 1083): TNFRSFeB (8771) ⁇ GPAT (84619) APP (35l); ADA Bl (ltM>, LSS (4047): HK: 2 (23n9): MAPKK5594): PPM1F (9647): MlF (4282
- SDF4 (51150); B3GALT6C126792): UBE2J2 (118424); CENTB5 (116983); SKIi: 6497): C 1 orf93 (127281 SPSBI (80176); PIK3CD (5293); TINAGL1 (64129); KIAA0319L (79932); IGSF4B (79932) 57863 NF648 (127665); WNT3A (89780); OR2W5C4 41 32) ⁇ R2C31 ⁇ 21472); ATAD3C (219293>: INPP5D (3635): ANKRDi23 (200539); Ali4P1 (10267): raSl C25907): PH-4 (5 4681 > JHPia (9807): PLXNA1 (5361): CLDN18 (5!
- BRF1 (2972): PACS2C23241); C 1 orf37 (283687); UBE2K7329): IFn40 (9742); CAS IN1 (575243 ⁇ 4ZNF213 (7760) ZN
- E2F2 (1870> .CCDC21 (647 3); LAPTM5 805>: ZBTB8 (127 57): MGC33556 (3395 1); RA33Bf (586Ei); CDC42SE1 (56.882>; UHMK1 (127933): lL24 (11009); TRAF5 (7188>: C1orf95 (375057): VANGL1 (81839>: SFX 5 (9 097) ⁇ ASP10C843; CD28 (940); COL4A3a2B5); J10996 (5 520) ⁇ RM7C29n): SRGAP3 (990l); PH “4 (54681 ): RASSFKl1186); PraCK LE2 (166336); ST3GAL6n0402); PCNP (57092): RNF7 (96l6>; HIP2 (3093): TMPf3 ⁇ 4SS11E (289835: OSMR (9180: F2R (2l49); T ⁇ CAM2
- DIP13B (551 ⁇ ): LATS2 (26524): TNFRSF19 is 5504): FLn (232; HSPH1 (10808>: FOXO1A (2308); S
- AP3K9 4293 n4orf43 (91748): LTBP2 (4053); DIO2 (173); rrPK1 (3705): EIF5O983): iJAG2 (37W); GOLGA8G (2e37
- tTP53BP1 (7l58): FGF7 (2252): NARG2 (79664); FEM1Bi: iOn6); IREB2 (3658): ABHD2 (11057): GSPT1 (2935): MKL
- soo rain oozai / e soo rain oozai / e :) d 6 ⁇ 80 / 800Z OAV O / iAV 6lio8 / D / isIId ii
- the nucleic acid of the present invention can be used as a method of screening for a substance that promotes or suppresses the expression or function of nucleic acid such as microRNA or microRNA precursor using the nucleic acid of the present invention. Any method can be used as long as it is a method for screening for substances that promote or suppress the expression or function of nucleic acids, such as DNA precursors and microRNA precursors. For example, by introducing into a cell a vector that expresses a nucleic acid such as the microRNA or microRNA precursor of the present invention, a substance that suppresses the expression of the target gene or a substance that promotes the expression of the target gene. A screening method is mentioned.
- the substance that suppresses the expression of the target gene may be any substance that suppresses the expression of the target gene mRNA, but siRNA for the target gene that is preferred by the nucleic acid is further included. preferable.
- siRNA for the target gene any substance that promotes the expression of the target gene mRNA may be used.
- a nucleic acid is preferable, and the expression of the target gene is suppressed.
- SiRNA against microRNA is more preferred.
- the cell into which the nucleic acid or vector of the present invention has been introduced may be any cell as long as it is a cell into which the nucleic acid or vector of the present invention has been introduced outside the body.
- progenitor cells and mast cell progenitor cells or cells formed by differentiation of mesenchymal stem cells and mesenchymal stem cells, such as skin, lung, small intestine, nose, tonsils, eyelid conjunctiva, blood vessel wall Cells present in tissues such as bone marrow, or tissues such as bone marrow, adipose tissue, umbilical cord blood, endometrium, dermis, skeletal muscle, periosteum, dental follicle, periodontal ligament, dental pulp, and tooth germ Examples of cells include osteoblasts, fat cells, and muscle cells.
- mast cells are cells that are activated by various stimuli, cause degranulation, release and produce many inflammatory mediators, and are also involved in the pathogenesis of various allergic diseases. Let's do it.
- mesenchymal stem cells are present in mesenchymal tissues such as bone marrow, adipose tissue, umbilical cord blood, endometrium, dermis, skeletal muscle, periosteum, dental follicle, periodontal ligament, dental pulp, and tooth germ.
- mesenchymal tissues such as bone marrow, adipose tissue, umbilical cord blood, endometrium, dermis, skeletal muscle, periosteum, dental follicle, periodontal ligament, dental pulp, and tooth germ.
- the term refers to cells having the ability to differentiate into mesenchymal cells such as osteoblasts, adipocytes, and muscle cells.
- the medicament comprising the nucleic acid of the present invention as an active ingredient can be used for diagnosis or treatment of diseases caused by abnormalities of mast cells.
- Abnormalities in mast cells include abnormal degranulation.
- the nucleic acid of the present invention can also be used as a degranulation promoter or degranulation inhibitor for mast cells.
- substances that promote or repress the expression or function of nucleic acids such as the microRNAs and microRNA precursors of the present invention, and substances that suppress or promote the expression of target genes of nucleic acids such as the microRNAs of the present invention. It can also be used for diagnosis or treatment of diseases caused by abnormal mast cells. These substances can also be used as mast cell degranulation promoters or degranulation inhibitors.
- diseases caused by abnormal mast cells include atopic dermatitis, asthma, chronic obstructive pulmonary disease, and allergic diseases.
- the medicament comprising the nucleic acid of the present invention as an active ingredient can be used for diagnosis or treatment of a disease caused by abnormal proliferation and / or differentiation of mesenchymal stem cells. It also promotes or suppresses the expression or function of nucleic acids such as the microphone RNA and microRNA precursor of the present invention. Substances that suppress or promote the expression of target genes of nucleic acid such as the microRNA of the present invention are also used for diagnosis or treatment of diseases caused by abnormal mesenchymal stem cell proliferation and Z or differentiation. be able to.
- Specific examples of the diseases caused by abnormal proliferation and / or differentiation of mesenchymal stem cells include cancer, osteogenesis imperfecta, cartilage dysplasia, diabetes and the like.
- the medicament comprising the nucleic acid of the present invention as an active ingredient can be used for diagnosis or treatment of diseases caused by abnormalities such as cell proliferation or tissue hyperplasia.
- the nuclear acid of the present invention can also be used as a cell growth inhibitor or growth promoter.
- a substance that promotes or suppresses the expression or function of a nucleic acid such as the microRNA or microRNA precursor of the present invention, or a substance that suppresses or promotes the expression of a target gene of a nucleic acid such as the microRNA of the present invention is also a cell. It can be used for diagnosis or treatment of diseases caused by abnormalities such as growth of tissues and tissue hyperplasia. These substances can also be used as cell growth inhibitors or growth promoters.
- abnormal cell proliferation refers to a state in which cells proliferate at a rate that is not normal in vivo.
- diseases caused by abnormal cell proliferation or tissue hyperplasia include cancer, arteriosclerosis, rheumatoid arthritis, benign prostatic hyperplasia, percutaneous transvascular coronary artery Examples include vascular restenosis after plasty, pulmonary fibrosis, glomerulonephritis, and autoimmune diseases.
- nucleic acid of the present invention is a microRNA or a microRNA precursor.
- Human mast cells are not particularly limited as long as they are obtained safely and efficiently.
- known methods from human lung, skin, fetal liver, etc. [J. Immunol. Methods, 169, 1 53 (1994); J. Immunol., 138, 861 (1987); J. Allergy Clin. Immunol, 107, 322 (2001); J. Immunol. Methods., 240, 101 (2000)] it can. Further, known methods [J. Immunol., 157, 343, (1996); Blood, 91, 187 (1998); J. Allergy Clin.
- the prepared mononuclear cells can be prepared by culturing in the presence of stem cell factor (hereinafter also referred to as SCF) and differentiating into fertile cells.
- SCF stem cell factor
- a cell line with established human mast cell power can also be used.
- LAD2 Leuk. Res., 27, 671 (2003); Leuk. Res., 27, 677 (2003) is known to retain the properties of human mast cells. )] Etc.
- RNA Total RNA is extracted from mast cells obtained by the various methods described above, and small RNAs containing microRNAs expressed in mast cells can be obtained using the RNA as follows. ,
- RNA separation of small RNA by 15% polyacrylamide gel electrophoresis is performed according to the method described in Genes & Development, 15, 188-200 (2000).
- small molecule through 5′-end dephosphorylation, 3′-adapter ligation, phosphorylation, 5, one adapter-one ligation, reverse transcription, PCR amplification, concatamerization, vector ligation Examples include a method of cloning RNA and determining the base sequence of the clone.
- RNA Cloning Kit manufactured by Takara Bio Inc.
- RNA sequence is a microRNA can be determined by following the criteria described in RNA, 9, 277-279 (2003). For example, in the case of a low molecular weight RNA obtained by the above method and determined in base sequence, it can be carried out as follows.
- peripheral genome sequence information obtained by extending the DNA sequence corresponding to the obtained small RNA base sequence by about 50 nt to the 5 'end side and 3' end side, respectively, is obtained, and the genome sequencing power is also transcribed. It predicts the secondary structure of RNA. As a result, when it has a hairpin structure and the base sequence of the low molecular weight RNA is located in one strand of the hairpin structure, it can be determined that the low molecular weight RNA is a microRNA. Genome sequences are publicly available and Example L is available from UCS and ijenome Bioinformatics (http: //genome.ucsedu/).
- RNAfold Nucleic Acids Research, 31, 3429-3431 (2003)
- Mfold Nucleic Acids Research, 31, 3406-3415 (2003). You can use it.
- existing microRNA sequences are registered in the miRBase (http://microrna.sanger.ac.uk/) database, and the existing microRNA sequences are determined according to whether they are identical to the sequences described here. It can be determined whether or not it is identical to RNA.
- Examples of the microRNAs thus identified and expressed in mast cells include nucleic acids having a base sequence represented by any one of SEQ ID NOs: 1 to 1336.
- the genome sequence corresponding to the identified microRNA is compared with the genome sequence of another organism, and the nucleotide sequence represented by any one of SEQ ID NOs: 1 to 1336 is 90% or more, preferably 95% or more.
- a sequence containing a sequence encoding microRNA can be identified as a sequence encoding microRNA precursor.
- the microRNA precursor expressed in the mast cell of the present invention include a nucleic acid having a base sequence represented by any one of SEQ ID NOs: 1337 to 2851.
- the genome sequence corresponding to the identified microRNA precursor is compared with the genome sequence of another organism, and the base sequence represented by any of SEQ ID NOs: 1337 to 2851 is preferably 80% or more, preferably Can identify a nucleic acid having a base sequence with 90% or more, more preferably 95% or more, and still more preferably 97% or more as a microRNA precursor in the organism.
- RNA which is a ribonucleotide polymer
- DNA a polymer of nucleotides
- the DNA base sequence can be determined based on the RNA base sequence identified in 1. above.
- the DNA base sequence corresponding to the RNA base sequence can be uniquely determined by replacing U (uracil) contained in the RNA sequence with T (thymine). Further, it can be synthesized in the same manner as a polymer in which ribonucleotides and deoxyribonucleotides are mixed, or a polymer containing nucleotide analogues.
- the method for synthesizing the nucleic acid such as the microRNA or microRNA precursor of the present invention is not particularly limited. can do. Examples of methods using known chemical synthesis methods include phosphoramidite method, phosphorothioate method, phosphotriester method, CEM method [Nucleic Acid Research, 35, 3 287 (2007)], and the like. It can be synthesized with an ABI3900 high-throughput nucleic acid synthesizer (manufactured by Applied Biosystems).
- Examples of the enzymatic transcription method include a transcription method using a typical phage RNA polymerase, for example, T7, ⁇ 3, or SP6 RNA polymerase, with a plasmid or DNA having a target base sequence as a cage.
- a typical phage RNA polymerase for example, T7, ⁇ 3, or SP6 RNA polymerase
- MicroRNA is a precursor of microRNA that has a hairpin structure. MicroRNA is produced through processing by a protein called Dicer, a kind of RNase III endonuclease, in the cytoplasm, and suppresses translation of mRNA having a target base sequence. Therefore, it is possible to detect whether the nucleic acid obtained based on whether or not it has the function is a microRNA. [0126] For example, the ability to function as a microRNA precursor can be measured based on whether RNA is processed by RNaselll endonuclease.
- RNA whose function is to be detected is reacted with RNaselll endonuclease and the reaction product is electrophoresed, it has a function as a microRNA precursor, and if it has been processed, it is processed 20-25 bases.
- RNaselll endonuclease is not particularly limited as long as it has an activity to process a microRNA precursor, but it is preferable to use a Dicer protein.
- si-RNAse IIITM (Takara Bio), Cold Shock-DICER (Takara Bio), Recomb inant Dicer Enzyme (Stratagene), BLO K iT Dicer RNAi Transfection Kit (Invi trogen) And X-treme GENE siRNA Dicer Kit (Roche Applied Science), etc .; and can be measured by following the reaction conditions in the attached instructions.
- Examples of a method for detecting the function of microRNA include a method for measuring the force having the function based on the ability to suppress translation of mRNA having the target base sequence.
- MicroRNA is known to suppress the translation of mRNA containing its target nucleotide sequence in the 3 'terminal untranslated region (3' UTR) [Current Biology, 15, R458-R460 (20 '05)] . Therefore, a DNA in which the target base sequence for the RNA to be measured is inserted into the 3 ′ UTR of an appropriate reporter gene expression vector is prepared and introduced into a host cell suitable for the expression vector. By measuring the expression of the reporter gene when RNA is expressed, it is possible to detect whether or not it has the function of a microRNA.
- the reporter gene expression vector may have any promoter as long as it has a promoter upstream of the reporter gene and can express the reporter gene in the host cell.
- any reporter gene can be used.
- firefly 'luciferase gene renilla luciferase gene, chloramphenicol acetyltransferase gene, j3
- the gene, 0-galactosidase gene, 0-lactamase gene, equorin gene, green'fluorescent protein gene and DsRed fluorescent gene can be used.
- RNA can be expressed by the method described in 6. below.
- the function of the microRNA can be detected as follows. First, the host cells are cultured in a multi-well plate or the like to express a reporter gene expression vector having a target nucleotide sequence and RNA. Then, the function of the microRNA is detected by measuring the reporter activity and detecting that the reporter activity decreases when the RNA is expressed compared to the case where the RNA is not expressed. be able to. '4. Method for detecting the expression of nucleic acids such as microRNA and microRNA precursors using the nucleic acid of the present invention
- nucleic acid ⁇ Such as microRNA or microRNA precursor using the nucleic acid of the present invention will be described.
- Examples of methods for detecting the expression of microphone 0RNA, microRNA precursors, etc. include:
- Examples include U hybridization, (4) quantitative PCR, (5) differential, hybridization, (6) microarray, and (7) ribonuclease protection assay.
- sample-derived RNA is separated by gel electrophoresis, and then transferred to a support such as a nylon filter, and a probe appropriately labeled based on the base sequence of the nucleic acid of the present invention is prepared.
- a method of detecting a band specifically bound to the nucleic acid of the present invention by performing hybridization and washing specifically, for example, the method described in Science 294, 853-858 (2001), etc. Can be done according to.
- the labeled probe may be a radioisotope, piotin, digoxigenin, fluorescent group, chemiluminescent group, etc. by a method such as nick 'translation, random priming or phosphorylation at the 5' end. It can be prepared by incorporating it into DNA, RNA, or LNA having a sequence complementary to the base sequence.
- the amount of labeled probe binding reflects the expression level of nucleic acids such as microRNA and microRNA precursors. Therefore, by quantifying the amount of bound labeled probe, the expression level of microRNA and microRNA precursors can be reduced. It can be quantified. Electrophoresis, transfer to membrane, probe preparation, hybridize —The detection of nucleic acids and nucleic acids can be performed by the method described in Molecular 'Cloning 3rd Edition, Cold Spring Harbor Laboratory Press, NY, USA (2001).
- nucleic acids extracted from tissues and cells are spot-fixed on the membrane in a spot form, hybridized with the probe, and specifically hybridized with the probe. It is a method for detecting a nucleic acid.
- a probe similar to the Northern hybridization can be used.
- Nucleic acid preparation, spotting, hybridization, and detection can be performed by the methods described in Molecular 'Cloning 3rd Edition'.
- the in dm hybridization is performed using a paraffin or cryostat section of tissue obtained from vital force or a fixed cell as a specimen, a labeled probe and a hybridization, and a washing process.
- This is a method for examining the distribution and localization of microRNAs and microRNA precursors in tissues and cells by microscopic observation [Methods in Enzymology, 254, 419 (1995)].
- a probe similar to Northern hybridization can be used. Specifically, microRNA, microRNA precursors, and the like can be detected according to the method described in Nature Method 3, 27 (2006).
- cDNA synthesized from a sample-derived RNA using a reverse transcription primer and reverse transcriptase (hereinafter, this cDNA is also referred to as a sample-derived cDNA) is used for measurement.
- a primer for reverse transcription used for cDNA synthesis a random primer or a specific RT ply or mer can be used.
- the specific RT primer is a primer having a sequence complementary to the base sequence corresponding to the microRNA of the present invention, the micromouth RNA precursor, etc., and the surrounding genomic sequence.
- the nucleotide sequence corresponding to the microRNA, the microRNA precursor and the surrounding genomic sequence, or the nucleotide sequence corresponding to the reverse transcription primer was designed. PCR is performed using type-specific primers, cDNA fragments are amplified, and the number of cycles required to reach a certain amount is detected. The amount of microRNA and microRNA precursor contained in the sample-derived RNA is detected. As a type-specific primer, select an appropriate region corresponding to the microRNA or microRNA precursor and its surrounding genomic sequence, and the 5 'end of the base sequence in that region has a sequencing capacity of 20 to 40 bases.
- a pair of DNA or LNA consisting of DNA or LNA and a mating IJ complementary to 20 to 40 bases at the 3 ′ end can be used. Specifically, it can be performed according to the method described in Nucleic Acids Research, 32, e43 (2004).
- a specific RT primer having a stem'loop structure can also be used as a reverse transcription primer for cDNA synthesis. Specifically, it can be performed according to the method described in Nucleic Acid Research, 33, el79 (2005) or using TaqMan MicroRNA Assays (manufactured by Applied Biosystems).
- reverse transcription reaction is performed by adding p, olyA sequence to the sample-derived RNA using polyA polymerase and using the base sequence containing oligo dT sequence as a primer for reverse transcription. It can also be done. Specifically, miScript System (Qiagen) or QuantiMir RT Kit (System Biosciences) can be used.
- a sample-derived cDNA By subjecting the sample-derived cDNA to hybridization and washing, the change in the amount of microRNA, microRNA precursor, etc. can be detected.
- differential hybridization (Trends Genet., 7, 314 (1991)]
- microarray Gene Res., 6, 639 (1996)
- an internal control such as a nucleotide sequence corresponding to U6 RNA is immobilized on a filter or substrate, so that the difference in the amount of microRNA, microRNA precursor, etc. between the control sample and the target sample can be reduced. It can be detected accurately.
- labeled cDNA is synthesized using dNTPs (mixtures of dATP, dGTP, dCTP, and dTTP) of different labels based on RNA derived from the control sample and target sample, and 2 on a single filter or single substrate. By hybridizing two labeled cDNAs simultaneously, accurate quantification of microRNA and microRNA precursors can be performed.
- microRNA, microRNA precursors, and the like can be quantified.
- microRNAs can be detected using microarrays described in Pro Natl. Acad. Sci. USA, 101, 9740-9744 (2004), Nucleic Acid Research, 32, el88 (2004), etc.
- microRNA and the like can be detected or quantified using mirVana miRNA Bioarray (Ambion).
- a promoter sequence such as T7 promoter or SP 6 promoter is bound to the 3 'end of the base sequence corresponding to the microRNA of the present invention, the microRNA precursor or the genomic sequence surrounding the some, and labeled.
- Labeled antisense RNA is synthesized by an in vitro transcription system using NTP (mixture of ATP, GTP, CTP, UTP) and RNA polymerase.
- NTP mixture of ATP, GTP, CTP, UTP
- the labeled antisense RNA is bound to the sample-derived RNA to form an RNA-RNA hybrid, and then digested with ribonuclease A that degrades only single-stranded RNA.
- the digested product is subjected to gel electrophoresis to detect or quantify RNA fragments protected by digestion by forming RNA-RiMA hybrids as microRNAs or microRNA precursors.
- RNA-RiMA hybrids as microRNAs or microRNA precursors.
- microRNA and the like can be detected or quantified using mirVana miRNA Detection Kit (Ambion).
- nucleic acids such as microRNA and microRNA precursors using the nucleic acid of the present invention
- Methods for detecting heteroduplex include (1) heteroduplex detection by polyacrylamide gel electrophoresis [Trends genet., 7, 5 (1991)], (2) —single strand conformation polymorphism Analytical methods [Genomics, 16, 325-332 (1993)], (3) Chemical cleavage of mismatches (CCM, Human Genetics (1996), Tom Strachan and Andre P. Read, BIOS Scientific Publishers Limited], (4) Enzymatic cleavage method of mismatches [Nature Genetics, 9, 103-104 (1996)], (5) Denaturing gel electrophoresis [Mutat. Res., 288, 103 -112 ⁇ 993) And the like.
- the heteroduplex detection method by polyacrylamide gel electrophoresis is, for example, as follows. Do it like this. First, sample-derived DNA or sample-derived cDNA is amplified as a fragment smaller than 200 bp using a template designed based on the genomic base sequence including the base sequence of the microRNA or microRNA precursor of the present invention. To do. When heteroduplexes are formed, those that are slower in mobility than homoduplexes without mutations can be detected as extra bands. The degree of separation is better when special gels (Hydro-link, MDE, etc.) are used. Searching for fragments smaller than 200 bp can detect insertions, deletions, and most single base substitutions. Heteroduplex analysis is preferably performed with a single genolet combined with the single-strand conformation analysis described below.
- sample-derived DNA or sample-derived cDNA is used as a template to base sequences such as microRNA and microRNA precursors.
- base sequences such as microRNA and microRNA precursors.
- DNA amplified as a fragment smaller than 200 bp is denatured and run in native polyacrylamide gel.
- the amplified DNA can be detected as a band by labeling the primer with an isotope or fluorescent dye, or by silver-staining the unlabeled amplification product.
- fragments with mutations can be detected from the difference in mobility.
- sample-derived DNA or sample-derived cDNA was used as a template and amplified with primers designed based on the genomic base sequence including the base sequence of microRNA and microRNA precursors.
- the DNA fragment is hybridized with a labeled nucleic acid that is isotopically associated with the nucleic acid of the present invention, and treated with osmium tetroxide to cleave one strand of the mismatched DNA. Mutations can be detected.
- CCM is one of the most sensitive detection methods and can be applied to specimens of kilobase length.
- the mismatch can be cleaved enzymatically by combining T4 phage resol base and endonuclease VII, which is involved in mismatch repair in cells and RNaseA. it can.
- DGGE denaturing gradient gel electrophoresis
- Amplified DNA fragments move to the position where they are denatured into single strands in the gel and do not move after denaturation.
- the presence of the mutation can be detected because the movement of the amplified DNA in the gel differs in some cases.
- Mutations in microRNA and microRNA precursors can also be detected by directly determining and analyzing the base sequence of specimen-derived DNA or specimen-derived cDNA.
- Nucleic acids such as the microRNA and microRNA precursor of the present invention can be expressed by using an expression vector encoding the nucleic acid.
- the expression vector is capable of autonomous replication in a host cell or can be integrated into a chromosome, and contains a promoter at a position where a nucleic acid gene such as the microRNA or microRNA precursor of the present invention can be transcribed. And plasmids and viral vectors are preferably used. Any promoter can be used as long as it can be expressed in the host cell.For example, the RNA polymerase iKpol II) promoter and the RNA polymerase IlKpol III) promoter, which is a transcription system for U6 RNA and HI RNA, etc. Can be raised.
- Examples of the pol II promoter include the IE (immediate early) gene promoter of cytomegalovirus (human CMV), the early promoter of SV40, and the like.
- Examples of expression vectors using them include PCDNA6.2-GW / miR (Invitrogen) pSilencer 4.1-CMV (Ambion).
- Examples of pol III promoters include U6.RNA, HI RNA, and tRNA promoters. Examples of expression vectors using them include SINsi-hHl DNA (Takara Bio), pSINsi-hU6 DNA (Takara Bio), pENTR / U6 (Invitrogen) and the like.
- an expression vector having a T7 promoter, T3 promoter or SP6 promoter is preferred. You can use it. Examples of vectors having these include pBluescript II SK (+) (Stratagene). .
- the base sequence having the base sequence of the microRNA or microRNA precursor of the present invention includes a hairpin portion based on the base sequence of the genome including the base sequence.
- a recombinant viral vector is constructed by inserting a gene containing the nucleic acid base sequence of the present invention, such as the microRNA or microRNA precursor, downstream of the promoter in the viral vector.
- a gene containing the nucleic acid base sequence of the present invention such as the microRNA or microRNA precursor
- a packaging cell is a cell capable of supplying a deficient protein of a recombinant viral vector that lacks or lacks a gene encoding a protein required for viral packaging. Any cells can be used, for example, HEK293 cells derived from human kidney, mouse fibroblasts NIH3T3 * cells, and the like.
- Proteins supplemented by packaging cells include protein strength such as gag, pol, and env derived from mouse retrovirus in the case of retrovirus vector, and gag, pol, env, vpr, and vpu derived from HIV virus in the case of lentiviral vector , vif, tat, rev, ne proteins, adenoviral vectors such as ⁇ , ⁇ , etc., and adeno-associated viral vectors Rep (p5, pl9, p40), Vp ( Proteins such as Cap) can be used.
- protein strength such as gag, pol, and env derived from mouse retrovirus in the case of retrovirus vector
- gag, pol, env, vpr, and vpu derived from HIV virus in the case of lentiviral vector
- vif, tat, rev ne proteins
- adenoviral vectors such as ⁇ , ⁇ , etc.
- adeno-associated viral vectors Rep p5, pl9, p
- nucleic acid such as the microRNA or microRNA precursor of the present invention can be directly introduced into a cell without using a vector.
- Nucleic acids used in this method can be DNA, RNA, or nucleotide analogues, as well as these chimeric molecules or nucleic acid derivatives. Specifically, Pre-miR TM miRNA Precursor Moleculars (Ambion) or miRIDIAN microRNA Mimics (GE Healthcare) can be used. 7. Methods for promoting or inhibiting or promoting the expression or function of nucleic acids such as the microRNAs and microRNA precursors of the present invention
- Nucleic acids such as microRNAs and microRNA precursors of the present invention can be used in antisense technology and science, 50, 322 (1992), Chemistry, .46, 681 (1991), Biotechnology, 9, 358. (1992), Trends in Biotechnology, 10, 87 (1992), Trends in Biotechnology, 10 0, 152 (1992), Cell Engineering, 16, 1463 (1997)], Triple Helix Technology [Trends in Biotechnology, 10, 132 (1992)], ribozyme technology [Current Opinion in Chemical Biology, 3, 274 (1999), FEMS Microbiology Reviews, 23, 257 (1999), Frontiers in Bioscience, 4, D497 (1999), Chemistry & Biology, 6, R33 (1999), Nucleic Acids Research, 26, 52 37 (1998), Trends In Biotechnology, 16, 438 (1998)], Decoy DNA method [Nippon Rinsho-Japanese Journal of Clinical Medicine, 56, 563 (1998), Circulation Research, 82, 1 023 (1998), Experimental Nephrology, 5, 429 (1997) Nippon Rinsho-J
- Antisense refers to a nucleic acid having a base sequence complementary to a base sequence of a certain target nucleic acid, which can specifically hybridize to the base sequence and suppress the expression or function of the target nucleic acid. .
- these chimeric molecules or derivatives of the nucleic acids can be used as the nucleic acid used for antisense.
- antisense can be produced by following the method described in Nature 432, 226 (2004), etc., and its expression or function can be suppressed. Specifically, by using Anti-miR TM miRNA Inhibitors (Ambion) or miRIDIAN microRNA Inhibitors (GE Healthcare), expression of nucleic acids such as the microRNA or microRNA precursor of the present invention or Can suppress the function. '
- siRNA is a short double-stranded RNA containing a base sequence of a certain target nucleic acid, and can suppress the expression or function of the target nucleic acid by RNA interference (RN Ai).
- the siRNA sequence can be appropriately designed based on the conditions of the literature [Genes Dev., 13, 3191 (1999)] from the target nucleotide sequence.
- a siRNA can be produced by synthesizing two RNAs with a nucleic acid synthesizer and annealing them.
- siRNA expression vectors such as pSilencer 1.0-U6 (Ambion), pSUPER (01igoEngine) etc. are selected from 17 to 30 bases, preferably 18 to 25 bases, more preferably 19 to 23 bases. By inserting a DNA corresponding to this sequence, a vector expressing siRNA capable of suppressing the expression or function of the gene can be prepared.
- [0153] Expression in mast cells, mesenchymal stem cells or cancer cells using antisense or siRNA specific to microRNAs or microRNA precursors expressed in mast cells, mesenchymal stem cells or cancer cells It is possible to suppress the expression or function of microRNA or microRNA precursor. That is, by administering antisense or siRNA specific to the microRNA, the expression or function of the microRNA is suppressed, and the action of the microRNA or microRNA precursor on mast cells, mesenchymal stem cells or cancer cells Can be controlled.
- a microRNA represented by a sequence number of 1, 2, 3, 8, 14, 20, 22, 25, 32, or 36, or an IJ number 1337, 1338, 1339, 1352, 1363, 1371, 1373, 1377, 1386 and anti-sense or siRNA specific to microRNA precursors expressed by the differential force of f 1390 suppresses degranulation of mast cells It can be used as an agent.
- a microRNA represented by SEQ ID NO: 1, 8, 21 or 36, or a specific RNA / antisense of a microRNA precursor represented by any one of SEQ ID NO: 1337, 1352, 1372 or 1390 or siRNA can be used as a growth inhibitor or growth promoter for mesenchymal stem cells.
- Antisense or siRNA specific to micro RNRN precursor expressed by the above-mentioned differential force can be used as a cell growth promoter.
- antisense or siRNA specific to the microRNAs or precursors thereof By administering to patients, control the function of mast cells, mesenchymal stem cells or cancer cells, and treat diseases that develop due to the above abnormal expression Can power s . That is, antisense or siRNA specific to the microRNA or its precursor is useful as a therapeutic agent for diseases caused by abnormalities in mast cells and mesenchymal stem cells or diseases caused by abnormal cell proliferation.
- antisense or siRNA specific to the microRNA or its precursor is used as the therapeutic agent, antisense or siRNA is used alone, or there is a retrovirus vector, adenovirus vector, adeno-associated. After being inserted into a suitable vector such as a viral vector, it can be administered as a pharmaceutical preparation according to the conventional method described in 11. below.
- microRNA and microRNA precursor of the present invention As a substance that promotes the expression or function of nucleic acids such as the microRNA and microRNA precursor of the present invention, the microRNA and microRNA precursor, and the microRNA and microRNA precursor having the same target base sequence as those, As well as expression vectors encoding them, and factors such as Dicer involved in processing of microRNA precursors.
- Expression vectors encoding microRNA, microRNA precursors and the like can be prepared by the method described in the above 6.
- microRNA or microRNA precursor expressed in mast cells, mesenchymal stem cells or cancer cells a microRNA or microRNA precursor having the same target base sequence as these, and an expression vector encoding them
- the expression or function of microRNA or microRNA precursor expressed in mast cells, mesenchymal stem cells or cancer cells can be promoted. That is, by administering these, the expression or function of the microRNA can be promoted, and the action of the microRNA and the microRNA precursor in mast cells, mesenchymal stem cells or cancer cells can be controlled.
- a micro RN ⁇ represented by any one of SEQ ID NO: 1, 8, 21 or 36 or a microphone represented by any one of 1337, 1352, 1372 or 1390 Mouth RNA precursors, microRNA and microRNA precursors having the same target base sequence as these, and expression vectors encoding them can be used as growth promoters or growth inhibitors of mesenchymal stem cells.
- MicroRNA precursors expressed by shear force, microRNA and microRNA precursors with the same target base sequence as these, and expression vectors encoding them can be used as cell growth inhibitors. it can.
- microRNAs or microRNA precursors expressed in mast cells, mesenchymal stem cells or cancer cells the microRNAs and their precursors, and expression vectors that code them, these And the target nucleotide sequence are administered to patients with microRNA and microRNA precursors, and expression vectors encoding them, to control the function of mast cells, mesenchymal stem cells or cancer cells, and It is possible to treat diseases that develop due to abnormalities.
- the microRNA or a precursor thereof, an expression vector encoding them, a microRNA or a microphone RNA precursor having the same target base sequence as these, and an expression vector encoding them are mast cells, mesenchymal systems It is useful as a therapeutic agent for diseases caused by abnormal stem cells or diseases caused by abnormal cell proliferation.
- microRNA or a precursor thereof and an expression vector encoding them are used as the therapeutic agent, the microRNA or a precursor thereof and an expression vector encoding them are used alone, Alternatively, an appropriate vector such as a retrovirus vector, an adenovirus vector, or an adeno-associated virus vector can be used as a pharmaceutical preparation according to a conventional method described in the following 11.
- Method of suppressing or promoting the expression of a target gene of a nucleic acid such as microRNA of the present invention As a method of suppressing the expression of a target gene of a nucleic acid such as microRNA of the present invention, the expression of a target gene is suppressed. Any method can be used. For example, by expressing or administering a nucleic acid such as the microRNA or microRNA precursor of the present invention and increasing the amount of microRNA in the cell, the expression of mRNA having the target sequence is suppressed. And a method for suppressing the expression of the target gene.
- the nucleic acid such as the microRNA or microRNA precursor of the present invention can be expressed by the method described in 6. above.
- any method for promoting the expression of a target gene of a nucleic acid such as the microRNA of the present invention any method may be used as long as it promotes the expression of a target gene.
- a method for promoting gene expression can be mentioned. Endosense and siRNA can be prepared by the method described in 7. above.
- Examples of the target gene of the microRNA having the nucleotide sequence ability represented by any one of SEQ ID NOs: 1 to 1336 include the gene groups shown in Table 2 above.
- a method for separating cells expressing nucleic acid such as microRNA or microRNA precursor of the present invention from various cells taken out a method complementary to the nucleotide sequence of the nucleic acid such as microRNA or microRNA precursor is used.
- Probes that are fluorescently labeled with nucleic acids having a correct base sequence are introduced into cells and hybridized with nucleic acids such as microRNA and microRNA precursors, and only cells that have hybridized with labeled probes are sorted. This can be done by separating with a functional flow cytometer.
- any fluorescently labeled probe that emits specific fluorescence when hybridized can be used.
- a molecular beacon Biochimica et Biophysica Acta, 1479, 178 (1998)] And FRET [Proc. Natl. Acad. Sci. USA, 103, 263 (2006)].
- Molecular beacons are nucleic acids in which a fluorescent functional group is introduced into one end via a covalent bond and a dabsyl group or the like that causes fluorescence quenching is introduced into the other end.
- a base is formed so as to have a hairpin structure.
- the array is designed. Since the fluorescent functional group and the fluorescence quencher introduced at both ends are adjacent to each other, no fluorescence is observed with the probe alone.
- Strength When hybridized with a nucleic acid such as the microRNA or microRNA precursor of the present invention, the fluorescent functional group and the fluorescence quencher are separated, and strong fluorescence can be observed.
- FRET is a molecular excitation energy transfer phenomenon between two or more fluorescent functional groups.
- two types are prepared: a nucleic acid probe with an energy donor introduced at the end and a nucleic acid probe with an energy acceptor introduced at the end.
- the base sequences of the two probes are designed so that the two fluorescent functional groups introduced after hybridization with nucleic acids such as microRNA and microRNA precursors are in close proximity.
- the power that only luminescence is observed
- a nucleic acid such as a microRNA or microRNA precursor of the present invention and a probe cause hybridization the energy of the donor is transferred to the acceptor because two: / lobes are close to each other. It moves and acceptor-based luminescence can be observed mainly.
- Examples of cell separation methods using a flow cytometer having a sorting function include a water charge method and a cell capture method (free flow cytometer, pl4-23, Shujunsha, 1999). Both methods measure fluorescence of cells, convert fluorescence intensity into an electrical signal, quantify fluorescence intensity, and can separate cells according to the amount. Specifically, cells can be separated by measuring fluorescence using a BD FACS Aria cell sorter (Becton's Dickinson) or EPICS ALTRA HyPerSort (Beckman's Coulter).
- a nucleic acid such as microRNA or microRNA precursor of the present invention can be used to screen for a substance that promotes or suppresses the expression or function of the microRNA or its precursor. For example, from the base sequences of the microRNA and microRNA precursor of the present invention, a base sequence to be screened is selected, and a cell that expresses a nucleic acid having the base sequence is used to select the selected microRNA or Substances that promote or suppress the expression or function of the precursor can be screened.
- Cells used for screening that express nucleic acids having the base sequences of microRNA and microRNA precursor include mast cells, mesenchymal stem cells or cancer cells, as described in 6 above.
- a vector expressing a nucleic acid having a base sequence can be used as an animal cell or A transformed cell obtained by introduction into a host cell such as yeast or a cell into which a nucleic acid having the base sequence has been directly introduced without using a vector can also be used.
- Specific screening methods include: (a) a method that uses changes in the expression level of the target microRNA or its precursor as an index, and microRNA suppresses translation of mRNA that has the target sequence. Therefore, (b) a method using as an index a change in the expression level of mRNA having a target sequence of microRNA or a precursor thereof as a screening target can be mentioned.
- a test substance is brought into contact with a cell that expresses a nucleic acid having the base sequence, and a substance that promotes or suppresses the expression of microRNA or a precursor thereof is used by using a change in the expression level of the selected nucleic acid as an index.
- the expression level of the nucleic acid can be detected by the method described in 4. above.
- a test substance is brought into contact with a cell that expresses a nucleic acid having the base sequence, and selected.
- the expression or function of a microRNA or a precursor thereof is promoted or changed by using a change in the expression level of an mRNA having a nucleic acid target sequence as an index Get the substance to be suppressed.
- a DNA in which the target sequence for the single-stranded RNA having the base sequence of the present invention is inserted into the 3 ′ UTR for an appropriate reporter gene expression vector is prepared and introduced into a host cell suitable for the expression vector.
- Contact the cell with the test substance and obtain a substance that promotes or suppresses the expression or function of the microRNA or its precursor using the change in the expression level of the reporter gene as an indicator.
- Selection of the target sequence can be performed by the method described above, and as a target gene of the microRNA consisting of the base arrangement IJ represented by SEQ ID NOs: 1 to 1: 36,
- the gene groups shown in Table 2 above can be exemplified.
- Nucleic acids such as the microRNAs and microRNA precursors of the present invention express the target gene or the nucleic acid of the present invention. By controlling, it can be used as a therapeutic agent for diseases caused by abnormalities of mast cells, mesenchymal stem cells, etc., or diseases caused by abnormal cell proliferation.
- the nucleic acid of the present invention can be used to treat diseases caused by abnormalities in mast cells, mesenchymal stem cells, etc., or abnormal cell proliferation, by quantifying or detecting mutations in nucleic acids such as the microRNA or microRNA precursor of the present invention. It can be used as a diagnostic agent for a disease caused by the disease.
- Abnormalities of mast cells include abnormalities such as mast cell differentiation and degranulation, inflammatory mediator production, cytoforce-in production, chemokine production, etc.
- Diseases resulting therefrom include atopic dermatitis, asthma, Examples include chronic obstructive pulmonary disease and allergic disease.
- Examples of abnormal mesenchymal stem cells include abnormal proliferation and differentiation, and examples of diseases resulting therefrom include cancer, osteogenesis imperfecta, cartilage imperfecta and diabetes.
- Diseases caused by abnormal cell proliferation include cancer, abnormal cell proliferation and tissue hyperplasia, arteriosclerosis, rheumatoid arthritis, prostatic hypertrophy, percutaneous transvascular coronary artery Examples include vascular restenosis after plasty, pulmonary fibrosis, glomerulonephritis, autoimmune diseases and the like. '
- nucleic acids having a base sequence complementary to those base sequences can be used as diagnostic or therapeutic agents for diseases caused by abnormalities in mast cells. See also SEQ ID NO: 1, 8, 21, or micro RNA or distribution ⁇ IJ ID force represented by any one of 36 1337, 1352, the 1372 or 1390 Les, 1 f Re Ca ⁇ C micro RNA precursor represented.
- nucleic acids having nucleotide sequences complementary to those nucleotide sequences can be used as diagnostic or therapeutic agents for diseases caused by abnormal proliferation and / or differentiation of mesenchymal stem cells.
- IJ number power 1, 3, 8, 20, 21, 22, 32, or 36 micro RNA expressed by displacement force or IJ number power 1337, 1339, 1352, 1371, 1372 , 1373, 1386, or 1390, and a nucleic acid having a base sequence complementary to the base sequence thereof, can be used as a diagnostic or therapeutic agent for diseases caused by abnormal cell growth. You can use it with -
- the diagnostic agent containing the nucleic acid of the present invention is a micro RN of the present invention depending on the target diagnostic method.
- Reagents necessary for quantification of nucleic acids such as A and microRNA precursors or detection of mutations, such as buffers, salts, reaction enzymes, and labels that bind to nucleic acids such as the microRNA and microRNA precursors of the present invention , which contains the purified protein and the color former for detection.
- the medicament containing the nucleic acid of the present invention or a nucleic acid having a base sequence complementary to the base sequence as an active ingredient can be administered alone, but there is usually one pharmacologically acceptable label, Is preferably mixed with a further carrier and administered as a pharmaceutical preparation prepared by the method of the commission well known in the technical field of pharmaceutics.
- the route of administration is preferably oral, for which it is desirable to use the most effective treatment, or parenteral, such as buccal, respiratory, rectal, subcutaneous, intramuscular, and intravenous.
- parenteral such as buccal, respiratory, rectal, subcutaneous, intramuscular, and intravenous.
- intravenous administration can be given.
- Examples of the dosage form include sprays, capsules, tablets, granules, syrups, emulsions, suppositories, injections, ointments, tapes and the like.
- Suitable formulations for oral administration include emulsions, syrups, capsules, tablets, powders, granules and the like.
- Liquid smoked products such as emulsions and syrups include sugars such as water, sucrose, sorbitol and fructose, glycols such as polyethylene glycol and propylene glycol, oils such as sesame oil, olive oil and soybean oil, P -Can be produced using preservatives such as hydroxybenzoates, flavors such as stove leaf flavors and peppermint as additives.
- Capsules, tablets, powders, granules, etc. are excipients such as lactose, glucose, sucrose and mannitol, disintegrants such as starch and sodium alginate, lubricants such as magnesium stearate and talc, polyvinyl It can be produced using a binder such as alcohol, hydroxypropylcellulose, gelatin, a surfactant such as fatty acid ester, a plasticizer such as glycerin, and the like as additives.
- a binder such as alcohol, hydroxypropylcellulose, gelatin, a surfactant such as fatty acid ester, a plasticizer such as glycerin, and the like as additives.
- Suitable preparations for parenteral administration include injections, suppositories, sprays and the like.
- An injection is prepared using a salt solution, a glucose solution or a carrier capable of mixing the two.
- Suppositories are prepared using a carrier such as cacao butter, hydrogenated fat or carboxylic acid.
- the propellant does not irritate the recipient's oral cavity and airway mucosa and is an active ingredient Is prepared using a carrier or the like that can be dispersed as fine particles to facilitate absorption.
- carrier examples include lactose and glycerin.
- preparations such as aerosols and dry powders are possible. Also
- ingredients exemplified as additives for oral preparations can also be added to these parenteral preparations.
- the dose or frequency of administration varies depending on the intended therapeutic effect, administration method, treatment period, age, body weight, etc.
- the usual adult dose is 10 ⁇ g / kg to 20 mg / kg per day.
- the therapeutic agent containing the nucleic acid of the present invention or a nucleic acid having a base sequence complementary to the base sequence as an active ingredient is used as a vector and nucleic acid therapeutic agent for expressing the nucleic acid.
- a base used for a nucleic acid therapeutic agent any base that is usually used for injections can be prepared.
- distilled water sodium chloride or a salt solution such as a mixture of sodium chloride and an inorganic salt
- a solution such as mannitol, ratatose, dextran, glucose, an amino acid solution such as glycine or arginine, an organic acid solution or A mixed solution of a salt solution and a glucose solution, etc.
- these bases include osmotic pressure adjusting agents, pH adjusting agents, vegetable oils such as sesame oil and dice oil, lecithin or surfactants.
- osmotic pressure adjusting agents osmotic pressure adjusting agents
- pH adjusting agents vegetable oils such as sesame oil and dice oil, lecithin or surfactants.
- An injection may be prepared as a dispersion. These injections can be prepared as preparations for dissolution at the time of use by operations such as powdering and freeze-drying.
- the therapeutic agent of the present invention can be used for treatment as it is in the case of a liquid just before the treatment, or in the case of a solid, dissolved in the above sterilized base if necessary.
- Examples of the vector encoding the nucleic acid of the present invention include the recombinant virus vector prepared in 6. above, and more specifically, a retrovirus vector and a lentivirus vector. .
- a vector encoding the nucleic acid of the present invention is combined with a polylysine-conjugated antibody specific for an adenovirus hexon protein to produce a complex, and the resulting complex is bound to an adenovirus vector.
- a viral vector can be prepared. The virus vector reaches the target cell stably and ends Nucleic acids can be efficiently expressed by being taken up into cells by the somesomes and degraded in the cells.
- the nucleic acid of the present invention and the vector encoding the same can also be transferred by a non-viral nucleic acid transfer method.
- a non-viral nucleic acid transfer method For example, calcium phosphate coprecipitation method [Virology, 52, 456-467 ⁇ (1973); Science, 209, 1414-1422 (1980)], microinjection method [Proc. Natl. Acad. Sci. US A, 77, 5399- 5403 (1980); Proc. Natl. Acad. Sci. USA, 77, 7380-7384 (1980); Cell, 27,
- Ribosome-mediated membrane fusion—mediated transfer involves direct administration of a ribosome preparation to a target tissue to incorporate the nucleic acid of the present invention or a vector encoding the same into a local site of the tissue. And can be expressed [Hum. Gene Ther., 3, 399 (1992)].
- Receptor-mediated DNA transfer can be performed, for example, by binding DNA (usually in the form of a covalently closed supercoiled plasmid) to a protein ligand via polylysine. Can do.
- the ligand is on the cell surface of the target cell or tissue Select based on the presence of the corresponding ligand receptor.
- the ligand-DNA conjugate can be injected directly into the blood vessel, if desired, and can be directed to the target tissue where receptor binding and internalization of the DNA-protein complex occurs. In order to prevent intracellular destruction of DNA, it is possible to simultaneously sense adenovirus and disrupt endosome function.
- nucleic acids such as the microRNA and microRNA precursor of the present invention, as well as antisense and siRNA against the target gene of the microRNA are introduced into a fertile cell, cultured with IgE added, and then added with anti-IgE antibody Activated and released human mast cells (i) histamine and ⁇ - ⁇ -xazominidase as indicators of degranulation, (ii) inflammatory mediators such as LTC4, LTD4, LTE4, PGD2, (iii) TNF- It can be confirmed by measuring site power ins such as ⁇ and GM-CSF, and (iv) chemokines such as IL-8, 1-309, MIP-1 ⁇ , etc., and comparing them with the case where nothing was introduced.
- chemokines such as IL-8, 1-309, MIP-1 ⁇ , etc.
- mast cells activation of mast cells is degranulation, not only production of site force in, such as TNF-a and GM-CSF, production of chemo force in, such as IL-8, 1-309, MIP-1 ⁇ , It can also be examined by measuring the production of inflammatory mediators such as LTC4, LTD4, LTE4, and PGD2 [Blood, 100, 3861 (2002) 1
- nucleic acids such as the microRNA and microRNA precursor of the present invention, and further antisense and siRNA to the target gene of the microRNA have an apoptosis-inducing action. It can be detected by introducing it into mast cells and measuring the fragmentation of chromatin DNA or the TUNEL method.
- the mesenchymal stem cell is not particularly limited as long as it is a method that can be obtained safely and efficiently.
- Examples of a method for obtaining human bone marrow force include the method described in SE Haynesworth et al. Bone, 13, 81 (1992). Can be given.
- Bone marrow cell solution is obtained by suspending in a cell culture medium such as A friendship method for isolating mesenchymal stem cells from bone marrow cell fluid is a method that can remove other cells mixed in the bone marrow cell fluid such as blood cells, hematopoietic stem cells, hemangioblasts, fibroblasts, etc. If it is, it will not specifically limit, For example, the method as described in M. F.
- the bone marrow cell solution is overlaid on Percoll with a density of 1.073 g / ml, and then centrifuged at 1,100 X g for 30 minutes to isolate the cells in the interface as mesenchymal stem cells. Also, add 10 times concentrated PBS to the bone marrow cell solution and mix the Percoll diluted to 9/10 with the same volume, and then centrifuge at 20,000 X g for 30 minutes to obtain cells with a density of 1.075 to 1.060. Can also be isolated as mesenchymal stem cells. .
- mesenchymal stem cells derived from human bone marrow can be purchased from Cambrex and Takara Bio. '
- Examples of the method for obtaining mesenchymal stem cells from human umbilical cord include the method described in Stem Cells, 21, 105-11 (2003). Insert force neuules at both ends of the umbilical vein and wash with an appropriate buffer, eg EBSS (Earle's balanced salt solution). Antibiotics are added to a 199 medium containing a proteolytic enzyme such as 0.1% collagenase, injected into the blood vessel, and incubated at 4 to 40 ° C, preferably 37 ° C for 1 to 60 minutes.
- a proteolytic enzyme such as 0.1% collagenase
- DMEM medium DMEM-LG, Gibco
- DMEM-LG low concentrations of glucose
- 20 mM HEPES 100 units / ml penicillin
- 100 g / ml streptomycin 100 units / ml
- 2 mM L-glutamine 1 mM sodium pyruvate
- 10 Suspend in medium supplemented with% FBS. Inoculate a culture flask with a cell density of 10 2 to 10 6 cells and culture under conditions of 37 ° C and 5% CO. Change medium every 1-7 days In other words: mesenchymal stem cells can be obtained by continuing the culture for 3 weeks.
- Human eclampsia endometrial tissue removed by surgery is minced and cultured in a culture medium, preferably a-MEM, DMEM, IMDM, etc. 1-20% of animal-derived serum, preferably 5-10% Incubate in medium supplemented with FBS. It is also possible to add antibiotics such as penicillin or streptomycin to the culture medium. Furthermore, in order to improve the separation of cells, collagenase such as type 3 collagenase and DNA-degrading enzyme such as deoxyribonuclease I are added to the medium and kept at 20 to 40 ° C, preferably 37 minutes for 10 minutes. Shake gently for ⁇ 5 hours, preferably 1 hour. Individual endometrial glands are isolated while observing under a microscope, and mesenchymal stem cells are obtained by culturing them in an appropriate culture vessel such as 24-well culture dish at 37 ° C and 5% CO. Can
- Mesenchymal stem cells can be obtained by removing tissue residues using a strainer, mesh, filter, etc. In addition, the surface of the extracted third molar is washed with PBS, etc., and the cementum and enamel joints are cut to expose the medulla, carefully separating the crown and root force and pulp tissue. Mesenchymal stem cells can also be obtained by removing tissue residues after proteolytic enzyme treatment in the same manner as described above.
- a method for isolating mesenchymal stem cells other than the above using a reporter vector having a surface antigen expressed in mesenchymal stem cells, a promoter of a gene specific to mesenchymal stem cells, and an enhancer.
- a method for isolating leaf stem cells is exemplified. Specifically, A
- Method for isolating stem cells using C133 antigen (US6468794), Sox gene (US2002 / 0135 539), Nestin gene or Musashi gene (JP 2002-0334580) promoter and Examples include a method of isolating mesenchymal stem cells using a reporter vector having an enhancer.
- a method of concentrating stem cells in side population (SP) using FACS fractionation method using Hoechst33342 as an index of extracellular efflux can also be used to isolate stem cells.
- SH2 positive, SH4 positive, CD29 positive, CD44 positive, CD71 positive, CD90 positive, CD106 positive, CD1 20a positive, CD124 positive, CD14 negative, CD34 negative, and CD45 negative cells are mesenchymal stem cells.
- a method of separation using a cell sorter or magnetic beads [Science, 284, 143-14 7 (1999)] can also be used.
- Examples of the medium used for culturing mesenchymal stem cells include cell culture media described in "Technical basics of tissue culture, 3rd edition” Asakura Shoten (1996), etc.
- cell culture media such as a-MEM, DMEM, IMDM, etc. supplemented with 1-20% of serum such as the above are used.
- the culture conditions may be any conditions as long as the cells can be fed, but the culture temperature is preferably 33 to 37 ° C. An incubator filled with 5 to 10% CO gas is preferred.
- the mesenchymal stem cells are preferably allowed to grow by adhering them to a normal plastic culture dish for tissue culture. When the cells grow on the entire surface of the culture dish, remove the medium and add the trypsin EDTA solution to suspend the cells. Suspended cells can be further subcultured by washing with PBS or cell culture medium, diluting 2 to 20 times with cell culture medium, and seeding in a culture dish. Can do.
- Whether a certain nucleic acid controls the proliferation of mesenchymal stem cells can be determined by, for example, nucleic acid such as microRNA or microRNA precursor of the present invention, and further antisense to the target gene of the microRNA. Or siRNA or the like is introduced into mesenchymal stem cells, and the degree of cell proliferation can be confirmed by comparing with a negative control.
- the method for measuring the degree of cell proliferation can be performed by the method described in 14. below.
- Examples of a method for examining the influence of the mesenchymal stem cell force on the differentiation process into osteoblasts include a method of confirming as follows. Specifically, under conditions that induce differentiation from mesenchymal stem cells to osteoblasts, the nucleic acid, microRNA and microRNA precursor of the present invention, as well as antisense and siRNA against the target gene of the microRNA. etc are introduced into mesenchymal stem cells and cultured. Analyze genes or proteins that increase in expression as osteoblasts differentiate and compare with negative controls.
- any method for inducing differentiation from mesenchymal stem cells to osteoblasts can be used as long as it can induce differentiation from mesenchymal stem cells to osteoblasts. , 284, 143-147 (1999). Specifically, after seeding mesenchymal stem cells in an incubator, continue culturing for 1 to 4 weeks in a cell culture medium containing dexamethasone, ascorbic acid-2 phosphate, and J3-glycose oral phosphate. Thus, mesenchymal stem cells can be differentiated into osteoblasts.
- Quantitative analysis of genes whose expression increases with osteoblast differentiation includes RT-PCR (reverse transcription—polymerase chain reaction), ⁇ ⁇ Sanoplot Kakuto, and dot blot hybridizers. Examples include the Chillon method and DNA microarray analysis. Quantitative analysis of proteins whose expression increases with the occurrence of osteoblastic shrimp includes Western plot analysis using antibodies that specifically react with the protein, immunohistochemical staining, ELISA, etc. It is done.
- Genes or proteins whose expression increases with osteoblast differentiation include type I collagen, osteopower / resin, osteonectin, osteopontin, bone sialoprotein, Runx2 (runt—related gene 2), Anole Caliphosphatase (ALP), etc. ''
- Examples of a method for evaluating the degree of differentiation into osteoblasts include staining cells using the ALP enzyme activity in the osteoblasts, or measuring the ALP enzyme activity.
- a more specific method of the cell staining is a method in which the alcohol portion of the phosphate ester of the substrate hydrolyzed by the ALP enzyme in osteoblasts is coupled with a diazonium salt and precipitated on the enzyme active site with an azo dye.
- the substrate include naphthol AS-MX phosphoric acid, and examples of the azo dye include first violet blue.
- a kit containing these may be used, for example, leukocyte alkaline phosphatase (manufactured by Sigma).
- a kit for measuring ALP enzyme activity for example, alkaline phosphate B-test KOKO (manufactured by Wako Pure Chemical Industries, Ltd.) can be used.
- calcified components produced by osteoblasts it is also possible to identify them as osteoblasts. It can also be confirmed.
- the method for detecting the calcified component include staining methods such as von Kossa staining and Alizarin Red staining.
- Von Kossa staining is a method of detecting calcium phosphate, which is a calcifying component, using silver nitrate. Specifically, the cells fixed with paraffin or the like are reacted with 1 to 5% silver nitrate aqueous solution and exposed to light, and the portion where the black calcium phosphate is present is quantified, for example, the bone area is measured by measuring the colored area. The degree of differentiation into blast cells can be evaluated.
- Alizarin red staining is a method utilizing the fact that alizarin red S shows specific binding to calcium and forms a rake. Specifically, by reacting 0.01 to 5% alizarin red S solution with cells fixed with paraffin or the like, the colored portion of reddish purple to orange red is quantified, for example, by measuring the colored area. The degree of differentiation into osteoblasts can be evaluated.
- the method for measuring cell proliferation is not particularly limited as long as it is a method capable of measuring an index reflecting the number of cells and the cell proliferation rate. Measurements of viable cell count, DNA synthesis rate, total protein mass, etc. can be used.
- Examples of a method for evaluating the number of viable cells include a method of measuring the amount of ATP in the cells.
- the amount of ATP in cells is proportional to the number of cells in culture (I. Immunol. Meth., 160, 81-88 (1993)). More specific methods for measuring the amount of ATP in cells include the MTT method and the XTT method (J. Immunol. Meth., 65, 55-63 (1983)).
- Another example is a method for measuring the amount of ATP by luminescence of a luciferin substrate by an ATP-dependent enzyme luciferase.
- Cell Tite “Glo R Luminescent Cell Viability Assay (manufactured by Promega)” or the like may be used as a kit for measuring the amount of ATP in cells.
- a method for measuring the degree of cell death a method of staining dead cells with a dye such as Propium Iodide, a method of measuring the activity of an enzyme leaked out of the cell due to cell death, and the like can be used.
- a method for measuring the enzymatic activity of adenylate kinase leaked out of the cell can be used.
- ToxiLight (R) Non-Destructiv e Cytotoxicity BioAssay Kit (Lonza) may be used.
- the degree of apoptosis can be measured by limiting to apoptosis (programmed cell death) which is particularly important in relation to cancer among cell death.
- Methods for assessing cell apoptosis include measuring the degree of DNA fragmentation, measuring changes in lipids in cell membranes, and caspers, which are proteases in cells induced by apoptosis.
- a method for measuring the activity of 3/7 A more specific method for measuring caspase 3/7 activity in cells is to measure luciferin substrate released by caspase 3/7 activity by luciferin luminescence by luciferase enzyme reaction.
- Caspase_Glo R 3/7 Assay manufactured by Promega
- LAD2 is a recently established human mast cell line that is known to retain the properties of human mast cells well [Leuk. Res., 27, 671 (2003); Leuk. Res., 27 , 677 (2003)]. Therefore, microRNA was extracted from LAD2.
- LAD2 is obtained from National Institute of Allergy and Infectious Diseases, National Institutes of Health (Bethesda, MD 20892-1881, USA) and is 37 ° in Stem Pro-34 medium (Invitrogen) containing 100 ng / ml SCF. C. was cultured in an incubator with 5% CO concentration.
- the low molecular RNA obtained in Example 1 was selected when the base sequence did not match compared to miRBase (http: ⁇ microrna.sanger.ac.uk/), a known microRNA database. did.
- Peripheral genomic sequences obtained by extending the DNA sequences corresponding to these nucleotide sequences to the 5 'and 3' sides by about 50 nt were also obtained by UCSC Genome Bioinformatics (http: ⁇ genom e.ucsc.edu/) RNA secondary structure predicted to be transcribed from the sequence was predicted using RNAfold.
- 1336 species were found to be novel microRNAs located on one strand of the hairpin structure.
- Table 1 shows the nucleotide sequences and the nucleotide sequences of the microRNA precursors containing these microRNAs.
- the names KHK_miR_1001 to 2344 were assigned to the microRNAs having the respective nucleotide sequences (Table 1). All cases where one microRNA can have a hairpin structure derived from a genomic sequence at a different position are described.
- the hairpin structure of KHKjniR_1194 is shown in FIG.
- microRNA obtained in Example 2 has a function as a microRNA can be examined by examining whether or not the precursor protein is processed by the icer protein.
- the function of the microRNA indicated by KHKjniR_l 194 can be detected as follows. First, the salt represented by SEQ ID NO: 1580 The single-stranded RNA having the base sequence is reacted with the synthetic Dicer Enzyme attached to the synthetic X-treme GENE siRNA Dicer Kit (Roche Applied Science). Next, the reaction product is electrophoresed on a 15% polyacrylamide gel, and a band having a size of 20-25 bases can be detected, so that it can be detected that it has a function as a microRNA.
- the microRNA precursor obtained in Example 2 was introduced into LAD2, a human mast cell line, to induce degranulation, and the influence of the microRNA precursor was examined.
- LAD2 was cultured in Stem Pro-34 medium (Invitrogen) containing 100 ng / mL SCF. LAD2 is seeded in a 6-well plate so that there are about 5xl0 5 per well, and the microRNA precursor is prepared using the lipofusion method, specifically, Gene Silencer (Genlantis), with a final concentration of 3 ⁇ 40 nM. Introduced to be.
- the precursors of microRNA (hereinafter referred to as miRNA) are KH K.miR_1001, 1002, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036 Pre- mi R TM miRNA Precursor Molecules The one synthesized by Ambion was used.
- Nucleic acids consisting of the base sequences represented by SEQ ID NOs: 1, 2, 3, 8, 14, 20, 21, 22, 2, 25, 32, and 36, respectively.
- the miRNA is designed to have the same function as miRNA by being incorporated into a complex similar to RISC that causes activity.
- a nucleic acid consisting of a sequence (SEQ ID NO: 2852) in which 1 base 5 ′ from SEQ ID NO 1 and 4 bases from 3 ′ are deleted is prepared, and KHK_miR— 1001_2 Pre-miR TM miRNA Precursor Molecules were also synthesized by Ambion.
- Pre-miR TM miRNA Precursor Molecules-Negative Control # 2 (hereinafter referred to as miR-negacon # 2) (Ambion) was introduced into AD2 in the same manner. Lipofexion followed the method attached to the product.
- the absorbance at 405 nm of a sample containing 100 L of 0.2 mol / L glycine (pH 10.7) was measured by using a plate reader 1420 ARVOsx (manufactured by Perkin Elmer).
- the total j3-hexosaminidase activity in LAD2 was measured by adding a final concentration of 1% Triton X-100 instead of the rabbit anti-human IgE antibody.
- the percentage of degranulation was calculated as the percentage of 3-hexosaminidase activity (%) in the supernatant to the total 3_ hexosaminidase activity, and the percentage of degranulation in the control group (Gene Silencer only) was 1.0 for each. The relative degranulation activity was calculated. The results are shown in Table 3.
- Example 5 Breeding activity, osteoblast differentiation, viable cell rate of intermittent stem cells with forced expression of microRNA
- the microRNA precursor obtained in Example 2 was introduced into human mesenchymal stem cells (hereinafter also referred to as hMSC), and the effect of the microRNA precursor on proliferation and osteoblast differentiation was examined.
- Leaf stem cells are obtained from Cambrex, IMDM medium (Invitrogen) containing 20% urine fetal serum (FBS) (manufactured by JRH Bioscience), and an incubator with 5% CO concentration at 37 ° C.
- microRNA precursors are KHKjniR— 1001, 1001_2, 1002, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036 Pre-miR TM miRNA Precur sor Molecules synthesized by Ambion Using. Lipofexion followed the method attached to the product.
- the medium was treated with an osteoblast differentiation medium (in IMDM medium containing 20% FBS, 0.1 ⁇ mol / L dexamethasone, 50 ⁇ mol / L scorbic acid). 2 phosphoric acid (manufactured by Sigma), 10 mmol / L ⁇ -glyce mouth phosphite (manufactured by Sigma)), and the osteoblast differentiation induction medium was replaced once every three days to continue the culture. Two weeks after the start of the culture, the cell morphology was observed under a phase contrast microscope (Nikon Corp.) and further stained with alkaline phosphatase to detect osteoblasts.
- an osteoblast differentiation medium in IMDM medium containing 20% FBS, 0.1 ⁇ mol / L dexamethasone, 50 ⁇ mol / L scorbic acid. 2 phosphoric acid (manufactured by Sigma), 10 mmol / L ⁇ -glyce mouth phosphite (manufactured by Sigma)
- the cells were washed once with a phosphate buffer (hereinafter also referred to as PBS (phosphate-buffered saline)) (manufactured by Invitrogen) and fixed with a fixative (10% formalin ZPBS) for 5 minutes.
- PBS phosphate-buffered saline
- a fixative 10% formalin ZPBS
- an alkaline phosphatase reaction was carried out in the dark by reacting with a mixed solution of Naphthol AS-MX phosphoric acid (Sigma) and Fast Violet B solution (Sigma) for 30 minutes. Further, it was washed with distilled water, and the osteoblasts stained in red under a phase contrast microscope were observed, and photographed with a digital nore camera (manufactured by Nikon Corporation).
- hMSCs into which KHK_miR_1008, 1021, 1036 Pre-miRTM miRNA Precursor Molecules were introduced had fewer cells than hMSCs without microRNA precursors. It was found that the number of positive cells stained with Lucariphosphatase was also low. Since microRNA precursors are converted into microRNAs in the cells, 'microRNAs derived from these precursors have the activity of inhibiting proliferation and inhibiting osteoblast differentiation against hMSCs. It became clear to have.
- hMSCs into which KHK_miR_1001, 100 and 2 Pre-miRTM miRNA Precursor Molecules were introduced had a higher number of positive cells stained with alkaline phosphatase than hMSCs without microRNA precursors. It was done. These facts revealed that microRNAs derived from these precursors have an activity to promote differentiation into osteoblasts against hMSC.
- the microRNA precursor obtained in Example 2 was introduced into a colon cancer-derived cell line, and the influence of the microRNA precursor on the viable cell rate and apoptotic activity was examined.
- DLD-1 human colon cancer-derived cell line (hereinafter also referred to as DLD-1) was obtained from American Type Culture Collection (ATCC) (hereinafter referred to as ATCC) (ATCC CCL-221). DLD-1 was cultured in RPMI1640 medium (Invitrogen) containing 10% ushi fetal serum (FBS) (manufactured by JRH Biosciences) in an incubator at 37 ° C and 5% CO concentration.
- ATCC American Type Culture Collection
- FBS 10% ushi fetal serum
- DLD-1 was seeded in a 96-well slate so as to have about 2500 cells per well, and cultured in RPMI medium containing 10% FBS.
- the microRNA precursor was subjected to the lipofection method, specifically, Lipofectamine 2000 (manufactured by Invitrogen), to a final concentration of 5 nM or 25 Introduced to DLD-1 to be nM.
- Pre-miR TM miRNA Pre cursor Molecules of KHK_miR_1001, 100 and 1,2 002, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036 synthesized by Ambion Using. MiR- negacon # 2 (Ambion) was also introduced into DLD-1 and used as a negative control. Lipofection followed the method attached to the product. ,
- the viable cell rate was measured using CellTiter-Glo TM Luminescent Cell Viability Assay (Promega).
- the relative viable cell ratio of each control group (Lipofectamine 2000 only) was calculated assuming that the viable cell ratio of DLD-1 was 1.0.
- the introduction of KHK_miR_1001, 100 and 2,1032, 1036 showed a decrease in the viable cell ratio of 40% or more.
- Viable cell rate in ovarian cancer-derived cell lines forcibly expressing macro RNA The microRNA precursor obtained in Example 2 was introduced into an ovarian cancer-derived cell line, and the influence of the microRNA precursor on the viable cell rate was examined.
- A2780 human ovarian cancer cell line (Nature, 295, 116-119, (1982); Science, 224, 994-99 6, (1984); Semin. Oncol., 11, 285-298 (1984); Was cultured in RPMI1640 medium (Invitrogen) containing 5% FBS (manufactured by JRH Biosciences) in an incubator with a 5% C02 concentration of 37 ° C.
- A2780 was seeded in a 96-well plate so as to have about 2500 cells per well, and cultured in RPMI medium containing 10% FBS.
- the microRNA precursor was introduced into the A2780 to a final concentration of 5 nM or 25 nM using the lipofection method, specifically, Lipofectamine 2000 (Invitrogen).
- MicroRNA precursors are KHK_miR_1001, 100, 2, 100 2, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, and 1036 Pre-miR TM miRNA Precursor Molecules. Using. MiR-negacon # 2 (Ambion) was also introduced into A2780 and used as a negative control.
- the viable cell ratio was measured using CellTiter-Glo TM Luminescent Cell Viability Assay (manufactured by Promega). The relative viable cell ratio of each control cell (Lipofectamine 2000 only) was calculated by taking the viable cell ratio of A2780 as 1.0. The results are shown in Table 7. As shown in Table 7, a 40% or more reduction in the viable cell rate was observed after introduction of KHK_miR_1003, 1008, 1020, 1021, 1022, 1032, 1036.
- a nucleic acid having a novel sequence such as microRNA or a microRNA precursor.
- the nucleic acid of the present invention can be used to detect or detect microRNA expression or mutation.
- Cell isolation, suppression of target sequence gene expression, screening for substances that promote or suppress microRNA function, diseases caused by abnormal mast cells, diseases caused by abnormal proliferation or differentiation of mesenchymal stem cells, cancer In addition, it is possible to diagnose and treat diseases caused by abnormal cell proliferation or tissue hyperplasia.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Pulmonology (AREA)
- Immunology (AREA)
- Heart & Thoracic Surgery (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本発明により新規な配列を有するマイクロRNAやマイクロRNA前駆体などの核酸が提供される。本発明の核酸は、マイクロRNAの発現または変異の検出、細胞の分離、標的配列を有する遺伝子の発現抑制、マイクロRNAの機能の促進または抑制させる物質のスクリ-ニング、肥満細胞の異常に起因する疾患、間葉系幹細胞の増殖または分化の異常に起因する疾患、癌及び細胞の増殖異常や組織の過形成等が原因となっている疾患の診断や治療に有用である。
Description
明 細 書
新規核酸
技術分野
[0001] 本発明は、新規核酸、ならびに、該核酸を発現または抑制させる方法、該核酸を含 有する診断薬または治療薬に関する。
背景技術
[0002] 核酸の 1種であるマイクロ RNA(miRNA)は、蛋白質に翻訳されない約 22ヌクレオチド の小さな非コード一本鎖 RNAであり、ヒトを含む生物に多数存在することが確認され ている (非特許文献 1、 2)。
マイクロ RNAは、単一又はクラスター化されたマイクロ RNA前駆体に転写される遺伝 子から生成される。すなわち、まず、遺伝子力、ら一次転写産物である primary- microR NA (pri- miRNA)が転写され、次いで、 pri-miRNAから成熟型マイクロ RNAへの段階的 プロセシングにおレ、て、 pri- miRNA力 特徴的なヘアピン構造を有する約 70塩基の pr ecursor-microRNA (pre- miRNA)が生成される。さらに、 Dicer介在によるプロセシング により pre-miRNAから成熟型マイクロ RNAが生成される(非特許文献 3)。 '
[0003] 成熟型マイクロ RNAは、標的となる mRNAに相補的に結合して mRNAの翻訳を抑制 する、あるいは mRNAを分解することにより、遺伝子発現の転写後制御に関与してい ると考えられてレ、る。 2006年 5月現在、マイクロ RNAのデータベース miRBase(http:〃 microrna.sanger.ac.uk/)には、ヒトで 455種、全生物種で 3685種のマイクロ RNAが登 録されている。ヒトを含む哺乳類で発現するマイクロ RNAの中で、その生理的機能に 関してわかってレ、るものは、血球系分化に関与する miR-181 (非特許文献 4)やインシ ュリン分泌に関与する miR- 375 (非特許文献 5)など一部のみであり、多くはその生理 的活性が未解明である。ただし、線虫やショウジヨウバエを用いた研究力もマイクロ R NAが生物の発生、分化に様々な重要な役割を果たしてレ、ることが明ら力となってき ており、ヒト疾患との関係においても特に癌との関係を示唆する報告が出てきている( 非特許文献 6)。
[0004] マイクロ RNAを同定する方法には、細胞力 低分子 RNAをクローニングする方法や
、ゲノム配列情報力 バイオインフォマティクスを用レ、る方法などがある。 miRBaseにマ イク口 RNAとして登録されるためには、発現に関する情報と生合成及び構造に関する 情報の両方が必要であり、ゲノム配列情報からの構造の予測だけではマイクロ RNAと して認められていない(非特許文献 7)。
[0005] 肥満細胞は各種刺激により活性化され、脱顆粒を起こし、数多くの炎症性メデイエ 一ターを遊離、産生することが知られている(非特許文献 8〜: 10)。例えば肥満細胞 に抗原が認識されると、脱顆粒によりヒスタミンやトリプターゼが速やかに放出されると 共に、プロスタグランジン D2 (PGD2)、ロイコトリェン (LT)、血小板活性化因子(PAF) などのケミカルメディエータ一、およびマクロファージ炎症性蛋白質 (MIP) - 1 α等の 各種のケモカインや顆粒球マクロファ一ジコロニー刺激因子(GM- CSF)等の各種サ イト力インが新たに合成され、放出されることが知られてレ、る。また、これまで好酸球が 作ると考えられていた細胞障害性蛋白質である主要塩基性蛋白質 (major basic prot ein)に関しても、ヒトの場合は肥満細胞が多量につくることが最近明らかになつている (非特許文献 11)。
[0006] このように、肥満細胞は種々のアレルギー疾患の病態形成において主要な役割を 演じていると考えられることから、肥満細胞の機能を制御することにより、アレルギー 疾患の治療が可能であると考えられる。
しかしながら、げっ歯類肥満細胞とヒト肥満細胞では、薬剤への反応性が異なること が知られている(非特許文献 9)。具体的には、炎症性メディエーター遊離抑制薬とし " て使用されてレ、るクロモグリク酸ナトリウムは、ラット腹腔肥満細胞においては IgE依存 性の炎症性メディエーター遊離を顕著に抑制するが、ヒト肥満細胞に対する作用は 強いものではない(非特許文献 12)。塩酸ァゼラスチンは、高濃度においてはヒト培 養肥満細胞からのヒスタミン、 PGD2、 LTの遊離、 GM- CSFおよび MIP- 1 aの産生を 抑制する力 .いずれの活性も強レ、ものではない。また、抗サイト力イン薬として使用さ . れているトシノレ酸スプラタストは、ラット肥満細胞に対しては炎症性メディエーター遊 離抑制作用を示すが、ヒト肥満細胞に対する作用はない(非特許文献 12)。
[0007] また、'ヒト肥満細胞とマウス肥満細胞で発現する遺伝子について比較された結果、 各種刺激により発現する遺伝子が必ずしも一致しなレ、ことが知られている(非特許文
献 13)。
マイクロ RNAについては、マウス骨髄由来肥満細胞で発現するマイクロ RNAは報告 されてレ、るが(非特許文献 14)、マイクロ RNAと肥満細^の機能との関係は知られて いない。ヒト肥満細胞で発現するマイクロ RNAについては報告されておらず、上記の ' ようなヒトとマウス間の種差 考慮すると、マウス肥満細胞のマイクロ RNAの発現情報 をもとに、ヒト月巴満細胞のマイクロ RNAの発現情報を予測することは困難である。
[0008] 間葉系幹細胞は、哺乳類の骨髄、脂肪組織、臍帯血等に存在し、脂肪細胞、軟骨 細胞、骨細胞等に分化する多能性の幹細^として知られている。間葉系幹細胞は、 その分化多能性の故に、—骨、軟骨、腱、筋肉、脂肪、歯周組織など、多くの組織の再 生医療のための移植材料として注目されてレ、る(非特許文献 15)。
間葉系幹細胞は、薬剤やサイト力イン等の添加により in vitroで特定の細胞へ分化 させることができる。例えば、脂肪細胞へは卜メチル -3-イソブチルキサンチン、デキ サメタゾン、インスリンおよびインドメタシンを作用させることにより、骨芽細胞へはデキ サメタゾン、 β—グリセロールフォスフェイト、およびァスコルビン酸を作用させることに より誘導できる (非特許文献 16)。しかし、これらの分化の過程における分子的なメカ ニズムに関しての詳細は不明である。遺伝子ノックアウトマウスや分化段階での遺伝 子発現解析の結果から、脂肪細胞へは PPAR yおよび C/EBPファミリー力 骨芽細胞 分化時には Cbfal/Runx2および Osterixなどの遺伝子発現が関与してレ、ることが知ら れてレ、る(非特許文献 17)が、これらの遺伝子群のみで間葉系幹細胞からの分化メ 力二ズムを説明することはできず、人為的に分化及び増殖を制御するには至ってい ' なレ、。また、間葉系幹細胞の分化及び増殖に作用するマイクロ RNAは知られていな レ、。
[0009] マイクロ RNAは様々な遺伝子の発現制御に関与することから、マイクロ RNAの異常 はヒトの種々の疾患に関与していることが予想される。特に癌においては研究が進展 しており、多くの癌においてマイクロ RNAの発現が正常組織と異なっていること、マイ クロ RNAの発現プロファイル解析により癌の分類が可能であることなどが報告されて . レ、る(非特許文献 18)。また、これまでに見出されたヒトのマイクロ RNAの約半数力 ヒ ト癌で知られてレ、る染色体異常あるいは染色体の脆弱部位に存在することも知られ
ている(非特許文献 19)。今までに報告されてレ、る癌とマイクロ RNAの関係の例としヤ は、 B細胞慢性リンパ性白血病(B-CLL)で欠失が見られる染色体 13ql4に miR - 15a/ miR- 16クラスターが含まれ、その欠失が B-CLLの原因の一つになってレ、ると予測さ れていること(非特許文献 20)、肺癌ではマイクロ RNAの一つである Let-7の発現が低 下しており、その標的の一つが癌原遺伝子として知られる Rasであること(非特許文 21、 22)などがある。多くのマイクロ RNAは癌細胞で発現が低下してレ、る力 逆に癌 で遺伝子増幅や過剰発現が見られるマイクロ RNAもある。例えば、悪性リンパ腫で遺 伝子増幅が見られる領域には 6種のマイクロ RNA力 なるクラスター(miR - 17-92)が 存在し、この miRNAクラスター遺伝子をヒト B細胞リンパ腫のモデノレマウスに強制発現 させるとリンパ腫の発生が促進されることが報告されてレ、る(非特許文献 23)。また以 前力 蛋白質をコードしない、ホジキンリンパ腫で過剰発現する癌遺伝子候補とされ ていた BICと呼ばれる遺伝子は、 miR - 155をコードしていることも明ら力、となっている( 非特許文献 24)。
このように癌とマイクロ RNAの関係は近年.多数報告されている力 その殆どは癌細 胞でめ発現異常を示すものであり、マイクロ RNAの機能を示した研究は、 Let-7を肺 癌細胞株に強制発現させることで癌細胞株の増殖を阻害したという報告' (非特許文 献 25)など、わずかしかなレ、。体外力もマイクロ RNAあるレ、はその前駆体、あるレ、はそ のアンチセンスオリゴヌクレオチドを投与してマイクロ RNAの発現を増大あるいは減少 させることで、動物モデノレで癌の増殖を抑制させたとレ、う報告は現在のところ存在し ない。
非特許文献 1: Science, 294, 853-858 (2001)
非特許文献 2: Cell, 113, 673-676 (2003)
非特許文献 3: Nature Reviews Genetics, 5, 522-531 (2004)
非特許文献 4 : Science, 303, 83-86 (2004)
非特許文献 5 : Nature, 432, 226-230 (2004)
非特許文献 6: Nature Reviews Cancer, 6, 259-269 (2006)
非特許文献 7 : RNA, 9, 277-279 (2003)
非特許文献 8 :黒沢元博編, 「肥満細胞の臨床」,先端医学社, pl42 (2001);
非特許文献 9 :黒沢元博編,「肥満細胞の臨床」,先端医学社, P559 (2001);
非特許文献 10 : Crit. Rev. Immunol., 22, 115-140 (2002)
非特許文献 11 : Blood, 98, 1127-1134 (2001)
非特許文献 12 : Clin. Exp. Allergy, 28, 1228-1236 (1998)
非特許文献 13 : Blood, 100, 3861-3868 (2002)
非特許文献 14 : Genome Biology, 6, R71 (2005)
非特許文献 15 :「遺伝子医学」、 2000年、 4卷、 p. 58-61
非特許文献 16 : Science, 284, 143-147 (1999)
非特許文献 17 :「実験医学」、 2002年、 20巻、 ρ· 2459- 2464
非特許文献 18 : Nature, 435, 839-843 (2005)
非特許文献 19 : Proc.Natl.Acad.Sci.USA, 101, 2999-3004 (2004)
非特許文献 20 : Pnx;.NatLAcad.Sd.USA, 99, 15524-15529 (2002)
非特許文献 21: Cancer Research, 64, 3753-3756 (2004)
非特許文献 22 : Cell, 120, 635- 647 (2005)
非特許文献 23: Nature, 435, 823-833 (2005)
非特許文献 24 : Prcx;.Natl.Acad.Sci.USA, 102, 3627-3632 (2005)
非特許文献 25 : Cancer Research, 64, 3753-3756 (2004)
発明の開示
発明が解決しょうとする課題
[0011] ヒトの種々の臓器で発現してレ、るマイクロ RNAを同定し、その機能を解析し、疾患と の関係を解明することにより、新しい治療薬及び診断薬が開発されることが期待され る。
肥満細胞で作用してレ、るマイクロ RNAを見出すことは、肥満細胞の分化や脱顆粒、 炎症性メディエーター産生、サイト力イン産生、ケモカイン産生等の機能解明につな .がり、肥満細胞の単離 ·培養 ·分化制御 ·脱顆粒制御 ·炎症性メディエーター産生制 御-サイト力イン産生制御 'ケモカイン産生制御法の開発およびそれらを利用した新し いアレルギー疾患等の治療法につながると期待できる。
[0012] また、間葉系幹細胞で作用してレ、るマイクロ RNAを見出すことは、間葉系幹細胞に
おける分化及び増殖の機能解明につながり、間葉系幹細胞力 特定の細胞への分 化制御法の開発および分化制御を利用した新しレ、治療法につながると期待できる。 さらに、癌細胞の増殖または抑制を引き起こすマイクロ RNAを見出すことは、発癌の - メカニズムの理解に役立つのみならず、ヒトの癌の診断薬や治療薬の開発、さらには それらを利用した癌の新しい診断法や治療法につながることが期待される。さらに癌 以外の疾患に関しても、動脈硬化、慢性関節リウマチ、前立腺肥大症、経皮的経血 管的冠動脈形成術後の血管再狭窄、肺線維症、糸球体腎炎、自己免疫疾患など細 胞の異常増殖、組織の過形成等が原因となってレ、る疾患の診断薬 ·治療薬やそれら を利用した診断法 ·治療法の開発に貢献することが期待される。
[0013] 本発明の目的は、マイクロ RNA群を取得し、肥満細胞の単離 ·培養 ·分化制御-脱 顆粒制御 ·炎症性メディエータ一産生制御 ·サイト力イン産生制御 ·ケモカイン産生制 御、及びアレルギー疾患の診断 '治療、間葉系幹細胞の分化及び増殖の制御、癌細 胞の分化や増殖の制御、癌等の疾患の診断'治療に有用な核酸及び、それらの利 用法を提供することにある。
課題を解決するための手段
[0014] 本発明は以下の(1)〜(64)に関する。. -
( 1 ) 配列番号:!〜 1336のレ、ずれかで表される塩基配列からなる核酸。
(2) 配列番号 1〜1336のいずれかで^される塩基配列と 90%以上の同一性を有 . する塩基配列からなる核酸。
(3) 配列番号 1〜: 1336のいずれかで表される塩基配列力 なる核酸の相補鎖とス トリンジェントな条件でハイブリダィズする核酸。
(4) (1)〜(3)のいずれ力 1項に記載の核酸を含む核酸。
(5) 配列番号 1337〜2851のいずれかで表される塩基配列力もなる核酸。
(6) 配列番号 1337〜2851のいずれかで表される塩基配列と 80%以上の同一性 を有する塩基配列力 なる核酸。
(7) 配列番号 1337〜2851のいずれかで表される塩基配列からなる核酸の相補鎖 とストリンジェントな条件でハイブリダィズする核酸。
(8) (1)〜(7)のレ、ずれか 1項に記載の核酸に対して相補的な塩基配列からなる核
酸。
(9) (1)〜(7)のいずれか 1項に記載の核酸と、該核酸の塩基配列に対して相補的 な塩基配列力 なる核酸とからなる二本鎖核酸。
(10) (1)〜(9)のレ、ずれか 1項に記載の核酸を発現するベクター。
(11) (1)〜(9)のいずれ力 1項に記載の核酸を用レ、ることを特徴とする、(1)〜(9) のいずれ力 4項に記載の核酸の発現または変異を検出する方法。
(12) (1)〜(9)のいずれカ 項に記載の核酸を用レ、ることを特徴とする、(1)〜(9) のレ、ずれか 1項に記載の核酸の発現または機能を促進或レ、は抑制させる物質めスク リーユング方法。 '
(13) (1)〜(9)のいずれ力 4項に記載の核酸を用いることを特徴とする、(1)〜(9) のレ、ずれか;!項に記載の核酸を発現する細^を分離する方法。
(14) (1)〜(9)のいずれ力 1項に記載の核酸を用レ、ることを特徴とする、(1)〜(9) のいずれか 1項に記載の核酸の標的遺伝子の発現を抑制する方法。.
(15) )〜(9)のいずれか 1項に記載の核酸を有効成分として含有する、肥満細 胞の異常に起因する疾患の診断薬または治療薬。
(16) (1)〜(9)のいずれか 1項に記載の核酸の発現または機能を促進或いは抑制 させる物質を有効成分として含有する、肥満細胞の異常に起因する疾患の診断薬ま たは治療薬。
(17) (1)〜(9)のいずれ力 1項に記載の核酸の発現または機能を促進或いは抑制 させることを指標とする、肥満細胞の異常に起因する疾患の診断率または治療薬の スクリーニング方法。
(18) (1)〜(9)のいずれか 1項に記載の核酸の標的遺伝子の発現を抑制する物 質を有効成分として含有する、肥満細胞の異常に起因する疾患の診断薬または治 療藥。
(19) (1)〜(9)のいずれ力 4項に記載の核酸の標的遺伝子の発現を抑制させるこ とを指標とする、肥満細胞の異常に起因する疾患の診断薬または治療薬のスクリー ニング方法。
(20) (1)〜(10)のいずれ力 1項に記載の核酸またはベクターを導入した細胞。
(21) 酉己歹リ番号力 i、 2、 3、 8、 14、 20、 22、 25、 32また ίま 36のレヽずれ力であるく ( 1)〜 (4)のレ、ずれか 1項に記載の核酸を看効成分として含有する、肥満細胞の脱頼 粒促進剤。
(22) 酉己歹 IJ番号力 1337、 1338、 1339、 1352、 1363、 1371、 1373、 1377、 138 6または 1390のいずれかである、(5)〜(7)のいずれか 1項に記載の核酸を有効成 分として含有する、,肥満細胞の脱顆粒促進剤。
(23) (21)または (22)に記載の核酸に対して相補的な塩基配列からなる核酸を有 効成分として含有する、肥満細胞の脱.顆粒抑制剤。
(24) (21)または (22)に記載の核酸と、該核酸の塩基配列に対して相補的な塩基 配列力 なる核酸とからなる二本鎖核酸を有効成分として含有する、肥満細胞の脱 顆粒促進剤または脱顆粒抑制剤。
(25) (21)または(22)に記載の核酸の発現または機能を促進或いは抑制させる物 質を有効成分として含有する、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤。
(26) (21)または(22)に記載の核酸の発現または機能を促進或いは抑制させるこ とを指標とする、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤のスクリーニング方 法。 .
(27) (21)または(22)に記載の核酸の標的遺伝子の発現を抑制または促進する 物質を有効成分として含有する、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤。
(28) (21)または(22)に記載の核酸の標的遺伝子の発現を抑制または促進させ ることを指標とする、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤のスクリーニング 方法。
(29) 配列番号が 1、 8、 21または 36のいずれかである、(1)〜(4)のいずれか 1項 に記載の核酸を有効成分として含有する、間葉系幹細胞の増殖および/または分 化の異常に起因する疾患の診断薬または治療薬。
(30) 配列番号が 1337、 1352、 1372または 1390のいずれかである、(5)〜(7) のいずれか 1項に記載の核酸を有効成分として含有する、間葉系幹細胞の増殖およ び Ζまたは分化の異常に起因する疾患の診断薬または治療薬。
(31) (29)または(30)に記載の核酸に対して相補的な塩基配列力 なる 酸を有
¾成分として含有する、間葉系幹細胞の増殖および または分化の異常に起因する 疾患の診断薬または治療薬。
(32) (29)または (30)に記載の核酸と、該核酸の塩基配列に対して相補的な塩基 配列からなる核酸とからなる二本鎖核酸を有 ¾5成分として含有する、間葉系幹細胞 の増殖および/または分化の異常に起因する疾患の診断薬または治療薬。
(33) (29)または(30)に記載の核酸の発現または機能を促進或レ、は抑制させる物 質を有効成分として含有する、間葉系幹細胞の増殖および/または分化の異常に 起因する疾患の診断薬または治療薬。
(34) (29)または(30)に記載の核酸の発現または機能を促進或レ、は抑制させるこ とを指標とする、間葉系幹細胞の増殖および/または分化の異常に起因する疾患の 診断薬または治療薬のスクリーニング方法。
(35) (29)または(30)に記載の核酸の標的遺伝子の発現を抑制または促進する 物質を有効成分として含有する、間葉系幹細胞の増殖おょぴ または分化の異常 に起因する疾患の診断薬または治療薬。
(36) (29)または (30)に記載の核酸の標的遺伝子の発現を抑制または促進させ ることを指標とする、間葉系幹細胞の増殖および または分化の異常に起因する疾 患の診断薬または治療薬のスクリーニング方法。
(37) 配列番号が 1である、(1)〜(4)のいずれか 1項に記載の核酸を有効成分とし' て含有する、間葉系幹細胞の増殖促進剤。
(38) 配列番号が 1337である、(5)〜(7)のいずれ力 4項に記載の核酸を有効成 分として含有する、間葉系幹細胞の増殖促進剤。
(39) (37)または(38)に記載の核酸に対して相補的な塩基配列からなる核酸を有 効成分として含有する、間葉系幹細胞の増殖抑制剤。 、
(40) 配列番号が 8、 21または 36のいずれかである、(1)〜(4)のぃずれか1項に 記載の核酸を有効成分として含有する、間葉系幹細胞の増殖抑制剤。
(41) 配列番号が 1352、 1372または 1390のいずれかである、(5)〜(7)のいずれ か 1項に記載の核酸を有効成分として含有する、間葉系幹細胞の増殖抑制剤。
(42) (37)または (38)に記載の核酸に対して相補的な塩基配列からなる核酸を有
効成分として含有する、間葉系幹細胞の増殖促進剤。
(43) (37)〜(42)のいずれ力 1項に記載の核酸と、該核酸の塩基配列に対して相 補的な塩基配列力もなる核酸とからなる二本鎖核酸を有効成分として含有する、間 葉系幹細胞の増殖促進剤または増殖抑制剤。
(44) (37)〜 (42)のレ、ずれ力、 1項に記載の核酸の発現または機能を促進或レ、は 抑制させる物質を有効成分として含有する、間葉系幹細胞の増殖促進剤または増殖 抑制剤。
(45) (37)〜 (42)のいずれ力 1項に言己載の核酸の発現または機能を促進或いは 抑制させることを堉標とする、間葉系幹細胞の増殖促進剤または増殖抑制剤のスクリ 一ユング方法。
(46) (37)〜 (42)のいずれ力 4項に記載の核酸の標的遺伝子の発現を抑制また ほ促進する物質を有効成分として含有する、間葉系幹細胞の増殖促進剤または増 殖抑制剤。
(47) (37)〜 (42)のいずれ力 1項に記載の核酸の標的遺伝子の発現を抑制また は促進させることを指標とする、間葉系幹細胞の増殖促進剤または増殖抑制剤のス クリーニング方法。
(48) 配列番号が 1、 3、 8、 20、 21、 22、 32または 36のいずれかである、 (1)〜(4 )のいずれか 1項に記載の核酸を有効成分として含有する、細胞の増殖異常に起因 する疾患の診断薬または治療薬。
(49) 酉己歹 IJ番号力 337、 1339、 1352、 1371、 1372、 1373、 1386または 1390 のレ、ずれかである、 (5)〜 (7)のレ、ずれか 1項に記載の核酸を有効成分として含有す る、細胞の増殖異常に起因する疾患の診断薬または治療薬。
(50) (48)または (49)に記載の核酸に対して相補的な塩基配列からなる核酸を有 効成分として含有する、細胞の増殖異常に起因する疾患の診断薬または治療薬。
(51) (48)または (49)に記載の核酸と、該核酸に対して相補的な塩基配列力 な る核酸とからなる二本鎖核酸を有効成分として含有する、細胞の増殖異常に起因す る疾患の診断薬または治療薬。
(52) (48)または (49)に記載の核酸の発現または機能を促進或レ、は抑制させる物
質を有効成分として含有する、細胞の増殖異常に起因する疾患の診断薬または治 療薬。
(53) (48)または (49)に記載の核酸の発現または機能を促進或 、は抑制させるこ とを指標とする、細胞の増殖異常に起因する疾患の診断薬または治療薬のスクリー ユング方法。
(54) (48)または (49)に記載の.核酸の標的遺伝子の発現を抑制または促進する 物質を有効成分として含有する、細胞の増殖異常に起因する疾患の診断薬または 治療薬。
(55) (48)または (49)に記載の核酸の標的遺伝子の発現を抑制または促進させ ることを指標とする、細胞の増殖異常に起因する疾患の診断薬または治療薬のスクリ 一二ング方法。
(56) 細胞の増殖異常に起因する疾患が癌、動脈硬化、慢性関節リウマチ、前立腺 肥大症、経皮的経血管的冠動脈形成術後の血管再狭窄、肺線維症、糸球体腎炎お よび自己免疫疾患からなる群から選ばれる疾患である(48)〜(55)のレ、ずれか 1項 に記載の診断薬、治療薬またはスクリーニング方法。
(57) 配列番号が 1、 3、 8、 20、 21、 22、 32または 36のいずれかである、 (1)〜(4 )のいずれか 1項に記載の核酸を有効成分として含有する、細胞の増殖抑制剤。
(58) 酉己歹 IJ番号力 1337、 1339、. 1352、 1371、 1372、 1373、 1386または 1390 のレ、ずれかである、 (5)〜(7)のレ、ずれ力、 1項に記載の核酸を有効成分として含有す る、細胞の増殖抑制剤。
(59) (57)または (58)に記載の核酸に対して相補的な塩基配列からなる核酸を有 効成分として含有する、細胞の増殖促進剤。
(60) (57)または(58)に記載の核酸と、該核酸の塩基配列に対して相補的な塩基 配列からなる核酸とからなる二本鎖核酸を有効成分として含有する、細胞の増殖抑 制剤または増殖促進剤。
(61) (57)または (58)に記載の核酸の発現または機能を促進或いは抑制させる物 '質を有効成分として含有する、細胞の増殖抑制剤または増殖促進剤。
(62) (57)または(58)に記載の核酸の発現または機能を促進或レ、は抑制させるこ
とを指標とする、細胞の増殖抑制剤または増殖促進剤のスクリーニング方法。
(63) (57)または(58)に記載の核酸の標的遺伝子の発現を抑制または促進する . 物質を有効成分として含有する、細胞の増殖抑制剤または増殖促進剤。
(64) (57)または(58)に記載の核酸の標的遺伝チの発現を抑制または促進させ ることを指標とす 、細胞の増殖抑制剤または増殖促進剤のスクリーニング方法。 発明の効果
[0015] 本発明により、新規核酸、該核酸を発現するべクタ一、該核酸の発現及び変異を 検出する方法、該核酸を制御する物質のスクリーニング方法、該核酸を発現する細 胞の分離方法、該核酸の標的遺伝子の発現制御方法、該核酸もしくは該核酸を制 御/ Tる物質を有効成分として含有する診断薬または医薬、該核酸の標的遺伝子の 発現制御物質を含有する診断薬または医薬、並びに肥満細胞または間葉系幹細胞 等の異常に起因する疾患や癌等の疾患の診断薬または治療薬、細胞の分化や増殖 の制御剤などを提供することができる。
図面の簡単な説明
[0016] [図 1]KHK— miR_1194の配列番号 1580で表される塩基配列の 2次構造を示す。
発明を実施するための最良の形態
[0017] 本発明における核酸としては、以下の核酸があげられる。該核酸は、マイクロ RNA またはその誘導体、マイクロ RNA前駆体またはその誘導体、および二本鎖核酸 (以 下、本発明の核酸ともいう')であることが好ましい。
( 1 )配列番号 1〜: 1336のいずれかで表される塩基配列からなる核酸。
(2)配列番号 1〜:336のいずれかで表される塩基配列と 90%以上の同一性を有す る塩基配列からなる核酸。
(3)配列番号 1〜: 1336のいずれかで表される塩基配列からなる核酸の相補鎖とスト リンジェントな条件でハイブリダィズする核酸。
(4) (1)〜(3)のいずれか 1項に記載の核酸を含む核酸。
(5)配列番号 1337〜2851のいずれかで表される塩基配列からなる核酸。
(6)配列番号 1337〜2851のいずれかで表される塩基配列と 80%以上の同一性を 有する塩基配列力 なる核酸。
(7)配列番号 1337〜2851のいずれかで表される塩基配列力もなる核酸の相補鎖と ストリンジェントな条件でハイブリダィズする核酸。
(8) (1)〜(7)のレ、ずれか 1項に記載の核酸に対して相補的な塩基配列力 なる核 酸。
(9) (1)〜(7)のいずれか 1項に記載の核酸と、該核酸の塩基配列に対して相補的 な塩基配列力 なる核酸とからなる二本鎖核酸。
[0018] 本発明においてマイクロ RNAとは、細胞に由来する一本鎖 RNAであり、かつ、該 配列を含む周辺ゲノム配列がヘアピン構造を形成し得る配列を有しており、ヘアピン のいずれか片鎖から切り出され得る RNAをいう。マイクロ RNAの長さとしては、 15〜 28塩基が好ましぐ 16〜28塩基力はり好ましぐ 16〜26塩基がさらに好ましく、 16〜 24塩基が特に好ましレ、。マイクロ RNAは、その標的となる mRNAに相補的に結合し て mRNAの分解あるいは翻訳を抑制し、遺伝子発現の転写後制御を行う。本発明の マイクロ RNAとしては、配列番号 1〜: 1336のいずれかで表される塩基配列力もなる 核酸、配列番号 1〜: 1336のいずれかで表される塩基配列と 90%以上、好ましくは 9 5%以上の同一性を有する塩基配列力もなる核酸をあげることができる。また、配列 番号 1〜 1336のレ、ずれかで表される塩基配列からなる!^酸の相補鎖とストリンジェン 卜な条件でハイブリダィズする核酸をあげることができる。また本発明のマイクロ RNA として、これらの核酸を含む核酸をあげることができる。
[0019] 本発明においてマイクロ RNA前駆体とは、マイクロ RNAを含む約 50〜約 200塩 基長、好ましくは約 70〜約 100塩基長の核酸であり、かつ、ヘアピン構造を形成し得 る核酸である。マイクロ RNAは、マイクロ RNA前駆体力 Dicerと呼ばれる蛋白質に よるプロセシングを経て生成される。本発明のマイクロ RNA前駆体としては、配列番 号 1337〜2851のレ、ずれかで表される塩基配列からなる核酸、配列番号 1337〜2 851のいずれかで表される塩基配列と 80%以上、好ましくは 90%以上、より好ましく は 95%以上の同一性を有する塩基配列からなる核酸、配列番号 1337〜2851のい ずれかで表される塩基配列力もなる核酸の相補鎖とストリンジェン卜な条件でハイプリ ダイズする核酸があげられる。なおマイクロ RNA前駆体は、マイクロ RNAの配列を含 んでおり、該マイクロ RNAがマイクロ RNA前駆体力 プロセシングを経て生成されれ
ば、前駆体としての機能を有するため、配列番号 1337〜2851のいずれかで表され る塩基配列と 80%以上の相同性を有してレ、る核酸であれば、マイクロ RNA前駆体と しての機能を有するものと考えられる。
表 1— 1〜1 _40に、マイクロ RNAとして具体的に挙げられる配列番号 1〜1336で 表される塩基配列と、その前駆体として挙げられるマイクロ RNA前駆体の塩基配列 の関係を示す。
ほ 1一 1]
表 1一 1
[表 1一 4]
表
[表 1一 12]
表 1一 12
1— 21]
核酸名 マイク PRIMA マイクロ RNA前駆体
K一HK.miR.1674 配列番号 674 配列番号 2117
KH 2K.miR.1675 配列番号 675 配列番号 2118
KHK.miR.1676 配列番号 676 -配列番号 21Ί9
KHK.miR.1677 . 配列番号 677 配列番号 2120
KHK.miR.1678 配列番号 678 配列番号 2121 配列番号 W 22 HK miR 1679 S列番号 679 ¾列番号2123
KH .mi 1680 S列番号 680 列番号 2124
Κ列番号 2125 列番号 2126
.配列番号 2127
KHK.miR.1681 ffi列番号 681 配列番号 2128
KHK.miR.1682 配列番^ 682 列番号 2129
KHK.miR.1683 £列番号 683 配列番号 2130 HK nriiRJ684 配列番号 684 列番号 2131
KHK.miR_1685 配列番号 685 配列番号 21'32
KHK.miR 1686 配列番号 686 IE列番号 2133
KHK.miR.1687 配列番号 687 配列番号 21-34
KHK.miR.1688 配列番号 688! 配列番号 2135—
KHK.miR.1689 配列番号 689 配列番号 2136 H mi .1690 配列番号 β90 E列番号 2 7 HKjTliR.1691 配列番号 691 配列番号 2138' 配列番号 2 9
KHK.miRJ692 配列番号 692 配列番号 2140
KHK.iniR.1693 列番号 693 配列番号 2141
KHK.miRJ694 配列番号 69—4 配列番号 2"2
KHK.mi J695 配列番号 695 配列番号21'43
KH .mi _1696 配列番号 696 配列番号 2H4
KHK.miR 1697 配列番号 697 配列番号 2145
KHK.miR.1698 列番号 698 配列番号 2146
KHK.mi J699 配列番号 699 配.列番号 2M7
KHK.miR.1700 配列番号 700 配列番号 2148'
KHK.miR.1701 配列番号 701 配列番号 21
KHKmiR 1702 配列番号 702 E列番号 2150
KHK.miR.1703 配列番号 703 配列番号 2151
KHK.miR.1704 配列番号 704 S列番号 2152
KHK.miR.1705 配列番号 705 配列番号 21.53
KHK.miR.1706 Ε列番号 706 - 配列番号 2154
KHK.miR.1707 配列番号 707 配列番号 2155 一 22]
表 1—22
43
表 1 -29
表 1一 30]
表 1—30
[表 1一 31]
、 表 1—31
1] [表 1一 32]
表 1一 32
1— 34]
表 1 -3
また本発明の核酸として、上記にあげられた核酸に対して相補的な塩基配列から なる核酸、上記にあげられた核酸と、該核酸の塩基配列に対して相補的な塩基配列 力 なる核酸とからなる二本鎖核酸をあげることができる。
本発明において、配列番号 1〜: 1336のいずれかで表される塩基配列と 90%以上 の同一性を有する塩基配列からなる核酸とは、 BLAST (J. Mol. Biol, 215, 403 (199 0)〕や FASTA [Methods in Enzymology, 183, 63 (1990)〕等の解析ソフトを用いて計 算したときに、配列番号 1〜: 1336のいずれかで表される塩基配列からなる核酸と少
なくとも 90%以上、好ましくは 91%以上、より好ましくは 92%以上、さらに好ましくは 9 3%以上、特に好ましくは 94%以—上、最も好ましくは 95%以上である核酸であること を意味する。また本発明において、配列番号 1337〜2851のいずれかで表される塩 . 基配列と 80%以上の同一性を有する塩基配列からなる核酸とは、 BLAST [J. Mol. Biol., 215, 403 (1990)〕や FASTA [Methods in Enzymology, 183, 63 (1990)〕等の解 析クフトを用いて計算したときに、配列番号 1337〜2851のいずれかで表される塩基 酉己列からなる核酸と少なくとも 80%以上、好ましくは 85%以上、より好ましくは 90% 以上、さらに好ましくは 92%以上、特に好ましくは 95%以上、最も好ましくは 96%以 上である核酸であることを意味する。
[0061] 本発明におレ、て、ストリンジェントな条件下でハイブリダィズする核酸としては、例え ば配列番号 1〜2851のいずれかで表される塩基配列を有する核酸またはその一部 の断片をプロ一プとして、 20xSSC 7.5 mL、 1M Na HPO (pH7.2) 0.6 mL
2 4 . · 、 10% SDS 21 mL、.50xDenhardt's solution 0.6 mし、 10 mg/mL sonicated salmon sperm DNA 0.3 mLから成る Hybridization bufferに、 γ -32P-ATPで標識したプローブ RNAを加え、 50 °Cでー晚反応させた後、 50 °Cで 10分間、 5xSSC/5%SDS液で洗浄し、更に 50°Cで 10 分間、 lxSSC/l%SDS液で洗浄し、その後メンブレンを取り出し、 X線フィルムに感光さ せることにより同定できる核酸をあげることができる。
[0062] 本発明において、核酸とはヌクレオチドおよび該ヌクレオチドと同等の機能を有する 分子が重合した分子であればいかなるものでもよぐ例えば、リボヌクレオチドの重合 体である RNA、デォキシリボヌクレオチドの重合体である DNA、 RNAおよび DNAが混 合した重合体、および、ヌクレオチド類似体を含むヌクレオチド重合体をあげることが でき、さらに、核酸誘導体を含むヌクレオチド重合体であってもよぐ一本鎖核酸また は二本鎖核酸であってもよレ、。マイクロ RNAまたはその誘導体、マイクロ RNA前駆 体またはその誘導体も本発明の核酸に含まれる。
[0063] 本発明において、ヌグレオチド類似体とは、 RNAまたは DNAと比較して、ヌクレア一 ゼ耐性の向上または、安定化させるため、相補鎖核酸とのァフイ二ティーをあげるた め、あるいは細胞透過性をあげるため、あるいは可視化させるために、リボヌクレオチ ド、デォキシリボヌクレオチド、 RNAまたは DNAに修飾を施した分子であればいかなる
分子でもよぐ天然に存在する分子でも非天然の分子でもよく、例えば、糖部修飾ヌ クレオチド類似体やリン酸ジエステル結合修飾ヌクレオチド類似体等があげられる。
[0064] 糖部修飾ヌクレオチド類似体とは、ヌクレオチドの糖の化学構造の一部あるいは全 てに対し、任意の化学構造物質を付加あるいは置換したものであればレ、かなるもの でもよく、例えば、 2' _0—メチルリボースで置換されたヌクレオチド類似体、 2' -0 —プロピルリボースで置換されたヌクレオチド類似体、 2 '—メトキシエトキシリボースで 置換されたヌクレオチド類似体、 2'—0—メトキシェチルリボースで置換されたヌクレ ォチド類似体、 2'— 0_ [2— (グァニジゥム)ェチル]リボースで置換されたヌクレオチ ド類似体、 2'—◦_フルォロリボースで置換されたヌクレオチド類似体、糖部に架橋 構造を導入することにより 2つの環状構造を有する架橋構造型人工核酸 (Bridged Nu cleic Acid) (BNA)、より具体的には、 2'位の酸素原子と 4,位の炭素原子カ チレン を介して架橋したロックト人工核酸(Locked Nucleic Acid) (LNA)、およびエチレン 架橋構造型人工核酸(Ethylene bridged nucleic acid) (ENA) [Nucleic Acid Researc h, 32, el75 (2004)]があげられ、さらにペプチド核酸(PNA) [Ac Chem. Res., 32, 62 4 (1999)]、ォキシペプチド核酸(OPNA)LJ. Am. Chem. Soc., 123, 4653 (2001)]、お よびペプチドリボ核酸(PRNA) QJ. Am. Chem. Soc, 122, 6900 (2000)]等をあげること ができる。
[0065] リン酸ジエステル結合修飾ヌクレオチド類似体とは、ヌクレオチドのリン酸ジエステ ル結合の化学構造の一部あるレ、は全てに対し、任意の化学物質を付加あるいは置 ^したものであればレ、かなるものでもよぐ例えば、ホスフォロチォエート結合に置換 - されたヌクレオチド類似体、 Ν3'-Ρ5'ホスフォアミデート結合に置換されたヌクレオチド 類似体等をあげることができる [細胞工学, 16, 1463-1473 (1997)、 RNAi法 アンチセ ンス法,講談社 (2005)]。
[0066] 本発明において核酸誘 体とは、核酸に比べ、ヌクレア一ゼ耐性を向上させるため 、安定化させるため、相補鎖核酸とのァフィ二ティーをあげるため、細胞透過性をあ げるため、あるいは可視化させるために、該核酸に別の化学物質を付加した分子で あればレ、かなる分子でもよ 例えば、 5'—ポリアミン付加誘導体、コレステロール付 加誘導体、ステロイド付加誘導体、胆汁酸付加誘導体、ビタミン付加誘導体、 Cy5付
加誘導体、 Cy3付加誘導体、 6— FAM付加誘導体、およびピオチン付加誘導体等を あげることができる。 . '
[0067] 別の核酸の誘導体として、例えば、糖の修飾体としては、 2'- 0_プロピルリボースで 置換されたオリゴヌクレオチド誘導体、 2'—メトキシェトキシリボースで置換されたオリ ゴヌクレオチド誘導体、 2' - 0-メチルリボースで置換されたオリゴヌクレオチド誘導体、 2 ' -0 -メトキシェチルリボースで置換されたオリゴヌクレオチド誘導体、 2 ' -0- [2- (グ ァニジゥム)ェチル]リボースで置換されたオリゴヌクレオチド誘導体、 2' - 0-フルォロ リボースで置換されたオリゴヌクレオチド誘導体等をあげることができ、リン酸基の修 飾体としては、オリゴヌクレオチド中のリン酸ジエステル結合がホスフォロチォエート結 合 変換されたオリゴヌクレオチド誘導体、オリゴヌクレオチド中のリン酸ジエステル ' 結合が N3' - P5'ホスフォアミデート結合に変換されたオリゴヌクレオチド誘導体等をあ げることができる [細胞工学, 16, 1463-1473 (1997)、 RNAi法とアンチセンス法,講談 社 (2005)]。
[0068] 本発明において、マイクロ RNA誘導体とは、当該マイクロ RNAと同等の機能を有 するリボヌクレオチド以外の分子を含む重合体であればレ、かなるものでもよぐ例えば 、デォキシリボヌクレオチドの重合体である DNA、 RNAおよび DNAが混合した重合体 、および、ヌクレオチド類似体を含むヌクレオチド重合体をあげることができ、さらに、 核酸誘導体を含むヌクレオチド重合体であってもよぐ一本鎖核酸または二本鎖核 酸であってもよい。 -
[0069] マイクロ RNA前駆体の誘導体とは、当該マイクロ RNA前駆体と同等の機能を有す るリボヌクレオチド以外の分子を含む重合体であればいかなるものでもよぐ例えば、 デォキシリボヌクレオチドの重合体である DNA、 RNAおよび DNAが混合した重合体、' および、ヌクレオチド類似体を含むヌクレオチド重合体をあげることができ、さらに、核 酸誘導体を含むヌクレオチド重合体であってもよく、一本鎖核酸または二本鎖核酸で あってもよい。
[0070] 本発明の核酸を製造する方法としては、特に限定されず、公知の化学合成法を用 いる方法、あるいは、酵素的転写法等にて製造することができる。公知の化学合成法 を用いる方法として、ホスホロアミダイト法、ホスフォロチォエー卜法、ホスホトリエステ
ル法、 CEM法 [Nucleic Acid Research, 35, 3287 (2007)]等をあげることができ、例え ば、 ABI3900ハイスループット核酸合成機 (アプライドバイオシステムズ社製)により合 成することができる。酵素的転写法としては、目的の塩基配列を有したプラスミドまた. は DNAを铸型として典型的なファージ RNAポリメラーゼ、例えば、 T7、 Τ3、または SP6 RNAポリメラ一ゼを用いた転写法をあげることができる。
[0071] 本発明の核酸を用いて、マイクロ RNAやマイクロ RNA前駆体などの核酸の発現を 検出する方法としては、検体中の核酸を検出できる方法であればレ、かなる方法でも よぐ例えば、(1)ノーザンハイブリダィゼーシヨン、(2)ドットブロットハイブリダィゼー シヨン、 (3) in situハイブリダィゼ一シヨン、 (4)定量的 PCR、(5)デフアレンシャル 'ハ イブリダィゼ一シヨン、(6)マイクロアレイ、(7)リボヌクレアーゼ保護アツセィ等の方法 があげられる。
[0072] 本発明の核酸を用いて、マイクロ RNAやマイクロ RNA前駆体などの核酸の変異を 検出する方法としては、検体中の核酸の塩基配列の変異を検出できる方法であれば 、レ、かなる方法でもよぐ例えば、非変異型塩基配列を有する核酸と変異型塩基配列 を有する核酸とのハイブリダィズにより形成されるへテロ二本鎖を検出する方法や、 あるいは、検体由来の塩基配列を直接配列決定して変異の有無を検出する方法等 をあげることができる。
[0073] 本発明の核酸を用いて、マイクロ RNAやマイクロ RNA前駆体などの核酸を発現す る細胞を分離する方法としては、種々の細胞の混合物より、マイクロ RNAやマイクロ RNA前駆体などの核酸を発現する細胞を分離できる方法であればいかなる方法で もよぐ例えば、本発明の核酸の塩基配列と相補的な配列を有する核酸に蛍光標識 したプローブを細胞に導入し、該プローブとハイブリダィゼ一シヨンさせ、標識プロ一 ブとハイブリダィゼーシヨンした細胞のみを、ソーティング機能を有したフローサイトメ 一ターで分離する方法等をあげることができる。 -
[0074] 本発明の核酸を発現するベクターとは、細胞内もしくは試験管内で転写されること により本発明の核酸が生合成されるように設計されたベクターをレ、い、細胞内もしくは 試験管内で本発明の核酸を転写することができるプロモーターを有していればレ、か なるベクターでもよい。具体的には、 PCDNA6.2- GW/miR(Invitrogen社製)、 pSilencer
4.1 - CMV(Ambion社製)、 pSINsi-hHl DNA (タカラバイオ社製)、 pSINsi_hU6 DNA ( タカラバイオ社製)、 PENTR/U6 (Invitrogen社製)等をあげることができる。
[0075] 本発明のマイクロ RNAなどの核酸の標的塩基配列を有する遺伝子(以下、標的遺 伝子という)の発現を抑制する方法としては、本発明のマイクロ RNAなどの核酸を用 いて、標的塩基配列を有する mRNAの発現を抑制する活性を利用して、標的遺伝子 の発現を抑制する方法であれば、いかなる方法でもよい。なお、ここで、発現を抑制 するとは、 mRNAの翻訳を抑制する場合、および mRNAを切断あるいは分解すること によって、結果として mRNA力、ら翻訳される蛋白質の量を減少させる場合も含む。
[0076] 標的塩基配列とは、本発明のマイクロ RNAなどの核酸によって認識される数塩基 力 なる核酸の塩基配列をレ、う。該塩基配列を有する mRNAの翻訳は本発明のマイ クロ RNAなどの核酸により抑制される。マイクロ RNAの 5'末端側 2〜8番目の塩基配 , 列に対して相補的な塩基配列を有する mRNAは、該マイクロ RNAによって翻訳が抑 制される [Current Biology, 15, R458-R460 (2005)]ので、本発明のマイクロ RNAなど の核酸の 5'末端側 2〜8番目と相補的な塩基配列を該マイクロ RNAなどの核酸の標 的塩基配列としてあげることができる。例えば、マイクロ RNAの 5'末端側 2 - 8番目の 塩基配列に対して相補的な標的配列を用意し、ヒト mRNAの 3'UTR塩基配列群に対 して、完全一致配列を含有する mRNAを、文字列探索などの方法で選抜することで 決定することができる。ヒト mRNAの 3'UTR塩基配列群は、「UCSC Human Genome Br owser Gateway (http:// genome.ucsc.edu/cgi-bm/hgijateway)」より取ネ守できるヮノム 配列および遺伝子位置情報を用いて作製することができる。配列番号 ί〜1336で表 されるマイクロ RNAの標的塩基配列を有した遺伝子の具体的な例としては、米国国 立バイオテクノロジ一'【青報センタ一 National Center for Biotechnology Information(N CBI)の EntreGeneデータベース(http:〃 www.ncbi.nlm.nih.gov/Entrez/)で使われて レ、る名前(Official Symbolと Gene ID)で表記された表 2—:!〜 2— 35に記載の遺伝子 をあげることができる。遺伝子名は、 EntreGeneデータベースの 2006年 3月時点での 名前を使用した。
ほ 2— 1]
配列番号 標 Kit伝子
PRKCZ(5590);TNFRSF14(8764):TNFRSF9(360 );RCC2(5592P);NBL1(4681〉:LDLRAD2(4019 );CDC42(998〉;E2
1
F2(l870):RC:Cn(1104):SDC3(9672〉:KHDRBSKl0657):HPCA(i3208〉;RlMS3(9783);TOE1(11403 >:SERBPl(2ei35〉 : SYPL2(284612);SLC6A17( 88662):MCL1(4170);TNRC4("189);C orf60(65l23 IL6R(3570)"ZBTB7B , 0 3);LM NA(4000:MEF2p(4209)PEAl5(86^):DEDD(9191〉:<aSCN6(57 8〉:ADO Al 34):H_24("00 :TMEM63A©725);R HOB(388):KCNK3(3777);ZFP36L2(678);HT A2(27429):ADRA2B(15l);BRI¾N1(23397):BCL2U1(10(n8) BS5Cl2 9880> 5?10(843>" 1_520819("7583)^^(3623) 0八04(9759〉:1<1「1八(547):5^^2(4735):1^£1;4(1∑9807) Kは 1776):OGG1W&68¾HDAC"(79885):ZNF651(9299>:Z F445C353274>.DAG1(1^05):H£MK1(51409):RBM15B(
SB(411):SEMA6A(57556);RAD50a01.">PFD 1(5201¾WDR55(54853):N BP3(23l38);ATXN1(6 0)f 21^30871〉 ;IER3(3870);MC )1(^01250):C6ori 7(57827 BTBl2(221527);CREBL1(138S>;PBX2(508 ;BAK1(578>JHPK3a 17283〉:CDKN1A(10 6):2FANb3(60685);KCNK5(8e 5〉:NFYA(4800):FOXO3A(2i09):SNX8(29 8 (5476 >.CARD4(10392); WHBA(3624);DKFZp76112123(83637〉:ADCY1 (107〉:YWHAG(7532):FLJ39237(375607);LRRC4(6
37970);ΕΧ"Π(21 ): DG^T1(8694);MGC70857Ml4919XGAS1(26l9);SEMA4D(10507):TRAn(7 5):CDK9(1025>:
>,SPOCK2(9806):LOC439985(439985):PTEN(5728 Un(6585):NOLCl(922l);Ci0orf 6(143384>;FAM53B(9€79 >;FU46300(399827):MUCDHL ( 3841);TOLUP(54 72):BRSK2(9024¾lGF2(3481);OSBPL5(U4879):C11orf49(79 096):VEGFB(7«3);CDCA 1131¾)):0??2(5977):5550 1 053 ); LA(5970 PPP1C:A(5499):RPS6KB2(6199): 。(^0 595)^ 0(8772):»0? 1_1(3636);0½2 846〉;501^^(6330)^004(64137)^124(9538)^丁3<¾1_4(6484); CACNA1 C(775〉;TSPAN9(10867);CCND2(8M) G4(5" 47);PTMS(5763 FGD4121512 F 20489(55652);HDA C7A(51564>,RN (27289):MCRS1(10 5);FAfti2(230n);RARG(59l6):GDFlKl022CO:CENTG1(116986 PPTC7( 160760);PPP1CC(5501):SCARB1(99〉:RAN(590 D1P13B(55198);SLC7A1(6541):F 40296122183):POU4F1(5 «7〉:i_AMP1(3916):BCL2UK599);TM9Sn(10548〉:irLJ39779(400223):ERH(2079);VASH1(22846):CHESl(ni2):T RAF3(7,87>,FU42486(38802,):AKT,(207): DN(4692):KLR3(iiie21):BMF(9027)SAHDt(22393):CSK(, 45)G F1 R(3480):PIGQ(9091):KIA/ 924(197335 CCDC78 24093)^1QTNF8(390664);N E3(4832):TBL300607):TSC 2(724 ); TRAF 84231 ):CCNF(8^);TNFRSn 2A(51330);MMPL1 (4328):Ν-ΡΑΧ84$56)^Ρ C5B(51704);PLK1 (5 347):MAPK3(5595):FBXIJ9(54620):POLR2C(5432):TRADD(8717):LOC283849(28^849):E2 4(1874):SLC12A4(6 560 1_07 6(9057 1^03^5512):1£ 2(7014);11^0513(976 )^001^3(5"9)^^31«^1"05)^;^0^(508 55>,ALOX15B(247):PAFAH1B1(5iMa)i5HX33(56919):VAMP2(684);GA 7:8522XCORO6(849 0>.GOSRl(9527>: RASL10B(91608):DUSP3 845>.UBTFa33¾SLC4A1 (6521 >: APT(4137):CDK5RAP3(80279)^ROP(517 7);MSI 2(124540〉:ERN1(2081>尸 RKCA(5578);SPHK1(8877);TMC611322):BIRC5(332);SOCS3(9Ci21):FLJ21865(6 772): CARD14(79092):C EA(n49);CABLES1(91768):MAPI¾E2U0982):BCL2(59e):TXN A(10907XAPC2(l0297):MK NK2(2872):C orf3 UlT7):FZR1(5133):MATK(4M5):DAPK3(l613):2BTB7A(513 1);TNFAIP3U(t26282):M AP2K7(5609):CDKM2D(1032);T PO2(3lHra0);GAD M5GP1(90480):BTBm4B(n2939):DPn(8193):MAP3K10(4 294〉 (208);PRX(5771 e AXUSSS^RHGEFI (9138〉:E RF(2077);1GSF4C 99731 >APOE(3 8〉:SPHK2(568 8); RPS11 (6205);SPIBC0689):L0C2843ei ):SAPS 1 (22870〉;HMG20B(10362);GRLF1 (2909);θέΝΚ2Α1(1457〉: TM9SF4(9777);E2Flil869);GGTL3(2686>;|_PIN3(64900):MYBL2(4605):DIDOl(11083):BIRC7(79444);ARFGAP1( 55738):PLAC 09 85):FU4n33(400870)^21orf123(378832)^CL2L13(23786》:TSSK2(236 );DGCR14(8220): LOCi28977(128977):SEPT&i5413);HK;2(23"9);MAPK1(5594);SMARCBK6598):ADORA2An35):MNn(433D);GA
1993(4O0935);SAPS2(970l);SBn(6305);MAPK8IP2(2352>.MGC373l(79159〉:PCTK1(5127);SMC1Li(8243);SN X 12(29934):BTK(695);AGT 2(186)- DHHC9(5111 >,E MD(2010) AFF2(233 );
E2F2 870):C )C21(64793):SDG3(9672):RBBP4(5928):KIAA0319U79932 ;'orf84(149469);AGBL4(8487i):CE
2
LSR2(1952);RAPlA(5906);SV2A(990tft iorf60(65 3>-SHC1(6464〉:UBQLN4(56893); EF2D(4209);BGAN(6382
7) iKiSF4B(57863): AV1(89796);PPPim2B(4§60);RPK5(25778);C1orf95(375057);YPEL5(516 6):TEX2ei(1134
.AB6B(5l560):SLCO2A1(6578);SLC26AUl08ei)fVC(212l):FLJ46 8lD891^7):S TD7(80854): IAA1909(153 7
8) ;PCDHi(5097):PDGFRB , 59):NDSTK3340 :PLX2(10814):N4BP3(2313W:RNF5(6048);PBX2(5089)SAK1(57 -8):PACSIN1(29993):MOCS1(4337):FOXP ("6"3〉:MGC45 91(221416》:TRAM2( 697);PSCD3(92e5):AQP1(358 );ΡΟΜ12ί 883):CASP¾835):yiP 2;:7434>C9orf25.(203259):TPM2(7169):NTR 2¼915)^9orf47(286223):ST6G ALNAC6(30815);SPOCK2(9^);SH3PXD2A(9644);VA)O(11023);MTG1(92n0):SPR (50352):C11orMK747):P 468):MYL6(4637);GLS2C27l65):CTDSP2(l010^:DDX54(79039):B4GALN"n(2583);SLC8A3(6547)J»CNX(22990):
2〉;cnorf63(55731)ACACA(31);MLLT6(4i02>:LASP1(3927);WIREn47179):PTRFC28 119):MAPT(41373tPNPO 5163>NGFR(4804):NXPH3(1l248):UMD2(80774):CDC42EP C23580 :norf28C283987):SEPT9 080i):PC:YT 5 833 (4097);RNF165C494470):FZR1(513 3);TUBB4(10382);PDE4A(5141 (C4784);RAB8A(4218>ZNF58 5A(199704)APOE(348):DMWD(176 : SHAlK1(509'44〉:MG ^752(65996):L0C389286(389286〉;C20orf2 5 976); SOX12(6666);ProSARP1(9762);RI S4Cl40730);DIDOlCl1083);BTBD4Cl40685);TRP 2(7226):POFUT2(23275): Mに AL-L1(85377;MGAT3(4248);TEF 00 :NFAM1(1503 2):TTLL12(23170);SSX4B(548in3):SYNK6853)^SX 2— 2]
6(280657);RP11-114H20.K401589);SSX2C6757);SMC1 LU8243);
TNFRSF14(876 》:NBL1(4681):CDC42(998);LIN28(79727);KHDRBS1(10657):J JD2A(9682〉:GFn(2iB72):CDC14
3 A(8556);AMraO1(57463);MCL1(417p);RORC(6097)WEF2D(4209);PEAl5(8682);UHMKl027933 ADORAl(134):
1^< 1<51(6 710>:1 538?2(7159)^10 9(200205):1<11^13(23046):1^08(388〉;1«^1<3 3777) 1¾»«^(5581〉:1^(
D1(4084);KCNlP3(30818)eRF»n(23397〉;BBS5n29880):CFLAR(8837):CASPi0(8«〉;CTDSP 58190) NHA(362
3):PAX3(5077):HDAC4(9759); IF1A(547);SRGAP3C99m>.VHLi7428);RBMS3(27303);AXUD 6 651);ZNF65K92
999》;RBM 15B(29890); AGn (9223>.FXS1 (8087);TP73L(3626):PPP1 R2(5^04):G38P2(9908);PRL (5618):FU391
55(133584):iTGA2C3673);RAD17C5884):SEMA6A(57556);RAD50(10l 11 >.PHF15(23338):HNRPAa(10949)^DC23C
8697〉;CAM 2A(815);CD74(972 NDST1(3340〉;DD (780);ZBTB12(22 ' 527);SK!V2L(e499):SYNGAFM (8831 λΒΑ
K1(578>,MAPK13C5603>ZFA D3(60e85):T AM2(9697):FOXO3A(2309);L3MBTL3(84456);STX7(84n¾TNFAIP3(
7128〉:PDE10A(,0846);PDCD2(5134):TRIAD3(54 76):SCRNK9805):IGFBP3(3486): GFR(1^6):YWHAG 7532^
EP(3952);FASTK(l0922);TNFRSF10B(8795);TNFRSFlOA(8797):TRlM35(23037>;CUJ(119l IF13B(23303);DUS
P4(1846);l®E2V2(7336);MTSSl(9788>rCDC37L1 (55664):CDK9Cl 025½9orfl 40(89958);GPR107(57720);ADARB
2(105);SPOCK2(980^:NOLC1(9221):TCF7L2(6934):C10orf46(143384);TIAU(7073);LRRC56〔115399);IGF2(348
1):IPO7(10527>APl5(e539);P PF19(27339):GANAB(23193〉:CDCA5 l3130):DPF2(5977):SSSCAK10534〉:NPA
S4(266743)pPP1CA(5 99);TOF4 2249);^ESN3(143686 YAP1(104,3〉;PPP2R1B ( 19):FU25530C220296)fi24 538>ARF3(377):012orf22(81566>:LOC 01720(40,720):GDn i(10220):SUDS3(e 26〉:HNRPA1(317a):LATrS2(
26524〉;FU40296(122183);P。U4n(5457):Ba^L2(599):JPH4(8 502):ERH(2079):VASHi(2284e):CHES1(1"2);
ANKRD9022416)AKT1(207):KLF13(51621 );TPM1C7168〉;GSK(1 45>,lGnR(3480);CCDC78(124093 ;iQTNF8(
39066 :TSC2(7249);TRAF7(8 231):TNFRSF12A(51330〉:£RN2(10595 ; APK3(5¾95);FBXU9(54S20);CiAPIN
57019):CMTM4(14e223):TrRADD(87n〉:l_OC283849は 83849¾SLC12A (6560):SMPP3(55512):KIAA0513(976 ):C
DT1 (81620>:RPI_13(W 37 し OX, 5Β 47);ΜΜΤ(4335)·«ΡΑ ΑΗ 1 B1 (5048);DLG (17«〉:TNFSF12(¾742):GOSR1 (9
527);NF1(4763》:RAB11 F1P4(8^M0);RASIJ0B(91608):NR1D1(9572):HDAC5(10014):CRHRKU94); APT(4137):
NGFR(4804):SPHia(8877):TMCe(11322);SOGS3(902i);PCYT2は 833):aDEA(1 M9);CABLES1(91768):PHLPP(2
3239);BCL2{596);T)(NL4A(10907¾FZm la^ ZBTBTA^IMUSE AeBdOSOl TNFSF^ST^^CDCSTUl "!)
):CDKN2D(1032)JLF3(36O9):DN 2(1785XRAB3D(9545>;LPPR2(64748);ELAVL3(1995):T PO2(30000);BTBD14
B(1 l2939〉f2RL3(9002)fLU81 )i)Pn(8193): AP3K10(«94〉;ERR;2077>;IGSF C(199731〉:BCL3(e02):APOE(
348):FOSB(2354>,BBC3<27" 3);SLG8A2C65 3);BAX(581〉;CD37(951)SCL2L12(83596)^ 281 A(5518): YADM
(91663¾CACNG7(59284);U2AF2(11338):Z F26 (9422):ZNF17C7565½RLF1(2909);SCRT2(85508);E2F1(1869>
UB£2V1(7335):CABL£S2(8l928);DID01(11083 ADARBKl04):BCL2L13(23786);DGCRi4(8220):SEPT5(5413);
MAPK1(559 ):SMARCB1(6598):MN1(4330〉;GAS2L1(10634 UF(3976〉:MCM5(4174); IAA1904("4794):CARD10
C29775);C22orf5C25829)^BX6C23 66);CBX7C23492);TCF20C6942)PHF21BCl 12885);PPARA(5465);SAPS2(9701
);SBF1(6305);MAPK8IP2(23542);RS1(6247〉:PCTK1(5127):ELK1(2002〉:ZNF81(3473 ):SMC1L1 (8243);RP1-112
K5.2(90121):MLLT7(4303);BRWD3(254065):SEPT6(23157);MTCP1C4515>,AFF2(2334):
4 BOKC666)
5 GAS7C8522)
ΡΠ 5(51050)
6
TAGLN(6876)
J
8 SA D"(148398);CDC2L2(985):TP73(7161);HES2(54626〉:THAP3(90326):TNFRSF9(36O >;LOLRAP1(26119);N UDC(10726〉:RCCU"04);TRihW2(55223):KIAA0319L 79932):MPU4352);CDC20( 91):SH3GLB1(5n00):PROI C84432);KC J9(3765);DEDD(9191 5PR161 (23432):TNNI1 (7135>;TMEMe3A(9725)^1orf95(375057):C 1 orf69(20 0205);MTR(4548);RHOB(388)^GREF1(10669):BRRN1(23397):BCL21J 1(10018):WDR33(55339>>PLEKHB¾550 1); C 6C4175);KiF1A(5 7);RAF1i5894)^XUDl(64651); ASSFlCl 1186); EK4C6787>.TMEM110(375346);CLSTN 64084>:LOG285382(285¾?〉;LETM1(3954);SH3BP2(6452):HD(3064):BTC(e85):U C5C(8633):NEi (4750):TP PP("076):ERBB2IP(559"》;MRPS27(23107);CDC23(86&7):PDGFRB(5159>:HMP19(51617 )HX16(8 49〉;AIF1(1 99);MAPK13(5e03〉:CDI<iN1AO026);LATS1(9n3>:ESRK2099):RPSe A2(6196):LOC90639(90639):MAmい (8379 〉;FOXK1(22 37):Τί¾ΑΟ3(5 76〉:ΗΟΑΟ9(973 〉:ΙΝΗΒΑ(3624);ΤΜΕΟ4(222068)·ΛΟΟΥ1(107):ΪΟΡΒΡ3(;Μ86);Υνΐ/" AG(7532): IAA0773(97,5):LOC1550600550eO):RBM33(,55435):MAFK(7975)^LN8 2055):BW3(55909):TNFRS Fi 0CX87M):CLU(" 91 BAGI (573);SHBC646 l);C9orf47(286223):TRI 14(9830) TRAF1 (71 ): ASB6( 14M59>;FN BP1(23048):ABL1(25〉:TSC1(7248〉:QSCN6L1 (169714);UNC5B(2l9699):C10orf104(119504):FAS(355>;LZTS2<8 445):SUFU(51684);SPRN(503542); (348 :KCNQ1(378 : WT1(7490):SLC15A3(5i296):LOC144097(14 097): CDC^EPZ tMSS^RM 1(25855)^CND1(595);FADD(8772):LRRC51(220074):GAB2(9846):SESN3(143686):CA SP5(838):£XPH5(23086):TAGLNi:6876〉:ETV6(2120〉:F 20489(55652》;HDAC7Ai:5 64>,MCRS i0445〉:FMNL3( 91010〉:FAIM2(23017);CBX (23468);RBMS2(5939〉:BTG1(694》:SOCS2C8835):GAS2L3(28343l):TCn(6927¾C12 0rf43(64897):DIAB (5681 : SCARB1(949);LATS2(26524):WDFY2(115825):LTB4R2(56413>:SPTB(6710〉;RAB1 5(376267):LTBP2(4053);\ SHlC22846);SLC24A4(1230 ):TRAF3(7187);PACiS2(232 ): klAAtn25(983 ):FU43 339(388l 15):CA12(77 :DAPK2(23e04):PDGD7(l0081);CLNe(54932):ARNT2(i)915): 15orf38(343l 10);IDH2(341 8): 3Π Rt3480〉:LOC440313(440313):LRRK1 (79705); RAB 0C(57799);K1AA1924(197335);CCDC78U 24093)^LC N7(1 186);TRAF7(8423l)^:CNF(899)":PK YT1(9088〉BTBD12(84464):DNAJA3(9093):C16orf5(29965);GSPT1(29 35);XYLT1(64131):RPS15A(6210);PLi (5347):SBK1(388228):STX1B2(112755):FTS(64400):GNAO1(2775):UN1 3]
CD40LG(&5&>^FF2(2334):
D— FF (1676);TNFRSnB(7133):NBL1(46ei);NUDC(1072^;SESN2(83667);RpC1(1l0 ):TTMB(39M74);KIAA0319 L 79 2¾NFYC(4802):TES 2(10420):COC7i83n);RAPlAi5 06 ^AS( 893);SNX27(81609);CD84(8832):UHMK 27933>^SCN6C5768):PPF R12B(4660>:CCNL2(81669)£2ド6(1076):RBJ 1277); ^K(3795 OXER1(165140); TGFAC7039); CNIP3(30818};BCL2L11(100, 8)ANAPG1 C64682); IF1 (55183);CASP10(843);OGG1 (4968);FANCD 2(2Π7〉:5ΤΑαΐ(10274)^ΗΙ¾ 86 6):ΤΡ73Ι_(8β26):ΡΟΟΡ3θ0336》;ΟΟ38(952〉:ΕΡίΕΟ(2069〉:ΒΤΟ(β85):5ΕΡΤΊ1(55 752);t A> 909053478):1^<52(10309 21¾2149):「0 1 (224β):ί¾ΝΠ 30(55819): RPK1 737):LY86(9450):E2F3(18 7 103(5603〉:丁^¾«2(9697):05丌667):5 5 (23328)^1^34503(285759) 00112 7(84310):了«1^03(5 47 6):0^8八(3624>尸リ^(58"):。八1^1(83698):0>16(,021);(½5?2(835)^503(23362)^00?30 61);81«3(55909) 0B(8795):BNIP3LC665>.CLU(1191 UNC5D(, 37970XUBE2V2(7336):STK3(6788); IAA1875(3 0390 5 51(2619);5£»^40(10¾)7)^003(89846);丁?¾^114(9830):^1 (6709)^0 1^5 3("093):^^9(6 170>;2^1 YND11(10T71);2WINT(111^);SmT1(234l1);UNC¾(219699):LZTS2i8445);SUFU(51684):Cl0or46(143384):H RAS(3265)fARVA(55742):HlPK3Cl0114);DAK(26007)i)PF2(5977)i)LG2(170):SCN4B(6330):MU_(4297);H2AF (3014);SRPR(6734):RAD52(5893):CCND2(894):TMFR F7(939);CDK nB(1027);IAPP(3375);HDAC7A(51564):F ΑΙΜ2(23017 η2θΓί22(81566〉:ΡΟΕ1Β«,53);0ΟΪΤ3Ο649 ϊΕΜΤαΐ(11β986): σΓ 2(5ΐ28>«ΑΡΑΠ(3Π);ΗΒΚ(87 3¾EP 00NL(347918);fNFRSF19(55504>;RB1(5925):KLF12(n278)^UL4A(8451);AClN1(22985);BCL2L2(599):J PH (84502):MNAT,(433');PSEN1(5663);TGFB3a043):VASHlC2284e):PPPim3^ 336 MAPK6(5597〉: J38 723(2551 W ):IGF1 R(380):ALPK3(57538);RAB 0C(5 99):TRAR(84231 );PK YTi (9088); 3( M93)^5SPT1(2935'PUa(53 7)£R 2(10595):PRRT2U1247e);Rf4F40i9810):FTS(e400)^IAPI 1(570l9K:TC FO066 );S PD3(555 ); CDt O(3558>.A APC,i(5 29);M T( 335VrNFSF12(8742)^AS7(8522):HCP1("323 5);CD 5RAP3(80279);C17orf73(55018);MPO(43533tABCn (63897);BIRC5(332):EMIUN2(8403 >;GNAL(2774);CA BLES;K91768〉:PHLPP 23239):BCL2(59e):FZR1(513^3):DPF1(8193):Sn:lT2(22933):SAMD4B〔55095);LYPD5(28
143 )ZGPAT(84619):MAPK1 (5594):NF2(4771 );CARD10(29775);NPTXR(23467XTNRCeB(23112);TOB2(1076 FIGF(2277);S C1 LI (8243);SEPT6C23157); ECP2(4204,
CDC2L2(985);TNFRSn4(8764):C;HD5(26038):CDC42C998):E2 iia870);WASF2(10ie3):RCCK"04);KHD BSl( 10657);LCK(3932):KIAA0319lX79932):raMS3(9783):CDC20(991 DKN2C(1031):NOTCH2(4853):CKS1B0l63>; C1orf21(81563>PPP1R12B(4660);SYT2O 27833;ADORA1(i34¾PH3C2BC5287) L10(3586〉:IL24("009);PlJ(NA 2(5362):VANGL1 (81839);KiF21 B(23046):RHOB ( 8》:MAPF^E322924):TGFA(7039>;HK2(3099);BRRNi(23397);W HBBC3625)f RCC3(2071):PROCC5e2 ):TAIP-2(8003 ):TI_K1 C9874):BARD 1 (580);TNS1 (7145)PAX3(5077>.HDAC 4(9759)SOK(6e6)"ZA (5l776):ZNF6^1(92999):RASSFKl11 ); HEMK1(51409);RBM15B(29890);RNF7( 616):TP 73U862e FAM43A(131 3>,LCTM1(3954):HD(3064):EREG(20e9 ;CN<32(901>,TPPP(l1076):DAP(ie PR A AK5562 PL37(6167);ERBB2!P(55914):APC(324):MCC0n63);HDAC3^8841):CPLX2 0814):NS (64324):ER3 (8870):C¾717〉BAK1(578):IHPK3(117283〉:PACSIMl(29993>,MAPi 3C5603〉:CDKN1A(1026):T EML2C79865);PT ^(S S^SRFCe VEGFt/^Z SUPTaHCS e LnOeOS FOXOSAttSOS^HECAは 1696〉;ELM01(9844):FOXK 1(221937);TRlAD3(5 76);HDAC9(973 ADCYKl07);K3FBP3(38e);EGFR(1956XF 3753S(222950);CASP2(83 5):K1AAD7730715)VIPR2C7434):LZTS1 (1 Ί 178J3OLR3DC661):BI 3(5ra09);TNF SF10A(8797>.TRIM35(23087): PTK2BC2185);DUSP4(1846):UNC5D(137970):TERn(7013):TP53INP1(9241);LYNX1(660W):MGC21881(389741 );UHRF2( 15426 CDK 2BC1030);TAF1 L(138474>.BAG1 C573);FANCG(2189);SE A4D00507);TNFSF15C9966);T NFSra(9 );TRAn(7185):DAB2IP(153090):FAM102A(399665);ADA B2(105):ZWINT(11130):SIRT1(23411):SGP LI C8879);C10orf54(64115);CHST3C9469);KIF113832);L2TS2C8445);FGF8C2253j;C 10orf76(79591 );SUFU(51684 PDCDiiC22984); NEURLC9148>BAG3C9531 );FA 53B(9679>,APBB1 (322); DK(4192);CDCA5(1 i 3130);DPF2C59 77>CLCF1(23529);PPP1CAC5499);FADDC8772); AB30(27314);SC 2BC6327);H FX(3014):EI24C9538);CDCA¾ 83461 )3CAT1 (586): KRAS(3845>HDAC7A(51564);MCRS1 (104 5>,TEGT(7009):FA!M2C23017);CBX5C23468>,PD EiK5i53>:rTGA7(3679);MYi_6i4637);C ADD(8738);FOXOiA(2308):RFP2(l0206〉:POU4n(5457):LOC283487(2 83487)BCL2L2(59 ):RG (9628):PSEN1(5663〉;LTBP2(4053)NEK9(91754):VASH1(2286>:TRAF3i7l87):BAG5 (9529 KTK207): JAG2(3714);BMF(90«7):FU43339(388115);FU38723(255180);SNX1 (6642尸 DCD7(1008ひ Ο5Κ(1445)·ΛΒΗΟ2(11057);ΐαΡ1Β(380):ΝΜΕ3(4832>;Τ5Ο2(7249):ΤΡΑΡ7(84231)^ί ΝΚ899):ΤΝΡί?5Ρ12Α(5133 i3);ERN2(10595);P8(2647 ^?^丁2("2476);。丫1_0(1540); 5(64400);し00283849^83849)£2 (1874):01"。1^10
ΪΝΡ5 12(8742);ΤΡ53(7157〉:0Α57(8522);ΤΟΜ1Ι_2(146691);ΡΟίΟΙΡ2(2β073):ΤΡΑ (9618):ΝΡ1(4763λΜυ_Τ6(4 302>尸 TRF(284"9〉:BRCAl(672):TB BP1(9755):K3F2BP1(10642)PHB(5245):MGFR(4S04):CROP(51747):DYNL Ι_2Π 0735);ΜΡΟ(4353>'ΡΓ¾Κ€:Α(5578);ΟΟΚ3(1018):5ΟΟ53(9021>·ΒΑΙΑΡ2(ΐ0458):ΟΑΒΙ 51(91768);ΒΝΠ65(49 70λΚ1ΑΑ0427(981ひ•BCL^SSe NFATClM TZ S iA^S s G GTU?^);^?^^^ )^!^^?^)^!^^?^ 11 «)):TNP 2(30000.LPHN 1 (22859);SIRT2(22933>. 3SF4GC199731 );FOSBC2354.D WD(1762);BBC3{2711 Z R PS"(6205〉;PPP2R1A(551 GF¾LF1(2909);ZNF343a9n5):C20orf"6(65992):E2Fl(1869):CEP250(】n90);PPP 1 R16Β(2β 1 >ZHX3(23051〉: MS (140730);STK4(6789):DIDOKl 1083):TNFRSFeB(8771 )^GPAT(84619)APP( 35l);ADA Bl(ltM>,LSS(4047):HK:2(23n9):MAPKK5594):PPM1F(9647):MlF(4282〉;ADORA2A(l35〉:NF2(4771); ΚΪΑΑ1 40l4794〉:MGAT3(42«):ZC3H7B(23264〉:NHP2U(4809);SEPT3(559e4):GTSE1(51512);PCTia(5l27):l QjSEO2(230 e);TMEM28(271 2):MLLT7(«03〉: P6-213m9,1(5!*765);CD 0LG(359>;HCFn(305 ; PRKY(5616):
ANKRD36(375248) .
NFDCC4784)
SDF4(51150);B3GALT6C126792): UBE2J2(118424);CENTB5(116983);SKIi:6497):C 1 orf93(127281 SPSBI (80176) ; PIK3CD(5293);TINAGL1 (64129);KIAA0319L(79932);IGSF4B(57863 NF648(127665);WNT3A(89780);OR2W5C4 41さ 32)^R2C3½1472);ATAD3C(219293>:INPP5D(3635):ANKRDi23(200539); Ali4P1(10267):raSl C25907):PH-4(5 4681>JHPia(9807〉:PLXNA1(5361〉:CLDN18(5!208;i:UPH(2d0879 3P5(28M):CPLX1(10815); AEA(10296〉:RGS i2(6002);し OC9 622(93622): CAMKL2(166614):DUX4(22947)AHR (57491):TPPP(11076):CTNND2(1501) ITX 1(5307XPCDHA1(56147¾PCDHA2(56146):PCDHA3(561 5):PCDHA (56144);PCDHA5(561^3〉;PCDHA6(56142); 。0 7(56"1)^00 56"0>^0^9(9752)^0^10(56139);?00^1(56138〉尸00^12(56137)^0^ A13(5613 :PCDHAC 1 (56135);PCDHAC2{5ei 34>.SH3PXD2B(285590);UNC5AC90249)i)BN10627);LOC51149C5 1149)^6orf85(63027):Ceorf 1 (221749);TULP1 (7287):COiLl ΣΑ1! (1303::TCF21 (6943):RPS6I^A2(ei 96):VGF(742 5):80^9(55973> ^1(2041)^了098(285973):1^。^4«03 :10^,688(80728)^01^28(1030);84<^し丁1(26 83):10^687> 》<(64768〉:0 2»^153090)©^03(8019):?了005(5730〉:^45224(40 62 C9orM40(89958):M GC61598(4 1478);LOC399706(399706)i:i0orf1 l4(399726 .LOC439985(439985)^l0orf116(10974>.FRATKl00 23¾ ARVELD1(83742)^10orf39(282973):STK32C(28i974) NPP5A(3632):FBXO3(26273)^T:r (2017)£)LG2(, 740)J)KFZp547C19K257160〉:KIRREL3(8 623):HOM- TES-,03C25900);DDN(23109);METTし 7A(25840);HOXC13(
7):BRF1 (2972):PACS2C23241 );C 1 orf37(283687);UBE2K7329):IFn40(9742);CAS IN1 (57524¾ZNF213(7760)ZN
KR013BO24930)^CDC55(8408 RAB"FFM(84 0):LHX1(3975尸 CGF2(7703):HLF(3131):KIAA0195(9772 : 1QTNfM(114897);HOXB8(3218):C18orf43(10650:|:RNFie5( 4 70):KIAA0«K98n :DH20( 8316);TX^L4A(10 907);WDR (57418):MKNK2(2872);MOBKL2ACl26308):L NB2C8 823)J)APK3a613);TNFAIP8L1(l26282>;JMJD 2B(23030);T画 4 (104e9);RAV£R1(,25950>.NnX(4784);F2RL3(9002):ZBTB32(27033);RASGRP4("5727〉:CAP N12(M79^8);PSCD2C9266》:SPHK2C56848〉:BCAT2(587);UN7B(6 ' 0);PRKCG(5582);LENG8(n4823):LOC3529 09(352909) CAM4(3386):EEF2(1938 ;GRLFK290&);UBOX5(22888>,BLCAP(1090 );SPATA2(9825)O21S2056E( 8568>^0^2(23275);5£?75(5 13>JBX 1 (6899 LOC 150223(150223)^RD 1 3774 ΕΟΑθ 896);FAM 11A(S4548 );CHM(1121):
ZFP4K286128)
PRDM16C63976)
CLASPK23332)
ZNF655C79027)
FAIM2C23017)
ZGPATC84619)
E2F2(1870>.CCDC21(647 3);LAPTM5 805〉:ZBTB8(127 57):MGC33556(3395 1);RA33Bf(586Ei);CDC42SE1(56. 882〉;UHMK1(127933):lL24(11009);TRAF5(7188>:C1orf95(375057):VANGL1(81839〉:SFX 5(9 097)^ASP10C843 ; CD28(940);COL4A3a2B5); J10996(5 520)^RM7C29n):SRGAP3(990l);PH"4(54681):RASSFKl1186);PraCK LE2(166336);ST3GAL6n0402);PCNP(57092):RNF7(96l6〉;HIP2(3093):TMPf¾SS11E(289835:OSMR(9180 :F2R(2l 49);T}CAM2(353376);SEMAeA(57556);M4BP3(23138);ELOVL2 4898);IHPK3(1 l7283》;CCND3(89e);HSP 0ABK 3326>尸 AQR8(85315 ;CNC(892);ATG5(9474):FOXO3^(2309):SLC22A3^6581 ):ELMO1(984<1):NUDCD3(23386 CALN1(83698)©CAP29(55973): SR1 (4481 )i)USP4( 1846);U NC5DC 137970):TACC 1 (6867):UBE2V2C7336):YTH DF3(253943);EXT1 (2131 ):LRRC6i23639);ST3GALt(6 82):C8orf30Ai51236): GC21881(389741 );KIAA 815(799 56);RECK(S434);SE A4D(10507);TNFSF8(944):C10orf9(219771 )^RD5B(84159¾SGPL1 C8879);HIF1 AN(55662); FAM26C(255022):C1 OorH 37(26098);FLJ 154(1962 6):TRAF6(7189):ACAT1 (38〉:SNF1 LK2( 235):CDON(509 37);KCNA6(3742):PTMS(5763):BCAT1(586〉;KRASC3845):HDAC7A(51564):TEGT(70 9):C12orf22(:81566):ZBTB3 9(9880);Π_ϋ11259(55332〉:ΤΗΡΑΡ2(23389);ΒΡΡ2(10206);5ΤΒ 3(29966 ほ 5668);UBE3A(7337):KLF13 (51621);Gcoml(145781>;rHSD4(79875);GRlN2A(2903)^TC:FCl0664):MPHOSPH6U0200);POLDIP2(26073):SAR (^1(23098):»^1(4763 1(10209):丁《£^ 101(8 336)^1^10(8493): 89(3219):8012(596)^1«<(57716〉£8
5964 SX4B(548313)P Y"nB 468): RPX(8406) )ATL1(4943);SMC 1(8243);SPRY3(10251〉:
ADCY1C107)
CNNM4(26504)
FUT3C2525) ,
«R1(11079);SASS6Cl63786):CDC14A(855e):RAPlAC5906):MCLi(4n0〉:CKS (1163);n iR(50848):BRP44C25 874>Ι)Ν 3(26052);ΒΟ52(5997>;ΜΡ5Ο (148808):ΡΡΚΡΒ2(5208);ΡΒΟΧΚ5629):(^Ν1_2(8ΐ669);Μ5Η2(4436):5ΕΒ TAD 9792);EDAR(10913):ZC3H6(376940);WDR33(55339)i CM6(4175XCYBRD1(79901 );PTD0tM(29789>STAT 1(6772);CASP10(8 3):CUL3(8452〉:HDAC4(9759)fLJ4596 (401(Mp):SRGAP3(9901 ):TMEM16K(55129);TDGF1(
699 ): ^026060) £061(285203) 80 (60675):011^01(56650)^0^(55);<3し3丁 (6408 )^1^1(5 46 );5 MC: L1(10051);i HL6(89857):YEATS 55 89):SENP2(59343);tP73L(8626);MGG 75( 070〉:HD(30^^DKF2 Ρ7β1Β107(91050):ΙΙ (3576〉;Π¾Α5ϊ(80ί44):ΡΒΚ<32(5593):Ο >υΒ.14(79982);ΤΪΡΑ(92β10): ΑΟ2Ι_Κ4085);ίΌ「2(
C(324》:MCC(4163):SLC12A2(6558);FGn(2246) i3BP(10, 6>:GCNT2(2651>;TCn9(694l>'TNFRSF21(27242)J CK(22858 :OL1i)A1(1310);C RK 68》:HACE1(57531);BVES l l49);ATG5(9474):SESNlt272 4);SERIN n(57 515);HEY2(23493):TNFAIP3(7128>:LOC90e39(00 9>:TFWAD3(54476):I_OC90693(90693 YC (54205):C EB5( 9586);CDKe(1021 );NAPE-PLD(222236):REL (56 9):ZC3HAV 1 (56829):CNOT7(29883):MTMR7(91 p8〉:AD A( 148);U C5D(l37970);SPFH2(l1160);BRF2(55290):UBE2V2(7336):UBE2W(55284);L RCClC85444)f2F5(1875); 1«^55:1(9788):<3 0(2776):090 47(236223)^0 43(85^5)^ 八3(8013): 01_ (389941)^/^^)3(56288):;^ 365(22891 SGPL1 (8879)^0X15(1355); NOLC1 (9221);GPR26(28 9)f F4G2C1982XDLG2(1740>GUL5(8065);PP
7);EEA1(841 l);APAn(317〉:HCFC2(29915):FBXO21(23014):15El.2C283 59):P2RX7(5027):TM|EM132B(U4795):
ETNK 55500);DIP13B(551^):LATS2(26524):TNFRSF19は 5504):FLn(232 ;HSPH1(10808>:FOXO1A(2308);S
UGT1(l0910);RAP2A(59"):FLJ107e9(55739 ;CUL4A(8451);METTL3(56339);KlAA1443(57594):PPM1A(5 943:M
AP3K9(4293 n4orf43(91748):LTBP2(4053);DIO2(173 );rrPK1(3705):EIF5O983):iJAG2(37W);GOLGA8G(2e37
_68]tTP53BP1(7l58):FGF7(2252):NARG2(79664);FEM1Bi:iOn6);IREB2(3658):ABHD2(11057):GSPT1(2935):MKL
2(57496)^ABARAPL2("345);QANC8139¾CDH13(1012):MNT(«35):TRAF4(9618);BRCA1(672):NPEPPSC9520):
— ΜΧΡΑ7( 3992ΐ);θΑΒΟ14(79092);ΡΑΒΐ2(201475);νλΡΑ ( 18);CEP192(55l25>;C18orf1(753):CTAGE1(64i593);
MALT1 CI∞92);PHiPPC23239):CLEC4M(10332)^3GTL3(2e86)i;20orf117(140710):RBL1 C5933);UBE2V1(7335)^
STF1(1477);CABLES2(81928):SON(6651):SLC5A3(652e CDC45L(831¾:MAPKW5594);MN1(4330):DEPDC5C96
81 CM5( 174);TNRC6BC23112>.LOC63929C63929);SEPT3(55964 ATXN10(2581 >;2BED (9889>.PRKXC5ei 3);
AGTR2086>;SEPT6(23157):AmB4(23439);RP6-213 9.1(51765);FMR1(2332);DKCl(n36);AFF2(233 );
37 ZKSCAN1C7586)
38 TPPP 1076)
SRGAP3C9901)
39
40 DFFAC1676)
UMDK8994)
41
42 FSTL3(10272)
43 NUDCD3C23386)
44 GIPC3(126326)
45 IQCEC23288)
46 C TM4C146223)
47 LETM1C395 )
AS GMFBC2764)
49 NFKC4784)
50 PIK3RK5295)
51 ATXNK6310)
52 RP5-875H10.1C389432)
53 TPIK7167)
54 ZNF192C7745)
55 ABO(28)
56 PRXC57716)
57 PALM2(114299)
OAV 6Ϊ80/:osoI>d
) (Hoi¾mi
雷 s .リミ- ) sx¾d 舊
/ O 80800ίAV//:otooAOOZSl>d
(52
達 π。Νν>
息リ § - )盲-xnal
ト vdoz 5
SSasyNlI )。
( K90
OAV2/u/ald sooso卜 Ooz
S (OSVHdlv
()isiSJNZ
〔〕〔量OI— 0卜
SGd一。
(ss 09ovndlv1
)に
〔〕〔〕¾—
GOLGA3
匚
/:iaI£ sooso.oo
oo
e
( S8に9£s
/ O soosoI 6Ϊ80AV
息
き
s£ys
賺AGd soi OSI
S (謹98S 82
280 ENTPD7(57089) 281 AFG3LK172)
282 APH1 (65059)
283 SLC36AK206358)
284 RBJ(51277)
285 UCDHU53841)
286 K THB5(3891)
287 SEMA3E0723) :
288 WDR35(57539) [表 2— 13]
289 S1PA1L3(23094)
290 GGTL3(2686) 291 PCYT2(5833)
292 ENAHC55740)
293 ANK 1(286)
294 G 1A 1(2890)
295 GIPC3(126326)
296 VAPB(9217)
297 PDPR(55066)
298 BRCC3(79184)
299 LETM 1(3954)
300 SARM 1(23098) 301 DCP2(167227)
302 TAGLNC6876)
303 ΤΡΡΡ(Π076)
304 SEC 14し 1(6397)
305 H-plk(51351)
306 GIPC3C126326)
/ O 6180800AV3賺/d soi 0SII
§3ョ £ .
3ε
)MX
//d iiisll
sNyiiv
F
目
(-
β§ΰίυ U
/ O180800iAV 6://l>d sotooAOOZS
養)Vリ U 9ια
/ O 2fl80800AV//Jd sosoAOOZSl.
舊
) (is一 asv
〔〕2600
us,
OAV/u/islld soio
() ε£Ην
) viasvf
舊)0wi
§§リー OΐS
§§
(St-68)3ai9 089
(0i-i99)HVN3
(ZZ98)ZSVO 8i9
(6i00I)V6dIV S
(6S9)2MdM8 9i9
(Si8I8) i02DSI 5iS (εΐ 952)ΐ·6ϊ399ΐ-9ίίΜ
(9iOH)dddI
(EZ8ZZ)IdIZa 2Z5
( 88)TMS US
(EIC992)r6lD99T-9dy 0Z9
(98iZ)fON9 69S
(n9½2)820lWVJ 899
(miil)D6WVH 999
(956l)Hd9H 595
. [61— S挲] [2600]
(66"S)30^9VM £9S
(ZZZU)9Dm 29S
(Z6I£)ndaNH T9S '
(εΐΚ2)0ΗΗΗ 09S
(86£8H)IIC VS 659
(9 iS)Xyd 899
(T9i6)HdNS i99
(i-668)iawn 9SS
(09")£I Z S5S
I EMJ ½S 8
soo雨ん oozai/ェ:) d 6Ϊ 80/800Z OAV
(seovlvo
羣
(S9USX
9 〕〕¾00?60
雷
一
( SSS-HNi les。5¾ . ,
()にϋ1
i
曹
舊)Hii §
)トlw »ト
) nsodv 989
(OSSSSHVM
691 CSNK1GK53944)
692 SH3BP2(6452)
693 FMN 3(91010)
694 GM632(57473)
695 PALM2(114299)
696 ZFP41(286128)
697 FOX K221937)
698 PRKAA2(5563)
699 L RC27(80313)
ZF(58487)
701 BRCAK672)
702 MGAT4A(11320) [表 2— 22]
703 TR1M33C51592)
704 LTBP3(4054)
705 CUGBP2(10659)
ZNF440L(284390)
707 ISG20 1(64782)
708 BDK B2C624)
ALPK3(57538)
TFRC(7037)
PCYT2(5833)
YEATS2C55689)
FDPSC2224)
BO (666)
BBS5C129880) .
ZBTB7A(51341)
TUBBK81027)
O/AV//: 680800ZsoLooaII>d soo
//: O soosoLooaII>d 6Ϊ80AV
/ O80800AVu//ld sosoAOOZS.
舊 i
()6一。
)ss££
言。
/ Ofl80800∑AV 2://l>d S0000L00zs.
6
賺AG soi OSId
雷
§雷
ミ
PNMA5
(C6iOI)dIHDNAS 9Z6
(66Zig)Do 8 ¾ e
(90S9)3VI31S ZE6
X wom ιεβ
(069gS)TSDVd 0E6
(ΑΐΙ6)Π 3 S LZ6
(8 SSZS)9SOi iNV 926
(eWTdVcftn 9Z6
(6C8I8)nONVA ZZ6
N \Z6 ' (^ 6£)IWi31 ZB
(tm)IdVcftn 616
(8Η6)Τ«η N 8Ϊ6
(ZASOI) SJ AT6
£61 I XOd Z\6
' (Z9299)SMMM Π6 (90Π9)Μΐ9Η1 016
sooroo/-oozai/i3d 6 丽 800 OAV
¾ενϋΊΟ
き
965 CE 1C9350)
966 SH3G B2(56904)
967 ILF3(3609)
968 SYNGAP1C8831)
969 PEX19(5824)
970 LUZPK7798) 971 L RC27C80313)
972 GRHL2C79977)
973 FAM53A(152877)
974 HOXB8(3218)
975 GRIN2A(2903)
976 1F13B(23303)
977 RAIK10743)
978 ADCYK107) [表 2— 28]
979 FGD3(89846)
980 BCRC613) 981 R]MS3(9783)
982 FA 53A(152877)
983 TMED4C222068)
984 SLAC6503)
985 TMTC 1(83857)
986 ARL5B(221079)■
987 PERQ 1(64599)
988 FADS 1(3992)
989 TRAM20697)
990 NRCAM(4897) 991 BIRC4BP(54739)
雷?一
(き 6
O/00ZAV SH808/3oozaI1dotoo..
ミ
。
(雷206 so su
)ΓΟΠΛ
OV/0ZA SC080/u/LoozalIdotoo
//:00L00∑alI>d S001.
£雷〕
OAV//JdsoLooalI soo
(〕09SU H
一 ョ
靈I
3舊SV 08
1129 ZNF72K170960)
1133 NFATC 1(4772)
1134 DISC1(27185)
1135 MAP K5594)
1136 POLR3H(l71568)
1137 NKT C4820) '
1138 ABI2(10152)
1139 APOL6(80830)
1140 HOXAl 1(3207)
1141 RNFl 2(51132)
1142 TP531NPK94241)
1143 CREB5(9586)
1144 TPP 11076)
1145 H-pik(51351)
1146 ENTPD7(57089)
1147 ZNF440U284390)
1148 AKNA(80709)
OAV/:/zaI>d soosoAoo
(¾3。¾¾n
§)9 df
〔s【〕?90οszΐ
§)髮132
§sas卜
)£1V¾。V
き 1D9 Is
(き ΐλυαγ
)5s匿 1
23s
舊S O。。
雷ト
(O8SS8 is .
一
(9896)mOA 162
)6IVWaV
z\
m
ョ
Oi l
soo雨ん oozai/ェ:) d 6Ϊ 80/800Z OAV
O/iAV 6lio8/D/isIId ii
()I6sssi
setilN )τδ
1321 MAGI 1(9223)
1322 TMEM132B(114795)
1323 FAM78A(286336)
1324 VGLL3(389136)
1325 CPLX2(10814)
1326 NT K2(4915)
1327 RIMS4(140730)
1328 SPTLC2C9517)
1329 AFG3LK172)
1330 RP11-145H9.1C340156)
1331 NDEK54820)
【332 THRB(7068)
[333 GABRB2(2561)
ί334 RCP9(27297)
1335 AFG3LK172)
.336 PRLR(5618)
[0110] 本発明の核酸を用いた、マイクロ RNAやマイクロ RNA前駆体などの核酸の発現ま だは機能を促進或いは抑制させる物質をスクリーニングする方法としては、本発明の 核酸を用いて、マイクロ RNAやマイクロ RNA前駆体などの核酸の発現または機能を 促進或いは抑制させる物質をスクリーニングする方法であれば、いかなる方法でもよ レ、。例えば、本発明のマイクロ RNAやマイクロ RNA前駆体などの核酸を発現するべ クタ一を細胞に導入し、それらの標的遺伝子の発現を抑制する物質、もしくはそれら の標的遺伝子の発現を促進する物質をスクリーニングする方法があげられる。
[0111] 標的遺伝子の発現を抑制する物質としては、標的遺伝子の mRNAの発現を抑制す る物質であればいかなる物質であってもよいが、核酸が好ましぐ標的遺伝子に対す る siRNAがさらに好ましい。標的遺伝子の発現を促進する物質としては、標的遺伝子 の mRNAの発現を促進する物質であればレ、かなる物質であってもよレ、が、核酸が好 ましく、標的遺伝子の発現を抑制するマイクロ RNAに対する siRNAがさらに好ましい
[0112] 本発明の核酸またはベクターを導入した細胞とは、本発明の核酸またはベクターを 体外において導入した細胞であればレ、かなる細胞であってもよい。具体的には、肥 満細胞および肥満細胞の前駆細胞、または、間葉系幹細胞および間葉系幹細胞が 分化してできた細胞、例えば皮膚、肺、小腸、鼻、扁桃、眼瞼結膜、血管壁、骨髄等 の組織に存在する細胞、または、骨髄、脂肪組織、臍帯血、子宮内膜、真皮、骨格' 筋、骨膜、歯小嚢、歯根膜、歯髄、および歯胚等の組織に存在する細胞であり、例え ば、骨芽細胞、脂肪細胞、および筋肉細胞等をあげることができる。
[0113] 本発明において肥満細胞とは、各種刺激により活性化され、脱顆粒を起こし、数多 くの炎症性メディエーターを遊離、産生する細胞で、種々のアレルギー疾患の病態 形成にも関与する細胞をレ、う。
本発明において間葉系幹細胞とは、骨髄、脂肪組織、臍帯血、子宮内膜、真皮、 骨格筋、骨膜、歯小嚢、歯根膜、歯髄、および歯胚等の間葉系組織に存在し、少な くとも骨芽細胞、脂肪細胞、および筋肉細胞等の間葉系細胞への分化能を有する細 胞をいう。
[0114] 本発明の核酸を有効成分とする医薬は、肥満細胞の異常に起因する疾患の診断 または治療に用レ、ることができる。肥満細胞の異常としては、脱顆粒の異常があげら
. れるため、本発明の核酸は、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤として用 いることもできる。また、本発明のマイクロ RNAやマイクロ RNA前駆体などの核酸の 発現または機能を促進或レ、は抑制させる物質や、本発明のマイクロ RNAなどの核酸 の標的遺伝子の発現を抑制または促進する物質もまた、肥満細胞の異常に起因す る疾患の診断または治療に用いることができる。これらの物質は肥満細胞の脱顆粒 促進剤または脱顆粒抑制剤として用いることもできる。
[0115] 肥満細胞の異常に起因する疾患としては、具体的には、アトピー性皮膚炎、喘息、 慢性閉塞性肺疾患、及びアレルギー疾患等をあげることができる。
本発明の核酸を有効成分とする医薬は、間葉系幹細胞の増殖および/または分 化の異常に起因する疾患の診断または治療に用いることができる。また、本発明のマ イク口 RNAやマイクロ RNA前駆体などの核酸の発現または機能を促進或レ、は抑制
させる物質や、本発明のマイクロ RNAなどの核酸の標的遺伝子の発現を抑制または 促進する物,質もまた、間葉系幹細胞の増殖および Zまたは分化の異常に起因する 疾患の診断または治療に用いることができる。
[0116] 間葉系幹細胞の増殖および/または分化の異常に起因する疾患としては、具体的 には、癌、骨形成不全症、軟骨形成不全症、糖尿病等をあげることができる。
本発明の核酸を有効成分とする医薬は、細胞の増殖などの異常や、組織の過形成 等が原因となってレ、る疾患の診断または治療に用レ、ることができる。また本発明の核 酸は、細胞の増殖抑制剤もしくは増殖促進剤として用レ、ることもできる。また、本発明 のマイクロ RNAやマイクロ RNA前駆体などの核酸の発現または機能を促進或いは 抑制させる物質や、本発明のマイクロ RNAなどの核酸の標的遺伝子の発現を抑制 または促進する物質もまた、細胞の増殖などの異常や、組織の過形成等が原因とな つている疾患の診断または治療に用いることができる。これらの物質は細胞の増殖抑 制剤もしくは増殖促進剤として用レヽることもできる。ここで細胞の増殖の異常とは、生 体内における通常の増殖速度ではなレヽ速度で細胞が増殖してレ、る状態をレ、う。
[0117] 細胞の増殖異常や組織の過形成等が原因となってレ、る疾患としては、具体的には 、癌、動脈硬化、慢性関節リウマチ、前立腺肥大症、経皮的経血管的冠動脈形成術 後の血管再狭窄、肺線維症、糸球体腎炎、自己免疫疾患等をあげることができる。
. 以下、本発明の核酸がマイクロ RNAやマイクロ RNA前駆体である場合を例として、 本発明を詳細に説明する。
1:肥満細胞で発現するマイクロ RNAおよびマイクロ RNA前駆体の同定
(1— ί)肥満細胞の取得、培養
ヒト肥満細胞は、安全かつ効率的に取得される方法であれば特に限定されなレ、が、 例えば、ヒトの肺、皮膚、胎児肝臓などから公知の方法 [J. Immunol. Methods, 169, 1 53 (1994); J. Immunol., 138, 861 (1987); J. Allergy Clin. Immunol, 107, 322 (2001); J. Immunol. Methods., 240, 101 (2000)]により調製することができる。また、公知の方 法 [J. Immunol., 157, 343, (1996); Blood, 91, 187 (1998); J. Allergy Clin. Immunol, 106, 141 (2000); Blood, 97, 1016 (2001); Blood, 98, 1127 (2001); Blood, 100, 3861 (2002); Blood, 97, 2045 (2001)]に従って、ヒトの臍帯血、末梢血、骨髄、肺あるいは
皮膚力 調製した単核球を、幹細胞因子 (以下、 SCFともいう)の存在下で培養し、肥 満細胞に分化させることにより、調製することができる。
[0118] また、ヒト肥満細胞力も樹立した細胞株を用レ、ることもできる。ヒト肥満細胞株として は、ヒト肥満細胞の性質をよく保持していることが知られてレ、る LAD2[Leuk. Res., 27, 671 (2003); Leuk. Res., 27, 677 (2003)]等があげられる。
( 1一 2)低分子 RNAと配列情報の取得
上記の各種方法で取得した肥満細胞から全 RNAを抽出し、該 RNAを用いて肥満細 胞で発現するマイクロ RNAを含有する低分子 RNAを以下のようにして取得することが でさる。 ,
[0119] 低分子 RNAの取得法としては、具体的には、 Genes & Development, 15, 188-200 ( 2000)に記載の方法に準じて、 15%ポリアクリルアミドゲル電気泳動による低分子 RNA の分離及び切り出し、 5'末端脱リン酸化、 3'—アダプターライゲーシヨン、リン酸化、 5 ,一アダプタ一ライゲーシヨン、逆転写、 PCR増幅、コンカテマ一化、ベクタ一へのライ ゲーシヨンを順次経て、低分子 RNAをクローニングし、そのクローンの塩基配列を決 定する方法等があげられる。あるいは、例えば、 Science, 294, 858 - 862 (2001)に記載 の方法に準じて、 15%ポリアクリルアミドゲル電気泳動による低分子 RNAの分離及び 切り出し、 5'—アデニル化 3'—アダプターライゲーシヨン、 5'—アダプターライゲーシ ヨン、逆転写、 PCR増幅、コンカテマ一化、ベクターへのライゲーシヨンを順次経て、 低分子 RNAをクローユングし、そのクローンの塩基配列を決定する方法等があげられ る。
[0120] あるいは、 Nucleic Acids Research, 34, 1765-1771 (2006)に記載の方法により、 15% ポリアクリルアミドゲル電気泳動による低分子 RNAの分離及び切り出し、 5'末端脱リン 酸化、 3'—アダプタ一ライゲーシヨン、リン酸化、 5'—アダプターライゲーシヨン、逆転 写、 PCR増幅、マイクロビーズベクターへのライゲ一シヨンを順次経て、低分子 RNAを クローニングし、そのマイクロビーズの塩基配列を読み取ることで塩基配列を決定す ることにより低分子 RNAを取得することちでさる。
[0121] また、 small RNA Cloning Kit (タカラバイオ社製)を用いて低分子 RNAを取得するこ とちでさる。
(1— 3)マイクロ RNAの同定
取得した低分子 RNA配列がマイクロ RNAであるかは、 RNA, 9, 277-279 (2003)に 記載の基準に従うか否かで判定できる。例えば、上記方法で取得して塩基配列を決 定した低分子 RNAの場合、以下のようにしておこなうことができる。
[0122] すなわち、取得した低分子 RNA塩基配列に対応する DNA配列を 5'末端側および 3 '末端側にそれぞれ 50 nt程度伸ばした周辺ゲノム配列情報を取得し、そのゲノム配 列力も転写されることが予測される RNAの 2次構造を予測する。その結果、ヘアピン 構造を有し、且つ該低分子 RNAの塩基配列がヘアピン構造の片鎖に位置する場合 、該低分子 RNAはマイクロ RNAであると判定できる。ゲノム配列は一般に公開され わり、例 Lは、 UCSし ijenome Bioinformatics (http://genome.ucs edu/)力ら入手口/ 能である。また、 2次構造予測も様々なプログラムが公開されており、例えば、 RNAfold [Nucleic Acids Research, 31, 3429-3431 (2003)]や Mfold [Nucleic Acids Research, 31, 3406-3415 (2003)]等を用レ、ることができる。また、既存のマイクロ RNA配列は mi RBase (http://microrna.sanger.ac.uk/)とレ、うデータベースに登録されており、ここに 記載の配列と同一か否かで、既存のマイクロ RNAと同一か否かを判定することがで きる。
[0123] このようにして同定した、肥満細胞で発現するマイクロ RNAとして、例えば、配列番 号 1〜: 1336のいずれかで表される塩基配列を有する核酸をあげることができる。 また、同定したマイクロ RNAに対応するゲノム配列と、他の生物のゲノム配列とを比 較し、配列番号 1〜: 1336のいずれかで表される塩基配列と 90%以上、好ましくは 95 %以上の同一性を有する塩基配列を有する核酸を、その生物におけるマイクロ RNA として同定することができる。
(1一 4)マイクロ RNA前駆体の同定
上記(1一 3)で同定しだマイクロ RNAの塩基配列をもとに、マイクロ RNAをコード する配列を含む配列をマイクロ RNA前駆体をコードする配列として同定することがで きる。本発明の肥満細胞で発現するマイクロ RNA前 体としては、例えば、配列番 号 1337〜2851のいずれかで表される塩基配列を有する核酸等をあげることができ る。
[0124] 更に、同定したマイクロ RNA前駆体に対応するゲノム配列と、他生物のゲノム配列 とを比較し、配列番号 1337〜2851のいずれかで表される塩基配列と 80%以上、好 ましくは 90%以上、より好ましくは 95%以上、さらに好ましくは 97%以上の同一性を 有する塩基配列を有する核酸を、その生物におけるマイクロ RNA前駆体として同定 することができる。
2.核酸の合成
上記 1.のようにして一旦、肥満細胞で発現するマイクロ RNAおよびマイクロ RNA 前駆体が同定された後は、その塩基配列に基づいてリボヌクレオチドの重合体であ る RNAだけでなぐデォキシリボヌクレオチドの重合体である DNAも合成することがで きる。例えば、上記 1.で同定した RNAの塩基配列をもとに、. DNAの塩基配列を決定 することができる。 RNAの塩基配列に対応する DNAの塩基配列は、 RNAの配列に含 まれる U (ゥラシル)を T (チミン)に読み替えることで一義的に決定できる。また、リボヌ クレオチドとデォキシリボヌクレオチドが混合した重合体や、ヌクレオチド類似体を含 む重合 同様にして合成することができる。
[0125] 本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸を合成する 法としては、 特に限定されず、公知の化学合成法を用いる方法、あるレ、は、酵素的転写法等にて 製造することができる。公知の化学合成法を用いる方法として、ホスホロアミダイト法、 ホスフォロチォエート法、ホスホトリエステル法、 CEM法 [Nucleic Acid Research, 35, 3 287 (2007)]等をあげることができ、例えば、 ABI3900ハイスループット核酸合成機(ァ プライドバイオシステムズ社製)により合成することができる。酵素的転写法としては、 目的の塩基配列を有したプラスミドまたは DNAを铸型として典型的なファージ RNAポ リメラーゼ、例えば、 T7、 Τ3、または SP6 RNAポリメラーゼを用いた転写法をあげること ができる。
3.マイクロ RNAおよび該マイクロ RNA前駆体の機能 検出する方法
マイクロ RNAは、ヘアピン構造を有するマイクロ RNA前駆体力 細胞質内で RNase III endonucleaseの一種である Dicerと呼ばれる蛋白質によるプロセシングを経て生成 され、標的塩基配列を有する mRNAの翻訳を抑制する。従って、当該機能を有してい るか否かで得られた核酸がマイクロ RNAであるか否かを検出することができる。
[0126] 例えば、 RNAが RNaselll endonucleaseによりプロセシングされるか否かでマイクロ R NA前駆体としての機能を有する力、を測定することができる。具体的には、機能を検 出したい RNAを RNaselll endonucleaseと反応させ、反応産物を電気泳動した際、マイ クロ RNA前駆体としての機能を有して 、れば、プロセシングを受けた 20 - 25塩基長程 度のバンドが検出されることを利用して、該機能を有する力を測定することができる。 RNaselll endonucleaseは、マイクロ RNA前駆体をプロセシングする活性を有するもの であれば特に限定ざれないが、 Dicer蛋白質を用いることが好ましい。具体的には、 si -RNAse IIITM (タカラバイオ社製)、 Cold Shock- DICER (タカラバイオ社製)、 Recomb inant Dicer Enzyme (Stratagene社製)、 BLOし K一 iT Dicer RNAi Transfection Kit (Invi trogen社製)、 X- treme GENE siRNA Dicer Kit (ロシュ'アプライド-サイエンス社製) などを用いる;とができ、添付された説明書の反応条件に従うことで測定できる。
[0127] マイクロ RNAの機能を検出する方法としては、標的塩基配列を有する mRNAの翻 訳を抑制する力否かで該機能を有する力を測定する方法をあげることができる。 マイクロ RNAは、その標的塩基配列を 3'末端側 untranslated region (3' UTR)に含 む mRNAの翻訳を抑制することが知られている [Current Biology, 15, R458-R460 (20 ' 05)]。そこで、測定しょうとする RNAに対する標的塩基配列を、適当なレポーター遺 伝子発現ベクターの 3' UTRに挿入した DNAを作製して、発現ベクターに適合した宿 主細胞に導入し、その細胞に該 RNAを発現させた時に、レポ一ター遺伝子の発現を 測定することで、マイクロ RNAの機能を有してレ、るか否力を検出することができる。
[0128] レポーター遺伝子発現ベクターは、レポーター遺伝子の上流にプロモーターを有し ており、宿主細胞においてレポーター遺伝子が発現できるものであればレ、かなるもの でもよい。レポーター遺伝子としては、あらゆるレポ一ター遺伝子を使用することが可 能であるが、例えば、ホタル 'ルシフェラーゼ遺伝子、ゥミシィタケ'ルシフェラーゼ遺 伝子、クロラムフエ二コール'ァセチルトランスフェラーゼ遺伝子、 j3—ダルク口ニダ一 ゼ遺伝子、 0—ガラクトシダーゼ遺伝子、 0 -ラクタマーゼ遺伝子、ェクオリン遺伝子 、グリーン 'フルォレツセント ·プロテイン遺伝子および DsRed蛍光遺伝子などが利用 できる。こうした性質を有するレポ一ター遺伝子発現ベクターとして、例えば、 psiCHE CK-1 (Promega社製)、 psiCHECK- 2 (Promega社製)、 pGL3_Control (Promega社製)
、 PGL4 (Promega社製)、 pRNAi- GL (タカラバイオ社製)、 pCMV- DsRed- Express (CL ONTECH社製)等をあげることができる。また RNAは、後述の 6.に記載した方法で発 現させることができる。
[0129] マイクロ RNAの機能は、具体的には以下のようにして検出することができる。まず宿 主細胞をマルチウエルプレート等に培養し、標的塩基配列を有したレポーター遺伝 子発現ベクターと RNAを発現させる。その後、レポーター活性を測定し、該 RNAを発 現させなレ、場合と比較して、該 RNAを発現させた場合にレポーター活性が低下する ことを検出することで、マイクロ RNAの機能を検出することができる。 ' 4.本発明の核酸を用いたマイクロ RNAやマイクロ RNA前駆体等の核酸の発現を検 出する方法
以下 、本発明の核酸を用いて、マイクロ RNAやマイクロ RNA前駆体等の核酸 φ. 発現を検出する方法について説明する。
[0130] マイク 0RNAやマイクロ RNA前駆体等の発現を検出する方法としては、例えば、 (
1)ノーザンノヽイブリダィゼーシヨン、 (2)ドットブロットハイブリダィゼ一シヨン、 (3)in sii
Uハイブリダィゼーシヨン、 (4)定量的 PCR、 (5)デフアレンシャル ヽイブリダィゼーシ ヨン、(6)マイクロアレイ、(7)リボヌクレアーゼ保護アツセィ等の方法があげられる。
[0131] ノーザンプロット法とは、検体由来 RNAをゲル電気泳動で分離後、ナイロンフィルタ 一等の支持体に転写し、本発明の核酸の塩基配列をもとに適宜標識をしたプローブ を作製し、ハイブリダィゼ一シヨンおよび洗浄をおこなうことで、本発明の核酸に特異 的に結合したバンドを検出する方法であり、具体的には、例えば、 Science 294, 853- 858 (2001)に記載の方法等に従って行うことができる。
[0132] 標識プローブは、例えば、ニック'トランスレーション、ランダム.プライミングまたは 5' 末端のリン酸化等の方法により放射性同位体、ピオチン、ジゴキシゲニン、蛍光基、 化学発光基等を、本発明の核酸の塩基配列と相補的な配列を有する DNAや RNA、 あるいは LNA等に取り込ませることで調製できる。標識プローブの結合量はマイクロ R NAやマイクロ RNA前駆体等の核酸の発現量を反映することから、結合した標識プ ローブの量を定量することでマイクロ RNAやマイクロ RNA前駆体等の発現量を定量 することができる。電気泳動、メンブレンへの移行、プローブの調製、ハイブリダィゼ
—シヨン、核酸の検出については、モレキュラー 'クローニング第 3版, Cold Spring Ha rbor Laboratory Press, NY, USA (2001)に記載の方法により行うことができる。
[0133] ドットプロットハイブリダィゼーシヨンは、組織や細胞から抽出した核酸をメンブラン 上に点状にスポットレて固定し、プロ一ブとハイブリダィゼーシヨンを行い、プローブと 特異的にハイブリダィズする核酸を検出する方法である。プローブとしてはノーザン ハイブリダィゼーシヨンと同様のものを用レ、ることができる。核酸の調製、スポット、ハイ ブリダィゼーシヨン、検出については、モレキュラー 'クローニング第 3版に記載の方 法により行なうことができる。
[0134] in dmノヽイブリダィゼーシヨンは、生体力 取得した組織のパラフィンまたはクリオス タツト切片、あるいは固定化した細胞を検体として用レ、、標識したプローブとハイプリ ダイゼーシヨンならびに洗浄の工程を行い、顕微鏡観察により、マイクロ RNAやマイ クロ RNA前駆体等の組織や細胞内での分布や局在を調べる方法である [Methods i n Enzymology, 254, 419 (1995)]。プローブとしてはノーザンハイブリダィゼーシヨンと 同様のものを用いることができる。具体的には、 Nature Method 3, 27 (2006)に記載の 方法に従って、マイクロ RNAやマイクロ RNA前駆体等を検出することができる。
[0135] 定量的 PCRでは、検体由来 RNAから、逆転写用プライマ一と逆転写酵素を用いて 合成した cDNA (以後、該 cDNAを検体由来 cDNAともいう)を測定に用いる。 cDNA合 成に供する逆転写用プライマーとして、ランダムプライマーあるレ、は特異的 RTプライ 、 マー等を用いることができる。特異的 RTプライマ一とは、本発明のマイクロ RNAやマ イク口 RNA前駆体等、およびその周辺ゲノム配列に対応する塩基配列に相補する 配列を有するプライマーをいう。
[0136] 例えば、検体由来 cDNAを合成後、これを铸型とし、マイクロ RNAやマイクロ RNA 前駆体およびその周辺ゲノム配列に対応する塩基配列、あるいは逆転写用プライマ 一に対応する塩基配列力 設計した铸型特異的なプライマーを用いて PCRを行い、 c DNAの断片を増幅させ、ある一定量に達するまでのサイクル数力 検体由来 RNAに 含まれるマイクロ RNAやマイクロ RNA前駆体の量を検出する。铸型特異的なプライ マ一としては、マイクロ RNAやマイクロ RNA前駆体およびその周辺ゲノム配列に対 応する適当な領域を選択し、その領域の塩基配列の 5'端 20〜40塩基の配列力 なる
DNAまたは LNA、および 3'端 20〜40塩基と相補的な配歹 IJからなる DNAまたは LNAの . 組を用レ、ることができる。具体的には、 Nucleic Acids Research, 32, e43 (2004)に記 載の方法等に準じて行うことができる。
[0137] または、 cDNA合成に供する逆転写用プライマーとして、ステム'ループ構造を有し た特異的 RTプライマーを用いることもできる。具体的には、 Nucleic Acid Research, 3 3, el79 (2005)に記載の方法に従い、あるいは、 TaqMan MicroRNA Assays (アプライ ドバイォシステムズ社製)を用レ、て行うことができる。
別の検体由来 cDNA合成法として、検体由来 RNAに対して polyAポリメラ一ゼにより p , olyA配列を付加し、オリゴ dT配列を含む塩基配列を逆転写用プライマーとして用い ることにより、逆転写反応を行うこともできる。具体的には、 miScript System (キアゲン 社製)や QuantiMir RT Kit (System Biosciences社製)を用いて行うことができる。
[0138] また、本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸を少なくとも 1つ以上 含む塩基配列に対応する DNAあるレ、は LNAを固定化させたフィルターあるレ、はスラ イドガラスやシリコンなどの基盤に対して、検体由来 cDNAをハイブリダィゼーシヨンし 、洗浄を行うことにより、マイクロ RNAやマイクロ RNA前駆体等の量の変動を検出す ることができる。このようなハイブリダィゼーシヨンに基づく方法には、ディファレンシャ ルハイブリダィゼーシヨン [Trends Genet., 7, 314 (1991)]やマイクロアレイ [Genome R es., 6, 639 (1996)]を用レ、る方法があげられる。いずれの方法もフィルターあるいは基 盤上に U6 RNAに対応する塩基配列などの内部対照を固定化することで、対照検体 と標的検体の間でのマイクロ RNAやマイクロ RNA前駆体等の量の違いを正確に検 出することができる。また対照検体と標的検体由来の RNAをもとにそれぞれ異なる標 識の dNTP(dATP、 dGTP、 dCTP、 dTTPの混合物)を用いて標識 cDNA合成を行い、 1枚のフィルターあるいは 1枚の基盤に 2つの標識 cDNAを同時にハイブリダィズさせ ることで、正確なマイクロ RNAやマイクロ RNA前駆体等の定量を行うことができる。 更に、対照検体および/または標的検体由来の RNAを直接標識してハイブリダィズ させることで、マイクロ RNAやマイクロ RNA前駆体等の定量を行うこともできる。例え ば、 Pro Natl.Acad.Sci. USA, 101, 9740-9744 (2004)や Nucleic Acid Research, 32, el88 (2004)等に記載のマイクロアレイを用いてマイクロ RNA等を検出することができ
る。具体的には、 mirVana miRNA Bioarray (Ambion社製)を用いてマイクロ RNA等を 検出または定量することができる。
[0139] リボヌクレアーゼ保護アツセィでは、まず本発明のマイクロ RNAやマイクロ RNA前 駆体あるいはそめ周辺ゲノム配列に対応する塩基配列の 3'端に T7プロモーター、 SP 6プロモーターなどのプロモーター配列を結合し、標識した NTP(ATP、 GTP、 CTP、 U TPの混合物)および RNAポリメラーゼを用いたイン'ビトロの転写系により、標識したァ ンチセンス RNAを合成する。該標識アンチセンス RNAを、検体由来 RNAと結合させて 、 RNA- RNAハイブリッドを形成させた後、 1本鎖 RNAのみを分解するリボヌクレアーゼ Aで消化する。該消化物をゲル電気泳動し、 RNA-RiMAハイブリッドを形成することに より消化力 保護された RNA断片を、マイクロ RNAやマイクロ RNA前駆体として検出 または定量する。具体的には、 mirVana miRNA Detection Kit (Ambion社製)を用い てマイクロ RNA等を検出または定量することができる。
5.本発明の核酸を用いてマイクロ RNAやマイクロ RNA前駆体等の核酸の変異を検 出する方法 _
' 以下に本発明の核酸を用いて、マイクロ RNAやマイクロ RNA前駆体等の核酸の 変異を検出する方法について説明する。
[0140] マイクロ RNAやマイクロ RNA前駆体等の変異を検出する方法として、正常型のマ イク口 RNAと変異型のマイクロ RNA、および正常型のマイクロ RNA前駆体と変異型 のマイクロ RNA前駆体とのハイブリダィズにより形成されるへテロ二本鎖を検出する 方法を用レ、ることができる。
ヘテロ二本鎖を検出する方法としては、(1)ポリアクリルアミドゲル電気泳動による ヘテロ二本鎖検出法 [Trends genet., 7, 5 (1991)]、(2)—本鎖コンフオメーシヨン多 型解析法 [Genomics, 16, 325-332 (1993)]、(3)ミスマッチの化学的切断法(CCM, c hemical cleavage of mismatches) [Human Genetics (1996), Tom Strachan and Andre w P. Read, BIOS Scientific Publishers Limited], (4)ミスマッチの酵素的切断法 [Nat ure Genetics, 9, 103-104 (1996)]、(5)変性ゲル電気泳動法 [Mutat. Res., 288, 103 -112 α993)]等の方法があげられる。
[0141] ポリアクリルアミドゲル電気泳動法によるへテロ二本鎖検出法は、例えば、以下のよ
うにして行う。まず、検体由来 DNAあるいは検体由来 cDNAをテンプレートに対し、本 発明のマイクロ RNAやマイクロ RNA前駆体等の塩基配列を含むゲノムの塩基配列 を基に設計したプライマーにより、 200 bpよりも小さい断片として増幅する。ヘテロ二 本鎖が形成された場合は、変異を持たないホモ二本鎖よりも移動度が遅ぐそれらは 余分なバンドとして検出することができる。特製のゲル (Hydro - link, MDEなど)を用い たほうが分離度はよい。 200 bpよりも小さい断片の検索ならば、揷入、欠失、ほとんど の 1塩基置換を検出することができる。ヘテロ二本鎖解析は、次に述べる一本鎖コン フオメーシヨン解析と組み合わせた 1枚のゲノレで行うことが望ましい。
[0142] 一本鎖コンフオメーシヨン多型解析(SSCP^析; single strand conformation polymor phism analysis)では、検体由来 DNAあるいは検体由来 cDNAをテンプレートにして、 マイクロ RNAやマイクロ RNA前駆体等の塩基配列を含むゲノムの塩基配列に基づ き設計したプライマーを用いて、 200bpよりも小さい断片として増幅した DNAを、変性 後に、未変性ポリアクリルアミドゲル中で泳動する。 DNA増幅を行う際にプライマーを 同位体あるレ、は蛍光色素で標識するか、または未標識の増幅産物を銀染色すること により、増幅した DNAをバンドとして検出することができる。野生型のパターンとの相 違を明らかにするために、コントロールの検体も同時に泳動すると、変異を持った断 片を移動度の違いから検出できる。
[0143] ミスマッチ化学的切断法(CCM法)では、検体由来 DNAあるいは検体由来 cDNAを テンプレートに、マイクロ RNAやマイクロ RNA前駆体等の塩基配列を含むゲノムの 塩基配列に基づき設計したプライマーで増幅した DNA断片を、本発明の核酸に同位 体あるレ、は蛍光標識をとり込ませた標識核酸とハイブリダィズさせ、四酸化オスミウム で処理することでミスマッチしている場所の DNAの一方の鎖を切断させ変異を検出す ることができる。 CCMは最も感度の高い検出法の 1つであり、キロベースの長さの検 体にも適応できる。
[0144] 上記、四酸化オスミウムの代わりに T4ファージリゾルベースとエンドヌクレアーゼ VII のような細胞内でミスマッチの修復に関与する^素と RNaseAと組み合わせることで、 酵素的にミスマッチを切断することもできる。
変性ゲル電気泳動法(denaturing gradient gel electrophoresis : DGGE法)では、検
体由来 DNAあるいは検体由来 cDNAをテンプレートに、マイクロ RNAやマイクロ RNA 、 前駆体等の塩基配列を含むゲノムの塩基配列に基づき設計したプライマーで増幅し ' た DNA断片を化学的変性剤の濃度勾配や温度勾配を有するゲルを用レ、て電気泳 .動する。増幅した DNA断片はゲル内を一本鎖に変性する位置まで移動し、変性後は 移動しなくなる。変異がある場合となレ、場合では増幅した DNAのゲル内での移動が 異なることから、変異の存在を検出できる。検出感度を上げるにはそれぞれのプライ マーにポリ(G:C)端末を付けるとよい。
[0145] また、検体由来 DNAあるいは検体由来 cDNAの塩基配列を直接的に決定し、解析 することにより、マイクロ RNAやマイクロ RNA前駆体等の変異を検出することもできる
6.本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸を発現させる方法
本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸は、該核酸をコードする発 現ベクターを用いることにより発現させることができる。
[0146] 発現ベクターとしては、宿主細胞において自立複製可能もしくは染色体中への組 込みが可能で、本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸の遺伝子を 転写できる位置にプロモーターを含有してレ、るプラスミド、ウィルスベクター等が好ま しく用レ、られる。プロモーターとしては、宿主細胞中で発現できるものであれば、いか なるものでもよぐ例えば、 RNA polymerase iKpol II)系プロモーターや U6 RNAや HI RNAの転写系である RNA polymerase IlKpol III)系プロモータ二等をあげることができ . る。 pol II系プロモーターとしては例えば、サイトメガロウィルス(ヒト CMV)の IE(immedia te early)遺伝子のプロモーター、 SV40の初期プロモーター等をあげることができる。 それらを用いた発現ベクターとして、例えば、 PCDNA6.2- GW/miR(Invitrogen社製) pSilencer 4.1-CMV(Ambion社製)等を例示することができる。 pol III系プロモーター としては U6.RNAや HI RNAあるいは tRNAのプロモータ一をあげることができる。それ らを用いた発現ベクターとして、例えば、 SINsi-hHl DNA (タカラバイオ社製)、 pSINs i-hU6 DNA (タカラバイオ社製)、 pENTR/U6 (Invitrogen社製)等をあげることができる 。また試験管内でマイクロ RNAやマイクロ RNA前駆体等を発現させる場合には、 T7 プロモーター、 T3プロモーターもしくは SP6プロモーターを有する発現べクタ一が好ま
しく用レ、られる。これらを有するベクターとして、例えば pBluescript II SK (+) (Stratagen e社製)等をあげることができる。 .
[0147] プラスミドを用レ、る場合、本発明のマイクロ RNAやマイクロ RNA前駆体等の塩基配 列あるレ、は、その塩基配列を含むゲノムの塩基配列をもとに、ヘアピン部分を含む D NA断片を調製し、プラスミドのプロモーター下流に挿入して組換えプラスミドを造成し た後、該プラスミドを、該プラスミドに適合した宿主細胞に導入するか、試験管内で R NAポリメラーゼゃヌクレオチドなどと混合することにより、本発明のマイクロ RNAやマ イク口 RNA前駆体等の核酸を発現させることができる。
[0148] ウィルスベクターを用いる場合、本発明のマイクロ RNAやマイクロ RNA前駆体等の 核酸の塩基配列を含む遺伝子をウィルスベクター内のプロモーター下流に揷入して 組換えウィルスベクターを造成し、該ベクタ一をパッケージング細胞に導入して皡換 えウィルスを生産して、マイクロ RNAやマイクロ RNA前駆体等の核酸の遺伝子を発 現させることもできる。
[0149] パッケージング細胞は、ウィルスのパッケジーングに必要な蛋白質をコードする遺 伝子のレ、ずれかを欠損してレ、る組換えウィルスベクターの、該欠損する蛋白質を補 給できる細胞であればいずれの細胞もよぐ例えばヒト腎臓由来の HEK293細胞、マ ウス繊維芽細胞 NIH3T3由 *の細胞などを用いることができる。パッケージング細胞 で補給する蛋白質としては、レトロウイルスベクタ一の場合はマウスレトロウイルス由来 の gag, pol, envなどの蛋白質力 レンチウィルスベクターの場合は HIVウィルス由来の gag, pol, env, vpr, vpu, vif, tat, rev, neぬどの蛋白質、アデノウイルスベクターの場 合はアデノウイルス由来の ΕΙΑ,ΕΙΒなどの蛋白質、また、アデノ随伴ウィルスベクター の場合は Rep(p5, pl9, p40), Vp(Cap)などの蛋白質を用いることができる。 、
[0150] 発現ベクターを用レ、る以外にも、本発明のマイクロ RNAやマイクロ RNA前駆体等 の核酸を、ベクターを用いずに直接細胞に導入することもできる。本手法に用いる核 酸は DNAや RNA、あるいはヌクレオチド類似体の他、これらのキメラ分子、あるいは該 核酸の誘導体も用いることができる。具体的には、 Pre-miR™ miRNA Precursor Mole cules (Ambion社製)や miRIDIAN microRNA Mimics (GEヘルスケア社製)を用いること ができる。
7.本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸の発現または機能を促進 或レ、は抑制または促進する方法
本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸は、アンチセンス技術レくィ ォサイエンスとインダストリ一, 50, 322 (1992)、化学, .46, 681 (1991), Biotechnology, 9, 358 (1992)、 Trends in Biotechnology, 10, 87 (1992)、 Trends in Biotechnology, 1 0, 152 (1992)、細胞工学, 16, 1463 (1997)]、トリプル.ヘリックス技術 [Trends in Biote chnology, 10, 132 (1992)]、リボザィム技術 [Current Opinion in Chemical Biology, 3, 274 (1999)、 FEMS Microbiology Reviews, 23, 257 (1999)、 Frontiers in Bioscience, 4 , D497 (1999)、 Chemistry & Biology, 6, R33 (1999)、 Nucleic Acids Research, 26, 52 37 (1998)、 Trends In Biotechnology, 16, 438 (1998)]、デコイ DNA法 [Nippon Rinsho - Japanese Journal of Clinical Medicine, 56, 563 (1998)、 Circulation Research, 82, 1 023 (1998)、 Experimental Nephrology, 5, 429 (1997) Nippon Rinsho - Japanese Jou rnal of Clinical Medicine, 54, 2583 (1996)]、あるいは siRNA (short interfering RNA) を用いて、その発現または機能を抑制することができる。
[0151] アンチセンスとは、ある標的核酸の塩基配列に相補的な塩基配列を有する核酸を 塩基配列特異的にハイブリダィゼーシヨンさせ、該標的核酸の発現または機能を抑 制できるものをいう。アンチセンスに用レ、る核酸は DNAや RNAまたはヌクレオチド類似 体の他、これらのキメラ分子、あるいは該核酸の誘導体も用いることができる。具体的 には、 Nature 432, 226 (2004)等に記載の方法に従うことでアンチセンスを作製し、発 現または機能を抑制することができる。具体的には、 Anti-miR™ miRNA Inhibitors (A mbion社製)や miRIDIAN microRNA Inhibitors (GEヘルスケア社製)を用いることによ り本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸の発現または機能を抑制 すること力できる。 '
[0152] siRNAとは、ある標的核酸の塩基配列を含む短い二本鎖 RNAであり、 RNA干渉(RN Ai)により、該標的核酸の発現または機能を抑制できるものをいう。 siRNAの配列は、 標的とする塩基配列から文献 [Genes Dev., 13, 3191 (1999)]の条件に基づいて適宜 設計することができる。選択した 17〜30塩基、好ましくは 18〜25塩基、より好ましく は 19〜23塩基の配列および相補的な配列それぞれの 3'端に TTを付加した配列を
有する 2本の RNAを核酸合成機により合成し、アニーリングすることにより siRNAを作 製できる。また、 pSilencer 1.0-U6 (Ambion社製)、 pSUPER(01igoEngine社)等の siR NA発現用ベクターに上記の選択した 17〜30塩基、好ましくは 18〜25塩基、より好 ましくは 19〜23塩基の配列に相当する DNAを挿入することにより、該遺伝子の発現 または機能を抑制できる siRNAを発現するベクターを作製することができる。
[0153] 肥満細胞、間葉系幹細胞または癌細胞で発現するマイクロ RNAやマイクロ RNA 前駆体に特異的なアンチセンスまたは siRNAを用いて、肥満細胞、間葉系幹細胞ま たは癌細胞で発現するマイクロ RNAやマイクロ RNA前駆体の発現または機能の抑 制を行うことができる。すなわち、該マイクロ RNAに特異的なアンチセンスまたは siRN Aを投与することにより該マイクロ RNAの発現または機能を抑制し、肥満細胞、間葉 系幹細胞または癌細胞におけるマイクロ RNAやマイクロ RNA前駆体の作用を制御 することができる。
[0154] 具体的な一例をあげると、配列番号が 1、 2、 3、 8、 14、 20、 22、 25、 32または 36 のレヽずれ力、で表されるマイクロ RNAもしくは酉己歹 IJ番号カ 1337、 1338、 1339、 1352 、 1363、 1371、 1373、 1377、 1386また fま 1390のレヽずれ力で表されるマイクロ R NA前駆体に特異的なアンチセンスまたは siRNAは肥満細胞の脱顆粒抑制剤として 用レ、ることができる。また、配列番号が 1、 8、 21または 36で表されるマイクロ RNAも しくは配列番号が 1337、 1352、 1372または 1390のいずれかで表されるマイクロ R NA前駆体に特異的なァ/チセンスまたは siRNAは間葉系幹細胞の増殖抑制剤また は増殖促進剤として用いることができる。さらに、配列番号が 1、 3、 8、 20、 21、 22、 32または 36のいずれかで表されるマイクロ RNAもしくは配列番号が 1337、 1339、 1352、 1371、 1372、 1373、 1386また ίま 1390のレヽずれ力で表されるマイクロ RN Α前駆体に特異的なアンチセンスまたは siRNAは細胞増殖保進剤として用レ、ることが できる。
[0155] また、肥満細胞、間葉系幹細胞または癌細胞で発現するマイクロ RNAやマイクロ R NA前駆体の発現異常による患者の場合、該マイクロ RNAやその前駆体に特異的 なアンチセンスまたは siRNAを患者に投与することにより、肥満細胞、間葉系幹細胞 または癌細胞の機能を制御し、上記発現異常により発症する疾患の治療をすること
力 sできる。すなわち、該マイクロ RNAまたはその前駆体に特異的なアンチセンスまた は siRNAは、肥満細胞、間葉系幹細胞の異常に起因する疾患または細胞の増殖異 常に起因する疾患の治療剤として有用である。
[0156] 該マイクロ RNAまたはその前駆体に特異的なアンチセンスまたは siRNAを上記治 療剤として使用する場合は、アンチセンスまたは siRNAを単独、あるレ、はレトロウィル スベクター、アデノウイルスベクター、アデノ随伴ウィルスベクターなどの適当なベクタ 一に挿入した後、下記 11.に記載した常法に従って医薬製剤とし、投与することがで きる。
一方、本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸の発現または機能を 促進する物質としては、該マイクロ RNAやマイクロ RNA前駆体、それらと標的塩基 配列が同様であるマイクロ RNAやマイクロ RNA前駆体、およびこれらをコードする発 現ベクターの他、マイクロ RNA前駆体のプロセシングに関与する Dicer等の因子があ げられる。マイクロ RNAやマイクロ RNA前駆体等をコードする発現ベクターは、前記 6.であげられた方法により作成することができる。
[0157] 肥満細胞、間葉系幹細胞または癌細胞で発現するマイクロ RNAやマイクロ RNA 前駆体、これらと標的塩基配列が同様であるマイクロ RNAやマイクロ RNA前駆体、 およびこれらをコードする発現ベクターを用いて、肥満細胞、間葉系幹細胞または癌 細胞で発現するマイクロ RNAやマイクロ RNA前駆体の発現または機能の促進を行 うことができる。すなわち、これらを投与することにより該マイクロ RNAの発現または機 能を促進し、肥満細胞、間葉系幹細胞または癌細胞におけるマイクロ RNAやマイク 口 RNA前駆体の作用を制御することができる。 ,
[0158] 具体的な一例を げると、配列番号が 1、 2、 3、 8、 14、 20、 22、 25、 32または 36 のいずれ力で表されるマイクロ RNAもしくは酉己歹 IJ番号力 337、 1338、 1339、 1352 、 1363、 1371、 1373、 1377、 1386また ίま 1390のレヽずれ力で表されるマイクロ R ΝΑ前駆体、これらと標的塩基配列が同様であるマイクロ RNAやマイクロ RNA前駆 体、およびこれらをコードする発現ベクターは肥満細胞の脱顆粒促進剤として用いる こと力;できる。また、配列番号が 1、 8、 21または 36のいずれかで表されるマイクロ RN Αもしくは配列番号が 1337、 1352、 1372または 1390のいずれかで表されるマイク
口 RNA前駆体、これらと標的塩基配列が同様であるマイクロ RNAやマイクロ RNA前 駆体、およびこれらをコードする発現ベクターは間葉系幹細胞の増殖促進剤または 増殖抑制剤として用いることができる。さらに、配列番号が 1、 3、 8、 20、 21、 22、 32 または 36のいずれか 表されるマイクロ RNAもしくは配列番号が 1337、 1339、 13 52、 1371、 1372、 1373、 1386また iil390のレヽずれ力で表されるマイクロ RNA前 駆体、これらと標的塩基配列が同様であるマイクロ RNAやマイクロ RNA前駆体、お よびこれらをコードする発現ベクターは細胞の増殖抑制剤として用レ、ることができる。
[0159] 肥満細胞、間葉系幹細胞または癌細胞で発現するマイクロ RNAやマイクロ RNA 前駆体の発現異常による患者の場合、該マイクロ RNAやその前駆体、これらをコー ドする発現べクタ一、これらと標的塩基配列が同様であるマイクロ RNAやマイクロ RN A前駆体、およびこれらをコードする発現ベクターを患者に投与することにより、肥満 細胞、間葉系幹細胞または癌細胞の機能を制御し、上記発現異常により発症する疾 患の治療をすることができる。すなわち、該マイクロ RNAまたはその前駆体、これらを コードする発現ベクター、これらと標的塩基配列が同様であるマイクロ RNAやマイク 口 RNA前駆体、およびこれらをコードする発現ベクターは、肥満細胞、間葉系幹細 胞の異常に起因する疾患または細胞の増殖異常に起因する疾患の治療剤として有 用である。
[0160] 該マイクロ RNAまたはその前駆体、およびこれらをコードする発現ベクターを上記 治療剤として使用する場合は、該マイクロ RNAまたはその前駆体、およびこれらをコ ードする発現べクタ一を単独、あるいはレトロウイルスベクタ一、アデノウイルスベクタ 一、アデノ随伴ウィルスベクターなどの適当なベクターを用レ、、下記 11.に記載した 常法に従って医薬製剤とし、投与することができる。
8.本発明のマイクロ RNA等の核酸の標的遺伝子の発現を抑制または促進する方 本発明のマイクロ RNA等の核酸の標的遺伝子の発現を抑制する方法としては、標 .的遺伝子の発現を抑制する方法であれば、いかなる方法でもよい。例えば、本発明 のマイクロ RNAやマイクロ RNA前駆体等の核酸を発現させもしくは投与し、細胞内 のマイクロ RNAの量を増加させることにより、標的配列を有する mRNAの発現を抑制
し、標的遺伝子の発現を抑制する方法をあげることができる。なお、本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸を発現させるには、上記 6.で記載した方法に より行なうことができる。
[0161] 本発明のマイクロ RNA等の核酸の標的遺伝子の発現を促進する方法としては、標 的遺伝子の発現を促進する方法であれば、レ、かなる方法でもよい。例えば、本発明 のマイクロ RNAやマイクロ RNA前駆体等の核酸に対するアンチセンスや siRNAを発 現させもしくは投与することにより、マイクロ RNAやマイクロ RNA前駆体等の発現ま たは機能を抑制し、その標的遺伝子の発現を促進する方法をあげることができる。了 ンチセンスや siRNAは、上記 7.で記載した方法により作製することができる。
[0162] 配列番号 1〜; 1336のいずれかで表される塩基配列力 なるマイクロ RNAの標的 遺伝子としては、例えば、それぞれ前述の表 2で示される遺伝子群を例示することが できる。
9.本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸を用いて細胞を分離する 雄 .
生体内力 取り出した各種細胞から、本発明のマイクロ RNAやマイクロ RNA前駆 体等の核酸を発現する細胞を分離する方法としては、該マイクロ RNAやマイクロ RN A前駆体等の核酸の塩基配列と相補的な塩基配列を有する核酸を蛍光標識したプ ローブを細胞に導入し、マイクロ RNAやマイクロ RNA前駆体等の核酸とハイブリダィ ゼーシヨンさせ、標識プロ ^"ブとハイブリダィゼーシヨ した細胞のみを、ソーティング 機能を有したフローサイトメーターで分離することにより、行うことができる。
[0163] 蛍光標識プローブとしては、ハイブリダィゼーシヨンした時に特異的な蛍光を発する ものであれば、いかなるものでもよぐ例えば、モレキュラービーコン [Biochimica et Bi ophysica Acta, 1479, 178 (1998)]や FRET[Proc.Natl.Acad.Sci. USA, 103, 263 (2006 )]等があげられる。
モレキュラービーコンは、一方の末端に蛍光官能基を共有結合により導入し、もう一 方の末端に蛍光消光を引き起こすダブシル基等を導入した核酸で、通常の水溶液. 中ではヘアピン構造をとるように塩基配列が設計されている。両末端に導入した蛍光 官能基と蛍光消光団は互いに隣接するためプローブ単独では蛍光が観 されない
力 本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸とハイブリダィゼーシヨン すると蛍光官能基と蛍光消光団が引き離され、強い蛍光が観測できる。
[0164] FRETとは、 2種以上の蛍光官能基間の分子励起エネルギー移動現象である。具体 的にはエネルギー供与体を末端に導入した核酸プローブとエネルギー受^体を末 端に導入した核酸プローブの 2種を用意する。 2つのプローブの塩基配列は、マイク 口 RNAやマイクロ RNA前駆体等の核酸とハ^ブリダィゼーシヨンした後に導入した 2 つの蛍光官能基が近接するように設計すると、プローブ単独では供与体の発光のみ が観測される力 本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸とプローブ がハイブリダィゼーシヨンを引き起こすと、 2つの: /ローブが近接するため、供与体の エネルギーが受容体に移動し、受容体に基づく発光が主として観測できる。
[0165] ソーティング機能を有したフローサイトメーターによる細胞の分離の方式としては、 水電荷方式、セルキヤプチヤー方式などがあげられる(フローサイトメーター自由自在 、 pl4-23、秀潤社、 1999年)。どちらの方法も細胞の蛍光測定を行い、蛍光強度を電 気信号に変換することにより蛍光強度を定量し、その量に応じて細胞を分離すること ができる。具体的には、 BD FACS Ariaセルソーター(べクトン'ディッキンソン社製)や EPICS ALTRA HyPerSort (ベックマン'コールター社製)などを用いて蛍光を測定し、 細胞を分離することができる。
. 10.本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸の発現または機能を促 進或いは抑制させる物質をスクリーニングする方法
本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸を用いて、該マイクロ RNA やその前駆体の発現または機能を促進或いは抑制させる物質をスクリーニングする ことができる。例えば、本発明のマイクロ RNAおよびマイクロ RNA前駆体の塩基配 列から、スクリーニングの標的とする塩基配列を選択して、該塩基配列を有する核酸 を発現する細胞を利用して、選択したマイクロ RNAまたはその前駆体の発現または 機能を促進または抑制させる物質をスクリーニングすることができる。
[0166] スクリーニングに用いる、マイクロ RNAおよびマイクロ RNA前駆体の塩基配列を有 する核酸を発現する細胞としては、肥満細胞、間葉系幹細胞または癌細胞のほか、 上記 6で記載したように、該塩基配列を有する核酸を発現するベクターを動物細胞や
酵母などの宿主細胞に導入して得られる形質転換細胞や、該塩基配列を有する核 酸をベクターを用いずに直接導入した細胞等を用レ、ることもできる。
[0167] 具体的なスクリーニング方法としては、(a)スクリーニングの標的とするマイクロ RNA またはその前駆体の発現量の変化を指標にする方法 他、マイクロ RNAは標的配 列を有する mRNAの翻訳を抑制するため、(b)スクリーニングの標的とするマイクロ R NAまたはその前駆体の標的配列を有する mRNAの発現量の変化を指標にする方法 があげることができる。
(a)スクリーニングの標的とするマイクロ RNAまたはその前駆体の発現量の変化を指 標にするスクリーニング方法
該塩基配列を有する核酸を発現する細胞に対し、試験物質を接触させ、選択した 核酸の発現量の変化を指標に、マイクロ RNAやその前駆体の発現を促進または抑制 させる物質を る。核酸の発現量は、上記 4.で記載した方法により検出することがで きる。
(b)スクリーニングの標的とするマイクロ RNAまたはその前駆体の標的配列を有する mRNAの発現量の変化を指標にするスクリーニング方法
該塩基配列を有する核酸を発現する細胞に対し、試験物質を接触させ、選択した . 核酸の標的配列を有する mRNA発現量の変化を指標に、マイクロ RNAやその前駆 体の発現または機能を促進または抑制させる物質を得る。または、本発明の塩基配 列を有する一本鎖 RNAに対する標的配列を、適当なレポーター遺伝子発現ベクター め 3' UTRに挿入した DNAを作製して、発現べクタ一に適合した宿主細胞に導入し、 その細胞に試験物質を接触させ、.レポーター遺伝子の発現量の変化を指標に、マイ クロ RNAやその前駆体の発現または機能を促進または抑制させる物質を得る。
[0168] 標的配列の選択は、上記に記載した方法により行なうことができ、配列番号 1〜: 13 36でレ、ずれかで表される塩基配歹 IJからなるマイクロ RNAの標的遺伝子としては、例 えば、それぞれ前述の表 2で示される遺伝子群を例示することができる。
Ί Ί . 月の 》 する ^ および?台 藝
本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸、および、それらの塩基配 列と相補的な塩基配列を有する核酸は、その標的遺伝子や本発明の核酸の発現を
制御することにより、肥満細胞、間葉系幹細胞の異常等に起因する疾患、または細 胞の増殖異常に起因する疾患の治療薬として利用することができる。また本発明の 核酸は、本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸の定量または変異 の検出により、肥満細胞、間葉系幹細胞の異常等に起因する疾患、または細胞の増 殖異常に起因する疾患の診断薬として利用することができる。
[0169] 肥満細胞の異常としては、肥満細胞の分化や脱顆粒、炎症性メディエーター産生 、サイト力イン産生、ケモカイン産生等の異常が挙げられ、それに起因する疾患として 、アトピー性皮膚炎、喘息、慢性閉塞性肺疾患、アレルギー性疾患等をあげることが できる。間葉系幹細胞の異常としては、増殖または分化の異常等があげられ、それに 起因する疾患として、癌、骨形成不全症、軟骨形成不全症、糖尿病等をあげることが できる。細胞の増殖異常に起因する疾患としては、癌及び、細胞の異常増殖や組織 の過形成等が原因となってレ、る動脈硬化、慢性関節リウマチ、前立腺肥大症、経皮 的経血管的冠動脈形成術後の血管再狭窄、肺線維症、糸球体腎炎、自己免疫疾患 等をあげることができる。 '
[0170] 治療薬や診断薬としての具体的な一例をあげると、配列番号力 〜1336のいずれ かで表されるマイクロ RNAもしくは配列番号が 1337〜2851のいずれかで表される マイクロ RNA前駆体、並びにそれらの塩基配列と相補的な塩基配列を有する核酸 は肥満細胞の異常に起因する疾患の診断薬または治療薬として用いることができる .。また、配列番号が 1、 8、 21または 36のいずれかで表されるマイクロ RNAもしくは配 歹 IJ番号力 1337、 1352、 1372または 1390のレ、1 fれカ^ C表されるマイクロ RNA前駆 体、並びにそれらの塩基配列と相補的な塩基配列を有する核酸は間葉系幹細胞の 増殖および/または分化の異常に起因する疾患の診断薬または治療薬として用いる こと力 Sできる。さらに、酉己歹 IJ番号力 1、 3、 8、 20、 21、 22、 32または 36のレ、ずれ力で 表されるマイクロ RNAもしくは酉己歹 IJ番号力 1337、 1339、 1352、 1371、 1372、 137 3、 1386または 1390のいずれかで表されるマイクロ RNA前駆体、並びにそれらの 塩基配列と相補的な塩基配列を有する核酸は細胞の増殖異常に起因する疾患の診 断薬または治療薬としで用レ、ることができる。 -
[0171] 本発明の核酸を含有する診断薬は、目的の診断法に応じて、本発明のマイクロ RN
Aやマイクロ RNA前駆体等の核酸の定量あるいは変異の検出を行うために必要な 試薬、例えば緩衝剤、塩、反応用酵素、本発明のマイクロ RNAやマイクロ RNA前駆 体等の核酸と結合する標識された蛋白、および検出用発色剤等を含んでもょレ、。 本発明の核酸または、その塩基配列と相補的な塩基配列を有する核酸を有効成分 として含有する医薬は、単独で投与することもできるが、通常は薬理学的に許容され る 1つあるレ、はそれ以上の担体と一緒に混合し、製剤学の技術分野にぉレ、てよく知ら れる任章の方法により製造した医薬製剤として投与するのが望ましい。
[0172] 投与経路は、治療に際し最も効果的なものを使用するのが望ましぐ経口投与、ま . たは口腔内、気道内、直腸內、皮下、筋肉内および静脈内などの非経口投与をあげ ' ることができ、望ましくは静脈内投与をあげることができる。
投与形態としては、噴霧剤、カプセル剤、錠剤、顆粒剤、シロップ剤、乳剤、座剤、 注射剤、軟膏、テープ剤などがあげられる。
[0173] 経口投与に適当な製剤としては、乳剤、シロップ剤、カプセル剤、錠剤、散剤、顆粒 剤など力あげられる。
乳剤およびシロップ剤のような液体詾製物は、水、ショ糖、ソルビトール、果糖など の糖類、ポリエチレングリコール、プロピレングリコールなどのグリコール類、ごま油、 オリ一ブ油、大豆油などの油類、 P-ヒドロキシ安息香酸エステル類などの防腐剤、スト 口べリーフレーバー、ペパーミントなどのフレーバー類などを添加剤として用いて製造 できる。
[0174] カプセル剤、錠剤、散剤、顆粒剤などは、乳糖、ブドウ糖、ショ糖、マンニトールなど の賦形剤、デンプン、アルギン酸ナトリウムなどの崩壊剤、ステアリン酸マグネシウム、 タルクなどの滑沢剤、ポリビニルアルコール、ヒドロキシプロピルセルロース、ゼラチン などの結合剤、脂肪酸エステルなどの界面活性剤、グリセリンなどの可塑剤などを添 加剤として用いて製造できる。
[0175] 非経口投与に適当な製剤としては、注射剤、座剤、噴霧剤など力けあげられる。
注射剤は、塩溶液、ブドウ糖溶液あるいは两者の混合物力 なる担体などを用いて 調製される。座剤はカカオ脂、水素化脂肪またはカルボン酸などの担体を用いて調 製される。また、噴霧剤は受容者の口腔および気道粘膜を刺激せず、かつ有効成分
を微細な粒子として分散させ吸収を容易にさせる担体などを用レ、て調製される。
[0176] 担体として具体的には乳糖、グリセリンなどが例示される。本発明の核酸、さらには ' 用レ、る担体の性質により、エアロゾル、ドライパウダーなどの製剤が可能である。また
、これらの非経口剤におレ、ても経口剤で添加剤として例示した成分を添加することも できる。
投与量または投与回数は、目的とする治療効果、投与方法、治療期間、年齢、体 重などにより異なる力 通常成人 1日当たり 10 μ g/kg〜20 mg/kgである。
[0177] また、本発明の核酸または、その塩基配列と相補的な塩基配列を有する核酸を有 効成分として含有する治療薬は、それらの核酸を発現するベクターと核酸治療薬に 用レ、る基剤とを調合することにより製造することもできる [Nature Genet., 8, 42(1994)] 核酸治療剤に用いる基剤としては、通常注射剤に用いる基剤であればどのようなも のでもよぐ蒸留水、塩化ナトリウム又は塩化ナトリウムと無機塩との混合物等の塩溶 液、マンニト^ "ル、ラタトース、デキストラン、グルコース等の溶液、グリシン、アルギニ ン等のアミノ酸溶液、有機酸溶液又は塩溶液とグルコース溶液との混合溶液等があ げられる。また常法に従い、これらの基剤に浸透圧調整剤、 pH調整剤、ゴマ油、ダイ ズ油等の植物油又はレシチンもしくは界面活性剤等の助剤を用いて、溶液、懸濁液
、分散液として注射剤を調製してもよい。これらの注射剤を、粉末化、凍結乾燥等の 操作により用時溶解用製剤として調製することもできる。本発明の治療剤は、治療の 直前に液体の場合はそのままで、固体の場合は必要により滅菌処理をした上記の基 剤に溶解して治療に使用することができる。
[0178] 本発明の核酸をコードするベクターは、上記 6.で作製した組換えウィルスベクター をあげることができ、より具体的には、レトロウイルスベクター及ぴレンチウィルスベクタ —等をあげることができる。
例えば、本発明の核酸をコードするベクターを、アデノウイルス ·へキソン蛋白質に 特異的なポリリジンーコンジュゲート抗体と組み合わせてコンプレックスを作製し、得 られたコンプレックスをアデノウイルスベクタ一に結合させることにより、ウィルスベクタ 一を調製することができる。該ウィルスベクタ一は安定に目的の細胞に到達し、エンド
ソームによる細胞内に取り込まれ、細胞内で分解され核酸を効率的に発現させること ができる。
[0179] また、(-)鎖 RNAウィルスであるセンダイウィルスをベースにしたウィルスベクターも開 発されており (W097/16538、 W097/16539)、当該センダイウィルスを用いて、本発 明のマイクロ RNAやマイクロ RNA前駆体等の核酸を組み込んだセンダイウィルスを 作製することができる。
本発明の核酸やこれをコードするベクターは、非ウィルス核酸移入法によっても移 入することができる。例えば、リン酸カルシウム共沈法 [Virology, 52, 456-467^(1973) ; Science, 209, 1414-1422 (1980)]、マイクロインジェクション法 [Proc.Natl.Acad.Sci. US A, 77, 5399-5403 (1980) ; Proc.Natl.Acad.Sci. USA, 77, 7380-7384 (1980) ; Cell, 27,
223-231 (1981) ; Nature, 294, 92-94 (1981)]、リボソームを介した膜融合-介在移入 法 [Proc.Natl.Acad.Sci. USA, 84, 7413-7417 (1987) ; Biochemistry, 28, 9508—9514 ( 1989) ; J. Biol. Chem" 264, 12126-12129 (1989) ; Hum. Gene Ther" 3, 267-275, (19 92) ; Science, 249, 1285-1288 (1990) ; Circulation, 83, 2007-2011 (1992)]あるいは直 接 DNA取り込みおよび受容体-媒介 DNA移入法 [Science, 247, 1465-1468 (1990) ; J.
Biol. Chem., 266, 14338-14342 (1991); Proc.Natl.Acad.Sci. USA, 87, 3655-3659 ( 1991) ; Biol. Chem., 264, 16985—16987 (1989) ;BioTechniques, 11, 474-485 (1991 ) ; Proc.Natl.Acad.Sci. USA, 87, 3410-3414 (1990) ; Proc.Natl.Acad.Sci. USA, 88, 4 255-4259 (1991) ; Proc.Natl.Acad.Sci. USA, 87, 4033-4037 (1990) ;Proc. Natl. Acad. Sci. USA, 88, 8850-8854 (1991) ; Hum. Gene Ther., 3, 147-154 (1991)]等により移 : Λすることができる。
[0180] リボソームを介した膜融合—介在移入法は、リボソーム調製物を目的とする組織に 直接投与することにより、本発明の核酸やこれをコードするベクターを当該組織の局 所に取り込み、'および発現させることができる [Hum. Gene Ther., 3, 399 (1992)]。 DN Aを病巣に直接ターゲッティングするには、直接 DN'A取り込み技術が好ましレ、。
受容体一媒介 DNA移入は、例えば、ポリリジンを介して、蛋白質リガンドに DNA (通 常、共有的に閉環したスーパーコイルィ匕プラスミドの形態をとる)を結合することによ つて行う方法をあげることができる。リガンドは、目的細胞または組織の細胞表面上の
対応するリガンド受容体の存在に基づいて選択する。当該リガンド— DNAコンジュゲ ートは、所望により、血管に直接注射することができ、受容体結合および DNA—蛋白 質コンプレックスの内在化が起こる標的組織に指向し得る。 DNAの細胞内破壊を防 止するために、アデノウイルスを同時感^させて、エンドソーム機能を崩壊させること もできる。
12.肥満細胞の活性化の程度を測定する方法
ある核酸が肥満細胞に対し、活性化抑制、脱顆粒抑制、炎症性メディエーター産 生抑制、サイト力イン産生抑制およびケモカイン産生抑制のうちの少なくとも 1つの作 用を有していることは、例えば、本発明のマイクロ RNAやマイクロ RNA前駆体等の 核酸、更には該マイクロ RNAの標的遺伝子に対するアンチセンスや siRNAなどを肥 満細胞に導入し、 IgEを添加して培養した後、抗 IgE抗体の添加等によりヒト肥満細胞 を活性化し、放出された (i)脱顆粒の指標となるヒスタミンや β一^ ~キゾサミニダーゼ、 ( ii)LTC4、 LTD4、 LTE4、 PGD2等の炎症性メディエーター、(iii)TNF- αや GM- CSF等 のサイト力イン、(iv)IL- 8、 1-309、 MIP-1 α等のケモカイン等を測定し、何も導入しなか つた場合と比較することにより確認できる。このように肥満細胞の活性化は脱顆粒だ , けでなく、 TNF- aや GM- CSF等のサイト力イン産生、 IL- 8、 1-309、 MIP-1 α等のケモ 力イン産生、 LTC4、 LTD4、 LTE4、 PGD2等の炎症メディエーター産生等を測定する ことによつても調べることができる [Blood, 100, 3861 (2002) 1
[0181] また本発明のマイクロ RNAやマイクロ RNA前駆体等の核酸、更には該マイクロ RN Aの標的遺伝子に対するアンチセンスや siRNAなどがアポトーシスの誘導作用を有し てレ、ることは、これらを肥満細胞に導入し、クロマチン DNAの断片化の測定や TUNEL 法等による測定を行うことにより検出できる。
ΐ 3.間 榦細朐の増殖および骨芽細胞への分化および評 ¼方法
間葉系幹細胞は、安全かつ効率的に取得される方法であれば特に限定されない 、ヒト骨髄力 取得する方法としては、例えば S. E. Haynesworth et al. Bone, 13, 8 1 (1992)に記載の方法があげられる。
[0182] 胸骨または腸骨において、骨髄穿刺を行う場所の皮膚を消毒し、特に骨膜下を十 分に局所麻酔する。骨髄穿刺針の内筒を抜き、 5,000 unitsのへパリンを入れた 10 ml
注射器を装着して必要量、平均的には 10 ml〜20 mlの骨髄液を吸引する。骨髄穿刺 針を取り外し、 10分間程度圧迫止血する。取得した骨髄液を 1,000 X gで遠心分離し て骨髄細胞を回収した後、該骨髄細胞をリン酸緩衝液 (phosphate- buffered saline) (P BS)で洗浄する。遠心分離'洗浄を 2回繰り返した後、骨髄細胞を 10%のゥシ胎仔血清 (FBS)を含む a— MEM ( a -modified MEM), DME (Dulbecco's modified MEM), IM DM (Isocove's modified Dulbecco's medium)等の細胞培養用培地に浮遊させること により骨髄細胞液を得る。骨髄細胞液から間葉系幹細胞を単離する友法としては、 骨髄細胞液中に混在する他の細胞、例えば血球系細胞、造血幹細胞、血管幹細胞 、線維芽細胞等を除去することができる方法であれば特に限定されないが、例えば M . F. Pittenger et al. Science, 284, 143-147 (1999)に記載の方法があげられる。骨髄 細胞液を密度 1.073 g/mlの Percollに重舉した後、 1, 100 X gで 30分間遠心分離し、界 面の細胞を間葉系幹細胞として単離することができる。また、骨髄細胞液に 10倍濃度 の PBSを加えて 9/10に希釈した Percollを同容量カ卩えて混合した後に、 20,000 X gで 30 分間遠心分離し、密度 1.075〜1.060の画分の細胞を間葉系幹細胞として単離するこ ともできる。 .
また、ヒトの骨髄に由来する間葉系幹細胞は、 Cambrex社、タカラバイオ社より購入 することもできる。 '
ヒト臍帯から間葉系幹細胞を取得する方法としては、例えば Stem Cells, 21, 105-11 0 (2003)に記載された方法があげられる。臍帯静脈の両端に力ニューレを揷入し、適 当な緩衝液、例えば、 EBSS(Earle's balanced salt solution)で洗浄する。蛋白質分解 酵素、例えば、 0.1%コラゲナ一ゼを含む 199培地に抗生物質を添加して血管に注入 し、 4〜40 °C、好ましくは 37 °Cで、 1〜60分間インキュベートする。血管を EBSSで洗 浄し、臍帯を軽くマッサージした後、内皮細胞および内皮下層細胞の懸濁液を回収 - する ό該懸濁液を 600 X gで 10分間遠心分離し、得られた細胞を、例えば、低濃度の グルコースを含む DMEM培地(DMEM-LG、 Gibco)に、 20 mM HEPES、 100 units/ml ペニシリン、 100 g/mlストレプトマイシン、 2 mM L-グルタミン、 1 mMピルビン酸ナト リウムおよび 10% FBSを加えた培地に懸濁する。細胞密度を、 102〜106個ん mとして 培養フラスコに接種し、 37 °C、 5% COの条件下で培養する。培地を 1〜7日毎に交
換し、:!〜 3週間培養を継続することにより、間葉系幹細胞を取得することができる。
[0184] 子宮内膜から間葉系幹細胞を取得する方法としては、例えば、 Am.J.Pathol., 163,.
2259-2269 (2003)に記載の方法があげられる。外科手術により摘出されたヒト子宫内 膜組織を細切し、細胞を培養可能な培地、好ましくは a - MEM、 DMEM、 IMDM等に 1 〜20%の動物由来の血清、好ましくは 5〜 10%の FBSを加えた培地で培養する。培 地にはペニシリンやストレプトマイシン等の抗生物質を加えても良レ、。さらに、細胞の 分離を良くするために、 3型コラゲナーゼ等のコラーゲン分解酵素およびデォキシリ ボヌクレアーゼ I等の DNA分解酵素を培地に添加し、 20〜40 °C、好ましくは 37 の 条件で、 10分間〜 5時間、好ましくは 1時間、緩やかに振盪する。個々の子宮内膜腺 を顕微鏡で観察しながら分離し、適当な培養容器、例えば 24-ゥェル培養皿を用いて 37 °C 5% COの条件下で培養することにより、間葉系幹細胞を取得することができ
2
る。
[0185] 歯、歯胚、歯周辺組織から間葉系幹細胞を取得する方法としては、例えば Lancet, 364, 149-155(2004)、 Proc.Natl.Acad.Sci. USA, 97, 13625-13630 (2000)に記載の方 法があげられる。ヒトの歯としては、乳歯、または切歯、犬歯、小臼歯、大臼歯等の永 久歯のいずれでも良い。例えば、抜歯した第三大臼歯 (親知らず)の歯根の表面から 歯周靭帯 (periodontal ligament)を慎重に分離し、コラゲナーゼ、トリプシン、プロナー ゼ、エラスターゼ、デイスパーゼ、ヒアルロニダ一ゼ等の蛋白分解酵素を用いて、 37 °Cで 1時間消化反応を行う。ストレイナー、メッシュ、フィルタ一等を用いて、組織残渣 ' を除くことにより間葉系幹細胞を取得することができる。また、抜歯した第三大臼歯の .表面を PBS等で洗浄した後、セメント質とエナメル質の結合部を切断して髄質を露出 させ、歯冠および歯根力 歯髄組織を慎重に分離し、上記と同様の方法で蛋白分解 酵素処理した後、組織残渣を除くことにより間葉系幹細胞を取得することもできる。
[0186] また、上記以外の間葉系幹細胞の単離方法として、間葉系幹細胞に発現する表面 抗原、間葉系幹細胞特異的な遺伝子のプロモーターおよびェンハンサーを持つレポ 一ターベクターを用いて間葉系幹細胞を単離する方法があげられる。具体的には、 A
C133抗原を用いて幹細胞を単離する方法(US6468794)、 Sox遺伝子(US2002/0135 539)、 Nestin遺伝子または Musashi遺伝子 (特開 2002- 034580)のプロモーターおよび
ェンハンサ一を持つレポーターベクターを用レ、て間葉系幹細胞を単離する方法等が あげられる。
[0187] また、 Hoechst33342の細胞外排出能を指標にした FACS分画法を用いてサイドポピ ユレーシヨン(side population) (SP)中に幹細胞を濃縮させる方法 [Journal of Experime ntal Medicine, 183, 1797-806 (1996)]により幹細胞を分離することもできる。また、 SH 2陽性, SH4陽性, CD29陽性, CD44陽性, CD71陽性, CD90陽性, CD106陽性, CD1 20a陽性, CD124陽性, CD14陰性, CD34陰性,および CD45陰性の細胞を間葉系幹 細胞として、セルソーターや磁気ビーズを用いて分離する方法 [Science, 284, 143 - 14 7 (1999)]を用いることもできる。
[0188] 間葉系幹細胞の培養に用いる培地としては、例えば「組織培養の技術基礎編 第 三版」朝倉書店 (1996)等に記載された細胞培養用培地があげられるが、ゥシゃヒト等 の血清を 1〜20%添加した a - MEM、 DMEM、 IMDM等の細胞培養用培地が好ましく 用いられる。培養条件は、細胞が 養可能な条件であればいかなる条件でもよいが 、培養温度は 33〜37 °Cが好ましぐ 5〜10%の COガスで満たしたインキュベーターで
2
培養することが好ましい。また間葉系幹細胞は、通常の組織培養用のプラスチック製 培養皿に接着させて増殖させることが好ましい。細胞が培養皿一面に増殖する頃、 培地を除去レて、トリプシン EDTA溶液を加えることで細胞を浮遊させる。浮遊させた 細胞は、 PBSまたは細胞培養用の培地で洗浄後、細胞培養用の培地で 2倍から 20倍 に希釈して新しレ、培養皿に播種することで、さらに継代培養することができる。
[0189] ある核酸が間葉系幹細胞の増殖を制御しているかは、例えば、本発明のマイクロ R . NAやマイクロ RNA前駆体等の核酸、更には該マイクロ RNAの標的遺伝子に対す るアンチセンスや siRNA等を間葉系幹細胞に導入し、細胞増殖の程度を陰性対照と 比較することにより確認できる。細胞増殖の程度を測定する方法は後述の 14.で記 載した方法により行うことができる。
[0190] 間葉系幹細胞力、ら骨芽細胞へのへの分化過程における影響を調べる方法としては 、例えば以下のようにして確認する方法があげられる。具体的には、間葉系幹細胞か ら骨芽細胞へ分化を誘導する条件下で、本発明の核酸、マイクロ RNAやマイクロ R NA前駆体、更には該マイクロ RNAの標的遺伝子に対するアンチセンスや siRNA等
を間葉系幹細胞に導入し、培養する。骨芽細胞への分化が進むに伴レ、発現が上昇 する遺伝子または蛋白質を解析し、陰性対照と比較する。
[0191] 間葉系幹細胞から骨芽細胞へ分化誘導させる方法としては、間葉系幹細胞から骨 芽細胞へ分化誘導させることができる方法であればレ、かなる方法でもよいが、例えば 、 Science, 284, 143-147 (1999)に記載の方法があげられる。具体的には、間葉系幹 細胞を培養器に播種した後、デキサメサゾン、ァスコルビン酸— 2リン酸、および J3— グリセ口フォスフェートを含む細胞培養用培地中で 1〜4週間培養を続けることにより 、間葉系幹細胞を骨芽細胞へ分化させることができる。
[0192] 骨芽細胞への分化に伴い発現が上昇する遺伝子の定量的な解析法としては、 RT- PCR (reverse transcription— polymerase chain reaction)、ノ' ~サノプロット角琴 、ドット ブロットハイブリダィゼーシヨン法、 DNAマイクロアレイによる解析等があげられる。 骨芽細胞への分イビに伴レ、発現が上昇する蛋白質の定量的な解析法としては、該 蛋白質に特異的に反応する抗体を用いたウェスタンプロット解析、免疫組織染色、 E LISA等があげられる。
[0193] 骨芽細胞への分化に伴い発現が上昇する遺伝子または蛋白質としては、 I型コラー ゲン、ォステオ力/レシン、ォステオネクチン、ォステオポンチン、ボーンシァロプロティ ン(bone sialoprotein)、 Runx2 (runt— related gene 2)、ァノレカリフォスファターゼ (ALP) 等があげられる。 ' '
また、骨芽細胞への分化程度を評価する方法としては、該骨芽細胞中の ALP酵素 活性を利用して細胞を染色すること、あるいは、 ALP酵素活性を測定する方法があげ られる。該細胞染色のより具体的な方法は、骨芽細胞中の ALP酵素により加水分解 された基質のリン酸エステルのアルコール部分をジァゾニゥム塩でカップリングし、ァ ゾ色素で酵素活性部位に沈殿させる方法があげられる。基質としては、例えばナフト ール AS- MXリン酸を、ァゾ色素としては、例えばファーストバイオレット青をあげること ができる。これらが含まれているキット、例えば leukocyte alkaline phosphatase (Sigma 社製)等を用いてもよい。また、 ALP酵素活性の測定キットとして、例えばアルカリ性ホ スファ B-テストヮコー(和光純薬株式会社製)等を用レ、てもよレ、。
[0194] 更に、骨芽細胞が産生した石灰化成分を検出することによつても骨芽細胞への分
化を確認することもできる。石灰化成分を検出する方法としては、フォンコッサ (von K ossa)染色、ァリザリンレッド (Alizarin Red)染色等の染色法があげられる。
フォンコッサ染色とは、硝酸銀を用いて石灰化成分であるリン酸カルシウムを検出 する方法である。具体的には、パラフィン等で固定した細胞に対し 1〜5%の硝酸銀 水溶液を反応させ光に当て、黒く呈色したリン酸カルシウムが存在する部分を定量、 例えば該呈色面積を計測することにより骨芽細胞への分化程度を評価することがで きる。
[0195] ァリザリンレッド染色とは、ァリザリン赤 Sがカルシウムに対して特異的な結合を示し レーキを形成することを利用した方法である。具体的には、パラフィン等で固定した細 胞に対し 0.01〜5%ァリザリン赤 S溶液を反応させる、赤紫色〜橙赤色に呈色した部 分を定量、例えば該呈色面積を計測することにより骨芽細胞への分化程度を評価す ることができる。
14.癌細胞や他の細胞の増殖を測定する方法
細胞増殖の測定法としては、細胞数や細胞増殖速度を反映する指標を測定できる 方法であれば特に限定されなレ、。生細胞数測定、 DNA合成速度測定、総蛋白質量 測定などを用レ、ることができる。
[0196] 生細胞数を評価する方法としては、細胞中の ATP量を測定する方法があげられる。
細胞中の ATP量は培養下の細胞数と比例関係にあることが知られている I. Immunol. Meth., 160, 81-88 (1993))。細胞中の ATP量測定のより具体的な方法は、 MTT法、 X TT法などが挙げられる (J. Immunol. Meth., 65, 55-63 (1983))。また、 ATP依存性酵 素ルシフェラーゼによるルシフェリン基質の発光にて ATP量を測定する方法もあげら れる。細胞中の ATP量の測定キットとして、例えば Cell Tite「GloR Luminescent Cell viability Assay(Promega社製)等を用いてもよい。
15.癌細胞や仙,の細胞の細 死の程度を測定する方法. .
細胞死の程度を測定する方法としては、死細胞を Propium Iodide等の色素で染色 する方法や、細胞死に伴い細胞外に漏出した酵素の活性を測定する方法等を用い ることができる。後者については、例えば細胞外に漏出したアデニル酸キナーゼの酵 素活性を測定する方法が利用できる。より具体的には、 ToxiLight(R) Non-Destructiv
e Cytotoxicity BioAssay Kit (Lonza社製)等を用いて'もよい。
[0197] また、細胞死の中でも特に癌との関係で重要なアポトーシス(programmed cell deat h)に限定してその程度を測定することもできる。細胞のアポトーシスを評価する方法 としては、 DNAの断片化の程度を測定する方法や、細胞膜の構成脂質の変化を測 定する方法、アポト一シスに伴って誘導される細胞中のプロテアーゼであるカスパー ゼ 3/7活性を測定する方法があげられる。細胞中のカスパーゼ 3/7活性測定のより具 体的な方法は、カスバ一ゼ 3/7活性により遊離されたルシフェリン基質を、ルシフェラ ーゼ酵素反応によるルシフェリン発光にて測定する方法があげられる。細胞中のカス パーゼ 3/7活性の測定キットとして、例えば Caspase_GloR3/7 Assay(Promega社製)等 を用いてもよい。 .
[0198] 以下、実施例により本発明を具体的に説明する。
実施例 1
[0199] ヒト肥満細胞で発現するマイクロ RNAの柚出
(1) RNA抽出
LAD2は最近樹立されたヒト肥満細胞株で、ヒト肥満細胞の性質をよく保持してレ、る ことが知られている [Leuk. Res., 27, 671 (2003); Leuk. Res., 27, 677 (2003)]。そこで 、 LAD2からマイクロ RNAの抽出をおこなった。 LAD2は、 National Institute of Allergy and Infectious Diseases, National Institutes of Health (Bethesda, MD 20892-1881, USA)より入手し、 100 ng/mlの SCFを含む Stem Pro- 34培地(インビトロジェン社製)で 37°Cの 5%CO濃度のインキュベータ一中で培養した。
2
(2)低分子 RNAのクローニング
上記(1)で取得じた LAD2由籴 total RNA 200 /z gを用いて、 Lauらの方法 [Science, 2 94, 858-862, (2001)]に従い、 15%ポリアクリルアミドゲル電気泳動による低分子 RNA の切り出し、 5'—アデニル化 3'—アダプターライゲーシヨン、 5,一アダプターライゲー シヨン、逆転写、 PCR増幅、コンカテマ一化、 PCR2.1-TOPOベクターへのライゲーシ ヨンを順次進め、低分子 RNAのクローニングを行なった。次に、クロ一ニングした低分 子 RNAの塩基配列を決定した。なお 5'—アデニル化 3'—アダプターは、 Integrated DNA Technologies社製の miRNA Cloning Linkerを用いた。
[0200] また、上記方法とは別に、上記(1)で取得した LAD2由来 total RNA 200 を用い て、 Minenoらの方法 [Nucleic Acids Research, 34, 1765 - 1771, (2006)]に従レヽ、 15%ポ リアクリルアミドゲル電気泳動による低分子 RNAの分離及び切り出し、 5'末端脱リン酸 化、 3'一アダプターライゲーシヨン、リン酸化、 5'—アダプターライゲーシヨン、逆転写 、 PCR増幅、マイクロビーズベクターへのライゲーシヨンを順次経て、低分子 RNAをク ローニングし、そのマイクロビーズの塩基配列を読み取ることでも塩基配列を決定し た。
実施例 2 '
[0201] マイクロ RNAの同定
実施例 1で得られた低分子 RNAについて、まず、既知マイクロ RNAデータベースで ある miRBase (http:〃 microrna.sanger.ac.uk/)と比較して塩基酉己列が一致しなかった ものを選抜した。それらの塩基配列に対応する DNA配列を 5 '側および 3 '側にそれぞ れ 50nt程度伸ばした周辺ゲノム配列を UCSC Genome Bioinformatics (http:〃 genom e.ucsc.edu/)力も取得し、そのゲノム配列から.転写されることが予測される RNAの 2次 構造を RNAfoldを用いて予測した。その結果、 1336種がヘアピン構造の片鎖に位 置する新規マイクロ RNAであることが判明した。その塩基配列および、これらのマイ . クロ RNAを含むマイクロ RNA前駆体の塩基配列を表 1に示す。それぞれの塩基配 列を有するマイクロ RNAにっき、 KHK_miR_1001から 2344という名前を付与した(表 1 )。一つのマイクロ RNAが異なる位置のゲノム配列に由来するヘアピン構造を取り得 る場合はその全てを記載した。
[0202] 2次構造の一例として、 KHKjniR_1194のヘアピン構造を図 1に示す。
実施例 3
[0203] マイクロ RNAの機能の検出
実施例 2で得られたマイクロ RNAにつレ、て、その前駆体力 ¾icer蛋白質でプロセシ ングを受けるか否かを調べる とにより、マイクロ RNAとしての機能を有するか否かを 調べることができる。
実施例 2で得られたマイクロ RNAのうち、 KHKjniR_l 194で示されるマイクロ RNAの 機能の検出は以下のようにして行うことができる。まず、配列番号 1580で表される塩
. 基配列を有する一本鎖 RNAを合成レ、 X-treme GENE siRNA Dicer Kit (ロシュ'ァプ ライド '·サイエンス社製)に添付の Dicer Enzymeと反応させる。次に、反応産物を 15% ポリアクリルアミドゲルにて電気泳動し、 20-25塩基の大きさのバンドを検出できること でマイクロ RNAとしての機能を有していることを検出できる。
実施例 4
[0204] マイクロ RNAを強制発現したヒト肥満細胞の脱顆粒に及ぼす作用
実施例 2で得られたマイクロ RNAの前駆体を、ヒト肥満細胞株である LAD2に導入 して脱顆粒を誘導し、該マイクロ RNA前駆体の影響を調べた。
LAD2は 100 ng/mLの SCFを含む Stem Pro-34培地(Invitrogen社製)で培養した。 LAD2を 6穴プレートに 1穴あたり約 5xl05個になるように播種し、マイクロ RNA前駆 体をリポフエクシヨン法、具体的には、 Gene Silencer (Genlantis社製)を用いて、終濃 度力 ¾0nMとなるよう導入した。マイクロ RNA (以下、 miRNAともレ、う)の前駆体は、 KH K.miR_1001, 1002, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036の Pre— mi R™miRNA Precursor Moleculesとして Ambion社で合成されたものを用いた。これは化 学合成された二本鎖の核酸分子で、それぞれ配列番号 1、 2、 3、 8、 14、 20、 21、 2 2、 25、 32、 36で表される塩基配列からなる核酸が、 miRNAが活性を有する要因とな る RISCに類似した複合体に取り込まれて、 miRNAと同様の機能を有するようにデザィ ンされている。また、配列番号 1のヒトゲノム配列に対応する配列について、配列番号 1より 5 '側の 1塩基と 3 '側から 4塩基を欠失した配列 (配列番号 2852)からなる核酸を 用意し、 KHK_miR—1001_2の Pre- miR™miRNA Precursor Moleculesとして、 Ambion社 で合成したものも用いた。陰性対照としては、 Pre-miR™ miRNA Precursor Molecules -Negative Control #2 (以下、 miR- negacon#2と称す)(Ambion社製)を用レヽ、同様にし AD2に導入した。リポフエクシヨンは、製品 ίこ添付された方法に従った。
[0205] リポフエクシヨン法によりマイクロ RNA前駆体を導入した 2日後に、 1 g/mLのヒトミ エローマ IgE (コスモバイオ社製)を添加して 37°Cの 5%CO濃度のインキュベーター
2
中で一晩培養した。翌日、遠心分離により培地を除き、タイロード (Tyrode)緩衝液(1 26.1 mmol/L NaCl、 4.0 mmol/L KCK 1.0 mmol/L CaCl、 0.6 mmol/L MgCl、 0.6 m
2 2 mol/L KH PO、 10 mM HEPES、 5.6 mmol/L D_グルコース、 0.1%ゥシ血清アルブミ
ン、 pH7.4)で洗浄した後、タイロード緩衝液を 3.9mL添加して細胞を懸濁し、 96ゥエル •プレートに 1ゥヱルあたり 100 しずつ分注した。次いで、最終濃度 10 /i g/mLとなるよ うゥサギ抗ヒト IgE抗体 (ダコ社製)を加え、 37°Cの 5%CO濃度のインキュベータ一中
2
で 20分間インキュベートし、脱顆粒を誘導した。遠心により上清を回収し、上清中の ]3 -へキソサミニダーゼ活性を測定することにより、脱顆粒の程度を測定した。 β -へ キソサミニダーゼ活性は、回収した上清 50 μ Lに、 40 mmol/Lクェン酸緩衝液 (ρΗ.4.5 )に溶解した 4 mmol/L p-ニトロフエニル N-ァセチル- j3 _ダルコサミニド(シグマ社製) を 50 μ Lを力 Πえ、 37。Cで 1時間インキュベート後、 0.2 mol/Lグリシン (pH 10.7)を 100 Lカロえたサンプルの 405 nmにおける吸光度をプレートリーダー 1420 ARVOsx (パーキ ンエルマ一社製)を用レ、ることにより測定した。また、ゥサギ抗ヒト IgE抗体の代わりに 最終濃度 1%のトリトン X-100を添カ卩して同様の実験を行うことにより、 LAD2中の全 j3 -へキソサミニダーゼ活性を測定した。脱顆粒の割合を、全3 _へキソサミニダーゼ活 性に対する上清中の )3 -へキソサミニダーゼ活性の割合 (%)で算出し、それぞれに ついて対照区(Gene Silencerのみ)の脱顆粒の割合を 1.0とした時の脱顆粒相対活性 を計算した。その結果を表 3【こ示した。
[表 3]
その結果、 HK_miR_1001, 100し 2, 1002, 1003, 1008, 1014, 1020, 1022, 1025, 10 32, 1036導入により、 IgE受容体刺激による LAD2の脱顆粒が促進されることが明らか になった。
実施例 5
[0207] マイクロ RNAを強制発現させた間蔞系幹細朐の增殖活件、骨芽細朐分化、生細胞 率
実施例 2で得られたマイクロ RNAの前駆体をヒト間葉系幹細胞(以下、 hMSCともレ、う )に導入し、増殖および骨芽細胞分化に及ぼすマイクロ RNA前駆体の影響を調べた ヒト間葉系幹細胞は Cambrex社より入手し、 20%ゥシ胎児血清(FBS) (JRH Bioscienc e社製)を含む IMDM培地(Invitrogen社製)で 37°Cの 5%CO濃度のインキュベーター
2
中で培養した。 hMSCを 24穴プレートに 1穴あたり約 6.2xl03個になるように播種し、 20 % FBSを含む IMDM培地でー晚培養した。 1日後、マイクロ RNA前駆体をリポフエクショ ン法、具体的には、 Lipofectamine2000 (Invitrogen社製)を用いて、終濃度が 20nMと なるように hMSCに導入した。マイクロ RNAの前駆体は、 KHKjniR— 1001, 1001_2, 1002 , 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036の Pre- miRTMmiRNA Precur sor Moleculesとして Ambion社で合成されたものを用いた。リポフエクシヨンは、製品に 添付された方法に従った。
[0208] リポフエクシヨン法によりマイクロ RNA前駆体を導入した翌日、培地を骨芽分化誘 導培地(20%FBSを含む IMDM培地中に、 0.1 μ mol/Lデキサメサゾン、 50 μ mol/L了 スコルビン酸一 2リン酸(Sigma社製)、 10mmol/L β—グリセ口フォスフイト(Sigma社製 ) )へ交換し、 3日に一度の頻度で、骨芽分化誘導培地を交換して培養を続けた。 . 培養開始から 2週間後に、細胞の形態を位相差顕微鏡 (ニコン社製)下で観察し、 更にアルカリフォスファターゼ染色を行って、骨芽細胞を検出した。具体的にはまず 、細胞をリン酸緩衝液(以下、 PBS(phosphate-buffered saline)ともいう)(Invitrogen社 製)で 1回洗浄し、固定液(10%フオルマリン ZPBS)で 5分間固定した。蒸留水で洗浄 した後、暗所で Naphthol AS- MXリン酸 (Sigma社製)と Fast Violet B溶液との混合溶 液(Sigma社製)と 30分間反応させ、アルカリフォスファターゼ反応をおこなった。更に 蒸留水で洗浄し、位相差顕微鏡下で赤く染まっている骨芽細胞を観察し、デジタノレ カメラ (ニコン社製)で撮影した。
[0209] その結果、 KHK_miR_1008, 1021, 1036の Pre - miRTM miRNA Precursor Molecules を導入した hMSCは、マイクロ RNA前駆体非導入 hMSCと比べて、細胞数が少なぐァ
ルカリフォスファターゼ染色された陽性細胞の数も少なレ、ことが見出された。マイクロ RNA前駆体は細胞中でマイクロ RNAに変換されるので、'これらの前駆体に由来する マイクロ RNAは、 hMSCに対して、増殖を抑制する活性および骨芽細胞への分化を抑 制する活性を有することが明らかになった。また逆に、 KHK_miR_1001, 100し 2の Pre - miRTM miRNA Precursor Moleculesを導入した hMSCは、マイクロ RNA前駆体非導入 hMSCと比べて、アルカリフォスファターゼ染色された陽性細胞の数が多レ、ことが見出 された。このこと力ら、これらの前駆体に由来するマイクロ RNAは、 hMSCに対して、骨 芽細胞への分化を促進する活性を有することが明らかになった。
また、リポフエクシヨン法によりマイクロ RNA前駆体を導入した 4日後、 CellTiter- Glo ™ Luminescent Cell Viability Assay(Promega社製)を用いて生細胞率を測定した。 その結果を表 4に示す。表 4に示したように、 KHK_miR_1001導入により通常よりも生 細胞率が増加したことが認められた。
[0211] マイクロ RNAを強制発現させた大腸癌由来細朐株における生細胞率、アポトーシス 腿 .
実施例 2で得られたマイクロ RNAの前駆体を大腸癌由来細胞株に導入し、生細胞 率、アポトーシス活性に及ぼすマイクロ RNA前駆体の影響を調べた。
DLD- 1ヒト大腸癌由来細胞株(以下、 DLD-1ともいう)は American Type Culture Col lection (ATCC) (以下、 ATCCと称す)より入手した (ATCC CCL— 221)。 DLD- 1は 10%ゥシ胎児血清(FBS) (JRH Biosciences社製)を含む RPMI1640培地(Invitrogen 社製)で 37°Cの 5%CO濃度のインキュベータ一中で培養した。
2
[0212] DLD-1を 96穴ズレートに 1穴あたり約 2500細胞数になるように播種し、 10% FBSを 含む RPMI培地でー晚培養した。 1日後、マイクロ RNA前駆体をリポフエクシヨン法、 具体的には、 Lipofectamine2000 (Invitrogen社製)を用いて、終濃度が 5nM或いは 25
nMとなるよう DLD - 1に導入した。マイクロ RNAの前駆体は、 KHK_miR_1001, 100し 2, 1 002, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036の Pre-miR™miRNA Pre cursor Moleculesとして Ambion社で合成したものを用いた。また、 miR- negacon#2 (Am bion社製)も DLD- 1に導入し、陰性対照とした。リポフエクシヨンは、製品に添付された 方法に従った。 、
リポフエクシヨン法によりマイクロ RNA前駆体を導入した 3日後、 CellTiter-Glo™ Lu minescent Cell Viability Assay (Promega社製)を用いて生細胞率を測定した。対照区 (Lipofectamine2000のみ)の DLD- 1の生細胞率を 1.0としてそれぞれの相対生細胞率 を計算した。その結果、表 5に示したように、 KHK_miR_1001, 100し 2, 1032, 1036導入 により 40%以上の生細胞率の減少が認められた。
[表 5]
またリポフエクシヨン法により該マイクロ RNA前駆体を導入した 2日後に、 Caspase-G loR 3/7 asSay(Promega社製)を用いて製品に添付された方法に従レ、カスパーゼ 3/7 活性を測定した。対照区(Lipofectamine2000のみ)の DLD-1のカスパーゼ 3/7活性値 を 1.0としてそれぞれの 対カスパーゼ 3/7活性値を計算した。その結果を表 6に示す 。表 6に示したように、 KHK_miR_1001, 1001_2, 1036導入により 50%以上のカスパー ゼ 3/7活性の増加が認められた。
[表 6]
実施例 7
マ クロ RNAを強制発現させた卵巣癌由来細朐株における生細胞率
実施例 2で得られたマイクロ RNAの前駆体を卵巣癌由来細胞株に導入し、生細胞 率に及ぼすマイクロ RNA前駆体の影響を調べた。
A2780ヒト卵巣癌由来細胞株(Nature, 295, 116-119, (1982); Science, 224, 994 - 99 6, (1984); Semin. Oncol., 11, 285-298 (1984);以下, A2780と称す)は 5%FBS (JRH Biosciences社製)を含む RPMI1640培地(Invitrogen社製)で 37°Cの 5%C02濃度のィ ンキュベータ一中で培養じた。
[0216] A2780を 96穴プレートに 1穴あたり約 2500細胞数になるように播種し、 10%FBSを含 む RPMI培地でー晚培養した。 1日後、マイクロ RNA前駆体をリポフエクシヨン法、具 体的には、 Lipofectamine2000 (Invitrogen社製)を用いて、終濃度が 5nM或いは 25nM となるよう A2780に導入した。マイクロ RNAの前駆体は、 KHK_miR_1001, 100し 2, 100 2, 1003, 1008, 1014, 1020, 1021, 1022, 1025, 1032, 1036の Pre— miR™ miRNA Prec ursor Moleculesとして Ambion社で合成したもめを用いた。また、 miR- negacon#2 (Amb ion社製)も A2780に導入し、陰性対照とした。
[0217] リポフエクシヨン法により該マイクロ RNA前駆体を導入した 3日後、 CellTiter-Glo™ Luminescent Cell Viability Assay (Promega社製)を用いて生細胞率を測定した。対 照区(Lipofectamine2000のみ)の A2780の生細胞率を 1.0としてそれぞれの相対生細 胞率を計算した。その結果を表 7に示す。表 7に示したように、 KHK_miR_1003, 1008, 1020, 1021, 1022, 1032, 1036導入により 40%以上の生細胞率の減少が認められた。
[表 7] 、
[0218] 本発明により、新規な配列を有する、マイクロ RNAやマイクロ RNA前駆体等の核 酸が提供される。本発明の核酸により、マイクロ RNAの発現または変異の検出、細
胞の分離、標的配列遺伝子の発現抑制、マイクロ RNAの機能の促進または抑制さ せる物質のスクリーニング、肥満細胞の異常に起因する疾患、間葉系幹細胞の増殖 または分化の異常に起因する疾患、癌及び細胞の増殖異常や組織の過形成等が原 因となってレ、る疾患の診断や治療をすることができる。
Claims
請求の範囲
[I] 配列番号 1〜: 1336のいずれかで表される塩基配列力 なる核酸。
[2] 配列番号 1〜: 1336のいずれかで表される塩基配列と 90%以上の同一性を有する塩 基配列からなる核酸。 ,
[3] 配列番号 1〜: 1336のいずれかで表される塩基配列力もなる核酸の相補鎖とストリン ジェン卜な条件でハイブリダィズする核酸。
[4] 請求項:!〜 3のいずれか 1項に記載の核酸を含む核酸。
[5] 配列番号 1337〜2851のいずれかで表される塩基配列からなる核酸。 '
[6] 配列番号 1337〜2851のいずれかで表される塩基配歹【』と 80% ^上の同一性を有
' する塩基配列からなる核酸。
[7] 配列番号 1337〜2851のいずれかで表される塩基配歹 IJからなる核酸の相補鎖とスト リンジェントな条件でハイブリダィズする核酸。
[8] . 請求項 1〜7のいずれか 1項に記載の核酸に対して相補的な塩基配列力 なる核酸
[9] 請求項 1〜7のいずれか 1項に記載の核酸と、該核酸の塩基配列に対して相補的な 塩基配列カゝらなる核酸とからなる二本鎖核酸。
[10] 請求項 1〜9のいずれか 1項に記載の核酸を発現するベクター。
[II] 請求項 1〜9のいずれ力 4項に記載の核酸を用いることを特徴とする、請求項 1〜9の いずれカゝ 1項に記載の核酸の発現または変異を検出する方法。 -
[12] 請求項 1〜9のいずれ力 1項に記載の核酸を用いることを特徴とする、請求項 1〜9の レ、ずれか 1項に記載の核酸の発現または機能を促進或レ、は抑制させる物質のスクリ 一二ング方法。
[13] 請求項 1〜9のいずれか 1項に記載の核酸を用レ、ることを特徴とする、請求項 1〜9の レ、ずれか 1項に記載の核酸を発現する細胞を分離する方法。
[14] 請求項 1〜9のいずれか 1項に記載の核酸を用いることを特徴とする、請求項 1〜9の レ、ずれ力 1項に記載の核酸の標的遺伝子の発現を抑制する方法。
[15] 請求項 1〜9のいずれか 1項に記載の核酸を有効成分として含有する、肥満細胞の 異常に起因する疾患の診断薬または治療薬。
[16] 請求項 1〜9のいずれか 1項に記載の核酸の発現または機能を促進或いは抑制させ る物質を有効成分として含有する、肥満細胞の異常に起因する疾患の診断薬または 治療薬。 -
[17] 請求項 1〜9のいずれか 1項に記載の核酸の発現または機能を促進或いは抑制させ ることを指標とする、肥満細胞の異常に起因する疾患の診断薬または治療薬のスクリ 一二ング方法。
[18] 請求項 1〜9のいずれか 1項に記載の核酸の標的遺伝子の発現を抑制する物質を 有効成分として含有する、肥満細胞の異常に起因する疾患の診断薬または治療薬。
[19] 請求項 1〜9のいずれか 1項に記載の核酸の標的遺伝子の発現を抑制させることを 指標とする、肥満細胞の異常に起因する疾患の診断薬または治療薬のスクリーニン グ方法。
[20] 請求項 1〜: 10のいずれ力 1項に記載の核酸またはベクターを導入した細胞。
[21] 酉己歹 IJ番号力 1、 2、 3、 8、 14、 20、 22、 25、 32また ίま 36の ヽずれ力である、請求項 1 - ' 〜4のいずれか 1項に記載の核酸を有効成分として含有する、肥満細胞の脱顆粒促 進剤。
[22] , 酉己歹 IJ番号力 1337、 1338、 1339、 1352、 1363、 1371、 1373、 1377、 1386また は 1390のいずれかである、請求項 5〜7のいずれ力 1項に記載の核酸を有効成分と して含有する、肥満細胞の脱顆粒促進剤。
[23] 請求項 21または 22に記載の核酸に対して相補的な塩基配列からなる核酸を有効成 分として含有する、肥満細胞の脱顆粒抑制剤。
[24] 請求項 21または 22に記載の核酸と、該核酸の塩基配列に対して相補的な塩基配列 からなる核酸とからなる二本鎖核酸を有効成分として含有する、 S巴満細胞の脱顆粒 . 促進剤または脱顆粒抑制剤。
[25] 請求項 21または 22に記載の核酸の発現または機能を促進或いは抑制させる物質を . 有効成分として含有する、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤。 .
[26] 請求項 21または 22に記載の核酸の発現または機能を促進或いは抑制させることを 指標とする、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤のスクリーニング方法。
[27] 請求項 21または 22に記載の核酸の標的遺伝子の発現を抑制または促進する物質
を有効成分として含有する、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤。
[28] 請求項 21または 22に記載の核酸の標的遺伝子の発現を抑制または促進させること を指標とする、肥満細胞の脱顆粒促進剤または脱顆粒抑制剤のスクリーニング方法
[29] 配列番号が 1、 8、 21または 36のいずれかである、請求項 1〜4のいずれ力 4項に記 載の核酸を有効成分として含有す 、間葉系幹細胞の増殖および または分化の 異常に起因する疾患の診断薬または治療薬。
[30] 配列番号が 1337、 1352、 1372または 1390のいずれかである、請求項 5〜7のい ずれか 1項に記載の核酸を有効成分として含有する、間葉系幹細胞 増殖および または分化の異常に起因する疾患の診断薬または治療薬。
[31] 請求項 29または 30に記載の核酸に対して相補的な塩基配列力もなる核酸を有効成 分として含有する、間葉系幹細胞の増殖および/または分化の異常に起因する疾患 の診断薬または治療薬。. . ' ■
[32] 請求項 29または 30に記載の核酸と、該核酸の塩基配列に対して相補的な塩基配列 からなる核酸とからなる二本鎖核酸を有効成分として含有する、間葉系幹細胞の増 殖および/または分化の異常に起因する疾患の診断薬または治療薬。
[33] 請求項 29または 30に記載の核酸の発現または機能を促進或いは抑制させる物質を 有効成分として含有する、間葉系幹細胞の増殖および/または分化の異常に起因 する疾患の診断薬または治療薬。 .
[34] 請求項 29または 30に記載の核酸の発現または機能を促進或いは抑制させることを 指標とする、間葉系幹細胞の増殖および/または分化の異常に起因する疾患の診 断薬または治療薬のスクリーニング方法。
[35] 請求項 29または 30に記載の核酸の標的遺伝子の発現を抑制または促進する物質 を有効成分として含有する、間葉系幹細胞の増殖および または分化の異常に起 因する疾患の診断薬または治療薬。
[36] 請求項 29または 30に記載の核酸の標的遺伝子の発現を抑制または促進させること を指標とする、間葉系幹細胞の増殖および/または分化の異常に起因する疾患の 診断薬または治療薬のスクリーニング方法。
[37] 配列番号力 Siである、請求項 1〜4のいずれか 1項に記載の核酸を有効成分として含 有する、間葉系幹細胞の増殖促進剤。
[38] 配列番号が 1337である、請求項 5〜7のいずれか 1項に記載の核酸を有効成分とし て含有する、間葉系幹細胞の増殖促進剤。
[39] 請求項 37または 38に記載の核酸に対して相補的な塩基配列力 なる核酸を有効成 分として含有する、間葉系幹細胞の増殖抑制剤。
[40] 配列番号が 8、 21または 36のいずれかである、請求項 1〜4のいずれか 1項に記載 の核酸を有効成分として含有する、間葉系幹細胞の増殖抑制剤。
[41] 配列番号が 1352、 1372または 1390のいずれかである、請求項 5〜7のいずれか 1. 項に記載の核酸を有効成分として含有する、間葉系幹細胞の増殖抑制剤。
[42] 請求項 37または 38に記載の核酸に対して相補的な塩基配列力もなる核酸を有効成 分として含有する、間葉系幹細胞の増殖促進剤。
[43] 請求項 37〜42のいずれか 1項に記載の核酸と、該核酸の塩基配列に対して相補的 な塩基配列からなる核酸とからなる二本鎖核酸を有効成分として含有する、間葉系 幹細胞の増殖促進剤または増殖抑制剤。
[44] ' 請求項 37〜42のいずれか 1項に記載の核酸の発現または機能を促進或いは抑制 させる物質を有効成分として含有する、間葉系幹細胞の増殖促進剤または増殖抑制 剤。
[45] 請求項 37〜42のいずれ力 1項に記載の核酸の発現または機能を促進或いは抑制 させることを指標とする、間葉系幹細胞の増殖促進剤または増殖抑制剤のスクリー二 ング方法。
[46] 請求項 37〜42のいずれか 1項に記載の核酸の標的遺伝子の発現を抑制または促 進する物質を有効成分として含有する、間葉系幹細胞の増殖促進剤または増^!抑 制剤。
[47] 請求項 37〜42のいずれか 1項に記載の核酸の標的遺伝子の発現を抑制または促 進させることを指標とする、間葉系幹細胞の増殖促進剤または増殖抑制剤のスクリー エング方法。
[48] 酉己歹 IJ番号力 1、 3、 8、 20、 21、 22、 32また {ま36のレヽずれ力である、請求項:!〜 4のレヽ
ずれか 1項に記載の核酸を有効成分として含有する、細胞の増殖異常に起因する疾 患の診断薬または治療薬。
[49] 酉己歹 IJ番号力 1337、 1339、 1352、 1371、 1372、 1373、 1386また【ま 1390のレヽず れかである、請求項 5〜7のいずれ力 1項に記載の核酸を有効成分として含有する、 細胞の増殖異常に起因する疾患の診断薬または治療薬。
[50] 請求項 48または 49に記載の核酸に対して相補的な塩基配列力 なる核酸を有効成 分として含有する、細胞の増殖異常に起因する疾患の診断薬または治療薬。
[51] 請求項 48または 49に記載の核酸と、該核酸に対して相補的な塩基配列からなる核 酸とからなる二本鎖核酸を有効成分として含有する、細胞の増殖異常に起因する疾 患の診断薬または治療薬。
[52] 請求項 48または 49に記載の核酸の発現または機能を促進或いは抑制させる物質を 有効成分として含有する、細胞の増殖異常に起因する疾患の診断薬または治療薬。
[53] 請求項 48または 49に記載の核酸の発現または機能を促進或レ、は抑制させることを 指標とする、細胞の増殖異常に起因する疾患の診断薬または治療薬のスクリーニン グ方法。
[54] 請求項 48または 49に記載の核酸の標的遺伝子の発現を抑制または促進する物質 を有効成分として含有する、細胞の増殖異常に起因する疾患の診断薬または治療 薬。 ' . .
[55] 請求項 48または 49に記載の核酸の標的遺伝子の発現を抑制または促進させること を指標とする、細胞の増殖異常に起因する疾患の診断薬または治療薬のスクリー二 ング方法。 '
[56] 細胞の増殖異常に起因する疾患が瘙、動脈硬化、慢性関節リウマチ、前立腺肥大症 、経皮的経血管的冠動脈形成術後の血管再狭窄、肺線維症、糸球体腎炎および自 己免疫疾患力 なる群力も選ばれる疾患である請求項 48〜55のいずれ力 1項に記 載の診断薬、治療薬またはスクリーニング方法。
[57] ■ 配列番号力 、 3、 8、 20、 21、 22、 32または 36のレヽずれ力である、請求項:!〜 4のレヽ ずれか 1項に記載の核酸を有効成分として含有する、細胞の増殖抑制剤。
[58] 酉己歹 IJ番号力 1337、 1339、 1352、 1371、 1372、 1373、 1386または 1390のレヽず
れかである、請求項 5〜7のいずれか 1項に記載の核酸を有効成分として.含有する、 細胞の増殖抑制剤。
[59] 請求項 57または 58に記載の核酸に対して相補的な塩基配列力 なる核酸を有効成 分として含有する、細胞の増殖促進剤。
[60] 請求項 57または 58に記載の核酸と、該核酸の塩基配列に対して相補的な塩基配列 力 なる核酸とからなる二本鎖核酸を有効成分として含有する、細胞の増殖抑制剤 または増殖促進剤。
[61] 請求項 57または 58に記載の核酸の発現または機能を促進或いは抑制させる物質を 有効成分として含有する、細胞の増^抑制剤または増殖促進剤。
[62] 請求項 57または 58に記載の核酸の発現または機能を促進或レヽは抑制させることを 指標とする、細胞の増殖抑制剤または増殖促進剤のスクリーニング方法。
[63] 請求項 57または 58に記載の核酸の標的遺伝子の発現を抑制または促進する物質 を有効成分として含有する、細胞の増殖抑制剤または増殖促進剤。
[64] 請求項 57または.58に記載の核酸の標的遺伝子の発現を抑制または促進させること を指標とする、細胞の増殖抑制剤または増殖促進剤のスクリーニング方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/519,960 US20100099746A1 (en) | 2006-12-18 | 2007-12-18 | Novel nucleic acid |
| EP07859120A EP2123752A4 (en) | 2006-12-18 | 2007-12-18 | NOVEL NUCLEIC ACID |
| JP2008552924A JPWO2008084319A1 (ja) | 2006-12-18 | 2007-12-18 | 新規核酸 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006-339997 | 2006-12-18 | ||
| JP2006339997 | 2006-12-18 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2008084319A2 true WO2008084319A2 (ja) | 2008-07-17 |
| WO2008084319A3 WO2008084319A3 (ja) | 2008-09-25 |
Family
ID=39609102
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/IB2007/004005 WO2008084319A2 (ja) | 2006-12-18 | 2007-12-18 | 新規核酸 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20100099746A1 (ja) |
| EP (1) | EP2123752A4 (ja) |
| JP (1) | JPWO2008084319A1 (ja) |
| WO (1) | WO2008084319A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018023367A (ja) * | 2008-10-03 | 2018-02-15 | プロカルタ バイオシステムズ リミテッド | 転写因子デコイ |
| CN113999852A (zh) * | 2021-11-30 | 2022-02-01 | 杭州市富阳区第一人民医院 | circ_0001772作为结直肠癌诊断和治疗标志物的应用 |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20110021600A1 (en) * | 2006-09-04 | 2011-01-27 | Kyowa Hakko Kirin Co., Ltd. | Novel nucleic acid |
| CN101424640B (zh) * | 2007-11-02 | 2012-07-25 | 江苏命码生物科技有限公司 | 血清中微小核糖核酸的检测方法和用于检测的试剂盒、生物芯片及其制作和应用方法 |
| JPWO2009148137A1 (ja) * | 2008-06-04 | 2011-11-04 | 協和発酵キリン株式会社 | 肥満細胞の脱顆粒を制御する核酸 |
| US8563298B2 (en) | 2010-10-22 | 2013-10-22 | T2 Biosystems, Inc. | NMR systems and methods for the rapid detection of analytes |
| US8409807B2 (en) | 2010-10-22 | 2013-04-02 | T2 Biosystems, Inc. | NMR systems and methods for the rapid detection of analytes |
| BR122020001802B1 (pt) | 2010-10-22 | 2021-05-18 | T2 Biosystems, Inc | métodos para detectar a presença de um patógeno em uma amostra de sangue total e para detectar um analito em uma amostra |
| US20140315750A1 (en) * | 2011-11-15 | 2014-10-23 | The United States Of America, As Represented By The Secretary, Department Of Health | Selective detection of norovirus |
| EP3524692A1 (en) | 2012-04-20 | 2019-08-14 | T2 Biosystems, Inc. | Compositions and methods for detection of candida species |
| US20180201937A1 (en) * | 2015-08-04 | 2018-07-19 | The University Of Chicago | Inhibitors of cacna1a/alpha1a subunit internal ribosomal entry site (ires) and methods of treating spinocerebellar ataxia type 6 |
| WO2017127731A1 (en) | 2016-01-21 | 2017-07-27 | T2 Biosystems, Inc. | Nmr methods and systems for the rapid detection of bacteria |
| TWI780046B (zh) | 2016-05-10 | 2022-10-11 | 國立大學法人東京醫科齒科大學 | 炎症促進因子表現抑制劑、其有效成分之篩選方法、對於該方法為有用之表現匣、診斷藥及診斷方法 |
| US12018255B2 (en) * | 2017-12-08 | 2024-06-25 | University Of Connecticut | Compositions and methods for treating disorders of genomic imprinting |
| WO2022178411A1 (en) * | 2021-02-22 | 2022-08-25 | Alnylam Pharmaceuticals, Inc. | Folliculin irna compositions and methods thereof |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997016539A1 (fr) | 1995-11-01 | 1997-05-09 | Dnavec Research Inc. | Virus sendai recombinant |
| WO1997016538A1 (fr) | 1995-10-31 | 1997-05-09 | Dnavec Research Inc. | Vecteur de virus d'arn a brin negatif possedant une activite de replication autonome |
| JP2002034580A (ja) | 2000-01-05 | 2002-02-05 | Japan Science & Technology Corp | 多能性神経系前駆細胞を分離し、精製するための方法および多能性神経系前駆細胞 |
| US20020135539A1 (en) | 2001-02-22 | 2002-09-26 | Blundell Barry George | Interaction with a volumetric display system |
| US6468794B1 (en) | 1999-02-12 | 2002-10-22 | Stemcells, Inc. | Enriched central nervous system stem cell and progenitor cell populations, and methods for identifying, isolating and enriching for such populations |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6582908B2 (en) * | 1990-12-06 | 2003-06-24 | Affymetrix, Inc. | Oligonucleotides |
| US20040142325A1 (en) * | 2001-09-14 | 2004-07-22 | Liat Mintz | Methods and systems for annotating biomolecular sequences |
| US7250496B2 (en) * | 2002-11-14 | 2007-07-31 | Rosetta Genomics Ltd. | Bioinformatically detectable group of novel regulatory genes and uses thereof |
| EP2305813A3 (en) * | 2002-11-14 | 2012-03-28 | Dharmacon, Inc. | Fuctional and hyperfunctional sirna |
| WO2005024061A2 (en) * | 2003-09-03 | 2005-03-17 | Cancer Research Technology Limited | Compounds and methods for modulation of dna replication |
| US20080038819A1 (en) * | 2004-03-29 | 2008-02-14 | Haruo Sugiyama | Micro Rna Inhibiting the Expression of Wt1 Gene and Utilization of the Same |
| CA2566519C (en) * | 2004-05-14 | 2020-04-21 | Rosetta Genomics Ltd. | Micrornas and uses thereof |
| US7635563B2 (en) * | 2004-06-30 | 2009-12-22 | Massachusetts Institute Of Technology | High throughput methods relating to microRNA expression analysis |
| US8071306B2 (en) * | 2005-01-25 | 2011-12-06 | Merck Sharp & Dohme Corp. | Methods for quantitating small RNA molecules |
| US20060263798A1 (en) * | 2005-02-11 | 2006-11-23 | International Business Machines Corporation | System and method for identification of MicroRNA precursor sequences and corresponding mature MicroRNA sequences from genomic sequences |
| CA2605701C (en) * | 2005-04-29 | 2015-12-08 | Rockefeller University | Human micrornas and methods for inhibiting same |
| WO2007081196A1 (en) * | 2006-01-10 | 2007-07-19 | Koninklijke Nederlandse Akademie Van Wetenschappen | New nucleic acid molecules and collections thereof, their application and identification |
| US20090307788A1 (en) * | 2006-06-19 | 2009-12-10 | Kobenhavns Universitet | Ribozyme mediated stabilization of polynucleotides |
| US20110021600A1 (en) * | 2006-09-04 | 2011-01-27 | Kyowa Hakko Kirin Co., Ltd. | Novel nucleic acid |
| EP2090665A2 (en) * | 2006-10-20 | 2009-08-19 | Exiqon A/S | Novel human microRNAs associated with cancer |
| US8188255B2 (en) * | 2006-10-20 | 2012-05-29 | Exiqon A/S | Human microRNAs associated with cancer |
| JPWO2009148137A1 (ja) * | 2008-06-04 | 2011-11-04 | 協和発酵キリン株式会社 | 肥満細胞の脱顆粒を制御する核酸 |
-
2007
- 2007-12-18 JP JP2008552924A patent/JPWO2008084319A1/ja not_active Abandoned
- 2007-12-18 US US12/519,960 patent/US20100099746A1/en not_active Abandoned
- 2007-12-18 WO PCT/IB2007/004005 patent/WO2008084319A2/ja active Application Filing
- 2007-12-18 EP EP07859120A patent/EP2123752A4/en not_active Withdrawn
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997016538A1 (fr) | 1995-10-31 | 1997-05-09 | Dnavec Research Inc. | Vecteur de virus d'arn a brin negatif possedant une activite de replication autonome |
| WO1997016539A1 (fr) | 1995-11-01 | 1997-05-09 | Dnavec Research Inc. | Virus sendai recombinant |
| US6468794B1 (en) | 1999-02-12 | 2002-10-22 | Stemcells, Inc. | Enriched central nervous system stem cell and progenitor cell populations, and methods for identifying, isolating and enriching for such populations |
| JP2002034580A (ja) | 2000-01-05 | 2002-02-05 | Japan Science & Technology Corp | 多能性神経系前駆細胞を分離し、精製するための方法および多能性神経系前駆細胞 |
| US20020135539A1 (en) | 2001-02-22 | 2002-09-26 | Blundell Barry George | Interaction with a volumetric display system |
Non-Patent Citations (130)
| Title |
|---|
| "Himan Saibo no Rinsho", 2001, SENTAN IGAKU-SHA LTD., pages: 142 |
| "Himan Saibo no Rinsho", 2001, SENTAN IGAKU-SHA LTD., pages: 559 |
| "Human Genetics", 1996, BIOS SCIENTIFIC PUBLISHERS LIMITED |
| "Huro Saitometa Jiyu Jizai", 1999, SHUJUNSHA, pages: 14 - 23 |
| "Molecular Cloning", 2001, COLD SPRING HARBOR LABORATORY PRESS |
| "RNAi Method and Antisense Method", 2005, KODANSHA |
| ACC. CHEM. RES., vol. 32, 1999, pages 624 |
| AM. J. PATHOL., vol. 163, 2003, pages 2259 - 2269 |
| BAIOSAIENSU TO INDASUTORII, vol. 50, 1992, pages 322 |
| BIOCHEMISTRY, vol. 28, 1989, pages 9508 - 9514 |
| BIOCHIMICA ET BIOPHYSICA ACTA 1479, 1998, pages 178 |
| BIOTECHNIQUES, vol. 11, 1991, pages 474 - 485 |
| BIOTECHNOLOGY, vol. 9, 1992, pages 358 |
| BLOOD, vol. 100, 2002, pages 3861 |
| BLOOD, vol. 100, 2002, pages 3861 - 3868 |
| BLOOD, vol. 91, 1998, pages 187 |
| BLOOD, vol. 97, 2001, pages 1016 |
| BLOOD, vol. 97, 2001, pages 2045 |
| BLOOD, vol. 98, 2001, pages 1127 |
| BLOOD, vol. 98, 2001, pages 1127 - 1134 |
| CANCER RESEARCH, vol. 64, 2004, pages 3753 - 3756 |
| CELL, vol. 113, 2003, pages 673 - 676 |
| CELL, vol. 120, 2005, pages 635 - 647 |
| CELL, vol. 27, 1981, pages 223 - 231 |
| CHEMISTRY & BIOLOGY, vol. 6, 1999, pages R33 |
| CIRCULATION RESEARCH, vol. 82, 1998, pages 1023 |
| CIRCULATION, vol. 83, 1992, pages 2007 - 2011 |
| CLIN. EXP. ALLERGY, vol. 28, 1998, pages 1228 - 1236 |
| CRIT. REV. IMMUNOL., vol. 22, 2002, pages 115 - 140 |
| CURRENT BIOLOGY, vol. 15, 2005, pages R458 - R460 |
| CURRENT OPINION IN CHEMICAL BIOLOGY, vol. 3, 1999, pages 274 |
| EXPERIMENTAL NEPHROLOGY, vol. 5, 1997, pages 429 |
| FEMS MICROBIOLOGY REVIEWS, vol. 23, 1999, pages 257 |
| FRONTIERS IN BIOSCIENCE, vol. 4, 1999, pages D497 |
| GENES & DEVELOPMENT, vol. 15, 2000, pages 188 - 200 |
| GENES DEV., vol. 13, 1999, pages 3191 |
| GENOME BIOLOGY, vol. 6, 2005, pages R71 |
| GENOME RES., vol. 6, 1996, pages 639 |
| GENOMICS, vol. 16, 1993, pages 325 - 332 |
| HUM. GENE THER., vol. 3, 1991, pages 147 - 154 |
| HUM. GENE THER., vol. 3, 1992, pages 267 - 275 |
| HUM. GENE THER., vol. 3, 1992, pages 399 |
| IDENSHI IGAKU, vol. 4, 2000, pages 58 - 61 |
| J. ALLERGY CLIN. IMMUNOL., vol. 106, 2000, pages 141 |
| J. ALLERGY CLIN. IMMUNOL., vol. 107, 2001, pages 322 |
| J. AM. CHEM. SOC., vol. 122, 2000, pages 6900 |
| J. AM. CHEM. SOC., vol. 123, 2001, pages 4653 |
| J. BIOL. CHEM., vol. 264, 1989, pages 12126 - 12129 |
| J. BIOL. CHEM., vol. 264, 1989, pages 16985 - 16987 |
| J. BIOL. CHEM., vol. 266, 1991, pages 14338 - 14342 |
| J. IMMUNOL. METH., vol. 160, 1993, pages 81 - 88 |
| J. IMMUNOL. METH., vol. 65, 1983, pages 55 - 63 |
| J. IMMUNOL. METHODS, vol. 169, 1994, pages 153 |
| J. IMMUNOL. METHODS, vol. 240, 2000, pages 101 |
| J. IMMUNOL., vol. 138, 1987, pages 861 |
| J. IMMUNOL., vol. 157, 1996, pages 343 |
| J. MOL. BIOL., vol. 215, 1990, pages 403 |
| JIKKEN IGAKU, vol. 20, 2000, pages 2459 - 2464 |
| JOURNAL OF EXPERIMENTAL MEDICINE, vol. 183, 1996, pages 1797 - 806 |
| KAGAKU, vol. 46, 1991, pages 681 |
| KISO-HEN: "Soshiki Baiyou No Gijyutsu", 1996, ASAKURA SHOTEN |
| LANCET, vol. 364, 2004, pages 149 - 155 |
| LAU ET AL., SCIENCE, vol. 294, 2001, pages 858 - 862 |
| LEUK. RES, vol. 27, 2003, pages 677 |
| LEUK. RES., vol. 27, 2003, pages 671 |
| LEUK. RES., vol. 27, 2003, pages 677 |
| M.F. PITTENGER ET AL., SCIENCE, vol. 284, 1999, pages 143 - 147 |
| METHODS IN ENZYMOLOGY, vol. 183, 1990, pages 63 |
| METHODS IN ENZYMOLOGY, vol. 254, 1995, pages 419 |
| MINENO ET AL., NUCLEIC ACIDS RESEARCH, vol. 34, 2006, pages 1765 - 1771 |
| MUTAT. RES., vol. 288, 1993, pages 103 - 112 |
| NATURE GENET., vol. 8, 1994, pages 42 |
| NATURE GENETICS, vol. 9, 1996, pages 103 - 104 |
| NATURE METHOD, vol. 3, 2006, pages 27 |
| NATURE REVIEWS CANCER, vol. 6, 2006, pages 259 - 269 |
| NATURE REVIEWS GENETICS, vol. 5, 2004, pages 522 - 531 |
| NATURE, vol. 294, 1981, pages 92 - 94 |
| NATURE, vol. 295, 1982, pages 116 - 119 |
| NATURE, vol. 432, 2004, pages 226 |
| NATURE, vol. 432, 2004, pages 226 - 230 |
| NATURE, vol. 435, 2005, pages 823 - 833 |
| NATURE, vol. 435, 2005, pages 839 - 843 |
| NIPPON RINSHO, JAPANESE JOURNAL OF CLINICAL MEDICINE, vol. 54, 1996, pages 2583 |
| NIPPON RINSHO, JAPANESE JOURNAL OF CLINICAL MEDICINE, vol. 56, 1998, pages 563 |
| NUCLEIC ACID RESEARCH, vol. 32, 2004, pages 175 |
| NUCLEIC ACID RESEARCH, vol. 32, 2004, pages 188 |
| NUCLEIC ACID RESEARCH, vol. 33, 2005, pages 179 |
| NUCLEIC ACID RESEARCH, vol. 35, 2007, pages 3287 |
| NUCLEIC ACIDS RESEARCH, vol. 26, 1998, pages 5237 |
| NUCLEIC ACIDS RESEARCH, vol. 31, 2003, pages 3406 - 3415 |
| NUCLEIC ACIDS RESEARCH, vol. 31, 2003, pages 3429 - 3431 |
| NUCLEIC ACIDS RESEARCH, vol. 32, 2004, pages 43 |
| NUCLEIC ACIDS RESEARCH, vol. 34, 2006, pages 1765 - 1771 |
| PROC. NATL. ACAD. SCI. USA, vol. 101, 2004, pages 9740 - 9744 |
| PROC. NATL. ACAD. SCI. USA, vol. 97, 2000, pages 13625 - 13630 |
| PROC.NATL.ACAD.SCI. USA, vol. 103, 2006, pages 263 |
| PROC.NATL.ACAD.SCI. USA, vol. 77, 1980, pages 5399 - 5403 |
| PROC.NATL.ACAD.SCI. USA, vol. 77, 1980, pages 7380 - 7384 |
| PROC.NATL.ACAD.SCI. USA, vol. 84, 1987, pages 7413 - 7417 |
| PROC.NATL.ACAD.SCI. USA, vol. 87, 1990, pages 3410 - 3414 |
| PROC.NATL.ACAD.SCI. USA, vol. 87, 1990, pages 4033 - 4037 |
| PROC.NATL.ACAD.SCI. USA, vol. 87, 1991, pages 3655 - 3659 |
| PROC.NATL.ACAD.SCI. USA, vol. 88, 1991, pages 4255 - 4259 |
| PROC.NATL.ACAD.SCI. USA, vol. 88, 1991, pages 8850 - 8854 |
| PROC.NATL.ACAD.SCI.USA, vol. 101, 2004, pages 2999 - 3004 |
| PROC.NATL.ACAD.SCI.USA, vol. 102, 2005, pages 3627 - 3632 |
| PROC.NATL.ACAD.SCI.USA, vol. 99, 2002, pages 15524 - 15529 |
| RNA, vol. 9, 2003, pages 277 - 279 |
| S. E. HAYNESWORTH ET AL., BONE, vol. 13, 1992, pages 81 |
| SAIBO KOGAK, vol. 16, 1997, pages 1463 - 1473 |
| SAIBO KOGAKU, vol. 16, 1997, pages 1463 |
| SAIBO KOGAKU, vol. 16, 1997, pages 1463 - 1473 |
| SCIENCE, vol. 209, 1980, pages 1414 - 1422 |
| SCIENCE, vol. 224, 1984, pages 994 - 996 |
| SCIENCE, vol. 247, 1990, pages 1465 - 1468 |
| SCIENCE, vol. 249, 1990, pages 1285 - 1288 |
| SCIENCE, vol. 284, 1999, pages 143 - 147 |
| SCIENCE, vol. 294, 2001, pages 853 - 858 |
| SCIENCE, vol. 294, 2001, pages 858 - 862 |
| SCIENCE, vol. 303, 2004, pages 83 - 86 |
| See also references of EP2123752A4 |
| SEMIN. ONCOL., vol. 11, 1984, pages 285 - 298 |
| STEM, CELLS, vol. 21, 2003, pages 105 - 110 |
| TRENDS GENET, vol. 7, 1991, pages 314 |
| TRENDS GENET., vol. 7, 1991, pages 5 |
| TRENDS IN BIOTECHNOLOGY, vol. 10, 1992, pages 132 |
| TRENDS IN BIOTECHNOLOGY, vol. 10, 1992, pages 152 |
| TRENDS IN BIOTECHNOLOGY, vol. 10, 1992, pages 87 |
| TRENDS IN BIOTECHNOLOGY, vol. 16, 1998, pages 438 |
| VIROLOGY, vol. 52, 1973, pages 456 - 467 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018023367A (ja) * | 2008-10-03 | 2018-02-15 | プロカルタ バイオシステムズ リミテッド | 転写因子デコイ |
| CN113999852A (zh) * | 2021-11-30 | 2022-02-01 | 杭州市富阳区第一人民医院 | circ_0001772作为结直肠癌诊断和治疗标志物的应用 |
| CN113999852B (zh) * | 2021-11-30 | 2024-04-02 | 杭州市富阳区第一人民医院 | circ_0001772作为结直肠癌诊断和治疗标志物的应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2008084319A3 (ja) | 2008-09-25 |
| US20100099746A1 (en) | 2010-04-22 |
| EP2123752A4 (en) | 2010-08-11 |
| JPWO2008084319A1 (ja) | 2010-04-30 |
| EP2123752A2 (en) | 2009-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2008084319A2 (ja) | 新規核酸 | |
| US20230295631A1 (en) | Micrornas and methods of their use | |
| Kuhn et al. | Chromosome 21-derived microRNAs provide an etiological basis for aberrant protein expression in human Down syndrome brains | |
| Mor et al. | Species-specific microRNA roles elucidated following astrocyte activation | |
| CN107454843B (zh) | 包含微小核糖核酸作为活性成分的用于治疗癌症的药物组合物 | |
| EP2374884A2 (en) | Human miRNAs isolated from mesenchymal stem cells | |
| Ng et al. | Dysregulated microRNAs affect pathways and targets of biologic relevance in nasal-type natural killer/T-cell lymphoma | |
| Yi et al. | A skin microRNA promotes differentiation by repressing ‘stemness’ | |
| Lui et al. | Patterns of known and novel small RNAs in human cervical cancer | |
| Velu et al. | Gfi1 regulates miR-21 and miR-196b to control myelopoiesis | |
| Wahid et al. | MicroRNAs: synthesis, mechanism, function, and recent clinical trials | |
| US9388466B2 (en) | Precursor miRNA loop-modulated target regulation | |
| Zhan et al. | MicroRNA expression dynamics during murine and human erythroid differentiation | |
| US9953131B2 (en) | Multi-targeting short interfering RNAs | |
| JP6081798B2 (ja) | miRNAに関連する癌を検出および処置するための方法および組成物およびmiRNAインヒビターおよび標的 | |
| JPWO2009044899A1 (ja) | 細胞の増殖を制御する核酸 | |
| CN102892897A (zh) | 用于肺癌的微rna表达谱分析的组合物和方法 | |
| EP2298359A1 (en) | Nucleic acid capable of controlling degranulation of mast cell | |
| Hinton et al. | sRNA-seq analysis of human embryonic stem cells and definitive endoderm reveals differentially expressed microRNAs and novel IsomiRs with distinct targets | |
| Liu et al. | miR-371-5p down-regulates pre mRNA processing factor 4 homolog B (PRPF4B) and facilitates the G1/S transition in human hepatocellular carcinoma cells | |
| JP2011093892A (ja) | がん抑制的マイクロrnaを含む腫瘍増殖抑制剤 | |
| CN102770561B (zh) | 用于诊断不同亚型肺癌的基于组织的微-rna方法 | |
| WO2011111715A1 (ja) | 細胞周期を制御する核酸 | |
| CN115666590A (zh) | 口腔鳞癌相关生物标志物及诊断和治疗方法 | |
| CN111575381A (zh) | 生物标志物的新用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 2007859120 Country of ref document: EP |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 07859120 Country of ref document: EP Kind code of ref document: A2 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2008552924 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12519960 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |