WO2007101782A1 - Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung - Google Patents
Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung Download PDFInfo
- Publication number
- WO2007101782A1 WO2007101782A1 PCT/EP2007/051589 EP2007051589W WO2007101782A1 WO 2007101782 A1 WO2007101782 A1 WO 2007101782A1 EP 2007051589 W EP2007051589 W EP 2007051589W WO 2007101782 A1 WO2007101782 A1 WO 2007101782A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- general formula
- tetrahydrofuran
- compound
- group
- tetrahydropyran
- Prior art date
Links
- 0 *Oc(c(O*)c1)cc2c1N=CNC2=O Chemical compound *Oc(c(O*)c1)cc2c1N=CNC2=O 0.000 description 1
- ZJAMETKUFMIJQD-PXYINDEMSA-N C=[O](C1COCC1)c(cc(c1c2)N=CNC1=O)c2O[C@@H]1COCC1 Chemical compound C=[O](C1COCC1)c(cc(c1c2)N=CNC1=O)c2O[C@@H]1COCC1 ZJAMETKUFMIJQD-PXYINDEMSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
- C07D239/72—Quinazolines; Hydrogenated quinazolines
- C07D239/86—Quinazolines; Hydrogenated quinazolines with hetero atoms directly attached in position 4
- C07D239/94—Nitrogen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
Definitions
- Bicyclic heterocycles medicaments containing these compounds, their use and processes for their preparation
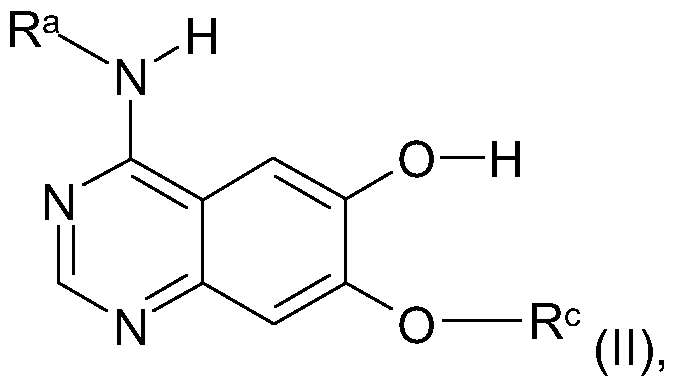
- the present invention relates to bicyclic heterocycles of the general formula
- R a represents a 3-chloro-2-fluoro-phenyl, 3-chloro-4-fluoro-phenyl or 3-ethynylphenyl group,
- R b is a tetrahydrofuran-3-yl, tetrahydropyran-3-yl or tetrahydropyran-4-yl group, and
- R c is a tetrahydrofuran-3-yl, tetrahydropyran-3-yl or tetrahydropyran-4-yl group, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally their pharmacologically acceptable acid addition salts, solvates and hydrates, preferably their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally their pharmacologically acceptable acid addition salts.
- the compounds of the general formula (I) can be prepared, for example, by the following processes:
- R a and R c are defined as mentioned above, with a compound of the general formula
- R b is defined as mentioned above and Z 1 represents a leaving group such as a halogen atom, for example a chlorine or bromine atom, a sulfonyloxy group such as a methanesulfonyloxy or p-toluenesulfonyloxy or a hydroxy group.
- Z 1 represents a leaving group such as a halogen atom, for example a chlorine or bromine atom, a sulfonyloxy group such as a methanesulfonyloxy or p-toluenesulfonyloxy or a hydroxy group.
- reaction is conveniently carried out in a solvent such as ethanol, isopropanol, acetonitrile, toluene, tetrahydrofuran, dioxane, dimethylformamide, dimethyl sulfoxide or N-methylpyrrolidinone, if appropriate in the presence of a base as potassium carbonate or N-ethyl-diisopropylamine, at temperatures ranging from 20 0 C to 160 0 C, preferably at temperatures ranging from 40 ° C to 120 0 C.
- a solvent such as ethanol, isopropanol, acetonitrile, toluene, tetrahydrofuran, dioxane, dimethylformamide, dimethyl sulfoxide or N-methylpyrrolidinone
- the reaction is carried out in the presence of a dehydrating agent, preferably in the presence of a phosphine and an azodicarboxylic acid derivative such as triphenylphosphine / Azodicarbonklarediethylester, conveniently in a solvent such as methylene chloride, acetonitrile, tetrahydrofuran, dioxane, toluene or Ethylenglycoldiethylether at temperatures in the range of -50 to 150 0 C, but preferably at temperatures in the range of 0 to 80 0 C performed.
- a dehydrating agent preferably in the presence of a phosphine and an azodicarboxylic acid derivative such as triphenylphosphine / Azodicarbonklathylester
- a solvent such as methylene chloride, acetonitrile, tetrahydrofuran, dioxane, toluene or Ethylenglycoldieth
- R a and R b are as defined above, with a compound of the general formula
- R c and Z 1 are defined as mentioned above.
- reaction is conveniently carried out in a solvent such as ethanol, isopropanol, acetonitrile, toluene, tetrahydrofuran, dioxane, dimethylformamide, dimethyl sulfoxide or N-methylpyrrolidinone, if appropriate in the presence of a base as potassium carbonate or N-ethyl-diisopropylamine, at temperatures ranging from 20 0 C to 160 0 C, preferably at temperatures ranging from 40 ° C to 120 0 C.
- a solvent such as ethanol, isopropanol, acetonitrile, toluene, tetrahydrofuran, dioxane, dimethylformamide, dimethyl sulfoxide or N-methylpyrrolidinone
- the reaction is carried out in the presence of a dehydrating agent, preferably in the presence of a phosphine and an azodicarboxylic acid derivative such as triphenylphosphine / Azodicarbonklarediethylester, conveniently in a solvent such as methylene chloride, acetonitrile, tetrahydrofuran, dioxane, toluene or Ethylenglycoldiethylether at temperatures in the range of -50 to 150 0 C, but preferably at temperatures in the range of 0 to 80 0 C performed.
- a dehydrating agent preferably in the presence of a phosphine and an azodicarboxylic acid derivative such as triphenylphosphine / Azodicarbonklathylester
- a solvent such as methylene chloride, acetonitrile, tetrahydrofuran, dioxane, toluene or Ethylenglycoldieth
- R a is as defined above, with a compound of the general formula
- Z 1 is defined as mentioned above and R d represents a tetrahydrofuran-3-yl, tetrahydropyran-3-yl or tetrahydropyran-4-yl group.
- reaction is conveniently carried out in a solvent such as ethanol, isopropanol, acetonitrile, toluene, tetrahydrofuran, dioxane, dimethylformamide, dimethyl sulfoxide or N-methylpyrrolidinone, if appropriate in the presence of a base as potassium carbonate or N-ethyl-diisopropylamine, at temperatures ranging from 20 0 C to 160 0 C, preferably at temperatures ranging from 40 ° C to 120 0 C.
- a solvent such as ethanol, isopropanol, acetonitrile, toluene, tetrahydrofuran, dioxane, dimethylformamide, dimethyl sulfoxide or N-methylpyrrolidinone
- the reaction is carried out in the presence of a dehydrating agent, preferably in the presence of a phosphine and an azodicarboxylic acid derivative such as triphenylphosphine / Azodicarbonklarediethylester, conveniently in a solvent such as methylene chloride, acetonitrile, tetrahydrofuran, dioxane, toluene or Ethylenglycoldiethylether at temperatures in the range of -50 to 150 0 C, but preferably at temperatures in the range of 0 to 80 0 C performed.
- a dehydrating agent preferably in the presence of a phosphine and an azodicarboxylic acid derivative such as triphenylphosphine / Azodicarbonklathylester
- a solvent such as methylene chloride, acetonitrile, tetrahydrofuran, dioxane, toluene or Ethylenglycoldieth
- a halogenating agent for example an acid halide such as thionyl chloride, thionyl bromide, phosphorus trichloride, phosphorus pentachloride or phosphorus oxychloride to form an intermediate of the general formula (IX),
- R b and R c are defined as mentioned above and Z 2 represents a halogen atom, such as a chlorine or bromine atom, and subsequent reaction with a compound of the general formula (X)
- the reaction with the halogenating agent is optionally carried out in a solvent such as methylene chloride, chloroform, acetonitrile or toluene and optionally in the presence of a base such as N, N-diethylaniline or N-ethyl-diisopropylamine at temperatures in the range of 20 0 C to 160 0 C, preferably carried out from 40 ° C to 120 0 C.
- the reaction is carried out with thionyl chloride and catalytic amounts of dimethylformamide at the boiling temperature of the reaction mixture, wherein the reaction can also be carried out with the addition of acetonitrile as the solvent.
- reaction of the compound of general formula (IX) with a compound of general formula (X) is conveniently carried out in a solvent such as ethanol, isopropanol, acetonitrile, dioxane or dimethylformamide, optionally in the presence of a base such as potassium carbonate or N-ethyl-diisopropylamine Temperatures in the range of 20 ° C and 160 ° C, preferably from 60 0 C to 120 ° C. Preferably, however, the reaction is carried out in isopropanol at the boiling temperature of the reaction mixture.
- a solvent such as ethanol, isopropanol, acetonitrile, dioxane or dimethylformamide
- a base such as potassium carbonate or N-ethyl-diisopropylamine
- the obtained compounds of the general formula (I) can be separated into their diastereomers, for example by chromatographic methods.
- the compounds of the formula (I) obtained can be converted into their salts, in particular for the pharmaceutical application, into their physiologically tolerated salts with inorganic or organic acids.
- acids for this example hydrochloric acid, hydrobromic acid, sulfuric acid, methanesulfonic acid, phosphoric acid, Fumaric acid, succinic acid, lactic acid, citric acid, tartaric acid or maleic acid into consideration.
- the compounds of the general formula (I) according to the invention and their physiologically tolerable salts have valuable pharmacological properties, in particular an inhibitory effect on the signal transduction mediated by the epidermal growth factor receptor (EGF-R), which is inhibited, for example, by inhibition of ligand binding Receptor dimerization or the tyrosine kinase itself can be effected.
- EGF-R epidermal growth factor receptor
- the inhibition of the human EGF receptor kinase was determined with the aid of the cytoplasmic tyrosine kinase domain (methionine 664 to alanine 1186 based on the sequence published in Nature 309 (1984), 418).
- the protein was expressed in Sf9 insect cells as a GST fusion protein using the baculovirus expression system.
- the measurement of enzyme activity was carried out in the presence or absence of the test compounds in serial dilutions.
- the polymer pEY (4: 1) from SIGMA was used as a substrate.
- Biotinylated pEY (bio-pEY) was added as a tracer substrate.
- Each 100 ⁇ l reaction solution contained 10 ⁇ l of the inhibitor in 50% DMSO, 20 ⁇ l of the substrate solution (200 mM HEPES pH 7.4, 50 mM magnesium acetate, 2.5 mg / ml poly (EY), 5 ⁇ g / ml bio-pEY) and 20 ⁇ l enzyme preparation.
- the enzyme reaction was made by adding 50 ⁇ l of a 100 ⁇ M ATP solution started in 10 mM magnesium chloride.
- the dilution of the enzyme preparation was adjusted so that the phosphate incorporation into the bio-pEY was linear in terms of time and amount of enzyme.
- the enzyme preparation was diluted in 20 mM HEPES pH 7.4, 1 mM EDTA, 130 mM saline, 0.05% Triton X-100, 1 mM DTT and 10% glycerol.
- the enzyme assays were performed at room temperature for a period of 30 minutes and terminated by addition of 50 ⁇ l of a stop solution (250 mM EDTA in 20 mM HEPES pH 7.4). 100 ⁇ l was placed on a streptavidin-coated microtiter plate and incubated for 60 minutes at room temperature. Thereafter, the plate was washed with 200 ⁇ l of a washing solution (50 mM Tris, 0.05% Tween 20). After addition of 100 ⁇ l of an HRPO-labeled anti-PY antibody (PY20H anti-PTyr: HRP from Transduction Laboratories, 250 ng / ml) was incubated for 60 minutes.
- a stop solution 250 mM EDTA in 20 mM HEPES pH 7.4
- 100 ⁇ l was placed on a streptavidin-coated microtiter plate and incubated for 60 minutes at room temperature. Thereafter, the plate was washed with 200 ⁇ l of a washing solution (
- microtiter plate was washed three times with 200 ul of washing solution.
- the data were fit by means of an iterative calculation using a sigmoid curve analysis program (Graph Päd Prism Version 3.0) with variable hill slope. All released iterative data had a correlation coefficient above 0.9 and the upper and lower values of the curves showed a spread of at least a factor of 5. From the curves, the drug concentration was derived, which inhibits the activity of the EGF receptor kinase by 50% (IC50) , The compounds according to the invention have IC 50 values of less than 100 ⁇ M.
- the compounds of the general formula I according to the invention thus inhibit the signal transduction by tyrosine kinases, as shown by the example of the human EGF receptor, and are therefore useful for the treatment of pathophysiological processes which are caused by hyperfunction of tyrosine kinases.
- pathophysiological processes which are caused by hyperfunction of tyrosine kinases.
- tyrosine kinases are, for example, benign or malignant tumors, in particular Tumors of epithelial and neuroepithelial origin, metastasis and abnormal proliferation of vascular endothelial cells (neoangiogenesis).
- the compounds of the invention are also useful for the prevention and treatment of respiratory and pulmonary diseases associated with increased or altered mucus production caused by stimulation of tyrosine kinases, e.g. in inflammatory diseases
- Respiratory tracts such as acute bronchitis, chronic bronchitis, chronic obstructive
- Bronchitis COPD
- asthma bronchiectasis
- allergic or non-allergic rhinitis or sinusitis nasal polyps
- cystic fibrosis ⁇ 1-antitrypsin deficiency
- hyperreactive airways pulmonary emphysema, pulmonary fibrosis and hyperreactive airways.
- the compounds are also useful in the treatment of inflammatory diseases of the gastrointestinal tract and the bile ducts and bladder associated with impaired activity of the tyrosine kinases, e.g. in acute or chronic inflammatory changes, such as cholecystitis, Crohn's disease, ulcerative colitis, and ulcers or polyposis in the gastrointestinal tract or as they occur in diseases of the gastrointestinal tract, which are associated with increased secretion such as M. Menetrier, secreting adenomas and protein loss syndromes,
- inflammatory diseases of the joints such as rheumatoid arthritis
- inflammatory diseases of the skin, eyes in inflammatory pseudopolyps, in colitis cystica profunda or in pneumatosis cystoides intestinales.
- the compounds are also contemplated for the treatment of CNS and spinal cord injuries.
- Preferred areas of application include inflammatory diseases of the respiratory organs or of the intestine, such as chronic bronchitis (COPD), chronic sinusitis, asthma, Crohn's disease, ulcerative colitis or polyposis of the intestine.
- COPD chronic bronchitis
- Particularly preferred indications are inflammatory diseases of the respiratory tract or the lungs, such as chronic bronchitis (COPD) or asthma or nasal polyps.
- the compounds of general formula (I) and their physiologically acceptable salts may be used for the treatment of other diseases caused by aberrant function of tyrosine kinases, e.g. epidermal hyperproliferation (psoriasis), benign prostatic hyperplasia (BPH), inflammatory processes, diseases of the immune system, hyperproliferation of hematopoietic cells, etc ..
- tyrosine kinases e.g. epidermal hyperproliferation (psoriasis), benign prostatic hyperplasia (BPH), inflammatory processes, diseases of the immune system, hyperproliferation of hematopoietic cells, etc .
- the compounds of the invention can be used alone or in combination with other pharmacologically active compounds, for example in tumor therapy in monotherapy or in combination with other anti-tumor therapeutics, for example in combination with topoisomerase inhibitors (eg etoposide), mitotic inhibitors (eg, vinblastine), nucleic acid-interacting compounds (eg, cisplatin, cyclophosphamide, adriamycin), hormone antagonists (eg, tamoxifen), inhibitors of metabolic processes (eg, 5-FU, etc.), cytokines (eg, interferons), antibodies, etc.
- topoisomerase inhibitors eg etoposide
- mitotic inhibitors eg, vinblastine
- nucleic acid-interacting compounds eg, cisplatin, cyclophosphamide, adriamycin
- hormone antagonists eg, tamoxifen
- inhibitors of metabolic processes eg, 5-FU, etc.
- these compounds alone or in combination with other respiratory therapies, such as secretolytically (e.g., ambroxol, N-acetylcysteine), broncholytically (e.g., tiotropium or ipratropium or fenoterol, salmeterol, salbutamol) and / or anti-inflammatory (e.g., theophylline or glucocorticoids) substances.
- secretolytically e.g., ambroxol, N-acetylcysteine
- broncholytically e.g., tiotropium or ipratropium or fenoterol, salmeterol, salbutamol
- anti-inflammatory e.g., theophylline or glucocorticoids
- the compounds according to the invention are generally used in warm-blooded vertebrates, in particular in humans, in dosages of 0.001-100 mg / kg body weight, preferably at 0.1-15 mg / kg.
- these are administered with one or more conventional inert carriers and / or diluents, e.g.
- lactose cane sugar, microcrystalline cellulose, magnesium stearate, polyvinylpyrrolidone, citric acid, tartaric acid, water, water / ethanol, water / glycerin, water / sorbitol, water / polyethylene glycol, propylene glycol, stearyl alcohol, carboxymethyl cellulose or fatty substances such as hard fat or their suitable mixtures in usual galenic preparations such as tablets, dragees, capsules, powders, suspensions, solutions, sprays or suppositories incorporated.
- composition 1 Drageekern contains: Active substance 75.0 mg
- the active substance is mixed with calcium phosphate, corn starch, polyvinylpyrrolidone, hydroxypropylmethylcellulose and half of the stated amount of magnesium stearate.
- a tableting machine compacts are produced with a diameter of about 13 mm, these are ground on a suitable machine through a sieve with 1.5 mm mesh size and mixed with the remaining amount of magnesium stearate. This granulate is pressed on a tabletting machine into tablets of the desired shape.
- coated dragee cores are coated with a film consisting essentially of hydroxypropylmethylcellulose.
- the finished film dragees are shined with beeswax.
- Composition 1 tablet contains:
- Active ingredient, lactose and starch are mixed and uniformly moistened with an aqueous solution of polyvinylpyrrolidone. After screening of the moist mass (2.0 mm mesh size) and drying in a rack oven at 50 0 C is again sieved (1.5 mm mesh) and the lubricant mixed. The ready-to-use mixture is processed into tablets.
- Tablet weight 220 mg Diameter: 10 mm, biplan with facet on both sides and one-sided part notch.
- Composition 1 tablet contains:
- the active substance mixed with milk sugar, corn starch and silica is moistened with a 20% strength aqueous solution of polyvinylpyrrolidone and beaten through a sieve with a mesh size of 1.5 mm.
- the granules dried at 45 ° C are again rubbed through the same sieve and mixed with the stated amount of magnesium stearate. From the mixture tablets are pressed.
- Composition 1 capsule contains:
- the active ingredient is mixed with the excipients, passed through a sieve of 0.75 mm mesh size and mixed homogeneously in a suitable device.
- the final mixture is filled into size 1 hard gelatin capsules.
- Capsule filling approx. 320 mg capsule shell: hard gelatine capsule size 1.
- Composition 1 suppository contains:
- Polyethylene glycol 1500 550.0 mg
- the active ingredient is distributed homogeneously therein and the melt is poured into pre-cooled molds.
- Carboxymethylcellulose Na salt 0.10 g p-hydroxybenzoic acid methyl ester 0.05 g p-hydroxybenzoic acid propyl ester 0.01 g
- Distilled water is heated to 70 0 C.
- p-hydroxybenzoic acid methyl ester and propyl ester and glycerol and carboxymethyl cellulose sodium salt are dissolved with stirring. It is cooled to room temperature and added with stirring, the active ingredient and dispersed homogeneously. After addition and dissolution of the sugar, the sorbitol solution and the aroma, the suspension is evacuated to vent with stirring.
- 5 ml of suspension contain 50 mg of active ingredient.
- the active ingredient is dissolved in the required amount of 0.01 N HCl, isotonic with saline, sterile filtered and filled into 2 ml ampoules.
- Active ingredient 50.0 mg 0.01 n hydrochloric acid s.g.
- the active ingredient is dissolved in the required amount 0.01 N HCl, made isotonic with sodium chloride, sterile filtered and filled into 10 ml ampoules.
- 1 capsule contains:
- the active substance is mixed with lactose for inhalation purposes.
- the mixture is filled into capsules on a capsule machine (weight of the empty capsule approx. 50 mg).
- 1 hub contains:
- the active substance and benzalkonium chloride are dissolved in ethanol / water (50/50).
- the pH of the solution is adjusted with 1 N hydrochloric acid.
- the adjusted solution is filtered and filled into containers suitable for the hand nebulizer (cartridges).
Abstract
Die vorliegende Erfindung betrifft bicyclische Heterocyclen der allgemeinen Formel (I), deren Tautomere, deren Stereoisomere, deren Gemische und deren Salze, insbesondere deren physiologisch verträgliche Salze mit anorganischen oder organischen Säuren, welche wertvolle pharmakologische Eigenschaften aufweisen, insbesondere eine Hemmwirkung auf die durch Tyrosinkinasen vermittelte Signaltransduktion, deren Verwendung zur Behandlung von Krankheiten, insbesondere von Tumorerkrankungen sowie der benignen Prostatahyperplasie (BPH), von Erkrankungen der Lunge und der Atemwege und deren Herstellung.
Description
Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung
Gegenstand der vorliegenden Erfindung sind bicyclische Heterocyclen der allgemeinen Formel
deren Tautomere, deren Stereoisomere, deren Gemische und deren Salze, insbesondere deren physiologisch verträgliche Salze mit anorganischen oder organischen Säuren, welche wertvolle pharmakologische Eigenschaften aufweisen, insbesondere eine Hemmwirkung auf die durch Tyrosinkinasen vermittelte Signaltransduktion, deren Verwendung zur Behandlung von Krankheiten, insbesondere von Tumorerkrankungen sowie der benignen Prostatahyperplasie (BPH), von Erkrankungen der Lunge und der Atemwege und deren Herstellung.
In der obigen allgemeinen Formel (I) bedeuten
Ra eine 3-Chlor-2-fluor-phenyl-, 3-Chlor-4-fluor-phenyl- oder 3-Ethinylphenyl- Gruppe,
Rb eine Tetrahydrofuran-3-yl-, Tetrahydropyran-3-yl- oder Tetrahydropyran-4-yl- Gruppe, und
Rc eine Tetrahydrofuran-3-yl-, Tetrahydropyran-3-yl- oder Tetrahydropyran-4-yl- Gruppe,
gegebenenfalls in Form ihrer Tautomeren, ihrer Racemate, ihrer Enantiomere, ihrer Diastereomere und ihrer Gemische, sowie gegebenenfalls ihrer pharmakologisch unbedenklichen Säureadditionssalze, Solvate und Hydrate, vorzugsweise ihrer Tautomeren, ihrer Racemate, ihrer Enantiomere, ihrer Diastereomere und ihrer Gemische, sowie gegebenenfalls ihrer pharmakologisch unbedenklichen Säureadditionssalze.
Die Verbindungen der allgemeinen Formel (I) lassen sich beispielsweise nach folgenden Verfahren herstellen:
a) Umsetzung einer Verbindung der allgemeinen Formel
Ra und Rc wie eingangs erwähnt definiert sind, mit einer Verbindung der allgemeinen Formel
Z1 - Rb
in der
Rb wie eingangs erwähnt definiert ist und Z1 eine Austrittsgruppe wie ein Halogenatom, z.B. ein Chlor- oder Bromatom, eine Sulfonyloxygruppe wie eine Methansulfonyloxy- oder p-Toluolsulfonyloxygruppe oder eine Hydroxygruppe darstellt.
Die Umsetzung erfolgt zweckmäßigerweise in einem Lösungsmittel wie Ethanol, Isopropanol, Acetonitril, Toluol, Tetrahydrofuran, Dioxan, Dimethylformamid, Dimethylsulfoxid oder N-Methylpyrrolidinon, gegebenfalls in Gegenwart einer Base
wie Kaliumcarbonat oder N-Ethyl-diisopropylamin, bei Temperaturen im Bereich von 200C bis 1600C, vorzugsweise bei Temperaturen im Bereich von 40°C bis 1200C. Mit einer Verbindung der allgemeinen Formel (III), in der Z1 eine Hydroxygruppe darstellt, wird die Umsetzung in Gegenwart eines wasserentziehenden Mittels, vorzugsweise in Gegenwart eines Phosphins und eines Azodicarbonsäurederivates wie z.B. Triphenylphosphin/Azodicarbonsäurediethylester, zweckmäßigerweise in einem Lösungsmittel wie Methylenchlorid, Acetonitril, Tetrahydrofuran, Dioxan, Toluol oder Ethylenglycoldiethylether bei Temperaturen im Bereich von -50 bis 1500C, vorzugsweise jedoch bei Temperaturen im Bereich von 0 bis 800C, durchgeführt.
b) Umsetzung einer Verbindung der allgemeinen Formel
Ra und Rb wie eingangs erwähnt definiert sind, mit einer Verbindung der allgemeinen Formel
Z1 - Rc (V),
in der
Rc und Z1 wie eingangs erwähnt definiert sind.
Die Umsetzung erfolgt zweckmäßigerweise in einem Lösungsmittel wie Ethanol, Isopropanol, Acetonitril, Toluol, Tetrahydrofuran, Dioxan, Dimethylformamid, Dimethylsulfoxid oder N-Methylpyrrolidinon, gegebenfalls in Gegenwart einer Base
wie Kaliumcarbonat oder N-Ethyl-diisopropylamin, bei Temperaturen im Bereich von 200C bis 1600C, vorzugsweise bei Temperaturen im Bereich von 40°C bis 1200C. Mit einer Verbindung der allgemeinen Formel (III), in der Z1 eine Hydroxygruppe darstellt, wird die Umsetzung in Gegenwart eines wasserentziehenden Mittels, vorzugsweise in Gegenwart eines Phosphins und eines Azodicarbonsäurederivates wie z.B. Triphenylphosphin/Azodicarbonsäurediethylester, zweckmäßigerweise in einem Lösungsmittel wie Methylenchlorid, Acetonitril, Tetrahydrofuran, Dioxan, Toluol oder Ethylenglycoldiethylether bei Temperaturen im Bereich von -50 bis 1500C, vorzugsweise jedoch bei Temperaturen im Bereich von 0 bis 800C, durchgeführt.
c) Umsetzung einer Verbindung der allgemeinen Formel
Ra wie eingangs erwähnt definiert ist, mit einer Verbindung der allgemeinen Formel
Z1 - Rd (VII),
in der
Z1 wie eingangs erwähnt definiert ist und Rd eine Tetrahydrofuran-3-yl-, Tetrahydropyran-3-yl- oder Tetrahydropyran-4-yl-Gruppe darstellt.
Die Umsetzung erfolgt zweckmäßigerweise in einem Lösungsmittel wie Ethanol, Isopropanol, Acetonitril, Toluol, Tetrahydrofuran, Dioxan, Dimethylformamid, Dimethylsulfoxid oder N-Methylpyrrolidinon, gegebenfalls in Gegenwart einer Base
wie Kaliumcarbonat oder N-Ethyl-diisopropylamin, bei Temperaturen im Bereich von 200C bis 1600C, vorzugsweise bei Temperaturen im Bereich von 40°C bis 1200C. Mit einer Verbindung der allgemeinen Formel (III), in der Z1 eine Hydroxygruppe darstellt, wird die Umsetzung in Gegenwart eines wasserentziehenden Mittels, vorzugsweise in Gegenwart eines Phosphins und eines Azodicarbonsäurederivates wie z.B. Triphenylphosphin/Azodicarbonsäurediethylester, zweckmäßigerweise in einem Lösungsmittel wie Methylenchlorid, Acetonitril, Tetrahydrofuran, Dioxan, Toluol oder Ethylenglycoldiethylether bei Temperaturen im Bereich von -50 bis 1500C, vorzugsweise jedoch bei Temperaturen im Bereich von 0 bis 800C, durchgeführt.
d) Umsetzung einer Verbindung der allgemeinen Formel (VIII)
in der Rb und Rc wie eingangs erwähnt definiert sind, mit einem Halogenierungsmittel, beispielsweise einem Säurehalogenid wie Thionylchlorid, Thionylbromid, Phosphortrichlorid, Phosphorpentachlorid oder Phorphoroxychlorid zu einer Zwischenverbindung der allgemeinen Formel (IX),
in der Rb und Rc wie eingangs erwähnt definiert sind und Z2 ein Halogenatom wie ein Chlor- oder Bromatom darstellt,
und anschließender Umsetzung mit einer Verbindung der allgemeinen Formel (X)
Ra - NH2 (X),
in der Ra wie eingangs erwähnt definiert ist.
Die Umsetzung mit dem Halogenierungsmittel wird gegebenfalls in einem Lösungsmittel wie Methylenchlorid, Chloroform, Acetonitril oder Toluol und gegebenfalls in Gegenwart einer Base wie N,N-Diethylanilin oder N-Ethyl- diisopropylamin bei Temperaturen im Bereich von 200C bis 1600C, vorzugsweise von 40°C bis 1200C durchgeführt. Vorzugsweise wird die Reaktion jedoch mit Thionylchlorid und katalytischen Mengen an Dimethylformamid bei der Siedetemperatur des Reaktionsgemisches durchgeführt, wobei die Reaktion auch unter Zusatz von Acetonitril als Lösemittel durchgeführt werden kann. Die Umsetzung der Verbindung der allgemeinen Formel (IX) mit einer Verbindung der allgemeinen Formel (X) erfolgt zweckmäßigerweise in einem Lösungsmittel wie Ethanol, Isopropanol, Acetonitril, Dioxan oder Dimethylformamid, gegebenfalls in Gegenwart einer Base wie Kaliumcarbonat oder N-Ethyl-diisopropylamin, bei Temperaturen im Bereich von 20°C und 160°C, vorzugsweise von 600C bis 120°C. Vorzugsweise wird die Reaktion jedoch in Isopropanol bei der Siedetemperatur des Reaktionsgemisches durchgeführt.
Die erhaltenen Verbindungen der allgemeinen Formel (I) können in ihre Diastereomeren aufgetrennt werden, beispielsweise durch chromatographische Methoden.
Desweiteren können die erhaltenen Verbindungen der Formel (I) in ihre Salze, insbesondere für die pharmazeutische Anwendung in ihre physiologisch verträglichen Salze mit anorganischen oder organischen Säuren, übergeführt werden. Als Säuren kommen hierfür beispielsweise Salzsäure, Bromwasserstoffsäure, Schwefelsäure, Methansulfonsäure, Phosphorsäure,
Fumarsäure, Bernsteinsäure, Milchsäure, Zitronensäure, Weinsäure oder Maleinsäure in Betracht.
Die als Ausgangsstoffe verwendeten Verbindungen der allgemeinen Formeln (II) bis (X) sind teilweise literaturbekannt oder können nach an sich literaturbekannten Verfahren (siehe Beispiele I bis VII), gegebenenfalls unter zusätzlicher Einführung von Schutzresten, erhalten werden.
Verbindungen der allgemeinen Formel Il und IV können beispielsweise wie in WO 02/018351 , WO 02/018372 oder WO 03/082290 beschrieben, erhalten werden.
Die erfindungsgemäßen Verbindungen der allgemeinen Formel (I) und ihre physiologisch verträglichen Salze weisen wertvolle pharmakologische Eigenschaften auf, insbesondere eine Hemmwirkung auf die durch den Epidermal Growth Factor- Rezeptor (EGF-R) vermittelte Signaltransduktion, wobei diese beispielsweise durch eine Inhibition der Ligandenbindung, der Rezeptordimerisierung oder der Tyrosinkinase selbst bewirkt werden kann. Außerdem ist es möglich, dass die Signalübertragung an weiter abwärtsliegenden Komponenten blockiert wird.
Die biologischen Eigenschaften der neuen Verbindungen werden wie folgt geprüft:
Die Hemmung der humanen EGF-Rezeptorkinase wurde mit Hilfe der cyto- plasmatischen Tyrosinkinase-Domäne (Methionin 664 bis Alanin 1186 basierend auf der in Nature 309 (1984), 418 publizierten Sequenz) bestimmt. Hierzu wurde das Protein in Sf9 Insektenzellen als GST-Fusionsprotein unter Verwendung des Baculovirus-Expressionssystems exprimiert.
Die Messung der Enzymaktivität wurde in Gegenwart oder Abwesenheit der Testverbindungen in seriellen Verdünnungen durchgeführt. Das Polymer pEY (4:1 ) von SIGMA wurde als Substrat verwendet. Biotinyliertes pEY (bio-pEY) wurde als Tracer-Substrat zugesetzt. Jede 100 μl Reaktionslösung enthielt 10 μl des Inhibitors in 50% DMSO, 20 μl der Substrat-Lösung (200 mM HEPES pH 7.4, 50 mM Magnesiumacetat, 2.5 mg/ml poly(EY), 5 μg/ml bio-pEY) und 20 μl Enzympräparation. Die Enzymreaktion wurde durch Zugabe von 50μl einer 100 μM
ATP Lösung in 10 mM Magnesiumchlorid gestartet. Die Verdünnung der Enzympräparation wurde so eingestellt, dass der Phosphat-Einbau in das bio-pEY hinsichtlich Zeit und Enzymmenge linear war. Die Enzympräparation wurde in 20 mM HEPES pH 7.4, 1 mM EDTA, 130 mM Kochsalz, 0.05% Triton X-100, 1 mM DTT und 10% Glycerin verdünnt.
Die Enzymassays wurden bei Raumtemperatur über einen Zeitraum von 30 Minuten ausgeführt und durch Zugabe von 50 μl einer Stopplösung (250 mM EDTA in 20 mM HEPES pH 7.4) beendet. 100 μl wurden auf eine Streptavidin-beschichtete Mikrotiterplatte gebracht und 60 Minuten bei Raumtemperatur inkubiert. Danach wurde die Platte mit 200 μl einer Waschlösung (50 mM Tris, 0.05% Tween 20) gewaschen. Nach Zugabe von 100 μl eines HRPO-gelabelten anti-PY Antikörpers (PY20H Anti-PTyr:HRP von Transduction Laboratories, 250 ng/ml) wurde 60 Minuten inkubiert. Danach wurde die Mikrotiterplatte dreimal mit je 200 μl Waschlösung gewaschen. Die Proben wurden dann mit 100 μl einer TMB-Peroxidase-Lösung (A:B = 1 :1 , Kirkegaard Perry Laboratories) versetzt. Nach 10 Minuten wurde die Reaktion gestoppt. Die Extinktion wurde bei OD45oπm mit einem ELISA-Leser gemessen. Alle Datenpunkte wurden als Triplikate bestimmt.
Die Daten wurden mittels einer iterativen Rechnung unter Verwendung eines Analysenprogrammes für sigmoidale Kurven (Graph Päd Prism Version 3.0) mit variabler Hill-Steigung angepaßt. Alle freigegebenen Iterationsdaten wiesen einen Korrelationskoeffizienten von über 0.9 auf und die Ober- und Unterwerte der Kurven zeigten eine Spreizung von mindestens einem Faktor von 5. Aus den Kurven wurde die Wirkstoffkonzentration abgeleitet, die die Aktivität der EGF-Rezeptorkinase zu 50% hemmt (IC50). Die erfindungsgemäßen Verbindungen weisen ICso-Werte von unter 100 μM auf.
Die erfindungsgemäßen Verbindungen der allgemeinen Formel I hemmen somit die Signaltransduktion durch Tyrosinkinasen, wie am Beispiel des humanen EGF- Rezeptors gezeigt wurde, und sind daher nützlich zur Behandlung pathophysiologischer Prozesse, die durch Überfunktion von Tyrosinkinasen hervorgerufen werden. Das sind z.B. benigne oder maligne Tumoren, insbesondere
Tumoren epithelialen und neuroepithelialen Ursprungs, Metastasierung sowie die abnorme Proliferation vaskulärer Endothelzellen (Neoangiogenese).
Die erfindungsgemäßen Verbindungen sind auch nützlich zur Vorbeugung und Behandlung von Erkrankungen der Atemwege und der Lunge, die mit einer vermehrten oder veränderten Schleimproduktion einhergehen, die durch Stimulation von Tyrosinkinasen hervorgerufen wird, wie z.B. bei entzündlichen Erkrankungen der
Atemwege wie akute Bronchitis, chronische Bronchitis, chronisch obstruktive
Bronchitis (COPD), Asthma, Bronchiektasien, allergische oder nicht-allergische Rhinitis oder Sinusitis, Nasenpolypen, zystische Fibrose, α1-Antitrypsin-Mangel, oder bei Husten, Lungenemphysem, Lungenfibrose und hyperreaktiven Atemwegen.
Die Verbindungen sind auch geeignet für die Behandlung entzündlicher Erkrankungen des Magen-Darm-Traktes und der Gallengänge und -blase, die mit einer gestörten Aktivität der Tyrosinkinasen einhergehen, wie sie z.B. bei akuten oder chronisch entzündlichen Veränderungen zu finden sind, wie Cholezystitis, M. Crohn, Colitis ulcerosa, und Geschwüren oder Polyposis im Magen-Darm-Trakt oder wie sie bei Erkrankungen des Magen-Darm-Traktes, die mit einer vermehrten Sekretion einhergehen, vorkommen, wie M. Menetrier, sezernierende Adenome und Proteinverlustsyndrome,
desweiteren zur Behandlung von entzündlichen Erkrankungen der Gelenke, wie rheumatoider Arthritis, von entzündlichen Erkrankungen der Haut, der Augen, bei entzündlichen Pseudopolypen, bei Colitis cystica profunda oder bei Pneumatosis cystoides intestinales. Die Verbindungen kommen auch zur Behandlung von ZNS- und Rückenmarksverletzungen in Betracht.
Als bevorzugte Anwendungsgebiete seien entzündliche Erkrankungen der Atemwegsorgane oder des Darmes genannt, wie chronische Bronchitis (COPD), chronische Sinusitis, Asthma, M. Crohn, Colitis ulcerosa oder Polyposis des Darmes.
Besonders bevorzugte Anwendungsgebiete sind entzündliche Erkrankungen der Atemwege oder der Lunge wie chronische Bronchitis (COPD) oder Asthma oder Nasenpolypen.
Außerdem können die Verbindungen der allgemeinen Formel (I) und deren physiologisch verträglichen Salze zur Behandlung anderer Krankheiten verwendet werden, die durch aberrante Funktion von Tyrosinkinasen verursacht werden, wie z.B. epidermaler Hyperproliferation (Psoriasis), benigner Prostatahyperplasie (BPH), inflammatorischer Prozesse, Erkrankungen des Immunsystems, Hyperproliferation hämatopoetischer Zellen, etc..
Auf Grund ihrer biologischen Eigenschaften können die erfindungsgemäßen Verbindungen allein oder in Kombination mit anderen pharmakologisch wirksamen Verbindungen angewendet werden, beispielsweise in der Tumortherapie in Monotherapie oder in Kombination mit anderen Anti-Tumor Therapeutika, beispielsweise in Kombination mit Topoisomerase-Inhibitoren (z.B. Etoposide), Mitoseinhibitoren (z.B. Vinblastin), mit Nukleinsäuren interagierenden Verbindungen (z.B. cis-Platin, Cyclophosphamid, Adriamycin), Hormon-Antagonisten (z.B. Tamoxifen), Inhibitoren metabolischer Prozesse (z.B. 5-FU etc.), Zytokinen (z.B. Interferonen), Antikörpern etc. Für die Behandlung von Atemwegserkrankungen können diese Verbindungen allein oder in Kombination mit anderen Atemwegstherapeutika, wie z.B. sekretolytisch (z.B. Ambroxol, N-Acetylcystein), broncholytisch (z.B. Tiotropium oder Ipratropium oder Fenoterol, Salmeterol, Salbutamol) und/oder entzündungshemmend (z.B. Theophylline oder Glucocorticoide) wirksamen Substanzen angewendet werden. Für die Behandlung von Erkrankungen im Bereich des Magen-Darm-Traktes können diese Verbindungen ebenfalls alleine oder in Kombination mit Motilitäts- oder Sekretions-beeinflussenden Substanzen gegeben werden. Diese Kombinationen können entweder simultan oder sequentiell verabreicht werden.
Die Anwendung dieser Verbindungen entweder alleine oder in Kombination mit anderen Wirkstoffen kann intravenös, subkutan, intramuskulär, intraperitoneal,
intranasal, durch Inhalation oder transdermal oder oral erfolgen, wobei zur Inhalation insbesondere Aerosolformulierungen geeignet sind.
Bei der pharmazeutischen Anwendung werden die erfindungsgemäßen Verbindungen in der Regel bei warmblütigen Wirbeltieren, insbesondere beim Menschen, in Dosierungen von 0.001-100 mg/kg Körpergewicht, vorzugsweise bei 0.1-15 mg/kg verwendet. Zur Verabreichung werden diese mit einem oder mehreren üblichen inerten Trägerstoffen und/oder Verdünnungsmitteln, z.B. mit Maisstärke, Milchzucker, Rohrzucker, mikrokristalliner Zellulose, Magnesiumstearat, Polyvinylpyrrolidon, Zitronensäure, Weinsäure, Wasser, Wasser/Ethanol, Wasser/Glycerin, Wasser/Sorbit, Wasser/Polyethylenglykol, Propylenglykol, Stearylalkohol, Carboxymethylcellulose oder fetthaltigen Substanzen wie Hartfett oder deren geeigneten Gemischen in übliche galenische Zubereitungen wie Tabletten, Dragees, Kapseln, Pulver, Suspensionen, Lösungen, Sprays oder Zäpfchen eingearbeitet.
Die nachfolgenden Beispiele sollen die vorliegende Erfindung näher erläutern ohne diese zu beschränken:
Herstellung der Ausgangsverbindungen:
Beispiel I
4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-hydroxy- chinazolin
a) 2-Nitro-4-benzyloxy-5-((S)-tetrahydrofuran-3-yloxy)-benzoesäure-benzylester:
Hergestellt durch Umsetzung von 6-Nitro-benzo[1 ,3]dioxol-5-carbonsäure mit (S)-3- Hydroxy-tetrahydrofuran in Gegenwart von Kalium-tert.-butanolat und anschließender Umsetzung des Reaktionsgemisches mit Benzylbromid. s. Beispiel VI (2), WO 03/082290 Massenspektrum (ESI+): m/z = 450 [M+H]+
b) 2-Amino-4-benzyloxy-5-((S)-tetrahydrofuran-3-yloxy)-benzoesäure-benzylester: Hergestellt durch katalytische Hydrierung von 2-Nitro-4-benzyloxy-5-((S)- tetrahydrofuran-3-yloxy)-benzoesäure-benzylester in Gegenwart von Raney-Nickel. s. Beispiel IV(1 ), WO 03/082290
Massenspektrum (ESI+): m/z = 420 [M+H]+
c) 6-((S)-Tetrahydrofuran-3-yloxy)-7-benzyloxy-3H-chinazolin-4-on: Hergestellt durch Umsetzung von 2-Amino-4-benzyloxy-5-((S)-tetrahydrofuran-3- yloxy)-benzoesäure-benzylester mit Formamidinacetat. s. Beispiel 111(1 ), WO 03/082290 Massenspektrum (ESI+): m/z = 339 [M+H]+
d) 4-Chlor-6-((S)-tetrahydrofuran-3-yloxy)-7-benzyloxy-chinazolin: Hergestellt durch Umsetzung von 6-((S)-Tetrahydrofuran-3-yloxy)-7-benzyloxy-3H- chinazolin-4-on mit Thionylchlorid in Gegenwart von N,N-Dimethylformamid in Acetonitril unter Rückfluß, s. Beispiel 11(1 ), WO 03/082290 Rf-Wert: 0.85 (Kieselgel, Essigester/Methanol = 9:1 )
e) 4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-benzyloxy- chinazolin-hydrochlorid:
Hergestellt durch Umsetzung von 4-Chlor-6-((S)-tetrahydrofuran-3-yloxy)-7- benzyloxy-chinazolin mit 3-Chlor-4-fluor-anilin in Isopropanol s. Beispiel 1(1 ), WO 03/082290
Massenspektrum (ESI+): m/z = 466, 468 [M+H]+
f) 4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-hydroxy- chinazolin:
Hergestellt durch Behandlung von 4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)- tetrahydrofuran-3-yloxy)-7-benzyloxy-chinazolin mit Trifluoressigsäure. s. Beispiel 6(1 ), WO 03/082290
Massenspektrum (ESI+): m/z = 376, 378 [M+H]+
Analog Beispiel I können erhalten werden:
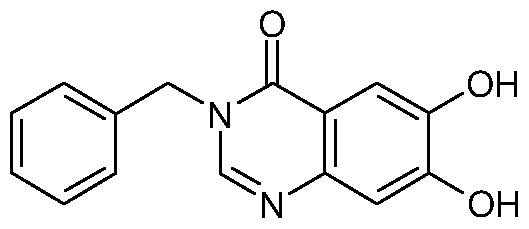
3-Benzyl-3,4-dihydro-4-oxo-6-hydroxy-7-methoxy-chinazolin
Verfahren A:
168.5 g 6-Hydroxy-7-methoxy-benzo[d][1 ,3]oxazin-4-on werden in 1200 ml Toluol gelöst und 74.7 ml Benzylamin werden zugegeben. Die Mischung wird 15 Stunden unter Rückfluss erhitzt und danach auf Raumtemperatur abgekühlt. Der Niederschlag wird abfiltriert und mit tert.-Butylmethylether gewaschen. Ausbeute 124 g (72% der Theorie)
Verfahren B:
200 g 3-Benzyl-3,4-dihydro-4-oxo-6-acetyloxy-7-methoxy-chinazolin werden in 200 ml Wasser und 1000 ml Ethanol suspendiert. 300 ml 10N Natriumhydroxid Lösung werden bei Raumtemperatur zugegeben und die Mischung 1 Stunde auf 300C erwärmt. Nach Zugabe von 172 ml Essigsäure und 2000 ml Wasser wird die Mischung 20 Stunden bei Raumtemperatur gerührt. Der Niederschlag wird abgesaugt, mit Wasser und Aceton gewaschen und bei 600C getrocknet. Ausbeute: 172,2 g (98% der Theorie) Rf-Wert: 0.25 (Kieselgel, Methylenchlorid/Ethanol = 19:1 ) Massenspektrum (ESI+): m/z = 283 [M+H]+
Beispiel III
6-Hydroxy-7-methoxy-benzo[d][1 ,3]oxazin-4-on
1 g 2-Amino-5-hydroxy-4-methoxy-benzoesäure (hergestellt durch Umsetzung von 2- Nitro-4,5-dimethoxy-benzoesäure-methylester mit Kalilauge zu 2-Nitro-5-hydroxy-4- methoxy-benzoesäure-Kaliumsalz und anschließender katalytischer Hydrierung in
Gegenwart von Palladium auf Aktivkohle) und 20 ml Orthoameisensäure-triethylester werden für 2.5 Stunden auf 1000C erhitzt. Nach Abkühlen auf Raumtemperatur wird der Niederschlag abgesaugt und mit Diethylether gewaschen. Ausbeute: 0.97 g (93% der Theorie)
Rf-Wert: 0.86 (Kieselgel, Methylenchlorid/Methanol/Essigsäure = 90:10:1)
Massenspektrum (ESI+): m/z = 194 [M+H]+
Beispiel IV
3-Benzyl-3,4-dihydro-4-oxo-6,7-dihydroxy-chinazolin
200 mg 3-Benzyl-3,4-dihydro-4-oxo-6-hydroxy-7-methoxy-chinazolin und 1 g Pyridin- hydrochlorid werden insgesamt 18 Stunden auf 1500C erhitzt. Nach dem Abkühlen wird das Reaktionsgemisch mit Wasser versetzt und gerührt. Der Feststoff wird abgesaugt, in Diethylether ausgerührt, erneut abgesaugt und getrocknet. Ausbeute: 130 mg (68% der Theorie) Massenspektrum (ESI+): m/z = 269 [M+H]+
Beispiel V
3-Benzyl-3,4-dihydro-4-oxo-6-((S)-tetrahydrofuran-3-yloxy)-7-((S)-tetrahydrofuran-3- yloxy)-chinazolin
hergestellt durch Umsetzung von 3-Benzyl-3,4-dihydro-4-oxo-6,7-dihydroxy- chinazolin mit (R)-3-[(4-Methylphenyl)sulfonyloxy]-tetrahydrofuran analog Beispiel 1
Analog Beispiel V können erhalten werden:
Beispiel VI
3,4-Dihydro-4-oxo-6-((S)-tetrahydrofuran-3-yloxy)-7-((S)-tetrahydrofuran-3-yloxy)- chinazolin
Hergestellt durch katalytische Hydrierung von 3-Benzyl-3,4-dihydro-4-oxo-6-((S)- tetrahydrofuran-3-yloxy)-7-((S)-tetrahydrofuran-3-yloxy)-chinazolin in Eisessig in Gegenwart von Palladium auf Aktivkohle (10% Pd) bei 800C und einem Wasserstoffdruck von 50 psi.
Analog Beispiel VI können erhalten werden:
Beispiel VII
4-Chlor-6-((S)-tetrahydrofuran-3-yloxy)-7-((S)-tetrahydrofuran-3-yloxy)-chinazolin
Hergestellt durch Umsetzung von 3,4-Dihydro-4-oxo-6-((S)-tetrahydrofuran-3-yloxy)- 7-((S)-tetrahydrofuran-3-yloxy)-chinazolin mit Thionylchlorid in Acetonitril unter Zusatz von N,N-Dimethylformamid.
Analog Beispiel VII können erhalten werden:
Herstellung der Endverbindungen:
Beispiel 1
4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-((R)- tetrahydrofuran-3-yloxy)-chinazolin
1 g 4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-hydroxy- chinazolin, 0.78 g (S)-3-[(4-Methylphenyl)sulfonyloxy]-tetrahydrofuran und 0.6 g Kaliumcarbonat werden in 10 ml Dimethylformamid 7 Stunden bei 600C gerührt. Nach Zugabe von 0.2 g 3-[(4-Methylphenyl)sulfonyloxy]-tetrahydrofuran und 0.2 g Kaliumcarbonat werden weitere 16 Stunden bei 600C gerührt. Nach Zugabe von 0.2 g 3-[(4-Methylphenyl)sulfonyloxy]-tetrahydrofuran und 0.2 g Kaliumcarbonat wird nochmals 4 Stunden bei 60°C gerührt. Das Reaktionsgemisch wird abgekühlt, mit Essigester verdünnt und mit Wasser und Kochsalzlösung ausgeschüttelt. Die organische Phase wird getrocknet, eingeengt und der Rückstand durch
Chromatographie über eine Kieselgelsäule mit Methylenchlorid/Methanol (98:2 bis
90:10) gereinigt. Der Rückstand wird mit Diisopropylether verrührt und der Feststoff abgesaugt und getrocknet.
Ausbeute: 990 mg (83% der Theorie)
Rf-Wert: 0.44 (Kieselgel; Methylenchlorid/Methanol = 9:1 )
Massenspektrum (ESI+): m/z = 446, 448 [M+H]+
Analog Beispiel 1 werden folgende Verbindungen erhalten:
(1 ) 4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-((S)- tetrahydrofuran-3-yloxy)-chinazolin
Massenspektrum (ESI+): m/z = 446, 448 [M+H]+
Beispiel 2
4-[(3-Chlor-4-fluor-phenyl)amino]-6-((S)-tetrahydrofuran-3-yloxy)-7-((S)- tetrahydrofuran-3-yloxy)-chinazolin
Hergestellt durch Umsetzung von 4-Chlor-6-((S)-tetrahydrofuran-3-yloxy)-7-((S)- tetrahydrofuran-3-yloxy)-chinazolin mit 3-Chlor-4-fluor-anilin in Isopropanol bei Rückflusstemperatur. Das Produkt kann je nach Aufarbeitung als Hydrochlorid oder als freie Base erhalten werden.
Analog den vorstehend genannten Beispielen und anderen literaturbekannten Verfahren können auch folgende Verbindungen hergestellt werden:
Beispiel 3
Dragees mit 75 mg Wirksubstanz
Zusammensetzung: 1 Drageekern enthält: Wirksubstanz 75.0 mg
Calciumphosphat 93.0 mg
Maisstärke 35.5 mg
Polyvinylpyrrolidon 10.0 mg
Hydroxypropylmethylcellulose 15.0 mg Magnesiumstearat 1.5 mg
230.0 mg
Herstellung:
Die Wirksubstanz wird mit Calciumphosphat, Maisstärke, Polyvinylpyrrolidon, Hydroxypropylmethylcellulose und der Hälfte der angegebenen Menge Magnesiumstearat gemischt. Auf einer Tablettiermaschine werden Preßlinge mit einem Durchmesser von ca. 13 mm hergestellt, diese werden auf einer geeigneten Maschine durch ein Sieb mit 1.5 mm-Maschenweite gerieben und mit der restlichen Menge Magnesiumstearat vermischt. Dieses Granulat wird auf einer Tablettiermaschine zu Tabletten mit der gewünschten Form gepreßt.
Kerngewicht: 230 mg Stempel: 9 mm, gewölbt
Die so hergestellten Drageekerne werden mit einem Film überzogen, der im wesentlichen aus Hydroxypropylmethylcellulose besteht. Die fertigen Filmdragees werden mit Bienenwachs geglänzt.
Drageegewicht: 245 mg.
Beispiel 4
Tabletten mit 100 mg Wirksubstanz
Zusammensetzung: 1 Tablette enthält:
Wirksubstanz 100.0 mg Milchzucker 80.0 mg
Maisstärke 34.0 mg
Polyvinylpyrrolidon 4.0 mg
Magnesiumstearat 2.0 mg 220.0 mg
Herstellungverfahren:
Wirkstoff, Milchzucker und Stärke werden gemischt und mit einer wäßrigen Lösung des Polyvinylpyrrolidons gleichmäßig befeuchtet. Nach Siebung der feuchten Masse (2.0 mm-Maschenweite) und Trocknen im Hordentrockenschrank bei 500C wird erneut gesiebt (1.5 mm-Maschenweite) und das Schmiermittel zugemischt. Die preßfertige Mischung wird zu Tabletten verarbeitet.
Tablettengewicht: 220 mg Durchmesser: 10 mm, biplan mit beidseitiger Facette und einseitiger Teilkerbe.
Beispiel 5
Tabletten mit 150 mg Wirksubstanz
Zusammensetzung: 1 Tablette enthält:
Wirksubstanz 150.0 mg
Milchzucker pulv. 89.0 mg
Maisstärke 40.0 mg
Kolloide Kieselgelsäure 10.0 mg Polyvinylpyrrolidon 10.0 mg
Magnesiumstearat 1.0 mg 300.0 mg
Herstellung:
Die mit Milchzucker, Maisstärke und Kieselsäure gemischte Wirksubstanz wird mit einer 20%igen wäßrigen Polyvinylpyrrolidonlösung befeuchtet und durch ein Sieb mit 1.5 mm-Maschenweite geschlagen.
Das bei 45°C getrocknete Granulat wird nochmals durch dasselbe Sieb gerieben und mit der angegebenen Menge Magnesiumstearat gemischt. Aus der Mischung werden Tabletten gepreßt.
Tablettengewicht: 300 mg
Stempel: 10 mm, flach
Beispiel 6
Hartgelatine-Kapseln mit 150 mg Wirksubstanz
Zusammensetzung: 1 Kapsel enthält:
Wirkstoff 150.0 mg Maisstärke getr. ca. 180.0 mg
Milchzucker pulv. ca. 87.0 mg
Magnesiumstearat 3.0 mg ca. 420.0 mg
Herstellung:
Der Wirkstoff wird mit den Hilfsstoffen vermengt, durch ein Sieb von 0.75 mm-Maschenweite gegeben und in einem geeigneten Gerät homogen gemischt.
Die Endmischung wird in Hartgelatine-Kapseln der Größe 1 abgefüllt.
Kapselfüllung: ca. 320 mg Kapselhülle: Hartgelatine-Kapsel Größe 1.
Beispiel 7
Suppositorien mit 150 mg Wirksubstanz
Zusammensetzung: 1 Zäpfchen enthält:
Wirkstoff 150.0 mg
Polyäthylenglykol 1500 550.0 mg
Polyäthylenglykol 6000 460.0 mg Polyoxyäthylensorbitanmonostearat 840.0 mg
2000.0 mg
Herstellung:
Nach dem Aufschmelzen der Suppositorienmasse wird der Wirkstoff darin homogen verteilt und die Schmelze in vorgekühlte Formen gegossen.
Beispiel 8
Suspension mit 50 mg Wirksubstanz
Zusammensetzung:
100 ml Suspension enthalten:
Wirkstoff 1.00 g
Carboxymethylcellulose-Na-Salz 0.10 g p-Hydroxybenzoesäuremethylester 0.05 g p-Hydroxybenzoesäurepropylester 0.01 g
Rohrzucker 10.00 g
Glycerin 5.00 g
Sorbitlösung 70%ig 20.00 g Aroma 0.30 g
Wasser dest.ad 100.00 ml
Herstellung:
Destilliertes Wasser wird auf 700C erhitzt. Hierin wird unter Rühren p-Hydroxybenzoesäuremethylester und -propylester sowie Glycerin und Carboxymethylcellulose-Natriumsalz gelöst. Es wird auf Raumtemperatur abgekühlt und unter Rühren der Wirkstoff zugegeben und homogen dispergiert. Nach Zugabe und Lösen des Zuckers, der Sorbitlösung und des Aromas wird die Suspension zur Entlüftung unter Rühren evakuiert.
5 ml Suspension enthalten 50 mg Wirkstoff.
Beispiel 9
Ampullen mit 10 mg Wirksubstanz
Zusammensetzung:
Wirkstoff 10.0 mg
0.01 n Salzsäure s.g.
Agua bidest ad 2.0 ml
Herstellung:
Die Wirksubstanz wird in der erforderlichen Menge 0.01 n HCl gelöst, mit Kochsalz isotonisch gestellt, sterilfiltriert und in 2 ml Ampullen abgefüllt.
Beispiel 10
Ampullen mit 50 mg Wirksubstanz
Zusammensetzung:
Wirkstoff 50.0 mg 0.01 n Salzsäure s.g.
Agua bidest ad 10.0 ml
Herstellung:
Die Wirksubstanz wird in der erforderlichen Menge 0.01 n HCl gelöst, mit Kochsalz isotonisch gestellt, sterilfiltriert und in 10 ml Ampullen abgefüllt.
Beispiel 11
Kapseln zur Pulverinhalation mit 5 mg Wirksubstanz
1 Kapsel enthält:
Wirksubstanz 5.0 mg
Lactose für Inhalationszwecke 15.0 mg
20.0 mg
Herstellung:
Die Wirksubstanz wird mit Lactose für Inhalationszwecke gemischt. Die Mischung wird auf einer Kapselmaschine in Kapseln (Gewicht der Leerkapsel ca. 50 mg) abgefüllt.
Kapselgewicht: 70.0 mg
Kapselgröße: 3
Beispiel 12
Inhalationslösung für Handvernebler mit 2.5 mg Wirksubstanz
1 Hub enthält:
Wirksubstanz 2.500 mg Benzalkoniumchlorid 0.001 mg
1 N-Salzsäure g.s.
Ethanol/Wasser (50/50) ad 15.000 mg
Herstellung:
Die Wirksubstanz und Benzalkoniumchlorid werden in Ethanol/Wasser (50/50) gelöst. Der pH-Wert der Lösung wird mit 1 N-Salzsäure eingestellt. Die eingestellte Lösung wird filtriert und in für den Handvernebler geeignete Behälter (Kartuschen) abgefüllt.
Füllmasse des Behälters: 4.5 g
Claims
1. Bicyclische Heterocyclen der allgemeinen Formel (I)
worin
Ra eine 3-Chlor-2-fluor-phenyl-, 3-Chlor-4-fluor-phenyl- oder 3-Ethinylphenyl- Gruppe,
Rb eine Tetrahydrofuran-3-yl-, Tetrahydropyran-3-yl- oder Tetrahydropyran-4-yl- Gruppe, und
Rc eine Tetrahydrofuran-3-yl-, Tetrahydropyran-3-yl- oder Tetrahydropyran-4-yl- Gruppe,
gegebenenfalls in Form ihrer Tautomeren, ihrer Racemate, ihrer Enantiomere, ihrer Diastereomere und ihrer Gemische, sowie gegebenenfalls ihrer pharmakologisch unbedenklichen Säureadditionssalze, Solvate und Hydrate, bedeuten.
2. Bicyclische Heterocyclen der allgemeinen Formel (I) nach Anspruch 1 , worin
Ra die angegebene Bedeutung haben kann,
Rb eine Tetrahydrofuran-3-yl-Gruppe bedeutet, und Rc eine Tetrahydrofuran-3-yl-Gruppe bedeutet.
3. Physiologisch verträgliche Salze der Verbindungen gemäß einem der Ansprüche 1 oder 2 mit anorganischen oder organischen Säuren.
4. Arzneimittel, enthaltend eine Verbindung gemäß einem der Ansprüche 1 bis 2 oder ein physiologisch verträgliches Salz gemäß Anspruch 3 neben gegebenenfalls einem oder mehreren inerten Trägerstoffen und/oder Verdünnungsmitteln.
5. Verwendung einer Verbindung gemäß einem der Ansprüche 1 bis 3 zur Herstellung eines Arzneimittels, das zur Behandlung von benignen oder malignen Tumoren, zur Vorbeugung und Behandlung von Erkrankungen der Atemwege und der Lunge sowie zur Behandlung von Erkrankungen des
Magen-Darm-Traktes und der Gallengänge und -blase geeignet ist.
6. Verfahren zur Herstellung der Verbindungen der allgemeinen Formel I gemäß Anspruch 1 oder 2, dadurch gekennzeichnet, dass
a) eine Verbindung der allgemeinen Formel (II)
worin, Ra und Rc wie in den Ansprüchen 1 bis 2 definiert sind, mit einer Verbindung der allgemeinen Formel
Z1 - Rb worin,
Rc wie in den Ansprüchen 1 bis 2 definiert ist, und
Z1 eine Austrittsgruppe oder Hydroxygruppe darstellt, umgesetzt wird, oder
b) eine Verbindung der allgemeinen Formel (IV)
Ra und R wie in den Ansprüchen 1 bis 2 definiert sind, mit einer Verbindung der allgemeinen Formel
Z1 - Rc (V),
in der
Rc wie in den Ansprüchen 1 bis 2 definiert ist, und
Z1 eine Austrittsgruppe oder Hydroxygruppe darstellt, umgesetzt wird, oder
Ra wie in den Ansprüchen 1 bis 2 definiert ist, mit einer Verbindung der allgemeinen Formel
in der
Rd eine Tetrahydrofuran-3-yl-, Tetrahydropyran-3-yl- oder Tetrahydropyran-4-yl- Gruppe darstellt, und
Z1 eine Austrittsgruppe oder Hydroxygruppe darstellt, umgesetzt wird, oder
d) eine Verbindung der allgemeinen Formel (VIII)
in der Rb und Rc wie in den Ansprüchen 1 bis 2 definiert sind, mit einem Halogenierungsmittel zu einer Zwischenverbindung der allgemeinen Formel (IX), Z2
in der Rb und Rc wie in den Ansprüchen 1 bis 2 definiert sind und Z2 ein Halogenatom darstellt,
und anschließend mit einer Verbindung der allgemeinen Formel (X)
Ra - NH2 (X),
in der Ra wie in den Ansprüchen 1 bis 2 definiert ist, umgesetzt wird.
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008557710A JP2009529511A (ja) | 2006-03-09 | 2007-02-20 | 二環式複素環化合物、これらの化合物を含む医薬組成物、その使用方法及び製造方法 |
| CA002643363A CA2643363A1 (en) | 2006-03-09 | 2007-02-20 | Bicyclic heterocycles, medicaments containing these compounds, their use and process for preparing them |
| EP07704659A EP1996561A1 (de) | 2006-03-09 | 2007-02-20 | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
| US12/281,190 US20090306105A1 (en) | 2006-03-09 | 2007-02-20 | Bicyclic heterocycles, medicaments containing these compounds, their use and process for preparing them |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP06110886.6 | 2006-03-09 | ||
| EP06110886 | 2006-03-09 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2007101782A1 true WO2007101782A1 (de) | 2007-09-13 |
Family
ID=37067472
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2007/051589 WO2007101782A1 (de) | 2006-03-09 | 2007-02-20 | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20090306105A1 (de) |
| EP (1) | EP1996561A1 (de) |
| JP (1) | JP2009529511A (de) |
| CA (1) | CA2643363A1 (de) |
| WO (1) | WO2007101782A1 (de) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102008012435A1 (de) * | 2008-02-29 | 2009-09-03 | Schebo Biotech Ag | Neue Pharmazeutika, Verfahren zu ihrer Herstellung und ihre Verwendung in der Therapie |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1921070A1 (de) * | 2006-11-10 | 2008-05-14 | Boehringer Ingelheim Pharma GmbH & Co. KG | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstelllung |
| ME01461B (me) | 2008-02-07 | 2014-04-20 | Boehringer Ingelheim Int | Spirociklični heterocikli, ljekovi koji sadrže navedeno jedinjenje, njihova primjena i postupak za njihovu proizvodnju. |
| EP2313397B1 (de) * | 2008-08-08 | 2016-04-20 | Boehringer Ingelheim International GmbH | Cyclohexyloxy-substituierte heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19911509A1 (de) * | 1999-03-15 | 2000-09-21 | Boehringer Ingelheim Pharma | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung |
| WO2002018351A1 (de) * | 2000-08-26 | 2002-03-07 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und vefahren zu ihrer herstellung |
| WO2002018372A1 (de) * | 2000-08-26 | 2002-03-07 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
| WO2003082290A1 (de) * | 2002-03-30 | 2003-10-09 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | 4- ( n-phenylamino ) -chinazoline/chinoline als tyrosinkinaseinhibitoren |
| WO2004108664A2 (de) * | 2003-06-06 | 2004-12-16 | Boehringer Ingelheim International Gmbh | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
-
2007
- 2007-02-20 WO PCT/EP2007/051589 patent/WO2007101782A1/de active Application Filing
- 2007-02-20 US US12/281,190 patent/US20090306105A1/en not_active Abandoned
- 2007-02-20 CA CA002643363A patent/CA2643363A1/en not_active Abandoned
- 2007-02-20 JP JP2008557710A patent/JP2009529511A/ja active Pending
- 2007-02-20 EP EP07704659A patent/EP1996561A1/de not_active Withdrawn
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19911509A1 (de) * | 1999-03-15 | 2000-09-21 | Boehringer Ingelheim Pharma | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung |
| WO2002018351A1 (de) * | 2000-08-26 | 2002-03-07 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und vefahren zu ihrer herstellung |
| WO2002018372A1 (de) * | 2000-08-26 | 2002-03-07 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
| WO2003082290A1 (de) * | 2002-03-30 | 2003-10-09 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | 4- ( n-phenylamino ) -chinazoline/chinoline als tyrosinkinaseinhibitoren |
| WO2004108664A2 (de) * | 2003-06-06 | 2004-12-16 | Boehringer Ingelheim International Gmbh | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung |
Non-Patent Citations (1)
| Title |
|---|
| HARRIS ET AL: "Selective alkylation of a 6,7-dihydroxyquinazoline", TETRAHEDRON LETTERS, ELSEVIER, AMSTERDAM, NL, vol. 46, no. 45, 7 November 2005 (2005-11-07), pages 7715 - 7719, XP005104155, ISSN: 0040-4039 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102008012435A1 (de) * | 2008-02-29 | 2009-09-03 | Schebo Biotech Ag | Neue Pharmazeutika, Verfahren zu ihrer Herstellung und ihre Verwendung in der Therapie |
Also Published As
| Publication number | Publication date |
|---|---|
| US20090306105A1 (en) | 2009-12-10 |
| EP1996561A1 (de) | 2008-12-03 |
| CA2643363A1 (en) | 2007-09-13 |
| JP2009529511A (ja) | 2009-08-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1345910B9 (de) | Chinazolinderivate, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| EP1966189A1 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| EP1315718B1 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| EP1731511B1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| EP1597240B1 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, ihre verwendung und verfahren zu ihrer herstellung | |
| EP1315720B1 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| DE10042058A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| EP1921070A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstelllung | |
| DE10042060A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| EP1641767A2 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| DE10217689A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, ihre Verwendung und Verfahren zu ihrer Herstellung | |
| DE10042061A1 (de) | Bicyclische Heterocyclen,diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| EP1919900A2 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| WO2008095847A1 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| DE10214412A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| WO2007101782A1 (de) | Bicyclische heterocyclen, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| DE10042064A1 (de) | Chinazoline, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| DE19908567A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel, deren Verwendung und Verfahren zu ihrer Herstellung | |
| WO2005033096A1 (de) | Chinolin- und chinazolin-derivate, diese verbindungen enthaltende arzneimittel, deren verwendung und verfahren zu ihrer herstellung | |
| EP1956010A1 (de) | Bicyclische Heterocyclen, diese Verbindungen enthaltende Arzneimittel,deren Verwendung und Verfahren zu ihrer Herstellung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2007704659 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2643363 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2008557710 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12281190 Country of ref document: US |