WO2006106823A1 - 分子マーカーを用いた間葉系幹細胞の識別方法及びその利用 - Google Patents
分子マーカーを用いた間葉系幹細胞の識別方法及びその利用 Download PDFInfo
- Publication number
- WO2006106823A1 WO2006106823A1 PCT/JP2006/306658 JP2006306658W WO2006106823A1 WO 2006106823 A1 WO2006106823 A1 WO 2006106823A1 JP 2006306658 W JP2006306658 W JP 2006306658W WO 2006106823 A1 WO2006106823 A1 WO 2006106823A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- gene
- transcription
- protein
- transport
- binding
- Prior art date
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6845—Methods of identifying protein-protein interactions in protein mixtures
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6881—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for tissue or cell typing, e.g. human leukocyte antigen [HLA] probes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/569—Immunoassay; Biospecific binding assay; Materials therefor for microorganisms, e.g. protozoa, bacteria, viruses
- G01N33/56966—Animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
Definitions
- the present invention relates to detection, identification, and separation of mesenchymal stem cells, and in particular, mesenchymal stem cells and connective tissue cells such as fibroblasts, osteoblasts, chondrocytes, and adipocytes,
- the present invention relates to a method of identifying mesenchymal stem cells using a genetic marker for detecting mesenchymal stem cells having different expression and a protein marker for detecting Z or mesenchymal stem cells, and its use.
- Mesenchymal stem cells are known as pluripotent stem cells that exist in mammalian bone marrow and the like and differentiate into adipocytes, chondrocytes, and bone cells. Mesenchymal stem cells are attracting attention as transplant materials for regenerative medicine in many tissues because of their pluripotency. In other words, it is “regenerative medicine by cell transplantation” that uses mesenchymal stem cells to regenerate tissues lost due to diseases and disorders that have not been regenerated by conventional treatment methods and restore their functions.
- transplantation of bone marrow mesenchymal stem cells to patients with lower limb ischemia (Burger's disease)
- transplantation of bone marrow mesenchymal stem cells to periodontal disease patients transplantation of bone marrow mesenchymal stem cells to periodontal disease patients
- bone marrow mesenchymal system to patients with osteoarthritis
- Treatments such as transplantation of stem cells, transplantation of amniotic epithelial sheets into burned areas, and transplantation of amniotic stem cells into diabetic patients have been started or planned.
- stem cells are collected from a living tissue, are proliferated undifferentiated, and further expanded undifferentiated stem cells are obtained as desired. It is necessary to induce differentiation into cells and prepare a tissue for regenerative treatment.
- the present inventors identified mesenchymal stem cells and fibroblasts that are morphologically similar and difficult to distinguish, as a genetic marker for detecting mesenchymal stem cells and A method for effectively identifying and separating using a protein marker for detecting Z or mesenchymal stem cells has been developed (see Patent Document 3).
- Patent Document 1 Japanese Patent Laid-Open No. 2003-52365 (Publication: February 25, 2003)
- Patent Document 2 Japanese Patent Laid-Open No. 2003-52360 (Publication: February 25, 2003)
- Patent Document 3 Japanese Patent Laid-Open No. 2005-27579 (Publication: February 3, 2005) Disclosure of Invention
- mesenchymal stem cells differentiate into bone, cartilage, fat, muscle, tendon, nerve, and the like, so that these tissues can be repaired from the viewpoint of use in regenerative medicine.
- mesenchymal stem cells in vitro or in vivo, it may be reliable in addition to proving its ability to function. There was no way.
- mesenchymal stem cells in order to put mesenchymal stem cells into practical use for tissue regenerative medicine, it is precisely necessary that the cells are mesenchymal stem cells and that the mesenchymal stem cells are likely to maintain their ability to function. It was necessary to check the accuracy and convenience.
- Patent Document 3 Certainly, the method disclosed in Patent Document 3 is sufficient for discriminating and separating mesenchymal stem cells from fibroblasts.
- connective tissue cells such as osteoblasts, chondrocytes, and adipocytes in addition to fibroblasts.
- the present invention has been made in view of the above problems, and its object is to connect mesenchymal stem cells and connective tissues such as fibroblasts, osteoblasts, chondrocytes, and adipocytes. It is intended to provide a method for accurately and accurately discriminating and Z or separating cells of a system and use thereof.
- a gene having the nucleotide sequence represented by the accession number described in Tables la to lj below, using at least one selected gene as a differentiation marker, and mesenchymal stem cells A method for identifying mesenchymal stem cells, comprising a step of discriminating mesenchymal stem cells from connective tissue cells by detecting a difference in expression of the differentiation marker between the cells and connective tissue cells.
- transport-4 SLC14A1 (urea transporter), member 1 NM— 015865
- solute carrier family 30 (zinc
- a classification marker a combination of at least one gene selected from each of classes 6, 7, 8, 10, and 13 described in Tables la to lj above is used.
- the detection of the differential expression of the discrimination marker is performed by detecting the expression of the gene or by detecting the expression of the protein encoded by the gene of (1) to (4).
- the method for identifying mesenchymal stem cells according to any one of the above.
- a mesenchymal stem cell comprising a gene having a base sequence indicated by any accession number described in Tables la to lj or a partial sequence thereof and a polynucleotide that hybridizes under stringent conditions; Probe for detection of discrimination marker gene.
- a cell-containing composition comprising mesenchymal stem cells isolated by the method for identifying and separating mesenchymal stem cells described in (9) above, or a product obtained by proliferating the mesenchymal stem cells.
- a pharmaceutical for regenerative medicine comprising the cell-containing composition according to (10) above.
- a mesenchymal stem that is any one of the polypeptides encoded by the genes having the nucleotide sequences indicated by the accession numbers shown in Tables la to lj above A differentiation marker for cell identification.
- nucleotide sequence represented by any accession number described in Table la to Table lj above A pharmaceutical for regenerative medicine that suppresses the undifferentiation of mesenchymal stem cells containing a siRNA for a gene having a partial sequence or a partial sequence thereof.
- genes that clearly have differences in expression patterns are used as classification markers. For this reason, for example, it is possible to identify undifferentiated mesenchymal stem cells and connective tissue cells contained in the bone marrow accurately, easily and accurately, and to perform Z or separation. Play.
- undifferentiated mesenchymal stem cells capable of differentiating into bone, cartilage, fat, muscle, tendon, nerve and the like are used for regenerative medicine.
- the problem can be overcome, that is, the problem of discriminating unidentified mesenchymal stem cells from other cell populations such as fibroblasts and connective tissue cells. Therefore, it can greatly contribute to the practical application of regenerative medicine using mesenchymal stem cells.
- mesenchymal stem cells and mesenchymal stem cell-containing filaments and compositions using this method for identifying mesenchymal stem cells can be used for regenerative medicine.
- FIG. 1 is a diagram schematically showing an outline of a procedure flow in the present embodiment.
- FIG. 2 shows the results of analyzing the difference in gene expression between mesenchymal stem cells (MSCs) and other connective tissue cells using DNA microarrays in this example.
- MSCs mesenchymal stem cells
- the present invention uses a DNA microarray or the like to detect a gene that specifically expresses in undifferentiated mesenchymal stem cells as a differentiation marker, and uses mesenchymal stem cells as connective tissue cells (for example, It is possible to construct a method for effectively discriminating and separating from other cell populations such as fibroblasts, osteoblasts, chondrocytes, and adipocytes). In addition, using the method of the present invention, it becomes possible to test the quality of mesenchymal stem cells grown in vitro (probably whether or not the ability to maintain the ability is maintained). It is also possible to contribute to the practical application of regenerative medicine.
- polypeptide is used interchangeably with “peptide” or "protein”.
- the polypeptides according to the invention may also be isolated from natural sources, recombinantly produced or chemically synthesized.
- polynucleotide is used interchangeably with “gene”, “nucleic acid” or “nucleic acid molecule” and is intended to be a polymer of nucleotides. “Gene” is intended to include not only DNA but also RNA (eg, mRNA).
- base sequence is used interchangeably with “gene sequence”, “nucleic acid sequence”, or “nucleotide sequence” and includes deoxyribonucleotides (A, G, And abbreviated as T).
- the method for identifying mesenchymal stem cells uses at least one gene among the genes having the nucleotide sequences indicated by the accession numbers described in Tables la to lj above as a differentiation marker, Other steps are acceptable as long as they have a step of detecting a difference in expression between the mesenchymal stem cells and connective tissue cells of the above-mentioned discrimination marker and distinguishing mesenchymal stem cells from connective tissue cells.
- the specific configuration of conditions, materials used, equipment used, etc. is not particularly limited.
- Class 1 is a force category related to ATPZGTP-binding protein, to which 8 types and 8 genes indicated by accession numbers belong.
- Class 2 is a category related to binding proteins, to which 10 types of genes indicated by 10 accession numbers belong. In this specification and table, this class 2 The “binding-1 to 10” shown means “DNA / metal ion / collagen binding-1 to 10”.
- Class 3 is a category of factors related to cell growth or maintenance, and includes 11 types and genes indicated by 11 accession numbers.
- Class 4 is a category related to site force-in, to which 6 types of genes indicated by 6 accession numbers belong.
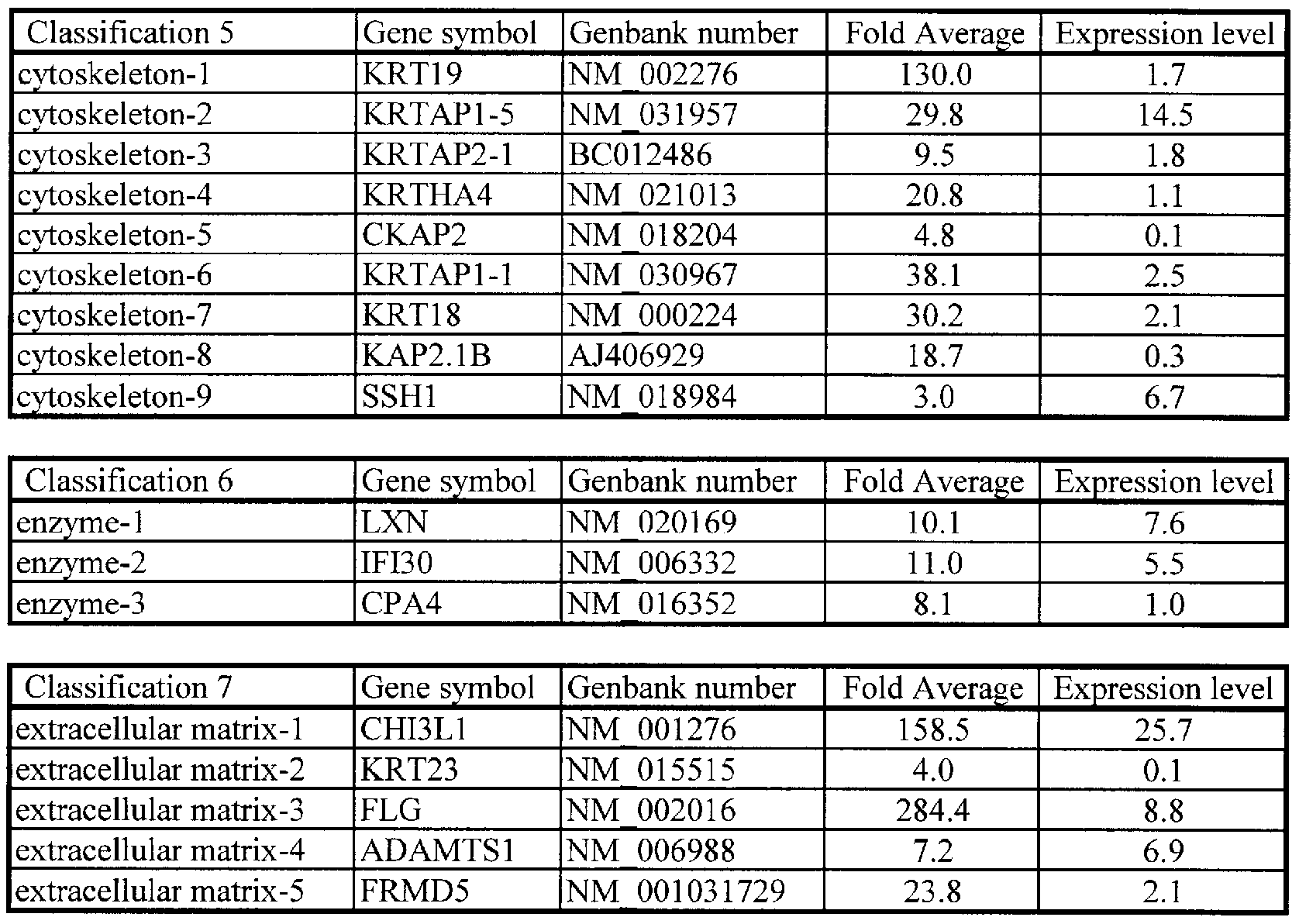
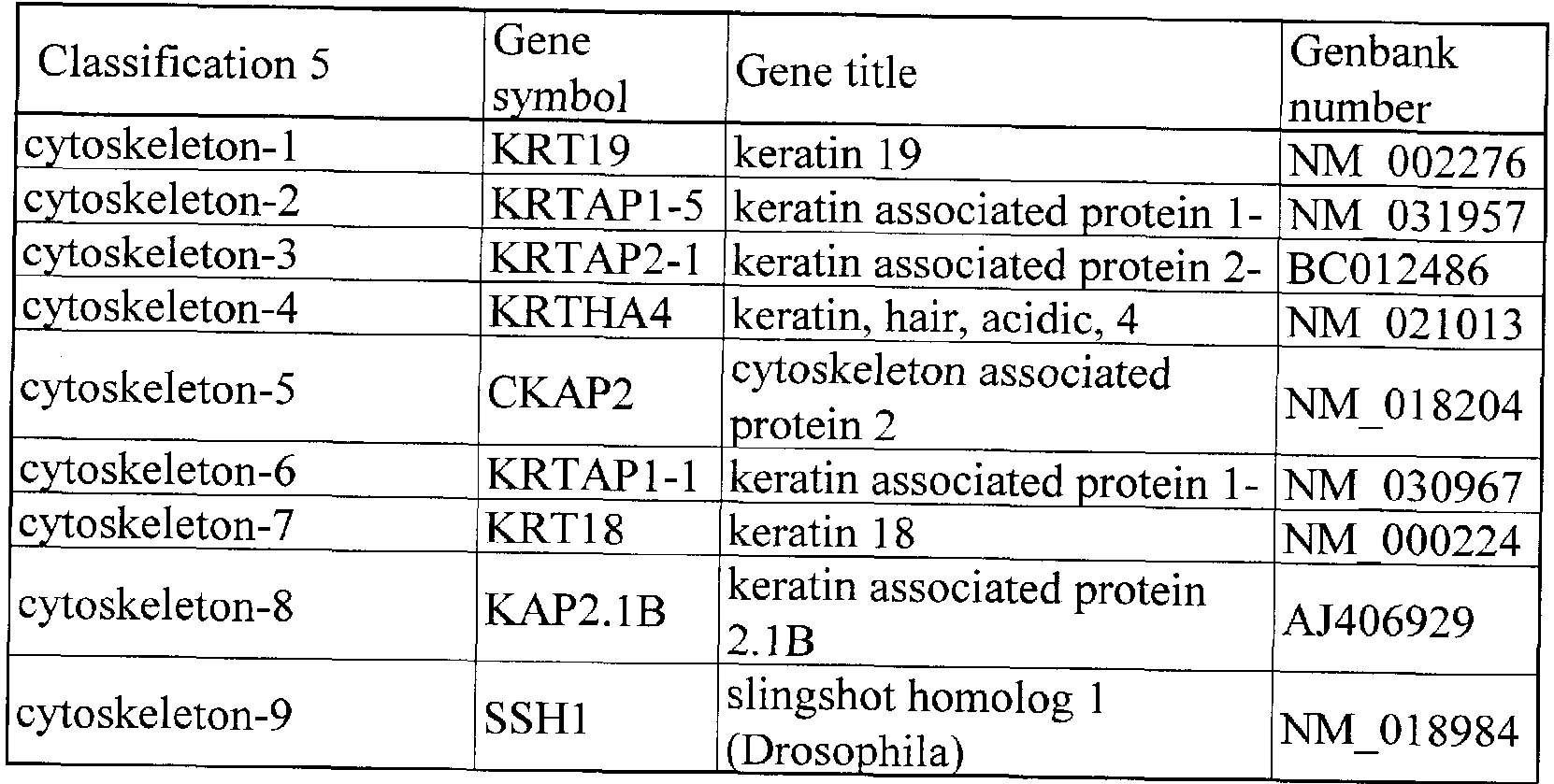
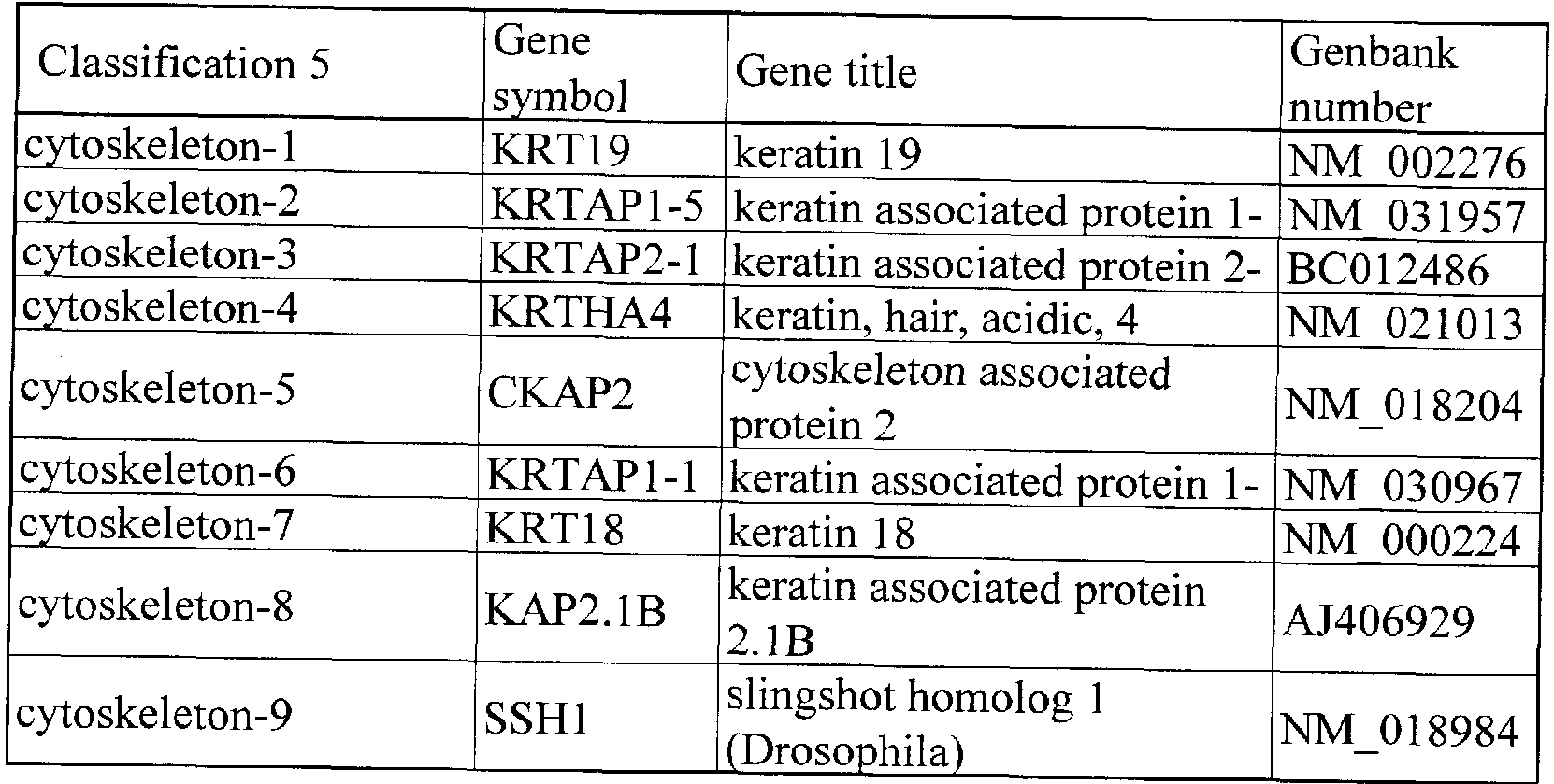
- Class 5 is a category related to the intracellular skeleton, and the genes indicated by nine types and nine accession numbers belong to it.
- Class 6 is a category of enzymes to which 3 types of genes indicated by 3 accession numbers belong.
- Class 7 is one of the categories relating to the extracellular matrix or the intracellular skeleton, and the genes indicated by five types and five accession numbers belong to it.
- Class 8 is a category relating to growth factors or receptors, to which 7 types and 7 genes indicated by accession numbers belong.
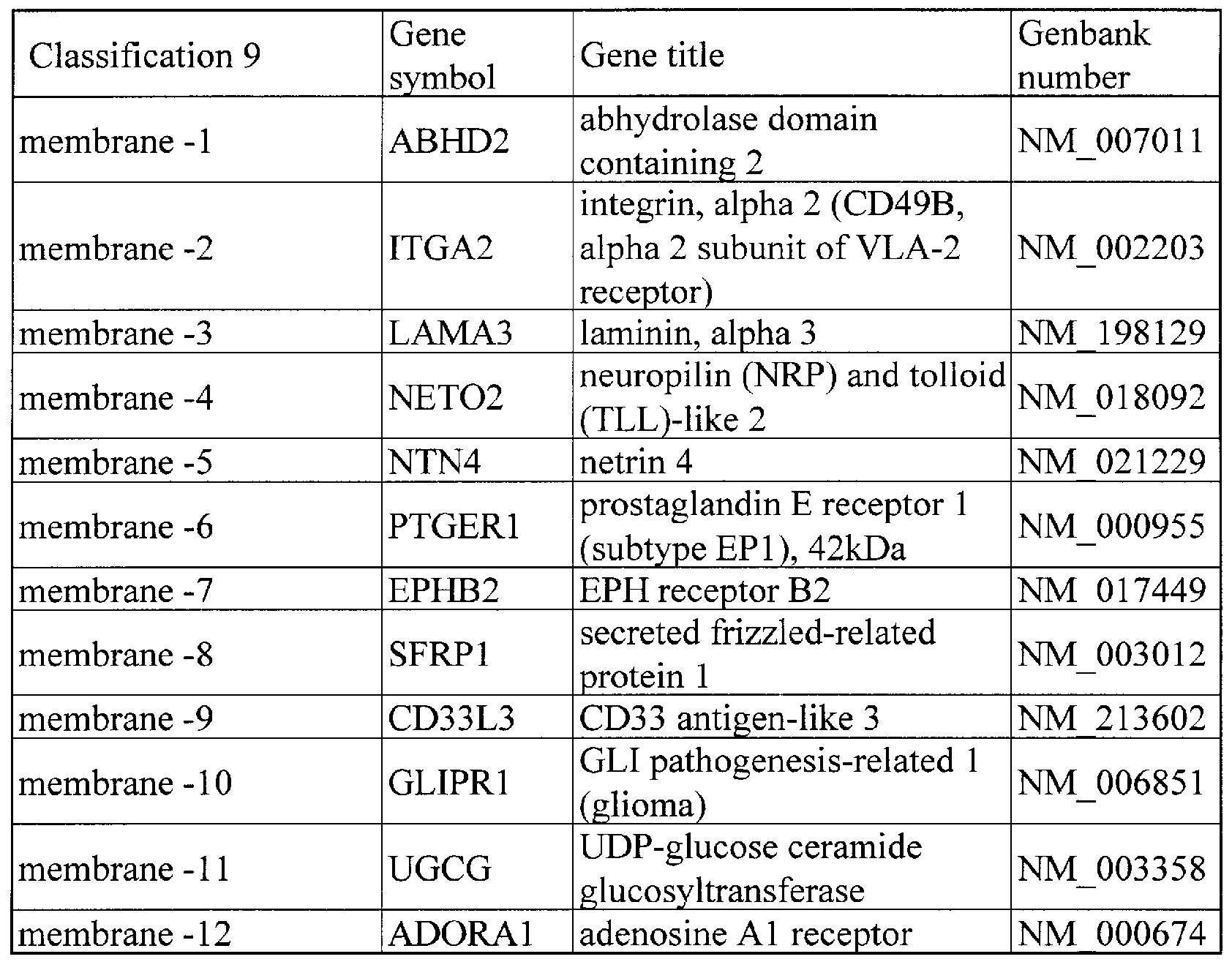
- Class 9 is a category related to membranes, to which 12 types of genes indicated by 12 accession numbers belong.
- Class 10 is a category related to membrane-bound proteins, and the genes indicated by 4 types and 4 accession numbers belong to it.
- Class 11 is a category of factors relating to protein binding, to which 10 types of genes indicated by 10 accession numbers belong.
- Class 12 (Classification 12) is a category of factors related to protein modification, and 8 types of genes with 8 accession numbers belong.
- Class 13 (Classification 13) is a category of factors involved in signal transduction, to which genes represented by 5 types and 5 accession numbers belong.
- Class 14 is a category related to transcription factors, to which 12 types of genes represented by 12 accession numbers belong.
- Class 15 is a category of factors related to intracellular transport, to which 13 types and 13 genes indicated by accession numbers belong.
- Class 16 is a category relating to other factors that do not belong to the above-mentioned class, to which 16 types of genes indicated by 16 accession numbers belong.
- the above category 1 is classified based on publicly known information disclosed to NCBI.
- the gene groups shown in Tables la to lj above are classified by focusing on the molecular functions of the proteins encoded by the genes. Therefore, by using these genes as differentiation markers, the mesenchymal stem cells and connective tissue cells are differentiated by focusing on the function and function of each gene in mesenchymal stem cells and connective tissue cells. can do.
- mesenchymal stem cells express a large amount of factors related to a specific extracellular matrix but not so much in connective tissue cells, class 7 By using the gene to which it belongs as a differentiation marker, mesenchymal stem cells can be easily and accurately identified.
- connective tissue refers to a general tissue of a support / connective tissue including cartilage tissue and bone tissue.
- Supportive tissue is a collective term for connective tissue in the narrow sense and connective tissue (cartilage tissue, bone tissue, blood and lymph) that are specially separated. It should be noted that, in a broad sense, the supporting tissue can be referred to as “connective tissue”. In ontogeny, it is derived from “mesoderm (some of which may be derived from ectoderm)” and has the role of maintaining the internal structure of the body. “Connective tissue cells” are cells constituting the above-mentioned supporting connective tissue.
- fibroblasts As fixed cells, fibroblasts, reticicular cells, adipose cells (Adipose) cells), free (migrating) cells such as macrophages (histosphere or macrophages) (Macrophages), mast cells (Pastma cells), lymphocytes (Lymphoid cells), granular leukocytes (Granulocytes) ), Chondrocytes, chondrocytes, osteoblasts, and bone cells that constitute bone tissue can be mentioned as fixed cells that constitute soft tissue.
- these fibroblasts, osteoblasts, chondrocytes, and adipocytes can be distinguished from mesenchymal stem cells. preferable.
- the gene groups in Tables la to lj used as the "fractionation marker" in the present invention are, as shown in Examples described later, using a DNA microarray, undifferentiated mesenchymal stem cells, An experiment that investigated the expression profiles of fibroblasts, osteoblasts, chondrocytes, and adipocytes, revealed that there was a significant difference between undifferentiated mesenchymal stem cells and other cell populations (connective tissue cells). The difference in expression was recognized.
- genes listed in Tables la to lj above those satisfying the criteria of judgment as shown in the examples described later are preferable.
- the classification marker it is preferable to use at least one gene that can select a gene force belonging to classes 6, 7, 8, 10, and 13 described in Tables la to lj above. It is preferable.
- Genes belonging to classes 6, 7, 8, 10, and 13 in Tables la to lj above are greatly different in expression patterns particularly in mesenchymal stem cells and connective tissue cells, and mesenchymal Many stem cells have high expression. For this reason, it can be suitably used as a classification marker. In addition, there is an advantage that the mesenchymal stem cells can be accurately identified by using these genes with high expression and small individual differences as the differentiation markers.
- each of classes 6, 7, 8, 10, and 13 listed in Tables la to lj above It is more preferable to use a combination of at least one gene selected from the lath. This means that if you select at least one gene from each class that has greatly different expression patterns between mesenchymal stem cells and connective tissue cells, and use them in combination as the best choice! . As described above, selecting at least one gene for each of the five class powers enables confirmation of the expression pattern for each of the genes belonging to the five categories, thus further improving the accuracy and precision of identification.
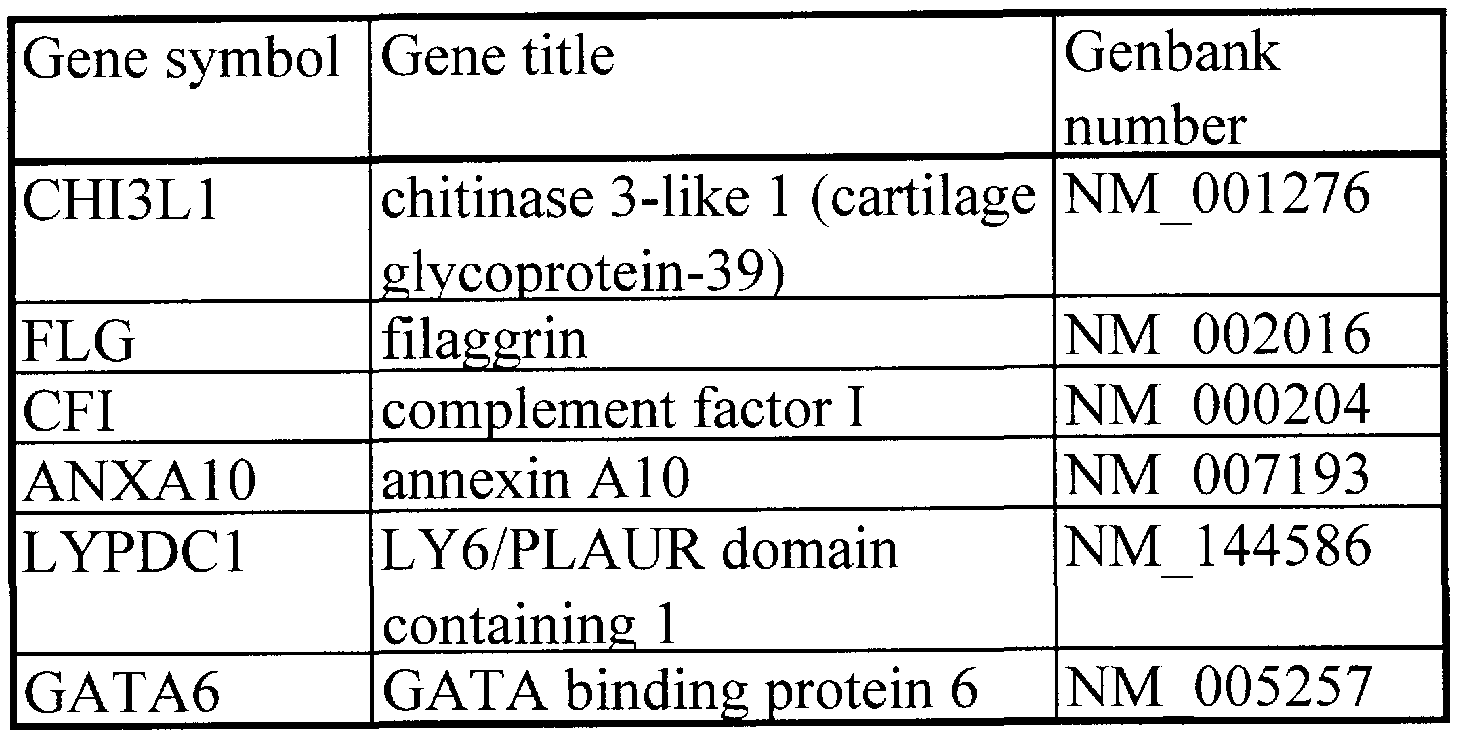
- Table 2 is a summary of six particularly preferred genes selected from the 139 genes listed in Tables la to lj above. These genes are most suitable when they are used as fractionation markers, in which the expression pattern is greatly different between mesenchymal stem cells and connective tissue cells, and the expression level of the gene itself is also large. In addition, by using these few markers, there is an advantage that convenience and cost reduction can be achieved in the identification of mesenchymal stem cells.
- genes belonging to the 16 classes a plurality of genes belonging to the same class can be used in combination. For example, by combining genes belonging to classes related to transcription factors and using them as a differentiation marker, it is possible to grasp upstream force as well as protein synthesis specific to mesenchymal stem cells. In addition, by using a combination of genes belonging to classes related to the cytoskeleton, it is possible to grasp the production of proteins characteristic of mesenchymal stem cells such as keratins. In addition, by using a combination of genes belonging to classes related to growth factors, it is possible to grasp cell growth factor production and the like. In addition, by using a combination of genes belonging to classes related to extracellular matrix, it is possible to grasp cell adhesion and the like.
- At least one gene is selected from each of 16 classes (other classes may be excluded), and the characteristics of each class are comprehensively selected. It is also possible to analyze. In such a case, at least one classification marker may be used in each class. In particular, the higher the “evaluation criterion” marker shown in the examples described later, As the number of markers used increases, the accuracy and accuracy of the identification 'analysis increases, and a reliable identification method can be implemented. Therefore, as described above, when combining a plurality of classification markers, it is preferable to preferentially adopt the one having a high “evaluation criterion” and increase the number of classification markers to be used as much as possible.
- the difference in expression of the discrimination marker can be detected by detecting the expression of the gene or by detecting the expression of the protein encoded by the gene.
- the difference in the expression of the differentiation marker gene as described above between mesenchymal stem cells and connective tissue cells is detected using a gene detection means known per se, which will be described later. Detect and identify mesenchymal stem cells. For this reason, in the present invention, among the genes having the nucleotide sequences indicated by the accession numbers described in any of the above tables la to lj, the differentiation for identifying mesenchymal stem cells, which is one of the genes, is one. Markers are included.
- a conventionally known method used for detecting the expression of a known gene can be suitably used to detect the expression of the gene group of the discrimination marker. For example, by detecting at least one of the following (a) to (d) using a microarray for identifying mesenchymal stem cells in which at least one of them is fixed, the expression of the gene group of the discrimination marker is detected.
- microarray examples include oligonucleotides directly on a silica substrate using a microfabrication technique used in semiconductor manufacturing, such as a DNA microarray of Stanford type DNA microarray of Aifymetrix, USA. Any conventionally known type of microarray, including DNA microarrays to be chemically synthesized, can be suitably used, and the specific size, shape, system and the like are not particularly limited.
- the present invention includes the above-described microarray for identifying mesenchymal stem cells.
- a plurality of sorting forces as an index.
- a combination of a plurality of differentiation markers that have sufficient expression differences and high expression levels between mesenchymal stem cells and other cell groups.
- CHI3L1, FLG, KRTAP1-5, RGS4, HNT, SLC14A1, IFI30, ZNF423, and LXN that have high Fold Average and Expression level can be used.
- the Northern blotting method can be used for detecting the expression of the gene group of the differentiation marker in the present invention.
- the fractionation marker having a nucleotide sequence that is noblyzed under stringent conditions with the full-length DNA sequence of the gene of the fractionation marker in the present invention or a partial sequence thereof A gene detection probe can be used.
- Detection of gene expression in mesenchymal stem cells and connective filamentous and woven cells using the above-described detection probe can be appropriately performed using a known method. For example, preparing a DNA probe of an appropriate length from the DNA sequence of a gene for a known fractionation marker, adding a label such as a fluorescent label as appropriate, and hybridizing it with a specimen Thus, the mesenchymal stem cells are detected.
- the detection probe it is possible to use a known detection marker for a single fractionation marker gene consisting of a full-length sequence or a partial sequence of the antisense strand of the base sequence of the gene of the fractionation marker.
- the condition of "nobbreviating under the stringent conditions with the DNA sequence of one marker gene” is as follows. Washing treatment at 42 ° C with a buffer containing 1 N SBR (0.15 M NaCl, 0.015 M sodium citrate), 0.1% SDS (Sodium dodecyl sulfate) More preferably, a hybridization at 65 ° C and a washing treatment at 65 ° C with a buffer containing 0.1 X SSC and 0.1% SDS are mentioned. I can make it.
- RNA for a differentiation marker when detecting the expression of a gene for a differentiation marker in a test cell, quantitative or semi-quantitative PCR can be used to amplify the gene of the test cell.
- quantitative or semi-quantitative PCR for example, RT-PCR (reverse transcription PCR) can be used.
- RT-PCR reverse transcription PCR
- a pair of primer sets consisting of a sense primer and an antisense primer for amplifying a single gene in the present invention is used.
- the method for identifying mesenchymal stem cells of the present invention can be simply performed using an Invader (registered trademark) method.
- a signal probe having a sequence specifically cleaved and hybridized to the above-described classification marker sequence and an enzyme cleavage site is designed, and the total RNA (which may be cDNA) extracted from the cell force of the test target is analyzed. Reaction at a given temperature, a given time (eg, 63 ° C, 2 hours, etc.) together with a reader oligo (Invader (registered trademark) Oligo), thalibase enzyme (Cleavase (registered trademark) Enzyme), and fret probe (FRET Probe) Can be performed.
- Invader registered trademark
- a signal probe having a sequence specifically cleaved and hybridized to the above-described classification marker sequence and an enzyme cleavage site is designed, and the total RNA (which may be cDNA) extracted from the cell force of the test target is analyzed. Reaction
- the method for identifying mesenchymal stem cells according to the present invention can also be performed using in situ hybridization.
- the above-described classification marker or a partial sequence thereof labeled is used as a probe, and a molecular hybrid is directly formed on a specimen of a cell to be inspected on a slide glass, and this portion is simply detected. Can do.
- a thin section (paraffin section, frozen section, etc.) of the cell to be examined is prepared on a slide glass, and the labeled probe is hybridized to it in the same manner as the Northern hybridization method.
- the probe is washed off, photographic emulsion is applied and exposed. After image formation, the hybridized location is identified from the silver particle distribution.
- the expression of the discrimination marker gene of the present invention is detected as a protein encoded by the gene, an antibody that specifically binds to the protein is prepared using the protein, By using this method, it is possible to identify mesenchymal stem cells by detecting expression in a mesenchymal stem cell and a connective tissue cell of a differentiation marker monoprotein by a method known per se.
- the antibody may be a polyclonal antibody or a monoclonal antibody.
- the above-mentioned antibody can be prepared by, for example, a conventionally known conventional method using the full-length sequence of a polypeptide encoded by the gene of the fractionation marker of the present invention or a partial sequence thereof as an antigen.
- a method for producing a monoclonal antibody is not particularly limited. For example, after immunizing a mouse with an antigen, the mouse spleen lymphocyte is fused with a mouse-derived myeloma cell. Monoclonal antibodies can be obtained using the antibody-producing hyperpridoma.
- Hypridoma production methods include conventionally known methods such as the Hypridoma method (Kohler, G. and Milstein, C, Nature 256, 495-497 (1975)), the trioma method, the human B-cell hyperidoma method.
- the antigen is not particularly limited as long as it is a polypeptide, but an antigen protein obtained by binding a substance having an antigenic determinant to a carrier protein may be used. Specifically, if the antigen is a hapten, the antibody cannot be produced because it does not have the ability to induce antibody production or the like, but the antigen also has biopolymer power such as proteins derived from different species. Antibody production can be induced by covalently binding to a carrier to obtain an antigenic protein, which is then immunized. As the above-mentioned carrier, various proteins conventionally known in this field such as ovalbumin, ⁇ globulin, hemocyanin and the like can be suitably used.
- Monoclonal antibodies can also be produced by gene recombination techniques.
- a method for producing a polyclonal antibody there can be mentioned a method in which an experimental animal is inoculated with an antigen and sensitized, and the humoral antibody component is purified and obtained.
- animals to be immunized conventionally known experimental animals such as mice, rats, rabbits, monkeys and horses can be used, and are not particularly limited.
- the interval and amount thereof can be appropriately determined according to a conventional method.
- detection of the expression of a protein of a differentiation marker in a test cell can be performed using an immunological assay using a known antibody.
- the immunoassay include known immunoassays such as RIA, ELISA, and fluorescent antibody method.
- Western blotting method, enzyme immunoassay method, method for observing agglutination, sedimentation and hemolysis reaction by antibody, morphological detection method such as yarn and tissue immunostaining and cell immunostaining Can also be used as needed.
- the difference in the expression of the differentiation marker is detected for a single differentiation marker, and as a result, the mesenchymal stem cells may be identified, but more accurately and more accurately.
- the identification method is preferably performed using the above-described microarray for identifying mesenchymal stem cells when a difference in gene expression is used as a differentiation marker.
- the method for identifying and separating mesenchymal stem cells according to the present invention may have a step of separating mesenchymal stem cells identified by the method for identifying mesenchymal stem cells described in the section ⁇ 1> above. There are no particular restrictions on the specific configuration of other processes, conditions, materials used, equipment used, etc.
- a fluorescence-activated cell sorter FACS
- the mesenchymal stem cells are labeled by the fluorescent antibody method using the antibody of the present invention, the expression of the differentiation marker polypeptide of the mesenchymal stem cells in the test cells is detected, and the mesenchymal stem cells are detected. Can be identified and separated.
- Undifferentiated mesenchymal stem by fluorescent antibody method In order to label cells, an antibody that specifically binds to the polypeptide of the differentiation marker in the present invention is fluorescently labeled, and this is bound to a mesenchymal stem cell that expresses the antigen, and then the mesenchymal The stem cells are labeled (direct fluorescent antibody method), or the mesenchymal stem cells expressing the antigen are bound to the unlabeled specific antibody of the present invention, and then the labeled secondary antibody ( Anti-immunoglobulin antibody) can be bound to label mesenchymal stem cells (indirect fluorescent antibody method).
- Mesenchymal stem cells labeled by the above-mentioned method can be collected by measurement and separation by flow cytometry. The separated sample can be removed by a filter and observed with an oblique fluorescent microscope.
- MACS magnetic cell sorting
- the target cells are specifically labeled with an antibody labeled with magnetic microbeads for MACS and applied to a separation column installed in a strong permanent magnet.
- a strong magnetic field is generated, magnetically labeled cells are retained on the column, and unlabeled cells pass through the column.
- the separation column is removed from the strong magnetic field, it is retained by the magnetic label!
- the soot cells are eluted and only the mesenchymal stem cells can be separated and acquired.
- a step of concentrating a sample by a membrane filter or an agglutination method may be included as a previous step of the separation step by FACS, MACS or the like.
- the mesenchymal stem cell identification / separation kit according to the present invention may be any other specific material, component, etc., as long as it comprises any of the substances described in (g) to (i) below. Is not particularly limited.
- the mesenchymal stem cell identification 'separation kit described above is used to easily perform the method for identifying mesenchymal stem cells in the ⁇ 1> column or the method for identifying and separating mesenchymal stem cells in the ⁇ 2> column. By providing any of the above (g) to (i), it can be easily commercialized.
- the cell-containing composition according to the present invention includes mesenchymal stem cells isolated by the mesenchymal stem cell identification and separation method described in the above ⁇ 2> column, or those obtained by proliferating the mesenchymal stem cells.
- mesenchymal stem cells isolated by the mesenchymal stem cell identification and separation method described in the above ⁇ 2> column, or those obtained by proliferating the mesenchymal stem cells.
- the specific composition such as the composition of the other buffer solution or the culture solution, the number of cells, etc.
- the cell-containing yarn and composition contain a secreted product (eg, growth factor) secreted from the cells contained in the present composition.
- the cell-containing composition contains undifferentiated mesenchymal stem cells having multipotency into bone, cartilage, fat, muscle, tendon, nerve, etc.
- a pharmaceutical for regenerative medicine It can be used as (pharmaceutical composition).
- the regenerative medicine medicament according to the present invention is not particularly limited as long as it contains the above cell-containing composition.
- the pharmaceutical agent can be used by separating undifferentiated mesenchymal stem cells into various cells suitable for use. Specifically, mesenchymal stem cells are differentiated into osteoblasts, chondrocytes, adipocytes, muscle cells, nerve cells, etc.
- the present invention includes a medicine for regenerative medicine including various cell compositions obtained by differentiating the undifferentiated mesenchymal stem cells in addition to the medicine containing undifferentiated mesenchymal stem cells.
- the administration conditions of the regenerative medicine for clinical application can be appropriately determined using a conventional model animal system or the like. That is, it is possible to examine the administration conditions including the dose, administration interval, and administration route using a model animal, and to determine the conditions for obtaining an appropriate preventive or therapeutic effect.
- a medicine for regenerative medicine is a medicine for "regenerative medicine by cell transplantation" that regenerates tissue lost due to disease or disorder and restores its function, which cannot be regenerated by conventional treatment methods. .
- the regenerative medicine is not particularly limited in terms of the specific disease 'symptoms' and the like that are used as long as it is used for the purpose of the above-mentioned "regenerative medicine by cell transplantation". It is not a thing. Specifically, for example, transplantation of bone marrow mesenchymal stem cells to patients with lower limb ischemia (Bürger's disease), transplantation of bone marrow mesenchymal stem cells to the affected area of periodontal disease, bone marrow mesenchymal system for patients with osteoarthritis Treatments such as transplantation of stem cells, transplantation of amniotic epithelial sheets into burned areas, transplantation of amniotic stem cells into diabetic patients and the like can be mentioned.
- the above regenerative medicine medicament can be combined with a desired pharmaceutically acceptable carrier to form a composition.
- Carriers include, for example, sterile water, saline, buffering agents, plant oils, emulsifiers, suspensions, salts, stabilizers, preservatives, surfactants, sustained release agents, other proteins (such as BSA), And transfer reagents (including lipofusion reagents and ribosomes).
- usable carriers include glucose, ratatoose, gum arabic, gelatin, mantol, starch paste, magnesium trisilicate, talc, corn starch, keratin, colloidal silica, potato starch, urea, hyaluronic acid, collagen And extracellular matrix substances such as polylactic acid and calcium phosphate carrier.
- the dosage form for formulation is not limited, and may be, for example, a solution (injection), a microcapsule, a tablet, or the like. Force that can be administered systemically or locally When systemic administration has side effects or a decrease in the effect, local administration is preferred.
- administration to patients depends on the nature of various cells and diseases, for example, surgical, percutaneous, intranasal, transbronchial, intramuscular, intraperitoneal, intravenous, intraarticular. Can be performed subcutaneously, subcutaneously, intrathecally, intraventricularly, or orally, but is not limited thereto. Force that can be administered systemically or locally When side effects due to systemic administration become a problem, local administration to the lesion site is preferred. Dosage, administration method, tissue migration of the active ingredient of this drug, treatment It will vary depending on the purpose, patient weight, age, symptoms, etc., but those skilled in the art can select as appropriate.
- an individual to be treated is a human subject, but other than this, it may be used for a therapeutic use for a pet animal (pet).
- pet animals include non-human mammals such as mice, rats, rabbits, cats, dogs, monkeys, horses, hidges, and ushi, and other vertebrates.
- the origin of mesenchymal stem cells and various cells differentiated from the mesenchymal stem cells contained in the medicament according to the present invention is the same origin as the individual to be treated (so-called autologous cells). This is preferable from the viewpoint of tolerance, but may be of a different origin (so-called allogeneic cells) in consideration of mass production. In this case, it is necessary to suppress the immune reaction by a conventional method such as an immunosuppressant.
- the mesenchymal stem cell identification method mesenchymal stem cell identification microarray, antibody, mesenchymal stem cell identification 'separation kit, and mesenchymal stem cell identification fraction according to the present invention
- a sample separated from a living body that does not directly treat a human body can be obtained from the human body by a conventional method.
- the sample from which the biological strength is also separated can be obtained from the human body by a conventional method.
- bone marrow fluid, peripheral blood, umbilical cord blood, adipose tissue, periosteum, muscle, synovial membrane, and oral tissue strength were also collected.
- Examples include cells (including mesenchymal stem cells).
- the sample preferably contains mesenchymal stem cells.
- the gene expression profile of the differentiation marker in the mesenchymal stem cells in healthy and diseased patients is examined in advance.
- the expression profile of the mesenchymal stem cells in the subject (patient) with the expression profile of the healthy person's diseased person, the ability of the subject to develop the disease or It is possible to determine the risk of developing a disease in the future.
- the term “healthy person” refers to a person suffering from a disease to be diagnosed
- the term “disease affected person” refers to a person who has literally developed a disease to be diagnosed. .
- the form of utilizing the mesenchymal stem cell identification method and the like is not limited to the above-mentioned one, and may be appropriately changed using the usual method at the time of filing. The only thing you can use!
- the above-mentioned "diseases associated with mesenchymal stem cells” are caused by related mesenchymal stem cells such as a conventionally known abnormality of mesenchymal stem cells or an abnormality of mesenchymal stem cell force.
- the specific disease is not particularly limited as long as it is a disease (so-called “regeneration failure syndrome”).
- mesenchymal stem cells such as abnormal number of cells
- qualitative changes in mesenchymal stem cells include diseases caused as a result of a decrease in changes (eg abnormal differentiation), that is, diseases caused by insufficient supply of mesenchymal stem cells.
- diseases caused as a result of a decrease in changes eg abnormal differentiation
- diseases caused by insufficient supply of mesenchymal stem cells e.g., lower limb ischemia (Burger's disease), periodontal disease, osteoarthritis, refractory skin disease, diabetes and osteoporosis, ischemic heart disease, liver disease, kidney disease, neurodegeneration Diseases (such as Alzheimer's disease) can be mentioned.
- examples of the disease that develops due to insufficient supply of mesenchymal stem cells include osteoarthritis.
- This disease is caused by abnormal changes in the quantity of mesenchymal stem cells in the body due to various causes such as aging and lifestyle (specifically, the number of mesenchymal stem cells decreases). It is estimated that Therefore, the identification method according to the present invention It is considered possible to diagnose and prevent the onset of disease by grasping quantitative changes of mesenchymal stem cells in vivo using In other words, since the quantitative change of mesenchymal stem cells can be known by using the identification method according to the present invention, the classification marker for identification, and the like, this technique can be used to reduce the supply of mesenchymal stem cells.
- a biological sample is collected from a subject (patient) periodically (every month to several years), and the quantitative method of mesenchymal stem cells in the biological sample is identified according to the above-described present invention. Inspect using the. Compare the test results with quantitative results of mesenchymal stem cells in healthy and diseased individuals who have been tested using the same method in advance! It is possible to accurately and accurately diagnose whether or not there is a force that is presently occurring in sexual arthropathy or a force that may develop in the future.
- the present invention provides a method for treating a gene having a base sequence represented by the accession number shown in any of the above-mentioned tables la to lj or a mesenchymal stem cell containing siRNA against a partial sequence thereof.
- Regenerative medicine drugs that suppress differentiation are included. This is a drug that uses RNAi to suppress the undifferentiation of mesenchymal stem cells. That is, suppression of undivided properties of mesenchymal stem cells using RNAi / siRNA using the gene having the base sequence indicated by the accession number shown in any of Tables la to lj above or a partial sequence thereof is suppressed. It can be rephrased as regenerative medicine.
- FB human fibroblasts
- MSC mesenchymal line
- OS 3 strains of osteoblasts
- CH chondrocytes
- AD adipocytes
- mesenchymal stem cells were differentiated into adipocytes, chondrocytes, or osteoblasts, and total RNA was collected. Specifically, it was performed as follows.
- a medium having the following composition was used as a basic medium, a fat differentiation induction medium, and a fat differentiation maintenance medium.
- Insulin 10 ⁇ g / mL (10 mg / mL acetic acid aqueous solution stock) (Wako: 090-03446)
- Dexamethason 1 ⁇ (10 mM EtOH stock) (Sigma: D4902)
- Insulin 10 ⁇ g / mL (10 mg / mL acetic acid aqueous solution stock) (Wako: 090-03446)
- L-glutmine 2 mM (200 mM PBS stock) (Sigma: G3126). Thereafter, re-add every 2 weeks.
- the medium was alternately replaced with the above-described adipose differentiation-inducing medium for 2 days and the adipose differentiation-maintaining medium for 3 days, and the total RNA was recovered after culturing for a total of 11 days.
- Medium exchange was old, leaving 10% of the medium, and gently adding new medium as it was dripped onto the water surface. All additives were prepared at the time of medium change.
- RNA extraction after fat content was performed as follows. First, cells ( ⁇ 100 mm dish) in which fat differentiation was induced were prepared for 11 days. Next, the medium was removed by aspiration and washed twice with PBS. TRIzol® (4000 L / ⁇ 100 mm dish) was then added and homogenized using a 21G needle, 1 ml syringe. Subsequently, 1/4 amount of black mouth form was added, vortexed, and allowed to stand at room temperature for 20 minutes. Next, centrifuge at 14000 rpm for 20 minutes at room temperature (Tomy, MCX-150) o Then transfer the supernatant to a new Eppendorf tube and add 70% EtOH (RNase free water) equivalent to the supernatant.
- EtOH RNase free water
- cartilage differentiation induction medium a medium having the following composition was used.
- Ascorbate 2 -phosphate 50 ⁇ g / ml (stock sol 50 mg / ml MQ) (Sigma: # A ⁇ 8960) D — (+) — glucose: 4.5 g / 1 (stock sol 450 g / 1) (Sigma: # G— 8769)
- TGF- j8 3 10 ng / ml (stock sol 10 ⁇ g / ml HC1 4 mM, HSA or BSA lmg / ml) (Pepro Tec ECL Ltd # 100-36)
- the chondrocyte induction medium was used up for 2 weeks. Also, TGF-
- the cartilage differentiation culture method a pellet culture method was used. Specifically, first, the sowing density is 2.
- the cells were cultured as 5 ⁇ 10 5 cells / tube and the initial amount of cartilage differentiation medium added was 0.5 ml / tube. Next, after seeding, it was centrifuged (500 g ⁇ 5 min). Subsequently, the day of cell seeding was defined as day 0, and the medium was changed every 3 days from the first medium change to an lmlZ test tube. The culture period was 28 days.
- a medium having the following composition was used as the basic medium and the bone differentiation-inducing medium.
- DMEM (Sigma D6046 containing glucose 1000mg / L)
- Figure 1 shows the general flow of the experiment after recovering total RNA.
- double-stranded cDNA was synthesized using T7 oligo dT primer as the sample RNA force. Subsequently, cRNA was synthesized by in vitro transcription using the resulting double-stranded cDNA. Incorporate piotin-labeled ribonucleotides during cRNA synthesis, and sample 7 samples.
- the piotin-labeled cRNA was fragmented and hybridized to a GeneChip (registered trademark, Alfymetrix) probe array.
- the streptavidin phycoerythrin was added to fluorescently label the sample.
- GeneChip Human Genome U133 Plus 2.0 Arrays (HG-U133 Plus 2.0) was used as GeneChip (registered trademark).
- GeneChip analysis conditions of the commissioned analysis service in the present embodiment are as follows.
- Hybridization Oven 640 110V (Affymetrix 8001 38) was used as a noisy hybridization oven.
- Fluidies Station 450 (Affymetrix 00-0079) was used.
- GeneChip Scanner 3000 (Affymetrix 00-0074) was used as a scanner.
- Software f f Gene hip 7 for Hip operating software verl.l (Affymetrix 690036).
- gene expression profiles of various cells related to 54675 human genes were analyzed.
- MSC mesenchymal stem cells
- OS mesenchymal stem cells
- CH cartilage
- AD adipose-differentiated cells
- FB MSC skin-gingiva-derived fibroblasts
- FIG. One broken line in the figure corresponds to one gene (probe) (that is, there are 54675 broken lines in the figure), and the gene expression intensity for each cell shown on the horizontal axis is shown on the vertical axis. It was. From the left of the horizontal axis, adipose-differentiated AD (3 strains), cartilage-differentiated CH (3 strains), skin and gingival FB (3 strains), stem cell MSC (3 strains), and bone separated OS (3 strains) ). For example, since the AD2 strain with the fat content at the left end is the same cell type, the same gene tends to exhibit the same expression level. For this reason, the polygonal lines also tend to be parallel
- FIG. 2 when FIG. 2 is shown in a color drawing, the broken line is colored based on the expression intensity of MSC, red is a gene that is strongly expressed in MSC, blue is weak expression in MSC, and yellow is medium Demonstrate the degree of expression. In the case of a monochrome drawing, the above information is not shown.
- the genes that are shown in red in the MSC3 strain lined up to the right in the middle of Fig. 2 and whose expression intensity is low in other cell types are used as specific undifferentiated markers for MSC. It is thought that it can be used.
- a gene group showing a characteristic expression profile of “high expression in MSC but low in other cells” is selected to distinguish bone, soft bone, fat, fibroblasts from mesenchymal stem cells. It was identified as one specific differential marker for MSC.
- a specific method for selecting a specific fractionation marker for MSC was performed as follows. [0130] First, as pre-processing for selecting a specific classification marker, flag information that can obtain the analysis result of GeneChip (registered trademark) was used.
- a gene indicating present call or margenal call indicating that the gene is expressed was selected from the flag information. This is because if the expression level of MSC is low, even if there is a difference in expression compared to other cell groups, it may not be detected accurately and accurately.
- MSC-specific fractionation markers were selected from the gene group satisfying the pretreatment conditions. Specifically, in this experiment, MSC, OS (MSC force was also differentiated), CH (MSC force differentiated from cartilage), AD (MSC force fat differentiated), FB 5 In two cells, the expression of various genes is examined and compared. For this reason, the relative expression intensity value of five cells is obtained for one gene. Of these five values, the MSC value is compared with the four values excluding the MSC value, and the expression intensity value of the cell with the smallest difference between the MSC expression intensity value and the MSC expression value. One of the selection criteria is that the value excluding the strength value is 2 or more.
- the expression level of MSC is more than twice the expression level of AD, more than twice the expression level of CH, and more than twice the expression level of FB, and One of the selection criteria was to show more than twice the OS expression level.
- the MSC and other cell groups are accurately and accurately identified. This is because they can be identified.
- the value of the difference in expression between MSC and other cell groups is 2 or more, it can be used as a practical marker.
- the numerical value of the difference in expression between MSC and other cell groups calculated in this way specifically shows how strongly each gene is expressed in MSC as compared to other cells. Can be an indicator. Therefore, “This value is 2 or more” is one of the selection criteria. That is, in the present invention, since the purpose is to search for a differentiation marker for specifically selecting undifferentiated mesenchymal stem cells, gene expression in mesenchymal stem cells is higher than that of other cells.
- the selection criteria were set as described above because the reasonably large one should be selected.
- 139 genes were selected as differential markers for undifferentiated MSCs.
- Tables 3a to 3e below show the 139 classification marker information and the evaluation of the selection criteria used as the criteria for selection.
- “Fold AverageJ is the expression of each gene.
- iS is an index indicating how strongly expressed compared to other cells, and is one of the selection criteria described above. In the present invention, it is determined that a value of 2 or more is preferable.
- “Expression levelj is an index of high expression intensity in MSC and is one of selection criteria. In the present invention, it is considered that this numerical value is 0.5 or more. 7
- the 139 genes shown in Tables 3a to 3e satisfy the above-mentioned selection criteria, and can be used as a discrimination marker according to the present invention. Of these genes, those satisfying the above two selection criteria are particularly preferred.
- these genes are differentially expressed in MSC and other connective tissue cells (FB, OS, CH, AD). Specifically, it is specifically expressed only in MSC, and it is weakly expressed in other connective tissue cells to such an extent that it can be distinguished from MSC. For this reason, only the MSC can be specifically identified by using the expression of these genes as a discrimination marker.
- undifferentiated mesenchymal stem cells can be divided into bone, cartilage, fat, muscle, tendon, nerve and the like. Therefore, from the viewpoint of use in regenerative medicine, it is expected as a cell for transplantation for repairing the damage of these tissues.
- the cells are mesenchymal stem cells, and the mesenchymal stem cells probably maintain their ability. The force that needs to be confirmed accurately, simply and accurately.
- the present invention the above technical problem can be solved. Therefore, it can play a very important role in the practical application of regenerative medicine using mesenchymal stem cells.
- the present invention as described above has a wide range of industrial applicability including medical industry, pharmaceutical industry, and the like that are not only academic.
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Cell Biology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Wood Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Food Science & Technology (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Virology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Computational Biology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
表1に記載のアクセッション番号に示される塩基配列を有する遺伝子のうち、少なくとも1つ以上の遺伝子を分別マーカーとし、上記分別マーカーの間葉系幹細胞と結合組織系細胞とにおける発現の差を検出して、間葉系幹細胞と結合組織系細胞とを識別する工程を有する間葉系幹細胞の識別方法によれば、未分化の間葉系幹細胞を、線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞等の他の結合組織系の細胞とを正確に、精度よく識別することができる。また、この間葉系幹細胞の識別方法を用いた間葉系幹細胞、間葉系幹細胞含組成物は再生医療用医薬に利用することができる。
Description
分子マーカーを用いた間葉系幹細胞の識別方法及びその利用 技術分野
[0001] 本発明は、間葉系幹細胞の検出、識別,分離に関し、特に、間葉系幹細胞と線維 芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞等の結合組織系の細胞とにおいて、 発現が異なる間葉系幹細胞検出用の遺伝子マーカー及び Z又は間葉系幹細胞検 出用のタンパク質マーカー等を用いて行う間葉系幹細胞の識別方法及びその利用 に関するものである。
背景技術
[0002] 間葉系幹細胞は、哺乳類の骨髄等に存在し、脂肪細胞、軟骨細胞、骨細胞に分化 する多能性の幹細胞として知られている。間葉系幹細胞は、その分ィ匕多能性の故に 、多くの組織の再生医療のための移植材料として注目されている。すなわち、間葉系 幹細胞を用いて、従来の治療方法では再生しな力つた、疾病や障害により失った組 織を再生し、機能を回復させる「細胞移植による再生医療」である。具体的には、例 えば、下肢虚血 (ビュルガー病)患者に対する骨髄間葉系幹細胞の移植、歯周病患 部への骨髄間葉系幹細胞の移植、変形性関節症患者に対する骨髄間葉系幹細胞 の移植、火傷患部への羊膜上皮シートの移植、糖尿病患者への羊膜幹細胞の移植 等の治療が開始又は計画されて 、る。
[0003] このように間葉系幹細胞を再生医療に利用するためには、まず、幹細胞を生体組 織から採取し、それを未分化のまま増殖させ、さらに増殖させた未分化幹細胞を所望 の細胞へ分化誘導し、再生治療用の組織の調製を行うことが必要となる。
[0004] ここで、本発明者らは以前に、間葉系幹細胞の採取に際して、採取母体に安全で、 且つ採取が容易な分離採取を行うために、口腔組織から間葉系幹細胞を分離採取 する方法を報告している (特許文献 1参照)。また、基底膜細胞外基質の存在下にお V、て、または線維芽細胞増殖因子 (FGF)等の含有培地で間葉系幹細胞を培養する ことによって、間葉系幹細胞が著しく速く増殖させ、かつ、その分ィ匕能を維持できるこ とを見出して、従来の培養方法と比較して顕著に多くの間葉系幹細胞を得る培養方
法を報告して!/ヽる (特許文献 2参照)。
[0005] しかし、間葉系幹細胞を用いた再生医療を実用化するためには、上述の技術のみ では十全とはいえない。具体的には、培養増殖させた間葉系幹細胞を所望の細胞 へ分化誘導し再生医療用の組織を調製する場合、まず培養した細胞が間葉系幹細 胞であることを確認する必要がある。すなわち、培養増殖させた間葉系幹細胞を検出 し、識別する方法を開発することが必要であった。
[0006] この技術的課題に対して、本発明者らは、形態的に類似しており、その区別が困難 な間葉系幹細胞と線維芽細胞とを、間葉系幹細胞検出用遺伝子マーカー及び Z又 は間葉系幹細胞検出用タンパク質マーカーを用いて効果的に識別し、分離する方 法を開発して ヽる (特許文献 3参照)。
特許文献 1:特開 2003 - 52365号公報 (公開:平成 15 (2003)年 2月 25日) 特許文献 2:特開 2003 - 52360号公報 (公開:平成 15 (2003)年 2月 25日) 特許文献 3:特開 2005 - 27579号公報 (公開:平成 17 (2005)年 2月 3日) 発明の開示
発明が解決しょうとする課題
[0007] 以上のように、間葉系幹細胞は、骨、軟骨、脂肪、筋肉、腱、神経などに分化するこ とから、再生医療への利用の観点から、これらの組織の障害を修復させるための移植 用細胞として期待されている細胞であるが、従来、間葉系幹細胞であることを確認す るためには、 in vitroまたは、 in vivoで多分ィ匕能を証明する以外に確実な方法はなか つた。しかし、間葉系幹細胞を組織再生医療に実用化するためには、その細胞が間 葉系幹細胞であること、及び該間葉系幹細胞が多分ィ匕能を維持して 、ることを正確 に、精度よぐかつ簡便に確認する必要があった。
[0008] 確かに、上記特許文献 3に開示の方法では、間葉系幹細胞と線維芽細胞とを識別 •分離するには十分である。し力しながら、骨髄等には、線維芽細胞の他にも骨芽細 胞、軟骨細胞、及び脂肪細胞等の他の結合組織系の細胞が数多く存在する。
[0009] このため、間葉系幹細胞を用いた再生医療の実用化のためには、間葉系幹細胞と 線維芽細胞とを識別する技術だけでは十分とはいえない。そこで、未分化の間葉系 幹細胞を、線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞等の他の結合組織系
の細胞とを正確に、精度よく簡便に識別し、分離する技術の開発が強く望まれていた 。また、力かる技術が開発された場合、未分ィ匕の間葉系幹細胞を大量に培養した際 に、多分ィ匕能を維持している間葉系幹細胞のみを識別し、再生医療に役立てること ちでさる。
[0010] 本発明は、上記の問題点に鑑みてなされたものであり、その目的は、間葉系幹細 胞と、線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞等の結合組織系の細胞とを 正確に、精度よく識別し、及び Z又は、分離する方法及びその利用を提供することに ある。
課題を解決するための手段
[0011] 本発明者らは、上記課題を解決すべく鋭意検討を行った結果、間葉系幹細胞と、 線維芽細胞及びそれ以外の結合組織系の細胞とにお 、て、 DNAマイクロアレイを 用いて遺伝子の発現プロファイルを調べたところ、間葉系幹細胞において特異的に 発現するが、線維芽細胞及びそれ以外の結合糸且織系の細胞では間葉系幹細胞に おける発現と明確な差を検出できる遺伝子が存在するという新事実を見出し、本願 発明を完成させるに至った。本発明は、力かる新規知見に基づいて完成されたもの であり、以下の発明を包含する。
[0012] (1)下記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺 伝子力 選択される、少なくとも 1つ以上の遺伝子を分別マーカーとして用い、 間葉系幹細胞と結合組織系細胞とにおける、上記分別マーカーの発現の差を検出 して、間葉系幹細胞と結合組織系細胞とを識別する工程を有する間葉系幹細胞の 識別方法。
[0013] [表 la]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding -1 BRIP1 NM— 032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK 丽— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 NM— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KIF18A kinesin family member 18 A NM— 031217
NIMA (never in mitosis
ATP/GTP binding - 5 NEK7 醒— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 丽— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 顧— 014674 mannosidase alpha-like 1
calciumん almodulin -
ATP/GTP binding -8 CAMK2D dependent protein kinase 雇— 172127
(CaM kinase) II delta
[表 lc]
[表 Id]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3-like 1 (cartilage
extracellular matrix- 1 CHI3L1 丽— 001276 glycoprotein-39)
keratin 23 (histone
extracellular matrix-2 K T23 NM— 015515 deacetylase inducible)
extracellular matrix- 3 FLG filaggrin 画— 002016 a disintegrin-like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
画 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729—
ほ If]
g¾〕〔l
[表 lh]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 NM 004956 ets variant gene 5 (ets- transcription-2 ETV5 爾— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI NM 032682 high mobility group AT- transcription-4 HMGA2 NM— 003483 hook 2
transcript! on-5 KLF12 Kruppel-like factor 12 NM 007249 transcription-6 PRDM16 PR domain containing 16 NM 0221 14 single-minded homolog 2
transcription- 7 SIM2 NM 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia-associated
transcription- 10 MITF 爾— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 丽— 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 雨— 022743 containing 3
[表 li]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V 1 G3 lysosomal 13kDa, VI NM— 133262 subunit G isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain NM— 020768 containin 16
transport-3 NUPL1 nucleoporin lik 1 NM 014089 solute carrier famil 14
transport-4 SLC14A1 (urea transporter), member 1 NM— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 醒— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate NM— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen NM— 032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽ー 016179 member 4
multiple coagulation factor
transport-9 MCFD2 NM— 139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 丽— 000441 member 4
transport- 11 MCOLN3 mucolipin 3 丽 018298 solute carrier family 25,
transport- 12 SLC25A37 雇— 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
[表 lj]
(2)上記分別マーカーとして、上記表 la〜表 ljに記載のクラス 6, 7, 8, 10,及び 1 3に記載の遺伝子から選択される、少なくとも 1つ以上の遺伝子を用いる(1)に記載 の間葉系幹細胞の識別方法。
(3)上記分別マーカーとして、上記表 la〜表 ljに記載のクラス 6, 7, 8, 10,及び 1 3に記載のクラスのそれぞれから、少なくとも 1つずつ選択された遺伝子を組み合わ せて用いる(2)に記載の間葉系幹細胞の識別方法。
[0015] (4)上記分別マーカーとして、下記表 2に記載の遺伝子力 選択される、少なくとも 1つ以上の遺伝子を用いる(1)〜(3)の 、ずれかに記載の間葉系幹細胞の識別方 法。
[0016] [表 2]
[0017] (5)上記分別マーカーの発現の差の検出は、上記遺伝子の発現の検出、又は上 記遺伝子がコードするタンパク質の発現の検出によって行われるものである(1)〜 (4 )の 、ずれかに記載の間葉系幹細胞の識別方法。
[0018] (6)下記 (a)〜(d)のいずれかのうち、少なくとも 1つ以上を固定ィ匕させてなる間葉 系幹細胞の識別用マイクロアレイ:
(a)上記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺伝 子のうち、少なくとも 1つ以上の遺伝子;
(b)上記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺伝 子のうち、少なくとも 1つ以上の遺伝子のアンチセンス鎖;
(c)上記 (a)又は (b)の部分塩基配列;及び
(d)上記 (a)〜(c)の 、ずれかに示される塩基配列を有するポリヌクレオチドとストリン ジェントな条件下でハイブリダィズするポリヌクレオチド。
[0019] (7)下記 (e)又は (f)に記載のポリペプチドを用いて誘導され、当該ポリペプチドに 特異的に結合する抗体:
(e)上記表 la〜表 ljに記載のいずれかのァクセッション番号に示される塩基配列を
有する遺伝子によってコードされるポリペプチド;及び
(f)上記 (e)の部分ポリペプチド。
[0020] (8)下記 (g)〜 (i)の 、ずれかに記載の物質を備える間葉系幹細胞の識別 ·分離キ ッ卜:
(g)上記(6)に記載の間葉系幹細胞の識別用マイクロアレイ;
(h)上記(7)に記載の抗体;及び
(i)上記表 la〜表 ljに記載のいずれかのァクセッション番号に示される塩基配列を 有する遺伝子又はその部分配列と、ストリンジヱントな条件下でハイブリダィズするポ リヌクレオチドからなる間葉系幹細胞の分別マーカー遺伝子の検出用プローブ。
[0021] (9)上記(1)〜(5)の 、ずれかに記載の間葉系幹細胞の識別方法によって識別さ れた間葉系幹細胞を、分離する工程を有する間葉系幹細胞の識別分離方法。
[0022] (10)上記 (9)に記載の間葉系幹細胞の識別分離方法によって分離された間葉系 幹細胞、又は当該間葉系幹細胞を増殖させたものを含む細胞含有組成物。
[0023] (11)上記(10)に記載の細胞含有組成物を含む再生医療用医薬。
[0024] (12)上記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺 伝子のうち、いずれか 1つの遺伝子であることを特徴とする間葉系幹細胞の識別用分 別マーカー。
[0025] (13)上記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺 伝子にコードされるポリペプチドのうち、いずれか 1つのポリペプチドである間葉系幹 細胞の識別用分別マーカー。
[0026] (14)生体力 分離した試料に対して、上記(1)〜(5)のいずれかに記載の間葉系 幹細胞の識別方法, (6)に記載の間葉系幹細胞の識別用マイクロアレイ, (7)に記 載の抗体, (8)に記載の間葉系幹細胞の識別'分離キット,及び(12)または(13)に 記載の間葉系幹細胞の識別用分別マーカーから選択される手段を、いずれか単独 、または複数を組み合わせて用いることにより、当該試料の提供者において間葉系 幹細胞が関連する疾患が発症している力 または将来発症する可能性があるかを判 定する方法。なお、本方法は、診断方法と予防方法の両方を意図したものである。
[0027] (15)上記表 la〜表 ljに記載のいずれかのァクセッション番号に示される塩基配列
を有する遺伝子又はその部分配列に対する siRNAを含む間葉系幹細胞の未分化性 を抑制する再生医療用医薬。
発明の効果
[0028] 本発明に係る間葉系幹細胞の識別方法及びその利用法によれば、未分化の間葉 系幹細胞における発現パターンと、線維芽細胞、骨芽細胞、軟骨細胞、脂肪細胞等 の結合組織系の細胞における発現パターンとを比較した場合、明確に発現パターン に差が存在する遺伝子等を分別マーカーとして用いている。このため、例えば、骨髄 中に含まれる未分化の間葉系幹細胞と、結合組織系の細胞とを正確に、精度よぐ かつ簡便に識別し、及び Z又は、分離することができるという効果を奏する。
[0029] それゆえ、本発明によれば、骨、軟骨、脂肪、筋肉、腱、神経等への分化が可能な 、多分化能を有する未分化の間葉系幹細胞を、再生医療へ利用する場合に障害と なって 、た問題、すなわち未分ィ匕の間葉系幹細胞と線維芽細胞や結合組織系の細 胞等の他細胞集団との識別の問題を克服することができる。したがって、間葉系幹細 胞を用いた再生医療の実用化に大きく貢献することができる。
[0030] また、この間葉系幹細胞の識別方法を用いた間葉系幹細胞、間葉系幹細胞含糸且 成物は再生医療用医薬に利用することができる。
図面の簡単な説明
[0031] [図 1]本実施例における手順の流れの概略を模式的に示す図である。
[図 2]本実施例において、 DNAマイクロアレイを用いて、間葉系幹細胞 (MSC)と他 の結合組織系の細胞とにおける遺伝子の発現の差を解析した結果を示す図である。 発明を実施するための最良の形態
[0032] 本発明は、 DNAマイクロアレイ等を用いて、未分化の間葉系幹細胞に特異的に発 現する遺伝子を分別マーカーとして検出し、間葉系幹細胞を結合組織系の細胞 (例 えば、線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞)等の他細胞集団から効果 的に識別'分離する方法を構築することが可能となる。また、本発明の方法を利用し て、試験管内で増殖させた間葉系幹細胞の品質 (多分ィ匕能を維持しているか否力) を検定することも可能となり、間葉系幹細胞を用いた再生医療の実用化に資すること も可能となる。
[0033] そこで、以下では、まず本発明の特徴的な部分である間葉系幹細胞の識別方法に ついて説明するとともに、併せて当該方法に使用する材料としての識別分離マーカ 一、マイクロアレイ、抗体について説明する。最後に、識別分離方法、細胞含有組成 物(さらに、細胞分泌物 (成長因子等)を含むことが好ましい)、再生医療用の医薬、 識別 ·分離キット等の各種応用技術につ!、て説明する。
[0034] なお、本明細書中で使用される場合、用語「ポリペプチド」は、「ペプチド」または「タ ンパク質」と交換可能に使用される。本発明に係るポリペプチドはまた、天然供給源 より単離されても、組換え生成されても、化学合成されてもよい。
[0035] また、本明細書中で使用される場合、用語「ポリヌクレオチド」は、「遺伝子」、「核酸 」または「核酸分子」と交換可能に使用され、ヌクレオチドの重合体が意図される。ま た、「遺伝子」には、 DNAのみならず、 RNA (例えば mRNA)をも含む意である。本 明細書中で使用される場合、用語「塩基配列」は、「遺伝子配列」、「核酸配列」また は「ヌクレオチド配列」と交換可能に使用され、デォキシリボヌクレオチド (A、 G、じお よび Tと省略される)の配列として示される。
[0036] < 1.間葉系幹細胞の識別方法 >
本発明に係る間葉系幹細胞の識別方法は、上記表 la〜表 ljに記載のァクセッショ ン番号に示される塩基配列を有する遺伝子のうち、少なくとも 1つ以上の遺伝子を分 別マーカーとして利用し、上記分別マーカーの間葉系幹細胞と結合組織系の細胞と における発現の差を検出して、間葉系幹細胞と結合組織系の細胞とを識別する工程 を有するものであればよぐその他の工程、条件、使用材料、使用機器等の具体的な 構成が特に限定されるものではな 、。
[0037] ここで、上記表 la〜表 ljには、 139個の遺伝子を 16のクラス(Classification)に分 類して表示している。この分類は、各遺伝子がコードするタンパク質の分子機能を Eu ropean Bioinformatics Institute【こよる Gene Ontology (^O)【こ ¾つ ヽて行った。
[0038] 具体的には、クラス 1 (Classification 1)は、 ATPZGTP結合タンパク質に関する力 テゴリーであり、 8種類、 8つのァクセッション番号で示す遺伝子が属する。また、クラ ス 2 (Classification 2)は、結合タンパク質に関するカテゴリーであり、 10種類、 10のァ クセッション番号で示す遺伝子が属する。なお、本明細書及び表では、このクラス 2に
示す" binding- 1〜10"は、 "DNA/metal ion/collagen binding- 1〜10"を意味する。クラ ス 3 (Classification 3)は、細胞増殖またはメンテナンスに関する因子のカテゴリーであ り、 11種類、 11つのァクセッション番号で示す遺伝子が属する。
[0039] クラス 4 (Classification 4)は、サイト力インに関するカテゴリーであり、 6種類、 6のァ クセッション番号で示す遺伝子が属する。クラス 5 (Classification 5)は、細胞内骨格に 関するカテゴリーであり、 9種類、 9つのァクセッション番号で示す遺伝子が属する。ク ラス 6 (Classification 6)は、酵素のカテゴリーであり、 3種類、 3つのァクセッション番号 で示す遺伝子が属する。
[0040] クラス 7 (Classification 7)は、細胞外マトリックスまたは細胞内骨格に関するカテゴリ 一であり、 5種類、 5つのァクセッション番号で示す遺伝子が属する。クラス 8 (Classific ation 8)は、増殖因子またはレセプターに関するカテゴリーであり、 7種類、 7つのァク セッション番号で示す遺伝子が属する。
[0041] クラス 9 (Classification 9)は、膜に関するカテゴリーであり、 12種類、 12のァクセッシ ヨン番号で示す遺伝子が属する。クラス 10 (Classification 10)は、膜結合タンパク質 に関するカテゴリーであり、 4種類、 4つのァクセッション番号で示す遺伝子が属する
[0042] クラス 11 (Classification 11)は、タンパク質結合に関する因子のカテゴリーであり、 1 0種類、 10のァクセッション番号で示す遺伝子が属する。クラス 12 (Classification 12) は、タンパク質修飾に関する因子のカテゴリーであり、 8種類、 8つのァクセッション番 号で示す遺伝子が属する。クラス 13 (Classification 13)は、シグナル伝達に関与する 因子のカテゴリーであり、 5種類、 5つのァクセッション番号で示す遺伝子が属する。
[0043] クラス 14 (Classification 14)は、転写因子に関するカテゴリーであり、 12種類、 12の ァクセッション番号で示す遺伝子が属する。クラス 15 (Classification 15)は、細胞内 輸送に関する因子のカテゴリーであり、 13種類、 13のァクセッション番号で示す遺伝 子が属する。
[0044] クラス 16 (Classification 16)は、上記クラスに属しない、その他の因子に関するカテ ゴリーであり、 16種類、 16のァクセッション番号で示す遺伝子が属する。なお、上記 カテゴリ一は、 NCBIに開示の公知の情報に基づき分類したものである。
[0045] このように、上記表 la〜表 ljに示す遺伝子群は、遺伝子がコードするタンパク質の 分子機能に着目して分類したものである。このため、これらの遺伝子を分別マーカー として利用することにより、間葉系幹細胞と結合組織系細胞とにおける各遺伝子の機 能や働きに着目して、間葉系幹細胞と結合組織系細胞とを分別することができる。具 体的には、例えば、間葉系幹細胞では、特定の細胞外マトリックスに関連する因子の 発現量が多ぐ一方結合組織系細胞ではそれほどでもないことが知られている場合 は、クラス 7に属する遺伝子を分別マーカーとして利用することで、簡便かつ正確に 間葉系幹細胞を識別できる。
[0046] また、これらの遺伝子を分別マーカーとして使用することにより、分子機能の面から 間葉系幹細胞のマーカーとして評価できる利点もある。
[0047] なお、上記表 la〜表 lj中、「Gene symbol]は遺伝子の略称を示し、「Gene titlejは 遺伝子の一般的な名称およびその他関連する情報を示し、「Genbank number」は Ge nbankのァクセッション番号を示している。遺伝子データベースに、同一の遺伝子に っ 、て複数のァクセッション番号が与えられて 、るものが存在する場合 (例えば Tran script variantなど)は、その全てのァクセッション番号で示される遺伝子についても本 願発明の権利範囲に属することはいうまでもない。
[0048] また、本明細書にぉ ヽて「結合組織」とは、軟骨組織、骨組織を含む支持 ·結合組 織全般の組織のことである。支持組織とは、狭義の結合組織 (Connective tissue)と、 特殊に分ィ匕した結合組織 (軟骨組織、骨組織、血液とリンパ)を総称したものである。 なお、広義に解釈し、支持組織のことを「結合組織」と称してもカゝまわない。個体発生 学的には「中胚葉 (一部、外胚葉に由来する場合もある)」に由来し、身体の内部構 造を保持する役割をもつものである。また「結合組織系の細胞」とは、上記支持'結合 組織を構成する細胞のことであり、例えば、固定細胞として、線維芽細胞 (Fibroblasts )、細網細胞(Reticular cells)、脂肪細胞 (Adipose cells)、自由(遊走)細胞として、マ クロファージ (組織球または大食細胞)(Macrophages)、肥満細胞 (Mast cells)、形質 細胞(Plasma cells)、リンパ球(Lymphoid cells)、顆粒性白血球(Granulocytes)、軟 骨組織を構成する固定細胞として軟骨細胞 (chondrocytes)、骨組織を構成する骨芽 細胞(Osteoblasts)、骨細胞(Osteocytes)を挙げることができる。本発明では、これら
各種細胞のなかでも特に、線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞 (これ らをまとめて結合組織系細胞と称する)と、間葉系幹細胞との識別を行うものであるこ とが好ましい。
[0049] また、本発明において「分別マーカー」として使用する上記表 la〜表 ljの遺伝子群 は、後述する実施例に示すように、 DNAマイクロアレイを用いて、未分化の間葉系幹 細胞、線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞のそれぞれの発現プロファ ィルを調べた実験により、未分化の間葉系幹細胞と他の細胞集団(結合組織系細胞 )との間に顕著な発現の差が認められたものである。
[0050] このため、これらの遺伝子群の発現の差を指標として、未分化の間葉系幹細胞を、 線維芽細胞、骨芽細胞、軟骨細胞、及び脂肪細胞と簡便、正確にかつ精度よく分別 することができる。上記表 1の遺伝子群の塩基配列及び当該遺伝子群がコードするタ ンパク質のアミノ酸配列情報は既に公知であり、特に、遺伝子群の塩基配列情報は 、 Genbankの遺伝子データベースにおいて、上記表 la〜表 ljに記載のァクセッション 番号によりアプローチすることができる。
[0051] また、上記表 la〜表 ljに記載の遺伝子のうち、後述の実施例に示すような判断基 準を満たすものが好ましい。例えば、「Fold AverageJ及び「Expression level」がともに 高い数値の遺伝子を単独で、又は適宜組み合わせて用いることが好ましい。さらに いえば、「Fold Averageが 2以上」及び Z又は「Expression levelが 0. 5以上」の遺伝 子をマーカーとして用いることが好まし!/、。
[0052] また、上記分別マーカーとしては、上記表 la〜表 ljに記載のクラス 6, 7, 8, 10,及 び 13に属する遺伝子力も選択される、少なくとも 1つ以上の遺伝子を用いることが好 ましい。
[0053] 上記表 la〜表 lj中のクラス 6, 7, 8, 10,及び 13に属する遺伝子は、特に、間葉 系幹細胞と結合組織系細胞とにおいて、大きく発現パターンが異なり、間葉系幹細 胞で発現が高いものが多い。このため、分別マーカーとして好適に用いることができ る。また、これらの発現の高い、かつ個体差が少ない遺伝子を分別マーカーとして使 用することにより、間葉系幹細胞の正確な識別を可能にするような利点もある。
[0054] さらに、上記表 la〜表 ljに記載されたクラス 6, 7, 8, 10,及び 13のそれぞれのク
ラスから、少なくとも 1つずつ選択された遺伝子を組み合わせて用いることがより好ま しい。これは、間葉系幹細胞と結合組織系細胞との間において発現パターンが大きく 異なるクラスから、それぞれ少なくとも 1つずつ遺伝子を選択し、組み合わせて分別マ 一力一として用いると!、う意である。上記のように 5つのクラス力も少なくとも 1つずつ 遺伝子を選択することにより、 5つのカテゴリーに属する遺伝子のそれぞれについて 発現パターンを確認できるため、識別の正確性と精度をより一層高めることができる。
[0055] また、上記分別マーカーとして、上記表 2に記載の遺伝子から選択される、少なくと も 1つ以上の遺伝子を用いることが特に好ましい。
[0056] 上記表 2は、上記表 la〜表 ljに記載されている 139個の遺伝子のうち、特に好まし いものを 6個選択して、まとめたものである。これらの遺伝子は、間葉系幹細胞と結合 組織系細胞とにおいて、特に発現パターンが大きく異なっており、かつ、遺伝子自体 の発現量も多ぐ分別マーカーとして使用する場合、最も好適なものである。また、こ れらの少数のマーカーを用いることにより、間葉系幹細胞の識別においては利便性 の向上、コストの削減ができるという利点もある。
[0057] さらに、上記 16クラスに属する遺伝子のうち、同一のクラスに属する遺伝子を複数 組み合わせて使用することもできる。例えば、転写因子に関連するクラスに属する遺 伝子を組み合わせて分別マーカーとして用いることにより、間葉系幹細胞に特異的 なタンパク質合成を力なり上流力も把握することができる。また、細胞骨格に関連する クラスに属する遺伝子を組み合わせて用いることにより、ケラチン類等の間葉系幹細 胞に特徴的なタンパク質の産生等について把握することができる。また、成長因子に 関連するクラスに属する遺伝子を組み合わせて用いることにより、細胞の成長因子産 生等について把握できる。また、細胞外基質に関連するクラスに属する遺伝子を組 み合わせて用いることにより、細胞の接着性等について把握できる。また、シグナル 伝達に関連するクラスに属する遺伝子を組み合わせて用いることにより、細胞外刺激 に対する応答性等を把握できる。また、輸送に関連するクラスに属する遺伝子を組み 合わせて用いることにより、細胞内輸送の状態等を把握できる。
[0058] このように、各カテゴリーに含まれる分別マーカーを組み合わせることにより、それぞ れのカテゴリーに特有の効果を期待でき、非常に有用性が高い。また、識別の正確
性と精度も高くなる。
[0059] また、上述のような利用以外にも、例えば、 16のクラス (その他のクラスは除いてもよ い)のそれぞれから少なくとも 1つずつ遺伝子を選択し、各クラスの特徴を網羅的に 解析することも可能である。なお、このような場合、上記分別マーカーの使用は、各ク ラスにおいて少なくとも 1つずつ用いればよいが、特に、後述する実施例に示す"評 価基準"の高いマーカーを使用するほど、また、使用するマーカーの数が増加するほ ど、識別'解析の正確性と精度が高まり、信頼性の高い識別方法を実行することがで きる。したがって、上述のように、複数の分別マーカーを組み合わせる場合は、 "評価 基準"が高いものを優先的に採用し、かつできる限り使用する分別マーカーの数を増 やすことが好ましい。
[0060] また、上記分別マーカーの発現の差の検出は、上記遺伝子の発現の検出、又は上 記遺伝子がコードするタンパク質の発現の検出によって行うことができる。具体的に は、まず、本発明においては、間葉系幹細胞と結合組織系の細胞とにおける上記の ような分別マーカー遺伝子の発現の差を、後記するそれ自体公知の遺伝子の検出 手段を用いて検出し、間葉系幹細胞の識別を行うことができる。このため、本発明に は、上記表 la〜表 ljのいずれかに記載のァクセッション番号に示される塩基配列を 有する遺伝子のうち、いずれ力 1つの遺伝子である間葉系幹細胞の識別用分別マー カーが含まれる。
[0061] 本発明において、上記分別マーカーの遺伝子群の発現を検出するには、公知の 遺伝子の発現の検出に用いられる従来公知の方法を好適に用いることができる。例 えば、下記 (a)〜(d)のいずれかを、少なくとも 1つ以上を固定ィ匕させてなる間葉系幹 細胞の識別用マイクロアレイを用いて分別マーカーの遺伝子群の発現を検出するこ とができる:
(a)上記表 la〜表 ljのいずれかに記載のァクセッション番号に示される塩基配列を 有する遺伝子のうち、少なくとも 1つ以上の遺伝子;
(b)上記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺伝 子のうち、少なくとも 1つ以上の遺伝子のアンチセンス鎖;
(c)上記 (a)又は (b)の部分塩基配列;及び
(d)上記 (a)〜(c)の 、ずれかに示される塩基配列を有するポリヌクレオチドとストリン ジェントな条件下でハイブリダィズするポリヌクレオチド。
[0062] 上記マイクロアレイとしては、例えば、米国 Aifymetrix社の DNAマイクロアレイゃス タンフォード(Stanford)型の DNAマイクロアレイ等、その他半導体製造で用いられる 微細加工技術を用いてシリカ基板上に直接オリゴヌクレオチドをィ匕学合成する DNA マイクロアレイを含む従来公知のあらゆるタイプのマイクロアレイを好適に用いること ができ、その具体的な大きさ、形状、システム等については特に限定されるものでは ない。
[0063] 上述した間葉系幹細胞の識別用マイクロアレイによれば、多数の分別マーカーの 遺伝子群の発現を網羅的 ·体系的に解析できるため、間葉系幹細胞と結合組織系の 細胞とを非常に簡便、正確かつ精度よく識別でき、極めて有用性が高い。したがって 、本発明には上記間葉系幹細胞の識別用マイクロアレイが含まれる。
[0064] 換言すれば、本発明に係る間葉系幹細胞の識別方法においては、複数の分別マ 一力一を指標として用いることが非常に好ましいといえる。特に、間葉系幹細胞と他 の細胞群とにおいて、発現の差が十分に存在し、発現レベルも高い分別マーカーを 複数組み合わせて使用することが好ましい。例えば、 Fold Average, Expression level が高いような CHI3L1, FLG, KRTAP1— 5, RGS4, HNT, SLC14A1, IFI30, ZNF423, LX Nを適宜組み合わせて使用する場合を挙げることができる。
[0065] また、上記間葉系幹細胞の識別用マイクロアレイ以外にも、例えば、本発明におけ る分別マーカーの遺伝子群の発現の検出のために、ノーザンブロッテイング法を用 いることができる。また、本発明における分別マーカーの遺伝子の発現を検出、識別 するために、本発明における分別マーカーの遺伝子の全長 DNA配列又はその部分 配列とストリンジェントな条件下でノヽイブリダィズする塩基配列を有する分別マーカー 遺伝子の検出用プローブを用いることができる。
[0066] 上記検出用プローブを用いて間葉系幹細胞と結合糸且織系の細胞とにおける遺伝 子の発現を検出するには、公知の方法を用いて適宜実施することができる。例えば、 公知の分別マーカーの遺伝子の DNA配列から適宜の長さの DNAプローブを作製 し、適宜蛍光標識等の標識を付与しておき、これを被検体とハイブリダィズすることに
より、間葉系幹細胞の検出を行う。上記検出用プローブとしては、公知の分別マーカ 一の遺伝子の塩基配列のアンチセンス鎖の全長配列又は部分配列からなる分別マ 一力一遺伝子の検出用のプローブを用いることができる。
[0067] なお、上記 DNAプローブの作製に際して、本発明の塩基配列において、「マーカ 一遺伝子の DNA配列とストリンジェントな条件下でノヽイブリダィズする」条件としては 、 ί列えば、、 42°Cでのノヽイブリダィゼーシヨン、及び 1 X SSC (0. 15M NaCl、 0. 015 Mクェン酸ナトリウム)、 0. 1%の SDS (Sodium dodecyl sulfate)を含む緩衝液による 42°Cでの洗浄処理を挙げることができ、より好適には、 65°Cでのハイブリダィゼーシ ヨン、及び 0. 1 X SSC、 0. 1%の SDSを含む緩衝液による 65°Cでの洗浄処理を挙 げることができる。なお、ハイブリダィゼーシヨンのストリンジエンシーに影響を与える 要素としては、上記温度条件以外に種々の要素があり、当業者であれば種々の要素 を組み合わせて、上記例示したノヽイブリダィゼーシヨンのストリンジエンシーと同等の ストリンジエンシーを実現することが可能である。
[0068] また、被検細胞における分別マーカーの遺伝子の発現を検出するに際しては、被 検細胞の遺伝子を増幅するために、定量的又は半定量的 PCRを用いることができる 。上記定量的又は半定量的 PCRとしては、例えば、 RT— PCR (逆転写 PCR)を用い ることができる。上記定量的又は半定量的 PCRを行うに際しては、本発明におけるマ 一力一遺伝子を増幅するためのセンスプライマー及びアンチセンスプライマーからな る 1対のプライマーセットを用いる。
[0069] また、本発明の間葉系幹細胞の識別方法は、インべーダ (Invader (登録商標))法 を利用して簡便に行うこともできる。例えば、上述の分別マーカーの配列に特異的に ノ、イブリダィズする配列と酵素切断部位とを有するシグナルプローブを設計し、被検 查対象の細胞力 抽出したトータル RNA(cDNAでも構わない)、インべーダオリゴ( Invader (登録商標) Oligo)、タリベース酵素(Cleavase (登録商標) Enzyme)、及びフ レットプローブ (FRET Probe)とともに所定の温度、所定の時間(例えば、 63°C、 2時 間等)反応させることにより行うことができる。なお、具体的な実験手法や条件につい ては、下記参考文献を参照して適宜行うことができる(参考文献 :G) T. J. Griffin et al ., Proc Natl Acad Sci U S A 96, 6301—6 (1999) 、 (ii) M. W. Kaiser et al., J Biol Che
m 274, 21387-94 (1999)、 (iii) V. Lyamichev et al., Nat Biotechnol 17, 292-6 (1999) 、 (iv) R. W. Kwiatkowski et al., Mol Diagn 4, 353—64 (1999)、 (v) J. G. Hall et al., P roc Natl Acad Sci U S A 97, 8272—7 (2000)、 (vi) M. Nagano et al" J Lipid Res 43, 1 011-8 (2002)等参照)。上記のように、インべ一ダ法を利用すれば、遺伝子増幅の必 要がない場合もあり、迅速かつ低コストで行うことができる。なお、市販のインべーダ 法キットを利用すれば、より一層簡便に本発明を実施できる。
[0070] また、 in situハイブリダィゼーシヨンを用いて、本発明に係る間葉系幹細胞の識別 方法を行うこともできる。例えば、上述の分別マーカー又はその部分配列を標識した ものをプローブとして用い、スライドグラス上の被検査対象細胞の標本に直接分子雑 種を形成させて、その部分を検出することにより簡易に行うことができる。具体的には 、スライドグラス上に被検査対象の細胞の薄切片 (パラフィン切片、凍結切片など)を 調製し、これに標識したプローブをハイブリダィズさせ、ノーザンハイブリダィゼーショ ン法と同じように、プローブを洗い落とし、写真用ェマルジヨンを塗布し、露光する。現 像後、銀粒子の分布から、ハイブリダィズした場所を特定する。より具体的な実験手 法や条件につ!、ては、下記参考文献を用いて適宜行うことができる (参考文献: (0「in situハイブリダィゼーシヨン法」、(1995年 7月)、古庄敏行、井村裕夫監修、金原出版 (株)発行、 932頁〜 937頁、 (ii) Tin situノヽイブリダィゼーシヨンによる遺伝子発現の解 析」、「遺伝子工学実験」、(1991年 5月)、野村慎太郎著、(社)日本アイソトープ協会 発行、 221頁〜 232頁等参照)。 in situハイブリダィゼーシヨン法には、ラジオァイソトー プ(主として3 H)標識した DNAをプローブとして、その座位をオートラジオグラフィー で検出する方法と、標識された DNAプローブの蛍光シグナルを蛍光顕微鏡下で検 出する方法があるが、いずれの方法を用いてもよい。
[0071] また、本発明の分別マーカー遺伝子の発現を、当該遺伝子がコードするタンパク質 として検出する場合には、このタンパク質を用いて、このタンパク質に特異的に結合 する抗体を作製し、この抗体を用いて、後記するそれ自体公知の方法で分別マーカ 一タンパク質の間葉系幹細胞と結合組織系の細胞とにおける発現を検出し、間葉系 幹細胞の識別を行うことができる。
[0072] このため、上記表 la〜表 ljのいずれかに記載のァクセッション番号に示される塩基
配列を有する遺伝子にコードされるポリペプチドのうち、いずれか 1つのポリペプチド である間葉系幹細胞の識別用分別マーカーが含まれる。さらに、下記 (e)又は (f)に 記載のポリペプチドを用いて誘導され、当該ポリペプチドに特異的に結合する抗体 が含まれる:
(e)上記表 la〜表 ljのいずれかに記載のァクセッション番号に示される塩基配列を 有する遺伝子のうち、いずれかの遺伝子によってコードされるポリペプチド;及び
(f)上記 (e)の部分ポリペプチド。
[0073] なお、上記抗体は、ポリクローナル抗体であってもよ 、し、モノクローナル抗体であ つてもよい。上記抗体の作製は、例えば、本発明の分別マーカーの遺伝子がコード するポリペプチドの全長配列又はその部分配列を抗原として、従来公知の常法により 作製することができる。
[0074] 例えば、モノクローナル抗体を生産する方法としては、特に限定されるものではなく 、例えば、抗原でマウスを免疫した後、そのマウス脾臓リンパ球とマウス由来のミエ口 一マ細胞とを融合させてなる抗体産生ハイプリドーマにより、モノクローナル抗体を得 ればよい。ハイプリドーマの生産方法は、従来公知の方法、例えば、ハイプリドーマ 法(Kohler, G. and Milstein, C, Nature 256, 495-497(1975))、トリオ一マ法、ヒト B— 細胞ハイプリドーマ法(Kozbor, Immunology Today 4, 72(1983))、及び EBV—ハイブ リド ~~マ法 (Monoclonal Antibodies and Cancer Therapy, Alan R Liss, Inc., 77-96(19 85))等を利用することが可能であり、特に限定されるものではない。
[0075] また、上記抗原としては、ポリペプチドであれば特に限定されるものではな 、が、抗 原決定基とする物質をキャリアタンパク質に結合してなる抗原タンパク質が用いられ てもよい。具体的には、上記抗原がハプテンであれば、抗体の産生等を誘導する能 力をもたないため、抗体を産生することができないが、抗原を異種由来のタンパク質 などの生体高分子力もなる担体と共有結合させて抗原タンパク質を得て、これで免疫 すれば、抗体産生を誘導することができる。上記担体としては、特に限定されるもの ではなぐオボアルブミン、 γグロブリン、へモシァニン等、この分野で従来公知の各 種タンパク質を好適に用いることができる。また、モノクローナル抗体は遺伝子組換え 技術等によっても生産できる。
[0076] また、ポリクローナル抗体を生産する方法としては、実験動物に抗原を接種'感作さ せ、その体液力 抗体成分を精製して取得する方法を挙げることができる。なお、免 疫させる動物としては、マウス、ラット、ゥサギ、サル、ゥマ等の従来公知の実験動物を 用いることができ、特に限定されるものではない。また、抗原を接種'感作させる場合 、その間隔や量についても常法にしたがって適宜行うことができる。
[0077] また、本発明の抗体を用いて、被検細胞における分別マーカーのタンパク質の発 現を検出するには、公知の抗体を用いた免疫学的測定法を用いて実施することがで きる。上記免疫学的測定法としては、例えば RIA法、 ELISA法、蛍光抗体法等の公 知の免疫学的測定法を挙げることができる。また、上述した以外にも、例えば、ウェス タンブロッテイング法、酵素免疫測定法、抗体による凝集や沈降や溶血反応を観察 する方法、糸且織免疫染色や細胞免疫染色などの形態学的検出法も必要に応じて利 用することができる。
[0078] なお、本発明において、分別マーカーの発現の差の検出は、単一の分別マーカー について行い、その結果力も間葉系幹細胞を識別してもよいが、より正確に、より精 度の高い識別を行うためには、複数の分別マーカーの発現の差を指標として識別す ることが好ましい。このような点からも、分別マーカーとして遺伝子の発現の差を指標 する場合、上述の間葉系幹細胞の識別用マイクロアレイを用いて識別方法を実施す ることが好ましいといえる。
[0079] < 2.間葉系幹細胞の識別分離方法 >
本発明に係る間葉系幹細胞の識別分離方法は、上記 < 1 >欄に記載の間葉系幹 細胞の識別方法によって識別された間葉系幹細胞を、分離する工程を有するもので あればよぐその他の工程、条件、使用材料、使用機器等の具体的な構成について は特に限定されるものではな 、。
[0080] 本発明において、間葉系幹細胞を分離する方法としては、例えば、蛍光活性化セ ルソーター(Fluorescence- Activated Cell Sorter : FACS)を用いることができる。具体 的には、本発明における抗体を用いて蛍光抗体法により、間葉系幹細胞を標識化し 、被検細胞における間葉系幹細胞の分別マーカーのポリペプチドの発現を検出し、 間葉系幹細胞を識別、分離することができる。蛍光抗体法により未分化の間葉系幹
細胞を標識ィ匕するには、本発明における分別マーカーのポリペプチドに特異的に結 合する抗体を蛍光標識し、これを、抗原を発現している間葉系幹細胞に結合させて、 間葉系幹細胞を標識化する (直接蛍光抗体法)か、或いは、抗原を発現している間 葉系幹細胞に、未標識の本発明の特異抗体を結合させた後に、標識化した二次抗 体 (抗免疫グロブリン抗体)を結合させて間葉系幹細胞を標識ィ匕することができる(間 接蛍光抗体法)。上述の手法により標識ィ匕した間葉系幹細胞は、フローサイトメトリー で測定分離を行い、採取することができる。なお、分離した試料をフィルターにとり落 斜蛍光顕微鏡で観察し確認してもよ ヽ。
[0081] また、上述の FACS以外にも、磁気セルソーティング(Magnetic Cell Sorting: MAC S)システムにより分離することもできる。 MACSは、蛍光標識に替えて磁性を帯びた マイクロビーズを標識ィ匕した抗体を用いる。 目的細胞は MACS用の磁性マイクロビ ーズにて標識化された抗体により特異的に標識され、強力な永久磁石に設置された 分離カラムにアプライされる。分離カラムでは強力な磁場が生じており、磁気標識さ れた細胞はカラムに保持され、標識されていない細胞はカラムを通過する。分離カラ ムを強磁場から外すと磁気標識により保持されて!ヽた細胞が溶出され、間葉系幹細 胞のみを分離 '取得することができる。
[0082] なお、上述の FACSや MACS等による分離工程の前段階として、メンブレンフィル ター又は凝集法により試料を濃縮する工程を含んで 、てもよ 、。
[0083] < 3.識別'分離キット >
本発明に係る間葉系幹細胞の識別 ·分離キットは、下記 (g)〜 (i)の 、ずれかに記 載の物質を備えるものであればよぐその他の具体的な材料、構成部品等について は特に限定されるものではな 、。
(g)上述の間葉系幹細胞の識別用マイクロアレイ;
(h)上述の抗体;及び
(i)上記表 la〜表 ljのいずれかに記載のァクセッション番号に示される塩基配列を 有する遺伝子又はその部分配列の 、ずれかと、ストリンジェントな条件下でハイブリダ ィズするポリヌクレオチドからなる間葉系幹細胞の分別マーカー遺伝子の発現の検 出用プローブ。
[0084] 上記間葉系幹細胞の識別'分離キットは、上記 < 1 >欄の間葉系幹細胞の識別方 法、又は < 2>欄の間葉系幹細胞の識別分離方法を容易に実施するためのもので あり、上記 (g)〜(i)のいずれかを備えることにより、容易に製品化することができる。
[0085] また、上述したように、上記表 la〜表 ljに記載の分別マーカーを複数用いて識別 方法等を実施することが、正確性、精度の面力も好ましいため、本識別'分離キットに は、複数の分別マーカーが含まれることが好ましい。例えば、上記 < 1 >欄で説明し たように、様々な好ましい組み合わせで遺伝子を選択し、分別マーカー用キットとし て使用することができる。
[0086] 上記のように、複数の分別マーカーを組み合わせた場合、単一の分別マーカーを 用いる場合に比べて、著しく正確性と精度のょ 、識別 ·分離を行うことができる。
[0087] <4.細胞含有組成物及び再生医療用の医薬 >
本発明に係る細胞含有組成物は、上記 < 2 >欄に記載の間葉系幹細胞の識別分 離方法によって分離された間葉系幹細胞、又は当該間葉系幹細胞を増殖させたも のを含むものであればよぐその他の緩衝液'培養液等の組成、細胞数等の具体的 な構成については特に限定されるものではない。さらに、上記細胞含有糸且成物には 、本組成物に含まれる細胞から分泌される分泌物 (例えば、増殖因子等)が含まれる ことが好ましい。
[0088] 上記細胞含有組成物は、骨、軟骨、脂肪、筋肉、腱、神経等への多分化能を有す る未分ィ匕の間葉系幹細胞を含むため、例えば、再生医療用医薬 (薬学的組成物)と して用いることができる。すなわち、本発明に係る再生医療用医薬は、上記細胞含有 組成物を含むものであればよぐその他の具体的な構成については特に限定されな い。なお、本医薬は、例えば、使用に際して、未分化の間葉系幹細胞を使用に適し た各種細胞へ分ィ匕させて使用することもできる。具体的には、各種サイト力イン等の 分化誘導物質を用いて間葉系幹細胞を骨芽細胞、軟骨細胞、脂肪細胞、筋肉細胞 、神経細胞等へ分化させ、当該分化させた各種細胞を再生医療の治療対象となる患 者に投与すればよい。したがって、本発明には、未分化の間葉系幹細胞を含む医薬 以外にも、上記未分化の間葉系幹細胞を分化させた各種細胞組成物を含む再生医 療用の医薬も含まれる。
[0089] また、臨床適用のための上記再生医療用の医薬の投与条件は、常法のモデル動 物系等を用いて適宜決定することができる。すなわち、モデル動物を用いて投与量、 投与間隔、投与ルートを含む投与条件を検討し、適切な予防または治療効果を得ら れる条件を決定することができる。このような再生医療用の医薬は、従来の治療方法 では再生しな力つた、疾病や障害により失った組織を再生し、機能を回復させる「細 胞移植による再生医療」のための医薬となる。
[0090] 上記再生医療用の医薬は、上述の「細胞移植による再生医療」を目的として使用さ れるものであればよぐ使用される具体的な疾患 '症状'病態等については特に限定 されるものではない。具体的には、例えば、下肢虚血 (ビュルガー病)患者に対する 骨髄間葉系幹細胞の移植、歯周病患部への骨髄間葉系幹細胞の移植、変形性関 節症患者に対する骨髄間葉系幹細胞の移植、火傷患部への羊膜上皮シートの移植 、糖尿病患者への羊膜幹細胞の移植等の治療等を挙げることができる。
[0091] また、上記再生医療用の医薬は、薬学的に許容できる所望の担体と組み合わせて 組成物とすることができる。担体としては、例えば、滅菌水、生理食塩水、緩衝剤、植 物油、乳化剤、懸濁剤、塩、安定剤、保存剤、界面活性剤、徐放剤、他のタンパク質 (BSAなど)、トランスフエクシヨン試薬(リポフエクシヨン試薬、リボソーム等を含む)等 が挙げられる。さらに、使用可能な担体としては、グルコース、ラタトース、アラビアゴ ム、ゼラチン、マン-トール、デンプンのり、マグネシウムトリシリケート、タルク、コーン スターチ、ケラチン、コロイドシリカ、ばれいしよデンプン、尿素、ヒアルロン酸、コラー ゲン等の細胞外マトリックス物質、ポリ乳酸、リン酸カルシウム担体などが挙げられる。
[0092] 製剤化する場合の剤型は制限されず、たとえば溶液 (注射剤)、マイクロカプセル、 錠剤などであってよい。投与は全身または局所的に行い得る力 全身投与による副 作用や効果の低下がある場合には、局所投与することが好ましい。
[0093] また、患者への投与は、各種細胞や疾患等の性質に応じて、例えば外科的、経皮 的、鼻腔内的、経気管支的、筋内的、腹腔内、静脈内、関節内、皮下、脊髄腔内、 脳室内、または経口的に行われうるがそれらに限定されない。投与は全身的または 局所的にされ得る力 全身投与による副作用が問題となる場合には病変部位への局 所投与が好ましい。投与量、投与方法は、本医薬の有効成分の組織移行性、治療
目的、患者の体重や年齢、症状などにより変動するが、当業者であれば適宜選択す ることが可能である。
[0094] 治療対象となる個体は、原則としてヒトを対象としているが、これ以外にも、愛玩動 物(ペット)用の治療用の用途へ使用してもよい。愛玩動物としては、例えば、マウス、 ラット、ゥサギ、ネコ、ィヌ、サル、ゥマ、ヒッジ、ゥシなどの非ヒト哺乳動物およびその 他の脊椎動物を挙げることができる。
[0095] また、本発明に係る医薬に含まれる間葉系幹細胞及び当該間葉系幹細胞から分 化した各種細胞の由来は、治療対象の個体と同じ由来 (いわゆる自家細胞)であるこ とが免疫寛容の点から好まし 、が、量産化等を考慮すると異なる由来 ( 、わゆる他家 細胞)であっても構わない。この場合は、別途免疫抑制剤等の常法により免疫反応を 抑制する必要がある。
[0096] < 5.その他の禾 lj用 >
間葉系幹細胞は生体内(例えば、骨髄中)でどのように局在しているかについては 、全く知見が得られていない。しかし、本発明に係る抗体を用いることにより、生体内 の間葉系幹細胞の局在を調べることができる。したがって、この技術を応用して、あら たな医薬品の開発等を行うことが可能になる。具体的には、生体内において、間葉 系幹細胞が傷害部分へ移動や遊走する知見が得られた場合、間葉系幹細胞の傷害 部分への移動'遊走を促進するような有効成分を含む医薬品を開発することができる
[0097] また、本発明に係る間葉系幹細胞の識別方法、間葉系幹細胞の識別用マイクロア レイ、抗体、間葉系幹細胞の識別'分離キット、及び間葉系幹細胞の識別用分別マ 一力一のいずれか単独、または複数を組み合わせて用いることにより、間葉系幹細 胞が関連する疾患が発症している力 または将来発症する可能性があるかを判定す ることもできる。本判定方法は、上記疾患の予防と診断の両方を意図したものである。
[0098] 本発明を実行する場合、直接人体に対して処置するのではなぐ生体から分離した 試料を対象とすることが好ましい。上記生体力も分離した試料とは、常法により人体よ り得ることが可能であるが、例えば、骨髄液、末梢血、臍帯血、脂肪組織、骨膜、筋肉 、滑膜、口腔組織力も採取した細胞(間葉系幹細胞を含む)等を挙げることができる。
特に、上記特許文献 1〜3に開示の方法により間葉系幹細胞が含まれる生体試料を 採取することが好ましい。なお、上記試料には、間葉系幹細胞が含まれていることが 好ましい。
[0099] 本判定方法は、例えば、本発明に係る間葉系幹細胞の識別方法等を用いることに より、健常者と疾病罹患者とにおける間葉系幹細胞における分別マーカーの遺伝子 発現プロファイルをあらかじめ調べておき、被験者 (患者)における間葉系幹細胞の 発現プロファイルが上記健常者'疾病罹患者のいずれの発現プロファイルと類似する かを比較検討することによって、被験者が現在疾病を発症している力 あるいは将来 的に疾病を発症する危険性がどの程度あるかを判定することができる。本明細書に ぉ 、て「健常者」とは診断対象とする疾患を罹患して 、な 、者を 、、「疾病罹患者」 とは文字通り診断対象となる疾患を発症している者をいう。なお、本発明に係る疾病 の発症を判定する方法において、間葉系幹細胞の識別方法等を利用する形態は上 述のものに限られるものではなぐ出願当時の常法を用いて適宜変更して利用するこ とができることは 、うまでもな!/、。
[0100] また上記「間葉系幹細胞が関連する疾患」としては、従来公知の間葉系幹細胞の 異常、又は間葉系幹細胞力 の分ィ匕異常等の間葉系幹細胞が関連して引き起こさ れる疾患 (所謂、「再生不良症候群」)であればよぐその具体的な疾患については特 に限定されるものではない。例えば、疾病や障害により失った組織を再生し、機能を 回復させる「細胞移植による再生医療」の対象となる疾患の他、間葉系幹細胞の量 的変化 (細胞数の異常等)や質的変化 (分化能の異常等)が低下する結果、引き起こ される疾患、つまり間葉系幹細胞の供給不足により発症する疾患等を挙げることがで きる。具体的には、例えば、下肢虚血 (ビュルガー病)、歯周病、変形性関節症、難治 性皮膚疾患、糖尿病、及び骨粗しょう症、虚血性の心疾患、肝疾患、腎疾患、神経 変性疾患 (アルツハイマー病等)等を挙げることができる。
[0101] また、上記間葉系幹細胞の供給不足により発症する疾患としては、例えば、変形性 関節症がある。この疾患は、加齢や生活習慣等の種々の原因により、生体内の間葉 系幹細胞の量的変化に異常が起こる (具体的には、間葉系幹細胞の数が減少する) ことにより引き起こされることが推定されている。このため、本発明に係る識別方法等
を利用して、生体内の間葉系幹細胞の量的変化を把握することにより、疾患の発症 の有無を診断 ·予防することが可能と考えられる。つまり、本発明に係る識別方法や 識別用分別マーカー等を用いることにより、間葉系幹細胞の量的変化を知ることがで きるため、この技術を利用して、間葉系幹細胞の供給不足により発症する疾患の発 症可能性を診断することが可能と考えられる。具体的には、例えば、被験者 (患者)か ら定期的 (数ケ月〜数年の間隔)に生体試料を採取し、生体試料中の間葉系幹細胞 の量的変化について上記本発明に係る識別方法等を利用して検査する。その検査 結果と、予め同様の手法により検査しておいた健常者 ·疾病罹患者とにおける間葉 系幹細胞の量的変化につ!、ての検査結果とを比較検討して、上記被験者が変形性 関節症に現在発症している力、または将来的に発症する可能性がある力否かを正確 に、精度よく診断することができる。
[0102] また、本発明には、上記表 la〜表 ljのいずれかに記載のァクセッション番号に示さ れる塩基配列を有する遺伝子又はその部分配列に対する siRNAを含む間葉系幹細 胞の未分化性を抑制する再生医療用医薬が含まれる。これは、 RNAiを利用して、間 葉系幹細胞の未分ィ匕性を抑制する医薬のことである。すなわち、上記表 la〜表 ljの いずれかに記載のァクセッション番号に示される塩基配列を有する遺伝子又はその 部分配列を用いた RNAi/siRNAを用いる間葉系幹細胞の未分ィ匕性を抑制する再生 医療用医薬とも換言できる。
[0103] 上記再生医療用医薬によれば、確実かつ効率的に間葉系幹細胞の未分ィ匕性を抑 制することができる。このため、再生医療に大きな利点をもたらすことができる。
[0104] 以下実施例を示し、本発明の実施の形態についてさらに詳しく説明する。もちろん 、本発明は以下の実施例に限定されるものではなぐ細部については様々な態様が 可能であることはいうまでもない。さらに、本発明は上述した実施形態に限定されるも のではなぐ請求項に示した範囲で種々の変更が可能であり、それぞれ開示された 技術的手段を適宜組み合わせて得られる実施形態についても本発明の技術的範囲 に含まれる。
実施例
[0105] 本実施例では、ヒトの線維芽細胞(以下、「FB」と称する場合もある)を 3株、間葉系
幹細胞(以下、「MSC」と称する場合もある)を 3株、骨芽細胞(以下、「OS」と称する 場合もある)を 3株、軟骨細胞(以下、「CH」と称する場合もある)を 3株、脂肪細胞(以 下、「AD」と称する場合もある) 3株を対象として、 DNAマイクロアレイを用いて、それ ぞれの細胞における遺伝子の発現プロファイルを調べた。なお、骨芽細胞、軟骨細 胞、及び脂肪細胞は、それぞれ間葉系幹細胞から試験管内にて分化誘導して得ら れたものである。
[0106] (0)分化誘導及びトータル RN Aの回収
まず、間葉系幹細胞を脂肪細胞、軟骨細胞、又は骨芽細胞へと分化させ、トータル RNAを回収した。具体的には、以下のように行った。
[0107] (0— 1)脂肪細胞への分ィ匕誘導及び RNA回収
基本培地及び脂肪分化誘導培地、脂肪分化維持培地として以下の組成の培地を 使用した。
•脂肪分化誘導培地
基本培地: DMEM (Sigma: D5796, high glucose =4500 mg/L)
添加物: 10%(V/V) FBS (Hyclone, Lot No.: ANC 18139)
Penicillin-Streptomycin (bigma: P0781)
以下は、用時添加する(2週間で使い切り)
Insulin: 10 μ g/mL (10 mg/mL酢酸水溶液ストック) (Wako: 090-03446) Dexamethason: 1 μ Μ (10 mM EtOHストック)(Sigma: D4902)
Indomethacin: 200 ^ Μ (2000 mM DMSOストック) (Wako: 097-02471)
3-isobutyl-l-methylxanthine: 500 μ Μ (1000 mM DMSOストック)(Wako: 537—7
2353)
脂肪分化維持培地
基本培地: DMEM (Sigma:#D- 5796, high glucose =4500mg/L)
添加物: 10%(V/V) FBS (Hyclone, Lot No.: ANC 18139)
Penicillin-Streptomycin (bigma: P0781)
以下は、用時添加する(2週間で使い切り)
Insulin: 10 μ g/mL (10 mg/mL酢酸水溶液ストック) (Wako: 090-03446)
なお、培地が 2週間経過した場合は、 L- glutamine: 2 mM (200mM PBSストック) (Sig ma: G3126)を添カ卩した。以後、 2週間毎に再添加する。
[0108] MSCがコンフルェントに達した後、上記脂肪分化誘導培地で 2日、脂肪分化維持 培地で 3日間交互に培地交換し、計 11日間培養後、トータル RNAを回収した。培地 交換は古 、メディウムを 10%残し、水面に滴下するようにして穏やかに新 、培地を 加えた。全ての添加物は、培地交換時に調製した。
[0109] 脂肪分ィ匕後の RNAの抽出は以下のように行った。まず、 11日間、脂肪分化誘導し た細胞( Φ 100 mmディッシュ)を準備した。次に、培地を吸引除去し、 PBSで 2回洗 浄した。次いで、 TRIzol (登録商標) (4000 L / φ 100 mmディッシュ) を加え、 21G ニードル、 1mlシリンジを使用してホモジナイズした。続いて、クロ口ホルムを 1/4量 加えてボルテックス後、 20分間室温で静置した。次に、 14000 rpm, 20分間室温で遠 心した(Tomy, MCX-150) oその後、上清を新しいエツペンドルフチューブに移し、上 清と等量の 70%EtOH (RNase free水使用)を加えた。サンプル 700 μ 1を RNeasy ( 登録商標) Miniカラムにアプライ後、バキュームを行った(Qiagen, QIAvac 24)。全て のサンプルが無くなるまで繰り返した(2カラム/ φ 100 mmディッシュ 1枚)。なお、以上 の処理は、 RNeasyキットに添付の説明書に従った。最後に、 Ambion社製のキット(# 1906)を使用し、 RNAの精製を行った。
[0110] (0— 2)軟骨細胞への分ィ匕誘導及び RNA回収
軟骨分化誘導培地として以下の組成の培地を使用した。
•軟骨分化誘導培地
a MEM (Sigma:#4526)
Penicillin Streptomycin: (bigma: #P0781)
L— glutamine: 2 mM (stock sol 200 mM PBS) (Sigma: #G3126)
Dexamethason: 10— 7 M (stock sol 1 M EtOH) (Sigma: #D— 1756)
Ascorbate 2 -phosphate: 50 μ g/ml (stock sol 50 mg/ml MQ) (Sigma: #A~8960) D—(+)— glucose: 4.5 g/1 (stock sol 450 g/1) (Sigma: #G— 8769)
Pyruvate: 100 μ g/ml (stock sol 100 mg/ml MQ) (Sigma: #28-4020-2)
ITS— plus: 1 % (V/V) (insulin 6.25 μ g/ml, transferring 6.25 μ g/ml, selenous acid 6.
25 μ g/ml, linoleic acid 5.33 μ g/ml, bovine serum albumim 1.25 mg/ml) (BD: #35 4352)
TGF- j8 3: 10 ng/ml (stock sol 10 μ g/ml HC1 4 mM, HSA or BSA lmg/ml) (Pepro Tec ECL Ltd #100-36)
なお、軟骨分ィ匕誘導培地は 2週間使い切りとした。また、 TGF- |8 3は最初に添加せ ず、培地交換の際に用時添加した。
[0111] 軟骨分化培養法は、ペレット培養法を用いた。具体的には、まず、播種密度は 2.
5 X 105cell/試験管とし、最初の軟骨分化培地添加量は、 0. 5ml/試験管として 培養した。次に、播種後、遠心した(500g X 5min)。続いて、細胞播種した日を day 0とし、 1回目の培地交換から lmlZ試験管とし、 3日ごとに培地交換を行った。培養 期間は 28日とした。
[0112] RNAの抽出は以下のように行った。まず、 28日間軟骨分化誘導した細胞( X 6ペレ ット以上)を準備した。次に、培地を吸引除去し、 PBSO. 4ml加えて、これを吸引した 。続いて、 TRIzol (登録商標) (Invitrogen: 15596- 018)を 0. 2ml/tube加え、ペレツ トぺッスルとシリカ粉末で粉砕抽出した。さらに 0. 8ml/tube追加し、抽出物をチュ ーブに移した後、クロ口ホルム処理、エタノール処理以後は RNeasy キットを用いた 。その後の処理は、上述の脂肪分化の場合と同様に抽出した。
[0113] (0— 3)骨芽細胞への分ィ匕誘導及び RNA回収
基本培地及び骨分化誘導培地として以下の組成の培地を使用した。
基本培地
•DMEM (Sigma D6046)
•終濃度 10% FBS (Hyclone社) (牛胎仔血清)
•饥'生剤 penicillin— streptmycin (¾igma:P0781)
骨分化誘導培地
•DMEM (Sigma D6046含 glucose 1000mg/L)
'終濃度 10% FBS (Hyclone社)
'終濃度 10— 7M Dexamethason (Sigma D- 1756)
'終濃度 lOmM β -glycerophosphate (東京化成工業 G- 0195)
'終濃度 50 g/ml Ascorbate 2- phosphate (Sigma: A- 8960)を 2週間おきに添カロ '終濃度 2mM L- glutamineを 2週間おきに添カロ
•饥'生剤 penicillin— streptmycin (¾igma:P0781)
なお、参考文献として、 Osteogenic differentiation of purified culture-expanded hu man、 mesenchymal stem cell in vitro.、 Jaiswal N. J. et al., Cell Biochem. 64, 295—3 12, 1997を参照した。
[0114] まず、 0. 01% Collagen typel溶液 (機能性ペプチド IFP9660)で、培養プレート 表面を 4°C、一昼夜浸した。その後、溶液を除き、 PBS (リン酸緩衝化生理食塩水)で 2回洗浄した。次に、間葉系幹細胞の上記基本培地で細胞を播種した(lOOOOcells /cm2)。コンフルェント状態 (集密状態)になるまで培養 (播種後 2〜3日)し、上記骨 分ィ匕誘導培地に培地交換した (dayO)。以降 3日おきに骨分化誘導培地で培地交換 した。 28日目にトータノレ RNAを回収した。なお、トータノレ RN Aの回収は上述した脂 肪細胞の欄で説明したものと同様の方法で行った。
[0115] トータル RNAを回収した後の実験の大まかな流れを、図 1に示す。
[0116] (l) cDNAZcRNA合成
まず、サンプル RNA力も T7オリゴ dTプライマーを使用して 2本鎖 cDNAを合成し た。続いて、得られた 2本鎖 cDNAを用いて、 in vitro Transcription反応により cRNA を合成。この cRNA合成の際にピオチン標識リボヌクレオチドを取り込み、サンプルを 標 し 7こ。
[0117] (2)ハイブリダィゼーシヨン
次に、ピオチン標識 cRNAを断片化して GeneChip (登録商標、 Alfymetrix社製)プ ローブアレイにハイブリダィズした。
[0118] (3)蛍光標識
次いで、オーバーナイトでノ、イブリさせたアレイを洗浄した後、ストレプトアビジン フィコエリスリンを投入しサンプルを蛍光標識した。
[0119] (4)スキャニング Zデータ解析
最後に、蛍光標識されたアレイをスキャニングし、イメージ画像を取得。得られた画 像を、専用解析ソフトを用いて、シグナルの数値化'発現解析を行った。
[0120] なお、上記(1)〜(4)の各工程については、(株) KURABOが提供する、 Afiymetri X社の作製する DNAマイクロアレイ「GeneChip (登録商標)」を使用した受託解析サ ~~ヒスを禾 IJ用し 7こ (http:/ 1 www.bio.kurabo.co.jp/ idensi/ genechip/ genecniptop.ntm) 。本受託解析サービスは、サンプル RNAを提供するだけで、 GeneChip (登録商標) の解析を行ってくれるものである。したがって、(2)〜(4)の各工程についての説明は 上記 URL及び同社の提供する受託解析サービスを参照することにより当業者であれ ば理解可能であるため、ここではその詳細な説明を省略する。
[0121] 本実施例では、 GeneChip (登録商標)は、 Human Genome U133 Plus 2.0 Arrays( HG-U133 Plus 2.0)を用いた。また、本実施例における上記受託解析サービスの Gen eChip解析条件は以下の通りである。
[0122] ピオチン標識ターゲット調製は、開始条件としてトータル RNAを 2 μ g用いた。解析 プロトコ■ ~"ノレとして、 One-cycle Target Labeling^ Geneし hip Expression Analysis Tech nial Manual, 701021 Rev.5、 Section 2 Eukaryotic Sample and Array Processings Cha pter 1 Eukaryotic Target Preparationを用いた。
[0123] ハイブリダィゼーシヨン/スキャンにおいては、解析プロトコールとして、 GeneChip E xpression Analysis Technial Manual, 70102丄 Rev.5、 section 2 Eukaryotic Sample an d Array Processings Chapter 2 Eukaryotic Target Hybridizationを用 ヽた。また、ノヽィ ブリダィゼーシヨンオーブンとしては、 Hybridization Oven 640 110V (Affymetrix 8001 38)を用いた。洗浄 Z染色装置として、 Fluidies Station 450 (Affymetrix 00- 0079)を用 いた。スキャナとして、 GeneChip Scanner 3000 (Affymetrix 00- 0074)を用いた。ソフト ゥエフ f 、 Geneし hip Operating software verl.l (Affymetrix 690036) 用 ヽ 7こ。
[0124] スキャン画像解析'数値化においては、解析プロトコールとして、 GeneChip Express ion Analysis Technial Manual, 701021 Rev.5、 Section 2 Eukaryotic sample and Arra y Processings Chapter 3 Washing, Staining, and Scanningを用 ヽた。ソフトウェアとし て、 GeneChip Operating Software verl.lを用い、アルゴリズムとして、 Statisticalを用 いた。解析パラメータとして、 CIIPファイル作成時に、 Scaling Factor; 1、 Target Value ; 500、 Detection Call; Alphal=0.05, Alpha2=0.065, Tau=0.015を用いた。
[0125] 上記 (4)のスキャニング Zデータ解析の結果得られたシグナルの数値化'発現解析
に関するデータを、 Silicon Genetics社製の遺伝子解析ソフトウェア GeneSpring (商品 名、トレ ~~ドマ ~~ク、 http://www.silicongenetics.com/cgi/SiG.cgi/Products/Gene pri ng/index.smf)を用いて遺伝子リストの作成等の解析作業を行った。なお、ソフトゥェ ァ GeneSpringの使用方法については、添付の取扱説明書にしたがった。
[0126] すなわち、本実施例では、ヒト遺伝子 (プローブ) 54675個に関する、各種細胞の 遺伝子発現プロファイルを解析した。具体的には、多様な細胞に分化する能力をも つた間葉系幹細胞 (MSC) 3株と、 MSCを骨分化させた細胞 (OS) 3株と、 MSCを 軟骨分化させた細胞 (CH) 3株と、 MSCを脂肪分化させた細胞 (AD) 2株と、 MSC と形は良く似ているが、多様な細胞に分化する能力をもたない皮膚'歯肉由来繊維 芽細胞 (FB) 3株と、の合計 15株に関して各々細胞に含まれる RNAを回収し、 5467 5個のヒト遺伝子 (プローブ)に関して発現強度を DNAマクロアレイで解析した。
[0127] 上述の解析結果を図 2に示す。図中の折れ線 1本は 1つの遺伝子 (プローブ)に対 応し (つまり、図中には 54675本の折れ線が存在する)、横軸に示した細胞毎の遺伝 子発現強度を縦軸に示した。横軸の左から、脂肪分化した AD (3株)、軟骨分化した CH (3株)、皮膚 ·歯肉の FB (3株)、幹細胞 MSC (3株)、骨分ィ匕した OS (3株)を示 す。なお、例えば、左端の脂肪分ィ匕させた AD2株は同種の細胞であるため、同じ遺 伝子は同じ発現レベルを示す傾向がある。このため、折れ線も平行になる傾向がある
[0128] また、図 2をカラー図面で示す場合、折れ線は MSCの発現強度を基準に色付けさ れており、赤色は MSCで強発現している遺伝子、青色は MSCにおいて弱い発現、 黄色は中程度の発現を示す。なお、モノクロ図面の場合、上記情報は示さない。
[0129] このため、図 2の中ほど右に並べた MSC3株において赤く示され、かつ、その他の 細胞種にぉ 、て発現強度が低くなる遺伝子は、 MSCの特異的未分ィ匕マーカーとし て利用可能であると考えられる。つまり、「MSCでは発現が高いが、その他の細胞で は低い遺伝子」という特徴的な発現プロファイルを示す遺伝子群を選び出し、骨、軟 骨、脂肪、線維芽細胞と、間葉系幹細胞とを区別できる MSCの特異的分別マーカ 一として同定した。上記 MSCの特異的な分別マーカーの具体的な選別方法にっ ヽ ては、以下のように行った。
[0130] まず、具体的な分別マーカーの選定の前処理として、 GeneChip (登録商標)の解析 結果力も得られる flag情報を用いた。具体的には、 flag情報のうち、遺伝子が発現して いることを示す present callまたは margenal callを示す遺伝子を選択した。これは、 M SCの発現レベルが低ければ、他の細胞群と比較して発現に差があった場合でも、正 確で精度よく検出できない可能性があるためである。
[0131] そして、上記前処理条件を満たす遺伝子群から、 MSC特異的な分別マーカーを 選別した。具体的には、今回の実験では、 MSC、 OS (MSC力も骨分ィ匕させたもの) 、 CH (MSCから軟骨分化させたもの)、 AD (MSC力 脂肪分化させたもの)、 FBの 5つの細胞において、種々の遺伝子の発現を調べて比較している。このため、 1つの 遺伝子に対して、 5つの細胞の相対的な発現強度の値が得られる。この 5つの値のう ち、 MSCの値を除いた 4つの値と、 MSCの値とを比較して、 MSCの発現強度の値 と最も差の小さな細胞の発現強度の値で、 MSCの発現強度の値を除した数値が、 2 以上であることを選定基準の 1つとした。
[0132] 換言すれば、 MSCの発現レベル力 ADの発現レベルの 2倍以上を示し、かつ、 C Hの発現レベルの 2倍以上を示し、かつ、 FBの発現レベルの 2倍以上を示し、かつ、 OSの発現レベルの 2倍以上を示すことを選定基準の 1つとした。これは、 MSCの発 現強度と最も差の少な 、細胞の発現強度との間にお 、て、少なくとも 2倍の違 、があ れば、正確に、精度よく MSCと他の細胞群とを識別することができるためである。つ まり、 MSCと他の細胞群との発現の差の値が 2以上であれば、実用的なマーカーと して使用に堪え得るわけである。
[0133] このようにして算出した MSCと他の細胞群とにおける発現の差の数値は、 MSCに おける各遺伝子の発現力 他の細胞に比べてどの程度強く発現しているかを具体的 に示す指標となり得る。このため、「この値が 2以上であること」を選択基準の 1つとし た。すなわち、本発明では、未分ィ匕の間葉系幹細胞を特異的に選択するための分別 マーカーの探索を目的としているため、間葉系幹細胞における遺伝子の発現が、他 の細胞に比べて、明らかに大きいものを選定すべきだとの理由から、上述のように選 択基準を設定した。
[0134] もう 1つの選択基準として、「MSCにおける遺伝子の発現強度が高いこと」を用いた
。これは、間葉系幹細胞における発現量の絶対値が小さくては、正確に精度の高い 検出が困難となったり、誤差が大きくなつたりする可能性があるためである。つまり、 絶対的な発現量が大きな遺伝子でなければ、分別マーカーの候補として不適切であ ると考えたため、この「MSCにおける遺伝子の発現強度が 0. 5以上であること」をもう 1つの選択基準とした。
[0135] 上述の選定基準を満たす遺伝子として、 139個の遺伝子を未分化の MSCの分別 マーカーとして選別した。その 139個の分別マーカー情報及び選別した際の基準と なった上記選定基準に関する評価を下記表 3a〜表 3eに示す。
[0136] [表 3a]
Classification 1 Gene symbol Genbank number Fold Average Expression level
ATP/GTP binding -1 BRIP1 NM 032043 4.7 0.2
ATP/GTP binding -2 PASK NM 015148 9.4 0.3
ATP/GTP binding -3 RAC2 NM 002872 13.6 1.0
ATP/GTP binding -4 KIF18A NM 031217 4.8 0.4
ATP/GTP binding -5 NEK7 丽 133494 2.9 34.2
ATP/GTP binding -6 ARL4C NM 005737 3.7 8.6
ATP/GTP binding -7 EDEM1 NM 014674 2.6 1.9
ATP/GTP binding -8 CAMK2D NM 172127 2.7 4.2
[表 3b]
Classification 4 Gene symbol Genbank number Fold Average Expression level cytokine - 1 GDF15 NM 004864 4.4 3.0 cytokine -2 IL6 NM 000600 14.9 3.9 cytokine -3 CTGF NM 001901 5.6 60.6 cytokine -4 VEGF NM 001025366 4.5 24.4 cytokine -5 VEGFC NM 005429 4.1 9.8 cytokine -6 HGF NM 000601 6.5 0.7
[表 3c]
Classification 9 Gene symbol Genbank number Fold Average Expression level membrane -1 ABHD2 NM 007011 4.5 2.1 membrane -2 ITGA2 NM 002203 7.7 2.2 membrane -3 LAMA3 NM 198129 6.6 1.3 membrane -4 NET02 NM 018092 7.9 4.9 membrane - 5 NTN4 NM 021229 5.5 6.5 membrane -6 PTGER1 NM 000955 5.2 0.5 membrane -7 EPHB2 NM 017449 12.4 0.4 membrane -8 SFRP1 NM 003012 0.4 0.6 membrane -9 CD33L3 NM 213602 11.9 1.3 membrane -10 GLIPR1 NM 006851 4.8 6.8 membrane -11 UGCG NM 003358 4.2 14.2 membrane -i2 ADORA1 NM 000674 3.5 0.5
[表 3d]
Classification 10 Gene symbol Genbank number Fold Average Expression level membrane binding
ANXA10 雇— 007193 24.5 1.2 protein- 1
membrane binding
RARRES1 NM 206963 7.2 0.5 protein-2
membrane binding
HNT 醒— 016522 13.1 16.0 protein-3
membrane binding
CNTNAP3 爾— 033655 22.3 1.2 protein-4
[表 3e]
Classification 14 Gene symbol Genbank number Fold Average Expression level transcription- 1 ETV1 NM 004956 6.9 3.6 transcription-2 ETV5 NM 004454 3.4 2.1 transcription-3 FOXP1 NM 032682 3.5 8.6 transcription-4 HMGA2 NM 003483 6.2 4.4 transcription-5 KLF12 NM 007249 5.2 0.4 transcription-6 PRDM16 NM 022114 8.1 0.7 transcription-7 SIM2 NM 009586 3.8 0.4 transcription-8 SUHW2 NM 080764 4.6 0.1 transcription-9 ENOl NM 001428 3.7 0.3 transcription- 10 MITF NM 198159 0.7 0.6 transcription- 1 1 TCF3 NM 003200 3.2 0.2 transcription- 12 SMYD3 NM 022743 3.0 7.5
Classification 15 Gene symbol Genbank number Fold Average Expression level transport- 1 ATP6V 1G3 NM 133262 3.9 0.3 transport-2 KCTD16 醒 020768 5.8 0.4 transport-3 NUPL1 固 014089 4.0 0.9 transport-4 SLC14A1 NM 015865 22.3 6.5 transport-5 SLC16A4 匪 004696 5.6 5.1 transport-6 SLC4A4 NM 003759 6.6 0.4 transport-7 SLC9A7 NM 032591 7.3 0.6 transport- 8 TRPC4 NM 016179 27.0 0.3 transport-9 MCFD2 NM 139279 3.7 10.0 transport- 10 SLC26A4 NM 000441 4.1 0.3 transport- 1 1 MCOLN3 NM 018298 3.1 0.6 transport- 12 SLC25A37 NM 016612 2.2 4.2 transport- 13 SLC30A7 NM 133496 2.7 3.5
ここで、 da〜表 3e中、「Classification」、「Gene symbol」、「Genbank numberj【ま、 上記表 la〜表 ljのそれらと同一である。また、「Fold AverageJは、各遺伝子の発現
iS 他の細胞に比べてどの程度強く発現しているかを示す指標であり、上述した選択 基準の 1つである。本発明では、この数値が 2以上であるものを好ましいものと判定し た。
[0138] また、「Expression leveljは、 MSCにおける発現強度が高いことの指標であり、選択 基準の 1つである。本発明では、この数値が 0. 5以上であるものを好ましいものと判 し 7こ。
[0139] また、「Fold Average]は以下のように算出した。本実施例における実験では、 1つ の遺伝子に対して、 5種類の細胞毎に相対的な発現強度の値が得られる。そこで、こ の 5つの値のうち、 MSCの値を除いた 4つの値と、 MSCの値とを比較して、 MSCの 発現強度の値と他の細胞の発現強度の値で、 MSCの発現強度の値を除したものを "Fold Change"とし、各細胞に対する Fold Changeの平均値を「Fold AverageJとした。 すなわち、例えば、 MSCにおける遺伝子の発現量の値が 4. 2、 OSの値が 0. 3、 C Hの値が 0. 4、 ADの値が 1. 5、FBの値が 1. 3である場合、 "Fold Change"の値は、 MSC/OS = 14. 0となる。同様に、各細胞に対する Fold Changeを求め、これらの 平均値を「Fold Average]とする。
[0140] 上記表 3a〜表 3eに示す 139個の遺伝子は、上述した選定基準を満たし、本発明 に係る分別マーカーとしての使用に堪えるものである。なお、これらの遺伝子の中で 、特に、上記 2つの選択基準を満たすものが好ましい。
[0141] したがって、これらの遺伝子は、 MSCと他の結合組織系の細胞(FB, OS, CH, A D)とにおいて、発現が異なる。具体的には、 MSCのみにおいて特異的に発現して おり、他の結合組織系の細胞においては、 MSCと識別できる程度に弱く発現してい る。このため、これらの遺伝子の発現を分別マーカーとして用いることにより、 MSCの みを特異的に識別することができる。
産業上の利用可能性
[0142] 以上のように、未分化の間葉系幹細胞は、骨、軟骨、脂肪、筋肉、腱、神経などに 分ィ匕することができる。このため、再生医療への利用の観点から、これらの組織の障 害を修復させるための移植用細胞として期待されている。再生医療の実用化に際し ては、その細胞が間葉系幹細胞であること、及び該間葉系幹細胞が多分ィ匕能を維持
していることを正確に、精度よぐかつ簡便に確認する必要がある力 本発明によれ ば、上記の技術的課題を解決することができる。このため、間葉系幹細胞を用いた再 生医療の実用化に非常に大きな役割を果たすことができる。このような本発明は、学 術的だけでなぐ医療業'製薬業等を含めた幅広い産業上の利用可能性がある。
Claims
請求の範囲
下記表 la〜表 ljに記載のァクセッション番号に示される塩基配列を有する遺伝子 から選択される、少なくとも 1つ以上の遺伝子を分別マーカーとして用い、
間葉系幹細胞と結合組織系細胞とにおける、上記分別マーカーの発現の差を検出 して、間葉系幹細胞と結合組織系細胞とを識別する工程を有することを特徴とする間 葉系幹細胞の識別方法。
[表 la]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding - 1 BRIP1 丽—032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK NM— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 丽— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KTF1 8A kinesin family member 18A 丽— 031217
NIMA (never in mitosis
ATP/GTP binding -5 NEK7 NM— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 雨— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 NM_014674 mannosidase alpha-like 1
calcium/calmodulin-
ATP/GTP binding -8 CAMK2D dependent protein kinase 雨— 172127
(CaM kinase) II delta
[表 lb]
Gene Genbank
Classification 3 Gene title
symbol number cell growth and/or cyclin Dl (PRADl :
CCND1 丽— 053056 maintenance -】 parathyroid adenomatosis 1)
cell growth and/or
CDC25A cell division cycle 25A NM— 001789 maintenance-2
cell growth and/or
IER3 immediate early response 3 丽— 052815 maintenance - 3
cell growth and/or
BCL2 B-cell CLL/lymphoma 2 丽 _000633 maintenance-4
cell growth and/or NACHT, leucine rich repeat
NALP1 雇— 033004 maintenance- 5 and PYD containing 1
cell growth and/or p21 (CDKNlA)-activated
PAK3 丽— 002578 maintenance-6 kinase 3
cell growth and/or NM— 001018
PODXL podocalyxin-like
maintenance-7 1 1 1 cell growth and/or chemokine (C-C motif)
CCL26 丽— 006072 maintenance- 8 ligand 26
cell growth and/or
FBLN1 fibulin 1 丽 006486 maintenance-9
cell growth and/or
LAMA1 laminin, alpha 1 丽— 005559 maintenance- 10
cell growth and/or
NTNG1 netrin Gl 丽— 014917 maintenance- 11
[表 lc]
Gene Genbank
Classification 5 Gene title
symbol number cytoskeleton- 1 KRT19 keratin 19 NM 002276 cytoskeleton-2 KRTAP1-5 keratin associated protein 1 - 丽 031957 cytoskeleton-3 KRTAP2-1 keratin associated protein 2- BC012486 cytoskeleton-4 K THA4 keratin, hair, acidic, 4 丽 021013 cytoskeleton associated
cytoskeleton- 5 CKAP2 雨— 01 8204 protein 2
cytoskeleton-6 KRTAPl-1 keratin associated protein 1- 丽 030967 cytoskeleton-7 KRT18 keratin 18 丽 000224 keratin associated protein
cytoskeleton- 8 KAP2.1B AJ406929
2.1B
slingshot homolog 1
cytoskeleton-9 SSH1 爾— 018984
(Drosophila)
Gene enbank
Classification 6 Gene title
symbol number enzyme- 1 LXN latexin 丽 020169 interferon, gamma-inducible
enzyme-2 IFI30 匪— 006332 protein 30
enzyme-3 CPA4 carboxvpeptidase A4 NM 016352
[表 Id]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雨— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽ー 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin-like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 丽— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 If]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 ; myeloid leukemia factor 1 匪 022443
CUB domain-containing
protein binding -3 丽— 022842 protein 1
protein binding - 4 K1AA0746 K1AA0746 protein NM 015187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, 丽— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI NM一 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 丽 031953 cadherin 6, type 2, K- protein binding -8 CDH6 丽— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG 丽— 0001 18
Weber syndrome 1 )
[表 lg]
[表 lh]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 i ets variant gene 1 丽 004956 ets variant gene 5 (ets- transcription-2 ETV5 丽—004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 022114 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 丽 001428 microphthalmia-associated
transcription- 10 MITF 固—198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer NM—003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 li]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit G isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 丽— 020768 containing 16
transport-3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 NM— 015865
(Kidd blood group)
solute carrier family 16
transport- 5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 丽— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽— 032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport-9 MCFD2 丽— 139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 丽— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 丽 018298 solute carrier family 25,
transport- 12 SLC25A37 NM_016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
[表 lj]
Gene Genbank
Classification 16 Gene title
symbol number
hypothetical protein
others - 1 FLJ38725 NM— 153218
FLJ38725
others -2 KIAA1913 KIAA1913 丽 052913 pleckstrin homology-like
others -3 PHLDB2 丽— 145753 domain, family B, member 2
phosphatidylinositol- others -4 PLCXD2 specific phospholipase C, X 丽— 153268 domain containing 2
sterile alpha motif domain NM— 001017 others -5 SAMD3
containing 3 373 others -6 Z F423 zinc finger protein 423 NM 015069 hypothetical protein 丽— 175894. others -7 FLJ33996
FLJ33996 2
pleckstrin homology domain
others -8 PLEKHK1 containing, family K 丽— 145307 member 1
prostate tumor
others -9 PTOV1 丽— 017432 overexpressed gene 1
family with sequence
others -10 FAM40B NM— 020704 similarity 40, member B
ABI gene family, member 3
others -1 1 ABI3BP 丽— 015429
(NESH) binding protein
Nance-Horan syndrome
others -12 NHS (congenital cataracts and 画— 198270 dental anomalies)
denticieless homolog
others -13 DTL NM— 016448
(Drosophila)
core 1 synthase,
others -14 C1GALT1 glycoprotein-N- 醒— 020156 acetylgalactosamine 3-beta- others -15 CP E8 copine VIII 匪 153634 others -16 TMEM49 transmembrane protein 49 NM 030938
上記分別マーカーとして、上記表 la〜表 ljに記載のクラス 6, 7, 8, 10,及び 13に 記載の遺伝子力 選択される、少なくとも 1つ以上の遺伝子を用いることを特徴とする 請求項 1に記載の間葉系幹細胞の識別方法。
上記分別マーカーとして、上記表 la〜表 ljに記載のクラス 6, 7, 8, 10,及び 13に 記載のクラスのそれぞれから、少なくとも 1つずつ選択された遺伝子を組み合わせて 用いることを特徴とする請求項 2に記載の間葉系幹細胞の識別方法。
上記分別マーカーとして、下記表 2に記載の遺伝子から選択される、少なくとも 1つ 以上の遺伝子を用いることを特徴とする請求項 1〜3のいずれか 1項に記載の間葉系 幹細胞の識別方法。
[表 2]
[5] 上記分別マーカーの発現の差の検出は、上記遺伝子の発現の検出、又は上記遺 伝子がコードするタンパク質の発現の検出によって行われるものであることを特徴と する請求項 1〜4のいずれ力 1項に記載の間葉系幹細胞の識別方法。
[6] 下記 (a)〜(d)のいずれかのうち、少なくとも 1つ以上を固定ィ匕させてなることを特徴 とする間葉系幹細胞の識別用マイクロアレイ:
(a)下記表 3a〜表 ¾に記載のァクセッション番号に示される塩基配列を有する遺伝 子のうち、少なくとも 1つ以上の遺伝子;
(b)下記表 3a〜表 ¾に記載のァクセッション番号に示される塩基配列を有する遺伝 子のうち、少なくとも 1つ以上の遺伝子のアンチセンス鎖;
(c)上記 (a)又は (b)の部分塩基配列;及び
(d)上記 (a)〜(c)のレ、ずれかに示される塩基配列を有するポリヌクレオチドとストリン ジェントな条件下でハイブリダィズするポリヌクレオチド。
[表 3a]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding - 1 BRIP1 雇— 032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK 丽— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 丽— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KIF18A kinesin family member 18A NM_031217
NIMA (never in mitosis
ATP/GTP binding -5 NEK7 丽— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 丽— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 NM 014674 mannosidase alpha-like 1
calcium/calmodulin-
ATP/GTP binding -8 CAMK2D dependent protein kinase NM— 172127
(CaM kinase) II delta
[表 3c]
[表 3d]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雇— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽一 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin - like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 3e]
[表 3f]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 myeloid leukemia factor 1 固 022443
CUB domain-containing
protein binding - 3 CDCP1 丽— 022842 protein 1
protein binding -4 KIAA0746 KIAA0746 protein NM 01 5187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, NM— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI 應— 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 固 031953 cadherin 6, type 2, - protein binding -8 CDH6 爾— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG NM— 0001 18
Weber syndrome 1)
[表 3g]
[表 3h]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 丽 004956 ets variant gene 5 (ets - transcription-2 ETV5 丽— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF 12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 0221 14 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia- associated
transcription- 10 MITF 丽— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 爾ー 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 3i]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 廻— 020768 containing 16
transport- 3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 丽— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 顺— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽—032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport - 9 MCFD2 NM_139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 NM— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 NM 018298 solute carrier family 25,
transport- 12 SLC25A37 丽一 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
下記 (e)又は (f)に記載のポリペプチドを用いて誘導され、当該ポリペプチドに特異 的に結合することを特徴とする抗体:
(e)下記表 4a〜表 4jに記載の!/、ずれかのァクセッション番号に示される塩基配列を 有する遺伝子によってコードされるポリペプチド;及び
(f)上記 (e)の部分ポリペプチド。
[表 4a]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding - 1 BRIP1 雇— 032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK 丽— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 丽— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KIF18A kinesin family member 18A NM_031217
NIMA (never in mitosis
ATP/GTP binding -5 NEK7 丽— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 丽— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 NM 014674 mannosidase alpha-like 1
calcium/calmodulin-
ATP/GTP binding -8 CAMK2D dependent protein kinase NM— 172127
(CaM kinase) II delta
[表 4c]
[表 4d]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雇— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽一 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin - like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 4e]
[表 4f]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 myeloid leukemia factor 1 固 022443
CUB domain-containing
protein binding - 3 CDCP1 丽— 022842 protein 1
protein binding -4 KIAA0746 KIAA0746 protein NM 01 5187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, NM— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI 應— 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 固 031953 cadherin 6, type 2, - protein binding -8 CDH6 爾— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG NM— 0001 18
Weber syndrome 1)
[表 4g]
[表 4h]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 丽 004956 ets variant gene 5 (ets - transcription-2 ETV5 丽— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF 12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 0221 14 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia- associated
transcription- 10 MITF 丽— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 爾ー 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 4i]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 廻— 020768 containing 16
transport- 3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 丽— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 顺— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽—032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport - 9 MCFD2 NM_139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 NM— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 NM 018298 solute carrier family 25,
transport- 12 SLC25A37 丽一 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
下記 (g)〜 (i)の 、ずれかに記載の物質を備えることを特徴とする間葉系幹細胞の 識別 ·分離キット:
(g)請求項 6に記載の間葉系幹細胞の識別用マイクロアレイ;
(h)請求項 7に記載の抗体;及び
(i)下記表 5a〜表 5jに記載の 、ずれかのァクセッション番号に示される塩基配列を 有する遺伝子又はその部分配列と、ストリンジェントな条件下でノ、イブリダィズするポ
リヌクレオチドからなる間葉系幹細胞の分別マーカー遺伝子の検出用プローブ。
[表 5a]
Gene Genbank
Classification 2 Gene title
symbol number phosphodiesterase 5 A,
binding -1 PDE5A NM— 001083 cGMP - specific
regulator of G-protein
binding - RGS4 丽— 005613 signalling 4
binding -3 EGFL3 EGF-like-domain, multiple 丽 001409 four and a half LIM domains
binding -4 FHL2 丽— 001450
2
binding -5 HRB2 HIV- 1 rev binding protein 2 画 007043 capping protein (actin
binding -6 CAPZA1 filament) muscle Z-line, 丽— 006135 alpha 1
binding -7 PAPPA2 pappalysin 2 画 020318 binding -8 LOXL2 lysyl oxidase-like 2 NM 002318 binding -9 LOX lysyl oxidase 固 002317
ADAM metal lopeptidase
binding -10 ADAMTS5 with thrombospondin type 1 NM— 007038 motif, 5 (aggrecanase-2)
[表 5b]
[表 5c]
[表 5d]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雇— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽一 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin - like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 5e]
[表 5f]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 myeloid leukemia factor 1 固 022443
CUB domain-containing
protein binding - 3 CDCP1 丽— 022842 protein 1
protein binding -4 KIAA0746 KIAA0746 protein NM 01 5187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, NM— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI 應— 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 固 031953 cadherin 6, type 2, - protein binding -8 CDH6 爾— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG NM— 0001 18
Weber syndrome 1)
[表 5g]
[表 5h]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 丽 004956 ets variant gene 5 (ets - transcription-2 ETV5 丽— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF 12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 0221 14 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia- associated
transcription- 10 MITF 丽— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 爾ー 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 5i]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 廻— 020768 containing 16
transport- 3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 丽— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 顺— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽—032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport - 9 MCFD2 NM_139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 NM— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 NM 018298 solute carrier family 25,
transport- 12 SLC25A37 丽一 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
[9] 請求項 1〜5のいずれ力 1項に記載の間葉系幹細胞の識別方法によって識別され た間葉系幹細胞を、分離する工程を有することを特徴とする間葉系幹細胞の識別分 離方法。
[10] 請求項 9に記載の間葉系幹細胞の識別分離方法によって分離された間葉系幹細 胞、又は当該間葉系幹細胞を増殖させたものを含むことを特徴とする細胞含有組成 物。
[11] 請求項 10に記載の細胞含有組成物を含むことを特徴とする再生医療用医薬。
[12] 下記表 6a〜表 6jに記載のァクセッション番号に示される塩基配列を有する遺伝子 のうち、いずれか 1つの遺伝子であることを特徴とする間葉系幹細胞の識別用分別マ 一力一。
[表 6a]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding - 1 BRIP1 雇— 032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK 丽— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 丽— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KIF18A kinesin family member 18A NM_031217
NIMA (never in mitosis
ATP/GTP binding -5 NEK7 丽— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 丽— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 NM 014674 mannosidase alpha-like 1
calcium/calmodulin-
ATP/GTP binding -8 CAMK2D dependent protein kinase NM— 172127
(CaM kinase) II delta
[表 6c]
[表 6d]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雇— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽一 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin - like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 6e]
[表 6f]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 myeloid leukemia factor 1 固 022443
CUB domain-containing
protein binding - 3 CDCP1 丽— 022842 protein 1
protein binding -4 KIAA0746 KIAA0746 protein NM 01 5187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, NM— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI 應— 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 固 031953 cadherin 6, type 2, - protein binding -8 CDH6 爾— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG NM— 0001 18
Weber syndrome 1)
[表 6g]
[表 6h]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 丽 004956 ets variant gene 5 (ets - transcription-2 ETV5 丽— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF 12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 0221 14 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia- associated
transcription- 10 MITF 丽— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 爾ー 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 6i]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 廻— 020768 containing 16
transport- 3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 丽— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 顺— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽—032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport - 9 MCFD2 NM_139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 NM— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 NM 018298 solute carrier family 25,
transport- 12 SLC25A37 丽一 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
下記表 7a〜表 7jに記載のァクセッション番号に示される塩基配列を有する遺伝子 にコードされるポリペプチドのうち、いずれか 1つのポリペプチドであることを特徴とす る間葉系幹細胞の識別用分別マーカー。
[表 7a]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding - 1 BRIP1 雇— 032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK 丽— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 丽— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KIF18A kinesin family member 18A NM_031217
NIMA (never in mitosis
ATP/GTP binding -5 NEK7 丽— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 丽— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 NM 014674 mannosidase alpha-like 1
calcium/calmodulin-
ATP/GTP binding -8 CAMK2D dependent protein kinase NM— 172127
(CaM kinase) II delta
[表 7c]
[表 7d]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雇— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽一 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin - like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 7e]
[表 7f]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 myeloid leukemia factor 1 固 022443
CUB domain-containing
protein binding - 3 CDCP1 丽— 022842 protein 1
protein binding -4 KIAA0746 KIAA0746 protein NM 01 5187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, NM— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI 應— 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 固 031953 cadherin 6, type 2, - protein binding -8 CDH6 爾— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG NM— 0001 18
Weber syndrome 1)
[表 7g]
[表 7h]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 丽 004956 ets variant gene 5 (ets - transcription-2 ETV5 丽— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF 12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 0221 14 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia- associated
transcription- 10 MITF 丽— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 爾ー 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 7i]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 廻— 020768 containing 16
transport- 3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 丽— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 顺— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽—032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport - 9 MCFD2 NM_139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 NM— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 NM 018298 solute carrier family 25,
transport- 12 SLC25A37 丽一 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
生体力 分離した試料に対して、請求項 1〜5のいずれか 1項に記載の間葉系幹細 胞の識別方法,請求項 6に記載の間葉系幹細胞の識別用マイクロアレイ,請求項 7 に記載の抗体,請求項 8に記載の間葉系幹細胞の識別'分離キット,及び請求項 12 または 13に記載の間葉系幹細胞の識別用分別マーカーから選択される手段を、い ずれか単独、または複数を組み合わせて用レ、ることにより、当該試料の提供者にお いて間葉系幹細胞が関連する疾患が発症しているか、または将来発症する可能性
があるかを判定する方法。
下記表 8a〜表 8jに記載の 、ずれかのァクセッション番号に示される塩基配列を有 する遺伝子又はその部分配列に対する siRNAを含む間葉系幹細胞の未分化性を 抑制する再生医療用医薬。
[表 8a]
Gene Genbank
Classification 1 Gene title
symbol number
BRCAl interacting protein
ATP/GTP binding - 1 BRIP1 雇— 032043
C -terminal helicase 1
PAS domain containing
ATP/GTP binding -2 PASK 丽— 015148 serine/threonine kinase
ras-related C3 botulinum
toxin substrate 2 (rho
ATP/GTP binding -3 RAC2 丽— 002872 family, small GTP binding
protein Rac2)
ATP/GTP binding -4 KIF18A kinesin family member 18A NM_031217
NIMA (never in mitosis
ATP/GTP binding -5 NEK7 丽— 133494 gene a)-related kinase 7
ADP-ribosylation factor-like
ATP/GTP binding -6 ARL4C 丽— 005737
4C
ER degradation enhancer,
ATP/GTP binding -7 EDEM1 NM 014674 mannosidase alpha-like 1
calcium/calmodulin-
ATP/GTP binding -8 CAMK2D dependent protein kinase NM— 172127
(CaM kinase) II delta
[表 8c]
[表 8d]
Gene Genbank
Classification 7 Gene title
symbol number chitinase 3 -like 1 (cartilage
extracellular matrix- 1 CHI3L1 雇— 001276 glycoprotein-39)
keratin 23 (hi stone
extracellular matrix-2 KRT23 丽一 015515 deacetylase inducible)
extracellular matrix-3 FLG filaggrin 丽— 002016 a disintegrin - like and
metalloprotease (reprolysin
extracellular matrix-4 ADAMTS1 NM— 006988 type) with thrombospondin
type 1 motif, 1
丽— 001031 extracellular matrix- 5 FRMD5 FERM domain containing 5
729
[表 8e]
[表 8f]
Gene Genbank
Classification 1 1 Gene title
symbol number protein binding -1 SYT1 synaptotagmin I 丽 005639 protein binding -2 MLF1 myeloid leukemia factor 1 固 022443
CUB domain-containing
protein binding - 3 CDCP1 丽— 022842 protein 1
protein binding -4 KIAA0746 KIAA0746 protein NM 01 5187 pleckstrin homology, Sec7
protein binding -5 PSCDBP and coiled-coil domains, NM— 004288 binding protein
v-ski sarcoma viral
protein binding -6 SKI 應— 003036 oncogene homolog (avian)
protein binding -7 SNX25 sorting nexin 25 固 031953 cadherin 6, type 2, - protein binding -8 CDH6 爾— 004932 cadherin (fetal kidney)
discoidin, CUB and LCCL
protein binding -9 DCBLD2 NM— 080927 domain containing 2
endoglin (Osler-Rendu- protein binding -10 ENG NM— 0001 18
Weber syndrome 1)
[表 8g]
[表 8h]
Gene Genbank
Classification 14 Gene title
symbol number transcription- 1 ETV1 ets variant gene 1 丽 004956 ets variant gene 5 (ets - transcription-2 ETV5 丽— 004454 related molecule)
transcription-3 FOXP1 forkhead box PI 丽 032682 high mobility group AT- transcription-4 HMGA2 丽— 003483 hook 2
transcription-5 KLF 12 Kruppel-like factor 12 丽 007249 transcription-6 PRDM16 PR domain containing 16 丽 0221 14 single-minded homolog 2
transcription-7 SIM2 丽— 009586
(Drosophila)
suppressor of hairy wing
transcription-8 SUHW2 NM— 080764 homolog 2 (Drosophila)
transcription-9 ENOl enolase 1 雇 001428 microphthalmia- associated
transcription- 10 MITF 丽— 198159 transcription factor
transcription factor 3 (E2A
transcription- 1 1 TCF3 immunoglobulin enhancer 爾ー 003200 binding factors E12/E47)
SET and MYND domain
transcription- 12 SMYD3 丽— 022743 containing 3
[表 8i]
Gene Genbank
Classification 15 Gene title
symbol number
ATPase, H+ transporting,
transport- 1 ATP6V1G3 lysosomal 13kDa, VI NM— 133262 subunit isoform 3
potassium channel
transport-2 KCTD16 tetramerisation domain 廻— 020768 containing 16
transport- 3 NUPL1 nucleoporin like 1 丽 014089 solute carrier family 14
transport-4 SLC14A1 (urea transporter), member 1 丽— 015865
(Kidd blood group)
solute carrier family 16
transport-5 SLC16A4 (monocarboxylic acid 丽— 004696 transporters), member 4
solute carrier family 4,
transport-6 SLC4A4 sodium bicarbonate 顺— 003759 cotransporter, member 4
solute carrier family 9
transport-7 SLC9A7 (sodium/hydrogen 丽—032591 exchanger), isoform 7
transient receptor potential
transport-8 TRPC4 cation channel, subfamily C, 丽— 016179 member 4
multiple coagulation factor
transport - 9 MCFD2 NM_139279 deficiency 2
solute carrier family 26,
transport- 10 SLC26A4 NM— 000441 member 4
transport- 1 1 MCOLN3 mucolipin 3 NM 018298 solute carrier family 25,
transport- 12 SLC25A37 丽一 016612 member 37
solute carrier family 30 (zinc
transport- 13 SLC30A7 丽— 133496 transporter), member 7
[表 8j]
Gene Genbank
Classification 16 Gene title
symbol number
hypothetical protein
others -1 FLJ38725 NM_153218
FLJ38725
others -2 KIAA1913 IAA1913 丽 052913 pleckstrin homology-like
others -3 PHLDB2 NM— 145753 domain, family B, member 2
phosphatidylinositol- others -4 PLCXD2 specilic phospholipase C, X NM— 153268 domain containing 2
sterile alpha motif domain NM— 001017 others -5 SAMD3
containing 3 373 others -6 ZNF423 zinc finger protein i^ NM 015069 hypothetical protein NM— 175894. others -7 FLJ33996
FLJ33996 2
pleckstrin homology domain
others -8 PLEKHK1 containing, family K NM— 145307 member 1
prostate tumor
others -9 PTOV1 丽— 017432 overexpressed gene 1
family with sequence
others -10 FAM40B 應— 020704 similarity 40, member B
ABI gene family, member 3
others -1 1 ABI3BP NM— 015429
(NESH) binding protein
Nance-Horan syndrome
others - 12 NHS (congenital cataracts and NM— 198270 dental anomalies)
denticleless homolog
others - 13 DTL NM— 016448
(Drosophila)
core 1 synthase,
others - 14 C1GALT1 glycoprotein-N- 應— 020156 acetylgalactosamine 3-beta- others - 15 CPNE8 copine VIII 醒 153634 others - 16 TMEM49 transmembrane protein 49 NM 030938
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/887,362 US9234897B2 (en) | 2005-03-31 | 2006-03-30 | Method for distinguishing mesenchymal stem cell using molecular marker and use thereof |
| JP2007512850A JP5190654B2 (ja) | 2005-03-31 | 2006-03-30 | 分子マーカーを用いた間葉系幹細胞の識別方法及びその利用 |
| EP06730606A EP1870455A4 (en) | 2005-03-31 | 2006-03-30 | METHOD FOR DISTINCTION OF MESENCHYMAL STEM CELL USING MOLECULAR MARKER AND USE THEREOF |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005-104563 | 2005-03-31 | ||
| JP2005104563 | 2005-03-31 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2006106823A1 true WO2006106823A1 (ja) | 2006-10-12 |
Family
ID=37073379
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2006/306658 WO2006106823A1 (ja) | 2005-03-31 | 2006-03-30 | 分子マーカーを用いた間葉系幹細胞の識別方法及びその利用 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US9234897B2 (ja) |
| EP (2) | EP2270226B1 (ja) |
| JP (1) | JP5190654B2 (ja) |
| TW (1) | TW200724677A (ja) |
| WO (1) | WO2006106823A1 (ja) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008092919A (ja) * | 2006-10-16 | 2008-04-24 | Hiroshima Univ | 病変間葉系幹細胞の検出マーカーの利用 |
| JP2010523124A (ja) * | 2007-04-06 | 2010-07-15 | ジェンザイム・コーポレーション | 細胞および細胞培養物を評価する方法 |
| JP2010189302A (ja) * | 2009-02-17 | 2010-09-02 | Hiroshima Univ | 病変間葉系幹細胞が関連する疾患の治療剤および間葉系幹細胞の検出マーカーの利用 |
| WO2010131315A1 (ja) * | 2009-05-12 | 2010-11-18 | 国立大学法人広島大学 | 誘導性間葉系幹細胞およびその作製方法 |
| WO2011105507A1 (ja) * | 2010-02-24 | 2011-09-01 | 財団法人神奈川科学技術アカデミー | 細胞分析装置 |
| WO2017022472A1 (ja) * | 2015-08-03 | 2017-02-09 | 国立大学法人名古屋大学 | 未分化間葉系幹細胞マーカー及びその用途 |
| US10973890B2 (en) | 2016-09-13 | 2021-04-13 | Allergan, Inc. | Non-protein clostridial toxin compositions |
| CN113302497A (zh) * | 2018-08-16 | 2021-08-24 | 豪夫迈·罗氏有限公司 | 循环tfpi-2(组织因子途径抑制剂2)在心房颤动和抗凝治疗评定中的应用 |
| CN114107191A (zh) * | 2021-12-09 | 2022-03-01 | 益诺思生物技术南通有限公司 | 一种89Zr标记人脐带间充质干细胞的方法 |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030114410A1 (en) * | 2000-08-08 | 2003-06-19 | Technion Research And Development Foundation Ltd. | Pharmaceutical compositions and methods useful for modulating angiogenesis and inhibiting metastasis and tumor fibrosis |
| SI2185198T1 (sl) | 2007-08-02 | 2015-04-30 | Gilead Biologics, Inc. | Inhibitorji LOX in LOXL2 ter njihova uporaba |
| WO2010080769A2 (en) | 2009-01-06 | 2010-07-15 | Arresto Biosciences, Inc. | Chemotherapeutic methods and compositions |
| AU2010284000A1 (en) * | 2009-08-21 | 2012-03-22 | Gilead Biologics, Inc. | In vitro screening assays |
| JP2013502437A (ja) * | 2009-08-21 | 2013-01-24 | ギリアド バイオロジクス,インク. | 治療方法及び組成物 |
| SG2014004816A (en) | 2009-08-21 | 2014-03-28 | Gilead Biologics Inc | Catalytic domains from lysyl oxidase and loxl2 |
| CA2789022A1 (en) | 2010-02-04 | 2011-08-11 | Gilead Biologics, Inc. | Antibodies that bind to lysyl oxidase-like 2 (loxl2) and methods of use therefor |
| KR101249041B1 (ko) * | 2010-04-28 | 2013-03-29 | 포항공과대학교 산학협력단 | 결합조직 성장인자를 이용한 약학적 조성물 |
| US9682105B2 (en) | 2010-07-14 | 2017-06-20 | University Of Southern California | Methods of promoting wound healing and attenuating contact hypersensitivity with gingiva-derived mesenchymal stem cells |
| EP2867375B1 (en) | 2012-06-27 | 2019-02-27 | Berg LLC | Use of markers in the diagnosis and treatment of prostate cancer |
| KR102657306B1 (ko) | 2014-12-08 | 2024-04-12 | 버그 엘엘씨 | 전립선암의 진단 및 치료에서 필라민을 포함하는 마커의 용도 |
| EP3429360A4 (en) * | 2016-03-16 | 2019-08-28 | Cell Medicine, Inc. | MESENCHYMAL STEM CELLS WITH IMPROVED EFFICACY |
| AU2018330458A1 (en) * | 2017-09-07 | 2020-03-19 | Regeneron Pharmaceuticals, Inc. | Solute Carrier Family 14 Member 1 (SLC14A1) variants and uses thereof |
| US20240018588A1 (en) * | 2020-12-07 | 2024-01-18 | Samsung Life Public Welfare Foundation | Method for selecting mesenchymal stem cells having improved self-maintenance ability, and mesenchymal stem cells selected thereby |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004290189A (ja) * | 2003-03-10 | 2004-10-21 | Japan Science & Technology Agency | 間葉系幹細胞検出用マーカー及び該マーカーを用いた間葉系幹細胞の識別方法 |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5147783A (en) * | 1988-05-27 | 1992-09-15 | Ube Industries, Ltd. | Methods to screen for ovarian cancer and myocardial infarction |
| US5338547A (en) * | 1990-09-06 | 1994-08-16 | Trustees Of The Univ. Of Pennsylvania | Bowman-Birk inhibitor product for use as an anticarcinogenesis agent |
| US5486359A (en) * | 1990-11-16 | 1996-01-23 | Osiris Therapeutics, Inc. | Human mesenchymal stem cells |
| FR2752842B1 (fr) * | 1996-08-30 | 1998-11-06 | Biomerieux Sa | Antigenes derives des filaggrines et leur utilisation pour le diagnostic de la polyarthrite rhumatoide |
| DE69907152D1 (de) * | 1998-02-18 | 2003-05-28 | Theryte Ltd | Krebsbehandlung |
| US20030161817A1 (en) * | 2001-03-28 | 2003-08-28 | Young Henry E. | Pluripotent embryonic-like stem cells, compositions, methods and uses thereof |
| US20020142457A1 (en) * | 1999-12-28 | 2002-10-03 | Akihiro Umezawa | Cell having the potentiality of differentiation into cardiomyocytes |
| US7309578B2 (en) * | 2000-02-29 | 2007-12-18 | The Trustees Of Columbia University In The City Of New York | Therapeutic treatment of chronic obstructive pulmonary disease |
| US20020068046A1 (en) * | 2000-12-04 | 2002-06-06 | Jianwu Dai | Use of stem cells derived from dermal skin |
| EP2322601A1 (en) * | 2000-12-06 | 2011-05-18 | Anthrogenesis Corporation | Method of collecting placental stem cells |
| AUPR703601A0 (en) * | 2001-08-15 | 2001-09-06 | Peter Maccallum Cancer Institute, The | Identification and isolation of somatic stem cells and uses thereof |
| JP2003052360A (ja) | 2001-08-20 | 2003-02-25 | Japan Science & Technology Corp | 基底膜細胞外基質を用いた間葉系幹細胞の培養方法 |
| JP2003052365A (ja) | 2001-08-20 | 2003-02-25 | Japan Science & Technology Corp | 哺乳動物からの間葉系幹細胞の分離及びその利用方法 |
| AU2003239016B2 (en) | 2002-06-14 | 2007-09-20 | Xintela Ab | Marker for stem cells and its use |
| DE10242338A1 (de) * | 2002-09-09 | 2004-03-18 | Eberhard-Karls-Universität Tübingen Universitätsklinikum | Antikörper zur Isolierung und/oder Identifizierung mesenchymaler Stammzellen und Verfahren zur Isolierung und/oder Identifizierung mesenchymaler Stammzellen |
| JP2006505380A (ja) * | 2002-11-05 | 2006-02-16 | ザ ブリガム アンド ウィメンズ ホスピタル インコーポレイテッド | 間葉幹細胞およびその使用方法 |
| US20060019256A1 (en) * | 2003-06-09 | 2006-01-26 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing cancer |
| JP4540948B2 (ja) * | 2003-07-07 | 2010-09-08 | 独立行政法人科学技術振興機構 | 分別マーカーを用いた間葉系幹細胞の識別・分離方法 |
| WO2006019357A1 (en) * | 2004-08-16 | 2006-02-23 | Cellresearch Corporation Pte Ltd | Isolation of stem/progenitor cells from amniotic membrane of umbilical cord. |
| WO2010045645A1 (en) * | 2008-10-17 | 2010-04-22 | Baxter International Inc. | Methods of obtaining cell populations from adipose tissue |
-
2006
- 2006-03-30 US US11/887,362 patent/US9234897B2/en active Active
- 2006-03-30 EP EP10013575.5A patent/EP2270226B1/en active Active
- 2006-03-30 JP JP2007512850A patent/JP5190654B2/ja active Active
- 2006-03-30 WO PCT/JP2006/306658 patent/WO2006106823A1/ja active Application Filing
- 2006-03-30 EP EP06730606A patent/EP1870455A4/en not_active Withdrawn
- 2006-03-31 TW TW095111518A patent/TW200724677A/zh unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004290189A (ja) * | 2003-03-10 | 2004-10-21 | Japan Science & Technology Agency | 間葉系幹細胞検出用マーカー及び該マーカーを用いた間葉系幹細胞の識別方法 |
Non-Patent Citations (3)
| Title |
|---|
| CONNOR J.R. ET AL.: "Human cartilage glycoprotein 39(HC gp-39) mRNA expression in adult and fetal, chondrocytes, osteoblasts and osteocytes by in-situ hybridization", OSTEOARTHRITIS AND CARTILAGE, vol. 8, 2000, pages 87 - 95, XP002965904 * |
| IGARASHI A. ET AL.: "Saisei Iryo ni Okeru Ishokuyo Kanyokei Kansaibo no Kentei no Juyosei to Kentei Hoho no Kento", SAISEI IRYO, vol. 4, no. SPECIAL EXTRA ISSUE, 10 February 2005 (2005-02-10), pages 115, PD-2-4, XP003004649 * |
| See also references of EP1870455A4 * |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008092919A (ja) * | 2006-10-16 | 2008-04-24 | Hiroshima Univ | 病変間葉系幹細胞の検出マーカーの利用 |
| JP2014036658A (ja) * | 2007-04-06 | 2014-02-27 | Genzyme Corp | 細胞および細胞培養物を評価する方法 |
| JP2010523124A (ja) * | 2007-04-06 | 2010-07-15 | ジェンザイム・コーポレーション | 細胞および細胞培養物を評価する方法 |
| JP2010189302A (ja) * | 2009-02-17 | 2010-09-02 | Hiroshima Univ | 病変間葉系幹細胞が関連する疾患の治療剤および間葉系幹細胞の検出マーカーの利用 |
| WO2010131315A1 (ja) * | 2009-05-12 | 2010-11-18 | 国立大学法人広島大学 | 誘導性間葉系幹細胞およびその作製方法 |
| US9023294B2 (en) | 2010-02-24 | 2015-05-05 | Kanagawa Academy Of Science And Technology | Cell analyzer |
| WO2011105507A1 (ja) * | 2010-02-24 | 2011-09-01 | 財団法人神奈川科学技術アカデミー | 細胞分析装置 |
| JP5807004B2 (ja) * | 2010-02-24 | 2015-11-10 | 公益財団法人神奈川科学技術アカデミー | 細胞分析装置 |
| WO2017022472A1 (ja) * | 2015-08-03 | 2017-02-09 | 国立大学法人名古屋大学 | 未分化間葉系幹細胞マーカー及びその用途 |
| US10973890B2 (en) | 2016-09-13 | 2021-04-13 | Allergan, Inc. | Non-protein clostridial toxin compositions |
| CN113302497A (zh) * | 2018-08-16 | 2021-08-24 | 豪夫迈·罗氏有限公司 | 循环tfpi-2(组织因子途径抑制剂2)在心房颤动和抗凝治疗评定中的应用 |
| CN113302497B (zh) * | 2018-08-16 | 2024-10-18 | 豪夫迈·罗氏有限公司 | 循环tfpi-2(组织因子途径抑制剂2)在心房颤动和抗凝治疗评定中的应用 |
| CN114107191A (zh) * | 2021-12-09 | 2022-03-01 | 益诺思生物技术南通有限公司 | 一种89Zr标记人脐带间充质干细胞的方法 |
| CN114107191B (zh) * | 2021-12-09 | 2024-03-12 | 益诺思生物技术南通有限公司 | 一种89Zr标记人脐带间充质干细胞的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2006106823A1 (ja) | 2008-09-11 |
| EP1870455A4 (en) | 2010-01-20 |
| EP1870455A1 (en) | 2007-12-26 |
| US20090232773A1 (en) | 2009-09-17 |
| EP2270226A3 (en) | 2011-06-29 |
| JP5190654B2 (ja) | 2013-04-24 |
| EP2270226B1 (en) | 2016-05-18 |
| US9234897B2 (en) | 2016-01-12 |
| EP2270226A2 (en) | 2011-01-05 |
| TW200724677A (en) | 2007-07-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2006106823A1 (ja) | 分子マーカーを用いた間葉系幹細胞の識別方法及びその利用 | |
| Contreras et al. | PDGF-PDGFR network differentially regulates the fate, migration, proliferation, and cell cycle progression of myogenic cells | |
| US20140235486A1 (en) | Methods and Compositions for the Treatment and Diagnosis of Breast Cancer | |
| WO2005075636A1 (en) | Molecular markers associated with metanephric development and renal progenitors | |
| JP5714327B2 (ja) | 心筋炎のトランスクリプトームのバイオマーカー | |
| Chen et al. | Periostin expression distinguishes between light and dark hypertrophic chondrocytes | |
| JP2013500474A (ja) | 発毛性真皮細胞を検出する/富化する方法、毛髪脱落を処置する方法における細胞およびその使用 | |
| EP4103045A1 (en) | Methods of therapeutic prognostication | |
| JP2006523444A (ja) | 骨芽細胞分化に関連する遺伝子発現 | |
| JP5243021B2 (ja) | 間葉系幹細胞などの細胞を検出するための遺伝子マーカー | |
| JP2008092919A (ja) | 病変間葉系幹細胞の検出マーカーの利用 | |
| Cong et al. | In vitro differentiation of bone marrow mesenchymal stem cells into endometrial epithelial cells in mouse: a proteomic analysis | |
| WO2010131315A1 (ja) | 誘導性間葉系幹細胞およびその作製方法 | |
| CN109182513B (zh) | 生物标志物scfd2在阿尔茨海默诊治中的应用 | |
| JP2010189302A (ja) | 病変間葉系幹細胞が関連する疾患の治療剤および間葉系幹細胞の検出マーカーの利用 | |
| JP2006349658A (ja) | 神経系癌幹細胞の検出試薬、神経系癌幹細胞を分離する方法、神経系癌幹細胞、及び神経芽腫の予後診断薬。 | |
| Nagata et al. | Altered levels of serotonin in lymphoblasts derived from migraine patients | |
| US20240191227A1 (en) | Use of CD56 to predict the differentiation potential of muscle stem cells | |
| KR102129380B1 (ko) | 단백질표지자 grp78을 이용한 고효율 줄기세포의 선별 방법 | |
| US20220057391A1 (en) | DIAGNOSTIC AND THERAPEUTIC FOR THE IDENTIFICATION AND TREATMENT OF SARS-CoV-2 | |
| Brugge et al. | Breast organoid suspension cultures maintain long-term estrogen receptor expression and responsiveness | |
| CN108179181B (zh) | Rdx基因在临床用药中的应用 | |
| EP2708605A1 (en) | ANKRD26 as a marker for diagnosis of thrombocytopenias | |
| Suárez-Calvet et al. | Decoding Duchenne muscular dystrophy transcriptome to single nuclei level reveals clinical-genetic correlations | |
| CN117327699A (zh) | 一种lncRNA及其抑制剂的应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2007512850 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 11887362 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2006730606 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: RU |
|
| WWP | Wipo information: published in national office |
Ref document number: 2006730606 Country of ref document: EP |