WO2002078659A1 - Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoïque cationique - Google Patents
Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoïque cationique Download PDFInfo
- Publication number
- WO2002078659A1 WO2002078659A1 PCT/FR2002/001138 FR0201138W WO02078659A1 WO 2002078659 A1 WO2002078659 A1 WO 2002078659A1 FR 0201138 W FR0201138 W FR 0201138W WO 02078659 A1 WO02078659 A1 WO 02078659A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- radical
- amino
- composition
- hydroxy
- composition according
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 102
- 238000004043 dyeing Methods 0.000 title claims abstract description 30
- 125000002091 cationic group Chemical group 0.000 title claims abstract description 13
- 239000000987 azo dye Substances 0.000 title claims abstract description 8
- 238000000034 method Methods 0.000 claims abstract description 16
- -1 alkyl radical Chemical class 0.000 claims description 79
- 239000000975 dye Substances 0.000 claims description 61
- 239000000835 fiber Substances 0.000 claims description 51
- 102000011782 Keratins Human genes 0.000 claims description 32
- 108010076876 Keratins Proteins 0.000 claims description 32
- 239000007800 oxidant agent Substances 0.000 claims description 26
- 150000003254 radicals Chemical class 0.000 claims description 22
- 230000003647 oxidation Effects 0.000 claims description 21
- 238000007254 oxidation reaction Methods 0.000 claims description 21
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 19
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 claims description 16
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 14
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 14
- BOKGTLAJQHTOKE-UHFFFAOYSA-N 1,5-dihydroxynaphthalene Chemical compound C1=CC=C2C(O)=CC=CC2=C1O BOKGTLAJQHTOKE-UHFFFAOYSA-N 0.000 claims description 13
- 229910052757 nitrogen Inorganic materials 0.000 claims description 13
- 230000001590 oxidative effect Effects 0.000 claims description 13
- 239000002253 acid Substances 0.000 claims description 12
- 125000003545 alkoxy group Chemical group 0.000 claims description 12
- 150000003839 salts Chemical class 0.000 claims description 12
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 claims description 9
- 125000003282 alkyl amino group Chemical group 0.000 claims description 9
- 230000008569 process Effects 0.000 claims description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 7
- 125000004432 carbon atom Chemical group C* 0.000 claims description 7
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 7
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 7
- 125000000623 heterocyclic group Chemical group 0.000 claims description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 6
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical class [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 claims description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 6
- 125000000143 2-carboxyethyl group Chemical group [H]OC(=O)C([H])([H])C([H])([H])* 0.000 claims description 5
- 150000002430 hydrocarbons Chemical group 0.000 claims description 5
- 229910052760 oxygen Inorganic materials 0.000 claims description 5
- 239000001301 oxygen Substances 0.000 claims description 5
- 229910052717 sulfur Inorganic materials 0.000 claims description 5
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 claims description 4
- 125000003118 aryl group Chemical group 0.000 claims description 4
- 125000005843 halogen group Chemical group 0.000 claims description 4
- ORTFAQDWJHRMNX-UHFFFAOYSA-N hydroxidooxidocarbon(.) Chemical compound O[C]=O ORTFAQDWJHRMNX-UHFFFAOYSA-N 0.000 claims description 4
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 claims description 4
- 229910052500 inorganic mineral Inorganic materials 0.000 claims description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 4
- 239000011707 mineral Substances 0.000 claims description 4
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 claims description 3
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims description 3
- WCYWZMWISLQXQU-UHFFFAOYSA-N methyl Chemical compound [CH3] WCYWZMWISLQXQU-UHFFFAOYSA-N 0.000 claims description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 3
- 125000004434 sulfur atom Chemical group 0.000 claims description 3
- LLAPDLPYIYKTGQ-UHFFFAOYSA-N 1-aminoethyl Chemical group C[CH]N LLAPDLPYIYKTGQ-UHFFFAOYSA-N 0.000 claims description 2
- QOXOZONBQWIKDA-UHFFFAOYSA-N 3-hydroxypropyl Chemical group [CH2]CCO QOXOZONBQWIKDA-UHFFFAOYSA-N 0.000 claims description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 2
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 claims description 2
- 125000003368 amide group Chemical group 0.000 claims description 2
- MDFFNEOEWAXZRQ-UHFFFAOYSA-N aminyl Chemical compound [NH2] MDFFNEOEWAXZRQ-UHFFFAOYSA-N 0.000 claims description 2
- 150000001450 anions Chemical class 0.000 claims description 2
- 125000004429 atom Chemical group 0.000 claims description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 2
- 229910052799 carbon Inorganic materials 0.000 claims description 2
- 125000005518 carboxamido group Chemical group 0.000 claims description 2
- 229910052801 chlorine Inorganic materials 0.000 claims description 2
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 2
- 125000000664 diazo group Chemical group [N-]=[N+]=[*] 0.000 claims description 2
- 229910052736 halogen Inorganic materials 0.000 claims description 2
- 150000002367 halogens Chemical class 0.000 claims description 2
- 239000001257 hydrogen Substances 0.000 claims description 2
- 229910052739 hydrogen Inorganic materials 0.000 claims description 2
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 claims description 2
- 229920006395 saturated elastomer Polymers 0.000 claims description 2
- 239000011593 sulfur Substances 0.000 claims description 2
- PQPYGYHIBMHXPC-UHFFFAOYSA-N 1,3-dichloro-1,3-bis(2,4,6-trichlorophenyl)urea Chemical compound ClC=1C=C(Cl)C=C(Cl)C=1N(Cl)C(=O)N(Cl)C1=C(Cl)C=C(Cl)C=C1Cl PQPYGYHIBMHXPC-UHFFFAOYSA-N 0.000 claims 3
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims 1
- 150000001875 compounds Chemical class 0.000 abstract description 14
- CBCKQZAAMUWICA-UHFFFAOYSA-N 1,4-phenylenediamine Chemical compound NC1=CC=C(N)C=C1 CBCKQZAAMUWICA-UHFFFAOYSA-N 0.000 description 15
- 239000000982 direct dye Substances 0.000 description 14
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 12
- 238000004040 coloring Methods 0.000 description 11
- 239000002585 base Substances 0.000 description 10
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 9
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 8
- 239000003795 chemical substances by application Substances 0.000 description 6
- VLTRZXGMWDSKGL-UHFFFAOYSA-M perchlorate Inorganic materials [O-]Cl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-M 0.000 description 5
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical compound N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N EtOH Substances CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 239000002535 acidifier Substances 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 125000000217 alkyl group Chemical group 0.000 description 3
- 239000002610 basifying agent Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000003086 colorant Substances 0.000 description 3
- 239000006071 cream Substances 0.000 description 3
- 238000009967 direct dyeing Methods 0.000 description 3
- 235000010755 mineral Nutrition 0.000 description 3
- 239000001044 red dye Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- CDAWCLOXVUBKRW-UHFFFAOYSA-N 2-aminophenol Chemical compound NC1=CC=CC=C1O CDAWCLOXVUBKRW-UHFFFAOYSA-N 0.000 description 2
- OBCSAIDCZQSFQH-UHFFFAOYSA-N 2-methyl-1,4-phenylenediamine Chemical compound CC1=CC(N)=CC=C1N OBCSAIDCZQSFQH-UHFFFAOYSA-N 0.000 description 2
- PLIKAWJENQZMHA-UHFFFAOYSA-N 4-aminophenol Chemical compound NC1=CC=C(O)C=C1 PLIKAWJENQZMHA-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- OKKJLVBELUTLKV-MZCSYVLQSA-N CD3OD Substances [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- SWXQKHHHCFXQJF-UHFFFAOYSA-N azane;hydrogen peroxide Chemical compound [NH4+].[O-]O SWXQKHHHCFXQJF-UHFFFAOYSA-N 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 150000002391 heterocyclic compounds Chemical class 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000001005 nitro dye Substances 0.000 description 2
- LQNUZADURLCDLV-UHFFFAOYSA-N nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1 LQNUZADURLCDLV-UHFFFAOYSA-N 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229920005862 polyol Polymers 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 150000003217 pyrazoles Chemical class 0.000 description 2
- 150000003222 pyridines Chemical class 0.000 description 2
- 229940083082 pyrimidine derivative acting on arteriolar smooth muscle Drugs 0.000 description 2
- 150000003230 pyrimidines Chemical class 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 2
- 239000002562 thickening agent Substances 0.000 description 2
- DBGXBYIIMVWCAT-UHFFFAOYSA-M (1,3-dimethylimidazol-1-ium-2-yl)-(4-methoxyphenyl)diazene;perchlorate Chemical compound [O-]Cl(=O)(=O)=O.C1=CC(OC)=CC=C1N=NC1=[N+](C)C=CN1C DBGXBYIIMVWCAT-UHFFFAOYSA-M 0.000 description 1
- GHGPIPTUDQZJJS-UHFFFAOYSA-N (2-chlorophenyl)hydrazine Chemical compound NNC1=CC=CC=C1Cl GHGPIPTUDQZJJS-UHFFFAOYSA-N 0.000 description 1
- SCZGZDLUGUYLRV-UHFFFAOYSA-N (2-methylphenyl)hydrazine Chemical compound CC1=CC=CC=C1NN SCZGZDLUGUYLRV-UHFFFAOYSA-N 0.000 description 1
- ZNXSFVXZQBETRJ-UHFFFAOYSA-N (3-aminophenyl)urea Chemical compound NC(=O)NC1=CC=CC(N)=C1 ZNXSFVXZQBETRJ-UHFFFAOYSA-N 0.000 description 1
- RQKQKYICHBSFNX-UHFFFAOYSA-N (4,5-diamino-1-ethylpyrazol-3-yl)methanol Chemical compound CCN1N=C(CO)C(N)=C1N RQKQKYICHBSFNX-UHFFFAOYSA-N 0.000 description 1
- LHGUPKWTLOUVPW-UHFFFAOYSA-N (4,5-diamino-1-methylpyrazol-3-yl)methanol Chemical compound CN1N=C(CO)C(N)=C1N LHGUPKWTLOUVPW-UHFFFAOYSA-N 0.000 description 1
- DPTWQNJCRFZYPL-UHFFFAOYSA-N (4,5-diamino-1-propan-2-ylpyrazol-3-yl)methanol Chemical compound CC(C)N1N=C(CO)C(N)=C1N DPTWQNJCRFZYPL-UHFFFAOYSA-N 0.000 description 1
- CBWPAXKVACVBLU-UHFFFAOYSA-N 1,3-bis[4-amino-n-(2-hydroxyethyl)anilino]propan-1-ol Chemical compound C1=CC(N)=CC=C1N(CCO)CCC(O)N(CCO)C1=CC=C(N)C=C1 CBWPAXKVACVBLU-UHFFFAOYSA-N 0.000 description 1
- WZCQRUWWHSTZEM-UHFFFAOYSA-N 1,3-phenylenediamine Chemical compound NC1=CC=CC(N)=C1 WZCQRUWWHSTZEM-UHFFFAOYSA-N 0.000 description 1
- ARXJGSRGQADJSQ-UHFFFAOYSA-N 1-methoxypropan-2-ol Chemical compound COCC(C)O ARXJGSRGQADJSQ-UHFFFAOYSA-N 0.000 description 1
- WSMJTXVQAZYLAV-UHFFFAOYSA-N 1-methylindol-4-ol Chemical compound C1=CC=C2N(C)C=CC2=C1O WSMJTXVQAZYLAV-UHFFFAOYSA-N 0.000 description 1
- YMRBWWVXSSYSGH-UHFFFAOYSA-N 1-methylpyrazole-3,4,5-triamine Chemical compound CN1N=C(N)C(N)=C1N YMRBWWVXSSYSGH-UHFFFAOYSA-N 0.000 description 1
- QXAUAKSIUQHEPR-UHFFFAOYSA-N 1-n-[4-(2-amino-4-methylanilino)butyl]-4-methylbenzene-1,2-diamine Chemical compound NC1=CC(C)=CC=C1NCCCCNC1=CC=C(C)C=C1N QXAUAKSIUQHEPR-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- XAWPKHNOFIWWNZ-UHFFFAOYSA-N 1h-indol-6-ol Chemical compound OC1=CC=C2C=CNC2=C1 XAWPKHNOFIWWNZ-UHFFFAOYSA-N 0.000 description 1
- WXFKWEVAPSWLOI-UHFFFAOYSA-N 1h-pyrazole-3,4,5-triamine Chemical compound NC1=NNC(N)=C1N WXFKWEVAPSWLOI-UHFFFAOYSA-N 0.000 description 1
- LHGQFZQWSOXLEW-UHFFFAOYSA-N 1h-pyrazole-4,5-diamine Chemical compound NC=1C=NNC=1N LHGQFZQWSOXLEW-UHFFFAOYSA-N 0.000 description 1
- SYEYEGBZVSWYPK-UHFFFAOYSA-N 2,5,6-triamino-4-hydroxypyrimidine Chemical compound NC1=NC(N)=C(N)C(O)=N1 SYEYEGBZVSWYPK-UHFFFAOYSA-N 0.000 description 1
- BWAPJIHJXDYDPW-UHFFFAOYSA-N 2,5-dimethyl-p-phenylenediamine Chemical compound CC1=CC(N)=C(C)C=C1N BWAPJIHJXDYDPW-UHFFFAOYSA-N 0.000 description 1
- BRMHZFZMBVIHMO-UHFFFAOYSA-N 2,5-dimethylpyrazole-3,4-diamine Chemical compound CC1=NN(C)C(N)=C1N BRMHZFZMBVIHMO-UHFFFAOYSA-N 0.000 description 1
- KEEQZNSCYCPKOJ-UHFFFAOYSA-N 2,6-diethylbenzene-1,4-diamine Chemical compound CCC1=CC(N)=CC(CC)=C1N KEEQZNSCYCPKOJ-UHFFFAOYSA-N 0.000 description 1
- LGZOJZFHAJJLCF-UHFFFAOYSA-N 2,7-dimethylpyrazolo[1,5-a]pyrimidine-3,5-diamine Chemical compound CC1=CC(N)=NC2=C(N)C(C)=NN21 LGZOJZFHAJJLCF-UHFFFAOYSA-N 0.000 description 1
- BQHMISUMCDYQTR-UHFFFAOYSA-N 2-(1,3-benzodioxol-5-ylamino)ethanol Chemical compound OCCNC1=CC=C2OCOC2=C1 BQHMISUMCDYQTR-UHFFFAOYSA-N 0.000 description 1
- SBASXUCJHJRPEV-UHFFFAOYSA-N 2-(2-methoxyethoxy)ethanol Chemical compound COCCOCCO SBASXUCJHJRPEV-UHFFFAOYSA-N 0.000 description 1
- SBUMIGFDXJIPLE-UHFFFAOYSA-N 2-(3-amino-4-methoxyanilino)ethanol Chemical compound COC1=CC=C(NCCO)C=C1N SBUMIGFDXJIPLE-UHFFFAOYSA-N 0.000 description 1
- JLEBZTSKNDQWIO-UHFFFAOYSA-N 2-(4-amino-2-methylanilino)ethanol Chemical compound CC1=CC(N)=CC=C1NCCO JLEBZTSKNDQWIO-UHFFFAOYSA-N 0.000 description 1
- GEDBTTQRNHWAQC-UHFFFAOYSA-N 2-(4-methoxyphenyl)pyridine-3,4-diamine Chemical compound C1=CC(OC)=CC=C1C1=NC=CC(N)=C1N GEDBTTQRNHWAQC-UHFFFAOYSA-N 0.000 description 1
- RHIPXPBQVGXJNL-UHFFFAOYSA-N 2-[(3-aminopyrazolo[1,5-a]pyrimidin-7-yl)amino]ethanol Chemical compound OCCNC1=CC=NC2=C(N)C=NN21 RHIPXPBQVGXJNL-UHFFFAOYSA-N 0.000 description 1
- DEZOGYCXWGTILF-UHFFFAOYSA-N 2-[(4-chlorophenyl)methyl]pyrazole-3,4-diamine Chemical compound NC1=C(N)C=NN1CC1=CC=C(Cl)C=C1 DEZOGYCXWGTILF-UHFFFAOYSA-N 0.000 description 1
- ZQLZWNDBBQUIEY-UHFFFAOYSA-N 2-[(7-aminopyrazolo[1,5-a]pyrimidin-3-yl)-(2-hydroxyethyl)amino]ethanol Chemical compound NC1=CC=NC2=C(N(CCO)CCO)C=NN12 ZQLZWNDBBQUIEY-UHFFFAOYSA-N 0.000 description 1
- HARBPHQCTIDSBX-UHFFFAOYSA-N 2-[(7-aminopyrazolo[1,5-a]pyrimidin-3-yl)amino]ethanol Chemical compound NC1=CC=NC2=C(NCCO)C=NN12 HARBPHQCTIDSBX-UHFFFAOYSA-N 0.000 description 1
- DMUXRIHPNREBPF-UHFFFAOYSA-N 2-[2-[2-[2-(2,5-diaminophenoxy)ethoxy]ethoxy]ethoxy]benzene-1,4-diamine Chemical compound NC1=CC=C(N)C(OCCOCCOCCOC=2C(=CC=C(N)C=2)N)=C1 DMUXRIHPNREBPF-UHFFFAOYSA-N 0.000 description 1
- FGYCMSFOZIRDLN-UHFFFAOYSA-N 2-[3-(2-hydroxyethylamino)-2-methylanilino]ethanol Chemical compound CC1=C(NCCO)C=CC=C1NCCO FGYCMSFOZIRDLN-UHFFFAOYSA-N 0.000 description 1
- BCQDCROHHKDXAT-UHFFFAOYSA-N 2-[4-amino-n-[4-[4-amino-n-(2-hydroxyethyl)anilino]butyl]anilino]ethanol Chemical compound C1=CC(N)=CC=C1N(CCO)CCCCN(CCO)C1=CC=C(N)C=C1 BCQDCROHHKDXAT-UHFFFAOYSA-N 0.000 description 1
- HCPJEHJGFKWRFM-UHFFFAOYSA-N 2-amino-5-methylphenol Chemical compound CC1=CC=C(N)C(O)=C1 HCPJEHJGFKWRFM-UHFFFAOYSA-N 0.000 description 1
- ALQKEYVDQYGZDN-UHFFFAOYSA-N 2-amino-6-methylphenol Chemical compound CC1=CC=CC(N)=C1O ALQKEYVDQYGZDN-UHFFFAOYSA-N 0.000 description 1
- BMTSZVZQNMNPCT-UHFFFAOYSA-N 2-aminopyridin-3-ol Chemical compound NC1=NC=CC=C1O BMTSZVZQNMNPCT-UHFFFAOYSA-N 0.000 description 1
- AJZRIOLJTXDFDY-UHFFFAOYSA-N 2-benzyl-5-methylpyrazole-3,4-diamine Chemical compound NC1=C(N)C(C)=NN1CC1=CC=CC=C1 AJZRIOLJTXDFDY-UHFFFAOYSA-N 0.000 description 1
- POAOYUHQDCAZBD-UHFFFAOYSA-N 2-butoxyethanol Chemical compound CCCCOCCO POAOYUHQDCAZBD-UHFFFAOYSA-N 0.000 description 1
- LRFYRWUMJLXTJH-UHFFFAOYSA-N 2-ethyl-5-(4-methoxyphenyl)pyrazole-3,4-diamine Chemical compound NC1=C(N)N(CC)N=C1C1=CC=C(OC)C=C1 LRFYRWUMJLXTJH-UHFFFAOYSA-N 0.000 description 1
- MEKRUGGNBTYVRV-UHFFFAOYSA-N 2-ethyl-5-methylpyrazole-3,4-diamine Chemical compound CCN1N=C(C)C(N)=C1N MEKRUGGNBTYVRV-UHFFFAOYSA-N 0.000 description 1
- LYEBIHUMFJCIMG-UHFFFAOYSA-N 2-methyl-5-phenylpyrazole-3,4-diamine Chemical compound NC1=C(N)N(C)N=C1C1=CC=CC=C1 LYEBIHUMFJCIMG-UHFFFAOYSA-N 0.000 description 1
- ZTMADXFOCUXMJE-UHFFFAOYSA-N 2-methylbenzene-1,3-diol Chemical compound CC1=C(O)C=CC=C1O ZTMADXFOCUXMJE-UHFFFAOYSA-N 0.000 description 1
- SRJCJJKWVSSELL-UHFFFAOYSA-N 2-methylnaphthalen-1-ol Chemical compound C1=CC=CC2=C(O)C(C)=CC=C21 SRJCJJKWVSSELL-UHFFFAOYSA-N 0.000 description 1
- XOAXOKSJNVLLHZ-UHFFFAOYSA-N 2-methylpyrazole-3,4-diamine Chemical compound CN1N=CC(N)=C1N XOAXOKSJNVLLHZ-UHFFFAOYSA-N 0.000 description 1
- HLTDBMHJSBSAOM-UHFFFAOYSA-N 2-nitropyridine Chemical compound [O-][N+](=O)C1=CC=CC=N1 HLTDBMHJSBSAOM-UHFFFAOYSA-N 0.000 description 1
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 description 1
- CTGVWWNOCSCKKI-UHFFFAOYSA-N 2-tert-butyl-5-methylpyrazole-3,4-diamine Chemical compound CC1=NN(C(C)(C)C)C(N)=C1N CTGVWWNOCSCKKI-UHFFFAOYSA-N 0.000 description 1
- YFIFCWQWZWDTQV-UHFFFAOYSA-N 3,4-dihydro-2h-1,4-benzoxazin-6-ol;2,6-dimethoxypyridine-3,5-diamine Chemical compound O1CCNC2=CC(O)=CC=C21.COC1=NC(OC)=C(N)C=C1N YFIFCWQWZWDTQV-UHFFFAOYSA-N 0.000 description 1
- XYRDGCCCBJITBH-UHFFFAOYSA-N 3-amino-2-chloro-6-methylphenol Chemical compound CC1=CC=C(N)C(Cl)=C1O XYRDGCCCBJITBH-UHFFFAOYSA-N 0.000 description 1
- FLROJJGKUKLCAE-UHFFFAOYSA-N 3-amino-2-methylphenol Chemical compound CC1=C(N)C=CC=C1O FLROJJGKUKLCAE-UHFFFAOYSA-N 0.000 description 1
- BGMAIXRJQFTHIH-UHFFFAOYSA-N 3-amino-4H-pyrazolo[1,5-a]pyrimidin-5-one Chemical compound C1=CC(O)=NC2=C(N)C=NN21 BGMAIXRJQFTHIH-UHFFFAOYSA-N 0.000 description 1
- CWLKGDAVCFYWJK-UHFFFAOYSA-N 3-aminophenol Chemical compound NC1=CC=CC(O)=C1 CWLKGDAVCFYWJK-UHFFFAOYSA-N 0.000 description 1
- 229940018563 3-aminophenol Drugs 0.000 description 1
- ZQBHGSSAKLGUBH-UHFFFAOYSA-N 4,5,6-triamino-1h-pyrimidin-2-one Chemical compound NC1=NC(=O)NC(N)=C1N ZQBHGSSAKLGUBH-UHFFFAOYSA-N 0.000 description 1
- MWKPYVXITDAZLL-UHFFFAOYSA-N 4-[3-(2,4-diaminophenoxy)propoxy]benzene-1,3-diamine Chemical compound NC1=CC(N)=CC=C1OCCCOC1=CC=C(N)C=C1N MWKPYVXITDAZLL-UHFFFAOYSA-N 0.000 description 1
- PZKNKZNLQYKXFV-UHFFFAOYSA-N 4-amino-2-(aminomethyl)phenol Chemical compound NCC1=CC(N)=CC=C1O PZKNKZNLQYKXFV-UHFFFAOYSA-N 0.000 description 1
- WSEFOZIMAJPJHW-UHFFFAOYSA-N 4-amino-2-(hydroxymethyl)phenol Chemical compound NC1=CC=C(O)C(CO)=C1 WSEFOZIMAJPJHW-UHFFFAOYSA-N 0.000 description 1
- RGKJLNMYCNSVKZ-UHFFFAOYSA-N 4-amino-2-(methoxymethyl)phenol Chemical compound COCC1=CC(N)=CC=C1O RGKJLNMYCNSVKZ-UHFFFAOYSA-N 0.000 description 1
- UPHYVIFVOBTQNW-UHFFFAOYSA-N 4-amino-2-[(2-hydroxyethylamino)methyl]phenol Chemical compound NC1=CC=C(O)C(CNCCO)=C1 UPHYVIFVOBTQNW-UHFFFAOYSA-N 0.000 description 1
- MXJQJURZHQZLNN-UHFFFAOYSA-N 4-amino-2-fluorophenol Chemical compound NC1=CC=C(O)C(F)=C1 MXJQJURZHQZLNN-UHFFFAOYSA-N 0.000 description 1
- HDGMAACKJSBLMW-UHFFFAOYSA-N 4-amino-2-methylphenol Chemical compound CC1=CC(N)=CC=C1O HDGMAACKJSBLMW-UHFFFAOYSA-N 0.000 description 1
- DHKIYDNMIXSKQP-UHFFFAOYSA-N 4-amino-3-(hydroxymethyl)phenol Chemical compound NC1=CC=C(O)C=C1CO DHKIYDNMIXSKQP-UHFFFAOYSA-N 0.000 description 1
- MNPLTKHJEAFOCA-UHFFFAOYSA-N 4-amino-3-fluorophenol Chemical compound NC1=CC=C(O)C=C1F MNPLTKHJEAFOCA-UHFFFAOYSA-N 0.000 description 1
- JQVAPEJNIZULEK-UHFFFAOYSA-N 4-chlorobenzene-1,3-diol Chemical compound OC1=CC=C(Cl)C(O)=C1 JQVAPEJNIZULEK-UHFFFAOYSA-N 0.000 description 1
- QGNGOGOOPUYKMC-UHFFFAOYSA-N 4-hydroxy-6-methylaniline Chemical compound CC1=CC(O)=CC=C1N QGNGOGOOPUYKMC-UHFFFAOYSA-N 0.000 description 1
- NLMQHXUGJIAKTH-UHFFFAOYSA-N 4-hydroxyindole Chemical compound OC1=CC=CC2=C1C=CN2 NLMQHXUGJIAKTH-UHFFFAOYSA-N 0.000 description 1
- VGNTUDBFWCGMGV-UHFFFAOYSA-N 4-n,1-dimethylpyrazole-3,4,5-triamine Chemical compound CNC=1C(N)=NN(C)C=1N VGNTUDBFWCGMGV-UHFFFAOYSA-N 0.000 description 1
- XBTWVJKPQPQTDW-UHFFFAOYSA-N 4-n,4-n-diethyl-2-methylbenzene-1,4-diamine Chemical compound CCN(CC)C1=CC=C(N)C(C)=C1 XBTWVJKPQPQTDW-UHFFFAOYSA-N 0.000 description 1
- QNGVNLMMEQUVQK-UHFFFAOYSA-N 4-n,4-n-diethylbenzene-1,4-diamine Chemical compound CCN(CC)C1=CC=C(N)C=C1 QNGVNLMMEQUVQK-UHFFFAOYSA-N 0.000 description 1
- TVARKMCEMIFLIP-UHFFFAOYSA-N 4-n-(2-aminoethyl)benzene-1,4-diamine Chemical compound NCCNC1=CC=C(N)C=C1 TVARKMCEMIFLIP-UHFFFAOYSA-N 0.000 description 1
- OAQDBKQAJRFJIY-UHFFFAOYSA-N 4-n-[2-(4-amino-n-ethyl-3-methylanilino)ethyl]-4-n-ethyl-2-methylbenzene-1,4-diamine Chemical compound C=1C=C(N)C(C)=CC=1N(CC)CCN(CC)C1=CC=C(N)C(C)=C1 OAQDBKQAJRFJIY-UHFFFAOYSA-N 0.000 description 1
- OOPWJBCZQDTTNE-UHFFFAOYSA-N 4-n-[4-(4-aminoanilino)butyl]benzene-1,4-diamine Chemical compound C1=CC(N)=CC=C1NCCCCNC1=CC=C(N)C=C1 OOPWJBCZQDTTNE-UHFFFAOYSA-N 0.000 description 1
- BBTNLADSUVOPPN-UHFFFAOYSA-N 5,6-diaminouracil Chemical compound NC=1NC(=O)NC(=O)C=1N BBTNLADSUVOPPN-UHFFFAOYSA-N 0.000 description 1
- RGJZYQQJISIEFA-UHFFFAOYSA-N 5-(2-aminoethyl)-1,3-dimethyl-3h-pyrazole-2,4-diamine Chemical compound CC1N(N)N(C)C(CCN)=C1N RGJZYQQJISIEFA-UHFFFAOYSA-N 0.000 description 1
- DBFYESDCPWWCHN-UHFFFAOYSA-N 5-amino-2-methylphenol Chemical compound CC1=CC=C(N)C=C1O DBFYESDCPWWCHN-UHFFFAOYSA-N 0.000 description 1
- CMYXTZPTHYRATM-UHFFFAOYSA-N 5-hydrazinyl-1,3-dimethylpyrazol-4-amine Chemical compound CC1=NN(C)C(NN)=C1N CMYXTZPTHYRATM-UHFFFAOYSA-N 0.000 description 1
- XKVUYEYANWFIJX-UHFFFAOYSA-N 5-methyl-1h-pyrazole Chemical compound CC1=CC=NN1 XKVUYEYANWFIJX-UHFFFAOYSA-N 0.000 description 1
- JSVCLRZBHIRDNZ-UHFFFAOYSA-N 5-methyl-2-phenylpyrazole-3,4-diamine Chemical compound NC1=C(N)C(C)=NN1C1=CC=CC=C1 JSVCLRZBHIRDNZ-UHFFFAOYSA-N 0.000 description 1
- CGTQMHXEGLHVFE-UHFFFAOYSA-N 5-methyl-2-propan-2-ylpyrazole-3,4-diamine Chemical compound CC(C)N1N=C(C)C(N)=C1N CGTQMHXEGLHVFE-UHFFFAOYSA-N 0.000 description 1
- NYEINRQDXMWWDE-UHFFFAOYSA-N 5-tert-butyl-2-methylpyrazole-3,4-diamine Chemical compound CN1N=C(C(C)(C)C)C(N)=C1N NYEINRQDXMWWDE-UHFFFAOYSA-N 0.000 description 1
- ATNZJTUJPNJYQS-UHFFFAOYSA-N 6-methoxy-2-(2-methoxyethyl)pyridine-3,4-diamine Chemical compound COCCC1=NC(OC)=CC(N)=C1N ATNZJTUJPNJYQS-UHFFFAOYSA-N 0.000 description 1
- WEPOCTWSRWLQLL-UHFFFAOYSA-N 6-methoxypyridine-2,3-diamine Chemical compound COC1=CC=C(N)C(N)=N1 WEPOCTWSRWLQLL-UHFFFAOYSA-N 0.000 description 1
- XGRCGWLFRPCJOC-UHFFFAOYSA-N 7-n,7-n,2,5-tetramethylpyrazolo[1,5-a]pyrimidine-3,7-diamine Chemical compound CN(C)C1=CC(C)=NC2=C(N)C(C)=NN12 XGRCGWLFRPCJOC-UHFFFAOYSA-N 0.000 description 1
- HJRJSALOMUZJBM-UHFFFAOYSA-N 7-n-[3-(1h-imidazol-2-yl)propyl]-5-methylpyrazolo[1,5-a]pyrimidine-3,7-diamine Chemical compound N12N=CC(N)=C2N=C(C)C=C1NCCCC1=NC=CN1 HJRJSALOMUZJBM-UHFFFAOYSA-N 0.000 description 1
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N DMSO Substances CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 1
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- UIOFUWFRIANQPC-JKIFEVAISA-N Floxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=C(F)C=CC=C1Cl UIOFUWFRIANQPC-JKIFEVAISA-N 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical class Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 108010029541 Laccase Proteins 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M Methanesulfonate Chemical compound CS([O-])(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- BZORFPDSXLZWJF-UHFFFAOYSA-N N,N-dimethyl-1,4-phenylenediamine Chemical compound CN(C)C1=CC=C(N)C=C1 BZORFPDSXLZWJF-UHFFFAOYSA-N 0.000 description 1
- SFEJLGXFERZHIP-UHFFFAOYSA-N NC1N(N(C(=C1CCO)N)C)N Chemical compound NC1N(N(C(=C1CCO)N)C)N SFEJLGXFERZHIP-UHFFFAOYSA-N 0.000 description 1
- PKACFTKQQUDJDA-UHFFFAOYSA-N OC1=CC=NC2=C(N)C=NN21 Chemical compound OC1=CC=NC2=C(N)C=NN21 PKACFTKQQUDJDA-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 108090000854 Oxidoreductases Proteins 0.000 description 1
- 102000004316 Oxidoreductases Human genes 0.000 description 1
- 108090000417 Oxygenases Proteins 0.000 description 1
- 102000004020 Oxygenases Human genes 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 108700020962 Peroxidase Proteins 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical class [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- LUSZGTFNYDARNI-UHFFFAOYSA-N Sesamol Natural products OC1=CC=C2OCOC2=C1 LUSZGTFNYDARNI-UHFFFAOYSA-N 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical class OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 108010092464 Urate Oxidase Proteins 0.000 description 1
- OYDQPYUVQAHEJH-UHFFFAOYSA-N [3-(dimethylamino)phenyl]urea Chemical compound CN(C)C1=CC=CC(NC(N)=O)=C1 OYDQPYUVQAHEJH-UHFFFAOYSA-N 0.000 description 1
- 235000011054 acetic acid Nutrition 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 230000003113 alkalizing effect Effects 0.000 description 1
- 150000008052 alkyl sulfonates Chemical class 0.000 description 1
- OYTKINVCDFNREN-UHFFFAOYSA-N amifampridine Chemical compound NC1=CC=NC=C1N OYTKINVCDFNREN-UHFFFAOYSA-N 0.000 description 1
- 229960004012 amifampridine Drugs 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 229920006318 anionic polymer Polymers 0.000 description 1
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Natural products CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 125000005228 aryl sulfonate group Chemical group 0.000 description 1
- 125000000751 azo group Chemical group [*]N=N[*] 0.000 description 1
- 150000001555 benzenes Chemical class 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical class OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000004061 bleaching Methods 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 229940106189 ceramide Drugs 0.000 description 1
- 150000001783 ceramides Chemical class 0.000 description 1
- OGEBRHQLRGFBNV-RZDIXWSQSA-N chembl2036808 Chemical class C12=NC(NCCCC)=NC=C2C(C=2C=CC(F)=CC=2)=NN1C[C@H]1CC[C@H](N)CC1 OGEBRHQLRGFBNV-RZDIXWSQSA-N 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- 238000002845 discoloration Methods 0.000 description 1
- 239000000986 disperse dye Substances 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- KIWBPDUYBMNFTB-UHFFFAOYSA-M ethyl sulfate Chemical compound CCOS([O-])(=O)=O KIWBPDUYBMNFTB-UHFFFAOYSA-M 0.000 description 1
- 238000005562 fading Methods 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 150000002475 indoles Chemical class 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 150000003893 lactate salts Chemical class 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- QDLAGTHXVHQKRE-UHFFFAOYSA-N lichenxanthone Natural products COC1=CC(O)=C2C(=O)C3=C(C)C=C(OC)C=C3OC2=C1 QDLAGTHXVHQKRE-UHFFFAOYSA-N 0.000 description 1
- 125000001434 methanylylidene group Chemical group [H]C#[*] 0.000 description 1
- JZMJDSHXVKJFKW-UHFFFAOYSA-M methyl sulfate(1-) Chemical compound COS([O-])(=O)=O JZMJDSHXVKJFKW-UHFFFAOYSA-M 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- BKEFUBHXUTWQED-UHFFFAOYSA-N n-(4-amino-3-hydroxyphenyl)acetamide Chemical compound CC(=O)NC1=CC=C(N)C(O)=C1 BKEFUBHXUTWQED-UHFFFAOYSA-N 0.000 description 1
- XSFMNFYLWHPZIQ-UHFFFAOYSA-N n-pyrrolidin-1-ylacetamide Chemical compound CC(=O)NN1CCCC1 XSFMNFYLWHPZIQ-UHFFFAOYSA-N 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000002891 organic anions Chemical class 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- JRKICGRDRMAZLK-UHFFFAOYSA-L persulfate group Chemical group S(=O)(=O)([O-])OOS(=O)(=O)[O-] JRKICGRDRMAZLK-UHFFFAOYSA-L 0.000 description 1
- 229960005323 phenoxyethanol Drugs 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 235000011118 potassium hydroxide Nutrition 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- FFNJDUZBKSGSIV-UHFFFAOYSA-N pyrazolo[1,5-a]pyrimidine-3,5-diamine Chemical compound C1=CC(N)=NC2=C(N)C=NN21 FFNJDUZBKSGSIV-UHFFFAOYSA-N 0.000 description 1
- PNFZIEOWPDFJBH-UHFFFAOYSA-N pyrazolo[1,5-a]pyrimidine-3,7-diamine Chemical compound NC1=CC=NC2=C(N)C=NN21 PNFZIEOWPDFJBH-UHFFFAOYSA-N 0.000 description 1
- MIROPXUFDXCYLG-UHFFFAOYSA-N pyridine-2,5-diamine Chemical compound NC1=CC=C(N)N=C1 MIROPXUFDXCYLG-UHFFFAOYSA-N 0.000 description 1
- PZRKPUQWIFJRKZ-UHFFFAOYSA-N pyrimidine-2,4,5,6-tetramine Chemical compound NC1=NC(N)=C(N)C(N)=N1 PZRKPUQWIFJRKZ-UHFFFAOYSA-N 0.000 description 1
- CSNFMBGHUOSBFU-UHFFFAOYSA-N pyrimidine-2,4,5-triamine Chemical compound NC1=NC=C(N)C(N)=N1 CSNFMBGHUOSBFU-UHFFFAOYSA-N 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000003352 sequestering agent Substances 0.000 description 1
- 239000002453 shampoo Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- JAOZKJMVYIWLKU-UHFFFAOYSA-N sodium 7-hydroxy-8-[(4-sulfonaphthalen-1-yl)diazenyl]naphthalene-1,3-disulfonic acid Chemical compound C1=CC=C2C(=C1)C(=CC=C2S(=O)(=O)O)N=NC3=C(C=CC4=CC(=CC(=C43)S(=O)(=O)O)S(=O)(=O)O)O.[Na+] JAOZKJMVYIWLKU-UHFFFAOYSA-N 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 235000011121 sodium hydroxide Nutrition 0.000 description 1
- 150000003890 succinate salts Chemical class 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 229910021653 sulphate ion Inorganic materials 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 150000003892 tartrate salts Chemical class 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 125000005490 tosylate group Chemical group 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 239000001003 triarylmethane dye Substances 0.000 description 1
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 1
- AQLJVWUFPCUVLO-UHFFFAOYSA-N urea hydrogen peroxide Chemical compound OO.NC(N)=O AQLJVWUFPCUVLO-UHFFFAOYSA-N 0.000 description 1
- 239000002888 zwitterionic surfactant Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q5/00—Preparations for care of the hair
- A61Q5/06—Preparations for styling the hair, e.g. by temporary shaping or colouring
- A61Q5/065—Preparations for temporary colouring the hair, e.g. direct dyes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/49—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds
- A61K8/494—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds with more than one nitrogen as the only hetero atom
- A61K8/4946—Imidazoles or their condensed derivatives, e.g. benzimidazoles
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B44/00—Azo dyes containing onium groups
- C09B44/10—Azo dyes containing onium groups containing cyclammonium groups attached to an azo group by a carbon atom of the ring system
- C09B44/101—Azo dyes containing onium groups containing cyclammonium groups attached to an azo group by a carbon atom of the ring system characterised by the coupling component having an amino directing group
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B44/00—Azo dyes containing onium groups
- C09B44/10—Azo dyes containing onium groups containing cyclammonium groups attached to an azo group by a carbon atom of the ring system
- C09B44/16—1,3-Diazoles or hydrogenated 1,3-diazoles ; (Benz)imidazolium
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/42—Colour properties
- A61K2800/43—Pigments; Dyes
- A61K2800/432—Direct dyes
- A61K2800/4322—Direct dyes in preparations for temporarily coloring the hair further containing an oxidizing agent
Definitions
- the subject of the invention is a new dye composition for dyeing keratin fibers, in particular human hair, containing a particular cationic azo dye, as well as the process for dyeing keratin fibers using such a composition.
- the subject of the invention is also new azo cationic dyes. It is known to dye keratin fibers and in particular human hair with dye compositions containing oxidation dye precursors, generally called oxidation bases, such as ortho or paraphenylenediamines, ortho or paraaminophenols and heterocyclic compounds. These oxidation bases are colorless or weakly colored compounds which, associated with oxidizing products, give rise, through an oxidative condensation process, to colored compounds.
- couplers or color modifiers the latter being chosen in particular from aromatic metadiamines, metaaminophenols, metadiphenols and certain heterocyclic compounds such as as indole compounds.
- the lightening of the fiber has the advantageous effect of generating a solid color in the case of gray hair, and in the case of naturally pigmented hair, of bringing out the color, that is to say making it more visible.
- dye keratin fibers by direct coloring.
- the method conventionally used in direct dyeing consists in applying to the keratin fibers direct dyes which are colored and coloring molecules having an affinity for the fibers, to allow to pause, then to rinse the fibers. It is known, for example, to use direct dyes of the nitro benzene, anthraquinone, nitropyridine type, dyes of the azo, xanthene, acridine azine type or triarylmethane dyes.
- the resulting colorings are particularly chromatic colors which are however temporary or semi-permanent because the nature of the interactions which bind the direct dyes to the keratin fiber, and their desorption from the surface and / or from the core of the fiber are responsible for their low dye power and their poor resistance to washing or perspiration.
- These direct dyes are also generally sensitive to light due to the low resistance of the chromophore vis-à-vis photochemical attacks and lead over time to a fading of the coloring of the hair. In addition, their sensitivity to light is dependent on their uniform or aggregate distribution in the keratin fiber.
- direct dyes are generally sensitive to the action of oxidizing agents such as hydrogen peroxide, and reducing agents such as sodium bisulfite, which generally make them difficult to use in lightening direct dye compositions based on hydrogen peroxide and based on an alkalizing agent or in oxidation dye compositions in combination with precursors of the oxidation base or coupler type.
- oxidizing agents such as hydrogen peroxide
- reducing agents such as sodium bisulfite
- patent application FR 2 741 798 has described dye compositions containing direct dyes comprising at least one quaternized nitrogen atom of the azo or azomethine type, said compositions being to be mixed extemporaneously at basic pH with an oxidizing composition.
- These compositions make it possible to obtain colorings with homogeneous, tenacious and brilliant reflections. However, they do not make it possible to dye the keratin fibers with as much power as with oxidation coloring compositions.
- - W 2 represents a divalent aromatic carbon or pyridine group of formulas (III) or (IV) below
- W 3 represents a 5 or 6-membered heterocycle of formula (V) below
- - Z 2 represents a nitrogen atom or a radical CR ⁇
- R 9 and R 12 represent, independently of each other, a CC 8 alkyl radical, optionally substituted by one or more radicals chosen from hydroxy, C
- R 10 and Ru represent, independently of one another, a hydrogen atom; a C 1 -C 4 alkyl radical, optionally substituted by one or more radicals chosen from a hydroxy, a C r C 2 alkoxy, a (poly) hydroxy C 2 -C 4 alkoxy radical, an amino, a (di ) C * -C 2 alkylamino, carboxy, sulfonic; an optionally substituted phenyl radical; a carboxy radical; a sulfonylamino radical;
- R 5 , R 6 , R 7 and R 8 represent, independently of one another, a hydrogen atom; a chlorine atom; a bromine atom; a linear or branched C r C 6 hydrocarbon chain, which can form one or more carbon rings having 3 to 6 members, and which can be saturated or unsaturated, of which one or more carbon atoms of the carbon chain can be replaced by an atom oxygen, nitrogen or sulfur or with an SO 2 group, and the carbon atoms of which may be, independently of one another, substituted by one or more halogen atoms; R 5 , R 6 , R 7 and R 8 having no peroxide bond, nor diazo or nitroso radicals,
- - n is an integer equal to 0 or 1
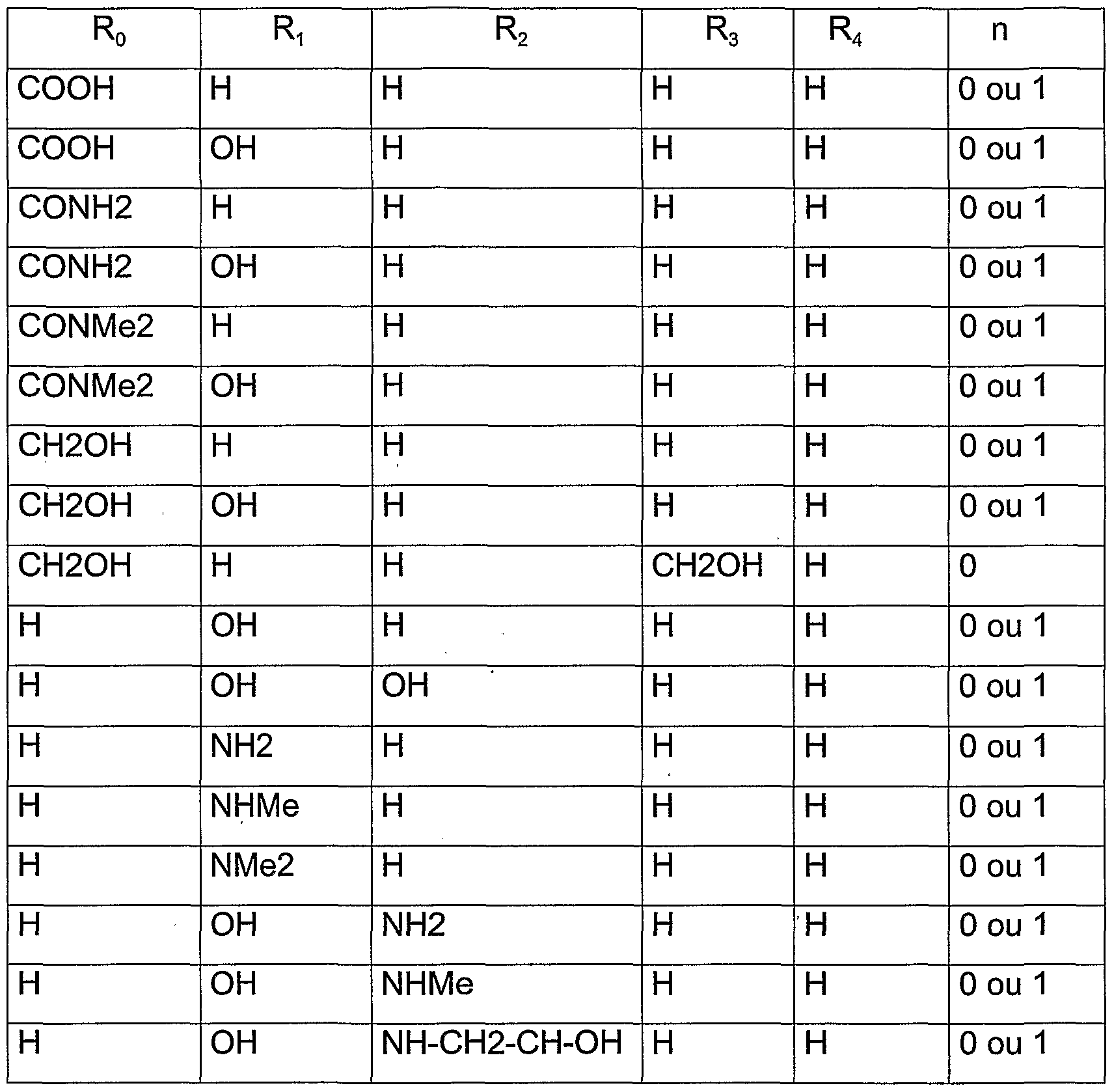
- Ri, R 2 , R 3 and R 4 represent, independently of one another, a hydrogen atom, a hydroxy radical; amino; acetoxy; a group -NR 13 R 14 , R 13 and R 14 independently of one another representing a hydrogen atom, a CC 4 alkyl radical substituted by one or more radicals chosen from a halogen atom, a radical hydroxy, C 1 -C 2 alkoxy, amino or amino (di) C r C 2 alkyl; a sulfonylamino radical; a carboxy radical; a carboxamido radical; an amido radical; a mono or di alkylamido radical; halogen; a CC 6 alkyl radical substituted by one or more radicals chosen from a hydroxy radical, C ⁇ Cs alkoxy, (poly) - C 2 -C 4 alkoxy, amino, (di) C 1 -C 2 alkylamino, being understood that at least one of the
- alkyl means, unless otherwise indicated, an alkyl radical comprising from 1 to 10 carbon atoms, preferably from 1 to 6 carbon atoms, which may be linear or branched.
- alkoxy means alkyl-O-, the term alkyl having the preceding meaning.
- branched hydrocarbon chain means a chain which can form one or more carbon rings comprising from 3 to 6 members.
- unsaturated hydrocarbon chain is understood to mean a chain which can comprise one or more double bonds and / or one or more triple bonds, this hydrocarbon chain being able to lead to aromatic groups.
- R 0 , Ri, R 2 , R 3 , R 4 can be of configuration (R) and / or (S).
- R 0, R,, R 2, R 3, R 4 preferably represent a hydroxyl group, acetoxy, amino, methylamino, dimethylamino, 2-hydroxyethylamino, carboxy, carboxamido, amido, mono or di alkylamido.
- R 0 , R * ,, R 2 , R 3 , R 4 and n are chosen from the following combinations:
- R 0 , R., R 2 , R 3 , R 4 are chosen from the following combinations:
- the radicals R 5 , R 6 , R 7 and R 8 are preferably chosen from a hydrogen atom, a methyl, ethyl, isopropyl, methoxymethyl, hydroxymethyl, 1-carboxymethyl, 1-aminomethyl, 1-aminoethyl, 2- radical. carboxyethyl, 2-hydroxyethyl, 3-hydroxypropyl, 1, 2-dihydroxyethyl, 1-hydroxy-2-aminoethyl, 2-hydroxy-1-aminoethyl, methoxy, ethoxy, 3-hydroxyethyloxy, 3-aminoethyloxy, amino, methylamino, dimethylamino , 2-hydroxyethylamino ,.
- R 5 , R 6 , R 7 and R 8 are chosen from a hydrogen atom, a methyl, hydroxymethyl, 2-hydroxyethyl, 1,2-dihydroxyethyl, methoxy, 2-hydroxyethoxy, amino radical. , 2-hydroxyethylamino, more preferably a hydrogen atom, a methyl radical, a methoxy, amino radical.
- R 9 and R 12 preferably represent a C 1 -C 4 alkyl radical, optionally substituted by one or more radicals chosen from hydroxy, C * -C 2 alkoxy, amino, (di ) C 1 -C 2 alkylamino, a carboxyl, a sulfonic, a phenyl, more preferably a methyl, ethyl, 2-hydroxyethyl, 1-carboxymethyl, 2-carboxyethyl, 2-sulfonylethyl radical.
- R 10 and R- I - I preferably represent a hydrogen atom, a C r C 4 alkyl radical optionally substituted by one or more radicals chosen from hydroxy, amino, (di) alkylamino in C 1 -C 2 , carboxy, phenyl, more preferably, R 10 and R *, ** represent a hydrogen atom, a methyl, ethyl, 2-hydroxyethyl, carboxy, 1-carboxymethyl, 2 - carboxyethyl, 2-sulfonylethyl.
- the composition comprises an azo dye of formula (I) as defined above in which Z1 is -NR 12 and W2 is a divalent group of formula (III).
- the composition of the present invention comprises an azo dye of formula (I) as defined above in which Z1 is -NR 12 , W2 is a divalent group of formula (III), Z 2 is CR ⁇ .
- the mineral or organic anion X can be chosen from a halide such as chloride, bromide, fluoride, iodide; a hydroxide; a sulfate; a hydrogen sulfate; a (C 1 -C 6 ) alkyl sulphate such as for example a methyl sulphate or an ethyl sulphate; an acetate; a tartrate; an oxalate; a (C * -C 6 ) alkyl sulfonate such as methylsulfonate; an arylsulfonate substituted or unsubstituted by a C r C 4 alkyl radical such as for example a 4-toluylsulfonate.
- the concentration of azo cationic dye of formula (I) can vary between 0.001 and 5% by weight approximately relative to the total weight of the dye composition, and preferably between approximately 0.05 and 2%.
- the composition of the invention may also comprise an oxidizing agent.
- This oxidizing agent can be any oxidizing agent conventionally used for bleaching keratin fibers.
- the oxidizing agent is preferably chosen from hydrogen peroxide, urea peroxide, alkali metal bromates, persalts such as perborates and persulfates. The use of hydrogen peroxide is particularly preferred.
- composition according to the invention can also comprise an oxidation base.
- This oxidation base can be chosen from the oxidation bases conventionally used in oxidation dyeing, for example paraphenylenediamines, bis-phenylalkylenediamines, para-aminophenols, ortho-aminophenols and heterocyclic bases.
- paraphenylenediamines there may be more particularly mentioned by way of example, paraphenylenediamine, paratoluylenediamine, 2-chloro paraphenylenediamine, 2,3-dimethyl paraphenylenediamine, 2,6-dimethyl paraphenylenediamine, 2,6-diethyl paraphenylenediamine , 2,5-dimethyl paraphenylenediamine, N, N-dimethyl paraphenylenediamine, N, N-diethyl paraphenylenediamine, N, N-dipropyl paraphenylenediamine, 4-amino N, N-diethyl 3-methyl aniline, NN- bis- ( ⁇ -hydroxyethyl) paraphenylenediamine, 4-N, N-bis- ( ⁇ - hydroxyethyl) amino 2-methyl aniline, 4-N, N-bis- ( ⁇ -hydroxyethyl) amino 2-chloro aniline, 2- ⁇ -hydroxyethyl paraphen
- paraphenylenediamine paratoluylenediamine, 2-isopropyl paraphenylenediamine, 2- ⁇ -hydroxyethyl paraphenylenediamine, 2- ⁇ -hydroxyethyloxy paraphenylenediamine, 2,6-dimethyl paraphenylenediamine para-phenylenediamine, 2,3-dimethyl para-phenylenediamine, N, N-bis- ( ⁇ -hydroxyethyl) para-phenylenediamine, 2-chloro para-phenylenediamine, 2- ⁇ -acetylaminoethyloxy para-phenylenediamine, and their addition salts with an acid are particularly preferred .
- bis-phenylalkylenediamines that may be mentioned by way of example,
- para-aminophenol there may be mentioned by way of example, para-aminophenol, 4-amino 3-methyl phenol, 4-amino 3-fluoro phenol, 4-amino 3-hydroxymethyl phenol, 4- amino 2-methyl phenol, 4-amino 2-hydroxymethyl phenol, 4-amino 2-methoxymethyl phenol, 4-amino 2-aminomethyl phenol, 4- amino 2- ( ⁇ -hydroxyethyl aminomethyl) phenol, 4- amino 2-fluoro phenol, and their addition salts with an acid.
- para-aminophenol 4-amino 3-methyl phenol, 4-amino 3-fluoro phenol, 4-amino 3-hydroxymethyl phenol, 4- amino 2-methyl phenol, 4-amino 2-hydroxymethyl phenol, 4-amino 2-methoxymethyl phenol, 4-amino 2-aminomethyl phenol, 4- amino 2- ( ⁇ -hydroxyethyl aminomethyl) phenol, 4- amino 2-fluoro phenol, and their addition salts with an acid.
- ortho-aminophenols there may be mentioned by way of example, 2-amino phenol, 2-amino 5-methyl phenol, 2-amino 6-methyl phenol, 5-acetamido 2-amino phenol, and their addition salts with an acid.
- heterocyclic bases for example, pyridine derivatives, pyrimidine derivatives and pyrazole derivatives.
- pyridine derivatives mention may be made of the compounds described for example in patents GB 1,026,978 and GB 1,153,196, such as 2,5-diamino pyridine, 2- (4-methoxyphenyl) amino 3-amino pyridine, 2,3-diamino 6-methoxy pyridine, 2- ( ⁇ -methoxyethyl) amino 3-amino 6-methoxy pyridine, 3,4-diamino pyridine, and their addition salts with an acid.
- pyrimidine derivatives mention may be made of the compounds described for example in patents DE 2,359,399; JP 88-169,571; JP 05 163 124; EP 0 770 375 or patent application WO 96/15765 such as 2,4,5,6-tetra-aminopyrimidine, 4-hydroxy 2,5,6-triaminopyrimidine, 2-hydroxy 4,5,6-triaminopyrimidine, 2,4-dihydroxy 5,6-diaminopyrimidine, 2,5,6-triaminopyrimidine, and pyrazolo-pyrimidine derivatives such as those mentioned in patent application FR-A-2 750 048 and among which may be mentioned pyrazolo - [1,5-a] -pyrimidine-3,7-diamine; 2,5-dimethyl pyrazolo- [1,5-a] -pyrimidine-3J-diamine; pyrazolo- [1,5-a] -pyrimidine-3,5-
- composition according to the invention may also contain one or more couplers conventionally used for dyeing keratin fibers.
- couplers conventionally used for dyeing keratin fibers.
- couplers mention may in particular be made of metaphenylenediamines, metaaminophenols, metadiphenols, naphthalene couplers and heterocyclic couplers.
- the coupler (s) are generally present in an amount between 0.001 and 10% by weight approximately of the total weight of the dye composition and more preferably from 0.005 to 6%.
- the oxidation base (s) are present in an amount preferably between 0.001 to 10% by weight approximately of the total weight of the dye composition, and more preferably from 0.005 to 6%.
- the addition salts with an acid which can be used in the context of the dye compositions of the invention for the oxidation bases and the couplers are in particular chosen from hydrochlorides, hydrobromides, sulfates, citrates, succinates, tartrates, lactates, tosylates, benzenesulfonates, phosphates and acetates.
- the dye composition in accordance with the invention may also contain direct dyes different from those of formula (I), these dyes being able in particular to be chosen from nitro dyes of the benzene series, cationic direct dyes, azo direct dyes, methine direct dyes.
- the medium suitable for dyeing also called dye support, generally consists of water or of a mixture of water and at least one organic solvent to dissolve the compounds which are not sufficiently soluble in water.
- organic solvent mention may, for example, be made of lower C 1 -C 4 alkanols, such as ethanol and isopropanol; polyols and polyol ethers such as 2-butoxyethanol, propylene glycol, propylene glycol monomethyl ether, monoethyl ether and diethylene glycol monomethyl ether, as well as aromatic alcohols such as benzyl alcohol or phenoxyethanol, and mixtures thereof.
- lower C 1 -C 4 alkanols such as ethanol and isopropanol
- polyols and polyol ethers such as 2-butoxyethanol, propylene glycol, propylene glycol monomethyl ether, monoethyl ether and diethylene glycol monomethyl ether, as well as aromatic alcohols such as benzyl alcohol or phenoxyethanol, and mixtures thereof.
- the solvents may be present in proportions preferably of between 1 and 40% by weight approximately relative to the total weight of the dye composition, and even more preferably between 5 and 30% by weight approximately.
- the pH of the dye composition according to the invention is generally between 3 and 12 approximately, and preferably between 5 and 11 approximately. It can be adjusted to the desired value by means of acidifying or basifying agents usually used in dyeing keratin fibers or even using conventional buffer systems.
- acidifying agents there may be mentioned, by way of example, mineral or organic acids such as hydrochloric acid, orthophosphoric acid, sulfuric acid, carboxylic acids such as acetic acid, tartaric acid, citric acid, lactic acid, sulfonic acids.
- mineral or organic acids such as hydrochloric acid, orthophosphoric acid, sulfuric acid, carboxylic acids such as acetic acid, tartaric acid, citric acid, lactic acid, sulfonic acids.
- basifying agents there may be mentioned, by way of example, ammonia, alkali carbonates, alkanolamines such as mono-, di- and triethanolamines as well as their derivatives, sodium or potassium hydroxides and compounds of formula (III) below:
- W is a propylene residue optionally substituted by a hydroxyl group or a C * -C 4 alkyl radical
- R 6 , R 7 , R 8 and R 9 identical or different, represent a hydrogen atom, a C 1 -C 4 alkyl or CC 4 hydroxyalkyl radical.
- the dye composition according to the invention can be in various forms, such as in the form of liquids, creams, gels, or in any other form suitable for dyeing keratin fibers, and in particular human hair.
- the invention also relates to a direct dyeing process which comprises the application of a dye composition containing a dye of formula (I) as defined above on keratin fibers. After a pause, the keratin fibers are rinsed leaving colored fibers to appear.
- the application to the fibers of the dye composition containing the azo cationic dye of formula (I) can be implemented in the presence of an oxidizing agent which causes discoloration of the fiber.
- This oxidizing agent can be added to the composition containing the cationic azo dye at the time of use or directly on the keratin fiber.
- the composition containing the azo cationic dye of formula (I) is free from oxidation base and from coupler.
- the invention also relates to a process for permanent oxidation dyeing which comprises applying to the fibers a dye composition which comprises a dye of formula (I), at least one oxidation base and optionally at least one coupler, in the presence of an oxidizing agent.
- the oxidation base, the coupler and the oxidizing agent are as defined above.
- oxidizing agent enzymes among which there may be mentioned peroxidases, 2-electron oxidoreductases such as uricases and 4-electron oxygenases such as laccases.
- the color can be revealed at acidic, neutral or alkaline pH and the oxidizing agent can be added to the composition of the invention just at the time of use or it can be used from an oxidizing composition containing it , applied to the fibers simultaneously or sequentially to the dye composition.
- the dye composition is mixed, preferably at the time of use, with a composition containing, in a medium suitable for dyeing, at least one oxidizing agent, this oxidizing agent being present in an amount sufficient to develop a coloration.
- the mixture obtained is then applied to the keratin fibers. After a pause time of approximately 3 to 50 minutes, preferably 5 to 30 minutes approximately, the keratin fibers are rinsed, washed with shampoo, rinsed again and then dried.
- the oxidizing composition may also contain various adjuvants conventionally used in compositions for dyeing the hair and as defined above.
- the pH of the oxidizing composition containing the oxidizing agent is such that after mixing with the dye composition, the pH of the resulting composition applied to the keratin fibers preferably varies between 3 and 12 approximately, and even more preferably between 5 and 11 It can be adjusted to the desired value by means of acidifying or basifying agents usually used in dyeing keratin fibers and as defined above.
- composition which is finally applied to the keratin fibers can be in various forms, such as in the form of liquids, creams, gels or in any other form suitable for dyeing keratin fibers, and in particular human hair.
- Another object of the invention is a device with several compartments or "kit” for dyeing in which a first compartment contains the dye composition of the invention and a second compartment contains the oxidizing composition.
- This device can be equipped with a means enabling the desired mixture to be delivered to the hair, such as the devices described in patent FR-2,586,913 in the name of the applicant.
- the subject of the invention is also the cationic azo dyes of formula (I) as defined above.
- These compounds can be obtained from the preparation methods described for example in documents EP 810824, GB 9619573, RO 106572, J. Chem. Res .., Synop. (1998), (10), 648-649, DE 19721619, US 5852179, Synth. Common 1999, 29 (13), 2271-2276.
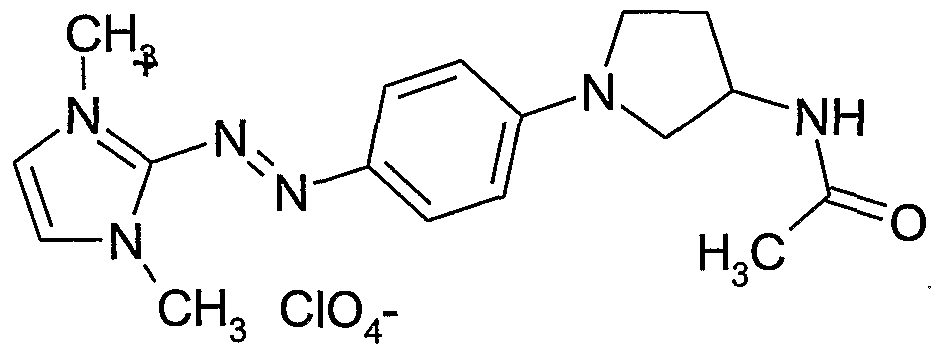
- a dye is thus obtained giving a purple red dye.
- composition is mixed with 20 volumes cream oxidant (1/1, 5 m / m) so that the final concentration of dye is 0.5%.
- the mixture is applied to locks of natural and permanent hair 90% white. 10 g of composition are applied to 1 g of wick. After 35 minutes of laying at room temperature, the locks are rinsed, shampooed, rinsed again and dried.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Birds (AREA)
- Epidemiology (AREA)
- Cosmetics (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
Claims
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP02724400A EP1377264A1 (fr) | 2001-04-02 | 2002-04-02 | Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoique cationique |
| JP2002576926A JP3748856B2 (ja) | 2001-04-02 | 2002-04-02 | カチオン性アゾ染料を含む、ケラチン繊維の染色のための染色性組成物 |
| US10/473,625 US7022143B2 (en) | 2001-04-02 | 2002-04-02 | Dyeing composition for dyeing keratinous fibers comprising a cationic azo-dye |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR01/04466 | 2001-04-02 | ||
| FR0104466A FR2822693B1 (fr) | 2001-04-02 | 2001-04-02 | Nouvelle composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoique cationique particulier |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2002078659A1 true WO2002078659A1 (fr) | 2002-10-10 |
Family
ID=8861847
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/FR2002/001138 WO2002078659A1 (fr) | 2001-04-02 | 2002-04-02 | Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoïque cationique |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US7022143B2 (fr) |
| EP (1) | EP1377264A1 (fr) |
| JP (1) | JP3748856B2 (fr) |
| FR (1) | FR2822693B1 (fr) |
| WO (1) | WO2002078659A1 (fr) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1428505A1 (fr) * | 2002-12-13 | 2004-06-16 | L'oreal | Composition tinctoriale comprenant une paraphénylènediamine tertiare cationique et un colorant direct cationique hétérocyclique, procédés et utilisations |
| US7101406B2 (en) * | 2002-12-13 | 2006-09-05 | L'oreal | Dyeing composition comprising a cationic tertiary para-phenylenediamine and a heterocyclic cationic direct dye, methods and uses |
| US7223759B2 (en) | 2003-09-15 | 2007-05-29 | Anadys Pharmaceuticals, Inc. | Antibacterial 3,5-diaminopiperidine-substituted aromatic and heteroaromatic compounds |
Families Citing this family (98)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2855967B1 (fr) * | 2003-06-16 | 2005-09-02 | Oreal | Composition tinctoriale eclaircissante comprenant au moins un colorant direct cationique a chromophores mixtes |
| US20070124872A1 (en) * | 2003-12-19 | 2007-06-07 | Eliu Victor P | Method of coloring with capped diazotized compound and coupling component |
| US20050235432A1 (en) * | 2004-01-28 | 2005-10-27 | Gregory Plos | Composition for dyeing keratin fibers, comprising at least one alcohol oxidase, at least one oxidation dye precursor, and at least one azo, methine or azomethine cationic direct dye, and process using this composition |
| US20060130244A1 (en) * | 2004-11-25 | 2006-06-22 | Franck Giroud | Aqueous composition for dyeing keratin fibres comprising a dye and a specific block copolymer |
| FR2878154B1 (fr) | 2004-11-25 | 2007-02-09 | Oreal | Composition aqueuse de coloration des fibres keratiniques comprenant un colorant et un copolymere blocs particulier |
| FR2879196B1 (fr) | 2004-12-15 | 2007-03-02 | Oreal | Composes diaz0iques symetriques a groupements 2-imidazolium et bras de liaison non cationique, compositions les comprenant, procede de coloration et dispositif |
| FR2879192B1 (fr) | 2004-12-15 | 2007-02-02 | Oreal | Composes diazoiques dissymetriques a groupement 2-pyridinium et bras de liaison cationique ou non, compositions les comprenant, procede de coloration et dispositif |
| FR2879195B1 (fr) | 2004-12-15 | 2007-03-02 | Oreal | Composes diazoiques symetriques a groupements 2-pyridinium et bras de liaison cationique ou non, compositions les comprenant, procede de coloration et dispositif |
| FR2879191B1 (fr) * | 2004-12-15 | 2007-08-24 | Oreal | Composes diazoiques dissymetriques particuliers et bras de liaison cationique ou non, compositions les comprenant, procede de coloration et dispositif |
| FR2879200B1 (fr) | 2004-12-15 | 2007-02-02 | Oreal | Composes diazoiques symetriques a groupements 4-pyridium et bras de liaison cationique ou non, compositions les comprenant, procede de coloration et dispositif |
| US7438728B2 (en) | 2004-12-15 | 2008-10-21 | L'oreal S.A. | Dissymmetrical diazo compounds comprising 2-pyridinium group and a cationic or non-cationic linker, compositions comprising them, method for coloring, and device |
| FR2879193B1 (fr) | 2004-12-15 | 2007-08-03 | Oreal | Composes diazoiques dissymetriques presentant au moins un motif 2-imidazolium et bras de liaison cationique ou non, compositions les comprenant, procede de coloration et dispositif |
| US7247713B2 (en) | 2004-12-15 | 2007-07-24 | L'oreal, S.A. | Symmetrical diazo compounds containing 2-pyridinium groups and cationic or non-cationic linker, compositions comprising them, method of coloring, and device |
| US7288639B2 (en) | 2004-12-15 | 2007-10-30 | L'oreal S.A. | Dyssymmetrical diazo compounds having at least one 4-pyridinium unit and a cationic or non-cationic linker, compositions comprising them, method of coloring, and device |
| US20090062517A2 (en) * | 2004-12-15 | 2009-03-05 | L'oreal S.A. | Dissymmetrical Diazo Compounds Containing Having at Least One 2-imidazolium Unit and a Cationic or Non-cationic Linker, Compositions Comprising Them, Method of Coloring, and Device |
| FR2879199B1 (fr) | 2004-12-15 | 2007-02-02 | Oreal | Composes diazoiques symetriques a groupements 2-imidazolium et bras de liaison cationique, compositions les comprenant, procede de coloration et dispositif |
| US7396368B2 (en) | 2004-12-15 | 2008-07-08 | L'oreal S.A. | Symmetrical diazo compounds comprising 4-pyridinium groups and a cationic or non-cationic linker, compositions comprising them, method for coloring, and device |
| FR2879190B1 (fr) | 2004-12-15 | 2007-03-02 | Oreal | Composes diazoiques dissymetriques presentant au moins un motif 4-pyridinium et bras de liaison cationique ou non, compositions les comprenant, procede de coloration et dispositif |
| US7429275B2 (en) * | 2004-12-23 | 2008-09-30 | L'oreal S.A. | Use of at least one compound chosen from porphyrin compounds and phthalocyanin compounds for dyeing human keratin materials, compositions comprising them, a dyeing process, and compounds therefor |
| FR2882521B1 (fr) | 2005-02-28 | 2008-05-09 | Oreal | Coloration de matieres keratiniques notamment humaines par transfert thermique a sec d'un colorant direct, composition comprenant ledit colorant et son procede de preparation |
| FR2882518B1 (fr) | 2005-02-28 | 2012-10-19 | Oreal | Coloration de matieres keratiniques notamment humaines par transfert thermique a sec d'un colorant direct anthraquinonique, composition comprenant ledit colorant et son procede de preparation |
| FR2882519B1 (fr) | 2005-02-28 | 2008-12-26 | Oreal | Coloration de matieres keratiniques notamment humaines par transfert thermique a sec d'un colorant direct azomethinique composition comprenant ledit colorant et son procede de preparation |
| US20060230546A1 (en) * | 2005-02-28 | 2006-10-19 | Eric Bone | Anhydrous composition in the form of a film comprising at least one film-forming polymer and at least one oxidation dye, preparation, and dyeing process |
| FR2882559B1 (fr) | 2005-02-28 | 2008-03-21 | Oreal | Composition anhydre sous forme de film comprenant un polymere filmogene et un agent oxydant, preparation et procede de traitement de fibres keratiniques la mettant en oeuvre |
| FR2882561B1 (fr) | 2005-02-28 | 2007-09-07 | Oreal | Composition anhydre sous forme de film comprenant un polymere filmogene et un colorant direct, preparation et procede de coloration la mettant en oeuvre |
| US20060242771A1 (en) * | 2005-02-28 | 2006-11-02 | Eric Bone | Anhydrous composition in the form of a film comprising a film-forming polymer and a direct dye, preparation and dyeing process using the composition |
| US20060236469A1 (en) * | 2005-02-28 | 2006-10-26 | Eric Bone | Anhydrous composition in the form of a film comprising a film-forming polymer and oxidizing agent, preparation and process for coloring keratinous fibers employing the anhydrous composition |
| FR2882560B1 (fr) | 2005-02-28 | 2007-05-18 | Oreal | Composition anhydre sous forme de film comprenant un polymere filmogene et un colorant d'oxydation, preparation et procede de coloration la mettant en oeuvre |
| FR2883738B1 (fr) | 2005-03-31 | 2007-05-18 | Oreal | Composition colorante comprenant un polymere associatif non ionique, procede de coloration de fibres keratiniques la mettant en oeuvre |
| US7550015B2 (en) * | 2005-03-31 | 2009-06-23 | L'oreal S.A. | Dye composition with a reduced content of starting materials, and process for dyeing keratin fibers using the same |
| US7575605B2 (en) * | 2005-03-31 | 2009-08-18 | L'oreal S.A. | Dye composition comprising at least one glycerol ester and a process for dyeing keratin fibers using the composition |
| FR2883736B1 (fr) | 2005-03-31 | 2007-05-25 | Oreal | Composition colorante comprenant un ester d'acide gras et procede de coloration de fibres keratiniques la mettant en oeuvre |
| FR2883737B1 (fr) | 2005-03-31 | 2009-06-12 | Oreal | Composition colorante comprenant un ester de glyceryle et procede de coloration de fibres keratiniques la mettant en oeuvre |
| FR2883735B1 (fr) | 2005-03-31 | 2009-06-12 | Oreal | Composition colorante a teneur diminuee en matieres premieres, procede de coloration de fibres keratiniques la mettant en oeuvre et dispositif |
| US7569078B2 (en) * | 2005-03-31 | 2009-08-04 | L'oreal S.A. | Dye composition comprising at least one cellulose and process for dyeing keratin fibers using the dye composition |
| US7442214B2 (en) * | 2005-03-31 | 2008-10-28 | L'oreal S.A. | Dye composition comprising at least one non-ionic associative polymer and process for dyeing keratin fibers using same |
| FR2883734B1 (fr) | 2005-03-31 | 2007-09-07 | Oreal | Composition colorante a teneur diminuee en matieres premieres et procede de coloration de fibres keratiniques la mettant en oeuvre |
| US7578854B2 (en) * | 2005-03-31 | 2009-08-25 | L'oreal S.A. | Dye composition comprising at least one fatty acid ester and process for dyeing keratin fibers using the same |
| FR2883746B1 (fr) | 2005-03-31 | 2007-05-25 | Oreal | Composition colorante comprenant une cellulose et procede de coloration de fibres keratiniques la mettant en oeuvre |
| US7651533B2 (en) | 2005-03-31 | 2010-01-26 | Oreal | Dye composition with a reduced content of starting materials, process for dyeing keratin fibers using the same and device therefor |
| FR2885045B1 (fr) | 2005-04-29 | 2007-06-08 | Oreal | Emulsion inverse comprenant une solution de peroxyde d'hydrogene et une phase inerte de solubilite dans l'eau inferieure a 1% |
| US7497878B2 (en) | 2005-06-30 | 2009-03-03 | L'oreal, S.A. | Azo dyes containing a sulphonamide or amide function for the dyeing of human keratin fibers and method of dyeing and dyeing compositions containing them |
| FR2889945B1 (fr) | 2005-08-25 | 2011-07-29 | Oreal | Composition de coloration directe comprenant des composes oxygenes insolubles, procedes mettant en oeuvre cette composition. |
| FR2889947B1 (fr) | 2005-08-25 | 2012-03-09 | Oreal | Composition oxydante comprenant des composes insolubles, procedes mettant en oeuvre cette composition |
| US7905925B2 (en) | 2005-08-25 | 2011-03-15 | L'oreal S.A. | Dye composition comprising at least one insoluble compound and processes using this composition |
| FR2889944B1 (fr) | 2005-08-25 | 2007-11-23 | Oreal | Composition tinctoriale comprenant des composes insolubles, procedes mettant en oeuvre cette composition. |
| US7481847B2 (en) | 2006-03-28 | 2009-01-27 | L'oreal S.A. | Dye composition comprising at least one cationic hydrazone direct dye, dyeing process, and multi-compartment devices |
| FR2901126B1 (fr) | 2006-05-22 | 2012-08-31 | Oreal | Utilisation d'un hydrotrope anionique pour la coloration de fibres keratiniques, composition le comprenant et procedes de coloration la mettant en oeuvre |
| FR2901127B1 (fr) | 2006-05-22 | 2012-08-31 | Oreal | Utilisation d'un hydrotrope cationique pour la coloration de fibres keratiniques, composition le comprenant et procedes de coloration la mettant en oeuvre |
| FR2917737B1 (fr) | 2007-06-22 | 2012-06-01 | Oreal | Composition de coloration comprenant un compose de type azomethinique a motif pyrazolinone |
| FR2925307B1 (fr) | 2007-12-21 | 2009-12-18 | Oreal | Procede de coloration directe eclaircissante ou d'oxydation en presence d'une amine organique particuliere et dispositif |
| FR2925323B1 (fr) | 2007-12-21 | 2009-12-18 | Oreal | Procede de coloration en presence d'un agent oxydant et d'une amine organique particuliere et dispositif |
| FR2929110B1 (fr) | 2008-03-28 | 2010-04-16 | Oreal | Dispersion aqueuse oxydante pour le traitement des fibres keratiniques comprenant un compose amphiphile non ionique a caractere hydrophobe |
| JP5815205B2 (ja) | 2008-12-19 | 2015-11-17 | ロレアル | 有機アミン及び無機塩基の存在下で、淡色化し、あるいは淡色化直接染色し、あるいは酸化染色する方法、及びそのためのデバイス |
| FR2940103B1 (fr) | 2008-12-19 | 2011-06-10 | Oreal | Procede de coloration eclaircissante de matieres keratiniques mettant en oeuvre une emulsion comprenant un colorant et un agent alcalin et une composition oxydante |
| EP2198843B1 (fr) | 2008-12-19 | 2017-09-13 | L'Oréal | Eclaircissement de fibres kératiniques humaines mettant en oeuvre une composition anhydre comprenant un melange monoethanolamine / acide amine basique et dispositif |
| US7927381B2 (en) | 2008-12-19 | 2011-04-19 | L'oreal S.A. | Process for lightening or lightening direct dyeing or oxidation dyeing in the presence of an aqueous composition comprising at least one fatty substance, and device |
| FR2940077B1 (fr) | 2008-12-19 | 2012-07-20 | Oreal | Procede de coloration eclaircissante de matieres keratiniques mettant en oeuvre une composition anhydre colorante comprenant un agent alcalin et une composition oxydante. |
| US7918902B2 (en) | 2008-12-19 | 2011-04-05 | L'oreal S.A. | Process for lightening or process for direct dyeing or oxidation dyeing of keratin fibers in the presence of at least one ammonium salt and device therefor |
| FR2940067B1 (fr) | 2008-12-19 | 2011-02-25 | Oreal | Composition oxydante pour le traitement des fibres keratiniques comprenant un polymere cationique, un amide gras et un agent-oxygene |
| BRPI0911109B8 (pt) | 2008-12-19 | 2017-05-30 | Oreal | processo de coloração ou de clareamento das matérias queratínicas humanas e dispositivo com múltiplos compartimentos |
| FR2940104B1 (fr) | 2008-12-19 | 2011-08-19 | Oreal | Procede de traitement des cheveux mettant en oeuvre une emulsion directe comprenant un agent oxydant et une composition contenant un agent alcalin |
| FR2940090B1 (fr) | 2008-12-19 | 2011-02-25 | Oreal | Composition oxydante pour le traitement des fibres keratiniques comprenant une huile, un alcool gras et un alcool gras oxyalkylene |
| BRPI0906138A2 (pt) | 2008-12-19 | 2013-04-09 | Oreal | processo de coloraÇço das fibras queratÍnicas humanas, processo de clareamento das fibras queratÍnicas humanas e dispositivo com vÁrios compartimentos |
| FR2942704B1 (fr) | 2009-03-04 | 2011-09-02 | Oreal | Dispositif de distribution d'une composition tinctoriale pour les fibres keratiniques et procede associe. |
| FR2944959B1 (fr) | 2009-04-30 | 2011-04-08 | Oreal | Utilisation pour la coloration des fibres keratiniques d'un compose de type azomethinique a motif pyrazolopyridine |
| FR2945041B1 (fr) | 2009-04-30 | 2011-04-08 | Oreal | Composes de type azomethinique a motif pyrazolopyridine cationique pour la coloration des fibres keratiniques |
| FR2949971B1 (fr) | 2009-09-17 | 2012-08-17 | Oreal | Procede d'eclaircissement ou de coloration en presence d'une composition anhydre particuliere et dispositif |
| FR2951080B1 (fr) | 2009-10-13 | 2012-01-20 | Oreal | Composition comprenant un corps gras et un acide organophosphonique ou l'un de ses sels, procede de coloration ou d'eclaircissement la mettant en oeuvre et dispositifs |
| WO2011076646A2 (fr) | 2009-12-22 | 2011-06-30 | L'oreal | Agent de coloration et/ou de blanchiment de fibres kératiniques, comprenant une émulsion inverse comprenant un agent oxydant |
| FR2954160B1 (fr) | 2009-12-22 | 2012-03-30 | Oreal | Composition de coloration ou d'eclaircissement comprenant un corps gras et un polymere amphotere |
| WO2011076647A2 (fr) | 2009-12-22 | 2011-06-30 | L'oreal | Emulsion inverse pour le traitement des cheveux, comprenant une substance grasse particulière et un agent alcalin |
| FR2954127B1 (fr) | 2009-12-22 | 2015-10-30 | Oreal | Agent de coloration et/ou de decoloration des fibres keratiniques en deux parties, comprenant un corps gras et un agent sequestrant. |
| FR2954093B1 (fr) | 2009-12-22 | 2012-02-24 | Oreal | Agent de coloration et/ou de decoloration des fibres keratiniques en deux parties ou plus sous forme d'emulsion et de dispersion |
| FR2954101B1 (fr) | 2009-12-22 | 2012-05-11 | Oreal | Agent de coloration et/ou de decoloration des fibres keratiniques en deux parties ou plus, comprenant une composition alcaline en emulsion inverse. |
| FR2954113B1 (fr) | 2009-12-22 | 2013-03-08 | Oreal | Agent de coloration et/ou de decoloration des fibres keratiniques en deux parties ou plus, sous forme d'emulsion. |
| FR2954121B1 (fr) | 2009-12-22 | 2016-03-25 | Oreal | Agent de coloration et/ou de decoloration des fibres keratiniques en deux parties, comprenant un corps gras particulier et une reductone. |
| FR2954161B1 (fr) | 2009-12-23 | 2012-03-02 | Oreal | Procede de coloration ou d'eclaircissement de fibres keratiniques en presence d'alcane(s) lineaire(s) volatil(s) et dispositif |
| FR2958161B1 (fr) | 2010-04-02 | 2012-04-27 | Oreal | Procede de traitement des cheveux mettant en oeuvre une emulsion directe comprenant un agent oxydant et une emulsion directe contenant un agent alcalin |
| FR2959127B1 (fr) | 2010-04-22 | 2016-01-01 | Oreal | Emulsion inverse pour le traitement des cheveux comprenant un solvant particulier |
| FR2960773B1 (fr) | 2010-06-03 | 2015-12-11 | Oreal | Procedes de traitement cosmetique utilisant un revetement a base d'un polymere polyamide-polyether |
| WO2015063122A1 (fr) | 2013-10-30 | 2015-05-07 | L'oreal | Composition de coloration expansible comprenant un gaz inerte, un colorant d'oxydation et un tensioactif non-ionique oxyalkyléné |
| FR3030246B1 (fr) | 2014-12-19 | 2017-02-10 | Oreal | Utilisation pour la coloration des fibres keratiniques d'un compose de type azomethinique a motif pyrazolopyridine |
| FR3030522B1 (fr) | 2014-12-19 | 2017-02-10 | Oreal | Utilisation pour la coloration des fibres keratiniques d'un compose de type azomethinique a deux motifs pyrazolopyridines |
| FR3037795B1 (fr) | 2015-06-25 | 2018-08-17 | L'oreal | Article de conditionnement comportant une enveloppe et une composition colorante, decolorante ou oxydante anhydre comprenant une argile fibreuse, et un compose choisi parmi un agent colorant et/ou un agent oxydant ; utilisation et procede pour colorer et/ou decolorer les fibres keratiniques |
| EP3389622B1 (fr) | 2015-12-18 | 2023-01-04 | L'Oréal | Composition oxydante pour le traitement des matières kératiniques, comprenant un corps gras et des tensioactifs oxyalkylénés |
| FR3045346B1 (fr) | 2015-12-21 | 2019-08-30 | L'oreal | Composition de coloration comprenant un colorant direct de structure triarylmethane, et une silicone |
| FR3045331B1 (fr) | 2015-12-21 | 2019-09-06 | L'oreal | Composition de coloration a ph acide comprenant un colorant direct de structure triarylmethane |
| FR3053041A1 (fr) | 2016-06-23 | 2017-12-29 | Oreal | Colorant direct de type azomethinique (dis)symetrique comprenant au moins un motif pyrazolopyridine, procede de coloration des fibres keratiniques a partir de ce colorant |
| FR3052969B1 (fr) | 2016-06-23 | 2020-02-21 | L'oreal | Utilisation pour la coloration des fibres keratiniques d’un compose de type azomethinique a motif derive de quinoline |
| FR3052970B1 (fr) | 2016-06-23 | 2018-06-29 | L'oreal | Procede de traitement des fibres keratiniques mettant en œuvre une composition anhydre comprenant un compose de type azomethinique a deux motifs pyrazolopyridines et une composition aqueuse |
| EP3512488B1 (fr) * | 2016-09-13 | 2023-12-06 | Wella Operations US, LLC | Compositions de coloration capillaire comprenant des imidazoliums stables bleu-violet à bleu |
| US10034823B2 (en) | 2016-09-16 | 2018-07-31 | Noxell Corporation | Method of coloring hair with washfast blue imidazolium direct dye compounds |
| FR3059233B1 (fr) | 2016-11-28 | 2019-07-26 | L'oreal | Composition tinctoriale comprenant l'acide 12-hydroxystearique, une amine organique et un colorant |
| FR3082119B1 (fr) | 2018-06-06 | 2020-05-15 | L'oreal | Procede de coloration et/ou d’eclaircissement des matieres keratiniques |
| FR3097761B1 (fr) | 2019-06-27 | 2021-05-28 | Oreal | Composition comprenant l’acide 12-hydroxystéarique, une amine organique et un corps gras liquide |
| US20230065360A1 (en) | 2019-12-24 | 2023-03-02 | L'oreal | Cosmetic composition comprising a polymer comprising at least one cationic (meth)acrylamide unit, a particular silicone and at least one surfactant |
| FR3113240B1 (fr) | 2020-08-10 | 2024-01-12 | Oreal | Composition comprenant au moins un silicone particulier, au moins un alcane et au moins une teinte directe et/ou au moins un pigment |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BE580029A (fr) * | ||||
| EP0850636A1 (fr) * | 1996-12-23 | 1998-07-01 | L'oreal | Composition de teinture d'oxydation des fibres kératiniques et procédé de teinture mettant en oeuvre cette composition |
| EP0852135A1 (fr) * | 1996-12-23 | 1998-07-08 | L'oreal | Composition de teinture d'oxydation des fibres kératiniques et procédé de teinture mettant en oeuvre cette composition |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL126606C (fr) | 1964-02-28 | |||
| JPS438949Y1 (fr) | 1964-04-14 | 1968-04-19 | ||
| JPS4215008Y1 (fr) | 1964-11-21 | 1967-08-28 | ||
| DE1544506A1 (de) | 1965-01-02 | 1970-04-16 | Hoechst Ag | Verfahren zur Herstellung von basischen Azofarbstoffen |
| DE2508884C3 (de) | 1975-02-28 | 1978-12-14 | Bayer Ag, 5090 Leverkusen | Kationische Mono- und Disazofarbstoffe und ihre Verwendung |
| TW311089B (fr) | 1993-07-05 | 1997-07-21 | Ciba Sc Holding Ag | |
| TW325998B (en) | 1993-11-30 | 1998-02-01 | Ciba Sc Holding Ag | Dyeing keratin-containing fibers |
| US5876463A (en) | 1995-06-07 | 1999-03-02 | Bristol-Myers Squibb Company | Compositions for coloring keratinous fibers comprising sulfo-containing, water dispersible colored polymers |
| FR2741798B1 (fr) | 1995-12-01 | 1998-01-09 | Oreal | Composition de teinture eclaircissante pour fibres keratiniques comprenant un colorant direct specifique |
| FR2757388B1 (fr) | 1996-12-23 | 1999-11-12 | Oreal | Composition de teinture d'oxydation des fibres keratiniques et procede de teinture mettant en oeuvre cette composition |
| FR2780883B1 (fr) | 1998-07-09 | 2001-04-06 | Oreal | Composition de teinture pour fibres keratiniques avec un colorant direct cationique et un polymere epaississant |
| FR2788433B1 (fr) | 1999-01-19 | 2003-04-04 | Oreal | Utilisation de composes phenyl-azo-benzeniques cationiques en teinture des fibres keratiniques, compositions tinctoriales et procedes de teinture |
| WO2001066646A1 (fr) | 2000-03-09 | 2001-09-13 | Ciba Specialty Chemicals Holding Inc. | Procede servant a teindre des cheveux au moyen de colorants cationiques |
-
2001
- 2001-04-02 FR FR0104466A patent/FR2822693B1/fr not_active Expired - Fee Related
-
2002
- 2002-04-02 EP EP02724400A patent/EP1377264A1/fr not_active Withdrawn
- 2002-04-02 US US10/473,625 patent/US7022143B2/en not_active Expired - Fee Related
- 2002-04-02 JP JP2002576926A patent/JP3748856B2/ja not_active Expired - Fee Related
- 2002-04-02 WO PCT/FR2002/001138 patent/WO2002078659A1/fr active Application Filing
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BE580029A (fr) * | ||||
| EP0850636A1 (fr) * | 1996-12-23 | 1998-07-01 | L'oreal | Composition de teinture d'oxydation des fibres kératiniques et procédé de teinture mettant en oeuvre cette composition |
| EP0852135A1 (fr) * | 1996-12-23 | 1998-07-08 | L'oreal | Composition de teinture d'oxydation des fibres kératiniques et procédé de teinture mettant en oeuvre cette composition |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1428505A1 (fr) * | 2002-12-13 | 2004-06-16 | L'oreal | Composition tinctoriale comprenant une paraphénylènediamine tertiare cationique et un colorant direct cationique hétérocyclique, procédés et utilisations |
| FR2848439A1 (fr) * | 2002-12-13 | 2004-06-18 | Oreal | Composition tinctoriale comprenant une paraphenylenediamine tertiaire cationique et un colorant direct cationique heterocyclique, procedes et utilisations |
| US7101406B2 (en) * | 2002-12-13 | 2006-09-05 | L'oreal | Dyeing composition comprising a cationic tertiary para-phenylenediamine and a heterocyclic cationic direct dye, methods and uses |
| US7223759B2 (en) | 2003-09-15 | 2007-05-29 | Anadys Pharmaceuticals, Inc. | Antibacterial 3,5-diaminopiperidine-substituted aromatic and heteroaromatic compounds |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2822693B1 (fr) | 2003-06-27 |
| US7022143B2 (en) | 2006-04-04 |
| US20040107513A1 (en) | 2004-06-10 |
| FR2822693A1 (fr) | 2002-10-04 |
| JP2004529137A (ja) | 2004-09-24 |
| EP1377264A1 (fr) | 2004-01-07 |
| JP3748856B2 (ja) | 2006-02-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2002078659A1 (fr) | Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoïque cationique | |
| EP1377265B1 (fr) | Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoique cationique | |
| EP1377262A1 (fr) | Composition tinctotiale pour la teinture des fibres keratiniques comprenant un colorant azoique cationique | |
| EP1377263B1 (fr) | Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant diazoique dicationique particulier | |
| EP1377261A1 (fr) | Composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant azoique cationique | |
| WO2002080869A2 (fr) | Nouvelle composition tinctoriale pour la teinture des fibres keratiniques comprenant un colorant monoazoique dicationique particulier | |
| CA2405024A1 (fr) | Composition pour la teinture des fibres keratiniques humaines comprenant un colorant monoazoique monocationique particulier | |
| FR2844269A1 (fr) | Composition pour la teinture des fibres keratiniques humaines comprenant un colorant monoazoique monocationique | |
| EP1399425A1 (fr) | Composition pour la teinture des fibres keratiniques comprenant un colorant diazo que dicationique particulier | |
| EP1399117A1 (fr) | Composition pour la teinture des fibres keratiniques comprenant un colorant diazo'ique dicationique particulier | |
| WO2002100369A2 (fr) | Composition pour la teinture des fibres keratiniques comprenant un colorant diazoique dicationique particulier | |
| FR2857258A1 (fr) | Composition comprenant au moins un derive substitue de 2-[2-(4-aminophenyl)ethenyl]-1-pyridinium, procede de traitement des fibres keratiniques la mettant en oeuvre, dispositif et utilisation | |
| EP1439812A2 (fr) | Composition contenant un derive de pyrazine et utilisation pour la teinture directe ou d'oxydation et/ou l'eclaircissement optique des fibres keratiniques | |
| FR2895904A1 (fr) | Utilisation pour la coloration avec effet eclaircissant des matieres keratiniques d'une composition comprenant un colorant fluorescent de type cyanine | |
| EP1413286A1 (fr) | Composition tinctoriale comprenant au moins une base d'oxydation hétérocyclique et au moins un coupleur 2,3-diaminopyridine substitué | |
| EP1593369A1 (fr) | Composition comprenant au moins un colorant mixte à base d'au moins un chromophore de type méthine et/ou carbonyle, procédé de coloration et colorants mixtes | |
| EP1129690A2 (fr) | Compositions de teinture des fibres keratiniques contenant des derives d'indolizine cationiques et procede de teinture | |
| FR3030246A1 (fr) | Utilisation pour la coloration des fibres keratiniques d'un compose de type azomethinique a motif pyrazolopyridine | |
| EP1879547A1 (fr) | Composition de coloration comprenant une matiere colorante et un derive du propylene glycol | |
| FR2923827A1 (fr) | Utilisation d'au moins un derive cationique de cyanine pour la coloration capillaire, composition le contenant, procede de traitement des fibres keratiniques mettant en oeuvre ladite composition, dispositif et utilisation. | |
| FR2912910A1 (fr) | Composition de coloration comprenant au moins un colorant azoique cationique a motif julolidine et au moins une base d'oxydation aminee particuliere et procede de coloration | |
| WO2003059888A1 (fr) | Derives de 4,5-diaminopyrazole sous forme de dimere et leur utilisation en teinture d'oxydation de fibres keratiniques | |
| FR2885044A1 (fr) | Composition tinctoriale contenant un colorant direct hydrazonique cationique particulier, procede de teinture, utilisation et dispositifs a plusieurs compartiments |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BY BZ CA CH CN CO CR CU CZ DE DK DM DZ EC EE ES FI GB GD GE GH GM HR HU ID IL IN IS JP KE KG KP KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NO NZ OM PH PL PT RO RU SD SE SG SI SK SL TJ TM TN TR TT TZ UA UG US UZ VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): GH GM KE LS MW MZ SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE CH CY DE DK ES FI FR GB GR IE IT LU MC NL PT SE TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2002724400 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2002576926 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 10473625 Country of ref document: US |
|
| WWP | Wipo information: published in national office |
Ref document number: 2002724400 Country of ref document: EP |
|
| REG | Reference to national code |
Ref country code: DE Ref legal event code: 8642 |