NOUVEAUX TAXOÏDES. LEUR PREPARATION ET LES COMPOSITIONS PHARMACEUTIQUES OUI LES CONTIENNENT
La présente invention concerne de nouveaux taxoïdes de formule générale :
OCOR4 dans laquelle :
Ra représente un atome d'hydrogène ou un radical hydroxy, alcoxy contenant
1 à 4 atomes de carbone, acyloxy contenant 1 à 4 atomes de carbone ou alcoxyacétoxy dont la partie alcoyle contient 1 à 4 atomes de carbone et RD représente un atome d'hydrogène ou bien Ra et R^ forment ensemble avec l'atome de carbone auquel ils sont liés une fonction cétone,
Z représente un atome d'hydrogène ou un radical de formule générale :
Rj représente un radical benzoyle éventuellement substitué par un ou plusieurs atomes ou radicaux, identiques ou différents, choisis parmi les atomes d'halogène et les radicaux alcoyles contenant 1 à 4 atomes de carbone, alcoxy contenant 1 à 4 atomes de carbone ou trifluorométhyle, thénoyle ou furoyle, ou un radical R2-O-CO- dans lequel R2 représente : - un radical alcoyle contenant 1 à 8 atomes de carbone, alcényle contenant 2 à 8 atomes de carbone, alcynyle contenant 3 à 8 atomes de carbone, cycloalcoyle contenant 3 à 6 atomes de carbone, cycloalcényle contenant 4 à 6 atomes de carbone, bicycloalcoyle contenant 7 à 10 atomes de carbone, ces radicaux étant éventuellement substitués par un ou plusieurs substituants choisis parmi les atomes d'halogène et les radicaux hydroxy, alcoxy contenant 1 à 4 atomes de carbone, dialcoylamino dont chaque partie alcoyle contient 1 à 4 atomes de carbone, pipéridino, morpholino, pipérazinyl-1 (éventuellement substitué en -4 par un radical alcoyle contenant 1 à 4
atomes de carbone ou par un radical phénylalcoyle dont la partie alcoyle contient 1 à 4 atomes de carbone), cycloalcoyle contenant 3 à 6 atomes de carbone, cycloalcényle contenant 4 à 6 atomes de carbone, phényle (éventuellement substitué par un ou plusieurs atomes ou radicaux choisis parmi les atomes d'halogène et les radicaux alcoyles contenant 1 à 4 atomes de carbone ou alcoxy contenant 1 à 4 atomes de carbone), cyano, carboxy ou alcoxycarbonyle dont la partie alcoyle contient 1 à 4 atomes de carbone,
- un radical phényle ou α- ou β-naphtyle éventuellement substitué par un ou plusieurs atomes ou radicaux choisis parmi les atomes d'halogène et les radicaux alcoyles contenant 1 à 4 atomes de carbone ou alcoxy contenant 1 à 4 atomes de carbone ou un radical hétérocyclique aromatique à 5 chaînons choisi de préférence parmi les radicaux furyle et thiényle,
- ou un radical hétérocyclyle saturé contenant 4 à 6 atomes de carbone éventuellement substitué par un ou plusieurs radicaux alcoyles contenant 1 à 4 atomes de carbone, R3 représente un radical alcoyle droit ou ramifié contenant 1 à 8 atomes de carbone, alcényle droit ou ramifié contenant 2 à 8 atomes de carbone, alcynyle droit ou ramifié contenant 2 à 8 atomes de carbone, cycloalcoyle contenant 3 à 6 atomes de carbone, phényle ou α- ou β-naphtyle éventuellement substitué par un ou plusieurs atomes ou radicaux choisis parmi les atomes d'halogène et les radicaux alcoyles, alcényles, alcynyles, aryles, aralcoyles, alcoxy, alcoylthio, aryloxy, arylthio, hydroxy, hydroxyalcoyle, mercapto, formyle, acyle, acylamino, aroylamino, alcoxycarbonyl- amino, amino, alcoylamino, dialcoylamino, carboxy, alcoxycarbonyle, carbamoyle, alcoylcarbamoyle, dialcoylcarbamoyle, cyano, nitro et trifluorométhyle, ou un hétérocycle aromatique ayant 5 chaînons et contenant un ou plusieurs hétéroatomes, identiques ou différents, choisis parmi les atomes d'azote, d'oxygène ou de soufre et éventuellement substitué par un ou plusieurs substituants, identiques ou différents, choisis parmi les atomes d'halogène et les radicaux alcoyles, aryles, amino, alcoylamino, dialcoylamino, alcoxycarbonylamino, acyle, arylcarbonyle, cyano, carboxy, carbamoyle, alcoylcarbamoyle, dialcoylcarbamoyle ou alcoxycarbonyle, étant entendu que, dans les substituants des radicaux phényle, α- ou β-naphtyle et hétérocyclyles aromatiques, les radicaux alcoyles et les portions alcoyles des autres radicaux contiennent 1 à 4 atomes de carbone et que les radicaux alcényles et alcynyles contiennent 2 à 8 atomes de carbone et que les radicaux aryles sont des radicaux phényles ou α- ou β-naphtyles, et R4 et R5, identiques ou différents, représentent
- un radical alcoyle droit ou ramifié contenant 1 à 8 atomes de carbone, alcényle droit ou ramifié contenant 2 à 8 atomes de carbone, alcynyle droit ou ramifié contenant 2 à 8 atomes de carbone, cycloalcoyle contenant 3 à 6 atomes de carbone, cycloalcényle contenant 4 à 6 atomes de carbone ou bicycloalcoyle contenant 7 à 11 atomes de carbone, ces radicaux étant éventuellement substitués par un ou plusieurs substituants choisis parmi les atomes d'halogène et les radicaux hydroxy, alcoyloxy contenant 1 à 4 atomes de carbone, dialcoylamino dont chaque partie alcoyle contient 1 à 4 atomes de carbone, pipéridino, morpholino, pipérazinyl-1 (éventuellement substitué en -4 par un radical alcoyle contenant 1 à 4 atomes de carbone ou par un radical phénylalcoyle dont la partie alcoyle contient 1 à 4 atomes de carbone), cycloalcoyle contenant 3 à 6 atomes de carbone, cycloalcényle contenant 4 à 6 atomes de carbone, phényle éventuellement substitué, cyano, carboxy ou alcoyloxycarbonyle dont la partie alcoyle contient 1 à 4 atomes de carbone, - ou un radical aryle éventuellement substitué par un ou plusieurs atomes ou radicaux choisis parmi les atomes d'halogène et les radicaux alcoyles, alcényles, alcynyles, aryles, aralcoyles, alcoxy, alcoylthio, aryloxy, arylthio, hydroxy, hydroxyalcoyle, mercapto, formyle, acyle, acylamino, aroylamino, alcoxycarbonyl-amino, amino, alcoylamino, dialcoylamino, carboxy, alcoxycarbonyle, carbamoyle, alcoylcarbamoyle, dialcoylcarbamoyle, cyano, nitro, azido, trifluorométhyle ou trifluorométhoxy, ou un radical hétérocyclyle saturé ou non saturé contenant 4 à 6 chaînons et éventuellement substitué par un ou plusieurs radicaux alcoyles contenant 1 à 4 atomes de carbone, étant entendu que R5 ne peut pas représenter un radical méthyle, étant entendu que les radicaux cycloalcoyles, cycloalcényles ou bicycloalcoyles peuvent être éventuellement substitués par un ou plusieurs radicaux alcoyles contenant 1 à 4 atomes de carbone.
De préférence les radicaux aryles pouvant être représentés par R3, R4 et/ou R5 sont des radicaux phényles ou α- ou β-naphtyles éventuellement substitués par un ou plusieurs atomes ou radicaux choisis parmi les atomes d'halogène (fluor, chlore, brome, iode) et les radicaux alcoyles, alcényles, alcynyles, aryles, arylalcoyles, alcoxy, alcoylthio, aryloxy, arylthio, hydroxy, hydroxyalcoyle, mercapto, formyle, acyle, acylamino, aroylamino, alcoxycarbonylamino, amino, alcoylamino, dialcoylamino, carboxy, alcoxycarbonyle, carbamoyle, dialcoylcarbamoyle, cyano, nitro, azido, trifluorométhyle et trifluorométhoxy, étant entendu que les radicaux alcoyles et les
portions alcoyles des autres radicaux contiennent 1 à 4 atomes de carbone, que les radicaux alcényles et alcynyles contiennent 2 à 8 atomes de carbone et que les radicaux aryles sont des radicaux phényles ou α- ou β-naphtyles, et que le radical R5 ne peut pas représenter un radical méthyle. De préférence les radicaux hétérocycliques pouvant être représentés par R3,
R4 et/ou R5 sont des radicaux hétérocycliques aromatiques ayant 5 chaînons et contenant un ou plusieurs atomes, identiques ou différents, choisis parmi les atomes d'azote, d'oxygène ou de soufre, éventuellement substitués par un ou plusieurs substituants, identiques ou différents, choisis parmi les atomes d'halogène (fluor, chlore, brome, iode) et les radicaux alcoyles contenant 1 à 4 atomes de carbone, aryles contenant 6 à 10 atomes de carbone, alcoxy contenant 1 à 4 atomes de carbone, aryloxy contenant 6 à 10 atomes de carbone, amino, alcoylamino contenant 1 à 4 atomes de carbone, dialcoylamino dont chaque partie alcoyle contient 1 à 4 atomes de carbone, acylamino dont la partie acyle contient 1 à 4 atomes de carbone, alcoxycarbonylamino contenant 1 à 4 atomes de carbone, acyle contenant 1 à 4 atomes de carbone, arylcarbonyle dont la partie aryle contient 6 à 10 atomes de carbone, cyano, carboxy, carbamoyle, alcoylcarbamoyle dont la partie alcoyle contient 1 à 4 atomes de carbone, dialcoylcarbamoyle dont chaque partie alcoyle contient 1 à 4 atomes de carbone ou alcoxycarbonyle dont la partie alcoxy contient 1 à 4 atomes de carbone.
Plus particulièrement, la présente invention concerne les produits de formule générale (I) dans laquelle Ra représente un radical hydroxy, alcoxy contenant 1 à 4 atomes de carbone, acyloxy contenant 1 à 4 atomes de carbone ou alcoxyacétoxy dont la partie alcoyle contient 1 à 4 atomes de carbone et R5 représente un atome d'hydrogène, Z représente un atome d'hydrogène ou un radical de formule générale (II) dans laquelle R^ représente un radical benzoyle ou un radical R2-O-CO- dans lequel R2 représente un radical tert-butyle et R3 représente un radical alcoyle contenant 1 à 6 atomes de carbone, alcényle contenant 2 à 6 atomes de carbone, cycloalcoyle contenant 3 à 6 atomes de carbone, phényle éventuellement substitué par un ou plusieurs atomes ou radicaux, identiques ou différents choisis parmi les atomes d'halogène (fluor, chlore) et les radicaux alcoyles (méthyle), alcoxy (méthoxy), dialcoylamino (diméthylamino), acylamino (acétylamino), _dcoxycarlx)nyl_-mino (tert- butoxycarbonylamino) ou trifluorométhyle ou un radical furyle-2 ou -3, thiényle-2 ou -3 ou thiazolyle-2, -4 ou -5 et R4 représente un radical phényle éventuellement substitué par un ou plusieurs atomes ou radicaux, identiques ou différents, choisis
parmi les atomes d'halogène et les radicaux alcoyles, alcoxy, amino, alcoylamino, dialcoylamino, acylamino, alcoxycarbonylamino, azido, trifluorométhyle et trifluoro¬ méthoxy, ou un radical thiényle-2 ou -3 ou furyle-2 ou -3 et R5 représente un radical alcoyle éventuellement substitué contenant 1 à 4 atomes de carbone, étant entendu que R5 ne peut pas représenter un radical méthyle.
Plus particulièrement encore, la présente invention concerne les produits de formule générale (I) dans laquelle Ra représente un atome d'hydrogène ou un radical hydroxy ou acétyloxy ou méthoxyacétoxy et R^ représente un atome d'hydrogène, Z représente un atome d'hydrogène ou un radical de formule générale (H) dans laquelle Rj représente un radical benzoyle ou un radical R2-O-CO- dans lequel R2 représente un radical tert-butyle et R3 représente un radical isobutyle, isobutényle, butényle, cyclohexyle, phényle, furyle-2, furyle-3, thiényle-2, thiényle-3, thiazolyle-2, thiazolyle-4 ou thiazolyle-5 et R4 représente un radical phényle éventuellement substitué par un atome d'halogène et R5 représente un radical alcoyle contenant 2 à 4 atomes de carbone.
Les produits de formule générale (I) dans laquelle Z représente un radical de formule générale (II) présentent des propriétés antitumorales et antileucémiques remarquables.
Selon la présente invention, les produits de formule générale (I) dans laquelle Ra représente un atome d'hydrogène ou un radical alcoxy, acyloxy ou alcoxyacétoxy, R^ représente un atome d'hydrogène, R4, R5 et Z sont définis comme précédemment peuvent être obtenus par action d'un halogénure de métal alcalin (chlorure de sodium, iodure de sodium, fluorure de potassium) ou d'un azoture de métal alcalin (azoture de sodium) ou d'un sel d'ammonium quaternaire ou d'un phosphate de métal alcalin sur un produit de formule générale :
OCOR4 dans laquelle Z, R4 et R5 sont définis comme précédemment, Ra représente un atome d'hydrogène ou un radical alcoxy, acyloxy, alcoxyacétoxy ou un radical hydroxy
protégé, et R^ représente un atome d'hydrogène, suivi, si nécessaire, du remplacement du groupement protecteur porté par Ra par un atome d'hydrogène.
Généralement, la réaction est effectuée dans un solvant organique choisi parmi les éthers (tétrahydrofuranne, diisopropyléther, méthyl tert-butyléther) et les nitriles (acétonitrile) seul ou en mélange à une température comprise entre 20°C et la température d'ébullition du mélange réactionnel.
Le produit de formule générale (III) dans laquelle Z représente un radical de formule générale (II) peut être obtenu par estérification d'un produit de formule générale :
0C0RA dans laquelle R4, R5 sont définis comme précédemment, et R
a représente un atome d'hydrogène ou un radical alcoxy, acyloxy, alcoxyacétoxy ou un radical hydroxy protégé, et R^ représente un atome d'hydrogène, au moyen d'un acide de formule générale :
N ° O
(V)
R. OH
O-R- dans laquelle Rj et R3 sont définis comme précédemment, ou bien Rg représente un atome d'hydrogène et R7 représente un groupement protecteur de la fonction hydroxy, et ou bien Rg et R7 forment ensemble un hétérocycle saturé à 5 ou 6 chaînons, ou d'un dérivé de cet acide pour obtenir un ester de formule générale :
0C0R<
dans laquelle R
a, R , Ri , R3, R4, R5, Rβ et R7 sont définis comme précédemment, suivi du remplacement des groupements protecteurs représentés par R7 et/ou R et R7 par des atomes d'hydrogène et éventuellement R
a, lorsqu'il représente un radical acyloxy, alcoxyacétoxy ou un radical hydroxy protégé, par un radical hydroxy. L'estérification au moyen d'un acide de formule générale (V) peut être effectuée en présence d'un agent de condensation (carbodiimide, carbonate réactif) et d'un agent d'activation (aminopyridines) dans un solvant organique (éther, ester, cétones, nitriles, hydrocarbures aliphatiques, hydrocarbures aliphatiques halogènes, hydrocarbures aromatiques) à une température comprise entre -10 et 90°C. L'estérification peut aussi être réalisée en utilisant l'acide de formule générale (V) sous forme d'anhydride en opérant en présence d'un agent d'activation (aminopyridines) dans un solvant organique (éthers, esters, cétones, nitriles, hydrocarbures aliphatiques, hydrocarbures aliphatiques halogènes, hydrocarbures aromatiques) à une température comprise entre 0 et 90°C. L'estérification peut aussi être réalisée en utilisant l'acide de formule générale (V) sous forme d'halogénure ou sous forme d'anhydride avec un acide aliphatique ou aromatique, éventuellement préparé in situ, en présence d'une base (aminé aliphatique tertiaire) en opérant dans un solvant organique (éthers, esters, cétones, nitriles, hydrocarbures aliphatiques, hydrocarbures aliphatiques halogènes, hydrocarbures aromatiques) à une température comprise entre 0 et 80°C.
Lorsque Ra représente un groupement protecteur de la fonction hydroxy, Ra est de préférence un radical trichloro-2,2,2 éthoxycarbonyloxy.
De préférence, R6 représente un atome d'hydrogène et R7 représente un groupement protecteur de la fonction hydroxy ou bien R et R7 forment ensemble un hétérocycle saturé à 5 ou 6 chaînons.
Lorsque Rβ représente un atome d'hydrogène, R7 représente de préférence un radical méthoxyméthyle, éthoxy-1 éthyle, benzyloxyméthyle, triméthylsilyle, triéthylsilyle, β-triméthylsilyléthoxyméthyle, benzyloxycarbonyle ou tétrahydro- pyrannyle. Lorsque Rg et R7 forment ensemble un hétérocycle, celui-ci est de préférence un cycle oxazolidine éventuellement mono-substitué ou gem-disubstitué en position -2.
Le remplacement des groupements protecteurs R7 et/ou Rβ et R7 par des atomes d'hydrogène et éventuellement de Ra par un radical hydroxy peut être effectué, selon leur nature de la manière suivante :
1) lorsque Rβ représente un atome d'hydrogène et R7 représente un groupement protecteur de la fonction hydroxy, Ra représente un radical alcoxy, acyloxy ou alcoxyacétoxy, le remplacement des groupements protecteurs par des atomes d'hydrogène s'effectue au moyen d'un acide minéral (acide chlorhydrique, acide sulfurique, acide fluorhydrique) ou organique (acide acétique, acide méthane- sulfonique, acide trifluorométhanesulfonique, acide p.toluènesulfonique) utilisé seul ou en mélange en opérant dans un solvant organique choisi parmi les alcools, les éthers, les esters, les hydrocarbures aliphatiques, les hydrocarbures aliphatiques halogènes, les hydrocarbures aromatiques ou les nitriles à une température comprise entre -10 et 60°C,
2) lorsque Rβ représente un atome d'hydrogène et R7 représente un groupement protecteur de la fonction hydroxy, Ra représente un radical trichloro-2,2,2 éthoxycarbonyloxy, le remplacement du groupement protecteur R7 est effectué dans les conditions décrites ci-dessus sous 1) et celui de Ra par traitement par le zinc, éventuellement associé à du cuivre, en présence d'acide acétique à une température comprise entre 30 et 60°C ou au moyen d'un acide minéral ou organique tel que l'acide chlorhydrique ou l'acide acétique en solution dans un alcool aliphatique contenant 1 à 3 atomes de carbone (méthanol, éthanol, propanol, isopropanol) ou dans un ester aliphatique (acétate d'éthyle, acétate d'isopropyle acétate de n.butyle) en présence de zinc éventuellement associé à du cuivre,
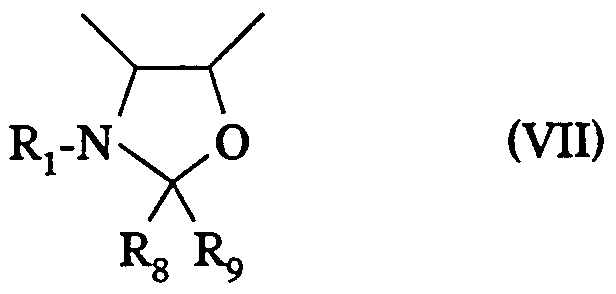
3) lorsque Rβ et R7 forment ensemble un hétérocycle saturé à 5 ou 6 chaînons et plus particulièrement un cycle oxazolidine de formule générale :
dans laquelle R est défini comme précédemment, Rg et R9, identiques ou différents, représentent un atome d'hydrogène ou un radical alcoyle contenant 1 à 4 atomes de carbone, ou un radical aralcoyle dont la partie alcoyle contient 1 à 4 atomes de carbone et la partie aryle représente, de préférence, un radical phényle éventuellement substitué par un ou plusieurs radicaux alcoxy contenant 1 à 4 atomes de carbone, ou un radical aryle représentant, de préférence un radical phényle éventuellement substitué par un ou plusieurs radicaux alcoxy contenant 1 à 4 atomes de carbone, ou bien Rg représente un radical alcoxy contenant 1 à 4 atomes de
carbone ou un radical trihalométhyle tel que trichlorométhyle ou un radical phényle substitué par un radical trihalométhyle tel que trichlorométhyle et R9 représente un atome d'hydrogène, ou bien Rg et R9 forment ensemble avec l'atome de carbone auquel ils sont liés un cycle ayant 4 à 7 chaînons, et Ra représente un radical acyloxy ou alcoxyacétoxy ou trichloro-2,2,2 éthoxycarbonyloxy, le remplacement du groupement protecteur formé par Rβ et R7 par des atomes d'hydrogène et de Ra par un radical hydroxy peut être effectué, selon les significations de Ra, Rj, Rg et R9, de la manière suivante : a) lorsque R\ représente un radical tert-butoxycarbonyle, Rg et R9, identiques ou différents, représentent un radical alcoyle ou un radical aralcoyle (benzyle) ou aryle (phényle), ou bien Rg représente un radical trihalométhyle ou un radical phényle substitué par un radical trihalométhyle, et R9 représente un atome d'hydrogène, ou bien Rg et R9 forment ensemble un cycle ayant de 4 à 7 chaînons, le traitement de l'ester de formule générale (VI) par un acide minéral ou organique éventuellement dans un solvant organique tel qu'un alcool conduit au produit de formule générale :
dans laquelle R
a, Rb, R3, R4 et R5 sont définis comme précédemment, qui est acylé au moyen de chlorure de benzoyle dans lequel le noyau phényle est éventuellemnt substitué, de chlorure de thénoyle, de chlorure de furoyle ou d'un produit de formule générale :
R2-O-CO-X (IX) dans laquelle R2 est défini comme précédemment et X représente un atome d'halogène (fluor, chlore) ou un reste -O-R2 ou -O-CO-O-R2, pour obtenir un produit de formule générale :
R
dans laquelle R
a, R^, Ri, R3, R4 et R5 sont définis comme précédemment, dont le groupement protecteur R
a, lorsqu'il représente un radical hydroxy protégé, est remplacé, si nécessaire, par un radical hydroxy. De préférence, le produit de formule générale (VI) est traité par l'acide formique à une température voisine de 20°C.
De préférence, l'acylation du produit de formule générale (VIII) au moyen d'un chlorure de benzoyle dans lequel le radical phényle est éventuellement substitué, de chlorure de thénoyle ou de chlorure de furoyle ou d'un produit de formule générale (IX) est effectuée dans un solvant organique inerte choisi parmi les esters tels que l'acétate d'éthyle, l'acétate d'isopropyle ou l'acétate de n.butyle et les hydrocarbures aliphatiques halogènes tels que le dichlorométhane ou le dichloro-1,2 éthane en présence d'une base minérale telle que le bicarbonate de sodium ou organique telle que la Iriéthylamine. La réaction est effectuée à une température comprise entre 0 et 50°C, de préférence voisine de 20°C.
De préférence, le remplacement du groupement protecteur de Ra, lorsqu'il représente un radical trichloro-2,2,2 éthoxycarbonyloxy, est effectué dans les conditions décrites précédemment sous 2), b) lorsque R représente un radical benzoyle éventuellement substitué, thénoyle ou furoyle ou un radical R2O-CO- dans lequel R2 est défini comme précédemment, Rg représente un atome d'hydrogène ou un radical alcoxy contenant 1 à 4 atomes de carbone ou un radical phényle substitué par un ou plusieurs radicaux alcoxy contenant 1 à 4 atomes de carbone et R9 représente un atome d'hydrogène, le remplacement du groupement protecteur formé par Rβ et R7 par des atomes d'hydrogène s'effectue en présence d'un acide minéral (acide chlorhydrique, acide sulfurique) ou organique (acide acétique, acide méthane-sulfonique, acide trifluorométhanesulfonique, acide p.toluènesulfonique) utilisé seul ou en mélange en quantité stoechiométrique ou catalytique, en opérant dans un solvant organique
choisi parmi les alcools, les éthers, les esters, les hydrocarbures aliphatiques, les hydrocarbures aliphatiques halogènes et les hydrocarbures aromatiques à une température comprise entre -10 et 60°C, de préférence entre 15 et 30°C et le remplacement du groupement protecteur de Ra, lorsqu'il représente un radical trichloro-2,2,2 éthoxycarbonyloxy par un atome d'hydrogène, s'effectue dans les conditions décrites précédemment sous 2).
4) lorsque Ra représente un radical alcoxyacétyle et Rβ et R7 sont définis comme au point 1) ci-dessus, on effectue d'abord le remplacement du groupement protecteur R7 par un atome d'hydrogène en opérant dans les conditions acides décrites au point 1) ci-dessus, puis remplace éventuellement Ra par un radical hydroxy par traitement en milieu alcalin ou par action d'un halogénure de zinc dans des conditions qui ne touchent pas au reste de la molécule. Généralement, le traitement alcalin est effectué par action de l'ammoniac en milieu hydro-alcoolique à une température voisine de 20°C. Généralement, le traitement par un halogénure de zinc, de préférence l'iodure de zinc est effectué dans le méthanol à une température voisine de 20°C.
5) lorsque Ra représente un radical alcoxyacétoxy et Rβ et R7 sont définis comme au point 2-a) ci-dessus, on effectue le remplacement du radical Ra par un radical hydroxy par traitement en milieu alcalin ou par traitement par un halogénure de zinc dans les conditions décrites au point 3) ci-dessus, puis traite le produit de formule générale (VI) obtenu dans les conditions de déprotection et d'acylation décrites au point 2-a) ci-dessus.
6) lorsque Ra représente un radical alcoxyacétoxy et Rβ et R7 sont définis comme au point 2-b) ci-dessus, on effectue le remplacement du radical Ra par un radical hydroxy par traitement en milieu alcalin ou par traitement par un halogénure de zinc dans les conditions décrites au point 3) ci-dessus, puis traite le produit obtenu dans les conditions décrites au point 2-b) ci-dessus.
Selon l'invention, les produits de formule générale (III) dans laquelle R4 et R5 sont définis comme précédemment, R
a représente atome d'hydrogène ou un radical alcoxy, acyloxy ou alcoxyacétoxy, et R
D représente un atome d'hydrogène, ou bien R
a et R^ forment ensemble avec l'atome de carbone auquel ils sont liés, une fonction cétone et Z représente un atome d'hydrogène peuvent être obtenus par action d'un dérivé de l'acide trifluorométhanesulfonique tel que l'anhydride ou le N-phényl trifluorométhanesiilf onimide sur un produit de formule générale :
OCOR4 dans laquelle Ra, R^, R4 et R5 sont définis comme précédemment
Généralement, la réaction s'effectue dans un solvant organique inerte (hydrocarbures aliphatiques éventuellement halogènes, hydrocarbures aromatiques) en présence d'une base organique telle qu'une aminé tertiaire aliphatique (triéthylamine) ou la pyridine à une température comprise entre -50 et +20°C.
Les produits de formule générale (XI) dans laquelle R4 et R5 sont définis comme précédemment, Ra représente un atome d'hydrogène ou un radical alcoxy, acyloxy ou alcoxyacétoxy ou un radical hydroxy protégé, Rb représente un atome d'hydrogène, peuvent être obtenus par action de l'acide fluorhydrique ou de l'acide trifluoroacétique dans un solvant organique basique, tel que la pyridine éventuellement substituée par un ou plusieurs radicaux alcoyles contenant 1 à 4 atomes de carbone, ou la triéthylamine éventuellement en association avec un solvant organique inerte tel que le chlorure de méthylène ou racétonitrile ou le tétrahydrofuranne à une température comprise entre 20 et 80°C sur un produit de formule générale :
OCOR4 dans laquelle R4 et R5 sont définis comme précédemment, Ra représente un atome d'hydrogène ou un radical alcoxy, acyloxy ou alcoxyacétoxy ou un radical hydroxy protégé, R représente un atome d'hydrogène, et les symboles Gj, qui sont identiques représentent un radical triacoylsilyle.
Le produit de formule générale (XII) peut être obtenu par action d'un produit de formule générale :
R-Y (XIII) dans laquelle R représente un radical alcoyle, alcanoyle ou alcoxyacétyle ou un groupement protecteur de la fonction hydroxy et Y représente un atome d'halogène sur un produit de formule générale :
OCOR4 dans laquelle R4, R5 et Gi sont définis comme précédemment
Lorsque R représente un radical alcoyle ou alcoxyacétyle il est particulièrement avantageux d'opérer dans un solvant organique basique tel que la pyridine ou dans un solvant organique inerte tel que le chlorure de méthylène, le chloroforme ou le dichloro-1,2 éthane en présence d'une aminé tertiaire telle que la triéthylamine ou la pyridine à une température voisine de 0°C.
Lorsque R représente un radical alcoyle, il est particulièrement avantageux de métaller préalablement la fonction hydroxy en -10 au moyen d'un hydrure alcalin (hydrure de sodium) ou d'un alcoylure métallique (butyllithium).
Le produit de formule générale (XIV) et éventuellement le produit de formule générale (XII) peuvent être obtenus par action d'un dérivé organométallique de formule générale : R4-M (XV) dans laquelle R4 est défini comme précédemment et M représente un atome métallique, de préférence un atome de lithium ou de magnésium, sur un produit de formule générale :
dans laquelle R
a, Rb, R5 et Gi sont définis comme précédemment.
Généralement, la réaction est effectuée dans un solvant organique tel qu'un éther (tétrahydrofuranne) à une température inférieure à -50°C, de préférence voisine de -78°C.
Le produit de formule générale (XVI) peut être obtenu par estérification d'un produit de formule générale :
dans laquelle R
a, Rb et Gi sont définis comme précédemment, au moyen d'un acide de formule générale :
R5-COOH (XVIII) dans laquelle R5 est défini comme précédemment, ou d'un dérivé de cet acide tel qu'un halogénure ou un anhydride en présence d'un agent de condensation ou d'une base minérale ou organique. Le produit de formule générale (XVII) peut être obtenu par action d'un produit de formule générale (XIII) sur un produit de formule générale :
dans laquelle G est défini comme précédemment dans les conditions décrites précédemment pour l'action d'un produit de formule générale (XIII) sur un produit de formule générale (XIV).
Le produit de formule générale (XIX) peut être préparé par action du phosgène ou d'un de ses dérivés tel que le triphosgène sur un produit de formule générale :
dans laquelle Gi est défini comme précédemment en opérant dans un solvant organique basique tel que la pyridine à une température inférieure à -50°C, de préférence voisine de -78°C.
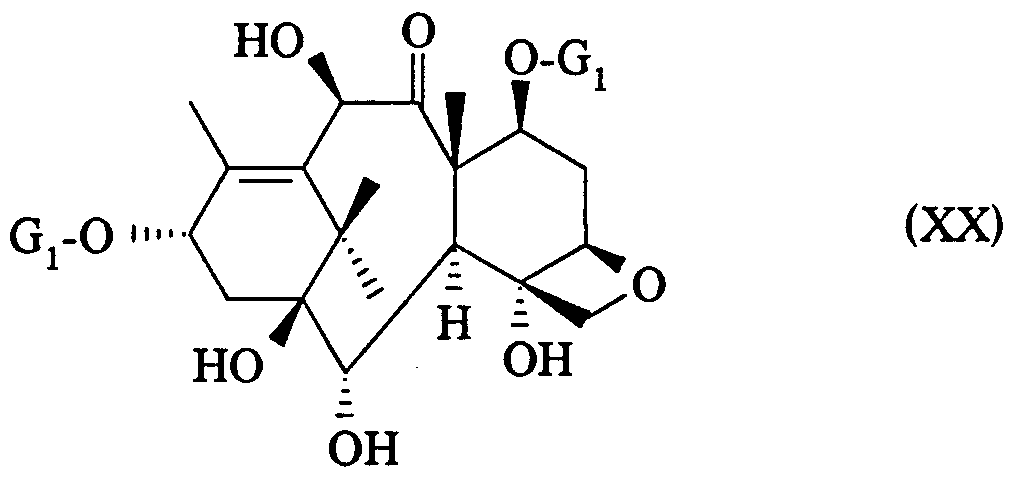
Le produit de formule générale (XX) peut être préparé par action d'un halogénotrialcoylsilane sur un produit de formule générale :
dans laquelle Gi est défini comme précédemment en opérant dans un solvant organique basique.
Le produit de formule générale (XXI) peut être préparé dans les conditions décrites par D.G.I. Kingston et coll., Journal of Nat Prod. , 5__L 884 (1993).
Les produits de formule générale (I) dans laquelle Ra et Rb représentent chacun un atome d'hydrogène peuvent être obtenus par réduction électrolytique d'un produit de formule générale (I) dans laquelle Ra représente un radical hydroxy ou un radical acyloxy ou alcoxyacétoxy ou dans les conditions décrites dans la demande internationale PCT WO 93/06093.
Les produit de formule générale (I) dans laquelle Ra et Rb forment ensemble avec l'atome de carbone auquel ils sont liés une fonction cétone peuvent être obtenus par oxydation d'un produit de formule générale (I) dans laquelle Ra représente un radical hydroxy et Rb représente un atome d'hydrogène au moyen, par exemple, de chlorochromate de pyridinium, de dichromate de pyridinium, de bichromate de potassium, de bichromate d'ammonium ou de bioxyde de manganèse.
Les nouveaux produits de formule générale (I) obtenus par la mise en oeuvre des procédés selon l'invention peuvent être purifiés selon les méthodes connues telles que la cristallisation ou la chromatographie. Les produits de formule générale (I) dans laquelle Z représente un radical de formule générale (II) présentent des propriétés biologiques remarquables.
In vitro, la mesure de l'activité biologique est effectuée sur la tubuline extraite de cerveau de porc par la méthode de M.L. Shelanski et coll., Proc. Natl. Acad. Sci. USA, 7J_, 765-768 (1973). L'étude de la dépolymérisation des microtu- bules en tubuline est effectuée selon la méthode de G. Chauvière et coll., C.R. Acad. Sci., 222, série II, 501-503 (1981). Dans cette étude les produits de formule générale (I) dans laquelle Z représente un radical de formule générale (II) se sont montrés au moins aussi actifs que le taxol et le Taxotère.
In vivo, les produits de formule générale (I) dans laquelle Z représente un radical de formule générale (II) se sont montrés actifs chez la souris greffée par le mélanome B16 à des doses comprises entre 1 et 10 mg/ g par voie intrapéritonéale, ainsi que sur d'autres tumeurs liquides ou solides.
Les nouveaux produits ont des propriétés anti-tumorales et plus particulièrement une activité sur les tumeurs qui sont résistantes au Taxol® ou au Taxotère®. De telles tumeurs comprennent les tumeurs du colon qui ont une expression élevée du gène mdr 1 (gène de la multi-drug résistance). La multi-drug résistance est un terme habituel se rapportant à la résistance d'une tumeur à différents produits de structures et de mécanismes d'action différents. Les taxoïdes sont généralement connus pour être fortement reconnus par des tumeurs expérimentales
telles que P388/DOX, une lignée cellulaire sélectionnée pour sa résistance à la doxorubicine (DOX) qui exprime mdr 1.
Les exemples suivants illustrent la présente invention.
EXEMPLE 1
A une solution de 0,193 g de tert-butoxycarbonylamino-3 hydroxy-2 phényl-4 propionate-(2R,4S) de benzoyloxy-2 époxy-5β,20 hydroxy-lβ méthoxy- acétoxy-lOβ oxo-9 propanoyloxy-4 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dans 2,5 cm3 d'acétonitrile et 0,250 cm3 de tétrahydrofurane, on ajoute successivement 0.096 g de tamis moléculaire 4À en poudre, 0,290 g de chlorure de sodium. Le milieu réactionnel est maintenu sous agitation à une température voisine de 75°C pendant 5 heures puis, à une température voisine de 20°C, additionné de 75 cm3 de dichlorométhane et 50 cm3 d'une solution aqueuse saturée de chlorure de sodium. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7kPa) à 40°C. On obtient 0,150 g d'un produit que l'on purifie par chromatographie sur 80 g de silice (0,063-0,2 mm) contenus dans une colonne de 1 cm de diamètre (éluant : dichlorométhane-méthanol : 98/2 en volumes) en recueillant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7kPa) à 40°C. On obtient 0,080 g de tert-butoxycarbonylamino-3 hydroxy-2 phenyl- 3 propionate-(2R,4S) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxy- acétoxy-lOβ méthylène-7β,8 nor-19 oxo-9 propanoyloxy-4α taxène-11 yle-13α dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (400 MHz, CDC13, δ en ppm) : 1,24 (t, J = 7.5 Hz, 3H : CH3 éthyle) ; 1,24 (s, 6H : CH3) ; 1,27 (s, 9H : C(CH-)3) ; 1,42 (mt, IH : H 7) ; 1,68 et 2,24 (2 mis. IH chacun : CH2 en 19) ; 1,86 (s, IH 0H en 1) ; 1,86 (s, 3H : CH3) ; 2,12 et 2,86 (respectivement d et dt, J = 16 et J = 16 et 5 Hz, IH chacun : CH2 en 6) ; de 2,15 à 2,30 et 2,41 (respectivement mt et dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,64 (mt, 2H : CH2 éthyle) ; 3,26 (mt, IH : OH en 2') ; 3,52 (s, 3H : OCH3) ; 4,07 (d, J = 7 Hz, IH : H en 3) ; 4,04 et 4,33 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,22 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,62 (mt, IH : H en 2') ; 4,70 (d, J = 4 Hz, IH : H en 5) ; 5,28 (md, 2H : H en 3' et CONH) ; 5,67 (d, J = 7 Hz, IH : H en 2); 6,26 (t large, J = 9 Hz, IH : H en 13) ; 6,42 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 5H: H aromatiques en 3") ; 7,52 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,62 (t,
J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,16 (d, J = 7.5 Hz, 2H : OCOC6H5 H en ortho).
Le tert-butoxycarbonylamino-3 hydroxy-2 phényl-4 propionate-(2R,4S) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy- A trifluorométhanesulfonyloxy-7β taxène-11 yle-13α peut être préparé de la manière suivante :
Une solution de 0,760 g de tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R,4S,5R) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α trifluorométhanesulfonate- 7β taxène-11 yle-13α dans 6,6 cm3 d'une solution 0,1N d'éthanol chlorhydrique est maintenue sous agitation à une température voisine de 0°C pendant 22 heures. Le milieu réactionnel est concentré à sec sous pression réduite (2,7kPa) à 20°C. Le brut réactionnel est dissous dans 80 cm3 de dichlorométhane et 80 cm3 d'une solution aqueuse saturée de bicarbonate de sodium. La phase organique est séparée par décantation puis extraite par 2 fois 50 cm3 de dichlorométhane. Les phases organiques sont réunies, lavées par 50 cm3 d'eau distillée puis séchées sur sulfate de magnésium, filtrées et concentrées à sec sous pression réduite (2,7 kPa) à 20°C. On obtient 0,9 g d'une meringue blanche que l'on purifie par chromatographie sur 150 g de silice (0,063-0,2 mm) contenus dans une colonne de 3 cm de diamètre (éluant : dichlorométhane-méthanol : 95-5 en volumes) en recueillant des fractions de 15 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7kPa) à 20°C. On obtient 0,456 g de tert- butoxyc_ιrbonyl__mino-3 hydroxy-2 phényl-4 propionate-(2R,4S) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α trifluoro- méthanesulfonyloxy-7β taxène-11 yle-13α et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. *Α (400 MHz, CDC13, δ en ppm) : 1,24 (s, 9H,: CH3 et CH3 éthyle) ; 1,34 (s, 9H : C(CH3)3) ; 1,74 (s, IH : 0H en 1) ; 1,88 (s, 3H : CH3) ; 2,05 (s large, 3H : CH3) ; 2,24 et 2,86 (2 mis, IH chacun : CH2 en 6) ; 2,33 (d, J = 9 Hz, 2H : CH2 en 14) ; 2,68 (mt, 2H : CH2 éthyle) ; 3,30 (mt, IH : OH en 2'); 3,52 (s, 3H : OCH3) ; 3,93 (mt, IH : H en 3) ; 4,19 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,20 et 4,36 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,64 (d large, J = 5,5 Hz, IH : H en 2') ; 4,86 (d large, J = 10 Hz, IH : H en 5) ; 5,22 (mt, IH : H en 3') ; 5,30 (d, J = 10 Hz, IH : CONH) ; 5,51 (dd, J = 10 et 7,5 Hz, IH : H en 7) ; 5,75 (d, J = 7 Hz, IH : H en 2) ; 6,20 (mt, IH : H en 13) ; 6,71 (s, IH : H en 10) ; de 7,30 à 7,45 (mt, 5H : H
aromatiques en 3') ; 7,52 (t, J = 7.5 Hz, 2H : OCOC6H5 H en meta) ; 7,64 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,13 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le tert-butoxycarbonyl-3 (méthoxy-4 phenyl) -2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R.4S.5R) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxy- acétoxy-lOβ oxo-9 propanoyloxy-4α trifluorOméthanesulfonyloxy-7β taxène-11 yle-13α peut être préparé de la manière suivante :
A une solution de 0,590 g de benzoyloxy-2α dihydroxy-lβ,13 époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α trifluorométhanesulfonyloxy-7β taxène-11 dans 10 cm3 d'acétate d'éthyle anhydre, on ajoute successivement 0,463 g d'acide tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine-1,3 carboxylique-5 (2R.4S.5R), 0,319 g de dicyclohexylcaiixxJiimide et 0,028 g de 4-diméthylamino-pyridine. Le mélange réactionnel est agité pendant 15 heures, sous atmosphère d'argon, à une température voisine de 20°C, puis additionné de 75 cm3 de dichlorométhane et 50 cm3 d'une solution aqueuse saturée de chlorure d'ammonium. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,980 g que l'on purifie par chromatographie sur 150 g de silice (0,063-0,2 mm) contenus dans une colonne de 3 cm de diamètre (éluant : dichlorométhane-méthanol : 95-5 en volumes) en recueillant des fractions de 15 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7kPa) à 40°C. On obtient 0,740 g de tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R,4S,5R) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxy- acétoxy-lOβ oxo-9 propanoyloxy-4α trifluorOméthanesulfonyloxy-7β taxène-11 yle-13α sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz, CDC13, δ en ppm) : 1,06 (s, 12H : CH3 et C(CH3)3) ; 1,20 (s, 3H,: CH3) ; 1,27 (t, J = 7,5 Hz, 3H : CH3 éthyle) ; 1,67 (s, IH : 0H en 1) ; 1,71 (s, 3H : CH3) ; 1,83 (s, 3H : CH3) ; de 2,00 à 2,30 et 2,83 (2 mt, IH chacun : CH2 en 6) ; de 2,00 à 2,30 (mt, 2H : CH2 éthyle) ; 2,08 et 2,22 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,52 (s, 3H : OCH3) ; 3,82 (s, 3H : ArOCH-) ; 3,82 (mt, IH : H en 3) ; 4,12 et 4,29 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,18 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,51 (d, J = 5 Hz, IH : H en 2') ; 4,80 (d large, J = 10 Hz, IH : H 5) ; de 5,35 à 5,45 (mt, IH : H en 3') ; 5,43 (dd, J = 10,5 et 7,5 Hz, IH : H en 7) ; 5,68 (d, J = 7 Hz, IH : H en 2) ; 6,01 (mt, IH : H en 13) ; 6,38 (mt,
IH: H en 5') ; 6,60 (s, IH : H en 10) ; 6,92 (d, J = 8.5 Hz, 2H : H aromatiques en ortho du OCH3) ; 7,39 (d, J = 8,5 Hz, 2H : H aromatiques en meta du OCH3) ; de 7,30 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,50 (t, J ≈ 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,65 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,03 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le benzoyloxy-2α dihyd_x.xy-lβ,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 propanoyloxy-4cc trifluoromémanesulfonyloxy-7β taxène-11 peut être préparé de la manière suivante :
A une solution de 0,660 g de benzoyloxy-2α époxy-5β,20 méthoxyacétoxy lOβ oxo-9 propanoyloxy-4α trihyd_Oxy-lβ,7β,13α taxène-11 dans 6,6 cm3 de dichlorométhane anhydre et 0,338 cm3 de pyridine, maintenue sous atmosphère d'argon, à une température voisine de 0°C, on ajoute goutte à goutte 0,354 cm3 d'anhydride trifluorométhanesulfonique. La solution orangée obtenue est agitée 10 minutes à une température voisine de 0°C, 30 minutes à une température voisine de 20°C, puis additionnée de 3 cm3 d'eau et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,800 g que l'on purifie par chromatographie sur 100 g de silice (0,063-0,2 mm) contenus dans une colonne de 2 cm de diamètre (éluant : dichlorométhane-méthanol : 95-5 en volumes) en recueillant des fractions de 15 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,591 g de benzoyloxy-2α d__hydroxy-lβ,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 propanoyloxy-4α trifluorométhanesulfonyloxy-7β taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. ÏH (400 MHz, CDC13, δ en ppm) : 1,05 (s, 3H : CH3) ; 1,19 (s, 3H : CH3) ; 1,23 (t, J = 7,5 Hz, 3H : CH3 éthyle) ; 1,62 (s, IH : 0H en 1) ; 1,89 (s, 3H: CH3) ; 2,12 (d, J = 5 Hz, IH : OH en 13) ; 2,24 et 2,90 (2 mts, IH chacun : CH2 en 6) ; 2,25 (s, 3H : CH3) ; 2,30 (AB limite, 2H : CH2 en 14) ; 2,64 (mt, 2H : CH2 éthyle) ; 3,52 (s, 3H : OCH3) ; 4,02 (d, J,= 7 Hz, IH : H en 3) ; 4,15 et 4,35 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,20 (AB limite, J = 16 Hz, 2H : OCOCH-O) ; 4,85 (mt, IH : H en 13) ; 4,91 (d large, J = 10 Hz, IH : H en 5) ; 5,57 (dd, J = 10 et 7 Hz, IH : H en 7) ; 5,69 (d, J = 7 Hz, IH : H en 2) ; 6,73 (s, IH : H en 10) ; 7,50 (t, J = 7.5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,11 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le benzoyloxy-2α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 propanoyloxy- Aa trihydroxy-lβ,7β,13 taxène-11 peut être préparé de la manière suivante :
A une solution de 1,21 g de benzoyloxy-2 ditriéthylsilyloxy-7β,13 époxy- 5β,20 hydroxy-lβ méthoxyacétoxy lOβ oxo-9 propanoyloxy-4α taxène-11 dans 15 cm3 de dichlorométhane, on ajoute, à une température voisine de 20°C, 23 cm3 de complexe triéthylamine-acide fluorhydrique. Le mélange réactionnel est agité pendant 20 heures à une température voisine de 20°C puis on ajoute 50 cm3 de dichlorométhane et 100 cm3 d'une solution aqueuse saturée d'hydrogénocarbonate de sodium. La phase organique est décantée, lavée par 2 fois 50 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1,04 g de benzoyloxy-2α époxy-5β,20 méthoxyacétyl-lOβ oxo-9 propanoyloxy-4 trihydroxy- lβ,7β,13α taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. ÏH (400 MHz, CDC13, δ en ppm) : 1,11 (s, 6H : CH3) ; 1,25 (t, J = 7,5 Hz, 3H : CH3 éthyle) ; 1,65 (s, IH : 0H en 1) ; 1,70 (s, 3H : CH3) ; 1,88 et 2,60 (2 mts, IH chacun : CH2 en 6) ; 2,08 (s, 3H : CHj) ; 2,30 (AB limite, 2H : CH2 en 14) ; 2,39 (d, J = 4 Hz, IH : OH en 7) ; 2,63 (mt, 2H : CH2 éthyle) ; 3,55 (s, 3H : OCH3) ; 3,90 (d, J = 7 Hz, IH : H en 3) ; 4,17 et 4,32 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,25 (AB Umite, J = 16 Hz, 2H : OCOCH2O) ; 4,51 (mt, IH : H en 7) ; 4,89 (mt, IH : H en 13) ; 4,95 (d large, J = 10 Hz, IH : H en 5) ; 5,64 (d, J = 7 Hz, IH : H en 2) ; 6,43 (s, IH : H en 10) ; 7,48 (t, J = 8 Hz, 2H : OCOC6H5 H en meta) ; 7,61 (t, J = 8 Hz, IH : OCOC6H5 H en para) ; 8,13 (d, J = 8 Hz, 2H : OCOC6H5 H en ortho).
Le benzoyloxy-2α ditriéthylsilyloxy-7β,13α époxy-5β,20 hydroxy-lβ méthoxyacétoxyl-lOβ oxo-9 propanoyloxy-4α taxène-11 peut être préparé de la manière suivante :
A une solution de 0,900 g de benzoyloxy-2α dihydroxy-lβ.lOβ bis(triéthylsilyloxy)-7β,13α époxy-5β,20 oxo-9 propanoyloxy-4α taxène-11 dans 15 cm3 de pyridine, on ajoute 0,520 cm3 de chlorure de méthoxyacétyle à une température voisine de 0°C. Le mélange réactionnel est agité pendant 2 heures à une température voisine de 20°C puis on ajoute 100 cm3 de dichlorométhane et 50 cm3 d'une solution aqueuse saturée de chlorure d'ammonium. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure d'ammonium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1,3 g que l'on purifie par
chromatographie sur 150 g de silice (0,063-0,2 mm) contenus dans une colonne de 2,5 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 25-75 en volumes) en recueillant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,780 g de benzoyloxy-2α bis(triéthyls_lyloxy)-7β,13α époxy-5β,20 hydroxy-lβ méthoxyacétoxy- lOβ oxo-9 propanoyloxy-4α taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. H (400 MHz, CDC13, δ en ppm) : de 0,50 à 0,70 (mt, 12 H : CH2 éthyle) ; 0,92 (t, J = 7,5 Hz, 9H : CH3 éthyle) ; 1,00 (t, J = 7.5 Hz, 9H : CH3 éthyle) ; 1,10 (s, 3H : CH3) ; 1,17 (s, 3H : CH3) ; 1,29 (t, J = 7,5 Hz, 3H : CH3 éthyle en 4) ; 1,61 (s, IH : 0H en 1) ; 1,68 (s, 3H : CH3) ; 1,84 et 2,51 (2 mts, IH chacun CH2 en 6) ; 2,09 et 2,21 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,10 (s, 3H CH3) ; 2,60 (mt, 2H : CH2 éthyle en 4) ; 3,50 (s, 3H : OCH3) ; 3,78 (d, J = 7 Hz, IH H en 3) ; 4,12 et 4,30 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,15 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,49 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,90 (mt, 2H : H en 5 et H en 13) ; 5,62 (d, J = 7 Hz, IH : H en 2) ; 6,52 (s, IH : H en 10) ; 7,45 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,58 (t, J = 7.5 Hz, IH : OCOC6H5 H en para) ; 8,09 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le benzoyloxy-2 dihydroxy-lβ.lOβ bis(ditriéthylsilyloxy)-7β,13 époxy- 5β,20 oxo-9 propanoyloxy-4α taxène-11 peut être préparé de la manière suivante :
A une solution de 1,105 g de carbonate- lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α taxène-11 dans 50 cm3 de tétrahydrofurane anhydride, on ajoute 1.8 cm3 d'une solution 1M de phényllithium dans le tétrahydrofurane à une température voisine de -78°C. Le mélange réactionnel est agité pendant 15 minutes à une température voisine de -78°C puis on ajoute 10 cm3 d'une solution aqueuse saturée de chlorure d'ammonium. A une température voisine de 20°C, on ajoute 20 cm3 d'une solution aqueuse saturée de chlorure d'ammonium et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 10 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1,3 g que l'on purifie par chromatographie sur 150 g de silice (0,063-0,2 mm) contenus dans une colonne de 5 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 10-90 en volumes) en recueillant des fractions de 18 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,840 g de benzoyloxy-2α dihydroxy-
lβ,10β bis(triéthylsilyloxy)-7β,13α époxy-5β,20 oxo-9 propanoyloxy-4α taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz, CDC13, δ en ppm) : 0,53 (mt, 6 H : CH2 éthyle) ; 0,65 (mt, 6 H : CH2 éthyle) ; 0,92 (t, J = 7,5 Hz, 9H : CH3 éthyle) ; 1,00 (t, J = 7,5 Hz, 9H : CH3 éthyle) ; 1,07 (s, 3H : CH3) ; 1,14 (s, 3H : CH3) ; 1,26 (t, J = 7,5 Hz, 3H : CH3 éthyle en 4) ; 1,40 (s, IH : 0H en 1) ; 1,71 (s, 3H : CH3) ; 1,88 et 2,45 (2 mis, IH chacun : CH2 en 6) ; 2,00 (s, 3H : CH-) ; 2,06 et 2,18 (2 dd, J = 16 et 9 Hz, IH chacun: CH2 en 14) ; 2,60 (q, J = 7.5 Hz, 2H : CH2 éthyle en 4) ; 3,84 (d, J = 7 Hz, IH : H en 3) ; 4,14 et 4,30 (2d, J = 8,5 Hz, IH chacun : CH2 en 20) ; 4,26 (d, J = 0,5 Hz, IH : OH en 10) ; 4,40 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,90 (d large, J = 10 Hz, IH : H en 5) ; 4,94 (t large, J = 9 Hz, IH : H en 13) ; 5,12 (d, J = 0,5 Hz, IH : H en 10) ; 5,58 (d, J = 7 Hz, IH : H en 2) ; 7,45 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,60 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,09 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho) .
Le carbonate- lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 méthoxy¬ acétoxy- lOβ oxo-9 propanoyloxy-4α taxène-11 peut être préparé de la manière suivante :
A une solution de 2,0 g de carbonate-lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy-4α méthoxyacétoxy lOβ oxo-9 taxène-11 dans 90 cm3 de dichlorométhane, on ajoute 3,37 g de 4-dimémylaminopyridine et 3,64 cm3 d'anhydride propionique. Le milieu réactionnel est chauffé à une température voisine de 42°C pendant 8 heures. On ajoute 50 cm3 d'une solution aqueuse saturée de chlorure de sodium et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 2,6 g que l'on purifie par chromatographie sur 100 g de silice (0,063-0,2 mm) contenus dans une colonne de 3 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 5-95 en volumes) en recueillant des fractions de 12 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1,97 g de carbonate- lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 méthoxyacétoxy lOβ oxo-9 propanoyl- oxy-4 taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. ÏH (400 MHz, CDC13, δ en ppm) : de 0,50 à 0,75 (mt, 12H : CH2 éthyl) ; 0,94 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,03 (t, J = 7,5 Hz, 9H : CH3 éthyl); 1,21 (mt, 6H : CH3 et CH3 éthyl) ; 1,28 (s, 3H : CH3) ;1,75 (s, 3H : CH3) ; 1,90 et 2,60 (2 mts, IH chacun CH2 en 6) ; 2,13 (s, 3H : CH3) ; 2,15 et 2,38 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,43 (mt, 2H : CH2 éthyl) ; 3,43 (d, J = 5,5 Hz, IH : H en 3) ; 3,51 (s, 3H : OCH3) ; 4,18 (s, 2H : OCOCH2O) ; 4,46 (dd, J =11 et 7 Hz, IH : H en 7) ; 4,48 et 4,65 (2d, J = 9Hz, 2H : CH2 en 20) ; 4,51 (d, J = 5,5 Hz, IH : H en 2) ; 4,93 (d large, J = 10Hz, IH : H en 5) ; 5,02 (t, J = 9 Hz, IH : H en 13) ; 6,51 (s, IH : H en 10). Le carbonate- lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy-4 méthoxyacétoxy-lOβ oxo-9 taxène-11 peut être préparé de la manière suivante:
A une solution de 4,12 g de carbonate- lβ,2 dihydroxy-4 ,10β bis(triéthylsilylo__y)-7β,13α époxy-5β,20 oxo-9 taxène-11 dans 80 cm3 de pyridine, on ajoute, sous agitation et à une température voisine de 0°C, 2 g de tamis moléculaire 4Â en poudre et 2,86 cm3 de chlorure de méthoxyacétyle. Le mélange réactionnel est agité pendant 15 minutes à une température voisine de 0°C puis on laisse remonter doucement la température du milieu réactionnel à une température voisine de 20°C. Après 4 heures d'agitation à une température voisine de 20°C, on ajoute 50 cm3 d'une solution aqueuse saturée de chlorure d'ammonium et 100 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure d'ammonium, 2 fois 25 cm3 d'une solution aqueuse saturée de sulfate de cuivre et 2 fois 25 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 5,3 g que l'on purifie par chromatographie sur 200 g de silice (0,063-0,2 mm) contenus dans une colonne de 4 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 25-75 en volumes) en recueillant des fractions de 12 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 4,21 g de carbonate-lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy-4α méthoxyacétoxy-lOβ oxo-9 taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. *H (400 MHz, CDC13, δ en ppm) : 0,59 (mt, 6H : CH2 éthyl) ; 0,73 (mt, 6H : CH2 éthyl) ; 0,91 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,02 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,15 (s, 3H : CH3) ; 1,18 (s, 3H : CH3) ;1,65 (s, 3H : CH3) ; 1,98 et 2,51 (2 mts, IH chacun : CH2 en 6) ; 2,15 (s, 3H : CH3) ; 2,54 et 2,72 (2 dd,
respectivement J = 16 et 9 Hz et J = 16 et 3 Hz, IH chacun : CH2 en 14) ; 2,93 (s, IH: OH en 4) ; 3,03 (d, J = 5 Hz, IH : H en 3) ; 3,51 (s, 3H : OCH3) ; 4,16 (mt, IH : H en 7) ; 4,17 (AB, J = 18 Hz, 2H : OCOCH2O) ; 4,37 (d, J = 5 Hz, IH : H en 2) ; 4,54 (AB, J = 9 Hz, 2H : CH2 en 20) ; 4,76 (d large, J = 10 Hz, IH : H en 5) ; 4,81 (dd, J = 9 et 3 Hz, IH : H en 13) ; 6,51 (s, lH : H en l0).
Le carbonate- lβ,2α dihydroxy-4α,10β bis(triéthylsilyloxy)-7β,13α époxy- 5β,20 oxo-9 taxène-11 peut être préparé de la manière suivante :
A une solution de 0,400 g de bis(triéthylsilyloxy)-7β,13α époxy-5β,20 oxo-9 tétrahydroxy-lβ,2 ,4α,10β taxène-11 dans 10 cm3 de dichlorométhane, on ajoute, sous agitation et à une température voisine de -78°C, 1 cm3 de pyridine et 0,560 g de triphosgène. Le mélange réactionnel est agité pendant 2 heures à une température voisine de -78°C puis on laisse remonter doucement le milieu réactionnel à une température voisine de 20°C. On ajoute 30 cm3 d'une solution aqueuse saturée de chlorure d'ammonium et 20 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,400 g d'une meringue jaune que l'on purifie par chromatographie sur 25 g de silice (0,063-0,2 mm) contenus dans une colonne de
2 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 20-80 en volumes) en recueillant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,330 g de carbonate- lβ,2α dihydroxy-4α,10β bis(triéthylsilyloxy)-7β,13α époxy- 5β,20 oxo-9 taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. !H (400 MHz, CDC13, δ en ppm) : 0,54 (mt, 6H : CH2 éthyl) ; 0,63 (mt, 6H : CH2 éthyl) ; 0,92 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,03 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,11 (s, 3H : CH3) ; 1,19 (s, 3H : CH3) ; 1,72 (s, 3H : CH3) ; 1,98 et 2,46 (2 mts, IH chacun : CH2 en 6) ; 2,06 (s, 3H : CH3) ; 2,55 et 2,66 (2 dd, respectivement J = 16 et 9 Hz et J = 16 et 3 Hz, IH chacun : CH2 en 14) ; 3,00 (s, IH: OH en 4) ; 3,13 (d, J = 5 Hz, IH : H en 3) ; 4,06 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,20 (d, J = 2,5 Hz, IH : OH en 10) ; 4,33 (d, J = 5 Hz, IH : H en 2) ; 4,55 (AB, J = 9 Hz, 2H : CH2 en 20) ; 4,76 (d large, J = 10Hz, IH : H en 5) ; 4,82 (dd, J = 9 et
3 Hz, IH : H en 13) ; 5,19 (d, J = 2,5 Hz, IH : H en 10).
Le bis(triéthylsilyloxy)-7β,13 éρoxy-5β,20 oxo-9 tétrahydroxy-lβ,2α,4α, lOβ taxène-11 peut être préparé de la manière suivante :
A une solution de 3,80 g de époxy-5β,20 oxo-9 pentahydroxy-lβ,2α,4α, 10β,13 triéthylsilyloxy-7β taxène-11 dans 100 cm3 de dichlorométhane, on ajoute, sous agitation et à une température voisine de 0°C, 1,20 cm3 de pyridine et 2,48 cm3 de chlorotriéthylsilane. Le mélange réactionnel est agité pendant 3 heures à une température voisine de 0°C. On ajoute 100 cm3 d'une solution aqueuse saturée de chlorure de sodium. La phase organique est décantée, lavée par 2 fois 100 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 5,34 g d'une huile orangée que l'on purifie par chromatographie sur 300 g de silice (0,063- 0,2 mm) contenus dans une colonne de 3 cm de diamètre (éluant : acétate d'éthyle- cyclohexane : 25-75 en volumes) en recueillant des fractions de 40 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 4,18 g de bis(triéthylsilyloxy)-7β,13α époxy- 5β,20 oxo-9 tétrahydroxy-lβ,2α,4α,10β taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. *H (400 MHz, CDC13, δ en ppm) : 0,53 (mt, 6H : CH2 éthyl) ; 0,75 (mt, 6H : CH2 éthyl) ; 0,91 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,01 (s, 3H : CH3) ; 1,03 (t, J = 7,5 Hz, 9H : CH3 éthyl) ; 1,09 (s, 3H : CH3) ; 1,63 (s, 3H : CH3) ; 1,97 (s, 3H : CH3) ; de 1,95 à 2,10 et 2,40 (2 mts, 2H chacun : CH2 en 14 et CH2 en 6) ; 3,17 (s, IH : OH) ; 3,18 (d, J = 5,5 Hz, IH : H en 3) ; 3,43 (d, J = 10 Hz, IH : OH en 2) ; 3,76 (dd, J = 10 et 5,5 Hz, IH : H en 2); 3,96 (dd, J = 11 et 6 Hz, IH : H en 7) ; 4,10 (s, IH : OH); 4,18 (d, J = 3 Hz, IH : OH en 10) ; 4,44 et 4,73 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,64 (d large, J = 10Hz, IH : H en 5) ; 4,74 (mt, IH : H en 13); 5,14 (d, J = 3 Hz, IH : H en 10).
EXEMPLE 2
A une solution de 20,5 mg de tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy- lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α trifluorométhanesulfonyloxy-7β taxène-11 yle 13 dans 0,2 cm3 d'acétonitrile et 0,025 cm3 de tétrahydrofurane, on ajoute 45 mg de chlorure de sodium et une spatule de tamis moléculaire activé 4À. Le mélange obtenu est porté au reflux, sous atmosphère d'argon, pendant 2 heures. Après refroidissement à une température voisine de 20°C, les solvants sont évaporés sous pression réduite (0,27 kPa) à une température voisine de 40°C, le résidu solide est repris avec 5 cm3 de dichlorométhane, filtré sur coton et rincé par 5 cm3 d'un
mélange acétate d'éthyle-dichlorométhane (50-50 en volumes). Les phases organiques sont concentrées sous pression réduite (0,27 kPa) à une température voisine de 40°C. On obtient ainsi 17,1 mg d'une meringue jaune que l'on purifie par chromatographie préparative sur couche mince [2 plaques préparatives Merck, Kieselgel 60F254, épaisseur 0,25 mm, dépôt en solution dans le dichlorométhane, éluant :' mélange méthanol-dichloro-méthane (6-94 en volumes)]. Après élution de la zone correspondant au produit principal par un mélange méthanol-dichlorométhane (10-90 en volumes), filtration sur verre fritte, puis évaporation des solvants sous pression réduite (0,27 kPa) à une température voisine de 40°C, on obtient 10,0 mg de tert- butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy- lOβ méthylène-7,8β oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α nor-19 taxène-11 yle-13 sous forme d'une laque blanche dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (400 MHz, CDCI3, δ en ppm) : 1,18 (t, J = 7,5 Hz, 3H : CH3 éthyle) ; 1,22 (s, 6H : CH3) ; 1,32 (s, 9H : C(CH3)3) ; 1.41 (mt, IH : H en 7); 1,69 et 2,23 (2 mts, IH chacun : CH2 en 19) ; 1,81 (s, IH : 0H en 1) ; 1,85 (s, 3H : CH3) ; 2,12 et 2,50 (respectivement d et dt, J = 16 et J = 16 et 4,5 Hz, IH chacun : CH2 en 6) ; 2,25 et 2,39 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,63 (mt, 2H : CH2 éthyle) ; 3,23 (mt, IH : OH en 2') ; 3,52 (s, 3H : OCH3) ; 4,03 (d, J = 7 Hz, IH : H en 3) ; 4,12 et 4,44 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,20 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,62 (mt, IH : H en 2') ; 4,70 (d, J= 4 Hz, IH : H en 5) ; 5,22 (mt, IH : H en 3') ; 5,28 (d, J =10 Hz, IH : CONH) ; 5,58 (d, J = 7 Hz. IH : H en 2) ; 6,23 (t large, J = 9 Hz, IH : H en 13) ; 6,41 (s, IH : H en 10) ; 7,18 (dd, J = 5 et 3,5 Hz, IH : H en 4 du thénoyle-2) ; de 7,30 à 7,50 (mt, 5H : H aromatiques en 3') ; 7,67 (d large, J = 5 Hz, IH : H en 5 du thénoyle-2) ; 7,96 (d large, J = 3,5 Hz, IH : H en 5 du thénoyle-2).
Le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4 (thénoyloxy-2)-2α trifluorométhanesulfonyloxy-7β taxène-11 yle-13α peut être préparé de la manière suivante :
Une solution de 75 mg de tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine-1,3 carboxylate-5 (2R.4S.5R) d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α trifluorométhane- sulfonyloxy-7β taxène-11 yle-13α dans 0,77 cm3 d'une solution d'acide chlorhydrique 0,1N dans l'éthanol est agitée à une température voisine de 5°C pendant 2 heures. Le
mélange réactionnel est ensuite dilué avec 10 cm3 de dichlorométhane, lavé par 2 fois 1 cm3 d'eau distiUée. Après extraction de la phase aqueuse par 1 cm3 de dichlorométhane, les phases organiques sont rassemblées, séchées sur sulfate de magnésium, filtrées sur verre fritte et concentrées sous pression réduite (0,27 kPa) à une température voisine de 40°C. On obtient ainsi 74,4 mg d'une laque jaune que l'on purifie par chromatographie à pression atmosphérique sur 8 g de silice (0,063- 0,2 mm) contenus dans une colonne de 1,5 cm de diamètre (gradient d'élution : acétate d'éthyle-dichlorométhane de 5-95 à 20-80 en volumes) en recueiUant des fractions de 8 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (0,27 kPa) à 40°C pendant 2 heures. On obtient ainsi 56,3 mg de tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate- (2R.3S) d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4 (thénoyloxy-2)-2α trifluorométhanesulfonyloxy-7β taxène-11 yle-13 sous forme d'une meringue jaune pâle dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (400 MHz, CDC13, δ en ppm) : 1,20 (s, 6H : CH3) ; 1,22 (t, J = 7.5 Hz, 3H : CH3 éthyle) ; 1,36 (s, 9H : C(CH3)3) ; 1,71 (s, IH,: 0H en 1) ; 1,89 (s, 3H : CH3) ; 2,05 (s, 3H : CH3) ; 2,25 et 2,86 (2 mts, IH chacun : CH2 en 6) ; 2,33 (d, J = 9 Hz, 2H : CH2 en 14) ; 2,66 (mt, 2H : CH2 éthyle) ; 3,28 (d, J = 5 Hz, IH : OH en 2') ; 3,52 (s, 3H : OCH3) ; 3.90 (d, J = 7 Hz, IH : H en 3) ; 4,20 (AB Umite, J = 16 Hz, 2H : OCOCH2O) ; 4,27 et 4,50 (2d, J= 9 Hz, IH chacun : CH2 en 20) ; 4,61 (mt, IH : H en 2') ; 4,88 (d large, J = 10 Hz, IH : H en 5) ; 5,20 (d large, J =10 Hz, IH : H en 3') ; 5,30 (d, J = 10 Hz, IH : CONH) ; 5,50 (dd, J = 10 et 7 Hz, IH : H en 7) ; 5,65 (d, J = 7 Hz. IH : H en 2) ; 6.18 (t large, J = 9 Hz, IH : H en 13) ; 6,70 (s, IH : H en 10) ; 7,18 (dd, J = 5 et 3,5 Hz, IH : H en 4 du thénoyle-2) ; de 7,30 à 7,50 (mt, 5H : H aromatiques en 3') ; 7,69 (dd, J= 5 et 1,5 Hz, IH : H en 5 du thénoyle-2) ; 7,92 (dd, J = 3,5 et 1,5 Hz, IH : H en 5 du thénoyle-2).
Le tert-butoxycarbonyl-3 (méthoxy-4 phenyl) -2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R.4S.5R) d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α trifluorométhanesulfonylo>_y-7β taxène-11 yle-13α peut être préparé de la manière suivante :
A une solution de 55,2 mg d'époxy-5β,20 dihydroxy-lβ,13α méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α trifluorométhane- sulfonyloxy-7β taxène-11 dans 0,1 cm3 de toluène anhydre, on ajoute successivement 41 mg d'acide tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine- 1,3 carboxyUque-5 (2R.4S.5R), 26 mg de dicyclohexylcarbodiimide, et 3 mg de
N,N-diméthylamino-4 pyridine. Le mélange réactionnel est agité pendant 2 heures, sous atmosphère d'argon, à une température voisine de 20°C, puis déposé sur une colonne de chromatographie à pression atmosphérique (15 g de siUce (0,063-0,2 mm) contenus dans une colonne de 1,5 cm de diamètre (gradient d'élution : acétate d'éthyle-dichlorométhane de 5-95 à 10-90 en volumes) en recueiUant des fractions de 10 cm3). Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (0,27 kPa) à 40°C pendant 2 heures. On obtient ainsi 75,3 mg de tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazoUdine-1,3 carboxylate-5 (2R.4S.5R) d'époxy-5β,20 hydroxy-lβ méthoxy- acétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α trifluorométhanesulfonyl- oxy-7β taxène-11 yle-13α sous forme d'une meringue blanche dont les caracté¬ ristiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz, CDCI3, δ en ppm) : 1,04 (s, 9H : C(CH )3) ; 1,04 (t, J = 7.5 Hz, 3H : CH3 éthyle) ; 1.14 (s, 3H : CH3) ; 1.16 (s, 3H : CH3) ; 1,61 (s, IH : 0H en 1) ; 1,68 (s, 3H : CH3) ; 1,81 (s, 3H : CH3) ; de 2.00 à 2,30 (mt, 4H : CH2 éthyle et CH2 en 14) ; 2,03 et 2,80 (2 mts, IH chacun : CH2 en 6) ; 3,50 (s, 3H: OCH3) ; 3,77 (d, J = 7 Hz, IH : H en 3) ; 3,81 (s, 3H : ArOCH3) ; 4,13 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,18 et 4,39 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,48 (d, J = 4 Hz, IH : H en 2') ; 4,78 (d large, J = 10 Hz, IH : H en 5) ; de 5,35 à 5,50 (mt, 2H : H en 3" et H en 7) ; 5,55 (d, J = 7 Hz, IH : H en 2) ; 5,96 (t large, J = 9 Hz, IH : H en 13) ; 6,34 (mt, IH : H en 5') ; 6,56 (s, IH : H en 10) ; 6,88 (d, J = 8 Hz, 2H : H aromatiques en ortho du OCH3) ; 7,13 (dd, J = 5 et 3,5 Hz, IH : H en 4 du thénoyle-2) ; de 7,30 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,36 (d, J = 8 Hz, 2H: H aromatiques en meta du OCH3) ; 7,62 (d large, J = 5 Hz, IH : H en 5 du thénoyle- 2) ; 7,80 (d large, J = 3,5 Hz, IH : H en 5 du thénoyle-2).
L'époxy-5β,20 dihydroxy-lβ,13α méthoxyacétoxy- lOβ oxo-9 propanoyloxy- Λa (thénoyloxy-2)-2α trifluorométhanesulfonyloxy-7β taxène-11 peut être préparé de la manière suivante :
A une solution de 50 mg d'époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α trihydrOxy-lβ,7β,13α taxène-11 dans 0,5 cm3 de dichlorométhane anhydre et 0,0255 cm3 de pyridine, maintenue sous atmosphère d'argon, à une température voisine de 0°C, on ajoute goutte à goutte 0,0265 cm3 d'anhydride trifluorométhanesulfonique. La solution orangée obtenue est agitée 10 minutes à une température voisine de 0°C, 45 minutes à une température voisine de 20°C, puis additionnée de 0,1 cm3 d'un mélange méthanol/dichlorométhane (5/95 en
volumes). La solution est déposée sur une colonne de chromatographie à pression atmosphérique (10 g de silice (0,063-0,2 mm) contenus dans une colonne de 1,5 cm de diamètre (gradient d'élution : méthanol-dichlorométhane de 2-98 à 5-95 en volumes) en recueiUant des fractions de 8 cm3). Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (0,27 kPa) à 40°C pendant 2 heures. On obtient ainsi 55,2 mg d'époxy-5β,20 dihydroxy-lβ,13α méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2 trifluorométhane- sulfonyloxy-7β taxène-11 sous forme d'une meringue blanche.
L'époxy-5β,20 trihydroxy-lβ,7β,13 méthoxyacétoxy-lOβ oxo-9 propanoyl- oxy-4α (thénoyloxy-2)-2α taxène-11 peut être préparé de la manière suivante :
A une solution de 0,302 g d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α bis(triéthylsilyloxy)-7β,13 taxène-11 dans 5 cm3 de dichlorométhane, on ajoute, à une température voisine de 20°C, 6 cm3 de complexe triéthylamine-acide fluorhydrique (Et3N.3HF). Le mélange réactionnel est agité pendant 24 heures à une température voisine de 20°C puis on ajoute 50 cm3 de dichlorométhane et 100 cm3 d'une solution aqueuse saturée en hydrogéno- carbonate de sodium. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7kPa) à 40°C. On obtient ainsi 0,24 g d'époxy-5β,20 trihydroxy-lβ,7β,13α méthoxyacétoxy-lOβ oxo-9 propanoyl- oxy-4α (thénoyloxy-2)-2α taxène-11 sous forme d'une meringue blanche dont les caractéristiques sont les suivantes :
- spectre de R.M.N. ^ (400 MHz, CDCI3, δ en ppm) : 1,07 (s, 3H : CH3) ; 1,10 (s, 3H : CH3) ; 1,22 (t. J = 7.5 Hz, 3H : CH3 éthyle) ; 1,62 (s, IH : OH en 1) ; 1,69 (s, 3H : CH3) ; 1,89 et 2,63 (2 mts, IH chacun : CH2 en 6) ; 2,03 (d, J = 5,5 Hz, IH : OH en 13) ; 2,07 (s, 3H : CH3) ; 2,27 (d, J = 9 Hz, 2H : CH2 en 14) ; 2.35 (d, J = 4.5 Hz, IH : OH en 7) ; 2,59 (mt, 2H : CH2 éthyle) ; 3,52 (s, 3H : OCH3) ; 3.84 (d. J = 7 Hz, IH : H en 3) ; 4,23 et 4,43 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,25 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,49 (mt, IH : H en 7) ; 4,87 (mt, IH : H en 13) ; 4,95 (d large, J = 10Hz, IH : H en 5) ; 5,53 (d, J = 7 Hz, IH : H en 2) ; 6,42 (s, IH : H en 10) ; 7,14 (dd, J = 4,5 et 3,5 Hz, IH : H en 4 du thénoyle-2) ; 7,61 (dd, J = 4,5 et 1,5 Hz, IH : H en 5 du thénoyle-2) ; 7,83 (dd, J = 3,5 et 1,5 Hz, IH : H en 3 du thénoyle-2).
L'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α bis(triéthylsilyloxy)-7β,13α taxène-11 peut être préparé de la manière suivante :
A une solution de 0,5 g d'époxy-5β,20 dihydroxy-lβ.lOβ oxo-9 propanoyl- oxy-4 (thénoyloxy-2)-2α bis(triéthylsUyloxy)-7β,13α taxène-11 dans 10 cm3 de pyridine, on ajoute 0,286 cm3 de chlorure de méthoxyacétyle à une température voisine de 0°C. Le mélange réactionnel est agité pendant 10 heures à une température voisine de 20°C puis on ajoute 100 cm3 de dichlorométhane et 50 cm3 d'une solution aqueuse saturée en chlorure d'ammonium. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée en chlorure d'ammonium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. Le résidu obtenu (0,6 g) est purifié par chromatographie sur 50 g de siUce (0,063-0,2 mm) contenus dans une colonne de 2 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 5-95 en volumes) en recueiUant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (0,27kPa) à 40°C. On obtient 0,320 g d'époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 propanoyloxy-4cc (thénoyloxy-2)-2α bis(triéthylsilyloxy)- 7β,13 taxène-11 sous forme d'une meringue blanche dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. *H (400 MHz, CDC13, δ en ppm) : de 0,50 à 0,70 (mt, 12 H,: CH2 éthyle) : 0,92 (t, J = 7,5 Hz, 9H : CH3 éthyle) ; 0,98 (t, J = 7,5 Hz, 9H : CH3 éthyle) ; 1,09 (s, 3H : CH3) ; 1,15 (s, 3H : CH3) ; 1,27 (t, J = 7,5 Hz, 3H : CH3 éthyle en 4) ; 1,59 (s, IH: OH en 1) ; 1,65 (s, 3H : CH3) ; 1,85 et 2,52 (2 mts, IH chacun CH2 en 6) ; 2,07 et 2,18 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,08 (s, 3H CH3) ; 2,58 (mt, 2H : CH2 éthyle en 4) ; 3,50 (s, 3H : OCHj) ; 3,73 (d, J = 7 Hz, IH H en 3) ; 4,13 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,20 et 4,41 (2d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,49 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,89 (t large, J = 9 Hz, IH : H en 13) ; 4,91 (d large, J = 10 Hz, IH : H en 5) ; 5,53 (d. J = 7 Hz, IH : H en 2) ; 6,51 (s, IH : H en 10) ; 7,12 (dd, J = 4,5 et 3 Hz, IH : H en 4 du thiénoyle-2) ; 7,61 (d, J = 4,5 Hz, IH: H en 5 du thiénoyle-2) ; 7,83 (d, J = 3 Hz, IH : H en 3 thiénoyle-2).
L'époxy-5β,20 dihydroxy-lβ,10β oxo-9 propanoyloxy-4α (thénoyloxy-2)-2 bis(triéthylsilyloxy)-7β,13α taxène-11 peut être préparé de la manière suivante :
A une solution de 0,5 g de carbonyldioxy-lβ,2α époxy-5β,20 méthoxy- acétoxy-lOβ oxo-9 propanoyloxy-4α bis(triéthylsilyloxy)-7β,13α taxène-11 dans
20 cm3 de tétrahydrofurane, sous atmosphère d'argon, à une température voisine de -78°C, on ajoute 1,5 cm3 d'une solution 1M de 2-thiényllithium dans le tétrahydrofurane. Le mélange réactionnel est agité pendant 35 minutes à une température voisine de -78°C puis on ajoute 1 cm3 d'une solution aqueuse saturée en chlorure d'ammonium. A une température voisine de 20°C, on ajoute 10 cm3 d'une solution aqueuse saturée en chlorure d'ammonium et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 10 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 0,65 g d'un solide que l'on purifie par chromatographie sur 90 g de siUce (0,063-0,2 mm) contenus dans une colonne de 1 cm de diamètre (éluant : acétate d'éthyle-cyclohexane : 10-90 en volumes) en recueillant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (0,27 kPa) à 40°C. On obtient 0,511 g d'époxy-5β,20 dihydroxy-lβ,10β oxo-9 propanoyloxy-4α (thénoyloxy-2)-2α bis(triéthyls_lyloxy)-7β,13α taxène-11 sous forme d'une meringue blanche dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. H (600 MHz, CDC13, δ en ppm) : 0,57 (mt, 6 H : CH2 éthyle) ; 0,68 (mt, 6 H : CH2 éthyle) ; 0,95 (t, J = 7,5 Hz, 9H : CH3 éthyle) ; 1,01 (t, J = 7.5 Hz, 9H : CH3 éthyle) ; 1,07 (s, 3H : CH3) ; 1.17 (s, 3H : CH3) ; 1,27 (t. J = 7,5 Hz, 3H : CH3 éthyle en 4) ; 1.73 (s, 3H : CH3) ; 1,90 et 2,47 (2 mts, IH chacun : CH2 en 6) ; 2,02 (s, 3H : CH3) ; 2,09 et 2.18 (2 dd, J = 16 et 9 Hz. IH chacun : CH2 en 14) ; 2.60 (mt, 2H : CH2 éthyle en 4) ; 3,82 (d, J = 7 Hz, IH : H en 3) ; 4,24 et 4,44 (2d, J = 9 Hz. IH chacun : CH2 en 20) ; 4,26 (d, J = 0,5 Hz, IH : OH en 10) ; 4,42 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,93 (d large, J = 10Hz, IH : H en 5) ; 4,97 (t large, J = 9 Hz, IH : H en 13) ; 5,13 (d, J = 0,5 Hz, IH : H en 10) ; 5,53 (d, J = 7 Hz, IH : H en 2) ; 7,15 (dd, J = 4,5 et 3 Hz, IH : H en 4 du thiénoyle-2) ; 7,63 (d, J = 4,5 Hz, IH: H en 5 du thénoyle-2) ; 7,85 (d, J = 3 Hz, IH : H en 3 du thiénoyle-2).
EXEMPLE 3
A une solution de 154 mg de tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α butanoyloxy-4α époxy-5β,20 hydroxy-lβ méthoxyacétoxy- lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dans 2 cm3 d'acétonitrile et 200 μl de tétrahydrofurane, on ajoute successivement 96 mg de tamis moléculaire 4Â en poudre, 225 mg de chlorure de sodium. Le mélange réactionnel est maintenu sous agitation à une température voisine de 75°C pendant
5 heures puis, à une température voisine de 20°C, additionné de 15 cm3 de dichlorométhane et 10 cm3 d'une solution aqueuse saturée de chlorure de sodium. La phase organique est décantée, lavée par 2 fois 20 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 133 mg que l'on purifie par chromatographie sur 80 g de silice (0,063-0,2 mm) contenus dans une colonne de 1 cm de diamètre en éluant avec un mélange dichlorométhane-méthanol (98-2 en volumes) et en recueiUant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 63 mg de tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α but__noyloxy-4α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ méthylène-7β,8 nor-19 oxo-9 taxène-11 yle-13α sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 0,92 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1,26 (s, 6H : CH3) ; 1,31 (s, 9H : C(CH3)3) ; 1,42 (mt, IH : H en 7) ; 1,71 et 2,26 (2 mts, IH chacun : CH2 en 19) ; de 1,60 à 1,85 (mt, 2H : CH2 du propyle) ; 1,86 (s, 3H : CH3) ; 1,88 (s, IH : OH en 1) ; 2,12 et 2,50 (respectivement d large et mt, J = 16 Hz, IH chacun : CH2 en 6) ; 2,23 et 2,39 (respectivement mt et dd, J = 16 et 9 Hz, 2H : CH2 en 14) ; 2,49 et 2,65 (2 mts, IH chacun : OCOCH2 du propyle) ; 3,25 (mt, IH : OH en 2') ; 3,51 (s, 3H : OCH3) ; 4,05 et 4,32 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,10 (d, J = 7 Hz, IH : H en 3) ; 4,16 et 4,22 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,62 (mt, IH : H en 2') ; 4,68 (d large, J = 4,5 Hz, IH H en 5) ; 5,25 (d large, J = 10 Hz, IH : H en 3') ; 5,30 (d, J = 10 Hz, IH : CONH) 5,65 (d, J = 7 Hz, IH : H en 2) ; 6,23 (t large, J = 9 Hz, IH : H en 13) ; 6,42 (s, IH H en 10) ; de 7,25 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,51 (t, J = 7,5 Hz, 2H OCOC6H5 H en meta) ; 7,62 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,16 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α butanoyloxy-4α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α peut être préparé de la manière suivante :
Une solution de 400 mg de tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R.4S.5R) de benzoyloxy-2α butanoyloxy-4 époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dans 6,4 cm3 d'une solution 0,1N d'éthanol chlorhydrique est
maintenue sous agitation à une température voisine de 0°C pendant 6 heures puis à une température voisine de 20°C pendant 15 heures. Le milieu réactionnel est concentré à sec sous pression réduite (2,7 kPa) à 20°C. Le produit brut de la réaction est dissous dans 20 cm3 de dichlorométhane et 10 cm3 d'une solution aqueuse saturée de bicarbonate de sodium. La phase aqueuse est séparée par décantation puis extraite par 2 fois 20 cm3 de dichlorométhane. Les phases organiques sont réunies, lavées par 30 cm3 d'eau distillée puis séchées sur sulfate de magnésium, filtrées et concentrées à sec sous pression réduite (2,7 kPa) à 20°C. On obtient 410 mg d'un produit que l'on purifie par chromatographie sur 60 g de siUce (0,063-0,2 mm) contenus dans une colonne de 1 cm de diamètre en éluant avec un mélange (dichlorométhane-méthanol 98,5-1,5 en volumes) et en recueiUant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 20°C. On obtient 307 mg de tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α butanoyloxy-4α époxy- 5β,20 hydroxy-lβ méthoxyacétoxy- lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13cc sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. *H (400 MHz ; CDC13 ; δ en ppm) : 0,93 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1,22 (s, 3H : CH3) ; 1,24 (s, 3H : CH3) ; 1,35 (s, 9H : C(CH3)3) ; de 1,65 à 1,85 (mt, 2H : CH2 du propyle) ; 1,74 (s, IH : OH en 1) ; 1,88 (s, 3H : CH3) ; 2,04 (s, 3H : CH3) ; 2,25 et 2,86 (2 mts, IH chacun : CH2 en 6) ; 2,33 (d, J = 9 Hz, 2H : CH2 en 14) ; 2,52 et 2,66 (2 mts, J = 14,5 et 6,5 Hz, IH chacun : OCOCH2 du propyle) ; 3,33 (d, J = 4 Hz, IH : OH en 2') ; 3,52 (s, 3H : OCH3) ; 3,94 (d, J = 7 Hz, IH : H en 3) ; 4,16 et 4,21 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,19 et 4,35 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,62 (mt, IH : H en 2') ; 4,86 (d large, J = 10 Hz, IH : H en 5) ; 5,22 (d large, J = 10 Hz, IH : H en 3') ; 5,33 (d, J = 10 Hz, IH : CONH) ; 5,50 (dd, J = 11 et 8 Hz, IH : H en 7) ; 5,73 (d, J = 7 Hz, IH : H en 2) ; 6,16 (t large, J = 9 Hz, IH : H en 13) ; 6,71 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 5H: H aromatiques en 3') ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,12 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho) .
Le tert-butoxycarbonyl-3 (méthoxy-4 phenyl) -2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R,4S,5R) de benzoyloxy-2α butanoyloxy-4α époxy-5β,20 hydroxy- lβ méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α peut être préparé de la manière suivante :
A une solution de 400 mg de benzoyloxy-2 butanoyloxy-4α dihydroxy- lβ,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 dans 10 cm3 d'acétate d'éthyle anhydre, on ajoute successivement 247 mg d'acide tert-butoxycarbonyl-3 (méthoxy-4 phenyl) -2 phényl-4 oxazolidine- 1,3 carboxyUque-5 (2R,4S,5R), 186 mg de dicyclohexylc_ιrt>cdiimide et 12,5 mg de 4-d-méΛylarninopyridine. Le mélange réactionnel est agité pendant 15 heures, sous atmosphère d'argon, à une température voisine de 20°C, puis concentré à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1 g d'un produit que l'on purifie par chromatographie sur 100 g de siUce (0,063-0,2 mm) contenus dans une colonne de 3 cm de diamètre en éluant avec un mélange dichlorométhane-méthanol (95-5 en volumes) et en recueillant des fractions de 12 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 410 mg de tert-butoxycarbonyl-3 (méthoxy-4 phenyl) -2 phényl-4 oxazoUdine-1,3 carboxylate-5 (2R,4S,5R) de benzoyloxy-2α butanoyloxy-4α époxy- 5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 tri_luorométhanesulfonyloxy-7β taxène-11 yle-13α sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. *H (400 MHz ; CDC13 ; δ en ppm) : 0,92 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1,07 (s, 9H : C(CH3)3) ; 1,17 (s, 6H : CH3) ; de 1,55 à 1,70 (mt, 3H : CH2 du propyle et OH en 1) ; 1,64 (s, 3H : CH3) ; 1,84 (s, 3H : CH3) ; 2,08 et de 2,15 à 2,30 (respectivement dd et mt, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; de 2,15 à 2,30 et 2,82 (2 mts, IH chacun : CH2 en 6) ; de 2,15 à 2,30 (mt, 2H : OCOCH2 du propyle) ; 3,51 (s, 3H : OCH3) ; 3,82 (s, 3H : ArOCH3) ; 3,83 (d, J = 7 Hz, IH : H en 3) ; 4,12 et 4,28 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,14 et 4,22 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,52 (d large, J = 4,5 Hz, IH : H en 2') ; 4,79 (d large, J = 10 Hz, IH : H en 5) ; de 5,35 à 5,50 (mt, IH : H en 3') ; 5,44 (dd, J = 9 et 7 Hz. IH : H en 7) ; 5,67 (d, J = 7 Hz, IH : H en 2) ; 5,99 (t large, J = 9 Hz, IH : H en 13) ; 6,40 (mf, IH : H en 5") ; 6,59 (s, IH : H en 10) ; 6,92 (d, J = 8.5 Hz, 2H : H aromatiques en ortho du OCH-) ; de 7,25 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,37 (d, J = 8,5 Hz, 2H : H aromatiques en meta du OCH3) ; 7,48 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t. J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,11 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le benzoyloxy-2α butanoyloxy-4α dihydroxy-lβ,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 peut être préparé de la manière suivante :
A une solution de 389 mg de benzoyloxy-2 butanoyloxy-4 époxy- 5β,20 méthoxyacétoxyl-lOβ oxo-9 trihydroxy-lβ,7β,13α taxène-11 dans 6 cm3 de dichlorométhane anhydre et 390 μl de pyridine, maintenue sous atmosphère d'argon, à une température voisine de 0°C, on ajoute goutte à goutte 410 μl d'anhydride trifluorométhanesulfonique. La solution orangée obtenue est agitée 15 minutes à une température voisine de 0°C puis additionnée de 3 cm3 d'eau et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 510 mg que l'on purifie par chromatographie sur 70 g de silice (0,063-0,2 mm) contenus dans une colonne de 1 cm de diamètre en éluant avec un mélange dichlorométhane- méthanol (95-5 en volumes) et en recueiUant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 410 mg de benzoyloxy-2 butanoyloxy-4 dihydroxy-lβ,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 trifluorométhane- sulfonyloxy-7β taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. H (400 MHz ; CDC13 ; δ en ppm) : 1,06 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1,06 (s, 3H : CH3) ; 1,20 (s, 3H : CH3) ; 1,63 (s, IH : OH en 1) ; 1,77 (mt, 2H : CH2 du propyle) ; 1,87 (s, 3H : CH3) ; 2,18 (d, J = 5 Hz, IH : OH en 13) ; de 2,15 à 2,40 (AB Umite, 2H : CH2 14) ; de 2,15 à 2,40 et 2,89 (2 mts, IH chacun : CH2 6) ; 2,25 (s, 3H : CH3) ; 2,59 (AB limite, J = 16 et 7.5 Hz, 2H : OCOCH2 du propyle) ; 3,51 (s, 3H : OCH3) ; 4,03 (d, J = 7 Hz, IH : H 3) ; 4,16 et 4,24 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,18 et 4,35 (2 d, J = 9 Hz, IH chacun : CH2 20) ; 4,85 (mt, IH : H 13) ; 4,92 (d large, J = 10 Hz, IH : H 5) ; 5,57 (dd, J = 10,5 et 7 Hz, IH : H 7) ; 5,68 (d, J = 7 Hz, IH : H 2) ; 6,73 (s, IH : H 10) ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H meta) ; 7.63 (t, J = 7,5 Hz, IH : OCOC6H5 H para) ; 8,10 (d, J = 7,5 Hz, 2H : OCOC6H5 H ortho).
Le benzoyloxy-2 butanoyloxy-4α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 trihydroxy- 1 β,7β, 13α taxène- 11 peut être préparé de la manière suivante :
A une solution de 580 mg de benzoyloxy-2α butanoyloxy-4α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 taxène-11 dans 5 cm3 de dichlorométhane, on ajoute, à une température voisine de 20°C, 5,5 cm3 de complexe triéthylamine-acide fluorhydrique. Le mélange réactionnel est agité pendant 23 heures à une température voisine de 20°C puis on ajoute 50 cm3
de dichlorométhane et 100 cm3 d'une solution aqueuse saturée d'hydrogénocarbonate de sodium. La phase organique est décantée, lavée par 2 fois 20 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 520 mg que l'on purifie par chromatographie sur 70 g de siUce (0,063-0,2 mm) contenus dans une colonne de 2 cm de diamètre en éluant avec un mélange méthanol-dichlorométhane (5-95 en volumes) et en recueillant des fractions de 10 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 389 mg de benzoyloxy-2α butanoyloxy-4α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 trihydroxy-lβ,7β,13α taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 1,05 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1,11 (s, 6H : CH3) ; 1,67 (s, 3H : CH3) ; 1,71 (s, IH : OH en 1) ; 1,75 (mt, 2H : CH2 du propyle) ; 1,85 et de 2,45 à 2,65 (2 mts, IH chacun : CH2 en 6) ; 2,05 (s, 3H : CH3) ; 2,24 (d, J = 5 Hz, IH : OH) ; 2,28 (AB limite, J = 16 et 9 Hz, 2H: CH2 en 14) ; 2,40 (d. J = 4 Hz, IH : OH) ; 2,56 (AB limite, 2H : OCOCH2 du propyle) ; 3,51 (s, 3H : OCH3) ; 3,88 (d, J = 7 Hz, IH : H en 3) ; 4,15 et 4,32 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,23 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,48 (mt, IH : H en 7) ; 4,86 (mt, IH : H en 13) ; 4,94 (d large, J = 10 Hz, IH : H en 5) ; 5,62 (d. J = 7 Hz. IH : H en 2) ; 6,43 (s, IH : H en 10) ; 7,49 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,62 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,12 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le benzoyloxy-2α butanoyloxy-4α bis(triéthylsilyloxy)-7β,13 époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 taxène-11 peut être préparé de la manière suivante :
A une solution de 906 mg de benzoyloxy-2 butanoyloxy-4α dihydroxy- lβ,10β bis(triéthylsilyloxy)-7β,13α époxy-5β,20 oxo-9 taxène-11 dans 18 cm3 de pyridine, on ajoute 1,03 cm3 de chlorure de méthoxyacétyle à une température voisine de 0°C. Le mélange réactionnel est agité pendant 14 heures à une température voisine de 20°C puis on ajoute 20 cm3 de dichlorométhane et 20 cm3 d'une solution aqueuse saturée de chlorure d'ammonium. La phase organique est décantée, lavée par 4 fois 20 cm3 d'une solution aqueuse saturée de sulfate de cuivre, 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure d'ammonium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 800 mg d'un produit que l'on purifie par chromatographie sur 100 g de siUce
(0,063-0,2 mm) contenus dans une colonne de 2,5 cm de diamètre en éluant avec un mélange méthanol-dichlorométhane (2-98 en volumes) et en recueiUant des fractions de 15 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 580 mg de benzoyloxy-2α butanoyloxy-4α bis(ditriéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy- lβ méthoxyacétoxy-lOβ oxo-9 taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. H (400 MHz ; CDC13 . δ en ppm) : 0,60 et 0,68 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,95 et 1,04 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,09 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1,13 (s, 3H : CH3) ; 1,18 (s, 3H : CHj) ; 1,64 (s, IH : OH enl) ; 1,68 (s, 3H : CH3) ; 1,84 (mt, 2H : CH2 du propyle) ; 1,89 et 2,50 (2 mts, IH chacun : CH2 en 6) ; 2,11 et 2,23 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,13 (s, 3H : CH3) ; 2,55 (mt, 2H : OCOCH2 du propyle) ; 3,53 (s, 3H : O CH3) ; 3,82 (d, J = 7 Hz, IH : H en 3) ; 4,13 et 4,31 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,16 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,52 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,91 (mt, IH : H en 13) ; 4,93 (d large, J = 10 Hz, IH : H en 5) ; 5,64 (d, J = 7 Hz, IH : H en 2) ; 6,54 (s, IH : H en 10) ; 7,47 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,61 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,11 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho). Le benzoyloxy-2 butanoyloxy-4α dihydroxy-lβ,10β bis(triéthylsilyloxy)-
7β,13α époxy-5β,20 oxo-9 taxène-11 peut être préparé de la manière suivante :
A une solution de 907 mg de butanoyloxy-4α carbonate-lβ,2 bis(triéthylsilyloxy)-7β,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 taxène-11 dans 50 cm3 de tétrahydrofurane anhydre, on ajoute 2,34 cm3 d'une solution 1M de phényUithium dans le tétrahydrofurane à une température voisine de -78°C. Le mélange réactionnel est agité pendant 1 heure à une température voisine de -78°C puis on ajoute 10 cm3 d'une solution aqueuse saturée de chlorure d'ammonium. A une température voisine de 20°C, on ajoute 20 cm3 d'une solution aqueuse saturée de chlorure d'ammonium et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 10 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1,3 g que l'on purifie par chromatographie sur 150 g de silice (0,063-0,2 mm) contenus dans une colonne de 5 cm de diamètre en éluant avec un mélange acétate d'éthyle-cyclohexane (10-90 en volumes) et en recueiUant des fractions de 18 cm3. Les fractions ne contenant que le produit cherché
sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 906 mg de benzoyloxy-2α butanoyloxy-4α dihydroxy-lβ.lOβ ditriéthylsUyloxy- 7β,13α époxy-5β,20 oxo-9 taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes : - spectre de R.M.N. ÏH (400 MHz ; CDC13 ; δ en ppm) : 0,56 et 0,67 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,95 et 1,03 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,08 (s, 3H : CH3) ; 1,10 (t, J = 7,5 Hz, 3H : CH3 du propyle) ; 1.18 (s, 3H : CH3) ; 1,60 (s, IH : OH en 1) ; 1,73 (s. 3H : CH3) ; 1,84 (mt, 2H : CH2 du propyle) ; 1,91 et 2,48 (2 mts, IH chacun : CH2 en 6) ; 2,03 (s, 3H : CH3) ; 2,11 et 2,22 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,58 (mt, 2H : OCOCH2 du propyle) ; 3,87 (d, J = 7 Hz, IH : H en 3) ; 4,18 et 4,32 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,28 (d, J = 2 Hz, IH : OH en 10) ; 4,42 (dd, J = 10,5 et 6,5 Hz, IH : H en 7) ; 4,93 (d large, J = 10 Hz, IH : H en 5) ; 4,98 (t. J = 9 Hz, IH : H en 13) ; 5,17 (d, J = 2 Hz, IH : H en 10) ; 5,62 (d, J = 7 Hz, IH : H en 2) ; 7,49 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,61 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,12 (d, J = 7,5 Hz, 2H : OCOC6H5 en ortho).
Le butanoyloxy-4 carbonate- lβ,2α bis(triéthylsUyloxy)-7β,13α époxy-
5β,20 méthoxyacétoxy- lOβ oxo-9 taxène-11 peut être préparé de la manière suivante :
A une solution de 870 mg de carbonate- lβ,2c. bis(triéthylsUyloxy)-7β,13α époxy-5β,20 hydroxy-4α méthoxyacétoxy-lOβ oxo-9 taxène-11 dans 15 cm3 de dichlorométhane, on ajoute 1,46 g de 4-dimémylaminopyridine et 3,90 cm3 d'anhydride butyrique. Le milieu réactionnel est chauffé à une température voisine de 42°C pendant 45 heures. On ajoute 50 cm3 d'une solution aqueuse saturée de chlorure de sodium et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 2,0 g que l'on purifie par chromatographie sur 170 g de siUce (0,063- 0,2 mm) contenus dans une colonne de 3 cm de diamètre en éluant avec un mélange acétate d'éthyle-cyclohexane (5-95 en volumes) et en recueiUant des fractions de 15 cm3. Les fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 1,00 g de butanoyloxy-4α carbonate- lβ,2 ditriéthylsilyloxy-7β,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 taxène-11 sous forme d'une meringue blanche et dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. 1H (400 MHz ; CDC13 : δ en ppm) : de 0,50 à 0,70 (mt, 12H : CH2 de l'éthyle) ; de 0,90 à 1,10 (mt, 21H : CH3 de l'éthyle et CH3 du propyle) ; 1,18 (s, 3H : CH3) ; 1,28 (s, 3H : CH3) ; 1,73 (mt, 2H : CH2 du propyle) ; 1,75 (s, 3H : CH3) ; 1,92 et 2,59 (2 mts, IH chacun : CH2 en 6) ; 2,13 (s, 3H : CH3) ; 2,14 et de 2,35 à 2,45 (respectivement dd et mt, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; de 2,35 à 2,45 (mt, 2H : OCOCH2 du propyle) ; 3,42 (d, J = 6,5 Hz, IH : H en 3) ; 3,51 (s, 3H : OCH3) ; 4,18 (s, 2H : OCOCH2O) ; 4,46 (dd, J = 10 et 6,5 Hz, IH : H en 7) ; 4,50 et 4,63 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,51 (d, J = 6,5 Hz, IH : H en 2) ; 4,93 (d large, J = 10 Hz, IH : H en 5) ; 5,02 (t large, J = 9 Hz, IH : H en 13) ; 6,51 (s, IH : H en 10).
EXEMPLE 4
En opérant comme dans l'exemple 3, et à partir de tert-butoxycarbonyl- amino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α phénylacétoxy-4α époxy-5β,20 hydroxy-lβ méthoxyacétoxy- lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α, on obtient le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ méthylène-7β,8 nor-19 oxo-9 phénylacétoxy-4α taxène-11 yle-13α dont les caractéristiques sont les suivantes :
- spectre de R.M.N. ÏH (400 MHz ; CDC13 ; δ en ppm) : 1,24 (s, 15H : CH3 - CH3 et C(CH3)3) ; 1,40 (mt, IH : H en 7) ; 1,66 et 2,24 (2 dd, J = 6 et 5 Hz et J = 10 et 6 Hz,
IH chacun : CH2 en 19) ; 1,92 (s, IH : OH en 1) ; 1,96 (s. 3H : CH^ ; 2,07 et 2,46 (respectivement d large et dt, J = 16 Hz et J = 16 et 4,5 Hz, IH chacun : CH2 en 6) ; 2,32 et 2,54 (respectivement dd et dd large, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,24 (mt, IH : OH en 2') ; 3,53 (s, 3H : OCH3) ; 3,90 et 4,14 (2 d, J = 15 Hz, IH chacun : OCOCH-Ar) ; 4,00 et 4,16 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,20 et 4,26 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,23 (d, J = 7 Hz, IH : H en 3) ; 4,55 (d large, J = 4,5 Hz. IH : H en 5) ; 4,63 (mt, IH : H en 2') ; 5,31 ( AB limite, 2H : H en 3' et CONH) ; 5,71 (d, J = 7 Hz, IH : H en 2) ; 6,34 (t large, J = 9 Hz, IH : H en 13) ; 6,44 (s, IH : H en 10) ; de 7,10 à 7,45 (mt, 10H : H aromatiques et H aromatiques en 3') ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,16 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de
benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxyacétoxy- lOβ oxo-9 phénylacétoxy- A trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dont les caractéristiques sont les suivnates :
- spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 1,24 (s, 6H : CH3) ; 1,36 (s, 9H : C(CH3)3) ; 1,74 (s, IH : OH en 1) ; 1,87 (s, 3H : CH3) ; 2,14 (s, 3H : CHj) ; 2,19 et 2,83 (2 mts, IH chacun : CH2 en 6) ; 2,39 et 2,48 (2 dd larges, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,38 (d, J = 4,5 Hz, IH : OH en 2') ; 3,53 (s, 3H : OCH,) ; 3,90 et 4,14 (2 d, J = 15 Hz, IH chacun : OCOCH2Ar) ; 4,01 (d, J = 7 Hz, IH : H en 3) ; 4,11 et 4,20 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,17 et 4,25 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,65 (mt, IH : H en 2') ; 4,68 (d large, J = 10 Hz, IH : H en
5) ; 5,28 (d large, J = 10 Hz, IH : H en 3') ; 5,35 (d, J = 10 Hz, IH : CONH) ; 5,50 (dd, J = 10 et 7 Hz, IH : H en 7) ; 5,77 (d, J = 7 Hz, IH : H en 2) ; 6,28 (t large, J = 9 Hz, IH : H en 13) ; 6,74 (s, IH : H en 10) ; de 7,15 à 7,45 (mt, 10H : H aromatiques et H aromatiques en 3') ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,66 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,08 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine-1,3 carboxylate-5 (2R.4S.5R) de benzoyloxy-2α époxy-5β,20 hydroxy-lβ méthoxy¬ acétoxy- lOβ oxo-9 phénylacétoxy-4α trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dont les caractéristiques sont les suivantes :
- spectre de R.M.N. lH (400 MHz ; CDC13 ; une température de 333°K, δ en ppm) : 1,06 (s, 9H : C(CH3)3) ; 1,12 (s, 3H : CH3) ; 1,24 (s, 3H : CH3) ; 1,66 (s, IH : OH en 1) ; 1,83 (s, 3H : CH3) ; 1,86 (s, 3H : CH3) ; 2,14 et 2,79 (2 mts, IH chacun : CH2 en
6) ; 2,24 et 2,30 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,45 et 3,58 (2 d, J = 15 Hz, IH chacun : OCOCH-Ar) ; 3,54 (s, 3H : OCH3) ; 3,85 (s, 3H : ArOCH3) ;
3,94 (d, J = 7 Hz, IH : H en 3) ; 4,08 et 4,17 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,14 et 4,22 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,59 (d large, J = 10 Hz, IH : H en 5) ; 4,63 (d, J = 5,5 Hz, IH : H en 2') ; 5,45 (d, J = 5,5 Hz, IH : H en 3') ; 5,47 (mt, IH : H en 7) ; 5,72 (d, J = 7 Hz, IH : H en 2) ; 6,14 (t large, J = 9 Hz, IH : H en 13) ; 6,34 (s, IH : H en 5') ; 6,65 (s, IH : H en 10) ; 6,94 (d, J = 8,5 Hz, 2H : H aromatiques en ortho du OCH3) ; de 7,20 à 7,45 (mt, 12H : H aromatiques et H aromatiques en meta du OCH3 et H aromatiques en 3') ; 7,48 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,64 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 7,98 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho)
En opérant dans des conditions analogues à celles décrites dans l'exemple 3, on prépare le benzoyloxy-2α dihydroxy-lβ,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 phénylacétoxy-4α trifluorométhanesulfonyloxy-7β taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 1,07 (s, 3H : CH3) ;' 1,21 (s , 3H : CH3) ; 1,64 (s, IH : OH en 1) ; 1,87 (s, 3H : CH3) ; 2,18 (d, J = 4,5 Hz, IH : OH enl3) ; 2,20 et 2,88 (2 mts, IH chacun : CH2 en 6) ; 2,30 (s, 3H : CH3) ; de 2,25 à 2,35 (mt, 2H: CH2 en 14) ; 3,52 (s, 3H : OCH3) ; 3,90 et 3,97 (2 d, J = 15 Hz, IH chacun : OCOCH2Ar) ; 4,08 (d, J = 7 Hz, IH : H en 3) ; 4,12 et 4,27 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,16 et 4,24 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,80 (d large, J = 10 Hz, IH : H en 5) ; 4,92 (mt, IH : H en 13) ; 5,55 (dd, J = 10 et 6,5 Hz, IH : H en 7) ; 5,71 (d, J = 7 Hz, IH : H en 2) ; 6,74 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 5H : H aromatiques) ; 7,48 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,64 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,03 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 phénylacétoxy- Ao. trihydroxy-lβ,7β,13 taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (400 MHz ; CDC13 ; Ô en ppm) : 1,12 (s, 3H : CH3) ; 1,14 (s, 3H : CH3) ; 1,66 (s, IH : OH en 1) ; 1,67 (s, 3H : CH3) ; 1,84 et 2,56 (2 mts, IH chacun : CH2 en 6) ; 2,11 (s, 3H : CH3) ; de 2,20 à 2,45 (2 mts, IH chacun : OH) ; 2,35 et 2,42 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,54 (s, 3H : OCH3) ; 3,94 (AB limite, J = 15 Hz, 2H : OCOCH2Ar) ; 3,94 (d, J = 7 Hz, IH : H en 3) ; 4,12 et 4,25 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,26 (AB Umite, J = 16 Hz, 2H : OCOCH2O) ; 4,50 (mt, IH : H en 7) ; 4,87 (d large, J = 10 Hz, IH : H en 5) ; 4,96 (mt, IH : H en 13) ; 5,66 (d, J = 7 Hz, IH : H en 2) ; 6,44 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 5H : H aromatiques) ; 7,47 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,62 (t, J = 7.5 Hz, IH : OCOC6H5 H en para) ; 8,04 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 phénylacétoxy-4α taxène-11 dont les caractéristiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 0,60 et 0,72 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,94 et 1,05 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,15 (s, 3H : CH3) ; 1,22 (s, 3H : CH3) ; 1,66 (s, 3H : CH3) ; 1,69 (s large, IH : OH en 1) ; 1,84 et 2,51 (2 mts, IH chacun : CH2 en 6) ; 2,20 (s, 3H : CH3) ; 2,24 et 2,36 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,54 (s, 3H : OCH3) ; 3,82 et 3,96 (2 d, J = 15 Hz, IH chacun : OCOCH-Ar) ; 3,89 (d, J = 7 Hz, IH : H en 3) ; 4.06 et 4,16 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,20 (AB Umite, J = 16 Hz, 2H : OCOCH2O) ; 4,52 (dd, J = 10 et 6 Hz, IH : H en 7) ; 4,79 (d large, J = 10 Hz, IH : H en 5) ; 4,96 (t large, J = 9 Hz, IH : H en 13) ; 5,66 (d, J = 7 Hz, IH : H en 2) ; 6,58 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 7H : H aromatiques et OCOC6H5 H en eta) ; 7,61 (t, J = 7,5 Hz, IH : OCOC6H5H en para) ; 8,00 (d, J = 7,5 Hz, 2H : OCOC6H5H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α dihydroxy-lβ.lOβ bis(triéthylsUyloxy)-7β,13 époxy-5β,20 oxo-9 phénylacétoxy-4α taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (600 MHz ; CDC13 ; δ en ppm) : 0,53 et 0,72 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,94 et 1,05 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,10 (s, 3H : CH3) ; 1,20 (s, 3H : CH3) ; 1,64 (s, IH : OH en 1) ; 1,70 (s. 3H : CHj) ; 1,86 et 2,45 (2 mts, IH chacun : CH2 en 6) ; 2,10 (s, 3H : CH3) ; 2,20 et 2,32 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,80 et 3,96 (2 d, J = 16 Hz, IH chacun : OCOCH2Ar) ; 3,95 (d, J = 7 Hz, IH : H en 3) ; 4,07 et 4,17 (2 d. J = 9 Hz, IH chacun : CH2 en 20) ; 4,29 (s large, IH : OH en 10) ; 4,43 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,79 (d large, J = 10 Hz, IH : H en 5) ; 5,03 (t large, J = 9 Hz, IH : H en 13) ;
5.19 (s large, IH : H en 10) ; 5,63 (d, J = 7 Hz, IH : H en 2) ; de 7,25 à 7,45 (mt, 7H : H aromatiques et OCOC6H5 H en meta) ; 7,60 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,00 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le carbonate- lβ,2 bis(triéthylsilyloxy)-7β,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 phénylacétoxy-4α taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 0,61 et 0,74 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,92 et 1,05 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ;
1.20 (s, 3H : CH3) ; 1,30 (s, 3H : CH3) ; 1,73 (s, 3H : CH3) ; 1,83 et 2,54 (2 mts, IH chacun : CH2 en 6) ; 2,18 (s, 3H : CH3) ; 2,27 et 2,48 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,50 (d, J = 6,5 Hz, IH : H en 3) ; 3,53 (s, 3H : OCH3) ; 3,65 (AB limite, J = 14 Hz, 2H : OCOCH-Ar) ; 4,18 (AB limite, 2H : OCOCH2O) ; 4,45 et
4,53 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,46 (mt, IH : H en 7) ; 4,53 (d, J = 6,5 Hz, IH : H en 2) ; 4,68 (d large, J = 10 Hz, IH : H en 5) ; 5,06 (t large, J = 9 Hz, IH: H en 13) ; 6,53 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 5H : H aromatiques).
EXEMPLE 5
En opérant comme dans l'exemple 3, et à partir de tert-butoxycarbonyl- amino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2 bis(méthoxy- acétoxy)-4α,10β époxy-5β,20 hydroxy-lβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α, on prépare le tert-butoxycarbonylamino-3 hydroxy- 2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α bis(méthoxyacétoxy)-4α,10β époxy-5β,20 hydroxy-lβ méthylène-7β,8 nor-19 oxo-9 taxène-11 yle-13cc dont les caractéristiques sont les suivantes :
- spectre de R.M.N. H (400 MHz ; CDC13 ; température de 333°K, δ en ppm) : 1,26 (s, 3H : CH3) ; 1,29 (s, 3H : CH3) ; 1,35 (s, 9H : C(CH3)3) ; 1,42 (mt, IH : H en 7) ; 1,71 et 2,29 (respectivement dd et mt, J = 6,5 et 5 Hz, IH chacun : CH2 en 19) ; 1,81 (s, IH : OH en 1) ; 1,91 (s, 3H : CH3) ; 2,15 et 2,54 (respectivement d large et dt, J = 16 Hz et J = 16 et 4,5 Hz, IH chacun : CH2 en 6) ; 2,32 (AB limite, 2H : CH2 en 14) ; 3,50 et 3,53 (2 s, 3H chacun : OCH3) ; 3,60 (mf, IH : OH en 2') ; 4,11 et 4,56 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,12 et 4,31 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,17 (d, J = 7 Hz, IH : H en 3) ; 4,19 et 4,24 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,67 (mt, IH : H en 2') ; 4,78 (d, J = 4,5 Hz, IH : H en 5) ; 5,29 (d large, J = 10 Hz, IH : H en 3') ; 5,47 (d, J = 10 Hz, IH : CONH) ; 5,70 (d, J = 7 Hz, IH : H en 2) ; 6,21 (t large, J = 9 Hz, IH : H en 13) ; 6,44 (s, IH : H en 10) ; 7,30 (t, J = 7,5 Hz, IH : H en para de l'aromatique en 3') ; 7,39 (t, J = 7,5 Hz, 2H : H en meta de l'aromatique en 3') ; 7,45 (d, J = 7,5 Hz, 2H : H en ortho de l'aromatique en 3') ; 7,51 (t, J= 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,61 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,12 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α bis(méthoxyacétoxy)-4α,10β époxy-5β,20 hydroxy-lβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dont les caractéristiques sont les suivantes :
- spectre de R.M.N. *H (400 MHz ; CDC13 ; température de 333°K, δ en ppm) : 1,22 (s, 3H : CH3) ; 1,27 (s, 3H : CH3) ; 1,38 (s, 9H : C(CH3)3) ; 1,64 (s, IH : OH en 1) ;
1.92 (s, 3H : CH3) ; 2,11 (s, 3H : CH3) ; 2,25 et 2,92 (2 mts, IH chacun : CH2 en 6) ; 2,26 et 2,36 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,47 et 3,52 (2 s, 3H chacun : OCH3) ; 3,66 (s large, IH : OH en 2') ; 3,99 (d, J = 7 Hz, IH : H en 3) ; 4,15 et 4,57 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,19 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,24 et 4,35 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,70 (mt, IH : H 2') ; 4,95 (d large, J = 10 Hz, IH : H en 5) ; 5,29 (d large, J = 10 Hz, IH : H en 3') ; 5,49 (d, J = 10 Hz, IH : CONH) ; 5,53 (dd, J = 11 et 8 Hz, IH : H en 7) ; 5,76 (d, J = 7 Hz, IH : H en 2) ; 6.18 (t large, J = 9 Hz, IH : H en 13) ; 6,74 (s, IH : H en 10) ; 7,30 (t, J = 7,5 Hz, IH : H en para de l'aromatique en 3') ; 7,38 (t, J = 7,5 Hz, 2H : H en meta de l'aromatique en 3') ; 7,45 (d, J = 7,5 Hz, 2H : H en ortho de l'aromatique en 3') ; 7,49 (t, J= 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,09 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine-1,3 carboxylate-5 (2R.4S.5R) de benzoyloxy-2α bis(méthoxyacétoxy)-4α,10β époxy- 5β,20 hydroxy-lβ oxo-9 trifluorométhanesu_fonyloxy-7β taxène-11 yle-13α dont les caractéristiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz ; CDC13 ; température de 333°K, δ en ppm) : 1,10 (s, 9H : C(CH3)3) ; 1,18 (s, 3H : CH3) ; 1,20 (s, 3H : CH3) ;1,64 (s, IH : OH en 1) ; 1,75 (s, 3H : CH3) ; 1,86 (s, 3H : CH3) ; 2,12 et 2,26 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,24 et 2,86 (2 mts, IH chacun : CH2 en 6) ; 3,33 et 3,53 (2 s, 3H : OCH3) ; 3,65 et 4,10 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 3,83 (s, 3H : ArOCH3) ; 3,86 (d, J = 7 Hz, IH : H en 3) ; 4,14 et 4,20 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,19 et 4,32 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,72 (d large, J = 4,5 Hz, IH : H en 2') ; 4,89 (d large, J = 10 Hz, IH : H en 5) ; 5,46 (mt, IH : H en 3') ; 5,45 (dd, J = 11 et 8 Hz, IH : H en 7) ; 5,69 (d, J = 7 Hz, IH : H en 2) ; 5,94 (t large, J = 9 Hz, IH : H en 13) ; 6,40 (s large, IH : H en 5') ; 6,63 (s, IH : H en 10)
6.93 (d, J = 8,5 Hz, 2H : H aromatiques en ortho du OCH3) ; de 7,30 à 7,45 (mt, 5H H aromatiques en 3') ; 7,38 (d, J = 8,5 Hz, 2H : H aromatiques en meta du OCHj) 7,48 (t, J= 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7.5 Hz, IH : OCOC6H5 H en para) ; 8,08 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α bis(méthoxyacétoxy)-4α,10β dihydroxy-lβ,13α époxy-
5β,20 oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 dont les caractéristiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 1,06 (s, 3H : CH3) ; 1,20 (s, 3H : CH3) ; 1,61 (s, IH : OH en 1) ; 1,89 (s, 3H : CH3) ; 2,23 (d, J = 5 Hz, IH : OH en 13) ; de 2,20 à 2,35 et 2,92 (2 mts, IH chacun : CH2 en 6) ; 2,26 (s, 3H : CH3) ; 2,32 (d, J = 9 Hz, 2H : CH2 en 14) ; 3,52 et 3,58 (2 s, 3H chacun : OCH3) ; 4,04 (d, J = 7 Hz, IH : H en 3) ; 4,19 et 4,32 (2 AB limite, J = 16 Hz, 2H chacun : OCOCH2O) ; 4,20 et 4,38 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,82 (mt, IH : H en 13) ; 4,99 (d large, J = 10 Hz, IH : H en 5) ; 5,55 (dd, J = 10 et 7 Hz, IH : H en 7) ; 5,69 (d, J = 7 Hz, IH : H en 2) ; 6,73 (s, IH : H en 10) ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,64 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,13 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α bis(méthoxyacétoxy)-4α,10β époxy-5β,20 oxo-9 trihydroxy-lβ,7β,13α taxène-11 dont les caractéristiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz ; CDC13 : δ en ppm) : 1,11 (s, 6H : CH3) ; 1,63 (s, IH : OH en 1) ; 1,70 (s, 3H : CH3) ; 1,92 et 2,63 (2 mts, IH chacun : CH2 en 6) ; 2,08 (s, 3H : CH3) ; de 2,20 à 2,30 (mt, 3H : CH2 en 14 et OH) ; 2,40 (d, J = 4 Hz, IH : OH) ; 3,54 et 3,59 (2 s, 3H chacun : OCH3) ; 3,92 (d, J = 7 Hz, IH : H en 3) ; 4,20 et 4,35 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,24 et 4,28 (2 AB limite, J = 16 Hz, 2H chacun : OCOCH2O) ; 4,50 (mt, IH : H en 7) ; 4,86 (mt, IH : H en 13) ; 5,03 (d large, J = 10 Hz, IH : H en 5) ; 5,65 (d, J = 7 Hz, IH : H en 2) ; 6,44 (s, IH : H en 10) ; 7,49 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,14 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α bis(méthoxyacétoxy)-4α,10β bis(triéthylsilyloxy)- 7β,13α époxy-5β,20 hydroxy-lβ oxo-9 taxène-11 dont les caractéristiques sont les suivantes :
- spectre de R.M.N. H (400 MHz ; CDC13 ; δ en ppm) : 0,60 et 0,70 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,94 et 1,02 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ;
1,12 (s, 3H : CH3) ; 1,20 (s, 3H : CH3) ; 1,64 (s, IH : OH en 1) ; 1,70 (s, 3H : CH3) ; 1,91 et 2,57 (2 mts, IH chacun : CH2 en 6) ; 2,12 (s, 3H : CH3) ; 2,13 et 2,23 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,53 et 3,57 (2 s, 3H chacun : OCH3) ; 3,83 (d, J = 7 Hz, IH : H en 3) ; 4,15 et 4,40 (2 d, J = 16 Hz, 2H : OCOCH2O) ; 4,19 (AB
limite, J = 16 Hz, 2H : OCOCH2O) ; 4,21 et 4,37 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,51 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,93 (t, J = 9 Hz, IH : H en 13) ; 5,02 (d large, J = 10 Hz, IH : H en 5) ; 5,64 (d, J = 7 Hz, IH : H en 2) ; 6,56 (s, IH : H en 10) ; 7,48 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5H en para) ; 8,19 (d, J = 7,5 Hz, 2H : OCOC6H5H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α dihydroxy-lβ,10β bis(triéthylsUyloxy)-7β,13α époxy- 5β,20 méthoxyacétoxy-4 oxo-9 taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. ÎH (400 MHz ; CDC13 ; δ en ppm) : 0,57 et 0,69 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,94 et 1,03 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,09 (s, 3H : CH3) ; 1,17 (s, 3H : CH3) ; 1,58 (s, IH : OH en 1) ; 1,75 (s, 3H : CH3) ; 1,93 et 2,49 (2 mts, IH chacun : CH2 en 6) ; 2,03 (s, 3H : CH3) ; 2,09 et 2,18 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,57 (s, 3H : OCH3) ; 3,88 (d, J = 7 Hz, IH : H en 3) ; 4,16 et 4,40 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,20 et 4,36 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,28 (s large, IH : OH en 10) ; 4,42 (mt, IH : H en 7) ; 4,97 (t, J = 9 Hz, IH : H en 13) ; 5,01 (d large, J = 10 Hz, IH : H en 5) ; 5,17 (s large, IH : H en 10) ; 5,62 (d, J = 7 Hz, IH : H en 2) ; 7,47 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,61 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,18 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho) .
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le bis(méthoxyacétoxy)-4α,10β carbonate- lβ,2α bis(triéthylsUyloxy)- 7β,13α époxy-5β,20 oxo-9 taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. H (400 MHz ; CDC13 ; δ en ppm) : 0,60 et 0,68 (2 mts, 6H chacun : CH2 de l'éthyle) ; 0,92 et 1,01 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,19 (s, 3H : CH3) ; 1,27 (s, 3H : CH3) ; 1,75 (s, 3H : CH3) ; 1,91 et 2,63 (2 mts, IH chacun : CH2 en 6) ; 2,08 et 2,41 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,12 (s, 3H : CH3) ; 3,44 (d, J = 6,5 Hz, IH : H en 3) ; 3,46 et 3,50 (2 s, 3H chacun : OCH3) ; 4,06 et 4,14 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,16 (s, 2H : OCOCH2O) ; 4,46 (dd, J = 10 et 7 Hz, IH : H en 7) ; 4,50 et 4,66 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,51 (d, J = 6,5 Hz, IH : H en 2) ; 4,99 (mt, IH : H en 13) ; 5,00 (d large, J = 10 Hz, IH : H en 5) ; 6,51 (s, IH : H en 10).
EXEMPLE 6
En opérant comme dans l'exemple 3, et à partir de tert-butoxycarbonyl- amino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α cyclopranoyloxy- 4 époxy-5β,20 hydroxy-lβ oxo-9 méthoxyacétoxy-lOβ trifluorométhanesulfonyloxy- 7β taxène-11 yle-13α, on prépare le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α cyclopropanoyloxy-4α époxy-5β,20 hydroxy- lβ méthoxyacétoxy-lOβ méthylène-7β,8 nor-19 oxo-9 taxène-11 yle-13α dont les caractéristiques sont les suivantes :
- spectre de R.M.N. ^ (400 MHz ; CDC13 ; température voisine de 333°K, δ en ppm) : de 0,80 à 1,40 (mt, 4H : CH2CH2 du cyclopropyle) ; 1,30 (s, 6H : CH3) ; 1,35
(s, 9H : C(CH3)3) ; de 1,30 à 1,40 (mt, IH : H en 7) ; 1,70 et 2,23 (2 dd, respectivement J = 6 et 5,5 Hz et J =10 et 5,5 Hz, IH chacun : CH2 en 19) ; 1,80 (mt, IH : CH du cyclopropyle) ; 1,85 (s, IH : OH en 1) ; 1,86 (s, 3H : CH3) ; 2,11 et 2,44 (respectivement d large et dt, J = 16 Hz et J = 16 et 4,5 Hz, IH chacun : CH2 en 6) ; 2,34 et 2,50 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,22 (d, J = 4 Hz, IH : OH en 2') ; 3,52 (s, 3H : OCH3) ; 4,08 et 4,28 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,13 (d, J = 7 Hz, IH : H en 3) ; 4,16 et 4,24 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,62 (d, J = 4,5 Hz, IH : H en 5) ; 4,70 (d large, J = 4 Hz, IH : H en 2') ; 5,28 (AB limite, 2H : H3' et CONH) ; 5,70 (d, J = 7 Hz, IH : H en 2) ; 6,23 (t large, J = 9 Hz, IH : H en 13) ; 6,42 (s, IH : H en 10) ; de 7,20 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,52 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,61 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,14 (d, J= 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le tert-butoxycarbonylamino-3 hydroxy-2 phényl-3 propionate-(2R,3S) de benzoyloxy-2α cyclopropanoyloxy-4α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13 dont les caractéristiques sont les suivantes :
- spectre de R.M.N. H (400 MHz ; CDC13 ; δ en ppm) : de 0,85 à 1,40 (mt, 4H CH2CH2 du cyclopropyle) ; 1,22 (s, 3H : CH3) ; l,24(s, 3H : CH3) ; 1,39 (s, 9H C(CH3)3) ; 1,70 (s, IH : OH en 1) ; 1,83 (mt, IH : CH du cyclopropyle) ; 1,88 (s, 3H CH3) ; 2,05 (s, 3H : CHj) ; 2,23 et 2,84 (2 mts, IH chacun : CH2 en 6) ; 2,34 et 2,42 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,35 (d, J = 5,5 Hz, IH : OH en 2') ; 3,52 (s, 3H : OCH3) ; 3,96 (d, J = 7 Hz, IH : H en 3) ; 4,16 et 4,25 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,17 et 4,28 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,72
(mt, IH : H en 2') ; 4,81 (d large, J = 10 Hz, IH : H en 5) ; 5,28 (d large, J = 10 Hz, IH : H en 3') ; 5,36 (d, J = 10 Hz, IH : CONH) ; 5,48 (dd, J = 10,5 et 7 Hz, IH : H en 7) ; 5,72 (d, J = 7 Hz, IH : H en 2) ; 6,11 (mt, IH : H en 13) ; 6,71 (s, IH : H en 10) ; de 7,25 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,52 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,65 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,08 (d, J= 7,5' Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le tert-butoxycarbonyl-3 (méthoxy-4 phényl)-2 phényl-4 oxazolidine- 1,3 carboxylate-5 (2R,4S,5R) de benzoyloxy-2α cyclopropanoyloxy-4α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 yle-13α dont les caractéristiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : de 0,50 à 1,50 (mt, 5H : CH et CH2 du cyclopropyle) ; 1,04 (s, 9H : C(CH3)3) ; 1,17 (s, 3H : CH3) ; 1,19 (s, 3H : CH3) ; 1,65 (s, IH : OH en 1) ; 1,72 (s, 3H : CH3) ; 1,84 (s, 3H : CH3) ; 2,14 et 2,32 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,16 et 2,79 (2 mts, IH chacun : CH2 en 6) ; 3,52 (s, 3H : OCH3) ; 3,82 (s, 3H : ArOCH3) ; 3,86 (d, J = 7 Hz, IH : H en 3) ; 4,11 et 4,24 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,15 et 4,22 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,60 (d, J = 4,5 Hz, IH : H en 2') ; 4,74 (d large, J = 10 Hz, IH : H en 5) ; 5,44 (dd, J = 10,5 et 8 Hz, IH : H en 7) ; 5,50 (mt, IH : H en 3') ; 5,67 (d, J = 7 Hz, IH : H en 2) ; 5,88 (mt, IH : H en 13) ; 6,41 (mf, IH : H en 5") ; 6,61 (s, IH : H en 10) ; 6,92 (d, J = 8,5 Hz, 2H : H aromatiques en ortho du OCH3) ; 7,38 (d, J = 8,5 Hz, 2H : H aromatiques en meta du OCH3) ; de 7,25 à 7,45 (mt, 5H : H aromatiques en 3') ; 7,49 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,02 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α cyclopropanoyloxy-4α dihydroxy-lβ,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-lldont les caractéristiques sont les suivantes :
- spectre de R.M.N. *H (400 MHz ; CDC13 ; température de 333°K, δ en ppm) : de 0,90 à 1,40 (mt, 4H : CH2CH2 du cyclopropyle) ; 1,10 (s, 3H : CH3) ; 1,22 (s, 3H :
CH3) ; 1,61 (s, IH : OH en 1) ; de 1,70 à 1,85 (mt, 2H : CH du cyclopropyle et OH en 13) ; 1,90 (s, 3H : CH3) ; 2,22 et 2,86 (2 mts, IH chacun : CH2 en 6) ; 2,26 (s, 3H : CH3) ; 2,36 (d, J = 9 Hz, 2H : CH2 en 14) ; 3,52 (s, 3H : OCH3) ; 4,05 (d, J = 7 Hz, IH : H en 3) ; 4,14 et 4,22 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,20 et 4,36 (2
d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,84 (mt, IH : H en 13) ; 4,85 (d large, J = 10 Hz, IH : H en 5) ; 5,54 (dd, J = 11 et 8 Hz, IH : H en 7) ; 5,72 (d, J = 7 Hz, IH : H en 2) ; 6,73 (s, IH : H en 10) ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,12 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho)
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α cyclopropanoyloxy-4α dihydroxy-lβ,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 trifluorométhanesulfonyloxy-7β taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. *H (400 MHz ; CDC13 ; température de 333°K, δ en ppm) : de 0,90 à 1,40 (mt, 4H : CH2CH2 du cyclopropyle) ; 1,10 (s, 3H : CH3) ; 1,22 (s, 3H : CH3) ; 1,61 (s, IH : OH en 1) ; de 1,70 à 1,85 (mt, 2H : CH du cyclopropyle et OH en 13) ; 1,90 (s, 3H : CH3) ; 2,22 et 2,86 (2 mts, IH chacun : CH2 en 6) ; 2,26 (s, 3H : CH3) ; 2,36 (d, J = 9 Hz, 2H : CH2 en 14) ; 3,52 (s, 3H : OCH3) ; 4,05 (d, J = 7 Hz, IH : H en 3) ; 4,14 et 4,22 (2 d, J = 16 Hz, IH chacun : OCOCH2O) ; 4,20 et 4,36 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,84 (mt, IH : H en 13) ; 4,85 (d large, J = 10 Hz, IH : H en 5) ; 5,54 (dd, J = 11 et 8 Hz, IH : H en 7) ; 5,72 (d, J = 7 Hz, IH : H en 2) ; 6,73 (s, IH : H en 10) ; 7,51 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,63 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,12 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho)
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α cyclopropanoyloxy~4α bis(triéthylsUyloxy)-7β,13α époxy-5β,20 hydroxy-lβ méthoxyacétoxy-lOβ oxo-9 taxène-11 dont les caractéristiques sont les suivantes : - spectre de R.M.N. ÏH (400 MHz ; CDC13 ; δ en ppm) : 0,60 et 0,68 (2 mts, 6H chacun : CH2 de l'éthyle) ; de 0,90 à 1,35 (mt, 4H : CH2CH2 du cyclopropyle) ; 0,94 et 1,03 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,14 (s, 3H : CH3) ; 1,20 (s, 3H : CH3) ; 1,64 (s, IH : OH en 1) ; 1,71 (s, 3H : CH3) ; 1,73 (mt, IH : CH du cyclopropyle) ; 1,87 et 2,50 (respectivement dd large et mt, J = 14 et 11 Hz, IH chacun : CH2 en 6) ; 2,11 et 2,29 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 2,15 (s, 3H : CH3) ; 3,53 (s, 3H : OCH3) ; 3,86 (d, J = 7 Hz, IH : H en 3) ; 4,14 et 4,26 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,19 (AB limite, J = 16 Hz, 2H : OCOCH2O) ; 4,52 (dd, J = 11 et 7 Hz, IH : H en 7) ; 4,84 (d large, J = 10 Hz, IH : H en 5) ; 4,95 (t large, J = 9 Hz, IH : H en 13) ; 5,65 (d, J = 7 Hz, IH : H en 2) ; 6,56 (s, IH : H en
10) ; 7,50 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,62 (t, J = 7,5 Hz, IH : OCOC6H5H en para) ; 8,09 (d, J = 7,5 Hz, 2H : OCOC6H5H en ortho).
En opérant dans des conditions analogues à ceUes décrites dans l'exemple 3, on prépare le benzoyloxy-2α cyclopropanoyloxy-4α dihydroxy-lβ.lOβ bis(triéthyl- sUyloxy)-7β,13α époxy-5β,20 oxo-9 taxène-11 dont lescaractéristiques sont les suivantes :
- spectre de R.M.N. XH (400 MHz ; CDC13 . δ en ppm) : 0,58 et 0,68 (2 mts, 6H chacun : CH2 de l'éthyle) ; de 0,90 à 1,35 (mt, 4H : CH2CH2 du cyclopropyle) ; 0,94 et 1,03 (2 1, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ; 1,12 (s, 3H : CH3) ; 1,22 (s, 3H : CH3) ; 1,59 (s, IH : OH en 1) ; 1,67 (mt, IH : CH du cyclopropyle) ; 1,73 (s, 3H : CH3) ; 1,90 et 2,44 (2 mts, IH chacun : CH2 en 6) ; 2,06 (s, 3H : CH3) ; 2,10 et 2,25 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,91 (d, J = 7 Hz, IH : H en 3) ; 4,16 et 4,26 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,28 (d, J = 1,5 Hz, IH : OH en en 10) ; 4,42 (dd, J = 11 et 6 Hz, IH : H en 7) ; 4,84 (d large, J = 10 Hz, IH : H en 5) ; 5,00 (t, J = 9 Hz, IH : H en 13) ; 5,16 (d, J = 1,5 Hz, IH : H en 10) ; 5,62 (d, J = 7 Hz, IH : H en 2) ; 7,50 (t, J = 7,5 Hz, 2H : OCOC6H5 H en meta) ; 7,62 (t, J = 7,5 Hz, IH : OCOC6H5 H en para) ; 8,09 (d, J = 7,5 Hz, 2H : OCOC6H5 H en ortho).
Le carbonate- lβ,2 cyclopropanoyloxy-4α bis(triéthylsUyloxy)-7β,13α époxy-5β,20 méthoxyacétoxy- lOβ oxo-9 taxène-11 peut être préparé de la manière suivante :
A une solution de 100 mg de carbonate- lβ,2α bis(triéthylsilyloxy)-7β,13α époxy-5β,20 hydroxy-4α méthoxyacétoxy-lOβ oxo-9 taxène-11 dans 7 cm3 de tétrahydrofurane, on ajoute, goutte à goutte, 345 μl d'une solution 1M de hexaméthyldisilazane de Uthium dans l'hexane, à une température voisine de -30°C. Le mélange réactionnel est agité pendant 15 minutes à cette température puis on ajoute, goutte à goutte, 39 μl de chlorure de cyclopropanoyle. Le mélange réactionnel est agité pendant 30 minutes à une température voisine de 0°C puis hydrolyse par addition de 1 cm3 d'une solution saturée de chlorure d'ammonium et 50 cm3 de dichlorométhane. La phase organique est décantée, lavée par 2 fois 40 cm3 d'une solution aqueuse saturée de chlorure de sodium puis séchée sur sulfate de magnésium, filtrée et concentrée à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 120 mg d'un produit que l'on purifie par chromatographie sur 70 g de siUce (0,063-0,2 mm) contenus dans une colonne de 2 cm de diamètre en éluant avec un mélange acétate d'éthyle-cyclohexane (20-80 en volumes) et en recueillant des fractions de 10 cm3. Les
fractions ne contenant que le produit cherché sont réunies et concentrées à sec sous pression réduite (2,7 kPa) à 40°C. On obtient 31 mg de carbonate- lβ,2α cyclopropanoyloxy-4α bis(triéthylsUyloxy)-7β,13α époxy-5β,20 méthoxyacétoxy-lOβ oxo-9 taxène-11 sous forme d'une meringue blanche dont les caractéristiques physiques sont les suivantes :
- spectre de R.M.N. !H (400 MHz ; CDC13 ; δ en ppm) : 0,60 et 0,66 (2 mts, 6H chacun : CH2 de l'éthyle) ; de 0,90 à 1,35 (mt, 4H : CH2CH2 du cyclopropyle) ; 0,92 et 1,02 (2 t, J = 7,5 Hz, 9H chacun : CH3 de l'éthyle) ;1,19 (s, 3H : CH3) ; 1,29 (s, 3H : CH3) ; 1,60 (s, IH : OH en 1) ; 1,62 (mt, IH : CH du cyclopropyle) ; 1,73 (s, 3H : CH3) ; 1,88 et 2,57 (respectivement dd large et mt, J = 15 et 10 Hz, IH chacun : CH2 en 6) ; 2,15 (s, 3H : CH3) ; 2,19 et 2,37 (2 dd, J = 16 et 9 Hz, IH chacun : CH2 en 14) ; 3,48 (d, J = 7 Hz, IH : H en 3) ; 3,51 (s, 3H : OCH3) ; 4,16 (s, 2H : OCOCH2O) ; 4,44 (mt, IH : H en 7) ; 4,45 et 4,54 (2 d, J = 9 Hz, IH chacun : CH2 en 20) ; 4,49 (d, J = 7 Hz, IH : H en 2) ; 4,85 (d large, J = 10 Hz, IH : H en 5) ; 5,02 (t large, J = 9 Hz, IH : H en 13) ; 6,52 (s, IH : H en 10).
Les nouveaux produits de formule générale (I) dans laquelle Z représente un radical de formule générale (II) manifestent une activité inhibitrice significative de la prolifération cellulaire anormale et possèdent des propriétés thérapeutiques permettant le traitement de malades ayant des conditions pathologiques associées à une prolifération cellulaire anormale. Les conditions pathologiques incluent la prolifération ceUulaire anormale de ceUules maUgnes ou non maUgnes de divers tissus et/ou organes, comprenant, de manière non limitative, les tissus musculaires, osseux ou conjonctifs, la peau, le cerveau, les poumons, les organes sexuels, les systèmes lymphatiques ou rénaux, les ceUules mammaires ou sanguines, le foie, l'appareU digestif, le pancréas et les glandes thyroïdes ou adrénales. Ces conditions pathologiques peuvent inclure également le psoriasis, les tumeurs solides, les cancers de l'ovaire, du sein, du cerveau, de la prostate, du colon, de l'estomac, du rein ou des testicules, le sarcome de Kaposi, le cholangiocarcinome, le choriocarcinome, le neuroblastome, la tumeur de Wilms, la maladie de Hodgkin, les mélanomes, les myélomes multiples, les leucémies lymphocytaires chroniques, les lymphomes granulocytaires aigus ou chroniques. Les nouveaux produits selon l'invention sont particulièrement utiles pour le traitement du cancer de l'ovaire. Les produits selon l'invention peuvent être utiUsés pour prévenir ou retarder l'apparition ou la réapparition des conditions pathologiques ou pour traiter ces conditions pathologiques.
Les produits selon l'invention peuvent être administrés à un malade selon différentes formes adaptées à la voie d'administration choisie qui, de préférence, est la voie parentérale. L'administration par voie parentérale comprend les adniinistrations intraveineuse, intrapéritonéale, intramusculaire ou sous-cutanée. Plus particulièrement préférée est radministration intrapéritonéale ou intraveineuse.
La présente invention comprend également les compositions pharmaceu¬ tiques qui contiennent au moins un produit de formule générale (I) en une quantité suffisante adaptée à l'emploi en thérapeutique humaine ou vétérinaire. Les compositions peuvent être préparées selon les méthodes habituelles en utiUsant un ou plusieurs adjuvants, supports ou excipients pharmaceutiquement acceptables. Les supports convenables incluent les diluants, les milieux aqueux stériles et divers solvants non toxiques. De préférence les compositions se présentent sous forme de solutions ou de suspensions aqueuses, de solutions injectables qui peuvent contenir des agents émuLsifiants, des colorants, des préservatifs ou des stabilisants. Le choix des adjuvants ou excipients peut être déterminé par la solubilité et les propriétés chimiques du produit, le mode particulier d'administration et les bonnes pratiques pharmaceutiques.
Pour radministration parentérale, on utilise des solutions ou des suspensions stériles aqueuses ou non aqueuses. Pour la préparation de solutions ou de suspensions non aqueuses peuvent être utiUsés des huUes végétales naturelles teUe que l'huile d'olive, l'huile de sésame ou l'huiïe de paraffine ou les esters organiques injectables tel que l'oléate d'éthyle. Les solutions stériles aqueuses peuvent être constituées d'une solution d'un sel pharmaceutiquement acceptable en solution dans de l'eau. Les solutions aqueuses conviennent pour administration intraveineuse dans la mesure où le pH est convenablement ajusté et où l'isotonicité est réaUsée, par exemple, par une quantité suffisante de chlorure de sodium ou de glucose. La stériUsation peut être réalisée par chauffage ou par tout autre moyen qui n'altère pas la composition.
Il est bien entendu que tous les produits entrant dans les compositions selon l'invention doivent être purs et non toxiques pour les quantités utilisées. Les compositions peuvent contenir au moins 0,01 % de produit thérapeuti- quement actif. La quantité de produit actif dans une composition est teUe qu'une posologie convenable puisse être prescrite. De préférence, les compositions sont préparées de telle façon qu'une dose unitaire contienne de 0,01 à 1000 mg environ de produit actif pour l'administration par voie parentérale.
Le traitement thérapeutique peut être effectué concuremment avec d'autres traitements thérapeutiques incluant des médicaments antinéoplastiques, des anticorps monoclonaux, des thérapies immunologiques ou des radiothérapies ou des modificateurs des réponses biologiques. Les modificateurs des réponses incluent, de manière non limitative, les lymphokines et les cytokines teUes que les interleukines, les interférons (α, β ou δ) et le TNF. D'autres agents chimiothérapeutiques utiles dans le traitement des désordres dus à la prolifération anormale des ceUules incluent, de manière non limitative, les agents alkylants tels que les moutardes à l'azote comme la mechloretamine, le cyclophosphamide, le melphalan et le chlorambucU, des sulfonates d'alkyle comme le busulfan, les nitrosourées comme la carmustine, la lomustine, la sémustine et la streptozocine, les triazènes comme la dacarbazine, les antimétabolites comme les analogues de l'acide folique tel que le méthotrexate, les analogues de pyrimidine comme le fluorouracil et la cytarabine, des analogues de purines comme la mercaptopurine et la thioguanine, des produits naturels tels que les alcaloïdes de vinca comme la vinblastine, la vincristine et la vendésine, des épipodophyUotoxines comme l'étoposide et le teniposide, des antibiotiques comme la dacώiomycine, la daunorubicine, la doxorubicine, la bléomycine, la plicamycine et la mitomycine, des enzymes comme la L-asparaginase, des agents divers comme les complexes de coordination du platine tel que le cisplatine, les urées substituées tel que rhydroxyurée, les dérivés de méthylhydrazine comme la procarbazine, les suppresseurs adrénocorticoïques comme le mitotane et l'aminoglutéthymide, les hormones et les antagonistes comme les adrénocorticostéroïdes comme la prednisone, les progestines comme le caproate d'hydroxyprogestérone, l'acétate de méthoxyprogestérone et l'acétate de megestrol, les oestrogènes comme le diéthylstilbestrol et réthynylestradiol, les antioestrogènes comme le tamoxifène, les androgènes comme le propionate de testostérone et la fluoxymesterone.
Les doses utiUsées pour mettre en oeuvre les méthodes selon l'invention sont ceUes qui permettent un traitement prophylactique ou un maximum de réponse thérapeutique. Les doses varient selon la forme d'administration, le produit particulier sélectionné et les caractéristiques propres du sujet à traiter. En général, les doses sont ceUes qui sont thérapeutiquement efficaces pour le traitement des désordres dus à une prolifération cellulaire anormale. Les produits selon l'invention peuvent être administrés aussi souvent que nécessaire pour obtenir l'effet thérapeutique désiré. Certains malades peuvent répondre rapidement à des doses relativement fortes ou faibles puis avoir besoin de doses d'entretien faibles ou nulles. Généralement, de
faibles doses seront utilisées au début du traitement et, si nécessaire, des doses de plus en plus fortes seront administrées jusqu'à l'obtention d'un effet optimum. Pour d'autres malades il peut être nécessaire d'administrer des doses d'entretien 1 à 8 fois par jour, de préférence 1 à 4 fois, selon les besoins physiologiques du malade considéré. Il est aussi possible que pour certains malades il soit nécessaire de n'utiliser qu'une à deux administrations journaUères.
Chez l'homme, les doses sont généralement comprises entre 0,01 et 200 mg/kg. Par voie intrapéritonéale, les doses seront en général comprises entre 0,1 et 100 mg/kg et, de préférence entre 0,5 et 50 mg/kg et, encore plus spécifiquement entre 1 et 10 mg/kg. Par voie intraveineuse, les doses sont généralement comprises entre 0,1 et 50 mg/kg et, de préférence entre 0,1 et 5 mg/kg et, encore plus spécifiquement entre 1 et 2 mg/kg. Il est entendu que, pour choisir le dosage le plus approprié, devront être pris en compte la voie d'administration, le poids du malade, son état de santé général, son âge et tous les facteurs qui peuvent influer sur l'effica- cité du traitement.
L'exemple suivant Ulustre une composition selon l'invention.
EXEMPLE
On dissout 40 mg du produit obtenu à l'exemple 1 dans 1 cm3 d'Emulphor EL 620 et 1 cm3 d'éthanol puis la solution est diluée par addition de 18 cm3 de sérum physiologique.
La composition est administrée par perfusion pendant 1 heure par introduc¬ tion dans du soluté physiologique.