TWI794616B - 藥劑溶出型支架 - Google Patents
藥劑溶出型支架 Download PDFInfo
- Publication number
- TWI794616B TWI794616B TW109123057A TW109123057A TWI794616B TW I794616 B TWI794616 B TW I794616B TW 109123057 A TW109123057 A TW 109123057A TW 109123057 A TW109123057 A TW 109123057A TW I794616 B TWI794616 B TW I794616B
- Authority
- TW
- Taiwan
- Prior art keywords
- stent
- cilostazol
- layer
- mass
- polymer
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/86—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure
- A61F2/88—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure the wire-like elements formed as helical or spiral coils
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/02—Inorganic materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/02—Inorganic materials
- A61L31/022—Metals or alloys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/06—Macromolecular materials obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/08—Materials for coatings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/08—Materials for coatings
- A61L31/10—Macromolecular materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/12—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/148—Materials at least partially resorbable by the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/16—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/86—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/20—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing organic materials
- A61L2300/204—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing organic materials with nitrogen-containing functional groups, e.g. aminoxides, nitriles, guanidines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/42—Anti-thrombotic agents, anticoagulants, anti-platelet agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/422—Anti-atherosclerotic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/60—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a special physical form
- A61L2300/602—Type of release, e.g. controlled, sustained, slow
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/60—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a special physical form
- A61L2300/606—Coatings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/60—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a special physical form
- A61L2300/63—Crystals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2420/00—Materials or methods for coatings medical devices
- A61L2420/08—Coatings comprising two or more layers
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Vascular Medicine (AREA)
- Heart & Thoracic Surgery (AREA)
- Epidemiology (AREA)
- Surgery (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- Cardiology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Molecular Biology (AREA)
- Inorganic Chemistry (AREA)
- Transplantation (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Materials Engineering (AREA)
- Composite Materials (AREA)
- Urology & Nephrology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Materials For Medical Uses (AREA)
- Media Introduction/Drainage Providing Device (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本發明之支架具有支架骨架、及於支架骨架上堆疊了複數層之堆疊層,堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物,且使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出5質量%以下之上述晶質西洛他唑。
Description
本發明係關於一種塗佈有西洛他唑之支架及其製造方法,進而詳細而言,係關於一種具有包含西洛他唑之複數層之支架及其製造方法。
近年來,心肌梗塞、心絞痛、腦中風、末梢血管疾病等動脈硬化性疾病不斷增加。作為針對動脈硬化性疾病之確實之治療法,例如廣泛使用心臟之冠狀動脈中之經皮冠狀動脈成形術等以外科之方式撐開血管之狹窄部或阻塞部之經皮血管成形術(Percutaneous Transluminal Angioplasty,以下,簡稱為「PTA」)。PTA之中特別是針對冠狀動脈之狹窄部或阻塞部所進行之治療法被稱為經皮冠狀動脈成形術(Percutaneous Transluminal Coronary Angioplasty,以下,簡稱為「PTCA」)。
PTCA係藉由如下方式使血流恢復之方法,即,將前端帶氣球(balloon)之較細之管(氣球導管)或支架自手臂或大腿部之動脈插入,通至心臟冠狀動脈之狹窄部後,使前端之氣球膨脹而擴張狹窄之血管。藉此,病變部之血管內腔得以擴張,由此,通過血管內腔之血流增加。該PTCA除了用於治療動脈硬化性疾病以外,亦用於治療血液透析患者之手臂上形成之分路血管之狹窄等。
一般而言,進行了PTCA之血管部位會受到內皮細胞之剝離或彈力板損傷等傷害,會發生血管壁之癒合反應即血管內膜之增生,因此藉由PTCA而成功撐開狹窄病變部之患者中約30~40%會發生再狹窄。
人類之再狹窄之成因主要認為有PTCA之1~3天後所發生之見於單核球之黏著及/或浸潤之炎症過程、及約45天後增生性為最高峰之平滑肌細胞所引起之內膜肥厚形成過程。於發生再狹窄之情形時,由於需要再次進行PTCA,故而確立其預防法及治療法為當務之急。
因此,盛行嘗試藉由使用於支架等之表面擔載有抗癌劑、免疫抑制劑、抗炎劑或平滑肌細胞之增生抑制劑的藥劑溶出型管腔內留置用醫療器件(支架),從而使藥劑於管腔內之留置部位局部地釋出數天左右,謀求再狹窄率之降低。
作為塗佈於藥劑溶出型支架之藥劑,一般為可作為抗癌劑及免疫抑制劑發揮作用之limus系藥劑。該等藥劑具有藉由其較強之細胞毒性而強力地抑制作為再狹窄之主要原因之血管平滑肌細胞之增生、即所謂內膜肥厚的效果。但亦存在由於亦強力地抑制血管內皮細胞之再生,故而可能誘發遲發性支架內血栓症的臨床上之較大課題。
亦嘗試使用除了limus系以外之藥劑,例如雖預想到因難溶於水而難以製備但無細胞毒性之西洛他唑。例如,專利文獻1提出一種藥劑溶出型支架,其於包含金屬或高分子材料之支架本體之表面塗佈有包含具有40,000~600,000分子量之生物吸收性聚合物及西洛他唑之混合物而包含西洛他唑(參照申請專利範圍及第[0015]段等)。進而,專利文獻1揭示:該支架於支架留置後之炎症過程或內膜肥厚形成過程中發生再狹窄之時期使藥物溶出而作用於血管內細胞,從而具有有效之內膜肥厚抑制作用,可大幅度改善曾以大概率發生之支架留置後之再狹窄(參照第[0028]段)。
[先前技術文獻]
[專利文獻]
[專利文獻1]WO2016/067994
[發明所欲解決之問題]
專利文獻1所揭示之支架用於心臟冠狀動脈等相對較粗之動脈等,要求作用於PTCA後之1~3天後所發生之見於單核球之黏著、浸潤之炎症過程。因此,要求專利文獻1所記載之支架自設置開始至數天之間釋出西洛他唑,發揮效果。
另一方面,近年來,由粗細度更細之末梢動脈之梗塞等所引起之末梢動脈疾病(PAD)正逐漸受到關注。例如有腳之血管發生動脈硬化,血管變細或堵塞,無法向腳流入充分之血液之疾病。因此,會出現步行時腳麻木、疼痛、寒冷等症狀。若疾病發展,則變得無法行走(間歇性跛行),或即便一動不動腳亦會疼痛。若進一步惡化,則亦存在腳會潰瘍或壞死之情形,於嚴重之情形時,亦存在必須對腳進行手術之情形。
即便PAD為僅顯示手腳之症狀者,動脈硬化亦可能不限於手腳而波及身體中之血管。若對PAD置之不理,則亦有引起心肌梗塞、心絞痛、及腦梗塞等之可能性。針對PAD,有藥物療法、理學療法、及手術等各種對應病狀之發展及治療目標之治療法。若可實現末梢動脈用之藥物留置型支架,則可提供低侵入地治療PAD之新穎之治療方法。
本發明者等人進行了各種研究,結果認為,需要可使有效成分相較心臟冠狀動脈用藥物留置型支架(例如,專利文獻1)更長期(例如,6~12個月)存在於病態血管動脈中之支架。
本發明之目的在於提供一種可使有效成分更長期(例如,6~12個月)存在於病態血管中之藥物留置型支架。此種藥物留置型支架可良好地用於末梢血管(例如,末梢動脈血管)之治療,可提供一種更加低侵入之治療方法。
[解決問題之技術手段]
本發明者等人反覆銳意研究,結果發現可獲得一種藥物留置型支架,其具有於支架骨架上堆疊了複數層之堆疊層,堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物,且對於上述晶質西洛他唑於活體外對溶出率進行試驗,於24小時後溶出5質量%以下之晶質西洛他唑。進而發現,此種藥物留置型支架適合用於末梢血管,從而完成本發明。
本說明書包括下述態樣。
1.一種支架,其具有支架骨架、及
於支架骨架上堆疊了複數層之堆疊層,
堆疊層之各層包含晶質西洛他唑(CLZ),
上述複數層之至少1層包含生物吸收性聚合物,且
使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出5質量%以下之上述晶質西洛他唑。
2.一種支架,其具有支架骨架、及
於支架骨架上堆疊了複數層之堆疊層,
堆疊層之各層包含晶質西洛他唑(CLZ),
上述複數層之至少1層包含生物吸收性聚合物,且
使支架於活體外於37℃下與包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之15天後,溶出20質量%以下之上述晶質西洛他唑。
3.如上述1或2所記載之支架,其中堆疊層具有至少2層,離支架較近之第1層之西洛他唑含量大於離支架較遠之第2層之西洛他唑含量。
4.如上述1至3中任一項所記載之支架,其中堆疊層具有至少2層,離支架較近之第1層之西洛他唑含量大於離支架較遠之第2層之西洛他唑含量,且2層皆包含生物吸收性聚合物。
5.如上述1至4中任一項所記載之支架,其中生物吸收性聚合物包含90質量%以上之聚乳酸。
6.如上述1至5中任一項所記載之支架,其中生物吸收性聚合物以6:4~8:2之質量比率包含L丙交酯與DL丙交酯,且具有1.8~4.5 dL/g之黏度。
7.如上述1至5中任一項所記載之支架,其中生物吸收性聚合物包含90質量%以上之L丙交酯,且具有0.6~1.4 dL/g之黏度。
8.如上述1至7中任一項所記載之支架,其用於末梢血管用。
9.一種支架,其包括支架骨架、
堆疊於支架骨架上之第1層、及堆疊於其上之第2層,
第1層及第2層分別包含西洛他唑及生物吸收性聚合物,
上述生物吸收性聚合物以6:4~8:2之質量比率包含L丙交酯與DL丙交酯,且具有1.8~4.5 dL/g之黏度,且
第1層包含470±47 μg之西洛他唑及313±31 μg之上述生物吸收性聚合物,第2層包含30±3 μg之西洛他唑及270±27 μg之上述生物吸收性聚合物。
[發明之效果]
本發明之實施形態之藥物留置型支架中,於活體外對晶質西洛他唑溶出率進行試驗,於24小時後可溶出5質量%以下。因此,本發明之實施形態之藥物留置型支架可使結晶性西洛他唑更長期地釋出,可更良好地用於末梢血管用。
本發明之一實施形態之支架具有
支架骨架、及
於支架骨架上堆疊了複數層之堆疊層,
堆疊層之各層包含晶質西洛他唑,
上述複數層之至少1層包含生物吸收性聚合物,且
使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出5質量%以下之上述晶質西洛他唑。
本發明之另一實施形態之支架具有
支架骨架、及
於支架骨架上堆疊了複數層之堆疊層,
堆疊層之各層包含晶質西洛他唑,
上述複數層之至少1層包含生物吸收性聚合物,且
使支架於活體外於37℃下與包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之15天後,溶出20質量%以下之上述晶質西洛他唑。
本發明之進一步之實施形態之支架包括
支架骨架、
堆疊於支架骨架上之第1層、及堆疊於其上之第2層,
第1層及第2層分別包含西洛他唑及生物吸收性聚合物,
上述生物吸收性聚合物以6:4~8:2之質量比率包含L丙交酯與DL丙交酯,且具有1.8~4.5 dL/g之黏度,且
第1層包含470±47 μg之西洛他唑及313±31 μg之上述生物吸收性聚合物,第2層包含30±3 μg之西洛他唑及270±27 μg之上述生物吸收性聚合物。
本發明之實施形態之支架具有支架骨架、及於該支架骨架上堆疊了複數層之堆疊層。
於本發明之實施形態中,「支架骨架」意指形成支架之骨架,通常例如使用金屬或高分子材料形成為粗孔之圓筒狀,只要可獲得本發明之目標支架即可,無特別限制。
作為金屬製之支架骨架,例如可例示鎳、鈷、鉻、鈦、及不鏽鋼等適當之合金製之支架骨架,較佳為以鈷鉻合金為主成分之金屬製支架骨架。
本發明之實施形態之支架具有於其支架骨架上堆疊了複數層之堆疊層。該堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物。
於本說明書中,「西洛他唑」係化學名為6-[4-(1-環己基-1H-四唑-5-基)丁氧基]-3,4-二氫喹諾酮。已知西洛他唑具有血小板凝集抑制作用、磷酸二酯酶(PDE)之阻礙作用、抗潰瘍作用、降壓作用及消炎作用,作為抗血栓症劑、腦循環改善劑、消炎劑、抗潰瘍劑、降壓劑、平喘劑、磷酸二酯酶阻礙劑等有用,只要可獲得本發明之目標支架即可,無特別限制。再者,西洛他唑亦包含其醫藥上可容許之鹽。
又,西洛他唑較佳為結晶。具有結晶結構之西洛他唑由於相較不具有結晶結構(非結晶)之西洛他唑可將溶出率抑制得較低,故而較佳。
於本發明之實施形態中,生物吸收性聚合物只要可獲得本發明之目標支架即可,無特別限制。作為生物吸收性聚合物,例如可列舉包含丙交酯之聚乳酸等,其分子量(Mw:重量平均分子量)可為40,000至700,000。又,其黏度可為0.4~5.0 dL/g,亦可為0.4~4.2 dL/g。進而,生物吸收性聚合物包含DL丙交酯、L丙交酯等,亦可包含乙交酯、己內酯等。更具體而言,可例示:分子量為10,000~1,000,000之包含DL丙交酯之聚合物、以6:4~8:2之質量比率包含L丙交酯與DL丙交酯且分子量為300,000~650,000或黏度為1.8~4.5 dL/g之聚合物、分子量為50,000~150,000或包含90質量%以上之L丙交酯且黏度為0.6~1.4 dL/g之聚合物(包含100質量%之L丙交酯之聚L乳酸)。作為生物吸收性聚合物,可使用市售品,例如可例示LR704S(商品名)、L206S(商品名)、LR706S(商品名)等。生物吸收性聚合物可單獨使用或組合使用。
生物吸收性聚合物較佳為包含90質量%以上之聚乳酸,更佳為包含93質量%以上,進而更佳為包含96質量%。於生物吸收性聚合物包含90質量%以上之聚乳酸之情形時,發揮能夠緩釋之有利效果。
較佳為堆疊層具有至少2層,離支架骨架較近之第1層之西洛他唑含量大於離支架骨架較遠之第2層之西洛他唑含量。於離支架骨架更近之層之西洛他唑之含量更大之情形時,發揮長時間緩釋之有利效果。
第1層之西洛他唑之含量較佳為300~750 μg,更佳為350~550 μg,進而較佳為440~480 μg。進而,第1層較佳為包含470±47 μg之西洛他唑。
第2層之西洛他唑之含量較佳為0~100 μg,更佳為10~80 μg,進而較佳為20~60 μg。進而,第2層亦較佳為包含30±3 μg之西洛他唑。
第1層之西洛他唑之含有率較佳為40~100質量%,更佳為50~70質量%,進而較佳為55~65質量%。
第2層之西洛他唑之含有率較佳為0~50質量%,更佳為2~20質量%,進而較佳為5~10質量%。
較佳為堆疊層具有至少2層,離支架較近之第1層之西洛他唑含量大於離支架較遠之第2層之西洛他唑含量,且2層皆包含生物吸收性聚合物。
第1層之生物吸收性聚合物之含量較佳為0~500 μg,更佳為250~350 μg,進而較佳為300~320 μg。進而,第1層較佳為包含313±31 μg之生物吸收性聚合物。
第2層之生物吸收性聚合物之含量較佳為180~540 μg,更佳為200~300 μg,進而較佳為260~285 μg。進而,第2層較佳為包含270±27 μg之生物吸收性聚合物。
第1層之生物吸收性聚合物之含有率較佳為0~60質量%,更佳為25~50質量%,進而較佳為35~45質量%。
第2層之生物吸收性聚合物之含有率較佳為70質量%以上,更佳為80質量%以上,進而較佳為90質量%以上。
於本發明之實施形態之支架中,於活體外使支架與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出3質量%以下之上述晶質西洛他唑。
於本發明之實施形態之支架中,較佳為於活體外使支架於37℃下與包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之15天後,溶出20質量%以下之上述晶質西洛他唑,較佳為使支架接觸後之8天後,溶出7質量%以下之上述晶質西洛他唑,較佳為使支架接觸後之1天後,溶出5質量%以下之上述晶質西洛他唑,更佳為溶出3質量%以下之上述晶質西洛他唑。
於本發明之實施形態之支架中,於活體外使支架於37℃下與包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之15天後,可溶出例如1.0質量%以上之上述晶質西洛他唑,亦可溶出0.1質量%以上之上述晶質西洛他唑,使支架接觸後之8天後,可溶出例如0.5質量%以上之上述晶質西洛他唑,亦可溶出0.05質量%以上之上述晶質西洛他唑,使支架接觸後之1天後,可溶出例如0.1質量%以上之上述晶質西洛他唑,亦可溶出0.01質量%以上之上述晶質西洛他唑。
於在活體外使支架與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之上述時間後,溶出上述比率以下之上述晶質西洛他唑之情形時,可釋出西洛他唑超過3個月,因此,可使西洛他唑極長時間地存在於生物內部。
因此,本發明之實施形態之支架可良好地用作例如末梢血管用,較佳為可良好地用作末梢動脈血管用。
進而,本發明之實施形態之支架亦可用於例如心臟之冠狀動脈、下肢動脈等先前使用支架之相對較粗之動脈等。
只要可獲得本發明之目標支架,則本發明之實施形態之支架之製造方法無特別限制。
本發明之實施形態之支架例如可使用如下之製造方法進行製造,該製造方法包括:(i)準備支架骨架;(ii)準備包含西洛他唑之混合物;(iii)使用該混合物塗佈支架骨架;及反覆進行(ii)及(iii)(其中,調整西洛他唑之含量等)。
包含西洛他唑之混合物除了包含西洛他唑以外,亦可包含上述生物吸收性聚合物。混合物進而可包含添加劑等溶劑。由於西洛他唑為難溶性,故而生物吸收性聚合物需要防止塗佈之剝離且維持高強度。
西洛他唑與生物吸收性聚合物例如聚乳酸之混合質量比率較佳為1:0.5~1:1.5。於為該比率之範圍內之情形時,可獲得更加良好之內膜肥厚效果。又,於混合質量比率為1:1.1~1:1.5之情形時,可更加提高塗佈強度及緩釋之效果。
於本發明之實施形態中,將西洛他唑與生物吸收性聚合物之混合物塗佈於支架骨架之方法只要可獲得本發明之目標支架即可,無特別限制,可使用先前所使用之例如簡易噴霧法、浸漬法、電沈積法、超音波噴霧法等,就塗佈之方面而言,較佳為使用超音波噴霧法。
再者,上述實施形態只要可能,則可進行適當組合。
以下,對於本發明之實施形態,一面參照圖式,一面詳細地進行說明。
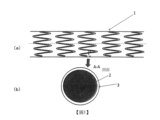
圖1(a)模式性地表示本發明之一形態之藥劑溶出型支架1。藥劑溶出型支架1具備具有長度方向軸線之圓筒狀之形態,具有管腔。關於圓筒狀之形態,藥劑溶出型支架1具有較粗之網眼狀之側面,形成為可向側方擴張。通常,網眼可藉由形成支架骨架之構件2(金屬或高分子材料等之線)形成。藥劑溶出型支架1通常係以未擴張形態插入至身體內,並於血管內之治療部位擴張而留置於該血管內。擴張亦可藉由氣球導管而於血管內達成。於圖1(a)中,模式性地記載有網眼。只要可獲得本發明之目標支架,則網眼狀之圖案無特別限制。
圖1(b)模式性地表示圖1(a)中之形成支架骨架之線之剖面(A-A剖面)。
本發明之一形態之藥劑溶出型支架1於支架骨架構件2上形成有堆疊層3。支架骨架構件2可使用任意之方法製作。例如,可藉由雷射、放電銑削加工、化學蝕刻或其他手段,由中空或形成之不鏽鋼管製作。支架骨架構件2可藉由鎳、鈷、鉻、鈦或不鏽鋼之適當之合金等而形成。
堆疊層3由至少兩層形成。於圖1(b)中,未顯示複數層。
圖2模式性地表示於支架骨架構件2上塗佈形成堆疊層3之超音波噴霧塗佈裝置4。於塗佈步驟中,首先,較佳為藉由電漿處理裝置(未圖示)於塗佈步驟前對支架骨架構件2之表面進行電漿處理。電漿處理後,將支架骨架構件2安裝於心軸,安裝於超音波噴霧塗佈裝置4。於超音波噴霧塗佈裝置4中,塗佈液藉由注射泵通過配管6進行輸送,藉由超音波噴霧噴嘴5被霧化而噴射。於噴霧中,使支架骨架構件2於超音波噴嘴5下一面旋轉一面直線移動,藉此使堆疊層3堆疊於支架骨架構件2上。其後,一面使支架骨架構件2旋轉一面直線移動,同時於氮氣氣流下進行乾燥,進而於減壓下於乾燥器中進行乾燥,藉此可製作藥劑溶出型支架1。根據堆疊層3所包含之層數而變更塗佈液,支架骨架構件經複數次塗佈而形成堆疊層3。
使用使西洛他唑與生物吸收性聚合物以與應形成之堆疊層3對應之比率溶於溶劑中而成的混合物,準備塗佈液。由於堆疊層3包含複數層,故而需要準備複數種塗佈液。作為塗佈溶劑,可使用沸點較低之揮發性溶劑以於塗佈後可容易去除。作為揮發性溶劑,例如可例示:甲醇、乙醇、三氟乙醇、六氟異丙醇、異戊醇、乙酸甲酯、乙酸乙酯、丙酮、甲基乙基酮、二氯甲烷、氯仿、二氯乙烷、及包含該等之中至少2種之混合溶劑。
[實施例]
以下,藉由實施例及比較例,具體且詳細地對本發明進行說明,該等實施例僅為本發明之一態樣,本發明並不受該等例任何限定。
將本實施例中所使用之各種聚合物示於下述表1。
[表1]
| 聚合物 | 黏度(dL/g) | 分子量 (Mw:重量平均分子量) | 組成 L:L-丙交酯 DL:DL-丙交酯 G:糖苷 C:己內酯 |
| (a) L206S | 0.8-1.2 | 102,000 | L=100 |
| (b) LR704S | 2.0-2.8 | >350,000 | L:DL=70:30 |
| (c) LR706S | 3.3-4.2 | >630,000 | L:DL=70:30 |
| (d) RG755S | 0.50-0.70 | 63,000 | DL:G=75:25 |
| (e) RG858S | 1.3-1.7 | 220,000 | DL:G=85:15 |
| (f) LC703S | 1.3-1.8 | 257,000 | L:C=70:30 |
上述聚合物之黏度意指極限黏度[η](dL/g),藉由毛細管黏度計法進行測定。極限黏度係準備濃度C(g/dL)之試樣溶液,根據該試樣溶液之流下時間(t)及溶劑之流下時間(t0
)之測定值,藉由下式而計算。
[數1]
使用烏氏黏度計作為裝置,使用氯仿(25℃)作為溶劑。
進而,使用Mark-Kuhn-Houwink之式(Mark-Howink-Sakurada之式),求出重量平均分子量(Mw)。
實施例1
使用鈷鉻合金作為支架骨架構件2,準備將西洛他唑(CLZ)溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於作為基底材料之鈷鉻合金上,形成藉由440 μg之西洛他唑形成之第1層。
其次,準備將西洛他唑與聚合物(a)以1:9(質量比)加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於第1層上,形成藉由540 μg之聚合物(a)與60 μg之西洛他唑形成之第2層,從而獲得實施例1之支架。
實施例2~3
將聚合物(a)變更為聚合物(b)或(c),除此以外,使用與實施例1所記載之方法相同之方法,製造實施例2~3之支架。
比較例1~3
將聚合物(a)變更為聚合物(d)~(f),除此以外,使用與實施例1所記載之方法相同之方法,製造比較例1~3之支架。
實施例4
使用鈷鉻合金作為支架骨架構件2,準備將西洛他唑與聚合物(b)以3:2之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於支架骨架構件之鈷鉻合金上,形成藉由313 μg之聚合物(b)與470 μg之西洛他唑形成之第1層。
其次,準備將西洛他唑與聚合物(b)以1:9(質量比)之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於第1層上,形成藉由270 μg之聚合物(b)與30 μg之西洛他唑形成之第2層,從而獲得實施例4之支架。
實施例5
使用鈷鉻合金作為支架骨架構件2,準備將西洛他唑與聚合物(b)以3:2之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於作為基底材料之鈷鉻合金上,形成藉由323 μg之聚合物(b)與485 μg之西洛他唑形成之第1層。
其次,準備將西洛他唑與聚合物(b)以1:19(質量比)之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於第1層上,形成藉由285 μg之聚合物(b)與15 μg之西洛他唑形成之第2層,從而獲得實施例5之支架。
實施例6
使用鈷鉻合金作為支架骨架構件2,準備將西洛他唑與聚合物(b)以3:2之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於作為基底材料之鈷鉻合金上,形成藉由313 μg之聚合物(b)與470 μg之西洛他唑形成之第1層。
其次,準備將西洛他唑與聚合物(c)以1:9(質量比)之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於第1層上,形成藉由270 μg之聚合物(c)與30 μg之西洛他唑形成之第2層,從而獲得實施例6之支架。
實施例7
使用鈷鉻合金作為支架骨架構件2,準備將西洛他唑與聚合物(b)以3:2之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於作為基底材料之鈷鉻合金上,形成藉由490 μg之聚合物(b)與735 μg之西洛他唑形成之第1層。
其次,準備將西洛他唑與聚合物(b)以1:19(質量比)之比率加以混合並溶解於二氯甲烷而成之溶液。藉由超音波噴霧塗佈將該溶液塗佈於第1層上而形成藉由285 μg之聚合物(b)與15 μg之西洛他唑形成之第2層,從而獲得實施例7之支架。
實施例8
形成藉由180 μg之聚合物(b)與270 μg之西洛他唑而形成之第1層,除此以外,使用與實施例4所記載之方法相同之方法,獲得實施例8之支架。
實施例9
形成藉由247 μg之聚合物(b)與370 μg之西洛他唑而形成之第1層,除此以外,使用與實施例4所記載之方法相同之方法,獲得實施例9之支架。
西洛他唑之溶出試驗(活體外)
1.西洛他唑之溶出試驗方法
使用溶出試驗器400-DS(Apparatus 7),試驗液使用10 mL之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液,於將溶出試驗液之溫度設為37℃、浸漬速度10之條件下進行試驗。
於0.5、1、3、6、9、12、18、24小時後進行取樣,每個採取時間對試驗液進行全量更換。
2.西洛他唑之溶出率測定(HPLC測定)
於以下之條件下對10 μL之各試樣溶液及標準溶液進行HPLC測定,根據西洛他唑之峰面積值AT
及As
計算溶出率。
溶出率之計算使用以下之式進行計算。
[數2]
1個支架中之西洛他唑之顯示量(C)使用根據塗佈質量所計算出之西洛他唑搭載量。
| Q:與西洛他唑顯示量對應之Q小時之溶出率(質量%) |
| MS :西洛他唑標準品之稱取量(mg) |
| AT :i小時後取樣之西洛他唑之峰面積 |
| AS :標準溶液之峰面積 |
| C:1個支架中之西洛他唑之顯示量(≒西洛他唑搭載量) |
| A:常數(0.5) |
| :p小時後至Q小時後之西洛他唑之峰面積之和 |
測定條件
檢測器:紫外線吸光光度計(測定波長:254 nm)
管柱:於內徑4.6 mm×長度150 mm之不鏽鋼管中填充有5 μm之液相層析法用十八烷基矽烷基化矽膠
管柱溫度:25℃附近之固定溫度
移動相:水/乙腈/甲醇混液(10:7:3,v/v/v)
流量:以西洛他唑之保持時間約為9分鐘之方式調整
藉由埋入兔髂骨動脈測得之動脈組織中之西洛他唑濃度及支架上之西洛他唑殘存量(活體內)
將實施例及比較例之各支架埋入至兔髂骨動脈。埋入係如下所述進行。
首先,切開兔之頸部,露出右頸動脈,留置導引器(introducer)。將氣球導管用導絲自導引器插入,於X射線透視下,移動至髂骨動脈之處理部位之遠端部。其後,沿著導絲插入造影用導管,進行髂骨動脈之處理部位之血管造影。處理部位之血管造影結束後,於X射線透視下,沿著氣球導管用導絲將檢體之氣球導管插入至處理部位。確認檢體之支架(標準徑擴張壓力為9 atm時支架徑為2.75 mm)位於髂骨動脈之處理部(預定血管徑為2.5 mm)後,使用充氣裝置(indeflator)以14 atm(過擴張,預定支架徑為3.0 mm,20質量%過擴張)以1次20秒使氣球保持擴張,確認支架擴張後,使氣球收縮,卸下充氣裝置,沿著氣球導管用導絲拔出氣球導管。使用相同之方法對左右之髂骨動脈進行處理。
其次,沿著氣球導管用導絲使造影用導管移動至處理部位之近前,使用稀釋造影劑進行血管造影。使用相同之方法對左右之髂骨動脈進行處理後,拔出造影用導管。最後,對鞘插入部位之血管進行結紮,對皮膚和肌肉層進行縫合。藉由以上而於兔之髂骨血管內留置支架。
自埋入起90天後,對各支架之埋入部位之動脈組織中之西洛他唑濃度及支架殘存量進行分析。
作為預處理,將各支架之埋入部位之動脈組織分離成支架及動脈組織。對由經分離之各個試樣藉由液液萃取法所獲得之有機層進行乾燥,設為試樣。對於所獲得之試樣,藉由使用電灑游離法之LC/MS/MS法(liquid chromatography-tandem mass spectrometry,液相層析-串聯質譜法),對西洛他唑進行定量,計算動脈組織中之西洛他唑濃度(1 g之組織中之西洛他唑之μg數:μg/g組織)及西洛他唑殘存量(支架上之西洛他唑之殘存率(%))。
藉由埋入豬髂骨動脈測得之動脈組織中之西洛他唑濃度及支架上之西洛他唑殘存量(活體內)
藉由埋入豬髂骨動脈測得之動脈組織中之西洛他唑濃度及西洛他唑殘存量之評估係使用與對兔所進行方法相同之方法,對豬分析藉由埋入髂骨動脈測得之動脈組織中之西洛他唑濃度(1 g之組織中之西洛他唑之μg數:μg/g組織)及西洛他唑殘存量(支架上之西洛他唑之殘存率(%))。
[表2]
| 實施例 | 比較例 | ||||||
| 1 | 2 | 3 | 1 | 2 | 3 | ||
| 第1層 | CLZ/聚合物質量比 CLZ:μg 聚合物:μg | CLZ/聚合物=100/0 CLZ:440 聚合物:0 | CLZ/聚合物=100/0 CLZ:440 聚合物:0 | CLZ/聚合物=100/0 CLZ:440 聚合物:0 | CLZ/聚合物=100/0 CLZ:440 聚合物:0 | CLZ/聚合物=100/0 CLZ:440 聚合物:0 | CLZ/聚合物=100/0 CLZ:440 聚合物:0 |
| 第2層 | CLZ/聚合物質量比 CLZ:μg 聚合物:μg | CLZ/聚合物(a)=1/9 CLZ:60 聚合物(a):540 | CLZ/聚合物(b)=1/9 CLZ:60 聚合物(b):540 | CLZ/聚合物(c)=1/9 CLZ:60 聚合物(c):540 | CLZ/聚合物(d)=1/9 CLZ:60 聚合物(d):540 | CLZ/聚合物(e)=1/9 CLZ:60 聚合物(e):540 | CLZ/聚合物(f)=1/9 CLZ:60 聚合物(f):540 |
| 合計 | CLZ:μg | 500 | 500 | 500 | 500 | 500 | 500 |
| CLZ溶出率(%) | 24小時 | 1.7 | 3.2 | 1.1 | 51.7 | 17.3 | 39.6 |
[表3]
a:表示1 g之組織中之西洛他唑之μg數。單位為μg/g組織。
| 實施例 | |||||
| 4 | 5 | 6 | 7 | ||
| 第1層 | CLZ/聚合物質量比 CLZ:μg 聚合物:μg | CLZ/聚合物(b)=3/2 CLZ:470 聚合物:313 | CLZ/聚合物(b)=3/2 CLZ:485 聚合物:323 | CLZ/聚合物(b)=3/2 CLZ:470 聚合物:313 | CLZ/聚合物(b)=3/2 CLZ:735 聚合物:490 |
| 第2層 | CLZ/聚合物質量比 CLZ:μg 聚合物:μg | CLZ/聚合物(b)=1/9 CLZ:30 聚合物(b):270 | CLZ/聚合物(b)=1/19 CLZ:15 聚合物(b):285 | CLZ/聚合物(c)=1/9 CLZ:30 聚合物(c):270 | CLZ/聚合物(b)=1/19 CLZ:15 聚合物(b):285 |
| 合計 | CLZ:μg | 500 | 500 | 500 | 750 |
| 兔 CLZ殘存率 (%) | 1個月後 3個月後 | 100 77 | 96 89 | 88 99.8 | 100 91 |
| 豬 CLZ組織內濃度a | 3個月後 6個月後 9個月後 | 87 57 11 | 未測定 | 未測定 | 未測定 |
| 豬 CLZ殘存率(%) | 3個月後 6個月後 9個月後 | 70 38 2 | 未測定 | 未測定 | 未測定 |
| CLZ溶出率(%) | 24小時 96小時 15天 | 1.6 4.3 13.2 | 未測定 | 未測定 | 未測定 |
[表4]
a:表示1 g之組織中之西洛他唑之μg數。單位為μg/g組織。
| 實施例 | |||
| 8 | 9 | ||
| 第1層 | CLZ/聚合物質量比 CLZ:μg 聚合物:μg | CLZ/聚合物(b)=3/2 CLZ:270 聚合物:180 | CLZ/聚合物(b)=3/2 CLZ:370 聚合物:247 |
| 第2層 | CLZ/聚合物質量比 CLZ:μg 聚合物:μg | CLZ/聚合物(b)=1/9 CLZ:30 聚合物(b):270 | CLZ/聚合物(b)=1/9 CLZ:30 聚合物(b):270 |
| 合計 | CLZ:μg | 300 | 400 |
| 豬 CLZ組織內濃度a | 3個月後 6個月後 | 84 46 | 78 36 |
| 豬 CLZ殘存率(%) | 3個月後 6個月後 | 66 23 | 60 14 |
| CLZ溶出率(%) | 24小時 96小時 | 1.7 3.8 | 2.7 5.6 |
實施例1~9之支架皆具有支架骨架、及於支架骨架上堆疊了複數層之堆疊層,堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物,且使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出5質量%以下之上述晶質西洛他唑。
又,實施例1~9之支架皆具有支架骨架、及於支架骨架上堆疊了複數層之堆疊層,堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物,且使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之15天後,溶出20質量%以下之上述晶質西洛他唑。
因此,實施例1~9之支架可緩釋出西洛他唑超過3個月。
再者,作為複數層,當然並不限於2層,亦可應用3層以上。
相對於此,比較例1~3之支架皆使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出超過5質量%之晶質西洛他唑。
因此,比較例1~3之支架無法緩釋出西洛他唑超過3個月。
[產業上之可利用性]
本發明之實施形態之藥物留置型支架於活體外對晶質西洛他唑溶出率進行試驗,於24小時後可溶出5質量%以下之晶質西洛他唑。或,本發明之實施形態之藥物留置型支架於活體外對晶質西洛他唑溶出率進行試驗,於15天後可溶出20質量%以下之晶質西洛他唑。因此,本發明之實施形態之藥物留置型支架可使結晶性西洛他唑更長期地釋出,可更良好地用於末梢血管用。
[相關申請]
再者,本申請主張以2019年7月9日於日本申請之申請號2019-127529為基礎申請之基於巴黎公約第4條之優先權。該基礎申請之內容藉由參照而引入至本說明書。
1:支架
2:支架骨架構件
3:堆疊層
4:超音波噴霧塗佈裝置
5:超音波噴霧噴嘴
6:配管
圖1模式性地表示本發明之一實施形態的支架之整個形狀(a)及支架之A-A間之剖面(b)。
圖2模式性地表示使用超音波噴霧器將塗佈劑塗佈於支架之情況。
Claims (10)
- 一種藥物留置型支架,其具有支架骨架、及於支架骨架上堆疊了複數層之堆疊層,堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物,堆疊層具有至少2層,離支架較近之第1層之西洛他唑含量大於離支架較遠之第2層之西洛他唑含量,且2層皆包含生物吸收性聚合物,且使支架於活體外與37℃之包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之24小時後,溶出5質量%以下之上述晶質西洛他唑。
- 一種藥物留置型支架,其具有支架骨架、及於支架骨架上堆疊了複數層之堆疊層,堆疊層之各層包含晶質西洛他唑,上述複數層之至少1層包含生物吸收性聚合物,堆疊層具有至少2層,離支架較近之第1層之西洛他唑含量大於離支架較遠之第2層之西洛他唑含量,且2層皆包含生物吸收性聚合物,且使支架於活體外於37℃下與包含0.25質量%月桂基硫酸鈉之磷酸鹽緩衝氯化鈉溶液之溶出介質接觸後之15天後,溶出20質量%以下之上述晶質西洛他唑。
- 如請求項1之藥物留置型支架,其中生物吸收性聚合物包含90質量% 以上之聚乳酸。
- 如請求項2之藥物留置型支架,其中生物吸收性聚合物包含90質量%以上之聚乳酸。
- 如請求項1至4中任一項之藥物留置型支架,其中生物吸收性聚合物以6:4~8:2之質量比率包含L丙交酯與DL丙交酯,且具有1.8~4.5dL/g之黏度。
- 如請求項1至4中任一項之藥物留置型支架,其中生物吸收性聚合物包含90質量%以上之L丙交酯,且具有0.6~1.4dL/g之黏度。
- 如請求項1至4中任一項之藥物留置型支架,其用於末梢血管用。
- 如請求項5之藥物留置型支架,其用於末梢血管用。
- 如請求項6之藥物留置型支架,其用於末梢血管用。
- 一種藥物留置型支架,其包括支架骨架、堆疊於支架骨架上之第1層、及堆疊於其上之第2層,第1層及第2層分別包含西洛他唑及生物吸收性聚合物,上述生物吸收性聚合物以6:4~8:2之質量比率包含L丙交酯與DL丙交酯,且具有1.8~4.5dL/g之黏度,且 第1層包含470±47μg之西洛他唑及313±31μg之上述生物吸收性聚合物,第2層包含30±3μg之西洛他唑及270±27μg之上述生物吸收性聚合物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019-127529 | 2019-07-09 | ||
| JP2019127529 | 2019-07-09 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| TW202116317A TW202116317A (zh) | 2021-05-01 |
| TWI794616B true TWI794616B (zh) | 2023-03-01 |
Family
ID=74113786
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW109123057A TWI794616B (zh) | 2019-07-09 | 2020-07-08 | 藥劑溶出型支架 |
| TW112105824A TW202322815A (zh) | 2019-07-09 | 2020-07-08 | 藥劑溶出型支架 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW112105824A TW202322815A (zh) | 2019-07-09 | 2020-07-08 | 藥劑溶出型支架 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US11806257B2 (zh) |
| EP (1) | EP3998049B1 (zh) |
| JP (2) | JP7033694B2 (zh) |
| CN (1) | CN114051417A (zh) |
| MX (2) | MX2022000389A (zh) |
| TW (2) | TWI794616B (zh) |
| WO (1) | WO2021006291A1 (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2023038112A1 (zh) * | 2021-09-10 | 2023-03-16 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN204542477U (zh) * | 2015-02-10 | 2015-08-12 | 东莞颠覆产品设计有限公司 | 一种多层可扩张血管支架 |
| CN107106309A (zh) * | 2014-10-28 | 2017-08-29 | 株式会社Jimro | 药物洗脱支架 |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5824048A (en) | 1993-04-26 | 1998-10-20 | Medtronic, Inc. | Method for delivering a therapeutic substance to a body lumen |
| WO2004002367A1 (fr) | 2002-06-27 | 2004-01-08 | Microport Medical (Shanghai) Co., Ltd. | Stent eluant des medicaments |
| CN100471469C (zh) * | 2002-06-27 | 2009-03-25 | 微创医疗器械(上海)有限公司 | 一种具有多层涂层的药物洗脱支架 |
| US7318945B2 (en) | 2003-07-09 | 2008-01-15 | Medtronic Vascular, Inc. | Laminated drug-polymer coated stent having dipped layers |
| EP1792582B1 (en) | 2004-09-08 | 2018-04-04 | Kaneka Corporation | Indwelling stent |
| KR100511618B1 (ko) * | 2005-01-17 | 2005-08-31 | 이경범 | 약물방출 조절형 다층 코팅 스텐트 및 이의 제조방법 |
| KR101265625B1 (ko) * | 2006-09-11 | 2013-05-22 | 엘지전자 주식회사 | 멀티 채널을 정의하는 방송 신호를 처리하는 방송 수신기 및 그 제어방법 |
| MX2009008064A (es) | 2007-01-30 | 2009-08-07 | Hemoteq Ag | Soporte vascular biodegradable. |
| CN101641059B (zh) * | 2007-02-14 | 2011-10-19 | 山东瑞安泰医疗技术有限公司 | 一种不对称药物控释涂层冠脉内支架 |
| EP2201966A4 (en) | 2007-09-04 | 2013-06-26 | Japan Stent Technology Co Ltd | STENT FOR THE CONTROLLED RELEASE OF MEDICAMENTS |
| US8067111B2 (en) * | 2008-06-30 | 2011-11-29 | Lg Chem, Ltd. | Battery module having battery cell assembly with heat exchanger |
| US20100241220A1 (en) | 2009-03-23 | 2010-09-23 | Mcclain James B | Peripheral Stents Having Layers |
| US20100280600A1 (en) | 2009-04-30 | 2010-11-04 | Vipul Bhupendra Dave | Dual drug stent |
| US20120130481A1 (en) | 2010-11-18 | 2012-05-24 | Robert Falotico | Local vascular delivery of adenosine a2a receptor agonists in combination with other agents to reduce myocardial injury |
| JP5784940B2 (ja) | 2011-03-18 | 2015-09-24 | テルモ株式会社 | 薬剤溶出ステント |
| KR101903443B1 (ko) * | 2012-02-02 | 2018-10-02 | 삼성전자주식회사 | 멀티미디어 통신 시스템에서 장면 구성 정보 송수신 장치 및 방법 |
| EP2911712B1 (en) | 2012-10-25 | 2017-11-29 | Boston Scientific Scimed, Inc. | Stent having a tacky silicone coating to prevent stent migration |
| TWI697337B (zh) | 2013-08-07 | 2020-07-01 | 學校法人近畿大學 | 奈米粒子或奈米粒子組成物之製造方法,及支架或球囊導管之製造方法 |
| CN203829101U (zh) | 2014-05-05 | 2014-09-17 | 加奇生物科技(上海)有限公司 | 颅内药物洗脱支架 |
| CN103948458A (zh) | 2014-05-05 | 2014-07-30 | 加奇生物科技(上海)有限公司 | 颅内药物洗脱支架 |
| US9475326B2 (en) * | 2014-09-09 | 2016-10-25 | Trodat Gmbh | Removable die plate for self-inking stamps |
| EP3421253B1 (en) * | 2017-06-28 | 2019-07-31 | HID Global Rastede GmbH | Thermochromic window |
| JP7142405B2 (ja) | 2018-01-24 | 2022-09-27 | 出光興産株式会社 | 潤滑油組成物及び冷凍機用組成物 |
-
2020
- 2020-07-08 TW TW109123057A patent/TWI794616B/zh active
- 2020-07-08 EP EP20837247.4A patent/EP3998049B1/en active Active
- 2020-07-08 TW TW112105824A patent/TW202322815A/zh unknown
- 2020-07-08 JP JP2021530714A patent/JP7033694B2/ja active Active
- 2020-07-08 WO PCT/JP2020/026688 patent/WO2021006291A1/ja unknown
- 2020-07-08 US US17/597,449 patent/US11806257B2/en active Active
- 2020-07-08 CN CN202080048831.XA patent/CN114051417A/zh active Pending
- 2020-07-08 MX MX2022000389A patent/MX2022000389A/es unknown
-
2022
- 2022-01-07 MX MX2023001542A patent/MX2023001542A/es unknown
- 2022-02-28 JP JP2022029319A patent/JP7200412B2/ja active Active
-
2023
- 2023-09-12 US US18/465,332 patent/US20230414383A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107106309A (zh) * | 2014-10-28 | 2017-08-29 | 株式会社Jimro | 药物洗脱支架 |
| CN204542477U (zh) * | 2015-02-10 | 2015-08-12 | 东莞颠覆产品设计有限公司 | 一种多层可扩张血管支架 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2021006291A1 (zh) | 2021-01-14 |
| US20220160525A1 (en) | 2022-05-26 |
| EP3998049B1 (en) | 2024-08-21 |
| JP7033694B2 (ja) | 2022-03-10 |
| CN114051417A (zh) | 2022-02-15 |
| TW202322815A (zh) | 2023-06-16 |
| EP3998049A1 (en) | 2022-05-18 |
| EP3998049A4 (en) | 2023-06-28 |
| US11806257B2 (en) | 2023-11-07 |
| MX2022000389A (es) | 2023-02-07 |
| JP7200412B2 (ja) | 2023-01-06 |
| MX2023001542A (es) | 2023-04-10 |
| JP2022078154A (ja) | 2022-05-24 |
| US20230414383A1 (en) | 2023-12-28 |
| TW202116317A (zh) | 2021-05-01 |
| WO2021006291A1 (ja) | 2021-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5636451B2 (ja) | 薬剤徐放性ステント | |
| EP1518517B1 (en) | Drug-delivery endovascular stent | |
| US7682387B2 (en) | Drug-delivery endovascular stent and method for treating restenosis | |
| US20040024450A1 (en) | Drug-delivery endovascular stent and method for treating restenosis | |
| EP2111818B1 (en) | Intracoronary stent with asymmetric drug releasing controlled coating | |
| JPWO2006027994A1 (ja) | 生体留置用ステント | |
| US20230414383A1 (en) | Drug-eluting stent including crystalline cilostazol | |
| CN101195048A (zh) | 一种复合药物洗脱支架及其制备方法 | |
| CN101081316A (zh) | 一种新型药物洗脱支架 | |
| KR20050092757A (ko) | 생체 유치용 스텐트 | |
| TWI721956B (zh) | 藥劑溶出型支架 | |
| CN112263360A (zh) | 生物体内药物洗脱支架和制备方法 | |
| KR101860877B1 (ko) | 자가 확장형 약물 방출 스캐폴드 | |
| JP2002193838A (ja) | 体内埋め込み医療材料および体内埋め込み医療器具 |