RU2799554C1 - Новый пробиотический препарат на основе консорциума спорообразующих бактерий для аквакультуры и животных и способ его получения - Google Patents
Новый пробиотический препарат на основе консорциума спорообразующих бактерий для аквакультуры и животных и способ его получения Download PDFInfo
- Publication number
- RU2799554C1 RU2799554C1 RU2022108049A RU2022108049A RU2799554C1 RU 2799554 C1 RU2799554 C1 RU 2799554C1 RU 2022108049 A RU2022108049 A RU 2022108049A RU 2022108049 A RU2022108049 A RU 2022108049A RU 2799554 C1 RU2799554 C1 RU 2799554C1
- Authority
- RU
- Russia
- Prior art keywords
- vkpm
- bacillus
- strains
- probiotic
- aquaculture
- Prior art date
Links
- 239000006041 probiotic Substances 0.000 title claims abstract description 56
- 235000018291 probiotics Nutrition 0.000 title claims abstract description 56
- 230000000529 probiotic effect Effects 0.000 title claims abstract description 43
- 244000144974 aquaculture Species 0.000 title claims abstract description 16
- 238000009360 aquaculture Methods 0.000 title claims abstract description 16
- 241000894006 Bacteria Species 0.000 title claims abstract description 10
- 238000004519 manufacturing process Methods 0.000 title claims description 11
- 238000000034 method Methods 0.000 title abstract description 8
- 241001465754 Metazoa Species 0.000 title description 9
- 241000194103 Bacillus pumilus Species 0.000 claims abstract description 25
- 241000012248 Bacillus toyonensis Species 0.000 claims abstract description 25
- 238000002360 preparation method Methods 0.000 claims abstract description 20
- 239000012141 concentrate Substances 0.000 claims abstract description 16
- 208000031513 cyst Diseases 0.000 claims abstract description 16
- 241000238582 Artemia Species 0.000 claims abstract description 15
- 241000238557 Decapoda Species 0.000 claims abstract description 13
- 229920002774 Maltodextrin Polymers 0.000 claims abstract description 13
- 239000005913 Maltodextrin Substances 0.000 claims abstract description 13
- 229940035034 maltodextrin Drugs 0.000 claims abstract description 13
- 239000002028 Biomass Substances 0.000 claims abstract description 9
- 238000002156 mixing Methods 0.000 claims abstract description 9
- 238000000855 fermentation Methods 0.000 claims abstract description 8
- 230000004151 fermentation Effects 0.000 claims abstract description 8
- 239000000945 filler Substances 0.000 claims abstract description 8
- 239000012531 culture fluid Substances 0.000 claims abstract description 5
- 241000238426 Anostraca Species 0.000 claims abstract description 4
- 238000004108 freeze drying Methods 0.000 claims abstract description 4
- 230000000959 cryoprotective effect Effects 0.000 claims abstract description 3
- 238000007710 freezing Methods 0.000 claims abstract 2
- 230000008014 freezing Effects 0.000 claims abstract 2
- 229940079593 drug Drugs 0.000 claims description 8
- 239000003814 drug Substances 0.000 claims description 8
- 230000003042 antagnostic effect Effects 0.000 abstract description 14
- 244000005700 microbiome Species 0.000 abstract description 14
- 238000011534 incubation Methods 0.000 abstract description 10
- 230000000694 effects Effects 0.000 abstract description 7
- 230000001717 pathogenic effect Effects 0.000 abstract description 5
- 239000000126 substance Substances 0.000 abstract description 2
- 241000588724 Escherichia coli Species 0.000 description 16
- 239000000047 product Substances 0.000 description 15
- 244000052616 bacterial pathogen Species 0.000 description 11
- 230000001580 bacterial effect Effects 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 8
- 241000218588 Lactobacillus rhamnosus Species 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 235000014469 Bacillus subtilis Nutrition 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- 230000018109 developmental process Effects 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- 235000015097 nutrients Nutrition 0.000 description 6
- 241000251468 Actinopterygii Species 0.000 description 5
- 244000063299 Bacillus subtilis Species 0.000 description 5
- 230000008092 positive effect Effects 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 241000238580 Artemia franciscana Species 0.000 description 4
- 241000222122 Candida albicans Species 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N Lactic Acid Natural products CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 4
- 241000191967 Staphylococcus aureus Species 0.000 description 4
- 229940095731 candida albicans Drugs 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- 210000000936 intestine Anatomy 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 241000193749 Bacillus coagulans Species 0.000 description 3
- 241001327110 Macrobrachium rosenbergii Species 0.000 description 3
- 230000008485 antagonism Effects 0.000 description 3
- 229940041514 candida albicans extract Drugs 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 244000005709 gut microbiome Species 0.000 description 3
- 230000012447 hatching Effects 0.000 description 3
- 230000001418 larval effect Effects 0.000 description 3
- 244000000010 microbial pathogen Species 0.000 description 3
- 244000005706 microflora Species 0.000 description 3
- 235000013379 molasses Nutrition 0.000 description 3
- 244000052769 pathogen Species 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 239000012138 yeast extract Substances 0.000 description 3
- 241000238567 Artemia parthenogenetica Species 0.000 description 2
- 241000194108 Bacillus licheniformis Species 0.000 description 2
- 241000238424 Crustacea Species 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 241000231626 Poecilia latipinna Species 0.000 description 2
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 241000293869 Salmonella enterica subsp. enterica serovar Typhimurium Species 0.000 description 2
- 241000607760 Shigella sonnei Species 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 240000008042 Zea mays Species 0.000 description 2
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 2
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 244000309464 bull Species 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 235000005822 corn Nutrition 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 239000004310 lactic acid Substances 0.000 description 2
- 235000014655 lactic acid Nutrition 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 229940115939 shigella sonnei Drugs 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 239000012137 tryptone Substances 0.000 description 2
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- DBTMGCOVALSLOR-UHFFFAOYSA-N 32-alpha-galactosyl-3-alpha-galactosyl-galactose Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(OC2C(C(CO)OC(O)C2O)O)OC(CO)C1O DBTMGCOVALSLOR-UHFFFAOYSA-N 0.000 description 1
- 241000607528 Aeromonas hydrophila Species 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 241001600449 Amphiprion ocellaris Species 0.000 description 1
- 241000334163 Amphiprion percula Species 0.000 description 1
- 241000238569 Artemia sp. Species 0.000 description 1
- 240000002900 Arthrospira platensis Species 0.000 description 1
- 235000016425 Arthrospira platensis Nutrition 0.000 description 1
- 241000193830 Bacillus <bacterium> Species 0.000 description 1
- 235000016068 Berberis vulgaris Nutrition 0.000 description 1
- 241000335053 Beta vulgaris Species 0.000 description 1
- 241001134770 Bifidobacterium animalis Species 0.000 description 1
- 241000186016 Bifidobacterium bifidum Species 0.000 description 1
- 241000208365 Celastraceae Species 0.000 description 1
- 240000001817 Cereus hexagonus Species 0.000 description 1
- 244000298479 Cichorium intybus Species 0.000 description 1
- 235000007542 Cichorium intybus Nutrition 0.000 description 1
- 241000193468 Clostridium perfringens Species 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 206010011732 Cyst Diseases 0.000 description 1
- RXVWSYJTUUKTEA-UHFFFAOYSA-N D-maltotriose Natural products OC1C(O)C(OC(C(O)CO)C(O)C(O)C=O)OC(CO)C1OC1C(O)C(O)C(O)C(CO)O1 RXVWSYJTUUKTEA-UHFFFAOYSA-N 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 241000194031 Enterococcus faecium Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 244000020551 Helianthus annuus Species 0.000 description 1
- 241000186660 Lactobacillus Species 0.000 description 1
- 240000001046 Lactobacillus acidophilus Species 0.000 description 1
- 244000199885 Lactobacillus bulgaricus Species 0.000 description 1
- 241000186673 Lactobacillus delbrueckii Species 0.000 description 1
- 241000186840 Lactobacillus fermentum Species 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- 239000001888 Peptone Substances 0.000 description 1
- 108010080698 Peptones Proteins 0.000 description 1
- 241000831652 Salinivibrio sharmensis Species 0.000 description 1
- 235000000336 Solanum dulcamara Nutrition 0.000 description 1
- 244000057717 Streptococcus lactis Species 0.000 description 1
- 235000014897 Streptococcus lactis Nutrition 0.000 description 1
- 241000194019 Streptococcus mutans Species 0.000 description 1
- 241000607598 Vibrio Species 0.000 description 1
- 241000607618 Vibrio harveyi Species 0.000 description 1
- 241000607493 Vibrionaceae Species 0.000 description 1
- 239000005862 Whey Substances 0.000 description 1
- 102000007544 Whey Proteins Human genes 0.000 description 1
- 108010046377 Whey Proteins Proteins 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 239000003674 animal food additive Substances 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 229940118852 bifidobacterium animalis Drugs 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 229960004494 calcium gluconate Drugs 0.000 description 1
- 239000004227 calcium gluconate Substances 0.000 description 1
- 235000013927 calcium gluconate Nutrition 0.000 description 1
- NEEHYRZPVYRGPP-UHFFFAOYSA-L calcium;2,3,4,5,6-pentahydroxyhexanoate Chemical compound [Ca+2].OCC(O)C(O)C(O)C(O)C([O-])=O.OCC(O)C(O)C(O)C(O)C([O-])=O NEEHYRZPVYRGPP-UHFFFAOYSA-L 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000000378 dietary effect Effects 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 239000002655 kraft paper Substances 0.000 description 1
- 229940039696 lactobacillus Drugs 0.000 description 1
- 229940066544 lactobacillus sporogenes Drugs 0.000 description 1
- FYGDTMLNYKFZSV-UHFFFAOYSA-N mannotriose Natural products OC1C(O)C(O)C(CO)OC1OC1C(CO)OC(OC2C(OC(O)C(O)C2O)CO)C(O)C1O FYGDTMLNYKFZSV-UHFFFAOYSA-N 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 230000029052 metamorphosis Effects 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 238000009343 monoculture Methods 0.000 description 1
- 235000013557 nattō Nutrition 0.000 description 1
- 230000007918 pathogenicity Effects 0.000 description 1
- 235000019319 peptone Nutrition 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 229960002181 saccharomyces boulardii Drugs 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 229940082787 spirulina Drugs 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- FYGDTMLNYKFZSV-BYLHFPJWSA-N β-1,4-galactotrioside Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@H](CO)O[C@@H](O[C@@H]2[C@@H](O[C@@H](O)[C@H](O)[C@H]2O)CO)[C@H](O)[C@H]1O FYGDTMLNYKFZSV-BYLHFPJWSA-N 0.000 description 1
Images
Abstract
Изобретение относится к микробиологии и биотехнологии, а именно к пробиотическому препарату для аквакультуры. Пробиотический препарат для аквакультуры, а именно для цист рачка артемии и креветок, который в своем составе содержит лиофильно высушенную биомассу штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 и наполнитель мальтодекстрин в следующем соотношении, мас. %: Bacillus toyonensis - 5, Bacillus pumilus - 15, мальтодекстрин - 80, количество жизнеспособных бактерий не менее 1×1010 КОЕ/г. Способ получения пробиотического препарата для аквакультуры, а именно для цист рачка артемии и креветок, включающий раздельное культивирование штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 на мелассно-кукурузной среде в ферментационных установках при рН 6,8-7,0 и температуре 37°С, расходе воздуха 100-150 л/мин, скорости перемешивания 250-500 об/мин; рО2 - 30-50% в фазе интенсивного роста культуры, продолжительность ферментации 18-24 ч до концентрации клеток в споровой форме 93-95%; концентрирование культуральной жидкости на проточной центрифуге при скорости 15000 об/мин со скоростью подачи культуральной жидкости 100-120 л/ч; смешивание концентратов штаммов с криопротекторной средой; замораживание и лиофильную сушку; тщательное смешивание в течение 30-60 минут полученной сухой биомассы бактерий в соотношении 1:3 с последующей добавкой наполнителя мальтодекстрина до 100% массы препарата. Вышеописанная группа изобретений обеспечивает получение препарата, который обладает высоким титром, антагонистической активностью в отношении патогенных, условно-патогенных микроорганизмов, долгим сроком хранения и эффективностью при инкубации цист рачка артемии и креветок Розенберга. 2 н.п. ф-лы, 2 ил., 3 табл., 4 пр.
Description
Изобретение относится к микробиологии и биотехнологии, в частности, к технологии получения пробиотических препаратов для использования в аквакультуре.
Аквакультура - это один из самых быстрорастущих секторов производства продуктов питания в мире. Различные заболевания водных животных и ухудшение состояния окружающей среды часто приводят к серьезным экономическим потерям. В качестве борьбы и профилактики с инфекционными заболеваниями очень часто применяются антибиотики, но их использование приводит к развитию резистентности патогенных микроорганизмов и подавлению иммунитета организма. В связи с этим, а также с растущим спросом на аквакультуру, в настоящее время широкое признание получает применение пробиотиков в качестве усиливающего иммунитет средства. Пробиотики характеризуются отсутствием патогенности, беспрепятственной пролиферацией in vitro, быстрым ростом в организме [1]. В дополнение к этому, их активность не должна ингибироваться кормовыми ингредиентами и для удобства они должны легко смешиваться с кормом. В аквакультуре пробиотики также добавляют в рыбный корм или, дополнительно, в воду.
К настоящему времени известно большое количество пробиотиков, получаемых с использованием различных видов и групп микроорганизмов: Bacillus subtilis, В. licheniformis, В. coagulans, В. cereus, Lactobacillus sporogenes, L. rhamnosus, L. aracasei, L. delbrueckii, L. acidophilus, L. bulgaricus, L. fermentum, Lactococcus lactis, Bifidobacterium animalis, B. bifidum, Saccharomyces boulardii, Enterococcus faecium и др. Пробиотики являются эффективным средством в борьбе с патогенными бактериями, которые вызывают заболевания, способствуют пролиферации кишечной микрофлоры, продуцируют молочную или уксусную кислоту, различные витамины, белки, ферменты и другие полезные вещества. Таким образом, оздоравливающие свойства пробиотиков заключаются в антагонистической активности против патогенных микробов и их метаболитов, в создании благоприятных условий для микрофлоры желудочно-кишечного тракта и снабжении организма животных биологически активными веществами, повышающими конвертируемость корма, улучшающими процессы жизнедеятельности и иммунный статус [2].
Известна кормовая добавка «Субтиспорин», с содержанием вегетативных клеток бактерий Bacillus subtilis ВКПМ В-2150 в количестве 5×109 КОЕ/мл.
Известен пробиотик «Моноспорин» как в жидком, так и сухом виде. В основе препарата - споровая форма штамма В. subtilis 945 (В-5225) с титром не менее 1×108 КОЕ/мл. В состав препарата так же входят меласса свекловичная, соевый гидролизат, вода.
Известен пробиотический препарат для обогащения Artemia franciscana, содержащий в своем составе S. boulardii. В литературе показано, что дрожжи усиливают резистентность и устойчивость артемий к возбудителю Vibrio harveyi при внесении дрожжей в концентрации в 1×104 КОЕ/мл [3].
Было проведено исследование на обогащение пробиотиком с В. subtilis A. franciscana с последующим ее скармливанием декоративным рыбам Poecilia latipinna. Результаты показали, что культивирование артемий с добавлением В. subtilis в конецентрации 1×105 КОЕ улучшает репродуктивные параметры, кишечную микрофлору и устойчивость к патогенным бактериям у рыб [4].
Известен препарат с пробиотическим штаммом L. rhamnosus IMC 501®, обладающий ингибирующим эффектом против таких патогенных микроорганизмов как Escherichia coli, Staphylococcus aureus, Candida albicans, Clostridium perfringens и Streptococcus mutans. Проведено исследование на влияние этого штамма на обогащение Artemia sp. с последующим ее скармливанием различным видам рыб. Было показано улучшение в развитии личинок рыб Amphiprion ocellaris [5]. Испанскими учеными [6] проведен эксперимент по введению пробиотика на основе L. rhamnosus в среду к A. metanauplii, чтобы проанализировать эффект от применения пробиотика в качестве средства борьбы с потенциально патогенными представителями микроорганизмов семейства Vibrionaceae. В результате ими доказано позитивное влияние на рачков L. rhamnosus и снижение уровня болезнетворных организмов на целый порядок по сравнению с контролем.
Индийскими учеными [7] проведены исследования по обогащению науплиусов А. parthenogenetica разными микроорганизмами: L. rhamnosus, В. coagulans. В ходе эксперимента изучалась нагрузка и время задерживания пробиотических добавок в кишечнике науплиусов артемий. В результате было выявлено, что науплиусы артемий, обогащенные L. rhamnosus, достигали наполненного состояния кишечника через 39±1,41 мин, а обогащенные науплиусы В. coagulans - через 39,5±0,71 мин. Нагрузка на кишечник и время задерживания в кишечнике варьировали в экспериментальных группах.
Из вышеприведенных данных видно, что в составе пробиотических препаратов чаще всего выступают хорошо изученные микроорганизмы родов Lactobacillus и Bacillus. Однако, для устойчивого развития аквакультуры необходимо увеличить пул микроорганизмов, используемых в качестве пробиотиков для гидробионтов, а также расширить линейку препаратов, базирующихся на консорциуме микробов, а не монокультурах. Кроме того, титр микроорганизмов в большинстве пробиотиков, как правило, не превышает 5×109 КОЕ/г. При этом экспериментально установлено, что чем выше численность микроорганизмов в биопрепарате, тем он эффективнее [8].
Наиболее близким, по технической сущности или аналогом, к заявляемому изобретению, является способ получения комбинированного пробиотического препарата для животноводства на основе спорообразующих бактерий Bacillus subtilis BKM-B-2998D и Bacillus licheniformis BKM-B-2999D. В качестве вспомогательных веществ или добавок - Bacillus subtilis (natto) ВКМ B-3057D, глюконат кальция, ферментный препарат «Кемзайм плюс» и наполнитель молочная сыворотка. Титр готового препарата - не менее 5×109 КОЕ/г [9].
Задачей, стоявшей перед авторами данного изобретения, являлось создание нового комбинированного пробиотического сухого препарата с повышенной эффективностью, высоким титром живых пробиотических микроорганизмов и длительным сроком хранения на основе уникальных штаммов В. toyonensis В-13249 и В. pumilus В-13250, выделенных из ризосферы растений Helianthus annus L. и Cichorium intybus L. соответственно.
Технический результат, получаемый при осуществлении изобретения, заключается в возможности получения пробиотика для аквакультуры и животных, с высоким значением титра за счет включения в состав уникальных штаммов микроорганизмов, обладающих широким спектром антагонистической активности по отношению к патогенным, условно-патогенным микроорганизмам и дрожжеподобным грибкам.
Технический результат достигается следующим образом: пробиотический препарат для использования в аквакультуре и животных в своем составе содержит лиофильно высушенную биомассу штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250, и наполнитель мальтодекстрин в следующем соотношении (%) по массе: Bacillus toyonensis - 5, Bacillus pumilus - 15, мальтодекстрин - 80, и представляет собой сыпучий порошок белого цвета с коричневыми вкраплениями. Количество жизнеспособных бактерий не менее 1×1010 КОЕ/г.
Способ получения пробиотического препарата включает последовательное, раздельное культивирование штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 на мелассно-кукурузной среде в ферментационных установках при рН 6,8-7,0, концентрирование культуральной жидкости на проточной центрифуге, сублимационную сушку концентратов, смешивание полученной сухой биомассы бактерий в соотношении 1:3 с последующей добавкой наполнителя мальто декстрина до 100% массы препарата, приводящей к получению пробиотика с содержанием жизнеспособных бактерий не менее 1×1010 КОЕ/г.
1. Штаммы и питательные среды для культивирования.
В качестве действующего компонента нового пробиотика использовался консорциум на основе штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250. Оба штамма бактерий были запатентованы в 2019 году [10, 11] как антагонисты по отношению к таким патогенным микроорганизмам, как Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis, Salmonella typhimurium, Shigella sonnei, Pseudomonas aeruginosa.
В колбах и чашках Петри штаммы культивировались на L-среде, содержащей 5 г дрожжевого экстракта, 5 г NaCl и 15 г пептона на 1 л дистиллированной воды. Для получения твердой питательной среды добавлялся агар из расчета 15 г/л.
Питательная среда для ферментации имела следующий состав на 1 л водопроводной воды: 25 г мелассы, 12,5 г кукурузного экстракта, 1 г дрожжевого экстракта, 0,5 г триптона, 0,25 г MgSO4, 0,03 г MnSO4, 0,046 г CoCl2, 1 г CaCl2, 0,001 г FeSO4, 0,001 г CuSO4 и 2 мл лапрола.
2. Антагонистическая активность концентратов и готового биопрепарата.
Лиофилизированные концентраты каждого из штаммов, а также их композиции и готовый пробиотик проявляют антагонистический эффект по отношению к штаммам Е. coli. За счет явления синергизма между штаммами, выражающегося в максимальном антагонистическом эффекте, выбранное соотношение бактерий Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 в готовом препарате - 1:3.
3. Технологическая схема производства препарата и его готовый вид.
Штаммы Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 культивируются раздельно в ферментере с мелассно-кукурузной средой следующего состава (г/л): 25 г мелассы, 12,5 г кукурузного экстракта, 1 г дрожжевого экстракта, 0,5 г триптона, 0,25 г MgSO4, 0,03 г MnSO4, 0,046 г CoCl2, 1 г CaCl2, 0,001 г FeSO4, 0,001 г CuSO4 и 2 мл лапрола. Ферментацию проводят при рН 6,8-7,0 и температуре 37°С, расходе воздуха 100-150 л/мин, скорости перемешивания 250-500 об/мин; pO2 - 30-50% в фазе интенсивного роста культуры. Продолжительность процесса ферментации 18-24 часа. Процесс считается законченным, если концентрация клеток в споровой форме составляет 93-95%. По окончании культивирования штаммов В. toyonensis ВКПМ В-13249 и В. pumilus ВКПМ В-13250 культуральную жидкость концентрируют на высокоскоростной центрифуге с периодической выгрузкой концентрата. Центрифугирование культуральной жидкости проводят при скорости вращения ротора - 15000 об/мин. Скорость подачи культуральной жидкости 100-120 л/ч. По окончании центрифугирования концентраты штаммов В. toyonensis и В. pumilus смешивают с криопротекторной средой, замораживают при -25-40°С в морозильном шкафу и затем, подвергают лиофильной сушке. На выходе получается сыпучий порошок от светло-кремового до темно-бурого цвета, сладко-горького вкуса, с легким специфическим запахом.
Для получения целевого продукта с общим содержанием жизнеспособных клеток бактерий не менее 1×1010 КОЕ/г используют смеситель периодического действия по типу «Пьяная бочка» и наполнитель мальтодекстрин - углевод, представляющий собой промежуточный продукт ферментного расщепления растительного крахмала, в результате чего молекулы крахмала делятся на фрагменты - декстрины, при этом образуются молекулы глюкозы (декстрозы), мальтозы, мальтотриозы. В смеситель вносят 48 кг мальтодекстрина и 2 кг концентратов В. toyonensis и В. pumilus в соотношении 1:3. Затем, содержимое тщательно перемешивается в течение 30-60 мин. (время смешивания выбрано экспериментальным путем, т.к. за такой промежуток времени концентрат бактерий равномерно распределяется по всему объему мальтодекстрина). После перемешивания содержимое смесителя ссыпается в полиэтиленовые мешки, соблюдая точный вес на весах, отбирается средняя проба для анализа. Мешки упаковываются в трехслойные kraft-мешки, зашиваются и отправляются в складское помещение на карантин, до получения результатов анализа на чистоту и содержание микроорганизмов. Общая схема получения готового пробиотического препарата для аквакультуры представлена на блок-схеме (Фиг. 1).
Весь процесс изготовления опытно-промышленных партий готового продукта происходил в лаборатории ИЦ «Промбиотех» АлтГУ на имеющимся оборудовании центра. Таким образом полученный препарат представляет из себя порошок белого цвета с коричневыми вкраплениями бактериального концентрата. Специфический запах бацилл фактически не идентифицируется.
4. Эффективность препарата при проращивании цист артемий и выращивании креветок.
Новый пробиотический препарат, содержащий консорциум штаммов В. toyonensis В-13249 и В. pumilus В-13250 оказывает положительный эффект на процент выклева цист и выход биомассы артемий. Рекомендуемая доза биопрепарата - 0,1 г на 2 г цист.
Новый пробиотик на основе споровых бактерий способствует более раннему выходу из личиночной стадии креветки М. rosenbergii по сравнению с контролем (на 18-й день).
Изобретение иллюстрируется следующими примерами:
Пример 1. Определение антагонистической активности концентратов штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 и препарата на их основе
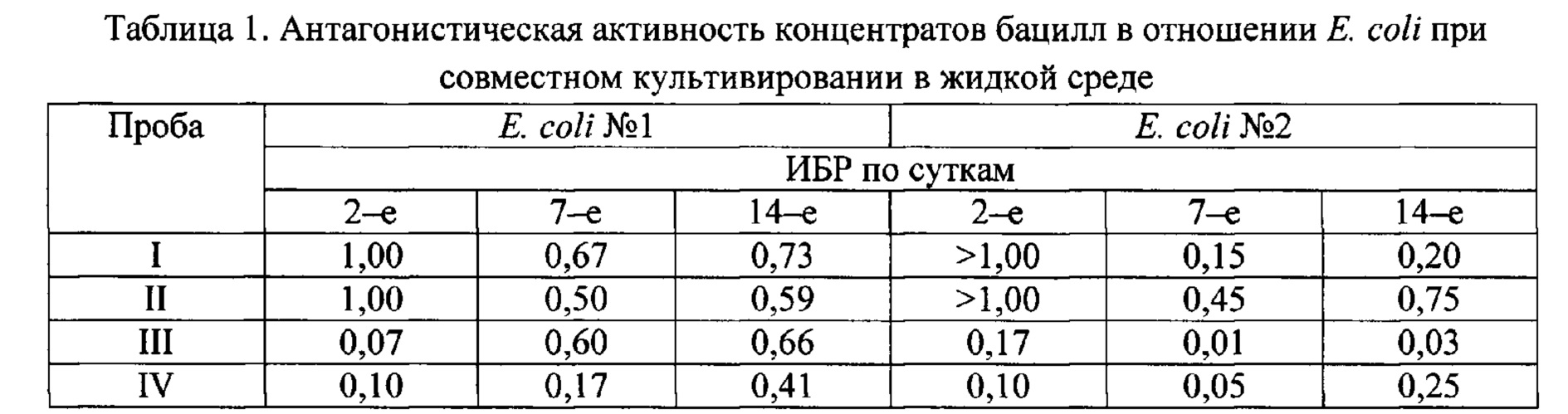
Антагонизм концентратов и бактериального препарата устанавливался по отношению к двум штаммам Е. coli из коллекции ИЦ «Промбиотех». Для этого использовали метод совместного культивирования антагонистов и тест культур в соотношении 1:1 в жидких питательных средах в течение 14-и суток при комнатной температуре. В контрольных колбах штаммы Е. coli выращивали без присутствия бацилл. На 2-е, 7-е и 14-е сутки осуществляли посев из всех колб на среду Эндо для установления индекса блокирования роста (далее ИБР). ИБР - отношение числа колониеобразующих единиц (КОЕ), выросших с контрольной колбы, к числу КОЕ, выросших с опытной колбы. Результат принимали за положительный при ИБР<1. В таблице 1 представлены результаты антагонистической активности лиофилизированных концентратов бацилл. Из них были составлены следующие комбинации: I - только штамм В. toyonensis, II - только штамм В. pumilus, III - штаммы В. toyonensis и В. pumilus в соотношении 1:1, IV - штаммы В. toyonensis и В. pumilus в соотношении 1:3.
В соответствии с полученными результатами через двое суток концентраты отдельных штаммов бацилл еще не оказывают антагонистическое действие в отношении обоих тест-культур, а пробы с бактериальными консорциумами уже снижают численность Е. coli в пределах порядка с контролем.
К 7-м суткам эксперимента пробы I и II начинают подавлять кишечную палочку, а консорциумы из штаммов В. toyonensis и В. pumilus и вовсе способствуют сокращению численности Е. coli №2 на целый порядок, именно на этом сроке достигается наилучший антагонистический эффект. Через две недели антагонистичекое действие бацилл снижается у всех проб, поэтому до 3-й недели эксперимент не продолжали.
Е. coli №1 бациллы лучше подавляют, находясь в соотношении 1:3, а Е. coli №2 - в соотношении 1:1, хотя разница не столь велика. На основании выше указанных данных для создания биопрепарата целесообразно использовать консорциум В. pumilus и В. toyonensis в соотношении 3:1.
Данные по антагонистическому действию готового бактериального препарата с мальтодекстрином, установленные при длительном культивировании на жидкой питательной среде его с тест-культурами, представлены в таблице 2.
Согласно установленным результатам пробиотик подавляет рост обоих штаммов кишечной палочки в пределах порядка уже на 2-е сутки, как и консорциумы концентратов бацилл. По штамму Е. coli №1 можно заметить, что пробиотик с каждой контрольной точкой эксперимента все сильнее действует на условно-патогенный микроорганизм. При действии биопрепарата на штамм Е. coli №2 зафиксирована особенность - снижение его антагонистической активности через неделю и достижение наилучшего значения ИБР к 14-м суткам эксперимента. Отличие в ИБР между концентратами и готовым препаратом можно объяснить тем, что численность бацилл в готовом пробиотике на порядок ниже, чем в концентрированных культурах В. toyonensis и В. pumilus.
Важно отметить, что в рамках этого опыта дополнительная доза пробиотического препарата не вносилась в питательную среду с кишечной палочкой, а антагонистическое действие бактериального препарата сохранялось на высоком уровне и даже улучшалось со временем. Это важно учитывать при промышленных испытаниях готового продукта, чтобы установить наиболее оптимальный план кормления креветок биопрепаратом и срок достижения максимального положительного эффекта от пробиотикотерапии, который может наступить после завершения профилактического курса приема пробиотической добавки.
Пример 2. Влияние пробиотика при инкубации цист артемий
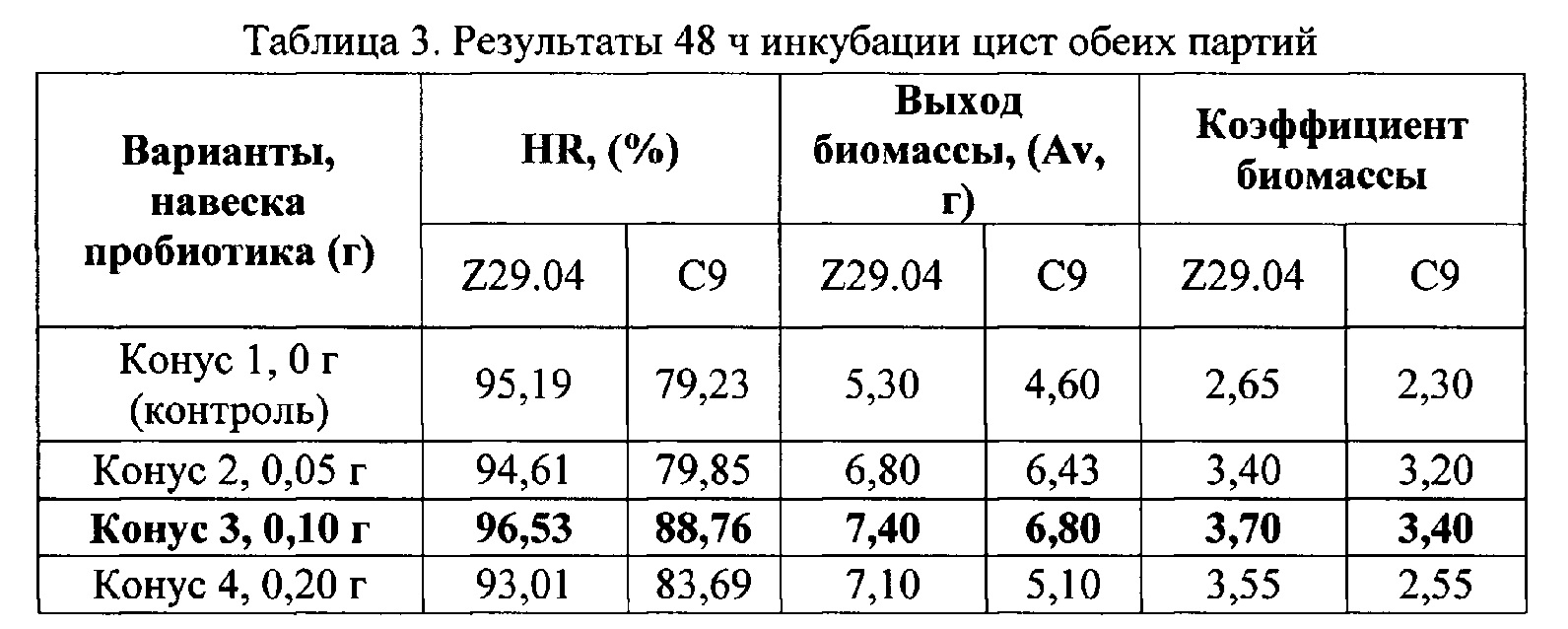
Проведены исследования по эффективности пробиотика при инкубации цист рачка артемий при содействии промышленного партнера - ООО «Ареал» (г. Яровое, Алтайский край). В эксперименте использовались цисты жаброногого рачка артемий A. franciscana двух партий: Z29.04 (озеро Большое Яровое) и С9 (озеро Кучукское) по 4 варианта для каждой из партий в 24-х повторностях. Инкубацию проводили, используя следующие дозы пробиотика (г): 0 (контроль), 0,05, 0,1, 0,2. Пробиотик непосредственно вносился в конус с инкубационным раствором одновременно с началом процесса инкубации. По истечении 48 часов инкубации в каждом конусе подсчитывали количество рачков или науплиусов (N), цист (С) и эмбрионов (U). После чего рассчитывали процент выклева (HR), применяя стандартный метод [12] и коэффициент биомассы [13]. Результаты по обеим партиям цист представлены в таблице 3.
Из таблицы видно, что лучшие результаты с обеих партий получены при добавлении 0,1 г пробиотика на 2 г сухих цист. Стоит заметить, что % выклева в партии Z29.04 меняется по сравнению с контролем на 1,4%, что хоть и не значительно, но в лучшую сторону. При добавлении биопрепарата к партии С9 отмечается прирост HR на 9,5%. Положительное влияние пробиотика сказывается и на выходе биомассы относительно контроля на 2,1 и 2,2 г в партиях Z29.04 и С9 соответственно.
Пример 3. Установление эффективности биопрепарата при выращивании креветок
Исследование проводилось на частной ферме в Республики Казахстан, в окрестностях г. Караганда. Объектом исследования явилась креветка Розенберга (Macrobrachium rosenbergii), разделенная на 2 группы: контрольная (в кормлении использовалась Artemia franciscana L., инкубированная без добавления пробиотика) и опытная (в кормлении использовалась артемия, инкубированная с добавлением пробиотика, т.н. «обогащенная» артемия) по 200 личинок в каждой, которые выращивались в одинаковых аквариумных системах по 600 литров каждая. Пробиотик вносили на 20 час инкубации цист артемий в количестве 1 г на 100 сухих цист при общей продолжительности инкубации 24 ч. При кормлении креветки на более поздней стадии развития (примерно 15 суток) использовались науплиусы 48 часов инкубации. Стоить отметить, что в ходе кормления на ранних стадиях развития креветки требовательны к подвижности корма. В связи с этим, при кормлении предличинок добавляли суспензию живой спирулины (5 мл на бассейн/сутки) для увеличения подвижности науплиусов. Известно, что вылупившаяся личинка креветки Розенберга проходит 11 различных личиночных стадий, чтобы достичь постличинкой. Этот процесс занимает приблизительно от 22 до 45 дней. Фиксирование линек креветок осуществляли визуально, чтобы не травмировать животных. При обнаружении в общей массе хотя бы одной креветки прошедшей линьку, считали, что вся группа прошла очередную линьку, так как начав, вся группа заканчивает линьку в течение суток. Согласно полученным результатам, в опытной группе наблюдался более ранний выход из личиночной стадии - на 18 день. В контрольной группе - на 28 день. Таким образом сказывается положительный эффект влияния пробиотика на сроки метаморфоза личинок М. rosenbergii.
Пример 4. Установление срока годности
Для установления срока годности готового препарата на протяжении времени хранения при 5°С проверяли изменение титра бацилл, а также наличие, либо отсутствие, посторонней микрофлоры (Фиг. 2).
Как показывают полученные результаты, после хранения препарата на протяжении 12 месяцев, содержание живых микробных клеток остается на высоком уровне, а также отсутствует посторонняя микрофлора.
Литература
1. Левахин В.И., Ласыгина Ю.А., Харламов А.В., Ворошилова Л.Н. Пробиотики в животноводстве // Животноводство и кормопроизводство, 2013. - Т. 1. - №79. - С. 7-10.
2. Соколенко Г.Г., Лазарев Б.П., Миньченко С.В. Пробиотики в рациональном кормлении животных // Технологии пищевой и перерабатывающей промышленности АПК - продукты здорового питания, 2015. - №1. - С.72-78.
3. Patra S.K., Mohamed K.S. Enrichment of Artemia nauplii with the probiotic yeast Saccharomyces boulardii and its resistance against a pathogenic Vibrio // Aquaculture International, 2003. - Vol. 11(5). - P. 505-514.
4. Ahmadifard N., Aminlooi R., V., Tukmechi A., Agh N. Evaluation of the Impacts of Long-Term Enriched Artemia with Bacillus subtilis on Growth Performance, Reproduction, Intestinal Microflora, and Resistance to Aeromonas hydrophila of Ornamental Fish Poecilia latipinna // Probiotics and Antimicrobial Proteins, 2019. - Vol. 11(3). - P. 957-965.
5. Avella M.A., Olivotto I., Silvi S., Place A.R., Carnevali O. Effect of dietary probiotics on clownfish: a molecular approach to define how lactic acid bacteria modulate development in a marine fish // Am. J. Physiol. Regul. Integr. Сотр. Physiol., 2010. - Vol. 298(2). - P. 359-371.
6. Ofelio С, Planas M, Pintado J. Administration of the probiotic Lactobacillus rhamnosus IMC 501 as a strategy for the control of Vibrio bacteria in the brine shrimp Artemia // Lett. Appl. Microbiol., 2021. - Vol. 73(3). - P. 336-342.
7. Isamma A., Divya Kan. R., Ramasubramanian V., Arunjith Th., Sureshkumar S. Standartization of the bioencapsulation of probiotics and oil emulsion in Artemia parthenogenetica // Int. J. Res. Fish. Aquae, 2014. - Vol. 4(3). - P. 122-125.
8. Amoah K., Huang, Q.C, Tan B.P., Zhang S., Chi S. Y., Yang Q. H., Dong X.H. Dietary supplementation of probiotic bacteria, Bacillus coagulans ATCC 7050, improves the growth performance, intestinal morphology, microflora, immune response, and disease confrontation of Pacific white shrimp, Litopenaeus vannamei // Fish and Shellfish Immunology, 2019. - Vol. 87. - P. 796-808.
9. Джавахия В.В., Глаголева Е.В., Воинова Т.М., Карташов М.И., Овчинников А.И. Комбинированный пробиотический препарат на основе спорообразующих бактерий рода Bacillus (варианты) для использования в животноводстве, способ его производства (варианты) и штамм Bacillus subtilis (natto), используемый в качестве добавки к препарату // Патент РФ №2675934, заявлено 10.04.2017, опубл. 25.12.2018.
10. Иркитова А.Н., Гребенщикова А.В. Штамм бактерий Bacillus toyonensis ВКПМ В-13249, обладающий выраженным антагонизмом по отношению к микроорганизмам Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis, Salmonella typhimurium, Shigella sonnei, Pseudomonas aeruginosa // Патент РФ №2693439, заявка 25.12.2018, опубл. 02.07.2019 Бюл. №19.
11. Иркитова А. Н., Гребенщикова А. В. Штамм бактерий Bacillus pumilus ВКПМ В-13250, обладающий выраженным антагонизмом по отношению к микроорганизмам Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis // Патент РФ №2694522, заявка 25.12.2018, опубл. 16.07.2019. Бюл. №20.
12. Lavens P., Sorgeloos. P. Manual on the production and use of live food for aquaculture. - Rome, FAO, 1996. - 295 p.
13. Baert P., Bosteels Т., Sorgeloos P. Pond production // Manual on the production and use of live food for aquaculture, 1996. - P. 196-251.
Claims (2)
1. Пробиотический препарат для аквакультуры, а именно для цист рачка артемии и креветок, отличающийся тем, что в своем составе содержит лиофильно высушенную биомассу штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 и наполнитель мальтодекстрин в следующем соотношении, мас. %: Bacillus toyonensis - 5, Bacillus pumilus - 15, мальтодекстрин - 80, количество жизнеспособных бактерий не менее 1×1010 КОЕ/г.
2. Способ получения пробиотического препарата по п. 1 для аквакультуры, а именно для цист рачка артемии и креветок, включающий раздельное культивирование штаммов Bacillus toyonensis ВКПМ В-13249 и Bacillus pumilus ВКПМ В-13250 на мелассно-кукурузной среде в ферментационных установках при рН 6,8-7,0 и температуре 37°С, расходе воздуха 100-150 л/мин, скорости перемешивания 250-500 об/мин; рО2 - 30-50% в фазе интенсивного роста культуры, продолжительность ферментации 18-24 ч до концентрации клеток в споровой форме 93-95%; концентрирование культуральной жидкости на проточной центрифуге при скорости 15000 об/мин со скоростью подачи культуральной жидкости 100-120 л/ч; смешивание концентратов штаммов с криопротекторной средой; замораживание и лиофильную сушку; тщательное смешивание в течение 30-60 минут полученной сухой биомассы бактерий в соотношении 1:3 с последующей добавкой наполнителя мальтодекстрина до 100% массы препарата.
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2799554C1 true RU2799554C1 (ru) | 2023-07-06 |
Family
ID=
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2675934C2 (ru) * | 2017-04-10 | 2018-12-25 | Общество с ограниченной ответственностью "Фермлаб" | Комбинированный пробиотический препарат на основе спорообразующих бактерий рода bacillus (варианты) для использования в животноводстве, способ его производства (варианты) и штамм bacillus subtilis (natto), используемый в качестве добавки к препарату |
| RU2693439C1 (ru) * | 2018-12-25 | 2019-07-02 | федеральное государственное бюджетное образовательное учреждение высшего образования "Алтайский государственный университет" | Штамм бактерий Bacillus toyonensis ВКПМ В-13249, обладающий выраженным антагонизмом по отношению к микроорганизмам Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis, Salmonella typhimurium, Shigella sonnei, Pseudomonas aeruginosa |
| RU2694522C1 (ru) * | 2018-12-25 | 2019-07-16 | федеральное государственное бюджетное образовательное учреждение высшего образования "Алтайский государственный университет" | Штамм бактерий Bacillus pumilus ВКПМ В-13250, обладающий выраженным антагонизмом по отношению к микроорганизмам Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis |
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2675934C2 (ru) * | 2017-04-10 | 2018-12-25 | Общество с ограниченной ответственностью "Фермлаб" | Комбинированный пробиотический препарат на основе спорообразующих бактерий рода bacillus (варианты) для использования в животноводстве, способ его производства (варианты) и штамм bacillus subtilis (natto), используемый в качестве добавки к препарату |
| RU2693439C1 (ru) * | 2018-12-25 | 2019-07-02 | федеральное государственное бюджетное образовательное учреждение высшего образования "Алтайский государственный университет" | Штамм бактерий Bacillus toyonensis ВКПМ В-13249, обладающий выраженным антагонизмом по отношению к микроорганизмам Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis, Salmonella typhimurium, Shigella sonnei, Pseudomonas aeruginosa |
| RU2694522C1 (ru) * | 2018-12-25 | 2019-07-16 | федеральное государственное бюджетное образовательное учреждение высшего образования "Алтайский государственный университет" | Штамм бактерий Bacillus pumilus ВКПМ В-13250, обладающий выраженным антагонизмом по отношению к микроорганизмам Escherichia coli, Candida albicans, Staphylococcus aureus, St. epidermidis |
Non-Patent Citations (1)
| Title |
|---|
| ГРЕБЕНЩИКОВA A.В., Изучение антагонистической активности бактериальных консорциумов на основе штаммов Bacillus subtilis, Труды молодых ученых Aлтайского Государственного Университета. //Материалы V региональной молодежной конференции "Мой выбор - наука", XIV научной конференции студентов, магистрантов, аспирантов и учащихся лицейных классов, 1-28 апреля 2018, вып. 15, с. 6-8. ОРЛОВA Т.Н. и др., Aнтагонистическая активность Bacillus subtilis, Вестник Aлтайского государственного аграрного университета, 2018, N 5 (163), с. 141-145. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103403146B (zh) | 用于针对弧菌的生物控制的益生菌 | |
| Nimrat et al. | Enhancement of growth performance, digestive enzyme activities and disease resistance in black tiger shrimp (Penaeus monodon) postlarvae by potential probiotics | |
| KR101536901B1 (ko) | 바실러스 서브틸러스 및 파지 혼합물을 유효성분으로 함유하는 어류용 프로바이오틱스 조성물 | |
| Wang et al. | Dietary supplementation of probiotics fermented Chinese herbal medicine Sanguisorba officinalis cultures enhanced immune response and disease resistance of crucian carp (Carassius auratus) against Aeromonas hydrophila | |
| MXPA03008563A (es) | Alimentos microbianos para acuacultural y agricultura. | |
| KR101663570B1 (ko) | 평위산 부산물 추출물을 유효성분으로 함유하는 사료첨가제 및 이를 이용한 기능성 사료 | |
| EP3198040A1 (en) | Probiotic fermented feed additives | |
| JP2009159955A (ja) | クルマエビ腸内から分離したプロバイオティクス乳酸菌 | |
| KR101230813B1 (ko) | 사프로레그니아 속 미생물에 대한 생물학적 방제용 프로바이오틱스 | |
| KR101047948B1 (ko) | 박테리오신을 생산하는 유산균 및 이를 함유하는 생균제 조성물 | |
| JP2010051247A (ja) | 病原細菌ならびに真菌に対して抗菌作用を示すバチルス・アミロリケファシエンスを有効成分とする生物的防除剤 | |
| Li et al. | Fish-derived lactic acid bacteria supplementation enhanced the immunity and resistance in Crucian carp (Carassius auratus) | |
| KR101670955B1 (ko) | 양식어류용 사료 조성물 및 이를 이용하여 양식시킨 양식어류 | |
| KR100371503B1 (ko) | 양식어류의 사료첨가제용 미생물 제제 및 그 제조방법 | |
| KR101616530B1 (ko) | 항균활성을 갖는 신규한 락토코쿠스 락티스 kr-w.w-2 균주 및 이의 용도 | |
| RU2799554C1 (ru) | Новый пробиотический препарат на основе консорциума спорообразующих бактерий для аквакультуры и животных и способ его получения | |
| Ali et al. | The effect of oral administration of lactic acid bacteria isolated from kefir on intestinal microbiota, growth performance and survival in juvenile rainbow trout, Oncorhynchus mykiss | |
| RU2723411C2 (ru) | Штамм bacillus cereus rcam04578, продуцент биологически активных соединений, обладающий пробиотическими свойствами | |
| Jahari et al. | Encapsulation of Lactobacillus plantarum with mannan and sodium alginate improves its cell production | |
| RU2768281C1 (ru) | Комбинированный пробиотик для аквакультуры на основе спорообразующих бактерий рода bacillus и способ его производства | |
| TWI460269B (zh) | A myristic yeast strain, a composition containing the strain and the use of the strain | |
| WO2023282354A1 (ja) | エビ目の生物の飼育用組成物、およびエビ目感染症に対する予防または治療用組成物 | |
| Chemlal-Kherraz et al. | The probiotic potential of lactobacilli isolated from Nile tilapia (Oreochromis niloticus)’s intestine | |
| WO2016037296A1 (es) | Método para producir probióticos autóctonos con actividad inmunoestimulante y su uso en profilaxis contra flavobacteriosis en salmónidos | |
| Das et al. | Effect of feed probiotic on the growth and their colonization performance on the intestine of rohu (Labeo rohita) |