RU2723936C2 - Комбинация электрофореза в геле и переноса с использованием проводящих полимеров и способ использования - Google Patents
Комбинация электрофореза в геле и переноса с использованием проводящих полимеров и способ использования Download PDFInfo
- Publication number
- RU2723936C2 RU2723936C2 RU2018121330A RU2018121330A RU2723936C2 RU 2723936 C2 RU2723936 C2 RU 2723936C2 RU 2018121330 A RU2018121330 A RU 2018121330A RU 2018121330 A RU2018121330 A RU 2018121330A RU 2723936 C2 RU2723936 C2 RU 2723936C2
- Authority
- RU
- Russia
- Prior art keywords
- plate
- gel
- membrane
- blotting
- separation
- Prior art date
Links
- 238000012546 transfer Methods 0.000 title claims abstract description 116
- 238000000034 method Methods 0.000 title claims abstract description 30
- 229920001940 conductive polymer Polymers 0.000 title claims description 66
- 238000001502 gel electrophoresis Methods 0.000 title description 9
- 239000002322 conducting polymer Substances 0.000 title description 2
- 239000012528 membrane Substances 0.000 claims abstract description 167
- 238000000926 separation method Methods 0.000 claims abstract description 105
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 99
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 99
- 238000001962 electrophoresis Methods 0.000 claims abstract description 88
- 229920002521 macromolecule Polymers 0.000 claims abstract description 36
- 239000000872 buffer Substances 0.000 claims abstract description 33
- 239000007788 liquid Substances 0.000 claims abstract description 9
- 229920000642 polymer Polymers 0.000 claims description 49
- 239000002131 composite material Substances 0.000 claims description 26
- 229920003023 plastic Polymers 0.000 claims description 17
- 230000003068 static effect Effects 0.000 claims description 16
- 239000004033 plastic Substances 0.000 claims description 15
- 229910052751 metal Inorganic materials 0.000 claims description 12
- 239000002184 metal Substances 0.000 claims description 12
- -1 poly (p-phenylene) Polymers 0.000 claims description 12
- 229920000767 polyaniline Polymers 0.000 claims description 12
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 claims description 10
- 239000012530 fluid Substances 0.000 claims description 9
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 claims description 8
- 238000001816 cooling Methods 0.000 claims description 8
- 150000002739 metals Chemical class 0.000 claims description 8
- 239000004065 semiconductor Substances 0.000 claims description 8
- 229920000123 polythiophene Polymers 0.000 claims description 7
- 229920002981 polyvinylidene fluoride Polymers 0.000 claims description 7
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 claims description 6
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 claims description 6
- 230000005012 migration Effects 0.000 claims description 6
- 238000013508 migration Methods 0.000 claims description 6
- 229920001197 polyacetylene Polymers 0.000 claims description 5
- 229920000265 Polyparaphenylene Polymers 0.000 claims description 4
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 claims description 4
- 229920000553 poly(phenylenevinylene) Polymers 0.000 claims description 4
- 239000011787 zinc oxide Substances 0.000 claims description 4
- 239000000020 Nitrocellulose Substances 0.000 claims description 3
- 230000008859 change Effects 0.000 claims description 3
- 150000002500 ions Chemical class 0.000 claims description 3
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 claims description 3
- 229920001220 nitrocellulos Polymers 0.000 claims description 3
- 239000004677 Nylon Substances 0.000 claims description 2
- 229910052759 nickel Inorganic materials 0.000 claims description 2
- 229920001778 nylon Polymers 0.000 claims description 2
- 238000003860 storage Methods 0.000 claims description 2
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 claims 2
- VPBPKFIZNWQANG-UHFFFAOYSA-N [F].[Sn] Chemical compound [F].[Sn] VPBPKFIZNWQANG-UHFFFAOYSA-N 0.000 claims 2
- JAONJTDQXUSBGG-UHFFFAOYSA-N dialuminum;dizinc;oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[O-2].[O-2].[Al+3].[Al+3].[Zn+2].[Zn+2] JAONJTDQXUSBGG-UHFFFAOYSA-N 0.000 claims 1
- 229910052738 indium Inorganic materials 0.000 claims 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 5
- 239000000126 substance Substances 0.000 abstract description 4
- 239000000499 gel Substances 0.000 description 209
- 229920000128 polypyrrole Polymers 0.000 description 21
- 239000007853 buffer solution Substances 0.000 description 17
- 230000005684 electric field Effects 0.000 description 16
- 239000000463 material Substances 0.000 description 12
- 239000010408 film Substances 0.000 description 11
- 239000000203 mixture Substances 0.000 description 11
- 239000004020 conductor Substances 0.000 description 9
- 229920002401 polyacrylamide Polymers 0.000 description 8
- 238000001262 western blot Methods 0.000 description 8
- 239000000523 sample Substances 0.000 description 7
- 235000012431 wafers Nutrition 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- PIEPQKCYPFFYMG-UHFFFAOYSA-N tris acetate Chemical compound CC(O)=O.OCC(N)(CO)CO PIEPQKCYPFFYMG-UHFFFAOYSA-N 0.000 description 6
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 5
- OWMVSZAMULFTJU-UHFFFAOYSA-N bis-tris Chemical compound OCCN(CCO)C(CO)(CO)CO OWMVSZAMULFTJU-UHFFFAOYSA-N 0.000 description 5
- 239000012212 insulator Substances 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 4
- 239000011248 coating agent Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 239000000975 dye Substances 0.000 description 4
- 230000005611 electricity Effects 0.000 description 4
- 239000012474 protein marker Substances 0.000 description 4
- 230000008901 benefit Effects 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- PAFYVDNYOJAWDX-UHFFFAOYSA-L calcium;2,2,2-trichloroacetate Chemical compound [Ca+2].[O-]C(=O)C(Cl)(Cl)Cl.[O-]C(=O)C(Cl)(Cl)Cl PAFYVDNYOJAWDX-UHFFFAOYSA-L 0.000 description 3
- 238000012512 characterization method Methods 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 229920001971 elastomer Polymers 0.000 description 3
- SXGZJKUKBWWHRA-UHFFFAOYSA-N 2-(N-morpholiniumyl)ethanesulfonate Chemical compound [O-]S(=O)(=O)CC[NH+]1CCOCC1 SXGZJKUKBWWHRA-UHFFFAOYSA-N 0.000 description 2
- AXAVXPMQTGXXJZ-UHFFFAOYSA-N 2-aminoacetic acid;2-amino-2-(hydroxymethyl)propane-1,3-diol Chemical compound NCC(O)=O.OCC(N)(CO)CO AXAVXPMQTGXXJZ-UHFFFAOYSA-N 0.000 description 2
- DVLFYONBTKHTER-UHFFFAOYSA-N 3-(N-morpholino)propanesulfonic acid Chemical compound OS(=O)(=O)CCCN1CCOCC1 DVLFYONBTKHTER-UHFFFAOYSA-N 0.000 description 2
- XWUCFAJNVTZRLE-UHFFFAOYSA-N 7-thiabicyclo[2.2.1]hepta-1,3,5-triene Chemical compound C1=C(S2)C=CC2=C1 XWUCFAJNVTZRLE-UHFFFAOYSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 239000004696 Poly ether ether ketone Substances 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 2
- 230000002349 favourable effect Effects 0.000 description 2
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 2
- 229920003055 poly(ester-imide) Polymers 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 229920002530 polyetherether ketone Polymers 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 238000006116 polymerization reaction Methods 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 229920002635 polyurethane Polymers 0.000 description 2
- 239000004814 polyurethane Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 239000012723 sample buffer Substances 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 238000009736 wetting Methods 0.000 description 2
- 229910052725 zinc Inorganic materials 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- GKWLILHTTGWKLQ-UHFFFAOYSA-N 2,3-dihydrothieno[3,4-b][1,4]dioxine Chemical compound O1CCOC2=CSC=C21 GKWLILHTTGWKLQ-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 229920006370 Kynar Polymers 0.000 description 1
- 239000007993 MOPS buffer Substances 0.000 description 1
- 229920001046 Nanocellulose Polymers 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 229920012266 Poly(ether sulfone) PES Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 241000251555 Tunicata Species 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 125000002777 acetyl group Chemical class [H]C([H])([H])C(*)=O 0.000 description 1
- 239000004676 acrylonitrile butadiene styrene Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- UDSAIICHUKSCKT-UHFFFAOYSA-N bromophenol blue Chemical compound C1=C(Br)C(O)=C(Br)C=C1C1(C=2C=C(Br)C(O)=C(Br)C=2)C2=CC=CC=C2S(=O)(=O)O1 UDSAIICHUKSCKT-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 239000011246 composite particle Substances 0.000 description 1
- 239000002826 coolant Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 239000004205 dimethyl polysiloxane Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 238000009415 formwork Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 239000012133 immunoprecipitate Substances 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 239000010416 ion conductor Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000011533 mixed conductor Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 239000002121 nanofiber Substances 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 239000002070 nanowire Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 230000011164 ossification Effects 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 239000011546 protein dye Substances 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 235000020183 skimmed milk Nutrition 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000010421 standard material Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 239000003656 tris buffered saline Substances 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 238000009827 uniform distribution Methods 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44704—Details; Accessories
- G01N27/44717—Arrangements for investigating the separated zones, e.g. localising zones
- G01N27/44739—Collecting the separated zones, e.g. blotting to a membrane or punching of gel spots
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44704—Details; Accessories
- G01N27/44713—Particularly adapted electric power supply
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44704—Details; Accessories
- G01N27/44717—Arrangements for investigating the separated zones, e.g. localising zones
- G01N27/44721—Arrangements for investigating the separated zones, e.g. localising zones by optical means
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Molecular Biology (AREA)
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Engineering & Computer Science (AREA)
- Power Engineering (AREA)
- Peptides Or Proteins (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Separation Using Semi-Permeable Membranes (AREA)
- Electrochromic Elements, Electrophoresis, Or Variable Reflection Or Absorption Elements (AREA)
Abstract
Группа изобретений относится к области биотехнологии. Предложен аппарат для электрофоретического разделения и блоттинга (варианты), система для электрофоретического разделения и блоттинга макромолекул, а также способ разделения и переноса макромолекул на мембрану для блоттинга после разделения. В одном варианте аппарат содержит первую и вторую электрически полупроводящие пластины, электрофорезный гель и мембрану для блоттинга. В другом варианте аппарат содержит первую и вторую пластины, электрически полупроводящий прозрачный слой, электрофорезный гель и мембрану для блоттинга. Система содержит резервуар для жидкости с верхней и нижней камерами буфера, первый и второй электроды фазы разделения в верхней и нижней камерах буфера соответственно, первый и второй электроды фазы блоттинга, комбинированный блок отлитого геля и мембраны, а также источник питания. Способ включает разделение макромолекул вдоль геля посредством приложения первой электрической движущей силы к паре электродов разделения, прекращение первой электрической движущей силы на паре электродов разделения, перенос макромолекул через гель на мембрану для блоттинга посредством приложения второй электрической движущей силы. Изобретения обеспечивают визуализированное разделение белков и их дальнейший перенос на мембрану для блоттинга. 4 н. и 14 з.п. ф-лы, 9 ил.
Description
ПЕРЕКРЕСТНАЯ ССЫЛКА НА СВЯЗАННЫЕ ЗАЯВКИ
[0001] По данной заявке испрашивают приоритет и эффект патентной заявки США № 15/348,803, поданной 10 ноября 2016 года, которая является частичным продолжением патентной заявки США № 15/017,540, поданной 5 февраля 2016 года, по которой испрашивали эффект предварительной патентной заявки США № 62/253,143, поданной 10 ноября 2015 года, каждая из которых включена, таким образом, посредством ссылки во всем их объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение в целом относится к электрофорезу в геле и переносу макромолекул и, более конкретно, к использованию единого комбинированного блока предварительно отлитого геля и мембраны, имеющего прозрачные проводящие полимеры.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0003] Несмотря на то, что вестерн-блоттинг является обыкновенным способом, все еще существует множество проблем, которые возникают на стадии переноса. Они включают попадание воздушных пузырьков при размещении гелей на мембранах и, поскольку гели стали тоньше для того, чтобы снижать необходимое количество белка, происходит разрыв гелей, когда пользователь перемещает гели из формы предварительной отливки на мембрану для блоттинга. Эти осложнения могут быть неприемлемыми, когда необходим анализ ограниченных количеств белка, в частности, когда больше белка недоступно или он представляет собой клинический образец. Кроме того, идея комбинированного блока для разделения белков и переноса пространственно затруднена текущим использованием изоляционных пластмасс для размещения предварительно отлитых гелей. Дополнительно, исследователи часто предпочитают наблюдать разделение белков во время электрофореза, что ограничивает использование непрозрачных материалов в качестве поддерживающих гель структурных пластин.
[0004] Упрощение способ вестерн-блоттинга уменьшает традиционный двухстадийный процесс (разделение белков и перенос белков) до одной стадии и использования одного аппарата вместо отдельных аппаратов для электрофореза и переноса белков. Однако одна проблема при создании единого комбинированного блока для электрофореза в геле и переноса белков включает создание аппарата, в котором пользователь может визуализировать степень разделения белков во время электрофореза и после этого переносить белки на мембрану для блоттинга без физического переноса геля на мембрану. Для такого аппарата для осуществления как электрофореза, так и переноса белков, пластины должны формировать структурную опору для геля, а также быть способными пропускать ток через несущие гель пластины к мембране для блоттинга. Проблема состоит в том, что электрический ток, необходимый для переноса белков на мембрану для блоттинга, должен идти перпендикулярно току, необходимому для разделения белков во время электрофореза.
[0005] Предпринято много попыток упрощения разделение и перенос белков и других макромолекул с использованием различных аппаратов и способов. В патенте США № 4994166 на Fernwood et al. описан единый аппарат для электрофореза в гелевом бруске и блоттинга, и то и другое осуществляют в единой резервуарной ячейке, имеющей электроды разделения вдоль противоположных вертикальных стенок и электроды блоттинга, расположенные горизонтально над и под уровнем геля. Ячейка работает в режимах разделения и блоттинга, в которых электроды разделения и блоттинга получают питание отдельно. Fernwood'у нужные пористые гелевые основы для того, чтобы сделать возможным прохождение электрического поля через мембрану, а также нужно удалять электрод переноса верхней пластины из контакта с буферным раствором во время фазы разделения. Fernwood также рассматривает некоторые проблемы использования поддерживающих гель пластин как для электрофореза, так и для переноса белков. Поскольку нужно поддерживать разность потенциалов между двумя концами геля во время фазы разделения, проводящие электроды блоттинга в контакте с буферным раствором во время разделения обнуляют поле около геля, тем самым препятствуя миграции и разделению белков. Fernwood решает эту проблему посредством использования проволочной решетки в качестве нижнего электрода блоттинга, и во избежание обнуления поля электрод нужно поднимать выше или опускать ниже уровня жидкого буфера в резервуаре. Другое предложенное решение состоит в том, что высоту пластины электрода можно фиксировать и поднимать или опускать уровень буфера по мере необходимости для установления или разрыва электрического контакта с несущей гель пластиной. Поднимание и опускание пластины или буфера между фазами электрофореза и переноса требует дополнительного уровня сложности в аппаратах и способах для разделения переноса белков на мембрану для блоттинга.
[0006] В патенте США № 5102524 на Dutertre описано электрофоретическое устройство и способ управления миграцией макромолекул через гелевые пластины, где различные наборы электродов используют в двухстадийном процессе для того, чтобы сначала разделять макромолекулы (например, белки) и затем переносить молекулы на мембрану для блоттинга.
[0007] В патенте США № 5593561 на Cognard также описано электрофоретическое устройство и способ управляемой миграции макромолекул и их переноса на мембрану в сосуде. Первое электрическое поле, создаваемое между электродами, обеспечивает средство разделения макромолекул в геле и второе электрическое поле, перпендикулярное первому, обеспечивает средство переноса макромолекул на мембрану. В описанном способе электроды и мембраны для блоттинга собраны в сосуде, который затем заполняют гелем. Затем гель разжижают, что позволяет удалять мембрану. Устройство Cognard предназначено для использования без предварительно изготовленного блока геля и мембраны.
[0008] В патенте США № 8173002 на Margalit раскрыта система сухого блоттинга для переноса белков на мембрану для блоттинга. Система не содержит электрофоретическое устройство, так что устройство не позволяет пользователю визуализировать разделение и блоттинг белков в одном устройстве. Устройство требует, чтобы пользователь присутствовал для переноса гель на мембрану для блоттинга в устройство блоттинга. Margalit говорит об использовании электропроводящих полимеров, но не в комбинации с единым устройством, которое может как разделять белки, так и переносить белки на мембрану для блоттинга. Margalit не говорит об использовании прозрачных несущих гель пластин с тем, чтобы пользователь мог визуализировать разделение белков во время электрофореза.
[0009] В публикации заявки на патент США № 2006/0042951 на Ohse раскрыт аппарат для разделения и переноса белков через использование маленькой канавки, электрода переноса и прозрачного проводящего материала, имеющего толщину приблизительно 0,1 мкм. Аппарат содержит пару электродов разделения, чтобы вызывать перемещение вещества в образце вдоль прохода, и пару электродов переноса, чтобы вызывать перенос вещества в образце на захватывающий материал посредством электрофореза. Прозрачный проводящий материал не способен быть несущей структурой из-за его толщины приблизительно 0,1 мкм, которая не будет иметь достаточной жесткости, чтобы служить в качестве опорных стенок для геля. Разделение и блоттинг осуществляют в электрофорезном буфере и не используют гелевом бруске или сборочном узле гелевого бруска, которые широко используют для вестерн-блоттинга.
[0010] В патенте США № 6602391 на Serikov раскрыт аппарат и способ капиллярного разделения макромолекул и блоттинга после разделения. Однако Serikov не раскрывает использование гелевого бруска, где пользователь может видеть разделение макромолекул и перенос макромолекул на мембрану для блоттинга для вестерн-блоттинга.
[0011] Проводящие полимеры описаны ранее, но не в сочетании с электрофорезом и блоттингом. Ates et al. описывают многие применения проводящих полимеров в «Conducting Polymers and their Applications» (Current Physical Chemistry, 2012, 2, 224-240). В международной патентной заявке № PCT/EP2013/065163 на Jung раскрыта проводящая полимерная композиция и прозрачный электрод для антистатического слоя. В международной патентной заявке № PCT/KR2008/002236 на Kim раскрыт проводящий полимер для применения в качестве прозрачного электрода и способ изготовления электрода с использованием струйного распылительного способа. В патентной заявке США № 13/616,804 раскрыта прозрачная панель и способ изготовления прозрачной панели, где проводящий полимер слой формируют для получения прозрачного электрода.
[0012] Прозрачные проводящие пластины с использованием проводящих полимеров не использовали в аппаратах электрофореза и блоттинга, где проводящие пластины используют как в качестве поддерживающих гель структур с тем, чтобы предварительно отлитый гель и его проводящую полимерную оболочку можно было использовать как для электрофореза, так и для блоттинга, не удаляя гель после разделения белков, так и все еще используют в качестве поддерживающей гель структуры, когда белки переносят на мембрану для блоттинга.
[0013] В настоящее время сохраняется потребность в устройствах и связанных способах, которые позволяют выполнять электрофорез в геле и перенос белков в едином комбинированном блоке предварительно отлитого геля и мембраны. Дополнительно, поскольку исследователи предпочитают наблюдать стадии электрофореза во время фазы электрофореза, сохраняется потребность в разработке структурных несущих гель пластин, которые допускают визуализацию, но также могут быть использованы как в фазе электрофореза, так и фазе переноса белков при вестерн-блоттинге.
[0014] Все патенты, патентные заявки и непатентные заявки, раскрытые в предпосылках и описании изобретения, включены, таким образом, посредством ссылки для всех целей во всей полноте.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0015] Настоящее изобретение благоприятно восполняет указанные выше изъяны, обеспечивая электрофорез в геле и перенос с использованием одного комбинированного блока предварительно отлитого геля и мембраны с использованием проводящих полимеров, который обеспечивает быстрый, надежный и легких способ осуществления разделения белков без участия человека, после чего следует эффективный перенос белков на мембрану для блоттинга.
[0016] Технологию определяют как любую технологию, изобретение, технический секрет, способ, композицию, устройство, машину, продукт, предмет потребления, формулу и любое их сочетание, которые относятся к любому использованию проводящих, полупроводящих и/или диссипативных материалов в структуре устройства для поддержки электрофорезного геля, где мембрану для блоттинга располагают смежно с гелем, тем самым позволяя электрическому току течь через гель в одном направлении во время фазы разделения белков, и после завершения фазы разделения белков ток течет через проводящую пластину или полупроводящую пластину в направлении, перпендикулярном направлению протекания тока во время фазы разделения. Это выполняют, не удаляя гель из комбинированного блока предварительно отлитого геля и мембраны.
[0017] Изобретение включает способ электрофореза в геле и переноса белков в комбинированном блоке предварительно отлитого геля и мембраны. Комбинированный блок предварительно отлитого геля и мембраны состоит из проводящей/полупроводящей полимерной опалубки, электрофорезного геля и мембраны для блоттинга для использования в вестерн-блоттинге. Пару из геля и мембраны располагают между двумя листами проводящего полимера. Гель способен разделять белки по размеру внутри геля, когда электрический ток течет между электродами на противоположных сторонах оси y геля. Мембрана для блоттинга позволяет иммобилизовать белки, перенесенные из геля после разделения белков, без физического переноса геля на мембрану для блоттинга после разделения белков.
[0018] Настоящее изобретение также может включать одно или несколько из следующего: тонкий слой менее проводящего геля (т. е. высокая процентная доля полиакриламида) между гелем и мембраной; электрофорезные гели различных типов, включая те, которые выполняют из полиакриламида, bis-Tris, Tris-ацетата и т. д.; различные мембраны для иммуноблоттинга, включая те, которые выполнены из нитроцеллюлозы, и поливинилидендифторида (PVDF); различные проводящие полимерные материалы; пластмассовые изоляторы; резервуар буфера и крышку буфера; кассета держателя предварительно отлитого геля и мембраны с электродами; камеру отрицательного электрода; камеру положительного электрода; электродный сборочный узел; анодный и катодный буферы; охлаждающий блок; и программируемый источник мощности.
[0019] Настоящее изобретение является уникальным в том отношении, что в нем используют инновационные проводящие полимеры с конкретным удельным электрическим сопротивлением в применениях вестерн-блоттинга для решения фундаментальных проблем в существующих способах и что делает возможными удобные одностадийные способы электрофореза и переноса. Более конкретно, настоящее изобретение обязано своей уникальностью тому факту, что в нем используют проводящие/полупроводящие полимеры, чтобы вмещать комбинацию предварительно отлитого геля и мембраны для блоттинга, которая выполняет функцию изолятора в одном сценарии (электрофорез) и электрода в другом сценарии (перенос белков), что благоприятно для устройства, которое разделяет белки по размеру в одном направлении с использованием одной пары электродов и переносит белки перпендикулярным образом на мембрану для блоттинга с использованием другой пары электродов. Проводящие полимеры, используемые для структурной поддержки предварительно отлитого геля, являются прозрачными, что позволяет пользователю визуализировать разделение белков во время электрофореза.
[0020] Цель настоящего изобретения состоит в том, чтобы предоставить электрофорез в геле и перенос с использованием одного комбинированного блока предварительно отлитого геля и мембраны для блоттинга с использованием проводящих полимеров, который не страдает какими-либо проблемами или изъянами, связанными с предшествующими решениями.
[0021] В одном из вариантов осуществления имеет место аппарат для электрофоретического разделения и блоттинга. Аппарат имеет первую электрически полупроводящую пластину, выполненную из прозрачного проводящего полимера, и вторую электрически полупроводящую пластину, по существу параллельную первой электрически полупроводящей пластине. Аппарат имеет электрофорезный гель и мембрану для блоттинга, где электрофорезный гель располагают между первой электрически полупроводящей пластиной и мембраной для блоттинга. Мембрана для блоттинга находится между электрофорезным гелем и второй электрически полупроводящей пластиной.
[0022] В другом варианте осуществления аппарат также содержит гель с низкой проводимостью (высоким удельным электрическим сопротивлением) между второй электрически полупроводящей пластиной и мембраной для блоттинга. Вариант осуществления также содержит фильтровальную бумагу между второй электрически полупроводящей пластиной и мембраной для блоттинга.
[0023] В еще одном другом варианте осуществления первая прозрачная электрически проводящая пластина имеет электропроводящие проволоки, расположенные сеткой или решеткой, чтобы рассредоточивать ток/заряд на всем протяжении пластины.
[0024] В еще одном другом варианте осуществления первую пластину в целом формируют из электрически непроводящего статического диссипативного материала. Аппарат имеет первую пластину, выполненную из прозрачного полимера, электрически полупроводящий прозрачный слой смежно с первой пластиной, вторую пластину, по существу параллельную первой пластине, электрофорезный гель и мембрану для блоттинга. В этом варианте осуществления электрически непроводящая статическая диссипативная пластина имеет тонкий прозрачный электрически проводящий полимерный слой или тонкую прозрачную электропроводящую пленку, расположенную по меньшей мере на внутренней поверхности первой пластины, чтобы действовать в качестве пластинчатого электрода во время фазы блоттинга и действовать в качестве изоляционной пластины во время электрофореза.
[0025] В еще одном другом варианте осуществления, аппарат содержит резервуар вместилища жидкости, который имеет верхнюю камеру буфера и нижнюю камеру буфера, каждая с электродом фазы разделения. Резервуар также имеет пару электродов фазы блоттинга, устроенных таким образом, чтобы электрическое поле, создаваемое электродами фазы разделения, было по существу перпендикулярным электрическому полю, создаваемому электродами фазы блоттинга. Аппарат также содержит источник питания, выполненный с возможностью автоматического или ручного переключения и подачи напряжения на электроды фазы разделения и напряжения на электроды фазы блоттинга после стадии разделения белков.
[0026] В еще одном другом варианте осуществления имеет место способ разделения и после разделения блоттинга макромолекул на мембрану для блоттинга. Пользователь предоставляет аппарат в первой ориентации в резервуаре вместилища жидкости. Аппарат имеет первую электрически полупроводящую пластину, состоящую из прозрачного проводящего полимера, вторую электрически проводящую пластину, по существу параллельную первой электрически проводящей пластине, электрофорезный гель и мембрану для блоттинга. Электрофорезный гель располагают между первой проводящей пластиной и мембраной для блоттинга, и мембрану для блоттинга располагают между электрофорезным гелем и второй электрически проводящей пластиной. Пользователь разделяет макромолекулы (например, белки) вдоль геля в аппарате посредством приложения первой электрической движущей силы к паре электродов разделения, что вызывает протекание тока вдоль оси y геля. Напряжение вызывает разделение биологических молекул в геле по размеру, то есть более крупные молекулы медленнее мигрируют вдоль оси y, чем менее крупные молекулы. Затем электрическую силу, подаваемую на электроды разделения, прерывают. Не удаляя гель и мембрану для переноса из резервуара вместилища жидкости, и также сохраняя ту же ориентацию геля и мембраны в резервуаре вместилища жидкости, вторую электрическую движущую силу прикладывают к паре электродов блоттинга по существу перпендикулярно первой электрической движущей силе. Ориентацию блока геля и мембраны сохраняют как относительно электродов разделения, так и относительно электродов блоттинга. Вторая электрическая движущая сила вызывает протекание тока вдоль оси z в геле в первой ориентации. Вторая электрическая движущая сила переносит биологические молекулы из геля на мембрану для блоттинга смежно с гелем. Стадии разделения биологических молекул и переноса биологических молекул на мембрану для блоттинга осуществляют, не удаляя блок из резервуара, тем самым объединяя стадии электрофореза и переноса белков на мембрану для блоттинга в одном резервуаре вместилища жидкости без необходимости изменять ориентацию комбинированного блока геля и мембраны между стадией разделения и стадией переноса.
[0027] Настоящее изобретение описано более полно в настоящем описании далее со ссылкой на сопроводительные рисунки, которые предназначены к прочтению в сочетании с этим кратким изложением, подробным описанием и любыми предпочтительными и/или конкретными вариантами осуществления, которые рассмотрены конкретно или раскрыты иным образом. Однако это изобретение можно осуществлять во многих различных формах, и его не следует толковать в качестве ограниченного вариантами осуществления, которые изложены в настоящем описании; точнее, эти варианты осуществления предоставлено только в качестве иллюстрации и с тем, чтобы это раскрытие было тщательным, полным и в полной мере передавало полный объем изобретения для специалистов в данной области.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[0028] Эти и другие признаки и преимущества настоящего изобретения будут оценены, поскольку это легче понять со ссылкой на описание, формулу изобретения и рисунки в настоящем описании:
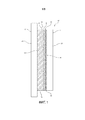
[0029] на фиг. 1 представлен вид сбоку общей компоновки комбинированного блока предварительно отлитого геля и мембраны для электрофореза и переноса;
[0030] на фиг. 2 представлен вид спереди типичного комбинированного блока предварительно отлитого геля и мембраны, обычно используемого для электрофореза, как известно в известном уровне техники;
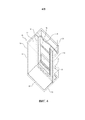
[0031] на фиг. 3 представлен вид в сечении сбоку комбинированного блока предварительно отлитого геля и мембраны в резервуаре для электрофореза и переноса;
[0032] на фиг. 4 представлен вид в перспективе резервуара для электрофореза и переноса без комбинированного блока предварительно отлитого геля и мембраны, расположенного внутри резервуара;
[0033] на фиг. 5 представлен вид спереди варианта осуществления комбинированного блока предварительно отлитого геля и мембраны;
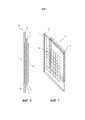
[0034] на фиг. 6 представлен вид сбоку варианта осуществления комбинированного блока геля и мембраны, имеющего проводящую проволочную сеть и тонкий проводящий полимер или пленку в контакте с электрофорезным гелем;
[0035] на фиг. 7 представлен вид в перспективе варианта осуществления комбинированного блока геля и мембраны;
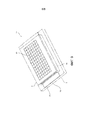
[0036] на фиг. 8 представлен вид сверху варианта осуществления комбинированного блока геля и мембраны, имеющего выступы на одной пластине для того, чтобы создавать зазор для геля и мембраны.
[0037] На фиг. 9 представлен вид в перспективе варианта осуществления с фиг. 8.
ПОДРОБНОЕ ОПИСАНИЕ ФИГУР
[0038] Изобретение описано более полно далее в настоящем описании со ссылкой на сопроводительные рисунки, на которых показаны варианты осуществления изобретения. Однако это изобретение можно осуществлять во многих различных формах, и его не следует толковать как ограниченное вариантами осуществления, изложенными в настоящем описании. Скорее, эти варианты осуществления предоставлены с тем, чтобы это раскрытие было тщательным и полным и полностью передавало объем изобретения специалистам в данной области.
[0039] Понятно, что когда элемент обозначают как находящийся «на» другом элементе, он может находить на другом элементе непосредственно или промежуточные элементы могут присутствовать между ними. Как используют в настоящем описании, термин «и/или» включает любые и все комбинации одного или нескольких из ассоциированных перечисленных пунктов.
[0040] Понятно, что, несмотря на то, что термины первый, второй, третий и т. д. можно использовать в настоящем описании для того, чтобы описывать различные элементы, компоненты, области, слои и/или сечения, эти элементы, компоненты, области, слои и/или сечения не должны быть ограничены этими терминами. Эти термины используют только для того, чтобы отличать один элемент, компонент, область, слой и/или сечение от другого элемента, компонента, области, слоя и/или сечения.
[0041] Понятно, что элементы, компоненты, области, слои и сечения, изображенные на фиг., не обязательно изображены в масштабе.
[0042] Терминология, используемая в настоящем описании, служит только цели описания конкретных вариантов осуществления и не предназначена для ограничения изобретения. Как используют в настоящем описании, формы единственного числа предназначены для того, чтобы также включать формы множественного числа, пока контекст явно не указывает на иное. Кроме того, ясно, что термины «содержит» и/или «содержащий» или «включает» и/или «включающий», когда используют в этом описании, определяют присутствие указанных признаков, областей, целых чисел, стадий, операций, элементов и/или компонентов, но не исключает присутствия или добавления одного или нескольких других признаков, областей, целых чисел, стадий, операций, элементов, компонентов и/или их групп.
[0043] Кроме того, относительные термины, такие как «нижний» или «низ», «верхний» или «верх», «левый» или «правый» можно использовать в настоящем описании для того, чтобы описывать взаимное расположение одного элемента относительно другого элемента(ов), как проиллюстрировано на фиг. Понятно, что относительные термины предназначены для того, чтобы охватывать различные ориентации устройства в дополнение к ориентации, изображенной на фиг.
[0044] Если не определено иное, все термины, используемые в настоящем описании, имеют то же значение, в котором их обычно понимает специалист в области, к которой относится это изобретение. Кроме того, следует понимать, что такие термины, как те, которые определены в широко используемых словарях, следует интерпретировать как имеющие значение, которое находится в соответствии с их значением в контексте релевантной области и настоящего раскрытия, и не следует интерпретировать в идеальном или слишком формальном смысле до тех пор, пока в явной форме так не определено в настоящем описании.
[0045] Образцовые варианты осуществления настоящего изобретения описаны в настоящем описании со ссылкой на идеальные варианты осуществления настоящего изобретения. По существу, следует ожидать вариации геометрических форм иллюстраций в результате, например, способов изготовления и/или допусков. Таким образом, варианты осуществления настоящего изобретения не следует толковать в качестве ограниченных конкретными геометрическими формами областей, проиллюстрированных в настоящем описании, но включать отклонения в геометрических формах, которые являются результатом, например, изготовления. Изобретение, иллюстративно раскрытое в настоящем описании подходящим образом, можно осуществлять на практике в отсутствие любых элементов, которые не раскрыты в настоящем описании конкретно.
[0046] Настоящее изобретение направлено на электрофорез в геле и перенос с использованием одного комбинированного блока 10 предварительно отлитого геля и мембраны с использованием проводящих полимеров. Электрофорез можно осуществлять с использованием различных способов, включая в качестве неограничивающих примеров электрофорез с додецилсульфатом натрия в полиакриламидном геле (SDS-PAGE).
[0047] В одном из вариантов осуществления изобретение выполняют из следующих компонентов: комбинированный блок 10 предварительно отлитого геля и мембраны, который содержит гель 6 и мембрану 12 для переноса/блоттинга, расположенную между двумя листами проводящих полимеров 2, 4. Дополнительно, гель 8, имеющий низкую проводимость, разделяет гель 6 и мембрану 12.
[0048] На фиг. 1 представлен вид сбоку одного из вариантов осуществления общей компоновки комбинированного блока 10 предварительно отлитого геля и мембраны для электрофореза и перенос. В целом, гель 6 и мембрану 12 располагают между двумя полупроводящими пластинами или листами 2, 4, состоящими из проводящих/полупроводящих полимеров. Дополнительно, гель 6 и мембрану 12 можно разделять тонким слоем низкопроводящего (т. е. высокая процентная доля полиакриламида) геля 8. Во время режима разделения ток течет от верхней поверхности 20 геля 6 к нижней поверхности 18 геля 6. Во время режима блоттинга (т. е. режима переноса белков), ток течет от первой полупроводящей пластины 2 ко второй полупроводящей пластине 4.
[0049] Первую полупроводящую пластину 2 выполняют из прозрачного проводящего материала. Эти проводящие материалы включают композиции полианилинов, полиприрролов, политиофенов или других прозрачных проводящих полимеров, более полно описанных далее. Первая проводящая пластина 2 имеет внешнюю поверхность 20 и внутреннюю поверхность 14. Вторую проводящую пластину 4 также выполняют из проводящего материала, но он не обязана быть прозрачной, поскольку пользователь может визуализировать миграцию белка, глядя только с одной стороны геля. Преимущество использования системы, которая содержит прозрачный проводящий материал вместо непрозрачного проводящего материала, состоит в том, что пользователи часто предпочитают наблюдать фазу разделения электрофореза для того, чтобы визуально определять степень движения/разделения белков во время электрофореза. Типичные пластинчатые электроды являются металлическими и, следовательно, непрозрачными. Однако если типичные металлические пластинчатые электроды используют вдоль поверхности геля, пользователи не могут определять, до которой степени белки разделены во время электрофореза. В одном из вариантов осуществления только одна проводящая пластина 2 должна быть прозрачной для пользователя, чтобы визуально определять, насколько белок продвинулся, поскольку движение белка можно наблюдать, глядя на одну сторону геля. Вторая сторона геля 6 будет блокирована для просмотра мембраной 12 для переноса/блоттинга. В предпочтительном варианте осуществления полимер, используемый для проводящей пластины 2, имеет объемное удельное электрическое сопротивление в диапазоне 103-105 Ом-см, но может составлять даже 108 Ом-см. Пластины 2, 4 могут иметь различные размеры для того, чтобы поддерживать гель. Типичные несущие гель пластины составляют приблизительно 10 см × 10 см, но пластины могут быть любого размера, чтобы вмещать гель.
[0050] Использование пластин с объемным удельным электрическим сопротивлением в диапазоне 103-105 Ом-см или выше препятствует обнулению электрического поля, когда ток подают на электроды около вертикальных концов геля, поскольку пластины имеют более высокое объемное удельное электрическое сопротивление, чем электрофорезный гель (обычно между 10 и 300 Ом-см), который окружают пластины 2, 4. Обнуление электрического поля предотвращают, поскольку ток выбирает путь наименьшего сопротивления и проходит от верхнего электрода разделения через гель к нижнему электроду разделения, не заставляя полупроводящие пластины 2, 4 создавать обнуляющее электрическое поле.
[0051] В целом, полимеры, используемые для того, чтобы создавать несущие структуры для электрофорезных гелей, представляют собой полимеры и, следовательно, являются электрически изолирующими. Однако существует особый класс полимеров, которые от природы проводят электричество на уровнях, значительно превышающих полупроводники (вплоть до 1000 См/см), и их проводимостями/удельными электрическими сопротивлениями можно управлять через различные способы получения. Проводящие полимеры представляют собой органические полимеры, которые проводят электричество. В частности, они предлагают меньшую электрическую проводимость, чем металлы, и могут обладать свойствами пластмасс, такими как прозрачность. Электрические свойства (т. е. удельное электрическое сопротивление) можно точно регулировать, используя способы органического синтеза и дисперсионные способы. Типы органических проводящих полимеров включают полиацетилен, поли(пиррол)ы (PPY), полианилины, поли(тиофен)ы (PT), поли(3,4-этилендиокситиофен) (PEDOT), поли(п-фениленсульфид (PPS), поли(ацетилен)ы (PAC), поли(п-фениленвинилен) (PPV) и их производные. Проводящие полимеры можно создавать из комбинаций проводящих полимеров или комбинаций производных полимеров и комбинации проводящих полимеров с непроводящими полимерами. В целом, электрическую проводимость полимера создают посредством удаления электрона из полимера конъюгированной π-орбитали через допирование и делокализацию электронов вдоль главной цепи полимера.
[0052] Чтобы гарантировать, что электрическое поле равномерно распределено по всей проводящей пластине, композиция пластины должна обладать высокими статическими диссипативными свойствами. Чтобы гарантировать, что по существу равное электрическое поле образуют все области каждой проводящей пластины, внешняя поверхность проводящей пластины может иметь одну или несколько тонких электропроводящих проволок (или нанопроволок), расположенных на или в первой электрически полупроводящей пластине. Проволоки можно располагать в виде решетчатой или сетчатой геометрической формы или сети. Проволоки не выдаются, поскольку они не мешают пользователю иметь возможность видеть гель через проволоки и проводящую пластину для того, чтобы позволять пользователю осуществлять мониторинг разделения белков во время электрофореза. Предпочтительные варианты осуществления, имеющие проволоки или сетки проволок, разнесенных на 0,5-1,0 см друг от друга, могут быть достаточными для того, чтобы создавать пластинчатый электрод, имеющий по существу равномерное электрическое поле, исходящее из его поверхности.
[0053] Снова со ссылкой на фиг. 1, смежно со внутренней поверхностью 14 первой проводящей пластины 2 находится электрофорезный гель 6. Электрофорезный гель 6 представляет собой типичный гелевый брусок. Гель 6 можно создавать из любого числа композиций, известных в данной области, в том числе агарозы, полиакриламида, Tris-глицина, bis-Tris и Tris-ацетата. Агарозные гели обычно используют для анализа ДНК и РНК и полиакриламидные гели, Tris-глицин, bis-Tris, Tris-ацетат для анализа белков. Типичные разрешающие гели для анализа белков получают из 6-15% полиакриламида. В предпочтительных вариантах осуществления bis-Tris гель находится в диапазоне от 10% до 12% и Tris-ацетат гель находится в диапазоне 7%-10%, но значения могут лежать вне этих диапазонов, в зависимости от размера белка, который хотят анализировать или исследовать в образце. Например, чем меньше известная масса макромолекулы, тем более высокую процентную долю геля следует использовать. Размеры электрофорезного геля 6 обычно представляют собой прямоугольник и в предпочтительном варианте осуществления составляют приблизительно 10 см × 10 см, но могут варьировать в зависимости от числа образцов, подлежащих одновременному прогону, типа образца и объема образца. В предпочтительном варианте осуществления комбинированный блок 10 предварительно отлитого геля и мембраны имеет толщину меньше 1 см, но также может быть разработан более тонким. На противоположной стороне электрофорезного геля 6 находится гель 8 с низкой проводимостью (т. е. высокой процентной долей).
[0054] Смежно с гелем 8 с низкой проводимостью находится мембрана 12 для переноса. Мембрана для переноса, также известная как мембрана для иммобилизации, может представлять собой любую из широкого диапазона материалов для блоттинга, таких как бумага для блоттинга, нитроцеллюлоза, PVDF, нейлон и другие материалы, а также такие материалы в обработанной или дериватизированной форме, как хорошо известно специалистам в данной области. Использование мембраны 12 и способа, с помощью которого макромолекулы переносят с электрофорезного геля 6 через гель 8 с низкой проводимостью на мембрану 12, рассмотрено более подробно ниже. Гель 8 с низкой проводимостью между мембраной 12 для переноса и электрофорезным гелем 6 предотвращает непосредственный контакт мембраны 12 для переноса с электрофорезным гелем 6 во время электрофореза. Поскольку белки имеют высокую аффинность к мембране 12 для переноса для вестерн-блоттинга, гель 8 с низкой проводимостью препятствует связыванию белков с поверхностью мембраны 12 во время электрофореза.
[0055] Смежно с мембраной 12 для переноса находится фильтровальная бумага 60. Фильтровальную бумагу 60 располагают между высокопроводящим гелем 8 и второй проводящей пластиной 4. Фильтровальная бумага 60, когда смочена, выполняет функцию вместилища ионов, тем самым содействуя переносу макромолекул на мембрану 12. Фильтровальная бумага также гарантирует, что мембрана 12 для переноса остается влажной. Мембрану 12 для переноса и фильтровальную бумагу 60 можно предварительно смачивать перед сборкой комбинированного блока геля и мембраны 10 метаноловым раствором, другим смачивающим буфером, или фильтровальную бумагу 60 можно смачивать буферным раствором, используемым в фазах электрофореза и блоттинга. Буфер для смачивания мембраны для переноса обычно содержит метанол.
[0056] Комбинированный блок 10 геля и мембраны с фиг. 1 содержит электрофорезный гель 6, гель 8 с низкой проводимостью, мембрану 12 для переноса и фильтровальную бумагу 60, все расположено между прозрачной первой проводящей пластиной 2 и второй проводящей пластиной 4. Варианты осуществления без геля 8 с низкой проводимостью и/или фильтровальной бумаги 60 также могут служить как для разделения макромолекул, так и для переноса макромолекул на мембрану 12 для переноса.
[0057] На фиг. 2 представлен вид спереди комбинированного блока 10 предварительно отлитого геля и мембраны для электрофореза и переноса белков. Во время фазы электрофоретического разделения, белки перемещают вертикально вниз из верхней части геля 20 в нижнюю часть геля 18. Во время электрофореза более крупные белки (показаны в виде верхних полос 62) двигаются медленнее через гель 6, чем менее крупные белки (показаны в виде нижних полос 64). В одном из вариантов осуществления имеют место две непроводящие изоляционные пластмассовые полоски 26, 28, которые фланкируют боковые части геля 6, но которые также располагают между проводящими пластмассовыми/полимерными листами 2, 4 для того, чтобы направлять ток через гель 6 во время стадии электрофореза. Эти полоски также обеспечивают структурную опору и жесткость для кассеты. Движение белков во время стадии переноса/блоттинга происходит вдоль оси z, перпендикулярной направлению разделения белков вдоль оси y.
[0058] Резервуарный аппарат 30 с фиг. 3, который вместе с комбинированным блоком 10 предварительно отлитого геля и мембраны служит в качестве системы как для фазы электрофоретического разделения, так и для фазы переноса. Резервуарный аппарат 30 представляет собой вместилище жидкости, которое содержит переднюю панель 32, заднюю панель 68, первую боковую панель 70, вторую боковую панель 72, нижнюю панель 66, закраину 58 на задней панели 68 и крышку (не показано). Закраина 58 может представлять собой различные геометрические формы, но в предпочтительном варианте осуществления является по существу U-образной вдоль внутренних стенок первой и второй боковых панелей 70, 72 резервуарного аппарата 30.
[0059] Гели для разделения белков и переноса обычно погружают в электролит, содержащий буферный раствор, такой как буфер Tris-ацетат-EDTA (TAE), в резервуарном аппарате 30. Другие буферы можно использовать в зависимости от типа геля, используемого в комбинированном блоке 10 предварительно отлитого геля/мембраны. Например, Tris-ацетатный буфер можно использовать для Tris-ацетатных гелей, тогда как буферы 2-(N-морфолино)этансульфоновой кислоты (MES) или 3-(N-морфолино)пропансульфоновой кислоты (MOPS) можно использовать для bis-Tris гелей. Буферы в этой системе должны быть эффективны как для фазы электрофореза, так и для фазы переноса. Резервуарный аппарат 30 имеет верхнюю камеру 34 и нижнюю камеру 36. Первый отрицательный электрод (катод) 38 фазы разделения располагают в верхней камере 34. Второй положительный электрод (анод) 40 фазы разделения располагают в нижней камере 36. Каждый из первого и второго электродов 38, 40 фазы разделения соединяют с программируемым источником мощности (не изображен) для того, чтобы питать электроды 38, 40 разделения. Источники мощности для резервуарных аппаратов для использования в электрофорезе и блоттинге хорошо известны в данной области. Желаемое напряжение между первым и вторым электродами 38, 40 фазы разделения составляет между 80 и 150 В. Источник мощности использует переключающее средство для электрической изоляции указанных электродов 38, 40 фазы разделения от указанных электродов 50, 52 переноса блоттинга.
[0060] Каждую из верхней камеры 34 и нижней камеры 36 заполняют буферным раствором 56 и электрически соединяют друг с другом через комбинированный блок 10 электропроводящего геля/мембраны, который позволяет отрицательным зарядам проходить от первого электрода 38 разделения через буфер 56 в верхнюю камеру 34, через гель 6 в буфер 56 в нижней камере 36 ко второму электроду 40 разделения. Это выполняют отчасти благодаря проводящим полимерам, вмещающим гель, которые имеют более высокое сопротивление, чем гель, который они вмещают. Задняя панель 68 имеет одно или несколько отверстий 74 в ее нижней области для того, чтобы позволять заполнять буферный раствор 56 из нижней камеры 36 вплоть до нижней поверхности 18 геля 6, чтобы обеспечивать электрическое соединение от второго электрода 40 разделения до геля 6. Буферный раствор 56 в верхней камере 34 и нижней камере 36 может представлять собой один и тот же буферный раствор или может представлять собой различные буферные растворы, где в некоторых вариантах осуществления буферный раствор 56 в верхней камере 34 может содержать антиоксидант.
[0061] Проволоки снабжают электричеством буферный раствор 56, что заставляет раствор в верхней камере 34 действовать в качестве катода (-) и раствор в нижней камере 36 действовать в качестве анода (+). Белки в буфере образцов, содержащем додецилсульфат натрия (SDS), или другие буферы, которые хорошо известны в данной области, придают белкам отрицательный суммарный заряд с тем, чтобы, находясь в геле 6, они двигались от катода (-) 38 к аноду (+) 40 посредством электродвижущей силы (ЭДС), создаваемой источником мощности, как известно в данной области. Помещая белки в лунки 84 в геле и накладывая электрическое поле, белки будут двигаться через гель 6 с различными скоростями, определяемыми главным образом их массами. Таким образом, первый электрод 38 разделения и второй электрод 40 разделения действуют в качестве катода и анода, соответственно, во время фазы электрофореза, который разделяет белки и другие макромолекулы по размеру.
[0062] Буферный раствор 56 в верхней камере 34 и нижней камере 36 не находятся в жидкостном контакте друг с другом, но все еще в электрическом контакте друг с другом. Контакт буферного раствора 56 в каждой камере 34, 36 предотвращают с помощью комбинированного блока 10 геля и мембраны и прокладок 44, 46, которые предотвращают заполнение всего резервуарного аппарата 30 буферным раствором 56. Прокладку 46 задней панели располагают на внутренней поверхности задней панели 68 резервуарного аппарата 10. Прокладка 46 задней панели препятствует контакту буфера 56 с электродом 52 блоттинга, что вызывало бы нежелательное протекание электрического тока во время фазы разделения. Дополнительно, имеет место прокладка 44 закраины, расположенная вдоль внешней поверхности закраины 58. Прокладка 44 закраины препятствует контакту буферного раствора 56, необходимого для фазы разделения, с охлаждающим раствором 54, используемым в охлаждающей камере 42. Охлаждающую камеру можно заполнять водой, буфером или охлаждающим средством другого типа. Прокладки в предпочтительных вариантах осуществления выполняют из резины, силикона или других материалов, общеизвестных в данной области, которые образуют уплотнения, которые предотвращают просачивание жидкости.
[0063] Прокладку 46 задней панели располагают с тем, чтобы, когда комбинированный блок 10 предварительно отлитого геля и мембраны помещают в резервуарный аппарат 30, внешняя поверхность 24 второй проводящей пластины 4 контактировала и прижималась к прокладке 46. Прокладку 44 закраины располагают с тем, чтобы прижимать внутреннюю поверхность первой проводящей пластины 2 к прокладке 44 закраины. Как показано на фиг. 4, прокладка 46 задней панели представляет собой непрерывное кольцо вдоль внутренней поверхности задней панели 68. Прокладка 44 закраины имеет открытую геометрическую форму, имеющую нижнюю область, соединенную с двумя боковыми областями (без верхней область для формирования кольцевой прокладки). Отсутствие резиновой уплотнительной структуры наверху позволяет буферу 56 находиться в электрическом контакте с верхней частью 20 геля 6. В общем, прокладки 44, 46 располагают так, что когда комбинированный блок 10 предварительно отлитого геля/мембраны помещают правильно в резервуарный аппарат 10, прокладки 44, 46 формируют уплотнения, которые сохраняют верхнюю камеру 34 и нижние камеры 36 (необходимые для фазы электрофореза) отделенными от охлаждающей камеры 42 и других структур, необходимых во время фазы переноса белков. Другой признак для предотвращения нахождения камер 34, 36, 42 в жидкостном и/или электрическом контакте друг с другом состоит в том, что первая проводящая пластина 2 больше второй проводящей пластины 4. В предпочтительном варианте осуществления первая проводящая пластина составляет приблизительно 12 см × 12 см и вторая проводящая пластина 4 составляет приблизительно 10 см × 10 см (приблизительно те же размеры, что у геля 6). Более крупная первая проводящая пластина 2 позволяет первой проводящей пластине 2 контактировать с прокладкой 44 закраины и меньшей второй проводящей пластине 4 находиться в контакте с прокладкой 46 задней панели. Меньшая вторая проводящая пластина 4 позволяет буферному раствору 56 проходить над и под второй проводящей пластиной 4 в верхней камере 34 и нижней камере 36, соответственно, чтобы достигать геля 6, но не обходить более крупную первую проводящую пластину 2. Это предотвращает попадание буферного раствора 56 в охлаждающую камеру 42 и контакт с электродами 50, 52 переноса, используемыми во время фазы переноса/блоттинга.
[0064] После фазы разделения, в которой белки разделяли вертикально вдоль геля 6 благодаря электрическому полю, создаваемому верхним и нижним электродами 38, 40 разделения, затем электрический ток переключают с электродов 38, 40 разделения на электроды 50, 52 переноса для использования в фазе переноса/блоттинга, который заставляет белки перемещаться из геля 6 на мембрану 12 через ЭДС, сообщаемую с помощью электродов 50, 52 переноса на первую проводящую пластину 2 и вторую проводящую пластину 4. Первая проводящая пластина 2 находится в электрическом контакте с первым электродом 50 переноса, соединенным с источником мощности, и вторая проводящая пластина 4 находится в электрическом контакте со вторым электродом 52 переноса. Поскольку первую и вторую проводящие пластины 2, 4 выполняют из проводящих пластмасс, когда ток подают на электроды 50, 52 переноса, проводящие пластины 2, 4 действуют в виде пластинчатых электродов.
[0065] В варианте осуществления, представленном на фиг. 3, первый электрод 50 переноса представляет собой дугообразную металлическую скобу для обеспечения достаточного натяжения, чтобы удерживать комбинированный блок 10 предварительно отлитого геля/мембраны на месте напротив прокладок 44, 46 для того, чтобы формировать различные камеры 34, 36, 42. Электрод 50 переноса, также может представлять собой элемент, отдельный от структуры, которая напрягает/натягивает комбинированный блок 10 предварительно отлитого геля и мембраны внутри резервуара 30, напротив различных прокладок 44, 46 в резервуаре 30. В других вариантах осуществления первый электрод 50 переноса можно разделять на две или больше скоб (например одна слева, одна справа) с тем, чтобы пользователь все же мог видеть гель 6, но этот комбинированный блок 10 предварительно отлитого геля/мембраны оставался прочно удерживаемым на месте. Скобы/подвесы/натяжители других типов также можно помещать внутрь охлаждающей камеры 42, не отступая от сущности изобретения до тех пор, пока имеет место натяжение и электрический контакт от электрода 50 переноса до первой проводящей пластины.
[0066] Второй электрод 52 переноса располагают вдоль внутренней поверхности задней панели 68, и он выполняет функцию анода (+) во время режима переноса белков/блоттинга. В варианте осуществления, представленном на фиг. 3, второй электрод 52 переноса обладает пружинным или откатным действием с тем, чтобы электрод 52 переноса образовывал достаточный контакт со второй проводящей пластиной 4. В других вариантах осуществления электрод 52 переноса может представлять собой элемент, отдельный от элемента, обладающего пружинным или откатным действием, чтобы помогать подпирать комбинированный блок 10 предварительно отлитого геля/мембраны внутри резервуара 30 к противолежащему распорному элементу. Электрический источник мощности соединяет первый электрод 50 переноса со вторым электродом 52 переноса и снабжает электроды 50, 52 переноса так, что первая проводящая пластина 2 выполняет функцию катода (-) и вторая проводящая пластина выполняет функцию анода (+) во время фазы переноса/блоттинга. Электрический источник должен давать достаточно электричества, чтобы достигать разности напряжений между двумя пластинчатыми электродами, чтобы достигать достаточного переноса белков в направлении второй проводящей пластины 4 на мембрану 12 для переноса, расположенную в комбинированном блоке 10 предварительно отлитого геля/мембраны. Типичное напряжение, подаваемое во время режим блоттинга, составляет приблизительно 30 В.
[0067] На фиг. 4 представлен вид в перспективе резервуарного аппарата 30 без комбинированного блока 10 предварительно отлитого геля/мембраны. Комбинированный блок 10 предварительно отлитого геля/мембраны помещают смежно (на левой стороне) с закраиной 58, имеющей прокладку 44 закраины. Поскольку первая проводящая пластина 2 больше второй проводящей пластины 4, первая проводящая пластина 2 лежит на внешней поверхности, тогда как электрофорезный гель 6, гель 8 с низкой проводимостью, мембрана 12 для переноса и фильтровальная бумага 60 находятся во внутренней полости закраины 58 и вторую проводящую пластину 4 прижимают к прокладке 46 задней панели.
[0068] На фиг. 5 представлен вид спереди комбинированного блока 10 предварительно отлитого геля/мембраны. Как описано ранее, первая проводящая пластина 2 больше второй проводящей пластины 4. Гель 6, гель 8 с низкой проводимостью, мембрана 12 для переноса и фильтровальная бумага 60 (не видна на фиг. 5, поскольку ее блокируют второй проводящей пластиной 4), все расположены между первой и второй проводящими пластинами 2, 4. В варианте осуществления с фиг. 5, гель 6, гель 8 с низкой проводимостью, мембрана 12 для переноса и фильтровальная бумага 60 имеют приблизительно ту же высоту, но могут иметь слегка меньшую ширину для того, чтобы позволять вставлять изоляционные пластмассовые полоски 26, 28, которые фланкируют боковые части геля 6. Во время формирования геля с помощью гребенки для геля в геле 6 можно создавать лунки 84, в которые можно помещать белки.
[0069] На фиг. 6-7 представлен другой вариант осуществления комбинированного блока 10 предварительно отлитого геля/мембраны. Вместо первой пластины 2, выполняемой полностью из проводящего полимера, первую пластину выполняют из прозрачной пластмассы, обладающей статическими диссипативными свойствами, с объемным удельным электрическим сопротивлением в диапазоне приблизительно от 108 до 1010 Ом-см. На внутренней поверхности первой пластины 2 или встроенными в первую пластину 2 имеет место множество проводящих проволок или сеть 76, которые могут быть расположены сеткой или решеткой. Сеть 76 распределяет электрический ток вдоль внутренней поверхности первой пластины 2. Также вдоль внутренней поверхности первой пластины 2 и в электрическом контакте с сетью 76 располагают тонкий прозрачный проводящий слой 78, который можно создавать из тонкого прозрачного проводящего полимера или прозрачной проводящей пленки (TCF) 78, имеющей объемное удельное электрическое сопротивление в диапазоне приблизительно от 104 до 105 Ом-см. TCF известны в данной области, и в вариантах осуществления с фиг. 6-7, первую пластину 2 покрывают TCF пленкой 76 или слоем прозрачного проводящего полимера, тем самым формируя пластинчатый электрод. Проволочная сетка 76 гарантирует равномерное распределение электрического заряда по пленке 78 или тонкому прозрачному проводящему полимеру. TCF может представлять собой проводящий полимер, но также может представлять собой прозрачный проводящий металл, включая в качестве неограничивающих примеров оксид индия-олова (ITO), допированное фтором олово (FTO), допированный оксид цинка, допированный алюминием оксид цинка (AZO). В предпочтительном варианте осуществления TCF представляет собой ITO, поскольку он химически устойчив к влаге, что благоприятно для длительного хранения комбинированного блока 10 предварительно отлитого геля и мембраны.
[0070] Одно возможное преимущество системы с использованием TCF из тонкого покрытия из прозрачного проводящего полимера состоит в том, что прозрачность проводящего полимера снижается с увеличением толщины, даже среди известных прозрачных проводящих полимеров. При ограничении проводящей области первой жесткой проводящей пластины 2 тонкой областью пластины (или наслоив поверх пластины 2), комбинированный блок 10 геля и мембраны сохраняет высокую прозрачность и высокую жесткость для того, чтобы формировать структурную опору электрофорезного геля 6. Тонкая пленка оксида индия-олова является прозрачной и проводящей. Однако если необходима и толщина и жесткость (например, в случае несущих гель пластин), толстые пластины оксида индия-олова утрачивают свою прозрачность и, таким образом, не являются идеальными для формирования всей проводящей пластины, поскольку пластина не позволит пользователю визуализировать разделение белков во время электрофореза. Первую электрически полупроводящую пластину можно охарактеризовать как имеющую внешнюю электрически полупроводящий прозрачный слой, лежащий поверх статической диссипативной пластмассы. Этот слой может быть очень тонким (меньше чем 1 мм или даже меньше чем 100 мкм).
[0071] На фиг. 6-7 представлен вид сбоку и вид в перспективе, соответственно, первой пластины 2, проволочной сетки 76, TCF или тонкого прозрачного проводящего полимера 78, электрофорезного геля 6, мембраны 12 для переноса, второй пластины 4 и дополнительной проволочной сетки 76, расположенных на внешней поверхности 24 второй пластины 4. Проволочная сетка 76, расположенная вдоль внешней поверхности второй 4, эффективно распределяет электрический ток вдоль задней пластины 4 для более эффективного переноса макромолекул из геля 6 на мембрану 12 для переноса.
[0072] На фиг. 8-9 проиллюстрирован другой пример комбинированного блока 10 предварительно отлитого геля и мембраны. На фиг. 8 представлен вид сверху и на фиг. 9 представлен вид в перспективе комбинированного блока 10 предварительно отлитого геля/мембраны. Этот вариант осуществления содержит два опорных выступа 80 непроводящей статической диссипативной передней пластины 2, упирающейся во внутреннюю поверхность задней пластины 4. Вторая пластина 4 покоится на опорах 80, тем самым образуя зазор между внутренней поверхностью первой пластины 2 и внутренней поверхностью второй пластины 16. Зазор может варьировать в зависимости от толщины геля. В одном из вариантов осуществления зазор находится в диапазоне приблизительно от 0,1 см приблизительно до 0,5 см. Зазор содержит различные компоненты, необходимые для надлежащего разделения и блоттинга макромолекул, как описано ранее, такие как электрофорезный гель 6, гель 8 с низкой проводимостью, мембрана 12 для переноса и фильтровальная бумага 60. В этом варианте осуществления вся первая пластина 2 является прозрачной, но не высокопроводящей. Проводимость вдоль внутренней поверхности первой пластины осуществляют через использование тонкого проводящего полимерного слоя или прозрачной проводящей пленки 78 другого типа, которая лежит поверх или соединена с первой проволочной сеткой 76, которая визуально не мешает видеть гель 6 через первую пластину 2. Первая проволочная сетка 76 распределяет электрический заряд по существу равномерно вдоль всего проводящего полимерного слоя 78 с тем, чтобы создавать электрическое поле на тонком проводящем полимерном слое 78, который затем выполняет функцию пластинчатого электрода. В предпочтительном варианте осуществления пленка или тонкий прозрачный полимер имеет толщину меньше чем 1 мм и имеет объемное удельное электрическое сопротивление между 104 и 105 Ом-см. Задняя пластина 4 имеет вторую проволочную сетку 82, которая создает по существу равномерный заряд вдоль всей задней пластины 4, тем самым создавая по существу равномерное электрическое поле с тем, чтобы эффективно и равномерно переносить макромолекулы из геля 6 на мембрану 12 для переноса во время фазы блоттинга.
[0073] В предпочтительном варианте осуществления буфер 56 для разделения/переноса имеет объемное удельное электрическое сопротивление приблизительно 10-200 Ом-см. Проводящая пластмассовая передняя пластина 2 и задняя пластина 4 имеет объемные удельные электрические сопротивления в диапазоне от 103 до 105 Ом-см. В варианте осуществления с использованием тонкого проводящего покрытия или пленки 78 на внутренней поверхности передней пластины 2 объемное удельное электрическое сопротивление покрытия или пленки находится в диапазоне от 104 до 105 Ом-см и переднюю пластину 2 выполняют из статической диссипативной прозрачной пластмассы с объемным удельным электрическим сопротивлением от 108 до 1010 Ом-см. Эти диапазоны допускают протекание электрического тока через гель во время фазы разделения, когда источник мощности подают на электроды 38, 40 разделения, а не через переднюю и заднюю пластины 2, 4. Затем, когда источник мощности подают на 50 и 52 или на 76 и 52, электрический ток будет течь по существу перпендикулярно длине геля от передней пластины 2, через гели 6, 8 и мембрану 12 к задней пластине 4, позволяя белкам погружаться в мембрану 12 для блоттинга во время фазы блоттинга. Хотя эти диапазоны описаны в терминах образцовых вариантов осуществления, следует понимать, что они не являются ограничивающими, поскольку любой вариант осуществления, в котором буфер 56 и гель 6 имеют обоснованно более низкое удельное электрическое сопротивление, чем проводящие полимеры (т. е. пластины 2, 4), которые вмещают их, и наоборот что проводящие полимеры (т. е. пластины 2, 4) имеют обоснованно более высокую проводимость, чем буфер 56 и гель 6, будет допускать описанные фазы разделения и переноса.
Свойства проводящих/полупроводящих полимеров для использования в несущих гель пластинах
[0074] Термин «проводящий», как он относится к полимерам в настоящем изобретении, связан с отсутствием электрической проводимости, встречаемым в большинстве полимеров, которые являются изоляционными. Проводящие полимеры являются менее проводящими, чем металлы, и следовательно являются полупроводящими, но термин «проводящий полимер» все же в целом используют и относят ко всем полимерам, которые попадают в диапазон, обычно рассматриваемый как полупроводящий. Полипирролы обычно имеют проводимость между 103 и 7,5×105 См/м. Политиофены имеют проводимость 101-103 См/м. Полифенилен и его аналоги поли(парафенилен) имеют проводимость 104-105 См/см. Поли(п-фениленвинилен) имеет проводимость 3-5×105 См/м, и полианилины имеют проводимость 3×103-2×104 См/м. Проводимость может возрастать при добавлении молекул для p-допирования или n-допирования полимера (например, допирования с использованием I2, AsF5, Na, K). Недопированные проводящие полимеры, такие как политиофены и полиацетилены, в целом имеют проводимость приблизительно 10-8-10-6 См/м. Удельное электрическое сопротивление, которое также широко используют для того, чтобы описывать характеристики материалов, представляет собой обратное значение проводимости.
[0075] Проводимость проводящих полимеров составляет порядка величины выше таковой у типичных изоляторов, таких как стекло, которое имеет проводимость между 10-11 и 10-15 См/м. Аналогичным образом, резина имеет проводимость приблизительно 10-14 См/м. В отличие от изоляторов, проводимость большинства металлов составляет порядка величины выше таковой у проводимых полимеров. Серебро, медь, золото, алюминий, вольфрам или большинство других металлов, которые имеют проводимость приблизительно 106-107 См/м. Свойство промежуточной проводимости проводящих полимеров позволяет этим проводящим полимерам действовать в качестве изоляторов или проводников, в зависимости от электрического заряда, подаваемого на них, и композиций окружающих проводящих полимеров. Полупроводящая природа пластин не позволяет пластинам вносить вклад в обнуление электрического поля, которое будет происходить, если несущие гель пластины являются высокопроводящими, как металлы.
Прозрачность несущих гель пластин
[0076] Термин «прозрачный», как понимают в данной области при обсуждении прозрачных проводящих полимеров, не только включают полимеры, которые являются на 100% оптически прозрачными, но также включают полимеры, которые являются полупрозрачными и позволяют некоторому количеству света проходить через полимер. С увеличением толщины прозрачных проводящих полимеров происходит некоторое ослабление и спектральная абсорбция, но полимеры все еще позволяют существенному количеству света проходить в количестве, достаточном, чтобы позволять пользователю визуализировать фронт красителя в геле через прозрачную пластину. Следовательно, термин «прозрачный проводящий полимер» или «прозрачный полупроводящий полимер» включает те полимеры и пластины, которые выполнены из полимеров, которые позволяют достаточно света пропускать через пластину, что позволяет пользователю визуализировать фронт красителя через пластину.
[0077] ПРОТОКОЛ ПРИМЕРА
Электрофорез в геле
1. Образцы белков (клеточные лизаты, иммунопреципитаты, рекомбинантные белки и т. д.) получают следующим образом:
a. Добавить 10 мкл 4× буфера образцов с додецилсульфатом натрия (SDS) [например, Tris-HCL 250 мМ; SDS 8%; глицерин 40%; β-меркаптоэтанол 4%; этилендиаминтетрауксусная кислота (EDTA) 50 мМ; бромфеноловый синий 0,8% масс./об.] в 30 мкл образца белка.
b. Инкубировать образцы при 70°C в течение 10 мин.
2. Приблизительно 20 мкл образцов загружают на гель 6 (например, 10% полиакриламид), который находится смежно с мембраной 12, которые вместе находятся между двумя проводящими/полупроводящими пластмассовыми пластинами 2, 4, что составляет комбинированный блок 10 предварительно отлитого геля и мембраны.
3. Приблизительно 10 мкл предварительно окрашенного белкового маркера загружают на гель. Поскольку передняя пластина прозрачна, предварительно окрашенный белковый маркер можно загружать в любую лунку.
4. Белки разделяют электрофоретически при постоянном напряжении на электродах 38, 40 фазы разделения. Напряжение и время, используемые для разделения, зависят от размера целевого белка(ов), желаемой степени разделения целевого белка(ов) и процентной доли геля (например 150 В в течение 60 мин для 10% полиакриламидного геля). Поскольку передняя пластина прозрачна, пользователь может осуществлять мониторинг относительной степени разделения через переднюю пластину посредством визуальной оценки продвижения предварительно окрашенного белкового маркера и фронта красителя из образцов белков.
Перенос разделенных образцов на мембраны
1. Осуществляли электроперенос разделенных белков на мембрану 12 при постоянной силе тока через электроды 50, 52 переноса. Используемые сила тока и время зависят от размера целевого белка(ов), подлежащего переносу (например, 500 мА, 30 мин). Напряжение, необходимое для достижения этой силы тока, выше такового по сравнению со стандартными устройствами переноса, в которых используют металлические пластинчатые электроды, поскольку выше сопротивление, таким образом конечное напряжение и сила тока будут зависеть от сопротивления используемого полимера и возможностей источника питания в отношении напряжения и силы тока.
Исследование разделенных и перенесенных образцов
1. Комбинированный блок 10 предварительно отлитого геля и мембраны разбирают для того, чтобы удалять мембрану с разделенными белками.
2. Мембрану инкубируют в блокирующем буфере [например, 5% обезжиренное сухое молоко в Tris-буферном физиологическом растворе с 1% Tween 20 (TBST)] в течение 1 часа при комнатной температуре (или альтернативно в течение ночи при 4°C).
3. Мембрану 12 инкубируют с подходящим разведением первичного антитела в блокирующем буфере (например 1:200-1:1000 для многих коммерчески доступных антител) в течение 1 часа при комнатной температуре (или альтернативно в течение ночи при 4°C).
4. Мембрану 12 промывают три раза в TBST, по 5 мин каждый.
5. Мембрану 12 инкубируют с рекомендованным разведением конъюгированного вторичного антитела в блокирующем буфере в течение 1 часа при комнатной температуре (например, 1:5000 для HRP-конъюгатов при 1 мг/мл).
6. Мембрану промывают три раза в TBST, по 5 мин каждый.
7. Для развития сигнала используют рекомендованный производителем субстрат.
8. Изображения получают с использованием стандартных способов проявки в темном помещении для хемилюминесценции или обычных способов сканирования изображений для колориметрического обнаружения.
ПРИМЕРЫ КОМПОЗИЦИЙ ПОЛУПРОВОДЯЩИХ ПЛАСТИН
[0078] Многие составы прозрачных полимеров могут подлежать использованию в качестве несущих гель пластин. Прозрачные проводящие/полупроводящие полимерные пластины можно выполнять из поли(пиррол)ов (PPY), полиацетилена, полианилинов (PANi), поли(тиофен)ов (PT), поли(3,4-этилендиокситиофена) (PEDOT), поли(п-фениленсульфида (PPS), поли(ацетилен)ов (PAC), и поли(п-фениленвинилена) (PPV) и их композитов. Например, PPY, один из наиболее хорошо охарактеризованных среди проводящих/полупроводящих полимеров, встраивали в композиты со стандартными/изоляционными полимерами, включающими акриловые полимеры (см. «Surface Characterization of Conductive Poly(methyl methacrylate)/Polypyrrole Composites», Journal of Materials Science 35 (2000) 1743-1749), целлюлозу (см. «A Nano cellulose Polypyrrole Composite Based on Tunicate Cellulose», International Journal of Polymer Science, том 2013, ID статьи 175609), полистирол (см. «Synthesis and Characterization of Nano sized Polypyrrole Polystyrene Composite Particles», Journal of Applied Polymer Science, том 91, 1360-1367 (2004)), полиуретан (см. «Polypyrrole Composites for shielding applications», Synthetic Metals 151 (2005) 211-217), полидиметилсилоксаны (см. «Flexible and Conducting Composites of Polypyrrole and Polydimethylsiloxane», Journal of Applied Polymer Science, том 93, 736-741 (2004)), полиэтиленгликоль (PEG) (см. «Studying the Characteristics of Polypyrrole and its Composites», World Journal of Chemistry 2 (2: 67-74, 2007) и поли(акрилонитрил-ко-винилацетат (см. «Characterization of Conductive Poly(Acrylonitrio-co-Vinyl Acetate Composites: Matrix Polymerization of Pyrrole Derivatives», Fibers and Polymers 2011, том 12, № 2, 151-158). Что важно, создавали композиты PPy с этими стандартными сополимерами, где композитные материалы сохраняют механические и физические свойства стандартного материала и электрическую проводимость проводящего полимера (см. «Chemical in situ polymerization of polypyrrole on poly(methyl methacrylate) substrate», Thin Solid Film 515 (2007) 5324-5328). Эти композиты согласованно получали в пределах или ниже диапазона объемного удельного электрического сопротивления, который необходим для фазы переноса в комбинированном блоке предварительно отлитого геля и мембраны, что указывает на то, что низкая процентная доля PPy в композите со стандартными сополимерами имеет удельное электрическое сопротивление, достаточно высокое для использования в фазе разделения во время электрофореза с тем, чтобы не возникал эффект обнуления поля, и достаточную проводимость для фазы переноса, чтобы осуществлять перенос белков из геля, расположенного между пластинами, на мембрану для блоттинга.
[0079] Проводимость можно корректировать, варьируя величину концентрация мономерного инициатора, добавляемого к PPy (см. «The Regulation of Osteogenesis Using Electroactive Polypyrrole Films. Polymers, 2016; 8(7): 258). PPy можно смешивать со стандартными пластмассами с тем, чтобы смесь могла сохранять прозрачность и жесткость стандартных пластмасс, а также электрическую проводимость PPy. Композиты, содержащие 99% полиуретана (стандартный полимер) и 1% PPy-Ni (PPy-никелевый композит, обладающий полупроводящими свойствами), имеют проводимость, достаточную для использования гелевой пластины как для электрофоретического разделения белков, так и блоттинга (см. «Polypyrrole Composites for Shielding Applications», Synthetic Metals 151 (2005) 211-217). 95% стандартный полимер 5% PPy полимер 2 мм толщиной (или пластина толщиной 1 мм из композита из 90% стандартного полимера, 10% PPy) является достаточно жестким, прозрачным и проводящим для использования в настоящих вариантах осуществления. Вариации диапазонов толщины между 0,5 мм и 4 мм или выше также можно создавать для использования в настоящих вариантах осуществления, при условии, что стандартный полимер отвечает требованиям к жесткости и прозрачности, среди которых многие хорошо известны и доступны в данной области. Композиты между 1% и 10% PPy могут обеспечивать первую электрически полупроводящую пластину достаточным объемным удельным электрическим сопротивлением, чтобы действовать в качестве изоляционной пластины во время фазы разделения белков, и достаточной проводимостью для того, чтобы сделать возможным перенос белков из геля на мембрану для блоттинга во время переноса белков.
[0080] В вариантах осуществления, где полупроводящие пластины не состоят из полупроводящего полимера на протяжении всей пластины, слой PPy можно наносить на листы статической диссипативной жесткой пластмассы с тонкой проволочной сеткой между пластиной и PPy можно использовать для достижения той же цели. Слои PPy толщиной 100 мкм или тоньше могут сохранять достаточную прозрачность для того, чтобы позволять видеть предварительно окрашенный белковый маркер и краситель для загрузки образцов (фронт красителя) при покрывании прозрачной статической диссипативной пластины.
[0081] Другая композиция для использования в прозрачных полупроводящих пластинах включает композиты полианилинов (PANI), которые являются электрохромными и меняют цвет/прозрачность в зависимости от подаваемого напряжения (см. «Electrochromic Properties of Polyaniline-Based Hybrid Organic/Inorganic Materials», J. Braz. Chem. Soc., том 27, № 10, 1847-1857, 2016»). Например, когда на композит на подают напряжение, PANI композит прозрачный желтый. Композит меняется на зеленый/синий, когда подают напряжение. При использовании этого полимера композит будет непрозрачным и будет иметь низкое оптическое пропускание, когда аппарат работает, но когда пользователь выключает напряжение, пользователь может оценивать степень разделения белков в любое время во время выполнения электрофореза и затем повторно подавать ток, чтобы продолжать разделение белков. Тонкие слои PANI можно наносить на прозрачные статические диссипативные листы или PANI можно смешивать с другими полимерами, чтобы сохранять желтую прозрачность в состоянии без напряжения при увеличенных толщинах.
[0082] Другой класс материалов для использования, когда прозрачность не требуется (т. е. для задней пластины, которой не нужна прозрачность) представляет собой смесь ионных электрических проводников (MIEC). Эти материалы имеют как ионную, так и электрическую проводимость. Например, непрозрачную электрически проводящую/полупроводящую пластину, которая также представляет собой ионный проводник, можно выполнять из нановолокнистого целлюлоза-поли[3,4-этилендиокситиофена] (NFC-PEDOT) (см. «An Organic Mixed Ion-Electron Conductor for Power Electronics», Advanced Science 2016, 3, 1500305). NFC-PEDOT обладает электрическими свойствами, совместимыми с использованием во время обеих фаз разделения и переноса, и повышает эффективность фазы переноса, поскольку он также действует в качестве вместилища ионов. Другие непрозрачные проводящие/полупроводящие полимеры, которые можно использовать для создания пластин, включают коммерчески доступные Tivar® EC, Tecaform® ELS, полиэфирэфиркетон (PEEK) с 30% заполнением углеродом, Tecapeek® ELS. проводящий полиэфиримид Tempalux® CN (PEI), проводящий полиэфирсульфон (PES CN), Kynar® PVDF CN (поливинилиденфторид) со статическим контролем, ацеталь Pomalux® со статическим контролем, полипропилен Propylux® со статическим контролем, акрилонитрил-бутадиен-стирол (ABS) Absylux® со статическим контролем и поликарбонат Zelux® со статическим контролем, доступные в Boedeker Plastics, Inc. (Texas)
[0083] Хотя изобретение описано в терминах образцовых вариантов осуществления, следует понимать, что слова, использованные в настоящем описании, являются словами описания, а не ограничения. Как поймут средние специалисты в данной области, различные модификации можно выполнять, не отступая от объема изобретения, которое определено следующей формулой изобретения, которая должна давать его полнейший истинный объем.
Claims (50)
1. Аппарат для электрофоретического разделения и блоттинга, который содержит:
первую электрически полупроводящую пластину, выполненную из прозрачного полупроводящего полимера;
вторую электрически полупроводящую пластину, выполненную из полупроводящего полимера, где вторая электрически полупроводящая пластина по существу параллельна первой электрически полупроводящей пластине;
электрофорезный гель и,
мембрану для блоттинга;
где электрофорезный гель находится между первой электрически полупроводящей пластиной и мембраной для блоттинга и
где мембрана для блоттинга находится между электрофорезным гелем и второй электрически полупроводящей пластиной.
2. Аппарат по п.1, который дополнительно содержит:
гель с низкой проводимостью, обладающий более низкой проводимостью, чем электрофорезный гель, где гель с низкой проводимостью находится между электрофорезным гелем и мембраной для блоттинга, в соответствии с чем гель с низкой проводимостью предотвращает миграцию макромолекул, чтобы они не диффундировали из электрофорезного геля и не прилипали к мембране для блоттинга во время фазы разделения макромолекул;
фильтровальную бумагу между второй полупроводящей пластиной и мембраной для блоттинга, в соответствии с чем фильтровальная бумага, когда увлажнена, выполняет функцию вместилища ионов и обеспечивает существенный электрический контакт между мембраной для блоттинга второй полупроводящей пластиной, чтобы содействовать переносу макромолекул из электрофорезного геля через гель с низкой проводимостью на мембрану для блоттинга;
где мембрана для блоттинга представляет собой по меньшей мере одно из нитроцеллюлозной мембраны, поливинилидендифторидной (PVDF) мембраны или нейлоновой мембраны.
3. Аппарат по п.1, который дополнительно содержит электропроводящие проволоки, расположенные на или в первой электрически полупроводящей пластине, где первая электрически полупроводящая пластина отличается наличием внешнего электрически полупроводящего прозрачного слоя, лежащего поверх статической диссипативной пластмассы.
4. Аппарат по п.3, в котором внешний электрически полупроводящий прозрачный слой составляет меньше чем 1 мм и расположен на внутренней поверхности первой электрически полупроводящей пластины, где внешний электрически полупроводящий прозрачный слой содержит по меньшей мере одно из оксида индия-олова, допированного фтором олова, допированного оксида цинка и допированного алюминием оксида цинка
5. Аппарат по п.1, в котором первая электрически полупроводящая пластина выполнена из полимера, содержащего прозрачные проводящие полимеры одного или нескольких типов, выбранных из группы, состоящей из полиацетилена, поли(пиррол)ов (PPy), полианилинов, политиофена, поли(3,4-этилендиокситиофена), поли(п-фенилен)сульфида, поли(п-фениленвинилена) и их производных, и где первая электрически полупроводящая пластина имеет объемное удельное электрическое сопротивление между 103 и 108 Ом-см.
6. Аппарат по п.5, в котором первая электрически полупроводящая пластина имеет толщину по меньшей мере 1 мм и состоит из композита прозрачного проводящего полимера и прозрачного непроводящего полимера.
7. Аппарат по п.6, в котором композит представляет собой композит PPy между 1% и 10%, тем самым предусматривая первую электрически полупроводящую пластину, имеющую достаточное объемное удельное электрическое сопротивление, чтобы действовать в качестве изоляционной пластины во время фазы разделения белков, и достаточную проводимость для того, чтобы сделать возможным миграцию белков к мембране для блоттинга во время фазы переноса белков, и достаточную жесткость, чтобы поддерживать электрофорезный гель, и достаточную прозрачность, чтобы позволять пользователю визуализировать фронт красителя через первую электрически полупроводящую пластину.
8. Аппарат по п.7, в котором PPy композит представляет собой PPy-никелевый композит, обладающий полупроводящими свойствами.
9. Аппарат для электрофоретического разделения и блоттинга макромолекул, который содержит:
первую пластину, выполненную из прозрачного полимера;
электрически полупроводящий прозрачный слой смежно с первой пластиной;
вторую пластину по существу параллельно первой пластине;
электрофорезный гель и,
мембрану для блоттинга;
где электрофорезный гель находится между электрически полупроводящим прозрачным слоем и мембраной для блоттинга и,
где мембрана для блоттинга находится между электрофорезным гелем и второй пластиной.
10. Аппарат по п.9, который дополнительно содержит
первую электрически проводящую проволочную решетку в контакте с первой пластиной и электрически полупроводящим прозрачным слоем; и,
в соответствии с чем первая электрически проводящая проволочная решетка распределяет заряд по электрически полупроводящему прозрачному слою.
11. Аппарат по п.10, в котором электрически полупроводящий прозрачный слой представляет собой электрически полупроводящую пленку, расположенную на внутренней поверхности первой пластины, где электрически полупроводящая пленка выполнена из пленки, содержащей проводящие прозрачные металлы одного или нескольких типов, выбранных из группы, состоящей из оксида индия-олова, допированного фтором олова, допированного оксида цинка, допированного алюминием оксид цинка и их производных.
12. Аппарат по п.9, в котором первая пластина выполнена из полимера, содержащего прозрачные проводящие полимеры одного или нескольких типов, выбранных из группы, состоящей из полиацетилена, поли(пиррол)ов (PPy), полианилинов, политиофена, поли(3,4-этилендиокситиофена), поли(п-фенилен)сульфида, поли(п-фениленвинилена) и их производных.
13. Аппарат по п.9, в котором прозрачный полупроводящий слой имеет объемное удельное электрическое сопротивление между 104 и 105 Ом-см и первая пластина имеет объемное удельное электрическое сопротивление между 108 и 1010 Ом-см.
14. Аппарат по п.9, который дополнительно содержит вторую электропроводящую проволочную решетку смежно со второй пластиной, в соответствии с чем вторая электропроводящая проволочная решетка распределяет электрический заряд по второй пластине.
15. Система для электрофоретического разделения и блоттинга макромолекул, которая содержит:
резервуар вместилища жидкости, имеющий верхнюю камеру буфера и нижнюю камеру буфера, переднюю панель, заднюю панель и дно;
первый электрод фазы разделения в верхней камере буфера;
второй электрод фазы разделения в нижней камере буфера;
первый электрод фазы блоттинга;
второй электрод фазы блоттинга;
комбинированный блок предварительно отлитого геля и мембраны, который имеет (i) первую электрически полупроводящую пластину, выполненную из прозрачного полупроводящего полимера, (ii) вторую электрически полупроводящую пластину, выполненную из полупроводящего полимера, где вторая электрически полупроводящая пластина по существу параллельна первой электрически полупроводящей пластине, (iii) электрофорезный гель и (iv) мембрану для блоттинга; и,
источник питания, где источник питания выполнен с возможностью подавать напряжение на первый электрод фазы разделения и второй электрод фазы разделения для того, чтобы осуществлять электрофоретическое разделение макромолекул вдоль электрофорезного геля, и где источник питания выполнен с возможностью автоматически переключать напряжение с первого и второго электродов фазы разделения на первый и второй электроды фазы блоттинга, в соответствии с чем переключение напряжения позволяет пользователю осуществлять электрофоретическое разделение белков и перенос белков на мембрану для блоттинга.
16. Система по п.15,
в которой резервуар вместилища жидкости дополнительно содержит охлаждающую камеру, вмещающую первый электрод фазы блоттинга; и,
прокладку, расположенную на задней панели резервуара вместилища жидкости, в соответствии с чем прокладка препятствует течению жидкости из верхней камеры в нижнюю камеру, когда комбинированный блок предварительно отлитого геля и мембраны помещают в резервуар вместилища жидкости.
17. Способ разделения и переноса макромолекул на мембрану для блоттинга после разделения, включающий стадии:
предоставления аппарата в первой ориентации в резервуаре вместилища жидкости, где аппарат имеет первую электрически полупроводящую пластину, выполненную из (i) прозрачного полупроводящего полимера, (ii) вторую электрически полупроводящую пластину, выполненную из полупроводящего полимера, вторая электрически полупроводящая пластина по существу параллельна первой электрически полупроводящей пластине, (iii) электрофорезный гель и (iv) мембрану для блоттинга, где электрофорезный гель находится между первой полупроводящей пластиной и мембраной для блоттинга и где мембрана для блоттинга находится между электрофорезным гелем и второй электрически полупроводящей пластиной;
разделения макромолекул вдоль геля аппарата посредством приложения первой электрической движущей силы к паре электродов разделения, где разделение макромолекул вдоль геля происходит в первой ориентации аппарата;
прекращения первой электрической движущей силы на паре электродов разделения;
переноса макромолекул через гель на мембрану для блоттинга посредством приложения второй электрической движущей силы по существу перпендикулярно первой электрической движущей силе, при этом сохраняя первую ориентацию аппарата, тем самым объединяя стадии разделения и переноса макромолекул на мембрану для блоттинга в одном резервуаре вместилища жидкости без необходимости менять ориентацию аппарата между стадией разделения и стадией переноса.
18. Способ по п.17, который дополнительно включает стадию:
предварительного программирования источника мощности, чтобы прикладывать первую электрическую движущую силу, прекращать первую электрическую движущую силу и прикладывать вторую электрическую движущую силу по существу перпендикулярно первой электрической движущей силе.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562253143P | 2015-11-10 | 2015-11-10 | |
| US62/253,143 | 2015-11-10 | ||
| US15/017,540 | 2016-02-05 | ||
| US15/017,540 US20170131234A1 (en) | 2015-11-10 | 2016-02-05 | Gel Electrophoresis and Transfer Combination using Conductive Polymers and Method of Use |
| US15/348,803 | 2016-11-10 | ||
| US15/348,803 US9753008B2 (en) | 2015-11-10 | 2016-11-10 | Gel electrophoresis and transfer combination using conductive polymers and method of use |
| PCT/US2016/061443 WO2017083591A1 (en) | 2015-11-10 | 2016-11-10 | Gel electrophoresis and transfer combination using conductive polymers and method of use |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2018121330A RU2018121330A (ru) | 2019-12-16 |
| RU2018121330A3 RU2018121330A3 (ru) | 2019-12-25 |
| RU2723936C2 true RU2723936C2 (ru) | 2020-06-18 |
Family
ID=58663609
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2018121330A RU2723936C2 (ru) | 2015-11-10 | 2016-11-10 | Комбинация электрофореза в геле и переноса с использованием проводящих полимеров и способ использования |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US9753008B2 (ru) |
| JP (1) | JP6803918B2 (ru) |
| KR (1) | KR20180081538A (ru) |
| AU (1) | AU2016353162B2 (ru) |
| CA (1) | CA3007754A1 (ru) |
| RU (1) | RU2723936C2 (ru) |
| WO (1) | WO2017083591A1 (ru) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2723936C2 (ru) * | 2015-11-10 | 2020-06-18 | ВУДХЭМ БАЙОТЕКНОЛОДЖИ ХОДИНГЗ, ЭлЭлСи | Комбинация электрофореза в геле и переноса с использованием проводящих полимеров и способ использования |
| US9702851B1 (en) * | 2016-06-17 | 2017-07-11 | Woodham Biotechnology Holdings, LLC | Gel electrophoresis and transfer combination using conductive polymers and method of use |
| WO2019237205A1 (en) * | 2018-06-14 | 2019-12-19 | Coastal Genomics Inc. | Device for capturing macromolecules and methods for manufacturing and using same |
| CN108878838B (zh) * | 2018-06-29 | 2020-06-05 | 北京理工大学 | 在中空硫球表面包覆聚吡咯的方法 |
| CN109239169A (zh) * | 2018-08-21 | 2019-01-18 | 昆明医科大学 | 一种凝胶电泳迁移实验的转膜方法 |
| JP2023534015A (ja) * | 2020-07-13 | 2023-08-07 | ライフ テクノロジーズ コーポレーション | 電気泳動及び電気泳動転写デバイス、システム、並びに方法 |
| USD975873S1 (en) | 2020-07-13 | 2023-01-17 | Life Technologies Corporation | Electrophoresis and electrotransfer device |
| US12449396B2 (en) * | 2020-07-28 | 2025-10-21 | Life Technologies Corporation | Electrotransfer and electrophoresis devices, systems, and methods |
| KR102552065B1 (ko) * | 2022-03-18 | 2023-07-06 | 동우 화인켐 주식회사 | 광학 적층체 및 이의 제조 방법 |
| JPWO2024231999A1 (ru) * | 2023-05-09 | 2024-11-14 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4994166A (en) * | 1989-08-22 | 1991-02-19 | Bio-Rad Laboratories, Inc. | Single apparatus for slab gel electrophoresis and blotting |
| RU2099696C1 (ru) * | 1996-07-22 | 1997-12-20 | Саратовский научно-исследовательский институт кардиологии при Саратовском государственном медицинском университете | Микроэлектрофоретическая камера |
| US20060187527A1 (en) * | 2005-02-23 | 2006-08-24 | Seiko Epson Corporation | Electrophoretic device and electronic equipment |
| US20080053829A1 (en) * | 2005-09-05 | 2008-03-06 | Chie Hayashida | Electrophoresis Apparatus and Device Therefor |
Family Cites Families (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6232145A (ja) | 1985-08-05 | 1987-02-12 | Yamauchi Rubber Ind Co Ltd | 透明半導電性材料 |
| US4840714A (en) * | 1987-05-13 | 1989-06-20 | American Bionetics, Inc. | Electroblotting technique for transferring specimens from a polyacrylamide electrophoresis or like gel onto a membrane |
| US4994416A (en) | 1988-02-04 | 1991-02-19 | Martin Marietta Energy Systems, Inc. | Ceramic composites reinforced with modified silicon carbide whiskers and method for modifying the whiskers |
| DE3816625A1 (de) * | 1988-05-16 | 1989-11-30 | Europ Lab Molekularbiolog | Vorrichtung zur gel-elektrophorese, insbesondere fluoreszenz-gelelektrophorese |
| FR2639253B2 (fr) | 1988-09-06 | 1991-07-26 | Bertin & Cie | Dispositif d'electrophorese multiple pour assurer la migration controlee de macromolecules dans des plaques rectangulaires de gel |
| FR2699423B1 (fr) | 1992-12-22 | 1995-03-17 | Bertin & Cie | Procédé et dispositif d'électrophorèse multiple pour la migration et le transfert de macromolécules. |
| JPH06192471A (ja) | 1992-12-25 | 1994-07-12 | Showa Electric Wire & Cable Co Ltd | 半導電性樹脂組成物 |
| US5449446A (en) | 1994-03-09 | 1995-09-12 | Verma; Sumeet | Multi-purpose electrophoresis apparatus |
| US6602391B2 (en) | 2001-03-05 | 2003-08-05 | Vladimir B. Serikov | Apparatus and method for combined capillary separation and blotting of biological macromolecules |
| DK2461156T3 (da) | 2001-06-29 | 2020-08-03 | Meso Scale Technologies Llc | Indretning til luminescenstestmålinger |
| US20030032201A1 (en) * | 2001-08-10 | 2003-02-13 | Flesher Robert W. | Method and device for electrophoresis and blotting |
| US6933051B2 (en) | 2002-08-17 | 2005-08-23 | 3M Innovative Properties Company | Flexible electrically conductive film |
| US7118836B2 (en) | 2002-08-22 | 2006-10-10 | Agfa Gevaert | Process for preparing a substantially transparent conductive layer configuration |
| DE10252177A1 (de) | 2002-11-09 | 2004-06-09 | Roche Diagnostics Gmbh | Trennvorrichtung und Trennverfahren für biomolekulares Probenmaterial |
| JP4619728B2 (ja) | 2004-09-02 | 2011-01-26 | 株式会社エンプラス | 試料分析装置 |
| US7427441B2 (en) | 2004-09-17 | 2008-09-23 | Eastman Kodak Co | Transparent polymeric coated conductor |
| EP1853696B1 (en) * | 2005-02-24 | 2019-04-17 | Life Technologies (Israel) Ltd. | Electro-blotting devices, systems, and kits, and methods for their use |
| WO2007106832A2 (en) * | 2006-03-13 | 2007-09-20 | Sage Science, Inc. | Multifunctional electrophoresis cassette |
| US8029657B1 (en) | 2006-03-14 | 2011-10-04 | University Of Tennessee Research Foundation | Parallel plate electrodes for particle concentration or removal |
| US20080296158A1 (en) | 2007-05-31 | 2008-12-04 | Sharp Kabushiki Kaisha | Device for electrophoresis, device for transfer, device for electrophoresis and transfer, chip for electrophoresis and transfer, and method for electrophoresis, method for transfer, and method for electrophoresis and transfer |
| JP5353705B2 (ja) * | 2007-10-26 | 2013-11-27 | コニカミノルタ株式会社 | 透明導電性フィルム及びその製造方法 |
| WO2009131257A1 (en) | 2008-04-21 | 2009-10-29 | Korea Institute Of Machinery & Materials | Conductive polymer transparent electrode and fabricating method thereof |
| ITMI20080927A1 (it) | 2008-05-20 | 2009-11-21 | Meccaniche Luigi Bander A S P | Pannello fotovoltaico relativo procedimento di produzione ed impianto per la realizzazione di tale procedimento |
| CN102150045A (zh) * | 2008-07-11 | 2011-08-10 | 生命技术公司 | 增强型电泳检测固相支持物上的分析物 |
| JP5256437B2 (ja) * | 2008-10-15 | 2013-08-07 | 凸版印刷株式会社 | 生体分子分離装置 |
| WO2010126876A1 (en) | 2009-04-27 | 2010-11-04 | Drexel University | Transparent conformal polymer antennas for rfid and other wireless communications applications |
| EP2433143B1 (en) | 2009-05-19 | 2016-03-02 | The Regents of The University of California | Multi-directional microfluidic devices and methods |
| KR101095097B1 (ko) | 2009-12-23 | 2011-12-20 | 삼성전기주식회사 | 투명 전극 필름 및 이의 제조 방법 |
| WO2011106693A2 (en) | 2010-02-26 | 2011-09-01 | The Regents Of The University Of Michigan | Microscale western blot |
| EP2572189B1 (en) | 2010-05-21 | 2017-07-19 | Agilent Technologies, Inc. | Western blot analytical technique |
| EP2577683B1 (en) | 2010-05-27 | 2018-01-03 | Prysmian Cables and Systems USA, LLC | Electrical cable with semi-conductive outer layer distinguishable from jacket |
| WO2012027219A1 (en) | 2010-08-23 | 2012-03-01 | Advanced Bioscience Technologies, Llc | Pre-assembled and pre-wet multilayer substrate for western blotting |
| TW201420720A (zh) | 2012-07-24 | 2014-06-01 | Solvay Korea Co Ltd | 導電聚合物組合物及由其製成之透明電極和/或防靜電層 |
| JP6244134B2 (ja) | 2013-08-02 | 2017-12-06 | 富士フイルム株式会社 | パターン形成方法、及び、電子デバイスの製造方法 |
| RU2723936C2 (ru) * | 2015-11-10 | 2020-06-18 | ВУДХЭМ БАЙОТЕКНОЛОДЖИ ХОДИНГЗ, ЭлЭлСи | Комбинация электрофореза в геле и переноса с использованием проводящих полимеров и способ использования |
-
2016
- 2016-11-10 RU RU2018121330A patent/RU2723936C2/ru active
- 2016-11-10 CA CA3007754A patent/CA3007754A1/en active Pending
- 2016-11-10 WO PCT/US2016/061443 patent/WO2017083591A1/en not_active Ceased
- 2016-11-10 JP JP2018543305A patent/JP6803918B2/ja not_active Expired - Fee Related
- 2016-11-10 KR KR1020187015637A patent/KR20180081538A/ko not_active Ceased
- 2016-11-10 US US15/348,803 patent/US9753008B2/en active Active
- 2016-11-10 AU AU2016353162A patent/AU2016353162B2/en not_active Ceased
-
2017
- 2017-08-28 US US15/688,738 patent/US9983168B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4994166A (en) * | 1989-08-22 | 1991-02-19 | Bio-Rad Laboratories, Inc. | Single apparatus for slab gel electrophoresis and blotting |
| RU2099696C1 (ru) * | 1996-07-22 | 1997-12-20 | Саратовский научно-исследовательский институт кардиологии при Саратовском государственном медицинском университете | Микроэлектрофоретическая камера |
| US20060187527A1 (en) * | 2005-02-23 | 2006-08-24 | Seiko Epson Corporation | Electrophoretic device and electronic equipment |
| US20080053829A1 (en) * | 2005-09-05 | 2008-03-06 | Chie Hayashida | Electrophoresis Apparatus and Device Therefor |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2018121330A (ru) | 2019-12-16 |
| JP6803918B2 (ja) | 2020-12-23 |
| US9983168B2 (en) | 2018-05-29 |
| RU2018121330A3 (ru) | 2019-12-25 |
| AU2016353162A1 (en) | 2018-06-14 |
| US20170131235A1 (en) | 2017-05-11 |
| US20170356876A1 (en) | 2017-12-14 |
| CA3007754A1 (en) | 2017-05-18 |
| AU2016353162B2 (en) | 2023-02-23 |
| US9753008B2 (en) | 2017-09-05 |
| WO2017083591A1 (en) | 2017-05-18 |
| JP2018536875A (ja) | 2018-12-13 |
| KR20180081538A (ko) | 2018-07-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2723936C2 (ru) | Комбинация электрофореза в геле и переноса с использованием проводящих полимеров и способ использования | |
| Gong et al. | Ultrathin flexible electrochromic devices enabled by highly transparent ion-conducting films | |
| Saab et al. | Determination of ionic and electronic resistivities in carbon/polyelectrolyte fuel-cell composite electrodes | |
| Denisevich et al. | Unidirectional current flow and charge state trapping at redox polymer interfaces on bilayer electrodes: principles, experimental demonstration, and theory | |
| JP4547852B2 (ja) | 電気部品の製造方法 | |
| CN108473531B (zh) | 使用导电聚合物的凝胶电泳和转移组合以及使用方法 | |
| Henning et al. | Polymer films on electrodes. 6. Bioconductive polymers produced by incorporation of tetrathiafulvalenium in a polyelectrolyte (Nafion) matrix | |
| KR20090014343A (ko) | 밀폐형 모노리식 광-전자화학 시스템과 밀폐형 모노리식 광-전자화학 시스템을 제조하는 방법 | |
| US20080296158A1 (en) | Device for electrophoresis, device for transfer, device for electrophoresis and transfer, chip for electrophoresis and transfer, and method for electrophoresis, method for transfer, and method for electrophoresis and transfer | |
| US11402349B2 (en) | High capacity redox electrodes and their use in cell lysis | |
| EP4060332A1 (en) | Horizontal electrophoresis apparatus | |
| US10203304B2 (en) | Gel electrophoresis and transfer combination using conductive polymers and method of use | |
| CN110184619B (zh) | 导电高分子膜的膜电位的产生方法 | |
| KR102823986B1 (ko) | 이온성 액체를 포함하는 마찰대전 나노발전기용 고분자 겔 및 이를 포함하는 마찰대전 나노발전기 | |
| Jernigan et al. | A benzimidazobenzophenanthroline polymer molecular transistor fabricated using club sandwich electrodes | |
| Fu et al. | Electrosynthesis and characterization of a novel electrochromic copolymer of N-methylpyrrole with cyclopenta [2, 1-b: 3, 4-b′] dithiophene | |
| Nishihara et al. | Electrochemical and electrical properties of poly (hexachlorobuta-1, 3-diene), an electrochemically graphitized film | |
| Pruteanu et al. | Electrochemical characterization of electro-active polymer-carbon nanocomposites | |
| GB2572346A (en) | Electrode, battery and method | |
| JPS5931565A (ja) | 高分子被覆電極 | |
| US10147543B1 (en) | Super dielectric capacitor using scaffold dielectric and electrically and ionically conducting electrodes | |
| Shukla et al. | Investigation of hetero-and homo-charges in pristine and iodine doped polymethylmethacrylate | |
| KR101996722B1 (ko) | 다채널 박막전극을 이용한 전기적 생체분자 이동방법 | |
| Gökçeören et al. | Electrochemical impedance spectroscopy and in situ UV‐vis spectroelectrochemistry studies of Poly (N‐vinyl carbazole)/Polydimethylsiloxane composite electrodes | |
| Li et al. | Square-Wave Voltammetry of ClO4−-Doped Poly (phenylenesulfidephenyleneamine) |