RU2714168C2 - Интраназальное введение - Google Patents
Интраназальное введение Download PDFInfo
- Publication number
- RU2714168C2 RU2714168C2 RU2017114951A RU2017114951A RU2714168C2 RU 2714168 C2 RU2714168 C2 RU 2714168C2 RU 2017114951 A RU2017114951 A RU 2017114951A RU 2017114951 A RU2017114951 A RU 2017114951A RU 2714168 C2 RU2714168 C2 RU 2714168C2
- Authority
- RU
- Russia
- Prior art keywords
- length
- nose tip
- protrusion
- nose
- tip according
- Prior art date
Links
- 0 *C(C1CC1)N Chemical compound *C(C1CC1)N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/08—Inhaling devices inserted into the nose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
- A61K38/095—Oxytocins; Vasopressins; Related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/28—Insulins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0043—Nose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M11/00—Sprayers or atomisers specially adapted for therapeutic purposes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/0001—Details of inhalators; Constructional features thereof
- A61M15/0013—Details of inhalators; Constructional features thereof with inhalation check valves
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/0001—Details of inhalators; Constructional features thereof
- A61M15/0021—Mouthpieces therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/009—Inhalators using medicine packages with incorporated spraying means, e.g. aerosol cans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/0091—Inhalators mechanically breath-triggered
- A61M15/0098—Activated by exhalation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M29/00—Dilators with or without means for introducing media, e.g. remedies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M31/00—Devices for introducing or retaining media, e.g. remedies, in cavities of the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/04—Liquids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/06—Solids
- A61M2202/064—Powder
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2210/00—Anatomical parts of the body
- A61M2210/06—Head
- A61M2210/0618—Nose
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Anesthesiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pulmonology (AREA)
- Epidemiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Zoology (AREA)
- Endocrinology (AREA)
- Otolaryngology (AREA)
- Diabetes (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Psychiatry (AREA)
- Emergency Medicine (AREA)
- Obesity (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Infusion, Injection, And Reservoir Apparatuses (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Группа изобретений относится к медицинской технике. Наконечник для носа для доставки вещества в носовую полость субъекта содержит первую, внутреннюю корпусную часть и вторую, внешнюю корпусную часть, которая расположена по меньшей мере вокруг дистальной области внутренней корпусной части и образует концевой элемент. Внутренняя корпусная часть содержит основание, которое содержит проточный канал, и выступ в форме лезвия в дистальном конце, который поддерживает концевой элемент и придает жесткость в сагиттальном направлении, что позволяет концевому элементу раскрывать мясистую ткань в верхней области носового клапана и, таким образом, увеличивать площадь сечения раскрытого носового клапана, а также гибкость в боковом направлении, перпендикулярном сагиттальной плоскости, которая облегчает введение концевого элемента в носовой клапан. Раскрыты альтернативный вариант выполнения наконечника для носа и устройство для интраназальной доставки, содержащее наконечник для носа. Изобретения обеспечивают эффективную доставку пептидов для лечения нарколепсии и диабета. 3 н. и 35 з.п. ф-лы, 14 ил., 10 табл.
Description
Область техники
Настоящее изобретение относится к интраназальному введению окситоцина (ОТ), в частности для модуляции социального распознавания и/или поведения, которые представляют собой свойства умственной деятельности и/или поведения, лежащие в основе социального взаимодействия, и также к интраназальному введению других пептидов, включая орексин-А в частности для лечения нарколепсии и инсулин в частности для лечения диабета.
Уровень техники
Многочисленные данные подтверждают влияние ОТ на социальное распознавание и поведение1-3. Например, отдельное введение ОТ обеспечивает повышение сочувствия4-5, доверия6, улучшение работы в группе7-8, восприимчивости к визуальному контакту9 и работе модели психического состояния у здоровых индивидуумов10 и пациентов с психиатрическими расстройствами11. ОТ также был предложен в качестве нового способа терапии расстройств, характеризующихся социальной дисфункцией, таких как аутизм и расстройства шизофренического спектра12-13.
Несмотря на начальные ожидания, тем не менее, недавние работы не смогли выявить изменения в социальном поведении после введения ОТ14 или получали результаты, которые были значимыми только для специфических подгрупп или условий15. Указанные смешанные результаты в значительной степени связывают с указанными различиями в условиях и между индивидуумами16, а факторы, которые могут влиять на биологическую активность экзогенного ОТ, нуждаются в подробном исследовании15-18.
Авторы настоящего изобретения установили, что другие факторы, касающиеся способа дозирования и доставки, могут влиять на биологическую эффективность экзогенного ОТ, а также других пептидов, включая орексин-А и инсулин.
Обонятельные нервные волокна иннервируют ограниченный сегмент удаленной верхней узкой части носового канала, при этом тройничный нерв обеспечивает сенсорную и парасимпатическую иннервацию в удаленных верхних и задних сегментах носа. Доставка лекарственных средств к указанным волокнам черепного нерва может обеспечивать прямой способ воздействия на центральную нервную систему (ЦНС)15,23 в обход гематоэнцефалического барьера (ГЭБ), и направленная доставка в указанный сегмент не может быть обеспечена должным образом при использовании традиционных устройств для интаразального распыления15,26.
Авторы настоящего изобретения установили, что за счет прямого переноса активности из носа в мозг направленное интраназальное введение ОТ в указанный иннервированный сегмент носового канала может обеспечивать фармакодинамическое действие в мозге, не пропорциональное тому, которое могло быть обеспечено при всасывании в кровоток, и указанный способ направленной доставки может улучшать надежность, терапевтический индекс и эффективность при лечении с применением ОТ за счет улучшенного размещения лекарственного средства15,31-32.
Неизученное в литературе предположение, которое может быть подтверждено при помощи подробного экспериментального исследования на людях, заключается в том, что интраназальное введение является наилучшим способом доставки ОТ для модуляции социального распознавания и поведения15.
Несмотря на то, что в ранних работах было продемонстрировано, что внутривенное (в.в.) введение может влиять на социальное поведение и распознавание33-34 - предположительно за счет всасывания в кровоток и последующего проникновения через ГЭБ - в последующих исследованиях влияния ОТ на когнитивные функции человека, использовали способы доставки ОТ через носовую полость. Несмотря на наличие сильной теоретической базы, указывабщей на то, что интраназальная доставка является более подходящим способом введения ОТ, сравнение в контролируемых условиях фармакодинамики (PD) при интраназальном (т.е. за счет передачи из носа в мозг) и внутривенном (т.е. при прохождении через ГЭБ) введении прежде не проводилось.
Кроме того, если рассматривать режимы введения, то в основной части исследований интраназального ОТ проводили оценку введения от 20 до 40 международных единиц (IU)36. Системные исследования для фактического обоснования указанной дозировки не проводили37-38, при этом ее успешно применяют в других дисциплинах (например, в акушерстве)39. Указанная доза была выбрана, несмотря на отрицательные эффекты долгосрочного лечения с применением ОТ, наблюдаемые у молодых млекопитающих, отличных от человека40, и наличие рецепторов ОТ и перекрестных рецепторов вазопрессина (AVP) в организме41, которые задействованы при различных гомеостатических функциях, связанных с наблюдаемыми побочными эффектами42.
Задачей настоящего изобретения является обеспечение улучшенной эффективности при интраназальном введении окситоцина (ОТ), в частности для модуляции социального распознавания и/или поведения, и других пептидов, включая орексин-А, в частности для лечения нарколепсии, и инсулина, в частности для лечения диабета.
Краткое описание изобретения
Согласно одному из аспектов в настоящем изобретении предложен способ модуляции состояний, связанных с социальным распознаванием и/или поведением, у субъекта-человека с применением окситоцина, его непептидных агонистов и/или антагонистов, включающий: обеспечение наконечника для носа в первой носовой полости субъекта; и введение менее чем 24 IU окситоцина, его непептидных агонистов и/или антагонистов в верхнюю область, расположенную позади носового клапана, которая иннервирована тройничным нервом.
Согласно другому аспекту в настоящем изобретении предложен способ модуляции состояния у субъекта-человека с применением пептида, его непептидных агонистов и/или антагонистов, включающий: обеспечение наконечника для носа в первой носовой полости субъекта; и введение менее чем 24 IU пептида, его непептидных агонистов и/или антагонистов через наконечник для носа в верхнюю область, расположенную позади носового клапана, которая иннервирована тройничным нервом.
Согласно дополнительному аспекту в настоящем изобретении предложен наконечник для носа для доставки вещества в носовую полость субъекта, где наконечник для носа содержит: первую внутреннюю корпусную часть; и вторую внешнюю корпусную часть, которая расположена по меньшей мере вокруг дистальной области внутренней корпусной части и образует концевой элемент; где внутренняя корпусная часть содержит основание, которое содержит проточный канал, и выступ в дистальном конце, в котором находится концевой элемент и который придает жесткость в сагиттальном направлении, что позволяет концевому элементу раскрывать мясистую ткань в верхней области носового клапана и, таким образом, увеличивать площадь сечения раскрытого носового клапана, а также гибкость в боковом направлении, перпендикулярном сагиттальной плоскости, которая облегчает введение концевого элемента в носовой клапан.
Согласно дополнительному аспекту в настоящем изобретении предложен наконечник для носа для доставки вещества в носовую полость субъекта, где наконечник для носа содержит корпусную часть, которая содержит основание, которое содержит проточный канал, и выступ в дистальном конце основания, в котором размещается по меньшей мере часть наконечника для носа и который придает жесткость в сагиттальном направлении, что позволяет концевому элементу раскрывать мясистую ткань в верхней области носового клапана и, таким образом, увеличивать площадь сечения раскрытого носового клапана, а также гибкость в боковом направлении, перпендикулярном сагиттальной плоскости, которая облегчает введение концевого элемента в носовой клапан.
Описание чертежей
Предпочтительные варианты реализации настоящего изобретения описаны далее при помощи прилагаемых чертежей, которые приведены исключительно в качестве примеров:
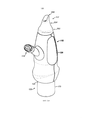
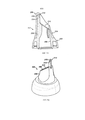
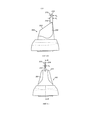
На фигурах 1(a)-(с) проиллюстрировано устройство для доставки согласно одному из вариантов реализации настоящего изобретения;
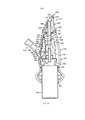
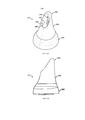
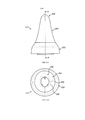
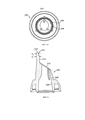
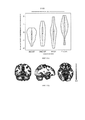
На фигурах 2(a)-(е) проиллюстрированы вид в перспективе, сбоку, спереди, снизу и продольный разрез (по плоскости А-А) наконечника для носа в устройстве, изображенном на фигурах 1(а)-(с);
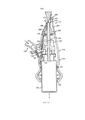
На фигурах 3(a)-(е) проиллюстрированы вид в перспективе, сбоку, спереди, снизу и продольный разрез (по плоскости В-В) внутренней корпусной части наконечника для носа в устройстве, изображенном на фигурах 1(а)-(с);
На фигуре 4 приведена схема исследования с использованием теста для изучения социального распознавания;
На фигурах 5(a)-(f) приведены средние рейтинги эмоциональной оценки в зависимости от стимула, такие как индекс гнева для лиц с неопределенными эмоциями (5(a)), индекс счастья для лиц с неопределенными эмоциями (5(b)), индекс счастья для счастливых лиц (5(c)), индекс гнева для счастливых лиц (5(d)), индекс гнева для гневных лиц (5(e)) и индекс счастья для гневных лиц (5(f)), и в зависимости от способов лечения, таких как интраназальное введение 8 IU ОТ (8IU-OT), интраназальное введение 24 IU ОТ (24IU-OT), внутривенная доставка 1 IU ОТ (IV-OT) и интраназальное введение состава с плацебо (плацебо);
На фигуре 6(a) приведено снижение в процентах индекса гнева после введения 8IU-ОТ по сравнению с плацебо для различных категорий стимулов;
На фигуре 6(b) приведено снижение в процентах индекса гнева после введения 8IU-ОТ по сравнению с введением 24IU-OT для различных категорий стимулов;
На фигуре 7(a) приведены средние значения концентрации ОТ в плазме в зависимости от времени после введения 8IU-OT, 24IU-OT, IV-OT и плацебо, где планки погрешностей соответствуют стандартной ошибке среднего;
На фигуре 7(b) приведены средние значения концентрации вазопрессина (AVP) в плазме в зависимости от времени после введения 8IU-OT, 24IU-OT, IV-OT и плацебо, где планки погрешностей соответствуют стандартной ошибке среднего;
На фигуре 7(c) приведены средние значения кортизола в плазме в зависимости от времени после введения 8IU-OT, 24IU-ОТ, IV-OT и плацебо, где планки погрешностей соответствуют стандартной ошибке среднего;
На фигуре 8 проиллюстрирована связь между средней площадью поперечного сечения носового клапана и индексом гнева в отношении изображений лиц с невыраженными эмоциями у субъектов после введения 8IU-OT, 24IU-OT, IV-OT и плацебо;
На фигуре 9(a) проиллюстрировано изменение пространственных карт со временем при определении в анализе фМРТ для независимой компоненты №37, где показаны выраженные миндалевидное тело, медиальная височная доля (MTL) и ствол мозга;
На фигуре 9(b) проиллюстрировано изменение пространственных карт со временем двух самых крупных кластеров (изображение в вокселях, р<0,01, нескорректированный) в независимой компоненте №37, которые локализованы в левом и правом миндалевидном теле, соответственно;
На фигуре 9(c) проиллюстрировано изменение пространственных карт со временем для двух самых крупных кластеров, в которых наблюдали значительное (р<0,05, скорректирован по размеру кластеров при помощи пермутационного теста) увеличение взаимосвязей при лечении 8IU-OT по сравнению с плацебо в левом и правом миндалевидном теле, соответственно;
На фигурах 10(a) и (b) проиллюстрированы коробчатые диаграммы средней взаимосвязи двух кластеров при определении в анализе фМРТ, на которых показан значительный (р<0,01, нескорректированный) главный эффект для данного условия введения ОТ;
На фигурах 11(a) и (b) проиллюстрированы коробчатые диаграммы средней взаимосвязи двух кластеров при определении в анализе фМРТ, на которых показано значительное (р<0,05, коррекция на размер кластеров) увеличение взаимосвязи после лечения 8IU-OT по сравнению с плацебо;
На фигурах 12(a) и (b) при помощи диаграммы «спагетти» приведены значения взаимосвязи для всех условий в каждом из значительных кластеров в миндалевидных телах, полученные при попарном сравнении способов лечения 8IU-OT и плацебо у каждого индивидуума;
На фигуре 13(a) проиллюстрированы скрипичные диаграммы, на которых показана активация правого миндалевидного тела, и диаграммы «ящик с усами», на которых показаны медианные значения и 50% интерквартильный диапазон после введения 8IU-OT, 24IU-OT, IV-OT и плацебо;
На фигуре 13(b) проиллюстрирован главный эффект при представлении изображений лиц в зависимости от эмоций и от способа лечения, включая 8IU-OT, 24IU-OT, IV-OT и плацебо; и
На фигурах 14(a)-(с) приведена взаимосвязь между средним размером зрачка и активностью правого миндалевидного тела после лечения 8IU-OT и обработки стимулов в виде изображений лиц, выражающих гнев, неопределенные эмоции и счастье.
Подробное описание вариантов реализации
Устройство
На фигурах 1(a)-(с) проиллюстрировано активируемое вручную устройство интраназальной доставки согласно одному из вариантов реализации настоящего изобретения.
Устройство для доставки содержит камеру 115, наконечник для носа 117 для введения в носовую полость субъекта, наконечник для рта 119, через который субъект, использующий данное устройство, выдыхает, для обеспечения тем самым доставки потока воздуха в носовые дыхательные пути субъекта и прохождения потока через них при выдохе субъекта через наконечник для рта 119, и блок доставки 120, который активируется вручную для доставки вещества в носовую полость субъекта.
Камера 115 содержит элемент-основу 121, который в указанном варианте реализации по существу представляет собой продолговатую трубчатую часть, включающий отверстие 123, расположенное на одном из концов, через которое перемещается активирующая часть блока доставки 120, которая в указанном варианте реализации определена как основа камеры для размещения вещества 173 блока подачи вещества 169.
Камера 115 дополнительно содержит клапанный блок 127, который соединен по текучей среде с наконечником для носа 117 и наконечником для рта 119 и перемещается между закрытым и открытым положением, как проиллюстрировано на фигурах 3 и 4, для обеспечения таким образом прохождения потока воздуха, который в указанном варианте реализации представляет собой мгновенный поток воздуха, через наконечник для носа 117 одновременно с активацией блока доставки 120, что будет более подробно описано далее в настоящем описании.
Клапанный блок 127 содержит элемент-основу 128, который включает седло клапана 129, определяющее отверстие клапана 130, и клапанный элемент 131, который расположен на элементе-основе 128 с возможностью перемещения между закрытым и открытым положениями, что проиллюстрировано на фигурах 1(b) и (с).
Как в частности проиллюстрировано на фигуре 1(c), элемент-основа 128 содержит шарнир 135, который в указанном варианте реализации размещен у одной нижней стороны седла клапана 129, к одному из концов 145 которого посредством шарнирного соединения прикреплен клапанный элемент 131, и поверхность скольжения 137, которая в указанном варианте реализации находится с другой верхней стороны седла клапана 129, относительно которой движется за счет скольжения другой конец 147 клапанного элемента 131.
Клапанный элемент 131 содержит удлиненное плечо 141, которое в указанном варианте реализации представляет собой гибкое плечо, один конец которого, в указанном варианте реализации нижний конец 145, посредством шарнирного соединения прикреплен к шарниру 135 в элементе-основе 128, и другой верхний конец 147 которого за счет скольжения взаимодействует с поверхностью скольжения 137 элемента-основы 128, и клапанный элемент 149, который поддерживается плечом 141.
В указанном варианте реализации плечо 141 содержит первую, в данном случае нижнюю, секцию плеча 151, которая смещается в данном случае внутрь, при этом, когда клапанный элемент 131 находится в закрытом, нейтральном положении, нижняя секция плеча 151 наклонена внутрь относительно продольной оси камеры 115 и взаимодействует с блоком подачи вещества 169, когда его активируют вручную для перемещения клапанного элемента 131 в открытое положение, как более подробно описано ниже.
В указанном варианте реализации плечо 141 дополнительно содержит вторую, в данном случае верхнюю, секцию плеча 153, которая взаимодействует с поверхностью скольжения 137 элемента-основы 128 и вызывает перемещение клапанного элемента 131 в закрытое положение.
В указанном варианте реализации клапанный элемент 149 содержит уплотнение 161, которое в указанном варианте реализации представляет собой гибкий или упругий элемент, который обеспечивает возможность закрытия отверстия клапана 130, образованного седлом клапана 129, когда клапанный элемент 131 находится в закрытом положении, и основание 163, которое поддерживает центральную часть уплотнения 161.
В данной конфигурации, где уплотнение 161 поддерживается в центральной части, когда клапанный элемент 131 перемещается в открытое положение, основание 163 смещает центральную часть уплотнения 161, что приводит к выгибанию уплотнения 161 наружу в указанной центральной части, что, таким образом, обеспечивает возможность взаимодействия уплотнения 161 с седлом клапана 129 только на периферической кромке уплотнения 161 до тех пор, пока не будет достигнута точка, в которой уплотнение 161 внезапно щелчком отбрасывается от седла клапана 129.
Указанный режим переключения считается особенно эффективным в настоящей заявке в случаях, в которых необходимо обеспечивать начальный мгновенный поток воздуха, когда по существу вся герметизирующая поверхность уплотнения 161 освобождается мгновенно, в отличие от альтернативного режима постепенного освобождения, когда сначала освобождается небольшая часть герметизирующей поверхности и затем остальная часть уплотняющей поверхности, что имеет тенденцию к снижению начального ударного давления.
В указанном варианте реализации блок доставки 120 содержит выходной блок 167 для доставки вещества в носовые дыхательные пути субъекта и блок для подачи вещества 169 для доставки вещества в выходной блок 167.
В указанном варианте реализации выходной блок 167 содержит выпускное отверстие 171 для доставки вещества в носовые дыхательные пути субъекта. В указанном варианте реализации выпускное отверстие 171 выполнено таким образом, чтобы обеспечивать распыление аэрозоля. В альтернативном варианте реализации при доставке жидкости выпускное отверстие 171 может быть выполнено таким образом, чтобы доставлять жидкую струю в виде столба жидкости.
В предпочтительном варианте реализации дистальный конец выходного блока 167 предназначен для введения внутрь носовой полости субъекта по меньшей мере примерно на 2 см, предпочтительно по меньшей мере примерно на 3 см и более предпочтительно от примерно 2 см до примерно 3 см.
В указанном варианте реализации блок для подачи вещества 169 представляет собой насосный блок, который содержит камеру для размещения вещества 173, содержащую вещество, соединенную посредством отверстия 123 с камерой 115 и представляющую собой активирующую часть блока для подачи вещества 169, и механический насос для доставки 175, который активируется в настоящем случае посредством нажатия на камеру для размещения вещества 173, как правило, пальцем или большим пальцем субъекта для доставки заданной дозы вещества из камеры для размещения вещества 173 в выходной блок 167 и далее из выпускного отверстия 171 в виде распыляемого аэрозоля.
В указанном варианте реализации камера для размещения вещества 173 при нажатии для активации блока для подачи вещества 169 взаимодействует с нижней секцией 151 плеча 141 клапанного элемента 131, для обеспечения таким образом одновременной активации блока для подачи вещества 169 и раскрытия уплотнения 161 клапанного элемента 131, за счет чего вещество, которое в данном случае является распыленным, и поток воздуха, который в данном случае является мгновенным, одновременно доставляются в носовую полость субъекта.
В указанном варианте реализации механический насос для доставки 175 представляет собой насос для доставки жидкости предназначенный для доставки заданной дозы вещества.
В указанном варианте реализации блок для подачи вещества 169 представляет собой блок, содержащий несколько доз, который обеспечивает доставку совокупности заданных доз вещества при последовательных операциях доставки.
В указанном варианте реализации камера 115 дополнительно содержит герметизирующий элемент 181, который в данном случае представляет собой кольцевое уплотнение в форме уплотнительного кольца, в котором за счет скольжения размещается камера для размещения вещества 173 блока для подачи вещества 169, для предотвращения таким образом утечки доставляемого потока воздуха из отверстия 123 в камере 115.
На фигурах 2(a)-(е) и 3(a)-(е) проиллюстрирован наконечник для носа 117 согласно описанному варианту реализации.
Как в частности проиллюстрировано на фигуре 2(e), наконечник для носа 117 состоит из двух корпусных частей 202, 204, где первая, внутренняя, часть 202 в данном случае изготовлена из пластикового материала, и вторая, внешняя, корпусная часть 204 в данном случае изготовлена из более мягкого упругого материала, такого как резина или эластомерный материал, и расположена вокруг дистального конца внутренней корпусной части 202, образуя концевой элемент 206.
В указанном варианте реализации внутренняя корпусная часть 202 изготовлена из акрил онитрил-бутадиен-стиролового (ABS) пластика, в данном случае из Guardian/Lustran (RTM) ABS 308 (поставляемого Ineos ABS (USA) Corporation).
В указанном варианте реализации внешняя корпусная часть 204 изготовлена из термопластичного эластомера (ТРЕ), в данном случае из Versaflex (RTM) ОМ 1040Х-1 (поставляемого GLS/PolyOne Corporation), имеющего твердость по Шору А 42.
Как в частности проиллюстрировано на фигурах 3(a)-(е), в указанном варианте реализации внутренняя корпусная часть 202 содержит основание 208, которое ограничивает проточный канал 209, проходящий через основание, и выступ 212 в дистальном наиболее удаленном конце, который поддерживает концевой элемент 206 наконечника для носа 117.
В указанном варианте реализации дистальный наиболее удаленный конец основания 208 имеет поверхность 210, которая сужается или имеет наклон относительно продольной оси наконечника для носа 117, таким образом, поверхность 210 основания 208 проходит с наклоном по направлению от дитсального конца выступа 212, и основание 208 является более коротким с той стороны, которая расположена напротив выступа 212.
Выступ 112 предназначен для придания жесткости в сагиттальном направлении, что позволяет концевому элементу 206 наконечника для носа 117 раскрывать мясистую ткань в верхней области носового клапана и увеличивать площадь сечения раскрытого носового клапана, и гибкости в боковом направлении, которая облегчает введение концевого элемента 206 наконечника для носа 117 в носовой клапан. В указанном варианте реализации согласно результатам измерения путем акустической ринометрии (AR) наконечник для носа 117 обеспечивает расширение площади носового клапана до такого размера, который по меньшей мере в два раза превышает площадь носового клапана в нерасширенном состоянии и состоянии покоя.
В указанном варианте реализации выступ 212 проходит в осевом направлении по существу параллельно продольной оси наконечника для носа 117.
В указанном варианте реализации выступ 212 имеет форму лезвия с длиной d1 в сагиттальном направлении, которая превышает длину d2 в боковом направлении.
В указанном варианте реализации длина d1 в сагиттальном направлении в 1,5 раза превышает среднюю длину d2 в боковом направлении.
В одном из вариантов реализации длина d1 в сагиттальном направлении в 1,7 раза превышает среднюю длину d2 в боковом направлении.
В указанном варианте реализации длина d1 в сагиттальном направлении в 1,9 раза превышает среднюю длину d2 в боковом направлении.
В указанном варианте реализации длина d1 в сагиттальном направлении в 2 раза превышает среднюю длину d2 в боковом направлении.
В указанном варианте реализации выступ 212 имеет длину d1 в сагиттальном направлении, составляющую примерно 2 мм.
В указанном варианте реализации выступ 212 имеет длину d2 в боковом направлении, составляющую примерно 1 мм.
В указанном варианте реализации выступ 212 имеет секцию основного корпуса 214 и секцию наконечника 216, которая имеет более низкую длину d3 в сагиттальном направлении по сравнению с длиной d1 секции основного корпуса 214, что в данном случае определяет ступеньку на внутренней кромке.
В указанном варианте реализации выступ 212 имеет боковое поперечное сечение, сужающееся вдоль длины, где длина d2 в боковом направлении сокращается в поперечном сечении вдоль длины выступа в направлении к дистальному концу.
В указанном варианте реализации длина d2 в боковом направлении уменьшается от примерно 1,1 мм до примерно 0,8 мм от ближнего конца к дистальному концу выступа 212.
Исследование
Проводили двойное слепое перекрестное исследование с двойной имитацией, для которого случайным образом отбирали 18 здоровых взрослых мужчин, 16 из которых подвергались четырем способам лечения с введением одной дозы; способы представляли собой (1) интраназальное введение путем распыления жидкого состава 8IU ОТ, который доставляли с применением устройства, изображенного на фигурах 1(a)-(с) (далее 8IU-OT), (2) интраназальное введение путем распыления жидкого состава 24IU ОТ, который доставляли с применением устройства, изображенного на фигурах 1(a)-(с) (далее 24IU-OT), (3) внутривенную доставку 1IU ОТ (далее IV), и (4) интраназальное введение путем распыления жидкого состава с плацебо с применением устройства, изображенного на фигурах 1(a)-(с) (далее плацебо).
В указанном исследовании проводили сравнение фармакодинамического (PD) воздействия ОТ на социальное распознавание и поведение, которые оценивали при помощи критериев с использованием эмоциональных стимулов и в частности по активности миндалевидного тела.
Для оценки нейронных коррелятов, определяющих действие ОТ на поведение и распознавание, исследователи использовали средства визуализации мозга, такие как функциональная магнитная резонансная томография (фМРТ). Согласно общему мнению специалистов в данной области техники миндалевидное тело, которое является ключевым участком мозга, отвечающим за регуляцию86, обработку87 и выявление113 эмоций, представляет собой важную мишень при введении ОТ. Модуляция активности миндалевидного тела в ответ на эмоциональные стимулы, возможно, является наиболее воспроизводимым и хорошо охарактеризованным результатом при визуализации мозга и интраназальных исследованиях ОТ88,89,114-117. Тем не менее, несмотря на наличие указанных более ранних работ, способ доставки ОТ к мозгу или доза ОТ, которая является наиболее подходящей для модуляции рекрутинга миндалевидного тела при представлении эмоциональных стимулов, остаются не выясненными. За счет сравнения активности миндалевидного тела после интраназального и внутривенного введения ОТ при достижении сравнимого уровня в крови исследователи могут определять возможное прохождение нейронной модуляции вследствие прямого переноса из носа в мозг (как предполагается в настоящем случае) или за счет системной циркуляции ОТ в кровотоке и проникновения через ГЭБ. Для того, чтобы определить возможное системное воздействие ОТ на социальное поведение и распознавание, проводили исследования на животных70 и человеке33-34 - тем не менее, в исследованиях до настоящего времени не проводили оценку активности миндалевидного тела после внутривенной доставки и сравнительной интраназальной доставки ОТ.
В выдвинутых недавно теориях подчеркивают влияние ОТ на поведение приближения118 и модуляцию осознания социальных стимулов16. С учетом установленной взаимосвязи между расположением когнитивных ресурсов и расширением зрачка119-120 пупиллометрия обеспечивает неинвазивный способ нейробиологического измерения взаимодействия в ответ на эмоциональные стимулы. В исследовании показано, что интраназальный ОТ увеличивает расширение зрачка55 и осознание социальных сигналов121. Тем не менее, взаимосвязь между активностью миндалевидного тела и когнитивным взаимодействием, определяемым по характеристикам зрачка, еще необходимо исследовать, что может помочь лучшему пониманию действия ОТ.
В качестве первичных результатов проводили оценку выражения эмоций при представлении изображений различных типов лиц, в частности активности миндалевидного тела, и вторичные результаты включали профили фармакокинетики (PK) и рейтинги степени доверия.
В указанном исследовании было сделано предположение о главном эффекте при введении 8IU-OT и 24IU-OT на кажущуюся интенсивность гнева, и о том, что указанный эффект может быть более выраженным при представлении неопределенных эмоциональных стимулов по сравнению со стимулами, в которых эмоции выражены более конкретно.
В указанном исследовании оценивали эффекты 8IU-OT и 24IU-OT в зависимости от дозы.
В указанном исследовании также определяли воздействие ОТ на рейтинги доверия для тех же лицевых стимулов.
Для определения характеристик PK и оценки возможных различных взаимосвязей PK и PD в зависимости от способа доставки, после проведения способа лечения измеряли изменение концентраций ОТ и физиологически взаимодействующих веществ, таких как вазопрессин (AVP) и кортизол, в плазме со временем. Модуляция социального распознавания после введения 8IU-OT и 24IU-OT, но не после IV-OT при обеспечении сравнимых концентраций в крови, может свидетельствовать о том, что введение 8IU-OT и 24IU-OT по меньшей мере отчасти обеспечивает прямое действие в мозге, но не посредством пересечения ГЭБ.
Допущенные участники представляли собой мужчин возрастом от 18 до 35 лет с хорошим физическим и психическим здоровьем. Критерии исключения включали использование каких-либо лекарственных средств в течение последних 14 дней, историю алкогольной или наркотической зависимости, клинически значимые случаи физических (включая нарушения почек, сердца, эндокринной системы, легких, печени, нервной системы, желудочно-кишечного тракта, гематологические и метаболические нарушения) или психиатрических заболеваний, и IQ<75. На стадии отбора проводили оценку пятидесяти семи здоровых добровольцев, были выбраны 18 участников возрастом 20-30 лет (М=23,81, СКО=3,33). После отбора были исключены два участника [1 был исключен после первого посещения, и другой был исключен после завершения трех стадий], и данные, полученные для указанных участников, не учитывали при анализе.
Посещение для скрининга проводили в течение 3-21 дня перед рандомизацией. Для определения IQ и подтверждения отсутствия психиатрических заболеваний использовали сокращенную шкалу Векслера для измерения интеллекта52 и краткий международный нейропсихиатрический опросник53, соответственно. Проводили медицинское обследование, включая ЭКГ и сбор стандартных образцов крови. Кроме того, отоларинголог подтверждал нормальную анатомию носа и назальную проходимость у участников (при помощи медицинского осмотра), собирали данные акустической ринометрии (AR) (SRE 2000; Rhinometrics, Lynge, Denmark).
По данным AR вычисляли три показателя: минимальную площадь поперечного сечения (МСА; т.е. самое узкую часть носовой полости), общий объем ноздри вглубь на 5 см (TV0-5), и общий объем на расстоянии 2-5 см (TV2-5).
Использовали схему рандомизированного плацебо-контролируемого двойного слепого перекрестного исследования с двойной имитацией и четырьмя периодами исследования. Участников случайным образом распределяли для проведения одной из четырех последовательностей способов лечения по методу латинских квадратов, включающему использование четырех периодов и четырех способов лечения (ACDB - BDCA - CBAD - DABC в отношении 4:4:4:4), где интервал между проведением способов лечения составлял по меньшей мере шесть дней для предотвращения возможных эффектов переноса. Проводили заслепление способа лечения для участников и группы исследователей путем использования визуально одинаковых устройств и в.в. оборудования при сборе данных.
В указанном исследовании действие устройства для доставки основано на двух аспектах анатомии носа для облегчения доставки к эпителию дыхательных путей и носа32. Во-первых, при выдохе пользователя через рот для преодоления сопротивления небная занавеска самопроизвольно закрывается, что приводит к отделению полости носа от полости рта и предотвращает осаждение в легких и ограничивает осаждение в желудочно-кишечном тракте23. Во-вторых, помимо закрытия небной занавески за счет применения оптимизированного наконечника для носа обеспечивается более глубокое введения для направления выдыхаемого воздуха и ОТ в верхние задние сегменты носовой полости23.
Составы 8IU-OT, 24IU-OT и плацебо получали в Sigma-Tau Industrie Farmaceutiche Riunite S.p.A. Состав плацебо содержал 0,9% хлорид натрия.
Состав IV-OT получали в AS Grindeks, Riga, Latvia, в виде 10 IU/мл состава, который добавляли к 0,9% раствору хлорида натрия для инфузии незадолго перед введением (600 мл/час в течение 20 минут). Дозировку и скорость внутривенной инфузии выбирали таким образом, чтобы обеспечивать концентрацию ОТ в периферической крови, эквивалентную концентрации при интраназальной доставке, что подтверждали экспериментально.
Для обеспечения надлежащего и стандартного использования участников обучали использованию устройства для интраназальной доставки при помощи просмотра демонстрационных видеоматериалов, изучения письменных инструкций и введения распыляемых солевых растворов на практике под наблюдением обученного исследовательского персонала во время скринингового посещения.
В начале каждой экспериментальной стадии подтверждали критерии исключения и включения и использовали опросник состояния и свойств тревожности 54. Собирали образцы крови для оценки стандартных показателей и проводили акустическую ринометрию (AR) (согласно процедуре, используемой во время скрининга) для подтверждения отсутствия значительных изменений среды носовой полости между посещениями, связанных с носовыми циклами24.
Участники выполняли задание для социального распознавания через 40 минут после лечения в сканере магнитной резонансной томографии (МРТ), при этом собирали данные функциональной МРТ и физиологические показатели.
Участникам представляли визуальные стимулы при помощи совместимых с МРТ очков (VisualSystem; NordicNeuroLab, Bergen, Norway) с использованием E-Prime 2.0 (Psychology Software Tools, PA, USA), ответы получали с использованием системы сбора ответов методом захвата (ResponseGrip, NordicNeuroLab, Bergen, Norway).
Участникам представляли изображения 20 мужских и 20 женских лиц55, которые выражали счастье, гнев или неопределенные эмоции [получали в базе данных Karolinska Directed Emotional Faces56] и 20 геометрических изображений. Задание на когнитивное распознавание включало пять блоков по 20 испытаний, как проиллюстрировано на фигуре 4. Каждое испытание продолжительностью примерно 140 секунд включало следующую последовательность: представление креста для фиксации взгляда продолжительностью 3 секунды -> представление стимула (лица/формы) продолжительностью 1 секунда -> Q1 продолжительностью 3,25 секунды (максимальное окно для ответа) -> Q2 продолжительностью 3,25 секунды (максимальное окно для ответа).
Для оценки изображений лиц участникам задавали первый вопрос (Q1), который звучал как: Насколько разгневан данный человек? (фиксированные ответы: не разгневан - очень разгневан), или Насколько счастлив данный человек? (фиксированные ответы: не счастлив - очень счастлив), и второй вопрос (Q2), который всегда звучал как: Насколько вы доверяете данному человеку? (фиксированные ответы: совсем не доверяю - очень сильно). Участников просили отмечать свой ответ на каждый из вопросов на визуальной аналоговой шкале (ВАШ) от 1 до 5, где курсор на ВАШ при появлении каждого вопроса отображался в случайных местах. Для каждого из вопросов во время каждого посещения получали средние рейтинги для каждой эмоциональной категории, что давало семь переменных поведения (Q1: Счастливое лицо - счастье, Счастливое лицо - гнев, лицо с неопределенными эмоциями - счастье, лицо с неопределенными эмоциями - гнев, гневное лицо - счастье, гневное лицо - гнев; Q2; доверие). Указанные стимулы и вопросы выбирали для оценки трех уровней восприятия эмоций; неопределенные эмоции, выраженные эмоции при соответствии стимулов и рейтингов (например, рейтинг гнева для гневных лиц) и выраженные эмоции при противоречии стимулов и рейтингов (например, рейтинги гнева для счастливых лиц).
Для оценки форм участникам задавали следующие вопросы: (Q1) Насколько желтая данная форма? (фиксированные ответы: не желтая - очень желтая), или Насколько синяя данная форма? (фиксированные ответы: не синяя - очень синяя). Q2 всегда звучал как: Насколько вам нравится данный цвет? (фиксированные ответы: совсем не нравится - очень сильно). Аналогично системе рейтингов для лиц участников просили отмечать свой ответ на визуальной аналоговой шкале (ВАШ) от 1 до 5, где курсор на ВАШ при появлении каждого вопроса отображался в случайных местах.
Данные визуализации мозга собирали на сканере 3Т General Electric Signa HDxt с 8-канальной катушкой для головы (GE Healthcare, Milwaukee, WI, USA).
Протокол получения данных МРТ включал последовательность Т2*-взвешенных изображений при градиентной эхо-планарной визуализации (EPI), полученную в поперечной плоскости со следующими параметрами: Продолжительность цикла (TR)=2400 мсек, продолжительность эха (ТЕ)=30 мсек, угол наклона вектора (FA)=90°, матрица 64×64. У каждого индивидуума для каждого состояния ОТ получали одну серию из 528 изображений (48 срезов; плоскостное разрешение 3,75×3,75 мм; толщина среза 3,2 мм, без задержки). Т1-взвешенные изображения, используемые для одновременной регистрации, получали при помощи последовательности быстрого очищенного градиентного эха (FSPGR) в сагиттальной плоскости, имеющей следующие параметры: TR=7,8 мсек, ТЕ=2,9 мсек, FA=12°, 166 срезов; плоскостное разрешение: 1×1, толщина среза: 1,2 мм, матрица 256×256.
Данные пупиллометрии собирали при помощи совместимой с MP размещенной на катушке инфракрасной системы EyeTracking (NNL EyeTracking camera®, NordicNeuroLab, Bergen, Norway) с частотой отбора проб 60 Гц. Данные записывали при помощи программного обеспечения iView X Software (SensoMotoric Instruments, Teltow, Germany), где компьютерная программа была синхронизирована с появлением стимула, и данные пупиллометрии начинали записывать при представлении стимула.
Во время экспериментальных посещений собирали образцы крови с использованием внутривенного катетера для оценки содержания ОТ, AVP и кортизола в периферической крови на исходном уровне и для пяти моментов времени после завершения 20-минутного внутривенного введения (0 минут, 10 минут, 30 минут, 60 минут и 120 минут) во время посещения. Образцы крови центрифугировали при 4°C в течение 20 минут после отбора крови, после чего плазму замораживали при -80°C до проведения фермент-связанного иммуносорбентного анализа (ELISA) с использованием коммерчески доступных наборов (Enzo Life Sciences, Farmingdale, NY) при помощи стандартных способов (включая экстракцию образцов).
Анализ фармакодинамики
Анализ проводили при помощи IBM SPSS Statistics версии 22 (IBM Inc.) для определения фармакокинетики и исследования влияния способа лечения на измеряемые результаты. Использовали линейную смешанную модель (LMM)58, соответствующую недавнему перекрестному исследованию интраназальных психотропных лекарственных средств95, для анализа выражения эмоций, оценки фармакокинетики, ситуационной тревожности и доверия. Подстановку всех моделей проводили при помощи неструктурированной матрицы. Для любого из значительных главных эффектов (т.е., где р<0,05), проводили вторичный анализ, в котором регулировали критические значения р для корректировки по множественным сравнениям с использованием 5% уровня ложноположительных результатов (FDR)59.
Для оценки влияния способа лечения на рейтинги эмоций и доверия способ лечения в модели LMM рассматривали в качестве фиксированного и повторяющегося эффекта. Кроме того, для исследования влияния способа лечения на концентрацию ОТ, AVP, кортизола в плазме и ситуационной тревожности в LMM вводили 3 фиксированных фактора (способ лечения, продолжительность, способ лечения × продолжительность), 1 повторяющийся фактор (способ лечения). Для исследования возможного изменения среды носовой полости проводили MANOVA повторных измерений с тремя зависимыми переменными: MCA, TV0-5 и TV2-5.
Ответы участников на задание приведены в таблице 1. Из-за проблем с оборудованием данные не были получены во время двух (из шестидесяти четырех) сессий исследования. В LMM был выявлен значительный главный эффект лечения в рейтингах гнева при представлении изображений лиц с неопределенными эмоциями [F(3, 14,72)=7,62, р=0,003; фигура 5(a)]. При последующих попарных сравнениях (q=0,05, пересмотренное критическое значение р<0,017) было показано, что рейтинги гнева в отношении изображений лиц с неопределенными эмоциями значительно снижали для способа лечения 8IU-OT по сравнению с плацебо (р=0,011; среднее снижение =17%, снижение SE 6%) и способом лечения 24IU-OT (р=0,003; среднее снижение =17%, снижение SE 5%). Для других рейтингов эмоциональных категорий или доверия основной эффект лечения не наблюдали (фигуры 5(b)-(f)).
Для оценки специфичности эффекта в отношении лиц с неопределенными эмоциями (по сравнению с лицами с выраженными эмоциями, где ответ соответствовал стимулу, и лицами с выраженными эмоциями, где ответ противоречил стимулу), вычисляли изменение индекса в процентах путем сравнения рейтингов, полученных при лечении 8IU-ОТ и плацебо, и сравнения способов лечения 8IU-OT и 24IU-OT (т.е. сравнения способов лечения, в которых были продемонстрированы значительные различия в рейтингах эмоций). Неопределенные = рейтинги гнева для лиц с неопределенными эмоциями; NA - соответствие = Рейтинги гнева для лиц с выраженными эмоциями, где ответ соответствовал стимулу; NA - противоречие = Рейтинги гнева для лиц с выраженными эмоциями, где ответ противоречил стимулу. Для оценки влияния категории стимула на снижение рейтингов гнева в LM использовали категорию стимула в качестве фиксированного и повторяющегося эффекта. При сравнении изменения в процентах в LMM между способом лечения 8IU-OT и плацебо для типов стимулов отмечали главный эффект [F(2, 14,42)=4,79, р=0,025; фигура 6(a)]. В последующих попарных сравнениях с категорией неопределенных стимулов (q=0,05, пересмотренное критическое значение р<0,025) было показано, что снижение в процентах рейтингов гнева при неопределенных стимулах было значительно понижено по сравнению с группой выраженных стимулов (NA)/c противоречащим ответом (р=0,012). При сравнении изменения в процентах в LMM между способами лечения 8IU-OT и 24IU-OT для типов стимулов отмечали главный эффект [F(2, 14,05)=7,01, р=0,007; фигура 6(b)]. В последующих попарных сравнениях с категорией неопределенных стимулов (q=0,05, пересмотренное критическое значение р<0,025) было показано, что снижение в процентах рейтингов гнева при неопределенных стимулах было значительно понижено по сравнению с группой выраженных стимулов/с противоречащим ответом (р=0,008).
Среди 384 возможных экспериментальных значений 19 значений ОТ, 26 значений AVP и 18 значений концентрации кортизола в плазме были исключены из-за технических проблем, связанных с отбором проб крови или анализом.
Концентрация окситоцина в плазме крови: Средние концентрации ОТ в плазме в различные моменты времени после введения 8IU-ОТ, 24IU-OT, IV-OT и плацебо (где планки погрешностей соответствуют стандартной ошибке среднего) приведены в таблице 2 и на фигуре 7(a). Для LMM 4 (способ лечения) ×6 (продолжительность) наблюдали значительный главный эффект способа лечения на концентрацию ОТ в плазме крови [F(3, 88,71)=4,25,р=0,007]. В последующих попарных сравнениях (q=0,05, пересмотренное критическое значение р<0,025) было показано, что концентрация ОТ в плазме значительно увеличивалась в способах IV-OT (р=0,009), 8IU-OT (р=0,001) и 24IU-OT (р=0,002) по сравнению с плацебо. Ни в одном из других попарных сравнений значимых различий не наблюдали. Также наблюдали значительный главный эффект для продолжительности [F(5, 90,29)=5,93, р<0,001], при последующих попарных анализах (q=0,05, пересмотренное критическое значение р<0,017) было показано значительное увеличение концентрации ОТ в плазме непосредственно после в.в. введения по сравнению с исходным уровнем (р<0,001) через 10 минут (р=0,01), 30 минут (р=0,001), 60 минут (р=0,001) и 120 минут после завершения в.в. введения (р<0,001). Значительные взаимодействия состояние × продолжительность отсутствовали, F(15, 88,69)=1, р=0,461.
Концентрация вазопрессина в плазме крови: Средние концентрации AVP в плазме в различные моменты времени после введения 8IU-OT, 24IU-OT, IV-OT и плацебо (где планки погрешностей соответствуют стандартной ошибке среднего) приведены в таблице 3 и на фигуре 7(b). Для LMM 4 (способ лечения) ×6 (продолжительность) наблюдали значительный главный эффект способа лечения на концентрацию AVP в плазме крови [F(3, 82,42)=4,55, р=0,005]. В последующих попарных сравнениях (q=0,05, пересмотренное критическое значение р<0,0083) было выявлено значительное снижение концентрации AVP в плазме после лечения 24IU-OT по сравнению с плацебо (р=0,008) и IV-OT (р=0,013), и значительное снижение после лечения 8IU-OT по сравнению с IV-OT (р=0,023). Значительный главный эффект продолжительности [F(5, 90,63)=1,81, р=0,12] или взаимодействия способ лечения × продолжительность, F(15, 82,46)=1,03, р=0,434, отсутствовали.
Концентрация кортизола в плазме крови: Средние концентрации кортизола в плазме в различные моменты времени после введения 8IU-OT, 24IU-OT, IV-OT и плацебо (где планки погрешностей соответствуют стандартной ошибке среднего) приведены в таблице 4 и на фигуре 7(c). Для LMM 4 (способ лечения) ×6 (продолжительность) наблюдали значительный главный эффект способа лечения на концентрацию кортизола в плазме крови [F(3, 84,77)=4,82, р=0,004]. В последующих попарных сравнениях (q<0,05, пересмотренное критическое значение р<0,017) было показано значительное увеличение концентрации кортизола после лечения IV-OT по сравнению с плацебо (р=0,01) и 24 IU-ОТ (р<0,001), но не 8IU-OT. Наблюдали значительный главный эффект продолжительности на концентрацию кортизола в плазме крови [F(5, 90,07)=2,4, р=0,04], но значительных различий в последующих попарных сравнениях отмечено не было. Наконец, значительное взаимодействие способ лечения × продолжительность отсутствовал [F(15, 84,72)=0,421, p=0,969].
В указанном исследовании было продемонстрировано, что способ лечения 8IU-OT снижает восприятие гнева при стимулах в виде изображений лиц с неопределенными эмоциями с минимальным системным воздействием. Важно отметить, что полученные данные впервые позволяют сделать предположение о том, что низкая доза ОТ является более эффективной по сравнению с более высокой дозой в отношении модуляции социального распознавания. Кроме того, результаты, полученные в исследовании поведения, подтверждают, что ОТ, доставляемый интраназально с применением устройства для доставки в указанном исследовании, достигает мозга и влияет на социальное распознавание, тогда как ОТ, вводимый периферически, при схожем повышении концентрации ОТ в плазме не имеет указанного действия.
Полученные данные подчеркивают незначительное действие ОТ на обработку стимулов в виде изображений лиц с неопределенными эмоциями для восприятия гнева, так как различия в рейтингах гнева или счастья отсутствовали. В то время, как специфические эффекты ОТ при представлении стимулов с неопределенными эмоциями указывают на то, что ОТ влияет только на эмоциональную оценку стимулов, в которых явная эмоциональная окраска отсутствует, отсутствие эффектов при представлении стимулов, выражающих счастье и гнев, также можно объяснить относительно низкими изменениями рейтингов для указанных стимулов. Следует отметить, что различия в рейтингах доверия между введением плацебо и любым способом ОТ отсутствовали. Несмотря на то, что данный факт может быть связан с тем, что вопрос «о доверии» был задан в явном виде [в большинстве исследований использовали более подробные экономические задания64], полученные результаты дополнительно подтверждают, что ОТ может не приводить к увеличению восприятия доверия96-97.
Особое преимущество режима доставки согласно настоящему изобретению, который является более эффективным при более низких концентрациях, заключается в том, что он также позволяет регулировать баланс концентраций ОТ и AVP49 за счет перекрестной реакционной активности с рецепторами AVP50,98-100. Кроме того, по сравнению с более высокими дозами было показано, что более низкие дозы увеличивают периферический уровень ОТ в слюне65, снижают стрессовый ответ кортизола66 и увеличивают восприимчивость к визуальному контакту у пациентов с синдромом ломкой Х-хромосомы67. Кроме того, было показано, что введение более низкой дозы ОТ сразу после рождения впоследствии делает субъекта более предпочтительным при выборе партнерами68. Аналогично, введение более низких доз связывают с более выраженным улучшением социального распознавания по сравнению с более высокими дозами69-70.
Подобно ОТ, рецепторы AVP расположены системно или периферически74-75 и играют важную роль при социальном поведении и психических патологиях49. Было установлено, что указанная «побочная» активность может приводить к нелинейной зависимости доза-ответ, что дополнительно подчеркивает важность определения режима дозирования с оптимизированным терапевтическим действием101.
Важно отметить, что данные зависимости доза-ответ, полученные в настоящем изобретении, подтверждают выбор оптимальной дозы для модуляции социального распознавания, демонстрируя тем самым, что более низкая доза в большей степени модулирует социальное распознавание по сравнению с повышенной дозой. Кроме того, у пациентов, состояние которых вызвано расстройствами различной природы, восприимчивыми к ОТ, ответ может быть выражен в более значительной степени по сравнению со здоровыми добровольцами.
Данные о восприятии лицевых стимулов, полученные в настоящем изобретении, в общем случае согласуются с результатами последних исследований человека, в частности эмоций с отрицательной валентностью81, так как различия были обнаружены только при восприятии гнева в отношении лиц с неопределенными эмоциями. Полученные результаты, подчеркивающие специфическое понижение негативной оценки лиц с неопределенными эмоциями, имеют особую важность в случае нарушений, характеризующихся негативной оценкой социальных стимулов (например, социального тревожного расстройства). В предыдущих исследованиях было выдвинуто предположение о том, что ОТ снижает тенденцию к восприятию негативной информации у индивидуумов с клиническими случаями тревоги82 и выраженной личностной тревожностью, тем не менее, насколько известно авторам настоящего изобретения, данное исследование является первым, в котором сделано предположение о снижении негативной оценки у здоровых индивидуумов.
Анализ размеров носового клапана
Анализ проводили с использованием статистического пакета R (версия 3.1.1; R Development Core Team, 2014) для оценки влияния площади поперечного сечения носового клапана, представляющего собой похожую на щель структуру, расположенную на стыке передней и задней областей каждой носовой полости, на фармакодинамику. Сначала проводили ANOVA повторных измерений для исследования возможных значительных изменений площади поперечного сечения носового клапана между сессиями (посещение для скрининга и каждое посещение для проведения лечения). Кроме того, так как площадь поперечного сечения может быть различной в зависимости от размера индивидуума и его возраста, то для оценки взаимосвязи между указанными факторами во время скрининга вычисляли коэффициенты корреляции Пирсона.
Корреляцию между рейтингом гнева для лиц с неопределенными эмоциями и средней площадью поперечного сечения носового клапана определяли для способов лечения 8IU-OT, 24IU-OT, IV-OT и плацебо. В указанном исследовании, так как введение проводили и в левую и в правую носовые полости, средние площади поперечного сечения определяли для каждой из левой и правой носовых полостей, и среднюю площадь поперечного сечения определяли при помощи суммы указанных средних значений для левой и правой носовых полостей.
Для оценки совокупности данных нулевой и альтернативной гипотез также вычисляли байесовские факторы при помощи способа Джеффриса-Цельнера-Сио60. Определение при помощи данного подхода является особенно уместным, если данные подтверждают нулевую гипотезу (т.е. отсутствие связи между двумя переменными) по сравнению с альтернативной гипотезой (т.е. где присутствует связь между двумя переменными), так как незначительный коэффициент р не может являться подтверждением нулевой гипотезы85. Значение байесовского фактора ниже 1/3 по существу подтверждает нулевую гипотезу, выше 3 подтверждает альтернативную гипотезу, и в диапазоне от 1/3 до 3 не подтверждает ни одну из указанных гипотез63.
Доверительные интервалы различий между корреляциями при каждом условии лечения вычисляли для сравнения величины корреляции и для исследования того, является ли взаимосвязь между средней площадью поперечного сечения носового клапана и рейтингом гнева для лиц с неопределенными эмоциями значительно более выраженной по сравнению со взаимосвязями, определенными для других способов лечения. Так как все переменные в значительной степени связаны друг с другом, и измерения проводили в одном образце62, то проводили корректировку ДИ для учета перекрывания58 с использованием Z-преобразования Фишера. Любой ДИ, включающий ноль, указывает на то, что нулевая гипотеза, в которой отсутствуют различия между корреляциями, не может быть опровергнута.
Также вычисляли взаимосвязь между уровнем в плазме крови и средней площадью поперечного сечения носового клапана, результаты приведены в таблице 6. Для исследования влияния площади поперечного сечения носового клапана на системную доступность ОТ, AVP и кортизола вычисляли изменение показателей по сравнению с концентрацией ОТ и AVP и кортизола на исходном уровне непосредственно перед оценкой социального распознавания (~ через 40 минут после лечения).
В ANOVA повторных измерений главный эффект продолжительности для средней площади поперечного сечения носового клапана [F(1,99, 29,86)=0,69, р=0,51; ] выявлен не был. Также отсутствовала взаимосвязь между возрастом [r=0,56, 95% ДИ (-0,45, 0,54), n=16, р=0,84] и ИМТ [r=-0,68, 95% ДИ (-0,55, 0,44), n=15, р=0,015] со средней площадью поперечного сечения носового клапана во время скрининга.
При вычислении коэффициентов корреляции Пирсона была показана значительная взаимосвязь между рейтингами гнева для нейтральных лиц и средней площадью поперечного сечения носового клапана после лечения 8IU-OT [r=-0,61, 95% ДИ (-0,85, -0,14), n=15, р=0,015], где соответствующий байесовский фактор (В) 3,62, по существу подтверждал, что две указанные переменные были взаимосвязаны. Взаимосвязь между рейтингами гнева для лиц с неопределенными эмоциями и средней площадью поперечного сечения носового клапана после лечения 8IU-OT показана на фигуре 8.
Как показано на фигуре 8, взаимосвязь между лечением и рейтингом гнева для нейтральных лиц после лечения 24IU-OT [r=-0,14, 95% ДИ (-0,59, 0,38), n=16, р=0,6; В=0,22], IV-OT [r=0,11, 95% ДИ (-0,43, 0,59), n=15, р=0,7; В=0,21] или плацебо [r=0,04, 95% ДИ (-0,46, 0,53), n=16, р=0,88; В=0,19] отсутствовала, где все соответствующие байесовские факторы по существу подтверждали, что указанные переменные не были связаны друг с другом.
Сравнение коэффициентов корреляции также выявило значительные различия корреляции для способов лечения 8IU-OT и IV [r=-0,72 (-1,4, -0,2)] и плацебо [r=-0,65 (-1,1, -0,06)], но отсутствие значительных различий при корреляции со способом лечения 24IU-OT [r=-0,42 (-0,97, 0,06)].
Кроме того, отсутствовала взаимосвязь между площадью поперечного сечения носового клапана и концентрацией ОТ, AVP или кортизола в плазме при любых условиях лечения.
В данном исследовании было подтверждено, что на эффективность ОТ в отношении социального распознавания можно влиять за счет контролирования площади поперечного сечения носового клапана при интраназальном введении определенной пониженной дозы ОТ, составляющей менее 24IU. В одном из вариантов реализации указанное контролирование обеспечивают за счет эффективного давления потока выдыхаемого воздуха и структурного эффекта наконечника для носа при раскрытии носового клапана.
Анализ фМРТ
Стандартную предварительную обработку данных фМРТ проводили при помощи анализа независимых компонент (ICA) и автоклассификации с использованием способа выявления шумов на основе ICA FMRIB (FIX) для подавления шумов в данных фМРТ.
Индивидуальные компоненты группировали при помощи подхода временного объединения в фиксированной модели MELODIC (многопараметровое поисковое линейное оптимизированное разложение на независимые компоненты) для 40 компонент.
Затем определяли компоненты с наиболее выраженным миндалевидным телом (также имеющие выраженную медиальную височную долю (MTL) и ствол мозга), которая в данном случае представляла собой независимую компоненту №37 (IC0037).
Затем проводили двойную регрессию для построения пространственных карт индивидуальных компонент для соответствующих периодов времени, как показано на фигуре 9(a), на которой показаны одновыборочные t-критерии для всех групп данных (t>5) после двойной регрессии.
Для оценки главного эффекта условия введения ОТ (F-тест для способов лечения IU08-OT, IU24-OT, IV-OT и плацебо) на отдельные пространственные карты канонического компонента (t>5) для IC0037 проводили исследование воксельной обобщенной линейной модели (GLM). Затем были выявлены самые крупные кластеры с нескорректированным вексельным р<0,01. Два самых крупных кластера, в которых был показан главный эффект условия введения ОТ, были локализованы в левом и правом миндалевидном телах, соответственно, что показано на фигуре 9(b).
Затем в попарном сравнении способов лечения 8IU-OT и плацебо были выявлены два кластера, в которых было показано значительное (р<0,05, скорректирован на размер кластеров при помощи теста пермутаций) увеличение взаимосвязей для способа лечения 8IU-OT по сравнению с плацебо в левом и правом миндалевидных телах, соответственно, как показано на фигуре 9(c). Выделяли главный средний показатель взаимосвязи для каждой группы данных в каждом из указанных четырех кластеров и использовали для дополнительного анализа (в данном случае при помощи MATLAB).
Проводили ANOVA повторных измерений. На фигурах 10(a) и (b) проиллюстрированы коробчатые диаграммы средней взаимосвязи двух кластеров, на которых показан значительный (р<0,01, нескорректированный) главный эффект для данного условия введения ОТ. На фигурах 11(a) и (b) проиллюстрированы коробчатые диаграммы средней взаимосвязи двух кластеров, на которых показано значительное (р<0,05, скорректированный на размер кластеров) увеличение взаимосвязи после способов лечения 8IU-OT и плацебо. Значения взаимосвязи нормировали (z-показатель) относительно среднего значения для каждого субъекта, полученного при различных условиях, для простоты сравнения.
На фигурах 12(a) и (b) при помощи графиков «спагетти» приведены значения взаимосвязи для всех условий в каждом из значительных кластеров миндалевидных тел, полученных в результате попарного сравнения, как проиллюстрировано на фигуре 9(c), для каждого индивидуума.
В соответствии с ожиданиями в ANOVA повторных измерений был выявлен значительный главный эффект условия введения в обоих кластерах (р=0,0032 и р=0,0039). Коробчатые диаграммы позволяют предположить, что главные эффекты условия введения ОТ наблюдаются при сравнении IU08-OT и плацебо и определяются повышенной взаимосвязью миндалевидных тел при лечении IU08-ОТ, что также подтверждается результатами последующих попарных сравнений (t=-2,54, р=0,016, и t=-2,24, р=0,033).
Миндалевидное тело является ключевой областью мозга при регуляции эмоций86, которая играет важную роль при обработке входящих социальных стимулов87. Действительно, данные, полученные при помощи конвергентных способов нейровизуализации, позволяют предположить, что миндалевидное тело является важной мишенью при введении ОТ. Например, сообщалось, что отдельное интраназальное введение ОТ обеспечивает как снижение88-89, так и повышение90-91 активности миндалевидного тела, если рассматривать широкий диапазон эмоциональных стимулов. В то время, как в указанных ранних исследованиях проводили измерение рекрутинга нейронов при представлении стимулов, в недавней работе начали исследовать активность мозга в состоянии покоя. Сообщается, что миндалевидное тело является ключевым компонентом более крупной «социальной мозговой сети», в котором наблюдают повышенный приток крови после введения ОТ92. Аналогично, данные указывают на то, что введение ОТ приводит к увеличению взаимосвязи между миндалевидным телом и ростральной медиальной лобной корой93.
В настоящем исследовании впервые проводили оценку взаимосвязи в состоянии покоя после введения различных доз ОТ (8IU и 24IU) при помощи различных способов (интраназального и внутривенного). Данные позволяют предположить, что низкая доза ОТ, доставляемая интраназально (но не внутривенно), модулирует взаимосвязь миндалевидного тела, что согласуется с возможной доставкой из носа в мозг.Повышенная взаимосвязь миндалевидного тела может способствовать повышению осознания социальных стимулов, которое, как полагают, лежит в основе наблюдаемого действия ОТ в отношении социального распознавания и поведения10. Полученные результаты также могут быть важны при лечении психиатрических расстройств, характеризующихся социальными нарушениями, при которых, как сообщается, происходит нарушение взаимосвязей между миндалевидным телом и другими областями мозга (например, шизофрении)94. Кроме того, полученные данные дополняют имеющиеся знания о влиянии различных доз и способов введения ОТ на рекрутинг нейронов в состоянии покоя.
Вкратце, в настоящем исследовании предложены новые идеи, связанные с усовершенствованием способа глубокой интраназальной доставки ОТ, и показано, что повышенная фармакодинамическая активность может быть обеспечена в частности при применении режима доставки ОТ согласно настоящему изобретению по сравнению с в.в. доставкой, обеспечивающей схожее системное воздействие, этот факт позволяет предположить, что активность обеспечивается за счет непосредственного переноса из носа в мозг. Полученные данные также позволяют предварительно судить о том, что выбор интраназальной дозы ОТ, основанный на предшествующих аналогичных данных, но не подтвержденный экспериментально, может быть ошибочным; в настоящем исследовании показано, что более низкая доза (8IU) может обеспечивать повышенную эффективность по сравнению с более высокой дозой (24IU) при надлежащем введении.
Анализ МРТ и пупиллометрии
FreeSurfer (http://surfer.nmr.mgh.harvard.edu) использовали для Т1-взвешенных данных, включая реконструкцию поверхности и полную сегментацию мозга123, для получения точных значений объема выделенных сегментов мозга для совместной регистрации данных фМРТ. Для обработки данных фМРТ использовали библиотеку программ FRRIB Software Library (FSL; http://fsl.fmrib.ox.ac.uk/fsl/fslwiki/124). Первые пять значений отбрасывали. Предварительную обработку данных фМРТ проводили при помощи инструмента экспертизы FMRIB Expert Analysis Tool (FEAT) версии 6.0128. Указанная обработка включала корректировку движений с использованием MCFLIRT124, пространственное сглаживание при помощи SUSAN125 с использованием гауссова ядра FWHM 7 мм и временного фильтра высоких частот 100 сек. Проводили отдельную стадию анализа независимых компонент (ICA) с использованием многопараметрового поискового линейного оптимизированного разложения на независимые компоненты (MELODIC ICA126) для автоматического снижения шумов (см. ниже). Инструменты линейной и нелинейной регистрации изображений FMRIB (FLIRT124), оптимизированные с использованием граничной регистрации (Boundary Based Registration, BBR127), использовали для приведения данных фМРТ каждого пациента к стандартному пространству (MNI-152) с использованием Т1-взвешенного объема в качестве промежуточного показателя.
Подстановку в обобщенные линейные модели индивидуального уровня (GLM) проводили с использованием FILM (FMRIB улучшенная линейная модель)127-128, в которой моделировали лицевые стимулы (лица, выражающие счастье/гнев/неопределенные эмоции) и геометрические формы в качестве событий, и промежуточных испытаний для скрытой фиксации исходного уровня. Q1 и Q2 моделировали в качестве одной независимой переменной для различных лицевых стимулов и форм. Затем выделяли средние контрастные оценочные значения параметров (СОРЕ) для масок левого и правого миндалевидного тела на основании анатомического атласа Гарвард-Оксфорд, поставляемого с FSL, и подставляли значения в линейные смешанные модели более высокого уровня в SPSS для исследования главного эффекта условия и способа лечения (см. ниже).
Предварительную обработку данных пупиллометрии проводили с использованием сделанного на заказ сценария MATLAB. Исходные данные переводили в значения диаметра, где невозможные с точки зрения физиологии значения размера зрачков (<2 мм или >9 мм) исключали из выборки для удаления шумов (например, вызванные морганием). Каждый раз проводили последовательность отдельных испытаний, при этом вычисляли средний размер зрачка для каждого условия стимулирования. Наконец, получали средние значения, полученные в первые 8 секунд во всех 20 испытаниях для каждого условия, для получения общего среднего значения диаметра зрачков.
Статистический анализ проводили с использованием IBM SPSS Statistics версии 22 (IBM, Armonk, N.Y) для оценки влияния способа лечения на активность миндалевидного тела. Как описано выше, для анализа активности миндалевидного тела использовали подход линейного смешанного моделирования (LMM). Подстановку во все модели проводили с использованием неструктурированной матрицы. Способ экспериментального лечения рассматривали в качестве фиксированного и повторяющегося эффекта в LMM при исследовании влияния способа лечения на активность миндалевидного тела. Такой же подход LMM использовали для оценки различий в средних значениях диаметра зрачка, значениях СОРЕ для различий активности левого и правого миндалевидного тела в отношении гневных лиц и форм, счастливых лиц и форм и счастливых лиц и гневных лиц. Проводили оценку нормированных остатков после подстановки в модель для выявления выпадающих значений. Z-показатели выше 2,58 или ниже -2,58 отбрасывали при анализе. Значения, выпадающие за указанные пределы, отбрасывали из выборок данных об активности миндалевидного тела (1 значение в выборке данных для правого миндалевидного тела при представлении стимулов гнева, счастья и неопределенных эмоций и форм, соответственно; 1 значение в выборке данных для левого миндалевидного тела при представлении стимулов гнева и счастья, соответственно; и 2 значения в выборке данных для левого миндалевидного тела при представлении стимулов с неопределенными эмоциями и формы, соответственно). Для любых значительных главных эффектов (р<0,05) проводили последующий анализ для сравнения каждого условия лечения для нормирования критических значений р для корректировки по множественным сравнениям с использованием 5% уровня ложноположительных результатов (FDR)59. Также проводили оценку взаимосвязи между активацией миндалевидного тела и средним расширением зрачка, рейтингами поведения и физиологией носовой полости. Наконец, для оценки совокупности данных нулевой и альтернативной гипотез также вычисляли байесовские факторы при помощи описанного ранее способа Джеффриса-Цельнера-Сио60.
В LMM был выявлен значительный главный эффект способа лечения на активность правого миндалевидного тела при представлении гневных лиц [F(3, 15,1)=4,54, р=0,019; фигуры 13(a) и (b)]. В последующих попарных сравнениях (q=0,05, пересмотренное критическое значение р<0,008) было показано, что активация правого миндалевидного тела была значительно понижена в условиях лечения 8IU-ОТ по сравнению с плацебо (р=0,002). Отмечали главный эффект способа лечения активности правого миндалевидного тела в ответ на представление счастливых лиц [F(3, 15)=3,44, р=0,04], где в последующих сравнениях было показано, что снижение после введения 8IU-OT по сравнению с плацебо находилось у порогового значения значимости FDR (р=0,01; q=0,05, пересмотренное критическое значение р<0,008). Отмечали главный эффект способа лечения на активность правого миндалевидного тела при представлении лиц с неопределенными эмоциями, примерно соответствующий пороговому значению значимости [F(3, 14,6)=3,15, р=0,057]. В последующих поисковых анализах было показано, что снижение активности правого миндалевидного тела в условиях введения 8IU-OT по сравнению с плацебо находилось у порогового скорректированного значения значимости FDR (р=0,01; q=0,05, пересмотренное критическое значение р<0,008). Также отмечали главный эффект способа лечения в отношении геометрических форм [F(3, 15)=3,56, р=0,04], тем не менее, в последующих анализах не были выявлены значительные различия после корректировки предельных значений FDR. Отмечали главный эффект в отношении контрастов «счастливые лица>гневные лица» для правого миндалевидного тела [F(3, 14,7)=4,46, р=0,02], но по результатам последующих сравнений значимость в рамках скорректированных пороговых значений FDR подтверждена не была. Что касается активности левого миндалевидного тела, то в LMM не был выявлен главный эффект условия введения при представлении гневных лиц [F(3, 15,1)=1,28, р=0,32], лиц с неопределенными эмоциями [F(3, 13,6)=1,14, р=0,37], счастливых лиц [F(3, 14)=2,14, р=0,14] или геометрических форм [F(3, 14,4)=1,87, р=0,18]. Отмечали главный эффект в отношении контрастов активности «счастливые лица > гневные лица» для левого миндалевидного тела [F(3, 14,7)=4,79, р=0,02], но по результатам последующих сравнений значимость в рамках скорректированных пороговых значений FDR подтверждена не была. Главные эффекты способа лечения на любое из контрастных значений СОРЕ «эмоция > форма» отсутствовали, что показано в таблице 7.
Значительный главный эффект способа лечения на средний диаметр зрачка при обработке эмоций при представлении гневных лиц [F(3, 15)=0,57, р=0,64], счастливых лиц [F(3, 15)=0,62, р=0,62] или лиц с неопределенными эмоциями [F(3, 15)=1,33, р=0,3] отсутствовал. Тем не менее, наблюдали значительную взаимосвязь между активацией правого миндалевидного тела и средним диаметром зрачка при представлении гневных лиц (р=0,02; фигура 14(a)), лиц с неопределенными эмоциями (р<0,001; фигура 14(b)) и счастливых лиц (р=0,01; фигура 14(c)) после лечения 8IU-ОТ, как показано в таблице 8. Все соответствующие байесовские факторы (В) составляли более 3, это по существу подтверждало130, что две указанные переменные являются взаимосвязанными. Значительные взаимосвязи при других способах лечения (во всех случаях р>0,05) отсутствовали, и во всех случаях В составлял менее 0,33, это по существу подтверждает, что никакие из указанных переменных не были взаимосвязаны. Наконец, отсутствовала значительная взаимосвязь между интенсивностью рейтингов гнева и активностью правого миндалевидного тела для всех способов лечения, как показано в таблице 9, или взаимосвязь между размерами носового клапана и активацией правого миндалевидного тела для любого из указанных способов лечения, как показано в таблице 10. Согласно приведенному выше описанию различия в размерах носового клапана перед проведением каждого способа лечения отсутствовали [F(9, 108)=0,41, р=0,93). Количество отмечаемых нежелательных явлений (например, краткосрочного головокружения) было эквивалентным для всех групп, в которых проводили лечение (8IU-OT, три сообщения; 24IU-OT, два сообщения, IV ОТ, три сообщения; плацебо, два сообщения).
В данном исследовании показано, что способ лечения 8IU-OT снижает активность правого миндалевидного тела по сравнению с плацебо. Полученные результаты впервые описывают прямое сравнение доставки ОТ из носа в мозг и системной доставки и указывают на то, что доставка ОТ по пути из носа в мозг - но не периферическая доставка ОТ, обеспечивающая схожий уровень в крови, - обеспечивает воспроизводимое хорошо охарактеризованное снижение активации правого миндалевидного тела в ответ на эмоциональные стимулы после лечения OT88,114-115.
Важно отметить, что полученные данные согласуются с фактами, обсуждаемыми выше, в том, что ОТ при доставке с применением устройства согласно настоящему изобретению модулирует восприятие гнева в лицевых стимулах, и с животными моделями в том, что пониженная доза ОТ обеспечивает более выраженное повышение социального распознавания69-70, что особенно важно с учетом значительной роли миндалевидного тела при социальном распознавании и поведении.
Указанные эффекты могут быть неспецифичными в отношении социальных стимулов с отрицательной валентностью, так как главные эффекты лечения на активность правого миндалевидного тела при представлении счастливых лиц и лиц с неопределенными эмоциями были значительными и соответствовали пограничному значению значимости, соответственно. Различия при последующих сравнениях способа лечения 8IU-OT и плацебо находились на границе статистической значимости. Наблюдаемое снижение активности правого миндалевидного тела при представлении стимулов с положительной и отрицательной валентностью для способа лечения ОТ согласуется с гипотезой о том, что ОТ увеличивает влияние на поведение приближения114,118.
Во вторичном анализе была выявлена значительная связь между активностью правого миндалевидного тела и средним диаметром зрачка при обработке гневных, неопределенных и счастливых лицевых стимулов после введения 8IU-OT. Несмотря на то, что главный эффект лечения на диаметр зрачка обнаружен не был, данные указывают на модуляцию когнитивных ресурсов в миндалевидном теле в ответ на лицевые стимулы независимо от их валентности после лечения 8IU-OT.
Миндалевидное тело представляет собой область, в которой расположено большое количество рецепторов окситоцина131-132. Было показано, что указанные рецепторы действуют путем ингибирования активности миндалевидного тела за счет увеличения ГАМК-эргической межнейронной активности133-134. Снижение активности миндалевидного тела после введения ОТ с применением устройства согласно настоящему изобретению согласуется с транспортом молекул из носа в мозг по путям, опосредованным обонятельными и тройничными нервными волокнами135. Поступление молекул в миндалевидное тело посредством обонятельных луковиц136-138 или транспорт через внеклеточную жидкость мозга139 из обонятельных луковиц и участков доставки в ствол мозга могут способствовать указанному снижению активности миндалевидного тела за счет локального ГАМК-эргического цикла после интраназальной доставки. Независимо от того, каким конкретным образом эндогенный ОТ действует на активность миндалевидного тела, за счет использования такого показателя сравнения, как уровень в периферической крови, в настоящем исследовании продемонстрировано, что пути доставки из носа в мозг обеспечивают эффекты, не наблюдаемые при сравнимом уровне чистого системного воздействия, что позволяет предположить упрощенное поступление в мозг.
Данные зависимости доза-ответ, приведенные в настоящем описании, позволяют предположить, что низкая доза ОТ, доставляемая с применением устройства согласно настоящему изобретению, является достаточной для модуляции активности миндалевидного тела. У пациентов, состояние которых вызвано расстройствами различной природы, восприимчивыми к ОТ, ответ может быть выражен в более значительной степени по сравнению со здоровыми добровольцами.
Тот факт, что эффект был обнаружен для дозы 8IU-OT, но не 24IU-OT, может объясняться несколькими причинами, включая перекрестную реакционную активность с рецепторами вазопрессина49 и возможное упрощенное достижение дозой 8IU-OT, доставляемой с применением устройства согласно настоящему изобретению, тех областей в носу, из которых может происходить прямой транспорт из носа в мозг.
Важно отметить, что подтверждение действия 1IU-OT при периферическом введении ОТ на активность миндалевидного тела получено не было. Несмотря на наличие противоречивых доказательств о возможности пересечения ГЭБ ОТ, вводимым периферически140-141, в настоящем исследовании сделано предположение о том, что даже если ОТ и пересекает указанный барьер в небольших количествах, то указанное количество является недостаточным, чтобы модулировать активность миндалевидного тела по сравнению с плацебо. Индивидуальные различия и условия могут влиять на ответ на введение ОТ16, таким образом, преимуществом настоящего исследования являлось использование схемы внутрисубъектного исследования для оценки активности миндалевидного тела. За счет использования указанной схемы эксперимента минимизируются любые индивидуальные различия, вызванные изменением эндогенной системы окситоцина142-143.
Вкратце, в настоящем исследовании неожиданно было обнаружено, что низкая доза ОТ, доставляемая интраназально при помощи описанного способа доставки, модулирует активность миндалевидного тела, и полученные результаты обеспечивают дополнительное подтверждение тому, что пониженная интраназальная доза ОТ может в большей степени способствовать модуляции социального распознавания и поведения, и периферическое действие ОТ впоследствии вероятно не оказывает никакого значительного воздействия на нейроны.
Список литературы
1. Guastella AJ, MacLeod С (2012): A critical review of the influence of oxytocin nasal spray on social cognition in humans: Evidence and future directions. Horm Behav. 61: 410-418.
2. Meyer-Lindenberg A, Domes G, Kirsch P, Heinrichs M. Oxytocin and vasopressin in the human brain: social neuropeptides for translational medicine. Nat Rev Neurosci 2011; 12: 524-538.
3. Striepens N, Kendrick KM, Maier W, Hurlemann R. Prosocial effects of oxytocin and clinical evidence for its therapeutic potential. Front Neuroendocrinol 2011; 32: 426-450.
4. Bartz JA, Zaki J, Bolger N, Hollander E, Ludwig NN, Kolevzon A, et al (2010): Oxytocin Selectively Improves Empathic Accuracy. Psychol Sci. 21: 1426-1428.
5. Hurlemann R, Patin A, Onur OA, Cohen MX, Baumgartner T, Metzler S et al. Oxytocin enhances amygdala-dependent, socially reinforced learning and emotional empathy in humans. J Neurosci 2010; 30: 4999-5007.
6. Kosfeld M, Heinrichs M, Zak PJ, Fischbacher U, Fehr E. Oxytocin increases trust in humans. Nature 2005; 435: 673-676.
7. Shalvi S, De Dreu CK. Oxytocin promotes group-serving dishonesty. Proc Natl Acad Sci USA 2014; 111: 5503-5507.
8. Van Ijzendoorn MH, Bakermans-Kranenburg MJ. A sniff of trust: meta-analysis of the effects of intranasal oxytocin administration on face recognition, trust to ingroup, and trust to out-group.Psychoneuroendocrinology 2012; 37: 438-443.
9. Guastella AJ, Mitchell PB, Dadds MR (2008): Oxytocin increases gaze to the eye region of human faces. Biol Psychiatry. 63: 3-5.
10. Domes G, Heinrichs M, Michel A, Berger C, Herpertz SC (2007): Oxytocin Improves "Mind-Reading" in Humans. Biol Psychiatry. 61: 731-733.
11. Guastella AJ, Einfeld SL, Gray KM, Rinehart NJ, Tonge BJ, Lambert TJ, et al (2010): Intranasal Oxytocin Improves Emotion Recognition for Youth with Autism Spectrum Disorders. Biol Psychiatry. 67: 692-694.
12. Modi ME, Young LJ (2012): The oxytocin system in drug discovery for autism: Animal models and novel therapeutic strategies. Horm Behav. 61: 340-350.
13. MacDonald K, Feifel D (2012): Oxytocin in schizophrenia: a review of evidence for its therapeutic effects. Acta Neuropsychiatrica. 24: 130-146.
14. Dadds MR, MacDonald E, Cauchi A, Williams K, Levy F, Brennan J (2014): Nasal oxytocin for social deficits in childhood autism: A randomized controlled trial. J Autism Dev Disord. 44: 521-531.
15. Guastella AJ, Hickie IB, McGuinness MM, Otis M, Woods EA, Disinger HM, et al (2013): Recommendations for the standardisation of oxytocin nasal administration and guidelines for its reporting in human research. Psychoneuroendocrinology. 38: 612-625.
16. Bartz JA, Zaki J, Bolger N, Ochsner KN (2011): Social effects of oxytocin in humans: context and person matter. Trends in cognitive sciences. 15: 301-309.
17. MacDonald K, Feifel D (2013): Helping oxytocin deliver: considerations in the development of oxytocin-based therapeutics for brain disorders. Front Neurosci.
18. Quintana DS, Alvares GA, Hickie IB, Guastella AJ (2015): Do delivery routes of intranasally administered oxytocin account for observed effects on social cognition and behavior? A two-level model. Neurosci Biobehav Rev. 49: 182-192.
19. Landgraf R, Neumann ID. Vasopressin and oxytocin release within the brain: a dynamic concept of multiple and variable modes of neuropeptide communication. Front Neuroendocrinol 2004; 25: 150-176.
20. Iliff JJ, Wang M, Liao Y, Plogg BA, Peng W, Gundersen GA et al. A paravascular pathway facilitates CSF flow through the brain parenchyma and the clearance of interstitial solutes, including amyloid β. Sci Transl Med 2012; 4:147ra111-147ra111.
21. Dhuria SV, Hanson LR, Frey WH II. Intranasal delivery to the central nervous system: Mechanisms and experimental considerations. J Pharm Sci 2009; 99: 1654-1673.
22. Ermisch A, Barth T, Rtihle H, Skopkova J, Hrbas P, Landgraf R. On the blood-brain barrier to peptides: accumulation of labelled vasopressin, DesGlyNH2-vasopressin and oxytocin by brain regions. Endocrinol Exp 1985; 19: 29-37.
23. Djupesland PG, Messina JC, Mahmoud RA (2014): The nasal approach to delivering treatment for brain diseases: an anatomic, physiologic, and delivery technology overview. Therapeutic delivery. 5: 709-733.
24. Cole P (2003): The four components of the nasal valve. Am J Rhinol. 17: 107-110.
25. Aggarwal R, Cardozo A, Homer J. The assessment of topical nasal drug distribution. Clin Otolaryngol Allied Sci 2004; 29: 201-205.
26. Djupesland PG, Skretting A, Winderen M, Holand T (2006): Breath Actuated Device Improves Delivery to Target Sites Beyond the Nasal Valve. The Laryngoscope. 116: 466-472.
27. Djupesland PG, Messina JC, Mahmoud RA. Breath powered nasal delivery: a new route to rapid headache relief. Headache 2013; 53: 72-84.
28. Eccles R. Nasal airflow in health and disease. Acta Otolaryngol 2000; 120: 580-595.
29. Merkus P, Ebbens FA, Muller B, Fokkens WJ. Influence of anatomy and head position on intranasal drug deposition. Eur Arch Otorhinolaryngol 2006; 263: 827-832.
30. Djupesland PG, Mahmoud RA, Messina JC (2013): Accessing the brain: the nose may know the way. Journal of Cerebral Blood Flow & Metabolism. 33: 793-794.
31. Djupesland PG, Skretting A (2012): Nasal Deposition and Clearance in Man: Comparison of a Bidirectional Powder Device and a Traditional Liquid Spray Pump.Journal of Aerosol Medicine and Pulmonary Drug Delivery. 25: 280-289.
32. Djupesland PG (2012): Nasal drug delivery devices: characteristics and performance in a clinical perspective - a review. Drug Delivery and Translational Research 2012; 3:42-62.
33. Hollander E, Novotny S, Hanratty M, Yaffe R, DeCaria CM, Aronowitz BR, et al (2003): Oxytocin Infusion Reduces Repetitive Behaviors in Adults with Autistic and Asperger & apos; s Disorders. Neuropsychopharmacology. 28: 193-198.
34. Hollander E, Bartz J, Chaplin W, Phillips A, Sumner J, Soorya L, et al (2007): Oxytocin Increases Retention of Social Cognition in Autism. Biol Psychiatry. 61: 498-503.
35. Striepens N, Kendrick KM, Hanking V, Landgraf R, Wiillner U, Maier W et al. Elevated cerebrospinal fluid and blood concentrations of oxytocin following its intranasal administration in humans. Sci Rep 2013; 3: 3440.
36. MacDonald E, Dadds MR, Brennan JL, Williams K, Levy F, Cauchi AJ (2011): A review of safety, side-effects and subjective reactions to intranasal oxytocin in human research. Psychoneuroendocrinology. 36: 1114-1126.
37. Bakermans-Kranenburg M, Van Ijzendoorn M (2013): Sniffing around oxytocin: review and meta-analyses of trials in healthy and clinical groups with implications for pharmacotherapy. Translational psychiatry. 3: e258.
38. de Oliveira DC, Zuardi AW, Graeff FG, Queiroz RH, Crippa JA (2012): Anxiolytic-like effect of oxytocin in the simulated public speaking test. J Psychopharmacol (Oxf). 26: 497-504.
39. Butwick A, Coleman L, Cohen S, Riley E, Carvalho В (2010): Minimum effective bolus dose of oxytocin during elective Caesarean delivery. Br J Anaesth. 104: 338-343.
40. Rault J-L, Carter CS, Garner JP, Marchant-Forde JN, Richert ВТ, Lay Jr DC (2013): Repeated intranasal oxytocin administration in early life dysregulates the HPA axis and alters social behavior. Physiol Behav. 112: 40-48.
41. Gimpl G, Fahrenholz F (2001): The oxytocin receptor system: structure, function, and regulation. Physiol Rev. 81: 629-683.
42. Mayer-Hubner В (1996): Pseudotumour cerebri from intranasal oxytocin and excessive fluid intake. The Lancet. 347: 623-623.
43. Kanat M, Heinrichs M, Schwarzwald R, Domes G. Oxytocin attenuates neural reactivity to masked threat cues from the eyes. Neuropsychopharmacology 2015; 40: 287-295.
44. Evans S, Shergill SS, Averbeck BB. Oxytocin decreases aversion to angry faces in an associative learning task. Neuropsychopharmacology 2010; 35: 2502-2509.
45. Domes G, Steiner A, Porges SW, Heinrichs M. Oxytocin differentially modulates eye gaze to naturalistic social signals of happiness and anger. Psychoneuroendocrinology 2013; 38: 1198-1202.
46. Jesso S, Morlog D, Ross S, Pell MD, Pasternak SH, Mitchell DG et al. The effects of oxytocin on social cognition and behaviour in frontotemporal dementia. Brain 2011; 134: 2493-2501.
47. Bertsch K, Gamer M, Schmidt B, Schmidinger I, Walther S, Kastel T et al. Oxytocin and reduction of social threat hypersensitivity in women with borderline personality disorder. Am J Psychiatry 2013; 170: 1169-1177.
48. MacDonald K, Feifel D. Oxytocin's role in anxiety: a critical appraisal. Brain Res 2014; 1580: 22-56.
49. Neumann ID, Landgraf R (2012): Balance of brain oxytocin and vasopressin: implications for anxiety, depression, and social behaviors. Trends Neurosci. 35: 649-659.
50. Legros J, Chiodera P, Geenen V, Smitz S, Frenckell Rv (1984): Dose-Response Relationship between Plasma Oxytocin and Cortisol and Adrenocorticotropin Concentrations during Oxytocin Infusion in Normal Men*. The Journal of Clinical Endocrinology & Metabolism. 58: 105-109.
51. Neumann ID. Involvement of the brain oxytocin system in stress coping: interactions with the hypothalamo-pituitary-adrenal axis. Prog Brain Res 2002; 139: 147-162.
52. Wechsler D (1999): Weschsler Abbreviated Scale of Intelligence. San Antonio, TX: Psychological Corporation.
53. Lecrubier Y, Sheehan D, Weiller E, Amorim P, Bonora I, Harnett Sheehan K, et al (1997): The Mini International Neuropsychiatric Interview (MINI). A short diagnostic structured interview: reliability and validity according to the CIDI. Eur Psychiatry. 12: 224-231.
54. Spielberger CD (1983): Manual for the State-Trait Anxiety Inventory STAI (форма Y) ("опросник для самооценки").
55. Leknes S, Wessberg J, Ellingsen DM, Chelnokova O, Olausson H, Laeng В (2012): Oxytocin enhances pupil dilation and sensitivity to 'hidden' emotional expressions. Soc Cogn Affect Neurosci. 8: 741-749.
56. Lundqvist D, Flykt A, A (1998): The Karolinska directed emotional faces (KDEF). CD ROM from Department of Clinical Neuroscience, Psychology section, KarolinskaInstitutet. 91-630.
57. McCullough ME, Churchland PS, Mendez AJ. Problems with measuring peripheral oxytocin: can the data on oxytocin and human behavior be trusted? NeurosciBiobehav Rev 2013; 37: 1485-1492.
58. Hamer R, Simpson P (2009): Last observation carried forward versus mixed models in the analysis of psychiatric clinical trials. Am J Psychiatry. 166: 639-641.
59. Benjamini Y, Hochberg Y (1995): Controlling the false discovery rate: a practical and powerful approach to multiple testing. Journal of the Royal Statistical Society Series В (Methodological). 289-300.
60. Wetzels R, Wagenmakers, E-J (2012). A default Bayesian hypothesis test for correlations and partial correlations. Psychon. Bull. Rev. 19, 1057-1064.
61. Zou GY (2007). Toward using confidence intervals to compare correlations. Psychol. Methods 12, 399.
62. Raghunathan T, Rosenthal R, Rubin, DB (1996). Comparing correlated but nonoverlapping correlations. Psychol. Methods 1, 178.
63. Dienes Z (2014). Using Bayes to get the most out of non-significant results. Front Psychol 2014; 5: 1-17.
64. Theodoridou A, Rowe AC, Penton-Voak IS, Rogers PJ (2009): Oxytocin and social perception: oxytocin increases perceived facial trustworthiness and attractiveness. Horm Behav. 56: 128-132.
65. Van Ijzendoorn MH, Bhandari R, Van der Veen R, Grewen KM, Bakermans-Kranenburg MJ (2012): Elevated salivary levels of oxytocin persist more than 7 h after intranasal administration. Front Neurosci. 6.
66. Cardoso C, Ellenbogen MA, Orlando MA, Bacon SL, Joober R (2013): Intranasal oxytocin attenuates the Cortisol response to physical stress: a dose-response study. Psychoneuroendocrinology. 38: 399-407.
67. Hall SS, Lightbody AA, McCarthy BE, Parker KJ, Reiss AL (2012): Effects of intranasal oxytocin on social anxiety in males with fragile X syndrome. Psychoneuroendocrinology. 37: 509-518.
68. Bales KL, Perkeybile AM, Conley OG, Lee MH, Guoynes CD, Downing GM, et al (2013): Chronic intranasal oxytocin causes long-term impairments in partner preference formation in male prairie voles. Biol Psychiatry. 74: 180-188.
69. Benelli A, Bertolini A, Poggioli R, Menozzi B, Basaglia R, Arletti R (1995): Polymodal dose-response curve for oxytocin in the social recognition test. Neuropeptides. 28: 251-255.
70. Popik P, Vetulani J, Van Ree JM (1992): Low doses of oxytocin facilitate social recognition in rats. Psychopharmacology (Berl). 106: 71-74.
71. Bloom DE, Cafiero E, Jane-Llopis E, Abrahams-Gessel S, Bloom LR, Fathima S et al. The Global Economic Burden of Noncommunicable Diseases: Program on the Global Demography of Aging, 2012.
72. Miller G. Is pharma running out of brainy ideas. Science 2010; 329: 502-504.
73. Abbott A. Novartis to shut brain research facility. Nature 2011; 480: 161-162.
74. Frank E, Landgraf R (2008): The vasopressin system-from antidiuresis to psychopathology. Eur J Pharmacol. 583: 226-242.
75. Li C, Wang W, Summer SN, Westfall TD, Brooks DP, Falk S, et al (2008): Molecular mechanisms of antidiuretic effect of oxytocin. J Am Soc Nephrol. 19: 225-232.
76. Weisman O, Schneiderman I, Zagoory-Sharon O, Feldman R. Salivary vasopressin increases following intranasal oxytocin administration. Peptides 2013; 40: 99-103.
77. Burri A, Heinrichs M, Sched1owski M, Kruger TH. The acute effects of intranasal oxytocin administration on endocrine and sexual function in males. Psychoneuroendocrinology 2008; 33: 591-600.
78. Gossen A, Hahn A, Westphal L, Prinz S, Schultz R, Grander G et al. Oxytocin plasma concentrations after single intranasal oxytocin administration-A study in healthy men. Neuropeptides 2012; 46: 211-215.
79. Charlton S, Davis S, Ilium L. Nasal administration of an angiotensin antagonist in the rat model: effect of bioadhesive formulations on the distribution of drugs to the systemic and central nervous systems. Int J Pharm 2007; 338: 94-103.
80. Dale O, Nilsen T, Loftsson T, Tonnesen HH, Klepstad P, Kaasa S et al. Intranasal midazolam: a comparison of two delivery devices in human volunteers. J Pharm Pharmacol 2006; 58: 1311-1318.
81. Shahrestani S, Kemp AH, Guastella AJ (2013): The impact of a single administration of intranasal oxytocin on the recognition of basic emotions in humans: a meta-analysis. Neuropsychopharmacology. 38: 1929-1936.
82. Guastella AJ, Howard AL, Dadds MR, Mitchell P, Carson DS (2009): A randomized controlled trial of intranasal oxytocin as an adjunct to exposure therapy for social anxiety disorder. Psychoneuroendocrinology. 34:917-923.
83. Elford RC, Nathan PJ, Auyeung B, Mogg K, Brad1ey BP, Sule A et al. Effects of oxytocin on attention to emotional faces in healthy volunteers and highly socially anxious males. Int J Neuropsychopharmacol 2014; 18: 1-11.
84. Alvares GA, Chen NTM, Balleine BW, Hickie IB, Guastella AJ (2012): Oxytocin selectively moderates negative cognitive appraisals in high trait anxious males. Psychoneuroendocrinology. 37: 2022-2031.
85. Fisher RA (1935). The design of experiments.
86. LeDoux JE (2001). Emotion circuits in the brain. The Science of Mental Health: Fear and anxiety 259.
87. Seeley WW, Menon V, Schatzberg AF, Keller J, Glover GH, Kenna H, Reiss AL, Greicius MD (2007). Dissociable intrinsic connectivity networks for salience processing and executive control. The Journal of neuroscience 27, 2349-2356.
88. Domes G, Heinrichs M, Glascher J, Biichel C, Braus DF, Herpertz SC (2007). Oxytocin attenuates amygdala responses to emotional faces regard1ess of valence. Biol. Psychiatry 62, 1187-1190.
89. Kirsch P, Esslinger C, Chen Q, Mier D, Lis S, Siddhanti S, Gruppe H, Mattay VS, Gallhofer B, Meyer-Lindenberg A (2005). Oxytocin modulates neural circuitry for social cognition and fear in humans. The Journal of neuroscience 25, 11489-11493.
90. Domes G, Lischke A, Berger C, Grossmann A, Hauenstein K, Heinrichs M, Herpertz SC (2010). Effects of intranasal oxytocin on emotional face processing in women. Psychoneuroendocrinology 35, 83-93.
91. Gamer M, Zurowski B, Buchel С (2010). Different amygdala subregions mediate valence-related and attentional effects of oxytocin in humans. PNAS 107, 9400-9405.
92. Paloyelis Y, Doyle OM, Zelaya FO, Maltezos S, Williams SC, Fotopoulou A, Howard MA (2014). A Spatiotemporal Profile of in vivo Cerebral Blood Flow Changes Following Intranasal Oxytocin in Humans. Biol. Psychiatry.
93. Sripada CS, Phan KL, Labuschagne I, Welsh R, Nathan PJ, Wood AG, (2013). Oxytocin enhances resting-state connectivity between amygdala and medial frontal cortex. The International Journal of Neuropsychopharmacology 16, 255-260.
94. Salvador R, Sarro S, Gomar JJ, J, Vila F, Capdevila A, Bullmore E, McKenna PJ, E (2010). Overall brain connectivity maps show abnormalities in schizophrenia. Hum. Brain Mapp. 31, 2003-2014.
95. Lapidus KA, Levitch CF, Perez AM, Brallier JW, Parides MK, Soleimani L, et al (2014): A Randomized Controlled Trial of Intranasal Ketamine in Major Depressive Disorder. Biol Psychiatry.
96. Ebert A, Kolb M, Heller J, Edel M-A, Roser P, Brtine M (2013): Modulation of interpersonal trust in borderline personality disorder by intranasal oxytocin and childhood trauma. Soc Neurosci. 8: 305-313.
97. Klackl J, Pfundmair M, Agroskin D, Jonas E (2013): Who is to blame? Oxytocin promotes nonpersonalistic attributions in response to a trust betrayal. Biol Psychol. 92: 387-394.
98. Akerlund M, Bossmar T, Brouard R, Kostrzewska A, Laudanski T, Lemancewicz A, et al (1999): Receptor binding of oxytocin and vasopressin antagonists and inhibitory effects on isolated myometrium from preterm and term pregnant women. В JOG: An International Journal of Obstetrics & Gynaecology. 106: 1047-1053.
99. Manning M, Misicka A, Olma A, Bankowski K, Stoev S, Chini B, et al (2012): Oxytocin and vasopressin agonists and antagonists as research tools and potential therapeutics. J Neuroendocrinal. 24: 609-628.
100. Parker KJ, Buckmaster CL, Schatzberg AF, Lyons DM (2005): Intranasal oxytocin administration attenuates the ACTH stress response in monkeys. Psychoneuroendocrinology. 30: 924-929.
101. Calcagnoli F, Meyer N, de Boer SF, Althaus M, Koolhaas JM (2014): Chronic enhancement of brain oxytocin levels causes enduring anti-aggressive and pro-social explorative behavioral effects in male rats. Horm Behav. 65: 427-433.
102. McGregor IS, Bowen MT (2012): Breaking the loop: oxytocin as a potential treatment for drug addiction. Horm Behav. 61: 331-339.
103. Quintana DS, Guastella AJ, Westlye LT, Andreassen OA (in press): The promise and pitfalls of intranasally administering psychopharmacological agents for the treatment of psychiatric disorders. Mol Psychiatry.
104. McEwen BB (2004): Brain-fluid barriers: relevance for theoretical controversies regarding vasopressin and oxytocin memory research. Adv Pharmacol. 50: 531-592.
105. Pardridge WM (1998): CNS drug design based on principles of barrier transport. J Neurochem. 70: 1781-1792.
106. Fjellestad-Paulsen A, C, Lundin S (1995): Metabolism of vasopressin, oxytocin, and their analogues in the human gastrointestinal tract. Peptides. 16: 1141-1147.
107. Leng G, Ludwig M (2015): Intranasal oxytocin: myths and delusions. Biol Psychiatry.
108. Quintana DS, Alvares GA, Hickie IB, Guastella AJ (2015): Do delivery routes of intranasally administered oxytocin account for observed effects on social cognition and behavior? A two-level model. Neurosci Biobehav Rev. 49: 182-192.
109. Quintana DS, Woolley JD (2015): Intranasal oxytocin mechanisms can be better understood but its effects on social cognition and behavior are not to be sniffed at. Biol Psychiatry.
110. Guastella AJ, Hickie IB (2015): Oxytocin treatment, circuitry and autism: a critical review of the literature placing oxytocin into the autism context. Biol Psychiatry.
111. Yamasue H (2015): Promising evidence and remaining issues regarding the clinical application of oxytocin in autism spectrum disorders. Psychiatry Clin Neurosci.
112. Quintana DS, Westlye LT, Rustan ∅G, Tesli N, Poppy CL, Smevik H, et al. (2015): Low dose oxytocin delivered intranasally with Breath Powered device affects social-cognitive behavior: a randomized 4-way crossover trial with nasal cavity dimension assessment. Translational Psychiatry. 5: 1-9.
113. Ousdal O, Jensen J, Server A, Hariri A, Nakstad P, Andreassen О (2008): The human amygdala is involved in general behavioral relevance detection: evidence from an event-related functional magnetic resonance imaging Go-NoGo task. Neuroscience. 156: 450-455.
114. Labuschagne I, Phan KL, Wood A, Angstadt M, Chua P, Heinrichs M, et al. (2010): Oxytocin Attenuates Amygdala Reactivity to Fear in Generalized Social Anxiety Disorder. Neuropsychopharmacology. 35: 2403-2413.
115. Petrovic P, Kalisch R, Singer T, Dolan RJ (2008): Oxytocin Attenuates Affective Evaluations of Conditioned Faces and Amygdala Activity. J Neurosci. 28: 6607-6615.
116. Riem MM, Bakermans-Kranenburg MJ, Pieper S, Tops M, Boksem MA, Vermeiren RR, et al. (2011): Oxytocin modulates amygdala, insula, and inferior frontal gyrus responses to infant crying: a randomized controlled trial. Biol Psychiatry. 70: 291-297.
117. Riem MM, van IJzendoora MH, Tops M, Boksem MA, Rombouts SA, Bakermans-Kranenburg MJ (2012): No laughing matter: intranasal oxytocin administration changes functional brain connectivity during exposure to infant laughter. Neuropsychopharmacology. 37: 1257-1266.
118. Kemp AH, Guastella AJ (2011): The role of oxytocin in human affect a novel hypothesis. Current Directions in Psychological Science. 20: 222-231.
119. Brad1ey MM, Miccoli L, Escrig MA, Lang PJ (2008): The pupil as a measure of emotional arousal and autonomic activation. Psychophysiology. 45: 602-607.
120. Prehn K, Heekeren HR, Van der Meer E (2011): Influence of affective significance on different levels of processing using pupil dilation in an analogical reasoning task. Int J Psychophysiol. 79: 236-243.
121. Prehn K, Kazzer P, Lischke A, Heinrichs M, Herpertz SC, Domes G (2013): Effects of intranasal oxytocin on pupil dilation indicate increased salience of socioaffective stimuli. Psychophysiology. 50: 528-537.
122. Djupesland PG, Mahmoud RA, Messina JC (2013): Accessing the brain: the nose may know the way. Journal of Cerebral Blood Flow & amp; amp; Metabolism. 33: 793-794.
123. Fischl B, Salat DH, Busa E, Albert M, Dieterich M, Haselgrove C, et al. (2002): Whole brain segmentation: automated labeling of neuroanatomical structures in the human brain. Neuron. 33: 341-355.
124. Jenkinson M, Bannister P, Brady M, Smith S (2002): Improved optimization for the robust and accurate linear registration and motion correction of brain images. Neuroimage. 17: 825-841.
125. Smith SM, Brady JM (1997): SUSAN - A new approach to low level image processing. International journal of computer vision. 23: 45-78.
126. Beckmann CF, Smith SM (2004): Probabilistic independent component analysis for functional magnetic resonance imaging. Medical Imaging, IEEE Transactions on. 23: 137-152.
127. Greve DN, Fischl В (2009): Accurate and robust brain image alignment using boundary-based registration. Neuroimage. 48: 63-72.
128. Woolrich MW, Ripley BD, Brady M, Smith SM (2001): Temporal autocorrelation in univariate linear modeling of FMRI data. Neuroimage. 14: 1370-1386.
129. Smith SM, Jenkinson M, Woolrich MW, Beckmann CF, Behrens ТЕ, Johansen-Berg H, et al. (2004): Advances in functional and structural MR image analysis and implementation as FSL. Neuroimage. 23:S208-S219.
130. Jeffreys H (1998): The theory of probability. Oxford, UK: Oxford University Press.
131. Veinante P, Freund-Mercier MJ (1997): Distribution of vasopressin - binding sites in the rat extended amygdala: a histoautoradiographic study. JCompNeurol. 383: 305-325.
132. Insel TR, Shapiro LE (1992): Oxytocin receptor distribution reflects social organization in monogamous and polygamous voles. Proceedings of the National Academy of Sciences. 89: 5981-5985.
133. Huber D, Veinante P, Stoop R (2005): Vasopressin and oxytocin excite distinct neuronal populations in the central amygdala. Science. 308: 245-248.
134. Knobloch HS, Charlet A, Hoffmann LC, Eliava M, Khrulev S, Cetin AH, et al. (2012): Evoked axonal oxytocin release in the central amygdala attenuates fear response. Neuron. 73: 553-566.
135. Thorne RG, Pronk GJ, Padmanabhan V, Frey I, W H (2004): Delivery of insulinlike growth factor-I to the rat brain and spinal cord along olfactory and trigeminal pathways following intranasal administration. Neuroscience. 127: 481-496.
136. Ikemoto S (2007): Dopamine reward circuitry: Two projection systems from the ventral midbrain to the nucleus accumbens-olfactory tubercle complex. Brain Research Reviews. 56: 27-78.
137. Kang N, Baum MJ, Cherry JA (2011): Different Profiles of Main and Accessory Olfactory Bulb Mitral/Tufted Cell Projections Revealed in Mice Using an Anterograde Tracer and a Whole-Mount, Flattened Cortex Preparation. Chem Senses. 36: 251-260.
138. Sosulski DL, Bloom ML, Cutforth T, Axel R, Datta SR (2012): Distinct representations of olfactory information in different cortical centres. Nature. 472: 213-216.
139. Neumann ID, Maloumby R, Beiderbeck Dl, Lukas M, Landgraf R (2013): Increased brain and plasma oxytocin after nasal and peripheral administration in rats and mice. Psychoneuroendocrinology. 38: 1985-1993.
140. Mens WB, Witter A, Van Wimersma Greidanus ТВ (1983): Penetration of neurohypophyseal hormones from plasma into cerebrospinal fluid (CSF): half-times of disappearance of these neuropeptides from CSF. Brain Res. 262: 143-149.
141. Modi ME, Connor-Stroud F, Landgraf R, Young LJ, Parr LA (2014): Aerosolized oxytocin increases cerebrospinal fluid oxytocin in rhesus macaques. Psychoneuroendocrinology. 45: 49-57.
142. Gouin J-P, Carter CS, Pournajafi-Nazarloo H, Glaser R, Malarkey WB, Loving TJ, et al. (2010): Marital behavior, oxytocin, vasopressin, and wound healing. Psychoneuroendocrinology. 35: 1082-1090.
143. Rodrigues SM, Saslow LR, Garcia N, John OP, Keltner D (2009): Oxytocin receptor genetic variation relates to empathy and stress reactivity in humans. Proceedings of the National Academy of Sciences. 106: 21437-21441.
Claims (41)
1. Наконечник для носа для доставки вещества в носовую полость субъекта, содержащий:
первую, внутреннюю корпусную часть и
вторую, внешнюю корпусную часть, которая расположена по меньшей мере вокруг дистальной области внутренней корпусной части и образует концевой элемент;
где внутренняя корпусная часть содержит основание, которое содержит проточный канал, и выступ в форме лезвия в дистальном конце, который поддерживает концевой элемент и придает жесткость в сагиттальном направлении, что позволяет концевому элементу раскрывать мясистую ткань в верхней области носового клапана и, таким образом, увеличивать площадь сечения раскрытого носового клапана, а также гибкость в боковом направлении, перпендикулярном сагиттальной плоскости, которая облегчает введение концевого элемента в носовой клапан.
2. Наконечник для носа по п. 1, отличающийся тем, что внутренняя корпусная часть выполнена из пластикового материала.
3. Наконечник для носа по п. 1, отличающийся тем, что внешняя корпусная часть выполнена из упругого материала.
4. Наконечник для носа по п. 3, отличающийся тем, что внешняя корпусная часть выполнена из термопластичного эластомера (TPE).
5. Наконечник для носа по п. 1, отличающийся тем, что основание на своем дистальном конце имеет по существу кольцевую поверхность, которая сужается или имеет наклон относительно продольной оси наконечника для носа, таким образом, поверхность основания проходит с наклоном по направлению от выступа в проксимальном направлении, и основание является более коротким с той стороны, которая расположена напротив выступа.
6. Наконечник для носа по п. 1, отличающийся тем, что выступ проходит в осевом направлении по существу параллельно продольной оси наконечника для носа и вынесен за указанную ось.
7. Наконечник для носа по п. 1, отличающийся тем, что выступ имеет длину (d1) в сагиттальном направлении, которая превышает длину (d2) в боковом направлении.
8. Наконечник для носа по п. 7, отличающийся тем, что длина (d1) в сагиттальном направлении в 1,5 раза превышает среднюю длину (d2) в боковом направлении.
9. Наконечник для носа по п. 7, отличающийся тем, что длина (d1) в сагиттальном направлении в 1,7 раза превышает среднюю длину (d2) в боковом направлении.
10. Наконечник для носа по п. 7, отличающийся тем, что длина (d1) в сагиттальном направлении в 1,9 раза превышает среднюю длину (d2) в боковом направлении.
11. Наконечник для носа по п. 7, отличающийся тем, что длина (d1) в сагиттальном направлении в 2 раза превышает среднюю длину (d2) в боковом направлении.
12. Наконечник для носа по п. 7, отличающийся тем, что выступ имеет длину (d1) в сагиттальном направлении менее 3 мм или менее 2,5 мм.
13. Наконечник для носа по п. 7, отличающийся тем, что выступ имеет длину (d1) в сагиттальном направлении более 1,5 мм.
14. Наконечник для носа по п. 7, отличающийся тем, что выступ имеет длину (d2) в боковом направлении менее 1,5 мм или менее 1,25 мм.
15. Наконечник для носа по п. 7, отличающийся тем, что выступ имеет длину (d2) в боковом направлении более 0,5 мм или более 0,75 мм.
16. Наконечник для носа по п. 7, отличающийся тем, что выступ имеет секцию основного корпуса и секцию наконечника, которая имеет меньшую длину (d3) в сагиттальном направлении по сравнению с длиной (d1) секции основного корпуса.
17. Наконечник для носа по п. 7, отличающийся тем, что выступ имеет боковое поперечное сечение, сужающееся вдоль длины, где длина (d2) в боковом направлении сокращается в поперечном сечении вдоль длины выступа в направлении к дистальному концу.
18. Наконечник для носа по п. 1, отличающийся тем, что концевой элемент наконечника для носа при введении в носовой клапан расширяет его до площади поперечного сечения в 1,5 раза, 1,75 раза или 2,0 раза большей по сравнению с площадью поперечного сечения носового клапана в нерасширенном состоянии.
19. Наконечник для носа для доставки вещества в носовую полость субъекта, содержащий корпусную часть, содержащую основание, которое содержит проточный канал, и выступ в форме лезвия в дистальном конце, в котором находится по меньшей мере отчасти концевой элемент наконечника для носа и который придает жесткость в сагиттальном направлении, что позволяет концевому элементу раскрывать мясистую ткань в верхней области носового клапана и, таким образом, увеличивать площадь сечения раскрытого носового клапана, а также гибкость в боковом направлении, перпендикулярном сагиттальной плоскости, которая облегчает введение концевого элемента в носовой клапан.
20. Наконечник для носа по п. 19, отличающийся тем, что корпусная часть выполнена из пластикового материала.
21. Наконечник для носа по п. 19, дополнительно содержащий внешнюю корпусную часть, расположенную по меньшей мере вокруг выступа.
22. Наконечник для носа по п. 21, отличающийся тем, что внешняя корпусная часть выполнена из упругого материала.
23. Наконечник для носа по п. 22, отличающийся тем, что внешняя корпусная часть выполнена из термопластичного эластомера (TPE).
24. Наконечник для носа по п. 19, отличающийся тем, что основание на своем дистальном конце имеет по существу кольцевую поверхность, которая сужается или имеет наклон относительно продольной оси наконечника для носа, таким образом, поверхность основания проходит с наклоном по направлению от выступа в проксимальном направлении, и основание является более коротким с той стороны, которая расположена напротив выступа.
25. Наконечник для носа по п. 19, отличающийся тем, что выступ проходит в осевом направлении по существу параллельно продольной оси наконечника для носа и вынесен за указанную ось.
26. Наконечник для носа по п. 19, отличающийся тем, что выступ имеет длину (d1) в сагиттальном направлении, которая превышает длину (d2) в боковом направлении.
27. Наконечник для носа по п. 26, отличающийся тем, что длина (d1) в сагиттальном направлении в 1,5 раза превышает среднюю длину (d2) в боковом направлении.
28. Наконечник для носа по п. 26, отличающийся тем, что длина (d1) в сагиттальном направлении в 1,7 раза превышает среднюю длину (d2) в боковом направлении.
29. Наконечник для носа по п. 26, отличающийся тем, что длина (d1) в сагиттальном направлении в 1,9 раза превышает среднюю длину (d2) в боковом направлении.
30. Наконечник для носа по п. 26, отличающийся тем, что длина (d1) в сагиттальном направлении в 2 раза превышает среднюю длину (d2) в боковом направлении.
31. Наконечник для носа по п. 26, отличающийся тем, что выступ имеет длину (d1) в сагиттальном направлении менее 3 мм или менее 2,5 мм.
32. Наконечник для носа по п. 26, отличающийся тем, что выступ имеет длину (d1) в сагиттальном направлении более 1,5 мм.
33. Наконечник для носа по п. 26, отличающийся тем, что выступ имеет длину (d2) в боковом направлении менее 1,5 мм или менее 1,25 мм.
34. Наконечник для носа по п. 26, отличающийся тем, что выступ имеет длину (d2) в боковом направлении более 0,5 мм или более 0,75 мм.
35. Наконечник для носа по п. 26, отличающийся тем, что выступ имеет секцию основного корпуса и секцию наконечника, которая имеет меньшую длину (d3) в сагиттальном направлении по сравнению с длиной (d1) секции основного корпуса
36. Наконечник для носа по п. 26, отличающийся тем, что выступ имеет боковое поперечное сечение, сужающееся вдоль длины, где длина (d2) в боковом направлении сокращается в поперечном сечении вдоль длины выступа в направлении к дистальному концу.
37. Наконечник для носа по п. 19, отличающийся тем, что концевой элемент наконечника для носа при введении в носовой клапан расширяет его до площади поперечного сечения в 1,5 раза, 1,75 раза или 2,0 раза большей по сравнению с площадью поперечного сечения носового клапана в нерасширенном состоянии.
38. Устройство для интраназальной доставки, содержащее наконечник для носа по любому из пп. 1-37.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462081742P | 2014-11-19 | 2014-11-19 | |
| US62/081,742 | 2014-11-19 | ||
| PCT/EP2015/077166 WO2016079271A1 (en) | 2014-11-19 | 2015-11-19 | Intranasal administration |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2017114951A RU2017114951A (ru) | 2018-12-19 |
| RU2017114951A3 RU2017114951A3 (ru) | 2019-04-16 |
| RU2714168C2 true RU2714168C2 (ru) | 2020-02-12 |
Family
ID=54695714
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2017114950A RU2017114950A (ru) | 2014-11-19 | 2015-11-19 | Интраназальное введение |
| RU2017114951A RU2714168C2 (ru) | 2014-11-19 | 2015-11-19 | Интраназальное введение |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2017114950A RU2017114950A (ru) | 2014-11-19 | 2015-11-19 | Интраназальное введение |
Country Status (18)
| Country | Link |
|---|---|
| US (5) | US11052204B2 (ru) |
| EP (3) | EP3733235B1 (ru) |
| JP (2) | JP6937690B2 (ru) |
| KR (2) | KR20170086599A (ru) |
| CN (3) | CN107106792B (ru) |
| AU (2) | AU2015348297A1 (ru) |
| BR (2) | BR112017010561A2 (ru) |
| CA (2) | CA2966797C (ru) |
| DK (2) | DK3220989T3 (ru) |
| ES (3) | ES2813442T3 (ru) |
| HK (2) | HK1244728A1 (ru) |
| IL (2) | IL251935A0 (ru) |
| MX (2) | MX2017006265A (ru) |
| MY (1) | MY188242A (ru) |
| RU (2) | RU2017114950A (ru) |
| SG (2) | SG11201703794TA (ru) |
| WO (2) | WO2016079267A1 (ru) |
| ZA (1) | ZA201704149B (ru) |
Families Citing this family (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0311570D0 (en) | 2003-05-20 | 2003-06-25 | Optinose As | Delivery device and method |
| GB0320171D0 (en) | 2003-08-28 | 2003-10-01 | Optinose As | Delivery devices |
| GB0420513D0 (en) | 2004-09-15 | 2004-10-20 | Optinose As | Powder delivery devices |
| GB0503738D0 (en) | 2005-02-23 | 2005-03-30 | Optinose As | Powder delivery devices |
| GB0604444D0 (en) * | 2006-03-06 | 2006-04-12 | Optinose As | Nasal devices |
| GB0605799D0 (en) | 2006-03-23 | 2006-05-03 | Optinose As | Nasal delivery devices |
| GB2438834A (en) | 2006-06-08 | 2007-12-12 | Optinose As | Intranasal protein administration |
| GB2440316A (en) | 2006-07-25 | 2008-01-30 | Optinose As | Nasal inhaler with scrubber |
| GB0623731D0 (en) | 2006-11-28 | 2007-01-10 | Optinose As | Delivery device |
| GB0623732D0 (en) | 2006-11-28 | 2007-01-10 | Optinose As | Powder delivery devices |
| GB0623728D0 (en) | 2006-11-28 | 2007-01-10 | Optinose As | Delivery devices |
| GB2448193A (en) | 2007-04-05 | 2008-10-08 | Optinose As | Nasal delivery device |
| GB2448183A (en) | 2007-04-05 | 2008-10-08 | Optinose As | Nasal powder delivery device |
| GB0719299D0 (en) | 2007-10-03 | 2007-11-14 | Optinose As | Nasal delivery devices |
| US9949923B2 (en) | 2011-03-15 | 2018-04-24 | Optinose As | Nasal delivery |
| PL2817052T3 (pl) | 2012-02-24 | 2018-01-31 | Optinose As | Urządzenia do podawania donosowego |
| USD761951S1 (en) | 2013-05-23 | 2016-07-19 | Optinose As | Nosepiece unit |
| CN107106792B (zh) | 2014-11-19 | 2020-08-18 | 奥普蒂诺斯公司 | 经鼻给药 |
| US10368502B2 (en) | 2017-09-25 | 2019-08-06 | Multiple Energy Technologies Llc | Bioceramic and carbon-based hydroponic systems, methods and devices |
| EP3773834A4 (en) | 2018-04-12 | 2021-12-22 | Rocket Science Health Corp. | DEVICE, SYSTEM AND METHOD FOR INTRANASAL DRUG ADMINISTRATION |
| KR102148613B1 (ko) * | 2019-01-28 | 2020-10-14 | 닉스 주식회사 | 이산화탄소를 이용한 수면 유도시스템 |
| CN110188836B (zh) * | 2019-06-21 | 2021-06-11 | 西安交通大学 | 一种基于变分自编码器的脑功能网络分类方法 |
| US20220313895A1 (en) * | 2019-08-14 | 2022-10-06 | Gsk Consumer Healthcare Sarl | Bi-material nozzle for nasal washes |
| CA3152988A1 (en) * | 2019-08-29 | 2021-03-04 | New York University | Oxytocin compositions for treatment of tinnitus |
| US20220161000A1 (en) * | 2020-11-24 | 2022-05-26 | Medtronic, Inc. | Multi-durometer attachment device for chronic fixation |
| CN114306207A (zh) * | 2021-12-30 | 2022-04-12 | 电子科技大学 | 一种以棒棒糖为载体的口腔给药方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09135901A (ja) * | 1995-11-15 | 1997-05-27 | Unisia Jecs Corp | 鼻腔用投薬器 |
| RU2383358C2 (ru) * | 2005-10-04 | 2010-03-10 | Омрон Хэлткэа Ко., Лтд. | Ингалятор и мундштук ингалятора |
| US20100282246A1 (en) * | 2007-04-05 | 2010-11-11 | Optinose As | Nasal delivery |
| RU112044U1 (ru) * | 2011-08-25 | 2012-01-10 | Наиль Минрахманович Нуртдинов | Тренажер-ингалятор |
| US8550073B2 (en) * | 2006-03-06 | 2013-10-08 | Optinose As | Nasal delivery |
Family Cites Families (66)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US605436A (en) | 1898-06-07 | Inhaler | ||
| US642748A (en) | 1899-02-23 | 1900-02-06 | Arthur Manners | Inhaler. |
| US658436A (en) | 1900-05-28 | 1900-09-25 | Hans Hennerich Groth | Insufflator. |
| US746749A (en) | 1903-03-18 | 1903-12-15 | George E Seidel | Nasal medicator. |
| US794641A (en) | 1905-03-06 | 1905-07-11 | Alfred H Ramey | Inhaler. |
| US902832A (en) | 1907-09-20 | 1908-11-03 | Edward F Philbrook | Inhaler. |
| EP0805696B1 (en) | 1995-01-23 | 2000-03-15 | Direct-Haler A/S | An inhaler |
| US5901703A (en) | 1995-02-06 | 1999-05-11 | Unisia Jecs Corporation | Medicine administering device for nasal cavities |
| US5797392C1 (en) | 1996-01-22 | 2001-01-09 | Direct Haler As | Inhaler |
| BR9809499A (pt) | 1997-05-27 | 2000-06-20 | Direct Haler A S | Inalador para medicamentos em pó |
| GB9719775D0 (en) * | 1997-09-18 | 1997-11-19 | Glaxo Group Ltd | Device |
| FR2771296B1 (fr) | 1997-11-25 | 2000-03-10 | Sofab | Embout nasal avec fermeture d'extremite |
| GB0121568D0 (en) | 2001-09-06 | 2001-10-24 | Optinose As | Nasal delivery device |
| GB0114272D0 (en) | 2001-06-12 | 2001-08-01 | Optinose As | Nasal delivery device |
| DE60045216D1 (de) | 1999-03-03 | 2010-12-23 | Optinose As | Nasales Verabreichungsgerät |
| US6894026B1 (en) | 2000-01-11 | 2005-05-17 | Atossa Healthcare, Inc. | Long-acting oxytocin analogues for the treatment and prevention of breast cancer and psychiatric disorders |
| US20070032410A1 (en) | 2000-01-11 | 2007-02-08 | Atossa Healthcare, Inc. | Compositions and methods for the treatment of psychiatric disorders |
| GB0015309D0 (en) | 2000-06-21 | 2000-08-16 | Djupesland Per G | Apparatus |
| ZA200306564B (en) | 2001-02-26 | 2004-10-15 | Optinose As | Nasal devices. |
| GB0207422D0 (en) | 2002-03-28 | 2002-05-08 | Optinose As | Nasal devices |
| GB0207817D0 (en) | 2002-04-04 | 2002-05-15 | Optinose As | Nasal devices |
| GB0209494D0 (en) | 2002-04-25 | 2002-06-05 | Optinose As | Nasal devices |
| GB0215270D0 (en) | 2002-07-02 | 2002-08-14 | Optinose As | Nasal devices |
| GB0215904D0 (en) | 2002-07-09 | 2002-08-21 | Team Holdings Uk Ltd | Drug delivery system and method |
| GB0300008D0 (en) | 2003-01-02 | 2003-02-05 | Optinose As | Delivery devices |
| GB2400565B (en) | 2003-04-17 | 2005-03-02 | Bespak Plc | Nasal drug delivery |
| GB0311570D0 (en) | 2003-05-20 | 2003-06-25 | Optinose As | Delivery device and method |
| GB0319119D0 (en) | 2003-08-14 | 2003-09-17 | Optinose As | Delivery devices |
| GB0320171D0 (en) | 2003-08-28 | 2003-10-01 | Optinose As | Delivery devices |
| GB0405477D0 (en) | 2004-03-11 | 2004-04-21 | Glaxo Group Ltd | A fluid dispensing device |
| USD530815S1 (en) | 2004-03-19 | 2006-10-24 | Optinose As | Nasal delivery device |
| GB0420513D0 (en) | 2004-09-15 | 2004-10-20 | Optinose As | Powder delivery devices |
| GB0503738D0 (en) | 2005-02-23 | 2005-03-30 | Optinose As | Powder delivery devices |
| US20090317377A1 (en) | 2005-08-26 | 2009-12-24 | Yeomans David C | Therapy procedure for drug delivery for trigeminal pain |
| AU2006335994A1 (en) | 2006-01-19 | 2007-07-26 | Optinose As | Nasal administration |
| GB0602980D0 (en) | 2006-02-14 | 2006-03-29 | Optinose As | Delivery device and method |
| GB2434990B (en) | 2006-02-14 | 2010-12-01 | Optinose As | Delivery device and method |
| GB0604319D0 (en) | 2006-03-03 | 2006-04-12 | Optinose As | Nasal delivery |
| GB0605799D0 (en) | 2006-03-23 | 2006-05-03 | Optinose As | Nasal delivery devices |
| GB2437488A (en) | 2006-04-25 | 2007-10-31 | Optinose As | Pharmaceutical oily formulation for nasal or buccal administration |
| GB2438834A (en) | 2006-06-08 | 2007-12-12 | Optinose As | Intranasal protein administration |
| GB2440316A (en) | 2006-07-25 | 2008-01-30 | Optinose As | Nasal inhaler with scrubber |
| JP2008062974A (ja) | 2006-09-07 | 2008-03-21 | Mitani Valve Co Ltd | 内容物放出用容器ならびに、この内容物放出用容器を備えたポンプ式製品およびエアゾール式製品 |
| GB0623731D0 (en) | 2006-11-28 | 2007-01-10 | Optinose As | Delivery device |
| GB0623732D0 (en) | 2006-11-28 | 2007-01-10 | Optinose As | Powder delivery devices |
| GB0623728D0 (en) | 2006-11-28 | 2007-01-10 | Optinose As | Delivery devices |
| US20100199984A1 (en) | 2007-04-02 | 2010-08-12 | Abbott Laboratories | Breath actuated nasal pump |
| GB2448183A (en) | 2007-04-05 | 2008-10-08 | Optinose As | Nasal powder delivery device |
| US8342173B2 (en) | 2007-07-19 | 2013-01-01 | Silver Eagle Labs Inc. | Nasal dilator with cushion layer and variable spring rate |
| GB0719299D0 (en) | 2007-10-03 | 2007-11-14 | Optinose As | Nasal delivery devices |
| ES2648196T3 (es) | 2008-02-07 | 2017-12-29 | The University Of Washington | Dispositivo aerosol circunferencial |
| CA2715302A1 (en) | 2008-02-15 | 2009-08-20 | Timothy Sean Immel | Aerosol therapy device with high frequency delivery |
| US20110318345A1 (en) | 2008-09-15 | 2011-12-29 | Optinose As | Nasal delivery |
| GB201015371D0 (en) | 2010-09-14 | 2010-10-27 | Optinose As | Nasal delivery |
| GB201020638D0 (en) | 2010-12-06 | 2011-01-19 | Liconsa Laboratorios Sa | Inhalator |
| US9949923B2 (en) | 2011-03-15 | 2018-04-24 | Optinose As | Nasal delivery |
| IN2014DN07610A (ru) | 2012-02-24 | 2015-05-15 | Optinose As | |
| EP2817054B1 (en) | 2012-02-24 | 2019-12-04 | Optinose AS | Nasal delivery devices |
| PL2817052T3 (pl) * | 2012-02-24 | 2018-01-31 | Optinose As | Urządzenia do podawania donosowego |
| US11554229B2 (en) | 2013-03-26 | 2023-01-17 | OptiNose Inc. | Nasal administration |
| CA2908232A1 (en) * | 2013-03-26 | 2014-10-02 | Optinose As | Nasal administration of fluticasone and carbon dioxide |
| USD761951S1 (en) | 2013-05-23 | 2016-07-19 | Optinose As | Nosepiece unit |
| USD725769S1 (en) | 2013-05-23 | 2015-03-31 | Optinose As | Nasal delivery device |
| USD723156S1 (en) | 2013-05-23 | 2015-02-24 | Optinose As | Nasal delivery device |
| CN107106792B (zh) | 2014-11-19 | 2020-08-18 | 奥普蒂诺斯公司 | 经鼻给药 |
| US20220296825A1 (en) | 2018-10-04 | 2022-09-22 | Optinose As | Exhalation delivery system for and method of treating sinus disease |
-
2015
- 2015-11-19 CN CN201580062178.1A patent/CN107106792B/zh active Active
- 2015-11-19 MX MX2017006265A patent/MX2017006265A/es unknown
- 2015-11-19 ES ES15798061T patent/ES2813442T3/es active Active
- 2015-11-19 ES ES20181431T patent/ES2949052T3/es active Active
- 2015-11-19 CA CA2966797A patent/CA2966797C/en active Active
- 2015-11-19 WO PCT/EP2015/077162 patent/WO2016079267A1/en active Application Filing
- 2015-11-19 RU RU2017114950A patent/RU2017114950A/ru not_active Application Discontinuation
- 2015-11-19 AU AU2015348297A patent/AU2015348297A1/en not_active Abandoned
- 2015-11-19 US US14/946,389 patent/US11052204B2/en active Active
- 2015-11-19 MY MYPI2017701760A patent/MY188242A/en unknown
- 2015-11-19 KR KR1020177016766A patent/KR20170086599A/ko unknown
- 2015-11-19 EP EP20181431.6A patent/EP3733235B1/en active Active
- 2015-11-19 CA CA2966802A patent/CA2966802C/en active Active
- 2015-11-19 EP EP15798061.6A patent/EP3220989B1/en active Active
- 2015-11-19 RU RU2017114951A patent/RU2714168C2/ru active
- 2015-11-19 BR BR112017010561A patent/BR112017010561A2/pt not_active Application Discontinuation
- 2015-11-19 CN CN201580062083.XA patent/CN106999684B/zh active Active
- 2015-11-19 EP EP15798058.2A patent/EP3220988B1/en active Active
- 2015-11-19 SG SG11201703794TA patent/SG11201703794TA/en unknown
- 2015-11-19 JP JP2017526941A patent/JP6937690B2/ja active Active
- 2015-11-19 ES ES15798058T patent/ES2906984T3/es active Active
- 2015-11-19 CN CN202010816000.4A patent/CN111921046B/zh active Active
- 2015-11-19 US US14/946,442 patent/US10940277B2/en active Active
- 2015-11-19 MX MX2017006268A patent/MX2017006268A/es unknown
- 2015-11-19 KR KR1020177016768A patent/KR20170085121A/ko not_active Application Discontinuation
- 2015-11-19 SG SG11201703792XA patent/SG11201703792XA/en unknown
- 2015-11-19 DK DK15798061.6T patent/DK3220989T3/da active
- 2015-11-19 BR BR112017010522-5A patent/BR112017010522B1/pt not_active IP Right Cessation
- 2015-11-19 WO PCT/EP2015/077166 patent/WO2016079271A1/en active Application Filing
- 2015-11-19 DK DK15798058.2T patent/DK3220988T3/da active
- 2015-11-19 AU AU2015348301A patent/AU2015348301B2/en active Active
- 2015-11-19 JP JP2017526959A patent/JP6990583B2/ja active Active
-
2017
- 2017-04-26 IL IL251935A patent/IL251935A0/en unknown
- 2017-04-26 IL IL251936A patent/IL251936B/en active IP Right Grant
- 2017-06-15 ZA ZA2017/04149A patent/ZA201704149B/en unknown
-
2018
- 2018-03-26 HK HK18104118.9A patent/HK1244728A1/zh unknown
- 2018-03-26 HK HK18104123.2A patent/HK1244729A1/zh unknown
-
2021
- 2021-01-29 US US17/162,475 patent/US11707586B2/en active Active
- 2021-06-04 US US17/338,962 patent/US11730904B2/en active Active
-
2023
- 2023-06-05 US US18/205,580 patent/US20230372647A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09135901A (ja) * | 1995-11-15 | 1997-05-27 | Unisia Jecs Corp | 鼻腔用投薬器 |
| RU2383358C2 (ru) * | 2005-10-04 | 2010-03-10 | Омрон Хэлткэа Ко., Лтд. | Ингалятор и мундштук ингалятора |
| US8550073B2 (en) * | 2006-03-06 | 2013-10-08 | Optinose As | Nasal delivery |
| US20100282246A1 (en) * | 2007-04-05 | 2010-11-11 | Optinose As | Nasal delivery |
| RU112044U1 (ru) * | 2011-08-25 | 2012-01-10 | Наиль Минрахманович Нуртдинов | Тренажер-ингалятор |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2714168C2 (ru) | Интраназальное введение | |
| Li et al. | Foot massage evokes oxytocin release and activation of orbitofrontal cortex and superior temporal sulcus | |
| WO2020237043A1 (en) | Human tactile prepulse inhibition assay | |
| Azabou et al. | Randomized controlled study evaluating efficiency of low intensity transcranial direct current stimulation (tDCS) for dyspnea relief in mechanically ventilated COVID-19 patients in ICU: the tDCS-DYSP-COVID protocol | |
| Lin et al. | The relationship between oxytocin and empathy for others’ pain: Testing the mediating effect of first-hand pain sensitivity | |
| Almarzooqi et al. | Skin Deep: An Overlap of Delusions | |
| Abdulraouf et al. | Skin Deep: An Overlap of Delusions | |
| Saad et al. | Autism spectrum disorder (ASD) is a neurodevelopmental disorder, which affects 1 in 44 children and may cause severe disabilities. Besides socio-communicational difficulties and repetitive behaviors, ASD also presents as atypical sensorimotor function and pain reactivity. While chronic pain is a frequent co-morbidity in autism, pain management in this population is often insufficient because of difficulties in pain | |
| Dornbush | Marijuana and the central nervous system |