RU2587439C1 - Способ получения наностержней диоксида марганца - Google Patents
Способ получения наностержней диоксида марганца Download PDFInfo
- Publication number
- RU2587439C1 RU2587439C1 RU2015109828/05A RU2015109828A RU2587439C1 RU 2587439 C1 RU2587439 C1 RU 2587439C1 RU 2015109828/05 A RU2015109828/05 A RU 2015109828/05A RU 2015109828 A RU2015109828 A RU 2015109828A RU 2587439 C1 RU2587439 C1 RU 2587439C1
- Authority
- RU
- Russia
- Prior art keywords
- mno
- manganese dioxide
- nanorods
- inorganic acid
- diameter
- Prior art date
Links
- NUJOXMJBOLGQSY-UHFFFAOYSA-N manganese dioxide Chemical compound O=[Mn]=O NUJOXMJBOLGQSY-UHFFFAOYSA-N 0.000 title claims abstract description 37
- 239000002073 nanorod Substances 0.000 title claims abstract description 18
- 238000000034 method Methods 0.000 title claims description 15
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 9
- 239000012153 distilled water Substances 0.000 claims abstract description 7
- 150000007522 mineralic acids Chemical class 0.000 claims abstract description 6
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 claims abstract description 6
- 239000000725 suspension Substances 0.000 claims abstract description 5
- 239000004809 Teflon Substances 0.000 claims abstract description 4
- 229920006362 Teflon® Polymers 0.000 claims abstract description 4
- 238000010908 decantation Methods 0.000 claims abstract description 4
- 238000010438 heat treatment Methods 0.000 claims abstract description 4
- 239000002245 particle Substances 0.000 claims abstract description 4
- 239000002244 precipitate Substances 0.000 claims abstract description 4
- 238000003756 stirring Methods 0.000 claims abstract description 4
- 239000007864 aqueous solution Substances 0.000 claims abstract description 3
- 239000012286 potassium permanganate Substances 0.000 claims abstract description 3
- 235000010288 sodium nitrite Nutrition 0.000 claims abstract description 3
- 239000012670 alkaline solution Substances 0.000 claims description 2
- 238000002156 mixing Methods 0.000 claims description 2
- 239000010406 cathode material Substances 0.000 abstract description 6
- 239000000243 solution Substances 0.000 abstract description 3
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 abstract description 2
- 229910052744 lithium Inorganic materials 0.000 abstract description 2
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 abstract 1
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 abstract 1
- 239000003513 alkali Substances 0.000 abstract 1
- 229910017604 nitric acid Inorganic materials 0.000 abstract 1
- 239000000126 substance Substances 0.000 abstract 1
- 229910006648 β-MnO2 Inorganic materials 0.000 abstract 1
- 230000015572 biosynthetic process Effects 0.000 description 12
- 238000012986 modification Methods 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 6
- 239000000463 material Substances 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 239000013078 crystal Substances 0.000 description 4
- 239000012467 final product Substances 0.000 description 4
- 229910001416 lithium ion Inorganic materials 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 230000002687 intercalation Effects 0.000 description 3
- 238000009830 intercalation Methods 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 150000001768 cations Chemical class 0.000 description 2
- 238000010335 hydrothermal treatment Methods 0.000 description 2
- 238000009434 installation Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 230000000877 morphologic effect Effects 0.000 description 2
- 239000002070 nanowire Substances 0.000 description 2
- 238000004626 scanning electron microscopy Methods 0.000 description 2
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- -1 biosensors Substances 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 238000004146 energy storage Methods 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000012456 homogeneous solution Substances 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000001000 micrograph Methods 0.000 description 1
- 239000002159 nanocrystal Substances 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 229910001414 potassium ion Inorganic materials 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G45/00—Compounds of manganese
- C01G45/02—Oxides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82B—NANOSTRUCTURES FORMED BY MANIPULATION OF INDIVIDUAL ATOMS, MOLECULES, OR LIMITED COLLECTIONS OF ATOMS OR MOLECULES AS DISCRETE UNITS; MANUFACTURE OR TREATMENT THEREOF
- B82B3/00—Manufacture or treatment of nanostructures by manipulation of individual atoms or molecules, or limited collections of atoms or molecules as discrete units
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Nanotechnology (AREA)
- Inorganic Chemistry (AREA)
- Manufacturing & Machinery (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
Abstract
Изобретение может быть использовано в неорганической химии и нанотехнологии. Для получения наностержней диоксида марганца смешивают водные растворы перманганата калия и нитрита натрия в мольном соотношении
, равном 2:(1-5), до образования однородной дисперсной фазы в сильнощелочном растворе. Затем при постоянном перемешивании медленно прикапывают неорганическую кислоту до достижения значения pH 2-0,5. Полученную суспензию помещают в тефлоновый автоклав, который устанавливают в гидротермально-микроволновую установку на 5-25 мин при 90-170°C, давлении 1-20 атм и мощности микроволнового нагрева 150-1000 Вт. Полученный осадок отделяют декантацией, промывают дистиллированной водой и высушивают на воздухе при температуре не выше 70°C. Получают кристаллический пиролюзит, частицы которого имеют форму стержней диаметром свыше 10 нм и длиной до 2 мкм. В качестве неорганической кислоты используют H2SO4 или HNO3. Изобретение позволяет получать наностержни β-MnO2 для использования в литиевых источниках тока в качестве катодного материала с высокой производительностью и относительно высокой однородностью фракций по диаметру стержней. 1 з.п. ф-лы, 2 ил., 1 табл., 5 пр.
Description
Изобретение относится к неорганической химии, конкретно к получению нанокристаллического диоксида марганца, полиморфные модификации которого, имеющие разнообразные морфологические формы, могут быть успешно использованы в составе катализаторов, биосенсоров, адсорбентов и особенно в источниках тока.
Основными структурными единицами полиморфных модификаций диоксида марганца являются октаэдры MnO6, различное взаимное сочленение которых приводит к формированию в структуре MnO2 слоев и каналов. Именно наличие каналов делает MnO2 интересным с точки зрения создания катодных материалов. Наименьшее содержание примесей в MnO2 характерно для пиролюзита (β-MnO2) и рамсделита (γ-MnO2). Для других модификаций MnO2 (α, λ, ε и δ) крайне характерно присутствие в их кристаллической структуре ионов Na+и K+.
В настоящее время актуальной задачей является разработка методов получения наностержней MnO2 β-модификации, представляющих большой практический интерес, ввиду того, что характерная для них анизотропия проводимости может приводить к появлению принципиально новых конструктивных решений при создании аккумуляторных элементов [Xu M.-W., Bao S.-J. // Energy Storage in the Emerging Era of Smart Grids; In tech: 2011; V. 12, P. 251-278].
Из [RU 2536649] известно, что при заряде и разряде Li-ионных аккумуляторов имеют место топотактические реакции, они состоят в инжекции электрона и внедрении катиона Li в твердую матрицу без разрушения внутренней структуры материала. Однако интеркаляция ионов Li в структуру материала может привести к существенным изменениям в строении материала: образование новой фазы, увеличение объема кристаллической ячейки, «вспучиванию» и т.п.
Материал, состоящий из однородных наностержней, в большей степени пригоден для интеркаляции ионов лития, поскольку он не будет испытывать серьезных структурных напряжений при прохождении катиона Li+ по каналам в структуре MnO2.
Известен способ [Xun Wang and Yadong Li // Synthesis and Formation Mechanism of Manganese Dioxide Nanowires/Nanorods, Chem. Eur. J: 2003, V. 9, №1, P. 19141-19147] получения наностержней диоксида марганца, заключающийся в том, что соли (NH4)2S2O8 и MnSO4·H2O растворяют в дистиллированной воде при комнатной температуре и перемешивают до образования однородного раствора. После чего его переносят в автоклав и подвергают гидротермальной обработке при температуре 140°C в течение 12 ч. Полученный продукт фильтруют, промывают дистиллированной водой и высушивают на воздухе. Образование наностержней α- и β-модификаций диоксида марганца проходит через промежуточную стадию образования δ-модификации диоксида марганца с пластинчатой морфологией.
Недостатком данного способа является то, что получаемая β-модификация диоксида марганца содержит примесь δ-модификации, имеющей слоистую структуру, что ухудшает фазовую однородность материала, необходимую при использовании в электрохимических ячейках.
Также недостатком этого метода является относительно высокая продолжительность синтеза.
Известен способ получения наностержней диоксида марганца, изложенный в [М. Wei, Y. Konishi, Н. Zhou, Н. Sugihara and Н. Arakawa // Synthesis of single-crystal manganese dioxide nanowires by soft chemical process, Nanotechnology: 2005, V. 16, P. 245-249] (прототип), заключается в том, что коммерческий γ-MnO2 смешивают с водой, и полученную суспензию подвергают гидротермальной обработке при температуре 140-200°C в течение 72 дней. Полученный продукт фильтруют, промывают водой и высушивают при температуре 60°C в течение 4 ч.
Существенным недостатком является относительно невысокая морфологическая однородность получаемого продукта.
Недостатком предложенного способа также является слишком большая продолжительность синтеза.
Техническая задача связана с тем, что коммерческий успех современных катодных материалов в значительной степени зависит от метода их получения, который должен обеспечивать возможность контроля морфологии и размера частиц.
Изобретение направлено на изыскание высокопроизводительного способа получения наностержней β-MnO2 для использования в литиевых источниках тока в качестве катодного материала с относительно высокой однородностью фракции по диаметру стержней, что значительно улучшает процесс интеркаляции ионов Li в структуру катодного материала.
Технический результат достигается тем, что предложен способ получения наностержней диоксида марганца, заключающийся в том, что смешивают водные растворы перманганата калия и нитрита натрия в мольном соотношении , равном 2:1÷5, до образования однородной дисперсной фазы в сильнощелочном растворе, после чего к нему при постоянном перемешивании медленно прикапывают неорганическую кислоту до достижения значения pH от 2 до 0,5, полученную суспензию помещают в тефлоновый автоклав, который устанавливают в гидротермально-микроволновую установку на 5÷25 мин при 90÷170°C при давлении 1÷20 атм и мощности микроволнового нагрева 150÷1000 Вт, полученный осадок отделяют декантацией, промывают дистиллированной водой и высушивают на воздухе при температуре не выше 70°C, в результате получают кристаллический пиролюзит β-MnO2, частицы которого имеют форму стержней диаметром свыше 10 нм и длиной до 2 мкм.
Целесообразно, что в качестве неорганической кислоты используют либо H2SO4, либо HNO3.
Мольные соотношения , равные 2:1÷5, выбирают из тех соображений, что при них образуется однородная дисперсная фаза.
Выбор диапазона кислотности обусловлен тем, что в среде с pH>2 в конечном продукте присутствует посторонняя примесь наночастиц δ-MnO2, которые характеризуются сфероидальной формой и шероховатой поверхностью, а при pH<0,5 в конечном продукте также присутствует посторонняя фаза.
Заявленный временной интервал 5÷25 минут определяется динамикой процесса формирования кристаллов, который в целом начинается с 5 минут и завершается через 25 минут, после чего линейные размеры наностержней не изменяются и улучшения функциональных свойств нанокристаллов не происходит.
Заявленный температурный интервал гидротермально-микроволновой обработки определен экспериментальным путем и является оптимальным для получения однородной фазы наностержней диоксида марганца, содержащей в своем составе кристаллы диаметром менее 100 нм. Минимальная температура автоклавной обработки обусловлена тем, что ниже 90°C наностержни не образуются. Верхний предел температуры обусловлен тем, что при температурах выше 170°C в получаемом конечном продукте качественных изменений не происходит. Оптимальным является автоклавная обработка в течение 8 минут при 150°C, при которой в конечном продукте однородность фракции 20÷25 нм составляет 90%.
В качестве гидротермально-микроволновой установки используют аппаратуру Berghof Speedwave MWS four, характеризующуюся давлением R20 атм и мощностью микроволнового нагрева 150÷1000 Вт.
Сущность изобретения заключается в том, что варьирование кислотности среды, продолжительности и температуры синтеза позволяет получать продукты с заданными параметрами однородности.
Изобретение проиллюстрировано следующими микрофотографиями.
Фиг. 1. Результаты растровой электронной микроскопии образца диоксида марганца, полученного по предложенному изобретению гидротермально микроволновой обработкой (ГТМВ) в течение 8 мин при 150°C из реакционной смеси с рН=1 (пример 1).
Фиг. 2. Результаты растровой электронной микроскопии образца диоксида марганца, полученного по прототипу.
Ниже приведены примеры иллюстрирующие, но не ограничивающие предложенный способ.
Пример 1
0,3 г KMnO4 растворяли в 38 мл дистиллированной воды, затем к полученному раствору добавляли 0,19 г NaNO2 (мольное соотношение составляло 2:3), после чего к смеси при постоянном перемешивании медленно прикапывали 0,5М H2SO4 до достижения рН=1. Полученную суспензию помещали в тефлоновый автоклав емкостью 100 мл (степень заполнения составляла 50%) и подвергали гидротермально-микроволновой обработке в установке Berghof Speedwave MWS four в течение 8 мин при 150°C. После завершения обработки автоклав извлекали и охлаждали на воздухе. Образовавшийся осадок отделяли декантацией, несколько раз промывали дистиллированной водой и сушили на воздухе при относительной влажности ~75% и температуре 60°C. Получали продукт с однородностью фракции 95% нм и диаметром наностержней 20÷25 нм.
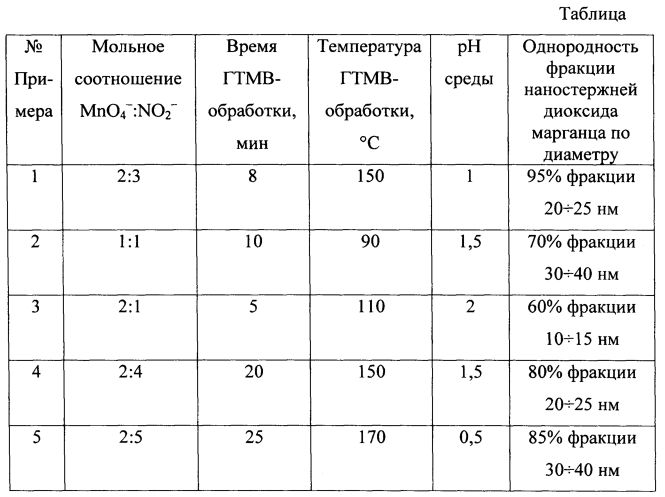
Примеры 2-5 осуществляли по Примеру 1, меняя мольное соотношение реагентов, кислотность среды, время и температуру синтеза. Результаты сведены в Таблицу: «Показатель однородности фракции наностержней диоксида марганца, синтезированных по предлагаемому способу».
Предлагаемый способ позволяет получать наностержни β-MnO2 с достаточно высокой производительностью, а также с относительно высокой однородностью фракции по диаметру стержней, что определяет пригодность их применения в катодных материалах.
Claims (2)
1. Способ получения наностержней диоксида марганца, заключающийся в том, что смешивают водные растворы перманганата калия и нитрита натрия в мольном соотношении MnO4 - : NO2 -, равном 2:(1÷5), до образования однородной дисперсной фазы в сильнощелочном растворе, после чего к нему при постоянном перемешивании медленно прикапывают неорганическую кислоту до достижения значения рН от 2 до 0,5, полученную суспензию помещают в тефлоновый автоклав, который устанавливают в гидротермально-микроволновую установку на 5÷25 мин при 90÷170°C при давлении 1÷20 атм и мощности микроволнового нагрева 150÷1000 Вт, полученный осадок отделяют декантацией, промывают дистиллированной водой и высушивают на воздухе при температуре не выше 70°C, в результате получают кристаллический пиролюзит β-MnO2, частицы которого имеют форму стержней диаметром свыше 10 нм и длиной до 2 мкм.
2. Способ по п. 1, отличающийся тем, что в качестве неорганической кислоты используют либо H2SO4, либо HNO3.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2015109828/05A RU2587439C1 (ru) | 2015-03-20 | 2015-03-20 | Способ получения наностержней диоксида марганца |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2015109828/05A RU2587439C1 (ru) | 2015-03-20 | 2015-03-20 | Способ получения наностержней диоксида марганца |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2587439C1 true RU2587439C1 (ru) | 2016-06-20 |
Family
ID=56132172
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2015109828/05A RU2587439C1 (ru) | 2015-03-20 | 2015-03-20 | Способ получения наностержней диоксида марганца |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2587439C1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116768272A (zh) * | 2022-12-20 | 2023-09-19 | 湖南大学 | 一种基于电化学原位引入氧缺陷的锰基正极材料的制备及其应用 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2108411C1 (ru) * | 1996-11-05 | 1998-04-10 | Открытое акционерное общество "Электростальский химико-механический завод" | Способ получения электролитического диоксида марганца |
| WO2001087775A1 (en) * | 2000-05-15 | 2001-11-22 | Eveready Battery Company Inc. | A method of preparation of porous manganese dioxide |
| RU2194666C2 (ru) * | 1996-11-18 | 2002-12-20 | Дзе Юниверсити оф Коннектикут | Наноструктурные окиси и гидроокиси и способы их синтеза |
| WO2009118526A2 (en) * | 2008-03-25 | 2009-10-01 | Nanotecture Ltd | Mesoporous manganese dioxide |
| US8962517B2 (en) * | 2011-11-29 | 2015-02-24 | Siluria Technologies, Inc. | Nanowire catalysts and methods for their use and preparation |
-
2015
- 2015-03-20 RU RU2015109828/05A patent/RU2587439C1/ru not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2108411C1 (ru) * | 1996-11-05 | 1998-04-10 | Открытое акционерное общество "Электростальский химико-механический завод" | Способ получения электролитического диоксида марганца |
| RU2194666C2 (ru) * | 1996-11-18 | 2002-12-20 | Дзе Юниверсити оф Коннектикут | Наноструктурные окиси и гидроокиси и способы их синтеза |
| WO2001087775A1 (en) * | 2000-05-15 | 2001-11-22 | Eveready Battery Company Inc. | A method of preparation of porous manganese dioxide |
| WO2009118526A2 (en) * | 2008-03-25 | 2009-10-01 | Nanotecture Ltd | Mesoporous manganese dioxide |
| US8962517B2 (en) * | 2011-11-29 | 2015-02-24 | Siluria Technologies, Inc. | Nanowire catalysts and methods for their use and preparation |
Non-Patent Citations (1)
| Title |
|---|
| WEI М. et al., Synthesis of single-crystal manganese dioxide nanowires by soft chemical process, Nanotechnology, 2005, v. 16, pp. 245-249. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116768272A (zh) * | 2022-12-20 | 2023-09-19 | 湖南大学 | 一种基于电化学原位引入氧缺陷的锰基正极材料的制备及其应用 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Zhang et al. | Microwave-assisted reflux rapid synthesis of MnO2 nanostructures and their application in supercapacitors | |
| Samadipakchin et al. | ZnO nanotubes: Preparation and photocatalytic performance evaluation | |
| CN102120619B (zh) | 一种脑珊瑚状水钠锰矿型二氧化锰的制备方法 | |
| Zhang et al. | Nearly monodisperse tungstate MWO4 microspheres (M= Pb, Ca): surfactant-assisted solution synthesis and optical properties | |
| US20090011235A1 (en) | Manganese oxide nanowires, films, and membranes and methods of making | |
| Zhang et al. | Two-step grain-growth kinetics of sub-7 nm SnO2 nanocrystal under hydrothermal condition | |
| Kozawa et al. | Wet mechanical route to synthesize morphology-controlled NH4MnPO4· H2O and its conversion reaction into LiMnPO4 | |
| Yu et al. | Formation of TiO2 hollow spheres through nanoscale Kirkendall effect and their lithium storage and photocatalytic properties | |
| CN108609599A (zh) | 氢氧化镍纳米片自组装磷酸镍钴棒状结构复合材料的制备方法 | |
| Liu et al. | Enhanced microwave absorption properties of MnS2 microspheres interspersed with carbon nanotubes | |
| RU2587439C1 (ru) | Способ получения наностержней диоксида марганца | |
| Xi et al. | Interpretation on a nonclassical crystallization route of prussian white nanocrystal preparation | |
| CN102173459A (zh) | 铁酸钇纳米粉体的微波制备方法 | |
| CN107108212A (zh) | 适于生产Li离子电池的阴极的磷酸盐化合物 | |
| JP5527630B2 (ja) | 水酸化ニッケルナノシートおよびその製造方法 | |
| CN108640095A (zh) | 一种纳米椭球状磷酸铋材料的制备方法 | |
| WO2008023597A1 (fr) | Corps poreux de nano-aiguille de dioxyde de manganèse de type r, nano-aiguille de dioxyde de manganèse de type r constituant celui-ci, oxyde de manganèse hydrogénée, matériau absorbant le rayonnement infra-rouge, filtre infrarouge et leurs procédés de production | |
| Gruen et al. | One-dimensional assemblies of Co3O4 nanoparticles formed from cobalt hydroxide carbonate prepared by bio-inspired precipitation within confined space | |
| CN103288137A (zh) | 一种微波水热制备二氧化钼纳米粒子的方法 | |
| CN102745750B (zh) | 一种低维锰氧化物纳米晶体的制备方法 | |
| Li et al. | A simple hydrothermal route to synthesis of rod-like MnOOH and spindle-shaped MnCO3 | |
| Dong et al. | Preparation of α-Fe2O3 particles with controlled shape and size via a facile hydrothermal route | |
| JP2010037163A (ja) | 水酸化ニッケルヘキサゴナルプレートおよびその製造方法 | |
| Raheem et al. | Hydrothermal Synthesis Of Γ-Mno 2 Nanostructures With Different Morphologies Using Different Mn+ 2 Precursors. | |
| CN109873139A (zh) | γ-MnOOH/SFC纳米复合电极材料的制备及应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20200321 |