RU2427373C1 - Средство для индукции эндогенного интерферона - Google Patents
Средство для индукции эндогенного интерферона Download PDFInfo
- Publication number
- RU2427373C1 RU2427373C1 RU2010145438/15A RU2010145438A RU2427373C1 RU 2427373 C1 RU2427373 C1 RU 2427373C1 RU 2010145438/15 A RU2010145438/15 A RU 2010145438/15A RU 2010145438 A RU2010145438 A RU 2010145438A RU 2427373 C1 RU2427373 C1 RU 2427373C1
- Authority
- RU
- Russia
- Prior art keywords
- substance
- interferon
- ifn
- hours
- neovir
- Prior art date
Links
- 102000014150 Interferons Human genes 0.000 title claims abstract description 36
- 108010050904 Interferons Proteins 0.000 title claims abstract description 36
- 229940079322 interferon Drugs 0.000 title claims abstract description 36
- 230000006698 induction Effects 0.000 title abstract description 3
- 238000000034 method Methods 0.000 title description 4
- 230000001939 inductive effect Effects 0.000 claims description 5
- 150000001875 compounds Chemical class 0.000 claims description 3
- MJTZXIOENMCZJW-UHFFFAOYSA-N methyl 3-(3-amino-2,6-dioxopyrimidin-4-yl)benzoate Chemical compound COC(=O)C1=CC=CC(C=2N(C(=O)NC(=O)C=2)N)=C1 MJTZXIOENMCZJW-UHFFFAOYSA-N 0.000 claims description 2
- 239000003814 drug Substances 0.000 abstract description 24
- 239000000126 substance Substances 0.000 abstract description 23
- 229940079593 drug Drugs 0.000 abstract description 21
- 230000000694 effects Effects 0.000 abstract description 11
- 238000002347 injection Methods 0.000 abstract description 2
- 239000007924 injection Substances 0.000 abstract description 2
- WDUQOKAMYKEBRG-UHFFFAOYSA-N methyl 3-[(2,4-dioxo-1h-pyrimidin-6-yl)amino]benzoate Chemical compound COC(=O)C1=CC=CC(NC=2NC(=O)NC(=O)C=2)=C1 WDUQOKAMYKEBRG-UHFFFAOYSA-N 0.000 abstract 1
- 229960000459 cridanimod Drugs 0.000 description 11
- FQMLTEAEJZVTAJ-UHFFFAOYSA-M sodium;2-(9-oxoacridin-10-yl)acetate Chemical compound [Na+].C1=CC=C2N(CC(=O)[O-])C3=CC=CC=C3C(=O)C2=C1 FQMLTEAEJZVTAJ-UHFFFAOYSA-M 0.000 description 11
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 10
- 239000000539 dimer Substances 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 239000000178 monomer Substances 0.000 description 8
- 239000000243 solution Substances 0.000 description 7
- 239000000825 pharmaceutical preparation Substances 0.000 description 6
- 238000011282 treatment Methods 0.000 description 6
- 238000010521 absorption reaction Methods 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 241000700605 Viruses Species 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 235000019441 ethanol Nutrition 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- IOLCXVTUBQKXJR-UHFFFAOYSA-M potassium bromide Chemical compound [K+].[Br-] IOLCXVTUBQKXJR-UHFFFAOYSA-M 0.000 description 4
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 208000036142 Viral infection Diseases 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 239000000411 inducer Substances 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- -1 sodium oxodihydroacridinyl acetate Chemical compound 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- 208000035143 Bacterial infection Diseases 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 208000022362 bacterial infectious disease Diseases 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 239000013553 cell monolayer Substances 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 235000010981 methylcellulose Nutrition 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 239000003883 ointment base Substances 0.000 description 2
- 235000019271 petrolatum Nutrition 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 229940068196 placebo Drugs 0.000 description 2
- 239000000902 placebo Substances 0.000 description 2
- 210000002381 plasma Anatomy 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 230000009385 viral infection Effects 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- FDCJDKXCCYFOCV-UHFFFAOYSA-N 1-hexadecoxyhexadecane Chemical class CCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCC FDCJDKXCCYFOCV-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- LNDZXOWGUAIUBG-UHFFFAOYSA-N 6-aminouracil Chemical compound NC1=CC(=O)NC(=O)N1 LNDZXOWGUAIUBG-UHFFFAOYSA-N 0.000 description 1
- 229910002012 Aerosil® Inorganic materials 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- UNKAKTJDNSSHIJ-UHFFFAOYSA-N COC(c1cc(NC(NC(C2)=O)=CC2=O)ccc1)=O Chemical compound COC(c1cc(NC(NC(C2)=O)=CC2=O)ccc1)=O UNKAKTJDNSSHIJ-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 102000002004 Cytochrome P-450 Enzyme System Human genes 0.000 description 1
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 206010019799 Hepatitis viral Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 239000004166 Lanolin Substances 0.000 description 1
- 206010023849 Laryngeal papilloma Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 208000007913 Pituitary Neoplasms Diseases 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- CZMRCDWAGMRECN-UHFFFAOYSA-N Rohrzucker Natural products OCC1OC(CO)(OC2OC(CO)C(O)C(O)C2O)C(O)C1O CZMRCDWAGMRECN-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- 206010046798 Uterine leiomyoma Diseases 0.000 description 1
- 241000711975 Vesicular stomatitis virus Species 0.000 description 1
- 108010046377 Whey Proteins Proteins 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 230000000798 anti-retroviral effect Effects 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 235000012216 bentonite Nutrition 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 201000003163 breast adenoma Diseases 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 229940081733 cetearyl alcohol Drugs 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 230000000120 cytopathologic effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 208000002672 hepatitis B Diseases 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 239000002799 interferon inducing agent Substances 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 244000000056 intracellular parasite Species 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 229940039717 lanolin Drugs 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 201000000089 larynx squamous papilloma Diseases 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 201000010260 leiomyoma Diseases 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 201000005296 lung carcinoma Diseases 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- VZDNXXPBYLGWOS-UHFFFAOYSA-N methyl 3-aminobenzoate Chemical compound COC(=O)C1=CC=CC(N)=C1 VZDNXXPBYLGWOS-UHFFFAOYSA-N 0.000 description 1
- DGBOCKNQMSJDRK-UHFFFAOYSA-N methyl 3-aminobenzoate;hydrochloride Chemical compound Cl.COC(=O)C1=CC=CC(N)=C1 DGBOCKNQMSJDRK-UHFFFAOYSA-N 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 229940042472 mineral oil Drugs 0.000 description 1
- 238000004264 monolayer culture Methods 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 1
- 230000000771 oncological effect Effects 0.000 description 1
- 229940127234 oral contraceptive Drugs 0.000 description 1
- 239000003539 oral contraceptive agent Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 1
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229940113124 polysorbate 60 Drugs 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 239000006215 rectal suppository Substances 0.000 description 1
- JQXXHWHPUNPDRT-WLSIYKJHSA-N rifampicin Chemical compound O([C@](C1=O)(C)O/C=C/[C@@H]([C@H]([C@@H](OC(C)=O)[C@H](C)[C@H](O)[C@H](C)[C@@H](O)[C@@H](C)\C=C\C=C(C)/C(=O)NC=2C(O)=C3C([O-])=C4C)C)OC)C4=C1C3=C(O)C=2\C=N\N1CC[NH+](C)CC1 JQXXHWHPUNPDRT-WLSIYKJHSA-N 0.000 description 1
- 229960001225 rifampicin Drugs 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000001839 systemic circulation Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- MPMFCABZENCRHV-UHFFFAOYSA-N tilorone Chemical compound C1=C(OCCN(CC)CC)C=C2C(=O)C3=CC(OCCN(CC)CC)=CC=C3C2=C1 MPMFCABZENCRHV-UHFFFAOYSA-N 0.000 description 1
- 229950006823 tilorone Drugs 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 201000008827 tuberculosis Diseases 0.000 description 1
- 238000002211 ultraviolet spectrum Methods 0.000 description 1
- 239000006216 vaginal suppository Substances 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 201000001862 viral hepatitis Diseases 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 235000021119 whey protein Nutrition 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/20—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D239/22—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with hetero atoms directly attached to ring carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/513—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim having oxo groups directly attached to the heterocyclic ring, e.g. cytosine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
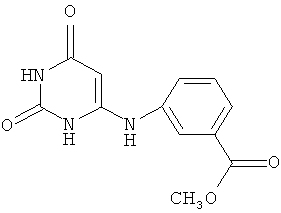
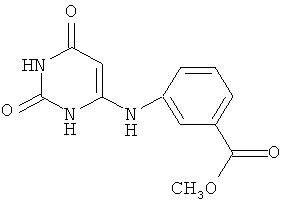
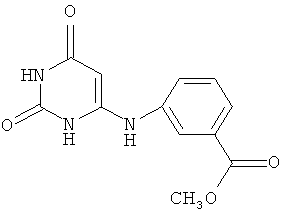
Изобретение относится к медицине и представляет собой средство для индукции эндогенного интерферона, а именно 6-(3-метоксикарбонилфенил)амино-2,4(1Н,3Н)-пиримидиндион C12H11N3O4 общей формулы
Изобретение обеспечивает более высокую активность при инъекционном, а также и при энтеральном введении. 2 табл., 1 ил.
Description
Изобретение относится к медицине и может быть использовано для лечения ряда заболеваний, в лечении которых используется интерферон.
К числу заболеваний, в лечении которых используют интерферон или индукторы его эндогенного синтеза, относится большинство вирусных инфекций, в том числе герпетическая инфекция, вирусные гепатиты A, B, C и некоторые опухоли: папилломы гортани, фибромиомы матки, аденомы молочной железы и гипофиза и др., RU 2105566.
Известны лекарственные средства, являющиеся индукторами синтеза собственного эндогенного интерферона - вещества, которое способствует формированию защитного барьера, препятствующего инфицированию организма вирусами и бактериями, а также регулирует состояние иммунной системы и ингибирует рост злокачественных клеток. Наиболее известными и распространенными лекарственными препаратами индукторами интерферона являются Неовир, идентичный ему по структуре циклоферон и тилорон (http://www.ingentaconnect.com/content/els/00207292/1996/00000055/00000001/art88729; http://www.rlsnet.ru/mnn_index_id_2731.htm.
Принятый в качестве прототипа препарат Неовир (оксодигидроакридинилацетат натрия) широко используется для лечения вирусных и бактериальных инфекций, особенно вызванных внутриклеточными паразитами. Неовир также применяют при лечении некоторых онкологических заболеваний. Некоторой активностью Неовир обладает при его инъекционном введении. При энтеральном приеме препарата обнаруживается его низкая эффективность.
После приема внутрь Неовира максимум продукции интерферона определяется в последовательности кишечник-печень-кровь через 4-24 ч. В лейкоцитах человека Неовир индуцирует образование интерферона, уровень которого в крови составляет 250 ЕД/мл.
При назначении Неовира, равно как и других известных индукторов интерферона, существует риск нежелательных взаимодействий с другими лекарствами, например с рифампицином, при лечении туберкулеза и антиретровирусными препаратами при лечении ВИЧ-инфекции, а также с оральными контрацептивами. Ввиду отсутствия детальных данных о взаимодействии Неовира с этими и некоторыми другими лекарствами их одновременное применение может быть опасным (http://ru.wikipedia.org/wiki/%D0%A2%D0%B8%D0%/BB%/D0%BE%D1%80%D0%BE%D0%BD Renton KW, Mannering GJ (1976). «Depression of hepatic cytochrome Р-450-dependent monooxygenase systems with administered interferon inducing agents». Biochem Biophys Res Commun. 73 (2): 343-348. DOI:http://dx.doi.org/10.1016/0006-291X(76)90713-0. PMID 187194).
Задачей настоящего изобретения является создание препарата, который имеет более высокую активность при инъекционном, а также и при энтеральном введении.
Согласно изобретению средство для индукции эндогенного интерферона представляет собой соединение 6-(3-метоксикарбонилфенил)амино-2,4(1Н,3H)-пиримидиндион C12H11N3O4 общей формулы
Заявленное вещество получают следующим образом. К 10 г гидрохлорида метилового эфира м-аминобензойной кислоты и 8.4 г метилового эфира м-аминобензойной кислоты добавляют 7 г 6-аминоурацила и тщательно перетирают смесь в ступке. При нагревании до 160°C смесь плавится и становится легкоподвижной, но уже через 0.5 ч затвердевает, нагревание прекращают через 1.5 ч. Смесь переносят в воду, перемешивают и фильтруют, промывают водой. Затем продукт кипятят в 100 мл этилового спирта в течение 2 ч. После охлаждения смеси до комнатной температуры продукт отфильтровывают, промывают этиловым спиртом и высушивают. Получают 10 г целевого продукта.
Этот продукт представляет собой смесь заявленного вещества (мономера) с его димером. Температура плавления смеси выше 300°C.
Разделение мономера и димера проводили следующим образом: растворяли указанный выше целевой продукт в смеси 2-пропанол-ДМФА при нагревании и охлаждали. По охлаждении димер выпадал в осадок, а мономер оставался в растворе. Для извлечения мономера раствор упаривали досуха, кристаллический остаток промывали этанолом и высушивали в вакууме. Масса полученного мономера в два раза больше, чем масса димера, возможно использование как мономера, так и димера, при этом димер легче проникает через клеточные мемебраны.
Инфракрасный спектр препарата, снятый в таблетках с калия бромидом (2 мг на 300 мг калия бромида), в области от 4000 см-1 до 400 см-1 должен иметь полное совпадение полос поглощения с полосами поглощения прилагаемого спектра по положению и относительной интенсивности полос.
Ультрафиолетовый спектр 0.025% раствора препарата в 0.1 н. растворе едкого натра в области от 200 до 370 нм имеет плечо при 252 нм, минимум поглощения при 265 нм и несимметричный максимум поглощения при 288 нм ± 1 нм.
Спектр протонного магнитного резонанса содержит следующие характерные сигналы, м.д.: 10.4 и 10.2 (NH эндоцикл.), 8.36 (экзоцикл. NH), 7.4-7.8 (4H, Ar,), 4.72 (1H, CH), 3.86 (3H, OCH3).
Указанные спектры для заявленного соединения и его димера практически совпадают.
При изготовлении фармацевтических препаратов на основе заявленного вещества могут быть использованы различные фармацевтически приемлемые наполнители, адъюванты и транспортеры: метилцеллюлоза, аксипропилметилцеллюлоза, карбоксиметилцеллюлоза, натрийкарбоксиметилцеллюлоза, кукурузный крахмал, тальк, каолин, бентониты, аэросил, сахар свекловичный, сахар молочный, натрия хлорид, натрия гидрокарбонат, окись алюминия, стеарат алюминия, лецитин, сывороточные белки, фосфаты, глицин, сорбиновая кислота, сорбат калия, смесь глицеридов насыщенных растительных жирных кислот, соли цинка, коллоидная двуокись кремния, трисиликат магния, воск, полиэтиленгликоль, ланолин и др.
Заявленное средство можно применять перорально, парентерально, ректально, назально, лингвально, вагинально или при помощи имплантантов; парентеральное применение в данном случае включает его введение подкожно, внутрикожно, внутривенно, внутримышечно, внутрисуставно, интрасиновиально, интрастернально, в спинномозговую жидкость, интракраниально.
Местное применение фармацевтических препаратов, созданных на основе изобретения, особенно показано, если лечения требуют участки организма, к которым их можно применить местно.
В фармацевтических препаратах для местного нанесения на кожу действующее вещество следует сочетать с подходящей мазевой основой, в которой активный компонент может находиться в растворенном состоянии или в виде суспензии. Мазевая основа может включать минеральные масла, жидкий вазелин, белый вазелин, пропиленгликоль, смесь полиоксиэтилена и полиоксипропилена, эмульгирующий воск, воду. Основой для фармацевтических препаратов наружного применения может также быть лосьон или крем, в котором заявленное вещество будет находиться в виде раствора или суспензии. В качестве наполнителей в этом случае могут быть, минеральное масло, сорбитана моностеарат, полисорбат 60, цетиловые эфиры, воск, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт, вода и другие подходящие ингредиенты. Фармацевтические препараты на основе заявленного вещества могут также быть применимы к нижним отделам кишечника в виде ректальных суппозиториев или другой подходящей лекарственной формы.
На основе заявленного вещества могут также быть созданы такие лекарственные формы для наружного применения, как пластырь, назальные аэрозоли, ингаляторы. В качестве жидкой фазы для растворения заявленного вещества можно использовать изотонический раствор хлорида натрия (физиологический раствор), при этом стабилизатором может служить бензиловый спирт или любое подходящее для этого вещество, активатором всасывания, чтобы увеличить биодоступность, могут служить фторкарбоны; для улучшения растворения и диспергирования могут быть использованы любые известные в производстве подобных фармацевтических форм вспомогательные вещества.
Лекарственный препарат, приготовленный на основе заявленного вещества, может быть использован в дозах примерно от 0.01 до 25 мг активного вещества на 1 кг веса пациента в сутки. Для профилактики и лечения вирусных инфекций и бактериальных инфекций, а также некоторых форм рака предпочтительна суточная доза примерно от 0.5 до 25 мг активного вещества на 1 кг веса. Фармацевтические препараты на основе изобретения можно вводить от 1 до 5 раз в день или в виде длительной инфузии.
Определение уровня индуцированного интерферона (ИФН) после введения заявленного вещества.
Количественное определение содержания ИФН в контрольных и опытных образцах производилось двумя способами:
1) с использованием иммуноферментной тест-системы на ИФН ProCon IF2 plus производства фирмы "Протеиновый контур" с пересчетом полученных результатов весового содержания ИФН в международные единицы (МЕ) активности ИФН;
2) с использованием оригинальной методики биологического тестирования содержания ИФН, заключающейся в следующем: ИФН вызывают торможение развития цитопатического действия вирусов, проявляющееся в деструкции монослоя специально подобранной линии клеточной культуры. Количественное определение содержания ИФН в пробе достигается количественным анализом интенсивности деструкции клеточного монослоя после преинкубации с ИФН-содержащими пробами и инкубации с индикаторным вирусом.
Краткое описание методики: монослойная культура клеток карциномы легкого человека L-41 инкубируется с раститрованными ИФН-содержащими пробами в микропланшетах в течение 24 часов в CO2-термостате при 37°C, после чего в микроплашеты вносится раствор индикаторного вируса (вируса везикулярного стоматита, штамм Индиана, ВВС) и происходит инкубация в течение 18 часов в CO2-термостате при 37°C. Затем микропланшеты окрашиваются кристаллическим фиолетовым для визуализации результатов. Излишки красителя отмываются дистиллированной водой, микропланшеты высушиваются, затем краситель, связавшийся с живыми клетками, экстрагируется 30% этанолом и микропланшеты фотометрируются на автоматическом фотометре типа "Multiscan" для 96-луночных микропланшетов в режиме многократного сканирования лунок при длине волны 590 нм. Полученное количество связавшегося красителя прямо пропорционально содержанию ИФН в определяемом образце. Количественное содержание ИФН в пробах определяют после интерполяции результатов в пределах зависимости от содержания ИФН в пробах и интенсивности деструкции клеточного монослоя. Данная зависимость получена после титрования в аналогичных условиях стандартного референс-препарата нативного человеческого ИФН. В качестве референс-препарата в каждом опыте использовали препарат нативного человеческого ИФН, стандартизированный по активности. Результаты анализа выражены в ME активности ИФН на 1 мл в данной индукционной системе, содержащей 3·106 лимфоцитов/мл. Опытные и контрольные точки исследованы в 4 параллелях.
Интерферониндуцирующая активность препаратов in vivo при введении мышам внутрибрюшинно (в ME) приведена в таблице 1.
| Таблица 1 | |||||
| Препарат | Время | ||||
| 2 часа | 4 часа | 6 часов | 8 часов | 24 часа | |
| Плацебо | 7-10* | 20 -25 | 7-10 | 7-10 | 7-10 |
| Неовир | 7-10 | 100-110 | 7-10 | 7-10 | 7-10 |
| Заявленное вещество, мономер | 30 | 10 | 160 | 25-30 | 30 |
| То же, димер | 40 | 50 | 210 | 30-35 | 15-40 |
| Препараты вводили в количестве 1000 мкг/мышь. | |||||
| *Фоновое значение активности интерферона 7-10 единиц. | |||||
Полученные данные указывают, что заявленное вещество индуцирует повышение уровня эндогенного интерферона с динамикой, отличающейся от препарата сравнения. Уровень эндогенного интерферона после введения заявляемых веществ превосходит таковой у прототипа.
Интерферониндуцирующая активность препаратов in vivo при энтеральном введении мышам (в ME) приведена в таблице 2.
| Таблица 2 | |||||
| Препарат | Время | ||||
| 2 часа | 4 часа | 6 часов | 8 часов | 24 часа | |
| Плацебо | - | 20-25 | - | - | - |
| Неовир | 7-10 | 40-60 | 10-12 | 7-10 | 7-10 |
| Заявленное вещество, мономер | 18 | 120 | 20 | 40 | 100 |
| То же, димер | 12-25 | 150 | 30 | 30-50 | 120 |
| Препараты вводили в количестве 5.0 мг/мышь. | |||||
| *Фоновое значение активности интерферона 7-10 единиц. | |||||
Полученные данные свидетельствуют, что заявленное вещество при введении энтерально вызывает выработку эндогенного интерферона и значительно более эффективно в сравнении с прототипом.
Концентрация в плазме крови экспериментальных животных при вагинальном применении заявленного вещества.
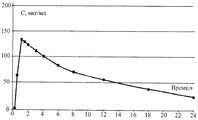
Результаты измерения концентрации вещества в плазме крови кроликов при вагинальном введении в форме «суппозитории вагинальные 0,1 г» в виде усредненных фармакокинетических кривых отображены на приведенной ниже диаграмме. После введения свечи вещество начинало проникать в системный кровоток примерно через 15 минут и достигало максимального уровня через 1 час (около 120 мкг/мл), после чего препарат постепенно выводился из организма и через 24 часа после введения определялся в плазме крови в минимальных количествах (около 20 мкг/мл). Разброс индивидуальных значений умеренный: коэффициент вариации CV составил 13-22%.
Результаты проведенных исследований указывают, что заявленное вещество при вагинальном введении в виде свечей проникает в кровь экспериментальных животных.
Таким образом, установлено, что заявляемое вещество обладает интерферониндуцирующей активностью при разных способах введения, при этом активность заявленного вещества превосходит таковую у прототипа (Неовира) как при парентеральном, так и энтеральном введении. Также было отмечено значительное уменьшение побочных явлений и нежелательных взаимодействий с другими лекарствами.
Claims (1)
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010145438/15A RU2427373C1 (ru) | 2010-11-08 | 2010-11-08 | Средство для индукции эндогенного интерферона |
| PCT/RU2011/000793 WO2012064222A1 (ru) | 2010-11-08 | 2011-10-10 | Средство для индукции эндогенного интерферона |
| ES11839763T ES2774663T3 (es) | 2010-11-08 | 2011-10-10 | Agente para inducir interferón endógeno |
| EP11839763.7A EP2638901B1 (en) | 2010-11-08 | 2011-10-10 | Agent for inducing endogenous interferon |
| US13/883,860 US10029990B2 (en) | 2010-11-08 | 2011-10-10 | Agent for inducing endogenous interferon |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010145438/15A RU2427373C1 (ru) | 2010-11-08 | 2010-11-08 | Средство для индукции эндогенного интерферона |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2427373C1 true RU2427373C1 (ru) | 2011-08-27 |
Family
ID=44756649
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010145438/15A RU2427373C1 (ru) | 2010-11-08 | 2010-11-08 | Средство для индукции эндогенного интерферона |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US10029990B2 (ru) |
| EP (1) | EP2638901B1 (ru) |
| ES (1) | ES2774663T3 (ru) |
| RU (1) | RU2427373C1 (ru) |
| WO (1) | WO2012064222A1 (ru) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013062445A1 (ru) * | 2011-10-26 | 2013-05-02 | ИВАЩЕНКО, Андрей Александрович | Фармацевтическая композиция и набор для лечения бактериальных инфекций |
| RU2568849C1 (ru) * | 2014-11-06 | 2015-11-20 | Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра Российской академии наук (ИОХ УНЦ РАН) | Средство, представляющее собой амид глицирризиновой кислоты с 5-аминоурацилом, проявляющее противовирусную активность в отношении вируса гриппа a/h1n1 |
| RU2669555C1 (ru) * | 2018-01-19 | 2018-10-12 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Санкт-Петербургский государственный химико-фармацевтический университет" Министерства здравоохранения Российской Федерации (ФГБОУ ВО СПХФУ Минздрава России) | 6-Оксо-1-фенил-2-(фениламино)-1,6-дигидропиримидин-4-олят натрия и способ его получения |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4314061A (en) * | 1979-10-31 | 1982-02-02 | Murdock Keith C | Certain 3,6-bis-(heteroaminoalkoxy) acridines |
| RU2222345C2 (ru) * | 2002-01-21 | 2004-01-27 | Волчек Игорь Анатольевич | Фармацевтическая композиция цитокинового и иммуномодулирующего действия |
| RU2328272C2 (ru) * | 2005-03-22 | 2008-07-10 | Общество с ограниченной ответственностью (ООО) "Диафарм" | Суппозитории индуктора интерферона |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9214720D0 (en) | 1992-07-10 | 1992-08-19 | Wellcome Found | Enzyme inhibitors |
| RU2105566C1 (ru) | 1995-06-06 | 1998-02-27 | Юрий Андреевич Севрук | Способ интерферонотерапии ю.а.севрука |
| RU2207337C2 (ru) * | 1998-11-18 | 2003-06-27 | Изаксон Елена Александровна | 6-(3-ацетилфенил)аминоурацил |
| MXPA03008691A (es) * | 2001-03-29 | 2003-12-12 | Bristol Myers Squibb Co | Metodo para tratamiento de enfermedades proliperativas usando inhibidores eg5. |
| UA85871C2 (ru) * | 2004-03-15 | 2009-03-10 | Такеда Фармасьютікал Компані Лімітед | Ингибиторы дипептидилпептидазы |
| US20060194821A1 (en) | 2005-02-18 | 2006-08-31 | The Brigham And Women's Hospital, Inc. | Compounds inhibiting the aggregation of superoxide dismutase-1 |
| KR20170078811A (ko) | 2014-11-07 | 2017-07-07 | 리폭센 테크놀로지즈 리미티드 | 원발성 호르몬 저항성 자궁내막암 및 유방암 치료 방법 |
-
2010
- 2010-11-08 RU RU2010145438/15A patent/RU2427373C1/ru active
-
2011
- 2011-10-10 ES ES11839763T patent/ES2774663T3/es active Active
- 2011-10-10 US US13/883,860 patent/US10029990B2/en active Active
- 2011-10-10 EP EP11839763.7A patent/EP2638901B1/en active Active
- 2011-10-10 WO PCT/RU2011/000793 patent/WO2012064222A1/ru not_active Ceased
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4314061A (en) * | 1979-10-31 | 1982-02-02 | Murdock Keith C | Certain 3,6-bis-(heteroaminoalkoxy) acridines |
| RU2222345C2 (ru) * | 2002-01-21 | 2004-01-27 | Волчек Игорь Анатольевич | Фармацевтическая композиция цитокинового и иммуномодулирующего действия |
| RU2328272C2 (ru) * | 2005-03-22 | 2008-07-10 | Общество с ограниченной ответственностью (ООО) "Диафарм" | Суппозитории индуктора интерферона |
Non-Patent Citations (1)
| Title |
|---|
| Неовир, РЛС, 2003, с.572. * |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013062445A1 (ru) * | 2011-10-26 | 2013-05-02 | ИВАЩЕНКО, Андрей Александрович | Фармацевтическая композиция и набор для лечения бактериальных инфекций |
| RU2496475C2 (ru) * | 2011-10-26 | 2013-10-27 | Александр Васильевич Иващенко | Фармацевтическая композиция и набор для лечения бактериальных инфекций |
| EA025927B1 (ru) * | 2011-10-26 | 2017-02-28 | Иващенко Александр Васильевич | Фармацевтическая композиция и набор для лечения бактериальных инфекций |
| RU2568849C1 (ru) * | 2014-11-06 | 2015-11-20 | Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра Российской академии наук (ИОХ УНЦ РАН) | Средство, представляющее собой амид глицирризиновой кислоты с 5-аминоурацилом, проявляющее противовирусную активность в отношении вируса гриппа a/h1n1 |
| RU2568849C9 (ru) * | 2014-11-06 | 2016-03-20 | Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра Российской академии наук (ИОХ УНЦ РАН) | Средство, представляющее собой амид глицирризиновой кислоты с 5-аминоурацилом, проявляющее противовирусную активность в отношении вируса гриппа a/h1n1 |
| RU2669555C1 (ru) * | 2018-01-19 | 2018-10-12 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Санкт-Петербургский государственный химико-фармацевтический университет" Министерства здравоохранения Российской Федерации (ФГБОУ ВО СПХФУ Минздрава России) | 6-Оксо-1-фенил-2-(фениламино)-1,6-дигидропиримидин-4-олят натрия и способ его получения |
Also Published As
| Publication number | Publication date |
|---|---|
| ES2774663T3 (es) | 2020-07-22 |
| EP2638901A1 (en) | 2013-09-18 |
| US20130261302A1 (en) | 2013-10-03 |
| WO2012064222A1 (ru) | 2012-05-18 |
| EP2638901A4 (en) | 2015-04-08 |
| US10029990B2 (en) | 2018-07-24 |
| EP2638901B1 (en) | 2019-12-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ferreira et al. | Chloroquine and hydroxychloroquine in antitumor therapies based on autophagy-related mechanisms | |
| TW201936596A (zh) | Tlr7/8拮抗劑及其用途 | |
| US11344531B2 (en) | Durable preparation of an injectable of melatonin exhibiting long-term stability | |
| TWI874925B (zh) | 癌症治療 | |
| US20190209567A1 (en) | A Specific Trifluoroethyl Quinoline Analogue For Use In The Treatment of APDS | |
| US20180344694A1 (en) | Use of indole compounds to stimulate the immune system | |
| RU2427373C1 (ru) | Средство для индукции эндогенного интерферона | |
| US20240316087A1 (en) | Compositions And Methods For Inducing Apoptosis In Anaerobic Cells And Related Clinical Methods For Treating Cancer And Pathogenic Infections | |
| EP3955911A1 (en) | Compositions and methods for inhibiting blood cancer cell growth | |
| US20130303611A1 (en) | Use of phenethyl caffeate derivatives in the preparation of a medicament against tumor angiogenesis | |
| RU2237475C1 (ru) | Комбинированный препарат для устранения симптомов простудных заболеваний и гриппа (варианты) | |
| RU2465912C1 (ru) | Фармацевтическая композиция на основе наномицелл, содержащих эпигаллокатехингаллат, и ее применение для лечения атопического дерматита, болезни крона, аденомиоза и гиперпластических заболеваний предстательной железы | |
| KR20020041451A (ko) | 세포내 원핵생물, dna 바이러스 및 레트로바이러스에의한 감염을 치료하기 위한 3-히드록시-4-피론의 갈륨착물 | |
| EP0914824A1 (en) | Preventive and remedy for viral infections | |
| CN116850289B (zh) | Plk4靶向药物在治疗对铂类药物耐药型肿瘤中的应用 | |
| CN103933048A (zh) | 一种熊果酸衍生物在制备预防和治疗肿瘤转移药物中的应用 | |
| HUP0303353A2 (hu) | Profilaktikus és terápiás szer diabeteses komplikációkhoz | |
| US9745337B2 (en) | Complex compounds of germanium, methods for producing same, and drugs | |
| CA2631166A1 (en) | Salts and mixture of -9-oxoacridine-10-acetic acid with 1-alkylamino-1-desoxy-polyols, pharmaceutical compositions containing said agents and treatment methods | |
| US11512073B2 (en) | Benzimidazole derivatives, pharmaceutical composition comprising the same, and use thereof | |
| US20240269112A1 (en) | Injectable melatonin composition for the treatment of viral diseases | |
| WO2017031914A1 (zh) | 依鲁替尼的药物组合物 | |
| CN113143924A (zh) | 硫代咪唑烷酮药物在治疗covid-19疾病中的用途 | |
| RU2295335C2 (ru) | Лекарственные препараты, обладающие иммуномодулирующим, противовоспалительным и противоопухолевым свойствами, и способ их получения | |
| CN103936710A (zh) | N-取代的胡椒基戊二烯酰胺衍生物及其制备方法和应用 |