RU2342133C2 - Применение производных феноксиуксусной кислоты для лечения гиперактивности мочевого пузыря - Google Patents
Применение производных феноксиуксусной кислоты для лечения гиперактивности мочевого пузыря Download PDFInfo
- Publication number
- RU2342133C2 RU2342133C2 RU2005137701/15A RU2005137701A RU2342133C2 RU 2342133 C2 RU2342133 C2 RU 2342133C2 RU 2005137701/15 A RU2005137701/15 A RU 2005137701/15A RU 2005137701 A RU2005137701 A RU 2005137701A RU 2342133 C2 RU2342133 C2 RU 2342133C2
- Authority
- RU
- Russia
- Prior art keywords
- acid
- ethyl
- group
- hydroxy
- bladder
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/216—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acids having aromatic rings, e.g. benactizyne, clofibrate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/191—Carboxylic acids, e.g. valproic acid having two or more hydroxy groups, e.g. gluconic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/235—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids having an aromatic ring attached to a carboxyl group
- A61K31/24—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids having an aromatic ring attached to a carboxyl group having an amino or nitro group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/10—Drugs for disorders of the urinary system of the bladder
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Emergency Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Urology & Nephrology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Изобретение относится к области медицины и фармацевтики и касается применения соединения общей формулы I для получения лекарственного средства для лечения гиперактивности мочевого пузыря и фармацевтической композиции для лечения гиперактивности мочевого пузыря, содержащей соединение формулы I. Изобретение позволяет реализовать указанное назначение. 2 н. и 18 з.п. ф-лы, 10 ил.
Description
ОПИСАНИЕ
Область техники
Настоящее изобретение относится к новой области показаний для производных феноксиуксусной кислоты в соответствии с заявкой на европейский патент EP 1095932. Было обнаружено, что описанные в ней соединения подходят для получения лекарственного средства для лечения гиперактивности мочевого пузыря (повышенная сократительная функция мочевого пузыря: OAB). Соответственно предложен способ лечения этого урологического синдрома при помощи данных активных веществ.
Уровень техники
Нарушение функции мочевого пузыря OAB представляет собой широко распространенный хронический недуг, который поражает по приблизительной оценке более 50 миллионов человек в промышленно развитых странах. В соответствии с новой терминологией Международного общества по проблемам держания (International Continence Society), опубликованной в 2002, OAB диагностируют симптоматически. Симптомами OAB являются императивные неотложные позывы к мочеиспусканию с неотложным недержанием мочи или без него, главным образом, но не обязательно в сочетании с поллакиурией и никтурией. OAB также характеризуется непроизвольными сокращениями детрузора, которые либо вызываются раздражением либо происходят спонтанно. Различают два типа повышенной сократительной активности детрузора: в том случае, когда повышенная сократительная активность детрузора вызвана неврологическими причинами (например, болезнь Паркинсона, инсульт, некоторые формы рассеянного склероза или поперечный срез костного мозга), она известна как нейрогенная повышенная сократительная активность детрузора. Если точная причина не может быть установлена, то такая повышенная сократительная активность детрузора известна как идиопатическая повышенная сократительная активность детрузора. OAB имеет свою собственную клиническую картину, которая отличается от других заболеваний, имеющих похожие симптомы, и ее не следует путать с заболеваниями такого типа, как, например, инфекции нижнего отдела мочевых путей, уротелиальная карцинома, заболевания, связанные с мочеиспусканием, и т.п.
Менее обоснованные способы лечения включают в себя лекарственные средства с антимускариновыми веществами в качестве активного вещества. Некоторые активные вещества этой категории могут плохо переноситься и вызывать сухость во рту вследствие слабой селективности в отношении мочевого пузыря. Побочные эффекты такого типа могут создавать ограничения для терапии.
В EP 1095932 описан ряд производных феноксиуксусной кислоты из серии катехоламинов. Эти соединения имеют боковую цепь, напоминающую норадреналин, за исключением того, что не только гидроксильная группа бензила, а также гомобензильная аминогруппа связана с ассимметричным атомом углерода. Считается, что описанные там соединения оказывают положительный эффект при лечении недержания мочи. В описании отсутствуют сведения, касающиеся действия этих веществ, связанного с лечением повышенной сократительной функции мочевого пузыря.
Было обнаружено, что эти соединения также подходят для лечения урологического феномена повышенной сократительной функции мочевого пузыря.
Раскрытие изобретения
1. Описание изобретения
Настоящее изобретение относится к лекарственным средствам для лечения повышенной сократительной функции мочевого пузыря.
Еще одним объектом изобретения является новое терапевтическое средство для лечения гиперактивности мочевого пузыря.
Данное изобретение дополнительно относится к новому медицинскому/фармацевтическому применению производных феноксиуксусной кислоты из группы катехоламинов.
Еще одной задачей данного изобретения является улучшение качества жизни людей, страдающих урологическими заболеваниями, дисфункцией или гиперактивностью, в частности людей с повышенной сократительной активностью мочевого пузыря, с использованием производных феноксиуксусной кислоты из группы катехоламинов.
Еще одним объектом настоящего изобретения являются лекарственные средства, которые оказывают специфическое лечебное воздействие на соответствующую физиологическую дисфункцию без нежелательных побочных эффектов, которые ухудшают качество жизни пациентов, страдающих этой дисфункцией.
2. Подробное описание изобретения
Настоящее изобретение относится к применению производных феноксиуксусной кислоты в соответствии с EP 1095932 для получения лекарственного средства для лечения повышенной сократительной активности мочевого пузыря и фармацевтической композиции для лечения повышенной сократительной активности мочевого пузыря, содержащей в качестве активного ингредиента производное феноксиуксусной кислоты в соответствии с EP 1095932. В соответствии с EP 1095932 соединения, лежащие в основе применения и получения композиции согласно данному изобретению, являются агонистами бета-3-адренорецепторов. Данные вещества могут быть использованы, в частности, для лечения нейрогенной гиперактивности мочевого пузыря, нейрогенной гиперактивности детрузора, а также для лечения идиопатической гиперактивности мочевого пузыря и идиопатической гиперактивности детрузора.
Соединения, лежащие в основе применения и получения композиции по данному изобретению, представлены следующей общей формулой I:
Формула I:
где X представляет собой хиральный атом углерода R или S, предпочтительно S конфигурации,
Y представляет собой хиральный атом углерода R или S, предпочтительно R конфигурации,
два стереоцентра X и Y предпочтительно находятся в противоположных конфигурациях, т.е. (R;S) или (S;R);
R1 представляет собой гидроксигруппу, C1-C6-алкоксигруппу, арил-C1-C6-алкоксигруппу, первичную аминогруппу или моно- или ди(C1-C6-алкил)аминогруппу;
одна из групп R2 и R3 представляет собой атом водорода, предпочтительно R2, другая группа представляет собой атом водорода, атом галогена, C1-C6-алкильную группу, трифторметильную группу или C1-C6-алкоксигруппу;
R4 представляет собой атом галогена, C1-C6-алкильную группу, группу гало(C1-C6-алкил), гидроксигруппу, C1-C6-алкоксигруппу, арил-C1-C6-алкоксигруппу, C1-C6-алкоксигруппу, цианогруппу, нитрогруппу, аминогруппу, моно- или ди(C1-C6-алкил)аминогруппу, карбамоильную группу, моно- или ди(C1-C6-алкил)карбамоильную группу или R4 соответствует группе -NHCOR5, где R5 представляет собой атом водорода или C1-C6-алкильную группу; или его фармацевтически приемлемую соль.
В описании настоящего изобретения термины определены следующим образом:
Атом галогена: фтор (F), хлор (Cl), бром (Br) или иод (I);
C1-C6-алкил: разветвленная или неразветвленная алкильная группа с 1-6 атомами углерода, такая как метильная, этильная, пропильная, изопропильная, бутильная, изобутильна, втор-бутильная, трет-бутильная, пентильная, изопентильная, гексильная и т.д.;
C1-C6-алкокси: разветвленная или неразветвленная алкоксигруппа с 1-6 атомами углерода, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентокси, изопентокси, гексокси и т.д.;
арил: фенил, нафтил;
моно- или ди(C1-C6-алкил)аминогруппа: означает аминогруппу с одной или двумя идентичными или различными C1-C6-алкильными группами;
моно- или ди(C1-C6-алкил)карбамоильная группа: означает карбамоильную группу с одной или двумя идентичными или различными С1-C6-алкильными группами у функционального N атома.
Способы получения вышеуказанных соединений описаны в EP 1095932. Аналогичные способы получения могут быть использованы для синтеза трифторметильных производных.
Предпочтительными соединениями являются соединения общей формулы I
где X представляет собой хиральный атом углерода S конфигурации,
Y представляет собой хиральный атом углерода R конфигурации,
R1 представляет собой гидроксигруппу, C1-C3-алкоксигруппу, арил-C1-C3-алкоксигруппу;
одна из групп R2 и R3 представляет собой атом водорода, предпочтительно R2, другая группа представляет собой C1-C3-алкильную группу;
R4 представляет собой C1-C3-алкильную группу;
или их фармацевтически приемлемые соли.
В объеме настоящего изобретения особенно предпочтительными являются соединения общей формулы II или их фармацевтически приемлемые соли.
Формула II:
где X представляет собой хиральный атом углерода R или S; предпочтительно S конфигурации,
Y представляет собой хиральный атом углерода R или S, предпочтительно R конфигурации,
два стереоцентра предпочтительно представляют собой противоположные конфигурации, т.е. (R;S) или (S;R);
R означает гидроксигруппу, метокси- или этоксигруппу, предпочтительно гидроксигруппу или этоксигруппу.
Наиболее предпочтительными являются соединения
- (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат и
- (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусная кислота.
Применение и получение композиции по данному изобретению можно проводить с нейтральными соединениями, а также с кислотно-аддитивной солью или сольватом. Примерами таких солей являются соли с неорганическими кислотами, такими как соляная кислота, бромистый водород, серная кислота, фосфорная кислота или органическими кислотами, такими как уксусная кислота, лимонная кислота, винная кислота, яблочная кислота, янтарная кислота, фумаровая кислота, п-толуолсульфоновая кислота, бензолсульфоновая кислота, метансульфоновая кислота, молочная кислота, аскорбиновая кислота, и т.д. Данные соли могут быть получены из нейтральных соединений известными способами.
В каждом случае предпочтительной формой соли является гидрохлорид. В связи с этим, в частности, может быть упомянута международная публикация WO 2003024916, и ссылка дана специально на нее. Из упомянутых выше солей соединение (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид, описанный в WO 2003024916, является особенно предпочтительным в объеме настоящего изобретения.
Соединения, охарактеризованные формулой I или II, являются частью фармацевтической композиции или лекарственного средства по данному изобретению.
В соответствии с данным изобретением повышенную сократительную активность мочевого пузыря лечат путем введения одного из соединений, фармацевтических композиций или лекарственных средств по данному изобретению.
Лекарственное средство по данному изобретению можно вводить пероральным, ингаляционным, внутривенным или чрескожным путем, или в виде суппозитория. Предпочтительным является пероральное введение.
Для определения оптимальной дозы активного вещества для применения и получения композиции по данному изобретению во внимание должны быть приняты различные параметры, такие как возраст пациента и масса тела, и природа и стадия заболевания, например.
Предпочтительная доза для людей составляет от 0,001 мг до 1 г в день, предпочтительно от 10 мг до 500 мг.
В некоторых случаях может быть достаточной меньшая доза, тогда как в других случаях может быть необходимым гораздо большее количество.
Суммарную дневную дозу можно вводить как единичную дозу или несколькими дозами на протяжении дня в зависимости от схемы лечения. Схема лечения также может предусматривать интервалы между дозами более одного дня.
Для перорального введения пригодны различные фармацевтические препараты, такие как твердые, жидкие, порошкообразные формы, таблетки, таблетки с сахарным покрытием, капсулы, таблетки с покрытием, гранулы, суспензии, растворы, сиропы, таблетки для подъязычного применения или другие формы.
Порошкообразная форма может быть получена, например, измельчением частиц активного вещества до нужного размера. Разбавленные порошки могут быть получены мелким измельчением порошкообразного активного вещества с нетоксическим носителем, таким как лактоза, и получением порошка из этой смеси. Другими подходящими веществами для носителей являются другие углеводы, такие как крахмал или маннит. Эти порошки необязательно могут содержать вкусовые добавки, консерванты, диспергирующие вещества, красители и другие фармацевтические эксципиенты.
Капсулы могут быть получены из порошка упомянутого выше типа или других порошкообразных веществ, которые заключают в капсулу, предпочтительно желатиновую капсулу, после чего капсулу герметично закупоривают.
В капсулу также можно вводить смазывающие вещества, известные из уровня техники, или использовать их для герметизации двух отделов капсулы. Эффективность капсулы при пероральном приеме может быть увеличена добавлением дезинтегрирующих веществ (разрыхлителей) или солюбилизаторов, таких как карбоксиметилцеллюлоза, карбоксиметилцеллюлоза кальция, низкозамещенная гидроксипропилцеллюлоза, карбонат кальция, карбонат натрия и другие вещества. Активное вещество может находиться в капсуле не только как твердое вещество, но и в суспензии, например, в растительном масле, полиэтиленгликоле, глицерине, с использованием поверхностно-активных веществ, и т.д.
Таблетки могут быть получены прессованием порошкообразной смеси и затем преобразованием, например, в форму гранул. Таблетки могут содержать различные эксципиенты, такие как крахмалы, лактозу, сахарозу, глюкозу (например, вагинальные таблетки), хлорид натрия, мочевину для таблеток для растворения или инъецирования, амилозу, различные виды целлюлозы, описанные выше, и так далее. Глицерин или крахмал могут быть использованы, например, в качестве веществ, сохраняющих влагу.
Крахмал, альгиновая кислота, альгинат кальция, пектиновая кислота, порошкообразный агар-агар, формальдегидный желатин, карбонат кальция, бикарбонат натрия, пероксид магния и амилоза могут быть использованы, например, в качестве дезинтегрирующих веществ.
В качестве антидезинтегрирующих веществ или агентов, замедляющих растворение, можно использовать, например, сахарозу, стеарин, твердый парафин (предпочтительно с температурой плавления в интервале 50-52°C); масло какао и гидрогенизированные жиры.
Подходящие ускорители поглощения включают, среди прочего, четвертичные аммонийные соединения, лаурилсульфат натрия и сапонины.
В качестве распределителя связующего может быть использован простой эфир, например, когда агент, используемый для повышения гидрофильности или добавка для ускорения распада, может представлять собой цетиловый спирт, глицеролмоностеарат, крахмал, лактозу и увлажняющие вещества (например, аэрозоль-OT, Pluronics, Tweens) и подобные.
В качестве дополнительных эксципиентов главным образом могут быть использованы следующие вещества: +Аэросил, Аэрозоль-OT этилцеллюлоза, Амберлит-смола, XE-88, Amijel, Амистерол, амилоза, Авицел-микрокристаллическая целлюлоза, бентонит, сульфат кальция, Карбовакс 4000 и 6000, карраген, гидрированное касторовое масло, целлюлоза, микрокристаллическая целлюлоза, декстран, декстрин, фармацевтическая основа для таблеток, каолин, высушенная распылением лактоза (USP), лактосил, стеарат магния, маннит, гранулированный маннит N. F. Метилцеллюлоза, Миглиол 812 нейтральное масло, молочный порошок, лактоза, «nal-tab», непол-амилоза, кристаллический сорбит Pöfizer, пласдон, полиэтиленгликоли, поливинилпирролидон, Прецирол, копытный жир (гидрогенизированный), мягкая основа для таблеток, силикон, стабилин, Sta-rx 1500, силоид, основа для таблеток Валдхофа (Waldhof), таблеттол, цетилат и стеарат талька (talcum cetylatum and stearatum), металлические мыла Тего (Tego), фруктоза и тилоза. Особенно подходят таблетирующий эксципиент K (M25), а также соответствующие требованиям следующих фармакопей: DAB, Ph, Eur, BP и NF.
Также могут быть использованы другие эксципиенты, известные из уровня техники.
Таблетки могут быть получены, например, прямым прессованием. Также можно получать другие препараты для перорального введения, такие как растворы, сиропы, эликсиры и т.д. При необходимости соединение может быть заключено в микрокапсулу.
Парентеральное введение можно осуществлять растворением соединения в жидкости и введением подкожно, внутримышечно или внутривенно с помощью инъекции. Подходящие растворители включают, например, воду или масляную среду.
Для получения суппозиториев, например вагинальных суппозиториев, соединения могут быть составлены в лекарственную форму с веществами с низкой температурой плавления и водорастворимыми или водонерастворимыми, такими как полиэтиленгликоль, кокосовое масло, высшие сложные эфиры (например, меристил, пальмитат) или их смеси.
Для получения препаратов для чрескожного введения могут быть использованы мази, кремы или пластыри.
Краткое описание чертежей
На Фиг.1 показан график, иллюстрирующий действие внутрижелудочного введения этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорида (Соединение 1) на интервал мочеиспускания у находящихся в сознании крыс с гиперактивностью мочевого пузыря, индуцированной PGE2, через 1 час после введения. По оси ординат отложен интервал мочеиспускания (% от исходного), и по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
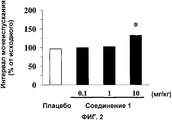
На Фиг.2 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на интервал мочеиспускания у находящихся в сознании крыс с гиперактивностью мочевого пузыря, индуцированной PGE2, через 2 часа после введения. По оси ординат отложен интервал мочеиспускания (% от исходного), и по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
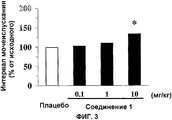
На Фиг.3 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на интервал мочеиспускания у находящихся в сознании крыс с гиперактивностью мочевого пузыря, индуцированной PGE2, через 4 часа после введения. По оси ординат отложен интервал мочеиспускания (% от исходного), и по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
На Фиг.4 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на объем мочеиспускания у находящихся в сознании крыс с гиперактивностью мочевого пузыря, индуцированной PGE2, через 1 час после введения. По оси ординат отложен объем мочеиспускания (% от исходного), и по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
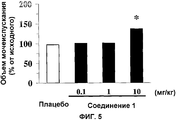
На Фиг.5 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на объем мочеиспускания у находящихся в сознании крыс с гиперактивностью мочевого пузыря, индуцированной PGE2, через 2 часа после введения. По оси ординат отложен объем мочеиспускания (% от исходного), и по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
На Фиг.6 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на объем мочеиспускания у находящихся в сознании крыс с гиперактивностью мочевого пузыря, индуцированной PGE2, через 4 часа после введения. По оси ординат отложен объем мочеиспускания (% от исходного), и по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
На Фиг.7 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на частоту самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения на модели гиперактивности мочевого пузыря, индуцированной повреждением спинного мозга. По оси ординат отложена частота самопроизвольных сокращений (% от исходного), а по оси абсцисс отложены типы лекарственных средств.
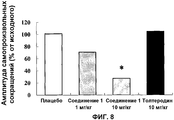
На Фиг.8 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на амплитуду самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения на модели гиперактивности мочевого пузыря с частичной обструкцией нижних мочевых путей. По оси ординат отложена амплитуда самопроизвольных сокращений (% от исходного), а по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
На Фиг.9 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на частоту самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения на модели гиперактивности мочевого пузыря с частичной обструкцией нижних мочевых путей. По оси ординат отложена частота самопроизвольных сокращений (% от исходного), а по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
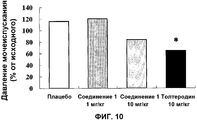
На Фиг.10 показан график, иллюстрирующий действие внутрижелудочного введения Соединения 1 на давление мочеиспускания самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения на модели гиперактивности мочевого пузыря с частичной обструкцией нижних мочевых путей. По оси ординат отложено давление мочеиспускания (% от исходного), а по оси абсцисс отложены типы и дозы (мг/кг) лекарственных средств. Знак * на графике показывает значимое отличие от группы плацебо при p<0,05.
Наилучший способ осуществления изобретения
Действие (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусной кислоты, активного метаболита (-)-этил-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетата, нового бета-3-агониста на изолированный детрузор обезьян и мочевой пузырь крыс.
Приведенные эксперименты демонстрируют действие (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусной кислоты на изолированный детрузор обезьян и мочевой пузырь крыс.
Пример 1
Действия на тонус изолированного детрузора обезьяны
Способ
Детрузор макак циномолгус (обоих полов) изолировали и иссекали. Также были приготовлены препараты трахеи, предсердия и мочеиспускательного канала. Затем изучали действие (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусной кислоты на тонус препарата детрузора. Также исследовали тонические сокращения препаратов трахеи, индуцированных карбахолом, частоту сокращений препаратов предсердий и тонические сокращения препаратов мочеиспускательного канала, индуцированных эндотелином-1, с использованием метода Магнуса (Magnus).
Результаты
(-)-2-[4-(2-{[(1S,2R)-2-Гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусная кислота, а также изопротеренол снижают тонус изолированного детрузора обезьяны. Значения EC50 этих двух веществ составляли 8,2×10-7 M и 1,9×10-7 M соответственно. Не наблюдалось значительного ослабления при использовании двух антимускариновых активных веществ пропиверина или оксибутинина. Изопротеренол уменьшал тоническое сокращение изолированной трахеи, индуцированное карбахолом (функция, стимулируемая бета 2-AR), и увеличивал частоту сокращений изолированного предсердия (функция, стимулируемая бета 1-AR), в каждом случае зависимым от концентрации образом. (-)-2-[4-(2-{[(1S,2R)-2-Гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусная кислота демонстрировала меньший эффект в отношении трахеи и предсердия. Избирательность в отношении детрузора (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусной кислоты была примерно в 1200 раз выше (по сравнению с трахеей) и в 80 раз выше (по сравнению с предсердием). (-)-2-[4-(2-{[(1S,2R)-2-Гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусная кислота не оказывала действия на тоническое сокращение изолированной уретры, индуцированное эндотелином-1.
Пример 2
Эффекты на модели гиперактивности мочевого пузыря, индуцированной простагландином (PG) E2
Способ
Крыс анестезировали фенобарбиталом натрия. Каждую канюлю имплантировали в мочевой пузырь и желудок, проводили под кожей, закрепляли на задней стороне шеи и закрывали. Через семь дней после имплантации канюли определяли цистометрограмму свободно передвигающихся, находящихся в сознании крыс. Физиологический раствор непрерывно вводили по каплям в мочевой пузырь со скоростью 6 мл/час и после стабилизации цитомерических параметров, в мочевой пузырь вместо физиологического раствора непрерывно вводили по каплям физиологический раствор, содержащий PGE2 (60 нмоль/л). После стабильного уменьшения интервала мочеиспускания, установившегося в этих условиях, внутрижелудочно вводили этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид (0 (плацебо), 0,1, 1 или 10 мг/кг как дозы свободного вещества). Цитометрические параметры измеряли в течение 4 часов после введения и выражали в процентах от показателей до введения (0 часов).
Результаты
Введение в мочевой пузырь PGE2 вызвало уменьшение интервала мочеиспускания и повышение объема мочеиспускания. Этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид удлинял интервал мочеиспускания и снижал объем мочеиспускания дозозависимым образом на модели гиперактивности мочевого пузыря у крыс, индуцированной PGE2 (Фиг. 1-6).
Пример 3
Эффекты на модели гиперактивности мочевого пузыря, индуцированной повреждением спинного мозга
Способ
Анестезированным эфиром крысам проводили операции на спинном мозге на уровне Th9-Th10. Каждой крысе в.м. вводили амикацин 10 мг/мышь, в течение 7 дней, и регуляцию мочеиспускания осуществляли 2 раза в день в течение 2 недель для профилактики чрезмерного растяжения мочевого пузыря. Примерно через 6 недель после операции на спинном мозге крыс анестезировали фенобарбиталом натрия и каждую канюлю (PE-50: Nihon Becton Dickinson) имплантировали в мочевой пузырь и желудок, проводили под кожей, закрепляли на задней стороне шеи и закрывали. Через семь дней после имплантации канюли выполняли цитометрограмму. Физиологический раствор вводили по каплям в мочевой пузырь со скоростью 12 мл/час. Введение физиологического раствора останавливали при каждом мочеиспускании. После установления стабильного самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения внутрижелудочно вводили этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид (0 (плацебо) или 10 мг/кг как доза свободного вещества). Измеряли параметр мочеиспускания через час после введения этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорида и выражали как процент от значения этого параметра до введения (0 часов).
Результаты
У крыс с повреждением спинного мозга появлялись самопроизвольные мелкие сокращения мочевого пузыря в фазу наполнения. Этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид снижал частоту самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения на модели гиперактивности мочевого пузыря, индуцированной повреждением спинного мозга (Фиг.7).
Пример 4
Эффекты на модели гиперактивности мочевого пузыря крыс, с частичной обструкцией нижних мочевых путей
Способ
Крыс анестезировали фенобарбиталом натрия. После лигирования мочеиспускательного канала с канюлей (ширина: 1 мм) лигатурой канюлю удаляли. Через шесть недель после операции на нижних мочевых путях имплантированную лигатуру удаляли и каждую канюлю имплантировали в мочевой пузырь и желудок, проводили под кожей, закрепляли на задней стороне шеи и закрывали. На следующий день определяли цитометрограмму свободно передвигающихся находящихся в сознании крыс. Физиологический раствор вводили по каплям в мочевой пузырь со скоростью 12 мл/час. Введение физиологического раствора останавливали при каждом мочеиспускании. После установления стабильного самопроизвольного мелкого сокращения мочевого пузыря в фазу наполнения внутрижелудочно вводили этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид (0 (плацебо), 1 или 10 мг/кг в виде дозы свободного вещества) или толтеродин (10 мг/кг). Параметры мочеиспускания определяли через 1 час после введения этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорида или толтеродина и выражали в виде процентов к значения параметров до введения (0 часов).
Результаты
Самопроизвольное мелкое сокращение мочевого пузыря в фазу наполнения наблюдали у крыс через 6 недель после частичной обструкции нижних мочевых путей. Вводимый внутрижелудочно этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид уменьшал амплитуду и частоту самопроизвольных мелких сокращений мочевого пузыря дозозависимым образом. Эффективность этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорида была выше, чем эффективность толтеродина, антимускаринового лекарственного средства (Фиг. 8 и 9). С другой стороны, этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид не оказывал воздействия на давление мочеиспускания (Фиг.10). Эти результаты показали, что этил(-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид подавляет самопроизвольное мелкое сокращение мочевого пузыря в фазу наполнения, влияя на давление мочеиспускания, и позволили предположить, что данное соединение является эффективным для профилактики и лечения повышенной сократительной функции мочевого пузыря.
Заключение
(-)-2-[4-(2-{[(1S,2R)-2-Гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусная кислота продемонстрировала избирательное действие в отношении детрузора. Кроме того, этил (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид удлинял интервал мочеиспускания, увеличивал объем мочеиспускания и уменьшал амплитуду и частоту самопроизвольных мелких сокращений мочевого пузыря дозо-зависимым образом при внутрижелудочном введении. Показано, что (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат может быть использован в качестве «пролекарства» (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусной кислоты как терапевтического средства для лечения повышенной сократительной функции мочевого пузыря и имеет меньше побочных эффектов, чем активные вещества, известные из уровня техники.
Промышленная применимость
Как описано выше, соединения, представленные выше общей формулой (I) и его фармацевтически приемлемые соли чрезвычайно эффективны для лечения повышенной сократительной функции мочевого пузыря.
Изготовление фармацевтической композиции по изобретению не составляет особого труда для специалиста в данной области и при изготовлении таких композиций могут быть использованы вспомогательные вещества, общепринятые в фармацеи. В качестве примера композиции по изобретению приводится следующий состав, включающий (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид (соединение 1):
| Соединение 1 | 40 мг |
| Маннит, высушенный распылением | 110 мг |
| Кукурузный крахмал | 48 мг |
| Тальк | 2 мг |
Claims (20)
1. Применение соединения общей формулы I или его фармацевтически приемлемой соли для получения лекарственного средства для лечения гиперактивности мочевого пузыря
где Х представляет собой хиральный атом углерода S;
Y представляет собой хиральный атом углерода R;
R1 представляет собой гидроксигруппу или C1-C6-алкоксигруппу;
R2 представляет собой атом водорода;
R3 представляет собой метильную группу; и
R4 представляет собой метильную группу.
2. Применение по п.1, отличающееся тем, что R1 представляет собой гидроксигруппу, метоксигруппу или этоксигруппу; или фармацевтически приемлемую соль.
3. Применение по п.2, отличающееся тем, что
R1 представляет собой гидроксигруппу или этоксигруппу;
или фармацевтически приемлемую соль.
4. Применение по п.1, отличающееся тем, что данное соединение представляет собой фармацевтически приемлемую соль с одной из кислот, выбранных из соляной кислоты, бромистого водорода, серной кислоты, фосфорной кислоты, уксусной кислоты, лимонной кислоты, винной кислоты, яблочной кислоты, янтарной кислоты, фумаровой кислоты, п-толуолсульфоновой кислоты, бензолсульфоновой кислоты, метансульфоновой кислоты, молочной кислоты или аскорбиновой кислоты.
5. Применение по п.1, отличающееся тем, что данное соединение представляет собой (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат, (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид или (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусную кислоту.
6. Применение по п.1, отличающееся тем, что лекарственное средство представляет собой препарат для перорального приема.
7. Применение по п.1, отличающееся тем, что лекарственное средство представляет собой суппозиторий.
8. Применение по п.1, отличающееся тем, что лекарственное средство представляет собой пластырь для чрескожного введения лекарственного средства.
9. Применение по п.1 для получения лекарственного средства для лечения нейрогенной гиперактивности мочевого пузыря.
10. Применение по п.1 для получения лекарственного средства для лечения идиопатической гиперактивности мочевого пузыря.
11. Фармацевтическая композиция для лечения гиперактивности мочевого пузыря, содержащая в качестве активного компонента соединение общей формулы I
где Х представляет собой хиральный атом углерода S;
Y представляет собой хиральный атом углерода R;
R1 представляет собой гидроксигруппу или C1-C6-алкоксигруппу;
R2 представляет собой атом водорода;
R3 представляет собой метильную группу; и
R4 представляет собой метильную группу.
12. Фармацевтическая композиция по п.11, в которой R1 представляет собой гидроксигруппу, метоксигруппу или этоксигруппу; или фармацевтически приемлемую соль.
13. Фармацевтическая композиция по п.12, в которой
R1 представляет собой гидроксигруппу или этоксигруппу;
или фармацевтически приемлемую соль.
14. Фармацевтическая композиция по п.11, в которой данное соединение представляет собой фармацевтически приемлемую соль с одной из кислот, выбранных из соляной кислоты, бромистого водорода, серной кислоты, фосфорной кислоты, уксусной кислоты, лимонной кислоты, винной кислоты, яблочной кислоты, янтарной кислоты, фумаровой кислоты, п-толуолсульфоновой кислоты, бензолсульфоновой кислоты, метансульфоновой кислоты, молочной кислоты или аскорбиновой кислоты.
15. Фармацевтическая композиция по п.11, в которой данное соединение представляет собой (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат, (-)-этил 2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]ацетат гидрохлорид или (-)-2-[4-(2-{[(1S,2R)-2-гидрокси-2-(4-гидроксифенил)-1-метилэтил]амино}этил)-2,5-диметилфенокси]уксусную кислоту.
16. Фармацевтическая композиция по любому из пп.11-15, отличающаяся тем, что композиция представляет собой препарат для перорального приема.
17. Фармацевтическая композиция по любому из пп.11-15, отличающаяся тем, что композиция представляет собой суппозиторий.
18. Фармацевтическая композиция по любому из пп.11-15, отличающаяся тем, что композиция представляет собой пластырь для чрескожного введения лекарственного средства.
19. Фармацевтическая композиция по любому из пп.11-15,
отличающаяся тем, что гиперактивность мочевого пузыря представляет собой нейрогенную гиперактивность мочевого пузыря.
20. Фармацевтическая композиция по любому из пп.11-15, отличающаяся тем, что гиперактивность мочевого пузыря представляет собой идиопатическую гиперактивность мочевого пузыря.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10320084A DE10320084A1 (de) | 2003-05-05 | 2003-05-05 | Verwendung von Phenoxyessigsäurederivaten zur Behandlung der hyperaktiven Blase |
| DE10320084.3 | 2003-05-05 | ||
| DE2003123837 DE10323837A1 (de) | 2003-05-23 | 2003-05-23 | Verwendung von Phenoxyessigsäurederivaten zur Behandlung der hyperaktiven Blase |
| DE10323837.9 | 2003-05-23 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2005137701A RU2005137701A (ru) | 2006-06-10 |
| RU2342133C2 true RU2342133C2 (ru) | 2008-12-27 |
Family
ID=33420009
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005137701/15A RU2342133C2 (ru) | 2003-05-05 | 2004-03-24 | Применение производных феноксиуксусной кислоты для лечения гиперактивности мочевого пузыря |
Country Status (26)
| Country | Link |
|---|---|
| US (1) | US20040229947A1 (ru) |
| EP (1) | EP1620085B1 (ru) |
| JP (1) | JP4602969B2 (ru) |
| KR (1) | KR101052804B1 (ru) |
| AR (1) | AR044169A1 (ru) |
| AT (1) | ATE401878T1 (ru) |
| AU (1) | AU2004236596B2 (ru) |
| BR (1) | BRPI0409980A (ru) |
| CA (1) | CA2524023C (ru) |
| CL (1) | CL2004000952A1 (ru) |
| CY (1) | CY1108425T1 (ru) |
| DE (1) | DE602004015272D1 (ru) |
| DK (1) | DK1620085T3 (ru) |
| ES (1) | ES2309513T3 (ru) |
| IL (1) | IL171713A (ru) |
| MX (1) | MXPA05011862A (ru) |
| MY (1) | MY141756A (ru) |
| NZ (1) | NZ543347A (ru) |
| PE (1) | PE20050524A1 (ru) |
| PL (1) | PL1620085T3 (ru) |
| PT (1) | PT1620085E (ru) |
| RU (1) | RU2342133C2 (ru) |
| SI (1) | SI1620085T1 (ru) |
| TW (1) | TWI351279B (ru) |
| UY (1) | UY28306A1 (ru) |
| WO (1) | WO2004098586A1 (ru) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI356699B (en) * | 2004-11-10 | 2012-01-21 | Kissei Pharmaceutical | Agent for treating interstitial cystitis and agent |
| WO2006123517A1 (ja) * | 2005-04-26 | 2006-11-23 | Kissei Pharmaceutical Co., Ltd. | ヒドロキシノルエフェドリン誘導体塩酸塩の結晶多形 |
| CA2605298A1 (en) * | 2005-04-26 | 2006-11-09 | Kissei Pharmaceutical Co., Ltd. | Crystal of hydroxynorephedrin derivative hydrochloride 1/4 hydrate |
| EP1769792A1 (de) * | 2005-09-30 | 2007-04-04 | Boehringer Ingelheim Pharma GmbH & Co.KG | Verwendung eines beta-3-Adrenozeptor-Agonisten zur Behandlung von Nieren- und Blasenbeschwerden |
| BR112019025636A2 (pt) | 2017-06-06 | 2020-08-25 | Urovant Sciences Gmbh | método para tratar bexiga hiperativa, método para aumentar relaxamento de músculo liso da bexiga, e composição de dosagem unitária farmacêutica |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6262115B1 (en) * | 1995-05-22 | 2001-07-17 | Alza Coporation | Method for the management of incontinence |
| US6720014B1 (en) * | 1997-08-13 | 2004-04-13 | Diversa Corporation | Phytase-containing foodstuffs and methods of making and using them |
| MY126489A (en) * | 1998-07-08 | 2006-10-31 | Kissei Pharmaceutical | Phenoxyacetic acid derivatives and medicinal compositions containing the same |
| DE60041110D1 (de) * | 1999-11-01 | 2009-01-29 | Sumitomo Chemical Co | 6-Hydroxy-5,6-dihydrouracile als Herbizide |
| WO2003024916A1 (fr) * | 2001-09-13 | 2003-03-27 | Kissei Pharmaceutical Co., Ltd. | Cristaux d'un derive d'hydroxynorephedrine |
-
2004
- 2004-03-24 AT AT04722967T patent/ATE401878T1/de active
- 2004-03-24 RU RU2005137701/15A patent/RU2342133C2/ru not_active IP Right Cessation
- 2004-03-24 EP EP04722967A patent/EP1620085B1/en not_active Expired - Lifetime
- 2004-03-24 NZ NZ543347A patent/NZ543347A/en not_active IP Right Cessation
- 2004-03-24 ES ES04722967T patent/ES2309513T3/es not_active Expired - Lifetime
- 2004-03-24 PT PT04722967T patent/PT1620085E/pt unknown
- 2004-03-24 WO PCT/JP2004/004048 patent/WO2004098586A1/en active IP Right Grant
- 2004-03-24 PL PL04722967T patent/PL1620085T3/pl unknown
- 2004-03-24 JP JP2006507687A patent/JP4602969B2/ja not_active Expired - Fee Related
- 2004-03-24 DK DK04722967T patent/DK1620085T3/da active
- 2004-03-24 SI SI200430884T patent/SI1620085T1/sl unknown
- 2004-03-24 DE DE602004015272T patent/DE602004015272D1/de not_active Expired - Lifetime
- 2004-03-24 MX MXPA05011862A patent/MXPA05011862A/es active IP Right Grant
- 2004-03-24 KR KR1020057020792A patent/KR101052804B1/ko not_active IP Right Cessation
- 2004-03-24 AU AU2004236596A patent/AU2004236596B2/en not_active Ceased
- 2004-03-24 BR BRPI0409980-0A patent/BRPI0409980A/pt not_active IP Right Cessation
- 2004-03-24 CA CA2524023A patent/CA2524023C/en not_active Expired - Fee Related
- 2004-03-26 US US10/809,346 patent/US20040229947A1/en not_active Abandoned
- 2004-04-21 TW TW093111093A patent/TWI351279B/zh not_active IP Right Cessation
- 2004-04-30 MY MYPI20041651A patent/MY141756A/en unknown
- 2004-05-04 CL CL200400952A patent/CL2004000952A1/es unknown
- 2004-05-05 PE PE2004000459A patent/PE20050524A1/es not_active Application Discontinuation
- 2004-05-05 AR ARP040101519A patent/AR044169A1/es not_active Application Discontinuation
- 2004-05-05 UY UY28306A patent/UY28306A1/es unknown
-
2005
- 2005-11-01 IL IL171713A patent/IL171713A/en not_active IP Right Cessation
-
2008
- 2008-10-16 CY CY20081101158T patent/CY1108425T1/el unknown
Also Published As
| Publication number | Publication date |
|---|---|
| AR044169A1 (es) | 2005-08-24 |
| CY1108425T1 (el) | 2014-04-09 |
| KR20060009886A (ko) | 2006-02-01 |
| CA2524023A1 (en) | 2004-11-18 |
| DE602004015272D1 (de) | 2008-09-04 |
| EP1620085A1 (en) | 2006-02-01 |
| EP1620085B1 (en) | 2008-07-23 |
| UY28306A1 (es) | 2004-12-31 |
| SI1620085T1 (sl) | 2008-12-31 |
| DK1620085T3 (da) | 2008-11-24 |
| US20040229947A1 (en) | 2004-11-18 |
| MXPA05011862A (es) | 2006-02-17 |
| PL1620085T3 (pl) | 2009-01-30 |
| RU2005137701A (ru) | 2006-06-10 |
| PT1620085E (pt) | 2008-08-07 |
| ES2309513T3 (es) | 2008-12-16 |
| CL2004000952A1 (es) | 2005-03-04 |
| ATE401878T1 (de) | 2008-08-15 |
| JP4602969B2 (ja) | 2010-12-22 |
| NZ543347A (en) | 2008-05-30 |
| BRPI0409980A (pt) | 2006-05-09 |
| CA2524023C (en) | 2011-11-22 |
| JP2006525318A (ja) | 2006-11-09 |
| AU2004236596A1 (en) | 2004-11-18 |
| AU2004236596B2 (en) | 2010-03-11 |
| PE20050524A1 (es) | 2005-07-07 |
| WO2004098586A1 (en) | 2004-11-18 |
| IL171713A (en) | 2011-12-29 |
| MY141756A (en) | 2010-06-30 |
| KR101052804B1 (ko) | 2011-07-29 |
| TW200509902A (en) | 2005-03-16 |
| TWI351279B (en) | 2011-11-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2388466C2 (ru) | Производные феноксиалкилкарбоновых кислот при лечении воспалительных заболеваний | |
| ZA200503282B (en) | Pharmaceutical composition comrpising a beta-3-adrenoceptor agonist and a serotonin and/or norepinephrine reuptake inhibitor and the use of said composition for treating bladder dysfunction | |
| CN113784717A (zh) | 一种治疗肺动脉高压和相关性肺动脉高压的方法以及每日给药 | |
| RU2342133C2 (ru) | Применение производных феноксиуксусной кислоты для лечения гиперактивности мочевого пузыря | |
| US6841575B2 (en) | Use of 1-phenyl-3-dimethylaminopropane compounds for treatment of urinary incontinence | |
| MXPA06004625A (es) | Composicion famaceutica que contiene un agonista de un adrenoceptor beta-3 y un antagonista alfa y/o un inhibidor de la 5-alfa-reductasa. | |
| AU2002223688B2 (en) | Use of substituted 6-dimethylaminomethyl-1-phenyl-cyclohexane compounds for treating urinary incontinence | |
| RU2280444C2 (ru) | Применение 6-диметиламинометил-1-фенилциклогексановых соединений для терапии недержания мочи | |
| CN100518731C (zh) | 苯氧基乙酸衍生物用于制备治疗机能亢进性膀胱的药物 | |
| JP2006525318A5 (ru) | ||
| RU2022119027A (ru) | Фармацевтическая композиция трициклического соединения двойного ингибитора фдэ3/фдэ4 | |
| WO2007018234A1 (ja) | 尿道内圧上昇作用剤 | |
| JP2007509868A (ja) | 緊張性尿失禁及び/又は混合型尿失禁治療用医薬組成物 | |
| SK9772003A3 (sk) | R- a S-enantiomér 2-amino-1-(4-hydroxy-3- metánsulfónamidofenyl)etanolu, farmaceutický prostriedok s ich obsahom a ich použitie |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20130325 |