RU2317980C1 - Способ получения индол-3-карбинола гидрата (варианты) - Google Patents
Способ получения индол-3-карбинола гидрата (варианты) Download PDFInfo
- Publication number
- RU2317980C1 RU2317980C1 RU2006132688/04A RU2006132688A RU2317980C1 RU 2317980 C1 RU2317980 C1 RU 2317980C1 RU 2006132688/04 A RU2006132688/04 A RU 2006132688/04A RU 2006132688 A RU2006132688 A RU 2006132688A RU 2317980 C1 RU2317980 C1 RU 2317980C1
- Authority
- RU
- Russia
- Prior art keywords
- indole
- hydrate
- carbinol
- water
- temperature
- Prior art date
Links
- OMEVEHLSJRKSEF-UHFFFAOYSA-N 1h-indol-3-ylmethanol;hydrate Chemical compound O.C1=CC=C2C(CO)=CNC2=C1 OMEVEHLSJRKSEF-UHFFFAOYSA-N 0.000 title claims abstract description 34
- 238000000034 method Methods 0.000 title claims abstract description 17
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 27
- 238000006243 chemical reaction Methods 0.000 claims abstract description 22
- OLNJUISKUQQNIM-UHFFFAOYSA-N indole-3-carbaldehyde Chemical compound C1=CC=C2C(C=O)=CNC2=C1 OLNJUISKUQQNIM-UHFFFAOYSA-N 0.000 claims abstract description 22
- 239000000126 substance Substances 0.000 claims abstract description 17
- 238000001035 drying Methods 0.000 claims abstract description 9
- 238000001816 cooling Methods 0.000 claims abstract description 6
- 238000010438 heat treatment Methods 0.000 claims abstract description 5
- 238000001953 recrystallisation Methods 0.000 claims abstract description 5
- 238000002955 isolation Methods 0.000 claims abstract description 4
- 238000001556 precipitation Methods 0.000 claims abstract 2
- 229910000033 sodium borohydride Inorganic materials 0.000 claims description 11
- 239000012279 sodium borohydride Substances 0.000 claims description 11
- 125000005233 alkylalcohol group Chemical group 0.000 claims 1
- 239000000047 product Substances 0.000 abstract description 10
- 230000015572 biosynthetic process Effects 0.000 abstract description 5
- 238000003786 synthesis reaction Methods 0.000 abstract description 4
- 239000007795 chemical reaction product Substances 0.000 abstract description 3
- 239000012535 impurity Substances 0.000 abstract description 3
- 239000002904 solvent Substances 0.000 abstract description 3
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 abstract 3
- 238000006722 reduction reaction Methods 0.000 abstract 2
- MOOAHMCRPCTRLV-UHFFFAOYSA-N boron sodium Chemical compound [B].[Na] MOOAHMCRPCTRLV-UHFFFAOYSA-N 0.000 abstract 1
- 150000001875 compounds Chemical class 0.000 abstract 1
- 238000002425 crystallisation Methods 0.000 abstract 1
- 230000008025 crystallization Effects 0.000 abstract 1
- 230000003247 decreasing effect Effects 0.000 abstract 1
- 230000000694 effects Effects 0.000 abstract 1
- IVYPNXXAYMYVSP-UHFFFAOYSA-N indole-3-methanol Chemical compound C1=CC=C2C(CO)=CNC2=C1 IVYPNXXAYMYVSP-UHFFFAOYSA-N 0.000 description 30
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 238000001228 spectrum Methods 0.000 description 14
- 235000002279 indole-3-carbinol Nutrition 0.000 description 13
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 239000000203 mixture Substances 0.000 description 10
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- 238000004519 manufacturing process Methods 0.000 description 6
- 239000008194 pharmaceutical composition Substances 0.000 description 6
- TWJAXIHBWPVMIR-UHFFFAOYSA-N diindolylmethane Natural products C1=CC=C2NC(CC=3NC4=CC=CC=C4C=3)=CC2=C1 TWJAXIHBWPVMIR-UHFFFAOYSA-N 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- 238000004809 thin layer chromatography Methods 0.000 description 5
- VFTRKSBEFQDZKX-UHFFFAOYSA-N 3,3'-diindolylmethane Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4NC=3)=CNC2=C1 VFTRKSBEFQDZKX-UHFFFAOYSA-N 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- -1 grinders Substances 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 235000002639 sodium chloride Nutrition 0.000 description 3
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 2
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 239000011782 vitamin Substances 0.000 description 2
- 229930003231 vitamin Natural products 0.000 description 2
- 229940088594 vitamin Drugs 0.000 description 2
- 235000013343 vitamin Nutrition 0.000 description 2
- RGHNJXZEOKUKBD-NRXMZTRTSA-N (2r,3r,4r,5s)-2,3,4,5,6-pentahydroxyhexanoic acid Chemical compound OC[C@H](O)[C@@H](O)[C@@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-NRXMZTRTSA-N 0.000 description 1
- WNWHHMBRJJOGFJ-UHFFFAOYSA-N 16-methylheptadecan-1-ol Chemical class CC(C)CCCCCCCCCCCCCCCO WNWHHMBRJJOGFJ-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 240000007124 Brassica oleracea Species 0.000 description 1
- 235000003899 Brassica oleracea var acephala Nutrition 0.000 description 1
- 235000011299 Brassica oleracea var botrytis Nutrition 0.000 description 1
- 235000011301 Brassica oleracea var capitata Nutrition 0.000 description 1
- 235000004221 Brassica oleracea var gemmifera Nutrition 0.000 description 1
- 235000017647 Brassica oleracea var italica Nutrition 0.000 description 1
- 235000001169 Brassica oleracea var oleracea Nutrition 0.000 description 1
- 240000003259 Brassica oleracea var. botrytis Species 0.000 description 1
- 244000308368 Brassica oleracea var. gemmifera Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 239000001828 Gelatine Substances 0.000 description 1
- 241000206672 Gelidium Species 0.000 description 1
- 239000004705 High-molecular-weight polyethylene Substances 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 244000269722 Thea sinensis Species 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 235000012216 bentonite Nutrition 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 235000010216 calcium carbonate Nutrition 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- PBAYDYUZOSNJGU-UHFFFAOYSA-N chelidonic acid Natural products OC(=O)C1=CC(=O)C=C(C(O)=O)O1 PBAYDYUZOSNJGU-UHFFFAOYSA-N 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 239000013065 commercial product Substances 0.000 description 1
- 239000012084 conversion product Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- IDGUHHHQCWSQLU-UHFFFAOYSA-N ethanol;hydrate Chemical compound O.CCO IDGUHHHQCWSQLU-UHFFFAOYSA-N 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 239000012259 ether extract Substances 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 230000022244 formylation Effects 0.000 description 1
- 238000006170 formylation reaction Methods 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 235000009569 green tea Nutrition 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- GBMDVOWEEQVZKZ-UHFFFAOYSA-N methanol;hydrate Chemical compound O.OC GBMDVOWEEQVZKZ-UHFFFAOYSA-N 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- OIPZNTLJVJGRCI-UHFFFAOYSA-M octadecanoyloxyaluminum;dihydrate Chemical compound O.O.CCCCCCCCCCCCCCCCCC(=O)O[Al] OIPZNTLJVJGRCI-UHFFFAOYSA-M 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 150000002895 organic esters Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 235000011083 sodium citrates Nutrition 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
Images
Landscapes
- Indole Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
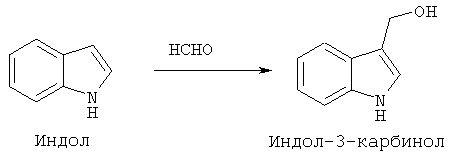
Изобретение относится к способам (вариантам) получения стабильной формы индол-3-карбинола гидрата. Индол-3-карбинола гидрат является известным соединением, используемым в фармацевтической промышленности. Способ получения индол-3-карбинол гидрата путем восстановления индол-3-карбоксальдегида боргидридом натрия в среде C1-С3 алкилового спирта. К полученной реакционной массе прибавляют воду и выдерживают при пониженной температуре до полного его выпадения с последующей сушкой при температуре окружающей среды. Либо из полученной после восстановления реакционной массы выделяют продукт и проводят перекристаллизацию из воды или водного C1-С3 алкилового спирта при слабом нагревании с последующим охлаждением и выдержкой полученного раствора при температуре, близкой к нулевой, и сушкой при температуре окружающей среды. При необходимости полученный индол-3-карбинол гидрат дополнительно перекристаллизовывают из воды или водного C1-С3 алкилового спирта с выдержкой полученного раствора при температуре от +3°С до -18°С и сушкой при температуре окружающей среды. Способы позволяют получить продукт с повышенной стабильностью и исключить нежелательные примеси побочных продуктов превращения и растворителей, используемых при перекристаллизации. 2 н. и 1 з.п. ф-лы, 7 ил.
Description
Данное изобретение относится к способу получения индол-3-карбинола гидрата. Более конкретно, настоящее изобретение относится к способу получения индол-3-карбинола гидрата, пригодного для использования в качестве субстанции в фармацевтических композициях и лекарственных препаратах для профилактики и лечения онкологических заболеваний.
Индол-3-карбинол является природным соединением, выделенным из капусты качанной, броколи, брюссельской капусты и зеленого чая. Его синтетический аналог получают восстановлением индол-3-карбоксальдегида с последующим выделением индол-3-карбинола из реакционной массы и перекристаллизацией из подходящего органического растворителя: диэтилового эфира [Le, B.M.; Pascal, M.; Muriel, D.; Benedicte, D.-S.; Sylvie, P.-R.; et al. Arch. Pharm. (Weinheim Ger.), 1997, 330(5), 141-145], пентана [Henry; Leete. J. Am. Chem. Soc., 1957, 79, 5254], этанола [Thesing, J. Chem. Ber., 1954, 87, 692-696] или бензола [Madinaveitia. Chem. Soc., 1937, 1927-1929. Leete; Marion. Can. J. Chem., 1953, 31, 775-777. Runti.; Gazz. Chim. Ital., 1951, 81, 613-618.].
Однако полученный известными способами индол-3-карбинол не может использоваться в качестве субстанции для получения фармацевтических композиций, так как он сильно лабилен и/или содержит примеси бензола в недопустимых количествах.
Известен способ получения индол-3-карбинол формилированием индола [Плихтяк И.Л.; Ярцева И.В.; Александрова Л.Г.; Подхалюзина Н.Я.; Преображенская М.Н. Хим. Фарм. Ж., 1991, 25 (6), 57-58]. Продукт реакции авторы экстрагируют эфиром и после отгонки эфира получают ИЗК в виде темного масла.
Однако приведенный в данной работе ПМР спектр полученного продукта не соответствует ПМР спектру индол-3-карбинола. Кроме того, мы воспроизвели приведенную в указанной работе методику формилирования индола и получили (как и авторы) маслообразный продукт, содержащий продукты превращения индол-3-карбинола и не содержащий, собственно, индол-3-карбинол. Как видно из этой хроматограммы (фиг.1), продукт реакции не содержит индол-3-карбинол, а содержит продукты его превращения, в частности дииндолилметан.
Известен способ получения индол-3-карбинола (WO 9850357 A2, опубл. 12.11.1998) восстановлением индол-3-карбоксальдегида боргидридом натрия в метаноле с последующим добавлением воды, охлаждением до 0°С, фильтрацией и сушкой в вакуум-эксикаторе при отсутствии света.
При использовании вакуума для осушки индол-3-карбинола происходит частичная или полная потеря воды исходного гидрата, что отрицательно сказывается на хранении вещества и его чистоте.
Недавно было предложено использовать для получения фармацевтических композиций в качестве субстанции индол-3-карбинол гидрат, обладающий повышенной стабильностью по сравнению с безводным индол-3-карбинолом [Заявка РФ №2006130506, приоритет 24.08.06].
Индол-3-карбинол гидрат является коммерческим продуктом (Акрос, Бельгия). Однако продукт этой фирмы не может использоваться в качестве субстанции, так как содержит в качестве примесей заметное количество толуола и бензола, обнаруженного при его исследовании независимой лабораторией (ЕСА, Analytikal Testing Report, 8-15-06). Следует отметить, что в научной и патентной литературе до настоящего времени отсутствовали сведения о способе получения индол-3-карбинол гидрата, пригодного для использования в качестве субстанции при получении фармацевтических композиций.
«Фармацевтическая композиция» обозначает композицию, включающую, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, витамины, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки, и/или активную субстанцию, представляющую собой, по крайней мере, один хемотерапевтический агент (физиологически активное химическое вещество). Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, витамины, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активное начало, одно или в комбинации с другим активным началом, может быть введено животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
Целью настоящего изобретения является создание нового способа получения индол-3-карбинола гидрата.
Поставленная цель достигается способом получения индол-3-карбинола гидрата путем восстановления индол-3-карбоксальдегида боргидридом натрия в среде низшего спирта с последующим выделением и перекристаллизацией целевого продукта из воды или водного низшего спирта.
Поставленная цель также достигается способом получения индол-3-карбинола гидрата путем восстановления индол-3-карбоксальдегида боргидридом натрия в среде низшего спирта с последующим прибавлением к реакционной массе воды и выдерживанием образующегося раствора при пониженной температуре, предпочтительно в интервале от плюс 5°С до минус 18°С.
Получаемый по настоящему способу индол-3-карбинола гидрат содержит от 0,2 до 5 молекул воды на одну молекулу индол-3-карбинола, причем количество воды в молекуле зависит от способа сушки, например, моно- (I3C·H2O), ди- (I3C·2H2O) и три-(I3C·3H2O) гидраты, образуются при сушке на воздухе.
Изобретение поясняется чертежами:
на фиг.1 представлена фотография тонкослойной хроматогарафии на силикагеле смесью этилацетет: гексан (1:3): 1-индол-3-карбинола (I3C), 2 - дииндолилметана (DIM), 3 - реакционная масса до нагрева (R-1), 4 - реакционная масса после нагрева (R-2), 5 - смесевая проба (R-1+DIM), 6 - смесевая проба (R-1+I3C), 7 - смесевая проба (R-2+DIM) и 8 - смесевая проба;
на фиг.2 представлен ПМР спектр (SGV-0726) в CDCl3;
на фиг.3 ПМР спектр (NMRSGV-0750) полученного индол-3-карбинола гидрата;
на фиг.4 ПМР спектр (NMRSGV-0756) полученного индол-3-карбинола гидрата;
на фиг.5 ПМР спектр (NMRSGV-0757) полученного индол-3-карбинола гидрата;
на фиг.6 ПМР спектр (SGV 0798) полученного индол-3-карбинола гидрата;
на фиг.7 ПМР спектр (SGV 0804) полученного индол-3-карбинола гидрата.
Ниже приводятся конкретные примеры, которые иллюстрируют, но не ограничивают данное изобретение.
Пример 1. Прибавляют при перемешивании 150 г (3.95 мол) боргидрида натрия к 1000 мл метанола, охлажденного льдом. Затем прибавляют 150 г (1.03 мол) индол-3-ил карбальдегида и выдерживают реакционную массу 2 часа при комнатной температуре. Реакционную массу разбавляют 1000 мл воды и экстрагируют трижды по 800 мл эфиром. Объединенные эфирные вытяжки сушат сульфатом натрия и упаривают в вакууме. Получают 116 г продукта с т.пл. 95-96°С. ПМР спектр (SGV-0726) в CDCl3 (фиг.2) свидетельствует о примерном содержание 0,2 молекулы воды на одну молекулу спирта и содержании основного вещества >97%. Растворяют 27.8 г полученного продукта в 3,4 л воды при температуре ниже 40°С. Полученный раствор охлаждают 4 часа при температуре 3-4°С, выпавшие кристаллы отфильтровывают и получают 1,2 г индол-3-карбинола гидрат с т.пл. 95-96°С. Спектр ПМР (NMRSGV-0748) после высушивания на воздухе в течение 48 часов (фиг.3) свидетельствует о содержание целевого продукта ~85%.
Пример 2. К суспензии 200 г (1.38 мол) индол-3-карбальдегида в 1400 мл метанола при охлаждении льдом прибавляют в несколько приемов при интенсивном перемешивании 26 г (0.69 мол) боргидрида натрия. Через 10-15 минут после прибавления всего боргидрида натрия и полного перехода осадка альдегида в раствор проводят контроль реакционной массы методом тонкослойной хроматографии на силикагеле (CHCl3:МеОН 19:1). В случаях, когда в реакционной массе присутствовал в небольшом количестве (<10%) исходный альдегид (Rf=0,72 для индол-3-карбоксальдегида, Rf=0,6 для индол-3-карбинола), к реакционной массе добавляют дополнительно 2.6 г (0.07 моль) боргидрида натрия и смесь выдерживают при перемешивании в течение получаса до завершения реакции (контроль ТСХ). Полученную реакционную массу, представляющую собой прозрачный окрашенный в желтый цвет раствор, разбавляют 2000 мл воды и оставляют на сутки в холодильнике (при температуре 3-4°С). Осадок фильтруют и сушат 48 часов на воздухе. Получают 111,4 г (56%) индол-3-карбинола гидрата в виде слегка желтоватых пластинок с т.пл. 96-98°С. ПМР спектр (NMRSGV-0756) полученного индол-3-карбинола гидрата (фиг.4) свидетельствует о примерном содержание 0,5 молекулы воды на одну молекулу спирта и содержании основного вещества >97%.
Пример 3. Синтез проводят, как описано в примере 2. Реакционную массу, полученную после завершения реакции, упаривают досуха в вакууме при температуре ниже 40°С. Получают 402 г кристаллического продукта, который перекристаллизовывают из воды, для чего 15 г полученного продукта растворяют в 2 л воды при слабом нагревании (температура водяной бани не выше 40°С). Полученный раствор выдерживают 4 ч при 3-4°С, выпавший осадок отфильтровывают и сушат на воздухе 48 ч. Получают 4,5 г индол-3-карбинола гидрата (60%) с т.пл. 97-99°С. ПМР спектр (NMRSGV-0757) полученного индол-3-карбинола гидрата (фиг.5) свидетельствует о примерном содержание 0,5 молекулы воды на одну молекулу спирта и содержании основного вещества >95%.
Пример 4. К суспензии 100 г (0,69 мол) индол-3-карбальдегида в 400 мл метанола при охлаждении льдом прибавляют в несколько приемов при интенсивном перемешивании 13 г (0.345 мол) боргидрида натрия. После завершения реакции (контроль ТСХ) в реакционную массу добавляют 600 мл воды, 5 г активированного угля, перемешивают 10 мин и фильтруют. Фильтрат выдерживают 12 ч при -18°С, выпавший осадок отфильтровывают и сушат на воздухе. Получают 96 г (95%) индол-3-карбинола гидрата в виде белых блестящих пластинок с т.пл. 95-96°С. Спектр (SGV 0798) полученного индол-3-карбинола гидрата (фиг.6), свидетельствует о примерном содержание 0,5 молекулы воды на одну молекулу спирта и содержании основного вещества >95%.
Пример 5. К суспензии 100 г (0,69 мол) индол-3-карбальдегида в 400 мл метанола при охлаждении льдом прибавляют в несколько приемов при интенсивном перемешивании 13 г (0.345 мол) боргидрида натрия. После завершения реакции (контроль ТСХ) в реакционную массу добавляют 600 мл воды, 5 г активированного угля, перемешивают 10 мин и фильтруют. Из фильтрата отгоняют в вакууме метанол, а в водном остатке растворяют 120 г NaCl, полученный раствор выдерживают 12 ч при 3°С, отфильтровывают, промывают холодной водой и сушат на воздухе. Получают 77,6 г (76%) индол-3-карбинола гидрата с т.пл. 95-96°С в виде светло-желтых блестящих пластинок.
При необходимости полученный индол-3-карбинола гидрат дополнительно можно очистить способами, приведенными в примерах 6 и 7.
Пример 6. Растворяют 90 г индол-3-карбинола гидрата, полученного по примеру 4, в 13,5 л смеси метанол-вода (2:3, рН 8). Полученный раствор выдерживают 30 мин, отфильтровывают, фильтрат выдерживают 12 ч при -18°С, отфильтровывают и сушат на воздухе. Получают 60,3 г (67%) индол-3-карбинола гидрата с т.пл. 95-96°С в виде белых блестящих пластинок. Спектр ПМР (SGV 0804) полученного индол-3-карбинола гидрата (фиг.7) свидетельствует о примерном содержание 0,5 молекулы воды на одну молекулу спирта и содержании основного вещества >98%.
Пример 7. Растворяют 1 г индол-3-карбинола гидрата, полученного по примеру 4, в 15 мл смеси этанол-вода (1:12, рН 8). Полученный раствор выдерживают 30 мин, отфильтровывают, фильтрат выдерживают 12 ч при -18°С, отфильтровывают и сушат на воздухе. Получают 0,65 г (65%) индол-3-карбинола гидрата с т.пл. 95-96°С в виде белых блестящих пластинок.
Claims (3)
1. Способ получения индол-3-карбинол гидрата путем восстановления индол-3-карбоксальдегида боргидридом натрия в среде C1-С3 алкилового спирта, с последующим прибавлением к реакционной массе воды, отличающийся тем, что полученный раствор выдерживают при пониженной температуре до полного выпадения вещества и сушат его при температуре окружающей среды.
2. Способ получения индол-3-карбинол гидрата путем восстановления индол-3-карбоксальдегида боргидридом натрия в среде C1-С3 алкилового спирта, с последующим выделением и перекристаллизацией целевого продукта, отличающийся тем, что перекристаллизацию проводят из воды или водного C1-С3 алкилового спирта при слабом нагревании, с последующим охлаждением и выдержкой полученного раствора при температуре близкой к нулевой и сушкой при температуре окружающей среды.
3. Способ по п.1 или 2, отличающийся тем, что при необходимости полученный индол-3-карбинол гидрат перекристаллизовывают из воды или водного C1-С3 алкилового спирта выдержкой полученного раствора при температуре от 3 до -18°С и сушкой при температуре окружающей среды.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2006132688/04A RU2317980C1 (ru) | 2006-09-13 | 2006-09-13 | Способ получения индол-3-карбинола гидрата (варианты) |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2006132688/04A RU2317980C1 (ru) | 2006-09-13 | 2006-09-13 | Способ получения индол-3-карбинола гидрата (варианты) |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2317980C1 true RU2317980C1 (ru) | 2008-02-27 |
Family
ID=39278937
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2006132688/04A RU2317980C1 (ru) | 2006-09-13 | 2006-09-13 | Способ получения индол-3-карбинола гидрата (варианты) |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2317980C1 (ru) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103864666A (zh) * | 2014-03-04 | 2014-06-18 | 苏州明锐医药科技有限公司 | 巴多昔芬中间体及其制备方法 |
| RU2760000C1 (ru) * | 2021-03-24 | 2021-11-22 | Общество с ограниченной ответственностью "Научно-внедренческий центр Агроветзащита" | Способ получения индол-3-карбинола |
| RU2772604C1 (ru) * | 2021-07-06 | 2022-05-23 | Всеволод Иванович Киселев | Способ получения индол-3-карбинола (варианты) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998050357A2 (en) * | 1997-03-07 | 1998-11-12 | The Texas A & M University System | Substituted analogs of indole-3-carbinol and of diindolymethane as antiestrogens |
-
2006
- 2006-09-13 RU RU2006132688/04A patent/RU2317980C1/ru not_active IP Right Cessation
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998050357A2 (en) * | 1997-03-07 | 1998-11-12 | The Texas A & M University System | Substituted analogs of indole-3-carbinol and of diindolymethane as antiestrogens |
Non-Patent Citations (1)
| Title |
|---|
| THESING JAN Chemistry of indole. III. The effect of alcali on quaternary salts of gramine, Chem. Ber., 1954, 87, 692-9. CHOUDARY BOYAPATI MANORANJAN et al. Selective reduction of aldehydes to alcohole by calcined Ni-Al hydrocalite J. of Moleculare Catalisis A:Chemical, 2003, 206 (1-2), 145-151. ПЛИХТЯК И.Л. и др. 3-гидроксиметилирование индолов и синтез аскорбигенов. - Химико-фармацевтический журнал, 1991, 25(6), 56-59. * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103864666A (zh) * | 2014-03-04 | 2014-06-18 | 苏州明锐医药科技有限公司 | 巴多昔芬中间体及其制备方法 |
| CN103864666B (zh) * | 2014-03-04 | 2016-04-06 | 苏州明锐医药科技有限公司 | 巴多昔芬中间体及其制备方法 |
| RU2760000C1 (ru) * | 2021-03-24 | 2021-11-22 | Общество с ограниченной ответственностью "Научно-внедренческий центр Агроветзащита" | Способ получения индол-3-карбинола |
| RU2772604C1 (ru) * | 2021-07-06 | 2022-05-23 | Всеволод Иванович Киселев | Способ получения индол-3-карбинола (варианты) |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0702010A1 (fr) | Nouveaux dérivés du benzopyrane, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| FI91748C (fi) | Menetelmä terapeuttisesti käyttökelpoisten kinolinonijohdannaisten valmistamiseksi | |
| JPH07505897A (ja) | フィブリノーゲンレセプター拮抗剤としての1‐ピペラジン酢酸誘導体 | |
| CN105924362B (zh) | 芳香环丙基胺类化合物、其药学上可接受的盐、其制备方法及其用途 | |
| JPH072770A (ja) | 新規な置換インドール類、その製造法及びそのインドール類を含有する製剤組成物 | |
| EP1118610B1 (fr) | Nouveaux dérivés de benzènesulfonamide, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| EA017631B1 (ru) | Кристаллическое основание транс-1-((1r,3s)-3-фенил-6-хлороиндан-1-ил)-3,3-диметилпиперазина | |
| RU2317980C1 (ru) | Способ получения индол-3-карбинола гидрата (варианты) | |
| LT3675B (en) | Indenoindole copounds ii, process for preraring them and pharmaceutical composition containing them | |
| FI63402B (fi) | Foerfarande foer framstaellning av nya terapeutiskt anvaendbara d- och d1-trans-5-fenyl-2,3,4,4a 5,9b-hexahydro-1h-pyrido(4,3-b)indolderivat | |
| EP0591027A1 (fr) | Dérivés de pipéridine, leur préparation et leur application en thérapeutique | |
| WO2003037904A1 (fr) | NOUVEAUX DERIVES AMIDES HETEROAROMATIQUES DE 3β-AMINO AZABICYCLOOCTANE, LEUR PROCEDE DE PREPARATION ET LEURS APPLICATIONS EN THERAPEUTIQUE | |
| EP3022177B1 (en) | Indole-3-carbinol derivatives | |
| FR2758329A1 (fr) | Derives d'imidazole-4-butane boronique, leur preparation et leur utilisation en therapeutique | |
| HU211579A9 (en) | 2-amino-5-cyano-1,4-dihydropyridines, and their use in medicaments | |
| US5071858A (en) | Antipsychotic benzothiopyranylamines | |
| EP2917204B1 (fr) | Derives de 1h-indole-3-carboxamide et leurs utilisation comme antagonistes du p2y12 | |
| FR2753970A1 (fr) | Derives de n-(benzothiazol-2-yl) piperidine-1-ethanamine, leur preparation et leur application en therapeutique | |
| JP5406194B2 (ja) | R−ゴシポールl−フェニルアラニノールジエナミンを調製するための方法 | |
| CN110698445A (zh) | 一类3-胺烷基苯酞类化合物、其制备方法和用途 | |
| CN110698411A (zh) | 一类4-(胺烷基)酞嗪-1-酮类化合物、其制备方法和用途 | |
| US5296497A (en) | 3,4-dehydropiperidine derivatives having psychotropic activity | |
| CN111592520A (zh) | 一类4,5-二取代基胡椒碱衍生物及其制备方法和应用 | |
| HU193619B (en) | Process for producing allyl-amine derivatives | |
| EA029363B1 (ru) | Фармацевтические составы, содержащие 3-(4-циннамил-1-пиперазинил)аминопроизводные 3-формил рифамицина sv и 3-формил рифамицина s, и способ их получения |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20090914 |