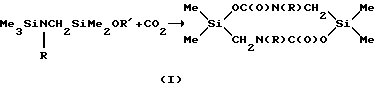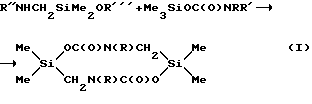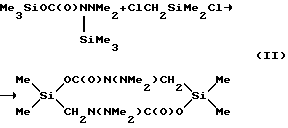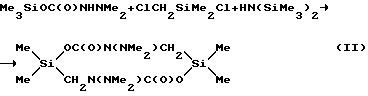RU2215744C1 - Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиаз адисилецин-5,10(2h,7h)-диона - Google Patents
Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиаз адисилецин-5,10(2h,7h)-диона Download PDFInfo
- Publication number
- RU2215744C1 RU2215744C1 RU2002116749A RU2002116749A RU2215744C1 RU 2215744 C1 RU2215744 C1 RU 2215744C1 RU 2002116749 A RU2002116749 A RU 2002116749A RU 2002116749 A RU2002116749 A RU 2002116749A RU 2215744 C1 RU2215744 C1 RU 2215744C1
- Authority
- RU
- Russia
- Prior art keywords
- dione
- tetrahydro
- tetramethyl
- dimethylamino
- bis
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 11
- AQPLOKQXZWJNSZ-UHFFFAOYSA-N 4,9-bis(dimethylamino)-2,2,7,7-tetramethyl-1,6,4,9,2,7-dioxadiazadisilecane-5,10-dione Chemical compound C[Si]1(OC(N(C[Si](OC(N(C1)N(C)C)=O)(C)C)N(C)C)=O)C AQPLOKQXZWJNSZ-UHFFFAOYSA-N 0.000 title claims abstract description 5
- FFUAGWLWBBFQJT-UHFFFAOYSA-N hexamethyldisilazane Chemical compound C[Si](C)(C)N[Si](C)(C)C FFUAGWLWBBFQJT-UHFFFAOYSA-N 0.000 claims abstract description 8
- 239000000203 mixture Substances 0.000 claims abstract description 6
- 238000009835 boiling Methods 0.000 claims abstract 2
- ITKVLPYNJQOCPW-UHFFFAOYSA-N chloro-(chloromethyl)-dimethylsilane Chemical compound C[Si](C)(Cl)CCl ITKVLPYNJQOCPW-UHFFFAOYSA-N 0.000 claims description 6
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 abstract description 3
- 239000000126 substance Substances 0.000 abstract description 3
- 230000003993 interaction Effects 0.000 abstract description 2
- 239000007795 chemical reaction product Substances 0.000 abstract 1
- BHLKIZCNPYDMOY-UHFFFAOYSA-N chloromethyl(dimethyl)silane Chemical compound C[SiH](C)CCl BHLKIZCNPYDMOY-UHFFFAOYSA-N 0.000 abstract 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 abstract 1
- 238000006243 chemical reaction Methods 0.000 description 4
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 4
- UUJLAXMSGWSEIY-UHFFFAOYSA-N 1,4,2,5-diazadisilinane Chemical class C1N[SiH2]CN[SiH2]1 UUJLAXMSGWSEIY-UHFFFAOYSA-N 0.000 description 3
- -1 derivatives of 4 Chemical class 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 230000035484 reaction time Effects 0.000 description 3
- 239000002253 acid Substances 0.000 description 2
- 150000004657 carbamic acid derivatives Chemical class 0.000 description 2
- 239000005051 trimethylchlorosilane Substances 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 235000013877 carbamide Nutrition 0.000 description 1
- 230000021523 carboxylation Effects 0.000 description 1
- 238000006473 carboxylation reaction Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- UQEAIHBTYFGYIE-UHFFFAOYSA-N hexamethyldisiloxane Chemical compound C[Si](C)(C)O[Si](C)(C)C UQEAIHBTYFGYIE-UHFFFAOYSA-N 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000006257 total synthesis reaction Methods 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
- 150000003673 urethanes Chemical class 0.000 description 1
Abstract
Описывается способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10(2Н, 7Н)-диона, заключающийся во взаимодействии О-силилуретана общей формулы Me3SiOC(О)NRR', где R= H, SiMe3; R'= NMe2, с диметилхлорметилсиланом или смесью его с гексаметилдисилазаном при кипячении в течение 30-40 мин. Техническим результатом является упрощение процесса и повышение выхода целевого продукта.
Description
Предлагаемое изобретение относится к области синтеза производных 2,5-дисилапиперазинов, а именно ранее неизвестного 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазасилецин-5,10(2Н, 7Н)-диона, для получения кремнийсодержащих карбаминоилхлоридов, используемых при получении уретанов, мочевин, биологически активных продуктов (А.Д. Кирилин, В.Д. Шелудяков, В.Ф. Миронов. А.с. 527436, 1976).
Известен способ получения производных 2,5-дисилапиперазина, близких по составу и строению соединений, а именно производных 4,9-диаза-2,7-диокса-1,6-дисилациклодекан-3,8-диона, путем карбоксилирования карбаминосиланов.
Время реакции составляет 3÷5 часов, выход целевого продукта 88,4÷96,8% (А.Д. Кирилин, В.Д. Шелудяков, В.Ф. Миронов. A.с. СССР 499266).
Наиболее близким по технической сущности и достигаемому результату является способ получения производных 2,5-дисилапиперазина, а именно производных 4,9-диаза-2,7-диокса-1,6-дисилациклодекан-3,8-диона (А.Д. Кирилин, В. Д. Шелудяков, И. Б. Кокурочинкова, В.Ф. Миронов. А.с. СССР 615083), заключающийся во взаимодействии карбаматов общей формулы Me3SiOC(O)NRR' (где R= R'=Et) с аминометилдиметилалкоксисиланами при нагревании.
Время реакции составляет 8÷10 часов, а выход целевого продукта 87÷96,8%.
Недостатком метода является низкий выход целевого продукта, который объясняется необходимостью синтеза исходных аминометилдиметилалкоксисиланов двухстадийным методом:
ClCH2SiMe2Cl+R'''OH-->ClCH2SiMe2OR'''+HCl - (1)
ClCH2SiMe2OR'''+2R''NH2-->R"NHCH2SiMe2OR'''+R''NH2HCl - (2)
Суммарное время синтеза аминометилдиметилалкоксисилана составляет 32-42 часа (реакция 1 - 2 часа, реакция 2 - 30+40 часов), а выход не превышает 40%, считая на исходный диметилхлорметилхлорсилан (E.С. Родионов, Дисс. канд. хим. наук, М., ГНИИХТЭОС, 1973, 173с.).
ClCH2SiMe2Cl+R'''OH-->ClCH2SiMe2OR'''+HCl - (1)
ClCH2SiMe2OR'''+2R''NH2-->R"NHCH2SiMe2OR'''+R''NH2HCl - (2)
Суммарное время синтеза аминометилдиметилалкоксисилана составляет 32-42 часа (реакция 1 - 2 часа, реакция 2 - 30+40 часов), а выход не превышает 40%, считая на исходный диметилхлорметилхлорсилан (E.С. Родионов, Дисс. канд. хим. наук, М., ГНИИХТЭОС, 1973, 173с.).
Целью настоящего изобретения является упрощение процесса и повышение выхода целевого продукта.
Поставленная цель достигается путем использования в реакции с карбаматами общей формулы Me3SiOC(O)NRR' (где R=H, SiMe3; R'=NМе2) диметилхлорметилхлорсилана или его смеси с гексаметилдисилазаном.
Процесс осуществляют путем нагревания исходных веществ до прекращения выделения триметилхлорсилана. Время реакции 30÷40 минут. Выход целевого продукта составляет 97÷98%.
Пример 1
К смеси 15,65 г (0,0888 моль) триметилсилилового эфира N,N-диметилкарбазиновой кислоты, 11,46 г (0,0710 моль) гексаметилдисилазана и 60 мл абсолютного гексана добавляли при перемешивании 25,41 г (0,1776 моль) диметилхлорметилхлорсилана. Кипятили 30 минут. Растворитель удалили. Получили 13,86 г (97,4%) 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10(2Н, 7Н)-диона с Т пл = 103-105oС. ИК-спектр, см-1: 1670 (С= O). ПМР-спектр (δ, м.д.): 0,13 (SiMe3), 2.57 (NMe2). Найдено, %: С 45,01; Н 8,85; N 8,91; Si 17,73. C12H28O4N2Si2 Вычислено, % С: 44,97; Н 8,81;N 8,74; Si 17,52.
К смеси 15,65 г (0,0888 моль) триметилсилилового эфира N,N-диметилкарбазиновой кислоты, 11,46 г (0,0710 моль) гексаметилдисилазана и 60 мл абсолютного гексана добавляли при перемешивании 25,41 г (0,1776 моль) диметилхлорметилхлорсилана. Кипятили 30 минут. Растворитель удалили. Получили 13,86 г (97,4%) 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10(2Н, 7Н)-диона с Т пл = 103-105oС. ИК-спектр, см-1: 1670 (С= O). ПМР-спектр (δ, м.д.): 0,13 (SiMe3), 2.57 (NMe2). Найдено, %: С 45,01; Н 8,85; N 8,91; Si 17,73. C12H28O4N2Si2 Вычислено, % С: 44,97; Н 8,81;N 8,74; Si 17,52.
Пример 2
Смесь 15 г (0,0851 моль) триметилсилилового эфира N,N-диметилкарбазиновой кислоты и 12,18 г (0,0851 моль) диметилхлорметилхлорсилана кипятили с головкой полной конденсации до прекращения выделения триметилхлорсилана. Реакционную массу отфильтровали. Получили 13,37 г (98%) 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10 (2Н, 7Н)-диона с Т пл = 104-105oС.
Смесь 15 г (0,0851 моль) триметилсилилового эфира N,N-диметилкарбазиновой кислоты и 12,18 г (0,0851 моль) диметилхлорметилхлорсилана кипятили с головкой полной конденсации до прекращения выделения триметилхлорсилана. Реакционную массу отфильтровали. Получили 13,37 г (98%) 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10 (2Н, 7Н)-диона с Т пл = 104-105oС.
Таким образом, предложенный способ позволяет легко, в одну стадию получить с высоким выходом ранее неизвестный 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10(2Н, 7Н)-дион.
Claims (1)
- Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиазадисилецин-5,10(2Н, 7Н)-диона, заключающийся в том, что осуществляют взаимодействие О-силилуретанов общей формулы Me3SiOC(О)NRR', где R= H, SiMe3; R'= NMe2, с диметил-хлорметилхлорсиланом или смесью диметилхлорметилхлорсилана с гекса-метилдисилазаном при кипячении в течение 30÷40 мин.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2002116749A RU2215744C1 (ru) | 2002-06-25 | 2002-06-25 | Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиаз адисилецин-5,10(2h,7h)-диона |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2002116749A RU2215744C1 (ru) | 2002-06-25 | 2002-06-25 | Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиаз адисилецин-5,10(2h,7h)-диона |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2215744C1 true RU2215744C1 (ru) | 2003-11-10 |
| RU2002116749A RU2002116749A (ru) | 2004-01-10 |
Family
ID=32028047
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2002116749A RU2215744C1 (ru) | 2002-06-25 | 2002-06-25 | Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиаз адисилецин-5,10(2h,7h)-диона |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2215744C1 (ru) |
-
2002
- 2002-06-25 RU RU2002116749A patent/RU2215744C1/ru not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| ШЕЛУДЯКОВ B.Д. и др. Кремнийалкилирование О-силилуретанов. ЖОХ. 1983, №2, с.469-470. * |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2002116749A (ru) | 2004-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2013507364A (ja) | 新規なtrpa1アンタゴニスト | |
| KR20230110575A (ko) | 7-클로로-6-플루오로-1-(2-이소프로필-4-메틸피리딘-3-일)피리도[2,3-d]피리미딘-2,4(1h,3h)-디온의 제조 방법 | |
| AU2017292811B2 (en) | Novel processes for preparation of soluble guanylate cyclase stimulators | |
| RU2215744C1 (ru) | Способ получения 2,2,7,7-тетраметил-4,9-бис(диметиламино)-тетрагидро-1,6,4,9,2,7-диоксадиаз адисилецин-5,10(2h,7h)-диона | |
| CA3029375A1 (en) | Novel processes for preparation of soluble guanylate cyclase stimulators | |
| JP2008515840A (ja) | 10−デアセチル−n−デベンゾイル−パクリタキセルの製造のための半合成方法 | |
| KR100847331B1 (ko) | 도세탁셀의 제조방법 및 이에 사용되는 중간체 | |
| RU2475489C1 (ru) | Способ получения 8-амино-1-имино-6-морфолин-4-ил-2-окса-7-азаспиро[4,4]нона-3,6,8-триен-9-карбонитрилов | |
| PL228423B1 (pl) | 1’-(3,7,11,15-Tetrametylo-3-winyloheksadecylo)-2’-hydroksy-snglicero- 3’-fosfatydylocholina i sposób jej otrzymywania | |
| RU2837459C1 (ru) | 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионы и способ их получения | |
| JP7710435B2 (ja) | アリピプラゾールラウロキシルの調製のためのプロセス | |
| Attia et al. | Synthesis and identification of four membered rings heterocyclic compounds derived from trimethoprim | |
| JP3418725B2 (ja) | 1,1−ビス(4−アミノフェニル)エタンの簡易製造方法 | |
| JP6928615B2 (ja) | 3−(ピリジル−2−アミノ)プロピオニトリル及びその類縁体の製造方法 | |
| JPH0586044A (ja) | β−ラクトンおよび大環状ケトンの製造法 | |
| HK40103206A (en) | Novel processes for preparation of soluble guanylate cyclase stimulators | |
| Nzabamwita et al. | Cycloadditions of 6-silyloxyfulvenes: access to 7-norborn-5-enyl and 7-norborna-2, 5-dienylaldehydes and ketones | |
| SU681058A1 (ru) | Способ получени 3-арил-или 3,4-арилзамещенных 6,7-диметоксиизокумаринов | |
| RU2196136C2 (ru) | Способ получения 6-арил-5-арилазо-3,4-дигидро-3,4-пиридазиндионов | |
| CN113754681A (zh) | 一种具有双螺环结构五取代环戊烷的合成方法 | |
| RU2312103C1 (ru) | Способ получения 2-имидозолилпропан-2-сульфокислоты | |
| RU2281287C1 (ru) | Способ получения хлорангидрида 2,4-дихлор-2-дихлорфосфорилбутановой кислоты | |
| Jacobo et al. | An efficient preparation of stereospecific β-hydroxy nitriles | |
| RU2468018C1 (ru) | Способ получения производных 4-оксо-4h-хроменов, содержащих винильную и енаминную группировки | |
| HK1215809B (en) | Method for producing tricyclic compound, and tricyclic compound capable of being produced by said production method |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20080626 |