RU2139286C1 - Замещенные арилалкилтиоалкилтиопиридины для борьбы с бактериями helicobacter - Google Patents
Замещенные арилалкилтиоалкилтиопиридины для борьбы с бактериями helicobacter Download PDFInfo
- Publication number
- RU2139286C1 RU2139286C1 RU97100641/04A RU97100641A RU2139286C1 RU 2139286 C1 RU2139286 C1 RU 2139286C1 RU 97100641/04 A RU97100641/04 A RU 97100641/04A RU 97100641 A RU97100641 A RU 97100641A RU 2139286 C1 RU2139286 C1 RU 2139286C1
- Authority
- RU
- Russia
- Prior art keywords
- alkyl
- hydrogen
- substituted
- compounds
- formula
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Air Filters, Heat-Exchange Apparatuses, And Housings Of Air-Conditioning Units (AREA)
- Other Air-Conditioning Systems (AREA)
- Mounting Of Printed Circuit Boards And The Like (AREA)
Abstract
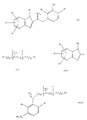
Замещенные арилалкилтиоалкилтиопиридины формулы I, где Х - СН или N; Y - S, SO, SO2, О, NH или N-С1-4алкил, R1 - Н, С1-4алкил, С1-4алкокси или галоген; R2 - Н, С1-4алкил, С1-4алкокси, галоген, СF3 (другие обозначения см. в п. 1 формулы), обладают антибактериальным действием в отношении бактерий Helicobacter. 11 з.п. ф-лы, 20 табл.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к соединениям, предназначенным для применения в фармацевтической промышленности в качестве действующих веществ при изготовлении лекарственных средств.
Настоящее изобретение относится к соединениям, предназначенным для применения в фармацевтической промышленности в качестве действующих веществ при изготовлении лекарственных средств.
Известный уровень техники
В европейской патентной заявке 150586 описываются 2-(пиридилметилтио-, соответственно -сульфинил)бензимидазолы, которые в пиридиновом фрагменте молекулы в положении 4 могут быть замещены, в частности, на алкилтио- или арилтиорадикалы. Описанные соединения обладают, как указано в публикации, продолжительным ингибирующим действием в отношении секреции кислоты желудочного сока.
В европейской патентной заявке 150586 описываются 2-(пиридилметилтио-, соответственно -сульфинил)бензимидазолы, которые в пиридиновом фрагменте молекулы в положении 4 могут быть замещены, в частности, на алкилтио- или арилтиорадикалы. Описанные соединения обладают, как указано в публикации, продолжительным ингибирующим действием в отношении секреции кислоты желудочного сока.
В международной заявке WO 89/03830 описаны эти же, равно как и другие сходные по их структуре соединения, пригодные, как полагают, для лечения остеопороза.
В международной заявке WO 92/12976 описываются замещенные определенным образом 2-(пиридилметилтио-, соответственно -сульфинил)бензимидазолы, которым приписывают эффективность по отношению к бактериям Helicobacter и которые, как полагают, пригодны для предупреждения и лечения целого ряда заболеваний желудка.
В международной заявке WO 93/24480 описываются другие, замещенные определенным образом 2-(пиридилметилтио-, соответственно -сульфинил)бензимидазолы, которые, как полагают, также эффективны против бактерий Helicobacter.
Описание изобретения
Предметом настоящего изобретения являются соединения формулы I (см. в конце описания), где
X означает CH или N,
Y означает S, SO, SO2, О, NH или N-C1-C4алкил,
R1 означает водород, C1-C4алкил, C1-C4алкокси или галоген,
R2 означает водород, C1-C4алкил, C1-C4алкокси, галоген, трифторметил, полностью либо преимущественно замещенный на фтор C1-C4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R3 при необходимости полностью либо частично замещенный на фтор C1-C2алкилендиокси или хлортрифторэтилендиокси,
R3 означает водород, полностью либо преимущественно замещенный на фтор C1-C4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R2 при необходимости полностью либо частично замещенный на фтор C1-C2алкилендиокси или хлортрифторэтилендиокси,
R4 означает водород, C1-C4алкил, замещенный на R14 C1-C4алкил, C1-C4алкилкарбонил, C2-C4алкенилкарбонил, галоген-C1-C4алкилкарбонил, N(R15)R16-C1-C4алкилкарбонил, ди-C1-C4алкилкарбамоил или C1-C4алкилсульфонил,
R5 означает водород, C1-C4алкил или C1-C4алкокси,
R6 означает моно- либо ди-C1-C4алкилкарбамоил или -тиокарбамоил, N-C1-C4aлкил-N'-цианамидин, 1-N-C1-C4алкиламино-2-нитроэтилен, N-2- пропинил-N'-цианамидин, аминосульфониламидино или замещенный на R8 и R9 цикл или бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, тиадиазол- 1-оксид, оксадиазол, пиридин, пиридин-N-оксид, пиримидин, триазин, пиридон, бензимидазол, имидазопиридин, бензтиазол и бензоксазол,
R7 означает водород, C1-C4алкил или C1-C4алкокси,
R8 означает водород, C1-C4алкил, гидрокси, C1-C4алкокси, галоген, нитро, гуанидино, карбокси, C1-C4алкоксикарбонил, замещенный на R10 C1- C4алкил или -N(R11)R12,
R9 означает водород, C1-C4алкил, гидрокси, C1-C4алкокси, фтор или трифторметил,
R10 означает гидрокси, C1-C4алкокси, карбокси, C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает водород, C1-C4алкил или -CO-R13 и
R12 означает водород или C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
R13 означает водород, C1-C4алкил или C1-C4алкокси,
R14 означает гидрокси, C1-C4алкокси, карбокси, C1-C4алкоксикарбонил или -N(R15)R16, причем
R15 означает C1-C4алкил и R16 означает C1-C4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
m означает число в интервале от 2 до 7,
n означает число 0 или 1,
p означает число 0 или 1,
q означает число 0, 1 или 2,
r означает число в интервале от 2 до 7,
t означает число 0 или 1 и
u означает число в интервале от 0 до 7,
и их соли, за исключением таких соединений формулы I, в которых Y означает S или SO и одновременно X означает CH, t означает число 0, и означает число 0, R4 означает водород или C1-C4алкил и R6 представляет собой замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, оксадиазол, пиридин, пиридин-N-оксид, пиримидин и бензимидазол, а также за исключением таких соединений формулы I, в которых Y означает NH или N-C1-C4алкил и одновременно t означает число 0 и R5 означает водород или C1-C4алкил.
Предметом настоящего изобретения являются соединения формулы I (см. в конце описания), где
X означает CH или N,
Y означает S, SO, SO2, О, NH или N-C1-C4алкил,
R1 означает водород, C1-C4алкил, C1-C4алкокси или галоген,
R2 означает водород, C1-C4алкил, C1-C4алкокси, галоген, трифторметил, полностью либо преимущественно замещенный на фтор C1-C4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R3 при необходимости полностью либо частично замещенный на фтор C1-C2алкилендиокси или хлортрифторэтилендиокси,
R3 означает водород, полностью либо преимущественно замещенный на фтор C1-C4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R2 при необходимости полностью либо частично замещенный на фтор C1-C2алкилендиокси или хлортрифторэтилендиокси,
R4 означает водород, C1-C4алкил, замещенный на R14 C1-C4алкил, C1-C4алкилкарбонил, C2-C4алкенилкарбонил, галоген-C1-C4алкилкарбонил, N(R15)R16-C1-C4алкилкарбонил, ди-C1-C4алкилкарбамоил или C1-C4алкилсульфонил,
R5 означает водород, C1-C4алкил или C1-C4алкокси,
R6 означает моно- либо ди-C1-C4алкилкарбамоил или -тиокарбамоил, N-C1-C4aлкил-N'-цианамидин, 1-N-C1-C4алкиламино-2-нитроэтилен, N-2- пропинил-N'-цианамидин, аминосульфониламидино или замещенный на R8 и R9 цикл или бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, тиадиазол- 1-оксид, оксадиазол, пиридин, пиридин-N-оксид, пиримидин, триазин, пиридон, бензимидазол, имидазопиридин, бензтиазол и бензоксазол,
R7 означает водород, C1-C4алкил или C1-C4алкокси,
R8 означает водород, C1-C4алкил, гидрокси, C1-C4алкокси, галоген, нитро, гуанидино, карбокси, C1-C4алкоксикарбонил, замещенный на R10 C1- C4алкил или -N(R11)R12,
R9 означает водород, C1-C4алкил, гидрокси, C1-C4алкокси, фтор или трифторметил,
R10 означает гидрокси, C1-C4алкокси, карбокси, C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает водород, C1-C4алкил или -CO-R13 и
R12 означает водород или C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
R13 означает водород, C1-C4алкил или C1-C4алкокси,
R14 означает гидрокси, C1-C4алкокси, карбокси, C1-C4алкоксикарбонил или -N(R15)R16, причем
R15 означает C1-C4алкил и R16 означает C1-C4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
m означает число в интервале от 2 до 7,
n означает число 0 или 1,
p означает число 0 или 1,
q означает число 0, 1 или 2,
r означает число в интервале от 2 до 7,
t означает число 0 или 1 и
u означает число в интервале от 0 до 7,
и их соли, за исключением таких соединений формулы I, в которых Y означает S или SO и одновременно X означает CH, t означает число 0, и означает число 0, R4 означает водород или C1-C4алкил и R6 представляет собой замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, оксадиазол, пиридин, пиридин-N-оксид, пиримидин и бензимидазол, а также за исключением таких соединений формулы I, в которых Y означает NH или N-C1-C4алкил и одновременно t означает число 0 и R5 означает водород или C1-C4алкил.
C1-C4алкил представляет собой прямоцепочечные либо разветвленные алкильные радикалы с 1-4 атомами углерода. В качестве примеров можно назвать такие радикалы, как бутил, изобутил, втор-бутил, трет-бутил, пропил, изопропил, этил и метил.
C1-C4алкокси представляет собой радикал, содержащий наряду с атомом кислорода один из вышеназванных C1-C4алкильных радикалов. В качестве примеров можно назвать такие радикалы, как метокси и этокси.
Галоген в контексте настоящего изобретения представляет собой бром, хлор и фтор.
В качестве полностью либо преимущественно замещенного на фтор C1-C4алкокси можно назвать, например, 1,2,2-трифторэтокси, 2,2,3,3,3- пентафторпропокси, перфторэтокси и прежде всего 1,1,2,2-тетрафторэтокси, трифторметокси, 2,2,2-трифторэтокси и дифторметокси.
В качестве необязательно полностью либо частично замещенного на фтор C1-C2алкилендиокси можно назвать, например, метилендиокси (-O-CH2-O-), этилендиокси (-O-CH2-CH2-О-), 1,1-дифторэтилендиокси (-O-CF2-CH2-O-), 1,1,2,2-тетрафторэтилендиокси (-O-CF2-CF2-O-) и прежде всего дифторметилендиокси (-O-CF2-O-) и 1,1,2-трифторэтилендиокси (-O-CF2-CHF-O-).
Если R2 и R3 оба вместе означают необязательно полностью либо частично замещенный на фтор C1-C2алкилендиокси или хлортрифторэтилендиокси, то заместители R2 и R3 в соседнем положении, предпочтительно в положениях 5 и 6, связаны по бензойному фрагменту бензимидазольного кольца.
В качестве примеров замещенных на R14 C1-C4алкильных радикалов можно назвать такие, как 2-метоксикарбонилэтил, 2-этоксикарбонилэтил, метоксикарбонилметил, карбоксиметил, 2-гидроксиэтил, метоксиметил, 2- метоксиэтил, диметиламинометил и 2-диметиламиноэтил.
C1-C4алкилкарбонил представляет собой радикал, содержащий наряду с карбонильной группой один из вышеуказанных C1-C4алкильных радикалов. В качестве примера можно назвать ацетил.
C2-C4алкенилкарбонил представляет собой радикал, содержащий наряду с карбонильной группой C2-C4алкенильный радикал, например, такой, как пропенил или бутенил. В качестве примера можно назвать акрилоил.
Галоген-C1-C4алкилкарбонил представляет собой радикал, содержащий наряду с карбонильной группой галогензамещенный C1-C4алкильный радикал. В качестве примера можно назвать, γ- хлорбутирил.
N(R15)R16-C1-C4алкилкарбонил представляет собой радикал, содержащий наряду с карбонильной группой замещенный на -N(R15)R16 C1-C4алкильный радикал. В качестве примера можно назвать 3-диметиламинопропионил.
Ди-C1-C4алкилкарбамоил представляет собой радикал, содержащий наряду с карбонильной группой ди-C1-C4алкиламинный радикал. Ди-C1-C4алкиламинный радикал является аминным радикалом, замещенным на два идентичных либо различных C1-C4алкильных радикала из числа указанных выше. В качестве примеров таких радикалов можно назвать диметиламино, диэтиламино и диизопропиламино. В качестве ди-C1-C4алкилкарбамоильных радикалов можно назвать, например, диметилкарбамоил и диэтилкарбамоил.
C1-C4алкилсульфонил представляет собой радикал, содержащий наряду с сульфонильной группой (-SO2-) один из вышеуказанных C1-C4алкильных радикалов. В качестве примера можно назвать метилсульфонил.
Моно- или ди-C1-C4алкилкарбамоильные радикалы представляют собой карбамоильные радикалы (-CO-NH2), замещенные на один или два идентичных либо различных C1-C4алкильных радикала из числа указанных выше. В качестве примеров таких радикалов можно назвать метилкарбамоил, изопропилкарбамоил и диметилкарбамоил.
Моно- или ди-C1-C4алкилтиокарбамоильные радикалы представляют собой тиокарбамоильные радикалы (-CS-NH2), замещенные на один или два идентичных либо различных C1-C4алкильных радикала из числа указанных выше. В качестве примеров таких радикалов можно назвать метилтиокарбамоил, изопропилтиокарбамоил и диметилтиокарбамоил.
В качестве N-C1-C4алкил-N'-цианамидинового радикала можно назвать, например, прежде всего N-метил-N'-цианамидино [-C(=NCN)-NH-CH3].
В качестве 1-N-C1-C4алкиламино-2-нитроэтиленового радикала можно назвать, например, прежде всего 1-N-метиламино-2-нитроэтилен [-C(NHCH3)=CHNO2].
В качестве примеров радикалов -Y-CuH2u-R6, где R6 означает N-C1-C4алкил-N'-цианамидино, 1-N-C1-C4алкиламино-2-нитроэтил или N-2- пропинил-N'-цианамидино, можно назвать прежде всего таковые, в которых Y имеет значение NH и u означает число 0. В этой связи в качестве радикала -Y-CuH2u-R6 особо можно назвать радикалы -NH-C(= NCN)NH-CH3, -NH-C(NHCH3)= CHNO2 и -NH-C(= NCN)NH-CH2=CH.
Группа CuH2u предпочтительно связана по атому углерода соответствующего цикла или бицикла R6, вследствие чего в качестве радикалов R6 (в случае, если R6 представляет собой цикл либо бицикл) можно назвать, например, следующие: фенил, 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 3-пирролил, 2- оксазолил, 4-оксазолил, 4-изоксазолил, 5-изоксазолил, 2-тиазолил, 3-изотиазолил, 2-имидазолил, 3-пиразолил, 4-пиразолил, 1,2,3-триазол-4-ил, 1,2,5-тиадиазол-4-ил, 1,2,5-тиадиазол-4-ил-1-оксид, 1,2,4-триазол-3-ил, тетразол-5-ил, 1,3,4-тиадиазол-2-ил, 1,2,3-тиадиазол-4-ил, 1,2,5-тиадиазол-4-ил, 1,2,5-тиадиазол-4-ил-1-оксид, 1,3,4-оксадиазол-2-ил, 2-пиридил, 4-пиридил, 2-пиримидинил, 1,3,4-триазин-2-ил, 2-бензимидазолил, 2-имидазопиридил, 2-бензтиазолил и 2-бензоксазолил.
C1-C4алкоксикарбонил представляет собой радикал, содержащий наряду с карбонильной группой один из указанных выше C1-C4алкоксильных радикалов.
В качестве примеров таковых можно назвать метоксикарбонил и этоксикарбонил.
Заместители R8 и R9 в циклах, соответственно бициклах R6 могут быть связаны в любом возможном положении. В качестве примеров замещенных на R8 и R9 радикалов R6 можно назвать следующие: 4-метилфенил, 3-диметиламинометилфенил, 3-пиперидинометилфенил, 3-карбоксиметилфенил, 2-диметиламинометил-5-метил-3-фурил, 1-метилпиррол-3-ил, 4,5-диметилоксазол-2-ил, 3,5-диметилизоксазол-4-ил, 4,5-диметилтиазол-2-ил, 4-метил-5-карбоксиметилтиазол-2-ил, 1-метилимидазол-2-ил, 1-метилпиразол-3-ил, 1-(2-диметиламиноэтил)пиразол-3-ил, 5-метил-1,3,4-оксадиазол-2-ил, 1-метил-1,2,3-триазол-4-ил, 1-метил-1,2,4-триазол-3-ил, 1-(2-диметиламиноэтил)-1,2,3-триазол-4-ил, 1-метилтетразол-5-ил, 1-(2-диметиламиноэтил)тетразол-5-ил, 1-карбоксиметилтетразол-5-ил, 5-метил-1,3,4-тиадиазол-2-ил, 5-трифторметил-1,3,4-тиадиазол-2-ил, 1-(2-гидроксиэтил)тетразол-5-ил, 2-амино-1,3,4-тиадиазол-2-ил, 3-амино-1,2,4-триазол-5-ил, 4-метил-5-трифторметил-1,2,4-триазол-3-ил и 4-аминопиримидин-2-ил.
В качестве радикалов -CmH2m-, -CrH2r- и -CuH2u- могут рассматриваться прямоцепочечные или разветвленные радикалы. В качестве таковых можно назвать, например, гептилен, изогептилен-(2-метилгексилен), гексилен, изогексилен-(2-метилпентилен), неогексилен-(2,2-диметилбутилен), пентилен, изопентилен-(3-метилбутилен), неопентилен-(2,2-диметилпропилен), бутилен, изо-бутилен, втор-бутилен, трет-бутилен, пропилен, изопропилен, этилен и (для -CuH2u) метилен.
В качестве радикалов -CmH2m - следует назвать предпочтительно этиленовый (-CH2CH2-), бутиленовый (-CH2CH2CH2CH2-) и прежде всего пропиленовый (-CH2CH2CH2-) радикалы.
В качестве радикалов -CrB2r - следует назвать предпочтительно этиленовый, пропиленовый и бутиленовый радикалы.
В качестве радикалов -CuH2u - следует назвать предпочтительно метиленовый, этиленовый и пропиленовый радикалы. В другом предпочтительном варианте выполнения u представляет собой число 0, вследствие чего обозначение CuH2u отсутствует или представлено в виде прямой связи, а радикал R6 непосредственно связан с группой Y.
В другом предпочтительном варианте выполнения t представляет собой число 0, вследствие чего обозначение S(=O)q-CrH2r отсутствует или представлено в виде прямой связи, а группа Y непосредственно связана с группой CmH2m.
В качестве примеров радикалов, связанных в положении 4 в пиридиновом кольце с группой S(=O)p, можно назвать следующие: фенилтиопентил, фенилтиоэтил, фенилтиопропил, фенилтиобутил, 4-метилфенилтиоэтил, 4-метилфенилтиопропил, 3-диметиламинометилфенилтиоэтил, 3-диметиламинометилфенилтиопропил, 3-пиперидинометилфенилтиоэтил, 3-пиперидинометилфенилтиопропил, 3-пиперидинометилфенилтиобутил, 1-метилпиррол-3-тиоэтил, 4,5-диметилоксазол-2-тиопропил, 3,5-диметилизоксазол-5-тиоэтил, 3,5-диметилизоксазол-5-тиопропил, тиазол-2-тиоэтил, тиазол-2-тиопропил, тиазол-2-тиобутил, 4-метил-5-карбоксиметилтиазол-2-тиопропил, 1-метилимидазол-2-тиоэтил, 1-метилимидазол-2-тиопропил, 1-метиимидазол-2-тиобутил, имидазол-2-тиоэтил, имидазол-2-тиопропил, пиразол-3-тиопропил, 1-(2-диметиламиноэтил)пиразол-2-тиоэтил, 1,3,4-оксадиазол-2-тиоэтил, 1,3,4- оксадиазол-2-тиопропил, 1,2,3-триазол-4-тиоэтил, 1,2,3-триазол-4-тиопропил, 1,2,3-триазол-4-тиобутил, 1-метил-1,2,3-триазол-4-тиоэтил, 1-метил-1,2,3-триазол-4-тиопропил, 1,2,4-триазол-3-тиоэтил, 1,2,4-триазол-3-тиопропил, 3-амино-1,2,4-триазол-5-тиоэтил, 3-амино-1,2,4-триазол-5-тиопропил, 4-метил-5-трифторметил-1,2,4-триазол-3-тиоэтил, 4-метил-5-трифторметил-1,2,4-триазол-3-тиопропил, 1-метил-1,2,4-триазол-3-тиоэтил, 1-метил-1,2,4-триазол-3-тиопропил, 1-метил-1,2,4-триазол-3-тиобутил, тетразол-5-тиоэтил, тетразол-5-тиопропил, тетразол-5-тиобутил, 1-метилтетразол-5-тиоэтил, 1-метилтетразол-5-тиопропил, 1-метилтетразол-5-тиобутил, 1-(2-диметиламиноэтил)тетразол-5-тиоэтил, 1-(2-диметиламиноэтил)тетразол-5-тиопропил, 1-(2-гидроксиэтил)тетразол-5-тиоэтил, 1-(2-гидроксиэтил)тетразол-5-тиопропил, 1,3,4-тиадиазол-2-тиоэтил, 1,3,4-тиадиазол-2-тиопропил, 5-метил-1,3,4-тиадиазол-2-тиоэтил, 5-метил-1,3,4-тиадиазол-2-тиопропил, 5-метил-1,3,4-тиадиазол-2-тиобутил, 5-трифторметил-1,3,4-тиадиазол-2-тиоэтил, 5-трифторметил-1,3,4-тиадиазол-2-тиопропил, 1,2,3-тиадиазол-4-тиоэтил, 1,2,3-тиадиазол-4-тиопропил, 1-карбоксиметилтетразол-5-тиоэтил, 1-карбоксиметилтетразол-5-тиопропил, 2-пиридилтиоэтил, 2-пиридилтиопропил, 2- пиридилтиобутил, 4-пиридилтиоэтил, 4-пиридилтиопропил, 4-пиридилтиобутил, 2-пиримидинтиоэтил, 2-пиримидинтиопропил, 2-пиримидинтиобутил, 4-аминопиримидин-2-тиоэтил, 4-аминопиримидин-2-тиопропил, 2-бензимидазолтиоэтил, 2-бензимидазолтиопропил, 4-метилтиазол-5-этилтиопропил, 2-гуанидинотиазол-4-метилтиопропил, фурил-2-метилтиопропил, 5-диметиламинометилфурил-2-метилтиопропил, имидазопиридин-2-тиопропил, бензоксазол-2-тиопропил, бензтиазол-2-тиопропил, 4-метил-фенилметилтиопропил, диметилкарбамоилтиопропил, диметилтиокарбамоилтиопропил, N-метил-N'-цианамидинотиопропил, феноксиэтил, феноксипропил, 4-метилтиазол-5-этилтиоэтил, 2-гуанидинотиазол-4-метилтиоэтил, фурил-2-метилтиоэтил, 5-диметиламинометилфурил-2-метилтиоэтил, имидазопиридин-2-тиоэтил, бензоксазол-2-тиоэтил, бензтиазол-2-тиоэтил, 4-метилфенилметилтиоэтил, диметилкарбамоилтиоэтил, диметилтиокарбамоилтиоэтил, N-метил-N'-цианамидинотиоэтил, 4-метилтиазол-5-этилтиобутил, 2-гуанидинотиазол-4-метилтиобутил, фурил-2-метилтиобутил, 5-диметиламинометилфурил-2-метил-тиобутил, имидазопиридин-2-тиобутил, бензоксазол-2-тиобутил, бензтиазол-2-тиобутил, 4-метилфенилметилтиобутил, диметилкарбамоилтиобутил, диметилтиокарбамоилтиобутил, N-метил-N'-цианамидинотиобутил, 4-метилтиазол-5-тиоэтил, 4-метилтиазол-5-тиопропил, 4-метилтиазол-5-тиобутил, 1-метоксикарбонилметилтетразол-5-тиоэтил, 1-метоксикарбонилметилтетразол-5-тиопропил, 1-метоксикарбонилметилтетразол-5-тиобутил, тиенил-2-метилтиоэтил, тиенил-2-метилтиопропил, тиенил-2-метилтиобутил, тиенил-2-этилтиоэтил, тиенил-2-этилтиопропил, тиенил-2-этилтиобутил, 5-хлортиенил-2-метилтиоэтил, 5-хлортиенил-2-метилтиопропил, 5-хлортиенил-2-метилтиобутил, 4-пиридилметилтиоэтил, 4-пиридилметилтиопропил, 4-пиридилметилтиобутил, 2-пиридилметилтиоэтил, 2-пиридилметилтиопропил, 2-пиридилметилтиобутил, 2-пиридинилэтилтиоэтил, 2-пиридинилэтилтиопропил, 2-пиридинилэтилтиобутил, 3-диметиламинометилфенилметилтиоэтил, 3-диметиламинометилфенилметилтиопропил, 3-диметиламинометилфенилметилтиобутил, 2-бензимидазолметилтиопропил, 2-бензимидазолметилтиобутил, 5-нитроимидазол-1-этилтиоэтил, 5-нитроимидазол-1-этилтиопропил, 5-нитроимидазол-1-этилтиобутил, 2-метил-5-нитроимидазол-1-этилтиоэтил, 2-метил-5-нитроимидазол-1-этилтиопропил, 2-метил-5-нитроимидазол-1-этилтиобутил, 5-нитроимидазол-1-пропилтиоэтил, 5-нитроимидазол-1-пропилтиопропил, 5-нитроимидазол-1-пропилтиобутил, 2-метил-5-нитроимидазол-1-пропилтиоэтил, 2-метил-5-нитроимидазол-1-пропилтиопропил, 2-метил-5-нитроимидазол-1-пропилтиобутил.
К солям соединений формулы I, в которых n означает число 0, можно отнести все кислотно-аддитивные соли. Среди таковых следует назвать прежде всего фармакологически приемлемые соли неорганических и органических кислот, обычно применяемых в галенике. Фармакологически неприемлемые соли, образующиеся в качестве первоначальных продуктов при осуществлении способа, например, при получении соединений согласно изобретению в промышленном масштабе, с помощью методов, известных специалисту в данной области техники, могут переводиться в фармакологически приемлемые соли. В качестве таковых пригодны водорастворимые и водонерастворимые кислотно-аддитивные соли с такими кислотами, как, например, соляная кислота, бромистоводородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота, D-глуконовая кислота, бензойная кислота, 2-(4-гидроксибензоил) бензойная кислота, масляная кислота, сульфосалициловая кислота, малеиновая кислота, лауриновая кислота, яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота, винная кислота, эмбоновая кислота, стеариновая кислота, толуолсульфоновая кислота, метансульфоновая кислота или 3-гидрокси-2-нафтойная кислота, причем при получении солей - в зависимости от того, используют ли одно- или многоосновную кислоту, и от того, какую соль требуется получить, - кислоты применяют в эквимолярном или несколько в другом количественном соотношении.
В качестве солей соединений формулы I, в которых n означает число 1, и/или соединений с карбоксильным радикалом могут рассматриваться также соли с основаниями. В качестве примеров таких основных солей можно назвать соли лития, натрия, калия, кальция, алюминия, магния, титана, аммония, меглумина или гуанидиния, причем и в этих случаях при получении солей применяют основания в эквимолярном или несколько в другом количественном соотношении.
Одной из модификаций изобретения являются соединения формулы I, в которых X имеет значение CH.
Другой модификацией изобретения являются соединения формулы I, в которых X имеет значение N.
Еще одной модификацией изобретения являются соединения формулы I, в которых t означает число 1.
Другой модификацией изобретения являются соединения формулы I, в которых u означает число в интервале от 1 до 7.
Еще одной модификацией изобретения являются соединения формулы I, в которых Y имеет значение О (кислород).
Одной из модификаций изобретения являются далее соединения формулы I, в которых X имеет значение CH, Y имеет значение S, t означает число 0 и u означает число в интервале от 1 до 7.
Другой модификацией изобретения являются соединения формулы I, в которых X имеет значение CH, Y имеет значение S, t означает число 0, u означает число 0 и R4 представляет собой замещенный на R14 C1-C4алкил, C1-C4алкилкарбонил, C1-C4алкенилкарбонил, галоген-C1-C4алкилкарбонил, N(R15)R16-C1-C4алкилкарбонил, ди-C1-C4алкилкарбамоил или C1-C4алкилсульфонил.
Еще одной модификацией изобретения являются соединения формулы I, в которых Y имеет значение S, t означает число 0, u означает число 0 и R6 представляет собой радикал из числа следующих: моно- либо ди-C1-C4алкилкарбамоил или -тиокарбамоил, N-C1-C4алкил-N'-цианамидино, 1-N-C1-C4алкиламино-2-нитроэтил, N-2-пропинил-N'-цианамидино, аминосульфониламидино или замещенный на R8 и R9 цикл, выбранный из группы, включающей тиадиазол-1-оксид, триазин, пиридон, имидазопиридин, бензтиазол и бензоксазол.
Другой модификацией изобретения являются соединения формулы I, в которых Y означает NH или N-C1-C4алкил, t означает число 0 и R5 означает C1-C4алкокси.
Среди соединений формулы I следует выделить таковые, в которых
X означает CH или N,
Y означает S, SO2, О или N-C1-C4алкил,
R1 означает водород, C1-C4алкокси или галоген,
R2 означает водород, C1-C4алкил, C1-C4алкокси или галоген,
R3 означает водород,
R4 означает водород, замещенный на R14 C1-C4алкил, N(R15)R16-C1-C4алкилкарбонил или C1-C4алкилсульфонил,
R5 означает водород, C1-C4алкил или C1-C4алкокси,
R6 представляет собой моно- либо ди-C1-C4алкилтиокарбамоил, N-C1-С4алкил-N'-цианамидино, 1-N-C1-C4алкиламино-2-нитроэтилен, N-2-пропинил-N'-цианамидино или замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, пиразол, триазол, тетразол, тиадиазол, тиадиазол-1-оксид, оксадиазол, пиридин, пиримидин, триазин, пиридон, бензимидазол, имидазопиридин, бензтиазол и бензоксазол,
R7 означает водород или C1-C4алкил,
R8 означает водород, C1-C4алкил, гидрокси, нитро, гуанидино, карбокси, C1-C4алкоксикарбонил или замещенный на R10 C1-C4алкил,
R9 означает водород, C1-C4алкил, гидрокси, C1-C4алкокси или фтор,
R10 означает гидрокси, C1-C4алкокси, карбокси, C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает C1-C4алкил или -CO-R13 и
R12 означает C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
R13 означает C1-C4алкил,
R14 означает гидрокси, C1-C4алкоксикарбонил или -N(R15)R16, причем
R15 означает C1-C4алкил и
R16 означает C1-C4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны,
представляют собой пиперидиновый или морфолиновый радикал,
m означает число в интервале от 2 до 4,
n означает число 0 или 1,
p означает число 0,
q означает число 0 или 2,
r означает число в интервале от 2 до 4,
t означает число 0 или 1 и
u означает число в интервале от 0 до 3,
и их соли, за исключением таких соединений формулы I, в которых Y означает S и одновременно X означает CH, t означает число 0, u означает число 0, R4 означает водород и R6 представляет собой замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, пиразол, триазол, тетразол, тиадиазол, оксадиазол, пиридин, пиримидин и бензимидазол, а также за исключением таких соединений формулы I, в которых Y означает N-C1-C4алкил и одновременно t означает число 0 и R5 означает водород или C1-C4алкил.
X означает CH или N,
Y означает S, SO2, О или N-C1-C4алкил,
R1 означает водород, C1-C4алкокси или галоген,
R2 означает водород, C1-C4алкил, C1-C4алкокси или галоген,
R3 означает водород,
R4 означает водород, замещенный на R14 C1-C4алкил, N(R15)R16-C1-C4алкилкарбонил или C1-C4алкилсульфонил,
R5 означает водород, C1-C4алкил или C1-C4алкокси,
R6 представляет собой моно- либо ди-C1-C4алкилтиокарбамоил, N-C1-С4алкил-N'-цианамидино, 1-N-C1-C4алкиламино-2-нитроэтилен, N-2-пропинил-N'-цианамидино или замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, пиразол, триазол, тетразол, тиадиазол, тиадиазол-1-оксид, оксадиазол, пиридин, пиримидин, триазин, пиридон, бензимидазол, имидазопиридин, бензтиазол и бензоксазол,
R7 означает водород или C1-C4алкил,
R8 означает водород, C1-C4алкил, гидрокси, нитро, гуанидино, карбокси, C1-C4алкоксикарбонил или замещенный на R10 C1-C4алкил,
R9 означает водород, C1-C4алкил, гидрокси, C1-C4алкокси или фтор,
R10 означает гидрокси, C1-C4алкокси, карбокси, C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает C1-C4алкил или -CO-R13 и
R12 означает C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
R13 означает C1-C4алкил,
R14 означает гидрокси, C1-C4алкоксикарбонил или -N(R15)R16, причем
R15 означает C1-C4алкил и
R16 означает C1-C4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны,
представляют собой пиперидиновый или морфолиновый радикал,
m означает число в интервале от 2 до 4,
n означает число 0 или 1,
p означает число 0,
q означает число 0 или 2,
r означает число в интервале от 2 до 4,
t означает число 0 или 1 и
u означает число в интервале от 0 до 3,
и их соли, за исключением таких соединений формулы I, в которых Y означает S и одновременно X означает CH, t означает число 0, u означает число 0, R4 означает водород и R6 представляет собой замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, пиразол, триазол, тетразол, тиадиазол, оксадиазол, пиридин, пиримидин и бензимидазол, а также за исключением таких соединений формулы I, в которых Y означает N-C1-C4алкил и одновременно t означает число 0 и R5 означает водород или C1-C4алкил.
Особенно следует выделить такие соединения формулы I, в которых
X означает CH или N,
Y означает S или SO2,
R1 означает водород, C1-C4алкокси или фтор,
R2 означает водород, C1-C4алкил или фтор,
R3 означает водород,
R4 означает водород, замещенный на R14 C1-C4алкил или C1-C4алкилсульфонил,
R5 означает водород или C1-C4алкил,
R6 представляет собой ди-C1-C1алкилтиокарбамоил, N-C1-C4алкил-N'-цианамидино или замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин, пиримидин и триазин,
R7 означает водород или C1-C4алкил,
R8 означает водород, C1-C4алкил, гидрокси, нитро, гуанидино, карбокси, C1-C4алкоксикарбонил или замещенный на R10 C1-C4алкил,
R9 означает водород, C1-C4алкил, гидрокси или фтор,
R10 означает гидрокси, C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает C1-C4алкил и
R12 означает C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
R14 означает C1-C4алкоксикарбонил или -N(R15)R16, причем
R15 означает C1-C4алкил и
R16 означает C1-C4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
m означает число в интервале от 2 до 4,
n означает число 0,
p означает число 0,
t означает число 0 и
u означает число в интервале от 0 до 3,
и их соли, за исключением таких соединений формулы I, в которых Y означает S и одновременно X означает CH, u означает число 0, R4 означает водород и R6 представляет собой замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин.
X означает CH или N,
Y означает S или SO2,
R1 означает водород, C1-C4алкокси или фтор,
R2 означает водород, C1-C4алкил или фтор,
R3 означает водород,
R4 означает водород, замещенный на R14 C1-C4алкил или C1-C4алкилсульфонил,
R5 означает водород или C1-C4алкил,
R6 представляет собой ди-C1-C1алкилтиокарбамоил, N-C1-C4алкил-N'-цианамидино или замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин, пиримидин и триазин,
R7 означает водород или C1-C4алкил,
R8 означает водород, C1-C4алкил, гидрокси, нитро, гуанидино, карбокси, C1-C4алкоксикарбонил или замещенный на R10 C1-C4алкил,
R9 означает водород, C1-C4алкил, гидрокси или фтор,
R10 означает гидрокси, C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает C1-C4алкил и
R12 означает C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
R14 означает C1-C4алкоксикарбонил или -N(R15)R16, причем
R15 означает C1-C4алкил и
R16 означает C1-C4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
m означает число в интервале от 2 до 4,
n означает число 0,
p означает число 0,
t означает число 0 и
u означает число в интервале от 0 до 3,
и их соли, за исключением таких соединений формулы I, в которых Y означает S и одновременно X означает CH, u означает число 0, R4 означает водород и R6 представляет собой замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин.
К предпочтительным соединениям формулы I относятся таковые, в которых
X означает CH или N,
Y означает S или SO2,
R1 означает водород, C1-C4алкокси или фтор,
R2 означает водород или фтор,
R3 означает водород,
R4 означает водород,
R5 означает C1-C4алкил,
R6 представляет собой ди-C1-C4алкилтиокарбамоил или замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин,
R7 означает водород,
R8 означает водород, нитро, C1-C4алкоксикарбонил или замещенный на R10 C1-C2алкил,
R9 означает водород или C1-C4алкил,
R10 означает C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает C1-C4алкил и
R12 означает C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
m означает число 2 или 3,
n означает число 0,
p означает число 0,
t означает число 0 и
u означает число в интервале от 1 до 3, и их соли.
X означает CH или N,
Y означает S или SO2,
R1 означает водород, C1-C4алкокси или фтор,
R2 означает водород или фтор,
R3 означает водород,
R4 означает водород,
R5 означает C1-C4алкил,
R6 представляет собой ди-C1-C4алкилтиокарбамоил или замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин,
R7 означает водород,
R8 означает водород, нитро, C1-C4алкоксикарбонил или замещенный на R10 C1-C2алкил,
R9 означает водород или C1-C4алкил,
R10 означает C1-C4алкоксикарбонил или -N(R11)R12, причем
R11 означает C1-C4алкил и
R12 означает C1-C4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал,
m означает число 2 или 3,
n означает число 0,
p означает число 0,
t означает число 0 и
u означает число в интервале от 1 до 3, и их соли.
Модификацией предпочтительных соединений являются таковые, в которых X имеет значение CH.
Другой модификацией предпочтительных соединений являются таковые, в которых X имеет значение N.
Еще одной модификацией предпочтительных соединений являются таковые, в которых Y имеет значение S.
Другой модификацией предпочтительных соединений являются те из них, в которых R1 и R2 означают водород.
Еще одной модификацией предпочтительных соединений являются те из них, в которых u означает число 1.
Другой модификацией предпочтительных соединений являются таковые, в которых u означает число 2.
Еще одной модификацией предпочтительных соединений являются таковые, в которых m означает число 2.
Другой модификацией предпочтительных соединений являются те из них, в которых m означает число 3.
К особенно предпочтительным соединениям формулы I относятся таковые, в которых
X означает CH или N,
Y означает S,
R1 означает водород,
R2 означает водород,
R3 означает водород,
R4 означает водород,
R5 означает C1-C4алкил,
R6 представляет собой замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин,
R7 означает водород,
R8 означает нитро,
R9 означает водород или C1-C4алкил,
m означает число 2 или 3,
n означает число 0,
p означает число 0,
t означает число 0,
u означает число в интервале от 1 до 3,
и их соли.
X означает CH или N,
Y означает S,
R1 означает водород,
R2 означает водород,
R3 означает водород,
R4 означает водород,
R5 означает C1-C4алкил,
R6 представляет собой замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин,
R7 означает водород,
R8 означает нитро,
R9 означает водород или C1-C4алкил,
m означает число 2 или 3,
n означает число 0,
p означает число 0,
t означает число 0,
u означает число в интервале от 1 до 3,
и их соли.
К наиболее предпочтительным соединениям формулы I относятся те из них, в которых
X означает CH или N,
Y означает S,
R1 означает водород,
R2 означает водород,
R3 означает водород,
R4 означает водород,
R5 означает C1-C4алкил,
R6 представляет собой замещенный на R8 и R9 имидазол,
R7 означает водород,
R8 означает нитро,
R9 означает водород или C1-C4алкил,
m означает число 2 или 3,
n означает число 0,
p означает число 0,
t означает число 0,
u означает число в интервале от 1 до 3,
и их соли.
X означает CH или N,
Y означает S,
R1 означает водород,
R2 означает водород,
R3 означает водород,
R4 означает водород,
R5 означает C1-C4алкил,
R6 представляет собой замещенный на R8 и R9 имидазол,
R7 означает водород,
R8 означает нитро,
R9 означает водород или C1-C4алкил,
m означает число 2 или 3,
n означает число 0,
p означает число 0,
t означает число 0,
u означает число в интервале от 1 до 3,
и их соли.
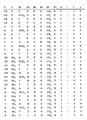
Примеры соединений согласно изобретению представлены в таблицах 1-19. К этим примерам относятся также соли соединений, указанных в таблицах.
Другим предметом изобретения является способ получения соединений формулы I и их солей.
Способ отличается тем, что
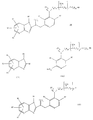
а) меркаптобензимидазолы формулы II (см. в конце описания), где X, R1, R2, R3 и R4 имеют вышеуказанные значения, подвергают взаимодействию с производными пиколина формулы III (см. в конце описания), где R5, R6, R7, Y, m, p, q, r, t и u имеют вышеуказанные значения, а A представляет собой соответствующую уходящую группу, или что
б) соединения формулы IV (см. в конце описания), где X, R1, R2, R3, R4, R5, R7, m, r и t имеют вышеуказанные значения, n, p и g означают число 0, а A представляет собой соответствующую уходящую группу, подвергают взаимодействию с соединениями R6-CuH2u-YH (где Y означает S, О, NH или N-C1-C4алкил), или что
в) соединения формулы V (см. в конце описания), где X, R1, R2, R3, R4, R5, R7 и n имеют вышеуказанные значения и Hal означает атом галогена, подвергают взаимодействию с тиолами формулы VI (см. в конце описания), где R6, Y, m, q, r, t и u имеют вышеуказанные значения, или что
г) бензимидазолы формулы VII (см. в конце описания), где R1, R2, R3, R4 и X имеют вышеуказанные значения, а A представляет собой соответствующую уходящую группу, подвергают взаимодействию с пиридинами формулы VIII (см. в конце описания), где R5, R6, R7, Y, m, p, q, r, t и u имеют вышеуказанные значения,
и что (в случае, если соединения формулы I, где n равно 1, соответственно p равно 1 и/или q равно 1 или 2, и/или Y означает SO, соответственно SO2, являются требуемыми конечными продуктами) затем полученные соединения, где n равно 0 и/или p равно 0, и/или q равно 0, и/или Y означает S, окисляют, и/или что полученные соединения при необходимости переводят затем в соли и/или что полученные соли при необходимости переводят в завершение в свободные соединения.
а) меркаптобензимидазолы формулы II (см. в конце описания), где X, R1, R2, R3 и R4 имеют вышеуказанные значения, подвергают взаимодействию с производными пиколина формулы III (см. в конце описания), где R5, R6, R7, Y, m, p, q, r, t и u имеют вышеуказанные значения, а A представляет собой соответствующую уходящую группу, или что
б) соединения формулы IV (см. в конце описания), где X, R1, R2, R3, R4, R5, R7, m, r и t имеют вышеуказанные значения, n, p и g означают число 0, а A представляет собой соответствующую уходящую группу, подвергают взаимодействию с соединениями R6-CuH2u-YH (где Y означает S, О, NH или N-C1-C4алкил), или что
в) соединения формулы V (см. в конце описания), где X, R1, R2, R3, R4, R5, R7 и n имеют вышеуказанные значения и Hal означает атом галогена, подвергают взаимодействию с тиолами формулы VI (см. в конце описания), где R6, Y, m, q, r, t и u имеют вышеуказанные значения, или что
г) бензимидазолы формулы VII (см. в конце описания), где R1, R2, R3, R4 и X имеют вышеуказанные значения, а A представляет собой соответствующую уходящую группу, подвергают взаимодействию с пиридинами формулы VIII (см. в конце описания), где R5, R6, R7, Y, m, p, q, r, t и u имеют вышеуказанные значения,
и что (в случае, если соединения формулы I, где n равно 1, соответственно p равно 1 и/или q равно 1 или 2, и/или Y означает SO, соответственно SO2, являются требуемыми конечными продуктами) затем полученные соединения, где n равно 0 и/или p равно 0, и/или q равно 0, и/или Y означает S, окисляют, и/или что полученные соединения при необходимости переводят затем в соли и/или что полученные соли при необходимости переводят в завершение в свободные соединения.
При проведении описанных выше обменных реакций исходные соединения могут применяться как таковые либо при необходимости в виде их солей.
В качестве соответствующих уходящих групп A можно назвать, например, атомы галогена, прежде всего атом хлора, или активированные путем этерификации (например, взаимодействием с пара-толуолсульфоновой кислотой) гидроксильные группы.
Взаимодействие соединений формулы II с соединениями формулы III осуществляют в соответствующих, предпочтительно полярных, протонных либо апротонных растворителях (таких, как метанол, этанол, изопропанол, диметилсульфоксид, ацетон, диметилформамид или ацетонитрил) с добавками воды или в безводных условиях. Реакцию проводят, например, в присутствии акцептора протонов. В качестве таковых пригодны гидроксиды щелочных металлов, такие как гидроксид натрия, карбонаты щелочных металлов, такие как карбонат калия, или третичные амины, такие как пиридин, триэтиламин или этилдиизопропиламин. В качестве альтернативы возможно также осуществление реакции без использования акцептора протонов, причем - в зависимости от вида исходных соединений - при необходимости можно сначала проводить отделение кислотно-аддитивных солей в особенно чистой форме. Температура реакции может находиться в диапазоне от 0oC до 150oC, причем в присутствии акцепторов протонов предпочтительны температуры в интервале от 20oC до 80oC, а без акцепторов протонов - в интервале от 60oC до 120oC, прежде всего предпочтительна температура кипения используемых растворителей. Время реакции составляет от 0,5 до 30 часов.
Взаимодействие соединений формулы IV с соединениями R6-CuH2u-YH осуществляют по аналогичной методике, которую применяют при проведении взаимодействия соединений формулы II с соединениями формулы III.
Взаимодействие соединений формулы V с тиолами формулы VI осуществляют по методике, известной специалисту в данной области техники для получения сульфидов из тиолов и галогенированных ароматических углеводородов. Предпочтительным атомом галогена Hal является атом хлора.
Взаимодействие соединений формулы VII с соединениями формулы VIII осуществляют в принципе по аналогичной методике, применяемой при взаимодействии соединений формулы II с соединениями формулы III.
Окисление сульфидов до сульфоксидов, соответственно до сульфонов осуществляют в условиях, известных специалисту в данной области техники, при проведении окисления сульфидов до сульфоксидов, соответственно до сульфонов [см. , например, J.Drabowicz и M.Mikolajczyk, Organic preparations and procedures int. 14(1-2), 45-89 (1982) или E.Block и S.Patai, The Chemistry of Functional Groups, Supplement E, часть 1, стр.539-608, John Wiley and Sons (Interscience Publication), 1980]. В качестве окислителей могут рассматриваться все реагенты, используемые обычно для окисления сульфидов до сульфоксидов, соответственно до сульфонов, прежде всего надкислоты, как, например, перуксусная кислота, трифторперуксусная кислота, 3,5-динитропербензойная кислота, пермалеиновая кислота, монопероксифталат магния или предпочтительно мета-хлорпербензойная кислота.
Температура реакции (в зависимости от реакционной способности окислителя и степени разбавления) находится в интервале от -70oC до температуры кипения используемого растворителя, предпочтительно, однако, в интервале от -30oC до +20oC. Предпочтительным оказалось также окисление галогенами, соответственно гипогалогенитами (например, водным раствором гипохлорита натрия), которое целесообразно проводить в диапазоне температур от 0oC до 50oC. Реакцию целесообразно осуществлять в инертных растворителях, например в ароматических или хлорированных углеводородах, таких как бензол, толуол, дихлорметан или хлороформ, предпочтительно в сложных или простых эфирах, таких как этиловый эфир уксусной кислоты, изопропиловый эфир уксусной кислоты или диоксан, либо в спиртах, предпочтительно изопропаноле.
Предлагаемые согласно изобретению сульфоксиды представляют собой оптически активные соединения. В зависимости от типа заместителей в молекуле могут иметься также другие центры хиральности. Изобретение включает поэтому как энантиомеры и диастереомеры, так и их смеси и рацематы. Энантиомеры могут быть выделены по известной методике (например, получением и разделением соответствующих диастереоизомерных соединений) (см., например, международную заявку WO 92/08716).
Соединения формулы II известны, например, из международной заявки WO 86/02646, европейских патентных заявок ЕР 134400 или ЕР 127763. Соединения формулы III, где p равно 0, соответственно q равно 0, могут быть получены по методике, описанной, в частности, в нижеследующих примерах.
Для соединений формулы III, где p равно 1, соответственно q равно 1 или 2, соответственно Y означает SO или SO2, соответствующие 2-гидроксиметил-4-меркаптозамещенные пиридины окисляют, например, мета-хлорпербензойной кислотой и затем хлорируют, например, тионилхлоридом. Обменная реакция с 2-меркаптобензимидазолами приводит к получению соединений формулы I, в которых p равно 1, соответственно q равно 1 или 2, соответственно Y означает SO или SO2.
В зависимости от типа заместителя R6 сульфоксиды, соответственно сульфоны получают также при окислении до сульфоксидов с n, равным 1. В остальных случаях соответствующие сульфиды, соответственно сульфоксиды или сульфоны могут быть получены за счет выбора пригодных для этой цели исходных соединений или применения селективных окислителей.
Необходимые для получения соединений формулы III исходные соединения можно получать, например, из соответствующих галогенсодержащих соединений аналогично тому, как это описано в Journ. Med. Chem. 14 (1971) 349.
Соединения формул V, VI, VII и VIII также известны либо могут быть получены с помощью известных способов из известных исходных соединений по аналогичной методике. Так, например, соединения формулы V получают взаимодействием соединений формулы II с 4-галогенпиридинами, используемыми соответственно для получения соединений формулы III.
Нижеследующие примеры предназначены для более подробного пояснения изобретения, не ограничивая его объем. Соединения согласно изобретению, равно как и исходные соединения, могут быть получены по методике, аналогичной описанной в примерах.
Примеры
Конечные продукты
1. 2-{ [[3-метил-4-[(2-фенокси)этилтио]-2-пиридинил]метил]тио}-1Н-бензимидазол
2-{ [[4-(2-хлорэтилтио)-3-метил-2-пиридинил] метил] тио}-1Н-бензимидазол (10 ммолей) перемешивают с фенолом (20 ммолей) и карбонатом калия (60 ммолей) в течение 24 ч при 100oC в ацетонитриле (25 мл). После фильтрации концентрируют, остаток растворяют в дихлорметане, промывают 0,1 H едким натром, сушат над сульфатом магния, концентрируют и хроматографируют на силикагеге (ЭЭ/МеOH).
Конечные продукты
1. 2-{ [[3-метил-4-[(2-фенокси)этилтио]-2-пиридинил]метил]тио}-1Н-бензимидазол
2-{ [[4-(2-хлорэтилтио)-3-метил-2-пиридинил] метил] тио}-1Н-бензимидазол (10 ммолей) перемешивают с фенолом (20 ммолей) и карбонатом калия (60 ммолей) в течение 24 ч при 100oC в ацетонитриле (25 мл). После фильтрации концентрируют, остаток растворяют в дихлорметане, промывают 0,1 H едким натром, сушат над сульфатом магния, концентрируют и хроматографируют на силикагеге (ЭЭ/МеOH).
Из чистых фракций после кристаллизации из диизопропилового эфира получают указанное в заголовке соединение в виде бесцветных кристаллов; Тпл 72-73oC; выход: 64% от теории.
2. 2-{[[3-метил-4-[(4-фенокси)бутилтио]-2-пиридинил]метил]тио}-1Н-бензимидазол
По методике, описанной в примере 1, взаимодействием 2-{[[4-(4-хлорбутилтио)-3-метил-2-пиридинил] метил] тио}-1H-бензимидазола с фенолом получают соединение, указанное в заголовке; Тпл 122-123oC; выход: 69% от теории.
По методике, описанной в примере 1, взаимодействием 2-{[[4-(4-хлорбутилтио)-3-метил-2-пиридинил] метил] тио}-1H-бензимидазола с фенолом получают соединение, указанное в заголовке; Тпл 122-123oC; выход: 69% от теории.
3. 2-{ [[3-метил-4-[5-(4-метилфенил)-1,4-дитиапент-1-ил] -2-пиридинил] метил]тио}-1H-бензимидазол
По методике, описанной в примере 1, взаимодействием 2-{[[4-(2-хлорэтилтио)-3-метил-2-пиридинил] метил] тио} -1Н-бензимидазола с 4-метилбензилмеркаптаном после перекристаллизации из метанол-толуола получают соединение, указанное в заголовке; Тпл 129-130oC; выход: 55% от теории.
По методике, описанной в примере 1, взаимодействием 2-{[[4-(2-хлорэтилтио)-3-метил-2-пиридинил] метил] тио} -1Н-бензимидазола с 4-метилбензилмеркаптаном после перекристаллизации из метанол-толуола получают соединение, указанное в заголовке; Тпл 129-130oC; выход: 55% от теории.
4. 2-{[[4-[3-диметилдитиокарбамоилпропилтио]-3-метил-2-пиридинил] метил] тио}-1H-бензимидазол
По методике, описанной в примере 5, взаимодействием 2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] тио} -1H-бензимидазола в этаноле без добавления воды с Na-солью диметилкарбамидовой кислоты получают указанное в заголовке соединение в виде бесцветных кристаллов; Тпл 115-117oC; выход: 94% от теории.
По методике, описанной в примере 5, взаимодействием 2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] тио} -1H-бензимидазола в этаноле без добавления воды с Na-солью диметилкарбамидовой кислоты получают указанное в заголовке соединение в виде бесцветных кристаллов; Тпл 115-117oC; выход: 94% от теории.
5. 2-{ [[4-[(6-фуран-2-ил)-1,5-дитиагекс-1-ил]-3-метил-2-пиридинил] метил]тио}-1H-бензимидазол
2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил]тио}-1H- бензимидазол (3 ммоля) перемешивают с 2-фурилметилтиолом (3,6 ммоля) и 1 H едким натром (4 мл) в этаноле (20 мл) в течение 20 ч с обратным холодильником. После выпаривания этанола под вакуумом добавляют 20 мл воды и экстрагируют этилацетатом (3х10 мл). Объединенные органические фазы концентрируют и остаток хроматографируют (ЭЭ/метанол/триэтиламин). После кристаллизации из дихлорметан-диизопропилового эфира получают указанное в заголовке соединение в виде порошка бежевого цвета; Тпл 113- 116oC; выход: 69% от теории.
2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил]тио}-1H- бензимидазол (3 ммоля) перемешивают с 2-фурилметилтиолом (3,6 ммоля) и 1 H едким натром (4 мл) в этаноле (20 мл) в течение 20 ч с обратным холодильником. После выпаривания этанола под вакуумом добавляют 20 мл воды и экстрагируют этилацетатом (3х10 мл). Объединенные органические фазы концентрируют и остаток хроматографируют (ЭЭ/метанол/триэтиламин). После кристаллизации из дихлорметан-диизопропилового эфира получают указанное в заголовке соединение в виде порошка бежевого цвета; Тпл 113- 116oC; выход: 69% от теории.
6. Тригидрохлорид 2-{[[4-[6-(2-диметиламинофуран-5-ил)-1,5- дитиагекс-1-ил]-3-метил-2-пиридинил]метил]тио}-1H-бензимидазола
По методике, описанной в примере 5, взаимодействием с 5-диметиламинометил-2-фурилметилтиолом получают свободное соединение, указанное в заголовке, в виде масла. С помощью газообразной соляной кислоты указанное в заголовке соединение можно осаждать из ацетона в виде гидрохлорида; Тпл 112oC (разложение).
По методике, описанной в примере 5, взаимодействием с 5-диметиламинометил-2-фурилметилтиолом получают свободное соединение, указанное в заголовке, в виде масла. С помощью газообразной соляной кислоты указанное в заголовке соединение можно осаждать из ацетона в виде гидрохлорида; Тпл 112oC (разложение).
7. Тригидрохлорид 2-{[[3-метил-4-[7-(5-метилтиазол-4-ил)-1,5- дитиагепт-1-ил]-2-пиридинил]метил]тио}-1H-бензимидазола
По методике, описанной в примере 5, взаимодействием с 2-(5-метил-4-тиазолил)этилтиолом после осаждения с помощью концентрированной соляной кислоты в ацетоне получают соединение, указанное в заголовке; Тпл 159-162oC; выход: 83% от теории.
По методике, описанной в примере 5, взаимодействием с 2-(5-метил-4-тиазолил)этилтиолом после осаждения с помощью концентрированной соляной кислоты в ацетоне получают соединение, указанное в заголовке; Тпл 159-162oC; выход: 83% от теории.
8. Тригидрохлорид 2-{ [[3-метил-4- [6-(2-гуанидинотиазол-4-ил)-1,5-дитиагекс-1-ил]-2-пиридинил]метил] тио}-1H-бензимидазола
По методике, описанной в примере 5, взаимодействием с 2-гуанидинотиазол-4-метилтиолом после осаждения с помощью эфирной соляной кислоты в ацетоне получают указанное в заголовке соединение в виде бесцветного, высокогигроскопичного порошка; выход: 29% от теории; Тпл 185oC (разложение).
По методике, описанной в примере 5, взаимодействием с 2-гуанидинотиазол-4-метилтиолом после осаждения с помощью эфирной соляной кислоты в ацетоне получают указанное в заголовке соединение в виде бесцветного, высокогигроскопичного порошка; выход: 29% от теории; Тпл 185oC (разложение).
9. 2-{ [[3-метил-4-[5-(1Н-бензимидазол-2-ил)-1,5-дитиапент-1-ил] -2-пиридинил]метил]тио}-1H-бензимидазол
2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил]тио}-1H- бензимидазол (1 ммоль) перемешивают с 2-меркапто-1Н-бензимидазолом (1,05 ммоля) и 1 H едким натром (3 мл) в 10 мл этанола в течение 20 ч при 60oC, после чего разбавляют дополнительно 10 мл воды. Затем дают остыть, отфильтровывают от выпавшего твердого вещества, промывают смесью этанол-вода 1:1 и сушат под вакуумом при 50oC. Таким путем получают указанное в заголовке соединение в виде серого порошка; Тпл 85-87oC; выход: 83% от теории.
2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил]тио}-1H- бензимидазол (1 ммоль) перемешивают с 2-меркапто-1Н-бензимидазолом (1,05 ммоля) и 1 H едким натром (3 мл) в 10 мл этанола в течение 20 ч при 60oC, после чего разбавляют дополнительно 10 мл воды. Затем дают остыть, отфильтровывают от выпавшего твердого вещества, промывают смесью этанол-вода 1:1 и сушат под вакуумом при 50oC. Таким путем получают указанное в заголовке соединение в виде серого порошка; Тпл 85-87oC; выход: 83% от теории.
10. 2-{ [[4-[(5-бензотиазол-2-ил)-1,5-дитиапент-1-ил] -3-метил-2- пиридинил]метил]тио}-1H-бензимидазол
По методике, описанной в примере 9, взаимодействием с 2-меркаптобензтиазолом получают соединение, указанное в заголовке; Тпл 126-128oC; выход: 85% от теории.
По методике, описанной в примере 9, взаимодействием с 2-меркаптобензтиазолом получают соединение, указанное в заголовке; Тпл 126-128oC; выход: 85% от теории.
11. 2-{ [[4-[(5-бензоксазол-2-ил)-1,5-дитиапент-1-ил] -3-метил-2- пиридинил]метил]тио}-1H-бензимидазол
По методике, описанной в примере 9, взаимодействием с 2-меркаптобензоксазолом получают соединение, указанное в заголовке; Тпл 73-76oC; выход: 72% от теории.
По методике, описанной в примере 9, взаимодействием с 2-меркаптобензоксазолом получают соединение, указанное в заголовке; Тпл 73-76oC; выход: 72% от теории.
12. 2-{[5-[2-[1H-бензимидазол-2-илтиометил] -3-метил-4-пиридинил]-1,5-дитиапент-1-ил}пиридин-3-карбоксилат натрия
2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил]тио}-1H- бензимидазол, метиловый эфир 2-меркаптоникотиновой кислоты (1,2 эквивалента) и карбонат кальция (5 эквивалентов) в течение 20 ч нагревают в метаноле с обратным холодильником до кипения. После охлаждения фильтруют, концентрируют досуха, смешивают с водой, экстрагируют дихлорметаном и остаточный дихлорметан отгоняют из водной фазы. Выпавшее в осадок из водной фазы твердое вещество отсасывают, промывают водой и сушат. Таким путем получают соединение, указанное в заголовке; Тпл 129-131oC; выход: 47% от теории.
2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил]тио}-1H- бензимидазол, метиловый эфир 2-меркаптоникотиновой кислоты (1,2 эквивалента) и карбонат кальция (5 эквивалентов) в течение 20 ч нагревают в метаноле с обратным холодильником до кипения. После охлаждения фильтруют, концентрируют досуха, смешивают с водой, экстрагируют дихлорметаном и остаточный дихлорметан отгоняют из водной фазы. Выпавшее в осадок из водной фазы твердое вещество отсасывают, промывают водой и сушат. Таким путем получают соединение, указанное в заголовке; Тпл 129-131oC; выход: 47% от теории.
13. 2-{[[4-[3-(2-карбоксифенилтио)пропилтио]-3-метил-2-пиридинил] метил] тио}-1H-бензимидазол
По методике, описанной в примере 12, взаимодействием с 2-меркаптобензойной кислотой после добавления водной соляной кислоты к водной фазе получают указанное в заголовке соединение в виде твердого вещества бежевого цвета; Тпл 142oC (разложение); выход: 57% от теории.
По методике, описанной в примере 12, взаимодействием с 2-меркаптобензойной кислотой после добавления водной соляной кислоты к водной фазе получают указанное в заголовке соединение в виде твердого вещества бежевого цвета; Тпл 142oC (разложение); выход: 57% от теории.
14. 2-{ [[3-метил-4-(3-(пиридин-4-илтио)пропилтио)-2-пиридинил] метил] тио}-1H-имидазо[4,5-b]пиридин
2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] тио} -1H-имидазо [2,3-b] пиридин нагревают с 4-меркаптопиридином (1,3 эквивалента) и едким натром (2 эквивалента) в течение 24 ч в смеси этанол-вода 2:1. Затем разбавляют водой и дают остыть. Выпавшее в осадок твердое вещество отсасывают и сушат. Таким путем получают соединение, указанное в заголовке; Тпл 69- 72oC; выход: 39% от теории.
2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] тио} -1H-имидазо [2,3-b] пиридин нагревают с 4-меркаптопиридином (1,3 эквивалента) и едким натром (2 эквивалента) в течение 24 ч в смеси этанол-вода 2:1. Затем разбавляют водой и дают остыть. Выпавшее в осадок твердое вещество отсасывают и сушат. Таким путем получают соединение, указанное в заголовке; Тпл 69- 72oC; выход: 39% от теории.
15. 2-{ [[3-метил-4-(3-(1-метилтетразол-5-илтио)пропилтио)-2-пиридинил] метил]тио}-1Н-имидазо[4,5-b]пиридин
По методике, описанной в примере 14, взаимодействием с 1-метил-2- меркаптотетразолом получают соединение, указанное в заголовке; Тпл 56oC (разложение); выход: 78% от теории.
По методике, описанной в примере 14, взаимодействием с 1-метил-2- меркаптотетразолом получают соединение, указанное в заголовке; Тпл 56oC (разложение); выход: 78% от теории.
16. 2-{[[3-метил-4-(3-(пиримидин-2-илтио)пропилтио)-2-пиридинил] метил] тио}-1H-имидазо[4,5-b]пиридин
По методике, описанной в примере 14, взаимодействием с 2-меркаптопиримидином получают соединение, указанное в заголовке; Тпл 136oC (разложение); выход: 90% от теории.
По методике, описанной в примере 14, взаимодействием с 2-меркаптопиримидином получают соединение, указанное в заголовке; Тпл 136oC (разложение); выход: 90% от теории.
17. Тригидрохлорид 2-{ [[4-[3-(1-(2-диметиламиноэтил)тетразол- 5-илтио)пропилтио]-2-пиридинил]метил]тио}-1H-имидазо[4,5-b]пиридина
По методике, описанной в примере 14, взаимодействием с 1-[(2-диметиламино)этил] -5-меркаптотетразолом получают свободное основание указанного в заголовке соединения в виде масла. Из этого продукта с помощью концентрированной соляной кислоты в ацетоне получают гидрохлорид, получая таким путем указанное в заголовке соединение в виде бесцветного твердого вещества; Тпл 81-83oC; выход: 39% от теории.
По методике, описанной в примере 14, взаимодействием с 1-[(2-диметиламино)этил] -5-меркаптотетразолом получают свободное основание указанного в заголовке соединения в виде масла. Из этого продукта с помощью концентрированной соляной кислоты в ацетоне получают гидрохлорид, получая таким путем указанное в заголовке соединение в виде бесцветного твердого вещества; Тпл 81-83oC; выход: 39% от теории.
18. 2-{[[4-[5-(N-циан-N'-метиламидино)-1,5-дитиапент-1-ил]-3-метил- 2-пиридинил]метил]тио}-1H-бензимидазол
По методике, описанной в примере 5, взаимодействием с Na-солью N-циан-N'-метилизотиомочевины в изопропаноле после добавления в реакционную смесь воды получают непосредственно указанное в заголовке соединение в виде светло-желтого твердого вещества; Тпл 136-138oC; выход: 79% от теории.
По методике, описанной в примере 5, взаимодействием с Na-солью N-циан-N'-метилизотиомочевины в изопропаноле после добавления в реакционную смесь воды получают непосредственно указанное в заголовке соединение в виде светло-желтого твердого вещества; Тпл 136-138oC; выход: 79% от теории.
19. 2-{ 4-[3-(5-хлортиофен-2-илметилтио)пропилтио] -3-метилпиридин- 2-илметилтио}-1H-бензимидазол
364 мг (1 ммоль) 2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил]-тио} -1Н-бензимидазола, 340 мг (1,4 ммоля) хлорида 5-хлор-2-тиофен-2-илметилизотиурония и 1,8 мл (3,5 ммоля) 2 Н NaOH кипятят в 10 мл этанола в течение 3 ч с обратным холодильником. Затем разбавляют водой и этанол отгоняют. Остаток трижды экстрагируют дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с помощью системы растворителей уксусный эфир-концентрированный аммиак 99:1. Указанное в заголовке соединение кристаллизуют растиранием с диизопропиловым эфиром. Тпл 74-77oC; выход: 240 мг (49% от теории).
364 мг (1 ммоль) 2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил]-тио} -1Н-бензимидазола, 340 мг (1,4 ммоля) хлорида 5-хлор-2-тиофен-2-илметилизотиурония и 1,8 мл (3,5 ммоля) 2 Н NaOH кипятят в 10 мл этанола в течение 3 ч с обратным холодильником. Затем разбавляют водой и этанол отгоняют. Остаток трижды экстрагируют дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с помощью системы растворителей уксусный эфир-концентрированный аммиак 99:1. Указанное в заголовке соединение кристаллизуют растиранием с диизопропиловым эфиром. Тпл 74-77oC; выход: 240 мг (49% от теории).
20. Тригидрохлорид 2-(3-метил-4-{ 3-[2-(2-метил-5-нитроимидазол-1- ил)этилтио]пропилтио}пиридин-2-илметилтио)-1H-бензимидазола
4,3 г (12 ммолей) иодида 2-[2-(2-метил-5-нитроимидазол-1-ил)этил] изотиурония растворяют в 80 мл этанола. Затем добавляют 0,96 г (24 ммоля) борогидрида натрия. После завершения газообразования добавляют 2,9 г (8 ммолей) 2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] тио}-1H-бензимидазола. Далее оставляют на 8 ч при комнатной температуре для перемешивания. После завершения реакции подкисляют для разложения избыточного борогидрида натрия. Затем разбавляют водой, этанол отгоняют и pH устанавливают приблизительно на 11. После этого трижды экстрагируют дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с помощью системы растворителей уксусный эфир-метанол-концентрированный аммиак 89:10:1. Неочищенный продукт растворяют в изопропаноле и подкисляют концентрированным HCl. Затем окончательно концентрируют. Указанное в заголовке соединение кристаллизуют при растирании с ацетоном. Тпл 144-149oC; выход: 1,6 г (32% от теории).
4,3 г (12 ммолей) иодида 2-[2-(2-метил-5-нитроимидазол-1-ил)этил] изотиурония растворяют в 80 мл этанола. Затем добавляют 0,96 г (24 ммоля) борогидрида натрия. После завершения газообразования добавляют 2,9 г (8 ммолей) 2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] тио}-1H-бензимидазола. Далее оставляют на 8 ч при комнатной температуре для перемешивания. После завершения реакции подкисляют для разложения избыточного борогидрида натрия. Затем разбавляют водой, этанол отгоняют и pH устанавливают приблизительно на 11. После этого трижды экстрагируют дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с помощью системы растворителей уксусный эфир-метанол-концентрированный аммиак 89:10:1. Неочищенный продукт растворяют в изопропаноле и подкисляют концентрированным HCl. Затем окончательно концентрируют. Указанное в заголовке соединение кристаллизуют при растирании с ацетоном. Тпл 144-149oC; выход: 1,6 г (32% от теории).
21. Дигидрохлорид 2-(3-метил-4-{3-[3-(2-метил-5-нитроимидазол-1-ил) пропилтио]пропилтио}пиридин-2-илметилтио)-1H-бензимидазола
По методике, описанной в примере 20, взаимодействием с хлоридом 2-[3-(2-метил-5-нитроимидазол-1-ил)пропил] изотиурония получают соединение, указанное в заголовке; Тпл 118oC (разложение); выход: 13% от теории.
По методике, описанной в примере 20, взаимодействием с хлоридом 2-[3-(2-метил-5-нитроимидазол-1-ил)пропил] изотиурония получают соединение, указанное в заголовке; Тпл 118oC (разложение); выход: 13% от теории.
22. 2-(3-метил-4-{ 2-[2-(2-метил-5-нитроимидазол-1-ил)этилтио] этилтио} пиридин-2-илметилтио)-1H-бензимидазол
По методике, описанной в примере 19, взаимодействием 2-{[[4-(2-хлорэтилтио)-3-метил-2-пиридинил] метил]тио}-1H-бензимидазола с иодидом 2-[2-(2-метил-5-нитроимидазол-1-ил)этил]изотиурония получали соединение, указанное в заголовке. Тпл 142-145oC; выход: 33% от теории.
По методике, описанной в примере 19, взаимодействием 2-{[[4-(2-хлорэтилтио)-3-метил-2-пиридинил] метил]тио}-1H-бензимидазола с иодидом 2-[2-(2-метил-5-нитроимидазол-1-ил)этил]изотиурония получали соединение, указанное в заголовке. Тпл 142-145oC; выход: 33% от теории.
23. 2-(3-метил-4-{ 4-[2-(2-метил-5-нитроимидазол-1-ил)этилтио]бутилтио} пиридин-2-илметилтио)-1Н-бензимидазол
2,5 г (6 ммолей) 2-хлорметил-3-метил-4-{4-[2-(2-метил-5- нитроимидазол-1-ил)этилтио] бутилтио} пиридина и 0,9 г (6 ммолей) 2-меркаптобензимидазола кипятят в 25 мл изопропанола в течение 1 ч с обратным холодильником. Затем охлаждают в ледяной бане и выпавшее твердое вещество отсасывают. Это твердое вещество растворяют в воде и смешивают с насыщенным раствором гидрокарбоната натрия, после чего экстрагируют дихлорметаном. Органическую фазу промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Указанное в заголовке соединение кристаллизуется, и после смешения с небольшим количеством метанола его очищают. Тпл 160-162oC; выход: 0,62 г (20% от теории).
2,5 г (6 ммолей) 2-хлорметил-3-метил-4-{4-[2-(2-метил-5- нитроимидазол-1-ил)этилтио] бутилтио} пиридина и 0,9 г (6 ммолей) 2-меркаптобензимидазола кипятят в 25 мл изопропанола в течение 1 ч с обратным холодильником. Затем охлаждают в ледяной бане и выпавшее твердое вещество отсасывают. Это твердое вещество растворяют в воде и смешивают с насыщенным раствором гидрокарбоната натрия, после чего экстрагируют дихлорметаном. Органическую фазу промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Указанное в заголовке соединение кристаллизуется, и после смешения с небольшим количеством метанола его очищают. Тпл 160-162oC; выход: 0,62 г (20% от теории).
24. 2-(3-метил-4-{3-[2-(2-метил-5-нитроимидазол-1-ил)этилтио] пропилтио} -пиридин-2-илметилтио)-1H-имидазо[4,5-b]пиридин
2,68 г (7,5 ммоля) иодида 2-[2-(2-метил-5-нитроимидазол-1-ил)этил] изотиурония растворяют в 30 мл этанола и смешивают с 0,57 г (15 ммолей) борогидрида натрия. После завершения газообразования добавляют 1,82 г (5 ммолей) 2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил]тио}-1H-имидазо [4,5-b] пиридина. Затем в течение 10 ч кипятят с обратным холодильником. После завершения реакции подкисляют для разложения избыточного борогидрида натрия. Затем разбавляют водой, этанол отгоняют и pH устанавливают приблизительно на 11. После этого экстрагируют трижды дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Остаток хроматографируют на силикагеле в системе растворителей уксусный эфир-метанол-концентрированный аммиак 75:20:5. Неочищенный продукт растворяют в изопропаноле и подкисляют концентрированным HCl. Затем окончательно концентрируют. Указанное в заголовке соединение кристаллизуется при растирании с ацетоном. Тпл 75oC (разложение); выход: 0,81 г (28% от теории).
2,68 г (7,5 ммоля) иодида 2-[2-(2-метил-5-нитроимидазол-1-ил)этил] изотиурония растворяют в 30 мл этанола и смешивают с 0,57 г (15 ммолей) борогидрида натрия. После завершения газообразования добавляют 1,82 г (5 ммолей) 2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил]тио}-1H-имидазо [4,5-b] пиридина. Затем в течение 10 ч кипятят с обратным холодильником. После завершения реакции подкисляют для разложения избыточного борогидрида натрия. Затем разбавляют водой, этанол отгоняют и pH устанавливают приблизительно на 11. После этого экстрагируют трижды дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Остаток хроматографируют на силикагеле в системе растворителей уксусный эфир-метанол-концентрированный аммиак 75:20:5. Неочищенный продукт растворяют в изопропаноле и подкисляют концентрированным HCl. Затем окончательно концентрируют. Указанное в заголовке соединение кристаллизуется при растирании с ацетоном. Тпл 75oC (разложение); выход: 0,81 г (28% от теории).
Исходные соединения
A1. 2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил]тио}-1H- бензимидазол
К раствору из 2-меркапто-1Н-бензимидазола (1,5 г/10 ммолей) в 40 мл этанола и 21 мл 1 H едкого натра в течение 20 мин при 40oC по каплям добавляют один эквивалент гидрохлорида 2-хлорметил-4-(3-хлорпропилтио)-3-метилпиридина, растворенного в 10 мл воды. Затем перемешивают в течение 2-3 ч при 50-60oC и далее продолжают перемешивание в течение 3-4 ч при комнатной температуре, после чего этанол отгоняют в ротационном испарителе (1 кПа/40oC), трижды экстрагируют порциями по 20 мл дихлорметана соответственно, промывают 0,1 H едким натром, сушат над карбонатом калия и окончательно концентрируют под вакуумом. Для очистки сырой продукт хроматографируют на силикагеле (дихлорметан-метанол 20:1-3:1); собранные чистые фракции совместно концентрируют под вакуумом и кристаллизуют из дихлорметан-диизопропилового эфира. Затем перекристаллизовывают из метанол-толуола. Выход: 2,67 г (74%) указанного в заголовке соединения в виде бесцветного твердого вещества с Тпл 112-114oC.
A1. 2-{ [[4-(3-хлорпропилтио)-3-метил-2-пиридинил]метил]тио}-1H- бензимидазол
К раствору из 2-меркапто-1Н-бензимидазола (1,5 г/10 ммолей) в 40 мл этанола и 21 мл 1 H едкого натра в течение 20 мин при 40oC по каплям добавляют один эквивалент гидрохлорида 2-хлорметил-4-(3-хлорпропилтио)-3-метилпиридина, растворенного в 10 мл воды. Затем перемешивают в течение 2-3 ч при 50-60oC и далее продолжают перемешивание в течение 3-4 ч при комнатной температуре, после чего этанол отгоняют в ротационном испарителе (1 кПа/40oC), трижды экстрагируют порциями по 20 мл дихлорметана соответственно, промывают 0,1 H едким натром, сушат над карбонатом калия и окончательно концентрируют под вакуумом. Для очистки сырой продукт хроматографируют на силикагеле (дихлорметан-метанол 20:1-3:1); собранные чистые фракции совместно концентрируют под вакуумом и кристаллизуют из дихлорметан-диизопропилового эфира. Затем перекристаллизовывают из метанол-толуола. Выход: 2,67 г (74%) указанного в заголовке соединения в виде бесцветного твердого вещества с Тпл 112-114oC.
A2. Гидрохлорид 2-хлорметил-4-(3-хлорпропилтио)-3-метилпиридина
a) N-оксид 2,3-диметил-4-(3-гидроксипропилтио)пиридина
К 50 мл сухого N-метилпирролидона (МП) добавляют порциями 6 г 60%-ного NaH, перемешивают в течение 15 мин, затем в течение 20 мин добавляют 9,5 г (0,11 моля) 3-гидроксипропилмеркаптана и продолжают перемешивание в течение 30 мин до завершения газообразования. Затем в течение 20 мин по каплям добавляют раствор из 14,4 г (0,1 моля) N-оксида 4-хлор-2,3-диметилпиридина в 100 мл МП, реакционную смесь перемешивают в течение 1 ч при комнатной температуре, продолжают перемешивание в течение 1 ч при 70oC и после этого еще в течение 1 ч при 100oC.
a) N-оксид 2,3-диметил-4-(3-гидроксипропилтио)пиридина
К 50 мл сухого N-метилпирролидона (МП) добавляют порциями 6 г 60%-ного NaH, перемешивают в течение 15 мин, затем в течение 20 мин добавляют 9,5 г (0,11 моля) 3-гидроксипропилмеркаптана и продолжают перемешивание в течение 30 мин до завершения газообразования. Затем в течение 20 мин по каплям добавляют раствор из 14,4 г (0,1 моля) N-оксида 4-хлор-2,3-диметилпиридина в 100 мл МП, реакционную смесь перемешивают в течение 1 ч при комнатной температуре, продолжают перемешивание в течение 1 ч при 70oC и после этого еще в течение 1 ч при 100oC.
После завершения обменной реакции дают остыть, разбавляют 500 мл воды и четырежды экстрагируют порциями по 300 мл дихлорметана соответственно. Объединенные органические фазы промывают водой, сушат над сульфатом магния, концентрируют и кристаллизуют из толуола. После перекристаллизации из метанол-толуола получают указанное в заголовке соединение в виде твердого вещества бежевого цвета с Тпл 106-107oC (после сублимации); выход: 68% от теории.
б) 2-гидроксиметил-4-(3-гидроксипропилтио)-3-метилпиридин
Полученное в а) желтое масло растворяют в 100 мл уксусного ангидрида и перемешивают в течение 2 ч при 100oC. После концентрирования под вакуумом коричневый маслянистый остаток перегоняют в трубчатом с шаровыми расширениями дистилляционном аппарате и без очистки используют в последующей реакции.
Полученное в а) желтое масло растворяют в 100 мл уксусного ангидрида и перемешивают в течение 2 ч при 100oC. После концентрирования под вакуумом коричневый маслянистый остаток перегоняют в трубчатом с шаровыми расширениями дистилляционном аппарате и без очистки используют в последующей реакции.
Маслянистый дистиллят при перемешивании нагревают в течение 2 ч в 100 мл 2 H едкого натра и 100 мл изопропанола до температуры дефлегмации, после чего изопропанол отгоняют, остаток трижды экстрагируют порциями по 100 мл дихлорметана соответственно, объединенные органические фазы промывают водой, сушат над карбонатом калия и концентрируют под вакуумом. Таким путем получают 5,0 г 2-гидроксиметил-4-(3-гидроксипропилтио)-3-метилпиридина, который без очистки используют в последующей реакции. Из изопропанола с помощью концентрированной соляной кислоты можно получить моногидрохлорид соединения, указанного в заголовке; Тпл 188-190oC (разложение).
в) Гидрохлорид 2-хлорметил-4-(3-хлорпропилтио)-3-метилпиридина
5,0 г масла, полученного в б), растворяют в 100 мл дихлорметана, по каплям добавляют 4 эквивалента тионилхлорида и перемешивают в течение 20 ч при комнатной температуре. Затем окончательно концентрируют, получая в результате 4,5 г указанного в заголовке соединения в виде маслянистого, постепенно кристаллизующегося остатка. После кристаллизации из пропанолдиизопропилового эфира получают указанное в заголовке соединение в виде бесцветного твердого вещества; Тпл 142-144oC (разложение).
5,0 г масла, полученного в б), растворяют в 100 мл дихлорметана, по каплям добавляют 4 эквивалента тионилхлорида и перемешивают в течение 20 ч при комнатной температуре. Затем окончательно концентрируют, получая в результате 4,5 г указанного в заголовке соединения в виде маслянистого, постепенно кристаллизующегося остатка. После кристаллизации из пропанолдиизопропилового эфира получают указанное в заголовке соединение в виде бесцветного твердого вещества; Тпл 142-144oC (разложение).
Б1. 2-{ [[4-(2-хлорэтилтио)-3-метил-2-пиридинил]метил]тио) -1H-бензимидазол
По методике, описанной в примере A1, взаимодействием 2-меркапто-1Н-бензимидазола с гидрохлоридом 4-(2-хлорэтилтио)-2-хлорметил-3-метилпиридина и NaOH после кристаллизации из уксусного эфира получают указанное в заголовке соединение (62% от теории) в виде бесцветного твердого вещества с Тпл 178-180oC.
По методике, описанной в примере A1, взаимодействием 2-меркапто-1Н-бензимидазола с гидрохлоридом 4-(2-хлорэтилтио)-2-хлорметил-3-метилпиридина и NaOH после кристаллизации из уксусного эфира получают указанное в заголовке соединение (62% от теории) в виде бесцветного твердого вещества с Тпл 178-180oC.
Б2. Гидрохлорид 4-(2-хлорэтилтио)-2-хлорметил-3-метилпиридина
a) N-оксид 2,3-диметил-4-(2-гидроксиэтилтио)пиридина
По методике, описанной в примере А2.а), взаимодействием N-оксида 4-хлор-2,3-диметилпиридина с 2-меркаптоэтанолом и гидридом натрия получают указанное в заголовке соединение в виде маслянистого остатка, который без дальнейшей очистки используют на последующей стадии.
a) N-оксид 2,3-диметил-4-(2-гидроксиэтилтио)пиридина
По методике, описанной в примере А2.а), взаимодействием N-оксида 4-хлор-2,3-диметилпиридина с 2-меркаптоэтанолом и гидридом натрия получают указанное в заголовке соединение в виде маслянистого остатка, который без дальнейшей очистки используют на последующей стадии.
б) 4-(2-гидроксиэтилтио)-2-гидроксиметил-3-метилпиридин
По методике, описанной в примере А2.б), взаимодействием полученного в а) масла с уксусным ангидридом и последующим омылением с помощью NaOH получают указанное в заголовке соединение в виде маслянистого остатка, который без дальнейшей очистки используют на последующей стадии.
По методике, описанной в примере А2.б), взаимодействием полученного в а) масла с уксусным ангидридом и последующим омылением с помощью NaOH получают указанное в заголовке соединение в виде маслянистого остатка, который без дальнейшей очистки используют на последующей стадии.
в) Гидрохлорид 4-(2-хлорэтилтио)-2-хлорметил-3-метилпиридина
По методике, описанной в примере А2.в), взаимодействием полученного в б) масла с тионилхлоридом получают указанное в заголовке соединение в виде маслянистого остатка, который в виде раствора в этаноле непосредственно используют для взаимодействия с 2-меркаптобензимидазолом.
По методике, описанной в примере А2.в), взаимодействием полученного в б) масла с тионилхлоридом получают указанное в заголовке соединение в виде маслянистого остатка, который в виде раствора в этаноле непосредственно используют для взаимодействия с 2-меркаптобензимидазолом.
В. Гидрохлорид 3-хлор-4-[N-(2-хлорэтил)-N-метиламино]-2- хлорметилпиридина
а) 3-хлор-4-[N-(2-гидроксиэтил)-N-метиламино]-2- гидроксиметилпиридин
Смесь из 3,4-дихлор-2-гидроксиметилпиридина (см. Journ. Med. Chem. 1989, 32, 1970) (2,5 г) в 2-метиламиноэтаноле (30 мл) нагревают в стальном автоклаве и выдерживают в течение 2,5 ч при 160oC, затем избыточный амин удаляют под высоким вакуумом и образовавшийся остаток хроматографируют на силикагеле (дихлорметан-метанол 95:5). Выход: 2,3 г в виде масла желтоватого цвета.
а) 3-хлор-4-[N-(2-гидроксиэтил)-N-метиламино]-2- гидроксиметилпиридин
Смесь из 3,4-дихлор-2-гидроксиметилпиридина (см. Journ. Med. Chem. 1989, 32, 1970) (2,5 г) в 2-метиламиноэтаноле (30 мл) нагревают в стальном автоклаве и выдерживают в течение 2,5 ч при 160oC, затем избыточный амин удаляют под высоким вакуумом и образовавшийся остаток хроматографируют на силикагеле (дихлорметан-метанол 95:5). Выход: 2,3 г в виде масла желтоватого цвета.
б) Гидрохлорид 3-хлор-4-[N-(2-хлорэтил)-N-метиламино] -2- хлорметилпиридина
Раствор 3-хлор-4-[N-(2-гидроксиэтил)-N-метиламино] -2-гидроксиметилпиридина (2,3 г) в дихлорметане (30 мл) при 0oC смешивают по каплям с раствором тионилхлорида (4 мл) в дихлорметане (20 мл). Затем дают температуре подняться до 20oC (20 мин) и далее температуру в течение 30 мин поддерживают на уровне 40oC. После удаления растворителя под вакуумом образовавшийся остаток хроматографируют на силикагеле (смесь петролейный эфир-этилацетат 7: 3, содержащая 1 мл концентрированного водного раствора NH3). Выход: 2,6 г.
Раствор 3-хлор-4-[N-(2-гидроксиэтил)-N-метиламино] -2-гидроксиметилпиридина (2,3 г) в дихлорметане (30 мл) при 0oC смешивают по каплям с раствором тионилхлорида (4 мл) в дихлорметане (20 мл). Затем дают температуре подняться до 20oC (20 мин) и далее температуру в течение 30 мин поддерживают на уровне 40oC. После удаления растворителя под вакуумом образовавшийся остаток хроматографируют на силикагеле (смесь петролейный эфир-этилацетат 7: 3, содержащая 1 мл концентрированного водного раствора NH3). Выход: 2,6 г.
Г1. Дигидрохлорид 2-{[[4-(3-хлорпропилтио)-3-метокси-2-пиридинил] метил] тио}-1H-бензимидазола
2-меркапто-1Н-бензимидазол (10 г) и гидрохлорид 2-хлорметил-4-(3-хлорпропилтио)-3-метоксипиридина (1 эквивалент) перемешивают в 150 мл изопропанола и 15 мл воды в течение 5 ч при 80oC, затем охлаждают, отфильтровывают от выпавшего твердого вещества и перекристаллизовывают из изопропанол-воды. Таким путем получают указанное в заголовке соединение в виде светло-коричневого порошка; Тпл 117-119oC (разложение); выход: 67% от теории.
2-меркапто-1Н-бензимидазол (10 г) и гидрохлорид 2-хлорметил-4-(3-хлорпропилтио)-3-метоксипиридина (1 эквивалент) перемешивают в 150 мл изопропанола и 15 мл воды в течение 5 ч при 80oC, затем охлаждают, отфильтровывают от выпавшего твердого вещества и перекристаллизовывают из изопропанол-воды. Таким путем получают указанное в заголовке соединение в виде светло-коричневого порошка; Тпл 117-119oC (разложение); выход: 67% от теории.
Г2. Гидрохлорид 2-хлорметил-4-(3-хлорпропилтио)-3-метоксипиридина
По методике, описанной в примере А2а), б), в), исходя из N-оксида 4-хлор-3-метокси-2-метилпиридина получают указанное в заголовке соединение в виде медленно кристаллизующегося масла, которое непосредственно используют в последующей реакции.
По методике, описанной в примере А2а), б), в), исходя из N-оксида 4-хлор-3-метокси-2-метилпиридина получают указанное в заголовке соединение в виде медленно кристаллизующегося масла, которое непосредственно используют в последующей реакции.
Д1. Дигидрохлорид 2-{[[4-(3-хлорпропилтио)-3-метил-2-пиридинил] метил] -тио}-1H-имидазо[4,5-b]пиридина
По методике, описанной в примере Г1, взаимодействием 2-меркапто-1Н-имидазо[2,3-b] пиридина с гидрохлоридом 2-хлорметил-4-(3-хлорпропилтио)-3-метилпиридина получают указанное в заголовке соединение в виде бесцветного порошка; Тпл 186-188oC; выход: 88% от теории.
По методике, описанной в примере Г1, взаимодействием 2-меркапто-1Н-имидазо[2,3-b] пиридина с гидрохлоридом 2-хлорметил-4-(3-хлорпропилтио)-3-метилпиридина получают указанное в заголовке соединение в виде бесцветного порошка; Тпл 186-188oC; выход: 88% от теории.
Е. 2-хлорметил-3-метил-4-{ 4-[2-(2-метил-5-нитроимидазол-1-ил) этилтио] бутилтио}пиридин
а) 2-гидроксиметил-4-(4-меркаптобутилтио)-3-метилпиридин
4,2 г (145 ммолей) гидрида натрия (80%-ного в парафине) растворяют при охлаждении льдом в 100 мл ДМФ. Затем медленно по каплям добавляют 35,5 г (290 ммолей) 1,4-бутандитиола. После завершения газообразования добавляют по каплям 15,3 г (97 ммолей) 4-хлор-2-гидроксиметил-3-метилпиридина в 20 мл ДМФ. Приблизительно через 30 мин смеси дают нагреться до комнатной температуры и перемешивают в течение 12 ч при этой температуре. Далее разбавляют 800 мл ледяной воды и нейтрализуют уксусной кислотой, после чего трижды экстрагируют дихлорметаном. Объединенные органические фазы четырежды промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Неочищенный продукт хроматографируют на силикагеле в системе растворителей уксусный эфир-концентрированный аммиак 99:1. Таким путем получают указанное в заголовке соединение в виде желтого кристаллизата. Тпл 58-63oC; выход: 13 г (55% от теории).
а) 2-гидроксиметил-4-(4-меркаптобутилтио)-3-метилпиридин
4,2 г (145 ммолей) гидрида натрия (80%-ного в парафине) растворяют при охлаждении льдом в 100 мл ДМФ. Затем медленно по каплям добавляют 35,5 г (290 ммолей) 1,4-бутандитиола. После завершения газообразования добавляют по каплям 15,3 г (97 ммолей) 4-хлор-2-гидроксиметил-3-метилпиридина в 20 мл ДМФ. Приблизительно через 30 мин смеси дают нагреться до комнатной температуры и перемешивают в течение 12 ч при этой температуре. Далее разбавляют 800 мл ледяной воды и нейтрализуют уксусной кислотой, после чего трижды экстрагируют дихлорметаном. Объединенные органические фазы четырежды промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Неочищенный продукт хроматографируют на силикагеле в системе растворителей уксусный эфир-концентрированный аммиак 99:1. Таким путем получают указанное в заголовке соединение в виде желтого кристаллизата. Тпл 58-63oC; выход: 13 г (55% от теории).
б) 2-гидроксиметил-3-метил-4-{4-[2-(2-метил-5-нитроимидазол-1- ил)этилтио]бутилтио}пиридин
0,43 г (15 ммолей) гидрида натрия растворяют при охлаждении льдом в 25 мл ДМФ. Затем добавляют 3,33 г (13,7 ммолей) 2-гидроксиметил-4-(4-меркаптобутилтио)-3-метилпиридина. После завершения газообразования по каплям добавляют 2,62 г (13,7 ммолей) 1-(2-хлорэтил)-2-метил-5-нитроимидазола в 10 мл ДМФ. При охлаждении льдом оставляют на 1 ч для перемешивания. Затем разбавляют 200 мл ледяной воды и нейтрализуют уксусной кислотой, после чего трижды экстрагируют дихлорметаном. Объединенные органические фазы четырежды промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Неочищенный продукт хроматографируют на силикагеле в системе растворителей уксусный эфир-метанол-концентрированный аммиак 89:10:1. Путем концентрирования указанное в заголовке соединение получают в виде желтого кристаллизата, очищаемого смешением с диэтиловым эфиром. Тпл 86-87oC; выход: 4 г (75% от теории).
0,43 г (15 ммолей) гидрида натрия растворяют при охлаждении льдом в 25 мл ДМФ. Затем добавляют 3,33 г (13,7 ммолей) 2-гидроксиметил-4-(4-меркаптобутилтио)-3-метилпиридина. После завершения газообразования по каплям добавляют 2,62 г (13,7 ммолей) 1-(2-хлорэтил)-2-метил-5-нитроимидазола в 10 мл ДМФ. При охлаждении льдом оставляют на 1 ч для перемешивания. Затем разбавляют 200 мл ледяной воды и нейтрализуют уксусной кислотой, после чего трижды экстрагируют дихлорметаном. Объединенные органические фазы четырежды промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Неочищенный продукт хроматографируют на силикагеле в системе растворителей уксусный эфир-метанол-концентрированный аммиак 89:10:1. Путем концентрирования указанное в заголовке соединение получают в виде желтого кристаллизата, очищаемого смешением с диэтиловым эфиром. Тпл 86-87oC; выход: 4 г (75% от теории).
в) 2-хлорметил-3-метил-4-{ 4-[2-(2-метил-5-нитроимидазол-1- ил)этилтио] бутилтио}пиридин
4 г (10 ммолей) 2-гидроксиметил-3-метил-4-{4-[2-(2-метил-5- нитроимидазол-1-ил)этилтио] бутилтио} пиридина растворяют в 40 мл дихлорметана. При охлаждении льдом по каплям добавляют 1,56 г (13,11 ммолей) тионилхлорида в 5 мл дихлорметана, после чего оставляют для перемешивания на 2 ч при 0oC. Затем смесь сливают на 250 мл ледяной воды и нейтрализуют насыщенным раствором гидрокарбоната натрия. Дихлорметановую фазу отделяют и водную фазу повторно экстрагируют дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Таким путем получают указанное в заголовке соединение в виде желтого масла, которое без дальнейшей очистки используют в последующей реакции. Выход: 4,15 г (100% от теории).
4 г (10 ммолей) 2-гидроксиметил-3-метил-4-{4-[2-(2-метил-5- нитроимидазол-1-ил)этилтио] бутилтио} пиридина растворяют в 40 мл дихлорметана. При охлаждении льдом по каплям добавляют 1,56 г (13,11 ммолей) тионилхлорида в 5 мл дихлорметана, после чего оставляют для перемешивания на 2 ч при 0oC. Затем смесь сливают на 250 мл ледяной воды и нейтрализуют насыщенным раствором гидрокарбоната натрия. Дихлорметановую фазу отделяют и водную фазу повторно экстрагируют дихлорметаном. Объединенные органические фазы промывают водой, сушат над сульфатом магния, фильтруют и концентрируют. Таким путем получают указанное в заголовке соединение в виде желтого масла, которое без дальнейшей очистки используют в последующей реакции. Выход: 4,15 г (100% от теории).
Промышленная применимость
Исключительно высокая эффективность соединений формулы I и их солей по отношению к бактериям Helicobacter позволяет применять их в медицине в качестве действующих веществ для лечения болезней, возбудителями которых являются бактерии Helicobacter.
Исключительно высокая эффективность соединений формулы I и их солей по отношению к бактериям Helicobacter позволяет применять их в медицине в качестве действующих веществ для лечения болезней, возбудителями которых являются бактерии Helicobacter.
Другим предметом изобретения в соответствии с этим является способ лечения млекопитающих, прежде всего человека, страдающих заболеваниями, обусловленными бактериями Helicobacter. Способ отличается тем, что заболевшему пациенту вводят терапевтически эффективное и фармакологически приемлемое количество одного или нескольких соединений формулы I и/или их фармакологически приемлемых солей.
Предметом изобретения, кроме того, являются соединения формулы I и их фармакологически приемлемые соли для применения при лечении болезней, возбудителями которых являются бактерии Helicobacter.
Изобретение включает также применение соединений формулы I и их фармакологически приемлемых солей при изготовлении лекарственных средств, предназначенных для борьбы с такими болезнями, которые обусловлены бактериями Helicobacter.
Еще одним предметом изобретения являются лекарственные средства для борьбы с бактериями Helicobacter, содержащие одно или несколько соединений общей формулы I и/или их фармакологически приемлемые соли.
Из штаммов бактерий Helicobacter, по отношению к которым соединения формулы I обладают активностью, следует назвать прежде всего штамм Helicobacter pylori.
Лекарственные средства изготавливают с помощью известных, обычных для специалиста в данной области техники способов. В качестве лекарственных средств фармакологически эффективные соединения формулы I и их соли (также являющиеся действующими веществами) применяют либо индивидуально, либо предпочтительно в комбинации с соответствующими фармацевтическими вспомогательными веществами, например, в виде таблеток, драже, капсул, эмульсий, суспензий, гелей или растворов, причем содержание действующих веществ предпочтительно составляет от 0,1 до 95%.
Какие именно вспомогательные вещества для требуемых лекарственных комбинаций следует выбрать, решает сам специалист на основе своих знаний и опыта. Наряду с растворителями, гелеобразователями, вспомогательными веществами для таблеток и другими носителями действующих веществ могут использоваться также, например, антиоксиданты, диспергаторы, эмульгаторы, антивспениватели, корригенты вкуса, консерванты, вещества, способствующие растворимости, красители или промоторы, улучшающие проницаемость, и комплексообразователи (в частности, циклодекстрины).
Действующие вещества могут назначаться, например, для парентерального (в частности, внутривенного) или прежде всего для орального введения.
Как правило, в медицине для достижения необходимого эффекта действующие вещества назначают в суточной дозировке порядка 0,2-50, предпочтительно 1-30 мг/кг веса тела, при необходимости разбивая суточную дозу на несколько, предпочтительно 2-6, разовых доз.
В соответствии с этим одним из существенных аспектов настоящего изобретения является то, что соединения формулы I, в которых n означает число 0, проявляют свою эффективность по отношению к бактериям Helicobacter при введении даже в такой дозировке, которую для достижения требуемого терапевтического эффекта необходимо, как полагают, назначать для подавления секреции желудочной кислоты.
Соединения формулы I, в которых n означает число 1, наряду с эффективностью по отношению к бактериям Helicobacter обладают также ярко выраженным ингибирующим действием касательно секреции желудочной кислоты. В соответствии с этим указанные соединения могут применяться также для лечения заболеваний, обусловленных повышенной секрецией желудочной кислоты.
Предлагаемые согласно изобретению соединения могут назначаться также для введения в строго определенной либо свободной комбинации совместно с субстанцией, нейтрализующей желудочную кислоту и/или подавляющей секрецию желудочной кислоты, и/или с субстанцией, применяемой в традиционных методах борьбы с бактериями Helicobacter pylori.
В качестве субстанций, нейтрализующих желудочную кислоту, можно назвать, например, гидрокарбонат натрия или другие антацидные средства, такие как гидроксид алюминия, алюминат магния или магальдрат. В качестве субстанций, ингибирующих секрецию желудочной кислоты, можно назвать, например, H2-блокатор (в частности, циметидин, ранитидин), ингибиторы H+/К+-АТФазы (в частности, лансопразол, омепразол или прежде всего пантопразол), а также так называемые периферийные антихолинергические средства (в частности, пирензепин, телензенпин).
Среди субстанций, применяемых в традиционных методах борьбы с бактериями Helicobacter pylori, следует назвать в первую очередь те из них, которые обладают противомикробным действием, как, например, пенициллин G, гентамицин, эритромицин, нитрофуразон, тинидазол, нитрофурантоин, фуразолидон, метронидазол и прежде всего амоксициллин, или же также соли висмута, как, например, цитрат висмута.
Биологические исследования
Соединения формулы I исследовали на их эффективность по отношению к бактериям Helicobacter pylori по методике, описанной Tomoyuki lwahi и др. в Antimicrobial Agents and Chemotherapy, 1991, 490-496, с использованием агара Columbia (оксоид) и периодом роста 4 дня. При этом в ходе исследований указанных соединений были выявлены приблизительные значения МИК-50, приведенные в таблице А (указанные номера соединений соответствуют номерам примеров в описании).
Соединения формулы I исследовали на их эффективность по отношению к бактериям Helicobacter pylori по методике, описанной Tomoyuki lwahi и др. в Antimicrobial Agents and Chemotherapy, 1991, 490-496, с использованием агара Columbia (оксоид) и периодом роста 4 дня. При этом в ходе исследований указанных соединений были выявлены приблизительные значения МИК-50, приведенные в таблице А (указанные номера соединений соответствуют номерам примеров в описании).
Claims (12)
1. Замещенные арилалкилтиоалкилтиопиридины формулы I:
где X означает СН или N;
Y означает S, SO, SO2, О, NH или N-С1-С4алкил;
R1 означает водород, С1-С4алкил, С1-С4алкокси или галоген;
R2 означает водород, С1-С4алкил, С1-С4алкокси, галоген, трифторметил, полностью либо преимущественно замещенный на фтор С1-С4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R3 при необходимости полностью либо частично замещенный на фтор С1-С2алкилендиокси или хлортрифторэтилендиокси;
R3 означает водород, полностью либо преимущественно замещенный на фтор С1-С4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R2 при необходимости полностью либо частично замещенный на фтор С1-С2алкилендиокси или хлортрифторэтилендиокси;
R4 означает водород, С1-С4алкил, замещенный на R14, С1-С4алкил, С1-С4алкилкарбонил, С2-С4алкенилкарбонил, галоген-С1-С4алкилкарбонил, N(R15)R16-C1-C4алкилкарбонил, ди-С1-С4алкилкарбамоил или С1-С4алкилсульфонил,
R5 означает водород, С1-С4алкил или С1-С4алкокси;
R6 означает моно- либо ди-С1-С4алкилкарбамоил или -тиокарбамоил, N-C1-С4алкил-N'-цианамидино, 1-N-С1-С4алкиламино-2-нитроэтилен, N-2-пропинил-N'-цианамидино, аминосульфониламидино или замещенный на R8 и R9 цикл или бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, тиадиазол-1-оксид, оксадиазол, пиридин, пиридин-N-оксид, пиримидин, триазин, пиридон, бензимидазол, имидазопиридин, бензтиазол и бензоксазол;
R7 означает водород, С1-С4алкил или С1-С4алкокси;
R8 означает водород, С1-С4алкил, гидрокси, С1-С4алкокси, галоген, нитро, гуанидино, карбокси, С1-С4алкоксикарбонил, замещенный на R10 С1-С1алкил или -N(R11)R12;
R9 означает водород, С1-С4алкил, гидрокси, С1-С4алкокси, фтор или трифторметил;
R10 означает гидрокси, С1-С4алкокси, карбокси, С1-С4алкоксикарбонил или -N(R11)R12, причем
R11 означает водород, С1-С4алкил или -CO-R13 и
R12 означает водород или С1-С4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал;
R13 означает водород, С1-С4алкил или С1-С4алкокси;
R14 означает гидрокси, С1-С4алкокси, карбокси, С1-С4алкоксикарбонил или -N(R15)R16, причем
R15 означает С1-С4алкил и
R16 означает С1-С4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал;
m означает число от 2 до 7;
n означает число 0 или 1,
p означает число 0 или 1;
q означает число 0, 1 или 2;
r означает число от 2 до 7;
t означает число 0 или 1 и
u означает число в интервале от 0 до 7,
и их соли, за исключением таких соединений формулы 1, в которых Y означает S или SO и одновременно Х означает СН, t означает число 0, u означает число О, R4 означает водород или С1-С4алкил и R6 представляет собой замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, оксадиазол, пиридин, пиридин-N-оксид, пиримидин и бензимидазол, а также за исключением таких соединений формулы 1, в которых Y означает NH или N-С1-С4алкил и одновременно t означает число 0 и R5 означает водород или С1-С4алкил.
где X означает СН или N;
Y означает S, SO, SO2, О, NH или N-С1-С4алкил;
R1 означает водород, С1-С4алкил, С1-С4алкокси или галоген;
R2 означает водород, С1-С4алкил, С1-С4алкокси, галоген, трифторметил, полностью либо преимущественно замещенный на фтор С1-С4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R3 при необходимости полностью либо частично замещенный на фтор С1-С2алкилендиокси или хлортрифторэтилендиокси;
R3 означает водород, полностью либо преимущественно замещенный на фтор С1-С4алкокси, хлордифторметокси, 2-хлор-1,1,2-трифторэтокси или совместно с R2 при необходимости полностью либо частично замещенный на фтор С1-С2алкилендиокси или хлортрифторэтилендиокси;
R4 означает водород, С1-С4алкил, замещенный на R14, С1-С4алкил, С1-С4алкилкарбонил, С2-С4алкенилкарбонил, галоген-С1-С4алкилкарбонил, N(R15)R16-C1-C4алкилкарбонил, ди-С1-С4алкилкарбамоил или С1-С4алкилсульфонил,
R5 означает водород, С1-С4алкил или С1-С4алкокси;
R6 означает моно- либо ди-С1-С4алкилкарбамоил или -тиокарбамоил, N-C1-С4алкил-N'-цианамидино, 1-N-С1-С4алкиламино-2-нитроэтилен, N-2-пропинил-N'-цианамидино, аминосульфониламидино или замещенный на R8 и R9 цикл или бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, тиадиазол-1-оксид, оксадиазол, пиридин, пиридин-N-оксид, пиримидин, триазин, пиридон, бензимидазол, имидазопиридин, бензтиазол и бензоксазол;
R7 означает водород, С1-С4алкил или С1-С4алкокси;
R8 означает водород, С1-С4алкил, гидрокси, С1-С4алкокси, галоген, нитро, гуанидино, карбокси, С1-С4алкоксикарбонил, замещенный на R10 С1-С1алкил или -N(R11)R12;
R9 означает водород, С1-С4алкил, гидрокси, С1-С4алкокси, фтор или трифторметил;
R10 означает гидрокси, С1-С4алкокси, карбокси, С1-С4алкоксикарбонил или -N(R11)R12, причем
R11 означает водород, С1-С4алкил или -CO-R13 и
R12 означает водород или С1-С4алкил или же
R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал;
R13 означает водород, С1-С4алкил или С1-С4алкокси;
R14 означает гидрокси, С1-С4алкокси, карбокси, С1-С4алкоксикарбонил или -N(R15)R16, причем
R15 означает С1-С4алкил и
R16 означает С1-С4алкил или же
R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал;
m означает число от 2 до 7;
n означает число 0 или 1,
p означает число 0 или 1;
q означает число 0, 1 или 2;
r означает число от 2 до 7;
t означает число 0 или 1 и
u означает число в интервале от 0 до 7,
и их соли, за исключением таких соединений формулы 1, в которых Y означает S или SO и одновременно Х означает СН, t означает число 0, u означает число О, R4 означает водород или С1-С4алкил и R6 представляет собой замещенный на R8 и R9 цикл либо бицикл, выбранный из группы, включающей бензол, фуран, тиофен, пиррол, оксазол, изоксазол, тиазол, тиазолин, изотиазол, имидазол, имидазолин, пиразол, триазол, тетразол, тиадиазол, оксадиазол, пиридин, пиридин-N-оксид, пиримидин и бензимидазол, а также за исключением таких соединений формулы 1, в которых Y означает NH или N-С1-С4алкил и одновременно t означает число 0 и R5 означает водород или С1-С4алкил.
2. Соединения формулы I по п. 1, в которых Y имеет значение О (кислород).
3. Соединения формулы I по п. 1, в которых Х имеет значение СН, Y имеет значение S, t означает число 0 и u означает число от 1 до 7.
4. Соединения формулы I по п. 1, в которых Х имеет значение СН, Y имеет значение S, t означает число 0, u означает число 0 и R4 представляет собой замещенный на R14, С1-С4алкил, С1-С4алкилкарбонил, С2-С4алкенилкарбонил, галоген-С1-С4алкилкарбонил, N(R15)R16-С1-С4алкилкарбонил, ди-С1-С4алкилкарбамоил или С1-С4алкилсульфонил.
5. Соединения формулы I по п. 1, в которых Y имеет значение S, t означает число 0, u означает число 0 и R6 представляет собой моно- либо ди-С1-С4алкилкарбамоил или -тиокарбамоил, N-С1-С4алкил-N'-цианамидино, 1-N-С1-С4алкиламино-2-нитроэтил, N-2-пропинил-N'-цианамидино, аминосульфониламидино или замещенный на R8 и R9 цикл, выбранный из группы, включающей тиадиазол-1-оксид, триазин, пиридон, имидазопиридин, бензтиазол и бензоксазол.
6. Соединения формулы I по п. 1, в которых Y означает NH или N-C1-С4алкил, t означает число 0 и R5 означает С1-С4алкокси.
7. Соединения формулы I по п. 1, в которых Х означает СН или N; Y означает S или SO2; R1 означает водород, С1-С4алкокси или фтор; R2 означает водород, С1-С4алкил или фтор, R3 означает водород, R4 означает водород, замещенный на R14, С1-С4алкил или С1-С4алкилсульфонил, R5 означает водород или С1-С4алкил; R6 представляет собой ди-С1-С4алкилтиокарбамоил, N-C1-C4алкил-N'-цианамидино или замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин, пиримидин и триазин; R7 означает водород или С1-С4алкил; R8 означает водород, С1-С4алкил, гидрокси, нитро, гуанидино, карбокси, С1-С4алкоксикарбонил или замещенный на R10, С1-С4алкил; R9 означает водород, С1-С4алкил, гидрокси или фтор; R10 означает гидрокси, С1-С4алкоксикарбонил или-N(R11)R12, причем R11 означает С1-С4алкил и R12 означает С1-С4алкил или же R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал; R14 означает С1-С4алкоксикарбонил или -N(R15)R16, причем R15 означает С1-С4алкил и R16 означает С1-С4алкил или же R15 и R16 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал; m означает число от 2 до 4; п означает число 0; р означает число 0, t означает число 0 и u означает число в интервале от 0 до 3, и их соли, за исключением таких соединений формулы I, в которых Y означает S и одновременно Х означает СН, u означает число 0, R4 означает водород и R6 представляет собой замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин.
8. Соединения формулы I по п. 1, в которых Х означает СН или N; Y означает S или SO2; R1 означает водород, С1-С4алкокси или фтор; R2 означает водород или фтор; R3 означает водород; R4 означает водород; R5 означает С1-С4алкил; R6 представляет собой ди-С1-С4алкилтиокарбамоил или замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин; R7 означает водород; R8 означает водород, нитро, С1-С4алкоксикарбонил или замещенный на R10, С1-С2алкил; R9 означает водород или C1-С4алкил; R10 означает С1-С4алкоксикарбонил или -N(R11)R12, причем R11 означает С1-С4алкил и R12 означает С1-С4алкил или же R11 и R12 вместе и включая атом азота, по которому они оба связаны, представляют собой пиперидиновый или морфолиновый радикал; m означает число 2 или 3; n означает число 0; р означает число 0; t означает число 0 и u означает число в интервале от 1 до 3, и их соли.
9. Соединения формулы I по п. 1, в которых Х означает СН или N; Y означает S; R1 означает водород; R2 означает водород; R3 означает водород; R4 означает водород; R5 означает С1-С4алкил; R6 представляет собой замещенный на R8 и R9 цикл, выбранный из группы, включающей бензол, фуран, тиофен, тиазол, имидазол, триазол, тетразол, тиадиазол, пиридин и пиримидин; R7 означает водород; R8 означает нитро; R9 означает водород или С1-С4алкил; m означает число 2 или 3; n означает число 0; р означает число 0; t означает число 0 и u означает число от 1 до 3, и их соли.
10. Соединения формулы I по п. 1, в которых X означает СН или N; Y означает S; R1 означает водород; R2 означает водород; R3 означает водород; R4 означает водород; R5 означает С1-С4алкил; R6 означает замещенный на R8 и R9 имидазол; R7 означает водород; R8 означает нитро; R3 означает водород или С1-С4алкил; m означает число 2 или 3; n означает число 0; р означает число 0; t означает число 0 и u означает число в интервале от 1 до 3,
и их соли.
и их соли.
11. Соединение по п.1, представляющее собой 2-(3-метил-4-{3-[2-(2-метил-5-нитроимидазол-1-ил)этилтио] пропилтио} пиридин-2-илметилтио)-1Н-бензимидазол и соли этого соединения.
12. Замещенные арилалкилтиоалкилтиопиридины по п.1 - 11, обладающие антибактериальным действием в отношении бактерий Helicobacter.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CH184594 | 1994-06-10 | ||
| CH1845/94-6 | 1994-06-10 | ||
| PCT/EP1995/002237 WO1995034554A1 (de) | 1994-06-10 | 1995-06-09 | Substituierte arylalkylthioalkylthiopyridine zur bekämpfung von helicobacter-bakterien |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU97100641A RU97100641A (ru) | 1999-02-20 |
| RU2139286C1 true RU2139286C1 (ru) | 1999-10-10 |
Family
ID=4219963
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU97100641/04A RU2139286C1 (ru) | 1994-06-10 | 1995-06-09 | Замещенные арилалкилтиоалкилтиопиридины для борьбы с бактериями helicobacter |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US5859030A (ru) |
| EP (1) | EP0764161A1 (ru) |
| JP (1) | JPH10501254A (ru) |
| CN (1) | CN1070488C (ru) |
| AU (1) | AU697572B2 (ru) |
| BG (1) | BG63502B1 (ru) |
| CA (1) | CA2192202A1 (ru) |
| CZ (1) | CZ288079B6 (ru) |
| EE (1) | EE03312B1 (ru) |
| FI (1) | FI964909L (ru) |
| HU (1) | HU220062B (ru) |
| MX (1) | MX9606300A (ru) |
| NO (1) | NO311618B1 (ru) |
| NZ (1) | NZ288609A (ru) |
| PL (1) | PL181801B1 (ru) |
| RO (1) | RO117792B1 (ru) |
| RU (1) | RU2139286C1 (ru) |
| SK (1) | SK281465B6 (ru) |
| WO (1) | WO1995034554A1 (ru) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6071961A (en) * | 1995-11-28 | 2000-06-06 | Wider; Michael D. | Antimicrobial composition and methods of use therefor |
| US6479514B1 (en) | 1998-05-23 | 2002-11-12 | Altana Pharma Ag | Quinoline-aminomethyl-pyridyl derivatives with anti-helicobacter activity |
| CA2362930C (en) * | 1999-02-26 | 2010-10-05 | Nitromed, Inc. | Nitrosated and nitrosylated proton pump inhibitors, compositions and methods of use |
| US6326384B1 (en) | 1999-08-26 | 2001-12-04 | Robert R. Whittle | Dry blend pharmaceutical unit dosage form |
| US6262086B1 (en) | 1999-08-26 | 2001-07-17 | Robert R. Whittle | Pharmaceutical unit dosage form |
| US6312712B1 (en) | 1999-08-26 | 2001-11-06 | Robert R. Whittle | Method of improving bioavailability |
| US6312723B1 (en) | 1999-08-26 | 2001-11-06 | Robert R. Whittle | Pharmaceutical unit dosage form |
| US6316020B1 (en) | 1999-08-26 | 2001-11-13 | Robert R. Whittle | Pharmaceutical formulations |
| US6369087B1 (en) * | 1999-08-26 | 2002-04-09 | Robert R. Whittle | Alkoxy substituted benzimidazole compounds, pharmaceutical preparations containing the same, and methods of using the same |
| US6268385B1 (en) | 1999-08-26 | 2001-07-31 | Robert R. Whittle | Dry blend pharmaceutical formulations |
| US6780880B1 (en) | 1999-08-26 | 2004-08-24 | Robert R. Whittle | FT-Raman spectroscopic measurement |
| US6262085B1 (en) | 1999-08-26 | 2001-07-17 | Robert R. Whittle | Alkoxy substituted Benzimidazole compounds, pharmaceutical preparations containing the same, and methods of using the same |
| BR0312802A (pt) * | 2002-07-19 | 2005-04-19 | Michael E Garst | Pró-drogas de inibidores de bombas de próton |
| US20100317689A1 (en) * | 2006-09-19 | 2010-12-16 | Garst Michael E | Prodrugs of proton pump inhibitors including the 1h-imidazo[4,5-b] pyridine moiety |
| RU2449805C1 (ru) | 2011-01-27 | 2012-05-10 | Общество С Ограниченной Ответственностью "Гармония" | Пептидная фармацевтическая композиция, средство на ее основе для лечения гастродуоденальных заболеваний, вызываемых helicobacter pylori, и способ его использования |
| CN110294751B (zh) * | 2018-03-21 | 2020-11-20 | 湖南化工研究院有限公司 | 具生物活性的咪唑[4,5-b]并吡啶类化合物及其制备方法和应用 |
| CN110156752B (zh) * | 2019-05-28 | 2021-03-19 | 沈阳药科大学 | 2-[(吡啶-2-基甲基)硫基]-1h-苯并咪唑类化合物及应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU795476A3 (ru) * | 1974-02-18 | 1981-01-07 | Аб Хессле (Фирма) | Способ получени производныхбЕНзиМидАзОлА или иХ СОлЕй |
| WO1993024480A1 (fr) * | 1992-06-01 | 1993-12-09 | Yoshitomi Pharmaceutical Industries, Ltd. | Compose de pyridine et son utilisation medicinale |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1234058A (ru) * | 1968-10-21 | 1971-06-03 | ||
| JPS604826B2 (ja) * | 1978-09-12 | 1985-02-06 | 藤沢薬品工業株式会社 | インダゾ−ル酢酸類の製造法 |
| US4387225A (en) * | 1981-01-15 | 1983-06-07 | William H. Rorer, Inc. | Heterocyclic alkylene triazinones |
| JPS57200386A (en) * | 1981-06-04 | 1982-12-08 | Yoshitomi Pharmaceut Ind Ltd | Novel 1,4-dihydropyridine-3,5-dicarboxylic ester derivative and its salts |
| IL71665A (en) * | 1983-05-03 | 1988-05-31 | Byk Gulden Lomberg Chem Fab | Fluoro-(2-pyridyl-methylthio)-dioxolo-(and dioxino-)benzimidazoles,processes for their preparation and pharmaceutical compositions containing the same |
| JP2563619B2 (ja) * | 1989-11-28 | 1996-12-11 | 株式会社東芝 | ダクト用換気扇 |
| US5504082A (en) * | 1992-06-01 | 1996-04-02 | Yoshitomi Pharmaceutical Industries, Ltd. | Pyridine compound and pharmaceutical compostions |
| WO1994019346A1 (de) * | 1993-02-17 | 1994-09-01 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Substituierte heteroarylalkylthiopyridine zur bekämpfung von helicobacter bakterien |
| JPH08512037A (ja) * | 1993-06-29 | 1996-12-17 | ビイク グルデン ロンベルク ヒェーミッシェ ファブリーク ゲゼルシャフト ミット ベシュレンクテル ハフツング | 置換されたアリールチオアルキルチオピリジン |
| JPH09509143A (ja) * | 1993-12-01 | 1997-09-16 | ビイク グルデン ロンベルク ヒェーミッシェ ファブリーク ゲゼルシャフト ミット ベシュレンクテル ハフツング | 置換アミノアルキルアミノピリジン |
-
1995
- 1995-06-09 SK SK1576-96A patent/SK281465B6/sk unknown
- 1995-06-09 WO PCT/EP1995/002237 patent/WO1995034554A1/de not_active Ceased
- 1995-06-09 RO RO96-02255A patent/RO117792B1/ro unknown
- 1995-06-09 RU RU97100641/04A patent/RU2139286C1/ru not_active IP Right Cessation
- 1995-06-09 CN CN95194562A patent/CN1070488C/zh not_active Expired - Fee Related
- 1995-06-09 HU HU9603339A patent/HU220062B/hu not_active IP Right Cessation
- 1995-06-09 CA CA002192202A patent/CA2192202A1/en not_active Abandoned
- 1995-06-09 EE EE9600189A patent/EE03312B1/xx not_active IP Right Cessation
- 1995-06-09 PL PL95317613A patent/PL181801B1/pl unknown
- 1995-06-09 AU AU27901/95A patent/AU697572B2/en not_active Ceased
- 1995-06-09 JP JP8501598A patent/JPH10501254A/ja not_active Withdrawn
- 1995-06-09 EP EP95923288A patent/EP0764161A1/de not_active Withdrawn
- 1995-06-09 NZ NZ288609A patent/NZ288609A/xx unknown
- 1995-06-09 CZ CZ19963624A patent/CZ288079B6/cs not_active IP Right Cessation
- 1995-06-09 US US08/750,785 patent/US5859030A/en not_active Expired - Fee Related
- 1995-06-09 FI FI964909A patent/FI964909L/fi unknown
-
1996
- 1996-11-21 BG BG101002A patent/BG63502B1/bg unknown
- 1996-12-03 NO NO19965162A patent/NO311618B1/no unknown
- 1996-12-10 MX MX9606300A patent/MX9606300A/es not_active IP Right Cessation
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU795476A3 (ru) * | 1974-02-18 | 1981-01-07 | Аб Хессле (Фирма) | Способ получени производныхбЕНзиМидАзОлА или иХ СОлЕй |
| WO1993024480A1 (fr) * | 1992-06-01 | 1993-12-09 | Yoshitomi Pharmaceutical Industries, Ltd. | Compose de pyridine et son utilisation medicinale |
Also Published As
| Publication number | Publication date |
|---|---|
| HU220062B (hu) | 2001-10-28 |
| HUT75516A (en) | 1997-05-28 |
| CN1159803A (zh) | 1997-09-17 |
| WO1995034554A1 (de) | 1995-12-21 |
| HU9603339D0 (en) | 1997-01-28 |
| BG101002A (bg) | 1997-08-29 |
| JPH10501254A (ja) | 1998-02-03 |
| CZ362496A3 (en) | 1997-08-13 |
| NO311618B1 (no) | 2001-12-17 |
| RO117792B1 (ro) | 2002-07-30 |
| NZ288609A (en) | 1998-12-23 |
| PL317613A1 (en) | 1997-04-14 |
| EP0764161A1 (de) | 1997-03-26 |
| CN1070488C (zh) | 2001-09-05 |
| CA2192202A1 (en) | 1995-12-21 |
| US5859030A (en) | 1999-01-12 |
| EE03312B1 (et) | 2000-12-15 |
| AU697572B2 (en) | 1998-10-08 |
| MX9606300A (es) | 1998-06-30 |
| SK281465B6 (sk) | 2001-04-09 |
| FI964909A0 (fi) | 1996-12-09 |
| NO965162L (no) | 1997-02-05 |
| FI964909A7 (fi) | 1996-12-09 |
| BG63502B1 (bg) | 2002-03-29 |
| CZ288079B6 (cs) | 2001-04-11 |
| PL181801B1 (pl) | 2001-09-28 |
| FI964909L (fi) | 1996-12-09 |
| HK1001957A1 (en) | 1998-07-24 |
| NO965162D0 (no) | 1996-12-03 |
| AU2790195A (en) | 1996-01-05 |
| SK157696A3 (en) | 1997-06-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2139286C1 (ru) | Замещенные арилалкилтиоалкилтиопиридины для борьбы с бактериями helicobacter | |
| RU2149872C1 (ru) | Пиридилтиосоединения для борьбы с бактериями helicobacter | |
| EP0983263A1 (en) | Novel benzimidazole derivatives as antiulcer agents, process for their preparation and pharmaceutical compositions containing them | |
| RU2142459C1 (ru) | Тиопиридины для борьбы с бактериями helicobakter | |
| RU2154062C2 (ru) | Замещенные арилтиоалкилтиопиридины, способ их получения, лекарственное средство на их основе и способ получения лекарственного средства. | |
| US5922720A (en) | Piperazinothiopyridines for the control of Helicobacter bacteria |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20030610 |