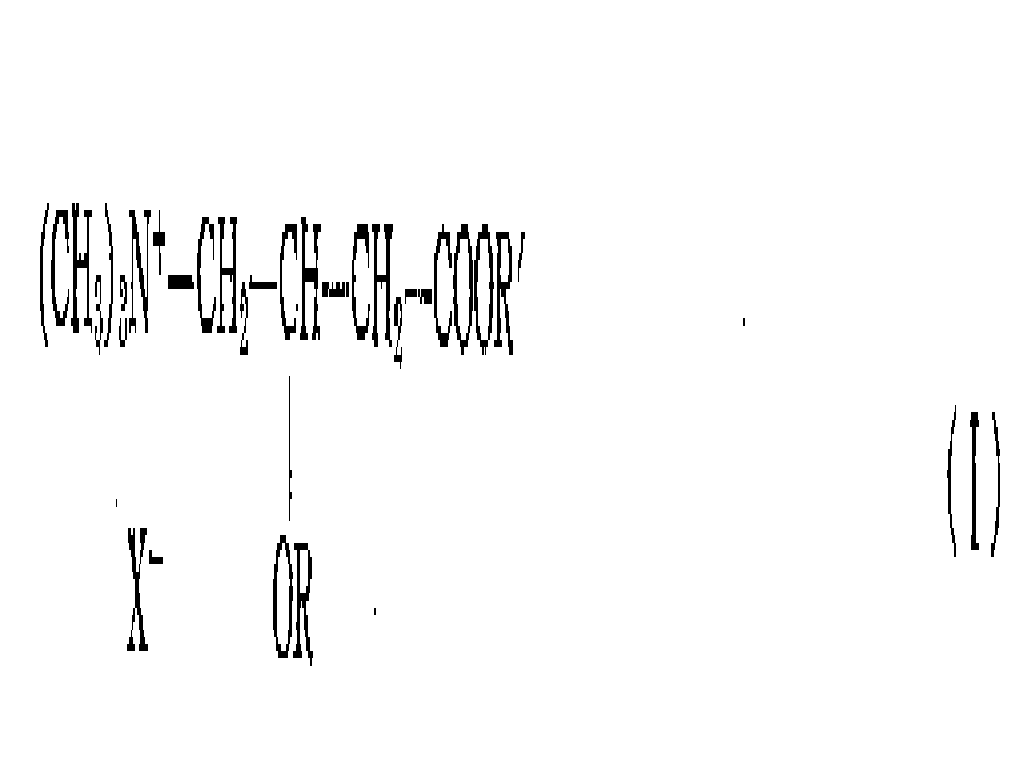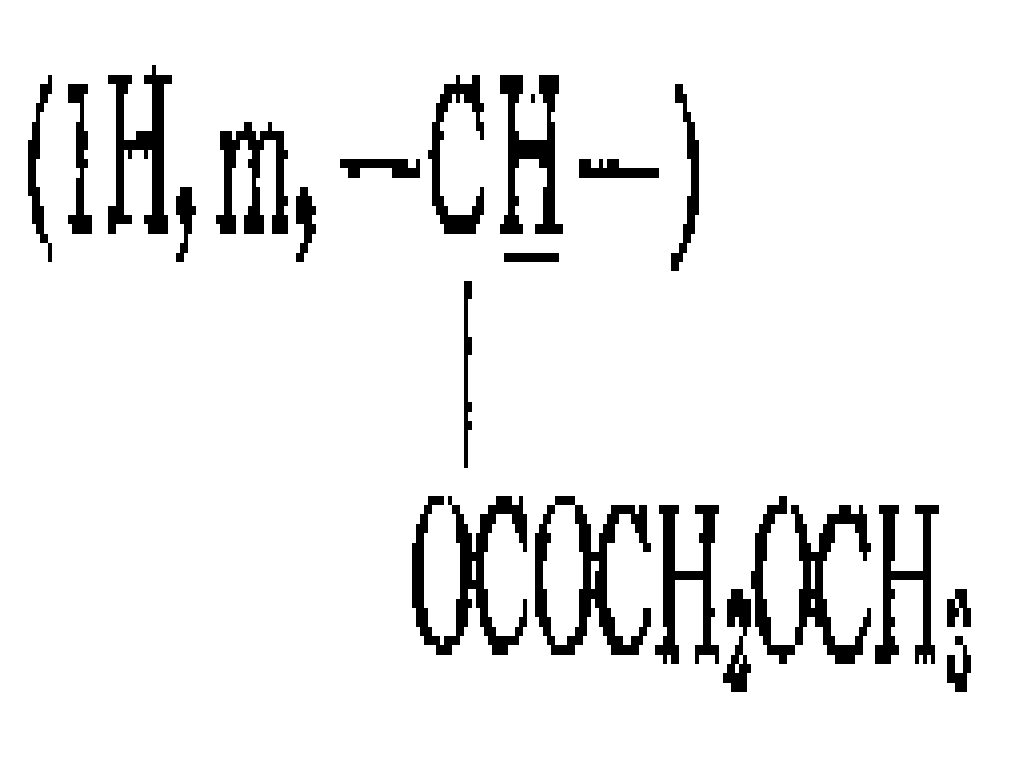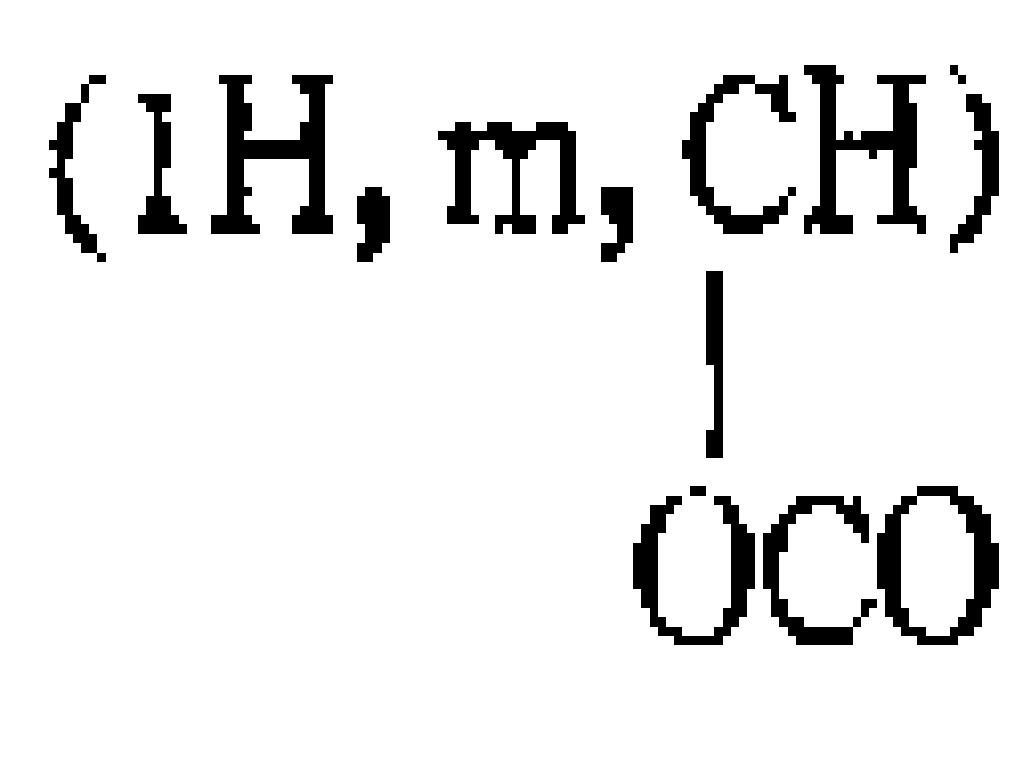KR850000570B1 - 카르니틴의 알콕시-아실유도체의 에스테르 제조방법 - Google Patents
카르니틴의 알콕시-아실유도체의 에스테르 제조방법 Download PDFInfo
- Publication number
- KR850000570B1 KR850000570B1 KR1019810001688A KR810001688A KR850000570B1 KR 850000570 B1 KR850000570 B1 KR 850000570B1 KR 1019810001688 A KR1019810001688 A KR 1019810001688A KR 810001688 A KR810001688 A KR 810001688A KR 850000570 B1 KR850000570 B1 KR 850000570B1
- Authority
- KR
- South Korea
- Prior art keywords
- carnitine
- ester
- alkoxy
- chloride
- mol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C219/00—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C219/02—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton
- C07C219/04—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated
- C07C219/06—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated having the hydroxy groups esterified by carboxylic acids having the esterifying carboxyl groups bound to hydrogen atoms or to acyclic carbon atoms of an acyclic saturated carbon skeleton
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C229/00—Compounds containing amino and carboxyl groups bound to the same carbon skeleton
- C07C229/02—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton
- C07C229/04—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated
- C07C229/22—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated the carbon skeleton being further substituted by oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Emergency Medicine (AREA)
- Cardiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Heart & Thoracic Surgery (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Steroid Compounds (AREA)
Abstract
Description
Claims (1)
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IT48853A/80 | 1980-05-30 | ||
| IT48853/80A IT1147079B (it) | 1980-05-30 | 1980-05-30 | Esteri di alcossi-acil derivati della carnitina procedimento per la loro preparatione e composizioni farmaceutiche che li contengono |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR830006183A KR830006183A (ko) | 1983-09-20 |
| KR850000570B1 true KR850000570B1 (ko) | 1985-04-29 |
Family
ID=11268800
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1019810001688A Expired KR850000570B1 (ko) | 1980-05-30 | 1981-05-16 | 카르니틴의 알콕시-아실유도체의 에스테르 제조방법 |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US4551477A (ko) |
| JP (1) | JPS5721354A (ko) |
| KR (1) | KR850000570B1 (ko) |
| AT (1) | AT373230B (ko) |
| AU (1) | AU540822B2 (ko) |
| BE (1) | BE888953A (ko) |
| CA (1) | CA1152098A (ko) |
| CH (1) | CH648545A5 (ko) |
| DE (1) | DE3120910A1 (ko) |
| ES (1) | ES502594A0 (ko) |
| FR (1) | FR2483408A1 (ko) |
| GB (1) | GB2076816B (ko) |
| IE (1) | IE51400B1 (ko) |
| IL (1) | IL62889A (ko) |
| IT (1) | IT1147079B (ko) |
| NL (1) | NL191366C (ko) |
| SE (1) | SE452005B (ko) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1177874B (it) * | 1984-07-04 | 1987-08-26 | Sigma Tau Ind Farmaceuti | Estere della acetil carnitina,procedimenti per la sua preparazione e composizioni farmaceutiche che lo contengono |
| IT1248321B (it) * | 1991-05-15 | 1995-01-05 | Sigma Tau Ind Farmaceuti | Uso di esteri di acil l-carnitine con l'acido gamma-idrossibutirrico per produrre composizioni farmaceutiche per il trattamento di epatopatie |
| IT1254136B (it) * | 1992-01-16 | 1995-09-08 | Sigma Tau Ind Farmaceuti | Esteri di acil carnitine con alcooli alifatici a lunga catena e composizioni farmaceutiche che li contengono, ad attivita' antimicotica. |
| IT1254135B (it) * | 1992-01-16 | 1995-09-08 | Sigma Tau Ind Farmaceuti | Esteri di acil carnitine con alcooli alifatici a lunga catena e composizioni farmaceutiche che li contengono, ad attivita' antibatterica. |
| IT1258370B (it) * | 1992-03-02 | 1996-02-26 | Sigma Tau Ind Farmaceuti | Esteri della l-carnitina e di acil l-carnitine dotati di attivita' miorilassante selettiva sull'apparato gastro-intestinale e composizioni farmaceutiche che li contengono. |
| IT1293794B1 (it) * | 1997-07-28 | 1999-03-10 | Acraf | Farmaco attivo nel ridurre la produzione di proteina mcp-1 |
| US20050232911A1 (en) * | 2004-04-19 | 2005-10-20 | Schreiber Brian D | Prevention and treatment of metabolic abnormalities associated with excess intramyocellular lipid |
| USD1060384S1 (en) * | 2022-11-25 | 2025-02-04 | The Pnc Financial Services Group, Inc. | Display screen or portion thereof with graphical user interface |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS531812B2 (ko) * | 1972-12-07 | 1978-01-23 | ||
| AU518617B2 (en) * | 1977-04-29 | 1981-10-08 | Sigma-Tau Industrie Farmaceutiche Riunite S.P.A. | Therapeutic application of acetyl-d, 1-carnitine |
| IT1156741B (it) * | 1978-05-15 | 1987-02-04 | Sigma Tau Ind Farmaceuti | Applicazione terapeutica della carnitina e di alcuni derivati acilati della carnitina nell'emodialisi |
| IT1156840B (it) * | 1978-06-27 | 1987-02-04 | Sigma Tau Ind Farmaceuti | Acil derivati della carnitina |
| IT1116037B (it) * | 1979-04-23 | 1986-02-10 | Sigma Tau Ind Farmaceuti | Esteri e ammidi di acil carnitine loro procedimenti di preparazione e loro uso terapeutico |
| JPS5633054A (en) * | 1979-08-29 | 1981-04-03 | Matsushita Electric Ind Co Ltd | Dehydrator |
| IT1145362B (it) * | 1980-03-06 | 1986-11-05 | Sigma Tau Ind Farmaceuti | Classe di acil-derivati della carnitina procedimento per la loro preparazione e loro uso terapeutico |
-
1980
- 1980-05-30 IT IT48853/80A patent/IT1147079B/it active
-
1981
- 1981-05-15 IE IE1096/81A patent/IE51400B1/en not_active IP Right Cessation
- 1981-05-16 KR KR1019810001688A patent/KR850000570B1/ko not_active Expired
- 1981-05-17 IL IL62889A patent/IL62889A/xx unknown
- 1981-05-19 AT AT0222881A patent/AT373230B/de not_active IP Right Cessation
- 1981-05-20 AU AU70884/81A patent/AU540822B2/en not_active Ceased
- 1981-05-22 NL NL8102537A patent/NL191366C/xx not_active IP Right Cessation
- 1981-05-22 GB GB8115913A patent/GB2076816B/en not_active Expired
- 1981-05-25 BE BE0/204896A patent/BE888953A/fr not_active IP Right Cessation
- 1981-05-26 JP JP8069481A patent/JPS5721354A/ja active Granted
- 1981-05-26 DE DE19813120910 patent/DE3120910A1/de active Granted
- 1981-05-27 FR FR8110640A patent/FR2483408A1/fr active Granted
- 1981-05-27 SE SE8103367A patent/SE452005B/sv not_active IP Right Cessation
- 1981-05-29 CA CA000378711A patent/CA1152098A/en not_active Expired
- 1981-05-29 ES ES502594A patent/ES502594A0/es active Granted
- 1981-05-29 CH CH3538/81A patent/CH648545A5/it not_active IP Right Cessation
-
1984
- 1984-06-28 US US06/625,715 patent/US4551477A/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| SE452005B (sv) | 1987-11-09 |
| BE888953A (fr) | 1981-09-16 |
| NL191366C (nl) | 1995-06-16 |
| GB2076816B (en) | 1983-11-23 |
| FR2483408A1 (fr) | 1981-12-04 |
| DE3120910A1 (de) | 1982-04-01 |
| IE811096L (en) | 1981-11-30 |
| ATA222881A (de) | 1983-05-15 |
| GB2076816A (en) | 1981-12-09 |
| IT8048853A0 (it) | 1980-05-30 |
| DE3120910C2 (ko) | 1990-06-07 |
| JPH0259136B2 (ko) | 1990-12-11 |
| ES8203330A1 (es) | 1982-04-01 |
| US4551477A (en) | 1985-11-05 |
| SE8103367L (sv) | 1981-12-01 |
| AT373230B (de) | 1983-12-27 |
| IL62889A (en) | 1984-10-31 |
| NL191366B (nl) | 1995-01-16 |
| JPS5721354A (en) | 1982-02-04 |
| CA1152098A (en) | 1983-08-16 |
| ES502594A0 (es) | 1982-04-01 |
| IT1147079B (it) | 1986-11-19 |
| CH648545A5 (it) | 1985-03-29 |
| AU540822B2 (en) | 1984-12-06 |
| IL62889A0 (en) | 1981-07-31 |
| IE51400B1 (en) | 1986-12-24 |
| FR2483408B1 (ko) | 1985-03-29 |
| NL8102537A (nl) | 1981-12-16 |
| AU7088481A (en) | 1981-12-03 |
| KR830006183A (ko) | 1983-09-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4443475A (en) | Amides of acyl-carnitines, process for preparing same and pharmaceutical compositions containing such amides | |
| CA1113117A (en) | Epinine esters, method for their preparation and related pharmaceutical compositions | |
| CH640824A5 (it) | Acil-derivati della carnitina e procedimento per la loro preparazione. | |
| KR850000570B1 (ko) | 카르니틴의 알콕시-아실유도체의 에스테르 제조방법 | |
| JP2883187B2 (ja) | L―カルニチンとγ―ヒドロキシ酪酸とのエステル | |
| US5010204A (en) | Acetazolamide-related compounds, process for their preparation, and pharmaceutical composition containing the same | |
| US4766222A (en) | Novel class of acyl-derivatives of carnitine process for preparing same and therapeutic use thereof | |
| US4590209A (en) | Alkoxy-acyl carnitines and pharmaceutical compositions containing same | |
| CA1148165A (en) | Esters of arylpropionic acids endowed with an anti- inflammatory activity, process for their preparation, and related pharmaceutical compositions | |
| US4379091A (en) | Esters of arylpropionic acids endowed with an anti-inflammatory activity | |
| US4487932A (en) | 2,6-Dimethyl-3,5-bis-(1-adamantylhydroxycarbonyl)-4-(2-difluoromethoxyphenyl)-1,4-dihydropyridine | |
| US4338320A (en) | Esters of 6'-hydroxycinchonine, and a method of treating arrythmia with them | |
| US4367176A (en) | Esters of arylpropionic acids endowed with an anti-inflammatory activity and related pharmaceutical compositions | |
| KR820001459B1 (ko) | 카르니틴의 아실유도체의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PG1605 | Publication of application before grant of patent |
St.27 status event code: A-2-2-Q10-Q13-nap-PG1605 |
|
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 8 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 9 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 10 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 11 |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 19960430 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 19960430 |