KR20230079470A - 결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 - Google Patents
결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 Download PDFInfo
- Publication number
- KR20230079470A KR20230079470A KR1020237017309A KR20237017309A KR20230079470A KR 20230079470 A KR20230079470 A KR 20230079470A KR 1020237017309 A KR1020237017309 A KR 1020237017309A KR 20237017309 A KR20237017309 A KR 20237017309A KR 20230079470 A KR20230079470 A KR 20230079470A
- Authority
- KR
- South Korea
- Prior art keywords
- compound
- disorder
- crystalline
- xrpd pattern
- xrpd
- Prior art date
Links
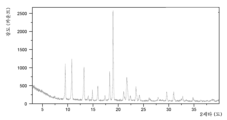
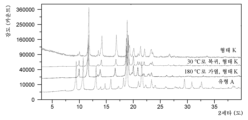
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 165
- 150000001875 compounds Chemical class 0.000 claims description 28
- 239000007787 solid Substances 0.000 abstract description 92
- 238000000034 method Methods 0.000 abstract description 68
- 239000000203 mixture Substances 0.000 abstract description 56
- 150000003839 salts Chemical class 0.000 abstract description 19
- 238000004519 manufacturing process Methods 0.000 abstract description 4
- 229940125904 compound 1 Drugs 0.000 description 139
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 74
- 206010010904 Convulsion Diseases 0.000 description 73
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 57
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 53
- 208000035475 disorder Diseases 0.000 description 50
- 206010044565 Tremor Diseases 0.000 description 48
- 238000002411 thermogravimetry Methods 0.000 description 40
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 36
- 239000000523 sample Substances 0.000 description 36
- 239000002904 solvent Substances 0.000 description 36
- 238000000113 differential scanning calorimetry Methods 0.000 description 33
- 238000006243 chemical reaction Methods 0.000 description 32
- 235000019439 ethyl acetate Nutrition 0.000 description 30
- 206010015037 epilepsy Diseases 0.000 description 26
- 208000024891 symptom Diseases 0.000 description 26
- -1 alginic acid Chemical compound 0.000 description 24
- 238000004458 analytical method Methods 0.000 description 24
- 239000013078 crystal Substances 0.000 description 24
- 208000005809 status epilepticus Diseases 0.000 description 24
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 24
- 238000002425 crystallisation Methods 0.000 description 22
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 21
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 108010029485 Protein Isoforms Proteins 0.000 description 21
- 102000001708 Protein Isoforms Human genes 0.000 description 21
- 230000008025 crystallization Effects 0.000 description 21
- 238000001035 drying Methods 0.000 description 21
- 239000002002 slurry Substances 0.000 description 20
- 238000002474 experimental method Methods 0.000 description 19
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 18
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 18
- 239000012296 anti-solvent Substances 0.000 description 18
- 238000011282 treatment Methods 0.000 description 18
- 208000019901 Anxiety disease Diseases 0.000 description 17
- 238000002360 preparation method Methods 0.000 description 17
- 230000004580 weight loss Effects 0.000 description 17
- 210000004556 brain Anatomy 0.000 description 16
- 210000004027 cell Anatomy 0.000 description 16
- 230000000694 effects Effects 0.000 description 15
- 239000008194 pharmaceutical composition Substances 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- 208000024714 major depressive disease Diseases 0.000 description 14
- 238000001704 evaporation Methods 0.000 description 13
- 230000008020 evaporation Effects 0.000 description 13
- 238000009472 formulation Methods 0.000 description 13
- 230000033001 locomotion Effects 0.000 description 13
- 239000012453 solvate Substances 0.000 description 13
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 12
- 238000005481 NMR spectroscopy Methods 0.000 description 12
- 229940079593 drug Drugs 0.000 description 12
- 239000003814 drug Substances 0.000 description 12
- 208000010118 dystonia Diseases 0.000 description 12
- 238000002844 melting Methods 0.000 description 12
- 230000008018 melting Effects 0.000 description 12
- 208000015122 neurodegenerative disease Diseases 0.000 description 12
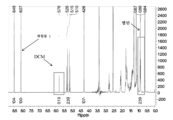
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 12
- 208000014094 Dystonic disease Diseases 0.000 description 11
- 208000016285 Movement disease Diseases 0.000 description 11
- 208000018737 Parkinson disease Diseases 0.000 description 11
- 229910052799 carbon Inorganic materials 0.000 description 11
- 201000006517 essential tremor Diseases 0.000 description 11
- 230000002085 persistent effect Effects 0.000 description 11
- 208000002193 Pain Diseases 0.000 description 10
- 208000028552 Treatment-Resistant Depressive disease Diseases 0.000 description 10
- 239000004480 active ingredient Substances 0.000 description 10
- 239000003795 chemical substances by application Substances 0.000 description 10
- 238000009792 diffusion process Methods 0.000 description 10
- 208000015706 neuroendocrine disease Diseases 0.000 description 10
- 206010008748 Chorea Diseases 0.000 description 9
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 9
- 208000012601 choreatic disease Diseases 0.000 description 9
- 230000002920 convulsive effect Effects 0.000 description 9
- 230000006378 damage Effects 0.000 description 9
- 238000001938 differential scanning calorimetry curve Methods 0.000 description 9
- 239000011159 matrix material Substances 0.000 description 9
- 210000003205 muscle Anatomy 0.000 description 9
- 230000036407 pain Effects 0.000 description 9
- 208000022821 personality disease Diseases 0.000 description 9
- 208000019116 sleep disease Diseases 0.000 description 9
- 208000011580 syndromic disease Diseases 0.000 description 9
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 9
- 238000001757 thermogravimetry curve Methods 0.000 description 9
- 238000005160 1H NMR spectroscopy Methods 0.000 description 8
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 8
- 208000019022 Mood disease Diseases 0.000 description 8
- 208000028017 Psychotic disease Diseases 0.000 description 8
- 239000000853 adhesive Substances 0.000 description 8
- 230000001684 chronic effect Effects 0.000 description 8
- 230000005021 gait Effects 0.000 description 8
- 239000011521 glass Substances 0.000 description 8
- 210000002414 leg Anatomy 0.000 description 8
- 239000012528 membrane Substances 0.000 description 8
- 210000002569 neuron Anatomy 0.000 description 8
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 8
- 208000019906 panic disease Diseases 0.000 description 8
- 239000000546 pharmaceutical excipient Substances 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 206010001497 Agitation Diseases 0.000 description 7
- 208000020925 Bipolar disease Diseases 0.000 description 7
- 208000030990 Impulse-control disease Diseases 0.000 description 7
- 208000012902 Nervous system disease Diseases 0.000 description 7
- 208000008234 Tics Diseases 0.000 description 7
- 230000001070 adhesive effect Effects 0.000 description 7
- 230000036506 anxiety Effects 0.000 description 7
- BTCSSZJGUNDROE-UHFFFAOYSA-N gamma-aminobutyric acid Chemical compound NCCCC(O)=O BTCSSZJGUNDROE-UHFFFAOYSA-N 0.000 description 7
- 238000005259 measurement Methods 0.000 description 7
- 208000020016 psychiatric disease Diseases 0.000 description 7
- 208000020685 sleep-wake disease Diseases 0.000 description 7
- 208000020401 Depressive disease Diseases 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 208000023105 Huntington disease Diseases 0.000 description 6
- 206010040030 Sensory loss Diseases 0.000 description 6
- 230000000202 analgesic effect Effects 0.000 description 6
- 210000003169 central nervous system Anatomy 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 239000006071 cream Substances 0.000 description 6
- 208000024732 dysthymic disease Diseases 0.000 description 6
- 229960003692 gamma aminobutyric acid Drugs 0.000 description 6
- 238000010438 heat treatment Methods 0.000 description 6
- 239000006210 lotion Substances 0.000 description 6
- 230000004770 neurodegeneration Effects 0.000 description 6
- 239000002674 ointment Substances 0.000 description 6
- 208000033300 perinatal asphyxia Diseases 0.000 description 6
- 229910052698 phosphorus Inorganic materials 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 238000010583 slow cooling Methods 0.000 description 6
- 206010003591 Ataxia Diseases 0.000 description 5
- 208000012661 Dyskinesia Diseases 0.000 description 5
- 206010073210 Dystonic tremor Diseases 0.000 description 5
- 208000013016 Hypoglycemia Diseases 0.000 description 5
- 208000007101 Muscle Cramp Diseases 0.000 description 5
- 206010052904 Musculoskeletal stiffness Diseases 0.000 description 5
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 5
- 208000027089 Parkinsonian disease Diseases 0.000 description 5
- 206010034010 Parkinsonism Diseases 0.000 description 5
- 201000009916 Postpartum depression Diseases 0.000 description 5
- 208000006011 Stroke Diseases 0.000 description 5
- 206010042458 Suicidal ideation Diseases 0.000 description 5
- 208000000323 Tourette Syndrome Diseases 0.000 description 5
- 208000016620 Tourette disease Diseases 0.000 description 5
- 230000002159 abnormal effect Effects 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 150000005215 alkyl ethers Chemical class 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 239000002552 dosage form Substances 0.000 description 5
- 230000004064 dysfunction Effects 0.000 description 5
- 230000001037 epileptic effect Effects 0.000 description 5
- 230000002218 hypoglycaemic effect Effects 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 230000002151 myoclonic effect Effects 0.000 description 5
- 230000001537 neural effect Effects 0.000 description 5
- 239000002858 neurotransmitter agent Substances 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- 230000000306 recurrent effect Effects 0.000 description 5
- 230000003252 repetitive effect Effects 0.000 description 5
- 230000002441 reversible effect Effects 0.000 description 5
- 201000000980 schizophrenia Diseases 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- 230000001960 triggered effect Effects 0.000 description 5
- 206010021143 Hypoxia Diseases 0.000 description 4
- 201000006792 Lennox-Gastaut syndrome Diseases 0.000 description 4
- 208000013716 Motor tics Diseases 0.000 description 4
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 4
- 208000029726 Neurodevelopmental disease Diseases 0.000 description 4
- 206010029897 Obsessive thoughts Diseases 0.000 description 4
- 206010033664 Panic attack Diseases 0.000 description 4
- 206010061334 Partial seizures Diseases 0.000 description 4
- 208000005392 Spasm Diseases 0.000 description 4
- 208000009205 Tinnitus Diseases 0.000 description 4
- 208000030886 Traumatic Brain injury Diseases 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- 150000008064 anhydrides Chemical class 0.000 description 4
- 208000025748 atypical depressive disease Diseases 0.000 description 4
- 230000006399 behavior Effects 0.000 description 4
- 230000003542 behavioural effect Effects 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 230000002490 cerebral effect Effects 0.000 description 4
- 230000036461 convulsion Effects 0.000 description 4
- 235000014113 dietary fatty acids Nutrition 0.000 description 4
- 230000002996 emotional effect Effects 0.000 description 4
- 239000000839 emulsion Substances 0.000 description 4
- 210000003414 extremity Anatomy 0.000 description 4
- 239000000194 fatty acid Substances 0.000 description 4
- 229930195729 fatty acid Natural products 0.000 description 4
- 238000009093 first-line therapy Methods 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- 229910052739 hydrogen Inorganic materials 0.000 description 4
- 206010022437 insomnia Diseases 0.000 description 4
- 239000000155 melt Substances 0.000 description 4
- 230000004118 muscle contraction Effects 0.000 description 4
- 238000000643 oven drying Methods 0.000 description 4
- 229910052700 potassium Inorganic materials 0.000 description 4
- 230000000750 progressive effect Effects 0.000 description 4
- 239000013557 residual solvent Substances 0.000 description 4
- 230000001020 rhythmical effect Effects 0.000 description 4
- 208000012672 seasonal affective disease Diseases 0.000 description 4
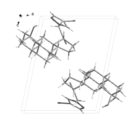
- 238000004467 single crystal X-ray diffraction Methods 0.000 description 4
- 238000001179 sorption measurement Methods 0.000 description 4
- 230000001148 spastic effect Effects 0.000 description 4
- 239000007921 spray Substances 0.000 description 4
- 238000013456 study Methods 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 231100000886 tinnitus Toxicity 0.000 description 4
- 230000000699 topical effect Effects 0.000 description 4
- 208000000103 Anorexia Nervosa Diseases 0.000 description 3
- 206010006100 Bradykinesia Diseases 0.000 description 3
- 206010008025 Cerebellar ataxia Diseases 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 3
- 206010011971 Decreased interest Diseases 0.000 description 3
- 206010012289 Dementia Diseases 0.000 description 3
- 206010012374 Depressed mood Diseases 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 206010017577 Gait disturbance Diseases 0.000 description 3
- 208000011688 Generalised anxiety disease Diseases 0.000 description 3
- 208000034308 Grand mal convulsion Diseases 0.000 description 3
- 208000006083 Hypokinesia Diseases 0.000 description 3
- 206010022998 Irritability Diseases 0.000 description 3
- 208000019430 Motor disease Diseases 0.000 description 3
- 206010069917 Orthostatic tremor Diseases 0.000 description 3
- 208000037158 Partial Epilepsies Diseases 0.000 description 3
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 3
- 208000008601 Polycythemia Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 206010072377 Psychogenic tremor Diseases 0.000 description 3
- 208000005793 Restless legs syndrome Diseases 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 238000002441 X-ray diffraction Methods 0.000 description 3
- 230000005856 abnormality Effects 0.000 description 3
- 208000028311 absence seizure Diseases 0.000 description 3
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 235000006708 antioxidants Nutrition 0.000 description 3
- 208000029560 autism spectrum disease Diseases 0.000 description 3
- 206010007776 catatonia Diseases 0.000 description 3
- 238000012512 characterization method Methods 0.000 description 3
- 230000002566 clonic effect Effects 0.000 description 3
- 208000010877 cognitive disease Diseases 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 206010016256 fatigue Diseases 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 208000029364 generalized anxiety disease Diseases 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 208000016354 hearing loss disease Diseases 0.000 description 3
- 239000005556 hormone Substances 0.000 description 3
- 229940088597 hormone Drugs 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 238000007918 intramuscular administration Methods 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 3
- 229940011051 isopropyl acetate Drugs 0.000 description 3
- GWYFCOCPABKNJV-UHFFFAOYSA-M isovalerate Chemical compound CC(C)CC([O-])=O GWYFCOCPABKNJV-UHFFFAOYSA-M 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 208000030159 metabolic disease Diseases 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- 230000000737 periodic effect Effects 0.000 description 3
- 208000033808 peripheral neuropathy Diseases 0.000 description 3
- 229940124531 pharmaceutical excipient Drugs 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 208000028173 post-traumatic stress disease Diseases 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 238000009094 second-line therapy Methods 0.000 description 3
- 230000007958 sleep Effects 0.000 description 3
- 239000011877 solvent mixture Substances 0.000 description 3
- 150000003431 steroids Chemical class 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 230000035882 stress Effects 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 150000005846 sugar alcohols Polymers 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 230000009529 traumatic brain injury Effects 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- 230000004584 weight gain Effects 0.000 description 3
- 235000019786 weight gain Nutrition 0.000 description 3
- 230000005186 women's health Effects 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- XDOFQFKRPWOURC-UHFFFAOYSA-N 16-methylheptadecanoic acid Chemical compound CC(C)CCCCCCCCCCCCCCC(O)=O XDOFQFKRPWOURC-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- 206010001541 Akinesia Diseases 0.000 description 2
- 208000024827 Alzheimer disease Diseases 0.000 description 2
- 208000000044 Amnesia Diseases 0.000 description 2
- 208000031091 Amnestic disease Diseases 0.000 description 2
- 208000007415 Anhedonia Diseases 0.000 description 2
- 206010002660 Anoxia Diseases 0.000 description 2
- 241000976983 Anoxia Species 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 206010003628 Atonic seizures Diseases 0.000 description 2
- 201000006474 Brain Ischemia Diseases 0.000 description 2
- 208000014644 Brain disease Diseases 0.000 description 2
- 206010008120 Cerebral ischaemia Diseases 0.000 description 2
- 206010010071 Coma Diseases 0.000 description 2
- 206010010144 Completed suicide Diseases 0.000 description 2
- 206010010219 Compulsions Diseases 0.000 description 2
- 206010011469 Crying Diseases 0.000 description 2
- 206010011878 Deafness Diseases 0.000 description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 2
- 208000026331 Disruptive, Impulse Control, and Conduct disease Diseases 0.000 description 2
- 201000007547 Dravet syndrome Diseases 0.000 description 2
- 206010014498 Embolic stroke Diseases 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- 208000001640 Fibromyalgia Diseases 0.000 description 2
- 208000010412 Glaucoma Diseases 0.000 description 2
- 206010019196 Head injury Diseases 0.000 description 2
- 208000010496 Heart Arrest Diseases 0.000 description 2
- 208000016988 Hemorrhagic Stroke Diseases 0.000 description 2
- 206010062767 Hypophysitis Diseases 0.000 description 2
- 206010065390 Inflammatory pain Diseases 0.000 description 2
- 208000015592 Involuntary movements Diseases 0.000 description 2
- 206010026749 Mania Diseases 0.000 description 2
- 208000026139 Memory disease Diseases 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 2
- 208000002740 Muscle Rigidity Diseases 0.000 description 2
- 208000008238 Muscle Spasticity Diseases 0.000 description 2
- 208000021642 Muscular disease Diseases 0.000 description 2
- 208000036572 Myoclonic epilepsy Diseases 0.000 description 2
- 208000002033 Myoclonus Diseases 0.000 description 2
- 206010028923 Neonatal asphyxia Diseases 0.000 description 2
- 208000037212 Neonatal hypoxic and ischemic brain injury Diseases 0.000 description 2
- 208000021384 Obsessive-Compulsive disease Diseases 0.000 description 2
- 208000030713 Parkinson disease and parkinsonism Diseases 0.000 description 2
- 229920002367 Polyisobutene Polymers 0.000 description 2
- 206010073211 Postural tremor Diseases 0.000 description 2
- ZTHYODDOHIVTJV-UHFFFAOYSA-N Propyl gallate Chemical compound CCCOC(=O)C1=CC(O)=C(O)C(O)=C1 ZTHYODDOHIVTJV-UHFFFAOYSA-N 0.000 description 2
- 208000001431 Psychomotor Agitation Diseases 0.000 description 2
- 206010038743 Restlessness Diseases 0.000 description 2
- 208000006289 Rett Syndrome Diseases 0.000 description 2
- 206010073677 Severe myoclonic epilepsy of infancy Diseases 0.000 description 2
- 208000013738 Sleep Initiation and Maintenance disease Diseases 0.000 description 2
- 208000032140 Sleepiness Diseases 0.000 description 2
- 206010041349 Somnolence Diseases 0.000 description 2
- 206010072148 Stiff-Person syndrome Diseases 0.000 description 2
- 208000007271 Substance Withdrawal Syndrome Diseases 0.000 description 2
- 206010065604 Suicidal behaviour Diseases 0.000 description 2
- 206010043994 Tonic convulsion Diseases 0.000 description 2
- 208000026911 Tuberous sclerosis complex Diseases 0.000 description 2
- 208000003443 Unconsciousness Diseases 0.000 description 2
- 206010048010 Withdrawal syndrome Diseases 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- OIPILFWXSMYKGL-UHFFFAOYSA-N acetylcholine Chemical compound CC(=O)OCC[N+](C)(C)C OIPILFWXSMYKGL-UHFFFAOYSA-N 0.000 description 2
- 229960004373 acetylcholine Drugs 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 230000001154 acute effect Effects 0.000 description 2
- UCTWMZQNUQWSLP-UHFFFAOYSA-N adrenaline Chemical compound CNCC(O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-UHFFFAOYSA-N 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 238000007605 air drying Methods 0.000 description 2
- 208000029650 alcohol withdrawal Diseases 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 230000006986 amnesia Effects 0.000 description 2
- 239000000538 analytical sample Substances 0.000 description 2
- 230000007953 anoxia Effects 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical compound CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 2
- 206010008118 cerebral infarction Diseases 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- ZPUCINDJVBIVPJ-LJISPDSOSA-N cocaine Chemical compound O([C@H]1C[C@@H]2CC[C@@H](N2C)[C@H]1C(=O)OC)C(=O)C1=CC=CC=C1 ZPUCINDJVBIVPJ-LJISPDSOSA-N 0.000 description 2
- 239000000084 colloidal system Substances 0.000 description 2
- 230000002354 daily effect Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000003412 degenerative effect Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 208000037765 diseases and disorders Diseases 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 239000002612 dispersion medium Substances 0.000 description 2
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 2
- 201000003104 endogenous depression Diseases 0.000 description 2
- 230000002964 excitative effect Effects 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 210000003128 head Anatomy 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 210000003016 hypothalamus Anatomy 0.000 description 2
- 230000007954 hypoxia Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 208000020658 intracerebral hemorrhage Diseases 0.000 description 2
- 208000001286 intracranial vasospasm Diseases 0.000 description 2
- 235000015110 jellies Nutrition 0.000 description 2
- 239000012669 liquid formulation Substances 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 201000003995 melancholia Diseases 0.000 description 2
- 230000015654 memory Effects 0.000 description 2
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 2
- 239000008108 microcrystalline cellulose Substances 0.000 description 2
- 229940016286 microcrystalline cellulose Drugs 0.000 description 2
- 235000013336 milk Nutrition 0.000 description 2
- 239000008267 milk Substances 0.000 description 2
- 210000004080 milk Anatomy 0.000 description 2
- 230000036651 mood Effects 0.000 description 2
- 230000004660 morphological change Effects 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 230000017311 musculoskeletal movement, spinal reflex action Effects 0.000 description 2
- 208000004296 neuralgia Diseases 0.000 description 2
- 230000000955 neuroendocrine Effects 0.000 description 2
- 230000008587 neuronal excitability Effects 0.000 description 2
- 230000002981 neuropathic effect Effects 0.000 description 2
- 208000021722 neuropathic pain Diseases 0.000 description 2
- 239000004090 neuroprotective agent Substances 0.000 description 2
- 231100000189 neurotoxic Toxicity 0.000 description 2
- 230000002887 neurotoxic effect Effects 0.000 description 2
- 208000030459 obsessive-compulsive personality disease Diseases 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 229920001542 oligosaccharide Polymers 0.000 description 2
- 150000002482 oligosaccharides Chemical class 0.000 description 2
- 208000007656 osteochondritis dissecans Diseases 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 230000035515 penetration Effects 0.000 description 2
- 208000019899 phobic disease Diseases 0.000 description 2
- 210000003635 pituitary gland Anatomy 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 229920001296 polysiloxane Polymers 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 230000001242 postsynaptic effect Effects 0.000 description 2
- 230000001144 postural effect Effects 0.000 description 2
- 230000036544 posture Effects 0.000 description 2
- 230000035935 pregnancy Effects 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000001107 psychogenic effect Effects 0.000 description 2
- 238000001671 psychotherapy Methods 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 230000001953 sensory effect Effects 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 238000000373 single-crystal X-ray diffraction data Methods 0.000 description 2
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 2
- 239000008247 solid mixture Substances 0.000 description 2
- 208000018198 spasticity Diseases 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 208000011117 substance-related disease Diseases 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 238000013268 sustained release Methods 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 2
- 208000016686 tic disease Diseases 0.000 description 2
- 230000001256 tonic effect Effects 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 208000019553 vascular disease Diseases 0.000 description 2
- 230000000007 visual effect Effects 0.000 description 2
- OGNSCSPNOLGXSM-UHFFFAOYSA-N (+/-)-DABA Natural products NCCC(N)C(O)=O OGNSCSPNOLGXSM-UHFFFAOYSA-N 0.000 description 1
- SNICXCGAKADSCV-JTQLQIEISA-N (-)-Nicotine Chemical compound CN1CCC[C@H]1C1=CC=CN=C1 SNICXCGAKADSCV-JTQLQIEISA-N 0.000 description 1
- JNYAEWCLZODPBN-JGWLITMVSA-N (2r,3r,4s)-2-[(1r)-1,2-dihydroxyethyl]oxolane-3,4-diol Chemical compound OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O JNYAEWCLZODPBN-JGWLITMVSA-N 0.000 description 1
- HOVAGTYPODGVJG-UVSYOFPXSA-N (3s,5r)-2-(hydroxymethyl)-6-methoxyoxane-3,4,5-triol Chemical compound COC1OC(CO)[C@@H](O)C(O)[C@H]1O HOVAGTYPODGVJG-UVSYOFPXSA-N 0.000 description 1
- ALSTYHKOOCGGFT-KTKRTIGZSA-N (9Z)-octadecen-1-ol Chemical compound CCCCCCCC\C=C/CCCCCCCCO ALSTYHKOOCGGFT-KTKRTIGZSA-N 0.000 description 1
- OYHQOLUKZRVURQ-NTGFUMLPSA-N (9Z,12Z)-9,10,12,13-tetratritiooctadeca-9,12-dienoic acid Chemical compound C(CCCCCCC\C(=C(/C\C(=C(/CCCCC)\[3H])\[3H])\[3H])\[3H])(=O)O OYHQOLUKZRVURQ-NTGFUMLPSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- FFJCNSLCJOQHKM-CLFAGFIQSA-N (z)-1-[(z)-octadec-9-enoxy]octadec-9-ene Chemical compound CCCCCCCC\C=C/CCCCCCCCOCCCCCCCC\C=C/CCCCCCCC FFJCNSLCJOQHKM-CLFAGFIQSA-N 0.000 description 1
- 229940058015 1,3-butylene glycol Drugs 0.000 description 1
- OKMWKBLSFKFYGZ-UHFFFAOYSA-N 1-behenoylglycerol Chemical compound CCCCCCCCCCCCCCCCCCCCCC(=O)OCC(O)CO OKMWKBLSFKFYGZ-UHFFFAOYSA-N 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- GJMPSRSMBJLKKB-UHFFFAOYSA-N 3-methylphenylacetic acid Chemical compound CC1=CC=CC(CC(O)=O)=C1 GJMPSRSMBJLKKB-UHFFFAOYSA-N 0.000 description 1
- HBTAOSGHCXUEKI-UHFFFAOYSA-N 4-chloro-n,n-dimethyl-3-nitrobenzenesulfonamide Chemical compound CN(C)S(=O)(=O)C1=CC=C(Cl)C([N+]([O-])=O)=C1 HBTAOSGHCXUEKI-UHFFFAOYSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- WBZFUFAFFUEMEI-UHFFFAOYSA-M Acesulfame k Chemical compound [K+].CC1=CC(=O)[N-]S(=O)(=O)O1 WBZFUFAFFUEMEI-UHFFFAOYSA-M 0.000 description 1
- 206010054196 Affect lability Diseases 0.000 description 1
- 206010001540 Akathisia Diseases 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 201000000736 Amenorrhea Diseases 0.000 description 1
- 206010001928 Amenorrhoea Diseases 0.000 description 1
- ITPDYQOUSLNIHG-UHFFFAOYSA-N Amiodarone hydrochloride Chemical compound [Cl-].CCCCC=1OC2=CC=CC=C2C=1C(=O)C1=CC(I)=C(OCC[NH+](CC)CC)C(I)=C1 ITPDYQOUSLNIHG-UHFFFAOYSA-N 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 208000009575 Angelman syndrome Diseases 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 1
- 208000035183 Benign hereditary chorea Diseases 0.000 description 1
- 206010048962 Brain oedema Diseases 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- 208000004434 Calcinosis Diseases 0.000 description 1
- 206010058019 Cancer Pain Diseases 0.000 description 1
- 206010008190 Cerebrovascular accident Diseases 0.000 description 1
- 201000001913 Childhood absence epilepsy Diseases 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- 208000000094 Chronic Pain Diseases 0.000 description 1
- 206010053398 Clonic convulsion Diseases 0.000 description 1
- 208000018652 Closed Head injury Diseases 0.000 description 1
- 206010009696 Clumsiness Diseases 0.000 description 1
- 208000028698 Cognitive impairment Diseases 0.000 description 1
- 208000023890 Complex Regional Pain Syndromes Diseases 0.000 description 1
- 208000033001 Complex partial seizures Diseases 0.000 description 1
- 206010010774 Constipation Diseases 0.000 description 1
- 208000034656 Contusions Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 208000011990 Corticobasal Degeneration Diseases 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- ZAKOWWREFLAJOT-CEFNRUSXSA-N D-alpha-tocopherylacetate Chemical compound CC(=O)OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C ZAKOWWREFLAJOT-CEFNRUSXSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 206010012239 Delusion Diseases 0.000 description 1
- 206010012390 Depression postoperative Diseases 0.000 description 1
- 208000007590 Disorders of Excessive Somnolence Diseases 0.000 description 1
- 201000010374 Down Syndrome Diseases 0.000 description 1
- 206010013752 Drug withdrawal convulsions Diseases 0.000 description 1
- 206010013786 Dry skin Diseases 0.000 description 1
- 208000000059 Dyspnea Diseases 0.000 description 1
- 206010013975 Dyspnoeas Diseases 0.000 description 1
- 208000032274 Encephalopathy Diseases 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 206010016275 Fear Diseases 0.000 description 1
- 208000002091 Febrile Seizures Diseases 0.000 description 1
- 206010016374 Feelings of worthlessness Diseases 0.000 description 1
- 206010016754 Flashback Diseases 0.000 description 1
- 208000001914 Fragile X syndrome Diseases 0.000 description 1
- 208000024412 Friedreich ataxia Diseases 0.000 description 1
- 201000009010 Frontal lobe epilepsy Diseases 0.000 description 1
- 102000005915 GABA Receptors Human genes 0.000 description 1
- 108010005551 GABA Receptors Proteins 0.000 description 1
- 206010017585 Gait spastic Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000003078 Generalized Epilepsy Diseases 0.000 description 1
- 201000004311 Gilles de la Tourette syndrome Diseases 0.000 description 1
- 208000004547 Hallucinations Diseases 0.000 description 1
- 208000002972 Hepatolenticular Degeneration Diseases 0.000 description 1
- 206010069099 Holmes tremor Diseases 0.000 description 1
- 101001072243 Homo sapiens Protocadherin-19 Proteins 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 208000000269 Hyperkinesis Diseases 0.000 description 1
- 206010020710 Hyperphagia Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010020850 Hyperthyroidism Diseases 0.000 description 1
- 201000001916 Hypochondriasis Diseases 0.000 description 1
- 206010021030 Hypomania Diseases 0.000 description 1
- 208000001953 Hypotension Diseases 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 206010021750 Infantile Spasms Diseases 0.000 description 1
- 208000035899 Infantile spasms syndrome Diseases 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- 206010022520 Intention tremor Diseases 0.000 description 1
- LPHGQDQBBGAPDZ-UHFFFAOYSA-N Isocaffeine Natural products CN1C(=O)N(C)C(=O)C2=C1N(C)C=N2 LPHGQDQBBGAPDZ-UHFFFAOYSA-N 0.000 description 1
- KLDXJTOLSGUMSJ-JGWLITMVSA-N Isosorbide Chemical compound O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 KLDXJTOLSGUMSJ-JGWLITMVSA-N 0.000 description 1
- 206010071082 Juvenile myoclonic epilepsy Diseases 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- WTDRDQBEARUVNC-UHFFFAOYSA-N L-Dopa Natural products OC(=O)C(N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 206010024870 Loss of libido Diseases 0.000 description 1
- 239000005913 Maltodextrin Substances 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 208000037490 Medically Unexplained Symptoms Diseases 0.000 description 1
- 208000036626 Mental retardation Diseases 0.000 description 1
- 244000246386 Mentha pulegium Species 0.000 description 1
- 235000016257 Mentha pulegium Nutrition 0.000 description 1
- 235000004357 Mentha x piperita Nutrition 0.000 description 1
- 206010027951 Mood swings Diseases 0.000 description 1
- 208000001089 Multiple system atrophy Diseases 0.000 description 1
- 208000010428 Muscle Weakness Diseases 0.000 description 1
- 208000029578 Muscle disease Diseases 0.000 description 1
- 206010028372 Muscular weakness Diseases 0.000 description 1
- 201000009623 Myopathy Diseases 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- 206010028813 Nausea Diseases 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 201000005625 Neuroleptic malignant syndrome Diseases 0.000 description 1
- 208000011644 Neurologic Gait disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 102000019315 Nicotinic acetylcholine receptors Human genes 0.000 description 1
- 108050006807 Nicotinic acetylcholine receptors Proteins 0.000 description 1
- 239000006057 Non-nutritive feed additive Substances 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 208000025174 PANDAS Diseases 0.000 description 1
- 208000021155 Paediatric autoimmune neuropsychiatric disorders associated with streptococcal infection Diseases 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 206010056242 Parkinsonian gait Diseases 0.000 description 1
- 206010056437 Parkinsonian rest tremor Diseases 0.000 description 1
- 208000012075 Paroxysmal dystonia Diseases 0.000 description 1
- 206010034912 Phobia Diseases 0.000 description 1
- 239000005062 Polybutadiene Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920002685 Polyoxyl 35CastorOil Polymers 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 206010062519 Poor quality sleep Diseases 0.000 description 1
- 208000036757 Postencephalitic parkinsonism Diseases 0.000 description 1
- 239000004820 Pressure-sensitive adhesive Substances 0.000 description 1
- 102100036389 Protocadherin-19 Human genes 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 238000001069 Raman spectroscopy Methods 0.000 description 1
- 206010071390 Resting tremor Diseases 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- 208000034189 Sclerosis Diseases 0.000 description 1
- 206010039966 Senile dementia Diseases 0.000 description 1
- 208000013140 Sensorimotor disease Diseases 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 206010040703 Simple partial seizures Diseases 0.000 description 1
- 201000007410 Smith-Lemli-Opitz syndrome Diseases 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 206010061372 Streptococcal infection Diseases 0.000 description 1
- 241000287181 Sturnus vulgaris Species 0.000 description 1
- 239000004376 Sucralose Substances 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 206010042464 Suicide attempt Diseases 0.000 description 1
- 208000035239 Synesthesia Diseases 0.000 description 1
- 206010043118 Tardive Dyskinesia Diseases 0.000 description 1
- 206010057040 Temperature intolerance Diseases 0.000 description 1
- 208000023655 Tic Diseases 0.000 description 1
- 206010044074 Torticollis Diseases 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 229940123445 Tricyclic antidepressant Drugs 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 206010046543 Urinary incontinence Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 201000006791 West syndrome Diseases 0.000 description 1
- 208000018839 Wilson disease Diseases 0.000 description 1
- 230000003187 abdominal effect Effects 0.000 description 1
- 208000028752 abnormal posture Diseases 0.000 description 1
- 208000003554 absence epilepsy Diseases 0.000 description 1
- 239000000619 acesulfame-K Substances 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 230000036626 alertness Effects 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 1
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 1
- 231100000540 amenorrhea Toxicity 0.000 description 1
- 229960005260 amiodarone Drugs 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 230000000181 anti-adherent effect Effects 0.000 description 1
- 239000003911 antiadherent Substances 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000002249 anxiolytic agent Substances 0.000 description 1
- 230000000949 anxiolytic effect Effects 0.000 description 1
- 230000036528 appetite Effects 0.000 description 1
- 235000019789 appetite Nutrition 0.000 description 1
- 230000004596 appetite loss Effects 0.000 description 1
- 230000037007 arousal Effects 0.000 description 1
- 229910052785 arsenic Inorganic materials 0.000 description 1
- RQNWIZPPADIBDY-UHFFFAOYSA-N arsenic atom Chemical compound [As] RQNWIZPPADIBDY-UHFFFAOYSA-N 0.000 description 1
- 230000002917 arthritic effect Effects 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 210000004227 basal ganglia Anatomy 0.000 description 1
- 201000008916 benign epilepsy with centrotemporal spikes Diseases 0.000 description 1
- 230000002146 bilateral effect Effects 0.000 description 1
- 208000028683 bipolar I disease Diseases 0.000 description 1
- 208000025307 bipolar depression Diseases 0.000 description 1
- 206010005159 blepharospasm Diseases 0.000 description 1
- 230000000744 blepharospasm Effects 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 230000007177 brain activity Effects 0.000 description 1
- 208000006752 brain edema Diseases 0.000 description 1
- 229940124630 bronchodilator Drugs 0.000 description 1
- 239000000168 bronchodilator agent Substances 0.000 description 1
- 235000019437 butane-1,3-diol Nutrition 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 229960001948 caffeine Drugs 0.000 description 1
- VJEONQKOZGKCAK-UHFFFAOYSA-N caffeine Natural products CN1C(=O)N(C)C(=O)C2=C1C=CN2C VJEONQKOZGKCAK-UHFFFAOYSA-N 0.000 description 1
- 230000002308 calcification Effects 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 230000001364 causal effect Effects 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 210000001638 cerebellum Anatomy 0.000 description 1
- 238000002144 chemical decomposition reaction Methods 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 230000035606 childbirth Effects 0.000 description 1
- 208000033205 childhood epilepsy with centrotemporal spikes Diseases 0.000 description 1
- 230000037326 chronic stress Effects 0.000 description 1
- 208000035850 clinical syndrome Diseases 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 229960003920 cocaine Drugs 0.000 description 1
- 230000001149 cognitive effect Effects 0.000 description 1
- 231100000870 cognitive problem Toxicity 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 231100000867 compulsive behavior Toxicity 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000009519 contusion Effects 0.000 description 1
- 208000012839 conversion disease Diseases 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 238000009223 counseling Methods 0.000 description 1
- 229960000913 crospovidone Drugs 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 1
- 231100000895 deafness Toxicity 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 231100000868 delusion Toxicity 0.000 description 1
- 230000003001 depressive effect Effects 0.000 description 1
- 230000000994 depressogenic effect Effects 0.000 description 1
- 238000004807 desolvation Methods 0.000 description 1
- AQEFLFZSWDEAIP-UHFFFAOYSA-N di-tert-butyl ether Chemical compound CC(C)(C)OC(C)(C)C AQEFLFZSWDEAIP-UHFFFAOYSA-N 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- GPLRAVKSCUXZTP-UHFFFAOYSA-N diglycerol Chemical compound OCC(O)COCC(O)CO GPLRAVKSCUXZTP-UHFFFAOYSA-N 0.000 description 1
- LVTYICIALWPMFW-UHFFFAOYSA-N diisopropanolamine Chemical compound CC(O)CNCC(C)O LVTYICIALWPMFW-UHFFFAOYSA-N 0.000 description 1
- 229940043276 diisopropanolamine Drugs 0.000 description 1
- 229940031578 diisopropyl adipate Drugs 0.000 description 1
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 208000002173 dizziness Diseases 0.000 description 1
- LQZZUXJYWNFBMV-UHFFFAOYSA-N dodecan-1-ol Chemical compound CCCCCCCCCCCCO LQZZUXJYWNFBMV-UHFFFAOYSA-N 0.000 description 1
- 229960003638 dopamine Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 230000037336 dry skin Effects 0.000 description 1
- 206010013932 dyslexia Diseases 0.000 description 1
- 230000000632 dystonic effect Effects 0.000 description 1
- 235000006694 eating habits Nutrition 0.000 description 1
- 238000002635 electroconvulsive therapy Methods 0.000 description 1
- 230000008451 emotion Effects 0.000 description 1
- 210000000750 endocrine system Anatomy 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 231100000321 erythema Toxicity 0.000 description 1
- MVPICKVDHDWCJQ-UHFFFAOYSA-N ethyl 3-pyrrolidin-1-ylpropanoate Chemical compound CCOC(=O)CCN1CCCC1 MVPICKVDHDWCJQ-UHFFFAOYSA-N 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 208000016253 exhaustion Diseases 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 208000027685 extreme exhaustion Diseases 0.000 description 1
- 231100000040 eye damage Toxicity 0.000 description 1
- 230000004424 eye movement Effects 0.000 description 1
- 206010016284 febrile convulsion Diseases 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 201000002904 focal dystonia Diseases 0.000 description 1
- 201000007186 focal epilepsy Diseases 0.000 description 1
- 208000028316 focal seizure Diseases 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000002695 general anesthesia Methods 0.000 description 1
- 239000003193 general anesthetic agent Substances 0.000 description 1
- 229940005494 general anesthetics Drugs 0.000 description 1
- 208000037870 generalized anxiety Diseases 0.000 description 1
- 208000028326 generalized seizure Diseases 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 150000002314 glycerols Chemical class 0.000 description 1
- 229940049654 glyceryl behenate Drugs 0.000 description 1
- 208000024963 hair loss Diseases 0.000 description 1
- 230000003676 hair loss Effects 0.000 description 1
- 235000001050 hortel pimenta Nutrition 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 239000008309 hydrophilic cream Substances 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 229920001600 hydrophobic polymer Polymers 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 229920000639 hydroxypropylmethylcellulose acetate succinate Polymers 0.000 description 1
- 230000001660 hyperkinetic effect Effects 0.000 description 1
- 230000002102 hyperpolarization Effects 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- 206010020765 hypersomnia Diseases 0.000 description 1
- 208000036260 idiopathic disease Diseases 0.000 description 1
- 201000001993 idiopathic generalized epilepsy Diseases 0.000 description 1
- 208000034287 idiopathic generalized susceptibility to 7 epilepsy Diseases 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000005414 inactive ingredient Substances 0.000 description 1
- 206010021654 increased appetite Diseases 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 208000000509 infertility Diseases 0.000 description 1
- 231100000535 infertility Toxicity 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- XUGNVMKQXJXZCD-UHFFFAOYSA-N isopropyl palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC(C)C XUGNVMKQXJXZCD-UHFFFAOYSA-N 0.000 description 1
- 229960002479 isosorbide Drugs 0.000 description 1
- 230000000366 juvenile effect Effects 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- WWDVNHHGXKIDDD-UHFFFAOYSA-N lambda1-arsanylsodium Chemical compound [Na].[As] WWDVNHHGXKIDDD-UHFFFAOYSA-N 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 229960004502 levodopa Drugs 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229960004488 linolenic acid Drugs 0.000 description 1
- KQQKGWQCNNTQJW-UHFFFAOYSA-N linolenic acid Natural products CC=CCCC=CCC=CCCCCCCCC(O)=O KQQKGWQCNNTQJW-UHFFFAOYSA-N 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000005923 long-lasting effect Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 208000019017 loss of appetite Diseases 0.000 description 1
- 235000021266 loss of appetite Nutrition 0.000 description 1
- 208000012866 low blood pressure Diseases 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 208000002780 macular degeneration Diseases 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229940057948 magnesium stearate Drugs 0.000 description 1
- 229940035034 maltodextrin Drugs 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 229960001855 mannitol Drugs 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000028161 membrane depolarization Effects 0.000 description 1
- 206010027175 memory impairment Diseases 0.000 description 1
- 230000002175 menstrual effect Effects 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 210000001259 mesencephalon Anatomy 0.000 description 1
- HOVAGTYPODGVJG-UHFFFAOYSA-N methyl beta-galactoside Natural products COC1OC(CO)C(O)C(O)C1O HOVAGTYPODGVJG-UHFFFAOYSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- STZCRXQWRGQSJD-GEEYTBSJSA-M methyl orange Chemical compound [Na+].C1=CC(N(C)C)=CC=C1\N=N\C1=CC=C(S([O-])(=O)=O)C=C1 STZCRXQWRGQSJD-GEEYTBSJSA-M 0.000 description 1
- 229940012189 methyl orange Drugs 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 229960001047 methyl salicylate Drugs 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000036640 muscle relaxation Effects 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- 201000003631 narcolepsy Diseases 0.000 description 1
- 230000008693 nausea Effects 0.000 description 1
- 230000007383 nerve stimulation Effects 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 239000003176 neuroleptic agent Substances 0.000 description 1
- 230000000701 neuroleptic effect Effects 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 230000002232 neuromuscular Effects 0.000 description 1
- 230000003955 neuronal function Effects 0.000 description 1
- 230000003961 neuronal insult Effects 0.000 description 1
- 229960002715 nicotine Drugs 0.000 description 1
- SNICXCGAKADSCV-UHFFFAOYSA-N nicotine Natural products CN1CCCC1C1=CC=CN=C1 SNICXCGAKADSCV-UHFFFAOYSA-N 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 238000011457 non-pharmacological treatment Methods 0.000 description 1
- 210000000869 occipital lobe Anatomy 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000003883 ointment base Substances 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 235000021313 oleic acid Nutrition 0.000 description 1
- 229940055577 oleyl alcohol Drugs 0.000 description 1
- XMLQWXUVTXCDDL-UHFFFAOYSA-N oleyl alcohol Natural products CCCCCCC=CCCCCCCCCCCO XMLQWXUVTXCDDL-UHFFFAOYSA-N 0.000 description 1
- 150000002891 organic anions Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 235000020830 overeating Nutrition 0.000 description 1
- QUANRIQJNFHVEU-UHFFFAOYSA-N oxirane;propane-1,2,3-triol Chemical compound C1CO1.OCC(O)CO QUANRIQJNFHVEU-UHFFFAOYSA-N 0.000 description 1
- 230000000803 paradoxical effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 239000003961 penetration enhancing agent Substances 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 238000011458 pharmacological treatment Methods 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920002857 polybutadiene Polymers 0.000 description 1
- 201000010065 polycystic ovary syndrome Diseases 0.000 description 1
- 239000008389 polyethoxylated castor oil Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000223 polyglycerol Polymers 0.000 description 1
- 229920001195 polyisoprene Polymers 0.000 description 1
- 229920000259 polyoxyethylene lauryl ether Polymers 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 1
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 1
- 230000004793 poor memory Effects 0.000 description 1
- 208000000170 postencephalitic Parkinson disease Diseases 0.000 description 1
- 229960003191 potassium methylparaben Drugs 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000003518 presynaptic effect Effects 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 208000002343 primary orthostatic tremor Diseases 0.000 description 1
- 230000002250 progressing effect Effects 0.000 description 1
- 201000002212 progressive supranuclear palsy Diseases 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 235000010388 propyl gallate Nutrition 0.000 description 1
- 239000000473 propyl gallate Substances 0.000 description 1
- 229940075579 propyl gallate Drugs 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 239000013074 reference sample Substances 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 238000005185 salting out Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 208000022610 schizoaffective disease Diseases 0.000 description 1
- 230000001932 seasonal effect Effects 0.000 description 1
- 229940124834 selective serotonin reuptake inhibitor Drugs 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- 235000019615 sensations Nutrition 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 208000013220 shortness of breath Diseases 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 230000037321 sleepiness Effects 0.000 description 1
- 210000002460 smooth muscle Anatomy 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- APSBXTVYXVQYAB-UHFFFAOYSA-M sodium docusate Chemical compound [Na+].CCCCC(CC)COC(=O)CC(S([O-])(=O)=O)C(=O)OCC(CC)CCCC APSBXTVYXVQYAB-UHFFFAOYSA-M 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 229940045902 sodium stearyl fumarate Drugs 0.000 description 1
- 229940001482 sodium sulfite Drugs 0.000 description 1
- 235000010265 sodium sulphite Nutrition 0.000 description 1
- AEQFSUDEHCCHBT-UHFFFAOYSA-M sodium valproate Chemical compound [Na+].CCCC(C([O-])=O)CCC AEQFSUDEHCCHBT-UHFFFAOYSA-M 0.000 description 1
- 238000010996 solid-state NMR spectroscopy Methods 0.000 description 1
- 238000007614 solvation Methods 0.000 description 1
- 238000000935 solvent evaporation Methods 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 201000002849 spasmodic dystonia Diseases 0.000 description 1
- 208000020431 spinal cord injury Diseases 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 229940032147 starch Drugs 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 229920006132 styrene block copolymer Polymers 0.000 description 1
- 201000009032 substance abuse Diseases 0.000 description 1
- 231100000736 substance abuse Toxicity 0.000 description 1
- BAQAVOSOZGMPRM-QBMZZYIRSA-N sucralose Chemical compound O[C@@H]1[C@@H](O)[C@@H](Cl)[C@@H](CO)O[C@@H]1O[C@@]1(CCl)[C@@H](O)[C@H](O)[C@@H](CCl)O1 BAQAVOSOZGMPRM-QBMZZYIRSA-N 0.000 description 1
- 235000019408 sucralose Nutrition 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 230000001502 supplementing effect Effects 0.000 description 1
- 238000004441 surface measurement Methods 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 230000000946 synaptic effect Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 201000008914 temporal lobe epilepsy Diseases 0.000 description 1
- 229960000278 theophylline Drugs 0.000 description 1
- 239000005495 thyroid hormone Substances 0.000 description 1
- 229940036555 thyroid hormone Drugs 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 229940042585 tocopherol acetate Drugs 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 238000011491 transcranial magnetic stimulation Methods 0.000 description 1
- 230000000472 traumatic effect Effects 0.000 description 1
- 230000003512 tremorgenic effect Effects 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- 239000003029 tricyclic antidepressant agent Substances 0.000 description 1
- 229940117957 triethanolamine hydrochloride Drugs 0.000 description 1
- HNJXPTMEWIVQQM-UHFFFAOYSA-M triethyl(hexadecyl)azanium;bromide Chemical compound [Br-].CCCCCCCCCCCCCCCC[N+](CC)(CC)CC HNJXPTMEWIVQQM-UHFFFAOYSA-M 0.000 description 1
- 229960004418 trolamine Drugs 0.000 description 1
- 208000009999 tuberous sclerosis Diseases 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 229940102566 valproate Drugs 0.000 description 1
- 230000001720 vestibular Effects 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 210000001260 vocal cord Anatomy 0.000 description 1
- 230000002747 voluntary effect Effects 0.000 description 1
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J43/00—Normal steroids having a nitrogen-containing hetero ring spiro-condensed or not condensed with the cyclopenta(a)hydrophenanthrene skeleton
- C07J43/003—Normal steroids having a nitrogen-containing hetero ring spiro-condensed or not condensed with the cyclopenta(a)hydrophenanthrene skeleton not condensed
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Pain & Pain Management (AREA)
- Psychiatry (AREA)
- Immunology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Steroid Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Epidemiology (AREA)
Abstract
Description
관련 출원에 대한 상호-참조
본 출원은 2016년 8월 23일에 출원된 U.S.S.N. 62/378,582의 우선권을 주장하며, 상기 출원은 그 전문이 본원에 참조로 포함된다.
뇌 흥분성은 혼수로부터 경련에 이르는 연속체인 동물의 각성 수준으로서 정의되며, 각종 신경전달물질에 의해 조절된다. 일반적으로, 신경전달물질은 뉴런 막을 가로지르는 이온의 전도도를 조절하는 것을 담당한다. 휴지 시, 뉴런 막은 대략 -70 mV의 전위 (또는 막 전압)를 가지며, 세포 내부는 세포 외부에 대해 음성이다. 전위 (전압)는 뉴런 반투과성 막을 가로지르는 이온 (K+, Na+, Cl-, 유기 음이온) 균형의 결과이다. 신경전달물질은 시냅스전 소포에 저장되고, 뉴런 활동 전위의 영향 하에 방출된다. 시냅스 간극으로 방출되는 경우, 흥분성 화학 전달물질 예컨대 아세틸콜린은 막 탈분극 (-70 mV로부터 -50 mV로의 전위 변화)을 유발할 것이다. 이러한 작용은 아세틸콜린에 의해 자극되는 시냅스후 니코틴성 수용체에 의해 매개되어, Na+ 이온에 대한 막 투과성을 증가시킨다. 감소된 막 전위는 시냅스후 활동 전위의 형태로 뉴런 흥분성을 자극한다.
γ-아미노부티르산 수용체 복합체 (GRC)의 경우에, 뇌 흥분성에 대한 작용은 신경전달물질인 γ-아미노부티르산 (GABA)에 의해 매개된다. 뇌 내 뉴런의 최대 40%가 신경전달물질로서 GABA를 이용하기 때문에, GABA는 전체 뇌 흥분성에 대해 막대한 영향을 미친다. GABA는 뉴런 막을 가로지르는 클로라이드 이온의 전도도를 조절함으로써 개별 뉴런의 흥분성을 조절한다. GABA는 GRC 상의 그의 인식 부위와 상호작용하여, 클로라이드 이온이 GRC의 전기화학 경사 하에 세포 내로 유동하는 것을 용이하게 한다. 상기 음이온 수준의 세포내 증가는 막횡단 전위의 과분극을 초래하여, 뉴런이 흥분성 입력에 덜 감수성이도록 한다 (즉, 감소된 뉴런 흥분성). 다시 말해서, 뉴런 내 클로라이드 이온 농도가 더 높을수록, 뇌 흥분성 (각성 수준)이 더 낮다.
뇌 흥분성에 대한 조정제 뿐만 아니라 CNS-관련 질환의 예방 및 치료를 위한 작용제로서 작용하는, 스테로이드의 신규의 개선된 신경활성 결정질 형태가 필요하다. 본원에 기재된 이러한 스테로이드의 결정질 형태는 이러한 목표에 관한 것이다.
본 발명은 부분적으로, 19-노르 (즉, C19 데스메틸) 화합물의 신규 형태 (예를 들어, 본원에 기재된 특정 결정질 형태)에 관한 것이다. 일반적으로, 고체 화합물의 약물로서의 효능은 그것이 구성하는 고체의 특성에 의해 영향을 받을 수 있다.
따라서, 한 측면에서, 본원에서 "화합물 1"로도 지칭되는 화학식 (I)의 결정질 화합물이 본원에 기재된다.
일부 실시양태에서, 화합물 1의 결정질 형태의 가용화된 형태는 저속 증발, 역용매(anti-solvent) 첨가, 저속 냉각, 용액 증기 확산, 고체 증기 확산, 고속 증발, 역(reverse) 역용매 첨가, 및 수분 활성 실험에 의해 화합물 1의 상이한 결정질 형태로 전환된다.
일부 실시양태에서, 화합물 1의 결정질 형태는 슬러리 전환에 의해 화합물 1의 상이한 결정질 형태로 전환된다.
일부 실시양태에서, 하기 분석 기술: X선 분말 회절 (XRPD) 분석, 예를 들어 가변-온도 XRPD (VT-XRPD) 분석, 단결정 X선 결정학, 열중량측정 분석 (TGA), 시차 주사 열량측정 (DSC), 핵 자기 공명 (NMR) 분광분석법 또는 고체-상태 NMR 분광분석법, 라만(Raman) 분광분석법, 또는 동적 증기 수착 (DVS) 중 1종 이상으로부터의 화합물 1의 고체 형태의 물리적 또는 화학적 파라미터가 평가된다.
실시양태에서, 각각의 고체 형태는, 상기 언급된 분석 방법 중 1종 이상으로부터 수득된 하기 파라미터를 사용하여 특징화 및 확인된다:
XRPD로의 분석에 의해 결정되는 바와 같은, 가로좌표로서의 도 2-세타 (2θ) 및 세로좌표로서의 피크 강도를 사용하여 제시된 X선 회절 패턴. 이들 패턴은 본원에서 XRPD 패턴으로도 지칭됨;
단결정 X선 결정학에 의해 결정되는 바와 같은, 고체 형태의 단결정 구조의 특성, 예를 들어 단위 셀, 결정계, 및 공간군;
단결정 X선 결정학으로부터의 데이터에 의해 결정되는 바와 같은, 결정질 형태에 대한 계산된 XRPD 패턴;
특정한 경사율에서 수행되는 DSC에 의해 결정되는 바와 같은, 용매의 손실, 한 결정질 형태로부터 또 다른 것으로의 변환, 또는 융점을 나타내는 개시 온도 T개시에 의해 명시되는 흡열;
TGA에 의해 결정되는 바와 같은 중량 손실에 대한 값;
DVS에 의해 결정되는 바와 같은, 25℃의 온도 및 5% 내지 95%의 상대 습도에서의 중량 증가에 대한 값; 및
중수소화 디메틸 술폭시드 (DMSO-d6) 중에 용해된 화합물 1의 예시적인 1H NMR 스펙트럼.
실시양태에서, 고체 형태는 상응하는 XRPD 패턴에서 발견되는 예리하고 뚜렷한 피크의 존재로 인해 결정질인 것으로 결정된다.
일부 실시양태에서, 화합물 1의 고체 형태가 실온보다 높은 온도에서 또 다른 고체 형태로 변환되었는지의 여부를 결정하기 위해, XRPD가 사용된다.
일부 실시양태에서, 결정질 화합물 1은 무수물이다.
일부 실시양태에서, 결정질 화합물 1은 용매화물이다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 11.6 내지 12.0 (예를 들어, 11.8), 13.7 내지 14.1 (예를 들어, 13.9), 14.0 내지 14.4 (예를 들어, 14.2), 16.6 내지 17.0 (예를 들어, 16.8), 18.9 내지 19.3 (예를 들어, 19.1), 19.1 내지 19.5 (예를 들어, 19.3), 19.9 내지 20.3 (예를 들어, 20.1), 21.1 내지 21.5 (예를 들어, 21.3), 21.9 내지 22.3 (예를 들어, 22.1), 및 23.0 내지 23.4 (예를 들어, 23.2)를 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 11.6 내지 12.0 (예를 들어, 11.8), 16.6 내지 17.0 (예를 들어, 16.8), 18.9 내지 19.3 (예를 들어, 19.1), 19.9 내지 20.3 (예를 들어, 20.1), 및 23.0 내지 23.4 (예를 들어, 23.2)를 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 11.8, 13.9, 14.2, 16.8, 19.1, 19.3, 20.1, 21.3, 22.1, 및 23.2에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 11.8, 16.8, 19.1, 20.1, 및 23.2에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 10a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.3 내지 9.7 (예를 들어, 9.5), 10.6 내지 11.0 (예를 들어, 10.8), 13.0 내지 13.4 (예를 들어, 13.2), 14.7 내지 15.1 (예를 들어, 14.9), 15.8 내지 16.2 (예를 들어, 16.0), 18.1 내지 18.5 (예를 들어, 18.3), 18.7 내지 19.1 (예를 들어, 18.9), 20.9 내지 21.3 (예를 들어, 21.1), 21.4 내지 21.8 (예를 들어, 21.6), 및 23.3 내지 23.7 (예를 들어, 23.5)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.3 내지 9.7 (예를 들어, 9.5), 10.6 내지 11.0 (예를 들어, 10.8), 13.0 내지 13.4 (예를 들어, 13.2), 18.7 내지 19.1 (예를 들어, 18.9), 및 21.4 내지 21.8 (예를 들어, 21.6)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.5, 10.8, 13.2, 14.9, 16.0, 18.3, 18.9, 21.1, 21.6, 및 23.5에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.5, 10.8, 13.2, 18.9, 및 21.6에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 1a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 1b에 도시된 바와 같은 단위 셀을 포함한다.
일부 실시양태에서, 화합물 1의 결정질 형태는, 약 150℃ 내지 약 195℃, 예를 들어 157℃ 내지 170℃의 온도에 적용 시, 10℃/분의 경사율에서 DSC에 의해 제시된 바와 같이 상이한 결정질 형태로 변환된다.
일부 실시양태에서, 결정질 화합물 1은 10℃/분의 경사율에서 DSC에 의해 측정 시, 약 200℃ 내지 약 225℃, 예를 들어 약 205℃ 내지 약 225℃, 예를 들어 약 208℃ 내지 약 215℃의 T개시에서 용융된다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.7 내지 10.1 (예를 들어, 9.9), 11.6 내지 12.0 (예를 들어, 11.8), 13.2 내지 13.6 (예를 들어, 13.4), 14.2 내지 14.6 (예를 들어, 14.4), 14.6 내지 15.0 (예를 들어, 14.8), 16.8 내지 17.2 (예를 들어, 17.0), 20.5 내지 20.9 (예를 들어, 20.7), 21.3 내지 21.7 (예를 들어, 21.5), 21.4 내지 21.8 (예를 들어, 21.6), 및 22.4 내지 22.8 (예를 들어, 22.6)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.7 내지 10.1 (예를 들어, 9.9), 14.6 내지 15.0 (예를 들어, 14.8), 16.8 내지 17.2 (예를 들어, 17.0), 20.5 내지 20.9 (예를 들어, 20.7), 및 21.3 내지 21.7 (예를 들어, 21.5)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.9, 11.8, 13.4, 14.4, 14.8, 17.0, 20.7, 21.5, 21.6, 및 22.6에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 하기 2θ 값 (도): 9.9, 14.8, 17.0, 20.7, 및 21.5에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 3a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 3b에 도시된 바와 같은 단위 셀을 포함한다.
일부 실시양태에서, 화합물 1의 결정질 형태는, 약 180℃ 내지 약 200℃, 예를 들어 약 184℃ 내지 약 200℃, 예를 들어 약 184℃ 내지 약 190℃의 온도에 적용 시, 10℃/분의 경사율에서 DSC에 의해 제시된 바와 같이 상이한 결정질 형태로 변환된다.
일부 실시양태에서, 결정질 화합물 1은 10℃/분의 경사율에서 DSC에 의해 측정 시, 약 200℃ 내지 약 225℃, 예를 들어 약 211℃ 내지 약 215℃의 T개시에서 용융된다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 2b에 도시된 바와 같은 XRPD 패턴 중 어느 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 4a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 5에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 6a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 7a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 8a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 9a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 11a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 12에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 13a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 14a에 도시된 바와 같은 XRPD 패턴을 갖는다.
일부 실시양태에서, 결정질 화합물 1은 실질적으로 도 16에 도시된 패턴 중 어느 패턴과 같은 XRPD 패턴을 갖는다.
한 측면에서, 본 발명은 화합물 1의 가용화된 형태로부터의 결정화 또는 슬러리 전환을 포함하는, 청구항 제5항의 결정질 화합물을 청구항 제10항의 결정질 화합물로 변환시키는 방법을 기재한다.
일부 실시양태에서, 변환은, 약 50℃ 내지 약 70℃, 예를 들어 60℃ 내지 65℃의 온도에서 용매로서 에틸 아세테이트를 사용하여 수행된다.
일부 실시양태에서, 변환은, 존재하는 화합물 1의 총량의 약 0.1% 내지 약 5.0%, 예를 들어 0.2% 내지 1.0%의 적재량으로의 청구항 제10항의 결정질 화합물의 시드 결정의 존재 하에 수행된다.
한 측면에서, 본 발명은 화합물 1의 결정질 형태, 및 제약상 허용되는 부형제를 포함하는 제약 조성물을 기재한다.
한 측면에서, 본 발명은 CNS-관련 장애의 치료를 필요로 하는 대상체에게 유효량의 화합물 1, 예를 들어 본원에 기재된 화합물 1의 결정질 고체 형태, 그의 제약상 허용되는 염, 또는 그의 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 CNS-관련 장애를 치료하는 방법을 기재한다.
일부 실시양태에서, CNS-관련 장애는 수면 장애, 기분 장애, 정신분열증 스펙트럼 장애, 경련성 장애, 기억 및/또는 인지 장애, 운동 장애, 인격 장애, 자폐증 스펙트럼 장애, 통증, 외상성 뇌 손상, 혈관 질환, 물질 남용 장애 및/또는 금단 증후군, 또는 이명이다.
일부 실시양태에서, 결정질 화합물 1은 경구로, 비경구로, 피내로, 척수강내로, 근육내로, 피하로, 질로, 협측으로, 설하로, 직장으로, 국소로, 흡입으로, 비강내로, 또는 경피로 투여된다.
일부 실시양태에서, 결정질 화합물 1은 만성적으로 투여된다.
또 다른 측면에서, 신경계 장애, 정신 장애, 발작 장애, 신경염증성 장애, 녹내장 또는 대사 장애, 감각 결핍 장애의 치료를 필요로 하는 대상체에게 유효량의 화합물 1 또는 그의 제약상 허용되는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 장애를 치료하는 방법이 본원에 제공된다.
또 다른 측면에서, 신경보호제를 필요로 하는 대상체에게 유효량의 화합물 1 또는 그의 제약상 허용되는 조성물을 투여하는 것을 포함하는, 화합물 1 또는 그의 제약상 허용되는 조성물을 신경보호제로서 사용하는 방법이 본원에 제공된다.
또 다른 측면에서, 진통제 또는 통증 조절을 위한 다른 작용제를 필요로 하는 대상체에게 유효량의 화합물 1 또는 그의 제약상 허용되는 조성물을 투여하는 것을 포함하는, 화합물 1 또는 그의 제약상 허용되는 조성물을 진통제 또는 통증 조절을 위한 다른 작용제로서 사용하는 방법이 본원에 제공된다. 일부 실시양태에서, 화합물 또는 제약상 허용되는 조성물은 염증성 통증, 신경병증성 통증, 섬유근육통, 또는 말초 신경병증을 치료하기 위해 진통제 또는 통증 조절을 위한 다른 작용제로서 사용된다.
본원에 사용된 "XRPD"는 X선 분말 회절을 지칭한다. 본원에 사용된 "VT-XRPD"는 가변 온도-X선 분말 회절을 지칭한다. 본원에 사용된 "TGA"는 열중량측정 분석을 지칭한다. 본원에 사용된 DSC는 시차 주사 열량측정을 지칭한다. 본원에 사용된 "NMR"은 핵 자기 공명을 지칭한다. 본원에 사용된 "DVS"는 동적 증기 수착을 지칭한다. 본원에 사용된 "DCM"은 디클로로메탄을 지칭한다. 본원에 사용된 "EtOAc"는 에틸 아세테이트를 지칭한다. 본원에 사용된 "MeOH"는 메탄올을 지칭한다. 본원에 사용된 "MBTE"는 메틸 tert-부틸 에테르를 지칭한다. 본원에 사용된 "RH"는 상대 습도를 지칭한다. 본원에 사용된 "RT"는 실온을 지칭한다.
본원에 사용된 "결정질"은 고도로 규칙적인 화학 구조를 갖는, 즉 결정 격자 내에 장범위 구조 규칙을 갖는 고체를 지칭한다. 분자는 격자의 3차원 공간 내에 규칙적이고 주기적인 방식으로 배열된다. 특히, 결정질 형태는 1종 이상의 단일 결정질 형태로서 생성될 수 있다. 본 출원의 목적을 위해, 용어 "결정질 형태", "단일 결정질 형태", "결정질 고체 형태", "고체 형태," 및 "다형체"는 동의어이며 상호교환가능하게 사용되고; 이들 용어는 상이한 특성 (예를 들어, 상이한 XRPD 패턴 및/또는 상이한 DSC 스캔 결과)을 갖는 결정들 사이를 구별한다.
용어 "실질적으로 결정질인"은 적어도 특정한 중량 퍼센트 결정질일 수 있는 형태를 지칭한다. 특정한 중량 백분율은 70%, 75%, 80%, 85%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 99.5%, 99.9%, 또는 70% 내지 100% 중의 어느 백분율이다. 특정 실시양태에서, 결정화도의 특정한 중량 퍼센트는 적어도 90%이다. 특정의 다른 실시양태에서, 결정화도의 특정한 중량 퍼센트는 적어도 95%이다. 일부 실시양태에서, 화합물 1은 본원에 기재된 결정질 고체 형태 (예를 들어, 형태 A, B, C, D, E, F, H, I, J, K, L, M, N, O 및 P) 중 어느 형태의 실질적으로 결정질인 샘플일 수 있다.
용어 "실질적으로 순수한"은 불순물 및/또는 화합물 1의 다른 고체 형태가 없는, 적어도 특정한 중량 퍼센트일 수 있는 화합물 1의 구체적 결정질 고체 형태의 조성을 지칭한다. 특정한 중량 백분율은 70%, 75%, 80%, 85%, 90%, 95%, 99%, 또는 70% 내지 100% 중의 어느 백분율이다. 일부 실시양태에서, 화합물 1은 본원에 기재된 결정질 고체 형태 (예를 들어, 형태 A, B, C, D, E, F, H, I, J, K, L, M, N, O 및 P) 중 어느 형태의 실질적으로 순수한 샘플일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 A일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 B일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 C일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 D일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 E일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 F일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 H일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 I일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 J일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 K일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 L일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 M일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 N일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 O일 수 있다. 일부 실시양태에서, 화합물 1은 실질적으로 순수한 형태 P일 수 있다.
화합물 1의 결정질 형태를 지칭하는 경우, 본원에 사용된 용어 "무수" 또는 "무수물"은 물 분자를 포함한 용매 분자가 결정질 형태의 단위 셀의 일부분을 형성하지 않는 것을 의미한다. 그럼에도 불구하고, 무수 결정질 형태의 샘플은 무수 결정질 형태의 단위 셀의 일부를 형성하지 않는 용매 분자를, 예를 들어 결정질 형태의 생성 이후에 남겨진 잔류 용매 분자로서 함유할 수 있다. 바람직한 실시양태에서, 용매는 무수 형태의 샘플의 전체 조성물의 0.5 중량%를 구성할 수 있다. 보다 바람직한 실시양태에서, 용매는 무수 형태의 샘플의 전체 조성물의 0.2 중량%를 구성할 수 있다. 일부 실시양태에서, 화합물 1의 무수 결정질 형태의 샘플은 용매 분자를 함유하지 않으며, 예를 들어 검출가능한 양의 용매를 함유하지 않는다. 화합물 1의 결정질 형태를 지칭하는 경우, 용어 "용매화물"은 용매 분자, 예를 들어 유기 용매 및 물이 결정질 형태의 단위 셀의 일부분을 형성하는 것을 의미한다. 용매로서 물을 함유하는 용매화물은 본원에서 "수화물"로도 지칭된다. 화합물 1의 결정질 형태를 지칭하는 경우, 용어 "동형"은 이러한 형태가 상이한 화학적 구성성분을 포함할 수 있으며, 예를 들어 단위 셀 내에 상이한 용매 분자를 함유할 수 있지만, 동일한 XRPD 패턴을 갖는 것을 의미한다. 동형 결정질 형태는 본원에서 때때로 "동형체"로 지칭된다.
본원에 기재된 화합물 1의 결정질 형태, 예를 들어 형태 K는 특정한 온도에서 또는 온도 범위에 걸쳐 용융될 수 있다. 이러한 특정한 온도 또는 온도 범위는 결정질 형태의 DSC 트레이스에서의 용융 흡열의 개시 온도 (T개시)에 의해 나타내어질 수 있다. 일부 실시양태에서, 이러한 개시 온도에서, 화합물 1의 결정질 형태의 샘플은 용융되고, 병행 발생 부공정(side-process), 예를 들어 재결정화 또는 화학적 분해를 겪는다. 일부 실시양태에서, 이러한 개시 온도에서, 화합물 1의 결정질 형태는 다른 병행 발생 공정의 부재 하에 용융된다.
화합물 1의 결정질 형태의 XRPD 패턴에서의 피크를 지칭하는 경우, 용어 "특징적인 피크"는, 0°-40° 범위에 걸친 2θ 값이 전체로서 화합물 1의 결정질 형태 중 1종에 특유하게 할당되는 것인 특정 피크의 집합을 지칭한다.
도 1a는 형태 A의 예시적인 XRPD 패턴을 도시한다.
도 1b는 b 축을 따르는 형태 A의 예시적인 단위 셀을 도시한다.
도 1c는 형태 A의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 1d는 형태 K의 예시적인 XRPD 패턴과 함께, 선택된 온도에서의 형태 A의 예시적인 VT-XRPD 패턴의 오버레이를 도시한다.
도 1e는 25℃에서의 형태 A의 예시적인 DVS 등온선을 도시한다.
도 1f는 25℃에서의 예시적인 DVS 측정 전후의 형태 A의 예시적인 XRPD 패턴을 도시한다.
도 2a는 형태 B의 동형체의 예시적인 XRPD 패턴을 도시한다.
도 2b는 형태 B의 3종의 동형체의 예시적인 XRPD 패턴을 도시한다.
도 2c는 형태 B의 동형체의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 2d는 형태 K의 예시적인 XRPD 패턴과 함께, 형태 B의 동형체의 예시적인 VT-XRPD 패턴의 오버레이를 도시한다.
도 2e는 형태 B의 동형체의 예시적인 TGA 곡선을 도시한다.
도 2f는 형태 B의 동형체의 예시적인 DSC 곡선을 도시한다.
도 2g는 DMSO-d6 중에 용해된 형태 B의 동형체의 예시적인 1H NMR 스펙트럼을 도시한다.
도 2h는 DMSO-d6 중에 용해된 형태 B의 동형체의 예시적인 1H NMR 스펙트럼을 도시한다.
도 2i는 DMSO-d6 중에 용해된 형태 B의 동형체의 예시적인 1H NMR 스펙트럼을 도시한다.
도 3a는 형태 C의 예시적인 XRPD 패턴을 도시한다.
도 3b는 b 축을 따르는 형태 C의 예시적인 단위 셀을 도시한다.
도 3c는 형태 C의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 3d는 선택된 온도에서의 형태 C의 예시적인 XRPD 패턴 뿐만 아니라 형태 K의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 3e는 N2 분위기의 존재 또는 부재 하의 선택된 온도에서의 형태 C의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 3f는 25℃에서의 형태 C의 예시적인 DVS 등온선을 도시한다.
도 3g는 25℃에서의 DVS 측정 전후의 형태 C의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 4a는 형태 D의 예시적인 XRPD 패턴을 도시한다.
도 4b는 형태 A의 예시적인 XRPD 패턴과 함께, 주위 조건에서의 건조 전후의 형태 D의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 5는 형태 E의 예시적인 XRPD 패턴을 도시한다.
도 6a는 형태 F의 예시적인 XRPD 패턴을 도시한다.
도 6b는 형태 F의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 6c는 형태 K의 예시적인 XRPD 패턴과 함께, 선택된 온도에서의 형태 F의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 6d는 DMSO-d6 중에 용해된 형태 F의 예시적인 1H NMR 스펙트럼을 도시한다.
도 7a는 형태 H의 예시적인 XRPD 패턴을 도시한다.
도 7b는 형태 A의 예시적인 XRPD 패턴 및 주위 조건에서의 건조 전후의 형태 H의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 8a는 형태 I의 예시적인 XRPD 패턴을 도시한다.
도 8b는 형태 A의 XRPD 패턴과 함께, 주위 조건에서 3일 동안의 건조 전후의 형태 I의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 9a는 형태 J의 예시적인 XRPD 패턴을 도시한다.
도 9b는 형태 A의 XRPD 패턴과 함께, 주위 조건에서 3일 동안의 건조 전후의 형태 J의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 10a는 형태 K의 예시적인 XRPD 패턴을 도시한다.
도 10b는 형태 K의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 10c는 25℃에서의 형태 K의 예시적인 DVS 등온선을 도시한다.
도 10d는 25℃에서의 예시적인 DVS 측정 전후의 형태 K의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 11a는 형태 L의 예시적인 XRPD 패턴을 도시한다.
도 11b는 형태 M 및 형태 B의 예시적인 XRPD 패턴과 함께, 3일 전후의 형태 L의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 11c는 형태 L의 예시적인 DSC 곡선을 도시한다.
도 12는 형태 M의 예시적인 XRPD 패턴을 도시한다.
도 13a는 형태 N의 예시적인 XRPD 패턴을 도시한다.
도 13b는 형태 A의 예시적인 XRPD 패턴과 함께, 주위 조건에서 밤새 건조 전후의 형태 N의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 13c는 형태 N의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 13d는 DMSO-d6 중에 용해된 형태 N의 예시적인 1H NMR 스펙트럼을 도시한다.
도 14a는 형태 O의 예시적인 XRPD 패턴을 도시한다.
도 14b는 형태 O의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 14c는 형태 C의 예시적인 XRPD 패턴과 함께, 선택된 온도에서의 형태 O의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 14d는 DMSO-d6 중에 용해된 형태 O의 예시적인 1H NMR 스펙트럼을 도시한다.
도 15는 형태 C의 시드 결정의 존재 하의 승온에서의 에틸 아세테이트 중 형태 A의 형태 C로의 시간-의존성 전환을 제시하는 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 16은 습윤 샘플 ("습윤 케이크"), 실온에서 공기 건조된 샘플 ("공기 건조된 것") 및 40℃에서 오븐-건조된 샘플 ("오븐 건조된 것")에 상응하는 형태 P의 예시적인 XRPD 패턴을 도시한다. 형태 A의 참조 샘플의 예시적인 XRPD가 또한 제공되어 있다.
도 17a는 실온에서의 공기-건조 후의 형태 P의 예시적인 1H NMR 스펙트럼을 도시한다.
도 17b는 40℃에서의 오븐-건조 후의 형태 P의 예시적인 1H NMR 스펙트럼을 도시한다.
도 18a는 실온에서의 공기-건조 후의 형태 P의 예시적인 TGA 곡선을 도시한다.
도 18b는 40℃에서의 오븐-건조 후의 형태 P의 예시적인 TGA 곡선을 도시한다.
도 19는 에틸 아세테이트 중 형태 A, C 및 P의 용해도 데이터의 예시적인 플롯을 도시한다.
도 20은 형태 A, C 및 P 사이의 예시적인 상 관계를 도시한다.
도 1b는 b 축을 따르는 형태 A의 예시적인 단위 셀을 도시한다.
도 1c는 형태 A의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 1d는 형태 K의 예시적인 XRPD 패턴과 함께, 선택된 온도에서의 형태 A의 예시적인 VT-XRPD 패턴의 오버레이를 도시한다.
도 1e는 25℃에서의 형태 A의 예시적인 DVS 등온선을 도시한다.
도 1f는 25℃에서의 예시적인 DVS 측정 전후의 형태 A의 예시적인 XRPD 패턴을 도시한다.
도 2a는 형태 B의 동형체의 예시적인 XRPD 패턴을 도시한다.
도 2b는 형태 B의 3종의 동형체의 예시적인 XRPD 패턴을 도시한다.
도 2c는 형태 B의 동형체의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 2d는 형태 K의 예시적인 XRPD 패턴과 함께, 형태 B의 동형체의 예시적인 VT-XRPD 패턴의 오버레이를 도시한다.
도 2e는 형태 B의 동형체의 예시적인 TGA 곡선을 도시한다.
도 2f는 형태 B의 동형체의 예시적인 DSC 곡선을 도시한다.
도 2g는 DMSO-d6 중에 용해된 형태 B의 동형체의 예시적인 1H NMR 스펙트럼을 도시한다.
도 2h는 DMSO-d6 중에 용해된 형태 B의 동형체의 예시적인 1H NMR 스펙트럼을 도시한다.
도 2i는 DMSO-d6 중에 용해된 형태 B의 동형체의 예시적인 1H NMR 스펙트럼을 도시한다.
도 3a는 형태 C의 예시적인 XRPD 패턴을 도시한다.
도 3b는 b 축을 따르는 형태 C의 예시적인 단위 셀을 도시한다.
도 3c는 형태 C의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 3d는 선택된 온도에서의 형태 C의 예시적인 XRPD 패턴 뿐만 아니라 형태 K의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 3e는 N2 분위기의 존재 또는 부재 하의 선택된 온도에서의 형태 C의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 3f는 25℃에서의 형태 C의 예시적인 DVS 등온선을 도시한다.
도 3g는 25℃에서의 DVS 측정 전후의 형태 C의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 4a는 형태 D의 예시적인 XRPD 패턴을 도시한다.
도 4b는 형태 A의 예시적인 XRPD 패턴과 함께, 주위 조건에서의 건조 전후의 형태 D의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 5는 형태 E의 예시적인 XRPD 패턴을 도시한다.
도 6a는 형태 F의 예시적인 XRPD 패턴을 도시한다.
도 6b는 형태 F의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 6c는 형태 K의 예시적인 XRPD 패턴과 함께, 선택된 온도에서의 형태 F의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 6d는 DMSO-d6 중에 용해된 형태 F의 예시적인 1H NMR 스펙트럼을 도시한다.
도 7a는 형태 H의 예시적인 XRPD 패턴을 도시한다.
도 7b는 형태 A의 예시적인 XRPD 패턴 및 주위 조건에서의 건조 전후의 형태 H의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 8a는 형태 I의 예시적인 XRPD 패턴을 도시한다.
도 8b는 형태 A의 XRPD 패턴과 함께, 주위 조건에서 3일 동안의 건조 전후의 형태 I의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 9a는 형태 J의 예시적인 XRPD 패턴을 도시한다.
도 9b는 형태 A의 XRPD 패턴과 함께, 주위 조건에서 3일 동안의 건조 전후의 형태 J의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 10a는 형태 K의 예시적인 XRPD 패턴을 도시한다.
도 10b는 형태 K의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 10c는 25℃에서의 형태 K의 예시적인 DVS 등온선을 도시한다.
도 10d는 25℃에서의 예시적인 DVS 측정 전후의 형태 K의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 11a는 형태 L의 예시적인 XRPD 패턴을 도시한다.
도 11b는 형태 M 및 형태 B의 예시적인 XRPD 패턴과 함께, 3일 전후의 형태 L의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 11c는 형태 L의 예시적인 DSC 곡선을 도시한다.
도 12는 형태 M의 예시적인 XRPD 패턴을 도시한다.
도 13a는 형태 N의 예시적인 XRPD 패턴을 도시한다.
도 13b는 형태 A의 예시적인 XRPD 패턴과 함께, 주위 조건에서 밤새 건조 전후의 형태 N의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 13c는 형태 N의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 13d는 DMSO-d6 중에 용해된 형태 N의 예시적인 1H NMR 스펙트럼을 도시한다.
도 14a는 형태 O의 예시적인 XRPD 패턴을 도시한다.
도 14b는 형태 O의 예시적인 TGA (상부) 및 DSC (하부) 곡선을 도시한다.
도 14c는 형태 C의 예시적인 XRPD 패턴과 함께, 선택된 온도에서의 형태 O의 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 14d는 DMSO-d6 중에 용해된 형태 O의 예시적인 1H NMR 스펙트럼을 도시한다.
도 15는 형태 C의 시드 결정의 존재 하의 승온에서의 에틸 아세테이트 중 형태 A의 형태 C로의 시간-의존성 전환을 제시하는 예시적인 XRPD 패턴의 오버레이를 도시한다.
도 16은 습윤 샘플 ("습윤 케이크"), 실온에서 공기 건조된 샘플 ("공기 건조된 것") 및 40℃에서 오븐-건조된 샘플 ("오븐 건조된 것")에 상응하는 형태 P의 예시적인 XRPD 패턴을 도시한다. 형태 A의 참조 샘플의 예시적인 XRPD가 또한 제공되어 있다.
도 17a는 실온에서의 공기-건조 후의 형태 P의 예시적인 1H NMR 스펙트럼을 도시한다.
도 17b는 40℃에서의 오븐-건조 후의 형태 P의 예시적인 1H NMR 스펙트럼을 도시한다.
도 18a는 실온에서의 공기-건조 후의 형태 P의 예시적인 TGA 곡선을 도시한다.
도 18b는 40℃에서의 오븐-건조 후의 형태 P의 예시적인 TGA 곡선을 도시한다.
도 19는 에틸 아세테이트 중 형태 A, C 및 P의 용해도 데이터의 예시적인 플롯을 도시한다.
도 20은 형태 A, C 및 P 사이의 예시적인 상 관계를 도시한다.
한 측면에서, 본 발명은 본원에서 "화합물 1"로도 지칭되는 화학식 (I)의 화합물이 다양한 분석 방법에 의해 제시된 바와 같이 상이한 결정질 형태로서 존재하는 것으로 밝혀졌음을 기재한다. 화합물 1 및 그의 화학적 합성은 미국 특허 출원 공개 번호 US 20160083417 및 PCT 출원 공개 번호 WO 2014169831에 이전에 개시되어 있다. 본 발명의 예시적인 개별 고체 형태는 하기 표 1에 제공되어 있다.
표 1. 화합물 1의 예시적인 결정질 형태의 요약.
화합물 1의 고체 형태, 그의 제조 방법
형태 B, C, D, E, F, H, I, J, K, N 및 O는 본원에 기재된 다양한 결정화 기술을 사용하여 형태 A로부터 제조되었다. 추가로, 형태 L 및 M은 본원에 기재된 다른 방법을 사용하여 형태 B로부터 제조되었다. 후속적으로, 이들 형태는 하기 분석 기술: X선 분말 회절 (XRPD), 예를 들어 가변-온도 X선 분말 회절 (VT-XRPD), 열중량측정 분석 (TGA), 시차 주사 열량측정 (DSC), 또는 동적 증기 수착 (DVS) 중 1종 이상에 의해 특징화되었다. 형태 A 및 형태 C의 단위 셀을 포함한 단결정 구조는 X선 회절계를 사용하여 수득된 데이터로부터 결정되었다. 또한, 형태 A 및 형태 C에 대한 계산된 XRPD 패턴은 그의 단결정 X선 회절 데이터로부터 수득되었다. 본 발명에서, DSC 및 TGA 데이터는 10℃/분의 경사율을 사용하여 수득되었다.
형태 A
형태 A는 에틸 아세테이트 중 슬러리로서의 조 화합물 1을 10℃ 미만에서 교반한 다음, 여과하고, 진공 하에 건조시킴으로써, 또는 조 화합물 1을 디클로로메탄 중에 용해시킨 다음, 에틸 아세테이트를 사용하여 상기 용액을 진공 하에 2회 재농축 건조시킴으로써 제조될 수 있다. 형태 A는 XRPD에 의해 화합물 1의 결정질 형태인 것으로 결정될 수 있다. 형태 A의 단결정 구조와 함께 TGA를 사용하면, 형태 A가 무수라는 결론을 내릴 수 있다. DSC를 사용하면, 300℃ 미만의 온도에서 발생하는 2회의 흡열: 형태 A의 형태 K로의 변환을 나타내는 157.2℃의 T개시를 갖는 1회의 흡열, 및 형태 K의 융점을 나타내는 203.8℃의 또 다른 흡열의 존재를 나타낼 수 있다. DVS를 사용하면, 형태 A가 95% 이하의 상대 습도 (RH)에서 0.30 중량 퍼센트 미만의 수분 흡수를 나타냄을 입증할 수 있다.
일부 실시양태에서, 형태 A는 실질적으로 도 1a에 도시된 바와 같은 XRPD 패턴을 가질 수 있다. 추가로, 형태 A의 XRPD 패턴으로부터의 대표적인 피크는, 예를 들어 하기 표 2에서와 같은 2θ 값, d-간격 및 상대 강도에 의해 제시될 수 있다.
표 2. 형태 A에 대한 선택된 실험적 XRPD 패턴 데이터.
일부 실시양태에서, 형태 A는 하기 2θ 값 (도): 9.3 내지 9.7 (예를 들어, 9.5), 10.6 내지 11.0 (예를 들어, 10.8), 13.0 내지 13.4 (예를 들어, 13.2), 14.7 내지 15.1 (예를 들어, 14.9), 15.8 내지 16.2 (예를 들어, 16.0), 18.1 내지 18.5 (예를 들어, 18.3), 18.7 내지 19.1 (예를 들어, 18.9), 20.9 내지 21.3 (예를 들어, 21.1), 21.4 내지 21.8 (예를 들어, 21.6), 및 23.3 내지 23.7 (예를 들어, 23.5)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다. 일부 실시양태에서, 형태 A는 하기 2θ 값 (도): 9.3 내지 9.7 (예를 들어, 9.5), 10.6 내지 11.0 (예를 들어, 10.8), 13.0 내지 13.4 (예를 들어, 13.2), 18.7 내지 19.1 (예를 들어, 18.9), 및 21.4 내지 21.8 (예를 들어, 21.6)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다. 일부 실시양태에서, 형태 A는 하기 2θ 값 (도): 9.5, 10.8, 13.2, 14.9, 16.0, 18.3, 18.9, 21.1, 21.6, 및 23.5에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다. 일부 실시양태에서, 형태 A는 하기 2θ 값 (도): 9.5, 10.8, 13.2, 18.9, 및 21.6에서 특징적인 피크를 갖는 XRPD 패턴을 갖는다.
선택된 피크에 대한 계산된 XRPD 데이터는, 표 2에서의 실험 데이터를 보충하는 하기 표 3에 제공된 바와 같은 형태 A의 단결정으로부터의 X선 회절 데이터로부터 수득될 수 있다.
표 3. 형태 A에 대한 선택된 계산된 XRPD 패턴 데이터.
형태 B
형태 B는 XRPD에 의해 결정된 바와 같이 화합물 1의 결정질 형태로서 존재할 수 있으며, 본원에 기재된 다양한 기술, 예를 들어 저속 증발, 슬러리 전환, 역용매 첨가, 고체 증기 확산, 또는 저속 냉각으로부터 제조될 수 있다. 또한, 상이한 용매계 예컨대 디클로로메탄 (DCM)/n-헵탄, 테트라히드로푸란 (THF)/n-헵탄, 또는 클로로포름 (CHCl3)/메틸 tert-부틸 에테르 (MBTE)로부터의 형태 B의 동형체가 제조될 수 있다. 표 4는 다양한 기기분석 방법, 예를 들어 TGA, DSC 및 1H NMR 분광분석법에 의해 결정된 바와 같은 이들 동형체의 특성을 요약하고 있다.
표 4. 형태 B의 예시적인 동형체의 요약
형태 C
형태 C는 XRPD에 의해 결정된 바와 같이 화합물 1의 결정질 무수물이며, 50℃에서 이소프로필 알콜 및 이소프로필 아세테이트에서의 슬러리 전환 결정화 기술을 사용하여 형태 A로부터 제조될 수 있다. TGA 및 단결정 X선 결정학을 사용하면, 형태 C 중 용매의 부재를 확인할 수 있다. DSC를 사용하면, 300℃ 미만에서의 2회의 흡열: 형태 C의 형태 K로의 변환에 상응하는 183.8℃의 T개시를 갖는 넓은 피크, 및 형태 K의 용융에 상응하는 211.0℃의 T개시를 갖는 예리한 피크를 나타낼 수 있다. DVS를 사용하면, 형태 C가 95% 이하의 RH에서 0.32 중량 퍼센트 미만의 수분 흡수를 나타냄을 입증할 수 있다.
일부 실시양태에서, 형태 C는 실질적으로 도 3a에 도시된 바와 같은 XRPD 패턴을 가질 수 있다. 추가로, 형태 C의 XRPD 패턴으로부터의 대표적인 피크는, 예를 들어 하기 표 5에서와 같은 2θ 값, d-간격 및 상대 강도에 의해 제시될 수 있다.
표 5. 형태 C에 대한 선택된 실험적 XRPD 패턴 데이터.
일부 실시양태에서, 형태 C는 하기 2θ 값 (도): 9.7 내지 10.1 (예를 들어, 9.9), 11.6 내지 12.0 (예를 들어, 11.8), 13.2 내지 13.6 (예를 들어, 13.4), 14.2 내지 14.6 (예를 들어, 14.4), 14.6 내지 15.0 (예를 들어, 14.8), 16.8 내지 17.2 (예를 들어, 17.0), 20.5 내지 20.9 (예를 들어, 20.7), 21.3 내지 21.7 (예를 들어, 21.5), 21.4 내지 21.8 (예를 들어, 21.6), 및 22.4 내지 22.8 (예를 들어, 22.6)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다. 일부 실시양태에서, 형태 C는 하기 2θ 값 (도): 9.7 내지 10.1 (예를 들어, 9.9), 14.6 내지 15.0 (예를 들어, 14.8), 16.8 내지 17.2 (예를 들어, 17.0), 20.5 내지 20.9 (예를 들어, 20.7), 및 21.3 내지 21.7 (예를 들어, 21.5)을 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다. 일부 실시양태에서, 형태 C는 하기 2θ 값 (도): 9.9, 11.8, 13.4, 14.4, 14.8, 17.0, 20.7, 21.5, 21.6, 및 22.6에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다. 일부 실시양태에서, 형태 C는 하기 2θ 값 (도): 9.9, 14.8, 17.0, 20.7, 및 21.5에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다.
선택된 피크에 대한 계산된 XRPD 데이터는, 하기 표 6에 제공된 바와 같은 형태 C의 단결정으로부터의 X선 회절 데이터를 사용하여 수득될 수 있다. 이들 모의 피크는 표 5에서의 실험 데이터를 보충할 수 있다.
표 6. 형태 C에 대한 선택된 계산된 XRPD 패턴 데이터.
형태 D
형태 D는 테트라히드로푸란 (THF)/물 (H2O)에서의 역용매 첨가 결정화 기술을 사용하여 제조될 수 있으며, 후속적으로 XRPD 분석에 의해 실온에서 건조 시에 형태 A로 다시 전환되는 화합물 1의 결정질 형태인 것으로 밝혀질 수 있다.
형태 E
형태 E는 실온에서 1,4-디옥산/n-헵탄에서의 역용매 결정화 기술로부터 제조될 수 있으며, XRPD에 의해 화합물 1의 결정질 습윤 샘플인 것으로 결정될 수 있다.
형태 F
형태 F는 주위 실온 조건에서 1,4-디옥산/n-헵탄에서의 역용매 첨가 결정화 기술을 사용하여 제조될 수 있으며, XRPD에 의해 화합물 1의 결정질 형태인 것으로 결정될 수 있다. 형태 F의 샘플에 대한 TGA는 200℃까지 19.7%의 중량 손실을 나타낸다. DSC를 사용하면, 형태 F가 각각 용매의 손실 (형태 K로의 변환) 및 형태 K의 융점에 상응하는 63.1℃ 및 210.7℃의 개시 온도에서 2개의 흡열 피크를 나타냄을 제시할 수 있다. 형태 F의 형태 K로의 변환은 VT-XRPD 측정을 통해 추가로 확인될 수 있다. 1H NMR 분광분석법에 기초하면, 형태 F는 잔류 n-헵탄이 1:0.9의 몰비로 존재하는 1,4-디옥산 용매화물이다.
형태 H
형태 H는 실온에서 n-헵탄에서의 용액 증기 확산 결정화 기술로부터 제조될 수 있다. 본 형태는 XRPD에 의해 결정질인 것으로 결정되었지만, 주위 조건에서 3일 동안 건조시킨 후에 형태 A로 변환됨으로 인해 준안정하였다.
형태 I
형태 I는 실온에서 메탄올 중에서 수행되는 저속 냉각 결정화 기술을 사용하여 제조될 수 있다. 형태 H와 마찬가지로, 형태 I는 XRPD 분석에 의해 결정질 물질인 것으로 결정될 수 있지만, 주위 조건에서 3일 동안 건조시킨 후에 형태 A로 변환됨으로 인해 준안정한 것으로 밝혀졌다.
형태 J
형태 J는 실온에서 메탄올에서의 고체 증기 확산 결정화 기술을 사용하여 제조될 수 있다. XRPD 분석을 사용하면, 형태 J가 주위 조건에서 3일 동안 건조시킨 후에 형태 A로 변환되는 결정질 준안정 샘플이라는 결론을 내릴 수 있다.
형태 K
형태 K는 화합물 1의 다양한 형태, 예를 들어 형태 A, 형태 B, 형태 C, 형태 E 및 형태 F를 승온으로 가열함으로써 제조될 수 있다. 본 형태의 분석 샘플은 XRPD 분석에 의해 결정질인 것으로 결정될 수 있다. TGA를 사용하면, 분해 온도 이전에는 중량 손실이 없음을 나타낼 수 있고, 형태 K가 무수임을 입증할 수 있다. DSC를 사용하면, 형태 K가 분석 샘플의 융점에 상응하는 211.6℃의 T개시를 갖는 단일 흡열을 나타낼 수 있음을 입증할 수 있다. DVS 측정을 수행하여, 형태 K가 95% 이하의 RH에서 0.35 중량 퍼센트 미만의 수분 흡수를 나타냄을 입증하였다.
일부 실시양태에서, 형태 K는 실질적으로 도 10a에 도시된 바와 같은 XRPD 패턴을 가질 수 있다. 추가로, 형태 K의 XRPD 패턴으로부터의 대표적인 피크는, 예를 들어 하기 표 7에서와 같은 2θ 값 및 상대 강도에 의해 제시될 수 있다.
표 7. 형태 K에 대한 선택된 실험적 XRPD 패턴 데이터.
일부 실시양태에서, 형태 K는 하기 2θ 값 (도): 11.6 내지 12.0 (예를 들어, 11.8), 13.7 내지 14.1 (예를 들어, 13.9), 14.0 내지 14.4 (예를 들어, 14.2), 16.6 내지 17.0 (예를 들어, 16.8), 18.9 내지 19.3 (예를 들어, 19.1), 19.1 내지 19.5 (예를 들어, 19.3), 19.9 내지 20.3 (예를 들어, 20.1), 21.1 내지 21.5 (예를 들어, 21.3), 21.9 내지 22.3 (예를 들어, 22.1), 및 23.0 내지 23.4 (예를 들어, 23.2)를 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다. 일부 실시양태에서, 형태 K는 하기 2θ 값 (도): 11.6 내지 12.0 (예를 들어, 11.8), 16.6 내지 17.0 (예를 들어, 16.8), 18.9 내지 19.3 (예를 들어, 19.1), 19.9 내지 20.3 (예를 들어, 20.1), 및 23.0 내지 23.4 (예를 들어, 23.2)를 포함하여 이들 사이에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다. 일부 실시양태에서, 형태 K는 하기 2θ 값 (도): 11.8, 13.9, 14.2, 16.8, 19.1, 19.3, 20.1, 21.3, 22.1, 및 23.2에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다. 일부 실시양태에서, 형태 K는 하기 2θ 값 (도): 11.8, 16.8, 19.1, 20.1, 및 23.2에서 특징적인 피크를 갖는 XRPD 패턴을 가질 수 있다.
형태 L
형태 L은 형태 B를 밀봉된 바이알 내에서 주위 조건에서 1개월 동안 저장함으로써 제조될 수 있다. 본 형태는 화합물 1의 결정질 준안정 형태인 것으로 결정될 수 있다. XRPD로 분석하면, 형태 L이 제조하고 나서 3일 후에 주위 조건에서 형태 B와 형태 M의 혼합물로 변환됨을 나타낼 수 있다. 형태 L은 화합물 1의 용매화물인 것으로 결정되었다.
형태 M
형태 M은 형태 B를 밀봉된 바이알 내에서 주위 조건에서 1개월 동안 저장함으로써 제조될 수 있다. 본 형태의 분석 샘플은 XRPD로의 분석에 의해 낮은 결정화도를 갖는 것으로 결정되었다.
형태 N
형태 N은 1,4-디옥산/n-헵탄에서의 역 역용매 첨가 결정화 기술로부터 제조될 수 있으며, XRPD에 의해 화합물 1의 결정질 형태인 것으로 결정될 수 있다. TGA를 사용하면, 형태 N이 60℃까지 2.5%의 중량 손실, 이어서 200℃까지 7.1%의 중량 손실을 나타내는 용매화물임을 결정할 수 있다. DSC를 사용하면, 2회의 흡열: 용매의 손실에 상응하는 75.4℃의 T개시에서의 1회의 흡열, 및 형태 K의 융점을 나타내는 210.4℃의 T개시에서의 나머지 흡열을 입증할 수 있다. VT-XRPD를 사용하면, 형태 N이 100℃에서 형태 K로 변환됨을 확인할 수 있다. 1H NMR 분광분석법에 기초하면, 형태 N은 화합물 1:1,4-디옥산의 몰비 1:0.3의 1,4-디옥산 용매화물이다.
형태 O
형태 O는 실온에서 물/아세토니트릴 혼합물 중 수분 활성 실험 (0.041 물:0.959 아세토니트릴 부피/부피; aw=0.6)을 사용하여 제조될 수 있으며, XRPD에 의해 화합물 1의 결정질 형태인 것으로 결정될 수 있다. 형태 O의 샘플에 대한 TGA는 55.1℃까지 5.3%, 이어서 200℃까지 5.9%의 중량 손실을 나타낼 수 있다. DSC를 사용하면, 형태 O가, 3회의 흡열: 형태 C의 생성을 위한 용매의 손실에 상응하는 T개시 = 65.0℃에서의 1회의 흡열, 형태 C의 형태 K로의 변환에 상응하는 T개시 = 168.5℃에서의 1회의 흡열, 및 형태 K의 용융에 상응하는 T개시 = 210.8℃에서의 1회의 흡열을 나타냄을 제시할 수 있다. 형태 O는 DMSO-d6에 중에 용해된 1H NMR 분광분석법에 의해 추가로 특징화될 수 있다.
형태 P
상기 기재된 형태 이외에도, 형태 P가 화합물 1의 에틸 아세테이트 (EtOAc) 용매화물이며, (a) 5℃ (1시간 후) 및 20℃ (2일 후)에서의 EtOAc 중 형태 A의 슬러리, (b) 5℃ (1시간 후) 및 20℃ (7일 후)에서의 EtOAc 중 형태 C의 슬러리 중에서 검출될 수 있다. 형태 P의 습윤 케이크 (~5분 공기)를 2종의 방식으로: (a) 공기 하에 실온에서 밤새, 및 (b) 진공 하에 40℃에서 3시간 동안 건조시킬 수 있다. 둘 다의 건조된 케이크를 XRPD, 1H-NMR 및 TGA에 의해 분석할 수 있다. 형태 P의 공기 건조된 케이크는 형태 P에 따른 XRPD 패턴, TGA에 의해 약 50℃까지 약 1%의 중량 손실, 및 1H NMR에 의해 EtOAc 피크를 제공할 수 있다. 다른 한편, 오븐 건조 후 형태 P의 샘플은 형태 A에 따른 XRPD 패턴, TGA에 의해 ≤ 100℃에서 중량 손실 없음, 및 1H-NMR에 의해 EtOAc 피크 없음을 제공할 수 있다. 따라서, 형태 P는 건조 시에 형태 A로 전환될 수 있다.
또 다른 측면에서, 본 발명은 화합물 1의 고체 형태 또는 화합물 1의 고체 형태들의 혼합물을 화합물 1의 상이한 무수물로 변환시키는 방법을 제공한다. 한 실시양태에서, 형태 A, 형태 A 또는 형태 K의 혼합물, 또는 형태 A, 형태 C 및 형태 K의 혼합물을 실온 또는 승온, 예를 들어 50℃ 또는 65℃에서 에틸 아세테이트, n-부탄올, 또는 메틸 tert-부틸 에테르에서의 슬러리 전환을 통해 형태 C로 전환시킬 수 있다. 이들 3종의 용매계 중에서는, 형태 C가 슬러리 전환 후에 남아있는 유일한 형태이며, 이는 상기 고체 형태가 형태 A 및 형태 K와 비교했을 때 실온 내지 50℃에서 더 열역학적으로 안정함을 보여준다. 또 다른 실시양태에서, 형태 C는 소량, 예를 들어 0.2%-1.0%의 형태 C의 시드 결정의 존재 하에 승온, 예를 들어 65℃에서 에틸 아세테이트 중에서 가용화된 화합물 1 (원래 형태 A)을 결정화시키고, 배치를 25℃ 이상 내지 30℃의 온도로 냉각시키는 것을 통해 수득될 수 있다. 형태 C의 시드 결정은 본원에 기재된 실시예 4에 기재된 절차를 사용하여 제조될 수 있다.
제약 조성물
또 다른 측면에서, 본 발명은 본 발명의 화합물의 고체 형태 ("활성 성분"으로도 지칭됨), 및 제약상 허용되는 부형제를 포함하는 제약 조성물을 제공한다. 특정 실시양태에서, 제약 조성물은 유효량의 활성 성분을 포함한다. 특정 실시양태에서, 제약 조성물은 치료 유효량의 활성 성분을 포함한다. 특정 실시양태에서, 제약 조성물은 예방 유효량의 활성 성분을 포함한다.
본원에 제공된 제약 조성물은 경구 (경장) 투여, 비경구 (주사에 의함) 투여, 직장 투여, 국소 투여, 경피 투여, 피내 투여, 척수강내 투여, 피하 (SC) 투여, 근육내 (IM) 투여, 설하 / 협측, 안구, 귀, 질, 및 비강내 또는 흡입 투여를 포함하나, 이에 제한되지는 않는 다양한 경로에 의해 투여될 수 있다.
일반적으로, 본원에 제공된 화합물 1의 고체 형태는 유효량으로 투여된다. 실제로 투여되는 화합물인 화합물 1의 고체 형태의 양은 전형적으로 의사에 의해, 치료될 상태, 선택된 투여 경로, 투여되는 실제 화합물, 개별 환자의 연령, 체중, 및 반응, 환자 증상의 중증도 등을 포함한 관련 상황에 비추어 결정될 것이다.
CNS-장애의 발병을 예방하기 위해 사용되는 경우, 본원에 제공된 화합물 1의 고체 형태는, 전형적으로 의사의 권고에 따라 그의 감독 하에, 상기 기재된 투여량 수준으로 이러한 상태가 발생할 위험이 있는 대상체에게 투여될 것이다. 특정한 상태가 발생할 위험이 있는 대상체는 일반적으로 이러한 상태의 가족력을 갖는 대상체, 또는 유전자 검사 또는 스크리닝에 의해 이러한 상태가 발생하기 특히 쉬운 것으로 확인된 대상체를 포함한다.
본원에 제공된 제약 조성물은 또한 만성적으로 투여될 수 있다 ("만성 투여"). 만성 투여는 연장된 기간, 예를 들어 3개월, 6개월, 1년, 2년, 3년, 5년 등에 걸친 화합물 1의 고체 형태 또는 그의 제약 조성물의 투여를 지칭하거나, 또는 무기한으로, 예를 들어 대상체의 나머지 일생 동안 지속될 수 있다. 특정 실시양태에서, 만성 투여는 연장된 기간에 걸쳐 혈액 중 화합물 1의 일정한 수준을, 예를 들어 치료 윈도우 내에서 제공하도록 의도된다.
추가로, 본 발명의 제약 조성물은 다양한 투여 방법을 사용하여 전달될 수 있다. 예를 들어, 특정 실시양태에서, 제약 조성물은, 예를 들어 혈액 중 화합물 1의 농도를 유효 수준으로 상승시키기 위해, 볼루스로서 주어질 수 있다. 볼루스 용량의 배치는 신체 전반에 걸쳐 원하는 활성 성분의 전신 수준에 따라 달라지며, 예를 들어 근육내 또는 피하 볼루스 용량은 활성 성분의 느린 방출을 가능하게 한다. 또한, 또 다른 실시양태에서, 제약 조성물은 먼저 볼루스 용량으로서 투여되고, 이어서 연속 주입될 수 있다.
경구 투여를 위한 조성물은 벌크 액체 용액 또는 현탁액 또는 벌크 분말의 형태를 취할 수 있다. 그러나, 보다 통상적으로, 조성물은 정확한 투여를 용이하게 하기 위해 단위 투여 형태로 제시된다. 용어 "단위 투여 형태"는 인간 대상체 및 다른 포유동물을 위한 단일 투여량으로서 적합한 물리적 이산 단위를 지칭하며, 각각의 단위는 원하는 치료 효과를 생성하도록 계산된 미리 결정된 양의 활성 물질을 적합한 제약 부형제와 함께 함유한다. 전형적인 단위 투여 형태는 액체 조성물의 예비충전된 미리 측정된 앰플 또는 시린지, 또는 고체 조성물의 경우에는 환제, 정제, 캡슐 등을 포함한다. 이러한 조성물에서, 화합물 1의 고체 형태는 통상적으로 소량 성분 (약 0.1 내지 약 50 중량%, 또는 바람직하게는 약 1 내지 약 40 중량%)이며, 나머지는 다양한 비히클 또는 부형제 및 원하는 투여 형태의 형성을 돕는 가공 조제이다.
경구 투여의 경우, 1일 1 내지 5회, 특히 2 내지 4회, 전형적으로 3회의 경구 용량이 대표적인 요법이다. 이들 투여 패턴을 사용하면, 각각의 용량은 약 0.01 내지 약 20 mg/kg의 본원에 제공된 화합물 1의 고체 형태를 제공하며, 바람직한 용량은 각각 약 0.1 내지 약 10 mg/kg, 특히 약 0.2 내지 약 5 mg/kg을 제공한다.
경피 용량은 일반적으로 주사 용량을 사용하여 달성되는 혈액 수준과 유사하거나 또는 그보다 더 낮은 혈액 수준을 제공하도록 선택되며, 예를 들어 경피 패치를 위한 약물 저장소 또는 약물-접착제 저장소의 일반적으로 약 0.01 내지 약 20 중량%, 바람직하게는 약 0.1 내지 약 20 중량%, 바람직하게는 약 0.1 내지 약 10 중량%, 보다 바람직하게는 약 0.5 내지 약 15 중량% 범위의 양이다.
고체 조성물은, 예를 들어 임의의 하기 성분, 또는 유사한 성질의 화합물 1의 고체 형태를 포함할 수 있다: 결합제, 계면활성제, 희석제 또는 충전제, 완충제, 부착방지제, 활택제, 친수성 또는 소수성 중합체, 지연제, 안정화제 또는 안정화제, 붕해제 또는 초붕해제, 분산제, 산화방지제, 소포제, 충전제, 향미제, 착색제, 윤활제, 흡착제, 보존제, 가소화제, 코팅, 또는 감미제, 또는 그의 혼합물. 예를 들어, 부형제 또는 부형제들은 결합제 예컨대 미세결정질 셀룰로스, 폴리비닐 피롤리돈, 히드록시프로필 셀룰로스, 저점도 히드록시프로필메틸셀룰로스, 트라가칸트 검 또는 젤라틴; 희석제 예컨대 만니톨, 미세결정질 셀룰로스, 말토덱스트린, 전분 또는 락토스, 붕해제 예컨대 알긴산, 프리모겔, 소듐 스타치 글리콜레이트, 소듐 크로스카르멜로스, 크로스포비돈, 또는 옥수수 전분; 윤활제 예컨대 스테아르산마그네슘, 소듐 스테아릴 푸마레이트 또는 글리세릴 베헤네이트; 활택제 예컨대 콜로이드성 이산화규소; 보존제 예컨대 소르브산칼륨 또는 메틸 파라벤, 계면활성제, 예컨대 소듐 라우릴 술페이트, 소듐 도큐세이트, 폴리소르베이트(polysorbate) 20, 폴리소르베이트 80, 세틸 트리에틸 암모늄 브로마이드, 폴리에틸렌 옥시드-폴리프로필렌 옥시드 공중합체, 또는 크레모포르(Cremophor) EL, 산화방지제 예컨대 부틸히드록시 톨루엔, 부틸 히드록시아니솔, 프로필 갈레이트, 아스코르브산, 토코페롤 또는 토코페롤 아세테이트, 아황산나트륨, 또는 메타중아황산나트륨, 히드록시프로필메틸셀룰로스, 폴리비닐 알콜, 메타크릴레이트 공중합체, 셀룰로스 아세테이트, 히드록시프로필메틸셀룰로스 아세테이트 숙시네이트, 쉘락 및 다른 것들 중 1종 이상을 포함하는 코팅, 감미제 예컨대 수크로스, 수크랄로스, 아세술팜 K, 소듐 아스파르탐 또는 사카린; 또는 향미제 예컨대 페퍼민트, 메틸 살리실레이트, 또는 오렌지 향미제일 수 있다. 임의의 널리 공지된 제약 부형제가 투여 형태에 혼입될 수 있으며, 모두 참조로 포함되는 FDA 불활성 성분 가이드, 문헌 [Remington: The Science and Practice of Pharmacy, Twenty-first Ed., (Pharmaceutical Press, 2005); Hnadbook of Pharmaceutical Excipients, Sixth Ed. (Pharmacrutical Press, 2009)]에서 찾아볼 수 있다.
경피 조성물은 전형적으로 활성 성분(들)을 함유하는 국소 연고 또는 크림으로서 제제화된다. 연고로서 제제화되는 경우, 활성 성분은 전형적으로 파라핀계 또는 수혼화성 연고 베이스와 조합될 것이다. 대안적으로, 활성 성분은, 예를 들어 수중유 크림 베이스와 함께 크림으로 제제화될 수 있다. 이러한 경피 제제는 관련 기술분야에 널리 공지되어 있으며, 일반적으로 활성 성분 또는 제제의 피부 침투 및 안정성을 증진시키기 위한 추가의 성분을 포함한다. 모든 이러한 공지된 경피 제제 및 성분이 본원에 제공된 범주 내에 포함된다. 관심 국소 전달 조성물은 액체 제제, 예컨대 로션 (스프레이 로션을 포함한, 외부 적용을 위해 의도된 현탁액 또는 에멀젼 형태의, 불용성 물질을 함유하는 액체), 및 수용액, 반고체 제제, 예컨대 겔 (분산 상이 분산 매질과 조합되어 반고체 물질, 예컨대 젤리를 생성하는 것인 콜로이드), 크림 (연질 고체 또는 농후 액체), 및 연고 (연질의 기름진 제제), 및 고체 제제, 예컨대 국소 패치를 포함한다. 이에 따라, 관심 전달 비히클 성분은 수중유 (O/W) 및 유중수 (W/O) 유형의 에멀젼, 밀크 제제, 로션, 크림, 연고, 겔, 혈청, 분말, 마스크, 팩, 스프레이, 에어로졸, 스틱, 및 패치를 포함하나, 이에 제한되지는 않는다.
본원에 제공된 화합물 1의 고체 형태는 또한 경피 장치에 의해 투여될 수 있다. 따라서, 경피 투여는 저장소 또는 막 유형, 또는 접착제 매트릭스 또는 다른 매트릭스 종류의 패치를 사용하여 달성될 수 있다. 관심 전달 조성물은 액체 제제, 예컨대 로션 (스프레이 로션을 포함한, 외부 적용을 위해 의도된 현탁액 또는 에멀젼 형태의, 불용성 물질을 함유하는 액체) 및 수용액, 반고체 제제, 예컨대 겔 (분산 상이 분산 매질과 조합되어 반고체 물질, 예컨대 젤리를 생성하는 것인 콜로이드), 크림 (연질 고체 또는 농후 액체) 및 연고 (연질의 기름진 제제), 및 고체 제제, 예컨대 국소 패치를 포함한다. 이에 따라, 관심 전달 비히클 성분은 수중유 (O/W) 및 유중수 (W/O) 유형의 에멀젼, 밀크 제제, 로션, 크림, 연고, 겔, 세럼, 분말, 마스크, 팩, 스프레이, 에어로졸, 스틱, 및 패치를 포함하나, 이에 제한되지는 않는다. 경피 패치의 경우, 활성제 층이 1종 이상의 활성제를 포함하며, 이들 중 1종이 화합물 I이다. 특정 실시양태에서, 매트릭스는 접착제 매트릭스이다. 매트릭스는 중합체 물질을 포함할 수 있다. 접착제 매트릭스를 위한 적합한 중합체는 폴리우레탄, 아크릴레이트, 스티렌계 블록 공중합체, 실리콘 등을 포함하나, 이에 제한되지는 않는다. 예를 들어, 접착제 매트릭스는 아크릴레이트 중합체, 폴리실록산, 폴리이소부틸렌 (PIB), 폴리이소프렌, 폴리부타디엔, 스티렌계 블록 중합체, 그의 조합 등을 포함할 수 있으나, 이에 제한되지는 않는다. 접착제의 추가의 예는 그 개시내용이 본원에 참조로 포함되는 문헌 [Satas, "Acrylic Adhesives," Handbook of Pressure-Sensitive Adhesive Technology, 2nd ed., pp. 396-456 (D. Satas, ed.), Van Nostrand Reinhold, New York (1989)]에 기재되어 있다.
특정 실시양태에서, 활성제 층은 침투 증진제를 포함한다. 침투 증진제는 지방족 알콜, 예컨대 비제한적으로 12 내지 22개의 탄소 원자를 갖는 포화 또는 불포화 고급 알콜, 예컨대 올레일 알콜 및 라우릴 알콜; 지방산, 예컨대 비제한적으로 리놀산, 올레산, 리놀렌산, 스테아르산, 이소스테아르산 및 팔미트산; 지방산 에스테르, 예컨대 비제한적으로 이소프로필 미리스테이트, 디이소프로필 아디페이트, 및 이소프로필 팔미테이트; 알콜 아민, 예컨대 비제한적으로 트리에탄올아민, 트리에탄올아민 히드로클로라이드, 및 디이소프로판올아민; 다가 알콜 알킬 에테르, 예컨대 비제한적으로 다가 알콜 알킬 에테르 내의 알킬 기 모이어티의 탄소 원자의 수가 바람직하게는 6 내지 20개인 다가 알콜의 알킬 에테르 예컨대 글리세롤, 에틸렌 글리콜, 프로필렌 글리콜, 1,3-부틸렌 글리콜, 디글리세롤, 폴리글리세롤, 디에틸렌 글리콜, 폴리에틸렌 글리콜, 디프로필렌 글리콜, 폴리프로필렌 글리콜, 소르비탄, 소르비톨, 이소소르비드, 메틸 글루코시드, 올리고사카라이드, 및 환원 올리고사카라이드; 폴리옥시에틸렌 알킬 에테르, 예컨대 비제한적으로 알킬 기 모이어티의 탄소 원자의 수가 6 내지 20개이고 폴리옥시에틸렌 쇄의 반복 단위 (예를 들어 -OCH2CH2-)의 수가 1 내지 9개인 폴리옥시에틸렌 알킬 에테르, 예컨대 비제한적으로 폴리옥시에틸렌 라우릴 에테르, 폴리옥시에틸렌 세틸 에테르, 폴리옥시에틸렌 스테아릴 에테르, 및 폴리옥시에틸렌 올레일 에테르; 글리세리드 (즉, 글리세롤의 지방산 에스테르), 예컨대 비제한적으로 6 내지 18개의 탄소 원자를 갖는 지방산의 글리세롤 에스테르, 디글리세리드, 트리글리세리드 또는 그의 조합을 포함할 수 있으나, 이에 제한되지는 않는다. 일부 실시양태에서, 중합체 매트릭스는 폴리비닐피롤리돈을 포함한다. 조성물은 1종 이상의 충전제 또는 1종 이상의 산화방지제를 추가로 포함할 수 있다. 일부 실시양태에서, 기재된 경피 제제는 다층 구조를 가질 수 있다. 예를 들어, 경피 제제는 접착제 매트릭스 및 백킹을 가질 수 있다.
경구로 투여가능하거나, 주사가능하거나 또는 국소로 투여가능한 조성물을 위한 상기 기재된 성분은 단지 대표예이다. 다른 물질 뿐만 아니라 가공 기술 등은 본원에 참조로 포함되는 문헌 [Remington's Pharmaceutical Sciences, 17th edition, 1985, Mack Publishing Company, Easton, Pennsylvania]의 파트 8에 제시되어 있다.
또한, 본 발명의 화합물 1의 고체 형태는 지속 방출 형태로 투여되거나, 또는 지속 방출 약물 전달 시스템으로부터 투여될 수 있다. 대표적인 지속 방출 물질의 설명은 문헌 [Remington's Pharmaceutical Sciences]에서 찾아볼 수 있다.
사용 방법
장애, 예를 들어 CNS-관련 장애의 치료를 필요로 하는 대상체에게 유효량의 화학식 (I)의 화합물, 예를 들어 본원에 기재된 고체 형태로서의 화합물 1, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 상기 장애를 치료하는 방법이 본원에 제공된다. 특정 실시양태에서, 장애는 수면 장애, 기분 장애, 정신분열증 스펙트럼 장애, 경련성 장애, 기억 및/또는 인지 장애, 운동 장애, 인격 장애, 자폐증 스펙트럼 장애, 통증, 외상성 뇌 손상, 혈관 질환, 물질 남용 장애 및/또는 금단 증후군, 및 이명으로 이루어진 군으로부터 선택된 CNS-관련 장애이다. 일부 실시양태에서, 장애는 동반이환 장애 (예를 들어, 인격 장애가 동반이환된 우울증, 또는 인격 장애가 동반이환된 수면 장애)이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 신경계 장애이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 신경계 장애이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 정신 장애이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 발작 장애이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 신경염증성 장애이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 녹내장 또는 대사 장애이다. 일부 실시양태에서, 장애는 본원에 기재된 바와 같은 감각 결핍 장애이다. 화합물 1, 예를 들어 본원에 기재된 고체 형태로서의 화합물 1, 또는 그의 제약상 허용되는 염 또는 제약 조성물을 신경보호제로서 사용하는 방법이 또한 본원에 기재된다. 화합물 1, 예를 들어 본원에 기재된 고체 형태로서의 화합물 1, 또는 그의 제약상 허용되는 염 또는 제약 조성물을 진통제 또는 통증 조절을 위한 다른 작용제로서 사용하는 방법이 본원에 또한 제공된다.
신경계 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 본원에 기재된 장애 예컨대 신경계 장애의 치료에 사용될 수 있다. 예시적인 신경계 장애는 본원에 기재된 바와 같은 신경변성 장애, 신경발달 장애, 신경내분비 장애 및 기능장애, 운동 장애, 및 수면 장애를 포함하나, 이에 제한되지는 않는다.
신경변성 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 신경변성 장애의 치료에 사용될 수 있다.
용어 "신경변성 질환"은 뉴런의 구조 또는 기능의 진행성 손실, 또는 뉴런의 사멸과 연관된 질환 및 장애를 포함한다. 신경변성 질환 및 장애는 알츠하이머병 (경증, 중등도 또는 중증 인지 손상의 연관 증상 포함); 근위축성 측삭 경화증 (ALS); 무산소성 및 허혈성 손상; 양성 건망; 뇌 부종; 맥레오드 신경유극적혈구증가증 증후군 (MLS)을 포함한 소뇌 운동실조; 폐쇄성 두부 손상; 혼수; 좌상성 손상 (예를 들어, 척수 손상 및 두부 손상); 다발경색 치매 및 노인성 치매를 포함한 치매; 의식 장애; 다운 증후군; 유약 X 증후군; 질 드 라 투렛 증후군; 두부 외상; 청각 장애 및 상실; 헌팅톤병; 레녹스 증후군; 정신 지체; 안구 손상, 망막병증 또는 안구의 황반 변성을 포함한 뉴런 손상; 뇌졸중, 혈전색전성 졸중, 출혈성 졸중, 뇌 허혈, 뇌 혈관연축, 저혈당증, 기억상실, 저산소증, 무산소증, 주산기 질식 및 심장 정지 이후의 신경독성 손상; 파킨슨병; 졸중; 이명; 세관 경화증, 및 바이러스 감염 유발 신경변성 (예를 들어, 후천성 면역결핍 증후군 (AIDS) 및 뇌병증으로 인함)을 포함하나, 이에 제한되지는 않는다. 신경변성 질환은 또한 뇌졸중, 혈전색전성 졸중, 출혈성 졸중, 뇌 허혈, 뇌 혈관연축, 저혈당증, 기억상실, 저산소증, 무산소증, 주산기 질식 및 심장 정지 이후의 신경독성 손상을 포함하나, 이에 제한되지는 않는다. 신경변성 질환을 치료 또는 예방하는 방법은 신경변성 장애의 뉴런 기능 특징부의 손실을 치료 또는 예방하는 것을 또한 포함한다.
신경발달 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 본원에 기재된 장애 예컨대 신경발달 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 자폐증 스펙트럼 장애이다. 일부 실시양태에서, 신경발달 장애는 스미스-렘리-오피츠 증후군이다.
신경내분비 장애
신경내분비 장애 및 기능장애를 치료하기 위해 사용될 수 있는 방법이 본원에 제공된다. 본원에 사용된 "신경내분비 장애" 또는 "신경내분비 기능장애"는 뇌과 직접 관련된 신체의 호르몬 생산에서의 불균형으로 인한 다양한 상태를 지칭한다. 신경내분비 장애는 신경계와 내분비계 사이의 상호작용을 수반한다. 시상하부 및 뇌하수체는 호르몬의 생산을 조절하는 2개의 뇌 영역이기 때문에, 예를 들어 by 외상성 뇌 손상에 의한, 시상하부 또는 뇌하수체의 손상은 호르몬의 생산 및 뇌의 다른 신경내분비 기능에 영향을 미칠 수 있다. 일부 실시양태에서, 신경내분비 장애 또는 기능장애는 여성의 건강 장애 또는 상태 (예를 들어, 본원에 기재된 여성의 건강 장애 또는 상태)와 연관되어 있다. 일부 실시양태에서, 여성의 건강 장애 또는 상태와 연관된 신경내분비 장애 또는 기능장애는 다낭성 난소 증후군이다.
신경내분비 장애의 증상은, 행동, 정서 및 수면-관련 증상, 생식 기능과 관련된 증상, 및 피로, 부족한 기억력, 불안, 우울증, 체중 증가 또는 감소, 정서 불안정, 집중력 결여, 주의력 곤란, 리비도의 손실, 불임, 무월경, 근육 질량의 손실, 증가된 복부 체지방, 저혈압, 감소된 심박수, 탈모, 빈혈, 변비, 저온 불내성, 및 건성 피부를 포함하나, 이에 제한되지는 않는 체성 증상을 포함하나, 이에 제한되지는 않는다.
운동 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 운동 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 운동 장애는 본태성 진전, 강직-인간 증후군, 경직, 프리드리히 운동실조, 소뇌 운동실조, 이상긴장증, 투렛 증후군, 유약 X-연관 진전 또는 운동실조 증후군, 약물-유발 또는 의약-유발 파킨슨증 (예컨대 신경이완제-유발 급성 정좌불능, 급성 이상긴장증, 파킨슨증, 또는 지연성 이상운동증, 신경이완제 악성 증후군, 또는 의약-유발 체위성 진전), 운동실조,맥레오드 신경유극적혈구증가증 증후군 (MLS)을 포함한 소뇌 운동실조, 레보도파-유발 이상운동증, 무운동증 및 무운동성 (경직) 증후군을 포함한 운동 장애 (기저 신경절 석회화, 피질기저 변성, 다계통 위축, 파킨슨증-ALS 치매 복합증, 파킨슨병, 뇌염후 파킨슨증, 및 진행성 핵상 마비 포함); 무도병을 포함한, 근육 경직 또는 약화와 연관된 근육 연축 및 장애 (예컨대 양성 유전성 무도병, 약물-유발 무도병, 편측발리즘, 헌팅톤병, 신경유극적혈구증가증, 시데남 무도병, 및 증후성 무도병), 이상운동증 (틱 예컨대 복합 틱, 단순 틱, 및 증후성 틱 포함), 근간대성경련 (전신 근간대성경련 및 국소 근간대성경련 포함), 진전 (예컨대 안정시 진전, 체위성 진전, 및 의도 진전), 또는 이상긴장증 (축성 이상긴장증, 이상긴장성 서경, 편마비성 이상긴장증, 발작성 이상긴장증, 및 초점성 이상긴장증 예컨대 안검연축, 구강하악 이상긴장증, 및 연축성 발성장애 및 사경 포함)이다.
본원에 사용된 "운동 장애"는 과다운동성 운동 장애 및 관련 근육 제어 이상과 연관된 다양한 질환 및 장애를 지칭한다. 예시적인 운동 장애는 파킨슨병 및 파킨슨증 (특히 운동완만에 의해 규정됨), 이상긴장증, 무도병 및 헌팅톤병, 운동실조, 진전 (예를 들어, 본태성 진전), 근간대성경련 및 놀람, 틱 및 투렛 증후군, 하지 불안 증후군, 강직 인간 증후군, 및 보행 장애를 포함하나, 이에 제한되지는 않는다. 예시적인 운동 장애는 파킨슨병 및 파킨슨증 (특히 운동완만에 의해 규정됨), 이상긴장증, 무도병 및 헌팅톤병, 운동실조, 진전 (예를 들어, 본태성 진전), 근간대성경련 및 놀람, 틱 및 투렛 증후군, 하지 불안 증후군, 강직 인간 증후군, 및 보행 장애를 포함하나, 이에 제한되지는 않는다.
진전
본원에 기재된 방법은 진전을 치료하기 위해 사용될 수 있으며, 예를 들어 화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은 소뇌 진전 또는 의도 진전, 이상긴장성 진전, 본태성 진전, 기립성 진전, 파킨슨병 진전, 생리학적 진전, 심인성 진전, 또는 적색핵 진전을 치료하기 위해 사용될 수 있다. 진전은 유전성, 퇴행성 및 특발성 장애 예컨대 윌슨병, 파킨슨병, 및 본태성 진전 각각; 대사 질환 (예를 들어, 갑상선-부갑상선-, 간 질환 및 저혈당증); 말초 신경병증 (샤르코-마리-치아, 루시-레비, 당뇨병, 복합 부위 통증 증후군과 연관됨); 독소 (니코틴, 수은, 납, CO, 망가니즈, 비소, 톨루엔); 약물-유발 수면발작 (트리시클릭, 리튬, 코카인, 알콜, 아드레날린, 기관지확장제, 테오필린, 카페인, 스테로이드, 발프로에이트, 아미오다론, 갑상선 호르몬, 빈크리스틴); 및 심인성 장애를 포함한다. 임상적 진전은 생리학적 진전, 증진된 생리학적 진전, 본태성 진전 증후군 (전형적 본태성 진전, 원발성 기립성 진전, 및 과제- 및 위치-특이적 진전 포함), 이상긴장성 진전, 파킨슨병 진전, 소뇌 진전, 홈즈 진전 (즉, 적색핵 진전), 구개 진전, 신경병증성 진전, 독성 또는 약물-유발 진전, 및 심인성 진전으로 분류될 수 있다.
진전은 1개 이상의 신체 부분 (예를 들어, 손, 팔, 눈, 얼굴, 머리, 성대 주름, 몸통, 다리)의 진동 또는 비틀림을 수반할 수 있는, 비자발적이며 때로는 리듬성인 근육 수축 및 이완이다.
소뇌 진전 또는 의도 진전은 의도적인 운동 후에 발생하는 사지의 느린 광범위한 진전이다. 소뇌 진전은, 예를 들어 종양, 졸중, 질환 (예를 들어, 다발성 경화증, 유전성 퇴행성 장애)으로 인한 소뇌 내의 병변 또는 소뇌에 대한 손상에 의해 유발된다.
이상긴장성 진전은, 지속적인 불수의근 수축이 비틀림 및 반복적인 움직임 및/또는 통증성 및 비정상적 자세 또는 위치를 유발하는 운동 장애인 이상긴장증에 이환된 개체에서 발생한다. 이상긴장성 진전은 신체 내의 임의의 근육에 영향을 미칠 수 있다. 이상긴장성 진전은 불규칙적으로 발생하며, 종종 완전한 휴식에 의해 완화될 수 있다.
본태성 진전 또는 양성 본태성 진전은 진전의 가장 흔한 유형이다. 본태성 진전은 일부에서는 경증이고 비진행성일 수 있으며, 신체의 한 측면에서 시작하지만 3년 내에 양 측면에 영향을 미쳐 천천히 진행될 수 있다. 손은 가장 종종 영향을 받지만, 머리, 음성, 혀, 다리 및 몸통이 또한 수반될 수 있다. 사람이 노화함에 따라, 진전 빈도가 감소될 수 있지만, 중증도가 증가될 수 있다. 고조된 감정, 스트레스, 열, 신체적 탈진, 또는 저혈당은 진전을 촉발하고/거나 그의 중증도를 증가시킬 수 있다. 증상은 일반적으로 시간 경과에 따라 진화하며, 발병 후 가시적이면서도 지속성일 수 있다.
기립성 진전은 기립 직후에 다리 및 몸통에서 발생하는 빠른 (예를 들어, 12 Hz 초과) 리듬성인 근육 수축을 특징으로 한다. 넓적다리 및 다리에서 경련이 느껴지며, 환자는 한 지점에서 기립하도록 요청된 경우에 제어불가능하게 흔들릴 수 있다. 기립성 진전은 본태성 진전을 갖는 환자에서 발생할 수 있다.
파킨슨병 진전은 운동을 제어하는 뇌 내의 구조에 대한 손상에 의해 유발된다. 파킨슨병 진전은 종종 파킨슨병의 전조이며, 전형적으로 턱, 입술, 다리 및 몸통에도 영향을 미칠 수 있는 손의 "환약말이(pill-rolling)" 행동으로 나타난다. 파킨슨병 진전의 발병은 전형적으로 60세 이후에 시작된다. 운동은 한쪽 사지 또는 신체의 한 측면에서 시작되고, 다른 측면을 포함하도록 진행될 수 있다.
생리학적 진전은 정상 개체에서 발생할 수 있고, 임상 유의성을 갖지 않을 수 있다. 이는 모든 수의근 군에서 나타날 수 있다. 생리학적 진전은 특정 약물, 알콜 금단, 또는 과다활동 갑상선 및 저혈당증을 포함한 의학적 상태에 의해 유발될 수 있다. 진전은 통상적으로 약 10 Hz의 진동수를 갖는다.
심인성 진전 또는 히스테리성 진전은 휴식 시에 또는 자세 또는 동적 운동 도중에 발생할 수 있다. 심인성 진전을 갖는 환자는 전환 장애 또는 또 다른 정신 질환을 가질 수 있다.
적색핵 진전은 휴식 시에, 자세에서, 및 의도적으로 존재할 수 있는 거칠고 느린 진전을 특징으로 한다. 진전은 중뇌에서의 적핵에 영향을 미치는 상태, 전형적 비통상적 졸중과 연관되어 있다.
파킨슨병은 도파민을 생산하는 뇌 내의 신경 세포에 영향을 미친다. 증상은 근육 강직성, 진전, 및 언어 및 보행의 변화를 포함한다. 파킨슨증은 진전, 운동완만, 강직성, 및 자세 불안정성을 특징으로 한다. 파킨슨증은 파킨슨병에서 발견되는 증상들을 공유하지만, 진행성 신경변성 질환이 아니라 증상 복합체이다.
이상긴장증은, 비정상적이며 종종 반복적인 운동 또는 자세를 유발하는 지속적 또는 간헐적 근육 수축을 특징으로 하는 운동 장애이다. 이상긴장성 운동은 패턴화된 비틀림일 수 있으며, 진전성일 수 있다. 이상긴장증은 종종 자발적 행동에 의해 개시 또는 악화되며, 오버플로우 근육 활성화와 연관되어 있다.
무도병은 전형적으로 어깨, 둔부 및 얼굴에 영향을 미치는 갑작스러운 불수의 운동을 특징으로 하는 신경계 장애이다. 헌팅톤병은 뇌 내의 신경 세포가 소모되도록 하는 유전성 질환이다. 증상은 비제어된 운동, 둔함(clumsiness), 및 균형 문제를 포함한다. 헌팅톤병은 걷기, 말하기 및 삼키기를 방해할 수 있다.
운동실조는 신체 운동의 완전한 제어가 상실되는 것을 지칭하고, 손가락, 손, 팔, 다리, 신체, 언어, 및 안구 운동에 영향을 미칠 수 있다.
근간대성경련 및 놀람은, 음향, 촉각, 시각 또는 전정 자극일 수 있는 돌발적인 예상외의 자극에 대한 반응이다.
틱은 통상적으로 돌발적으로 발병되고 짧고 반복적이지만 비-리듬성인 불수의 운동이며, 전형적으로 정상 행동을 모방하고, 종종 정상 활성의 배경으로부터 발생한다. 틱은 운동 또는 음성 틱으로서 분류될 수 있으며, 운동 틱은 운동과 연관되어 있고, 음성 틱은 소리와 연관되어 있다. 틱은 단순 또는 복합으로 특징화될 수 있다. 예를 들어, 단순 운동 틱은 특정한 신체 부분에 한정된 몇 개의 근육만을 수반한다.
투렛 증후군은 다수의 운동 틱 및 적어도 1종의 음성 틱을 특징으로 하는, 소아기에 발병되는 유전성 신경정신 장애이다.
하지 불안 증후군은 휴식 시에 다리를 움직이고자 하는 압도적인 충동을 특징으로 하는 신경계 감각운동 장애이다.
강직 인간 증후군은 통상적으로 하배부 및 하지에 수반되는 근육의 불수의 통증성 연축 및 강직성을 특징으로 하는 진행성 운동 장애이다. 과도한 요추 과전만을 동반하는 강직-하지 보행이 전형적으로 발생한다. 척추주위 축 근육의 연속 운동 단위 활성을 갖는 EMG 기록 상의 특징적인 이상이 전형적으로 관찰된다. 변이체는, 전형적으로 원위 다리 및 발에 영향을 미치는 초점성 강직을 유발하는 "강직-사지 증후군"을 포함한다.
보행 장애는 신경근육, 관절염성, 또는 다른 신체 변화로부터 유발되는 걷는 방식 또는 스타일에서의 이상을 지칭한다. 보행은 비정상적 이동의 원인이 되는 계에 따라 분류되며, 편마비성 보행, 양마비성 보행, 신경병증성 보행, 근병증성 보행, 파킨슨병 보행, 무도병형 보행, 운동실조성 보행, 및 감각 보행을 포함한다.
수면 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 수면 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 수면 장애는 또 다른 장애와 동반이환된다 (예를 들어, 인격 장애가 동반이환된 수면 장애).
정신 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 본원에 기재된 장애 예컨대 정신 장애의 치료에 사용될 수 있다. 예시적인 정신 장애는 본원에 기재된 바와 같은 기분 장애, 불안 장애, 정신병적 장애, 및 충동 조절 장애를 포함하나, 이에 제한되지는 않는다.
기분 장애
기분 장애, 예를 들어 임상 우울증, 산후 우울증 또는 산후 우울증, 주산기 우울증, 비정형 우울증, 멜랑콜리성 우울증, 정신병적 주요 우울증, 긴장성 우울증, 계절성 정동 장애, 기분저하증, 이중 우울증, 우울성 인격 장애, 재발성 단기 우울증, 경도 우울 장애, 양극성 장애 또는 조울 장애, 만성 의학적 상태로 인한 우울증, 동반이환 우울증, 치료-저항성 우울증, 불응성 우울증, 자살경향성, 자살 관념, 또는 자살 행동을 치료하는 방법이 본원에 또한 제공된다. 일부 실시양태에서, 본원에 기재된 방법은 우울증 (예를 들어, 중등도 또는 중증 우울증)을 앓고 있는 대상체에 대해 치료 효과를 제공한다. 일부 실시양태에서, 기분 장애는 본원에 기재된 질환 또는 장애 (예를 들어, 신경내분비 질환 및 장애, 신경변성 질환 및 장애 (예를 들어, 간질), 운동 장애, 진전 (예를 들어, 파킨슨병), 여성의 건강 장애 또는 상태)와 연관되어 있다.
임상 우울증은 주요 우울증, 주요 우울 장애 (MDD), 중증 우울증, 단극성 우울증, 단극성 장애, 및 재발성 우울증으로도 공지되어 있으며, 낮은 자존감 및 일상적인 즐거운 활동에 대한 흥미 또는 기쁨의 상실을 동반하는, 전반적이고 지속적인 저조한 기분을 특징으로 하는 정신 장애를 지칭한다. 임상 우울증을 갖는 일부 사람들은 수면 곤란, 체중 감소, 및 일반적으로 흥분되고 과민한 느낌을 갖는다. 임상 우울증은 개체가 느끼고 생각하고 행동하는 방식에 영향을 미치며, 다양한 정서적 및 신체적 문제를 초래할 수 있다. 임상 우울증을 갖는 개체는 일상 활동을 하기에 곤란할 수 있으며, 개체가 삶을 더 이상 살아갈 가치가 없는 것으로 느끼도록 할 수 있다.
분만전후 우울증은 임신 중의 우울증을 지칭한다. 증상은 과민성, 울음, 안절부절한 느낌, 수면 곤란, 극단적인 소진 (정서적 및/또는 신체적), 식욕 변화, 집중 곤란, 증가된 불안 및/또는 걱정, 아기 및/또는 태아로부터 단절된 느낌, 및/또는 이전의 즐거운 활동에 대한 관심 상실을 포함한다.
산후 우울증 (PND)은 산후 우울증 (PPD)으로도 지칭되며, 출산 후 여성에게 이환되는 임상 우울증의 유형을 지칭한다. 증상은 슬픔, 피로, 수면 및 식사 습관의 변화, 감소된 성욕, 울음 삽화, 불안, 및 과민성을 포함할 수 있다. 일부 실시양태에서, PND는 치료-저항성 우울증 (예를 들어, 본원에 기재된 바와 같은 치료-저항성 우울증)이다. 일부 실시양태에서, PND는 불응성 우울증 (예를 들어, 본원에 기재된 바와 같은 불응성 우울증)이다.
일부 실시양태에서, PND를 갖는 대상체는 임신 동안 우울증 또는 우울증의 증상을 또한 경험하였다. 이러한 우울증은 본원에서 주산기 우울증으로 지칭된다. 한 실시양태에서, 주산기 우울증을 경험한 대상체는 PND를 경험할 위험이 증가된다.
비정형 우울증 (AD)은 기분 반응성 (예를 들어, 역설적 무쾌감증) 및 긍정성, 유의한 체중 증가 또는 증가된 식욕을 특징으로 한다. AD를 앓고 있는 환자는 과도한 수면 또는 졸림 (과다수면), 사지가 무거운 감각, 및 지각된 대인관계 거부에 대한 과민성의 결과로서의 유의한 사회적 장애를 또한 가질 수 있다.
멜랑콜리성 우울증은 대부분의 또는 모든 활동에서의 기쁨의 상실 (무쾌감증), 즐거운 자극에 반응하는 것에 대한 실패, 슬픔 또는 상실감보다 더 현저한 우울한 기분, 과도한 체중 감소, 또는 과도한 죄책감을 특징으로 한다.
정신병적 주요 우울증 (PMD) 또는 정신병적 우울증은 개체가 정신병적 증상 예컨대 망상 및 환각을 경험하는, 특히 멜랑콜리성 성질의 주요 우울 삽화를 지칭한다.
긴장성 우울증은 운동 행동 장애 및 다른 증상을 수반하는 주요 우울증을 지칭한다. 개체는 묵음 및 혼미상태가 될 수 있으며, 부동성이거나, 또는 목적없는 또는 기이한 운동을 나타낸다.
계절성 정동 장애 (SAD)는 개체가 가을 또는 겨울에 오는 우울 삽화의 계절성 패턴을 갖는 계절성 우울증의 유형을 지칭한다.
기분저하증은 동일한 실체적 및 인지 문제가 명백한 단극성 우울증과 관련된 상태를 지칭한다. 이들은 중증이 아니며, 더 장기간 (예를 들어, 적어도 2년) 지속되는 경향이 있다.
이중 우울증은 적어도 2년 동안 지속되고 주요 우울증의 기간이 간간이 끼어드는 매우 우울한 기분 (기분저하증)을 지칭한다.
우울성 인격 장애 (DPD)는 우울 양상을 갖는 인격 장애를 지칭한다.
재발성 단기 우울증 (RBD)은, 개체가 1개월에 약 1회의 우울 삽화를 가지며 각각의 삽화가 2주 이하, 전형적으로 2-3일 미만 지속되는 것인 상태를 지칭한다.
경도 우울 장애 또는 경도 우울증은 적어도 2종의 증상이 2주 동안 존재하는 우울증을 지칭한다.
만성 의학적 상태로 인한 우울증은 만성 의학적 상태 예컨대 암 또는 만성 통증, 화학요법, 만성 스트레스으로 인한 우울증을 지칭한다.
치료-저항성 우울증은 개체가 우울증에 대해 치료받았으나 증상이 개선되지 않은 상태를 지칭한다. 예를 들어, 치료-저항성 우울증을 갖는 개체의 경우에는 항우울제 또는 심리 상담 (정신요법)이 우울증 증상을 경감시키지 못한다. 일부 경우에, 치료-저항성 우울증을 갖는 개체에서는 증상이 개선되더라도 복귀된다. 불응성 우울증은 삼환계 항우울제, MAOI, SSRI, 및 이중 및 삼중 흡수 억제제 및/또는 불안완화제 약물을 포함한 표준 약리학적 치료, 뿐만 아니라 비-약리학적 치료 (예를 들어, 정신요법, 전기경련 요법, 미주 신경 자극 및/또는 경두개 자기 자극)에 대해 저항성인 우울증을 앓고 있는 환자에서 발생한다.
수술후 우울증은 외과적 절차 이후의 우울증의 느낌 (예를 들어, 누군가의 사망을 직면한 결과로서)을 지칭한다. 예를 들어, 개체는 슬픔 또는 지속적으로 공허한 기분, 통상적으로 즐거운 취미 및 활동에 대한 기쁨 또는 흥미의 상실, 또는 무가치 또는 절망의 지속적인 감정을 느낄 수 있다.
여성 건강의 상태 또는 장애와 연관된 기분 장애는 여성 건강의 상태 또는 장애 (예를 들어, 본원에 기재된 바와 같음)와 연관된 (예를 들어, 그로부터 유발된) 기분 장애 (예를 들어, 우울증)를 지칭한다.
자살경향성, 자살 관념, 자살 행동은 개체가 자살하는 경향을 지칭한다. 자살 관념은 자살에 대한 생각 또는 비통상적인 집착에 관한 것이다. 자살 관념의 범위는 매우 넓으며, 예를 들어 잠깐의 생각에서부터, 상세한 계획, 역할 수행, 불완전한 시도에 이른다. 증상은 자살에 대해 말하는 것, 사회적 접촉으로부터 회피하는 것, 죽음에 대해 집착하는 것, 특정 상황에 대해 갇혀있거나 희망없는 것으로 느끼는 것, 알콜 또는 약물의 사용이 증가하는 것, 위험하거나 자기-파괴적인 일들을 행하는 것, 사람들에게 다시 보지 못할 것처럼 작별을 고하는 것을 포함한다.
우울증 또는 인격 장애에는 또한 또 다른 장애가 동반이환될 수 있다. 예를 들어, 우울증에는 인격 장애가 동반이환될 수 있다. 또 다른 예에서, 인격 장애에는 수면 장애가 동반이환될 수 있다.
우울증의 증상은 지속적인 불안 또는 슬픈 느낌, 무력감, 절망, 비관, 무가치, 낮은 활력, 안절부절, 수면 곤란, 불면, 과민성, 피로, 운동 문제, 즐거운 활동 또는 취미에 대한 흥미의 상실, 집중력 상실, 활력 상실, 부족한 자존감, 긍정적 생각 또는 계획의 부재, 과도한 수면, 과식, 식욕 상실, 불면증, 자해, 자살 생각, 및 자살 시도를 포함한다. 증상의 존재, 중증도, 빈도 및 지속기간은 사례별로 달라질 수 있다. 우울증의 증상 및 그의 완화는 의사 또는 심리학자에 의해 (예를 들어, 정신 상태 검사에 의해) 확인될 수 있다.
불안 장애
불안 장애 (예를 들어, 범불안 장애, 공황 장애, 강박 장애, 공포증, 외상후 스트레스 장애)를 치료하는 방법이 본원에 제공된다. 불안 장애는 비정상적 및 병리학적 공포 및 불안의 여러 다양한 형태를 포괄하는 포괄적 용어이다. 현재의 정신과 진단 기준은 매우 다양한 불안 장애를 인식하고 있다.
범불안 장애는 어느 하나의 대상 또는 상황에 집중하지 못하는 장기-지속성 불안을 특징으로 하는 흔한 만성 장애이다. 범불안을 앓고 있는 환자는 비-특이적 지속적 공포 및 걱정을 경험하며, 일상 사항을 지나치게 걱정하게 된다. 범불안 장애는 노인에게 이환되는 가장 흔한 불안 장애이다.
공황 장애에서, 사람은 종종 진전, 동요, 혼동, 어지럼증, 오심, 호흡 곤란에 의해 나타나는 강한 두려움 및 염려의 짧은 발작으로 고생한다. 갑자기 발생하고 10분 미만 내에 절정에 이르는 공포 또는 불쾌감으로서 APA에 의해 정의되는 이들 공황 발작은 수시간 동안 지속될 수 있고, 스트레스, 공포 또는 심지어 운동에 의해 촉발될 수 있으며; 구체적 원인이 항상 분명하지는 않다. 재발성인 예상외의 공황 발작 이외에도, 공황 장애의 진단은 또한 상기 발작이 만성 결과: 발작의 잠재적 연관성에 대한 걱정, 미래의 발작에 대항 지속적인 공포, 또는 발작과 관련된 행동에서의 유의한 변화를 갖는 것을 필요로 한다. 따라서, 공황 장애를 앓고 있는 사람은 특정한 공황 삽화를 훨씬 벗어난 증상을 경험한다. 종종, 심박동의 정상적인 변화가 공황 환자에 의해 인지되어, 상기 환자가 그의 심장에 문제가 있다고 생각하게 하거나 또는 또 다른 공황 발작을 가질 것이라고 생각하게 한다. 일부 경우에, 신체 기능에 대한 높아진 인식 (과다각성)이 공황 발작 동안 발생하며, 여기서 임의의 지각되는 생리학적 변화는 가능한 생명 위협 질병 (즉, 극단적인 심기증)으로서 해석된다.
강박 장애는 주로 반복적 강박사고 (고통적, 지속적 및 침투적 사고 또는 이미지) 및 강박행위 (특정 행동 또는 의식을 수행하려는 욕구)를 특징으로 하는 불안 장애의 유형이다. OCD 사고 패턴은, 실제로는 존재하지 않는 인과적 관계에서의 신념을 수반하는 한, 미신에 비유될 수 있다. 종종, 과정은 전적으로 비논리적이며; 예를 들어, 임박한 피해에 대한 강박사고를 완화시키기 위해 특정 패턴으로 걷는 강박행위가 사용될 수 있다. 또한 다수의 경우에, 강박행위는 전적으로 설명불가능하며, 단순하게는 신경과민에 의해 촉발되는 의식을 완성시키려는 욕구이다. 소수의 경우에, OCD 환자는 어떠한 명백한 강박행위 없이 강박사고만을 경험할 수도 있으며; 훨씬 더 적은 수의 환자는 단지 강박행위만을 경험한다.
불안 장애의 가장 큰 단일 카테고리는 특정한 자극 또는 상황에 의해 공포 및 불안이 촉발되는 모든 경우를 포함한 공포증 카테고리이다. 환자는 전형적으로 동물에서부터 장소 내지는 체액에 이르는 임의의 것일 수 있는 그의 두려움의 대상을 대면하는 것으로부터의 괴로운 결과를 예상한다.
외상후 스트레스 장애 또는 PTSD는 외상 경험으로부터 발생하는 불안 장애이다. 외상후 스트레스는 극단적인 상황, 예컨대 싸움, 강간, 인질극 상황, 또는 심지어 중대 사고로부터 유발될 수 있다. 이는 또한 중증 스트레스원에 대한 장기간 (만성) 노출로부터 발생할 수 있으며, 예를 들어 개별 전투는 견뎌내지만 연속적인 싸움에 대응할 수 없는 군인이 그러하다. 공통 증상은 플래쉬백, 회피성 행동 및 우울증을 포함한다.
정신병적 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 정신병적 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 충동 조절 장애는 정신분열증 또는 양극성 장애이다. 일부 실시양태에서, 정신병적 장애는 정신분열증이다. 일부 실시양태에서, 정신병적 장애는 양극성 장애이다.
양극성 장애 또는 조울 장애는 감정의 고조 (조증 또는 경조증) 및 저조 (우울증)를 포함한 극단적인 기분 동요를 유발한다.
충동 조절 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 충동 조절 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 충동 조절 장애는 신경성 식욕부진 또는 알콜 금단이다. 일부 실시양태에서, 충동 조절 장애는 신경성 식욕부진이다. 일부 실시양태에서, 충동 조절 장애는 신경성 식욕부진이다.
발작 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 발작 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 발작 장애는 간질이다. 일부 실시양태에서, 발작 장애는 간질 지속상태, 예를 들어 경련성 간질 지속상태, 예를 들어 초기 간질 지속상태, 확립된 간질 지속상태, 불응성 간질 지속상태, 또는 초-불응성 간질지속 상태이다. 일부 실시양태에서, 발작 장애는 운동 (자동증, 무긴장성, 간대성, 간질성 연축, 과다운동성, 근간대성, 및 긴장성) 또는 비-운동 (자율, 행동 정지, 인지, 정서적, 및 감각적) 개시를 갖는 초점성 발작, 운동 (긴장성-간대성, 간대성, 근간대성, 근간대성-긴장성-간대성, 근간대성-무긴장성, 무긴장성, 간질성 연축) 또는 비-운동 (결신) 개시를 갖는 전신 발작, 미지의 운동 (긴장성-간대성, 간질성 연축) 또는 비-운동 (행동 정지) 개시를 갖는 발작, 임상 증후군, 예컨대 드라베 증후군, 레트 증후군, 레녹스 가스토 증후군, 결절성 경화증, 안젤만 증후군, 월경성 간질과 연관된 발작이다. 일부 실시양태에서, 발작 장애는, 분열정동 장애로 인한 또는 정신분열증 치료에 사용된 약물로 인한 발작이다.
간질
간질은 시간 경과에 따라 반복되는 발작을 특징으로 하는 뇌 장애이다. 간질의 유형은 전신 간질, 예를 들어 소아기 결신 간질, 소아 근간대성 간질, 각성시 대발작을 갖는 간질, 웨스트 증후군, 레녹스-가스토 증후군, 부분 간질, 예를 들어 측두엽 간질, 전두엽 간질, 소아기의 양성 초점성 간질을 포함할 수 있으나 이에 제한되지는 않는다.
간질 지속상태 (SE)
간질 지속상태 (SE)는 예를 들어 경련성 간질 지속상태, 예를 들어 초기 간질 지속상태, 확립된 간질 지속상태, 불응성 간질 지속상태, 또는 초-불응성 간질지속 상태; 비-경련성 간질 지속상태, 예를 들어 전신 간질지속 상태, 복합 부분 간질지속 상태; 전신 주기성 간질양 뇌파; 및 주기성 편측 간질양 뇌파를 포함할 수 있다. 경련성 간질 지속상태는 경련성 간질성 발작 지속상태의 존재를 특징으로 하며, 초기 간질 지속상태, 확립된 간질 지속상태, 불응성 간질 지속상태, 초-불응성 간질 지속상태를 포함할 수 있다. 초기 간질 지속상태는 1차 요법으로 치료된다. 확립된 간질 지속상태는 1차 요법으로의 치료에도 불구하고 지속되는 간질성 발작 지속상태를 특징으로 하며, 2차 요법이 투여된다. 불응성 간질 지속상태는 1차 및 2차 요법으로의 치료에도 불구하고 지속되는 간질성 발작 지속상태를 특징으로 하며, 전신 마취제가 일반적으로 투여된다. 초불응성 간질 지속상태는 1차 요법, 2차 요법 및 24시간 이상 동안의 전신 마취제로의 치료에도 불구하고 지속되는 간질성 발작 지속상태를 특징으로 한다.
비-경련성 간질 지속상태는, 예를 들어 초점성 비-경련성 간질 지속상태, 예를 들어 복합 부분 비-경련성 간질 지속상태, 단순 부분 비-경련성 간질 지속상태, 비정형적 비-경련성 간질 지속상태; 전신 비-경련성 간질 지속상태, 예를 들어 후기 발병 결신 비-경련성 간질 지속상태, 비정형 결신 비-경련성 간질 지속상태, 또는 정형 결신 비-경련성 간질 지속상태를 포함할 수 있다.
발작
발작은 뇌에서의 비정상적 전기 활성의 삽화 후에 발생하는 신체적 소견 또는 행동 변화이다. 용어 "발작"은 종종 "경련"과 상호교환가능하게 사용된다. 경련은 사람의 신체가 급격하고 제어불가능하게 흔들리는 경우이다. 경련 동안, 사람의 근육은 반복적으로 수축 및 이완된다.
행동 및 뇌 활성의 유형에 기초하여, 발작은 2종의 넓은 카테고리: 전신 및 부분 (국부 또는 초점성으로도 칭함)으로 나누어진다. 발작의 유형을 분류하는 것은 환자가 간질에 걸렸는지의 여부를 의사가 진단하는 것을 돕는다.
전신 발작은 전체 뇌 전반에 걸쳐 전기 임펄스에 의해 유발되는 반면에, 부분 발작은 뇌의 상대적으로 작은 부분에서의 전기 임펄스에 의해 (적어도 초기에) 유발된다. 발작을 생성하는 뇌의 부분은 때때로 초점으로 칭해진다.
전신 발작의 6종의 유형이 존재한다. 가장 흔하고 현저하며 따라서 가장 널리 공지된 것은 대발작으로도 칭하는 전신 경련이다. 이러한 유형의 발작에서, 환자는 의식을 상실하고 통상적으로 쓰러진다. 의식 상실에 이어서, 30 내지 60초 동안의 전신 강직 (발작의 "긴장" 기로 칭함), 이어서 30 내지 60초 동안의 격렬한 떨림 ("간대" 기)이 후속하며, 그 후 환자는 깊은 잠에 빠진다 ("발작후" 또는 발작-후 기). 대발작 동안, 상해 및 사고, 예컨대 교설벽 및 요실금이 발생할 수 있다.
결신 발작은 증상이 거의 또는 전혀 없는 단기 의식 상실 (단지 몇 초)을 유발한다. 환자, 매우 종종 아동은 전형적으로 활동을 중단하고 멍하게 응시한다. 이들 발작은 갑자기 시작 및 종료되며, 1일 수회 발생할 수 있다. 환자는 "놓친 시간"을 인지할 수 있는 것을 제외하고는, 통상적으로 발작이 있었음을 인지하지 못한다.
근간대성 발작은 통상적으로 신체의 양 측면 상의 산발성 떨림으로 이루어진다. 환자는 때때로 떨림을 단기 전기 충격으로도 설명한다. 격렬한 경우, 이들 발작은 물체를 떨어뜨리거나 또는 불수의적으로 던지는 것을 유발할 수 있다.
간대성 발작은 신체의 양 측면을 동시에 수반하는 반복적인 리듬성 떨림이다.
긴장성 발작은 근육 강직을 특징으로 한다.
무긴장성 발작은, 특히 팔 및 다리에서의 근긴장도의 돌발적이고 전반적인 상실로 이루어지며, 이는 종종 넘어짐을 유발한다.
본원에 기재된 발작은 간질성 발작; 급성 반복 발작; 군발성 발작; 연속 발작; 지속 발작; 장기 발작; 재발성 발작; 간질 지속상태 발작, 예를 들어 불응성 경련성 간질 지속상태, 비-경련성 간질 지속상태 발작; 불응성 발작; 근간대성 발작; 긴장성 발작; 긴장성-간대성 발작; 단순 부분 발작; 복합 부분 발작; 속발성 전신 발작; 비정형 결신 발작; 결신 발작; 무긴장성 발작; 양성 롤란딕 발작; 열성 발작; 정서적 발작; 초점성 발작; 홍소 발작; 전신 개시 발작; 영아 연축; 잭슨 발작; 괌범성 양측성 근간대성경련 발작; 다초점성 발작; 신생아 발병 발작; 야간 발작; 후두엽 발작; 외상후 발작; 비정형적 발작; 실반 발작; 시각 반사 발작; 또는 금단 발작을 포함할 수 있다. 일부 실시양태에서, 발작은 드라베 증후군, 레녹스-가스토 증후군, 결절성 경화증 복합증, 레트 증후군 또는 PCDH19 여성 소아 간질과 연관된 전신 발작이다.
신경염증성 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 본원에 기재된 장애 예컨대 신경염증성 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 신경염증성 장애는 다발성 경화증, 또는 스트렙토코쿠스 감염과 연관된 소아 자가면역 신경정신 장애 (PANDAS)이다.
무통각/통증 조절
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 예를 들어 진통제 또는 통증 조절을 위한 다른 작용제로서 본원에 기재된 방법에 사용될 수 있다. 일부 실시양태에서, 화합물 1의 고체 형태 또는 그의 제약상 허용되는 조성물은 염증성 통증, 신경병증성 통증, 섬유근육통, 또는 말초 신경병증을 치료하기 위해 진통제 또는 통증 조절을 위한 다른 작용제로서 사용될 수 있다.
감각 결핍 장애
화학식 (I)의 화합물, 예를 들어 화합물 1의 고체 형태, 또는 그의 제약상 허용되는 염 또는 제약상 허용되는 조성물은, 본원에 기재된 방법, 예를 들어 본원에 기재된 장애 예컨대 감각 결핍 장애의 치료에 사용될 수 있다. 일부 실시양태에서, 감각 결핍 장애는 이명 또는 공감각이다. 일부 실시양태에서, 감각 결핍 장애는 청각 장애 및/또는 상실이다.
실시예
본원에 기재된 본 발명이 더 완전히 이해될 수 있도록 하기 위해, 하기 실시예가 제시되어 있다. 본 출원에 기재된 실시예는 본원에 제공된 결정질 고체 형태를 설명하기 위해 제공되며, 어떠한 방식으로도 그의 범주를 제한하는 것으로 해석되어서는 안 된다.
실시예 1. 고체 형태 A의 제조.
형태 A는 조 화합물 1을 에틸 아세테이트 중 슬러리로서 10℃ 미만에서 교반한 다음, 여과하고, 진공 하에 건조시킴으로써 제조되었다. 이는 또한, 조 화합물 1을 디클로로메탄 중에 용해시킨 다음, 진공 하에 에틸 아세테이트로 2회 재농축 건조시킴으로써 형성되었다.
실시예 2. 본 발명의 다른 고체 형태를 수득하기 위한 결정화의 다양한 습식 방법.
새로운 결정질 형태를 찾기 위해, 다양한 결정화 방법이 형태 A를 출발 물질로서 사용하여 평가되었다. 형태 A 이외에도, 13종의 결정질 형태 (B, C, D, E, F, H, I, J, K, L, M, N 및 O)가 이들 방법을 사용하여 확인되었다.
저속 증발
저속 증발 결정화 실험을 8종의 상이한 용매 시스템에 걸쳐 수행하였다. 각각의 실험에서, 형태 A 대략 10 mg을 1.5 mL 유리 바이알 내에서 용매 0.4 내지 1.0 mL 중에 용해시켰다. 유리 바이알을, 용매 증발을 가능하게 하기 위해 3 내지 5개의 구멍이 천공된 파라필름(Parafilm)®을 사용하여 밀봉하였다.
슬러리 전환
각각의 실험에서, 형태 A 대략 10 내지 20 mg을 용매 또는 용매 혼합물 0.5 mL 중에 현탁시켰다. 실온 또는 50℃에서 48시간 동안 교반한 후, 고체를 분석을 위해 원심분리에 의해 단리하였다 (습윤 샘플). 현탁액이 투명한 용액으로 변하면, 투명한 용액을 저속 증발을 위한 주위 조건에서 유지시켰다.
역용매 첨가
각각의 실험에서, 형태 A 대략 10 mg을 각각의 용매 0.1 내지 1 mL 중에 용해시켜 투명한 용액을 수득하였다. 침전이 관찰되거나 또는 역용매의 총 부피가 용매 부피의 20배에 도달할 때까지, 역용매를 50 μL의 증분으로 첨가하였다. 이어서, 침전물을 분석을 위해 원심분리에 의해 단리하였다 (습윤 샘플). 투명한 용액이 관찰되는 경우에는, 저속 증발 실험을 수행하였다.
저속 냉각
각각의 실험에서, 형태 A 대략 10 mg을 50℃에서 각각의 용매 혼합물 0.8 내지 1.0 mL 중에 현탁시켰다. 생성된 현탁액을 즉시 0.2 μm 필터로 여과하고, 여과물을 수집하고, 50℃로부터 5℃로 0.1℃/분의 속도로 냉각시켰다. 이어서, 침전물을 분석을 위해 10,000 rpm에서 3 내지 5분 동안의 원심분리에 의해 단리하였다 (습윤 샘플).
용액 증기 확산
각각의 실험에서, 형태 A 대략 10 mg을 3-mL 유리 바이알 내에서 적절한 용매 중에 용해시켜 투명한 용액을 수득하였다. 이어서, 바이알을 역용매 3 mL를 함유하는 20-mL 유리 바이알에 넣고, 밀봉하였다. 시스템을 실온에서 7일 동안 유지시켜, 고체 침전에 충분한 시간을 허용하였다. 고체를 10,000 rpm에서 3 내지 5분 동안의 원심분리에 의해 단리하고, 분석하였다 (습윤 샘플). 침전이 관찰되지 않는 경우에는, 샘플을 저속 증발을 위한 주위 조건에서 유지시켰다.
고체 증기 확산
각각의 실험에서, 형태 A 대략 10 mg을 3-mL 유리 바이알에 넣고, 이어서 이를 특정한 용매 3 mL를 함유하는 20-mL 유리 바이알 내에 밀봉해 넣었다. 시스템을 실온에서 7일 동안 유지시켜, 유기 증기가 고체와 상호작용하기에 충분한 시간을 허용하였다. 이어서, 고체를 분석하였다 (습윤 샘플).
고속 증발
각각의 실험에서, 형태 A 대략 10 mg을 1.5-mL 유리 바이알 내에서 각각의 용매 0.5 내지 1.0 mL 중에 용해시켰다. 시각적으로 투명한 용액을 마개 없이 고속 증발을 위한 주위 조건에서 유지시켰다. 이어서, 증발에 의해 수득된 고체를 분석하였다 (건조 샘플).
역 역용매 첨가
각각의 실험에서, 형태 A 대략 20 mg을 각각의 용매 0.2 내지 0.6 mL 중에 용해시켜 투명한 용액을 수득하였다. 용액을 각각의 역용매 2.0 mL를 함유하는 유리 바이알에 실온 조건에서 첨가하였다. 형성된 침전물을 분석을 위해 10,000 rpm에서 3 내지 5분 동안 원심분리하였다 (습윤 샘플). 침전이 관찰되지 않는 경우에는, 남아있는 용액에 대해 저속 증발 실험을 수행하였다.
수분 활성 실험
0.2 간격으로 0 내지 1의 수분 활성 (aw) 범위인 수분 활성 실험을, H2O 및 아세토니트릴을 사용하여 수행하였다. 형태 A 약 10 mg을 1.5 mL 바이알에 칭량해 넣고, 용매 혼합물 0.5 mL를 첨가하였다. 현탁액을 실온에서 1000 rpm의 속도로 교반하였다. 잔류 용매를 원심분리 (10000 rpm, 3분 동안)에 의해 샘플로부터 제거하였다.
실시예 3. 고체 형태 B의 제조.
형태 B는 저속 증발, 디클로로메탄 (DCM)/n-헵탄 용매계에서의 슬러리 전환, 역용매 첨가, 고체 증기 확산, 및 다양한 용매계에서의 저속 냉각 결정화 기술에 의해 제조되었다. 본 발명에서 특징화된 형태 B의 동형체들은 디클로로메탄 (DCM)/n-헵탄에서의 슬러리 전환 기술 및 테트라히드로푸란 (THF)/n-헵탄 또는 클로로포름 (CHCl3)/메틸 tert-부틸 에테르 (MBTE)에서의 역용매 첨가 기술로부터 수득되었다.
실시예 4. 고체 형태 C의 제조.
형태 C는 형태 A로부터 50℃에서 이소프로필 알콜 (IPA) 및 이소프로필 아세테이트 (IPAc)에서의 슬러리 전환 결정화 기술에 의해 제조되었다.
실시예 5. 고체 형태 D의 제조.
형태 D는 형태 A로부터 실온 (RT) 조건에서 테트라히드로푸란 (THF)/물 (H2O)에서의 역용매 첨가 결정화 기술로부터 제조되었다.
실시예 6. 고체 형태 E의 제조.
형태 E는 형태 A로부터 주위 실온 (RT) 조건에서 1,4-디옥산/n-헵탄에서의 역용매 첨가 결정화 기술에 의해 제조되었다.
실시예 7. 고체 형태 F의 제조.
형태 F는 형태 A로부터 주위 실온 (RT) 조건에서 1,4-디옥산/n-헵탄에서의 역 역용매 첨가 결정화 기술에 의해 제조되었다.
실시예 8. 고체 형태 H의 제조.
형태 H는 실온 (RT) 조건에서 n-헵탄에서의 용액 증기 확산 결정화 기술에 의해 제조되었다.
실시예 9. 고체 형태 I의 제조.
형태 I는 실온 (RT) 조건에서 메탄올 (MeOH)에서의 저속 냉각 결정화 기술에 의해 제조되었다.
실시예 10. 고체 형태 J의 제조.
형태 J는 실온 (RT) 조건에서 MeOH에서의 고체 증기 확산 결정화 기술에 의해 제조되었다.
실시예 11. 고체 형태 K의 제조.
형태 K는 형태 A, B, C, E 또는 F를 승온으로 가열함으로써 제조되었다. 분석된 형태 K의 샘플은 형태 F를 100℃로 가열함으로써 제조되었다.
실시예 12. 고체 형태 L의 제조.
형태 L은 형태 B를 밀봉된 바이알 내에서 주위 조건에서 1개월 동안 저장함으로써 제조되었다.
실시예 13. 고체 형태 M의 제조.
형태 M은 형태 B를 밀봉된 바이알 내에서 주위 조건에서 1개월 동안 저장함으로써 제조되었다.
실시예 14. 고체 형태 N의 제조.
형태 N은 형태 F의 반복 형성을 시도하는 경우에 1,4-디옥산/n-헵탄에서의 역 역용매 첨가 결정화 기술로부터 제조되었다.
실시예 15. 고체 형태 O의 제조.
형태 O는 H2O/아세토니트릴 (ACN)에서의 수분 활성 결정화 기술 (0.041:0.959 v/v; aw=0.6)로부터 제조되었다. 아세토니트릴은 형태 O의 형성에서 필수적인 역할을 하며, 본 형태를 생성시키기 위해서는 상기 용매가 필요할 수 있다.
실시예 16. XRPD에 의한 고체 형태 A-O의 특징화.
본 연구 전반에 걸친 분석을 위해, 12-웰 오토샘플러 스테이지를 갖는 패널리티컬 엠피리언(PANalytical Empyrean) X선 분말 회절계가 사용되었다. 사용된 XRPD 파라미터는 표 8에 열거되어 있다. 기기의 해상도 보정은 6개월마다 수행되었고, 감도 측정은 샘플 스테이지를 변경한 후에 수행되었다. 규소 (Si) 압축 분말 샘플이 참조 표준물로서 사용되었다.
표 8. XRPD에 대한 파라미터
형태 A: 형태 A는 도 1a에 제시된 바와 같은 XRPD에 의해 결정질인 것으로 관찰되었다.
형태 B: 도 2a에서의 XRPD 패턴은 형태 B-1이 결정질임을 제시한다. 도 2b에서의 XRPD 패턴은 형태 B-1, B-2 및 B-3가 결정질임을 제시한다.
형태 C: 도 3a에서의 XRPD 패턴은 형태 C가 결정질임을 제시한다.
형태 D: 도 4a에 제공된 수득된 XRPD 패턴에 제시된 바와 같이, 형태 D는 결정질이다. XRPD 분석은 또한 형태 D가 도 4b에 도시된 바와 같이 주위 조건에서 건조시킨 후에 형태 A로 변환되었음을 나타내었다.
형태 E: 도 5a에서의 습윤 샘플의 수득된 XRPD 패턴에 기초하여, 형태 E는 결정질인 것으로 관찰되었다. 주위 실온 조건에서 건조시킨 후, 형태 E는 낮은 결정화도를 나타내는 형태 A와 형태 C의 혼합물로 변환되었다.
형태 F: 도 6a에서의 진공 하에 건조된 샘플의 수득된 XRPD 패턴은 형태 F가 결정질임을 제시한다.
형태 H: 도 7a에서의 습윤 샘플의 수득된 XRPD 패턴은 형태 H가 결정질임을 제시한다. XRPD 분석은 도 7b에 도시된 바와 같이 형태 H가 주위 조건에서 3일 동안 건조시킨 후에 형태 A로 변환됨을 나타낸다.
형태 I: 도 8a에서의 습윤 샘플의 수득된 XRPD 패턴은 형태 I가 결정질임을 제시한다. XRPD 분석은 도 8b에 도시된 바와 같이 형태 I가 주위 조건에서 3일 동안 건조시킨 후에 형태 A로 변환됨을 나타낸다.
형태 J: 도 9a에서의 습윤 샘플의 수득된 XRPD 패턴은 형태 J가 결정질임을 제시한다. XRPD 분석은 도 9b에 도시된 바와 같이 형태 J가 주위 조건에서 3일 동안 건조시킨 후에 형태 A로 변환됨을 나타낸다.
형태 K: 도 10a에서의 수득된 XRPD 패턴은 형태 K가 결정질임을 제시한다.
형태 L: 도 11a에서의 수득된 XRPD 패턴은 형태 L이 결정질임을 제시한다. 주위 조건에서 3일 후, 형태 L은 도 11b에 제공된 XRPD 패턴에 제시된 바와 같이 형태 B와 형태 M의 혼합물로 변환된다.
형태 M: 도 12에서의 수득된 XRPD 패턴은 형태 M이 낮은 결정화도를 가짐을 제시한다.
형태 N: 도 13a에서의 주위 조건에서 건조된 샘플의 XRPD 패턴은 형태 N이 결정질임을 제시한다. 도 13b에서의 XRPD 패턴은 주위 조건 하에 밤새, 형태 N이 형태 A로 변환됨을 제시한다.
형태 O: 도 14a에서의 수득된 XRPD 패턴은 형태 O가 결정질임을 제시한다.
실시예 17. 형태 A 및 형태 C의 단결정을 제조하는 방법.
형태 A: 이소프로필 알콜에서의 50℃로부터 5℃로의 저속 냉각에 의해, 구조 결정에 적합한 단결정이 수득되었다.
형태 C: 형태 C 시드 포함 이소프로필 아세테이트/아세톤 (6:1, v/v) 공용매에서의 25℃로부터 5℃로의 0.01℃/분의 속도로의 저속 냉각에 의해, 구조 결정에 적합한 단결정이 수득되었다.
실시예 18. 형태 A 및 형태 C의 단결정 X선 회절 데이터.
형태 A (표 9) 및 형태 C (표 10)의 프리즘상 결정으로부터의 X선 강도 데이터는 브루커 D8 벤처(Bruker D8 Venture) 회절계 (Mo Kα 방사선, λ = 0.71073 Å)를 사용하여 290(2) K에서 수집되었다. 형태 A 및 C의 결정 구조는 수득된 데이터로부터 해석되었다.
표 9. 형태 A의 단결정에 대한 결정 데이터 및 구조 정밀화:
표 10. 형태 C의 단결정에 대한 결정 데이터 및 구조 정밀화:
실시예 19. 형태 A 및 형태 C의 단결정 구조의 단위 셀.
b 축에 따르는 형태 A의 단위 셀이 도 1b에 도시되어 있다. b 축을 따르는 형태 C의 단위 셀이 도 3b에 도시되어 있다.
실시예 20. 온도-의존성 기기분석 방법 (TGA, DSC 및 VT-XRPD)에 의한 고체 형태 A-O의 특징화.
열중량측정 분석 (TGA) 데이터는 TA 인스트루먼츠(TA Instruments)로부터의 TA Q500/Q5000 TGA를 사용하여 수집되었고, 시차 주사 열량측정 (DSC)은 TA 인스트루먼츠로부터의 TA Q200/Q2000 DSC를 사용하여 수행되었다. 사용된 기기 파라미터는 표 11에 제공되어 있다.
표 11. TGA 및 DSC 시험에 대한 파라미터
온도-의존성 연구를 보충하고 고체 형태의 용매화 상태를 확인하기 위해, 용액 NMR이 브루커 400 MHz NMR 분광계 상에서 중수소화 디메틸 술폭시드 (DMSO-d6)를 용매로서 사용하여 수집되었다.
형태 A: TGA 및 DSC를 수행하였으며, 세부사항은 도 1c에 제공되었다. 형태 A의 열중량측정 분석하여, 200℃까지 1.0%의 중량 손실이 생성되었다. DSC 곡선 상에서, 형태 A의 형태 K로의 변환을 나타내는 157.2℃ (개시 온도)에서의 흡열, 이어서 203.8℃ (개시 온도)에서의 형태 K에 대한 예리한 용융 피크가 관찰되었다. 형태 K로의 변환의 확인은 도 1d에 제시된 바와 같은 VT-XRPD에 의해 수행되었다.
형태 B-1: TGA 및 DSC를 수행하였으며, 이들 각각의 곡선은 도 2c에 제공되었다. TGA 곡선은 76℃까지 잔류 용매의 5.7% 손실, 이어서 200℃까지 8.5% 손실 (탈용매화)로 2-단계 중량 손실을 나타낸다. DSC 곡선은, 각각 용매의 손실 (형태 K로의 변환) 및 형태 K의 융점에 상응하는 87.2℃ 및 211.7℃ (개시 온도)에서의 2개의 흡열 피크를 나타낸다. XPRD에 의한 분석은 도 2d에 제시된 바와 같이 형태 B-1이 100℃로 가열 시 형태 K로 변환됨을 나타낸다. 도 2g에 제시된 1H NMR 데이터에 기초하여, 형태 B는 화합물 1:n-헵탄의 몰비 1:0.4 (중량 기준으로 ~8.9%의 n-헵탄)의 n-헵탄 용매화물이며, 이는 TGA 결과와 잘 일치한다. 1H NMR 데이터에서, 잔류 DCM이 또한 화합물 1:DCM의 몰비 1:0.06 (1.2 중량%)으로 관찰된다.
형태 B-2: 본 동형체의 TGA는, 나머지 2종의 동형체의 TGA 곡선과 함께 도 2e에 제시되어 있다. 나머지 2종의 동형체의 오버레이와 함께 도 2f에 도시된 본 동형체의 DSC 곡선은 2회의 흡열: 85.4℃의 T개시에서의 1회의 흡열 및 212.2℃의 T개시에서의 1회의 흡열을 나타낸다. 도 2h에서의 1H NMR 스펙트럼은 형태 B가 화합물 1:n-헵탄의 몰비 1:0.3의 n-헵탄 용매화물이며 THF가 관찰되지 않았음을 나타내었다.
형태 B-3: 본 동형체의 TGA는, 나머지 2종의 동형체의 TGA 곡선과 함께 도 2e에 제시되어 있다. 나머지 2종의 동형체의 오버레이와 함께 도 2f에 도시된 본 동형체의 DSC 곡선은, 1회는 69.2℃의 T개시이고 1회는 211.6℃의 T개시인 2회의 흡열을 나타낸다. 도 2i에서의 1H NMR 스펙트럼은 형태 B가 화합물 1:클로로포름의 몰비 1:0.5의 클로로포름 용매화물이며 잔류 메틸 tert-부틸 에테르가 검출되었음을 나타내었다.
형태 C: TGA 및 DSC를 수행하였으며, 이들 각각의 곡선은 도 3c에 제공되어 있다. TGA 곡선은 50℃ 미만에서 4.3%의 중량 손실이 발생함을 나타내며, 이는 가능하게는 불충분한 건조로 인해 존재하는 우발적 용매 또는 느슨하게 유지된 용매의 지표이다. DSC 곡선은 183.8℃ 및 211.0℃ (개시 온도)에서의 2개의 흡열 피크를 나타낸다. 형태 C를 185℃로 가열함으로써 183.8℃에서의 흡열에 대해 추가 조사를 수행하였으며, 이는 도 3d에 제시된 바와 같이 형태 K로의 형태 변환을 유발하였다. 질소 (N2) 유동을 사용하여 또는 상기 유동 없이 형태 C에 대한 VT-XRPD에 의한 분석을 수행하여, 공기로부터의 가능한 재수화를 조사하였다. 도 3e에 제시된 바와 같이, N2를 사용한 경우와 N2가 없는 경우에 차이가 없음이 관찰되었으며, 이는 형태 C가 무수물임을 나타낸다.
형태 F: TGA 및 DSC를 수행하였으며, 이들 각각의 곡선은 도 6b에 제공되어 있다. TGA 곡선은 200℃까지 19.7%의 총 중량 손실을 나타낸다. DSC 곡선은, 각각 용매의 손실 (형태 K로의 변환) 및 형태 K의 융점에 상응하는 63.1℃ 및 210.7℃ (개시 온도)에서의 2개의 흡열 피크를 나타낸다. 이는 도 6c에 제시된 바와 같이 100℃로 가열 후의 형태 F의 형태 K로의 변환에 의해 더욱 명백하다. 도 6d에 제시된 1H NMR 스펙트럼에 기초하여, 형태 F는 몰비 1:0.9 (중량 기준으로 16.2%의 1,4-디옥산)의 1,4-디옥산 용매화물이며, 이는 TGA 결과와 잘 일치한다. 1H NMR 데이터에서, 잔류 n-헵탄이 또한 몰비 1:0.03 (중량 기준으로 0.7%의 n-헵탄)으로 관찰된다.
형태 K: TGA 및 DSC를 수행하였으며, 이들 각각의 곡선은 도 11b에 제공되어 있다. TGA 곡선은 200℃까지 1.6%의 중량 손실을 나타내고, DSC 곡선은 형태 K의 용융 흡열에 상응하는 211.6℃ (개시 온도)에서의 흡열 피크를 나타낸다. 저휘발성 함량에 기초하여, 형태 K는 비용매화 물질이다.
형태 L: 도 12c에 제시된 형태 L의 DSC 곡선은, 81.7℃ 및 210.6℃ (개시 온도)에서의 2개의 흡열 피크를 나타낸다. 제1 흡열 피크는 가능한 용매의 손실 또는 형태 변환에 기인한다. DSC 곡선에서의 제2 흡열 피크는 형태 K의 용융 흡열에 부합한다.
형태 N: 도 14c에서의 TGA 곡선은 60℃까지 2.5%, 이어서 200℃까지 7.1%의 2-단계 중량 손실을 나타낸다. DSC 곡선은, 각각 용매의 손실 (1H NMR 기준) 및 형태 K의 융점에 기인하는 75.4℃ 및 210.4℃ (개시 온도)에서의 2개의 흡열 피크를 나타낸다. 도 14d에서의 1H NMR 결과에 기초하여, 형태 N은 화합물 1:1,4-디옥산의 몰비 1:0.3 (중량 기준으로 6.1% 1,4-디옥산)의 1,4-디옥산 용매화물이며, 이는 TGA 분석에서의 제2 단계 중량 손실과 일치한다.
형태 O: 도 15b에 제시된 TGA 곡선에서, 55.1℃까지 5.3%, 이어서 200℃까지 5.9%의 2-단계 중량 손실이 관찰된다. DSC 곡선은, 각각 형태 C의 생성을 위한 용매의 손실, 형태 C의 형태 K로의 변환, 및 형태 K의 융점에 상응하는 65.0℃, 168.5℃, 및 210.8℃ (개시 온도)에서의 3개의 흡열 피크를 나타낸다. DSC 분석에서 관찰된 흡열을 조사하기 위해, 도 15c에 제시된 바와 같이 형태 O를 120℃로 가열하여 형태 C로의 변화를 유발하였다. 1H NMR 스펙트럼은, 도 15d에 도시된 바와 같이 잔류 용매를 제거하기 위해 50℃로 가열한 후 형태 O: ACN (1.9 중량%)에 대해 1:0.2의 몰비를 보여주었다.
실시예 21. DVS에 의해 측정 시 형태 A, C 및 K의 흡습성.
동적 증기 수착 (DVS)은 SMS (서피스 메저먼트 시스템즈(Surface Measurement Systems)) DVS 고유 시스템에 의해 측정되었다. 25℃에서의 상대 습도는 LiCl, Mg(NO3)2, 및 KCl의 조해점에 대해 보정되었다. 본 연구 전반에 걸쳐 사용된 DVS 시스템 기기 파라미터는 표 12에 열거되어 있다.
표 13. DVS 시험에 대한 파라미터
형태 A, 형태 C 및 형태 K의 흡습성을 DVS를 사용하여 25℃에서 조사하였다. DVS 전후의 각각의 샘플의 XRPD 패턴을 비교하여 임의의 잠재적인 형태 변화를 조사하였다.
도 1e에 제시된 형태 A의 DVS 등온 플롯은 0.06 중량%의 80% RH에서의 수분 흡수 및 0.12 중량% 미만의 95% RH에서의 수분 흡수를 나타내어, 형태 A가 비-흡습성임을 보여준다. 도 1f에서의 XRPD 패턴은 형태 A의 경우 DVS 전후에 형태 변화가 없음을 나타낸다.
유사하게, 도 3f에 제시된 형태 C의 DVS 등온 플롯은 0.12 중량%의 80% RH에서의 수분 흡수 및 0.30 중량% 미만의 95% RH에서의 수분 흡수를 나타내어, 형태 C가 비-흡습성임을 나타낸다. 도 3g에서의 XRPD 패턴은 형태 C의 경우 DVS 전후에 형태 변화가 없음을 나타낸다.
도 11c에 제시된 형태 K의 DVS 등온 플롯은 0.18 중량%의 80% RH에서의 수분 흡수 및 0.35 중량% 미만의 95% RH에서의 수분 흡수를 나타내어, 형태 K가 비-흡습성임을 보여준다. 도 11d에서의 XRPD 패턴은 형태 K의 경우 DVS 전후에 형태 변화가 없음을 나타낸다.
실시예 22. 슬러리 전환을 통한 형태 A, C 및 K의 상호전환.
한 실시양태에서, 형태 A, C 및 K 사이의 상호전환은 실온 (RT) 및 50℃ 둘 다에서 에틸 아세테이트, n-부탄올, 및 메틸 tert-부틸 에테르 (MBTE) 중에서 수행되는 일련의 슬러리 전환 실험으로 연구될 수 있다. 화합물 1은 보통의 용해도를 나타낼 수 있으며, 이들 스크리닝 실험 도중에 용매화 형태를 생성시킬 수 있다. 슬러리 전환 실험의 결과는 표 14에 요약되어 있다. 형태 A와 형태 C 사이의 전환 온도는 ~17℃인 것으로 추정되었고, 형태 K와 형태 C 사이의 전환 온도는 100℃ 초과였다.
표 14. 슬러리 전환 실험의 요약
실시예 23. 형태 C 시드 결정을 사용한 형태 A의 형태 C로의 전환.
에틸 아세테이트 중 대략 200 g/L-225 g/L의 가용화된 화합물 1 (원래 형태 A)을 0.2%-1.0%의 형태 C의 시드 결정의 존재 하에 65℃의 온도로 1-3시간 동안 가열하였다. 이어서, 배치를 25℃-30℃의 온도로 3시간 이상 동안 서서히 냉각시켜 형태 C를 수득할 수 있다. 형태 C의 시드 결정은 실시예 4에 기재된 절차를 사용하여 수득될 수 있다.
XRPD를 리가쿠(Rigaku) 미니플렉스(MiniFlex) 600 (40 kV 튜브 전압 및 15 mA 튜브 전류에서의 Cu Kα 방사선)을 사용하여 2θ에 대해 2° 내지 40 °의 스캔 범위, 0.01°의 스텝 크기, 및 분당 1° 또는 2°의 스캔 속도로 수행하였다. XRPD를 사용하여, 도 15에 제시된 바와 같이, 시간 경과에 따라, 1.0%의 형태 C의 시드 결정을 사용한 65℃에서의 에틸 아세테이트 중 225 g/L의 형태 A로부터 형태 C로의 전환을 모니터링하였다.
실시예 24. 형태 P의 제조 및 특징화.
용해도 측정 동안, (a) 5℃ (1시간 후) 및 20℃ (2일 후)에서의 EtOAc 중 형태 A의 슬러리, (b) 5℃ (1시간 후) 및 20℃ (7일 후)에서의 EtOAc 중 형태 C의 슬러리에서 XRPD 패턴을 검출하였다. 이러한 고체 형태의 XRPD 패턴은 화합물 1의 다른 결정 형태에 직접 부합되지는 않았다. 이러한 결과는, 형태 P로 명명된 EtOAc 중 화합물 1의 이러한 고체 형태가, 적어도 ≤ 20℃에서 EtOAc 중에서 형태 A 및 C 둘 다보다 더 안정함을 나타낸다.
형태 P의 습윤 케이크 (~5분 공기)를 2종의 방식으로: (a) 공기 하에 실온에서 밤새, 및 (b) 진공 하에 40℃에서 3시간 동안 건조시켰다. 둘 다의 건조된 케이크를 XRPD, 1H-NMR 및 TGA에 의해 분석하였다. XRPD 데이터는 도 16에 제시되어 있다. NMR 데이터는 도 17a 및 도 17b에 제시되어 있다. TGA 데이터는 도 18a 및 도 18b에 제시되어 있다. 공기 건조된 케이크는 형태 P에 따른 XRPD 패턴, TGA에 의해 약 50℃까지 약 1%의 중량 손실, 및 1H NMR에 의해 EtOAc 피크를 제공하였다. 이는 형태 P가 화합물 1의 EtOAc 용매화물임을 나타낸다. 다른 한편, 오븐 건조-후 형태 P의 샘플은 형태 A에 따른 XRPD 패턴, TGA에 의해 ≤ 100℃에서 중량 손실 없음, 및 1H-NMR에 의해 EtOAc 피크 없음을 제공하였다. 따라서, 데이터는 형태 P가 형태 A의 용매화물이며 건조 시에 형태 A로 전환됨을 시사한다.
실시예 25. 형태 A, C 및 P의 용해도 및 상대적 안정성.
광범위한 온도에 걸친 형태 A, C 및 P의 용해도 프로파일은 다양한 온도 범위 내에서의 상이한 형태들의 상대적 안정성의 지표를 제공할 수 있다. 5-70℃를 포괄하는 충분한 평형 용해도 데이터를 실험적으로 수집하였다. 그 결과는 표 15 및 도 19에 제시되어 있다.
데이터는 (1) 전체 가공 온도 범위에 걸쳐 형태 C가 형태 A보다 더 안정하고; (2) ≤ 20℃에서는 형태 P가 형태 C보다 더 안정해지고; (3) 대략 25~30℃에서는 느린 전환 반응속도로 인해 3종의 형태들 사이의 상호전환이 거의 없고; (4) ≥ 35℃에서는 형태 P가 EtOAc 중에서 불안정해지며 형태 A로 전환되고; (5) 공기 또는 N2 중에서 건조 시에는 형태 P가 형태 A로 전환됨을 나타낸다.
EtOAc 중 형태 A, C 및 P의 상 관계는 도 20에 도시되어 있다. 저온에서 EtOAc 중에서는 형태 A 및 C가 형태 P로 전환될 수 있다. 또한 매우 낮은 온도에서는 형태 A가 형태 C로부터 생성될 수 있다 (예를 들어, 더 우수한 단리 수율을 목적으로 함).
표 15. 형태 A, C 및 P의 용해도 데이터.
다른 실시양태
청구범위에서, 단수 표현은 달리 나타내지 않는 한 또는 달리 문맥으로부터 명백하지 않는 한, 하나 또는 하나 초과를 의미할 수 있다. 군의 1개 이상의 구성원들 사이에 "또는"을 포함하는 청구범위 또는 설명은 달리 나타내지 않거나 또는 문맥으로부터 달리 명백하지 않는 한, 군 구성원 중 하나, 하나 초과, 또는 모두가 주어진 생성물 또는 공정에 존재하거나, 그에 사용되거나, 또는 그와 달리 관련되어 있는 경우에 충족된 것으로 간주된다. 본 발명은 군의 정확하게 하나의 구성원이 주어진 생성물 또는 공정에 존재하거나, 그에 사용되거나, 또는 그와 달리 관련되어 있는 실시양태를 포함한다. 본 발명은 군 구성원 중 하나 초과, 또는 모두가 주어진 생성물 또는 공정에 존재하거나, 그에 사용되거나, 또는 그와 달리 관련되어 있는 실시양태를 포함한다.
또한, 본 발명은 열거된 청구항 중 한 항 이상으로부터의 1개 이상의 제한, 요소, 항목 및 서술적 용어가 또 다른 청구항에 도입된 모든 변형, 조합 및 순열을 포괄한다. 예를 들어, 또 다른 청구항에 대해 종속항인 임의의 청구항은 동일 기반 청구항에 대해 종속항인 임의의 다른 청구항에서 발견되는 1개 이상의 제한을 포함하도록 변형될 수 있다. 요소가, 예를 들어 마쿠쉬 군 포맷의 목록으로서 제시되는 경우에, 요소의 각각의 하위군이 또한 개시되고, 임의의 요소(들)는 군으로부터 제거될 수 있다. 일반적으로, 본 발명 또는 본 발명의 측면이 특정한 요소 및/또는 특색을 포함하는 것으로 지칭되는 경우에, 본 발명 또는 본 발명의 측면의 특정 실시양태는 이러한 요소 및/또는 특색으로 이루어지거나 또는 본질적으로 이루어지는 것으로 이해되어야 한다. 단순성의 목적을 위해, 이들 실시양태는 본원에 구체적으로 제시되지 않았다. 또한, 용어 "포함하는" 및 "함유하는"은 개방적이고 추가의 요소 또는 단계의 포함을 허용하는 것으로 의도됨을 주목한다. 범위가 주어진 경우, 종점들이 포함된다. 추가로, 달리 나타내지 않는 한 또는 달리 문맥 및 관련 기술분야의 통상의 기술자의 이해로부터 명백하지 않는 한, 범위로서 표현된 값은 본 발명의 상이한 실시양태에서 언급된 범위 내의 임의의 구체적 값 또는 하위-범위를, 문맥이 달리 명백하게 지시하지 않는 한 범위의 하한치 단위의 1/10까지 가정할 수 있다.
본원은 다양한 허여된 특허, 공개 특허 출원, 학술지 및 다른 간행물을 인용하며, 이들 모두는 본원에 참조로 포함된다. 임의의 포함된 참고문헌과 본 명세서 사이에 상충이 존재하는 경우에, 본 명세서가 우선할 것이다. 추가로, 선행 기술 내에 해당하는 본 발명의 임의의 특정한 실시양태는 청구항 중 어느 한 항 이상으로부터 명시적으로 제외될 수 있다. 이러한 실시양태는 관련 기술분야의 통상의 기술자에게 공지된 것으로 여겨지기 때문에, 이들은 이러한 제외가 본원에 명시적으로 제시되지 않았더라도 제외될 수 있다. 본 발명의 임의의 특정한 실시양태는 선행 기술의 존재와 관련되어 있든지 아니든지 간에, 임의의 이유로, 임의의 청구항으로부터 제외될 수 있다.
관련 기술분야의 통상의 기술자는 단지 상용 실험을 사용하여, 본원에 기재된 구체적 실시양태에 대한 많은 등가물을 인식 또는 확인할 수 있을 것이다. 본원에 기재된 본 실시양태의 범주는 상기 설명에 제한되도록 의도된 것은 아니며, 오히려 첨부된 청구범위에 제시된 바와 같다. 관련 기술분야의 통상의 기술자는 이러한 설명에 대한 다양한 변화 및 변형이 하기 청구범위에 정의된 바와 같은 본 발명의 취지 또는 범주로부터 벗어나지 않으면서 이루어질 수 있음을 인지할 것이다.
Claims (1)
- 도 1a에 도시된 XRPD 패턴을 갖는 결정질 화합물.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662378582P | 2016-08-23 | 2016-08-23 | |
| US62/378,582 | 2016-08-23 | ||
| KR1020197008069A KR20190040043A (ko) | 2016-08-23 | 2017-08-23 | 결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 |
| PCT/US2017/048267 WO2018039378A1 (en) | 2016-08-23 | 2017-08-23 | A crystalline 19-nor c3, 3-disubstituted c21-n-pyrazolyl steroid |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020197008069A Division KR20190040043A (ko) | 2016-08-23 | 2017-08-23 | 결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230079470A true KR20230079470A (ko) | 2023-06-07 |
Family
ID=59772778
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237017309A KR20230079470A (ko) | 2016-08-23 | 2017-08-23 | 결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 |
| KR1020197008069A KR20190040043A (ko) | 2016-08-23 | 2017-08-23 | 결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020197008069A KR20190040043A (ko) | 2016-08-23 | 2017-08-23 | 결정질 19-노르 c3,3-이치환된 c21-n-피라졸릴 스테로이드 |
Country Status (23)
| Country | Link |
|---|---|
| US (3) | US11236121B2 (ko) |
| EP (2) | EP3981763A1 (ko) |
| JP (2) | JP2019524853A (ko) |
| KR (2) | KR20230079470A (ko) |
| CN (4) | CN110088091A (ko) |
| AR (3) | AR109393A1 (ko) |
| AU (3) | AU2017315682B2 (ko) |
| BR (1) | BR112019003637A2 (ko) |
| CA (1) | CA3034262A1 (ko) |
| CL (2) | CL2019000477A1 (ko) |
| CO (1) | CO2019002596A2 (ko) |
| EA (1) | EA201990565A1 (ko) |
| EC (1) | ECSP19020141A (ko) |
| IL (1) | IL302480A (ko) |
| JO (1) | JOP20190022B1 (ko) |
| MA (1) | MA46042A (ko) |
| MX (2) | MX2019002193A (ko) |
| PE (1) | PE20190915A1 (ko) |
| PH (1) | PH12019500375A1 (ko) |
| SG (1) | SG11201901445TA (ko) |
| TW (2) | TWI808945B (ko) |
| WO (1) | WO2018039378A1 (ko) |
| ZA (1) | ZA201901051B (ko) |
Families Citing this family (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3572417A3 (en) | 2011-10-14 | 2020-03-25 | Sage Therapeutics, Inc. | 3,3 disubstituted 19-nor pregnane compounds, compositions, and uses thereof |
| US9512165B2 (en) | 2013-04-17 | 2016-12-06 | Sage Therapeutics, Inc. | 19-nor C3, 3-disubstituted C21-N-pyrazolyl steroids and methods of use thereof |
| WO2014169836A1 (en) | 2013-04-17 | 2014-10-23 | Sage Therapeutics, Inc. | 19-nor neuroactive steroids and methods of use thereof |
| US9725481B2 (en) | 2013-04-17 | 2017-08-08 | Sage Therapeutics, Inc. | 19-nor C3, 3-disubstituted C21-C-bound heteroaryl steroids and methods of use thereof |
| PL2986624T3 (pl) | 2013-04-17 | 2020-11-16 | Sage Therapeutics, Inc. | Neuroaktywne steroidy 19-NOR do stosowania w sposobach leczenia |
| CA2918735C (en) | 2013-07-19 | 2023-08-01 | Sage Therapeutics, Inc. | Neuroactive steroids, compositions, and uses thereof |
| EP3035940B1 (en) | 2013-08-23 | 2018-10-17 | Sage Therapeutics, Inc. | Neuroactive steroids, compositions, and uses thereof |
| WO2015195962A1 (en) | 2014-06-18 | 2015-12-23 | Sage Therapeutics, Inc. | Neuroactive steroids, compositions, and uses thereof |
| NZ769042A (en) | 2014-10-16 | 2023-12-22 | Sage Therapeutics Inc | Compositions and methods for treating cns disorders |
| CN117024501A (zh) | 2014-10-16 | 2023-11-10 | 萨奇治疗股份有限公司 | 靶向cns障碍的组合物和方法 |
| PT3224269T (pt) | 2014-11-27 | 2020-06-01 | Sage Therapeutics Inc | Composições e métodos para tratamento de distúrbios do snc |
| SI3250210T1 (sl) | 2015-01-26 | 2021-07-30 | Sage Therapeutics, Inc. | Sestavki in metode za zdravljenje CNS motenj |
| WO2016134301A2 (en) | 2015-02-20 | 2016-08-25 | Sage Therapeutics, Inc. | Neuroactive steroids, compositions, and uses thereof |
| CN109689673B (zh) | 2016-07-11 | 2023-03-14 | 萨奇治疗股份有限公司 | C17、c20和c21取代的神经活性类固醇及其使用方法 |
| AU2017296295B2 (en) | 2016-07-11 | 2022-02-24 | Sage Therapeutics, Inc. | C7, C12, and C16 substituted neuroactive steroids and their methods of use |
| JOP20190022B1 (ar) | 2016-08-23 | 2023-03-28 | Sage Therapeutics Inc | ستيرويد 19- نور c3، 3- به استبدال ثنائي لـ c21-n بيرازوليل بلوري |
| TW202342058A (zh) * | 2017-09-07 | 2023-11-01 | 美商賽吉醫療公司 | 神經活性類固醇及其使用方法 |
| WO2019055764A1 (en) * | 2017-09-14 | 2019-03-21 | Sage Therapeutics, Inc. | C21-N-PYRAZOLYL C3,3-DISUBSTITUTED STEROID 19 NOR, AND METHODS OF USING THE SAME |
| KR20200096596A (ko) | 2017-12-08 | 2020-08-12 | 세이지 테라퓨틱스, 인크. | Cns 장애의 치료를 위한 중수소화 21 -[4-시아노-피라졸-1 -일]-19-노르-프레간-3. 알파-올-20-온 유도체 |
| CN112533611A (zh) * | 2018-06-12 | 2021-03-19 | 萨奇治疗股份有限公司 | 19-去甲基c3,3-二取代的c21-n-吡唑基类固醇及其使用方法 |
| MA54594A (fr) | 2018-12-05 | 2022-04-06 | Sage Therapeutics Inc | Stéroïdes neuroactifs et leurs procédés d'utilisation |
| CN111454318A (zh) * | 2019-01-20 | 2020-07-28 | 浙江易众化工有限公司 | 抗抑郁药物sage-217的晶型及其制备方法 |
| CN111770915A (zh) * | 2019-01-31 | 2020-10-13 | 深圳仁泰医药科技有限公司 | γ-氨基丁酸调节剂的晶型X及其制备方法和应用 |
| WO2020242772A1 (en) | 2019-05-28 | 2020-12-03 | Teva Czech Industries S.R.O | Solid state forms of sage-217 and processes for preparation thereof |
| BR112021024033A2 (pt) | 2019-05-31 | 2022-02-08 | Sage Therapeutics Inc | Esteroides neuroativos e suas composições |
| KR20220066262A (ko) * | 2019-08-07 | 2022-05-24 | 상하이 한서 바이오메디컬 컴퍼니 리미티드 | 스테로이드 유도체 조절제의 염 및 결정형 |
| US10857163B1 (en) | 2019-09-30 | 2020-12-08 | Athenen Therapeutics, Inc. | Compositions that preferentially potentiate subtypes of GABAA receptors and methods of use thereof |
| US20230346801A1 (en) | 2020-03-25 | 2023-11-02 | Sage Therapeutics, Inc. | Use of agents for treatment of respiratory conditions |
| AR123018A1 (es) | 2020-07-20 | 2022-10-26 | Sage Therapeutics Inc | Formulaciones del esteroide c21-n-pirazolilo 19-nor c3,3-disustituido y métodos de uso de este |
| AU2022214187A1 (en) | 2021-01-28 | 2023-07-13 | Sage Therapeutics, Inc. | Use of neuroactive steroids for treatment of sexual dysfunction |
| AU2022238365A1 (en) | 2021-03-17 | 2023-09-21 | Sage Therapeutics, Inc. | A 19-nor c3,3-disubstituted c21-n-pyrazolyl steroid for the treatment of major depressive disorder |
| EP4329769A1 (en) | 2021-04-29 | 2024-03-06 | Sage Therapeutics, Inc. | Neuroactive steroid for use in treating major depressive disorder and postpartum depression in a lactating female |
| JP2024515829A (ja) | 2021-04-29 | 2024-04-10 | セージ セラピューティクス, インコーポレイテッド | 大うつ病性障害および産後うつ病の処置における使用のための19-ノルc3,3-二置換c21-n-ピラゾリルステロイド |
| WO2023009584A1 (en) | 2021-07-28 | 2023-02-02 | Sage Therapeutics, Inc. | Crystalline forms of a neuroactive steroid |
| WO2023158668A1 (en) | 2022-02-16 | 2023-08-24 | Sage Therapeutics, Inc. | Neuroactive steroids for treatment of cns-related disorders |
| TW202341996A (zh) | 2022-02-28 | 2023-11-01 | 美商賽吉醫療公司 | 用於治療腸胃疾病或病狀之神經活性類固醇 |
Family Cites Families (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5120723A (en) | 1987-08-25 | 1992-06-09 | University Of Southern California | Method, compositions, and compounds for modulating brain excitability |
| US7018406B2 (en) | 1999-11-17 | 2006-03-28 | Corevalve Sa | Prosthetic valve for transluminal delivery |
| CA2396079A1 (en) * | 2000-01-07 | 2001-07-19 | Transform Pharmaceuticals, Inc. | High-throughput formation, identification, and analysis of diverse solid-forms |
| KR100960062B1 (ko) | 2002-02-08 | 2010-05-31 | 오노 야꾸힝 고교 가부시키가이샤 | 피페리딘 유도체 화합물 및 상기 화합물을 유효성분으로서 함유하는 약제 |
| WO2011079047A1 (en) | 2009-12-23 | 2011-06-30 | Drugtech Corporation | Methods for reducing the occurrence of preterm delivery and other pregnancy-related conditions |
| EP2736919A4 (en) | 2011-07-29 | 2015-01-14 | Univ California | NEW 17-BETA-HETEROARYL-SUBSTITUTED STEROIDS AS MODULATORS OF GABAA RECEPTORS |
| WO2013043985A1 (en) | 2011-09-23 | 2013-03-28 | The Regents Of The University Of California | Edible oils to enhance delivery of orally administered steroids |
| US9765110B2 (en) | 2012-10-08 | 2017-09-19 | Washington University | Neuroactive 19-alkoxy-17(20)-Z-vinylcyano-substituted steroids, prodrugs thereof, and methods of treatment using same |
| WO2014085668A1 (en) | 2012-11-30 | 2014-06-05 | The Regents Of The University Of California | Anticonvulsant activity of steroids |
| TR201808616T4 (tr) | 2012-12-18 | 2018-07-23 | Sage Therapeutics Inc | Nöroaktif 19-alkoksi-17-ikameli steroidler, bunların ön ilaçları ve bunları kullanan tedavi yöntemleri. |
| US9725481B2 (en) | 2013-04-17 | 2017-08-08 | Sage Therapeutics, Inc. | 19-nor C3, 3-disubstituted C21-C-bound heteroaryl steroids and methods of use thereof |
| US9512165B2 (en) * | 2013-04-17 | 2016-12-06 | Sage Therapeutics, Inc. | 19-nor C3, 3-disubstituted C21-N-pyrazolyl steroids and methods of use thereof |
| WO2015195962A1 (en) | 2014-06-18 | 2015-12-23 | Sage Therapeutics, Inc. | Neuroactive steroids, compositions, and uses thereof |
| JOP20200195A1 (ar) | 2014-09-08 | 2017-06-16 | Sage Therapeutics Inc | سترويدات وتركيبات نشطة عصبياً، واستخداماتها |
| CN117024501A (zh) | 2014-10-16 | 2023-11-10 | 萨奇治疗股份有限公司 | 靶向cns障碍的组合物和方法 |
| NZ769042A (en) | 2014-10-16 | 2023-12-22 | Sage Therapeutics Inc | Compositions and methods for treating cns disorders |
| UY36741A (es) | 2015-06-21 | 2016-12-30 | Prevacus Inc | Compuesto de esteroide c-20, sus composiciones y usos para tratar la lesión cerebral traumática (tbi), que incluye las conmociones cerebrales |
| JP2018526423A (ja) | 2015-09-08 | 2018-09-13 | ビューポイント セラピューティクス, インコーポレイテッド | 眼科疾患を処置するための化合物および製剤 |
| AU2016338672A1 (en) | 2015-10-16 | 2018-04-12 | Marinus Pharmaceuticals, Inc. | Injectable neurosteroid formulations containing nanoparticles |
| WO2017087864A1 (en) | 2015-11-20 | 2017-05-26 | Sage Therapeutics, Inc. | Compounds and methods of their use |
| JOP20170059B1 (ar) | 2016-03-08 | 2021-08-17 | Sage Therapeutics Inc | ستيرويدات وتركيبات نشطة عصبيًا واستخداماتها |
| US10226550B2 (en) | 2016-03-11 | 2019-03-12 | Brigham Young University | Cationic steroidal antimicrobial compositions for the treatment of dermal tissue |
| CN109689673B (zh) | 2016-07-11 | 2023-03-14 | 萨奇治疗股份有限公司 | C17、c20和c21取代的神经活性类固醇及其使用方法 |
| AU2017296295B2 (en) | 2016-07-11 | 2022-02-24 | Sage Therapeutics, Inc. | C7, C12, and C16 substituted neuroactive steroids and their methods of use |
| JOP20190022B1 (ar) | 2016-08-23 | 2023-03-28 | Sage Therapeutics Inc | ستيرويد 19- نور c3، 3- به استبدال ثنائي لـ c21-n بيرازوليل بلوري |
| CN108727453A (zh) | 2017-04-20 | 2018-11-02 | 华东理工大学 | 新型pd-1抑制剂及其应用 |
| WO2019018119A1 (en) | 2017-07-18 | 2019-01-24 | Pairnomix, Llc | METHODS FOR TREATING EPILEPSY AND DISORDERS ASSOCIATED WITH KCNTI |
| CN116370475A (zh) | 2017-08-31 | 2023-07-04 | 武田药品工业株式会社 | 中枢神经系统病症的治疗 |
| TW202342058A (zh) | 2017-09-07 | 2023-11-01 | 美商賽吉醫療公司 | 神經活性類固醇及其使用方法 |
| WO2019051477A1 (en) | 2017-09-11 | 2019-03-14 | Sage Therapeutics, Inc. | METHODS OF TREATING EPILEPSY OR EPILEPTIC MALE CONDITION |
| WO2019055764A1 (en) | 2017-09-14 | 2019-03-21 | Sage Therapeutics, Inc. | C21-N-PYRAZOLYL C3,3-DISUBSTITUTED STEROID 19 NOR, AND METHODS OF USING THE SAME |
| WO2019094724A1 (en) | 2017-11-10 | 2019-05-16 | Marinus Pharmaceuticals, Inc. | Ganaxolone for use in treating genetic epileptic disoders |
| KR20200096596A (ko) | 2017-12-08 | 2020-08-12 | 세이지 테라퓨틱스, 인크. | Cns 장애의 치료를 위한 중수소화 21 -[4-시아노-피라졸-1 -일]-19-노르-프레간-3. 알파-올-20-온 유도체 |
| US20220315621A1 (en) | 2017-12-22 | 2022-10-06 | Sage Therapeutics, Inc. | Compositions and methods for treating cns disorders |
| MA51315A (fr) | 2017-12-22 | 2020-10-28 | Sage Therapeutics Inc | Compositions et méthodes permettant de traiter des troubles du snc |
| TW201930269A (zh) | 2018-01-12 | 2019-08-01 | 美商賽吉醫療公司 | 用於治療cns病症之組合物及方法 |
| CN112533611A (zh) | 2018-06-12 | 2021-03-19 | 萨奇治疗股份有限公司 | 19-去甲基c3,3-二取代的c21-n-吡唑基类固醇及其使用方法 |
| AR116695A1 (es) | 2018-10-12 | 2021-06-02 | Sage Therapeutics Inc | Los neuroesteroides y sus métodos de uso |
| TW202027754A (zh) | 2018-10-19 | 2020-08-01 | 美商賽吉醫療公司 | 神經活性類固醇及其使用方法 |
| MA54594A (fr) | 2018-12-05 | 2022-04-06 | Sage Therapeutics Inc | Stéroïdes neuroactifs et leurs procédés d'utilisation |
| WO2020132504A1 (en) | 2018-12-21 | 2020-06-25 | Sage Therapeutics, Inc. | 3.alpha.-hydroxy-17.beta.-amide neuroactive steroids and compositions thereof |
| TW202110824A (zh) | 2019-05-24 | 2021-03-16 | 美商賽吉醫療公司 | 化合物、組合物及使用方法 |
| BR112021024033A2 (pt) | 2019-05-31 | 2022-02-08 | Sage Therapeutics Inc | Esteroides neuroativos e suas composições |
| JP2023504517A (ja) | 2019-12-05 | 2023-02-03 | セージ セラピューティクス, インコーポレイテッド | 19-ノルc3,3-二置換c21-n-ピラゾリルステロイドおよびその使用方法 |
| AU2021238346A1 (en) | 2020-03-18 | 2022-09-29 | Sage Therapeutics, Inc. | Neuroactive steroids and their methods of use |
| US20230346801A1 (en) | 2020-03-25 | 2023-11-02 | Sage Therapeutics, Inc. | Use of agents for treatment of respiratory conditions |
| AR123018A1 (es) | 2020-07-20 | 2022-10-26 | Sage Therapeutics Inc | Formulaciones del esteroide c21-n-pirazolilo 19-nor c3,3-disustituido y métodos de uso de este |
-
2017
- 2017-08-23 JO JOP/2019/0022A patent/JOP20190022B1/ar active
- 2017-08-23 CN CN201780063826.4A patent/CN110088091A/zh active Pending
- 2017-08-23 CN CN202210890025.8A patent/CN115974955A/zh active Pending
- 2017-08-23 CN CN202210890054.4A patent/CN115974956A/zh active Pending
- 2017-08-23 TW TW106128611A patent/TWI808945B/zh active
- 2017-08-23 IL IL302480A patent/IL302480A/en unknown
- 2017-08-23 MA MA046042A patent/MA46042A/fr unknown
- 2017-08-23 AR ARP170102330A patent/AR109393A1/es unknown
- 2017-08-23 MX MX2019002193A patent/MX2019002193A/es unknown
- 2017-08-23 JP JP2019510657A patent/JP2019524853A/ja not_active Withdrawn
- 2017-08-23 SG SG11201901445TA patent/SG11201901445TA/en unknown
- 2017-08-23 EP EP21190443.8A patent/EP3981763A1/en active Pending
- 2017-08-23 AU AU2017315682A patent/AU2017315682B2/en active Active
- 2017-08-23 KR KR1020237017309A patent/KR20230079470A/ko not_active Application Discontinuation
- 2017-08-23 KR KR1020197008069A patent/KR20190040043A/ko not_active Application Discontinuation
- 2017-08-23 CN CN202210890024.3A patent/CN115974954A/zh active Pending
- 2017-08-23 PE PE2019000416A patent/PE20190915A1/es unknown
- 2017-08-23 TW TW112101437A patent/TW202342059A/zh unknown
- 2017-08-23 EP EP17761714.9A patent/EP3504189A1/en not_active Withdrawn
- 2017-08-23 CA CA3034262A patent/CA3034262A1/en active Pending
- 2017-08-23 EA EA201990565A patent/EA201990565A1/ru unknown
- 2017-08-23 BR BR112019003637A patent/BR112019003637A2/pt active Search and Examination
- 2017-08-23 WO PCT/US2017/048267 patent/WO2018039378A1/en active Application Filing
- 2017-08-23 US US16/326,977 patent/US11236121B2/en active Active
-
2019
- 2019-02-19 ZA ZA2019/01051A patent/ZA201901051B/en unknown
- 2019-02-21 PH PH12019500375A patent/PH12019500375A1/en unknown
- 2019-02-22 CL CL2019000477A patent/CL2019000477A1/es unknown
- 2019-02-22 MX MX2022007432A patent/MX2022007432A/es unknown
- 2019-03-20 CO CONC2019/0002596A patent/CO2019002596A2/es unknown
- 2019-03-22 EC ECSENADI201920141A patent/ECSP19020141A/es unknown
- 2019-12-10 CL CL2019003610A patent/CL2019003610A1/es unknown
-
2021
- 2021-08-06 US US17/396,464 patent/US11884696B2/en active Active
-
2022
- 2022-02-08 AU AU2022200811A patent/AU2022200811B9/en active Active
- 2022-04-08 AR ARP220100895A patent/AR125321A2/es unknown
- 2022-04-08 AR ARP220100894A patent/AR125320A2/es unknown
- 2022-11-07 JP JP2022178009A patent/JP2023002846A/ja active Pending
-
2023
- 2023-08-24 US US18/455,324 patent/US20230399357A1/en active Pending
-
2024
- 2024-02-06 AU AU2024200732A patent/AU2024200732A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11884696B2 (en) | Crystalline 19-nor C3,3-disubstituted C21-n-pyrazolyl steroid | |
| TWI815800B (zh) | 氧固醇(oxysterol)及其使用方法 | |
| TWI772331B (zh) | 氧固醇(oxysterol)及其使用方法 | |
| JP2023105082A (ja) | CNS障害を処置するためのジュウテリウム化された21-[4-シアノ-ピラゾール-1-イル]-19-ノル-プレガン-3.α-オール-20-オン誘導体 | |
| TW201930269A (zh) | 用於治療cns病症之組合物及方法 | |
| TW202143976A (zh) | 神經活性類固醇及其使用方法 | |
| TW202038967A (zh) | 神經活性類固醇及其組合物 | |
| CA3226489A1 (en) | Crystalline forms of a neuroactive steroid | |
| OA19368A (en) | A crystalline 19-Nor C3, 3-disubstituted C21-N-Pyrazolyl steroid. | |
| NZ791594A (en) | A crystalline 19-nor C3, 3-disubstituted C21-N-pyrazolyl steroid | |
| EA044239B1 (ru) | Кристаллический 19-нор c3,3-дизамещенный c21-n-пиразолил стероид | |
| TWI835884B (zh) | 神經活性類固醇及其使用方法 | |
| NZ791591A (en) | A crystalline 19-nor C3, 3-disubstituted C21-N-pyrazolyl steroid | |
| WO2023250185A1 (en) | Crystalline forms of a neuroactive steroid | |
| WO2024015201A1 (en) | Crystalline form of a neuroactive steroid | |
| WO2024026337A1 (en) | Crystalline forms of a neuroactive steroid | |
| TW202027753A (zh) | 神經活性類固醇及其使用方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| E902 | Notification of reason for refusal |