KR20210021530A - 신규한 구조적 컴포넌트들을 갖는 나노입자 백신들 - Google Patents
신규한 구조적 컴포넌트들을 갖는 나노입자 백신들 Download PDFInfo
- Publication number
- KR20210021530A KR20210021530A KR1020217001153A KR20217001153A KR20210021530A KR 20210021530 A KR20210021530 A KR 20210021530A KR 1020217001153 A KR1020217001153 A KR 1020217001153A KR 20217001153 A KR20217001153 A KR 20217001153A KR 20210021530 A KR20210021530 A KR 20210021530A
- Authority
- KR
- South Korea
- Prior art keywords
- subunit
- nanoparticle
- vaccine composition
- seq
- nanoparticles
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/002—Protozoa antigens
- A61K39/015—Hemosporidia antigens, e.g. Plasmodium antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/21—Retroviridae, e.g. equine infectious anemia virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/6425—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the peptide or protein in the drug conjugate being a receptor, e.g. CD4, a cell surface antigen, i.e. not a peptide ligand targeting the antigen, or a cell surface determinant, i.e. a part of the surface of a cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6927—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores
- A61K47/6929—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
- A61P33/06—Antimalarials
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55516—Proteins; Peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55555—Liposomes; Vesicles, e.g. nanoparticles; Spheres, e.g. nanospheres; Polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6031—Proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y40/00—Manufacture or treatment of nanostructures
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16111—Human Immunodeficiency Virus, HIV concerning HIV env
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/10011—Arenaviridae
- C12N2760/10034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/14011—Filoviridae
- C12N2760/14111—Ebolavirus, e.g. Zaire ebolavirus
- C12N2760/14134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/18011—Paramyxoviridae
- C12N2760/18511—Pneumovirus, e.g. human respiratory syncytial virus
- C12N2760/18534—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/20011—Coronaviridae
- C12N2770/20034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/24011—Flaviviridae
- C12N2770/24111—Flavivirus, e.g. yellow fever virus, dengue, JEV
- C12N2770/24134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/24011—Flaviviridae
- C12N2770/24211—Hepacivirus, e.g. hepatitis C virus, hepatitis G virus
- C12N2770/24234—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Virology (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Tropical Medicine & Parasitology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Organic Chemistry (AREA)
- Mycology (AREA)
- Communicable Diseases (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oncology (AREA)
- Nanotechnology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- AIDS & HIV (AREA)
- Genetics & Genomics (AREA)
- Hematology (AREA)
- Cell Biology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Plant Pathology (AREA)
- Biochemistry (AREA)
- Optics & Photonics (AREA)
Abstract
본 발명은 잠금 도메인으로 안정화된 신규 나노입자 제시된 백신 조성물들을 제공한다. HIV-1 바이러스 면역원 및 에볼라 바이러스 면역원과 같은 바이러스 면역원, 및 박테리아 종, 기생충들 종 및 포유류 종으로부터 유래된 면역원과 같은 비-바이러스 면역원을 포함하는, 다양한 면역원들이 백신 조성물들의 조제에 채용될 수 있다. 본 발명은 또한 예를 들어, 바이러스 감염들을 예방하거나 치료하기 위한, 다양한 치료 적용예에서 이러한 백신 조성물들을 사용하는 방법들을 제공한다.
Description
관련 출원들에 대한 교차 참조
본 특허 출원은 (2018 년 6 월 13 일 출원된; 현재 계류 중인) 미국 특허 가출원 번호 62/684,229의 우선권의 이익을 주장한다. 우선권 출원의 전체 개시는 이의 전체가 모든 목적들을 위해 참조로서 본 명세서에 인용된다.
정부 지원 성명
본 발명은 미국 국립 보건원이 수여하는 보조금 번호 R01 AI129698-02 및 R56 AI125078-01 하의 정부의 지원으로 이루어졌다. 정부는 본 발명에 일정 권리를 갖는다.
바이러스들과 같은 다양한 병원체의 감염들에 대항하기 위한 백신들의 설계에서 상당한 진전이 있어왔다. 합리적 백신 설계 전략과 HIV-1 백신 분야에서 최근 확립된 신규한 기술들은 상이한 바이러스 병원체들 및 비-바이러스 질병 표적들을 위한 백신 개발에 잠재적인 해결책을 제공한다. 합리적인 백신 설계 전략은 광범위하게 중화항체들 (broadly neutralizing antibodies; bNAb) 의 식별, bNAb-항원 복합체들의 구조 분석, 및 구조-기반 면역원 설계 및 평가로 구성된다. 면역원 설계의 맥락에서, 몇몇의 바이러스들에 대한 외피 (envelope; Env) 단백질들의 안정화 및 재설계에서 그리고 바이러스-유사 입자들 (virus-like particles; VLP들) 또는 유사한 기하 구조의 나노입자들 상의 최적화된 외피 단백질들의 다가 표지 (multivalent presentation) 에서 상당한 획기적인 개발을 보여 왔다. VLP들은 표면 항원들의 큰 크기 및 치밀한 표지 (display) 로 인해 강하고, 오래 지속되는 면역 반응들을 도출할 수 있다. VLP들은 동족 바이러스들에 대한 성공적인 백신들 (인유두종바이러스 (Human Papillomavirus) 에 대한 Gardasil®로서 또는 외래 항원들에 대한 담체들로서 개발되었다. B 세포 활성화를 위한 최적의 항원 간격은 5 내지 10 ㎚만큼 이격된 최소 20 내지 25 개의 에피토프들로 결정되어 왔다. 따라서, VLP의 분자적 특성들 (공-형상, 10 내지 100 nm, 등) 을 갖는 자가-조립 나노입자들은 효과적인 VLP-형 백신들의 개발을 위해 다양한 항원들을 표지하도록 리엔지니어링 (reengineering) 될 수도 있다.
몇몇의 바이러스들에 대한 외피 단백질들의 안정화 및 재설계에서 상당한 진전이 이루어져왔다. 예를 들어, HIV-1 백신 연구는 현재 bNAb들 및 외피 구조들에 축적된 풍부한 정보로 인해 항원 선택 및 평가에 초점을 맞추고 있다. 네이티브-유사 (native-like) 삼량체들은 BG505 SOSIP.664 gp140 삼량체로부터의 유망한 초기 데이터로 인해 바람직한 백신 플랫폼으로서 등장하였다. sc-gp140 및 NFL과 같은, 상이한 gp140 설계들은, 또한 네이티브-유사 삼량체들을 생산하였다. 그러나, 모든 이들 설계들은 비-BG505 외피들에 적용될 때 삼량체 수율, 순도, 및 안정성에서 상당한 손실을 겪을 것이고, 그리고 네이티브-유사 삼량체들을 획득하기 위해 부가적 외피-안정화 돌연변이들 및 복잡한 정제 방법들을 필요로 한다. 최근까지만 해도 외피 준 안정성의 주요 원인은 - gp41 엑토도메인 (gp41 ectodomain) (gp41ECTO) 의 HR1 벤딩 (아미노산 547 내지 아미노산 569) - 이 확인되고 합리적 재설계에 의해 직접적으로 표적화되었다. 발생되는 삼량체 구성 (trimer construct) 은 "절단되지 않은 사전융합-최적화된 (uncleaved prefusion-optimized; UFO)" 설계로 명명된다. gp41ECTO가 외피 준 안정성의 유일한 소스이고, 삼량체 기반 HIV-1 백신 설계를 위한 단순하고, 일반적이고, 그리고 효과적인 전략을 제공하는, UFO 설계의 BG505 gp41ECTO가 실질적인 삼량체 수율, 순도 및 안정성을 갖는 다양한 HIV-1 아형들을 안정화하도록 사용될 수 있다는 것이 또한 최근에 입증되었다.
특히 개별적인 항원들에 대해 관찰된 불량한 면역원성을 고려하여, 백신 후보들로서 외피 항원들을 표지하기 위해 자가-조립 나노입자들의 사용에서 상당한 진전이 이루어져왔다. 예를 들어, HIV-1 삼량체 면역원성은 야생형 (wild-type; WT) 마우스, 인간 Ig 삽입 마우스, 래빗들, 및 비인간 영장류 (non-human primates; NHP) 에서 SOSIP 및 NFL에 대해 평가되었고, WT 마우스에 대해서가 아니라 래빗 및 NHP들에 대해서 자가 티어-2 NAb (autologous tier-2 NAb) 를 이용한 반응들이 관찰되었다. 이러한 티어-2 NAb 반응들의 유도는 종종 6 내지 12 개월의 면역화들을 요구하고, 이는 수용성 삼량체들이 최적 백신 형태가 아닐 수도 있다는 것을 암시한다. 일관되게, 보다 최근의 연구들은 고유한 안정성 및 순도를 갖는, UFO 삼량체들이 고수율 고순도를 갖는 24량체의 페린틴 (ferritin; FR), 60량체의 E2p, 및 60량체의 I3-01을 포함하는 3 개의 나노입자들 상에 표지될 수 있다는 것을 입증하였다. He et al., Nat. Commun. 7:12041, 2016를 참조하라. 이러한 나노입자들은, 처음에는, 8 주 후 마우스에서 주목할만한 티어-2 HIV-1 중화 항체 반응을 도출하였고, 반면에 모든 수용성 삼량체들은 실패하였다. 이러한 나노입자들 중 하나는 6 주 후에 래빗들에서 주목할만한 티어-2HIV-1 중화 항체 반응들을 유도한 반면에, 수용성 삼량체는 이러한 반응들을 개발시키기 위해 또 상이한 8 주 (14 주) 가 요구된다. He et al., Sci. Adv. 4 (11): eaau6769, 2018을 참조하라.
백신 설계의 실질적인 진전에도 불구하고, 예를 들어, 다양한 바이러스 병원체 또는 비-바이러스 병원체들의 감염 (예를 들어, HIV-1 감염) 을 방지하기 위한, 보다 효과적이고 강력한 백신 면역원에 대한 요구들이 여전히 의료 분야에서 존재한다. 본 발명은 당업계의 충족되지 않은 요구들을 해결한다.
일 양태에서, 본 발명은 (1) 자가-조립 나노입자의 표면 상에 표지된 폴리펩타이드 면역원 및 (2) 나노입자 내부에 임베딩되고 (embedded) 자가-조립 나노입자의 서브유닛에 결합된 잠금 도메인을 포함하는 백신 조성물을 제공한다. 이들 백신 조성물들에서, 잠금 도메인은 계면에서 비-공유 상호 작용들을 통해 용액 내 근처의 나노입자 서브유닛에 부착된 또 상이한 잠금 도메인과 자연적으로 이량체를 형성할 수 있는 단백질 서브유닛이다. 일부 실시예들에서, 채용된 잠금 도메인은 또 상이한 동일한 단백질 도메인 또는 서브유닛과 동종이량체를 형성하는 단백질 도메인 또는 서브유닛이다. 이들 실시예들 중 일부에서, 채용된 잠금 도메인의 서브유닛은 서열 번호: 1 내지 서열 번호: 9, 이의 보존적으로 변형된 변이체 또는 이의 실질적으로 동일한 서열 중 임의의 하나에 나타낸 바와 같이 아미노산 서열을 포함한다.
본 발명의 일부 백신 조성물에서, 잠금 도메인은 나노입자의 서브유닛에 공유 결합된다. 이들 실시예들 중 일부에서, 잠금 도메인의 N-말단은 링커 서열을 통해 나노입자 서브유닛의 C-말단에 융합된다. 본 발명의 일부 백신 조성물은 범-반응성 T-세포 에피토프를 부가적으로 포함할 수 있다. 이들 실시예들 중 일부에서, T 세포 에피토프의 N-말단이 잠금 도메인의 C-말단에 융합된다. 본 발명의 일부 백신 조성물은 면역원과 나노입자 서브유닛 사이에 삽입된 넥 영역을 부가적으로 포함할 수 있다. 이들 실시예들에서, 넥 영역은 나노입자의 표면으로부터 보다 멀리 면역원을 상승시키는 3-나선 단백질 도메인일 수 있다. 내부로부터 나노입자들을 안정화시키는 잠금 도메인에 부가적으로, 본 발명의 일부 백신 조성물들은 면역원 폴리펩타이드를 더 안정화시키기 위해 면역원과 나노입자 서브유닛 사이에 삽입된 단백질 도메인을 부가적으로 포함할 수 있다. 일부 바람직한 실시예들에서, 본 발명의 백신 조성물들을 구성하기 위해 활용된 나노입자는 회전 대칭을 갖는 공-형상 나노입자다. 이들 실시예들 중 일부에서, 회전 대칭은 3-폴드 축 및/또는 5-폴드 축을 갖는다. 이들 실시예들 중 일부에서, 채용된 나노입자는 20 면체 구조이다.
본 발명의 일부 백신 조성물들에서, 나노입자 상에 표지된 폴리펩타이드 면역원은 바이러스 면역원이다. 이들 실시예들 중 일부에서, 표지된 폴리펩타이드 면역원은 클래스-I 융합 메커니즘을 활용하는 바이러스로부터의 바이러스 면역원이다. 예시들로서, 면역원은 HIV-1 바이러스, 에볼라 바이러스 (Ebola virus), 마르부르그 바이러스 (Marburg virus), 아레나바이러스들 (Arenaviruses), 호흡기 세포 융합 바이러스들 (respiratory syncytial viruses; RSV), 및 코로나바이러스들 (coronaviruses) 로부터 유도될 수 있다. 일부 상이한 실시예들에서, 표지된 폴리펩타이드 면역원은 클래스-II 융합 메커니즘을 활용하는 바이러스로부터의 바이러스 면역원이다. 예시들로서, 면역원은 HCV 또는 지카 바이러스로부터 유도될 수 있다. 여전히 일부 상이한 실시예들에서, 표지된 폴리펩타이드 면역원은 비-바이러스 면역원이다. 예시들로서, 표지된 면역원은 열대열원충 (Plasmodium falciparum) 으로부터의 항원, 결핵균 (Mycobacterium tuberculosis; TB) 으로부터의 항원, 또는 인간 단백질 전구단백질 (proprotein) 변환 효소 서브틸리신/켁신 9 형 (proprotein convertase subtilisin/kexin type 9; PCSK9) 일 수 있다.
본 발명의 일부 백신 조성들은 HIV-1 외피-유래된 삼량체 단백질을 표지하는 HIV-1 백신이다. 이들 실시예들 중 일부에서, 잠금 도메인의 N-말단은 GGGGS (서열 번호: 17) 의 하나 이상의 탠덤 카피들 (tandem copies) 을 포함하는 링커 서열을 통해 나노입자 서브유닛의 C-말단에 융합된다. 일부 실시예들에서, 백신 조성물은 범-반응성 T-세포 에피토프를 더 포함할 수 있다. 이들 실시예들 중 일부에서, T-세포 에피토프의 N-말단은 잠금 도메인의 C-말단에 융합된다. 이들 실시예들 중 일부에서, T-세포 에피토프는 서열 AKFVAAWTLKAAA (서열 번호: 18) 를 갖는다. 일부 실시예들에서, HIV-1 삼량체 단백질의 서브유닛의 C-말단은 나노입자의 서브유닛의 N-말단에 공유 결합된다. 일부 실시예들에서, HIV-1 삼량체 단백질 서브유닛은 링커 서열을 통해 나노입자 서브유닛에 융합된다. 다양한 실시예들에서, 채용된 링커 서열은 서열 (GaSb)n을 가질 수 있고, 여기서 a는 1 내지 5의 정수이고, b는 1 내지 2의 정수이고, 그리고 n은 1 내지 5의 정수이다.
본 발명의 일부 백신 조성물에서, 자가-조립 나노입자는 삼량체를 형성하는 삼량체성 서열을 갖는다. 이들 실시예들 중 일부에서, 자가-조립 나노입자의 서브유닛은 서열 번호: 26 (페린틴), 서열 번호: 21 (E2p), 서열 번호: 22 (I3-01) 또는 서열 번호: 25 (I3-01 변이체), 이의 보존적으로 변형된 변이체 또는 이의 실질적으로 동일한 서열로 나타낸 바와 같이 서열을 갖는 폴리펩타이드다. 일부 HIV-1 백신 조성물에서, 표지된 HIV-1 외피-유래된 삼량체 단백질은 gp140으로부터 유래된다. 일부 실시예들에서, HIV-1 외피-유래된 삼량체 단백질은 절단되지 않은 사전융합-최적화된 (UFO) gp140 삼량체이다. 이들 실시예들 중 일부에서, UFO gp140 삼량체는 HIV-1 균주 BG505로부터의 변형된 gp41ECTO 도메인을 포함하는 키메라 삼량체이다. 일부 실시예들에서, UFO gp140 삼량체의 서브유닛은 서열 번호: 23에 나타낸 아미노산 서열, 이의 보존적으로 변형된 변이체 또는 이의 실질적으로 동일한 서열을 갖는다.
일부 특정 HIV-1 백신 조성물들은 N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 바와 같이 HIV-1 외피-유래된 UFO gp140 삼량체 서브유닛, 서열 번호: 21에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (E2p), 서열 번호: 1에 나타낸 바와 같이 잠금 도메인 (LD4), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함하는 서브유닛 서열이 포함된다. 이들 실시예들 중 일부에서, 서브유닛 서열은 gp140 삼량체 서브유닛과 나노입자 서브유닛 사이에 제 1 링커 서열 (GGGGS)2 (서열 번호: 24), 및/또는 나노입자 서브유닛과 잠금 도메인 사이에 제 2 링커 서열 GGGGS (서열 번호: 17) 을 더 포함할 수 있다. 일부 상이한 특정 HIV-1 백신 조성물들은 N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 바와 같이 HIV-1 외피-유래된 UFO gp140 삼량체, 서열 번호: 22 또는 서열 번호: 25에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (I3-01), 서열 번호: 2에 나타낸 바와 같이 잠금 도메인 (LD7), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함하는 서브유닛 서열이 포함된다. 이들 실시예들 중 일부에서, 서브유닛 서열은 gp140 삼량체 서브유닛과 나노입자 서브유닛 사이에 제 1 링커 서열 (GGGGS)2 (서열 번호: 24), 및/또는 나노입자 서브유닛과 잠금 도메인 사이에 제 2 링커 서열 GGGGS (서열 번호: 17) 을 더 포함할 수 있다.
관련된 양태에서, 본 발명은 본 명세서에 기술된 백신 조성물들을 포함하는 약제용 조성물들을 제공한다. 약제용 조성물들은 통상적으로 또한 약제용으로 허용가능한 담체를 포함한다. 일부 실시예들에서, 약제용 조성물들은 또한 보조제를 포함할 수 있다.
또 상이한 양태에서, 본 발명은 N-말단에 면역원 폴리펩타이드, 자가-조립 나노입자 서브유닛, 및 잠금 도메인의 서브유닛을 포함하는 융합 단백질을 코딩하는 폴리뉴클레오타이드들을 제공한다. 융합 단백질의 잠금 도메인은 계면에서 비-공유 상호 작용들을 통해 용액에서 근처의 나노입자 서브유닛에 부착된 또 상이한 잠금 도메인과 자연적으로 이량체를 형성할 수 있는 단백질 서브유닛이다. 본 발명의 일부 폴리뉴클레오타이드들에서, 코딩된 융합 단백질의 잠금 도메인은 또 상이한 동일한 단백질 서브유닛과 동종이량체를 형성하는 단백질 서브유닛이다. 일부 실시예들에서, 코딩된 융합 단백질의 면역원 폴리펩타이드는 나노입자 서브유닛의 N-말단에 융합된다. 일부 실시예들에서, 코딩된 융합 단백질의 면역원 폴리펩타이드는 다량체 (multimeric) 단백질의 서브유닛이다. 일부 실시예들에서, 코딩된 융합 단백질의 잠금 도메인은 나노입자 서브유닛의 C-말단에 위치된다. 일부 실시예에서, 코딩된 융합 단백질은 C-말단에 T 세포 에피토프를 더 포함한다. 일부 실시예들에서, 코딩된 융합 단백질의 면역원 폴리펩타이드는 HIV-1 외피-유래된 삼량체 단백질의 서브유닛이다. 이들 실시예들 중 일부에서, 코딩된 융합 단백질은 부가적으로 단백질의 상이한 구성 요소 사이의 하나 이상의 링커 서열을 포함할 수 있다. 이들 실시예들 중 일부에서, 코딩된 융합 단백질은 면역원 폴리펩타이드 및 나노입자 서브유닛 사이에 제 1 링커 서열, 및/또는 나노입자 서브유닛과 잠금 도메인 사이에 제 2 링커 서열을 포함할 수 있다. 다양한 실시예들에서, 채용된 링커 서열들은 각각 독립적으로 (GaSb)n의 서열을 가질 수 있고, 여기서 a는 1 내지 4의 정수이고, b는 1 내지 2의 정수이고, 그리고 n은 1 내지 6의 정수이다.
본 발명의 일부 특정 폴리뉴클레오타이드들은 본 명세서에 기술된 HIV-1 폴리펩타이드 백신 조성물을 코딩한다. 이들 실시예들 중 일부에서, 코딩된 융합 단백질은 N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 UFO gp140 삼량체 서브유닛, 서열 번호: 21에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (E2p), 서열 번호: 1에 나타낸 바와 같이 잠금 도메인 (LD4), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함한다. 일부 실시예들에서, 코딩된 융합 폴리펩타이드는gp140 삼량체 서브유닛과 나노입자 서브유닛 사이에 제 1 링커 서열 (GGGGS) 2(서열 번호: 24), 및/또는 나노입자 서브유닛과 잠금 도메인 사이에 제 2 링커 서열 GGGGS (서열 번호: 17) 를 더 포함할 수 있다. 일부 상이한 실시예들에서, 코딩된 융합 단백질은 N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 바와 같이 UFO gp140 삼량체, 서열 번호: 22 또는 서열 번호: 25에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (I3-01), 서열 번호: 2에 나타낸 바와 같이 잠금 도메인 (LD7), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 을 포함한다. 일부 실시예들에서, 코딩된 융합 폴리펩타이드는gp140 삼량체 서브유닛과 나노입자 서브유닛 사이에 제 1 링커 서열 (GGGGS)2 (서열 번호: 24), 및/또는 나노입자 서브유닛과 잠금 도메인 사이에 제 2 링커 서열 GGGGS (서열 번호: 17) 를 더 포함할 수 있다.
일부 관련된 실시예들에서, 본 발명은 본 명세서에 기술된 폴리뉴클레오타이드들에 의해 코딩된 폴리펩타이드들을 제공한다. 일부 관련된 실시예들에서, 본 발명은 본 명세서에 기술된 폴리뉴클레오타이드들 중 하나 이상을 포함하는 벡터들을 제공한다. 일부 상이한 관련된 실시예들에서, 본 발명은 본 명세서에 기술된 하나 이상의 폴리뉴클레오타이드들 또는 벡터들을 포함하는 약제용 조성물들을 제공한다.
상이한 양태에서, 본 발명은 개체에서 HIV-1 감염을 치료 또는 예방하는 방법을 제공한다. 이들 방법들은 본 명세서에 기술된 HIV-1 폴리펩타이드 백신 조성물의 치료적 유효량을 포함하는 약제용 조성물을 피험자에게 투여하는 것을 수반한다. 이들 실시예들 중 일부에서, 투여된 HIV-1 백신 조성물은 N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 UFO gp140 삼량체 서브유닛, 서열 번호: 21에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (E2p), 서열 번호: 1에 나타낸 바와 같이 잠금 도메인 (LD4), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함한다. 일부 상이한 실시예들에서, 투여된 HIV-1 백신 조성물은: 서열 번호: 23에 나타낸 바와 같이 UFO gp140 삼량체, 서열 번호: 22 또는 서열 번호: 25에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (I3-01), 서열 번호: 2에 나타낸 바와 같이 잠금 도메인 (LD7), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 을 포함한다. 일부 관련된 실시예들에서, 본 발명은 본 명세서에 기술된 폴리뉴클레오타이드 또는 발현 벡터의 치료적 유효량을 포함하는 약제용 조성물을 피험자에게 투여함으로써 피험자에서 HIV-1 감염을 치료하거나 예방하는 방법을 제공한다. 이들 실시예들 중 일부에서, 투여된 폴리뉴클레오타이드 또는 벡터는 N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 UFO gp140 삼량체 서브유닛, 서열 번호: 21에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (E2p), 서열 번호: 1에 나타낸 바와 같이 잠금 도메인 (LD4), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함하는 융합 단백질을 코딩한다. 일부 상이한 실시예들에서, 투여된 폴리뉴클레오타이드 또는 벡터는N-말단으로부터 C-말단까지: 서열 번호: 23에 나타낸 UFO gp140 삼량체 서브유닛, 서열 번호: 22 또는 서열 번호: 25에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (I3-01), 서열 번호: 2에 나타낸 바와 같이 잠금 도메인 (LD7), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함하는 융합 단백질을 코딩한다.
본 발명의 본질 및 이점들의 추가 이해는 명세서 및 청구항들의 나머지 부분들을 참조하여 실현될 수도 있다.
도1은 HIV-1 UFO gp140 나노입자 백신의 구조를 도시한다.
도 2는 본 명세서에 기술된 잠금 도메인 안정화된 HIV-1 나노입자 면역원들의 예를 표현하는 CMV 벡터의 구조를 개략적으로 도시한다.
도 3은 몇몇의 분석들을 통해 CHO/ExpiCHO-생산된 나노입자 단백질들의 품질 평가 결과들을 도시한다.
도 4는 2 개의 잠금 도메인 안정화된 HIV-1 나노입자 면역원들의 항원성 분석 및 구조 분석의 인 비트로 (in vitro) 평가를 도시한다.
도 5는 마우스들 및 래빗들에서 2 개의 예시된 잠금 도메인 안정화된 HIV-1 나노입자 면역원들의 면역원성 활성들의 인 비보 (in vivo) 연구를 도시한다.
도 6은 상이한 잠금 도메인들에 의해 안정화된 HIV-1 나노입자 면역원들의 구성 설계뿐만 아니라 ExpiCHO 세포들에서 일시적으로 발현된 백신 면역원들의 수율 및 순도를 보여주는 크기 배제 크로마토그래피 (size exclusion chromatography; SEC) 프로파일들을 개략적으로 도시한다.
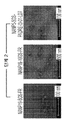
도 7은 상이한 잠금 도메인들로 안정화된 HIV-1나노입자 면역원들의 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (blue native polyacrylamide gel electrophoresis; BN-PAGE) 분석 및 일부 잘-형성된 나노입자들의 매질 염색 (negative-stain) 전자 현미경 (electron microscopy; EM) 이미지들을 도시한다.
도 8은 에볼라 (Ebola) GPMuc 삼량체를 표지하는- 나노입자들의 분자 모델들, 크기 배제 크로마토그래피 (SEC) 및 매질 염색EM 이미지들을 도시하고, 이어서 설계 개념 및 분자 모델들, SEC 및 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (blue native polyacrylamide gel electrophoresis; BN-PAGE) 와 같은 생화학적 분석 및 생물 물리학적 분석, 다양한 잠금 도메인들을 갖는 에볼라 GPMuc 삼량체를 표지하는-나노입자들에 대한 ELISA (enzyme-linked immunosorbent assay) 와 같은 항원 특성화를 도시한다. SEC 프로파일들은 모두 에볼라GPMuc 삼량체들을 표지하는, E2p와 조합된 LD1-LD7 대하여 그리고 I3-01과 조합된 LD4-LD9에 대하여 도시된다.
도 9는 라사 바이러스 (Lassa virus; LASV) GPC 삼량체를 표지하는- 나노입자들의 분자 모델들뿐만 아니라 24-량체 페린틴 나노입자 상의 그리고 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의 GPC 삼량체들의 매질 염색 EM 이미지들을 도시한다.
도 10은 인간 호흡기 세포 융합 바이러스 (human respiratory syncytial virus; hRSV) F 삼량체를 표지하는- 나노입자들의 분자 모델들뿐만 아니라 24-량체 페린틴 나노입자 상의, 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD7 및 PADRE를 갖는 60-량체 I3-01 나노입자 상의 hRSV F 삼량체들의 매질 염색 EM 이미지들을 도시한다.
도 11은 MERS 코로나바이러스 S 삼량체를 표지하는 나노입자들의 분자 모델들뿐만 아니라 24-량체 페린틴 나노입자 상의, 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD7 및 PADRE를 갖는 60-량체 I3-01 나노입자 상의 MERS 코로나바이러스 S 삼량체 파이크들 (pikes) 의 매질 염색 EM 이미지들을 도시한다.
도 12는 백신 개념, 분자 모델, 크기 배제 크로마토그래피 (SEC), 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (BN-PAGE) 및 매질 염색EM 이미지들과 같은 생화학적 분석 및 생물 물리학적 분석, 및 잠금 도메인들을 갖는 C형 간염 바이러스 (hepatitis C virus; HCV) 당단백질 E2 코어를 표지하는-나노입자들 및 잠금 도메인을 갖지 않는 C형 간염 바이러스 당단백질 E2 코어-를 표지하는 나노입자들에 대한 ELISA 바인딩 (binding) 과 같은 항원 특성을 도시한다.
도 13은 지카 바이러스 (Zika virus; ZIKV) DIII-10GS-I3-01 나노입자의 분자 모델을 도시하고, 이어서 24-량체 페린틴 나노입자 상의, 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 나노입자 상에 표지된 DIII 도메인에 대한 크기 배제 크로마토그래피 (SEC), 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (BN-PAGE) 및 매질 염색EM 분석과 같은 생화학적 분석 및 생물 물리학적 분석을 도시한다.
도 14는 열대열원충 (P. falciparum) (말라리아) 항원 Pfs25 및 공지된 중화 항체들을 갖는 이의 복합체의 구조들, 넥 도메인을 갖는 Pfs25 나노입자의 설계 개념, 및 모두 Pfs25와 나노입자 사이에 삽입된 넥 도메인을 갖는, 24-량체 페린틴 나노입자 상의, 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD4 및 PADRE를 갖는 60-량체 I3-01 상의 Pfs2의 매질 염색 EM 이미지들을 도시한다.
도 15는 열대열원충 (plasmodium falciparum) (말라리아) 항원 포자소체 단백질 (circumsporozoite protein; CSP) 의 개략적 조성물, GSK RTS, S 백신의 개략적 조성물, CSP 기반 나노입자 백신을 설계하기 위한 단계적 전략의 플로우차트 (flowchart), 60-량체 페린틴 상의 그리고 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 나노입자 상의 항원 CSP의 다양한 컴포넌트들의 매질 염색 EM 이미지들, 및 크기 배제 크로마토그래피 (SEC) 프로파일들을 도시한다.
도 16은 단백질 전구단백질 (proprotein) 변환 효소 서브틸리신/켁신 9 형 (proprotein convertase subtilisin/kexin type 9; PCSK9) 의 구조, 넥 도메인을 갖는 PCSK9 나노입자의 설계 개념, 및 모두 PCSK9 와 나노입자 사이에 삽입된 넥 도메인을 갖는, 24-량체 페린틴 나노입자 상의 그리고 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 나노입자 상의 PCSK9의 매질 염색 EM 이미지들을 도시한다.
도 2는 본 명세서에 기술된 잠금 도메인 안정화된 HIV-1 나노입자 면역원들의 예를 표현하는 CMV 벡터의 구조를 개략적으로 도시한다.
도 3은 몇몇의 분석들을 통해 CHO/ExpiCHO-생산된 나노입자 단백질들의 품질 평가 결과들을 도시한다.
도 4는 2 개의 잠금 도메인 안정화된 HIV-1 나노입자 면역원들의 항원성 분석 및 구조 분석의 인 비트로 (in vitro) 평가를 도시한다.
도 5는 마우스들 및 래빗들에서 2 개의 예시된 잠금 도메인 안정화된 HIV-1 나노입자 면역원들의 면역원성 활성들의 인 비보 (in vivo) 연구를 도시한다.
도 6은 상이한 잠금 도메인들에 의해 안정화된 HIV-1 나노입자 면역원들의 구성 설계뿐만 아니라 ExpiCHO 세포들에서 일시적으로 발현된 백신 면역원들의 수율 및 순도를 보여주는 크기 배제 크로마토그래피 (size exclusion chromatography; SEC) 프로파일들을 개략적으로 도시한다.
도 7은 상이한 잠금 도메인들로 안정화된 HIV-1나노입자 면역원들의 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (blue native polyacrylamide gel electrophoresis; BN-PAGE) 분석 및 일부 잘-형성된 나노입자들의 매질 염색 (negative-stain) 전자 현미경 (electron microscopy; EM) 이미지들을 도시한다.
도 8은 에볼라 (Ebola) GPMuc 삼량체를 표지하는- 나노입자들의 분자 모델들, 크기 배제 크로마토그래피 (SEC) 및 매질 염색EM 이미지들을 도시하고, 이어서 설계 개념 및 분자 모델들, SEC 및 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (blue native polyacrylamide gel electrophoresis; BN-PAGE) 와 같은 생화학적 분석 및 생물 물리학적 분석, 다양한 잠금 도메인들을 갖는 에볼라 GPMuc 삼량체를 표지하는-나노입자들에 대한 ELISA (enzyme-linked immunosorbent assay) 와 같은 항원 특성화를 도시한다. SEC 프로파일들은 모두 에볼라GPMuc 삼량체들을 표지하는, E2p와 조합된 LD1-LD7 대하여 그리고 I3-01과 조합된 LD4-LD9에 대하여 도시된다.
도 9는 라사 바이러스 (Lassa virus; LASV) GPC 삼량체를 표지하는- 나노입자들의 분자 모델들뿐만 아니라 24-량체 페린틴 나노입자 상의 그리고 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의 GPC 삼량체들의 매질 염색 EM 이미지들을 도시한다.
도 10은 인간 호흡기 세포 융합 바이러스 (human respiratory syncytial virus; hRSV) F 삼량체를 표지하는- 나노입자들의 분자 모델들뿐만 아니라 24-량체 페린틴 나노입자 상의, 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD7 및 PADRE를 갖는 60-량체 I3-01 나노입자 상의 hRSV F 삼량체들의 매질 염색 EM 이미지들을 도시한다.
도 11은 MERS 코로나바이러스 S 삼량체를 표지하는 나노입자들의 분자 모델들뿐만 아니라 24-량체 페린틴 나노입자 상의, 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD7 및 PADRE를 갖는 60-량체 I3-01 나노입자 상의 MERS 코로나바이러스 S 삼량체 파이크들 (pikes) 의 매질 염색 EM 이미지들을 도시한다.
도 12는 백신 개념, 분자 모델, 크기 배제 크로마토그래피 (SEC), 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (BN-PAGE) 및 매질 염색EM 이미지들과 같은 생화학적 분석 및 생물 물리학적 분석, 및 잠금 도메인들을 갖는 C형 간염 바이러스 (hepatitis C virus; HCV) 당단백질 E2 코어를 표지하는-나노입자들 및 잠금 도메인을 갖지 않는 C형 간염 바이러스 당단백질 E2 코어-를 표지하는 나노입자들에 대한 ELISA 바인딩 (binding) 과 같은 항원 특성을 도시한다.
도 13은 지카 바이러스 (Zika virus; ZIKV) DIII-10GS-I3-01 나노입자의 분자 모델을 도시하고, 이어서 24-량체 페린틴 나노입자 상의, 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 나노입자 상에 표지된 DIII 도메인에 대한 크기 배제 크로마토그래피 (SEC), 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (BN-PAGE) 및 매질 염색EM 분석과 같은 생화학적 분석 및 생물 물리학적 분석을 도시한다.
도 14는 열대열원충 (P. falciparum) (말라리아) 항원 Pfs25 및 공지된 중화 항체들을 갖는 이의 복합체의 구조들, 넥 도메인을 갖는 Pfs25 나노입자의 설계 개념, 및 모두 Pfs25와 나노입자 사이에 삽입된 넥 도메인을 갖는, 24-량체 페린틴 나노입자 상의, 잠금 도메인 LD4 및 T-세포 에피토프 PADRE를 갖는 60-량체 E2p 나노입자 상의, 그리고 잠금 도메인 LD4 및 PADRE를 갖는 60-량체 I3-01 상의 Pfs2의 매질 염색 EM 이미지들을 도시한다.
도 15는 열대열원충 (plasmodium falciparum) (말라리아) 항원 포자소체 단백질 (circumsporozoite protein; CSP) 의 개략적 조성물, GSK RTS, S 백신의 개략적 조성물, CSP 기반 나노입자 백신을 설계하기 위한 단계적 전략의 플로우차트 (flowchart), 60-량체 페린틴 상의 그리고 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 나노입자 상의 항원 CSP의 다양한 컴포넌트들의 매질 염색 EM 이미지들, 및 크기 배제 크로마토그래피 (SEC) 프로파일들을 도시한다.
도 16은 단백질 전구단백질 (proprotein) 변환 효소 서브틸리신/켁신 9 형 (proprotein convertase subtilisin/kexin type 9; PCSK9) 의 구조, 넥 도메인을 갖는 PCSK9 나노입자의 설계 개념, 및 모두 PCSK9 와 나노입자 사이에 삽입된 넥 도메인을 갖는, 24-량체 페린틴 나노입자 상의 그리고 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 나노입자 상의 PCSK9의 매질 염색 EM 이미지들을 도시한다.
I
개요
본 발명은 부분적으로 다양한 바이러스 표적 또는 비-바이러스 표적 (예를 들어, HIV-1 외피, Ebola GP, HCV E2 단백질 또는 M. 결핵 항원들) 에 대한 본 발명자들의 신규 백신 면역원들의 개발 및 개선된 안정성 및 활성을 입증하는 나노입자-표지된 면역원들 (즉, 백신 조성물들) 을 전제로 한다. 통상적으로, 본 발명의 백신들 또는 백신 조성물들은 자가-조립 나노입자 또는 바이러스-유사 입자 (virus-like particle; VLP) 상에 표지되는 면역원 폴리펩타이드 또는 단백질 (예를 들어, HIV-1 외피-유래된 삼량체 단백질) 을 포함한다. 나노입자 백신들은 또한 본 명세서에 기술된 하나 이상의 신규 구조적 컴포넌트들을 포함한다. 이들 부가적 구조적 컴포넌트들은 나노입자들의 표면 상에 면역원 표지를 쉽게 하고, 표지된 면역원들의 안정성을 향상시키고, 그리고/또는 자가-조립된 단백질 백신들의 수율 및 순도를 개선하도록 기능한다. 일부 실시예들에서, 본 발명의 나노입자 백신들은 나노입자를 안정화시키는 잠금 도메인을 포함한다. 본 명세서의 예들에서 구체화된 바와 같이, 면역원 폴리펩타이드 (예를 들면, HIV-1 외피 유래된 삼량체 단백질) 를 표지하는 나노입자가 제조, 백신 제제화, 및 면역화 (immunization) 동안 온전히 남아있도록 잠금 도메인은 내부로부터 나노입자들을 안정화한다. 이렇게 구성된 신규 백신 면역원들은 현저하게 향상된 안정성을 갖는다. 또한, 잠금 메커니즘은 나노입자 플랫폼들과 독립적이다. 본 명세서에 예시된 바와 같이 (예를 들어, HIV-1 백신), 이는 SEC, BN-PAGE, DSC, 매질 염색 EM 및 항원 프로파일링으로 나타낸 바와 거의 동일한 결과들을 갖는, 상이한 나노입자들, 예를 들어, 60-량체 I3-01 및 E2p 나노입자들에 적용될 수 있다.
잠금 도메인 외에, 백신들을 코딩하는 구성들은 부가적으로 또는 대체 가능하게 다양한 상이한 구조적 컴포넌트들을 포함할 수 있다. 예를 들어, T4 피브리틴 ("폴돈 (foldon)") 의 삼량체화 모티프와 같은, 면역원 폴리펩타이드를 안정화시키도록, 또는 3-나선 다발 ("넥 도메인") 과 같은 나노입자 표면으로부터 면역원 폴리펩타이드를 상승시키도록, 또는 공지된 바인딩 항체들을 갖는 단백질 도메인과 같은, 면역 친화도 정제를 쉽게 하도록 역할을 하는 단백질 도메인의 코딩 서열이 면역원 폴리펩타이드 서열과 나노입자 서브유닛 서열 사이에 부가될 수 있다. 화학적 접합을 위한 활성 부위로서 역할을 하는 폴리펩타이드 단편 또는 모티프의 코딩 서열은 적절한 위치에서 구성 내로 삽입될 수 있다. CD4+ T-헬퍼 에피토프 또는 CD8+ T-세포 에피토프와 같은 부가적 구조적 컴포넌트들은 또한 본 명세서에 기술된 바와 같이 적절한 위치에서 구성 내로 삽입될 수 있다. 본 명세서에 예시된 바와 같이, 하나 이상의 링커들 (링커 서열들, 모티프들 또는 모이어티들) 이 구성들에서 다양한 구조적 컴포넌트들을 연결하도록 사용될 수 있다.
본 명세서에 상세히 기술된 바와 같이, 본 발명의 백신 조성물들은 본 명세서에 기술된 구조적 컴포넌트들의 동작 가능하게 연결된 코딩 서열들을 포함하는 구성들로부터 발현되고 자가-조립된다. 구성들에서, 면역원 폴리펩타이드 코딩 서열은 이의 나노입자 서브유닛 코딩 서열의 C-말단에서 나노입자 서브유닛 코딩 서열의 N-말단에 직접적으로 또는 간접적으로 융합된다. 상이한 구조적 컴포넌트들을 코딩하는 서열들은 본 명세서에 기술된 바와 같이 적절한 위치들에서 구성들 내로 삽입된다. 예를 들어, 잠금 도메인이 사용될 때, 잠금 도메인 코딩 서열은 나노입자 서브유닛 코딩 서열의 C-말단에 직접적으로 또는 간접적으로 융합될 수 있다.
본 명세서에 예시된 나노입자 백신 구성들은 표면 상에 표지된 네이티브-유사 항원 구조들, 향상된 네이티브-유사 항원 프로파일들, 및 동물들에서 향상된 면역원성을 갖는, 고수율, 고순도, 및 고안정성을 입증하였다. 예를 들어, HIV-1 나노입자 백신들은 6 내지 8 주 이내의 야생형 마우스들 및 래빗들에서 티어-2 자가 중화 항체 반응들 (autologous neutralizing antibody responses) 을 도출하였고, 반면에 수용성 삼량체는 마우스들에서 어떠한 티어-2 중화 항체를 유도할 수 없고 항체 도출을 위해 2 내지3 달의 최소 시간이 필요하다. 따라서, 본 발명의 개선된 HIV-1 백신 면역원들은 백신 생산에보다 적합하고 백신 접종 시 보다 우수한 면역 반응들을 가능하게 한다.
본 명세서에 달리 명시되지 않는 한, 본 발명의 백신 면역원들, 코딩 폴리뉴클레오타이드들, 발현 벡터들 및 숙주 세포들뿐만 아니라 관련된 치료적 적용들은 모두 본 명세서에 예시된 절차들 또는 당업계에 공지된 통상적으로 실시되는 방법들에 따라 생성되거나 수행될 수 있다. 예를 들어, Methods in Enzymology, Volume 289: Solid-Phase Peptide Synthesis, J. N. Abelson, M. I. Simon, G. B. Fields (Editors), Academic Press; 1st edition (1997) (ISBN-13: 978-0121821906); U.S. Pat. Nos. 4,965,343, 및 5,849,954; Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, N.Y., (3rd ed., 2000); Brent et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc. (ringbou ed., 2003); Davis et al., Basic Methods in Molecular Biology, Elsevier Science Publishing, Inc., New York, USA (1986); or Methods in Enzymology: Guide to Molecular Cloning Techniques Vol. 152, S. L. Berger and A. R. Kimmerl Eds., Academic Press Inc., San Diego, USA (1987); Current Protocols in Protein Science (CPPS) (John E. Coligan, et. al., ed., John Wiley and Sons, Inc.), Current Protocols in Cell Biology (CPCB) (Juan S. Bonifacino et. al. ed., John Wiley and Sons, Inc.), 및Culture of Animal Cells: A Manual of Basic Technique by R. Ian Freshney, Publisher: Wiley-Liss; 5th edition (2005), Animal Cell Culture Methods (Methods in Cell Biology, Vol. 57, Jennie P을 참조하라. 다음의 섹션들은 본 발명의 조성물들 및 방법들을 실시하기 위한 부가적 지침을 제공한다.
II.
정의
달리 정의되지 않는 한, 본 명세서에 사용된 모든 기술적 용어 및 과학적 용어는 본 발명이 속하는 기술 분야에서 통상의 지식을 가진자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 이하의 참조들은 본 발명에서 사용된 많은 용어들의 일반적인 정의를 당업자에게 제공한다: Academic Press Dictionary of Science and Technology, Morris (Ed.), Academic Press (1st ed., 1992); Oxford Dictionary of Biochemistry and Molecular Biology, Smith et al. (Eds.), Oxford University Press (revised ed., 2000); Encyclopaedic Dictionary of Chemistry, Kumar (Ed.), Anmol Publications Pvt. Ltd. (2002); Dictionary of Microbiology and Molecular Biology, Singleton et al. (Eds.), John Wiley & Sons (3rd ed., 2002); Dictionary of Chemistry, Hunt (Ed.), Routledge (1st ed., 1999); Dictionary of Pharmaceutical Medicine, Nahler (Ed.), Springer-Verlag Telos (1994); Dictionary of Organic Chemistry, Kumar and Anandand (Eds.), Anmol Publications Pvt. Ltd. (2002); 및A Dictionary of Biology (Oxford Paperback Reference), Martin and Hine (Eds.), Oxford University Press (4th ed., 2000). 본 발명에 구체적으로 적용되는 이들 용어들 중 일부 추가 설명이 본 명세서에 제공된다.
본 명세서에 사용된 바와 같이, 단수 형태들 "a", "an"및 "the"는 문맥이 달리 명확하게 나타내지 않는 한, 단수뿐만 아니라 복수 둘 다를 지칭한다. 예를 들어, "외피-유래된 삼량체 (an Env-derived trimer)"는 단일의 외피-유래된 삼량체 분자 또는 복수의 외피-유래된 삼량체 분자들 둘 다를 지칭할 수 있고, 어구 "적어도 하나의 외피-유래된 삼량체 (at least one Env-derived trimer)"와 동등한 것으로 간주될 수 있다.
본 명세서에 사용된 바와 같이, 용어들 "항원 (antigen)" 또는 "면역원 (immuigen)"은 피험자에서 면역 반응을 유도할 수 있는 물질, 통상적으로 단백질을 지칭하도록 상호교환 가능하게 사용된다. 이 용어는 또한 일단 피험자에게 투여되면 (직접적으로 또는 피험자에게 단백질을 코딩하는 뉴클레오타이드 서열 또는 벡터를 투여함으로써) 그 단백질에 대한 체액형 및/또는 세포형 면역 반응을 도출할 수 있다는 점에서 면역학적으로 활성인 단백질들을 지칭한다. 달리 언급되지 않는 한, 용어 "백신 면역원"은 "단백질 항원” 또는 "면역원 폴리펩타이드"와 상호교환 가능하게 사용된다.
용어 "보존적으로 변형된 변이체 (conservatively modified variant)"는 아미노산 및 핵산 서열들 둘 다에 적용된다. 특정 핵산 서열들과 관련하여, 보존적으로 변형된 변이체들은 동일하거나 본질적으로 동일한 아미노산 서열들을 코딩하는, 또는 본질적으로 동일한 서열들로 핵산이 아미노산 서열을 코딩하지 않는, 이들 핵산들을 지칭한다. 유전 코드의 축퇴 (degeneracy) 로 인해, 많은 수의 기능적으로 동일한 핵산이 임의의 주어진 단백질을 코딩한다. 폴리펩타이드 서열들에 대해, "보존적으로 변형된 변이체들"은 유사한 전하를 갖는 측쇄를 갖는 상이한 아미노산 잔기들로 대체된, 보존적 아미노산 치환들을 갖는 변이체를 지칭한다. 유사한 전하를 갖는 측쇄들을 갖는 아미노산 잔기들의 패밀리는 당업계에 규정되었다. 이들 패밀리는 염기성 측쇄들 (예를 들어, 리신, 아르기닌, 히스티딘), 산성 측쇄들 (예를 들어, 아스파라긴산, 글루타민산), 비대전 (uncharged) 극성 측쇄들 (예를 들어, 글라이신, 아스파라긴, 글루타민, 세린, 트레오닌, 타이로신, 시스테인), 비극성 측쇄들 (예를 들어, 알라닌, 발린, 류신, 이소류신, 프롤린, 페닐알라닌, 메티오닌, 트립토판), 베타-분지된 측쇄들 (예를 들어, 트레오닌, 발린, 이소류신) 및 방향족 측쇄들 (예를 들어, 티로신, 페닐알라닌, 트립토판, 히스티딘) 을 갖는 아미노산들을 포함한다.
에피토프 (epitope) 는 항원 결정자를 지칭한다. 이들은 특정 면역 반응을 도출하도록, 예를 들어, 에피토프가 B 세포 및/또는 T 세포가 반응하는 항원의 영역이도록, 항원성인 분자 상의 특정 화학 기들 또는 펩타이드 서열들이다. 에피토프들은 연속적인 아미노산들 또는 단백질의 3 차 폴딩에 의해 병치된 비 연속적인 아미노산들 둘 다로부터 형성될 수 있다.
백신 또는 상이한 제제의 유효량 (effective amount) 은 상태 또는 에이즈와 같은, 질병의 징후 (sign) 또는 증상 (symptom) 을 감소시키거나 제거하는 것과 같은, 목표된 반응을 생성하기에 충분한 것이다. 예를 들어, 이는 바이러스 복제를 억제하기 위해 또는 HIV-1 감염의 경우에 T 세포 수의 향상과 같은, 바이러스 감염의 외향적 증상들을 측정 가능하게 변경하기 위해 필요한 양일 수 있다. 일반적으로, 이 양은 바이러스 (예를 들어, HIV) 복제 또는 감염을 측정 가능하게 억제하기에 충분할 것이다. 피험자에게 투여될 때, 일반적으로 바이러스 복제의 인 비트로 억제를 달성하는 것으로 나타낸 (예를 들어, 림프구에서) 표적 조직 농도들을 달성할 용량들 (dosage) 이 사용될 것이다. 일부 실시예들에서, "유효량"은 예를 들어, HIV-1 감염을 치료하기 위해 모든 이상 또는 질병의 하나 이상의 증상들 및/또는 기저 원인들을 치료하는 (예방을 포함하는) 것이다. 일부 실시예들에서, 유효량은 치료 유효량이다. 일부 실시예들에서, 유효량은 에이즈와 연관된 하나 이상의 징후들 또는 증상들과 같은, 특정 질병 또는 상태의 하나 이상의 징후들 또는 증상들이 발생하는 것을 방지하는 양이다.
본 명세서에 사용된 바와 같이, 융합 단백질은 단일 단백질을 만들기 위해, 펩타이드 본드 (bond) 를 통해, 함께 접합된 적어도 2 개의 관련되지 않은 단백질들로부터의 아미노산 서열을 포함하는 재조합 단백질이다. 관련되지 않은 아미노산 서열들은 서로 직접적으로 접합 (join) 될 수 있거나 또는 링커 서열을 사용하여 접합될 수 있다. 본 명세서에 사용된 바와 같이, 단백질들은 이들의 천연 환경(들) 에서 (예를 들어, 세포 내부에서) 펩타이드 본드를 통해 함께 접합된 아미노산 서열이 정상적으로 발견되지 않는다면, 관련이 없다. 예를 들어, B. 스테로써모필러스 (B. stearothermophilus) 디하이드로리포일 아실스텐스퍼레이즈 (dihydrolipoyl acyltransferase) (E2p) 와 같은 박테리아 효소의 아미노산 서열들 및 HIV-1 gp120 또는 gp41 당단백질들의 아미노산 서열들은 일반적으로 펩타이드 본드를 통해 함께 접합된 것으로 발견되지 않는다.
헵타드 반복 (heptad repeat; HR) 은 7 개의 아미노산의 반복되는 패턴으로 구성된 구조적 모티프를 지칭한다: abcdefg HPHCPC. 여기서 H는 소수성 잔기들을 나타내고, C는, 통상적으로, 대전된 잔기들을 나타내고, 그리고 P는 극성 (그리고, 따라서, 친수성) 잔기들을 나타낸다.
HIV-1 외피 단백질 (Env) 은 처음에 gp160으로 지정된 845 내지 870 개의 아미노산 크기 보다 긴 전구체 단백질 (precursor protein) 로서 합성된다. gp160은 동종삼량체를 형성하고 골지체 내에서 글리코실화를 겪는다. 인 비보, gp160 당단백질은 성숙한 외피 당단백질 gp120 및 gp41로 엔도-단백질 분해적으로 (endo-proteolytically) 처리되고, 이는 바이러스의 표면 상의 복합체에서 서로 비공유적으로된다. gp120 표면 단백질은 인간 CD4에 대한 고친화도 바인딩 부위, HIV에 대한 1 차 수용체뿐만 아니라 케모카인 (chemokine) 수용체 CCR5 및 CXCR4와 같은 융합 공 수용체와 상호 작용하는 도메인들을 포함한다. gp41 단백질은 바이러스 막에 걸쳐 있고 아미노-말단에서 바이러스 막 및 세포 막의 융합에 중요한 아미노산 서열을 포함한다. HIV-1 외피 당단백질 복합체의 천연, 융합-능력 (fusion-competent) 형태는 3 개의 gp120 서브유닛 및 3 개의 gp41 서브유닛으로 구성된 삼량체 구조이다. 수용체-바인딩 (CD4 및 공-수용체) 부위들은 gp120 모이어티들에 위치되고, 반면에 융합 펩타이드들은 gp41 컴포넌트들에 위치된다. 야생형 gp160 폴리펩타이드들의 예시적인 서열은 예를 들어, 수탁 번호들 AAB05604 및 AAD12142하에 GenBank에 나타낸다.
gp140은 모든 gp120 및 전체 gp41 엑토도메인 (ectodomain) 을 포함하는, HIV 외피 단백질의 올리고머 형태를 지칭한다. 본 명세서에 사용된 바와 같이, HIV-1 gp140 삼량체 면역원은 통상적으로 gp140 도메인 및 변형되거나 재설계된 gp140의 엑토도메인 (gp41ECTO) 을 포함한다.
gp120은 인간 면역 결핍 바이러스 (HIV) 의 외피 단백질이다. gp120은 대부분의 외부, 표면-노출된, HIV 외피 당단백질 복합체의 도메인들을 포함하고, 그리고 이는 세포 CD4 수용체들 및 (CCR5 와 같은) 세포 케모카인 수용체들 둘 다에 바인딩하는 gp120이다. 성숙한 gp120 야생형 폴리펩타이드는 1 차 서열에 약 500 개의 아미노산들을 갖는다. Gp120은 강하게 N-글리코실화되어 120 kD의 겉보기 분자량 (apparent molecular weight) 을 발생시킨다. 폴리펩타이드는 5 개의 보존된 영역들 (C1-05) 및 5 개의 고 가변성의 영역 (V1 내지 V5) 으로 구성된다. 3 차 구조에서, gp120 당단백질은 3 개의 주요 구조적 도메인들 (외측 도메인, 내측 도메인, 및 브리징 시트 (bridging sheet)) 에 추가로 가변 루프들로 구성된다. 예를 들어, Wyatt et al., Nature 393, 705-711, 1998; 및 Kwong et al, Nature 393, 649-59, 1998을 참조하라. 내측 도메인은 gp41 외피 당단백질과 상호 작용하는 것으로 여겨지지만, 외측 도메인은 조립된 외피 당단백질 삼량체 상에 노출된다.
gp120의 가변 영역 1 및 가변 영역 2 (V1/V2 도메인) 는 HIV-1의 대부분의 가변 부분들 (V1 루프 및 V2 루프) 중 2 개를 포함하는 약 50 내지 90 개의 잔기들로 구성되고, 그리고 V1/V2 도메인의 10 개의 잔기 중 하나는 N-글리코실화된다.
gp41은 전구체 HIV 외피 단백질의 단백질 분해 생성물이다. 이는 N-말단 융합 펩타이드 (N-terminal fusion peptide; FP), 막횡단 (transmembrane) 도메인뿐만 아니라 융합 펩타이드 및 막횡단 도메인을 연결하는 엑토도메인을 포함한다. gp41은 삼량체 구성으로 남아 있고 비-공유 방식으로 gp120과 상호 작용한다. 예시적인 gp41의 아미노산 서열은 수탁 번호 CAD20975하에, GenBank에 제시된다.
BG505 SOSIP.664 gp140은 클레이드-A 균주 BG505로부터의 gp140 삼량체를 사용하여 개발된 HIV-1 외피 면역원이다. 이는 절단된 gp120과 엔지니어링된 디설파이드 본드 (SOS로 명명됨) 를 갖는 gp41 ECTO 사이의 공유 결합을 포함한다. 또한, 이는 사후-융합 (post-fusion) 입체형태 (conformation) 를 불안정화하도록 I559P 돌연변이 (IP로 명명됨) 를 갖고 또한 용해도를 개선하도록 잔기 664에서 막-근위 외부 영역 (membrane-proximal external region; MPER) 의 절단 (truncation) 을 갖는다. 이 HIV-1 면역원은 뛰어난 항원 프로파일 및 천연 스파이크 (native spike) 의 우수한 구조적 모방 (structural mimicry) 을 갖는다. 분류 프로브로서 SOSIP 삼량체를 사용하여, 신규한 bNAb들이 식별되고 특성화되어 왔다. SOSIP 설계는 또한 상이한 HIV-1 균주들로 확장되었고 부가적 안정화 돌연변이들의 통합이 허용되었다. 최근, 인간 백신 임상들을 위한 길을 닦는, 래빗들 및 비인간 영장류들에서 SOSIP 삼량체의 면역원성이 보고되었다.
면역원은 병원체에 감염되거나 감염될 위험이 있는 포유류와 같은, 포유류에서 면역 반응을 유도할 수 있는 단백질 또는 이의 일부다. 면역원의 투여는 관심 있는 병원체에 대한 보호 면역 및/또는 사전 면역 (protective immunity) 을 야기할 수 있다.
면역 반응은 자극에 대한, B 세포, T 세포, 또는 단핵구와 같은, 면역 시스템의 세포 반응을 지칭한다. 일부 실시예에서, 반응은 특정 항원에 대해 특이적다 ("항원-특이 반응"). 일부 실시예들에서, 면역 반응은 CD4+ 반응 또는 CD8+ 반응과 같은, T 세포 반응이다. 일부 상이한 실시예들에서, 반응은 B 세포 반응이고, 특이 항체들의 생성을 야기한다.
면역원성 조성물은 면역원성 폴리펩타이드를 발현하는 바이러스에 대해 측정 가능한 CTL 반응을 유도하거나, 또는 면역원성 폴리펩타이드에 대한 측정 가능한 (항체의 생성과 같은) B 세포 반응을 유도하는 면역원성 폴리펩타이드를 포함하는 조성물을 지칭한다.
둘 이상의 핵산 서열들, 또는 둘 이상의 아미노산 서열들 사이의 서열 동일성 또는 유사성은, 서열들 사이의 동일성 또는 유사성의 측면에서 표현된다. 서열 동일성은 동일성 백분율의 측면에서 측정될 수 있다; 백분율이 보다 높을수록, 서열들이 보다 동일하다. 비교 윈도우 (comparison window), 또는 다음의 서열 비교 알고리즘들 중 하나를 사용하여 측정되거나 또는 수동 정렬 (comparison window) 및 육안 검사 (visual inspection) 에 의해 지정된 영역 (designated region) 에 걸쳐 최대 대응 (maximum correspondence) 을 위해 비교 및 정렬될 때, 2 개의 서열이 동일한 아미노산 잔기들 또는 뉴클레오타이드들의 명시된 백분율 (즉, 전체 서열에 걸쳐, 명시된 영역에 대해 60 % 동일성, 선택 가능하게 65 %, 70 %, 75 %, 80 %, 85 %, 90 %, 95 % 또는 99 % 동일성, 또는 명시되지 않은 경우) 을 갖는 경우, 2 개의 서열은 "실질적으로 동일"하다. 선택 가능하게, 동일성은 적어도 길이가 약 50 개의 뉴클레오타이드 (또는 10 개의 아미노산) 인 영역에 걸쳐, 또는 보다 바람직하게 길이가 100 내지 500 개 또는 1000 개 이상인 뉴클레오타이드 (또는 20개, 50 개, 200 개 이상의 아미노산들) 인 영역에 걸쳐 존재한다.
핵산 또는 아미노산 서열의 상동체 (Homologs) 또는 종분화적 상동체 (orthologs) 는 표준 방법을 사용하여 정렬될 때 상대적으로 높은 정도의 서열 동일성/유사성을 갖는다. 비교를 위한 서열들의 정렬 방법들은 당업계에 잘 공지되어 있다. 다양한 프로그램들 및 정렬 알고리즘들은: Smith & Waterman, Adv. Appl. Math. 2:482, 1981; Needleman & Wunsch, J. Mol. Biol. 48:443, 1970; Pearson & Lipman, Proc. Natl. Acad. Sci. USA 85:2444, 1988; Higgins & Sharp, Gene, 73:237-44, 1988; Higgins & Sharp, CABIOS 5:151-3, 1989; Corpet et al., Nuc. Acids Res. 16:10881-90, 1988; Huang et al. Computer Appls. in the Biosciences 8, 155-65, 1992; 및 Pearson et al., Meth. Mol. Bio. 24:307-31, 1994. Altschul et al., J. Mol. Biol. 215:403-10, 1990에 기술되고, 서열 정렬 방법들 및 상동성 (homology) 산출들의 상세한 고려 사항을 나타낸다.
용어 "피험자"는 포유 동물, 예를 들어, 인간 및 비-인간 포유 동물들로서 분류된 임의의 동물을 지칭한다. 비-인간 동물들의 예들은 개들, 고양이들, 소들, 말들, 양들, 돼지들, 염소들, 래빗들, 등을 포함한다. 달리 언급되지 않는 한, 용어 "환자” 또는 "피험자"는 본 명세서에 상호교환 가능하게 사용된다. 바람직하게, 피험자는 인간이다.
용어 "치료하는 (treating)” 또는 "완화시키는 (alleviating)"은 질병 (예를 들어, HIV 감염) 의 증상들, 합병증들 (complications), 또는 생화학적 지표 의 온셋 (onset) 을 예방하거나 지연시키기 위해, 증상을 완화시키거나 질병, 상태, 또는 이상의 추가 발달을 저지하거나 (arresting) 억제하는 것을 포함한다. 치료를 필요로 하는 피험자들은 이미 질병 또는 이상으로 고통 받고 있는 이들뿐만 아니라 이 이상이 발전할 위험이 있는 이들을 포함한다. 치료는 (질병의 온셋를 예방하거나 지연시키거나, 또는 이의 임상적 증상 또는 무증상적 증상의 징후 (manifestation) 를 예방하기 위한) 예방적 (prophylactic) 또는 질병의 징후 이후 증상들의 치료적 억제 또는 완화일 수도 있다.
절단되지 않은 사전-융합-최적화 (UFO) 삼량체들은 gp120 단백질 및 재설계된 gp41ECTO도메인으로 형성된 HIV-1 gp140 삼량체 단백질들을 지칭하고, 이는 보다 안정화된 HIV-1 gp140 삼량체를 발생시킨다 (도 1). 재설계된 gp41ECTO 도메인은 프로토타입 HIV-1 균주 BG505 (및 프로토타입 gp140 삼량체 BG505 SOSIP.664 gp140) 에 기반하고 야생형 BG505 gp41ECTO 서열에 대해 하나 이상의 변형들을 포함한다. 이들 변형들은 (1) 사전-융합 gp140 구조를 안정화하기 위해 보다 짧은 루프 서열로 HR1의 21 개의 잔기 N-말단 (잔기 548 내지 잔기 568) 의 대체 및 (2) GGGGS (서열 번호: 17) 모티프의 탠덤 반복과 같은 플렉서블 (flexible) 링커 서열을 갖는gp120과 gp41 사이의 퓨린 절단 부위 (잔기 508 내지 잔기 511) 의 대체를 포함한다. 일부 실시예들에서, UFO 삼량체는 gp120과 gp41 사이에 엔지니어링된 디설파이드 (disulfide) 본드 및/또는 gp41에서 안정화 돌연변이를 부가적으로 포함할 수 있다. 예를 들어, HIV-1 균주 BG505에 기반한 UFO 삼량체들은 잔기 A501C와 잔기 T605c 사이에 엔지니어링된 디설파이드 본드를 포함할 수 있다. UFO 삼량체들의 상세한 설명은 예를 들어, Kong et al., Nat. Comm. 7:12040, 2016에서 제공된다. BG505 균주 서열에 기반한 UFO 삼량체들에 부가적으로, 엔지니어링된 gp41ECTO도메인은 "키메라" gp140 삼량체를 형성하기 위해 많은 상이한 HIV-1 균주 또는 아형들로부터 gp120 폴리펩타이드와 쌍을 이루도록 사용될 수 있다. 이러한 키메라 삼량체들은 본 명세서에 예시된 바와 같이 "UFO-BG” 또는 "UFO2-BG"로서 명명된다. UFO-BG 및 UFO2-BG 삼량체의 상세한 설명은 예를 들어, He et al., Sci Adv. 4 (11):eaau6769, 2018에서 제공된다.
백신은 피험자에서 예방적 면역 반응 또는 치료적 면역 반응을 도출하는 약제용 조성물을 지칭한다. 일부 경우들에서, 면역 반응은 보호성 면역 반응이다. 통상적으로, 백신은 병원체의 항원, 예를 들어, 바이러스 병원체에 대한, 또는 병리학적 상태와 상관된 세포 구성 성분에 대한 항원-특이 면역 반응을 도출한다. 백신은 (개시된 항원을 코딩하는 핵산과 같은) 폴리뉴클레오타이드, (개시된 항원과 같은) 펩타이드 또는 폴리펩타이드, 바이러스, 세포 또는 하나 이상의 세포 구성 성분들을 포함할 수도 있다. 본 발명의 일부 실시예들에서, 백신들 또는 백신 면역원들 또는 백신 조성물들은 융합 구성들로부터 발현되고 표면 상에 면역원 폴리펩타이드 또는 단백질을 표지하는 나노입자들로 자가-조립된다.
바이러스-유사 입자들 (Virus-like Particles; VLP) 은 임의의 몇몇의 바이러스들로부터 유래된, 비-복제, 바이러스 쉘 (viral shell) 을 지칭한다. VLP들은 일반적으로 캡시드 (capsid), 코트 (coat), 쉘, 표면 단백질 및/또는 외피 단백질, 또는 이들 단백질들로부터 유도된 입자-형성 폴리펩타이드들로 지칭되는 이들 단백질들과 같은 하나 이상의 바이러스 단백질들로 구성되지만, 이에 제한되는 것은 아니다. VLP들은 적절한 발현 시스템에서 단백질의 재조합 발현 시 자발적으로 형성될 수 있다. 특정 VLP들을 생성하는 방법들은 당업계에 공지되어 있다. 바이러스 단백질들의 재조합 발현 후에 VLP들의 존재는 전자 현미경, 생물 물리학 특성화 등과 같은, 당업계에 공지된 종래의 기법들에 의해 검출될 수 있다. 예를 들어, Baker et al. (1991) Biophys. J. 60:1445-1456; 및 Hagensee et al. (1994) J. Virol. 68:4503-4505를 참조하라. 예를 들어, VLP들은 밀도 기울기 원심 분리에 의해 분리될 수 있고 그리고/또는 특성 밀도 밴딩 (characteristic density banding) 에 의해 식별될 수 있다. 대체 가능하게, 저온 전자 현미경은 문제의 VLP 제제의 유리화된 수성 샘플들 및 적절한 노출 조건들 하에서 기록된 이미지들에 대해 수행될 수 있다.
자가-조립 나노입자들은 수십 나노 미터의 직경 및 VLP들과 유사한 외형을 가진 나노입자로 자동으로 조립할 수 있는 비-바이러스 단백질의 동일한 카피들에 의해 형성된 잘-규정된 표면 기하학적 구조를 갖는 공-형상의 단백질 쉘을 지칭한다. 공지된 예들은 종에 걸쳐 보존되고 24-량체를 형성하는 페린틴 (FR) 뿐만 아니라 모두 60-량체를 형성하는 B. 스테로써모필러스 (B. stearothermophilus) 디하이드로리포일 아실스텐스퍼레이즈 (dihydrolipoyl acyltransferase) (E2p), 아퀴펙스 에오리셔스 (Aquifex aeolicus) 루마진 신타아제 (lumazine synthase; LS), 및 써모토가 마리티마 (Thermotoga maritima) 인캡슐린 (encapsulin) 을 포함한다. 자가-조립 나노입자들은 적절한 발현 시스템에서 단백질의 재조합 발현 시 자발적으로 형성될 수 있다. 나노입자 생성, 검출, 및 특성화를 위한 방법들은 VLP들에 대해 개발된 동일한 기법들을 사용하여 수행될 수 있다.
III.
백신 조성물들을 생성하기 위한 면역원 폴리펩타이드들 또는 단백질들
임의의 폴리펩타이드 면역원들 또는 다량체 단백질들이 본 발명의 백신 설계에 사용될 수 있다. 이들은 도출된 면역 반응이 목표될 수도 있는 병원체들로부터의 임의의 단백질들 또는 폴리펩타이드들을 포함한다. 따라서, 본 발명의 백신 조성물들은 임의의 바이러스들, 박테리아 또는 상이한 병원성 유기체들로부터 유래된 면역원 폴리펩타이드를 활용할 수 있다. 본 발명에 적합한 면역원 폴리펩타이드들은 또한 도출된 면역 반응이 치료 효과를 가질 수도 있고, 질병 증상들을 완화시키거나, 일반적인 건강을 개선할 수도 있는, 인간 단백질들을 포함하는, 비-병원성 종들로부터 유래될 수 있다. 일반적으로, 면역원 폴리펩타이드는 적어도 약 10 개의 아미노산 잔기들을 포함하는 임의의 구조적 폴리펩타이드 또는 펩타이드 또는 기능적 폴리펩타이드 또는 펩타이드일 수 있다. 일부 실시예들에서, 면역원 폴리펩타이드들은 길이로 약 10 내지 약 10,000 개의 아미노산 잔기들을 포함한다. 일부 실시예들에서, 면역원 폴리펩타이드들은 길이로 약 25 내지 약 2,000 개의 아미노산 잔기들을 포함한다. 일부 실시예들에서, 면역원 폴리펩타이드들은 길이로 약 50 내지 약 500 개의 아미노산 잔기들을 포함한다. 따라서, 본 발명에 적합한 면역원 폴리펩타이드들 또는 단백질들은 약 1 kDa 내지 약 1,000 kDa, 바람직하게 약 2.5 kDa 내지 약 250 kDa의 분자량을 가질 수 있다. 일부 보다 바람직한 실시예들에서, 채용된 면역원 폴리펩타이드는 약 5 kDa 내지 약 25 kDa 또는 50 kDa의 분자량을 갖는다.
일부 실시예들에서, 본 발명의 백신 조성물에 사용된 면역원 폴리펩타이드 또는 단백질은 바이러스 표면 또는 코어 단백질 (표적 폴리펩타이드) 로부터 유래될 수 있다. 숙주 세포들의 바이러스 감염에 중요한 많은 공지된 바이러스 단백질이 있다. 예들은, HIV의 당단백질들 (또는 표면 항원들, 예를 들어, GP120 및 GP41) 및 캡시드 단백질들 (또는 구조적 단백질들, 예를 들어, P24 단백질); A 형 간염 바이러스, B 형 간염 바이러스, C 형 간염 바이러스, D 형 간염 바이러스 또는 E 형 간염 바이러스의 표면 항원들 또는 코어 단백질들 (예를 들어, 소형 B 형 간염 바이러스 표면 항원 (small hepatitis B virus surface antigen; S-HBsAg) 및 C 형 간염 바이러스의 코어 단백질들, NS3 항원, NS4 항원 및 NS5 항원); 앱스타인 바 바이러스(Epstein-Barr virus; EBV) 의 당단백질 gp350/220, 호흡기 세포 융합 바이러스 (respiratory syncytial virus; RSV) 의 당단백질 (G-protein) 또는 융합 단백질 (F-protein); 단순 헤르페스 바이러스 HSV-1 및 HSV-2의 표면 단백질 및 코어 단백질 (예를 들어, HSV-2로부터의 당단백질 D), 폴리오바이러스 (poliovirus) 의 표면 단백질들 (예를 들어, gB, gC, gD, gH 및 gL), 홍역 바이러스 (MV) 의 외피 당단백질들 헤마글루티닌 (hemagglutinin; H) 및 융합 단백질 (F), 림프구성 맥락 수막염 바이러스 (lymphocytic choriomeningitis virus; LCMV) 의 당단백질 G, 아데노 바이러스들의 파이버 (fiber) 및 펜톤 염기 단백질들 (penton base proteins), 코로나바이러스들의 S 스파이크, 뎅기열과 같은 플라비바이러스들, 황열병 바이러스 (yellow fever virus), 및 지카 바이러스의 외피 (E) 단백질들, 및 피코르나 바이러스들 (picornaviruses) 의 비-외피화된 (non-enveloped) 캡시드 단백질들을 포함하지만, 이에 제한되지 않는다.
일부 실시 예에서, 본 발명에 적합한 바이러스 면역원들은 감염을 위해 클래스-I 융합 메커니즘을 활용한 바이러스들로부터 유도될 수 있다. 클래스-I 바이러스 융합 단백질들은 세포 진입 동안 극적인 입체 형태적 변화를 겪을 삼량체들이다. 바이러스 단백질의 특정 영역들은 막 융합을 쉽게 하도록 완전히 리폴딩 (refolding) 될 수 있다. 본 명세서에 예시된 바와 같이, 클래스-I 융합 메커니즘을 활용하는 바이러스의 면역원들의 예들은 HIV-1로부터, (예를 들어, 에볼라 바이러스 및 마르부르그 바이러스들) 및 아레나바이러스들 (Arenaviruses) (예를 들어, 라사 바이러스) 과 같은 출혈열들 (hemorrhagic fevers) 을 야기하는 바이러스들로부터, 호흡기 세포 융합 바이러스 (respiratory syncytial virus; RSV) 로부터, 및 MERS-CoV 및 SARS-CoV과 같은 코로나바이러스들로부터 획득된 구조적 단백질들 또는 폴리펩타이드들을 포함한다. 본 명세서에 예시된 바와 같이, 적합한 면역원들은 HIV-1 UFO 삼량체, 에볼라 GP엑토도메인, LASV 당단백질 복합체 (glycoprotein complex; GPC), RSV 당단백질 F, 및 MERS-CoV 스파이크 단백질 S로부터 유래된 임의의 단백질들 및 폴리펩타이드들일 수 있다. 임의의 이들 면역원들, 또는 클래스-I융합 메커니즘을 활용하는 상이한 바이러스들의 구조적 단백질들로부터 유래된 면역원들은, 모두 본 발명의 백신 설계에 채용될 수 있다.
일부 실시예들에서, 본 발명에 적합한 바이러스 면역원들은 감염에 대해 클래스-II융합 메커니즘을 활용하여 바이러스들로부터 유래될 수 있다. 클래스-II 바이러스 융합 단백질들은 이종이량체 (예를 들어, C 형 간염 바이러스) 또는 동종이량체 (예를 들어, 뎅기열 바이러스 및 지카 바이러스) 의 형태로 존재하고, 막 융합 전에 삼량체 스파이크를 형성하도록 리폴딩될 것이다. 본 명세서에 예시된 바와 같이, 적합한 면역원들은 HCV 외피 당단백질 (예를 들어, E2), 지카 바이러스 E 단백질 (예를 들어, DIII 도메인) 으로부터 유래된 임의의 단백질들 및 폴리펩타이드들일 수 있고, 또는 클래스-II 융합 메커니즘을 활용하는 상이한 바이러스들의 임의의 구조적 단백질들일 수 있다. 이들 면역원들 중 임의의 면역원은 본 발명의 백신 설계에 모두 쉽게 채용될 수 있다.
일부 실시예들에서, 본 발명의 백신 조성물들에 사용되는 면역원 폴리펩타이드 또는 단백질은 비-바이러스 표적으로부터 유래될 수 있다. 이들은 임의의 비-바이러스 병원체들 (예를 들어, 박테리아 병원체들) 뿐만 아니라 인간과 같은 포유류 숙주들 내부의 기생 유기체들로부터 획득될 수 있는 면역원들을 포함한다. 일부 실시예들에서, 박테리아 감염에 중요한 박테리아 단백질들은 본 발명의 백신 설계에서 면역원 폴리펩타이드들을 획득하기에 적합하다. 적합한 면역원들은 박테리아, 예를 들어, 결핵균 (TB) 과 함께 본 명세서에 예시된 것으로서Ag85 복합체 및 Mtb72의 구조적 단백질들로부터 유래된 임의의 단백질들 및 폴리펩타이드들일 수 있다. 일부 실시예들에서, 기생충 전염 (parasite transmission), 숙주들에서의 번식 (reproduction), 및 수명 주기에 중요한 기생 단백질들은 본 발명의 백신 설계에서 면역원 폴리펩타이드들을 획득하는데 적합하다. 적합한 면역원들은 기생충들, 예를 들어 본 명세서에 예시된 바와 같이 Pfs25, 포자소체 단백질 (circumsporozoite protein; CSP), 및 열대열 원충 (말라리아) 의 망상적혈구 바인딩 단백질 동족체 5 (reticulocyte binding protein homolog 5; PfRH5) 의 구조적 단백질들로부터 유래되는 임의의 단백질들 및 폴리펩타이드들일 수 있다.
일부 실시예들에서, 채용된 면역원 폴리펩타이드는 도출된 면역 반응이 목표되는, 포유 동물 숙주 (예를 들어, 인간) 로부터의 내인성 단백질 (endogenous protein) 일 수 있다. 이들은 예를 들어, 본 명세서에 예시된 바와 같이 콜레스테롤 수준을 조절하기 위한 PCSK9, 및 식욕 (appetite) 을 조절하기 위한 그렐린 (ghrelin) 을 포함한다. 다양한 상이한 포유 동물 단백질들은 또한 본 발명의 설계에 따른 백신들을 구성하기 위한 적합한 면역원 폴리펩타이드들을 획득하기 위해 사용될 수 있다. 일부 실시예들에서, 백신 설계를 위한 비-바이러스 표적은 인간 질병에 연루된 상이한 단백질들이 될 수 있다. 이들은 암들의 발생에 수반된 단백질들을 포함한다. 암 관련된 면역원들의 예들은 또한 비-돌연변이된 자가-항원들, 예를 들어, MAGE-A3, Melan-A/Mart1, gp100, Her2/Neu, 및 NY-ESO-1을 포함한다. 일부 부가적 실시예들에서, 본 발명의 백신 조성물들에 사용하기 위한 면역원 폴리펩타이드들 또는 단백질들은 상이한 만성 인간 질병들 또는 이상들에 연루된 단백질들을 포함한다. 이러한 인간 표적의 예들은 예를 들어, 고혈압에 대한 Ang-II, 염증들에 대한 TNF-α, 병원체-유도 호산구 향상증 (eosinophilia) 에 대한 IL-9, 천식에 대한 IL-5, 뇌졸중 및 호르몬 수준 감소를 위한 인간 융모성 성선자극 호르몬 (human chorionic gonadotropin; hCG) 에 대한 N-메틸-D-아스파테이트 (N-methyl-D-aspartate) 수용체-1를 포함한다.
IV.
잠금 도메인들
상기 기록된 바와 같이, 본 발명의 일부 나노입자 백신들 또는 면역원들은 본 발명자들에 의해 개발된 잠금 메커니즘을 활용한다. 잠금 메커니즘은 면역원 단백질 또는 폴리펩타이드 (예를 들어, 외피-유래된 HIV-1 삼량체 단백질) 를 표지할 때 내부로부터 나노입자들을 안정화시키도록 기능하는 단백질 도메인 ("잠금 도메인") 을 지칭한다. 일반적으로, 잠금 도메인은 이량체를 형성할 수 있는 임의의 단백질일 수 있다. 다양한 실시예들에서, 잠금 도메인은 계면에서 비-공유 상호 작용들을 통해 용액에서 또 상이한 단백질 서브유닛과 자연적으로 이량체를 형성할 수 있는 단백질 서브유닛이다. 일부 바람직한 실시예들에서, 2 개의 단백질 서브유닛들은 서열에서 동일할 수 있고 동종이량체를 형성할 수 있다. 일부 상이한 경우들에서, 2 개의 단백질 서브유닛들은 상이한 단백질들, 또는 계면에서 비-공유 상호 작용들을 통해 용액에서 이종이량체를 형성할 수 있는, 엔지니어링을 통해 유래된 단일 단백질의 2 개의 상이한 도메인들일 수 있다. 통상적으로, 잠금 도메인은 면역원 폴리펩타이드 (예를 들어, HIV-1 외피 유래된 삼량체 단백질의 서브유닛) 가 결합된 나노입자 서브유닛에 공유적으로 융합된다. 일부 바람직한 실시예들에서, 잠금 도메인은 나노입자 쉘 내에 캡슐화될 수 있도록 약 500 개 이하의 아미노산들을 갖는 이량체성 단백질들로부터 선택된다. 일부 실시예들에서, 잠금 도메인은 약 400 개, 300 개, 250 개, 200 개, 150 개 이하의 아미노산들을 갖는 이량체성 단백질들로부터 유래된다. 일부 실시예들에서, 잠금 도메인은 약 30 내지 약 100 개의 아미노산들을 포함하는 이량체성 단백질들로부터 유도된다. 본 명세서에 기술된 바와 같이, 잠금 도메인은 소수성 (반 데르 발스 (van der Waals)) 콘택트들 (contacts), 수소 본드들, 및/또는 염 브리지들과 같은 특정 상호 작용들을 통해 계면을 형성할 수 있는 임의의 이량체성 단백질일 수 있다. 일부 실시예들에서, 잠금 도메인은 나선들, 시트들, 루프들, 또는 상기 언급된 구조적 엘리먼트들 (elements) 의 임의의 조합들의 상호 작용들을 통해 계면을 형성할 수 있는 임의의 이량체성 단백질일 수 있다. 일부 실시예들에서, 잠금 도메인은 디설파이드 본드 또는 특정 화학적 결합과 같은 공유 본드가 엔지니어링될 수 있는 계면을 형성할 수 있는 임의의 이량체성 단백질일 수 있다. 다양한 실시예들에서, 이량체의 2 개의 서브유닛들 사이의 친화도는 그렇지 않으면 이러한 잠금 도메인들이 결여된 야생형 (WT) 나노입자들에 의해 용인되지 않을, 열 프로세싱 및 화학적 프로세싱과 같은 외부 교란들을 견디도록 충분히 강하다.
당업계에 공지된 많은 단백질들이 본 발명의 실시에서 잠금 도메인으로서 채용될 수 있다. 이들은, 예를 들어, 이하의 예들에서 본 명세서에 예시된 2 개의 잠금 도메인들 LD4 (서열 번호: 1) 및 LD7 (서열 번호: 2) 을 포함한다. 본 발명에 적합한 일부 상이한 예시적인 잠금 도메인들은 서열 번호: 3 내지 서열 번호: 16에 도시된다. 본 명세서에서 HIV-1 백신들에 대해 예시된 바와 같이, 잠금 도메인 LD4 또는 잠금 도메인 D7을 통해 안정화된 HIV-1나노입자UFO삼량체 백신들은 놀랍게도 강한 면역원성을 입증하였다. 이들 예시된 서열들 중 임의의 서열을 갖는 잠금 도메인들에 부가적으로, 보존적으로 변형된 변이체들 또는 실질적으로 동일한 서열들을 갖는 변이체들이 또한 사용될 수 있다.
적합한 잠금 도메인들은 단백질 데이터베이스 (Protein database; PDB) 로부터 공지된 단백질들로부터 쉽게 식별될 수 있다. 예를 들어, 이량체성 단백질들은 단백질 데이터 뱅크 (PDB) (https://www.rcsb.org/) 또는 "동종이량체"와 같은 키워드들 또는 "단백질 화학량론 (protein stoichiometry) A2"와 같은 검색 기준을 사용하여 상이한 데이터베이스들로부터 발견될 수 있다. 이들 이량체성 단백질들은 이들의 크기, 구체적으로 30 내지 100 개의 아미노산에 기반하여 더 여과될 수 있다. 남아있는 단백질들은 콤팩트한 구조적 폴딩 또는 상이한 바람직한 특성들을 갖는 것들을 식별하기 위해 육안으로 검사될 수 있다. 본 명세서에 예시된 바와 같이, 다수의 이량체성 단백질들이 확인되고, 그리고 이들 절차들을 사용하여 이하에 상세히 기술된 바와 같이 필요에 따라 변형된다. 이렇게 확인된 약 20 개의 이량체성 단백질들 중에서, 9 개는 60-량체 나노입자 E2p 및 I3-01을 안정화시키기 위한 잠금 도메인들로서 평가되었다. 평가된 9 개의 잠금 도메인의 서열들은 이하에 열거된다. 원래의 서열들과 비교하여, 실제로 채용된 잠금 도메인 (서열 번호: 1 내지 서열 번호: 9) 의 서열들은 엔지니어링 목적을 위해 플렉서블 N-말단 및/또는 C-말단에 몇몇 잔기들의 절단들을 포함할 수도 있다. 엔지니어링된 LD9 (서열 번호: 9) 의 경우, 원래의 서열의 N-말단 및C-말단에서 절단들에 부가적으로, 이는 또한 잔기 42에서 S-> A 돌연변이를 포함한다.
LD1 1NI8_A:
SEALKILNNIRTLRAQARECTLETLEEMLEKLEVVVNERR (서열 번호: 3)
LD2 4aYA_B:
MNDCYSKLKELVPSIPQNKKVSKMEILQHVIDYILDLQIALDSH (서열 번호: 4)
LD3 1OVX_A:
LLYCSFCGKSQHEVRKLIAGPSVYICDECVDLCNDIIREEIKEVAPHRER (서열 번호: 5)
LD4 2MG4_A:
FSEEQKKALDLAFYFDRRLTPEWRRYLSQRLGLNEEQIERWFRRKEQQIGWSHPQFEK (서열 번호: 1)
LD5 2JV7_A:
DQPSVGDAFDKYNEAVRVFTQLSSAANCDWAACLSSLSASSAACIAAVGELGLDVPLDLACAATATSSATEACKGCLW (서열 번호: 6)
LD6 1JR5_A:
KNIDTVREIITVASILIKFSREDIVENRANFIAFLNEIGVTHEGRKLNQNSFRKIVSELTQEDKKTLIDEFNEGFEGVYRYLEMYTNK (서열 번호: 7)
LD7 1PZQ_A:
SPAVDIGDRLDELEKALEALSAEDGHDDVGQRLESLLRRWNSRRAD (서열 번호: 2)
LD8 1R2A_A:
PPGLTELLQGYTVEVLRQQPPDLVDFAVEYFTRLREARR(서열 번호: 8)
LD9 2JRX_A:
YSDEQVEQLLAELLNVLEKHKAPTDLSLMVLGNMVTNLINTAIAPAQRQA IANSFARALQSSINE (서열 번호: 9)
이들 평가된 LD들에 부가적으로, 유사한 구조적 특성들을 갖는 상이한 이량체성 단백질들이 나노입자 표면을 안정화시키기 위해 사용될 수도 있다. 이러한 부가적 서열들의 예들은:
1L6E_A:
HMGHIQIPPGLTELLQGYTVEVLRQQPPDLVDFAVEYFTRLREARR (서열 번호: 10)
1PZR_A:
ASDDELFSMLDQRFGGGEDLLMSGDNGMTEEKLRRYLKRTVTELDSVTARLREVEHRAGE (서열 번호: 11)
1R05_A:
MADKRAHHNALERKRRDHIKDSFHSLRDSVPSLQGEKASRAQILDKATEYIQYMRRKVHTLQQDIDDLKRQNALLEQQVRALEGSGC (서열 번호: 12)
1TKV_A:
MNKNIDTVREIITVASILIKFSREDIVENRANFIAFLNEIGVTHEGRKLNQNSFRKIVSELTQEDKKTLIDEFNEGFEGVYRYLEMYTNK (서열 번호: 13)
2DSM_A:
MVENPMVINNWHDKLTETDVQIDFYGDEVTPVDDYVIDGGEIILRENLERYLREQLGFEFKNAQLE (서열 번호: 14)
2JPQ_A:
MPITSKYTDEQVEKILAEVALVLEKHAASPELTLMIAGNIATNVLNQRVAASQRKLIAEKFAQALMSSLETPKTHLE (서열 번호: 15)
2K01_A:
GMKPVSLSYRCPCRFFESHVARANVKHLKILNTPNCACQIVARLKNNNRQVCIDPKLKWIQEYLEKCLNK (서열 번호: 16) 을 포함한다.
이들 특이 LD들 및 이량체성 단백질들에 부가적으로, 이미 존재하거나 단백질 데이터 뱅크 (PDB) 로부터 쉽게 유래될 수 있는, 상기 기술된 기준들과 매칭하는 상이한 단백질들이, 또한 본 발명에서 잠금 도메인들로서 활용될 수 있다. 또한, 대형 이량체성 단백질의 계면-형성 부분 또는 도메인은 상기 기술된 구조적 요건 및 기능적 요건과 매칭한다면 독립형의 잠금 도메인으로서 사용될 수 있다.
V.
부가적 구조적 구성 요소 또는 모티프
잠금 도메인과 상이한, 나노입자 표지된 면역원 백신 구성들 및 발생된 본 발명의 백신 조성물들은 부가적으로 또는 대체 가능하게 상이한 구조적 컴포넌트들 또는 모티프들을 포함할 수 있다. 일부 실시예들에서, 본 발명의 잠금 도메인 안정화된 나노입자 백신들은 또한 견고한 T-세포 (robust T-cell) 반응들을 촉진하고 bNAb들을 향하여 B 세포 개발을 조정하기 위해 T-세포 에피토프를 포함한다. T-세포 에피토프는 나노입자 표면 상의 면역원 폴리펩타이드의 표지에 영향을 주지 않는 한, 상이한 구조적 컴포넌트들과 관련하여 임의의 위치에 위치될 수 있다. 따라서, 일부 실시예들에서, T-세포 에피토프는 예를 들어, T-세포 에피토프의 N-말단을 나노입자 서브유닛의 C-말단에 융합시킴으로써, 나노입자 서브유닛의 C-말단에 위치된다. 일부 상이한 실시예들에서, T-세포 에피토프는 면역원 폴리펩타이드의 C-말단과 나노입자 서브유닛의 N-말단 사이에 위치한다. 당업계에 공지된 임의의 T-세포 에피토프 서열들 또는 펩타이드들이 본 발명의 실시에 채용될 수도 있다. 그들은 MHC 클래스-II 에피토프들을 포함하고 면역화 시 CD4+ T 세포 및 CD8+ T 세포를 효과적으로 활성화할 수 있는 임의의 폴리펩타이드 서열, 예를 들어, CD4+ T 헬퍼 세포들을 활성화하는 T-헬퍼 에피토프를 포함한다. 예를 들어, Alexander et al., Immunity 1, 751-761,1994; Ahlers et al., J. Clin. Invest. 108:1677-1685, 2001; Fraser et al., Vaccine 32, 2896-2903, 2014; De Groot et al., Immunol. Cell Biol. 8:255-269, 2002; 및Gene Ther. 21: 225-232, 201를 참조하라. 일부 바람직한 실시예들에서, 채용된 T-헬퍼 에피토프는 보편적인 범-반응성 T-세포 에피토프 펩타이드, AKFVAAWTLKAAA (서열 번호: 18) (Alexander et al., Immunity 1, 751-761,1994) 이다. 적합한 T-세포 에피토프들의 상이한 예들은 펩타이드QSIALSSLMVAQAIP (서열 번호: 19) 및 펩타이드 ILMQYIKANSKFIGIPMGLPQSIALSSLMVAQ (서열 번호: 20), 또는 보존적으로 변형된 변이체들 또는 임의의 이들 예시된 T-세포 에피토프 펩타이드의 실질적으로 동일한 (예를 들어, 적어도 90%, 95% 또는 99% 동일한) 서열들을 포함한다.
본 명세서에 기술된 잠금 도메인 및 상이한 구조적 컴포넌트들에 대체 가능하게 또는 부가적으로, 본 발명의 일부 나노입자 백신들은 나노입자들의 표면 상의 면역원의 표지를 쉽게 하도록 넥 영역 또는 도메인을 포함한다. PCSK9 백신 및 말라리아 백신에 대한 열대열원충 면역원들 Pfs25로 본 명세서에 예시된 바와 같이, 넥 영역은 바이러스 단백질로부터 유래된 3-나선 다발을 구성한다. 통상적으로, 넥 도메인은 면역원과 나노입자 서브유닛 사이에 삽입됨으로써, 나노입자 표면으로부터 면역원 폴리펩타이드를 상승시킨다. 선택 가능하게, 링커 서열 (예를 들어, 10GS 링커) 이 넥 도메인의 삽입을 위해 사용될 수 있다. 넥 도메인에 적합한 단백질들의 예들은 본 명세서에 예시된 바와 같이 헨드라 (Hendra) 바이러스 도메인 (PDB ID: 4HEO) 으로부터 유래된 나선 다발들 및 홍역 바이러스 도메인 (PDB ID: 1OKS) 을 포함한다. 입증된 바와 같이, 이러한 구조적 설계는 발생된 나노입자 백신들의 수율 및 순도를 더 개선할 수 있다.
본 명세서에 기술된 잠금 도메인 및 상이한 구조적 컴포넌트들에 대체 가능하게 또는 부가적으로, 본 발명의 일부 나노입자 백신들은 면역원 폴리펩타이드를 안정화시키는 역할을 하는 단백질 도메인을 포함할 수 있다. 일부 실시예들에서, 이 목표를 달성하기 위해 채용된 단백질 도메인은 당업계에 공지된 T4 피브리틴 (폴돈) 의 C-말단 삼량체화 모티프일 수 있다. 이 폴돈 도메인은 박테리오파지 (bacteriophage) T4로부터 삼량체성 단백질 피브리틴의 C-말단 30 개의 아미노산 잔기를 구성하고, 피브리틴의 폴딩 및 삼량체화를 촉진하는 기능을 한다. 예를 들어, Papaanikolopoulou et al., J. Biol. Chem. 279: 8991-8998, 2004; 및 Guthe 등, J. Mol. Biol. 337: 905-915, 2004을 참조하라. MERS-CoV 백신을 위한 S 스파이크 삼량체로 본 명세서에 예시된 바와 같이, 이 단백질 도메인은 S 스파이크 서브유닛과 나노입자 서브유닛 사이에 쉽게 삽입될 수 있다. 선택 가능한 링커 (예를 들어, 10GS 링커) 가 삽입을 위해 사용될 수 있다. 나노입자 서브유닛의 C-말단에 삽입되는 잠금 도메인과 달리, 이 단백질 도메인 (폴돈) 은 나노입자 서브유닛의 N-말단에 삽입된다. MERS-CoV 백신으로 본 명세서에서 입증된 바와 같이, 이러한 구조적 컴포넌트 (예를 들어, 폴돈) 는 단독으로 또는 잠금 도메인과 조합으로 사용될 때, 나노입자들의 표면 상에 표지되는 면역원의 안정성을 향상시킬 수 있다.
다양한 실시예들에서, 본 명세서에 기술된 임의의 면역원 폴리펩타이드들 또는 단백질들 (예를 들어, HIV-1 외피-유래된된 삼량체 면역원들) 을 표지하는 나노입자들은 다량체 면역원 단백질 (예를 들어, 삼량체 면역원) 의 면역원 폴리펩타이드 또는 서브유닛을 나노입자의 서브유닛 (예를 들어, E2p 또는 I3-01 서브유닛) 및 잠금 도메인의 서브유닛뿐만 아니라 본 명세서에 기술된 상이한 선택 가능한 또는 대체 가능한 컴포넌트들과 융합함으로써 구축될 수 있다. 본 발명의 나노입자 표지된 융합 백신 면역원을 구축하기 위해, 하나 이상의 링커 모티프들 또는 모이어티들이 상이한 컴포넌트들의 연결을 가능하게 하고 구조적 무결성을 유지하도록 채용될 수도 있다. 따라서, 일부 실시예들에서, 링커 모티프는 나노입자 서브유닛의 N말단에 면역원 폴리펩타이드 (예를 들어, HIV-1 삼량체 단백질 서브유닛) 의C-말단을 연결하기 위해 채용될 수 있다. 부가적으로 또는 대체 가능하게, 제 2 링커 모티프는 나노입자 서브유닛의 C-말단 (또는 면역원 폴리펩타이드의 C-말단) 을 잠금 도메인의 N-말단에 결합하도록 사용될 수 있다. 일부 상이한 실시예들에서, 제 3 링커 모티프는 T-세포 에피토프를 연결하기 위해, 예를 들어, 잠금 도메인의 C-말단을 T-세포 에피토프의 N-말단에 결합하거나, 또는 잠금 도메인의 N-말단을 T-세포 에피토프의 C-말단에 결합하도록 채용될 수도 있다. 본 명세서에 예시된 바와 같이, 링커들은 또한 넥 도메인 또는 폴돈 도메인을 나노입자 백신 구성 내로 삽입하도록 사용될 수 있다. 통상적으로, 링커 모티프들은 짧은 펩타이드 서열들을 포함한다. 다양한 실시예들에서, 링커들 또는 링커 모티프들은 이들의 기능들을 방해하지 않고 2 개의 단백질 도메인들을 연결하는 임의의 플렉서블 펩타이드들일 수 있다. 예를 들어, 구성에 사용된 임의의 이들 링커들은 (GaSb)n의 서열을 갖는 GC-풍부 펩타이드일 수 있고, 여기서 a는 약 1 내지 5의 정수이고, b는 약 0 내지 2의 정수이고, n은 약 1 내지 5의 정수이다. 일부 상이한 실시예들에서, T-세포 에피토프는 면역원 폴리펩타이드의 C-말단과 나노입자 서브유닛의 N-말단 사이의 링커 또는 링커의 일부로서 사용될 수 있다.
본 발명의 본 명세서에 기술된 바와 같이 신규 구조적 컴포넌트들 (예를 들어, 잠금 도메인으로 안정화된 HIV-1 삼량체 면역원들) 을 갖는 백신 조성물은 본 명세서에 기술된 프로토콜들 (예를 들어, 예 1 내지 예 15) 및/또는 당업계 예를 들어, He et al., Nat. Comm. 7, 12041, 2016; Kong et al., Nat. Comm. 7, 12040, 2016; 및 He et al., Sci Adv. 4 (11):eaau6769, 2018에서 기술된 상이한 방법들에 따라 재조합적으로 구축될 수 있다. 예시로서, 2 개의 특정 HIV-1 나노입자 백신 구성들이 본 명세서에 기술된다. 제 1 구성은 N-말단으로부터 C-말단까지: HIV-1 UFO BG505.SOSIP.664 gp140 서브유닛, E2p 서브유닛 (예를 들어, 서열 번호: 21), 상기 기록된 링커 모티프 (GaSb)n (예를 들어, (GGGGS)2 (서열 번호: 24)), 서열 번호: 1 (LD4) 에 나타낸 바와 같이 잠금 도메인, 및 T-세포 에피토프 (예를 들어, 서열 번호: 18에 나타낸PADRE 에피토프) 를 포함하는 융합 폴리펩타이드를 발현한다. 선택 가능하게, 면역원 폴리펩타이드 (예를 들어, HIV-1 백신에 대한 gp140 서브유닛) 는 링커 서열, 예를 들어, GGGGS (서열 번호: 17) 또는 (GGGGS)2 (예를 들어, 서열 번호: 24) 을 통해 나노입자 서브유닛 (예를 들어, E2p) 에 연결될 수 있다. 제 2 구성은 N-말단으로부터 C-말단까지: HIV-1 UFO BG505.SOSIP.664 gp140, 링커 서열 (GGGGS)2 (서열 번호: 24), I3-01 서브유닛 (예를 들어, 서열 번호: 22 또는 서열 번호: 25), 상기 기록된 제 2 링커 (GaSb)n (예를 들어, GGGGS (서열 번호: 17)), 서열 번호: 2에 나타낸 바와 같이 잠금 도메인 (LD7), 및 T-세포 에피토프 (예를 들어, 서열 번호: 18로 도시된 바와 같은 에피토프) 를 포함하는 융합 폴리펩타이드를 발현한다. 선택 가능하게, 디펩타이드 링커, GS는 본 발명의 임의의 백신 구성에서 잠금 도메인과 T-세포 에피토프 사이에 삽입될 수 있다. 백신 면역원들 (예를 들어, HIV-1 나노입자 면역원들) 의 항원성 및 구조적 무결성은 표준 분석들, 예를 들어, 항체 결합 분석들 및 매질 염색 전자 현미경 (EM) 을 통해 쉽게 분석될 수 있다. 본 명세서에 예시된 바와 같이, 융합 분자들은 모두 외피-유래된 삼량체 (예를 들어, gp140) 의 면역원성 에피토프들을 표지하는 나노입자들로 자가-조립될 수 있다. 견고한 삼량체-특이 bnAb들을 도출함으로써, 본 발명의 나노입자 백신들은 본 명세서에 예시된 바와 같이 넓은 범위의 바이러스들 (예를 들어, HIV-1 바이러스, 에볼라 바이러스, 라사 바이러스, 및 HCV 바이러스) 에 대해 개인들을 백신 접종 (vaccinating) 하는데 유용하다.
VI.
비계 (scaffold) 표지
임의의 이종성 비계가 본 발명의 백신들의 구성에서 면역원 단백질 또는 폴리펩타이드 (예를 들어, HIV-1 외피 삼량체 단백질) 를 제공하도록 사용될 수 있다. 이는 박테리오파지 Qb VLP 및 나노입자와 같은 바이러스-유사 입자 (VLP) 를 포함한다. 일부 바람직한 실시예들에서, 삼량체성 HIV-1 단백질을 나타내거나 표지하기 위한 이종성 비계는 자가-조립 나노입자다. 다양한 나노입자 플랫폼들이 본 발명의 백신 조성물들을 생성하는데 채용될 수 있다. 일반적으로, 본 발명에 채용된 나노입자들은 단일 서브유닛의 복수의 카피에 의해 형성되어야 한다. 나노입자들은 통상적으로 공-유사 형상이고, 그리고/또는 예를 들어, 본 명세서에 예시된 20 면체 구조를 갖는, 회전 대칭형 (예를 들어, 3-폴드 축 및 5-폴드 축을 갖는) 을 갖는다. 부가적으로 또는 대체 가능하게, 입자 서브유닛의 아미노-말단은 노출되어야 하고 3-폴드 축에 매우 근접해야 하고, 3 개의 아미노-말단의 간격은 다양한 HIV-1 삼량체성 컴포넌트들의 카르복실-말단 (carboxyol-termini) 의 간격과 근접하게 매칭해야 한다. 일부 바람직한 실시예들에서, 면역원들은 약 20 ㎚ 이하의 직경 (보통 12 개, 24 개, 또는 60 개의 서브유닛들로부터 조립됨) 및 입자 표면 상에 3-폴드 축을 갖는 자가-조립 나노입자들을 포함한다. 이러한 나노입자들은 본 명세서에 예시된 바와 같이 다가 백신들, 예를 들어, HIV-1 삼량체 백신들을 생산하기 위해 적합한 입자 플랫폼들을 제공한다.
일부 바람직한 실시예들에서, 면역원 단백질 또는 폴리펩타이드 (예를 들면, HIV-1 삼량체 단백질) 는 본 명세서에 예시된 바와 같이 자가-조립 페린틴 (FR), E2p 및 I3-01 로부터 유도된 자가-조립 나노입자들과 같은 자가-조립 나노입자 상에 존재한다. E2p는 내열성 60-량체 나노입자로 자가-조립 하는 것으로 나타낸 바실러스 스테아로더모필러스 (Bacillus stearothermophilus) 로부터의 디하이드로리포일 아실트랜스퍼레이즈 (dihydrolipoyl acyltransferase) 의 재설계된 변이체이다. 예를 들어, He et al., Nat. Commun. 7:12041, 2016을 참조하라. 유사하게, I3-01은 초안정 나노입자들로 자가-조립될 수 있는 엔지니어링된 단백질이다. 예를 들어, Hsia et al., Nature 535, 136-139, 2016 참조하라. 이들 단백질들의 서브유닛들의 서열들은 당업계에 공지되어 있다. 예를 들어, WO2017/192434를 참조하라. 본 명세서에 예시된 바와 같이 E2p 및 I3-01 나노입자 서브유닛들의 아미노산 서열들은, 각각 서열 번호: 21 및 서열 번호: 22에 나타낸다. 원래의 서열에 비해, 서열 번호: 21에 나타낸 E2p 서열은 이하의 서열에서 강조된 바와 같이 잔기 92에 Ala 치환을 포함한다. 서열 번호: 22에 나타낸 I3-01 서브유닛 서열에 부가적으로, 서열 번호: 25에 나타낸 재설계된 I3-01 서브유닛 서열이 또한 본 발명의 실시에 채용될 수 있다. 다양한 실시예들에서, 본 발명의 HIV-1 나노입자 백신들은 이들 공지된 나노입자들뿐만 아니라 이들의 보존적으로 변형된 변이체들 또는 실질적으로 동일한 (예를 들어, 적어도 90%, 95% 또는 99% 동일한) 서열을 갖는 변이체들을 채용할 수 있다.
E2p 서브유닛 서열 (서열 번호: 21)
AAAKPATTEGEFPETREKMSGIRRAIAKAMVHSKHTAPHVTLMDEADVTKLVAHRKKFKAIAAEKGIKLTFLPYVVKALVSALREYPVLNT A IDDETEEIIQKHYYNIGIAADTDRGLLVPVIKWFHADRKPIFALAQEINELAEKARDPEGVALLTPGEMASCTN
I3-01 서브유닛 서열 (서열 번호: 22)
MKMEELFKKHKIVAVLRANSVEEAKKKALAVFLGGVHLIEITFTVPDADTVIKELSFLKEMGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVGPQWFVKLATEVVGPQFVKAMKGVGSAFVKFVPTGGV
I3-01-jz9 변이 서열 (서열 번호: 25)
MKMEELFKKHKIVAVLRANSVEEAKMKALAVFVGGVHLIEITFTVPDADTVIKELSFLKELGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVVGPQFAGVTEGGVANLVCEKVKG
페린틴 서열 (서열 번호: 26)
MKMEELFKKHKIVAVLRANSVEEAKMKALAVFVGGVHLIEITFTVPDADTVIKELSFLKELGAIIGAGTVTSVEQCRKAVESGAEFIVSPHLDEEISQFCKEKGVFYMPGVMTPTELVKAMKLGHTILKLFPGEVVVGPQFAGVTEGGVANLVCEKVKG
이들 예시된 나노입자 서열들에 부가적으로, 당업계에 공지된 많은 상이한 나노입자들 또는 VLP들이 또한 본 발명의 실시에 사용될 수도 있다. 이들은 예를 들어, 아퀴펙스 에오리셔스 루마진 신타아제 (lumazine synthase), 써모토가 마리티마 인캡슐린 (Thermotoga Maritima encapsulin), 믹소코커스 잔투스 (Myxococcus xanthus) 인캡슐린, 박테리오파지 Qbeta 바이러스 입자, 플록 하우스 바이러스 (Flock House Virus; FHV) 입자, ORSAY 바이러스 입자, 및 전염성 낭질병 바이러스 (infectious bursal disease virus; IBDV) 입자를 포함한다.
상기 기술된 바와 같이, 많은 백신 면역원들이 본 발명의 백신 설계에 사용될 수 있다. 이들은 다양한 바이러스 면역원 및 비-바이러스 단백질들을 포함한다. HIV-1 백신의 경우, 임의의 외피-유래된 HIV-1 삼량체 단백질들이 나노입자-표지된 백신 조성물에 사용될 수 있다. 외피 유래 삼량체 단백질은 다양한 HIV-1 균주로부터 수득할 수 있다. 일부 실시예들에서, 나노입자들은 HIV-1 외피 기반 당단백질들 또는 도메인들, 예를 들어, gp140, gp120 또는 V1V2 도메인들의 천연 삼량체 형태를 나타낸다. 일부 실시예들에서, 채용된 HIV-1 외피-유래된 삼량체 단백질은 절단되지 않은 사전-융합-최적화 (UFO) gp140 삼량체이다. 일부 실시예들에서, 외피-유래된 삼량체는 HIV-1 균주 BG505, 예를 들어, BG505. SOSIP.664 gp140 삼량체로부터이다. 일부 실시예들에서, 나노입자들은 변형된 gp140 삼량체 면역원, 예를 들어, Kong 등, Nat. Comm. 7, 12040, 2016에 기술된 HR1-변형된 gp140 삼량체 (“UFO 삼량체“) 를 나타낸다. HR1-변형된 gp140 삼량체 단백질의 서브유닛의 아미노산 서열은 서열 번호: 23에 나타난다. 일부 실시예들에서, 본 발명에 사용된 HIV-1 삼량체성 면역원은 UFO2-BG 삼량체일 수 있다. UFO2-BG 삼량체는 (1) 재설계된 HR1 N-말단 벤딩 (bend) 및 절단-부위 링커를 갖는 BG505 gp41 도메인 (Kong et al., Nat. Comm. 7, 12040, 2016에 기술된) 및 (2) 상이한 다양한 HIV-1 균주 또는 아형들 중 하나로부터의 gp120 단백질을 포함하는 키메라 gp140 삼량체들이다. BG505 균주로부터의 재설계된 gp41ECTO 도메인에 부가적으로, 본 발명에 적합한 키메라 gp140 삼량체의 gp41 도메인은 또한 HIV-1 서열 데이터베이스로부터 유래된 교감 gp41 ECTO 도메인일 수 있다. 본 명세서에 기술된 다양한 HIV-1 삼량체 단백질들의 보존적으로 변형된 변이체들, 또는 실질적으로 동일한 서열들을 갖는 변이체들이 본 발명의 HIV-1 나노입자 백신들을 구성하는데 또한 사용될 수 있다.
HR1-변형된 gp140 삼량체의 서열 (서열 번호: 23)
AENLWVTVYYGVPVWKDAETTLFCASDAKAYETEKHNVWATHACVPTDPNPQEIHLENVTEEFNMWKNNMVEQMHTDIISLWDQSLKPCVKLTPLCVTLQCTNVTNNITDDMRGELKNCSFNMTTELRDKKQKVYSLFYRLDVVQINENQGNRSNNSNKEYRLINCNTSAITQACPKVSFEPIPIHYCAPAGFAILKCKDKKFNGTGPCPSVSTVQCTHGIKPVVSTQLLLNGSLAEEEVMIRSENITNNAKNILVQFNTPVQINCTRPNNNTRKSIRIGPGQAFYATGDIIGDIRQAHCNVSKATWNETLGKVVKQLRKHFGNNTIIRFANSSGGDLEVTTHSFNCGGEFFYCNTSGLFNSTWISNTSVQGSNSTGSNDSITLPCRIKQIINMWQRIGQAMYAPPIQGVIRCVSNITGLILTRDGGSTNSTTETFRPGGGDMRDNWRSELYKYKVVKIEPLGVAPTRCKRRVVG GGGGSGGGGS AVGIGAVFLGFLGAAGSTMGAASMTLTVQARNLLSG NPDWLPDM TVWGIKQLQARVLAVERYLRDQQLLGIWGCSGKLIC C TNVPWNSSWSNRNLSEIWDNMTWLQWDKEISNYTQIIYGLLEESQNQQEKNEQDLLALD
VII.
폴리뉴클레오타이드들 및 발현 구성들
본 발명의 백신 조성물들은 통상적으로 본 명세서에 기술된 다양한 구조적 컴포넌트들의 작동 가능하게 결합된 코딩 서열들을 포함하는 발현 구성들 (즉, 발현 벡터들) 을 먼저 생성함으로써 생산된다. 따라서, 일부 관련된 양태들에서, 본 발명은 본 명세서에 기술된 바와 같이 신규 구조적 컴포넌트들을 갖는 나노입자 표지된 면역원들 (예를 들어, 잠금 도메인으로 안정화된 나노입자들을 표지하는 HIV-1 외피 삼량체) 을 코딩하는 실질적으로 정제된 폴리뉴클레오타이드들 (DNA 또는 RNA) 뿐만 아니라 이러한 폴리뉴클레오타이드들을 품는 (harbor) 발현 벡터들 (예를 들어, 본 명세서에 예시된 CMV 벡터들) 및 백신 면역원들을 생산하기 위한 숙주 세포들 (예를 들어, 본 명세서에 예시된 ExpiCHO 세포들) 을 제공한다. 폴리뉴클레오타이드들에 의해 코딩되고 또는 벡터들로부터 발현된 융합 폴리펩타이드들 또한 본 발명에 포함된다. 본 명세서에 기술된 바와 같이, 이러한 폴리펩타이드들은 이의 표면 상에 면역원 폴리펩타이드들 또는 단백질들을 표지하는 나노입자 백신들로 자가-조립될 것이다.
폴리뉴클레오타이드들 및 관련된 벡터들은 표준 분자 생물학 기법들 또는 본 명세서에 예시된 프로토콜들을 사용하여 쉽게 생성될 수 있다. 예를 들어, 클로닝 (cloning), 트랜스펙팅 (transfecting), 일시적인 (transient) 유전자 발현 및 안정한 트랜스펙션된 세포주들을 획득하기 위한 일반적인 프로토콜들은 당업계에, 예를 들어, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, N.Y., (3rd ed., 2000); 및 Brent et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc. (ringbou ed., 2003) 에 기술된다. PCR에 의해 폴리뉴클레오타이드 서열에 돌연변이를 도입하는 것은 예를 들어, PCR Technology: Principles and Applications for DNA Amplification, H.A. Erlich (Ed.), Freeman Press, NY, NY, 1992; PCR Protocols: A Guide to Methods and Applications, Innis et al. (Ed.), Academic Press, San Diego, CA, 1990; Mattila et al., Nucleic Acids Res. 19:967, 1991; and Eckert et al., PCR Methods and Applications 1:17, 1991에 기술된 바와 같이 수행될 수 있다.
특정 벡터의 선택은 융합 폴리펩타이드들의 의도된 용도에 따른다. 예를 들어, 선택된 벡터는 세포 형이 원핵이든 진핵이든, 목표된 세포 형에서 융합 폴리펩타이드의 발현을 구동할 수 있어야 한다. 많은 벡터들은 작동 가능하게 결합된 유전자 서열들의 원핵 벡터 복제 및 진핵 발현을 둘 다 허용하는 서열들을 포함한다. 본 발명에 유용한 벡터들은 자동적으로 복제할 수도 있고, 즉, 벡터는 염색체 외로 존재하고 이의 복제는 반드시 숙주 세포의 게놈의 복제에 직접적으로 결합되는 것은 아니다. 대체 가능하게, 벡터의 복제는 숙주의 염색체 DNA의 복제에 결합될 수도 있고, 예를 들어, 벡터는 레트로 바이러스 벡터들에 의해 그리고 안정하게 트랜스펙션된 세포주들에서 달성될 때 숙주 세포의 염색체 내로 통합될 수도 있다. 바이러스-기반 발현 벡터 및 비 바이러스 발현 벡터는 둘 다 포유류 숙주 세포에서 면역원들을 생산하기 위해 사용될 수 있다. 비 바이러스 벡터들 및 비 바이러스 시스템들은 통상적으로 단백질 또는 RNA를 발현하기 위한 발현 카세트 (cassette) 를 갖는 플라스미드들, 에피솜 벡터 (episomal vectors), 및 인간 인공 염색체 (예를 들어, Harrington et al., Nat. Genet. 15:345, 1997를 참조하라) 를 포함한다. 유용한 바이러스 벡터들은 렌티 바이러스들 또는 상이한 레트로 바이러스들, 아데노 바이러스들, 아데노 연관 바이러스들, 사이토메갈로 바이러스, 헤르페스 바이러스들에 기반한 벡터들, SV40, 유두종 바이러스, HBP 엡스타인 바 바이러스, 백시니아 바이러스 벡터들 및 셈리키 포레스트 바이러스 (Semliki Forest virus; SFV) 에 기반한 벡터들을 포함한다. Brent et al., supra; Smith, Annu. Microbiol. 49: 807, 1995; 및 Rosenfeld et al., Cell 68: 143, 1992를 참조하라.
융합 폴리펩타이드를 발현하기 위해 사용된 특정 벡터에 따라, 다양한 공지된 세포들 또는 세포주들이 본 발명의 실시에 채용될 수 있다. 숙주 세포는 본 발명의 융합체를 운반하는 재조합 벡터들이 도입될 수도 있고, 벡터들이 융합 폴리펩타이드의 발현을 유도하도록 허용되는 임의의 세포일 수 있고, 본 발명에 유용하다. 이는 다수의 박테리아 균주들 중 임의의 것과 같은 원핵일 수도 있고, 또는 효모 또는 상이한 진균 세포들, 곤충 세포 또는 양서류 세포, 또는 예를 들어 설치류 세포, 유인원 세포 또는 인간 세포를 포함하는 포유류 세포들과 같은 진핵 생물일 수도 있다. 본 발명의 융합 폴리펩타이드를 발현하는 세포들은 일차 배양된 세포일 수도 있고 확립된 세포 주일 수도 있다. 따라서, 본원에 예시된 세포주들 (예를 들어, CHO 세포들) 에 부가적으로, 당업계에 공지할 수 있는 다수의 상이한 숙주 세포 주들은 또한 본 발명의 실시에 사용될 수 있다. 이들은, 예를 들어 다양한 Cos 세포주들, HeLa 세포들, HEK293 세포, AtT20 세포, BV2 세포 및 N18 세포, 골수종 세포주, 형질 전환된 B-세포들 및 하이브리도마들을 포함한다.
폴리펩타이드를 발현하기 위한 포유 동물 조직 세포 배양의 사용은 일반적으로 예를 들어, Winnacker, From Genes to Clones, VCH Publishers, NY, NY, 1987에서 논의된다. 융합 폴리펩타이드-발현 벡터들은 당업자에게 공지된 임의의 다수의 적합한 방법에 의해 선택된 숙주 세포들로 도입될 수도 있다. 포유류 세포들로의 융합 폴리펩타이드-코딩 벡터의 도입을 위해, 사용된 방법은 벡터의 형태에 종속될 것이다. 플라스미드 벡터들에 대해, 융합 폴리펩타이드 서열들을 코딩하는 DNA는 예를 들어, 지질-매개 트랜스펙션 (“lipofection"), DEAE-덱스트란-매개 트랜스펙션, 전기천공 (electroporation) 또는 칼슘 포스페이트 침전을 포함하는, 임의의 다수의 트랜스펙션 방법들에 의해 도입될 수도 있다. 이들 방법들은 예를 들어, 앞선 Brent et al.,에서 상술되었다. 광범위하게 다양한 형질 전환된 세포 및 비-형질 전환된 세포 또는 일차 세포의 일시적인 트렌스펙션에 적합한 리포펙션 (Lipofection) 시약들 및 방법들이 널리 이용 가능하고, 리포펙션을 구성들을 배양 시 진핵 생물 세포, 그리고 특히 포유류 세포에 도입하는 매력적인 방법이 되게 한다. 예를 들어, LipofectAMINE™ (Life Technologies) 키트 또는 LipoTaxi™(Stratagene) 키트가 입수 가능하다. 리포펙션을 위한 시약 및 방법들을 제공하는 상이한 회사들은 Bio-Rad Laboratories, CLONTECH, Glen Research, Life Technologies, JBL Scientific, MBI Fermentas, PanVera, Promega, Quantum Biotechnologies, Sigma-Aldrich, 및 Wako Chemicals USA를 포함한다.
재조합 융합 폴리펩타이드들의 장기간 고수율 생산을 위해, 안정한 발현이 바람직하다. 복제의 바이러스 원래들을 포함하는 발현 벡터들을 사용하는 대신, 숙주 세포들은 적절한 발현 제어 엘리먼트들 (예를 들어, 프로모터, 인핸서 (enhancer), 서열들, 전사 종결자들, 폴리아데닐화 부위들, 등) 및 선택 가능한 마커에 의해 제어된 융합 폴리펩타이드-코딩 서열들로 형질 전환될 수 있다. 재조합 벡터 내의 선택 가능한 마커는 선택에 대한 내성을 부여하고 세포들로 하여금 벡터를 그들이 염색체들 내로 안정적으로 통합하는 것을 허용한다. 흔히 사용되는 선택 가능한 마커들은 아미노글리코사이드 G-418에 내성을 부여하는, 네오 (neo) (Colberre-Garapin, et al., J. Mol. Biol., 150:1,1981); 및 하이그로마이신 (hygromycin) 에 대한 내성을 부여하는, 하이그로 (Santerre et al., Gene, 30:147,1984) 를 포함한다. 적절한 선택들을 통해, 트랜스펙션된 세포들은 융합 폴리펩타이드 코딩 서열의 통합된 카피들을 포함할 수 있다.
VIII.
약제용 조성물 및 치료적 적용예들
또 상이한 양태에서, 본 발명은 본 명세서에 기술된 바와 같이 신규 구조적 컴포넌트들 (예를 들어, 잠금 도메인) 을 갖는 나노입자 백신 조성물을 사용하는 약제용 조성물들 및 관련된 치료 방법들을 제공한다. 일부 실시예들에서, HIV-1 외피 삼량체 백신 조성물들은 HIV-1 감염들을 예방하고 치료하기 위해 사용될 수 있다. 다양한 상이한 실시예들에서, 본 명세서에 기술된 상이한 바이러스 면역원 또는 비-바이러스 면역원을 포함하는 나노입자 백신들은 대응하는 질병들, 예를 들어, 다양한 병원체들에 의해 도출된 감염들을 예방하거나 치료하도록 채용될 수 있다. 본 발명의 일부 실시예들은 에볼라 바이러스 감염들을 예방하거나 치료하기 위한 EBOV 백신들의 사용에 관한 것이다. 본 발명의 일부 실시예들은 라사 바이러스 감염들을 예방하거나 치료하기 위한 LASV 백신들의 사용에 관한 것이다. 본 발명의 일부 상이한 실시예들은 RSV 감염들을 예방하거나 치료하기 위해 본 명세서에 기술된 RSV 백신들을 사용하는 것에 관한 것이다. 본 발명의 일부 상이한 실시예들은 HCV 감염들을 예방하거나 치료하기 위해 본 명세서에 기술된 HCV 백신들을 사용하는 것에 관한 것이다. 본 발명의 여전히 일부 상이한 실시예들은 MERS-CoV 감염들을 예방하거나 치료하기 위해 본 명세서에 기술된 CoV 백신들을 사용하는 것에 관한 것이다. 일부 상이한 실시예들에서, 본 발명은 지카 바이러스 감염들을 예방하거나 치료하기 위해 ZIKV 백신들을 사용하는 방법들을 제공한다. 일부 상이한 실시예들에서, 본 발명은 말라리아를 예방하거나 치료하기 위해 열대열원충 면역원 (예를 들어, Pfs25) 유래된 백신들을 사용하는 방법들을 제공한다. 일부 상이한 실시예들에서, 본 발명은 결핵을 예방하거나 치료하기 위해 M. 결핵균 면역원 Ag85A 또는 Mtb72로부터 유래된 백신들을 사용하는 방법들을 제공한다. 여전히 일부 상이한 실시예들에서, 본 발명은 인간 피험자들의 LDL 콜레스테롤을 낮추기 위해 PCSK9 백신을 사용하는 방법들을 제공한다.
본 발명의 다양한 치료 방법들의 실시에서, 질병 또는 상태 (예를 들어, HIV-1 감염 또는 말라리아) 의 예방 또는 치료를 필요로 하는 피험자들은 본 명세서에 기술된 대응하는 나노입자 백신, 면역원 폴리펩타이드 또는 코딩 폴리뉴클레오타이드로 투여된다. 통상적으로, 본 명세서에 개시된 나노입자 백신, 면역원 폴리펩타이드 또는 코딩 폴리뉴클레오타이드는 약제용 조성물에 포함된다. 약제용 조성물은 치료적 제제 또는 예방적 제제가 될 수 있다. 통상적으로, 조성물은 하나 이상의 약제용으로 허용 가능한 부형액들 (vehicles) 및, 선택 가능하게, 상이한 치료 성분들 (예를 들어, 항생제 또는 항 바이러스 약물들) 을 부가적으로 포함한다. 다양한 약제용으로 허용되는 첨가제들이 또한 조성물들에 사용될 수 있다.
따라서, 본 발명의 약제용 조성물 중 일부는 백신 조성물들이다. 백신 조성물들에 대해, 적절한 보조제들이 부가적으로 포함될 수 있다. 적합한 보조제의 예들은 예를 들어, 알루미늄 하이드록사이드 (aluminum hydroxide), 레시틴 (lecithin), Freund의 보조제, MPLTM및 IL-12를 포함한다. 일부 실시예들에서, 본 명세서에 개시된 백신 조성물들 또는 나노입자 면역원들 (예를 들어, HIV-1 백신 또는 말라리아 백신 조성물) 은 제어된-방출 제제 또는 시간-방출 제제로서 제제화될 수 있다. 이는 저속 방출 폴리머를 포함하는 조성물에서 또는 마이크로 캡슐화된 전달 시스템 또는 생체접착성 겔 (bioadhesive gel) 을 통해 달성될 수 있다. 다양한 약제용 조성물들은 당업계에 공지된 표준 절차들에 따라 제조될 수 있다. 예를 들어, Remington's Pharmaceutical Sciences, 19thEd., Mack Publishing Company, Easton, Pa., 1995; 지속된 방출 약물 전달 시스템 및 제어된 방출 약물 전달 시스템, JR Robinson, ed., Marcel Dekker, Inc., New York, 1978); US특허 번호 4,652,441 및 US 특허 번호4,917,893; US 특허 번호 4,677,191 및 US 특허 번호 4,728,721; 및 US 특허 번호 4,675,189를 참조하라.
본 발명의 약제용 조성물들은 예를 들어, HIV-1 감염 또는 말라리아를 치료하거나, 피험자에서HIV-1 또는 열대열원충에 대한 면역 반응을 유도하기 위한 다양한 치료적 적용예 또는 예방적 적용예에서 쉽게 채용될 수 있다. 다양한 실시예들에서, 백신 조성물들은 나노입자 백신의 표지된 면역원 폴리펩타이드가 유래되는 병원체에 의해 기인한 감염들을 치료하거나 예방하기 위해 사용될 수 있다. 따라서, 본 발명의 백신 조성물은 다양한 바이러스들 (예를 들어, HIV-1, 에볼라 바이러스, 마르부르그 바이러스, 라사 바이러스, RSV, MERS-CoV, SARS-CoV, HCV, 뎅기열 바이러스, 또는 지카 바이러스) 또는 상이한 병원체들 (예를 들어, 결핵균과 같은 박테리아 및 열대열원충과 같은 기생 유기체들) 에 기인한 감염들을 치료 또는 예방하기 위한 다양한 임상 환경들 (clinical settings) 에서 사용될 수 있다. 이들은 또한 포유 동물 피험자들 (예를 들어, 인간) 에서 내인성 표적들에 대한 목표된 면역 반응을 유도하고, 예를 들어 PCSK9 또는 그렐린 (ghrelin) 에 대한 항체 반응들을 도출하기 위해 사용될 수 있다. 달리 언급되지 않는 한, HIV-1 백신 조성물들의 치료적 적용예들을 예시하기 위해 본 명세서에 제공된 개시는 임의의 상이한 바이러스 면역원 또는 비-바이러스 면역원을 표지하는 나노입자 백신들에 유사하게 적용될 수 있다.
예시로서, HIV-1 나노입자 백신 조성물은 예를 들어, HIV-1에 대한 면역 반응을 유도하도록, 예를 들어, HIV-1에 대한 광범위하게 중화항체들의 생산을 유도하도록 피험자에게 투여될 수 있다. HIV 감염이 발생할 위험이 있는 피험자들에 대해, 본 발명의 백신 조성물은 바이러스 감염에 대한 예방적 보호를 제공하도록 투여될 수 있다. 본 명세서에 기술된 상이한 면역원들로부터 유래된 백신들의 치료적 적용예 및 예방적 적용예는 유사하게 수행될 수 있다. 특정 피험자 및 상태들에 따라, 본 발명의 약제용 조성물들은 당업자에게 공지된 다양한 투여 모드들, 예를 들어, 근육 내 경로, 피하 경로, 정맥 내 경로, 동맥 내 경로, 관절 내 경로, 복강 내 경로 또는 비 경구 경로에 의해 피험자에게 투여될 수 있다. 일반적으로, 약제용 조성물은 선택된 질병 또는 상태 또는 이들의 하나 이상의 증상(들)을 예방, 억제, 및/또는 개선하기 충분한 시간 동안 그리고 조건들 하에 이러한 치료를 필요로 하는 피험자에게 투여된다. 면역원성 조성물은 HIV-1에 대한 면역 반응을 유도하기에 충분한 양으로 투여된다. 치료적 적용예들을 위해, 조성물들은 본 명세서에 기술된 HIV-1 나노입자 면역원의 치료적 유효량을 포함해야 한다. 예방적 적용예를 위해, 조성물들은 본 명세서에 기술된 치료적 유효량의 HIV-1 나노입자 면역원을 포함해야 한다. 적절한 양의 면역원은 치료되거나 또는 예방될 특정 질병 또는 상태, 중증도, 피험자의 연령, 및 특정 피험자의 상이한 개인적인 속성들 (예를 들어, 피험자의 건강의 일반적인 상태 및 피험자의 면역 시스템의 견고함) 에 기반하여 결정될 수 있다. 효과적인 도즈량들의 결정은 부가적으로 동물 모델 연구들에 이어 인간 임상 평가들로 가이드되고 그리고 피험자에서 표적화된 질병 증상들 또는 상태들의 발생 또는 중증도를 현저하게 감소시키는 투여 프로토콜들에 의해 가이드된다.
예방적 적용예들을 위해, 면역원성 조성물들은 임의의 증상 전에, 예를 들어 감염 전에 제공된다. 면역원성 조성물들의 예방적 투여는 임의의 후속 감염을 예방하거나 개선하는 역할을 한다. 따라서, 일부 실시예들에서, 치료될 피험자는, 예를 들어 바이러스에 대한 노출 또는 바이러스에 대한 노출의 가능성 (예를 들어, HIV 감염) 때문에, 감염 (예를 들어, HIV 감염) 되거나, 또는 감염 (예를 들어, HIV 감염) 발생할 위험이 있는 피험자이다. 개시된 치료적 조성물의 치료적 유효량의 투여 후, 피험자는 감염 (예를 들어, HIV-1 감염), 감염 (예를 들어, HIV-1 감염) 과 연관된 증상들, 또는 둘 다에 대해 모니터링될 수 있다.
치료적 적용예들을 위해, 면역원성 조성물은 질병 또는 감염의 증상의 온셋 후, 예를 들어, 감염 (예를 들어, HIV-1 감염) 의 증상의 발생 후, 또는 감염의 진단 후에 제공된다. 면역원성 조성물은 따라서 바이러스에 대한 노출 또는 바이러스에 대한 의심되는 노출 후, 또는 감염의 실제 개시 후 HIV 바이러스에 예상되는 노출에 앞서 예상된 중증도, 감염의 지속 기간 또는 정도 및/또는 연관된 질병 증상들의 정도를 감쇠시키기 위해 제공될 수 있다.
본 발명의 약제용 조성물은 관련 병원체에 의한 감염 (예를 들어, HIV 감염) 을 치료하거나 예방하기 위해 당업계에 공지된 상이한 제제들 (agents) 과 조합될 수 있다. 다시, 예시로서 HIV-1 감염을 사용하여, 이들 공지된 제제들은 예를 들어 아바카비르 (abacavir), AZT, 디다노신 (didanosine), 앰트리시타빈 (emtricitabine), 라미부딘 (lamivudine), 스타부딘 (stavudine), 테노포비르 (tenofovir), 잘시타빈 (zalcitabine), 지도부딘 (zidovudine), 등과 같은 뉴클레오사이드 역전사 효소 억제제들 (nucleoside reverse transcriptase inhibitors), 데라비르딘 (delavirdine), 에파비렌즈 (efavirenz), 네비라파인 (nevirapine) 과 같은 비-뉴클레오사이드 역전사 효소 억제제들 (non-nucleoside reverse transcriptase inhibitors), 엠프레나비르 (amprenavir), 아타자나비르 (atazanavir), 인디나비르 (indinavir), 로피나비르 (lopinavir), 넬피나비르 (nelfinavir), 오삼프레나비르 (osamprenavir), 리토나비르 (ritonavir), 사퀴나비르 (saquinavir), 티프라나비르 (tipranavir), 등과 같은 프로타아제 억제제들 (protease inhibitors), 및 엔푸버타이드 (enfuvirtide), 등과 같은 융합 단백질 억제제들과 같은 항체들 또는 상이한 항 바이러스제들 (antiviral agents) 을 포함한다. 약제용 조성물 및 공지된 항-HIV 제제들의 투여는 동시에 또는 순차적일 수 있다.
본 발명에 기술된 바와 같이 신규 구조적 컴포넌트들 (예를 들어, 잠금 도메인을 사용하여 안정화된 HIV-1 백신) 나노입자 백신 조성물들 또는 본 발명의 약제용 조성물들은 키트의 컴포넌트들로서 제공될 수 있다. 선택 가능하게, 이러한 키트는 패키징 (packaing), 인스트럭션들 (instructions), 완충제들, 기질들, 제어 항체들 또는 리간드들과 같은, 항체들 또는 리간드들과 같은, 다양한 상이한 시약들, 및 검출 시약들을 포함하는 부가적 컴포넌트들을 포함한다. 선택 가능한 인스트럭션 시트는 키트들에 부가적으로 제공될 수 있다.
예들
다음의 예들은 예시하기 위해 제공되고, 본 발명을 제한하지 않는다.
예 1
다양한 LD들을 갖는 BG505 gp140 나노입자들의 수율 및 순도
상이한 잠금 도메인들 (locking domains; LDs) 의 유용성은 표면 상에 표지된 HIV-1 BG505 UFO 삼량체들을 사용하여, 60-량체 E2p 나노입자 및 60-량체 I3-01 나노입자에 대해 검증되었다. 구성 설계는 도 6에 개략적으로 묘사된다. LD-포함 나노입자들은 100 mL ExpiCHO 세포들에서 일시적으로 발현되었고 이어서 2G12 항체 컬럼 또는 PGT145 항체 컬럼을 사용하여 정제되었다. 이어서 나노입자 샘플들은 그들의 수율 및 순도에 대해 Superose 6 10/300 GL 컬럼 상에서 크기 배제 크로마토그래피 (SEC) 에 의해 특성화되었다. SEC 프로파일들은 대부분의 LD들이 다양한 정도의 수율 및 순도로, HIV-1 BG505 UFO gp140 나노입자들을 안정화할 수 있다는 것을 나타낸다. E2p에 대해, LD4 및 LD5는 상이한 LD 들보다 고-품질 BG505 UFO gp140 나노입자들의 보다 큰 수율을 산출하고, 반면에 I3-01에 대해, LD4, LD5 및 LD7은 나노입자 수율 및 순도 면에서 상이한 LD들을 능가한다. 주목할 점은, E2p-LDx나노입자들은 또한 상청액으로부터 부분적으로 조립된 나노입자들 및 단일 삼량체들을 추출하는 2G12 항체 컬럼에 의해 정제되고, 반면에 I3-01-LDx나노입자들은, 완전히 조립된 나노입자에 대하여 매우 특이적인, PGT145 항체 컬럼에 의해 정제되었다. 따라서, E2p-LDx 와 I3-01-LDx 사이의 순도의 차이는 나노입자 플랫폼 또는 LD 설계에 의한 것이 아니라, 정제에 사용된 항체 컬럼에 의해 기인하였다.
예 2
구조적 어셈블리 다양한 LD들을 갖는 BG505 gp140 나노입자들
LD 포함 HIV-1 gp140 BG505 나노입자들의 어셈블리를 더 검증하기 위해, 먼저 청색 네이티브 폴리아크릴아마이드 겔 전기 영동법 (BN-PAGE) 에 의해 E2p-LDx 나노입자 및I3-01-LDx 나노입자를 분석하였다. 결과들은 도 7에 도시된다. 예상된 바와 같이, BN-PAGE는 어떠한 저 분자량 밴드들 (bands) 도 나타내지 않았고 모든 샘플들이 큰 크기 및 고 분자량의 나노입자들로 인해 레인 (lane) 의 상단에서 웰 (well) 에 포획된다는 것을 확인하였다. 선택된 E2p-LDx및 I3-01-LDx구성은 잘-형성된 나노입자들을 표지하는, 매질 염색 전자 현미경 (EM) 에 의해 분석되었다. 미가공 EM 이미지들에서, E2p-LDx나노입자들은 때때로 덜 엄격한 항체 컬럼의 사용으로 인해, 단일 삼량체들 또는 부분적으로 조립된 나노입자들과 혼합되었다. 그럼에도 불구하고, BN-PAGE 분석 및 매질 염색 EM 분석은 잠금 도메인들이 네이티브-유사 HIV-1 gp140 삼량체들을 표지하기 위해 2 개의 대형 나노입자 플랫폼들을 효과적으로 안정화시킬 수 있다는 것을 입증하였다.
예 3
잠금 메커니즘을 갖는 HIV-1 나노입자 백신의 설계
2 개의 구조는 BG505 UFO.664 gp140, (I3-01에 대해서만) 10-아미노산 GS링커, 나노입자 서브유닛 (E2p 또는 I3-01), 5-아미노산 GS 링커, 자가-어셈블리 나노입자 백본을 안정화시키는 잠금 도메인 (LD), 및 bNAb들을 향해 B 세포 발생을 가이드하기 위해 강한 T-소포 헬퍼 (T-follicular helper; Tfh) 반응을 유도하는 범-반응성 T-세포 에피토프 (PADRE 에피토프) 각각을 코딩하는, 제 1-세대 백신 구성들로서 선택된다. DNA 플라스미드들은 벡터 내로 삽입된 "항원" 유전자를 이용하여, 포유류 발현을 위해 흔히 사용되는 CMV 벡터에 기반하여 설계되었다 (도 2). 이들 2 개의 나노입자 구성들은 "UFO-E2p-LD4-PADRE" 및 "UFO-10GS-I3-01-LD7-PADRE"로 명명된다. 잠금 메커니즘은 도 2의 우측 코너에 개략적으로 묘사된다. 간략하게, 이량체성 LD 단백질의 N-말단은 나노입자 서브유닛의 C-말단에 융합된다. 자가-어셈블리 동안, 2 개의 나노입자 서브유닛들이 이량체 계면을 형성하기 위해 함께 모일 때, 이들 안정성을 현저하게 향상시키는, 이들은 나노입자 쉘 바로 아래에 제 2의 훨씬 강한 계면을 형성하도록 부착된 LD들을 매우 가깝게 가져올 것이다.
예 4
잠금 메커니즘을 갖는 나노입자 백신들의 생산
백신들은 정제된 나노입자 단백질들이고, 이는 용액 상 (phase) 으로 보조제와 혼합된다. 단백질 재료는 일시적인 ExpiCHO 세포들 또는 GMP 설비에서 안정화된 CHO-S 세포들로 생산될 수 있다. 제조 프로세스는: CHO 세포들에서의 발현, PGT145 친화도 컬럼에 의한 정제, 및 품질 관리 (QC) 의 3 단계를 수반한다.
실험실 규모의 생산에서, UFO gp140 나노입자들은 ExpiCHO 세포들 (Thermo Fisher) 에서 일시적으로 발현된다. 간략하게, ExpiCHO 세포들은 해동되고 135 rpm 및 8% CO2로, 37 ℃의 쉐이커 인큐베이터 (shaker incubator) 에서 ExpiCHOTM Expression Medium (Thermo Fisher) 를 사용하여 인큐베이션된다. 세포들이 10 x 106 ㎖-1의 밀도에 도달할 때, ExpiCHOTM Expression Medium은 트랜스펙션을 위해 6 x 106 ㎖-1로 세포 밀도를 감소 시키도록 첨가된다. ExpiFectamineTMCHO/플라스미드 DNA 복합체는 제조사의 인스트럭션들에 따라 ExpiCHO 세포들에서 100 ml 트랜스펙션을 위해 준비된다. 총 100 μg 의 플라스미드 및 320 μl의 ExpiFectamine™CHO 시약이 7.7 ml 의 저온 OptiPRO™배지 (Thermo Fisher) 에서 혼합된다. 제 1 영양 공급 (feed) 1일차 후, ExpiCHO 세포들은 (Thermo Fisher) Max Titer 프로토콜을 따라 5일 차에 부가적 영양 공급되어 120 rpm 및 8% CO2로, 32 ℃의 쉐이커 인큐베이터에서 배양된다. 트랜스펙션 후 13 내지 14 일차에 배양 상청액들을 수집하고, 20 분 동안 4000 rpm으로 원심 분리에 의해 정화되고, 0.45 mm 필터 (Thermo Fisher) 를 사용하여 여과된다. 나노입자들은 PGT145 항체 친화도 컬럼을 사용하여 배양 상청액들로부터 추출될 수 있다. 플라스미드 DNA 시드들은 이 실험실에서 준비될 수 있고 계약자 (Contractor) 의 GMP 생산 시설에서 대규모 생산을 위해 계약자에 제공될 수 있다.
예 5
잠금 메커니즘을 갖는 나노입자 백신들의 품질 관리
CHO/ExpiCHO-생산된 나노입자 단백질의 품질은 (1) 수율 및 순도에 대해Superose 6 10/300 GL 컬럼 및 청색 네이티브 폴리아크릴아마이드 겔 전기 영동 (BN-PAGE); (2) 열 안정성에 대해 MicroCal VP-Capillary 열량계 (Malvern) 상의 시차 주사 열량계 (differential scanning calorimetry; DSC); (3) 항원성에 대해 Octet RED96, 정량화 바이오 센서들, 및 bNAb들의 패널 및 비-Nab들의 패널을 사용하는 바이오-레이어 간섭법 (bio-layer interferometry; BLI); 및 (4) 나노입자 어셈블리 및 구조적 무결성에 대해 매질 염색 전자 현미경 (EM) 에 의해 평가될 수 있다. QC 프로세스는 선택된 나노입자 구성들에 대해 이 실험실에서 검증되었다 (이하 참조하라). 주목할 점은, QC 단계 (1) 및 단계 (2) 는 단백질 발현, 생산 및 정제를 따르는 임의의 GMP 설비의 현장에서 쉽게 수행될 수 있다.
100ml ExpiCHO 세포들에서 일시적인 발현 및 PGT145 항체 친화도 컬럼을 사용하여 세포 상청액으로부터의 정제 후, 나노입자들은 Superose 6 10/300 GL 컬럼 상에서 크기-배제 크로마토그래피 (SEC) 에 의해 분석되었다 (도 3a). 8 ㎖에서 단일의 날카로운 피크가 SEC 프로파일들에서 관찰되었고, 이는 구성들 둘 다에 대해 나타낸다. 또한, UV280 값은, E2p-기반 구성 및 I3-01-기반 구성에 대해 각각, 450까지 및 350까지 도달하고, 구성들 둘 다에 대해 15 내지 20 ㎎/ℓ로 추정되는, 고수율을 나타낸다. 특히 주목할 점은, 잠금 메커니즘이 안정성뿐만 아니라, I3-01 및 E2p에 대해 2 내지 3 배까지, 순수한 나노입자들의 수율을 개선할 수 있었다. 사전-SEC 나노입자 샘플들은 또한 겔 상의 저 분자량 종에 대응하는 밴드들을 나타내지 않는 BN-PAGE에 의해 분석되었고, 모든 샘플들은 나노입자들의 큰 크기 및 높은 분자량으로 인해 레인의 상단에서 포획되었다 (도 3b). BN-PAGE는 따라서 SEC 분석에서 관찰된 고순도를 확인하였다.
정제된 나노입자들은 이어서, BG505 UFO 삼량체의 열 안정성, Tm=68.24°C과 비교 가능한 높은 정도의 열 안정성을 나타내는, E2p-기반 구성 및 I3-01-기반 구성에 대한 각각 69.52 및 68.26 °C의 용융 온도 (melting temperatures; Tm) 를 산출하는, 열 안정성을 측정하기 위해 DSC에 의해 평가되었다 (도 3c). 따라서, 잠금 메커니즘을 사용하여, Tm은 나노입자 플랫폼에 독립적이고 표지된 항원들, 이 경우, UFO gp140 삼량체들의 열 안정성에 의해서만 결정된다. 2 개의 선택된 나노입자 구성은 또한 화학 물질들에 내성이 있고 -80 °C내지 4°C의 넓은 온도 범위에서 안정한 것으로 밝혀졌다. 예를 들어, 냉동되고-이어서-해동된 샘플들 또는 일주일 동안 4°C에 저장된 샘플들은 매질 염색 EM으로 분석되었고, 온도 변화로 인한 붕해는 관찰되지 않았다.
GMP-생산된 나노입자의 구조 및 항원성은 이하에 기술된 바와 같이 더 특징화되었다.
예 6
항원성 및 면역원성 평가
간단하고, 견고한 제조 프로세스 및 우수한 생화학적 특성 및 생물 물리학 특성에 부가적으로, 추가의 인 비트로 및 인 비보 평가는 잠금 메커니즘을 갖는 이들 UFO gp140 나노입자들이 가장 유망한 HIV-1 백신 후보들을 제공할 수도 있다는 것을 나타낸다.
인 비트로 평가 - 항원 및 구조 분석들 (또는 QC 단계 3 및 단계 4): 2 개의 선택된 나노입자들은 BLI 및 5 개의 bNAb들의 패널 (도 4a) 및 4 개의 비-NAb들 (도 4b) 의 패널들을 사용하여 항체 바인딩에 대해 평가되었다. UFO 삼량체는 대조군으로서 포함되었다. 전반적으로, 나노입자들은 둘 다 V2 apex, N332 슈퍼사이트 (supersite), 및 CD4b들을 인식하는 bNAb들에 대해 현저하게 향상된 바인딩을 나타내지만, gp120-gp41 계면에 대한 바인딩을 35O22만큼 감소 시켰고, 이는 나노입자 표면 상의 이 사이트에 대한 액세스 (access) 가 막혔기 때문일 수 있다. 나노입자 표지가 적당히 향상된 19b 바인딩을 나타내는, V3 팁을 제외하고 CD4b들, CD4i 사이트, 및 면역 우성 gp41 에피토프에 대한 비-NAb 바인딩을 향상시키지 않는다는 것은 또한 주목할 가치가 있다.
2 개의 선택된 나노입자들은 또한 매질 염색 EM에 의해 구조적으로 분석되었고, 이는 표면으로부터 돌출하는 네이티브-유사 UFO gp140 삼량체들의 치밀한 층 (dense layer) 을 갖는, 잘-형성된, 균질한 나노입자들을 나타낸다 (도 4c). 주목할 점은, 대부분의 경우에서 나노입자 쉘 내의 잠금 도메인들 (LDs) 은 이 저해상도에서 보이지 않았다. 그러나, 때때로 이는 일단 LD 단백질들에 대응하는, 나노입자 표면으로부터 내측으로 돌출하는 구조들을 인식할 수 있다.
작은 동물 모델들의 인 비보 평가: 마우스들과 래빗들에서 UFO 삼량체들 및 나노입자들의 서브 세트를 평가하였다. 마우스들에서, (스캐폴딩된 (scaffolded) gp140.681 구성을 제외한) 모든 삼량체들은 자가 (autologous) 티어-2 NAb들을 도출하지 못하였다. 페린틴 나노입자 및 I3-01 나노입자 설계의 초기 버전 (“UFO-PADRE-I3-01"로 명명됨) 은 I3-01에 대해 보다 강한 반응이 관찰된, 8 주차에 자가 티어-2 NAb를 유도하였다 (도 5a). TZM-bl HIV 중화 분석들은 마우스 혈청에서 비특이적 항 바이러스 활성을 제거하기 위해 정제된 IgG를 사용하여 수행되었다. 주목할 점은, 이는 WT 마우스에서 외피-유래된 티어-2 NAb 반응들의 최초 관찰인 반면, 이전 연구에서 BG505 SOSIP 삼량체는 16 주 면역화 후 WT 마우스에서 임의의 자가 티어-2 NAb 반응을 도출하는 것을 실패하였다. UFO 삼량체 및 페린틴 나노입자의 면역원성은 또한 항체 반응들이 종 방향으로 (longitudinally) 측정된, 래빗들에서 평가되었다. 결과들은 페린틴 나노입자가 8 주차에 자가 티어-2 NAb들을 유도하는 반면, BG505 UFO 삼량체는 이러한 티어-2 NAb 반응들을 유도하기 위해 또 상이한 2 달이 필요하다는 것을 나타낸다 (도 5b). 최근 연구에서, Zhu 실험실은 최종 나노입자 구성들 중 하나인, UFO-E2p-LD4-PADRE로 WT 마우스를 면역화하였다. 평가된 8 마리의 마우스들 중, 1 마리는 상이한 마우스들보다 훨씬 보다 강한 티어-2 NAb 반응들을 나타냈고, 반면에 모든 동물들은 11 주차에 1mg/ml의 IgG 농도에서 50 내지 95% 중화를 갖는 티어-2 NAb 반응들을 보였다 (데이터는 미도시). 따라서, 잠금 메커니즘을 갖는 최종 나노입자 백신 구성들이 아직 인 비보 평가되지 않았지만, 인 비보 데이터는 이 UFO gp140 나노입자들의 백신 잠재력을 모호하게 (unambitiously) 입증하였다. 이들 2 개의 나노입자 구성들이 이들 티어-2 단리체들에 대해보다 광범위하고 강력한 중화 항체 반응을 유도할 것으로 예상한다.
예 7
클래스-I 융합을 활용하는 상이한 바이러스들에 대한 백신 - 필로바이러스들 (Filoviruses)
필로바이러스를 위한 나노입자 백신을 개발하였다. 에볼라 바이러스들 (EBOV) 및 마르부르그 바이러스들과 같은 필로바이러스들은 인간들과 비인간 영장류들 (NHPs) 에서 치명적인 출혈열 (hemorrhagic fever) 을 유발할 수 있다. 필로바이러스들은 과거에 인간의 질병을 발병시킨 (outbreak) 반면에, 에볼라 바이러스는 2013 년 내지 2016 년 동안 역사상 가장 큰 발병에 전적으로 책임이 있고, 이는 9 개 아프리카 국가에 확산하여 28,600 건의 사례들과 11,325 명의 사망자들이 발생하였다. 현재, 콩고 민주 공화국 (DRC) 에서 600 명이 넘는 목숨들을 앗아간 에볼라 발병이 계속 진행 중이다. 필로바이러스 당단백질 (GP) 은 부착 및 막 융합을 개시함으로써 세포 진입을 매개하고 백신 설계의 주요 표적이다. GP는 인간 생존자들 및 면역화된 동물들로부터 단리된 항체들을 중화함으로써 인식될 수 있다 (Saphire et al., Cell 174 (4): 938-952, 2018 참조하라).
이 연구에서, GP (아미노산 33 내지 아미노산 632) 의 엑토도메인을 포함하지만 구조화되지 않은 뮤신-유사 도메인 (MLD, 아미노산 313 내지 아미노산463) 을 제거하여 GPDMuc로 명명되는, 다양한 GP 융합 구성들을 설계하기 위한 에볼라 바이러스의 자이르 (Zaire) 균주의 아미노산 서열 (GenBank: NP_066246) 을 사용하였다. GP의 GPDMuc형태는 구조적 연구들 (Lee et al., Nature 454 (7201): 177-182, 2008를 참조하라) 에서 널리 사용되었기 때문에, 이는 필로바이러스 백신 설계를 위한 합리성 기준 (rational basis) 을 제공한다. 야생형 (WT) GPDMuc 및 페린틴, E2p, 및 I3-01 나노입자 플랫폼들 상의 GPDMuc의 일반 UFO (UFOg) 형태를 표지하였다 (도 8a). ExpiCHO 세포들에서 일시적인 발현 후, 융합 단백질들은 Superose 6 10/300 컬럼 상의 정제 전 (페린틴 및 E2p에 대해) MAb100 항체 컬럼 또는 (I3-01에 대해) MAb114 항체 컬럼을 사용하여 융합 단백질들을 상청액들로부터 추출하였다. 전반적으로, SEC 프로파일들로 나타낸 바와 같이, GPDMuc-UFOg를 표지하는 나노입자들에 대해 WT GPDMuc를 표지하는 것들 보다 큰 수율과 순도를 관찰하였다 (도 8b). 페린틴의 경우, GPDMuc-UFOg-페린틴은 WT GPDMuc-페린틴보다 나노입자들의 뚜렷한 피크들이 나타났다. E2p의 경우, WT GPDMuc-E2p는 나노 입자들의 피크 및 조립되지 않은 단백질의 피크를 나타내는 반면에 GPDMuc-UFOg-E2p는 주로 나노입자들의 높은 피크를 나타냈다. I3-01의 경우, 융합 구성들 둘다는 SEC 프로파일들에서 15 내지 16 ㎖에서 조립되지 않은 융합 단백질들의 높은 피크들과 함께, 나노입자 어셈블리에서 어려움을 겪는 것처럼 보였다. 그럼에도 불구하고, 매질 염색 EM은 WT GPDMuc삼량체들을 나타내는 잘-형성된 페린틴, E2p, 및 I3-01 나노입자 및 GPDMuc-UFOg 삼량체들을 표지하는 잘-형성된 페린틴, E2p, 및 I3-01 나노입자를 증명하였다 (도 8c).
이전에, HIV-1 UFO 삼량체를 표지하는-E2p 나노입자 및 I3-01 나노입자에 대한 잠금 도메인들을 체계적으로 스크리닝하였다. 이 연구에서, 에볼라GPMuc-UFOg 삼량체를 표지하는-E2p 나노입자 및 I3-01 나노입자에 대한 잠금 도메인을 체계적으로 스크리닝하였다. 잠금 메커니즘은 개략적 도면으로 예시될 수 있다 (도 8d, 좌측). 잠금 도메인들을 갖는 60-량체 나노입자의 구조를 시각화하기 위해, E2p 나노입자에 대한 원자 모델을 구축하고, 단계적 방식으로 모델에 잠금 도메인 (LD4) 및 T-세포 에피토프 (PADRE) 를 통합하였다 (도 8d, 우측). 이 연구에서, 7 개의 GPDMuc-UFOg-E2p-LDn 구성들 (n = 1 내지 7) 및 5 개의 GPDMuc-UFOg-10GS-I3-01-LDn 구성 (n=4/5/7/8/9) 은 ExpiCHO 세포들에서 일시적으로 발현되었다. GPDMuc 융합 단백질들은 Superose 6 10/300 컬럼 상의 정제 전 (페린틴 및 E2p에 대해) MAb100 항체 컬럼 또는 (I3-01에 대해) MAb114 항체 컬럼을 사용하여 융합 단백질들을 상청액들로부터 추출하였다. 모든 E2p-기반 구성들 중에서, LD4 및 LD7이 가장 높은 수율 및 순도를 나타냈고, 반면에 모든 I3-01-기반 구성들 중에서, LD7 및 LD8이 최상의 결과들을 제공한다 (도 8e). 이는 LD4 및 LD7이, 각각, E2p 및 I3-01과 가장 호환 가능한 것으로 보이는, HIV-1 UFO gp140 나노입자들에 대한 이 이전 발견들과 대체로 일치한다. 그러므로, LD4와 조합된 E2p 및 LD7과 조합된 I3-01은 표지된 면역원과 무관하게, 백신 개발을 위한 2 개의 일반적인 나노입자 플랫폼들로서 사용될 수 있다.
HIV-1 gp140 나노입자들에 대한 이 이전의 관찰과 일치하는 또 상이한 발견은 잠금 도메인의 C-말단에 T-세포 에피토프를 추가하면 발생된 나노입자들, 이 경우, GPDMuc-UFOg 나노입자들의 수율 및 순도가 현저하게 개선된다는 것이다 (도 8f). 이는 중공형 나노입자의 중심에 소수성 T-세포 에피토프 클러스터 (cluster) 의 형성에 의해 설명될 수 있다 (도 8d, 우측). BN-PAGE는 겔 상에 고분자량 밴드들로 나타냄으로써 나노입자 어셈블리를 더 확인하였다 (도 8g). 그러나, 모든 GPDMuc-I3-01 융합 구성들은 조립되지 않은 이량체 종 및 단량체 종을 나타냈다. 마지막으로, 3 개의 WT GPDMuc 나노입자들의 항원 프로파일 및 3 개의 GPDMuc-UFOg 나노입자들의 항원 프로파일은 ELISA에서, 그들 각각의 GPDMuc 삼량체들과 비교되었다 (도 8h). 전반적으로, GPDMuc 나노입자들은 GPDMuc 삼량체들보다 중화 항체들에 훨씬 보다 강한 바인딩을 나타냈다.
예 8
클래스-I 융합을 활용하는 상이한 바이러스들에 대한 백신 - 아레나바이러스들 (Arenaviruses)
동일한 설계 전략에 기반하여, 아레나바이러스에 대한 나노입자 백신들을 개발하였다. 아레나바이러스들은 또한 인간에게 심각한 출혈열을 도출하는 것으로 공지되어 있다. 라사 맘마레나바이러스 (Lassa mammarenavirus; LASV) 는 라사 열병의 병인 인자 (etiologic agent) 이고 서 아프리카의 주요 공중 보건 부담 (burden) 이다. LASV 당단백질 복합체 (glycoprotein complex; GPC) 는 수용체-바인딩 서브유닛 GP1 및 막횡단, 융합-매개 서브유닛 GP2를 각각 포함하는, 이종이량체들의 삼량체이다. HIV-1 gp160 및 Ebola GP와 같은 상이한 클래스-I 융합 단백질들과 유사하게, LASV GPC는 세포 진입을 담당하고 항체 반응을 중화하기 위한 주요 표적을 나타낸다. 현재, LASV 감염에 대한 예방 가능한 백신은 없다. 최근에, 인간 중화 항체를 갖는 복합체의 LASV GPC의 결정 구조가 보고되었다 (Hastie et al., 356 (6341): 923-928, 2017를 참조하라).
이 연구에서, LASV 균주의 엑토도메인 (GenBank: NP_694870) 의 아미노산 서열에 기반하여 GPC 융합 구성을 설계하였다. LASV GPC 및 나노입자들의 태그-없는 (tag-free) 정제를 위해 중화 항체 37.7H에 기반하여 항체 컬럼을 패킹하였다 (Hastie et al., Science 356 (6341): 923-928, 2017를 참조하라). 2 개의 융합 구성들 (GPC-10GS-FR 및 GPC-5GS-E2p-LD4-PADRE) 은, 각각, 26.3 ㎚ 및 37.6 ㎚의 직경을 갖는 나노입자들로 이어질, LASV 나노입자 백신 개념을 평가하도록 설계되었다 (도 9a). 이들 2 개의 융합 구성들은 ExpiCHO 세포들에서 일시적으로 발현되고 37.7H 항체 컬럼을 사용하여 정제되었다. 37.7H는 염기에서 LASV GPC 삼량체의 GP2에 바인딩하기 때문에, 나노입자 표면 상의 GP2 로의 제한된 액세스로 인해 GPC 나노입자들의 정제에 최적이 아닐 수도 있다. 이는 구성들 둘 다에 대해 관찰된 낮은 수율을 설명한다. 그럼에도 불구하고, 37.7H-정제된 단백질들은 매질 염색 EM에 의해 분석되었고, 이는 조립되지 않은 단백질들과 혼합된 잘-형성된 나노입자들을 나타냈다 (도 9b). GPC와 페린틴 나노입자 사이의 긴 플렉서블 링커로 인해, GPC 스파이크들은 페린틴 나노입자 표면 상에서 인식될 수 없다 (도 9b, 좌측). 대조적으로, GPC-5GS-E2p-LD4-PADRE에 대한 EM 이미지들의 클로즈업 뷰 (close-up-view) 는 E2p 나노입자 표면 상에 GPC 삼량체 층을 드러냈다 (도 9b, 우측). 종합하면, 이 연구는 보다 효과적인 항체 컬럼이 GPC 나노입자들의 순도를 더 개선할 수도 있지만, LASV GPC가 잠금 도메인을 갖는 60-량체 나노입자 상에 표지될 수 있다는 것을 확인하였다.
예 9
클래스-I 융합 메커니즘을 활용하는 상이한 바이러스들에 대한 백신들 - RSV
호흡기 세포 융합 바이러스 (RSV) 에 대한 나노입자 백신을 부가적으로 개발하였다. 인간 호흡기 세포 융합 바이러스 (hRSV) 감염은 유아들, 어린이 및 노인의 세기관지염 (bronchiolitis) 및 입원 (hospitalization) 의 주요 원인이다. 융합 당단백질 (F) 은 세포 진입을 매개하고 백신 설계의 주요 표적이다. F는 감염된 공여자들로부터 단리된 항체를 중화함으로써 인식될 수 있다. HIV-1 gp160, 에볼라 GP 및 라사 GPC와 같이, hRSVF는 N-말단에 신호 펩타이드 (아미노산 1 내지 아미노산25) 및 C-말단 근처의 막 앵커 (membrane anchor) 를 갖는 클래스-I 막횡단 표면 단백질이다. F는 먼저 불활성 전구체 단백질, 퓨린 셀룰러 엔도프로타아제 (cellular endoprotease) 또는 퓨린-유사 셀룰러 엔도프로타아제에 의한 트랜스-골지 복합체 (trans-Golgi complex) 의 절단에 의해 활성화 시 동종삼량체로 조립되는, F0로서 합성된다. 절단은 NH2-F2-F1-COOH의 형태로 2 개의 디설파이드-결합된 서브유닛들을 야기한다. 절단의 결과로서, F1의 N-말단은 융합을 촉발하기 위해 숙주 세포막 내로 직접적으로 삽입되는 소수성 펩타이드인, 융합 펩타이드 (아미노산들 137 내지 아미노산154) 를 포함한다. F1 서브유닛은 또한 융합 동안 연관되고 바이러스 막과 세포 막을 근접하게 가져오는 헵타드 반복들 (HRs) 의 2 개의 영역을 포함한다. 중화 항체들과의 복합체에서 사전-융합 F의 결정 구조들은 원자 분해능으로 결정되었다 (McLellan et al., 340 (6136): 1113-1117, 2013를 참조하라).
이 연구에서, 다양한 잠금 도메인들을 갖는 페린틴, E2p 나노입자 및 I3-01 나노입자 및 E2p 60-량체 및 I3-01 60-량체를 사용하여 평가된 링커들 상에 사전-융합 hRSV F를 표지하였다. 분자 모델링은 hRSV F FR 나노입자가 33.9 ㎚ 이상의 크기를 가질 것이고 hRSV FE2p (또는 I3-01) 이 적어도 45.2 ㎚의 직경을 가질 것이라는 것을 나타낸다 (도 10a). 사전-융합 F-특이 인간 중성화 항체 D25를 사용하여 hRSV F 및 F-표지 나노입자들을의 태그-없는 정제를 위해 항체 컬럼을 패킹하였다 (McLellan et al., 340 (6136): 1113-1117, 2013를 참조하라). 모든 hSV F 융합 구성은 ExpiCHO 세포에서 일시적으로 발현되었다. F 융합 단백질들은 D25 항체 컬럼을 사용하여 상청액들로부터 추출되고 매질 염색 EM에 의해 분석되었다. F의 C-말단과 페린틴의 N-말단 사이에 10-아미노산 (G4S)2링커를 표지하는, F-10GS-FR 구성은, 분자 모델링과 일치하는 (도 10a), 페린틴 표면 상의 가시성있는 "엄지-유사" 사전-융합 F 삼량체들을 갖는 나노입자들을 형성하였다 (도 10b). 사전-융합 F는 이어서 잠금 도메인 (LD4) 및 T-세포 에피토프 (PADRE) 를 포함하는 E2p 나노입자들 상에 표지된다. F의 C-말단과 E2p 서브유닛의 N-말단 사이에 10-아미노산 (G4S)2 링커를 갖거나 갖지 않는 2 개의 구성들이 평가되었다. 긴 링커들 없이, 사전-융합 F 삼량체들은 E2p 나노입자 표면 상에 입상 돌출부들로서 보여지는 (도 10c, 좌측) 반면에, 긴 링커들을 갖는, "엄지-유사" 사전-융합 F 삼량체들의 어레이 (array) 는 E2p 나노입자 표면 상에서 인식될 수 있다 (도 13c, 우측). 마지막으로, 사전-융합 F는 잠금 도메인 (LD7) 및 PADRE를 포함하는 I3-01 나노입자 상에 표지되었다. T-세포 에피토프 (PADRE) 가 F와 E2p (외측) 사이에 삽입되고 LD7의 C-말단 (내측) 에 부착된, 2 개의 구성들은 잠금 도메인의 존재 하에 나노입자 어셈블리 상의 T-세포 에피토프 위치의 효과를 조사하기 위해 생성되었다. 전자 (F-5GS-PADRE-I3-01-LD7) 의 경우, 잘-형성된 나노입자들을 관찰했지만 나노입자 표면 상의 사전-융합 F 스파이크들을 인식할 수 없었다 (도 11d, 좌측). 후자 (F-10GS-I3-01-LD7-PADRE) 의 경우, 조립되지 않은 F 삼량체들의 존재에도 불구하고, "엄지-유사" 사전-융합 F 삼량체의 층으로 꾸며진 잘-형성된 나노입자들을 관찰하였다 (도 11d, 우측).
종합하면, 이 결과들은 hRSV F가 잠금 도메인들을 갖는 E2p 나노입자 및 I3-01 나노입자 상에 표지될 수 있다는 것을 입증하고, 상이한 길이들의 링커들을 사용하고 상이한 위치들에 T-세포 에피토프를 배치하기 위한 예들을 제공한다.
예 10
클래스-I 융합 메커니즘을 활용하는 상이한 바이러스들에 대한 백신들 -CoV들
또한 코로나바이러스들 (CoV들) 에 대한 나노입자 백신을 개발하였다. CoV들은 양성-가닥화된 (positive-stranded) RNA 게놈 (genome) 을 갖는 외피화된 바이러스들이다. 2002 년에, 아시아에서 중증 급성 호흡기 증후군 (severe acute respiratory syndrome; SARS) 의 발병은 나중에 SARS-CoV로 명명된 신규한 코로나바이러스의 발견으로 이어졌다. 급증 동안, SARS-CoV는 최대 10 %까지의 치사율로 8,000 명이 넘는 사람들을 감염시켰다. 2012 년에, 코로나바이러스의 신규한 종인 중동 호흡기 증후군 코로나바이러스 (Middle East respiratory syndrome coronavirus; MERS-CoV) 가 확인되었고 이래로 35 %까지의 치사율로 27 개국에서 2000 명이 넘는 사람들이 감염되었다. 두 코로나바이러스들에 대한, 바이러스 게놈은 스파이크 (S) 구조적 단백질, 외피 (E) 구조적 단백질, 막 (M) 구조적 단백질, 및 뉴클레오캡시드 (N) 구조적 단백질을 코딩하고, 이들 중 S 단백질은 S1 서브유닛, 및 후속 막 융합 및 바이러스 진입에서 수용체-바인딩 도메인 (RBD) 을 통해 숙주 수용체에 대한 바인딩을 맡는다. RBD는 코어 서브 도메인 (core subdomain) 및 수용체-바인딩 모티프 (receptor-binding motif; RBM) 를 포함한다. 코어 서브 도메인들은 2 개의 코로나바이러스들 사이에서 매우 유사하지만, 그들의 RBM들은 상이한 수용체 특이성들을 나타낸다: SARS-CoV는 안지오텐신-변환 효소 2 (angiotensin-converting enzyme 2; ACE2) 를 인식하는 반면, MERS-CoV는 디펩티딜 펩티다제 4 (dipeptidyl peptidase 4; DPP4) 에 바인딩한다. 코로나바이러스들 둘 다에 대해, S 단백질은 감염을 맡고 따라서 백신 설계를 위한 주요 표적이 된다.
이 연구에서, E2p 구성 및 I3-01 구성에 통합된 잠금 도메인을 갖는, 페린틴, E2p, 및 I3-01 나노입자들 상에 MERS-CoV S 삼량체 (Pallesen et al., PNAS, 114: E7348-E7357 및 PDB ID: 5W9K를 참조하라) 를 표지하였다. S 구성은 특정 MERS-CoV 균주 (GenBank: JX869059) 로부터 유래된다. 분자 모델링은 MERS S FR 나노입자가 34.0 ㎚ 이상의 크기를 가질 것이고 MERS S E2p (또는 I3-01) 나노입자가 적어도 45.2 ㎚의 직경을 가질 것이라는 것을 나타낸다 (도 11a). RBD-지향 중성화 항체, MCA1을 사용하여 MERS-CoV S 및 S 나노입자들의 태그-없는 정제를 위한 항체 컬럼을 개발하였다. ExpiCHO 세포들에서 일시적인 발현 후, MCA1 항체 컬럼을 사용하여 상청액들로부터 S 융합 단백질들은 추출되었고 매질 염색 EM에 의해 직접 분석되었다. S의 C-말단과 페린틴 서브유닛의 N-말단 사이에 10-아미노산 GS 링커 (서열 번호: 24) 를 포함하는, MERS S-10GS-FR은, 표면 상에 가시적인 큰 S 스파이크들을 갖는 나노입자들을 형성하였다 (도 11b, 좌측). MERS S-10GS-E2p-LD4-PADRE (도 11b, 중앙) 및 S-10GS-I3-01-LD7-PADRE (도 11b, 우측) 는 표면 상에 표지된 20 개의 S 스파이크들을 갖는 보다 큰 나노입자들을 형성하였다. 그러나, EM 이미지들은 또한 조립되지 않은 S 융합 단백질들을 나타냈다.
나노입자들 상의 S 단백질의 안정성을 감쇠시키기 위해, S와 나노입자 서브유닛 사이에, "T4 피브리틴의C-말단 삼량체화 모티프”, 또는 폴돈을 삽입하였다. S-폴돈-10GS-FR (도 11c, 좌측) 및 S-폴돈-10GS-I3-01-LD4-PADRE (도 11c, 우측) 에 의해 형성된 나노입자들 상의, S 스파이크들이 부가적 구조적 컴포넌트들이 잠금 도메인들을 갖는 나노입자들로 통합될 수 있다는 것을 확인하는, EM 이미지들에서 명확하게 인식될 수 있다.
예 11
클래스-II 융합 메커니즘을 활용한 바이러스 백신 - HCV
HCV E2 코어 나노입자 백신들의 개발에 동일한 백신 설계 전략을 적용하였다. C 형 간염 바이러스 (HCV) 는 플라비비리대 (Flaviviridae) 과의 헤파시바이러스 (Hepacivirus) 속의 작고, 외피화된, 단일-가닥화된, 양성-센스 (sense) RNA 바이러스이다. 전 세계 인구의 1 내지2 %를 감염시키는, HCV는 매년 약 500,000 명이 사망하고 매년 150만 내지 2백만 건으로 추정되는 신규한 감염으로 이어지는 주요 건강 부담이다. HCV는 유전적 다양성이 높고 7 개의 주요 제노타입들 (genotypes) 과 86 개의 서브타입들로 분류될 수 있다. HCV는 숙주 면역 시스템을 탈출하기 위해 감염된 개인들 내에서 바이러스 준종들 (viral quasispecies) 을 발생시키는 신속한 돌연변이를 겪을 수 있다. 그러나, 급성으로 감염된 환자들의 20 내지 30 %에서 자발적인 바이러스 제거 (spontaneous viral clearance) 는 HCV 감염이 백신 접종에 의해 유도된 효과적인 면역 반응으로 예방 가능하다는 것을 암시한다. E1 외피 당단백질 및 E2 외피 당단백질은 숙주 간세포들 (hepatocytes) 로의 바이러스 진입을 매개하는 HCV 외피 상에 이종이량체를 형성한다. 수용체 바인딩 단백질로서, E2는 숙주 세포 수용체들 CD81 및 SR-B1과 직접적으로 상호 작용하고 주로 CD81 상호 작용들을 블로킹 (blocking) 함으로써 HCV를 중화하는 중화항체들에 대한 1 차 표적이다. E2 코어들로 명명된, 매우 가변 영역 1 (highly variable region 1; HVR1) 및 가변 영역 (variable region) 2 및 가변 영역3 (VR2/3) 에서 절단한 (truncations) E2 구성들은, 구조 분석을 쉽게 하도록 개발되었다. 광범위하게 중화항체 AR3c (Kong et al., Science 342 (6162): 1090-1094, 2013을 참조하라) 와의 복합체에서 단리체 H77 (제노타입1a) 로부터 유래된 E2 코어의 결정 구조 및 중화항체 2A12 (Khan et al., Nature, 509 (7500): 381-384, 2014) 에 바인딩하는 단리체 J6 (제노타입 2a) 로부터 유래된 절단된 E2의 결정 구조는 HCV 외피 당단백질들의 면역 인식에 대한 최초의 통찰을 제공하였다. 그러나, 현재 HCV 감염을 예방하기 위해 사용 가능한 허가된 백신은 없다.
이 연구에서, HCV 백신들로 E2 코어 나노입자들을 설계하였다. 표면 상에 24 내지 60 개의 E2 코어들을 각각 표지하는 나노입자들이 보존된 E2 에피토프들에 대한 효과적인 중화 항체 반응들을 도출할 수 있고 따라서 유망한 HCV 백신 후보들을 제시할 수 있다는 가설을 세웠다 (도 12a). 이 가설을 검증하기 위해, 3 개의 나노입자 플랫폼들, 24-량체 페린틴 (FR) 및 60-량체 E2p 및 60-량체 I3-01을 평가하였고, 이는 24.5 내지 37.5nm의 E2 코어 나노입자들을 유도할 것이다 (도 12b). 이 연구에서 사용된 E2 코어 구성들은 2 개의 단리체들, H77 (제노타입 1a) 및 HK6a (제노타입 6a) 의, E2의 아미노산 서열들로부터 유래되었다. 이 설계에서, E2 코어의 C-말단은 10-GS 링커 (서열 번호: 24) 를 통해 나노입자 서브유닛의 N-말단에 유전적으로 융합되었다. E2 코어 융합 구성들은 ExpiCHO 세포 또는 293 F 세포들에서 일시적으로 발현되었고 AR3c 항체 컬럼에 이어서 Superose 6 10/300 GL 컬럼을 사용하는 SEC에 의해 정제되었다 (도 12c). 구성 유래된 H77 단리체의 경우, 24-량체 및 60-량체에 대해 상이한 패턴들이 관찰된, SEC 프로파일들이 모든 E2 코어 나노입자들에 대해 고수율 및 고순도를 입증하였다. E2-코어-10GS-FR은 응집체들에 대응하는 8 내지 9 ㎖에서 피크를 생성한 반면, E2-코어-10GS-E2p 구성 및 I3-01 구성 둘 다 나노입자 피크에 이어지는 (tailing) 는 15 내지 20 ㎖에서 피크를 나타냈다 (도 12c). 구성 유래된 HK6a 단리체의 경우, 입자 수율 및 순도의 감소가 저 분자량 종들의 향상을 수반한다. SEC-정제된 E2 코어 융합 단백질은, BN-PAGE 및 매질 염색 EM에 의해 분석되었고, 각각, 고 분자량 밴드들 및 균일 나노입자들을 나타냈다 (도 12d 및 도 12e). 가장 광범위하게 중화 항체들에 대한 EC50에서 최대 100 배까지의 변화로 나타낸 바와 같이, E2 코어 나노입자들에 대한 향상된 항체 바인딩을 관찰하였다 (도 12f). 항원성에 대한 다량체 표지의 효과를 더 조사하기 위해, Octet 및 작은 항체들의 패널을 사용하여 H77-유래된 E2 코어 나노입자 및 HK6a-유래된 E2 코어 나노입자를 그들의 각각의 E2 코어들에 대하여 평가하였다 (도 12g). 피크 항체 바인딩 신호와 항원 원자가 (valency) 사이의 상관 관계는 H77 유래된 나노입자 및 HK6a 유래된 나노입자 둘 다에 대해: 60-량체> 24-량체> 단량체로 관찰되었다.
마지막으로, E2 코어 나노입자들에서 잠금 도메인의 사용을 조사하였다. 이를 위해, HCV H77 단리체로부터 유래된 E2-코어-10GS-E2p-LD4-PADRE 구성 및 E2-코어-10GS-I3-01-LD7-PADRE 구성을 평가하였다. 매질 염색 EM은 구성 둘 다에 대해 깨끗하고, 균질한 나노입자들을 나타냈다 (도 12h). 주목할 점은, E2-코어-10GS-E2p-LD4-PADRE는 LD4 및 PADRE에 의해 형성된 치밀한 내측 쉘로 인해 EM 이미지들에서 단단한 표면을 나타냈고, 반면에 LD4 및 PADRE가 없는 상대 (counterpart) 는 중공형 (hollow) 으로 보였다. 그럼에도 불구하고, 이 결과들은 HCV E2 코어들이 잠금 도메인들을 갖는 나노입자들 상에 표지될 수 있다는 것을 확인하였다.
예 12
클래스-II 융합 메커니즘을 활용한 바이러스들에 대한 백신 - ZIKV
본 발명자들은 또한 지카 바이러스 (ZIKV) DIII 나노입자 백신들의 개발을 위해 본 명세서에 기술된 백신 설계 전략을 적용하였다. ZIKV는 뎅기열 (DENV) 바이러스, 웨스트 나일 (West Nile; WNV) 바이러스, 일본 뇌염 (Japanese encephalitis; JEV) 바이러스 및 황열병 (YFV) 바이러스를 또한 포함하는, 플라비비리대의 양성-가닥화된 RNA 바이러스이다. ZIKV 유전체는 3 개의 구조적 단백질들 (캡시드, prM, 및 외피) 과 7 개의 비-구조적 단백질들 (NS1, NS2a/ NS2b, NS3, NS4a/ NS4b, 및 NS5) 을 코딩한다. 2015 내지 2016년에 ZIKV 발병은 전 세계적으로 공중 보건 위기를 야기하였다. 주로 에데스 (Aedes) 종들 모기들에 의해 전염되는 (transmitted), ZIKV는 성인들에서 길랭-바레 증후군 (Guillain-Barr syndrome; GBS) 을 야기하고 신생아들에서 소두증 (microcephaly) 을 야기할 수 있다. 마우스들 및 NHP들에서 ZIKV 감염을 방지하기 위한 몇몇의 외피 (E)-기반 백신 후보들이 보고되었다. 그러나, 기존의 (preexisting) 항-플라비바이러스 면역성으로 인한 ZIKV 감염 및 병인의 항체-종속성 향상 (antibody-dependent enhancement; ADE) 은 현재의 백신 전략들에 대한 안전 문제들을 제기한다. ZIKV 감염을 예방하기 위해 사용 가능한 상이한 보다 안전하고 보다 효과적인 백신들은 없다.
ZIKV E 단백질은 DI, DII 및 DIII의, 3 개의 구조적 도메인들로 구성된다. 3 개의 도메인들 중, 연장된 핑거-유사 DII는 E 이량체화를 맡고 바이러스와 숙주 세포 막들의 융합에 의해 pH-종속성 진입을 촉발하는 보존된 융합 루프 (fusion loop; FL) 를 포함한다. DIII는 바이러스 부착에 기여하는 C-말단 면역글로불린 (immunoglobulin; Ig)-유사 도메인을 형성한다. 많은 중화 항체 및 비-중화 항체가 DENV에 대한 사전 노출을 갖고 그리고 갖지 않는 ZIKV-감염된 공여자들로부터 확인되었다. 일반적으로, DIII-지향된 항체들은 DI/II-지향된 항체들보다 ZIKV-특이적이고 보다 강력하게 중화되는 경향이 있다. 후자는 종종 DENV와 교차-반응성이고, 중화가 불량하고, 그리고 일부 경우들에서, 인 비보 바이러스 감염을 뚜렷하게 향상시킨다.
이 연구에서, 잠재적인 ZIKV 백신 후보 물질들로서 24-량체 페린틴 (FR) 과 60-량체 E2p 및 60-량체 I3-01을 기반으로 DIII 나노입자들을 설계하였다. DIII 융합 구성들은 아프리카 균주 MR766 (GenBank: MK105975) 의 E 단백질 및 아시아 균주 BeH818995 (GenBank: KU365777) 의 E 단백질로부터 유래된 DIII의 아미노산 서열에 기반한다. 또한 DIII-지향적 중화 항체 ZK2B10을 사용하여 DIII 나노입자들의 태그-없는 정제를 위한 항체 컬럼을 개발하였다 (Yu et al., JCI Insight 2 (12): 93042, 2017를 참조하라). 모든 DIII-FR 융합 구성들은 ExpiCHO 세포들에서 일시적으로 발현되었고 ZK2B10 항체 컬럼에 의해 정제되었다. 분자 모델링은 표면 상에 DIII 층을 갖는 60-량체 I3-01이 35 ㎚까지의 나노입자를 렌더링 (rendering) 할 것이라는 것을 나타낸다 (도 13a, 좌측). SEC 프로파일에서, 잘-형성된 DIII-페린틴 나노입자들에 대응하는 높은 피크를 관찰하였다 (도 13a, 우측). Superose 6 10/300 GL 컬럼 상의 14 ㎖로 용리된 SEC 분획은 BN-PAGE에 의해 분석되고, 이는 FR의 나노입자들의 고 분자량 밴드 특성을 나타냈다 (도 13b). 매질 염색 EM은 잘-형성된 DIII 나노입자들을 나타냈다 (도 13c, 좌측). 그러나, DIII의 작은 크기와 플렉서블10GS 링커의 사용으로 인해, 나노입자 표면 상의 DIII를 인식할 수 없었다. 동일한 프로토콜에 따라, I3-01 융합 단백질 및 E2p 융합 단백질을 생산하고 매질 염색 EM에 의해 그들의 나노입자 어셈블리를 평가하였다 (도 13c, 중앙 및 우측). DIII-10GS-I3-01 나노입자들이 EM 이미지들에서 쉽게 보일 수 있었던 반면에, E2p는 낮은 수율을 발생시키는, 나노입자 어셈블리에 어려움을 갖는 것으로 보였다.
마지막으로, 잠금 메커니즘이 I3-01 나노입자 상의 DIII 표지를 더 개선할 수 있는지를 조사하였다. 실제로, 매질 염색 EM은 고수율 및 고순도를 갖는 ExpiCHO 세포들에서 생산된 균질한 DIII-10GS-I3-01-LD7-PADRE 나노입자들을 나타냈다 (도 13d). 요약하면, 잠금 도메인 LD7 및 T-세포 에피토프 PADRE를 포함하는 I3-01 나노입자 구성에 대해 관찰된 최적의 특성들을 갖는 다양한 나노입자 플랫폼들 상에서 ZIKV DIII을 성공적으로 표지하였다.
예 13
비 바이러스 표적들에 대한 백신 개발 - 말라리아 백신
이 백신 연구를 열대열원충 (말라리아) 및 결핵균 (TB) 와 같은 세포 내 병원체 및 전구단백질 (proprotein) 변환 효소 서브틸리신/켁신 9 형 (proprotein convertase subtilisin/kexin type 9; PCSK9) 과 같은 인간 단백질로 확장하였다. 이 주요 가설은 나노입자 표지가 세포 내 병원체에 대한 면역 반응을 향상시키고 인간 단백질들에 대한 면역 내성 (immune tolerance) 을 파괴한다는 것이다. 항체 반응 및 T 세포 반응은 주요 면역학적 판독 값들 (immunologic readouts) 로 측정될 것이다.
말라리아 백신. 열대열원충 (Plasmodium (P.) falciparum) 은 인간들에서, 생명을 위협하는 질병인, 말라리아를 야기하는 단세포 원생동물 기생충 (unicellular protozoan parasite) 이다. 열대열원충은 감염된 암컷 아노펠레스 (Anopheles) 모기들의 묾들을 통해 사람들에게 전염될 수 있다. 2017 년에, 열대열원충은 87 개 국가들에서 2 억 1900 만 명이 감염되었고 약 435,000 건이 말라리아 관련 사망들이 발생하였다. 현재, 열대열원충 감염을 예방하기 위한 허가된 백신은 없지만 말라리아는 치료될 수 있다. 이 연구에서, 이 기생충의 수명주기에 중요한 3 개의 항원들에 기반한 말라리아 나노입자 백신들: Pfs25, 포자소체 단백질 (circumsporozoite protein; 망상적혈구 바인딩 단백질 동족체 5 (reticulocyte binding protein homolog 5; PfRH5) 를 개발하였다.
제 1 항원, Pfs25는, 기생충의 접합체 (zygote) 형태 및 오키니트 (ookinete) 형태의 표면 상에 발현된 25-kDa의 성기 (sexual stage) 항원이다. 항-Pfs25 항체들은 모기 벡터의 중장 (midgut) 에서 열대열원충 난모낭들 (oocysts) 의 발생을 차단할 수 있다. 현재, Pfs25는 가장 많이 개발된 전염-차단 백신 (TBV) 후보이고 인간 임상 평가들에서 평가되었다. 보조의 (adjuvant) 몬타니드 (Montanide) ISA 51에서 수용성 Pfs25를 사용한 인간 백신 접종에 의해 유도된 항-Pfs25 항체들은 표준 막 공급 분석 (standard membrane feeding assay; SMFA) 에서 기능적이고열대열원충의 실험실 단리체 및 현장 단리체 둘 다의 발생을 차단한다. 인간화된 마우스들로부터 단일클론 항체들 (monoclonal antibodies) 과의 복합체인 Pfs25의 구조들이 결정되었고 (Scally et al., Nat Commun, 8: 1568, 2017를 참조하라), 합리적인 백신 설계를 위한 기반을 제공한다 (도 14a).
세포 상청액들로부터 Pfs25를 정제하는 능력에 대해, 2 개의 항-Pfs25 항체들, Fab1260 및 Fab1269 (도 14b) 를 평가하였다. ELISA 데이터에 기반하여, Fab1260은 Pfs25 나노입자들의 태그-없는 정제를 위해 항체 컬럼을 패킹하기 위해 선택되었다. 또한 나노입자 표면 상의, 편평한 L-형 구조를 갖는, Pfs25의 다량체 표지를 쉽게 하도록 "넥" 영역을 설계하였다 (도 14c). 보다 구체적으로, 바이러스 단백질로부터 유도된 3-나선 다발은 링커를 사용하거나 또는 링커를 사용하지 않고, Pfs25와 나노입자 서브유닛 사이에 삽입되었다 (도 14c). 넥 1 및 넥 2로 명명되는, 헨드라 (Hendra) 바이러스 도메인으로부터 유래된 2 개의 나선 다발들 (PDB ID: 4HEO) 및 홍역 바이러스 도메인 (PDB ID: 1OKS) 은 다양한 나노입자 플랫폼들과 함께 평가되었다. 모든 융합 구성들은 ExpiCHO 세포들에서 발현되었고 이어서 Fab1260 항체 컬럼을 사용하여 정제되었다. Fab1260-정제된 융합 단백질들은 매질 염색 EM에 의해 특징화되었고, 이는 넥1-포함 구성들에 대해서만 나노입자들을 나타냈다 (도 14d). 구체적으로, Pfs25-넥1-10GS-FR 나노입자들은 EM으로 나타낸 바와 같이, 가장 높은 수율 및 가장 높은 순도를 나타냈다 (도 14d, 좌측). Pfs25-넥1-E2p-LD4-PADRE 구성은 잘-형성된 나노입자들 및 응집체들의 혼합물을 생성하는 것으로 보였다 (도 14d, 중앙). Pfs25-넥1-10GS-I3-01-LD7-PADRE 구성은 페린틴 구성과 유사한 고순도를 갖지만 약간 낮은 수율을 갖는 나노입자들을 생산하였다 (도 14d, 우측). 이 결과는 3 폴드 (fold) 축 각각을 둘러싸는 I3-01의 N-말단이 5 ㎚의 큰 간격을 갖는 사실과 일치되었고, 이는 불규칙한 형상의 큰 단백질들, 예를 들어 Pfs25를 표지하는데 적합하다. 요약하면, Pfs25는 잠금 도메인들 및 T-세포 에피토프들을 갖는 60-량체 나노입자들 상에 표지될 수 있다.
제 2 항원, 포자소체 단백질 (CSP) 는, 변형체 기생충 (plasmodium parasite) 의 포자체 단계 (sporozoite stage) 의 분비된 단백질이고, 포자체 기능 및 간세포들 (hepatocytes) 의 침입에 중요하다. CSP는 RTS, S 백신 (Mosquirix™) 에서, 사용되는 항원이고, 이는 현재 인간 임상 평가 중이다. 가장 임상적으로 진보된 백신 후보, RTS, S / AS01 (RTS, S) 로서 어린이의 말라리아에 대한 부분적인 보호를 제공하기 위해 나타냈다. CSP는 신호 펩타이드 서열 및 헤파린 설페이트 프로테오글리칸들 (heparin sulfate proteoglycans) 에 바인딩하고 보존된 단백분해성 절단 (proteolytic cleavage) 부위를 갖는 영역 I을 포함하는 N-말단 영역; 4-아미노산 모티프, NANP 또는 NVDP의 많은 반복들을 포함하는 중심 영역; 및 영역 II [트롬보스폰딘 (thrombospondin; TSP)-유사 도메인] 및 표준 글리코실포스파티딜이노시톨 (glycosylphosphatidylinositol; GPI) 앵커 부가 서열을 포함하는 C-말단 영역을 포함한다 (도 15a, 상단). RTS, S 백신은 B 형 간염 바이러스 표면 항원 (HBsAg) 에 부착된, 마지막 18 개의 NANP 반복 및 GPI 앵커 부가 서열을 제외한 C-말단을 포함하는, CSP로부터의 189 개의 아미노산들 (아미노산 199 내지 아미노산387) 을 포함한다 (도 15a, 하단).
이 연구에서, 잠금 도메인들을 갖는 CSP 나노입자 백신들을 설계하기 위한 단계적 전략을 취하였고 (도 15b), 즉, 최소 B-세포 에피토프 (단계 1), 전장 B-세포 에피토프 (단계 2), 전장 B-세포 에피토프 + C-말단 T-세포 에피토프 (단계 3), 및 나노입자 상의 CSP 단백질의 RTS, S 항원 (단계 4) 을 표지하였다. 태그-없는 정제를 가능하게 하기 위해, Fab1450을 사용하여 항체 컬럼을 패킹하고, 이에 대해 NANP (서열 번호: 27) 반복들을 갖는 복합 구조가 결정되었다 (도 15a, 하단 좌측). 모든 CSP 융합 구성들은 25ml ExpiCHO 세포들에서 일시적으로 발현되고 이어서 Fab1450 정제 및 매질 염색 EM 분석이 이어진다. 단계 1에서, 2 개의 나노입자들 상에, 최소 B-세포 에피토프, 5 개의 NANP 반복들 (NANP5) 을 표지하였다. 평가된 모든 구성에 대해 극히 고수율들을 관찰하였다. 매질 염색 EM은 어떠한 상이한 단백질 종들이 없는 고순도의 NANP5-5GS-FR 나노입자 및 NANP5-10GS-FR 나노입자를 나타냈다 (도 15c, 좌측 및 중앙). 또한 고수율 및 고순도를 갖는 균질한 나노입자들을 형성하는, NANP5-5GS-PADRE-I3-01-LD7 구성을 발현시켰다 (도 15c, 우측). 이 결과들은 따라서 Fab1450 항체 컬럼 및 잠금 도메인들을 갖는 NANP5 나노입자 어셈블리 및 잠금 도메인들을 갖고 있지 않는 NANP5 나노입자 어셈블리의 활용을 확인하였다. 단계 2에서, 매질 염색 EM 분석을 위해, 3 개의 나노입자 플랫폼들 상에 RTS, S 백신 항원, NANP19 에서 전장 B-세포 에피토프를 표지하였다 (도 15d). NANP 반복들 수의 현저한 향상에도 불구하고, 모든 구성들은 고수율 및 고순도를 갖는 균질한 나노입자들을 형성하였다. 이 결과들은 따라서 잠금 도메인들을 갖는 어셈블리 NANP19 나노입자 어셈블리 및 잠금 도메인들을 갖지 않는 NANP19 나노입자 어셈블리를 확인하였다.
단계 3에서, 전장 B-세포 에피토프 NANP19 및 사이에 5GS 링커 (서열 번호: 17) 를 갖는 C-말단 T-세포 에피토프aTSR 도메인을 모두 포함하는 6 개의 융합 구성들을 설계하고 특성화하였다. 매질 염색 EM은 NANP19-5GS-aTSR이 잠금 도메인들을 갖는 그리고 잠금 도메인들을 갖지 않는, 모든 세 개의 나노입자 플랫폼들 상에 성공적으로 표지될 수 있다 (도 15e). NANP19-5GS-aTSR은 RTS, S 항원에서 모든 구조적으로 규정된 컴포넌트 및 기능적으로 규정된 컴포넌트를 포함하고 링커에서만 상이하기 때문에, 2 개의 항원들은 동일한 특성들을 공유해야 한다.
SEC를 사용하여 25ml ExpiCHO 세포들에서 생산된 이들 NANP19-5GS-aTSR 나노입자들의 수율 및 순도를 더 평가하였다 (도 15f). EM 데이터와 일치하게 NANP19-5GS-aTSR 나노입자들은 SEC 프로파일들에서 단일 피크에 의해 나타낸 바와 같이, 고순도를 나타냈다. 수율면에서, 나노입자에-특이 패턴들: FR> E2p> I3-01을 관찰하였다. 종합하면, CSP의 구조적 컴포넌트 및 항원성 컴포넌트의 다양한 조합들에 기반하여 일련의 말라리아 백신 후보들을 개발하였고, 이들 모두는 잠금 도메인들을 갖는 60-량체 나노입자들 상에 표지될 수 있다.
제 3 항원인, 열대열원충 망상적혈구 바인딩 단백질 동족체 5 (PfRH5) 는 적혈구 침습에 필요한 메로조이트 (merozoite) 접착부 (adhesin) 이다. PfRH5는 적혈구 표면 단백질 분지 (erythrocyte surface protein basigin) (또한 CD147 및 EMMPRIN으로 공지됨) 와의 상호 작용을 통해, 모든 평가된 균주들에서 적혈구 침습에 대해 필요한 것으로 입증된 유일한 구성원이다 (Wong et al., Nature 565: 118-121, 2019를 참조하라) . PfRH5의 결정 구조가 결정되었다 (Wright et al., Nature 515: 427-430, 2014 참조하라). 항체 9AD4 및 항체 QA1을 기반으로 PfRH5 나노입자 및 PfRH5 나노입자의 태그-없는 정제를 위해 항체 컬럼을 개발하였다. 잠금 도메인들을 갖는 나노입자들 및 잠금 도메인들을 가지 않는 나노입자 상에 PfRH5를 표지하도록 융합 구성들을 설계하였다.
예 14
비 바이러스 표적에 대한 백신 개발 - 결핵 백신
결핵 (TB) 은 주로 폐들에 감염되는, 결핵균 박테리아에 의해 야기되는 잠재적으로 심각한 전염성 질병이다. 전 세계 인구의 25%를 감염시킨, TB는 2017 년에 최대 천만 질병 사례들을 유발하여, 130 만명의 사망자가 발생하였다. 카르멧게란 균 (Bacille Calmette-Gurin; BCG) 백신이 TB가 흔한 국가에서 널리 사용되었지만, 이는 TB에 대한 완벽한 보호를 제공하지 못하였다. 다수의 신규 결핵 백신 후보들이 현재 인간 임상 평가 중에 있는 결핵균 에 대하여 개발되었다 (Khoshnood et al. Int. J. Biol. Macromol. 120:180-188, 2018를 참조하라).
이 연구에서, 나노입자들에 2 개의 TB 항원들을 표지하였다. 제 1 항원, Ag85 복합체는 미콜산들의 세포벽 아라비노갈락탄 (arabinogalactan) 으로의 전달을 촉진함으로써 그리고 트레할로스 디미 콜레이트 (trehalose dimycolate) (콜드 인자 (cord factor)) 의 합성을 통해 세포벽의 무결성을 유지한다. Ag85는 매우 면역원성이고 강력한 T-세포 반응 및 항체 반응을 유도할 수 있다. 최근의 백신 실험은 BCG 백신 접종 후 유아들에서 Ag85A에 대한 상승하는 항체 역가들 (antibody titers) 을 보고하였고, 보다 중요하게, Ag85A-특이 IgG는 감소된 결핵 TB위험과 연관되었다. HEK293 F 세포들에서 Ag85A, Ag85B 및 Ag85C를 개별적으로 발현시켰고 Ag85A 및 Ag85B에 대해 잘-폴딩된 (well-folded) 단량체들, 그러나 Ag85C에 대해 삼량체성 단백질들을 관찰하였다. 잠금 도메인들을 갖는 나노입자 및 잠금 도메인을 갖지 않는 나노입자에 Ag85A, Ag85B 및 Ag85C를 표지하도록 융합 구조를 설계하였다. Ag85에 대한 항체들이 보고되지 않았기 때문에, Ag85A 나노입자, Ag85B 나노입자 및 Ag85C 나노입자의 태그-없는 정제를 위해 Ag85-바인딩 항체를 식별하기 위한 파지 표지 기술을 활용하였다.
제 2 항원, Mtb72는, Mtb32와 Mtb39로 구성된 융합 단백질이다. Mtb72는 GSK 보조제 AS01과 조합하여 사용되었고, 임상 평가에서 54.0%의 효능을 입증하였다 (Meeren et al.,N. Engl. J. Med., 379: 1621-1634, 2018를 참조하라). HEK293 F 세포들에서 분리된 항원들로서 Mtb32 및 Mtb39를 발현시켰고 상대적으로 낮은 수율을 관찰하였다. 잠금 도메인들을 갖는 나노입자 및 잠금 도메인을 갖지 않는 나노입자 상의 표지된 Mtb32 및 Mtb39를 사용하여 융합 구성들을 설계하였다. 항체 컬럼들을 패킹하기 위한 항체들을 선택하기 위해 파지 라이브러리 스크리닝 (phage library screening) 을 수행하였다. 이들 TB 항원들은 HCV E2 및 ZIKV DIII과 유사한, 단량체들 (Ag85A, Ag85B, 및 Mtb32) 이거나, HIV-1 외피 및 에볼라GP와 유사한, 삼량체들 (Ag85C 및 Mtb39) 이기 때문에, 발생된 TB 나노입자들은 대체로 유사한 특성들을 나타냈다.
예 15
비 바이러스 표적에 대한 백신 개발 - PCSK9 백신
2 가지 형들의 지질단백질들은 저밀도 지질단백질 (또는 LDL) 및 고밀도 지질단백질 (또는 HDL) 의, 콜레스테롤을 세포들로 그리고 세포들로부터 운반한다. LDL은 동맥들에서 지방 축적들 (fatty buildups) 에 기여하기 때문에, LDL 콜레스테롤은 "나쁜" 콜레스테롤로 간주된다. 상승된 혈중 LDL 콜레스테롤 수치는 서양 국가들에서 조기 사망의 흔한 원인인, 심혈관 질병의 위험 향상과 연관이 있다. 전구단백질 변환 효소 서브틸리신/켁신 9 형 (proprotein convertase subtilisin/kexin type 9; PCSK9) 은 LDL 수용체 (LDL-R) 의 분해를 제어함으로써 혈청 LDL 콜레스테롤 (LDL-C) 을 조절한다. PCSK9는 세 개의 도메인들: N-말단 프로도메인, 서브틸리신-유사 촉매 도메인, 및 C-말단 시스테인/히스티딘-풍부 도메인 (cysteine/histidine-rich domain; CTD) 을 포함하는 74 kDa 세린 프로타아제다 (도 16a). PCSK9는 자가 촉매 절단 (autocatalytic cleavage) 을 겪지만, 14 kDa 프로도메인은 촉매 도메인에 비-공유적으로 부착된 채로 남아 있고 프로타아제 불활성화를 만든다. 기능-상실 PCSK9 돌연변이들은 보다 낮은 농도의 LDL 콜레스테롤 및 감소된 심장 질병 위험과 연관된 것으로 밝혀졌다. 이들 기능-상실 돌연변이들은 유해한 부작용들을 야기하지 않기 때문에, 백신-유래된 항체들에 의한 PCSK9 억제는 LDL 콜레스테롤 농도를 낮추기 위한 매력적인 치료 전략을 제시한다. 다양한 리간드들과의 복합체의 전장 PCSK9및 절단된 PCSK9의 결정 구조들이 해결되어, 백신 설계를 위한 합리적인 기반을 제공한다 (도 16a).
이 연구에서, 잠금 도메인들을 갖는 모든 3 개의 나노입자 플랫폼 또는 잠금 도메인을 갖지 않는 모든 3 개의 나노입자 플랫폼 상에 PCSK9를 표지하였다. PCSK9의 대형 및 불규칙한 형상으로 인해, Pfs25 나노입자들에 사용된 것과 유사한 "넥" 설계를 채택하였다 (도 16b). 간략하게, 바이러스 유래의 3-나선 다발 (헨드라 바이러스 도메인) 은 PCSK9와 나노입자 서브유닛 사이의 구성에 삽입되었다. PCSK9 및 PCSK9 나노입자들의 태그-없는 정제를 위해, J16, 화이자 (Pfizer) 에 의해 개발된 강력한 항-PCSK9 항체를 사용하여 항체 컬럼을 패킹하였다 (Liang et al., J Pharm Exp Ther,340 (2): 228-236, 2012를 참조하라). ExpiCHO 세포들에서 일시적인 발현 후, 융합 단백질들은 J16 항체 컬럼에 의해 상청액으로부터 추출되었고 매질 염색 EM에 의해 분석되었다. 먼저 넥 설계가 없는 2 개의 융합 구성들을 평가하였다 (도 16c). PCSK9-10GS-FR이 균질한 나노입자들을 형성하는 반면에 (도 16c, 좌측), PCSK9-5GS-PADRE-I3-01-LD7은 PCSK9의 대형 및 불규칙한 형상으로 인해 아마도 조립에 실패하였다 (도 16d, 우측). 이어서 넥1을 포함하는 나노입자 구성들 발현시켰다 (도 16d). 페린틴 구성들 둘 다 나노입자들을 형성하지만, 넥 1과 페린틴 사이에 보다 긴 링커, PCSK9-10GS-넥1-10GS-FR를 갖는 페린틴 구성은 보다 큰 수율 및 보다 큰 순도를 갖는 나노입자들을 생산하였다 (도 16d, 패널 1 및 패널 2). 외측에 표지되고 잠금 도메인 (LD7) 의 C-말단에 융합된 PADRE를 갖는, 2 개의 I3-01 구성들은, 조립되지 않은 융합 단백질들이 EM 이미지들 둘 다에서 관찰되었음에도 (도 16d, 패널 3 및 패널 4) 관찰되었지만 약간 상이한 형태들 (morphologies) 의 나노입자들을 형성하였다.
요약하면, PCSK9는 나노 입자가 자가-내성 (self-tolerance) 을 깨고 보다 높은 항체 반응의 역가를 유도할 수 있기 때문에 PCSK9보다 보다 효과적인 백신 후보를 제안하는, 24-량체 페린틴뿐만 아니라 넥 도메인, 잠금 도메인, 및 T-세포 에피토프 PADRE를 갖는 60-량체 I3-01 상에 표지될 수 있다.
***
따라서 본 발명은 상기 기술된 대표적인 실시예들을 참조하여 대략적으로 개시되고 예시되었다. 본 발명의 정신 및 범위로부터 벗어나지 않는 다양한 변화들이 본 발명에 대해 이루어질 수 있다는 것이 이해될 것이다.
본 명세서에 인용된 모든 간행물들, 서열 수탁 번호들, 특허들 및 특허 출원들은 각각이 개별적으로 언급된 것처럼 모든 목적들을 위해 전체가 참조로서 본 명세서에 명시적으로 인용된다는 점에 유의하라. 참조로서 인용된 문헌에 포함된 정의들은 본 개시의 정의들과 모순되는 정도로 제외된다.
<110> The Scripps Research Institute
<120> NANOPARTICLE VACCINES WITH NOVEL STRUCTURAL COMPONENTS
<130> 20PI4156KR
<150> PCT/US
<151> 2019-06-13
<160> 27
<170> KoPatentIn 3.0
<210> 1
<211> 58
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 1
Phe Ser Glu Glu Gln Lys Lys Ala Leu Asp Leu Ala Phe Tyr Phe Asp
1 5 10 15
Arg Arg Leu Thr Pro Glu Trp Arg Arg Tyr Leu Ser Gln Arg Leu Gly
20 25 30
Leu Asn Glu Glu Gln Ile Glu Arg Trp Phe Arg Arg Lys Glu Gln Gln
35 40 45
Ile Gly Trp Ser His Pro Gln Phe Glu Lys
50 55
<210> 2
<211> 46
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 2
Ser Pro Ala Val Asp Ile Gly Asp Arg Leu Asp Glu Leu Glu Lys Ala
1 5 10 15
Leu Glu Ala Leu Ser Ala Glu Asp Gly His Asp Asp Val Gly Gln Arg
20 25 30
Leu Glu Ser Leu Leu Arg Arg Trp Asn Ser Arg Arg Ala Asp
35 40 45
<210> 3
<211> 40
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 3
Ser Glu Ala Leu Lys Ile Leu Asn Asn Ile Arg Thr Leu Arg Ala Gln
1 5 10 15
Ala Arg Glu Cys Thr Leu Glu Thr Leu Glu Glu Met Leu Glu Lys Leu
20 25 30
Glu Val Val Val Asn Glu Arg Arg
35 40
<210> 4
<211> 44
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 4
Met Asn Asp Cys Tyr Ser Lys Leu Lys Glu Leu Val Pro Ser Ile Pro
1 5 10 15
Gln Asn Lys Lys Val Ser Lys Met Glu Ile Leu Gln His Val Ile Asp
20 25 30
Tyr Ile Leu Asp Leu Gln Ile Ala Leu Asp Ser His
35 40
<210> 5
<211> 50
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 5
Leu Leu Tyr Cys Ser Phe Cys Gly Lys Ser Gln His Glu Val Arg Lys
1 5 10 15
Leu Ile Ala Gly Pro Ser Val Tyr Ile Cys Asp Glu Cys Val Asp Leu
20 25 30
Cys Asn Asp Ile Ile Arg Glu Glu Ile Lys Glu Val Ala Pro His Arg
35 40 45
Glu Arg
50
<210> 6
<211> 78
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 6
Asp Gln Pro Ser Val Gly Asp Ala Phe Asp Lys Tyr Asn Glu Ala Val
1 5 10 15
Arg Val Phe Thr Gln Leu Ser Ser Ala Ala Asn Cys Asp Trp Ala Ala
20 25 30
Cys Leu Ser Ser Leu Ser Ala Ser Ser Ala Ala Cys Ile Ala Ala Val
35 40 45
Gly Glu Leu Gly Leu Asp Val Pro Leu Asp Leu Ala Cys Ala Ala Thr
50 55 60
Ala Thr Ser Ser Ala Thr Glu Ala Cys Lys Gly Cys Leu Trp
65 70 75
<210> 7
<211> 88
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 7
Lys Asn Ile Asp Thr Val Arg Glu Ile Ile Thr Val Ala Ser Ile Leu
1 5 10 15
Ile Lys Phe Ser Arg Glu Asp Ile Val Glu Asn Arg Ala Asn Phe Ile
20 25 30
Ala Phe Leu Asn Glu Ile Gly Val Thr His Glu Gly Arg Lys Leu Asn
35 40 45
Gln Asn Ser Phe Arg Lys Ile Val Ser Glu Leu Thr Gln Glu Asp Lys
50 55 60
Lys Thr Leu Ile Asp Glu Phe Asn Glu Gly Phe Glu Gly Val Tyr Arg
65 70 75 80
Tyr Leu Glu Met Tyr Thr Asn Lys
85
<210> 8
<211> 39
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 8
Pro Pro Gly Leu Thr Glu Leu Leu Gln Gly Tyr Thr Val Glu Val Leu
1 5 10 15
Arg Gln Gln Pro Pro Asp Leu Val Asp Phe Ala Val Glu Tyr Phe Thr
20 25 30
Arg Leu Arg Glu Ala Arg Arg
35
<210> 9
<211> 65
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 9
Tyr Ser Asp Glu Gln Val Glu Gln Leu Leu Ala Glu Leu Leu Asn Val
1 5 10 15
Leu Glu Lys His Lys Ala Pro Thr Asp Leu Ser Leu Met Val Leu Gly
20 25 30
Asn Met Val Thr Asn Leu Ile Asn Thr Ala Ile Ala Pro Ala Gln Arg
35 40 45
Gln Ala Ile Ala Asn Ser Phe Ala Arg Ala Leu Gln Ser Ser Ile Asn
50 55 60
Glu
65
<210> 10
<211> 46
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 10
His Met Gly His Ile Gln Ile Pro Pro Gly Leu Thr Glu Leu Leu Gln
1 5 10 15
Gly Tyr Thr Val Glu Val Leu Arg Gln Gln Pro Pro Asp Leu Val Asp
20 25 30
Phe Ala Val Glu Tyr Phe Thr Arg Leu Arg Glu Ala Arg Arg
35 40 45
<210> 11
<211> 60
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 11
Ala Ser Asp Asp Glu Leu Phe Ser Met Leu Asp Gln Arg Phe Gly Gly
1 5 10 15
Gly Glu Asp Leu Leu Met Ser Gly Asp Asn Gly Met Thr Glu Glu Lys
20 25 30
Leu Arg Arg Tyr Leu Lys Arg Thr Val Thr Glu Leu Asp Ser Val Thr
35 40 45
Ala Arg Leu Arg Glu Val Glu His Arg Ala Gly Glu
50 55 60
<210> 12
<211> 87
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 12
Met Ala Asp Lys Arg Ala His His Asn Ala Leu Glu Arg Lys Arg Arg
1 5 10 15
Asp His Ile Lys Asp Ser Phe His Ser Leu Arg Asp Ser Val Pro Ser
20 25 30
Leu Gln Gly Glu Lys Ala Ser Arg Ala Gln Ile Leu Asp Lys Ala Thr
35 40 45
Glu Tyr Ile Gln Tyr Met Arg Arg Lys Val His Thr Leu Gln Gln Asp
50 55 60
Ile Asp Asp Leu Lys Arg Gln Asn Ala Leu Leu Glu Gln Gln Val Arg
65 70 75 80
Ala Leu Glu Gly Ser Gly Cys
85
<210> 13
<211> 90
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 13
Met Asn Lys Asn Ile Asp Thr Val Arg Glu Ile Ile Thr Val Ala Ser
1 5 10 15
Ile Leu Ile Lys Phe Ser Arg Glu Asp Ile Val Glu Asn Arg Ala Asn
20 25 30
Phe Ile Ala Phe Leu Asn Glu Ile Gly Val Thr His Glu Gly Arg Lys
35 40 45
Leu Asn Gln Asn Ser Phe Arg Lys Ile Val Ser Glu Leu Thr Gln Glu
50 55 60
Asp Lys Lys Thr Leu Ile Asp Glu Phe Asn Glu Gly Phe Glu Gly Val
65 70 75 80
Tyr Arg Tyr Leu Glu Met Tyr Thr Asn Lys
85 90
<210> 14
<211> 66
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 14
Met Val Glu Asn Pro Met Val Ile Asn Asn Trp His Asp Lys Leu Thr
1 5 10 15
Glu Thr Asp Val Gln Ile Asp Phe Tyr Gly Asp Glu Val Thr Pro Val
20 25 30
Asp Asp Tyr Val Ile Asp Gly Gly Glu Ile Ile Leu Arg Glu Asn Leu
35 40 45
Glu Arg Tyr Leu Arg Glu Gln Leu Gly Phe Glu Phe Lys Asn Ala Gln
50 55 60
Leu Glu
65
<210> 15
<211> 77
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 15
Met Pro Ile Thr Ser Lys Tyr Thr Asp Glu Gln Val Glu Lys Ile Leu
1 5 10 15
Ala Glu Val Ala Leu Val Leu Glu Lys His Ala Ala Ser Pro Glu Leu
20 25 30
Thr Leu Met Ile Ala Gly Asn Ile Ala Thr Asn Val Leu Asn Gln Arg
35 40 45
Val Ala Ala Ser Gln Arg Lys Leu Ile Ala Glu Lys Phe Ala Gln Ala
50 55 60
Leu Met Ser Ser Leu Glu Thr Pro Lys Thr His Leu Glu
65 70 75
<210> 16
<211> 70
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 16
Gly Met Lys Pro Val Ser Leu Ser Tyr Arg Cys Pro Cys Arg Phe Phe
1 5 10 15
Glu Ser His Val Ala Arg Ala Asn Val Lys His Leu Lys Ile Leu Asn
20 25 30
Thr Pro Asn Cys Ala Cys Gln Ile Val Ala Arg Leu Lys Asn Asn Asn
35 40 45
Arg Gln Val Cys Ile Asp Pro Lys Leu Lys Trp Ile Gln Glu Tyr Leu
50 55 60
Glu Lys Cys Leu Asn Lys
65 70
<210> 17
<211> 5
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 17
Gly Gly Gly Gly Ser
1 5
<210> 18
<211> 13
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 18
Ala Lys Phe Val Ala Ala Trp Thr Leu Lys Ala Ala Ala
1 5 10
<210> 19
<211> 15
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 19
Gln Ser Ile Ala Leu Ser Ser Leu Met Val Ala Gln Ala Ile Pro
1 5 10 15
<210> 20
<211> 32
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 20
Ile Leu Met Gln Tyr Ile Lys Ala Asn Ser Lys Phe Ile Gly Ile Pro
1 5 10 15
Met Gly Leu Pro Gln Ser Ile Ala Leu Ser Ser Leu Met Val Ala Gln
20 25 30
<210> 21
<211> 166
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 21
Ala Ala Ala Lys Pro Ala Thr Thr Glu Gly Glu Phe Pro Glu Thr Arg
1 5 10 15
Glu Lys Met Ser Gly Ile Arg Arg Ala Ile Ala Lys Ala Met Val His
20 25 30
Ser Lys His Thr Ala Pro His Val Thr Leu Met Asp Glu Ala Asp Val
35 40 45
Thr Lys Leu Val Ala His Arg Lys Lys Phe Lys Ala Ile Ala Ala Glu
50 55 60
Lys Gly Ile Lys Leu Thr Phe Leu Pro Tyr Val Val Lys Ala Leu Val
65 70 75 80
Ser Ala Leu Arg Glu Tyr Pro Val Leu Asn Thr Ala Ile Asp Asp Glu
85 90 95
Thr Glu Glu Ile Ile Gln Lys His Tyr Tyr Asn Ile Gly Ile Ala Ala
100 105 110
Asp Thr Asp Arg Gly Leu Leu Val Pro Val Ile Lys Trp Phe His Ala
115 120 125
Asp Arg Lys Pro Ile Phe Ala Leu Ala Gln Glu Ile Asn Glu Leu Ala
130 135 140
Glu Lys Ala Arg Asp Pro Glu Gly Val Ala Leu Leu Thr Pro Gly Glu
145 150 155 160
Met Ala Ser Cys Thr Asn
165
<210> 22
<211> 173
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 22
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Lys Lys Lys Ala Leu Ala Val Phe
20 25 30
Leu Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Glu Leu Ser Phe Leu Lys Glu Met Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Gly Pro Gln Trp Phe Val Lys Leu
130 135 140
Ala Thr Glu Val Val Gly Pro Gln Phe Val Lys Ala Met Lys Gly Val
145 150 155 160
Gly Ser Ala Phe Val Lys Phe Val Pro Thr Gly Gly Val
165 170
<210> 23
<211> 625
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 23
Ala Glu Asn Leu Trp Val Thr Val Tyr Tyr Gly Val Pro Val Trp Lys
1 5 10 15
Asp Ala Glu Thr Thr Leu Phe Cys Ala Ser Asp Ala Lys Ala Tyr Glu
20 25 30
Thr Glu Lys His Asn Val Trp Ala Thr His Ala Cys Val Pro Thr Asp
35 40 45
Pro Asn Pro Gln Glu Ile His Leu Glu Asn Val Thr Glu Glu Phe Asn
50 55 60
Met Trp Lys Asn Asn Met Val Glu Gln Met His Thr Asp Ile Ile Ser
65 70 75 80
Leu Trp Asp Gln Ser Leu Lys Pro Cys Val Lys Leu Thr Pro Leu Cys
85 90 95
Val Thr Leu Gln Cys Thr Asn Val Thr Asn Asn Ile Thr Asp Asp Met
100 105 110
Arg Gly Glu Leu Lys Asn Cys Ser Phe Asn Met Thr Thr Glu Leu Arg
115 120 125
Asp Lys Lys Gln Lys Val Tyr Ser Leu Phe Tyr Arg Leu Asp Val Val
130 135 140
Gln Ile Asn Glu Asn Gln Gly Asn Arg Ser Asn Asn Ser Asn Lys Glu
145 150 155 160
Tyr Arg Leu Ile Asn Cys Asn Thr Ser Ala Ile Thr Gln Ala Cys Pro
165 170 175
Lys Val Ser Phe Glu Pro Ile Pro Ile His Tyr Cys Ala Pro Ala Gly
180 185 190
Phe Ala Ile Leu Lys Cys Lys Asp Lys Lys Phe Asn Gly Thr Gly Pro
195 200 205
Cys Pro Ser Val Ser Thr Val Gln Cys Thr His Gly Ile Lys Pro Val
210 215 220
Val Ser Thr Gln Leu Leu Leu Asn Gly Ser Leu Ala Glu Glu Glu Val
225 230 235 240
Met Ile Arg Ser Glu Asn Ile Thr Asn Asn Ala Lys Asn Ile Leu Val
245 250 255
Gln Phe Asn Thr Pro Val Gln Ile Asn Cys Thr Arg Pro Asn Asn Asn
260 265 270
Thr Arg Lys Ser Ile Arg Ile Gly Pro Gly Gln Ala Phe Tyr Ala Thr
275 280 285
Gly Asp Ile Ile Gly Asp Ile Arg Gln Ala His Cys Asn Val Ser Lys
290 295 300
Ala Thr Trp Asn Glu Thr Leu Gly Lys Val Val Lys Gln Leu Arg Lys
305 310 315 320
His Phe Gly Asn Asn Thr Ile Ile Arg Phe Ala Asn Ser Ser Gly Gly
325 330 335
Asp Leu Glu Val Thr Thr His Ser Phe Asn Cys Gly Gly Glu Phe Phe
340 345 350
Tyr Cys Asn Thr Ser Gly Leu Phe Asn Ser Thr Trp Ile Ser Asn Thr
355 360 365
Ser Val Gln Gly Ser Asn Ser Thr Gly Ser Asn Asp Ser Ile Thr Leu
370 375 380
Pro Cys Arg Ile Lys Gln Ile Ile Asn Met Trp Gln Arg Ile Gly Gln
385 390 395 400
Ala Met Tyr Ala Pro Pro Ile Gln Gly Val Ile Arg Cys Val Ser Asn
405 410 415
Ile Thr Gly Leu Ile Leu Thr Arg Asp Gly Gly Ser Thr Asn Ser Thr
420 425 430
Thr Glu Thr Phe Arg Pro Gly Gly Gly Asp Met Arg Asp Asn Trp Arg
435 440 445
Ser Glu Leu Tyr Lys Tyr Lys Val Val Lys Ile Glu Pro Leu Gly Val
450 455 460
Ala Pro Thr Arg Cys Lys Arg Arg Val Val Gly Gly Gly Gly Gly Ser
465 470 475 480
Gly Gly Gly Gly Ser Ala Val Gly Ile Gly Ala Val Phe Leu Gly Phe
485 490 495
Leu Gly Ala Ala Gly Ser Thr Met Gly Ala Ala Ser Met Thr Leu Thr
500 505 510
Val Gln Ala Arg Asn Leu Leu Ser Gly Asn Pro Asp Trp Leu Pro Asp
515 520 525
Met Thr Val Trp Gly Ile Lys Gln Leu Gln Ala Arg Val Leu Ala Val
530 535 540
Glu Arg Tyr Leu Arg Asp Gln Gln Leu Leu Gly Ile Trp Gly Cys Ser
545 550 555 560
Gly Lys Leu Ile Cys Cys Thr Asn Val Pro Trp Asn Ser Ser Trp Ser
565 570 575
Asn Arg Asn Leu Ser Glu Ile Trp Asp Asn Met Thr Trp Leu Gln Trp
580 585 590
Asp Lys Glu Ile Ser Asn Tyr Thr Gln Ile Ile Tyr Gly Leu Leu Glu
595 600 605
Glu Ser Gln Asn Gln Gln Glu Lys Asn Glu Gln Asp Leu Leu Ala Leu
610 615 620
Asp
625
<210> 24
<211> 5
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 24
Gly Gly Gly Gly Ser
1 5
<210> 25
<211> 159
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 25
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Lys Met Lys Ala Leu Ala Val Phe
20 25 30
Val Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Glu Leu Ser Phe Leu Lys Glu Leu Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Val Gly Pro Gln Phe Ala Gly Val
130 135 140
Thr Glu Gly Gly Val Ala Asn Leu Val Cys Glu Lys Val Lys Gly
145 150 155
<210> 26
<211> 159
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 26
Met Lys Met Glu Glu Leu Phe Lys Lys His Lys Ile Val Ala Val Leu
1 5 10 15
Arg Ala Asn Ser Val Glu Glu Ala Lys Met Lys Ala Leu Ala Val Phe
20 25 30
Val Gly Gly Val His Leu Ile Glu Ile Thr Phe Thr Val Pro Asp Ala
35 40 45
Asp Thr Val Ile Lys Glu Leu Ser Phe Leu Lys Glu Leu Gly Ala Ile
50 55 60
Ile Gly Ala Gly Thr Val Thr Ser Val Glu Gln Cys Arg Lys Ala Val
65 70 75 80
Glu Ser Gly Ala Glu Phe Ile Val Ser Pro His Leu Asp Glu Glu Ile
85 90 95
Ser Gln Phe Cys Lys Glu Lys Gly Val Phe Tyr Met Pro Gly Val Met
100 105 110
Thr Pro Thr Glu Leu Val Lys Ala Met Lys Leu Gly His Thr Ile Leu
115 120 125
Lys Leu Phe Pro Gly Glu Val Val Val Gly Pro Gln Phe Ala Gly Val
130 135 140
Thr Glu Gly Gly Val Ala Asn Leu Val Cys Glu Lys Val Lys Gly
145 150 155
<210> 27
<211> 4
<212> PRT
<213> Unknown
<220>
<223> Homo sapiens
<400> 27
Asn Ala Asn Pro
1
Claims (40)
- 백신 조성물에 있어서, 자가-조립 나노입자 (self-assembling nanoparticle) 의 표면 상에 표지되는 (displayed) 폴리펩타이드 면역원 (polypeptide immunogen) 을 포함하고, 잠금 도메인 (locking domain) 이 상기 나노입자 내부에 임베딩되고 (embeded) 그리고 상기 자가-조립 나노입자의 서브유닛 (subunit) 에 결합되고, 그리고 상기 잠금 도메인은 계면에서 비-공유 상호 작용들을 통해 용액 내 근처의 나노입자 서브유닛에 부착된 또 상이한 잠금 도메인과 자연적으로 이량체를 형성할 수 있는 단백질 서브유닛인, 백신 조성물.
- 제 1 항에 있어서, 상기 잠금 도메인은 또 상이한 동일한 단백질 도메인과 동종이량체 (homodimer) 를 형성하는 단백질 도메인인, 백신 조성물.
- 제 2 항에 있어서, 상기 잠금 도메인의 서브유닛은 서열 번호: 1 내지 서열 번호: 9, 이의 보존적으로 변형된 변이체 또는 이의 실질적으로 동일한 서열 중 임의의 하나에 나타낸 바와 같이 아미노산 서열을 포함하는, 백신 조성물.
- 제 1 항에 있어서, 상기 잠금 도메인은 상기 나노입자의 서브유닛에 공유 결합되는, 백신 조성물.
- 제 4 항에 있어서, 상기 잠금 도메인의 N-말단은 링커 (linker) 서열을 통해 상기 나노입자 서브유닛의 C-말단에 융합되는, 백신 조성물.
- 제 1 항에 있어서, 범-반응성 T-세포 에피토프 (epitope) 를 더 포함하는, 백신 조성물.
- 제 6 항에 있어서, 상기 T-세포 에피토프의 N-말단은 상기 잠금 도메인의 C-말단에 융합되는, 백신 조성물.
- 제 1 항에 있어서, 상기 면역원과 상기 나노입자 서브유닛 사이에 삽입된 넥 영역 (neck region) 을 더 포함하고, 상기 넥 영역은 상기 나노입자의 상기 표면으로부터 보다 멀리 상기 면역원을 상승시키는 3-나선 단백질 도메인을 포함하는, 백신 조성물.
- 제 1 항에 있어서, 상기 면역원과 상기 나노입자 서브유닛 사이에 삽입된 단백질 도메인을 더 포함하고, 상기 단백질 도메인은 상기 면역원 폴리펩타이드를 안정화하는, 백신 조성물.
- 제 1 항에 있어서, 상기 나노입자는 회전 대칭 (rotational symmetry) 을 갖는 공-형상의 나노입자인, 백신 조성물.
- 제 11 항에 있어서, 상기 회전 대칭은 3-폴드 축 및/또는 5-폴드 축을 갖는, 백신 조성물.
- 제 11 항에 있어서, 상기 나노입자는 20 면체 구조인, 백신 조성물.
- 제 1 항에 있어서, 상기 폴리펩타이드 면역원은 바이러스 면역원인, 백신 조성물.
- 제 13 항에 있어서, 상기 폴리펩타이드 면역원은 클래스-I 융합 메커니즘 (class-I fusion mechanism) 을 활용하는 바이러스로부터의 바이러스 면역원인, 백신 조성물.
- 제 14 항에 있어서, 상기 바이러스는 HIV-1 바이러스, 에볼라 바이러스 (Ebola virus), 마르부르그 바이러스 (Marburg virus), 아레나바이러스들 (Arenaviruses), 호흡기 세포 융합 바이러스들 (respiratory syncytial viruses; RSV), 및 코로나바이러스들 (coronaviruses) 로 구성된 그룹으로부터 선택되는, 백신 조성물.
- 제 13 항에 있어서, 상기 폴리펩타이드 면역원은 클래스-II 융합 메커니즘을 활용하는 바이러스로부터의 바이러스 면역원인, 백신 조성물.
- 제 16 항에 있어서, 상기 바이러스는 HCV 또는 지카 바이러스 (Zika virus) 인, 백신 조성물.
- 제 13 항에 있어서, 상기 폴리펩타이드 면역원은 비-바이러스 면역원인, 백신 조성물.
- 제 18 항에 있어서, 상기 폴리펩타이드 면역원은 열대열원충 (Plasmodium falciparum) 으로부터의 항원, 결핵균 (Mycobacterium tuberculosis; TB) 으로부터의 항원, 또는 인간 단백질 전구단백질 변환 효소 서브틸리신/켁신 9 형 (proprotein convertase subtilisin/kexin type 9; PCSK9) 인, 백신 조성물.
- 제 1 항에 있어서, 상기 폴리펩타이드 면역원은 HIV-1 외피-유래된 삼량체 (Env-derived trimer) 단백질인, 백신 조성물.
- 제 20 항에 있어서, 상기 잠금 도메인의 N-말단은 GGGGS (서열 번호: 17) 의 하나 이상의 탠덤 카피들 (tandem copies) 을 포함하는 링커 서열을 통해 상기 나노입자 서브유닛의 C-말단에 융합되는, 백신 조성물.
- 제 20 항에 있어서, 상기 범-반응성 T-세포 에피토프를 더 포함하는, 백신 조성물.
- 제 22 항에 있어서, 상기 T-세포 에피토프의 N-말단은 잠금 도메인의 C-말단에 융합되는, 백신 조성물.
- 제 22 항에 있어서, 상기 T-세포 에피토프는 서열 AKFVAAWTLKAAA (서열 번호: 18) 를 포함하는, 백신 조성물.
- 제 20 항에 있어서, 상기 HIV-1 삼량체 단백질의 서브유닛의 C-말단은 상기 나노입자의 서브유닛의 N-말단에 공유 결합되는, 백신 조성물.
- 제 20 항에 있어서, 상기 HIV-1 삼량체 단백질 서브유닛은 링커 서열을 통해 상기 나노입자 서브유닛에 융합되는, 백신 조성물.
- 제 26 항에 있어서, 상기 링커 서열은 서열 (GaSb)n을 포함하고, 여기서 a는 1 내지 5의 정수이고, b는 1 내지 2의 정수이고, 그리고 n은 1 내지 5의 정수인, 백신 조성물.
- 제 20 항에 있어서, 상기 자가-조립 나노입자는 삼량체성 (trimeric) 서열을 포함하는, 백신 조성물.
- 제 20 항에 있어서, 상기 자가-조립 나노입자의 서브유닛은 서열 번호: 21 (E2p), 서열 번호: 22 (I3-01), 서열 번호: 25 (I3-01 변이체) 또는 서열 번호: 26 (페린틴 (ferrintin)), 이의 보존적으로 변형된 변이체 또는 이의 실질적으로 동일한 서열로 나타낸 바와 같이 폴리펩타이드를 포함하는, 백신 조성물.
- 제 20 항에 있어서, 상기 HIV-1 외피-유래된 삼량체 단백질은 gp140으로부터 유래된, 백신 조성물.
- 제 20 항에 있어서, 상기 HIV-1 외피-유래된 삼량체 단백질은 절단되지 않은 사전융합-최적화된 (ncleaved prefusion-optimized; UFO) gp140 삼량체인, 백신 조성물.
- 제 31 항에 있어서, 상기 UFO gp140 삼량체는 HIV-1 균주 BG505로부터 변형된 gp41ECTO 도메인을 포함하는 키메라 삼량체 (chimeric trimer) 인, 백신 조성물.
- 제 31 항에 있어서, 상기 UFO gp140 삼량체의 서브유닛은 서열 번호: 23에 나타낸 서열, 이의 보존적으로 변형된 변이체 또는 이의 실질적으로 동일한 서열을 포함하는, 백신 조성물.
- 제 31 항에 있어서, 서브유닛 서열로서 상기 N-말단으로부터 상기 C-말단까지: 서열 번호: 23에 나타낸 바와 같이 HIV-1 외피-유래된 UFO gp140 삼량체 서브유닛, 서열 번호: 21에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (E2p), 서열 번호: 1에 나타낸 바와 같이 잠금 도메인 (LD4), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 을 포함하는 상기 서브유닛 서열을 갖는, 백신 조성물.
- 제 34 항에 있어서, 상기 gp140 삼량체 서브유닛과 상기 나노입자 서브유닛 사이에 제 1 링커 서열 (GGGGS)2(서열 번호: 24), 및/또는 상기 나노입자 서브유닛과 상기 잠금 도메인 사이에 제 2 링커 서열 GGGGS (서열 번호: 17) 를 더 포함하는, 백신 조성물.
- 제 31 항에 있어서, 서브유닛 서열로서 상기 N-말단으로부터 상기 C-말단까지: 서열 번호: 23에 나타낸 바와 같이 HIV-1 외피-유래된 UFO gp140 삼량체, 서열 번호: 22 또는 서열 번호: 25에 나타낸 바와 같이 자가-조립 나노입자 서브유닛 (I3-01), 서열 번호: 2에 나타낸 바와 같이 잠금 도메인 (LD7), 및 T-세포 에피토프 AKFVAAWTLKAAA (서열 번호: 18) 를 포함하는, 상기 서브유닛 서열을 갖는, 백신 조성물.
- 제 36 항에 있어서, 상기 gp140 삼량체 서브유닛과 상기 나노입자 서브유닛 사이에 제 1 링커 서열 (GGGGS)2(서열 번호: 24), 및/또는 상기 나노입자 서브유닛과 상기 잠금 도메인 사이에 제 2 링커 서열 GGGGS (서열 번호: 17) 를 더 포함하는, 백신 조성물.
- 제 1 항에 기재된 백신 조성물, 및 약제용으로 허용 가능한 담체를 포함하는, 약제용 조성물.
- N-말단의 면역원 폴리펩타이드, 자가-조립 나노입자 서브유닛, 및 잠금 도메인의 서브유닛을 포함하는 융합 단백질을 코딩하고; 상기 잠금 도메인은 계면에서 비-공유 상호 작용들을 통해 용액 내 근처의 나노입자 서브유닛에 부착된 또 상이한 잠금 도메인과 자연적으로 이량체를 형성할 수 있는 단백질 서브유닛인, 폴리뉴클레오타이드.
- 제 20 항에 기재된 HIV-1 백신 조성물의 치료적 유효량을 포함하는 약제용 조성물을 피험자에게 투여하여 피험자의 HIV-1 감염을 치료하거나 예방하는 단계를 포함하는, 피험자의 HIV-1 감염을 치료 또는 예방하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862684229P | 2018-06-13 | 2018-06-13 | |
| US62/684,229 | 2018-06-13 | ||
| PCT/US2019/036917 WO2019241483A1 (en) | 2018-06-13 | 2019-06-13 | Nanoparticle vaccines with novel structural components |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210021530A true KR20210021530A (ko) | 2021-02-26 |
Family
ID=68843607
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217001153A KR20210021530A (ko) | 2018-06-13 | 2019-06-13 | 신규한 구조적 컴포넌트들을 갖는 나노입자 백신들 |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US11097002B2 (ko) |
| EP (1) | EP3807210A4 (ko) |
| JP (1) | JP7555826B2 (ko) |
| KR (1) | KR20210021530A (ko) |
| CN (1) | CN112469661B (ko) |
| AU (1) | AU2019285048B2 (ko) |
| CA (1) | CA3103460A1 (ko) |
| EA (1) | EA202092808A1 (ko) |
| IL (1) | IL279351A (ko) |
| SG (1) | SG11202012313PA (ko) |
| WO (1) | WO2019241483A1 (ko) |
| ZA (1) | ZA202100032B (ko) |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2020323462A1 (en) * | 2019-07-26 | 2022-03-10 | The Scripps Research Institute | Engineered HCV E2 immunogens and related vaccine compositions |
| CN113121704B (zh) * | 2020-03-25 | 2023-04-07 | 昆山新蕴达生物科技有限公司 | 基于纳米颗粒的冠状病毒疫苗 |
| US11278617B2 (en) | 2020-03-31 | 2022-03-22 | Engimata, Inc | Immunogenic composition forming a SARS-CoV-2 vaccine, and a method for its manufacture |
| US11559577B2 (en) | 2020-03-31 | 2023-01-24 | Engimata, Inc. | Immunogenic composition forming a vaccine, and a method for its manufacture |
| CN112023035A (zh) * | 2020-04-07 | 2020-12-04 | 中国医学科学院医学生物学研究所 | 一种以SARS-CoV-2病毒S蛋白RBD区为抗原的纳米疫苗及其制备 |
| FI20215508A1 (en) | 2020-04-09 | 2021-10-10 | Niemelae Erik Johan | Mimetic nanoparticles to prevent the spread of new coronaviruses and reduce the rate of infection |
| FI20205382A1 (en) * | 2020-04-09 | 2021-05-07 | Niemelae Erik | Method for preventing the spread of pathogens and for reducing infections caused by them |
| US11192940B2 (en) | 2020-04-10 | 2021-12-07 | Adagio Therapeutics, Inc. | Compounds specific to coronavirus S protein and uses thereof |
| WO2021207730A1 (en) * | 2020-04-11 | 2021-10-14 | The Wistar Institute Of Anatomy & Biology | Vaccines for coronavirus and methods of using the same |
| WO2021210984A1 (en) * | 2020-04-17 | 2021-10-21 | Erasmus University Medical Center Rotterdam | Coronavirus vaccine |
| WO2021249116A1 (en) | 2020-06-10 | 2021-12-16 | Sichuan Clover Biopharmaceuticals, Inc. | Coronavirus vaccine compositions, methods, and uses thereof |
| WO2021262625A1 (en) * | 2020-06-24 | 2021-12-30 | Avalon GloboCare Corp. | S-layer vaccine fusion proteins and methods of use |
| US10906944B2 (en) * | 2020-06-29 | 2021-02-02 | The Scripps Research Institute | Stabilized coronavirus spike (S) protein immunogens and related vaccines |
| CN114230674B (zh) * | 2020-12-01 | 2023-09-26 | 中国医学科学院基础医学研究所 | 一种含Fc结构域的新型冠状病毒S蛋白受体结合域融合蛋白及其用途 |
| US20240226272A9 (en) * | 2020-12-18 | 2024-07-11 | The Scripps Research Institute | Immunogenic compositions |
| EP4262864A2 (en) * | 2020-12-18 | 2023-10-25 | The Scripps Research Institute | Immunogenic compositions |
| CN112979826B (zh) * | 2021-03-03 | 2022-04-08 | 华中农业大学 | 一种乙型脑炎病毒纳米颗粒疫苗及其制备方法和应用 |
| US20230181717A1 (en) * | 2021-12-14 | 2023-06-15 | The Scripps Research Institute | Methods and compositions related to hiv-1 nanoparticle vaccines with improved properties |
| WO2024006532A2 (en) * | 2022-06-30 | 2024-01-04 | La Jolla Institute For Immunology | Kari nanoparticle |
| WO2024050452A2 (en) * | 2022-08-30 | 2024-03-07 | Administrators Of The Tulane Educational Fund | Compositions and methods for raising immune responses to gram-negative bacteria |
| CN115894716B (zh) * | 2022-11-23 | 2024-02-09 | 华中农业大学 | 一种重组融合蛋白纳米颗粒及其制备方法 |
| WO2024123558A2 (en) * | 2022-12-05 | 2024-06-13 | The Scripps Research Institute | Engineered lassa viral immunogens and vaccine compositions |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3926839B2 (ja) | 1993-09-14 | 2007-06-06 | エピミューン,インコーポレイティド | 万能dr−結合性ペプチドを用いる免疫応答の改変 |
| US7550143B2 (en) * | 2005-04-06 | 2009-06-23 | Ibc Pharmaceuticals, Inc. | Methods for generating stably linked complexes composed of homodimers, homotetramers or dimers of dimers and uses |
| AU2006232310B9 (en) * | 2005-04-06 | 2011-07-21 | Ibc Pharmaceuticals, Inc. | Improved stably tethered structures of defined compositions with multiple functions or binding specificities |
| CA2667358A1 (en) | 2006-10-23 | 2008-05-29 | Progenics Pharmaceuticals, Inc. | Modified gp140 envelope polypeptides of hiv-1 isolates, compositions, stabilized trimeric complexes, and uses thereof |
| RU2540871C2 (ru) | 2008-02-01 | 2015-02-10 | Альфа-О Пептидес Аг | Самоорганизующиеся пептидные наночастицы, полезные в качестве вакцин |
| WO2010086294A2 (en) * | 2009-01-28 | 2010-08-05 | Epimmune Inc. | Pan-dr binding polypeptides and uses thereof |
| EP2473186A4 (en) * | 2009-08-31 | 2013-07-10 | Ibc Pharmaceuticals Inc | BIS SPECIFIC IMMUNOZYTOKIN DOCK-AND-LOCK COMPLEXES AND THERAPEUTIC USE THEREOF |
| US20140242104A1 (en) * | 2011-10-12 | 2014-08-28 | Alpha-O Peptides Ag | Self-assembling peptide nanoparticles as vaccines against infection with norovirus |
| EP2765138B1 (en) | 2012-11-05 | 2018-01-10 | International Aids Vaccine Initiative | HIV-1 envelope glycoprotein |
| EP2983686B1 (en) | 2013-01-07 | 2024-05-29 | Beth Israel Deaconess Medical Center, Inc. | Stabilized human immunodeficiency virus (hiv) envelope (env) trimer vaccines and methods of using the same |
| CA2934472A1 (en) * | 2014-01-09 | 2015-07-16 | Alpha-O Peptides Ag | Flagellin-containing protein nanoparticles as a vaccine platform |
| WO2016037154A1 (en) | 2014-09-04 | 2016-03-10 | The United States Of America, As Represented By The Secretary, Department Of Health & Human Services | Recombinant hiv-1 envelope proteins and their use |
| US10501733B2 (en) | 2015-02-27 | 2019-12-10 | University Of Washington | Polypeptide assemblies and methods for the production thereof |
| MX2018013455A (es) | 2016-05-02 | 2019-02-28 | Scripps Research Inst | Composiciones y metodos relacionados con inmunogenos de vih-1. |
| SG10202001956UA (en) | 2016-09-15 | 2020-04-29 | Janssen Vaccines & Prevention Bv | Trimer stabilizing hiv envelope protein mutations |
| EA201991918A1 (ru) * | 2017-03-23 | 2020-05-15 | Альфа-О Пептидс Аг | Самосборные белковые наночастицы со встроенными белками с шестиспиральным пучком |
| CA3057715A1 (en) * | 2017-04-04 | 2018-10-11 | Avidea Technologies, Inc. | Peptide-based vaccines, methods of manufacturing, and uses thereof for inducing an immune response |
| EP3704137A4 (en) | 2017-11-01 | 2021-08-11 | The Scripps Research Institute | Novel scaffolding-based HIV-1 vaccine immunogens |
| US10906944B2 (en) * | 2020-06-29 | 2021-02-02 | The Scripps Research Institute | Stabilized coronavirus spike (S) protein immunogens and related vaccines |
-
2019
- 2019-06-13 AU AU2019285048A patent/AU2019285048B2/en active Active
- 2019-06-13 JP JP2020568685A patent/JP7555826B2/ja active Active
- 2019-06-13 WO PCT/US2019/036917 patent/WO2019241483A1/en active Search and Examination
- 2019-06-13 KR KR1020217001153A patent/KR20210021530A/ko unknown
- 2019-06-13 CA CA3103460A patent/CA3103460A1/en active Pending
- 2019-06-13 CN CN201980048606.3A patent/CN112469661B/zh active Active
- 2019-06-13 US US16/440,067 patent/US11097002B2/en active Active
- 2019-06-13 SG SG11202012313PA patent/SG11202012313PA/en unknown
- 2019-06-13 EA EA202092808A patent/EA202092808A1/ru unknown
- 2019-06-13 EP EP19818872.4A patent/EP3807210A4/en active Pending
-
2020
- 2020-12-10 IL IL279351A patent/IL279351A/en unknown
-
2021
- 2021-01-04 ZA ZA2021/00032A patent/ZA202100032B/en unknown
- 2021-07-27 US US17/386,289 patent/US20220031835A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021527077A (ja) | 2021-10-11 |
| WO2019241483A1 (en) | 2019-12-19 |
| CA3103460A1 (en) | 2019-12-19 |
| CN112469661A (zh) | 2021-03-09 |
| ZA202100032B (en) | 2022-07-27 |
| EP3807210A1 (en) | 2021-04-21 |
| US11097002B2 (en) | 2021-08-24 |
| IL279351A (en) | 2021-01-31 |
| AU2019285048A1 (en) | 2021-01-07 |
| AU2019285048B2 (en) | 2023-06-08 |
| US20200009244A1 (en) | 2020-01-09 |
| JP7555826B2 (ja) | 2024-09-25 |
| EP3807210A4 (en) | 2022-05-11 |
| EA202092808A1 (ru) | 2021-08-24 |
| US20220031835A1 (en) | 2022-02-03 |
| CN112469661B (zh) | 2024-04-26 |
| SG11202012313PA (en) | 2021-01-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN112469661B (zh) | 具有新结构组分的纳米粒疫苗 | |
| US10906944B2 (en) | Stabilized coronavirus spike (S) protein immunogens and related vaccines | |
| Mengist et al. | Mutations of SARS-CoV-2 spike protein: Implications on immune evasion and vaccine-induced immunity | |
| Martínez-Flores et al. | SARS-CoV-2 vaccines based on the spike glycoprotein and implications of new viral variants | |
| AU2018358238B2 (en) | Novel scaffolded HIV-1 vaccine immunogens | |
| He et al. | Self-assembling nanoparticles presenting receptor binding domain and stabilized spike as next-generation COVID-19 vaccines | |
| US11872277B2 (en) | Compositions and methods related to ebolavirus vaccines | |
| de Santana et al. | Improved genetic stability of recombinant yellow fever 17D virus expressing a lentiviral Gag gene fragment | |
| US11008368B2 (en) | Engineered HCV E2 immunogens and related vaccine compositions | |
| EA046652B1 (ru) | Вакцины на основе наночастиц с новыми структурными компонентами | |
| US20220401546A1 (en) | HIV Immunogens, Vaccines, and Methods Related Thereto | |
| Rothen et al. | Preclinical Development of a Novel Zika Virus-like Particle Vaccine in Combination with Tetravalent Dengue Virus-like Particle Vaccines | |
| WO2024118544A2 (en) | Vaccines containing novel nanoparticle scaffolds |