KR20200093639A - 천연 항체 구조-유사 헤테로다이머 형태의 항 pd-l1/항 cd47 이중특이성 항체 및 이의 제조 - Google Patents
천연 항체 구조-유사 헤테로다이머 형태의 항 pd-l1/항 cd47 이중특이성 항체 및 이의 제조 Download PDFInfo
- Publication number
- KR20200093639A KR20200093639A KR1020207019202A KR20207019202A KR20200093639A KR 20200093639 A KR20200093639 A KR 20200093639A KR 1020207019202 A KR1020207019202 A KR 1020207019202A KR 20207019202 A KR20207019202 A KR 20207019202A KR 20200093639 A KR20200093639 A KR 20200093639A
- Authority
- KR
- South Korea
- Prior art keywords
- chain
- substitutions
- cells
- antigen
- amino acid
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/64—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising a combination of variable region and constant region components
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Microbiology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
천연 IgG 특징을 가지며, 중쇄와 경쇄의 미스매치 없이 고도로 안정한 헤테로다이머 형태의 항 PD-L1/항 CD47 이중특이성 항체, 및 그 제조방법이 제공된다. 이중특이성 항체의 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나는 위치 366 및 399에서의 아미노산 치환을 포함하며, 다른 하나는 위치 351, 407 및 409에서의 아미노산 치환을 포함한다.
Description
본 발명은 천연 항체 구조-유사 헤테로다이머 형태 항 PD-L1/항 CD47 이중특이성 항체 및 그 제조에 관한 것이다. 구체적으로, 본 발명은 천연 IgG 특징을 가지며, 중쇄 및 경쇄의 미스매치 없이 고도로 안정한 헤테로다이머 형태의 항 PD-L1/항 CD47 이중특이성 항체 및 그 제조방법을 제공한다.
프로그램된 사멸 리간드-1 (programmed death ligand 1, PD-L1)은 면역 체크포인트 프로그램된 사멸 수용체-1 (programmed death-1, PD-1)의 리간드이며, B7 패밀리에 속하고, T세포, B세포, 단핵구, 대식세포, DC세포 및 내피세포, 표피세포 등을 포함하는 다양한 면역 세포 표면에서 발현되도록 유도된다. PD-L1이 PD-1에 결합한 후, T 세포 활성화의 음성 조절에 주로 참여하여, 면역 반응의 강약 정도 및 지속 시간을 조절할 수 있다. PD-L1은 PD-1의 리간드일 뿐만 아니라 CD80의 리간드로서, T 세포에 음성 조절 신호를 전달하고, T 세포 면역 내성을 유도할 수 있다 (Autoimmun Rev, 2013, 12(11): 1091-1100. Front Immunol, 2013, 4: 481. Nat Rev Cancer, 2012, 12(4): 252-264. Trends Mol Med. 2015 Jan;21(1):24-33. Clin Cancer Res. 2012 Dec 15;18(24):6580-7.). 정상적인 상황에서, PD-L1 및 PD-1은 신체 조직의 자가 면역 내성을 매개 및 유지할 수 있고, 염증 반응 동안 면역 시스템이 과도하게 활성화되어 자기 조직을 손상시키는 것을 방지하고, 자가 면역 질환의 발생을 피하는 것에 긍정적인 효과를 가지며; 병리학적 상황에서, 이는 종양 면역 및 다양한 자가 면역 질환의 발생 및 발달에 관여한다. 다수의 연구에 따르면, PD-L1은 다양한 종양 조직에서 고도로 발현되고, PD-1은 종양 침윤성 림프구에서 고도로 발현되며, PD-L1 및 PD-1의 과발현은 종양의 나쁜 임상적 예후와 밀접한 관련이 있는 것으로 보고되었다 (Anticancer Agents Med Chem. 2015;15(3):307-13. Hematol Oncol Stem Cell Ther. 2014 Mar;7(1):1-17. Trends Mol Med. 2015 Jan;21(1):24-33. Immunity. 2013 Jul 25;39(1):61-73. J Clin Oncol. 2015 Jun 10;33(17):1974-82.). PD-L1 단일클론항체를 이용하여 PD-L1/PD-1 및 CD80/PD-L1의 상호 작용을 차단하는 것은, 전임상 실험 연구 및 임상 시험에서 모두 우수한 항종양 효과를 나타냈다. 현재 PD-L1 단일클론항체는 비소세포 폐암 및 요로상피암과 같은 다양한 종양을 치료하기 위해 승인되었다. 그러나, 소수의 종양 환자만이 이러한 유형의 단일클론항체 요법으로부터 혜택을 얻을 수 있으며, 다수의 환자는 이러한 유형의 단일클론항체에 반응하지 않는다 (Expert Opin Ther Targets. 2014 Dec;18(12):1407-20. Oncology (Williston Park). 2014 Nov;28 Suppl 3:15-28.).
CD47은 인테그린 관련 단백질(integrin-related protein)이라고도 하며, 50kD 막통과 단백질이고, 면역글로불린 슈퍼패밀리에 속한다. 다양한 세포에서 광범위하게 발현되지만, 다양한 종양 세포에서 발현이 현저히 증가한다 (Proc Natl Acad Sci U S A,2012,109(17): 6662- 6667). CD47의 리간드는 신호 조절 단백질 α (signal-regulatory protein α, SIRPα)이며, 주로 대식세포에서 발현되고, CD47과 결합 후에 "나를 먹지 마라"라는 신호를 전달하고, 대식세포의 식세포 작용을 억제한다 (Curr Opin Immunol, 2009,21(1):47-52). 항 CD47 항체의 사용을 통해 CD47-SIRPα 신호 전달 경로를 차단하여, 항 종양 효과를 발휘할 수 있다. 현재 다양한 항 CD47 단일클론항체가 다양한 혈액 종양 및 고형 종양의 치료를 위한 임상 연구 단계에 들어갔다. 그러나, 적혈구 등의 표면에도 CD47이 발현되기 때문에, 이러한 항 CD47 치료는 심각한 빈혈 및 혈소판 감소 등의 부작용, 및 낮은 생체 이용률을 초래할 수 있다.
본 기술분야에는 PD-L1 및 CD47 신호 전달 경로를 동시에 차단하는 신규한 치료 약물을 연구할 필요가 여전히 있다.
본 발명은 천연 IgG 구조 특징을 갖고, 중쇄와 경쇄의 미스매치(mismatch) 없이 고도로 안정한 헤테로다이머 형태를 가지며, PD-L1 및 CD47을 동시에 차단할 수 있는 신규한 이중작용성 항체, 및 그 제조방법을 제공한다. 상기 이중작용성 항체는 PD-L1 및 CD47을 동시에 과발현하는 종양 세포에 선택적으로 결합하는 경향이 있고, 이에 따라 고효율의 특이적인 사멸 효과를 발휘하는 반면, 독성 및 부작용이 낮다.
본 발명의 제1 양상은 헤테로다이머 형태의 이중특이성 항체로서, 제1 Fc 사슬 및 제2 Fc 사슬, 및 PD-L1과 특이적으로 결합할 수 있는 제1 항원-결합 기능 영역 및 CD47과 특이적으로 결합할 수 있는 제2 항원-결합 기능 영역을 포함하고;
상기 제1 Fc 사슬 및 제2 Fc 사슬은 모두 아미노산 치환을 포함하는 면역글로불린 G Fc 단편이고, 상기 제1 Fc 사슬 및 제2 Fc 사슬은 함께 Fc 수용체에 결합할 수 있는 헤테로다이머를 구성하고;
상기 제1 Fc 사슬 및 제2 Fc 사슬은 공유 결합 또는 링커를 통해 각각 상기 제1 항원-결합 기능 영역 및 제2 항원-결합 기능 영역에 연결되고;
상기 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나는 위치 366 및 위치 399에서 아미노산 치환을 포함하고, 다른 하나는 위치 351, 위치 407 및 위치 409에서 아미노산 치환을 포함하고, 상기 아미노산 위치는 카바트(Kabat) EU 인덱스 넘버링 시스템에 따라 번호가 지정되는 것에 관한 것이다.
본원에서 제1 Fc 사슬 및 제2 Fc 사슬은 2개의 Fc 사슬을 구분하기 위한 목적으로만 정의되며, 그 중요성이 다르거나 순서에 차이가 있음을 의미하는 것은 아니다. 동시에, 제1 Fc 사슬 및 제2 Fc 사슬의 제1 항원-결합 기능 영역 및 제2 항원-결합 기능 영역에의 연결도 임의적이며, 즉, 제1 Fc 사슬은 제1 항원-결합 기능 영역 또는 제2 항원-결합 기능 영역에 연결될 수 있고, 제2 Fc 사슬도 마찬가지이다.
일부 구체예에서, 제1 Fc 사슬 및 제2 Fc 사슬 아미노산 치환은 하기와 같다:
a) L351G, L351Y, L351V, L351P, L351D, L351E, L351K 또는 L351W;
b) T366L, T366P, T366W 또는 T366V;
c) D399C, D399N, D399I, D399G, D399R, D399T 또는 D399A;
d) Y407L, Y407A, Y407P, Y407F, Y407T 또는 Y407H; 및
e) K409C, K409P, K409S, K409F, K409V, K409Q 또는 K409R.
일부 구체예에서, 아미노산 치환은 하기를 포함한다:
a) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399R 치환, 다른 하나에서 L351E, Y407L 및 K409V 치환;
b) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399C 치환, 다른 하나에서 L351G, Y407L 및 K409C 치환;
c) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399C 치환, 다른 하나에서 L351Y, Y407A 및 K409P 치환;
d) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 D399N 치환, 다른 하나에서 L351V, Y407P 및 K409S 치환;
e) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366W 및 D399G 치환, 다른 하나에서 L351D, Y407P 및 K409S 치환;
f) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 D399I 치환, 다른 하나에서 L351P, Y407F 및 K409F 치환;
g) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366V 및 D399T 치환, 다른 하나에서 L351K, Y407T 및 K409Q 치환;
h) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399A 치환, 다른 하나에서 L351W, Y407H 및 K409R 치환.
일부 구체예에서, 아미노산 치환은 하기를 포함한다:
a) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409V 치환, 다른 하나에서 L351E, Y407L 및 D399R 치환;
b) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409C 치환, 다른 하나에서 L351G, Y407L 및 D399C 치환;
c) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409P 치환, 다른 하나에서 L351Y, Y407A 및 D399C 치환;
d) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 K409S 치환, 다른 하나에서 L351V, Y407P 및 D399N 치환;
e) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366W 및 K409S 치환, 다른 하나에서 L351D, Y407P 및 D399G 치환;
f) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 K409F 치환, 다른 하나에서 L351P, Y407F 및 D399I 치환;
g) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366V 및 K409Q 치환, 다른 하나에서 L351K, Y407T 및 D399T 치환;
h) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409R 치환, 다른 하나에서 L351W, Y407H 및 D399A 치환.
일부 구체예에서, 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나의 아미노산 치환은 T366L 및 D399R이고, 다른 하나의 아미노산 치환은 L351E, Y407L 및 K409V이다.
일부 구체예에서, 제1 항원-결합 기능 영역 및 제2 항원-결합 기능 영역은 Fab 단편, scFv 단편, 가변 도메인 단편 Fv 및 중쇄 항체의 중쇄 가변 영역 단편 VHH로부터 선택된다.
일부 구체예에서, 제1 항원-결합 기능 영역 및 제2 항원 결합 기능 영역은 모두 Fab 단편이다.
일부 구체예에서, 제1 항원-결합 기능 영역 및 제2 항원 결합 기능 영역 중 하나는 Fab 단편이고, 다른 하나는 scFv이다.
일부 구체예에서, Fab 단편은 상이한 제1 중쇄 가변 영역 및 제2 중쇄 가변 영역, 및 상이한 제1 경쇄 가변 영역 및 제2 경쇄 가변 영역을 포함한다.
일부 구체예에서, 제1 Fc 사슬 및 그에 공유적으로 연결된 제1 항원-결합 기능 영역, 및 제2 Fc 사슬 및 그에 공유적으로 연결된 제2 항원-결합 기능 영역은, 환원제가 존재하는 용액 중에 있고 상기 용액 중에 상기 제1 Fc 사슬 및 그에 공유적으로 연결된 제1 항원-결합 기능 영역과 제2 Fc 사슬 및 그에 공유적으로 연결된 제2 항원-결합 기능 영역 외에 다른 폴리펩티드를 포함하지 않을 때, 모든 폴리펩티드 사슬의 중량을 기준으로 50% 미만의 호모다이머를 형성한다.
일부 구체예에서, 제1 항원-결합 기능 영역은 서열번호 2 및 6의 아미노산 서열을 포함한다.
일부 구체예에서, 제2 항원-결합 기능 영역은 서열번호 10 및 12의 아미노산 서열을 포함한다.
일부 구체예에서, 제1 항원-결합 기능 영역은 서열번호 4 및 8의 아미노산 서열을 더 포함한다.
일부 구체예에서, 제2 항원-결합 기능 영역은 서열번호 4 및 14의 아미노산 서열을 더 포함한다.
일부 구체예에서, 이중특이성 항체의 아미노산 서열은 서열번호 2, 4, 6, 8, 10, 12 및 14의 상응하는 조합이다. 예를 들어, 서열번호 2, 4, 6 및 8가 서로 조합되고, 서열번호 10, 4, 12 및 14가 서로 조합된 후, 조합된 양자는 추가로 조합되어, 본 발명의 이중특이성 항체를 형성한다.
본 발명의 제2 양상은 제1 양상에 따른 헤테로다이머 형태의 이중특이성 항체를 암호화하는 단리된 폴리뉴클레오티드에 관한 것이다.
일부 구체예에서, 제1 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 1 및 5로부터 선택된다.
일부 구체예에서, 제2 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 9 및 11로부터 선택된다.
일부 구체예에서, 제1 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 3 및 7로부터 더 선택된다.
일부 구체예에서, 제2 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 3 및 13으로부터 더 선택된다.
일부 구체예에서, 폴리뉴클레오티드의 서열은 서열번호 1, 3, 5, 7, 9, 11 및 13의 상응하는 조합이다. 예를 들어, 서열번호 1, 3, 5 및 7이 서로 조합되고, 서열번호 9, 3, 11 및 13이 서로 조합된다.
본 발명의 제3 양상은 제2 양상에 따른 단리된 폴리뉴클레오티드를 포함하는 재조합 발현 벡터에 관한 것이다.
일부 구체예에서, 발현 벡터는 pCDNA로부터 변형된 플라스미드 벡터 X0GC이다.
본 발명의 제4 양상은 제2 양상에 따른 단리된 폴리뉴클레오티드, 또는 제3 양상에 따른 재조합 발현 벡터를 포함하는 숙주 세포에 관한 것이다.
일부 구체예에서, 숙주 세포는 인간 배아 신장 세포 HEK293 또는 HEK293 세포에서 변형된 HEK293T, HEK293F, HEK293E; 햄스터 난소 세포 CHO 또는 CHO 세포에서 변형된 CHO-S, CHO-dhfr-, CHO/DG44, ExpiCHO; 대장균 또는 대장균에서 변형된 대장균 BL21, BL21(DE3), Rosetta, Origami; 효모균 또는 효모균에서 변형된 피키아(Pichia) 효모, 사카로마이세스 세레비지애(Saccharomyces cerevisiae), 클루이베로마이세스 락티스(Kluyveromyces lactis), 한세눌라 폴리모르파(Hansenula polymorpha); 곤충 세포 또는 곤충 세포에서 변형된 세포 High5, SF9; 식물 세포; 체세포인 포유동물 유방 세포로부터 선택된다.
본 발명의 제5 양상은 제1 양상에 따른 헤테로다이머 형태의 이중특이성 항체 또는 제2 양상에 따른 단리된 폴리뉴클레오티드 또는 제3 양상에 따른 재조합 발현 벡터 또는 제4 양상에 따른 숙주 세포, 및 약학적으로 허용가능한 담체를 포함하는 조성물에 관한 것이다.
본 발명의 제6 양상은 제1 양상에 따른 헤테로다이머 형태의 이중특이성 항체를 제조하는 방법에 관한 것으로서, 하기 단계를 포함한다:
1) 제2 양상에 따른 단리된 폴리뉴클레오티드 또는 제3 양상에 따른 재조합 발현 벡터를 각각 숙주 세포에서 발현시키는 단계;
2) 상기 숙주 세포에서 각각 발현된 단백질을 환원시키는 단계; 및
3) 환원된 단백질을 혼합하고, 혼합물을 산화시키는 단계.
일부 구체예에서, 숙주 세포는 인간 배아 신장 세포 HEK293 또는 HEK293 세포에서 변형된 HEK293T, HEK293F, HEK293F; 햄스터 난소 세포 CHO 또는 CHO 세포에서 변형된 CHO-S, CHO-dhfr-, CHO/DG44, ExpiCHO; 대장균 또는 대장균에서 변형된 대장균 BL21, BL21(DE3), Rosetta, Origami; 효모균 또는 효모균에서 변형된 피키아(Pichia) 효모, 사카로마이세스 세레비지애(Saccharomyces cerevisiae), 클루이베로마이세스 락티스(Kluyveromyces lactis), 한세눌라 폴리모르파(Hansenula polymorpha); 곤충 세포 또는 곤충 세포에서 변형된 세포 High5, SF9; 식물 세포; 체세포인 포유동물 유방 세포로부터 선택된다.
일부 구체예에서, 환원 단계는 1) 환원제의 존재 하에 환원 반응을 수행하는 단계로서, 상기 환원제는 2-메르캅토에틸아민 (2-mercaptoethylamine), 디티오트레이톨 (dithiothreitol), 트리스(2-카르복시에틸)포스핀 (tris(2-carboxyethyl)phosphine) 또는 다른 화학적 유도체로부터 선택되는 것인 단계; 2) 상기 환원제를 제거하는 단계를 포함하며, 예를 들어 0.1mM 또는 더 높은 농도에서 디티오트레이톨 존재 하에 4℃에서 환원 반응을 적어도 3시간 수행한다. 상기 환원제 및 환원 반응 조건의 제한은 또한 본원의 환원제 및 환원 반응 사용과 관련된 다른 상황에도 적용된다.
일부 구체예에서, 산화 단계는 공기 중 산화이며, 산화제의 존재 하에 산화 반응을 수행하는 단계로서, 상기 산화제는 L-데히드로아스코르브산 (L-dehydroascorbic acid) 또는 이의 화학적 유도체로부터 선택되는 것인 단계를 포함하며, 예를 들어 0.5mM 도는 더 높은 농도에서 L-데히드로아스코르브산 존재 하에 4℃ 조건에서 산화 반응을 적어도 3시간 수행한다.
일부 구체예에서, 상기 방법은 분리 및 정제 단계를 더 포함한다.
본 발명의 제7 양상은 개체의 질병을 예방 및/또는 치료하기 위한 의약의 제조에서, 제1 양상에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 제2 양상에 따른 단리된 폴리뉴클레오티드 및/또는 제3 양상에 따른 재조합 발현 벡터 및/또는 제4 양상에 따른 숙주 세포 및/또는 제5 양상에 따른 조성물의 용도에 관한 것이다.
본 발명의 제8 양상은 개체의 질병을 예방 및/또는 치료하기 위한 의약으로 사용하기 위한, 제1 양상에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 제2 양상에 따른 단리된 폴리뉴클레오티드 및/또는 제3 양상에 따른 재조합 발현 벡터 및/또는 제4 양상에 따른 숙주 세포 및/또는 제5 양상에 따른 조성물에 관한 것이다.
본 발명의 제9 양상은 제1 양상에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 제2 양상에 따른 단리된 폴리뉴클레오티드 및/또는 제3 양상에 따른 재조합 발현 벡터 및/또는 제4 양상에 따른 숙주 세포 및/또는 제5 양상에 따른 조성물을 그것이 필요한 개체에게 투여하는 단계를 포함하는 질병을 예방 및/또는 치료하기 위한 방법에 관한 것이다.
일부 구체예에서 개체는 포유 동물, 바람직하게는, 인간 개체다.
일부 구체예에서, 상기 질병은 하기 종양으로부터 선택된다: 백혈병, 림프종, 골수종, 뇌종양, 두경부 편평세포암종, 비소세포 폐암, 비인두암종, 식도암, 위암, 췌장암, 담낭암, 간암, 대장암, 유방암, 난소암, 자궁경부암, 자궁내막암, 자궁육종, 전립선암, 방광암, 신장암, 흑색종, 소세포폐암, 골암.
본 발명은 항 PD-L1/항 CD47 천연 항체 구조-유사 헤테로다이머 형태의 신규한 이중특이성 항체를 설계하였고, 이는 천연 IgG 특징을 가지며, 중쇄 및 경쇄의 미스매치 없이 고도로 안정한 헤테로다이머 형태의 항 PD-L1/항 CD47 이중특이성 항체이다. 본 발명에 의해 제조된 이중특이성 항체는 2개의 표적 분자 PD-L1 및 CD47에 동시에 결합할 수 있고, 이를 복잡한 질병의 치료에 적용할 때 단일 치료제보다 더욱 우수한 효과를 발휘할 수 있다. 동시에, 다수의 약물의 조합 치료에 관하여, 상기 이중특이성 항체는 단일 치료 분자로서 환자 및 의료종사자의 사용을 용이하게 할 뿐만 아니라, 복잡한 신약 개발 과정을 단순화시킨다.
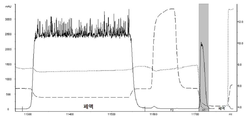
도 1은 항 PD-L1-Fc1의 용리 피크 크로마토그램을 나타낸다.
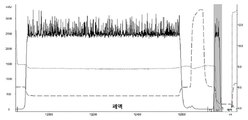
도 2는 항 CD47-Fc2의 용리 피크 크로마토그램을 나타낸다.
도 3은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 구조를 나타낸다.
도 4는 하나의 중쇄 및 하나의 경쇄의 반 항체 분자 구조도를 나타낸다.
도 5는 하나의 중쇄 및 하나의 경쇄의 반 항체 분자의 SEC-HPLC 분석 결과를 나타낸다. 여기에서 A 및 B는 각각 항 PD-L1 반 항체 분자 및 항 CD47 반 항체 분자의 결과를 나타낸다.
도 6은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 SEC-HPLC 분석 결과를 나타낸다.
도 7은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 RPC 분석 결과를 나타낸다.
도 8은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 CE 분석 결과를 나타낸다.
도 9의 A는 항 PD-L1/항 CD47 헤테로다이머 항체의 PD-L1에 대한 친화력을 나타내고, B는 항 PD-L1/항 CD47 헤테로다이머 항체의 CD47에 대한 친화력을 나타낸다.
도 10은 PD-L1 단일클론항체 및 CD47의 조합이 PD-LA 및 CD47에 동시에 결합할 수 없고, 항 PD-L1/항 CD47 헤테로다이머 항체만이 2개의 항원에 동시에 결합하는 활성을 갖는 것을 나타낸다.
도 11의 A 및 B는 각각 CD47 단일클론항체 및 항 PD-L1/항 CD47 헤테로다이머 항체의 HCC827 및 RBC에 대한 결합 활성을 나타낸다.
도 12는 항 PD-L1/항 CD47 헤테로다이머 항체의 T 세포 조절 활성을 나타낸다.
도 13은 항 PD-L1/항 CD47 헤테로다이머 항체에 의해 매개되는 대식세포의 종양 세포에 대한 식세포 활성을 나타낸다.
도 2는 항 CD47-Fc2의 용리 피크 크로마토그램을 나타낸다.
도 3은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 구조를 나타낸다.
도 4는 하나의 중쇄 및 하나의 경쇄의 반 항체 분자 구조도를 나타낸다.
도 5는 하나의 중쇄 및 하나의 경쇄의 반 항체 분자의 SEC-HPLC 분석 결과를 나타낸다. 여기에서 A 및 B는 각각 항 PD-L1 반 항체 분자 및 항 CD47 반 항체 분자의 결과를 나타낸다.
도 6은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 SEC-HPLC 분석 결과를 나타낸다.
도 7은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 RPC 분석 결과를 나타낸다.
도 8은 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 CE 분석 결과를 나타낸다.
도 9의 A는 항 PD-L1/항 CD47 헤테로다이머 항체의 PD-L1에 대한 친화력을 나타내고, B는 항 PD-L1/항 CD47 헤테로다이머 항체의 CD47에 대한 친화력을 나타낸다.
도 10은 PD-L1 단일클론항체 및 CD47의 조합이 PD-LA 및 CD47에 동시에 결합할 수 없고, 항 PD-L1/항 CD47 헤테로다이머 항체만이 2개의 항원에 동시에 결합하는 활성을 갖는 것을 나타낸다.
도 11의 A 및 B는 각각 CD47 단일클론항체 및 항 PD-L1/항 CD47 헤테로다이머 항체의 HCC827 및 RBC에 대한 결합 활성을 나타낸다.
도 12는 항 PD-L1/항 CD47 헤테로다이머 항체의 T 세포 조절 활성을 나타낸다.
도 13은 항 PD-L1/항 CD47 헤테로다이머 항체에 의해 매개되는 대식세포의 종양 세포에 대한 식세포 활성을 나타낸다.
정의:
공유 결합은 헤테로다이머 형태의 이중특이성 항체에서, 2개의 Fc 사슬 간에, 어느 하나의 FC 사슬 및 그와 서로 연결된 항원-결합 기능 영역 간에, 공유 결합을 통해 연결되어 하나의 분자가 되는 것을 의미한다. 여기에서 Fc 사슬은 하나 이상의 공유 결합(예: 이황화 결합 사슬)을 통해 연결된 제1 항원-결합 기능 영역 및 제2 항원-결합 기능 영역을 포함하고; 상기 제1 Fc 사슬 및 제2 Fc 사슬은 각각 공유 결합(예: 이민 결합 또는 아미드 결합)을 통해 하나의 항원-결합 기능 영역 상에 연결된다.
항원-결합 기능 영역은 항원과 같은 표적 분자와 특이적 상호 작용을 발생시킬 수 있는 영역을 의미하며, 그 작용은 고도의 선택성을 갖고, 하나의 표적 분자를 인식하는 서열은 통상적으로 다른 분자 서열을 인식할 수 없다. 대표적인 항원-결합 기능 영역은 다음을 포함한다: 항체의 가변 영역, 항체 가변 영역의 구조적 변이체, 수용체 결합 도메인, 리간드 결합 도메인 또는 효소 결합 도메인.
하나 이상의 이황화 결합 사슬 간의 연결은 제1 Fc 사슬 및 제2 Fc 사슬이 하나 이상의 이황화 결합 사슬 간의 연결을 통해 헤테로다이머 단편을 형성하는 것을 의미한다. 본 발명에서, 하나 이상의 이황화 결합의 형성은 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역이 동일한 세포 내에서 합성될 때 형성될 수 있고, 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역이 서로 다른 세포 내에서 각각 합성된 후, in vitro 환원 및 산화의 방법을 통해 합성될 수도 있다.
제1 Fc 사슬 및 제2 Fc 사슬은 공유 결합에 의해 형성된 결합 단편을 의미하며, 공유 결합은 이황화 결합을 포함하고, 각 사슬은 면역글로불린 중쇄의 불변 영역의 적어도 일부분을 포함하고; 상기 제1 Fc 사슬 및 제2 Fc 사슬은 아미노산 서열이 상이하며, 적어도 하나의 상이한 아미노산을 포함한다. 본 발명의 제1 Fc 사슬 및 제2 Fc 사슬은 동일한 사슬 간에 강렬한 상호 반발 작용이 존재하나, 상이한 사슬 간에는 끌어당기는 작용이 존재하며, 따라서 세포 내에서 공-발현 될 때, 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역은, 헤테로다이머를 형성하려는 경향이 있다. 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역을 각각 2개의 숙주 세포 내에서 발현시킬 때, 제1 Fc 사슬 또는 제1 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역은 호모다이머를 형성하려는 경향이 없고, 제2 Fc 사슬 또는 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역은 호모다이머를 형성하려는 경향이 없다. 본 발명에서, 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역이 각각 2개의 숙주 세포 내에서 발현될 때, 그리고 환원제가 존재할 때, 호모다이머의 비율은 50% 미만이고, 즉 단량체 (하나의 Fc 사슬 또는 하나의 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역) 비율은 50% 보다 크다.
면역글로불린은 4개의 폴리펩티드 사슬을 갖는 대칭 구조이며, 이 중 2개는 비교적 길고 상대적 분자량이 비교적 큰 동일한 중쇄이고, 450~550개의 아미노산 잔기를 함유하며, 상대적 분자 질량은 55000~70000Da 사이이고; 2개는 비교적 짧고 상대적 분자량이 비교적 작은 경쇄(L 사슬)이고, 약 210개의 아미노산 잔기를 함유하고, 상대적 분자 질량이 약 24000 Da이다. 상이한 면역글로불린 중쇄 및 경쇄는 N 말단 근처의 약 110개 아미노산의 서열에서 변화가 크고, 가변 영역 (variable region, V 영역)으로 불리며, C 말단 근처의 그 나머지 아미노산 서열은 상대적으로 안정하고, 불변 영역 (constant region, C 영역)으로 불린다. 중쇄에서 가변 영역은 중쇄 길이의 약 1/4를 점유하고, 불변 영역은 중쇄 길이의 약 3/4를 점유한다. 공지된 5개의 Ig의 경우, IgG (γ), IgA (α), IgD (δ), IgM (μ) 및 IgE (ε)이고, 전자의 3가지 Ig의 H 사슬 내에 3개의 불변 영역, 즉 CH1, CH2 및 CH3 구성을 가진다. 후자의 2가지(IgM 및 IgE)의 H 사슬 내에 하나의 VH 영역 및 4개의 불변 영역, 즉, CH1 내지 CH4를 가진다. 불변 영역은 면역글로불린 분자의 골격일 뿐만 아니라, 면역 반응을 활성화시키는 부위 중 하나이다. 본 발명 실시예는 IgG에 관한 것이지만, 당업자라면, 원하는 경우, 공지된 방법을 통해 본 발명의 항체의 종류를 전환할 수 있다는 것을 알고 있다. 예를 들어, 본래 IgM인 본 발명 항체는 본 발명의 IgG 항체로 분류 전환될 수 있다. 또한, 분류 전환 기술을 사용하여 하나의 IgG 서브 클래스를 다른 서브 클래스로 전환할 수 있고, 예를 들어 IgG1에서 IgG2로 전환할 수 있다. 따라서, 본 발명의 항체의 작동 기능(effector function)은 이소 타입 전환을 통해 예를 들어 IgG1, IgG2, IgG3, IgG4, IgD, IgA, IgE 또는 IgM 항체로 변할 수 있고, 각종 치료 용도에 사용된다. 일 실시예에서, 본 발명의 항체는 IgG1 항체, 예를 들어 IgG1,이다.
본 발명에서 불변 영역의 일부분은 적어도 제1 Fc 사슬 및 제2 Fc 사슬이 상호 작용하는 영역을 포함하며, 상기 영역은 IgG의 경우 CH3 영역의 일부분 아미노산에 있고, 적어도 GLN347, TYR349, THR350, LEU351, SER354, ARG355, ASP356, GLU357, LYS360, SER364, THR366, LEU368, LYS370, ASN390, LYS392, THR394, PRO395, VAL397, ASP399, SER400, PHE405, TYR407, LYS409, LYS439를 포함한다.
제1 Fc 사슬 및 제2 Fc 사슬이 각각 공유 결합 또는 링커를 통해 하나의 항원-결합 기능 영역 상에 연결된 것은 제1 Fc 사슬 및 제2 Fc 사슬이 각각 공유 결합 또는 링커를 통해 하나의 항체의 항원-결합 단편, 또는 항원을 인식할 수 있는 단일 사슬 항체, 또는 항원을 인식할 수 있는 다른 항체 단편 변이체, 또는 리간드를 인식할 수 있는 수용체, 또는 수용체를 인식할 수 있는 리간드에 연결되는 것을 의미하고, 여기에서 상기 공유 결합은 화학 결합의 일종으로, 둘 이상의 원자가 함께 그들의 외각 전자를 사용하여, 이상적인 상황에서 전자 포화 상태가 달성되어, 그에 의해 공유 결합이라고 불리는 비교적 안정한 화학 구조를 구성하고, 또는 공유 결합은 원자 간에 공유 전자 쌍에 의해 형성된 상호 작용이다. 동일한 원소의 원자 또는 상이한 원소의 원자는 모두 공유 결합을 통해 결합될 수 있고, 본 발명의 제1 Fc 사슬 및 제2 Fc 사슬 간의 공유 결합의 경우, 한 분자의 아미노산의 아미노기와 다른 분자의 아미노산의 카르복실기의 탈수 반응에 의해 형성된 아미드 결합, 또는 에틸렌글리콜 또는 폴리에틸렌글리콜 또는 다른 화합물 또는 그의 중합체의 알데히드기와 한 분자의 아미노산의 아미노기가 형성한 아미드 결합 또는 이미드 결합을 포함하나, 이에 제한되지 않는다. 여기에서 링커는 2개의 폴리펩티드 사슬을 공유 결합을 통해 연결할 수 있는 아미노산 서열 또는 화합물 또는 화합물의 다량체이며, 여기에서 아미노산 서열은 작은 펩티드, 예컨대 GGGGSGGGGSGGGGS를 포함하나, 이에 제한되지 않으며, 아미드 결합을 통해 제1 Fc 사슬 또는 제2 Fc 사슬, 및 항원을 인식할 수 있는 단일 사슬 항체, 또는 항원을 인식할 수 있는 다른 항체 단편 구조 변이체를 연결한다.
제1 Fc 사슬 및 제2 Fc 사슬은 헤테로다이머를 형성하는 경향이 있고, 각자 호모다이머를 형성하려는 경향이 없으며, 이는 제1 Fc 사슬 및 제2 Fc 사슬에서 동일한 폴리펩티드 사슬 간에 상호 반발하는 작용이 존재하고, 상이한 폴리펩티드 사슬 간에 인력 작용이 존재하기 때문에, 세포 내에 공-발현될 때, 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역은 헤테로다이머를 형성하려는 경향이 있음을 의미한다. 제1 Fc 사슬 및 제2 Fc 사슬, 또는 제1 Fc 사슬 및 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역이 각각 2개의 숙주 세포 내에 발현될 때, 제1 Fc 사슬 또는 제1 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역은 호모다이머를 형성하려는 경향이 없고, 제2 Fc 사슬 또는 제2 Fc 사슬 및 그와 서로 연결된 항원-결합 기능 영역은 호모다이머를 형성하려는 경향이 없다.
카바트(Kabat) EU 인덱스 넘버링 시스템은 Kabat가 일종의 방법을 이용하여 항체 서열의 각각의 아미노산에 숫자를 지정한 것을 의미하고, 각각의 잔기에 번호를 지정하는 이러한 방법은 당업계에 표준 방법이 되었다. Kabat 방법은 그의 연구 중에 존재하지 않던 다른 항체로 확장 가능하며, 보존된 아미노산에 기초하여, 표적 항체를 Kabat에 의해 식별된 공통 서열 중 하나와 정렬시킨다.
Fc 도메인은 결정화 가능한 조각 (fragment crystallizable, Fc)을 의미하며, Ig의 CH2 및 CH3 도메인에 해당하고, Ig와 이펙터 분자 또는 세포와 상호 작용하는 부위이다.
IgG는 면역글로불린 G (Immunoglobulin G, IgG)의 약자이며, 혈청에서 주요한 항체 성분이고, IgG 분자 중의 r 사슬 항원 차이에 따라, 인간 IgG는 4개의 서브 클래스를 갖는다: IgG1, IgG2, IgG3, IgG4.
반 항체 분자는 항체의 하나의 중쇄 및 하나의 경쇄로 형성된 구조를 의미하며, 여기에서 중쇄 및 경쇄는 공유 결합을 통해 연결될 수 있거나, 공유 결합을 통하지 않고 연결될 수 있고, 항원을 식별하는 1가 항체 구조이다.
Fab 단편은 분자 인식 서열이며, 항원-결합 단편 (fragment of antigen binding, Fab)이고, 항체 분자의 두 개의 아암에 해당하고, 온전한 경쇄 및 중쇄의 VH 및 CH1 도메인으로 구성된다. scFv는 분자 인식 서열이며, 항체의 경쇄 가변 영역 및 중쇄 가변 영역의 유전자 조작에 의해 변형하여 수득된 항체 단편의 구조 이성질체이다. 막 수용체의 세포외 영역은 분자 인식 서열이며, 막 수용체는 일반적으로 세포 외부에 위치하여 상응하는 항원 또는 리간드를 인식 및 결합하는 세포외 영역, 수용체를 세포 표면에 고정시키는 막 관통(transmembrane) 영역, 및 세포내 키나제 활성을 갖거나 신호 전달 경로를 전달할 수 있는 세포내 영역을 포함한다. 세포막 수용체의 리간드는 막 수용체의 세포외 영역에 인식되어 결합될 수 있는 단백질, 작은 펩티드, 또는 화합물을 의미한다. 사이토카인은 면역원, 미토겐(mitogen) 또는 다른 자극제에 의해 유도된 다양한 유형의 세포들에 의해 생성되는 저 분자량 가용성 단백질로서, 선천성 면역 및 적응성 면역의 조절, 조혈작용(hematopoiesis), 세포 성장, APSC 다능성 줄기세포 및 손상된 조직의 수복과 같은 다양한 기능들을 갖는다. 사이토카인은 인터루킨, 인터페론, 종양 괴사 인자 수퍼패밀리(tumor necrosis factor superfamily), 콜로니 자극 인자(colony stimulating factors), 케모카인(chemokines), 성장 인자 등으로 분류된다. 단백질 발현 태그(protein expression tag)는 표적 단백질의 N-말단 또는 C-말단에 부가된 아미노산 서열을 의미하며, 작은 펩티드 또는 일정 길이의 아미노산일 수 있고, 태그의 부가는 단백질의 정확한 폴딩에 유리할 수 있고, 단백질의 분리 및 정제에 유리할 수 있고, 단백질의 세포 내 분해의 감소에 유리할 수 있고, 일반적으로 사용되는 태그에는 HA, SUMO, His, GST, GFP 및 Flag가 포함되지만, 이에 제한되는 것은 아니다.
본 발명의 헤테로다이머 형태의 이중특이성 항체에 적용 가능한 항체에는 어떠한 제한도 없다. 바람직하게는, 질병을 치료 및/또는 예방하기 위해 사용할 수 있는 당업계에 공지된 항체는 모두 본 발명에서 사용될 수 있다.
본 발명의 헤테로다이머 형태의 이중특이성 항체는 하나 또는 다수의 치환, 제거, 첨가 및/또는 삽입을 가질 수 있다. 예를 들어, 어떤 아미노산은 단백질 구조에서 다른 아미노산을 치환하여도 다른 폴리펩티드(예: 항원) 또는 세포에 결합하는 능력의 상당한 손실이 없을 수 있다. 결합 능력 및 단백질의 성질은 단백질의 생물학적 기능적 활성을 결정하므로, 단백질 서열 상에 어떤 아미노산 서열의 치환이 수행되어도 그의 생물학적 효용 또는 활성의 현저한 손실이 없을 것이다.
많은 경우에, 폴리펩티드 변이체는 하나 또는 다수의 보존적 치환을 함유한다. "보존적 치환(conservative substitution)"은 아미노산이 유사한 성질을 갖는 다른 아미노산으로 치환되는 것을 의미하며, 이는 펩티드 화학 분야의 기술자라면 폴리펩티드의 2차적 구조 및 친수성 성질이 실질적으로 변하지 않을 것으로 예상할 것이다.
아미노산 치환은 일반적으로 아미노산의 측쇄 치환기의 상대적 유사성, 예컨대 이들의 소수성, 친수성, 전하, 크기 등에 기초한다. 상술한 다양한 특성을 고려할 때, 예시적인 치환은 당업자에게 잘 알려져 있는데, 아르기닌 및 리신; 글루탐산 및 아스파르트산; 세린 및 트레오닌; 글루타민 및 아스파라긴; 및 발린, 류신 및 이소류신을 포함한다.
본 발명에서 사용된 용어 "동일성(identity)"은 당업계에 일반적으로 알려진 의미를 가지며, 당업자라면 상이한 서열들 간의 동일성을 판단하는 규칙 및 기준을 숙지하고 있고, 서열을 정렬하고 갭을 도입(필요 시, 최대 상동율 %를 획득하기 위해)한 후, 폴리뉴클레오티드 또는 폴리펩티드 서열 변이체의 잔기와 비-변이체 서열이 동일한 백분율을 지칭한다. 본 발명에서, 동일성의 정의가 충족되는 경우, 그 수득된 변이체 서열은 모체 서열이 갖는 생물학적 활성을 보유함이 더 요구된다. 당업자라면 상술한 활성을 이용하여 변이체 서열을 스크리닝하는 방법 및 수단을 잘 알고 있다. 당업자라면 본 명세서에 공개된 내용으로부터, 이러한 변이체 서열을 용이하게 획득할 수 있다. 구체적인 실시 방식에서, 폴리뉴클레오티드 및 폴리펩티드 변이체는 본원에 따른 폴리뉴클레오티드 또는 폴리펩티드와 약 70% 이상, 약 75% 이상, 약 80% 이상, 약 90% 이상, 약 95% 이상, 약 98% 이상 또는 약 99% 이상, 또는 적어도 약 99.1%, 99.2%, 99.3%, 99.4%, 99.5%, 99.6%, 99.7%, 99.8% 또는 99.9% 폴리뉴클레오티드 또는 폴리펩티드 동일성을 갖는다. 유전자 코드의 중복성으로 인해, 이들 서열과 동일한 아미노산 서열을 암호화하는 변이체가 존재한다.
본 발명의 또 다른 구체예에서, 중간 정도 내지 매우 엄격한 조건 하에서 본 발명이 제공하는 폴리뉴클레오티드 서열 또는 그의 단편, 또는 그의 상보적 서열과 하이브리드화(hybridization) 가능한 폴리뉴클레오티드 조성물이 제공된다. 하이브리드화 기술은 분자 생물학 분야에서 잘 알려져 있다. 설명의 목적으로, 본 발명의 폴리뉴클레오티드와 다른 폴리뉴클레오티드의 하이브리드화를 테스트하기 위한 적당한 중간 정도의 엄격한 조건은 5xSSC, 0.5% SDS, 1.0mM EDTA (pH 8.0)의 용액에서 사전 세척하는 단계; 50℃내지 60℃에서 밤새 5xSSC의 조건하에서 하이브리드화 하는 단계; 및 65℃에서 20분 동안 0.1% SDS를 함유하는 2x, 0.5x 및 0.2x SSC로 각각 2회씩 세척하는 단계를 포함한다. 당업자라면, 예를 들어, 하이브리드화 용액의 염 함량 및/또는 하이브리드화 수행 온도를 변화시킴으로써 하이브리드화의 엄격성이 용이하게 조작될 수 있음을 이해할 것이다. 예를 들어, 또 다른 구체예에서, 적절한 매우 엄격한 하이브리드화 조건은 하이브리드화 온도를, 예컨대, 60-65℃ 또는 65-70℃로 상승시키는 것을 제외하고는, 상기한 조건들을 포함한다.
본 발명의 숙주 세포는 외인성 유전자 발현에 사용되는 모든 세포일 수 있고, 비제한적으로 대장균, 효모, 곤충 세포, 식물 세포, 포유동물 세포를 포함한다.
본 발명의 벡터는 임의의 유형의 세포 또는 생물체에서 복제할 수 있는 벡터를 포함하고, 예컨대, 플라스미드, 박테리오파지, 코스미드(cosmids) 및 미소염색체(minichromosomes)를 포함한다. 일부 구체예에서, 본 발명의 폴리뉴클레오티드를 포함하는 벡터는 폴리뉴클레오티드의 증식 또는 복제에 적합한 벡터, 또는 본 발명의 폴리펩티드의 발현에 적합한 벡터이다. 이러한 벡터는 당 업계에 공지되어 있으며 상업적으로 입수 가능하다.
"벡터(vector)"는 셔틀 벡터(shuttle vectors) 및 발현 벡터(expression vectors)를 포함한다. 일반적으로, 플라스미드 구성물도 박테리아에서 플라스미드 복제 및 선택에 각각 사용되는 복제 기점(origin of replication)(예: ColE1 복제 기점) 및 선별 마커(예: 암피실린 또는 테트라사이클린 내성)를 포함한다. "발현 벡터"는 박테리아 또는 진핵(eukaryotic) 세포에서 항체 단편을 포함하여 본 발명의 항체를 발현시키는데 필요한 제어 서열 또는 조절 요소를 포함하는 벡터를 말한다.
본 발명의 벡터는 외인성 유전자 발현에 사용되는 모든 벡터일 수 있고, 비제한적으로 플라스미드 벡터를 포함하며, 여기에서 플라스미드 벡터는 적어도 복제 기점, 프로모터, 목적 유전자, 다중 클로닝 부위(multiple cloning site) 및 선택적 마커 유전자를 포함하고, 바람직하게는, 본 발명에 따른 벡터는 X0GC 벡터와 같은 pCDNA에 기초하여 변형하여 얻은 플라스미드 벡터를 포함하나, 이에 제한되는 것은 아니다.
본 발명의 대상체는 가금류, 파충류, 포유동물 등을 포함한다. 바람직하게는, 포유동물은 설치류 동물 및 영장류 동물을 포함하고, 바람직하게는, 영장류 동물은 인간을 포함한다.
본 발명에 관련된 질병의 범위는 비제한적으로 종양을 포함하고, 바람직하게는 상기 종양은 하기를 포함한다: 백혈병, 림프종, 골수종, 뇌종양, 두경부 편평세포암종, 비소세포 폐암, 비인두암종, 식도암, 위암, 췌장암, 담낭암, 간암, 대장암, 유방암, 난소암, 자궁경부암, 자궁내막암, 자궁육종, 전립선암, 방광암, 신장암, 흑색종, 소세포폐암, 골암.
약학적으로 허용가능한 담체는 약학 분야에서 일반적으로 사용되는 약물 담체, 예를 들어, 희석제, 부형제, 물 등; 전분, 수크로스, 락토스, 미정질 셀룰로오스 등과 같은 충전제(fillers); 셀룰로오스 유도체, 알기네이트, 젤라틴 및 폴리비닐 피롤리돈(polyvinyl pyrrolidone)과 같은 결합제(binders); 글리세린과 같은 수화제(wetting agents); 카르복시메틸 나트륨 전분(sodium carboxymethyl starch), 히드록시프로필 셀룰로오스, 크로스카르멜로스(croscarmellose), 한천(agar), 탄산칼슘, 소듐 히드로겐카르보네이트 등의 붕해제(disintegrating agents); 4차 암모늄 화합물과 같은 흡수 증진제(absorption enhancers); 세타놀(cetanol), 라우릴 황산 나트륨(sodium lauryl sulfate) 등의 계면 활성제(surfactants); 카올리나이트(kaolinite), 벤토나이트(bentonite)와 같은 흡착 담체(adsorption carriers); 활석(talc), 스테아르산 칼슘(calcium stearate) 및 스테아르산 마그네슘(magnesium stearate), 미분화(micronized) 실리카겔, 폴리에틸렌 글리콜 등과 같은 윤활제를 말한다. 또한, 향미제, 감미제 등의 다른 보조제가 그 조성물에 첨가될 수도 있다.
일부 구체예에서, 본 발명은 하기 기술 방안에 관한 것이다.
기술방안 1. 헤테로다이머 형태의 이중특이성 항체로서, PD-L1과 특이적으로 결합할 수 있는 제1 항원-결합 기능 영역 및 CD47과 특이적으로 결합할 수 있는 제2 항원-결합 기능 영역을 포함하고, 상기 이중특이성 항체는 하나 또는 다수의 이황화 결합 사슬을 통해 연결된 제1 Fc 사슬 및 제2 Fc 사슬을 포함하고, 상기 제1 Fc 사슬 및 제2 Fc 사슬은 공유 결합 또는 링커를 통해 각각 PD-L1 항원-결합 기능 영역 및 CD47 항원-결합 기능 영역에 연결되거나, 또는 상기 제1 Fc 사슬 및 제2 Fc 사슬은 공유 결합 또는 링커를 통해 각각 CD47 항원-결합 기능 영역 및 PD-L1 항원-결합 기능 영역 상에 연결되고; 제1 Fc 사슬 및 제2 Fc 사슬은 하기 위치에 5개 아미노산 치환을 포함하고,
1) 제1 Fc 사슬 상의 위치 366 및 위치 399 아미노산 치환, 제2 Fc 사슬 상의 위치 351, 위치 407 및 위치 409 아미노산 치환; 또는
2) 제1 Fc 사슬 상의 위치 366 및 위치 409 아미노산 치환, 제2 Fc 사슬 상의 위치 351, 위치 399 및 위치 407 아미노산 치환;
상기 아미노산 치환된 제1 Fc 사슬 및 제2 Fc 사슬은 서로 헤테로다이머를 형성하려는 경향이 있고, 각자 호모다이머를 형성하려는 경향이 없으며,
상기 아미노산 위치는 카바트(Kabat) EU 인덱스 넘버링 시스템에 따라 번호가 지정된다.
기술방안 2. 기술방안 1에 있어서, 제1 Fc 사슬 및 제2 Fc 사슬 아미노산 치환은 하기와 같은 것인 헤테로다이머 형태의 이중특이성 항체,
a) 위치 351 상의 치환은 글리신, 티로신, 발린, 프롤린, 아스파르트산, 글루탐산, 리신 또는 트립토판이고;
b) 위치 366 상의 치환은 류신, 프롤린, 트립토판 또는 발린이고;
c) 위치 399 상의 치환은 시스테인, 아스파라긴, 이소류신, 글리신, 아르기닌, 트레오닌 또는 알라닌이고;
d) 위치 407 상의 치환은 류신, 알라닌, 프롤린, 페닐알라닌, 트레오닌 또는 히스티딘이고; 그리고
e) 위치 409 상의 치환은 시스테인, 프롤린, 세린, 페닐알라닌, 발린, 글루타민 또는 아르기닌이다.
기술방안 3. 기술방안 1 또는 2에 있어서, 아미노산 치환은 하기를 포함하는 것인 헤테로다이머 형태의 이중특이성 항체:
a) 제1 Fc 사슬에서 T366L 및 D399R 치환, 제2 Fc 사슬에서 L351E, Y407L 및 K409V 치환;
b) 제1 Fc 사슬에서 T366L 및 D399C 치환, 제2 Fc 사슬에서 L351G, Y407L 및 K409C 치환;
c) 제1 Fc 사슬에서 T366L 및 D399C 치환, 제2 Fc 사슬에서 L351Y, Y407A 및 K409P 치환;
d) 제1 Fc 사슬에서 T366P 및 D399N 치환, 제2 Fc 사슬에서 L351V, Y407P 및 K409S 치환;
e) 제1 Fc 사슬에서 T366W 및 D399G 치환, 제2 Fc 사슬에서 L351D, Y407P 및 K409S 치환;
f) 제1 Fc 사슬에서 T366P 및 D399I 치환, 제2 Fc 사슬에서 L351P, Y407F 및 K409F 치환;
g) 제1 Fc 사슬에서 T366V 및 D399T 치환, 제2 Fc 사슬에서 L351K, Y407T 및 K409Q 치환;
h) 제1 Fc 사슬에서 T366L 및 D399A 치환, 제2 Fc 사슬에서 L351W, Y407H 및 K409R 치환.
기술방안 4. 기술방안 1 내지 3 중 어느 하나에 있어서, 아미노산 치환은 하기를 포함하는 것인 헤테로다이머 형태의 이중특이성 항체:
a) 제1 Fc 사슬에서 T366L 및 K409V 치환, 제2 Fc 사슬에서 L351E, Y407L 및 D399R 치환;
b) 제1 Fc 사슬에서 T366L 및 K409C 치환, 제2 Fc 사슬에서 L351G, Y407L 및 D399C 치환;
c) 제1 Fc 사슬에서 T366L 및 K409P 치환, 제2 Fc 사슬에서 L351Y, Y407A 및 D399C 치환;
d) 제1 Fc 사슬에서 T366P 및 K409S 치환, 제2 Fc 사슬에서 L351V, Y407P 및 D399N 치환;
e) 제1 Fc 사슬에서 T366W 및 K409S 치환, 제2 Fc 사슬에서 L351D, Y407P 및 D399G 치환;
f) 제1 Fc 사슬에서 T366P 및 K409F 치환, 제2 Fc 사슬에서 L351P, Y407F 및 D399I 치환;
g) 제1 Fc 사슬에서 T366V 및 K409Q 치환, 제2 Fc 사슬에서 L351K, Y407T 및 D399T 치환;
h) 제1 Fc 사슬에서 T366L 및 K409R 치환, 제2 Fc 사슬에서 L351W, Y407H 및 D399A 치환.
기술방안 5. 기술방안 1 내지 4 중 어느 하나에 있어서, 제1 Fc 사슬의 아미노산 치환은 T366L 및 D399R이고, 제2 Fc 사슬의 아미노산 치환은 L351E, Y407L 및 K409V인 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 6. 기술방안 1 내지 5 중 어느 하나에 있어서, Fc 사슬은 IgG에서 유래된 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 7. 기술방안 1 내지 6 중 어느 하나에 있어서, PD-L1 및 CD47 항원-결합 기능 영역은 Fab 단편 또는 scFv 단편인 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 8. 기술방안 1 내지 7 중 어느 하나에 있어서, PD-L1 및 CD47 항원-결합 기능 영역은 모두 Fab 단편인 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 9. 기술방안 1 내지 7 중 어느 하나에 있어서, PD-L1 및 CD47 항원-결합 기능 영역 중 하나는 Fab 단편이고, 다른 하나는 scFv인 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 10. 기술방안 7 내지 9 중 어느 하나에 있어서, 상기 Fab 단편은 상이한 제1 중쇄 가변 영역 및 제2 중쇄 가변 영역, 및 상이한 제1 경쇄 가변 영역 및 제2 경쇄 가변 영역을 포함하는 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 11. 기술방안 1 내지 10 중 어느 하나에 있어서, 제1 Fc 사슬 및 그에 공유적으로 연결된 PD-L1 항원-결합 기능 영역, 및 제2 Fc 사슬 및 그에 공유적으로 연결된 CD47 항원-결합 기능 영역, 또는 제1 Fc 사슬 및 그에 공유적으로 연결된 CD47 항원-결합 기능 영역, 및 제2 Fc 사슬 및 그에 공유적으로 연결된 PD-L1 항원-결합 기능 영역은, 단독으로 존재하면서 동시에 환원제가 존재할 때 이는 중량비 약 50% 미만의 호모다이머를 형성하는 것인 헤테로다이머 형태의 이중특이성 항체.
기술방안 12. 기술방안 1 내지 11 중 어느 하나에 있어서, 이중특이성 항체의 아미노산 서열은 하기로부터 선택되는 것인 헤테로다이머 형태의 이중특이성 항체: 서열번호 2, 4, 6, 8, 10, 12 및 14.
기술방안 13. 기술방안 1 내지 12 중 어느 하나에 따른 헤테로다이머 형태의 이중특이성 항체를 암호화하는 단리된 폴리뉴클레오티드.
기술방안 14. 기술방안 13에 있어서, 그의 서열은 하기로부터 선택되는 것인 단리된 폴리뉴클레오티드: 서열번호 1, 3, 5, 7, 9, 11 및 13.
기술방안 15. 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드를 포함하는 재조합 발현 벡터.
기술방안 16. 기술방안 15에 있어서, 발현 벡터는 pCDNA로부터 변형된 플라스미드 벡터 X0GC인 것인 재조합 발현 벡터.
기술방안 17. 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드, 또는 기술방안 15 또는 16에 따른 재조합 발현 벡터를 포함하는 숙주 세포.
기술방안 18. 기술방안 17에 있어서, 인간 배아 신장 세포 HEK293 또는 HEK293 세포에서 변형된 HEK293T, HEK293E, HEK293F; 햄스터 난소 세포 CHO 또는 CHO 세포에서 변형된 CHO-S, CHO-dhfr-, CHO/DG44, ExpiCHO; 대장균 또는 대장균에서 변형된 대장균 BL21, BL21(DE3), Rosetta, Origami; 효모균 또는 효모균에서 변형된 피키아(Pichia) 효모, 사카로마이세스 세레비지애(Saccharomyces cerevisiae), 클루이베로마이세스 락티스(Kluyveromyces lactis), 한세눌라 폴리모르파(Hansenula polymorpha); 곤충 세포 또는 곤충 세포에서 변형된 세포 High5, SF9; 식물 세포; 체세포인 포유동물 유방 세포로부터 선택되는 것인 숙주 세포.
기술방안 19. 기술방안 1 내지 12 중 어느 하나에 따른 헤테로다이머 형태의 이중특이성 항체 또는 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드 또는 기술방안 15 또는 16에 따른 재조합 발현 벡터 또는 기술방안 17 또는 18에 따른 숙주 세포, 및 약학적으로 허용가능한 담체를 포함하는 조성물.
기술방안 20. 기술방안 1 내지 12 중 어느 하나에 따른 헤테로다이머 형태의 이중특이성 항체를 제조하는 방법으로서,
1) 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드 또는 기술방안 15 또는 16에 따른 재조합 발현 벡터를 각각 숙주 세포에서 발현시키는 단계;
2) 상기 숙주 세포에서 각각 발현된 단백질을 환원시키는 단계; 및
3) 환원된 단백질을 혼합하고, 혼합물을 산화시키는 단계를 포함하는 방법.
기술방안 21. 기술방안 20에 있어서, 숙주 세포는 인간 배아 신장 세포 HEK293 또는 HEK293 세포에서 변형된 HEK293T, HEK293F, HEK293F; 햄스터 난소 세포 CHO 또는 CHO 세포에서 변형된 CHO-S, CHO-dhfr-, CHO/DG44, ExpiCHO; 대장균 또는 대장균에서 변형된 대장균 BL21, BL21(DE3), Rosetta, Origami; 효모균 또는 효모균에서 변형된 피키아(Pichia) 효모, 사카로마이세스 세레비지애(Saccharomyces cerevisiae), 클루이베로마이세스 락티스(Kluyveromyces lactis), 한세눌라 폴리모르파(Hansenula polymorpha); 곤충 세포 또는 곤충 세포에서 변형된 세포 High5, SF9; 식물 세포; 체세포인 포유동물 유방 세포로부터 선택되는 것인 방법.
기술방안 22. 기술방안 20 또는 21에 있어서, 환원 단계는 1) 환원제를 첨가하는 단계로서, 상기 환원제는 2-메르캅토에틸아민, 디티오트레이톨, 트리스(2-카르복시에틸)포스핀 또는 다른 화학적 유도체로부터 선택되는 것인 단계; 2) 0.1mM 또는 더 높은 농도에서 디티오트레이톨의 존재 하에 4℃ 조건 하에 환원 반응을 3시간 이상 수행하는 단계; 3) 환원제를 제거하는 단계, 예컨대 탈염에 의해 수행되는 것인 단계를 포함하는 것인 방법.
기술방안 23. 기술방안 20 내지 22 중 어느 하나에 있어서, 산화 단계는 1) 공기 중 산화이며, 산화제를 첨가하는 단계로서, 상기 산화제는 L-데히드로아스코르브산 (L-dehydroascorbic acid) 또는 이의 화학적 유도체로부터 선택되는 것인 단계를 포함하고, 2) 0.5mM 또는 더 높은 농도에서 L-데히드로아스코르브산의 존재 하에 4℃ 조건 하에 산화 반응을 5시간 이상 수행하는 단계를 포함하는 것인 방법.
기술방안 24. 기술방안 20 내지 23 중 어느 하나에 있어서, 분리 및 정제 단계를 더 포함하는 방법.
기술방안 25. 개체의 질병을 예방 및/또는 치료하기 위한 의약의 제조에서, 기술방안 1 내지 12 중 어느 하나에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드 및/또는 기술방안 15 또는 16에 따른 재조합 발현 벡터 및/또는 기술방안 17 또는 18에 따른 숙주 세포 및/또는 기술방안 19에 따른 조성물의 용도.
기술방안 26. 개체의 질병을 예방 및/또는 치료하기 위한 의약으로 사용하기 위한, 기술방안 1 내지 12 중 어느 하나에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드 및/또는 기술방안 15 또는 16에 따른 재조합 발현 벡터 및/또는 기술방안 17 또는 18에 따른 숙주 세포 및/또는 기술방안 19에 따른 조성물.
기술방안 27. 기술방안 1 내지 12 중 어느 하나에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 기술방안 13 또는 14에 따른 단리된 폴리뉴클레오티드 및/또는 기술방안 15 또는 16에 따른 재조합 발현 벡터 및/또는 기술방안 17 또는 18에 따른 숙주 세포 및/또는 기술방안 19에 따른 조성물을 그것이 필요한 개체에게 투여하는 단계를 포함하는 질병을 예방 및/또는 치료하기 위한 방법.
기술방안 28. 기술방안 25에 따른 용도, 기술방안 26에 따른 헤테로다이머 형태의 이중특이성 항체, 단리된 폴리뉴클레오티드, 재조합 발현 벡터, 숙주 세포 또는 조성물, 또는 기술방안 27에 따른 방법에 있어서, 개체는 포유 동물, 바람직하게는, 인간 개체인 것인 용도, 헤테로다이머 형태의 이중특이성 항체, 단리된 폴리뉴클레오티드, 재조합 발현 벡터, 숙주 세포 또는 조성물, 또는 방법.
기술방안 29. 기술방안 25에 따른 용도, 기술방안 26에 따른 헤테로다이머 형태의 이중특이성 항체, 단리된 폴리뉴클레오티드, 재조합 발현 벡터, 숙주 세포 또는 조성물, 또는 기술방안 27에 따른 방법에 있어서, 상기 질병은 하기 종양으로부터 선택되는 것인, 용도, 헤테로다이머 형태의 이중특이성 항체, 단리된 폴리뉴클레오티드, 재조합 발현 벡터, 숙주 세포 또는 조성물, 또는 방법: 백혈병, 림프종, 골수종, 뇌종양, 두경부 편평세포암종, 비소세포 폐암, 비인두암종, 식도암, 위암, 췌장암, 담낭암, 간암, 대장암, 유방암, 난소암, 자궁경부암, 자궁내막암, 자궁육종, 전립선암, 방광암, 신장암, 흑색종, 소세포폐암, 골암.
이하, 하기의 비제한적인 실시예들을 통해 본 발명을 더 상세하게 설명할 것이다. 당업자라면 본 발명의 사상을 벗어나지 않으면서 본 발명에 대하여 다양한 변형이 이루어질 수 있음을 잘 이해할 것이며, 이러한 변형도 또한 본 발명의 범위 내에 속한다.
달리 명시되지 않는 한, 하기 실험 방법은 모두 일반적인 방법들이다. 사용된 실험 재료는 달리 명시되지 않는 한 상업적 회사로부터 쉽게 얻을 수 있을 것이다. 본 발명의 하기와 같은 실시예에서 사용된 항체는 모두 상업적 경로로 수득되는 표준 항체이다.
실시예 1: 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 벡터 구축
항 인간 PD-L1 항체의 중쇄 및 경쇄를 각각 포함하는 X0GC 발현 벡터를 구축하였으며, 여기에서 항체 가변 영역의 서열은 http://www.imgt.org/mAb-DB/mAbcard?AbId=472에서 유래하였고, 중쇄 불변 영역은 인간 IgG1 (Fc1, 여기에서 N297A 돌연변이가 도입되어 ADCC/CDC 효과를 제거함)이었다. 경쇄 가변 영역의 뉴클레오티드 서열은 서열번호 1로 표시되고, 그의 아미노산 서열은 서열번호 2로 표시되며; 경쇄 불변 영역의 뉴클레오티드 서열은 서열번호 3으로 표시되고, 그의 아미노산 서열은 서열번호 4로 표시되고; 중쇄 가변 영역의 뉴클레오티드 서열은 서열번호 5로 표시되고, 그의 아미노산 서열은 서열번호 6으로 표시되고; 중쇄 불변 영역의 뉴클레오티드 서열은 서열번호 7로 표시되고, 그의 아미노산 서열은 서열번호 8로 표시된다. 경쇄 가변 영역 및 경쇄 불변 영역, 중쇄 가변 영역 및 중쇄 불변 영역을 각각 PCR 방법으로 증폭시켰다. NEB, Inc.의 Phusion 고충실도(High-Fidelity) DNA 폴리머라제 (F-530L)가 본 출원의 모든 PCR 반응에 사용되었다. PCR 프라이머는 염기 상보성의 원리 및 효소 절단 부위의 필요에 따라 통상적으로 설계되었다. 모든 반응 시스템은, H2O 8.9 μl, 5×Phusion 고충실도 DNA 폴리머라제 버퍼 4 μl, 1 mM dNTP 4 μl, 상류(upstream) 프라이머 1 μl, 하류(downstream) 프라이머 1 μl, Phusion 고충실도 DNA 폴리머라제 0.1 μl, 및 주형 1 μl이었다. 가변 영역 및 불변 영역의 PCR 산물을 1.5% 아가로스 겔전기영동법(agarose gel electrophoresis)을 실시하고, DNA 회수 키트 (Promega, A9282, 이하 동일)를 사용하여 상응하는 단편을 회수하였다. 회수된 가변 영역 단편 및 불변 영역 단편을 주형으로 하여, 가변 영역의 상류 프라이머 및 불변 영역의 하류 프라이머를 사용하여 추가 PCR 반응을 수행하였고, 이어서, 상응하는 단편을 회수하여 경쇄 또는 중쇄의 전장 단편을 수득하였다. X0GC 벡터 및 전장 단편을 EcoRI (NEB, 품번 R3101L) 및 HindIIII (NEB, 품번 R3104L)로 효소 분해하였고, 효소 분해 반응 시스템은, 10×버퍼 3 2 μl, EcoRI 및 HindIII 각 0.5 μl, 겔로부터 회수된 전장 단편 3 μl, 및 H2O 14.5 μl였다. 효소 분해 시스템을 37℃에서 3시간 동안 반응시켰다. 효소 분해 생성물을 T4 DNA 리가아제(NEB, 품번 M0202V)로 라이게이션시켰고(이하 동일), 상기 반응 시스템은 10×리가아제 버퍼 2μl, 리가아제 0.5 μl, 겔로부터 전장 단편 3 μl, 겔로부터 회수된 X0GC 벡터 3 μl, 및 H2O 11.5 μl였다. 라이게이션을 실온에서 12시간 동안 수행하였다. 라이게이션 된 생성물을 대장균 컴피턴트 세포(competent cells) DH5α (Tiangen, CB104, 이하 동일)로 형질전환하였다. 항 인간 PD-L1 항체 중쇄 및 경쇄의 X0GC 발현 벡터를 수득하였고, 이는 각각 진핵 세포에서 항체의 중쇄 (Fc1) 및 경쇄를 발현시키기 위한 것이다.
본 발명은 항 인간 CD47 항체의 중쇄 및 경쇄를 각각 포함하는 X0GC 발현 벡터를 동시에 구축하였고, 여기에서 항체 가변 영역 서열은 WO2016109415A1에서 유래하였다. 경쇄 가변 영역의 뉴클레오티드 서열은 서열번호 9로 표시되고, 그의 아미노산 서열은 서열번호 10으로 표시되며; 경쇄 불변 영역의 뉴클레오티드 서열은 서열번호 3으로 표시되고, 그의 아미노산 서열은 서열번호 4로 표시되고; 중쇄 가변 영역의 뉴클레오티드 서열은 서열번호 11로 표시되고, 그의 아미노산 서열은 서열번호 12로 표시되고; 중쇄 불변 영역의 뉴클레오티드 서열은 서열번호 13으로 표시되고, 그의 아미노산 서열은 서열번호 14로 표시된다. 항 인간 CD47 항체 중쇄 및 경쇄의 X0GC 발현 벡터를 수득하였고, 각각 진핵 세포에서 항체의 중쇄(Fc2) 및 경쇄를 발현하기 위해 사용되었다.
실시예 2: 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 발현
항 인간 PD-L1 항체의 중쇄 및 경쇄를 포함하는 발현 벡터를 각각 293F 세포주 (FreeStyleTM 293-F Cells, 품번 R79007, Invitrogen)로 형질감염(transfection)시켰고, 항 인간 CD47 항체의 중쇄 및 경쇄를 포함하는 발현벡터도 293F 세포에 각각 형질감염시켰다. 형질감염 하루 전 세포에 접종하고, 형질감염 당일에 세포를 원심 분리에 의해 수집하고, 세포를 신선한 FreeStyleTM 293 발현 배지(FreeStyleTM 293 Expression Medium, 품번 12338001, Gibco)에 재현탁시키고, 세포 밀도는 200*105 세포/mL이었다. 형질감염 부피에 따라 플라스미드를 36.67ug/mL의 최종 농도로 첨가하고, 부드럽게 혼합하였다; 다음으로, 선형 PEI (폴리에틸렌이민, 선형, M.W. 25000, 품번 43896, Alfa Aesar)를 55 ug/mL의 최종 농도로 첨가하고 부드럽게 혼합하였다. 그 후, 세포 인큐베이터에 넣고, 진탕기(shaker)에서 120 rpm, 37℃에서 1시간 동안 인큐베이션 하였다. 이어서, 형질감염 부피의 19배 부피의 새로운 배양 배지를 첨가하였다. 120 rpm, 37℃에서 진탕기에서 인큐베이션을 계속하였다. 5-6 일 동안 형질감염된 세포 배양의 상층액(supernatants)을 원심 분리에 의해 수집하였다.
발현양은 ELISA 법으로 측정했다. 크로마토그래피 컬럼을 적용하여 정제하기 전에, 0.2㎛ 필터 막을 통한 여과에 의해 침전물을 제거하였다. 이 단계는 4℃에서 수행되었다.
실시예 3: 항 PD-L1/항 CD47 헤테로다이머 항체 분자 발현 산물의 정제
AKTA Explorer 100 단백질 정제 시스템 (GE Healthcare) 및 rProtein A Sepharose 고속(Fast Flow) 친화성 크로마토그래피 컬럼(16mm I.D., 22ml, GE Healthcare)을 사용하여 4℃에서 정제를 수행하였다. 먼저, 이동상 A (20 mM 인산나트륨 버퍼, 150 mM 염화나트륨, pH 7.4)로 크로마토그래피 컬럼을 평형화시키고, 기준선이 안정화된 후, 상기와 같이 처리된 세포 상층액을 5ml/분의 유속으로 로딩하였고, 로딩 후, 이동상 A로 평형을 수행하였다. 샘플은 각각 항 PD-L1 발현 산물 및 항 CD47 발현 산물이었다. 그 후, 먼저 이동상 B1 (0.5M 아르기닌이 함유된 이동상 A)으로 5 컬럼 부피를 세척하고; 이어서 이동상 B2 (100 mM 시트르산, pH 3.0)으로 5 컬럼 부피 용리하고, 용리 피크, 즉 목적 단백질 피크를 수집하였으며; 상기 용리 단계의 유속은 모두 5 ml/분이었다. 항 PD-L1-Fc1의 용리 피크 크로마토그램은 도 1에 도시되어 있고, 항 CD47-Fc2의 용리 피크는 도 2에 도시되어 있다. 표시된 용리 피크 (표시된 회색 영역)를 수집하고, 1M 아세트산나트륨 용액을 적가하여 pH를 5.0으로 조정하였다.
실시예 4: 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 제조 및 정제
항 PD-L1/항 CD47 헤테로다이머 항체 분자의 구조는 도 3에 도시된 바와 같다.
상기 rProtein A Sepharose Fast Flow (16 mm I.D., 22 ml, GE Healthcare) 방법에서 정제하여 수득한 산물을 시험관내 재조합하여 헤테로다이머를 수득하였다. 먼저, 상기 정제 및 수집된 단백질 용액을 한외여과(ultrafiltration) 농축 튜브를 통한 한외여과에 의해 농축하고(공칭 컷오프 분자량 10kDa), 그 용액을 인산염 완충 식염수(phosphate buffer saline, PBS) (pH = 7.4)로 대체시켰다. 수득된 항 PD-L1 및 항 CD47 정제 산물 용액을 각각 상기 PBS를 첨가하여 1 mg/ml로 조정하고, 1/200배 최종 부피의 1M DTT (DTT 최종 농도는 각각 0.1mM, 0.5mM, 1mM, 2mM, 5mM, 10mM, 20mM)를 첨가하고, 4℃에서 환원을 수행하고 (3 내지 8 시간), 환원 과정을 통해 이황화 결합을 파괴하였고, 항 PD-La 및 항 CD47 산물에 함유된 항체 호모다이머 분자의 힌지 영역에서 이황화 결합이 또한 파괴되어, 하나의 중쇄 및 하나의 경쇄를 함유하는 반 항체 분자를 형성하였으며, 그 구조는 도 4에 도시된 바와 같다. 환원된 샘플을 이동상 버퍼에 1mM DTT 환원제를 포함하는 SEC-HPLC (TOSOH, TSK gel super SW3000)로 분석하였고, 그 결과는 도 5에 도시된 바와 같다. 항 PD-L1 및 항 CD47의 호모다이머 분자 비율은 모두 10% 미만이었고, 반 항체 분자 비율은 모두 90% 이상이었다.
그 다음, 환원된 항 PD-L1 및 항 CD47 반 항체 분자를 등몰(equimolar) 비로 혼합하고, 4℃에서 재조합 반응을 수행하고 (0.5 내지 24 시간), 재조합 과정 중에, 항 PD-L1 및 항 CD47 반 항체 분자는 CH2 및 CH3 간의 비공유 작용력을 통해 항 PD-L1 및 항 CD47 반 항체 분자를 동시에 함유하는 헤테로다이머의 이중특이성 항체를 형성하였다. 그 후, 단백질 용액을 한외여과 농축 튜브를 통한 한외여과에 의해 농축시키고 (공칭 컷오프 분자량 10KDa), 그 용액을 인산염 완충 식염수(PBS, pH=7.4)로 대체하여 환원을 중지시켰다. 공기 중에서 또는 산화제로 산화 반응을 수행하여, 헤테로다이머 이중특이성 항체의 이황화 결합의 재형성을 가능하도록 하였다. 산화 반응의 조건은 공기 중에서 샘플을 1일, 3일, 4일 동안 두고, 산화제 100mM L-데히드로아스코르브산(L-dehydroascorbic acid)을 첨가하고 (단백질 최종 농도 1mg/ml, 산화제 최종 농도 0.5mM, 1mM, 5mM, 10mM) 4℃에서 산화를 수행하는 것을 포함하였고, 반응은 24시간 동안 수행하였다.
상기 항 PD-L1 및 항 CD47 발현 산물의 환원 및 산화에 의해 수득된 항 PD-L1/항 CD47 헤테로다이머 항체 분자는 한외여과 농축 튜브를 통한 한외여과에 의해 농축시켰고 (공칭 컷오프 분자량 10KDa), 그 용액은 10 mM 인산나트륨 완충액, pH 5.8로 대체시켰다. AKTA Explorer 100 Protein Purification 시스템(GE Healthcare) 및 이온 크로마토그래피 컬럼 소스 15S(16mm I.D., 17ml, GE Healthcare)를 사용하여 4℃에서 정제를 수행하였다. 먼저, 이동상 A (10 mM 인산나트륨, pH 7.0)로 크로마토그래피 컬럼을 평형화시키고, 기준선이 안정화된 후, 상기와 같이 처리된 단백질 용액을 3ml/분의 유속으로 로딩하였고, 로딩 후, 이동상 A로 평형을 수행하였다. 그 후, A (10 mM 인산나트륨, pH 5.8)에서 B (10 mM 인산나트륨, pH 5.8) 의 구배에서 20 컬럼 부피로 용리시키고 (0% B-100% B, 170분, 유속 2ml/분), 주요 용리 피크를 수집하고, 수집된 단백질 용액을 한외여과 농축 튜브를 통한 한외여과에 의해 농축하였고 (공칭 컷오프 분자량 10 KDa), 용액을 인산염 완충 식염수 (PBS, pH = 7.4)로 대체하고, 여과로 멸균하고, 4℃에서 저장하였다. 정제 생성물을 SEC-HPLC를 통해 순도 분석을 수행하였고, 그 결과는 도 6에 도시된 바와 같다. 순도는 99.3%였다; RPC-HPLC (Thermo Fisher, MAbPac RP) 분석을 수행하였고, 그 결과는 도 7에 도시된 바와 같다. 순도는 100%였다; CD 분석을 수행하였고, 그 결과는 도 8에 도시된 바와 같다. 순도는 97.1%였다.
실시예 5: 항 PD-L1/항 CD47 헤테로다이머 항체 분자의 표적-결합 활성
효소-결합 면역흡착 분석(enzyme-linked immunosorbent assay, ELISA)을 사용하여 항 PD-L1/항 CD47 헤테로다이머 항체의 단일 항원에 대한 결합 능력을 측정하였다.
ELISA의 구체적인 실시 과정은 다음과 같다: pH=9.6의 탄산염 완충용액 (0.05M)을 사용하여 96-웰 고흡수성 ELISA 플레이트 (Costar, 품번 42592) 상에 재조합 인간 PD-L1 (Beijing Sino Biological Inc., 품번 10377-H08H) 또는 인간 CD47 (Beijing ACROBiosystems, 품번 CD7-H5227)을 코팅하였고, 코팅 농도는 1㎍/mL이었으며, 웰당 100μL이었고, 코팅은 4℃에서 밤새 수행하였다. PBST로 5회 세척하였다. 1% BSA를 함유하는 PBST를 사용하여 300μL/웰로 차단하고, 25℃에서 1시간 동안 인큐베이션하였다. PBST로 5회 세척하였다. 1% BSA를 함유하는 PBST로 계열 희석된 헤테로다이머 항체 샘플 및 대조군을 웰당 100μL로 첨가하고, 25℃에서 1시간 동안 인큐베이션 하였다. PBST로 5회 세척하였다. 이어서, 1% BSA를 함유하는 PBST로 1:10000으로 희석된 홀스래디쉬 퍼옥시다제 표지된 항 인간 IgG 항체 (Chemicon, 품번. AP309P)를 웰당 100 μL로 첨가하고, 25℃에서 1시간 동안 인큐베이션 하였다. PBST로 5회 세척하였다. 비색 기질(colorimetric substrate) TMB를 100μL/웰로 첨가하고, 실온에서 10분 동안 전개시켰다. 1M H2SO4를 100μL/웰로 첨가하여 발색(Color development)을 종결시켰다. 450nm에서의 흡광도를 마이크로플레이트 리더기에서 독출하였다.
도 9의 A에 도시된 결과와 같이, 항 PD-L1/항 CD47 헤테로다이머 항체는 PD-L1에 대한 높은 친화도를 가지며, 이는 PD-L1 2가 단일클론 항체의 항원 결합 활성에 필적하였고; 도 9의 B에 도시된 결과와 같이, 항 PD-L1/항 CD47 헤테로다이머 항체는 CD47에 대한 높은 친화도를 가지며, 이는 CD47 2가 단일클론 항체의 항원 결합 활성에 필적한다.
실시예 6: 항 PD-L1/항 CD47 헤테로다이머 항체의 이중 표적 동시 결합 활성
효소-결합 면역흡착 분석(enzyme-linked immunosorbent assay, ELISA)을 사용하여 항 PD-L1/항 CD47 헤테로다이머 항체의 두 개의 다른 항원에 대한 동시 결합 능력을 측정하였다.
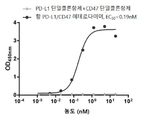
ELISA의 구체적인 실시 과정은 다음과 같다: pH=9.6의 탄산염 완충용액을 사용하여 96-웰 고흡수성 ELISA 플레이트 (Costar, 품번 42592) 상에 재조합 인간 CD47 (Beijing ACROBiosystems, 품번 CD7-H5227)을 코팅하였고, 코팅 농도는 1㎍/mL이었으며, 웰당 100μL이었고, 코팅은 4℃에서 밤새 수행하였다. PBST로 5회 세척하였다. 1% BSA를 함유하는 PBST를 사용하여 300μL/웰로 차단하고, 25℃에서 1시간 동안 인큐베이션하였다. PBST로 5회 세척하였다. 1% BSA를 함유하는 PBST로 계열 희석된 헤테로다이머 항체 샘플 및 대조군을 웰당 100μL로 첨가하고, 25℃에서 1시간 동안 인큐베이션 하였다. PBST로 5회 세척하였다. 이어서, 1% BSA를 함유하는 PBST로 희석된 비오틴 표지된 PD-1-Fc (북경한미약품), 0.5 μg/mL를 웰당 100 μL로 첨가하고, 25℃에서 1시간 동안 인큐베이션 하였다. 1% BSA를 함유하는 PBST로 1:1000으로 희석된 스트렙타비딘-홀스래디쉬 퍼옥시다제 컨쥬게이트 (BD Pharmingen, 품번 554066)를 웰당 100μL로 첨가하고, 25℃에서 1시간 동안 인큐베이션 하였다. PBST로 5회 세척하였다. 비색 기질 TMB를 100μL/웰로 첨가하고, 실온에서 10분 동안 전개시켰다. 1M H2SO4를 100μL/웰로 첨가하여 발색(Color development)을 종결시켰다. 450nm에서의 흡광도를 마이크로플레이트 리더기에서 독출하였다.
도 10에 도시된 결과와 같이, PD-L1 단일 항체 및 CD47의 조합은 PD-L1, CD47에 동시에 결합할 수 없고, 항 PD-L1/항 CD47 헤테로다이머 항체만이 2가지 항원에 동시에 결합하는 활성을 가졌다.
실시예 7: 항 PD-L1/항 CD47 헤테로다이머 항체의 종양세포/적혈구에의 결합
HCC877 종양세포는 PD-L1 및 CD47을 발현하며, 적혈구 (red blood cells, RBC)는 CD47만을 발현한다. HCC827 및 RBC를 혼합하고, 유세포분석(flow cytometry, FCM)을 사용하여 헤테로다이머가 혼합된 세포에서 두 세포의 결합에 대해 선택성이 있는지를 검출하였다.
이 방법의 구체적 실시 과정은 다음과 같다: HCC827 세포 (ATCC로부터 구입함) 및 RBC 세포 (건강한 사람으로부터 수집함)를 수집였다. 2% FBS (Hyclone, 품번 SH30084.03)를 함유하는 차가운 PBS (GIBCO, 품번 14190-235)로 1회 세척하였다. HCC827은 1×106 세포/튜브로, RBC는 10×106 세포/튜브로 혼합하였고, 2% FBS를 함유하는 200 μL 차가운 DPBS (GIBCO, 품번 14190-235)에 재현탁시키고, 각각 연속적으로 희석된 헤테로다이머 항체 샘플 및 대조군을 첨가하였다. 유세포분석 튜브를 아이스에서 30분 동안 인큐베이션하였다. 2% FBS를 함유하는 PBS로 2회 세척하였다. 2% FBS 및 1:1000으로 희석된 FITC-표지된 항-인간 IgG 항체 (Beijing Zhongshan Goldenbridge, 품번 ZF0306)를 함유하는 200 μL의 차가운 PBS에 다시 재현탁시켰다. 아이스에서 30분 동안 암흑에서 인큐베이션 하였다. 2% FBS를 함유하는 PBS로 2회 세척하였다. 500 μL 차가운 PBS에 재현탁시키고, 세포 현탁액을 유세포분석기 (BD, FACS, Calibur)로 검출 및 분석하였고, 혼합된 세포에서 두 세포 각각의 형광 강도를 판독하였다.
도 11에 도시된 결과와 같이, CD47 단일클론항체의 혼합된 HCC827 및 RBC와의 결합은 기본적으로 차이가 없었으나(A); 항 PD-L1/항 CD47 헤테로다이머는 PD-L1 및 CD47을 발현하는 HCC827 세포에 결합하는 경향을 가진 반면 CD47만을 발현하는 RBC에는 약하게 결합하여, 결합의 선택성을 보여주었다(B).
실시예 8: 항 PD-L1/항 CD47 헤테로다이머 항체의 T 세포 조절 활성
혼합 림프구 반응(mixed lymphocyte reaction: MLR)을 사용하여 항 PD-L1/항 CD47 헤테로다이머 항체의 T 세포 면역 반응에 대한 조절 활성을 측정하였다.
인간 수지상 세포(dendritic cells: DC)의 획득: 인간 PBMC 세포(Lonza, 품번 CC-2702)를 해동하여 수집하였다. 인간 PBMC 세포를 5×106/mL의 세포 밀도로 무혈청 RPMI 1640 배지 (GIBCO, 품번 22400-089)에 재현탁시키고, 세포 인큐베이션 플라스크에 접종하고, 37℃에서 90분 동안 CO2 인큐베이터에서 인큐베이션 하였다. 인큐베이션 상층액 및 현탁 세포를 버리고, 부착성 세포들을 완전 배지(10% FBS를 함유한 RPM 1640)에서 배양하고, 100ng/ml GM-CSF (Beijing Sino Biological Inc., 품번 10015-HNAH) 및 100ng/ml IL-4 (Beijing Sino Biological Inc., 품번 11846-HNAE)를 첨가하였다. 3일 동안 인큐베이션한 후, 그 배지를 교체하고, 추가로 3일 동안 인큐베이션 하였다. 이어서, 배양 배지를 100ng/ml GM-CSF, 100ng/ml IL-4 및 20ng/ml TNF-α를 함유하는 완전 배지 (10% FBS를 함유하는 RPMI 1640)로 교체하고, 1일 동안 인큐베이션 하였다. 그에 의해 DC 세포를 수득하였다.
인간 T 세포의 획득: 인간 PBMC 세포를 해동하여 수집하고, 그 PBMC와 DC 세포를 유도하는 PBMC는 상이한 개체로부터 유래되었음을 보장하였다. Pan T 세포 분리 키트(Miltenyi Biotech, 품번 5150414820) 사용설명서의 지시에 따라 인간 T 세포를 분리하였다. 간단하게, 먼저 PBMC를 PBS로 1회 세척하고, PBMC를 40 μL 분리 완충액 (2 mM EDTA, 0.5% BSA를 함유하는 PBS, pH = 7.2) 당 107 세포(이하, 양은 모두 107세포에서 계산되었음)에 재현탁시키고, 10 μL Pan T 셀 비오틴 항체 칵테일(Pan T 세포 비오틴 항체 혼합물)을 첨가하고, 4℃에서 5분 동안 인큐베이션 하였다. 그 후, 30 μL 분리 완충액 및 20 μL Pan T 세포 마이크로비드 칵테일(Pan T 세포 마이크로비드 혼합물)을 첨가하고, 4℃에서 10분 동안 인큐베이션 하였다. MACS 분리 컬럼을 통해 T 세포를 수득하였다.
수집된 인간 DC 세포 및 인간 T 세포를 완전 배지(10% FBS를 함유하는 RPM 1640)에 재현탁시키고, 96-웰 플레이트에 접종하였고, 접종된 DC 세포 및 T 세포는 각각 1×104/웰 및 1×105/웰이고, 혼합 배양하였다. 완전한 배지에 계열 희석된 헤테로다이머 항체의 샘플 및 대조군을 첨가하였다. 인큐베이션 플레이트를 37℃에서 CO2 인큐베이터에 두고 5일 동안 인큐베이션하였다. 인큐베이션이 완료된 후, 웰에서 상층액을 취하고, 키트 매뉴얼에 따라 사이토카인 IFN-γ (Ray Biotech, 품번 ELH-IFNg)를 검출하였다.
도 12에 도시된 바와 같이, 인간 T 세포는 동종이계(allogeneic) DC 세포의 자극 하에 IFN-γ의 분비를 활성화시킬 수 있다. PD-L1 항체의 첨가는 T 세포의 활성화를 증가시키고, 사이토카인의 분비를 촉진할 수 있다. 항 PD-L1/항 CD47 헤테로다이머 항체도 더욱 강한 T 세포 조절 활성을 나타냈으며, 사이토카인 IFN-γ의 분비를 현저히 촉진시킨다.
실시예 9: 항 PD-L1/항 CD47 헤테로다이머 항체 매개된 대식세포의 종양세포에 대한 식세포 활성
성숙 인간 대식세포의 제조: 인간 PBMC 세포 (Lonza, 품번 CC-2702)를 소생 해동하여 수집하였다. 인간 PBMC 세포를 무혈청 RPMI 1640 배지에 5×106/mL의 세포 밀도로 재현탁시키고, 세포 배양 플라스크에 접종하고, 37℃ CO2 인큐베이터에서 90분 동안 인큐베이션 하였다. 배양 상층액 및 현탁된 세포를 버리고, 부착된 세포를 완전 배지 (10% FBS를 함유하는 RPMI 1640)에서 배양하고, 25ng/mL M-CSF (Beijing Sino Biological Inc., 품번 10015-HNAH)를 첨가하여, 7일 동안 인큐베이션 하였다. 이어서, 대식세포를 수집하고 25ng/mL M-CSF 및 50ng/mL IFN-γ (Beijing Sino Biological Inc., 품번 11725-HNAS)를 함유하는 완전 배지 (10% FBS를 함유하는 RPMI 1640)에서 재현탁시켰다. 세포 현탁액을 48-웰 세포 배양 플레이트에 웰당 50000개 세포로 접종하고, 1일 동안 인큐베이션 하여 대식세포가 성숙되어 사용할 수 있도록 준비하였다.
CFSE 키트 (Life Technology, 품번 C34554)의 사용설명서에 따라 Raji 종양 세포를 염색하였다. 간단하게, PBS를 사용하여 CFSE를 5 μM의 작업 농도로 희석하고, 37℃에서 사전 가열 후, 1000 rpm으로 5분 동안 원심분리하여 Raji 세포를 수집하고, 사전 가열한 CFSE 작업 용액으로 Raji를 재현탁시킨 후, 37℃에서 15분 동안 인큐베이션 하였다. 세포를 완전 배지로 1회 세척하고, 완전 배지에서 재현탁시키고, 30분 동안 인큐베이션 하고, 완전 배지로 2회 세척한 다음, 사용을 위해 완전 배지에서 재현탁시켰다.
48-웰 플레이트를 완전 배지로 3회 세척하였다. CFSE-염색된 Raji 세포를 테스트될 헤테로다이머 샘플 및 대조군과 15분 동안 사전 인큐베이션 하고, 이어서 48-웰 배양 플레이트에 첨가하고, 37℃ CO2 인큐베이터에서 2시간 동안 인큐베이션 하였다. 인큐베이션 종료 후에, 48-웰 플레이트를 완전 배지로 3회 세척하였고, 완전 배지에 희석된 wheat germ agglutinin, alexa fluor 555 (Life technologies, 번호 W32464) 10 μg/mL를 첨가하고, 암흑에서 15분 동안 인큐베이션 하였다. 48-웰 플레이트를 다시 완전 배지로 3회 세척하고, 4% 파라포름알데히드를 첨가하여 15분 동안 고정시켰다. 48-웰 플레이트를 다시 완전 배지로 3회 세척하고, 완전 배지를 첨가하였다. 형광 현미경으로 사진을 찍어서 세포 수를 세었다. 식균 지수(%)의 계산 방법은 다음과 같다: 식균 녹색-표지된 Raji 세포의 수/존재하는 적색-표지된 대식세포의 수 × 100.
도 13에 도시된 바와 같이, 항 PD-L1/항 CD47 헤테로다이머 항체는 대식세포를 매개하여 Raji 종양 세포를 식세포 작용할 수 있으며, 이는 CD47 단일클론항체의 활성에 필적한다.
SEQUENCE LISTING
<110> BEIJING HANMEI PHARMACEUTICAL CO., LTD.
<120> ANTI-PD-L1/ANTI-CD47 BISPECIFIC ANTIBODY WITH STRUCTURE LIKE
NATURAL ANTIBODY AND IN FORM OF HETERODIMER AND PREPARATION
THEREOF
<130> LZ1707727CN01
<160> 14
<170> PatentIn version 3.5
<210> 1
<211> 321
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of light chain variable region of anti-human
PD-L1 antibody
<400> 1
gacatccaga tgacccagag ccctagcagc ctgagcgcta gcgtgggcga cagggtgacc 60
atcacctgca gggccagcca ggatgtgagc accgctgtgg cctggtatca acagaagccc 120
ggcaaggccc ccaagctgct gatctacagc gccagcttcc tgtacagcgg cgtgcccagc 180
agatttagcg gcagcggcag cggcaccgat ttcaccctga ccatcagcag cctgcagccc 240
gaggacttcg ccacctacta ctgccagcag tacctgtacc atcccgccac cttcggccag 300
ggcaccaagg tggagatcaa g 321
<210> 2
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of light chain variable region of anti-human
PD-L1 antibody
<400> 2
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Tyr His Pro Ala
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 3
<211> 321
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of light chain constant region of anti-human
PD-L1 antibody
<400> 3
cgaactgtgg ccgctccaag cgtcttcatt tttccaccct ctgacgaaca gctgaagtca 60
gggacagctt ccgtggtctg tctgctgaac aatttttacc ccagggaggc caaagtgcag 120
tggaaggtcg ataacgctct gcagagcgga aattctcagg agagtgtgac agaacaggac 180
tcaaaagatt ccacttatag cctgtctagt accctgacac tgtccaaggc agactacgaa 240
aagcataaag tgtatgcctg tgaggtcaca catcagggtc tgtcaagccc cgtcactaag 300
tccttcaatc gtggcgaatg c 321
<210> 4
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of light chain constant region of anti-human
PD-L1 antibody
<400> 4
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 5
<211> 354
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of heavy chain variable region of anti-human
PD-L1 antibody
<400> 5
gaggtgcagc tggtggagag cggaggagga ctggtgcagc ctggaggatc cctgagactg 60
agctgcgccg ccagcggctt caccttcagc gacagctgga tccactgggt gagacaggcc 120
cctggcaagg gcctggaatg ggtggcctgg atctcccctt acggcggcag cacctactac 180
gccgacagcg tgaagggcag gttcaccatc agcgccgaca ccagcaagaa caccgcctac 240
ctgcagatga acagcctgag ggccgaggac accgccgtgt actactgcgc cagaagacac 300
tggcccggcg gattcgacta ctggggacag ggcaccctgg tgaccgtgag cgcc 354
<210> 6
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of heavy chain variable region of anti-human
PD-L1 antibody
<400> 6
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 7
<211> 990
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of heavy chain constant region of anti-
PD-L1 antibody
<400> 7
gcttcaacaa aaggaccttc cgtgtttcca ctggcaccct ctagtaagag tacttcagga 60
ggaaccgcag cactgggatg tctggtgaag gactacttcc cagagcccgt caccgtgtct 120
tggaacagtg gagcactgac ctccggggtc catacatttc ctgccgtgct gcagtcatcc 180
ggtctgtata gcctgagctc tgtggtcaca gtcccaagtt catccctggg cacccagaca 240
tacatctgca acgtgaatca caaaccttcc aatactaagg tcgacaagaa agtggaaccc 300
aagtcctgcg ataagaccca cacatgccct ccctgtcctg ctcccgaact gctgggagga 360
ccctccgtct tcctgttccc ccccaagccc aaagacacac tgatgatcag caggacccct 420
gaagtgacct gcgtggtcgt ggacgtgagc cacgaggacc ccgaggtcaa gtttaactgg 480
tacgtggacg gcgtggaggt ccacaacgcc aagaccaagc ccagggagga gcagtacgcc 540
agcacctaca gggtcgtgtc cgtgctgacc gtgctccacc aagattggct caacggcaag 600
gagtataagt gcaaagtcag caacaaggcc ctccccgccc ccatcgagaa aaccatcagc 660
aaggccaagg gccaaccgcg ggaacctcaa gtgtataccc tccctcccag ccgggatgag 720
ctgaccaaga accaagtctc cctcttgtgc ctggtcaagg gattctaccc ttccgacatt 780
gccgtcgaat gggagagcaa tggccagccc gagaacaact acaagacaac cccccccgtc 840
ctgcgcagcg acggatcctt cttcctgtac tccaagctca ccgtggacaa gagccggtgg 900
caacagggca acgtgttctc ctgtagcgtg atgcacgaag ccctccacaa ccactatacc 960
cagaagagcc tgagcctcag ccccggcaaa 990
<210> 8
<211> 330
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of heavy chain constant region of anti-
PD-L1 antibody
<400> 8
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Leu Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Arg Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 9
<211> 321
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of light chain variable region of anti-human
CD47 antibody
<400> 9
aacatccaga tgacccagtc cccttccgcc atgagcgctt ccgtgggcga cagggtgacc 60
atcacatgca aggcctccca ggacatccac cgttatttaa gctggtttca gcagaagccc 120
ggcaaggtgc ccaagcacct gatctacagg gctaacaggc tggtgtccgg cgtgccttcc 180
aggttttccg gcagcggttc tggcaccgag tttaccctga ccatctcctc cctgcagccc 240
gaggacttcg ccacctacta ctgcctgcag tacgacgagt tcccctacac cttcggcggc 300
ggcaccaagg tggagatcaa g 321
<210> 10
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of light chain variable region of anti-human
CD47 antibody
<400> 10
Asn Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile His Arg Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys His Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 11
<211> 360
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of heavy chain variable region of anti-human
CD47 antibody
<400> 11
cagatgcagc tggtgcagtc cggcgccgag gtgaaaaagc ccggctcctc cgtgaaggtg 60
tcctgcaagg ccagcggctt caacatcaag gactactacc tgcactgggt gaggcaggct 120
cccggacagg ctctggagtg gatgggctgg atcgaccccg accagggcga taccgagtac 180
gcccagaagt tccagggccg ggtgacaatc accagggaca ggagcacctc caccgcctac 240
atggagctga ggtccctgag gtccgaggac accgccgtgt actactgcaa cgccgcttac 300
ggcagcagct cctaccccat ggactactgg ggccagggca caaccgtgac cgtgagctcc 360
<210> 12
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of heavy chain variable region of anti-human
CD47 antibody
<400> 12
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Leu His Trp Val Arg Gln Ala Pro Gly Gln Ala Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Asp Gln Gly Asp Thr Glu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Arg Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Asn Ala Ala Tyr Gly Ser Ser Ser Tyr Pro Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 13
<211> 990
<212> DNA
<213> Artificial Sequence
<220>
<223> nucleotide sequence of heavy chain constant region of anti-human
CD47 antibody
<400> 13
gctagcacaa aaggaccttc cgtgtttcca ctggcaccct ctagtaagag tacttcagga 60
ggaaccgcag cactgggatg tctggtgaag gactacttcc cagagcccgt caccgtgtct 120
tggaacagtg gagcactgac ctccggggtc catacatttc ctgccgtgct gcagtcatcc 180
ggtctgtata gcctgagctc tgtggtcaca gtcccaagtt catccctggg cacccagaca 240
tacatctgca acgtgaatca caaaccttcc aatactaagg tcgacaagaa agtggaaccc 300
aagtcctgcg ataagaccca cacatgccct ccctgtcctg ctcccgaact gctgggagga 360
ccctccgtct tcctgttccc ccccaagccc aaagacacac tgatgatcag caggacccct 420
gaagtgacct gcgtggtcgt ggacgtgagc cacgaggacc ccgaggtcaa gtttaactgg 480
tacgtggacg gcgtggaggt ccacaacgcc aagaccaagc ccagggagga gcagtacgcc 540
agcacctaca gggtggtcag cgtgctgacc gtgctgcacc aggattggct caacggcaag 600
gagtacaagt gcaaagtctc caacaaggcc ctgcccgccc ccatcgagaa gaccatctcc 660
aaggctaagg gacagcccag ggagccccaa gtgtacaccg agcctcccag ccgggatgag 720
ctgaccaaga accaagtctc cctcacctgc ctggtcaagg gattctaccc ttccgacatt 780
gccgtcgaat gggagagcaa tggccagccc gagaacaact acaagacaac cccccccgtc 840
ctggatagcg acggatcctt cttcctgctc tccgtgctca ccgtcgacaa gagcagatgg 900
cagcagggca acgtgttcag ctgtagcgtg atgcacgagg ccctgcacaa ccactacacc 960
cagaagagcc tgtccctcag ccccggcaag 990
<210> 14
<211> 330
<212> PRT
<213> Artificial Sequence
<220>
<223> amino acid sequence of heavy chain constant region of anti-human
CD47 antibody
<400> 14
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Glu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Leu Ser Val Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
Claims (34)
- 제1 Fc 사슬 및 제2 Fc 사슬, 및 PD-L1과 특이적으로 결합할 수 있는 제1 항원-결합 기능 영역 및 CD47과 특이적으로 결합할 수 있는 제2 항원-결합 기능 영역을 포함하고;
상기 제1 Fc 사슬 및 제2 Fc 사슬은 모두 아미노산 치환을 포함하는 면역글로불린 G Fc 단편이고, 상기 제1 Fc 사슬 및 제2 Fc 사슬은 함께 Fc 수용체에 결합할 수 있는 헤테로다이머를 구성하고;
상기 제1 Fc 사슬 및 제2 Fc 사슬은 공유 결합 또는 링커를 통해 각각 상기 제1 항원-결합 기능 영역 및 제2 항원-결합 기능 영역에 연결되고;
상기 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나는 위치 366 및 위치 399에서 아미노산 치환을 포함하고, 다른 하나는 위치 351, 위치 407 및 위치 409에서 아미노산 치환을 포함하고, 상기 아미노산 위치는 카바트(Kabat) EU 인덱스 넘버링 시스템에 따라 번호가 지정되는 것인,
헤테로다이머 형태의 이중특이성 항체. - 청구항 1에 있어서, 제1 Fc 사슬 및 제2 Fc 사슬 아미노산 치환은 하기와 같은 것인 헤테로다이머 형태의 이중특이성 항체:
a) L351G, L351Y, L351V, L351P, L351D, L351E, L351K 또는 L351W;
b) T366L, T366P, T366W 또는 T366V;
c) D399C, D399N, D399I, D399G, D399R, D399T 또는 D399A;
d) Y407L, Y407A, Y407P, Y407F, Y407T 또는 Y407H; 및
e) K409C, K409P, K409S, K409F, K409V, K409Q 또는 K409R. - 청구항 1 또는 2에 있어서, 아미노산 치환은 하기를 포함하는 것인 헤테로다이머 형태의 이중특이성 항체:
a) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399R 치환, 다른 하나에서 L351E, Y407L 및 K409V 치환;
b) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399C 치환, 다른 하나에서 L351G, Y407L 및 K409C 치환;
c) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399C 치환, 다른 하나에서 L351Y, Y407A 및 K409P 치환;
d) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 D399N 치환, 다른 하나에서 L351V, Y407P 및 K409S 치환;
e) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366W 및 D399G 치환, 다른 하나에서 L351D, Y407P 및 K409S 치환;
f) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 D399I 치환, 다른 하나에서 L351P, Y407F 및 K409F 치환;
g) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366V 및 D399T 치환, 다른 하나에서 L351K, Y407T 및 K409Q 치환;
h) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 D399A 치환, 다른 하나에서 L351W, Y407H 및 K409R 치환. - 청구항 1 내지 3 중 어느 한 항에 있어서, 아미노산 치환은 하기를 포함하는 것인 헤테로다이머 형태의 이중특이성 항체:
a) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409V 치환, 다른 하나에서 L351E, Y407L 및 D399R 치환;
b) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409C 치환, 다른 하나에서 L351G, Y407L 및 D399C 치환;
c) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409P 치환, 다른 하나에서 L351Y, Y407A 및 D399C 치환;
d) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 K409S 치환, 다른 하나에서 L351V, Y407P 및 D399N 치환;
e) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366W 및 K409S 치환, 다른 하나에서 L351D, Y407P 및 D399G 치환;
f) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366P 및 K409F 치환, 다른 하나에서 L351P, Y407F 및 D399I 치환;
g) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366V 및 K409Q 치환, 다른 하나에서 L351K, Y407T 및 D399T 치환;
h) 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나에서 T366L 및 K409R 치환, 다른 하나에서 L351W, Y407H 및 D399A 치환. - 청구항 1 내지 4 중 어느 한 항에 있어서, 제1 Fc 사슬 및 제2 Fc 사슬 중 어느 하나의 아미노산 치환은 T366L 및 D399R이고, 다른 하나의 아미노산 치환은 L351E, Y407L 및 K409V인 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 5 중 어느 한 항에 있어서, 제1 항원-결합 기능 영역 및 제2 항원-결합 기능 영역은 Fab 단편, scFv 단편, 가변 도메인 단편 Fv 및 중쇄 항체의 중쇄 가변 영역 단편 VHH로부터 선택되는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 6 중 어느 한 항에 있어서, 제1 항원-결합 기능 영역 및 제2 항원 결합 기능 영역은 모두 Fab 단편인 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 6 중 어느 한 항에 있어서, 제1 항원-결합 기능 영역 및 제2 항원 결합 기능 영역 중 하나는 Fab 단편이고, 다른 하나는 scFv인 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 7에 있어서, 상기 Fab 단편은 상이한 제1 중쇄 가변 영역 및 제2 중쇄 가변 영역, 및 상이한 제1 경쇄 가변 영역 및 제2 경쇄 가변 영역을 포함하는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 9 중 어느 한 항에 있어서, 제1 Fc 사슬 및 그에 공유적으로 연결된 제1 항원-결합 기능 영역, 및 제2 Fc 사슬 및 그에 공유적으로 연결된 제2 항원-결합 기능 영역은, 환원제가 존재하는 용액 중에 있고 상기 용액 중에 상기 제1 Fc 사슬 및 그에 공유적으로 연결된 제1 항원-결합 기능 영역과 제2 Fc 사슬 및 그에 공유적으로 연결된 제2 항원-결합 기능 영역 외에 다른 폴리펩티드를 포함하지 않을 때, 모든 폴리펩티드 사슬의 중량을 기준으로 50% 미만의 호모다이머를 형성하는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 10 중 어느 한 항에 있어서, 제1 항원-결합 기능 영역은 서열번호 2 및 6의 아미노산 서열을 포함하는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 10 중 어느 한 항에 있어서, 제2 항원-결합 기능 영역은 서열번호 10 및 12의 아미노산 서열을 포함하는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 11에 있어서, 제1 항원-결합 기능 영역은 서열번호 4 및 8의 아미노산 서열을 더 포함하는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 12에 있어서, 제2 항원-결합 기능 영역은 서열번호 4 및 14의 아미노산 서열을 더 포함하는 것인 헤테로다이머 형태의 이중특이성 항체.
- 청구항 1 내지 14 중 어느 한 항에 따른 헤테로다이머 형태의 이중특이성 항체를 암호화하는 단리된 폴리뉴클레오티드.
- 청구항 15에 있어서, 제1 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 1 및 5를 포함하는 것인 단리된 폴리뉴클레오티드.
- 청구항 15에 있어서, 제2 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 9 및 11을 포함하는 것인 단리된 폴리뉴클레오티드.
- 청구항 16에 있어서, 제1 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 3 및 7을 더 포함하는 것인 단리된 폴리뉴클레오티드.
- 청구항 17에 있어서, 제2 항원-결합 기능 영역의 아미노산을 암호화하는 뉴클레오티드 서열은 서열번호 3 및 13을 더 포함하는 것인 단리된 폴리뉴클레오티드.
- 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드를 포함하는 재조합 발현 벡터.
- 청구항 20에 있어서, 발현 벡터는 pCDNA로부터 변형된 플라스미드 벡터 X0GC인 것인 재조합 발현 벡터.
- 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드, 또는 청구항 20 또는 21에 따른 재조합 발현 벡터를 포함하는 숙주 세포.
- 청구항 22에 있어서, 인간 배아 신장 세포 HEK293 또는 HEK293 세포에서 변형된 HEK293T, HEK293E, HEK293F; 햄스터 난소 세포 CHO 또는 CHO 세포에서 변형된 CHO-S, CHO-dhfr-, CHO/DG44, ExpiCHO; 대장균 또는 대장균에서 변형된 대장균 BL21, BL21(DE3), Rosetta, Origami; 효모균 또는 효모균에서 변형된 피키아(Pichia) 효모, 사카로마이세스 세레비지애(Saccharomyces cerevisiae), 클루이베로마이세스 락티스(Kluyveromyces lactis), 한세눌라 폴리모르파(Hansenula polymorpha); 곤충 세포 또는 곤충 세포에서 변형된 세포 High5, SF9; 식물 세포; 체세포인 포유동물 유방 세포로부터 선택되는 것인 숙주 세포.
- 청구항 1 내지 14 중 어느 한 항에 따른 헤테로다이머 형태의 이중특이성 항체 또는 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드 또는 청구항 20 또는 21에 따른 재조합 발현 벡터 또는 청구항 22 또는 23에 따른 숙주 세포, 및 약학적으로 허용가능한 담체를 포함하는 조성물.
- 청구항 1 내지 14 중 어느 한 항에 따른 헤테로다이머 형태의 이중특이성 항체를 제조하는 방법으로서,
1) 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드 또는 청구항 20 또는 21에 따른 재조합 발현 벡터를 각각 숙주 세포에서 발현시키는 단계;
2) 상기 숙주 세포에서 각각 발현된 단백질을 환원시키는 단계; 및
3) 환원된 단백질을 혼합하고, 혼합물을 산화시키는 단계를 포함하는 방법. - 청구항 25에 있어서, 숙주 세포는 인간 배아 신장 세포 HEK293 또는 HEK293 세포에서 변형된 HEK293T, HEK293F, HEK293F; 햄스터 난소 세포 CHO 또는 CHO 세포에서 변형된 CHO-S, CHO-dhfr-, CHO/DG44, ExpiCHO; 대장균 또는 대장균에서 변형된 대장균 BL21, BL21(DE3), Rosetta, Origami; 효모균 또는 효모균에서 변형된 피키아(Pichia) 효모, 사카로마이세스 세레비지애(Saccharomyces cerevisiae), 클루이베로마이세스 락티스(Kluyveromyces lactis), 한세눌라 폴리모르파(Hansenula polymorpha); 곤충 세포 또는 곤충 세포에서 변형된 세포 High5, SF9; 식물 세포; 체세포인 포유동물 유방 세포로부터 선택되는 것인 방법.
- 청구항 25 또는 26에 있어서, 환원 단계는 1) 환원제의 존재 하에 환원 반응을 수행하는 단계로서, 상기 환원제는 2-메르캅토에틸아민 (2-mercaptoethylamine), 디티오트레이톨 (dithiothreitol), 트리스(2-카르복시에틸)포스핀 (tris(2-carboxyethyl)phosphine) 또는 다른 화학적 유도체로부터 선택되는 것인 단계; 2) 상기 환원제를 제거하는 단계를 포함하는 것인 방법.
- 청구항 25 내지 27 중 어느 한 항에 있어서, 산화 단계는 공기 중 산화이며, 산화제의 존재 하에 산화 반응을 수행하는 단계로서, 상기 산화제는 L-데히드로아스코르브산 (L-dehydroascorbic acid) 또는 이의 화학적 유도체로부터 선택되는 것인 단계를 포함하는 것인 방법.
- 청구항 25 내지 28 중 어느 한 항에 있어서, 분리 및 정제 단계를 더 포함하는 방법.
- 개체의 질병을 예방 및/또는 치료하기 위한 의약의 제조에서, 청구항 1 내지 14 중 어느 한 항에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드 및/또는 청구항 20 또는 21에 따른 재조합 발현 벡터 및/또는 청구항 22 또는 23에 따른 숙주 세포 및/또는 청구항 24에 따른 조성물의 용도.
- 개체의 질병을 예방 및/또는 치료하기 위한 의약으로 사용하기 위한, 청구항 1 내지 14 중 어느 한 항에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드 및/또는 청구항 20 또는 21에 따른 재조합 발현 벡터 및/또는 청구항 22 또는 23에 따른 숙주 세포 및/또는 청구항 24에 따른 조성물.
- 청구항 1 내지 14 중 어느 한 항에 따른 헤테로다이머 형태의 이중특이성 항체 및/또는 청구항 15 내지 19 중 어느 한 항에 따른 단리된 폴리뉴클레오티드 및/또는 청구항 20 또는 21에 따른 재조합 발현 벡터 및/또는 청구항 22 또는 23에 따른 숙주 세포 및/또는 청구항 24에 따른 조성물을 그것이 필요한 개체에게 투여하는 단계를 포함하는 질병을 예방 및/또는 치료하기 위한 방법.
- 청구항 30, 31 또는 32에 있어서, 개체는 포유 동물, 바람직하게는, 인간인 것인, 용도, 헤테로다이머 형태의 이중특이성 항체, 단리된 폴리뉴클레오티드, 재조합 발현 벡터, 숙주 세포 또는 조성물, 또는 방법.
- 청구항 30, 31 또는 32에 있어서, 상기 질병은 하기 종양으로부터 선택되는 것인, 용도, 헤테로다이머 형태의 이중특이성 항체, 단리된 폴리뉴클레오티드, 재조합 발현 벡터, 숙주 세포 또는 조성물, 또는 방법: 백혈병, 림프종, 골수종, 뇌종양, 두경부 편평세포암종, 비소세포 폐암, 비인두암종, 식도암, 위암, 췌장암, 담낭암, 간암, 대장암, 유방암, 난소암, 자궁경부암, 자궁내막암, 자궁육종, 전립선암, 방광암, 신장암, 흑색종, 소세포폐암, 골암.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201711261880 | 2017-12-04 | ||
| CN201711261880.8 | 2017-12-04 | ||
| PCT/CN2018/118800 WO2019109876A1 (zh) | 2017-12-04 | 2018-12-01 | 抗pd‐l1/抗cd47天然抗体结构样异源二聚体形式双特异抗体及其制备 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200093639A true KR20200093639A (ko) | 2020-08-05 |
Family
ID=66750763
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207019202A KR20200093639A (ko) | 2017-12-04 | 2018-12-01 | 천연 항체 구조-유사 헤테로다이머 형태의 항 pd-l1/항 cd47 이중특이성 항체 및 이의 제조 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US11739151B2 (ko) |
| EP (1) | EP3722322A4 (ko) |
| JP (1) | JP7231641B2 (ko) |
| KR (1) | KR20200093639A (ko) |
| CN (1) | CN111615521A (ko) |
| AU (1) | AU2018378529A1 (ko) |
| BR (1) | BR112020011295A2 (ko) |
| CA (1) | CA3084626A1 (ko) |
| EA (1) | EA202091364A1 (ko) |
| IL (1) | IL275135A (ko) |
| MX (1) | MX2020005792A (ko) |
| SG (1) | SG11202005216XA (ko) |
| WO (1) | WO2019109876A1 (ko) |
| ZA (1) | ZA202003382B (ko) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3035681A1 (en) * | 2016-09-29 | 2018-04-05 | Beijing Hanmi Pharmaceutical Co., Ltd. | Heterodimeric immunoglobulin constructs and preparation methods thereof |
| PE20191080A1 (es) | 2016-11-18 | 2019-08-20 | Beijing Hanmi Pharmaceutical Co Ltd | Anticuerpo biespecifico heterodimerico estructural de anticuerpo natural anti-pd-1/anti-her2 y metodo para preparar el mismo |
| WO2019153200A1 (zh) | 2018-02-08 | 2019-08-15 | 北京韩美药品有限公司 | 抗pd-1/抗her2天然抗体结构样异源二聚体形式双特异抗体及其制备 |
| WO2021124073A1 (en) * | 2019-12-17 | 2021-06-24 | Pfizer Inc. | Antibodies specific for cd47, pd-l1, and uses thereof |
| EP4112647A4 (en) * | 2020-02-28 | 2024-03-27 | Nanjing Sanhome Pharmaceutical Co., Ltd. | ANTI-CD47/ANTI-PD-L1 ANTIBODIES AND ITS USES |
| US10894812B1 (en) | 2020-09-30 | 2021-01-19 | Alpine Roads, Inc. | Recombinant milk proteins |
| US10947552B1 (en) | 2020-09-30 | 2021-03-16 | Alpine Roads, Inc. | Recombinant fusion proteins for producing milk proteins in plants |
| WO2022072718A1 (en) | 2020-09-30 | 2022-04-07 | Nobell Foods, Inc. | Recombinant milk proteins and food compositions comprising the same |
| CN116685348A (zh) * | 2020-10-07 | 2023-09-01 | 细胞基因公司 | 淋巴恶性肿瘤病状的双特异性抗体治疗 |
| WO2022095970A1 (zh) * | 2020-11-06 | 2022-05-12 | 百奥泰生物制药股份有限公司 | 双特异抗体及其应用 |
| EP4253415A4 (en) * | 2020-11-12 | 2024-10-02 | Mabwell Shanghai Bioscience Co Ltd | ANTIBODIES AND MANUFACTURING METHODS THEREFOR |
| CN116670289A (zh) * | 2021-01-08 | 2023-08-29 | 北京韩美药品有限公司 | 抗pd-l1/抗cd47天然抗体结构样异源二聚体形式双特异抗体及其制备 |
| EP4276113A1 (en) * | 2021-01-08 | 2023-11-15 | Beijing Hanmi Pharmaceutical Co., Ltd. | Antibody specifically binding to cd47 and antigen-binding fragment thereof |
| EP4313309A1 (en) * | 2021-03-22 | 2024-02-07 | Novimmune S.A. | Bispecific antibodies targeting cd47 and pd-l1 and methods of use thereof |
| CA3219221A1 (en) * | 2021-05-07 | 2022-11-10 | Immuneoncia Therapeutics, Inc. | Bispecific antibody specifically binding to cd47 and pd-l1 |
| CN115702931A (zh) * | 2021-08-06 | 2023-02-17 | 百奥泰生物制药股份有限公司 | 抗pd-l1/cd47双特异抗体在治疗疾病中的应用 |
| AU2022435471A1 (en) * | 2022-01-18 | 2024-05-30 | Fbd Biologics Limited | Cd47/pd-l1-targeting protein complex and methods of use thereof |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006031994A2 (en) | 2004-09-14 | 2006-03-23 | Xencor, Inc. | Monomeric immunoglobulin fc domains |
| CN108997498A (zh) | 2008-12-09 | 2018-12-14 | 霍夫曼-拉罗奇有限公司 | 抗-pd-l1抗体及它们用于增强t细胞功能的用途 |
| RS59589B1 (sr) * | 2010-11-05 | 2019-12-31 | Zymeworks Inc | Dizajniranje stabilnog heterodimernog antitela sa mutacijama u fc domenu |
| JP6326371B2 (ja) * | 2011-11-04 | 2018-05-16 | ザイムワークス,インコーポレイテッド | Fcドメインにおける変異を有する安定なヘテロ二量体抗体デザイン |
| AU2013249985B2 (en) * | 2012-04-20 | 2017-11-23 | Merus N.V. | Methods and means for the production of Ig-like molecules |
| US11059910B2 (en) * | 2012-12-03 | 2021-07-13 | Novimmune Sa | Anti-CD47 antibodies and methods of use thereof |
| WO2016023001A1 (en) | 2014-08-08 | 2016-02-11 | The Board Of Trustees Of The Leland Stanford Junior University | Multispecific high affinity pd-1 agents and methods of use |
| SG11201701189TA (en) * | 2014-08-15 | 2017-03-30 | Merck Patent Gmbh | Sirp-alpha immunoglobulin fusion proteins |
| SG10202007176TA (en) | 2014-12-30 | 2020-08-28 | Celgene Corp | Anti-cd47 antibodies and uses thereof |
| GEP20217326B (en) | 2015-08-07 | 2021-11-25 | Alx Oncology Inc | Constructs having a sirp-alpha domain or variant thereof |
| CA2998644A1 (en) * | 2015-09-18 | 2017-03-23 | Arch Oncology, Inc. | Therapeutic cd47 antibodies |
| CN106883297B (zh) | 2015-12-16 | 2019-12-13 | 苏州康宁杰瑞生物科技有限公司 | 基于ch3结构域的异二聚体分子、其制备方法及用途 |
| WO2017167350A1 (en) * | 2016-03-30 | 2017-10-05 | Horst Lindhofer | Multispecific antibodies for use in the treatment of a neoplasm of the urinary tract |
| CA3035681A1 (en) * | 2016-09-29 | 2018-04-05 | Beijing Hanmi Pharmaceutical Co., Ltd. | Heterodimeric immunoglobulin constructs and preparation methods thereof |
| PE20191080A1 (es) * | 2016-11-18 | 2019-08-20 | Beijing Hanmi Pharmaceutical Co Ltd | Anticuerpo biespecifico heterodimerico estructural de anticuerpo natural anti-pd-1/anti-her2 y metodo para preparar el mismo |
| WO2019047885A1 (en) * | 2017-09-07 | 2019-03-14 | Dingfu Biotarget Co., Ltd. | IMMUNOCONJUGATES COMPRISING ALPHA REGULATORY SIGNAL PROTEIN |
| EA039662B1 (ru) | 2017-10-03 | 2022-02-24 | Закрытое Акционерное Общество "Биокад" | Антитела, специфичные к cd47 и pd-l1 |
| JP7163399B2 (ja) | 2017-11-20 | 2022-10-31 | 泰州▲邁▼博太科▲薬▼▲業▼有限公司 | Cd47とpd-l1を標的にする二重機能の融合タンパク質 |
| EP4112647A4 (en) * | 2020-02-28 | 2024-03-27 | Nanjing Sanhome Pharmaceutical Co., Ltd. | ANTI-CD47/ANTI-PD-L1 ANTIBODIES AND ITS USES |
-
2018
- 2018-12-01 KR KR1020207019202A patent/KR20200093639A/ko unknown
- 2018-12-01 AU AU2018378529A patent/AU2018378529A1/en not_active Abandoned
- 2018-12-01 EA EA202091364A patent/EA202091364A1/ru unknown
- 2018-12-01 CN CN201880070773.3A patent/CN111615521A/zh active Pending
- 2018-12-01 US US16/769,108 patent/US11739151B2/en active Active
- 2018-12-01 BR BR112020011295-0A patent/BR112020011295A2/pt not_active IP Right Cessation
- 2018-12-01 CA CA3084626A patent/CA3084626A1/en active Pending
- 2018-12-01 MX MX2020005792A patent/MX2020005792A/es unknown
- 2018-12-01 SG SG11202005216XA patent/SG11202005216XA/en unknown
- 2018-12-01 WO PCT/CN2018/118800 patent/WO2019109876A1/zh unknown
- 2018-12-01 EP EP18887151.1A patent/EP3722322A4/en active Pending
- 2018-12-01 JP JP2020549852A patent/JP7231641B2/ja active Active
-
2020
- 2020-06-04 IL IL275135A patent/IL275135A/en unknown
- 2020-06-05 ZA ZA2020/03382A patent/ZA202003382B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| MX2020005792A (es) | 2020-11-06 |
| AU2018378529A1 (en) | 2020-06-18 |
| EA202091364A1 (ru) | 2020-10-13 |
| IL275135A (en) | 2020-07-30 |
| US11739151B2 (en) | 2023-08-29 |
| EP3722322A4 (en) | 2021-09-15 |
| SG11202005216XA (en) | 2020-07-29 |
| JP2021505195A (ja) | 2021-02-18 |
| BR112020011295A2 (pt) | 2020-11-24 |
| EP3722322A1 (en) | 2020-10-14 |
| CN111615521A (zh) | 2020-09-01 |
| ZA202003382B (en) | 2021-06-30 |
| US20210230277A1 (en) | 2021-07-29 |
| CA3084626A1 (en) | 2019-06-13 |
| JP7231641B2 (ja) | 2023-03-01 |
| WO2019109876A1 (zh) | 2019-06-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7231641B2 (ja) | 天然抗体様構造を有し、ヘテロ二量体形態の抗pd-l1/抗cd47二重特異性抗体、ならびにその製造方法 | |
| WO2019154349A1 (zh) | 抗pd-1/抗vegf天然抗体结构样异源二聚体形式双特异抗体及其制备 | |
| KR102247704B1 (ko) | 항 pd-1/항 her2 천연항체 구조 형태의 헤테로다이머 계의 이중특이성 항체 및 그 제조방법 | |
| US11591409B2 (en) | Anti-PD-L1/anti-PD-1 natural antibody structure-like heterodimeric bispecific antibody and preparation thereof | |
| TWI806961B (zh) | 抗pd-1/抗her2天然抗體結構樣異源二聚體形式雙特異抗體及其製備 | |
| WO2022148411A1 (zh) | 抗pd-l1/抗cd47天然抗体结构样异源二聚体形式双特异抗体及其制备 |