KR20200053524A - 염소를 포함하는 폐기물 또는 산업 부산물의 정제 방법 - Google Patents
염소를 포함하는 폐기물 또는 산업 부산물의 정제 방법 Download PDFInfo
- Publication number
- KR20200053524A KR20200053524A KR1020207009759A KR20207009759A KR20200053524A KR 20200053524 A KR20200053524 A KR 20200053524A KR 1020207009759 A KR1020207009759 A KR 1020207009759A KR 20207009759 A KR20207009759 A KR 20207009759A KR 20200053524 A KR20200053524 A KR 20200053524A
- Authority
- KR
- South Korea
- Prior art keywords
- chloride
- heat treatment
- waste
- industrial
- mass
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 90
- 239000000460 chlorine Substances 0.000 title claims abstract description 75
- 229910052801 chlorine Inorganic materials 0.000 title claims abstract description 61
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 title claims abstract description 60
- 239000002699 waste material Substances 0.000 title claims abstract description 57
- 239000006227 byproduct Substances 0.000 title claims abstract description 40
- 229910001385 heavy metal Inorganic materials 0.000 claims abstract description 126
- 238000010438 heat treatment Methods 0.000 claims abstract description 80
- 239000000203 mixture Substances 0.000 claims abstract description 44
- 239000011343 solid material Substances 0.000 claims abstract description 26
- 238000002156 mixing Methods 0.000 claims abstract description 14
- 150000001805 chlorine compounds Chemical class 0.000 claims abstract description 10
- 239000000126 substance Substances 0.000 claims abstract description 6
- 239000011701 zinc Substances 0.000 claims description 94
- 239000000428 dust Substances 0.000 claims description 77
- 239000000463 material Substances 0.000 claims description 73
- 238000004519 manufacturing process Methods 0.000 claims description 57
- 229910052725 zinc Inorganic materials 0.000 claims description 50
- 239000004568 cement Substances 0.000 claims description 46
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims description 43
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 29
- 229910000831 Steel Inorganic materials 0.000 claims description 29
- 239000010959 steel Substances 0.000 claims description 29
- 230000008569 process Effects 0.000 claims description 28
- 230000001590 oxidative effect Effects 0.000 claims description 27
- 239000010802 sludge Substances 0.000 claims description 27
- 239000012298 atmosphere Substances 0.000 claims description 22
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 claims description 19
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 18
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 16
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 15
- 239000007787 solid Substances 0.000 claims description 13
- 238000006243 chemical reaction Methods 0.000 claims description 12
- 238000001704 evaporation Methods 0.000 claims description 12
- 230000008020 evaporation Effects 0.000 claims description 12
- 239000011592 zinc chloride Substances 0.000 claims description 10
- 235000005074 zinc chloride Nutrition 0.000 claims description 10
- 238000001035 drying Methods 0.000 claims description 7
- 239000012071 phase Substances 0.000 claims description 7
- 239000012065 filter cake Substances 0.000 claims description 6
- 229910052742 iron Inorganic materials 0.000 claims description 6
- FBAFATDZDUQKNH-UHFFFAOYSA-M iron chloride Chemical compound [Cl-].[Fe] FBAFATDZDUQKNH-UHFFFAOYSA-M 0.000 claims description 6
- 229910001510 metal chloride Inorganic materials 0.000 claims description 6
- 229910052751 metal Inorganic materials 0.000 claims description 5
- 239000002184 metal Substances 0.000 claims description 5
- 238000005554 pickling Methods 0.000 claims description 5
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 claims description 4
- 239000003337 fertilizer Substances 0.000 claims description 4
- YDZQQRWRVYGNER-UHFFFAOYSA-N iron;titanium;trihydrate Chemical compound O.O.O.[Ti].[Fe] YDZQQRWRVYGNER-UHFFFAOYSA-N 0.000 claims description 4
- 239000011785 micronutrient Substances 0.000 claims description 4
- 235000013369 micronutrients Nutrition 0.000 claims description 4
- 239000000049 pigment Substances 0.000 claims description 4
- 229910010413 TiO 2 Inorganic materials 0.000 claims description 3
- 239000007788 liquid Substances 0.000 claims description 3
- 238000002844 melting Methods 0.000 claims description 3
- 230000008018 melting Effects 0.000 claims description 3
- 239000007791 liquid phase Substances 0.000 claims description 2
- 238000010310 metallurgical process Methods 0.000 claims description 2
- 238000012619 stoichiometric conversion Methods 0.000 claims description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N titanium dioxide Inorganic materials O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 claims description 2
- 229910052745 lead Inorganic materials 0.000 description 41
- 239000000243 solution Substances 0.000 description 17
- 239000000047 product Substances 0.000 description 16
- 239000007789 gas Substances 0.000 description 15
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 12
- 229910052799 carbon Inorganic materials 0.000 description 9
- 238000004064 recycling Methods 0.000 description 9
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 8
- 230000008901 benefit Effects 0.000 description 7
- 239000011575 calcium Substances 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 239000000446 fuel Substances 0.000 description 7
- 238000002411 thermogravimetry Methods 0.000 description 7
- 229910052786 argon Inorganic materials 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 5
- 229910017604 nitric acid Inorganic materials 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 4
- 230000009257 reactivity Effects 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 238000010891 electric arc Methods 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000004800 polyvinyl chloride Substances 0.000 description 3
- 239000002994 raw material Substances 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229910052793 cadmium Inorganic materials 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 238000002485 combustion reaction Methods 0.000 description 2
- 238000011109 contamination Methods 0.000 description 2
- 229910052593 corundum Inorganic materials 0.000 description 2
- 239000010431 corundum Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 238000004993 emission spectroscopy Methods 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 238000009616 inductively coupled plasma Methods 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 238000002386 leaching Methods 0.000 description 2
- 239000003077 lignite Substances 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- 235000010755 mineral Nutrition 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 229920000915 polyvinyl chloride Polymers 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 239000010453 quartz Substances 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- HBMJWWWQQXIZIP-UHFFFAOYSA-N silicon carbide Chemical compound [Si+]#[C-] HBMJWWWQQXIZIP-UHFFFAOYSA-N 0.000 description 2
- 229910010271 silicon carbide Inorganic materials 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- -1 tires Substances 0.000 description 2
- 229910018072 Al 2 O 3 Inorganic materials 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical class OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 229910004298 SiO 2 Inorganic materials 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 239000004566 building material Substances 0.000 description 1
- WETINTNJFLGREW-UHFFFAOYSA-N calcium;iron;tetrahydrate Chemical compound O.O.O.O.[Ca].[Fe].[Fe] WETINTNJFLGREW-UHFFFAOYSA-N 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 238000005660 chlorination reaction Methods 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 239000003245 coal Substances 0.000 description 1
- 239000000571 coke Substances 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000004567 concrete Substances 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 238000005260 corrosion Methods 0.000 description 1
- 230000007797 corrosion Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000011010 flushing procedure Methods 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 239000002803 fossil fuel Substances 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000003517 fume Substances 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 230000009931 harmful effect Effects 0.000 description 1
- 229910003439 heavy metal oxide Inorganic materials 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- QWPPOHNGKGFGJK-UHFFFAOYSA-N hypochlorous acid Chemical compound ClO QWPPOHNGKGFGJK-UHFFFAOYSA-N 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 239000011256 inorganic filler Substances 0.000 description 1
- 229910003475 inorganic filler Inorganic materials 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- 239000003345 natural gas Substances 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000005453 pelletization Methods 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000013502 plastic waste Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000013014 purified material Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 239000013049 sediment Substances 0.000 description 1
- 238000005245 sintering Methods 0.000 description 1
- 239000002893 slag Substances 0.000 description 1
- 239000000779 smoke Substances 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000009628 steelmaking Methods 0.000 description 1
- XTQHKBHJIVJGKJ-UHFFFAOYSA-N sulfur monoxide Chemical class S=O XTQHKBHJIVJGKJ-UHFFFAOYSA-N 0.000 description 1
- 229910052815 sulfur oxide Inorganic materials 0.000 description 1
- 229910052716 thallium Inorganic materials 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000004065 wastewater treatment Methods 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B09—DISPOSAL OF SOLID WASTE; RECLAMATION OF CONTAMINATED SOIL
- B09B—DISPOSAL OF SOLID WASTE NOT OTHERWISE PROVIDED FOR
- B09B3/00—Destroying solid waste or transforming solid waste into something useful or harmless
- B09B3/40—Destroying solid waste or transforming solid waste into something useful or harmless involving thermal treatment, e.g. evaporation
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B7/00—Hydraulic cements
- C04B7/36—Manufacture of hydraulic cements in general
- C04B7/364—Avoiding environmental pollution during cement-manufacturing
- C04B7/365—Avoiding environmental pollution during cement-manufacturing by extracting part of the material from the process flow and returning it into the process after a separate treatment, e.g. in a separate retention unit under specific conditions
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G9/00—Compounds of zinc
- C01G9/02—Oxides; Hydroxides
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G9/00—Compounds of zinc
- C01G9/04—Halides
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G9/00—Compounds of zinc
- C01G9/08—Sulfides
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B7/00—Hydraulic cements
- C04B7/14—Cements containing slag
- C04B7/147—Metallurgical slag
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B7/00—Hydraulic cements
- C04B7/24—Cements from oil shales, residues or waste other than slag
-
- C—CHEMISTRY; METALLURGY
- C04—CEMENTS; CONCRETE; ARTIFICIAL STONE; CERAMICS; REFRACTORIES
- C04B—LIME, MAGNESIA; SLAG; CEMENTS; COMPOSITIONS THEREOF, e.g. MORTARS, CONCRETE OR LIKE BUILDING MATERIALS; ARTIFICIAL STONE; CERAMICS; REFRACTORIES; TREATMENT OF NATURAL STONE
- C04B7/00—Hydraulic cements
- C04B7/36—Manufacture of hydraulic cements in general
- C04B7/60—Methods for eliminating alkali metals or compounds thereof, e.g. from the raw materials or during the burning process; methods for eliminating other harmful components
-
- C—CHEMISTRY; METALLURGY
- C05—FERTILISERS; MANUFACTURE THEREOF
- C05D—INORGANIC FERTILISERS NOT COVERED BY SUBCLASSES C05B, C05C; FERTILISERS PRODUCING CARBON DIOXIDE
- C05D9/00—Other inorganic fertilisers
-
- C—CHEMISTRY; METALLURGY
- C21—METALLURGY OF IRON
- C21B—MANUFACTURE OF IRON OR STEEL
- C21B15/00—Other processes for the manufacture of iron from iron compounds
- C21B15/006—By a chloride process
-
- C—CHEMISTRY; METALLURGY
- C21—METALLURGY OF IRON
- C21C—PROCESSING OF PIG-IRON, e.g. REFINING, MANUFACTURE OF WROUGHT-IRON OR STEEL; TREATMENT IN MOLTEN STATE OF FERROUS ALLOYS
- C21C5/00—Manufacture of carbon-steel, e.g. plain mild steel, medium carbon steel or cast steel or stainless steel
- C21C5/56—Manufacture of steel by other methods
- C21C5/562—Manufacture of steel by other methods starting from scrap
- C21C5/565—Preheating of scrap
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B1/00—Preliminary treatment of ores or scrap
- C22B1/005—Preliminary treatment of scrap
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B1/00—Preliminary treatment of ores or scrap
- C22B1/02—Roasting processes
- C22B1/08—Chloridising roasting
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B13/00—Obtaining lead
- C22B13/02—Obtaining lead by dry processes
- C22B13/025—Recovery from waste materials
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B19/00—Obtaining zinc or zinc oxide
- C22B19/30—Obtaining zinc or zinc oxide from metallic residues or scraps
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B7/00—Working up raw materials other than ores, e.g. scrap, to produce non-ferrous metals and compounds thereof; Methods of a general interest or applied to the winning of more than two metals
- C22B7/001—Dry processes
- C22B7/002—Dry processes by treating with halogens, sulfur or compounds thereof; by carburising, by treating with hydrogen (hydriding)
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B7/00—Working up raw materials other than ores, e.g. scrap, to produce non-ferrous metals and compounds thereof; Methods of a general interest or applied to the winning of more than two metals
- C22B7/02—Working-up flue dust
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25C—PROCESSES FOR THE ELECTROLYTIC PRODUCTION, RECOVERY OR REFINING OF METALS; APPARATUS THEREFOR
- C25C1/00—Electrolytic production, recovery or refining of metals by electrolysis of solutions
- C25C1/16—Electrolytic production, recovery or refining of metals by electrolysis of solutions of zinc, cadmium or mercury
-
- C—CHEMISTRY; METALLURGY
- C21—METALLURGY OF IRON
- C21B—MANUFACTURE OF IRON OR STEEL
- C21B2200/00—Recycling of non-gaseous waste material
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P10/00—Technologies related to metal processing
- Y02P10/10—Reduction of greenhouse gas [GHG] emissions
- Y02P10/134—Reduction of greenhouse gas [GHG] emissions by avoiding CO2, e.g. using hydrogen
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P10/00—Technologies related to metal processing
- Y02P10/20—Recycling
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P40/00—Technologies relating to the processing of minerals
- Y02P40/10—Production of cement, e.g. improving or optimising the production methods; Cement grinding
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Materials Engineering (AREA)
- Metallurgy (AREA)
- Manufacturing & Machinery (AREA)
- Mechanical Engineering (AREA)
- Environmental & Geological Engineering (AREA)
- Ceramic Engineering (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Life Sciences & Earth Sciences (AREA)
- Geology (AREA)
- Structural Engineering (AREA)
- Geochemistry & Mineralogy (AREA)
- Public Health (AREA)
- Health & Medical Sciences (AREA)
- Inorganic Chemistry (AREA)
- Environmental Sciences (AREA)
- Ecology (AREA)
- Biodiversity & Conservation Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Electrochemistry (AREA)
- Physics & Mathematics (AREA)
- Thermal Sciences (AREA)
- Processing Of Solid Wastes (AREA)
- Manufacture And Refinement Of Metals (AREA)
Abstract
본 출원은 폐기물 또는 산업 부산물을 정제하는 방법에 관한 것으로서, 상기 방법은
a) 염소를 포함하는 폐기물 또는 산업 부산물 (B)을, 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합함으로써 조성물 (C)을 제조하는 단계
b) (C)의 열처리에 의해 (B) 및 (HM)을 반응시키는 단계
c) 증발된 중금속 클로라이드 화합물 (HMCC)을 분리하는 단계
d) 열처리 단계 후 고체 물질을 수득하는 단계
를 포함한다.
a) 염소를 포함하는 폐기물 또는 산업 부산물 (B)을, 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합함으로써 조성물 (C)을 제조하는 단계
b) (C)의 열처리에 의해 (B) 및 (HM)을 반응시키는 단계
c) 증발된 중금속 클로라이드 화합물 (HMCC)을 분리하는 단계
d) 열처리 단계 후 고체 물질을 수득하는 단계
를 포함한다.
Description
본 발명은 열처리 및 상기 정제된 물질을 산업 공정으로 재순환함으로써 염소를 포함하는 폐기물 또는 산업 부산물을 정제하는 방법에 관한 것이다. 염소를 포함하는 폐기물 또는 산업 부산물은 예를 들어 시멘트 생산에서 발생하는 분진(dust)을 바이패스(bypass)할 수 있다.
시멘트 제조에서 공정으로 다시 재활용해야 하는 많은 양의 분진이 발생된다. 그러나, 생산 공정으로의 분진의 재순환은 바람직하지 않은 부작용, 예를 들어 산업 플랜트에서 클로라이드의 축적 및 결과적으로 시멘트 플랜트의 부식 및 시멘트에서의 클로라이드 함량의 증가로 이어질 수 있다.
바이패스 시스템은 시멘트 제조 시설에서 여러 가지 문제들, 예를 들어 시멘트 품질에 대한 유해 효과, 가마(kiln)에서 침전물 형성 또는 예열기 막힘을 일으킬 수 있는 염소를 제거하기 위해 사용되어 왔다. 바이패스는 예열기에 들어가기 전에, 분진이 함유된 노(furnace) 가스의 부분적인 제거 및 완전히 또는 부분적으로 응축된 구성성분의 제거를 야기한다.
석유, 리그나이트(lignite) 및 갈탄(brown coal)과 같은 화석 연료와 천연 가스의 가격 상승은 시멘트 생산 플랜트와 같은 산업 플랜트의 작동에서 점점 더 중요한 비용 인자를 나타낸니다. 이러한 개발로 인해 대체 연료(예컨대, 플라스틱 폐기물, 분류된 폐기물 분획, 동물 가루, 타이어, 용매 등)의 사용이 증가하여, 연료 비용을 줄이면서 클로라이드와 같은 원치 않는 성분의 투입이 증가한다. 그러나, 시멘트 생산 공정에서, 최종 시멘트 내 클로라이드에 대한 상한은 0.1%이다. 따라서, 높은 클로라이드 함량은 시멘트 생산에 불리하다.
대체 연료의 사용 증가로 인해, 염소의 양 및 발생되는 염소-함유 바이패스 분진의 양이 증가하였다. 시멘트 가마의 전체 노 가스 스트림 내 바이패스 가스의 비율은 일반적으로 3-15%이다.
바이패스 분진의 휘발성 구성분(1450℃에서)은 Na2O, K2O, 황 옥사이드, 염소 또는 클로라이드, 알칼리 금속 및 알칼리 토금속의 카르보네이트 및 비카르보네이트, 뿐만 아니라 암모늄 클로라이드이다. 또한, Zn 또는 Pb와 같은 일부 중금속이 통상적으로 바이패스 분진에 존재한다.
WO 2012/142638 A1은 시멘트 생산 공정에서 바이패스 분진의 처리 및 이용을위한 침출 공정을 기재하고 있다. 바이패스 분진의 습식 처리로부터 수득되는 염수는 존재하는 중금속을 분리하기 위해 후속적인 분별 결정화로 적절하게 처리된다.
그러나, 이 공정은 비용이 많이 들고, 습식 처리 형태의 추가의 어려운 공정 단계를 수반한다.
바이패스 분진에 대해 일부 다른 용도, 예를 들어 소정의 저급(low-quality) 시멘트 또는 시멘트질 물질의 제조가 존재하지만, 완전한 물질의 출구를 찾는 것은 항상 어려운 일이다. 따라서, 바이패스 분진은 때때로 매립되어야 한다.
도면의 간단한 설명
도 1은 비-산화 조건(생성물) 하에 1000℃에서 180분 동안 열처리된 다양한 물질의 Zn 및 Pb 농도를 출발 물질(유리체(educt))의 Zn 및 Pb 농도와 비교하여 도시한다; 실험 조건에 대해서는 표 1을 참조한다.
도 2는 실시예 2에서 관찰된 바와 같이 1000℃에서 공기 중 열처리 전(유리체) 및 열처리 후(생성물) BF 슬러지(sludge)에서의 Zn 및 Pb 농도를 도시한다.
도 3은 실시예 3에서 관찰된 바와 같이 1100℃에서 N2 분위기에서 열처리 전(유리체) 및 열처리 후(생성물) BF 슬러지에서의 Zn 및 Pb 농도를 도시한다.
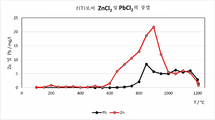
도 4는 실시예 4에서 관찰된 바와 같이 증발된 Zn 및 Pb의 양을 온도의 함수로서 나타내는, 질산 용액 중 Zn 및 Pb 농도를 도시한다. Zn 및 Pb의 (상대) 농도는 Zn 및 Pb의 (상대) 강도를 나타낸다.
도 5a는 실시예 4에서 열처리 동안 수합된 질산 용액 중 적분된 Zn 및 Pb 농도를 도시한다. 적분된 데이터는 모든 증분 분획을 지시된 온도까지 합계한 것을 의미한다.
도 5b는 800℃ 이하의 온도 범위를 도시하는 도 5a의 일부의 확대도이다.
이러한 배경으로부터, 본 발명은 클로라이드의 효율적인 제거에 의해 염소, 구체적으로는 시멘트 제조로부터의 바이패스 분진을 포함하는 폐기물 또는 산업 부산물의 정제 방법에 관한 것이다.
일반적으로, 염소-포함 폐기물 또는 산업 부산물의 임의의 처리는 비용(에너지, 장비, 인력 등)을 발생시킨다. 이러한 처리에 의해 발생되는 폐기물의 처리 및 폐기에 필요한 물질에 대해 추가 비용이 발생할 수 있다. 다른 한편으로는, 처리에 의해 발생된 생성물에 대해 약간의 상업적 가치가 있을 수 있다.
바이패스 분진의 처리에 관한 선행 기술을 고려할 때, 문제는 당업계에 알려진 공정, 즉, 습식 처리, 이러한 처리에 의해 발생되는 물질의 폐기 비용, 시멘트의 품질에 대한 유해 효과 및 시멘트 가마에서의 문제점의 단점 없이, 염소-함유 폐기물 또는 산업 부산물로부터 염소의 일부 또는 전부, 예를 들어 시멘트 제조로부터의 바이패스 분진을 제거하기 위한 기술적으로 실행 가능하고 비용-효율적인 공정을 찾는 것이었다. 특히 대량의 염소-포함 폐기물 또는 산업 부산물(독일에서 시멘트 생산으로 인한 바이패스 분진은 매년 수십만 톤에 달함)을 고려할 때, 적절한 물질의 가용성, 기술적 적합성 및 물류 기준이 고도로 중요하다.
문제점은 염소를 포함하는 폐기물 또는 산업 부산물 (B) 및 중금속 (HM)을 정제하기 위한 본 발명의 방법에 의해 해결되었으며, 상기 방법은
a)
염소를 포함하는 폐기물 또는 산업 부산물 (B)을, 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합함으로써 조성물 (C)을 제조하는 단계
b)
(C)의 열처리에 의해 (B) 및 (HM)을 반응시키는 단계
c)
증발된 중금속 클로라이드 화합물 (HMCC)을 분리하는 단계
d)
열처리 단계 후 고체 물질을 수득하는 단계
를 포함한다.
바람직하게는, 열처리 단계 후에 수득되는 고체 물질은 산업 공정으로, 바람직하게는 시멘트 제조 공정으로 재순환된다. 이는 특정 유형의 시멘트 또는 시멘트질 물질의 제조를 위해 시멘트 가마 내로 재순환되거나 고체 물질을 사용하는 단계를 포함할 수 있다.
염소를 포함하는 폐기물 또는 산업 부산물의 열처리를 위한 본 발명의 해결방안은 기술적 요건을 충족시키고 요구되는 양으로 이용 가능한, 철강 제조로부터의 분진과 같이 중금속을 적절한 시약으로서 포함하는 물질을 식별함으로써 가능해진다. 특히, 다량의 염소-포함 폐기물 또는 산업 부산물(이때, 시멘트 생산 단독으로부터의 바이패스 분진은 매년 수십만 톤임)의 측면에서, 적절한 물질의 가용성, 기술적 적합성 및 물류 기준은 고도로 중요하다.
본 발명의 해결방안은 당업계에 알려진 공정, 즉, 습식 처리의 단점, 이러한 처리에 의해 발생되는 물질의 폐기 비용, 바이패스 분진의 폐기, 바이패스 분진으로 인한 저급 시멘트질 물질, 시멘트의 품질에 대한 유해 효과 및 시멘트 가마에서의 문제점을 피한다.
이 문헌에서 중금속은 비중량(specific weight)이 5 g/cm3 초과인 금속, 예를 들어 Zn, Pb, Cd, Cu, Tl 또는 Hg이다.
다르게 언급되지 않는 한, 모든%-데이터는 중량-%이고, 모든 ppm-데이터는 중량 기준으로 한 중량이다.
염소를 포함하는 폐기물 또는 산업 부산물 (B)은 유의한 양, 바람직하게는 0.5% 초과의 염소를 갖는 임의의 물질일 수 있다. B의 구체적인 구현예는 시멘트 제조로부터의 바이패스 분진이다. B의 또 다른 구현예는 폴리비닐 클로라이드 (PVC) 또는 PVC를 포함하는 폐기물이다. B의 또 다른 구현예는 폐(waste) 염산, 특히 Fe 및/또는 다른 중금속을 포함하는 폐 염산이다. 다른 예는 폐 철 클로라이드, 바람직하게는 FeCl2, 또는 FeCl2 또는 FeCl3를 포함하는 물질, 예를 들어 일메나이트(ilmenite)의 침출로부터의 폐 금속 클로라이드 또는 일메나이트나 티타늄 슬래그(slag)의 염소화로부터의 폐 금속 클로라이드이다. 이들 물질은 반응 파트너 둘 모두에서 크롬의 유의한 함량으로 인해 전로강(electrosteel) 분진과의 열 반응에 특히 관심있다.
염소는 유기 형태 또는 무기 형태 또는 이들 둘 모두의 조합으로 존재할 수 있다. 무기 염소는 본 문헌의 맥락에서 클로라이드와 동일하다.
중금속 (HM)을 포함하는 물질은 B와 상이하고, 클로라이드로의 전환 후 더 높은 온도에서 휘발화될 수 있는 적어도 일부 중금속을 포함하는 임의의 물질일 수 있다. (HM)의 예는 제철소 분진("Gichtgasstaub") 또는 제철소 분진 또는 중금속을 포함하는 다른 분진의 가스 세정으로부터 수득되는 슬러지 또는 필터 케이크이다. (HM)의 다른 예는 전로강 분진, 안료 제조의 슬러지, 전환기 슬러지, 밀(mill) 스케일 또는 밀 스케일 슬러지 또는 이들 물질 중 하나 이상을 포함하는 임의의 혼합물이다. 다른 예는 중금속 화합물의 중화로부터 수득되는 중금속 또는 슬러지가 로딩된 활성 탄소이다.
본 발명의 일 구현예는 염소의 존재 하에 후속 열처리로 Zn 및/또는 Pb를 원소 또는 옥사이드로서 휘발시키는 제1 종래의 열처리이다. 이 2-단계 접근법은 원소 또는 옥사이드 형태로 일부 Zn 및/또는 Pb를 회복하고 정제 또는 재순환을 위해 확립된 기법을 활용한다(Waelz 공정).
바람직하게는, 중금속 (HM)을 포함하는 물질은 슬러지 또는 필터 케이크 형태이다. (HM)이 분진 또는 건조 물질인 경우, 혼합 단계 전에 약간의 물 또는 습윤 물질을 첨가하는 것이 유리할 수 있다. 이는 클로라이드 이온이 저 휘발성 화합물(예를 들어 KCl 또는 CaCl2)로부터 멀어지도록 하여, 보다 휘발성 화합물(예를 들어 ZnCl2 또는 PbCl2)을 발생시키는 것을 도울 수 있다. 실험 데이터는 일부 물의 존재 하에(열처리 전 후속 건조와 함께) (B)와 (HM)을 혼합할 때 상당한 이점 (즉, 열처리에서 더 휘발된 중금속)을 나타낸다.
높은 반응성으로 인해 (B) 및 (HM)에 대한 미세 물질이 바람직하다. 본 발명의 일 구현예는 열처리 전의 과립화 단계를 포함한다.
(C)의 열처리에 의한 (B) 및 (HM)의 반응은 바람직하게는 환원성 또는 불활성 분위기에서, 특히 탄소가 조성물 (C)에 존재하는 경우에 수행된다.
추가의 바람직한 구현예
본 발명의 구체적이고 바람직한 구현예는 시멘트 산업 (B)으로부터의 바이패스 분진과 철강 제조 (HM)로부터의 분진으로부터 수득되는 슬러지 또는 필터 케이크( "Gichtgasschlamm")의 혼합물의 열처리이다. (B)의 전형적인 염소 함량은 3 내지 15%이고, (HM) 내 Zn의 전형적인 함량은 1-5%이고 Pb는 0.1-2%이다.
따라서, 예를 들어, 6.4%의 Cl을 갖는 바이패스 분진과 2.3%의 Zn 및 0.5%의 Pb를 갖는 철강 산업으로부터의 분진의 43:57 혼합물은 조성물 (C)에 존재하는 상당한 양의 클로라이드 및 중금속을 휘발시키기에 충분하다.
Zn 및 Pb는 800-900℃의 온도에서 클로라이드로서 효율적으로 휘발된다. 열처리 후 수득된 고체 물질은 약 10%의 Fe 및 25%의 탄소를 포함한다. 열처리 단계 후에 수득된 고체 물질을 시멘트 가마 내로 재순환시키는 것은, Fe를 시멘트의 귀중한 원료로 공급하고 시멘트 가마에서 연료로서 탄소를 사용하는 추가적인 이점을 제공한다.
본 발명의 다른 구체적이고 바람직한 구현예는 시멘트 산업 (B)으로부터의 바이패스 분진과 전로강 제조 (HM)로부터의 분진의 혼합물의 열처리이다.
전로강 제조로부터의 분진은 전형적으로 유의한 양의 중금속, 예를 들어 30% 이하의 Zn 및 2% 이하의 Pb를 함유한다. 따라서, 꽤 소량의 전로강 분진(5-30%)은 바이패스 분진에서 클로라이드의 유의한 부분을 휘발시키기에는 충분할 수 있다.
중금속을 휘발시키기 위해 화학량론적으로 필요한 것보다 더 많은 염소, 10-20%의 화학양론적 초과량의 염소가 배합물에 취해질 수 있다. 이로 인해 중금속을 더 잘 제거할 수 있지만, 고체 잔류물에 더 많은 염소가 존재한다. 고체 잔류물이 시멘트 공정으로 다시 재순환되는 경우, 큰 문제는 발생하지 않습니다.
고체 잔류물을 철강 제조 공정으로 재순환하는 경우, 염소 함량은 가능한 낮아야 한다. 따라서, 이 경우 화학양론적으로 초과량의 염소는 없어야 한다.
예를 들어 예를 들어 건축 자재로서와 같이 고체 잔류물에 대한 다른 산업 용도를 선택하는 것이 가능하다. 이 적용에 대한 요건에 따라, 매우 낮은 염소 함량 또는 매우 낮은 HMCC 함량에 초점을 둘 수 있다.
염소를 포함하는 하나 이상의 물질 및/또는 중금속을 포함하는 하나 초과의 물질을 사용하는 것이 또한 가능하다. 열처리 후 휘발된 중금속 클로라이드 또는 고체 잔류물에 대한 비용, 가용성 또는 요건에 따라, 복잡한 혼합물은 기술 및/또는 경제적 이점을 가질 수있다.
공정의 매개변수는 산업 공정으로 재순환되는 고체 물질의 염소 및 중금속 함량에 관한 요건에 따라 달라질 수있다.
추가의 바람직한 구현예
본 발명의 구체적인 구현예는 하기이다:
[1] 염소를 포함하는 폐기물 또는 산업 부산물 (B)을 정제하는 방법으로서, 상기 방법은
a)
염소를 포함하는 폐기물 또는 산업 부산물 (B)을, 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합함으로써 조성물 (C)을 제조하는 단계
b)
(C)의 열처리에 의해 (B) 및 (HM)을 반응시키는 단계
c)
증발된 중금속 클로라이드 화합물 (HMCC)을 분리하는 단계
d)
열처리 단계 후 고체 물질을 수득하는 단계
를 포함하는, 방법.
[2] [1]에 있어서, 열처리 단계 후 수득되는 상기 고체 물질을 산업 공정으로, 바람직하게는 시멘트 제조 공정 또는 야금(metallurgical) 공정으로 재순환시키는, 방법.
또 다른 가능성은 열처리 단계 후 수득되는 고체 물질을 철강 제조, 예를 들어 소결 공정으로 재순환시키는 것이다.
[3] [1] 또는 [2]에 있어서, 염소를 포함하는 폐기물 또는 산업 부산물 (B)은 1-30 질량%, 바람직하게는 2-20 질량%, 보다 바람직하게는 3-15 질량%의 클로라이드를 포함하는, 시멘트 제조로부터의 분진, 바람직하게는 시멘트 분진으로부터의 바이패스 분진인 것을 특징으로 하는, 방법.
[4] [1] 내지 [3] 중 어느 하나에 있어서, 상기 중금속 (HM)은 하기 원소 세트로부터의 하나 이상인 것을 특징으로 하는, 방법: Zn, Pb, Hg, Cu, Cd, Tl, In, Sn, Ni, Co.
[5] [1] 내지 [4] 중 어느 하나에 있어서, 상기 조성물 (C) 내 중금속 (HM)의 함량은 0.5 내지 15 질량%, 바람직하게는 1 내지 12 질량%, 가장 바람직하게는 1.5 내지 10 질량%인 것을 특징으로 하는, 방법.
[6] [1] 내지 [5] 중 어느 하나에 있어서, 상기 중금속 (HM) 중 적어도 일부는, 1200℃ 미만, 바람직하게는 1000℃ 미만, 가장 바람직하게는 900℃ 미만의 온도에서 10 millibar(10000 Pa) 초과의 증기압을 갖는 클로라이드를 형성할 수 있는 것을 특징으로 하는, 방법.
[7] [1] 내지 [6] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 0.1 질량% 초과, 바람직하게는 0.5 질량% 초과, 보다 바람직하게는 2 질량% 초과, 가장 바람직하게는 20 질량% 초과의 Zn 및/또는 Pb를 포함하는 것을 특징으로 하는, 방법.
[8] [1] 내지 [7] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 50 ppm 초과의 Cu 및/또는 Cd를 포함하는 것을 특징으로 하는, 방법.
원칙적으로, 본 발명의 방법은 또한, 더 낮은 함량의 중금속으로 작동하지만, 이는 다량의 물질을 필요로 하고 상기 방법을 상업적인 관점에서 덜 매력적으로 만들 것이다.
[9] [1] 내지 [8] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 폐기 생성물 또는 산업 부산물인 것을 특징으로 하는, 방법.
이는 2가지 종류의 폐기물을 반응시키는 것을 의미할 것이며, 본 발명의 방법을 상업적인 관점에서 고도로 매력적으로 만들 것이다. 본 발명의 방법은, 산업 공정으로의 재순환을 위한 고체 물질을 수득하는 것 뿐만 아니라 증발되고 분리된 중금속 클로라이드 화합물 (HMCC)을 재순환한다면 훨씬 더 매력적으로 될 것이다. 이는 HMCC에 대한 공정에 투입되는 물질의 종류를 적절하게 선택함으로써, 그리고 최적화된 (분별화된) 분리 공정에 의해 달성될 수 있다.
[10] [1] 내지 [9] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 제철소 분진, 바람직하게는 제철소로부터 분진을 분리함으로써 수득되는 슬러지 또는 필터 케이크("Gichtgassschlamm"), 전로강 제조로부터 수득되는 분진 또는 사용된 활성 탄소를 포함하거나 이로 구성되는 것을 특징으로 하는, 방법.
[11] [1] 내지 [10] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 옥시딕(oxidic), 하이드록시딕(hydroxidic) 또는 금속성 형태의 Fe를 포함하는 특징으로 하는, 방법.
철 클로라이드의 발생 및 증발은 옥시딕 또는 하이드록시딕 형태의 Fe의 전환에 의해 방지된다.
[12] [1] 내지 [11] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 철 클로라이드, 예를 들어 클로라이드 공정에 따른 TiO2의 제조로부터 수득되는 폐 금속 클로라이드, 일메나이트로부터 합성 루틸(rutile)의 제조로부터 수득되는 폐 금속 클로라이드, 강철 산세(pickling)로부터 수득되는 폐 철 클로라이드, 또는 바람직하게는 Fe, Zn 및/또는 Pb와 같은 금속을 포함하는 폐 염산을 포함하는 것을 특징으로 하는, 방법.
철 클로라이드를 포함하는 물질은 바람직하게는, 열처리 단계의 온도에서 낮은 증기압으로 클로라이드를 Fe로부터 분리하고 Fe 화합물(승온에서 철 옥사이드로 전환될 Fe 하이드록사이드)을 발생시키기 위해 알칼리 물질(OH 이온을 포함함)의 처리를 필요로 할 수 있다.
[13] [1] 내지 [12] 중 어느 하나에 있어서, 상기 중금속 (HM)을 포함하는 물질은 코크스(coke), 카본 블랙 또는 석탄 형태의 탄소를 포함하는 것을 특징으로 하는, 방법. 이는 예를 들어 시멘트 가마로의 재순환 시, 열처리 후 수득되는 고체 물질에 추가의 가치를 가져다줄 수 있다.
[14] [1] 내지 [13] 중 어느 하나에 있어서, 상기 중금속 (HM) 중 적어도 일부가, 900℃ 미만, 바람직하게는 1000℃ 미만의 온도에서 증발될 수 있는 클로라이드를 형성할 수 없는 금속, 예를 들어 철인 것을 특징으로 하는, 방법.
[15] [1] 내지 [14] 중 어느 하나에 있어서, 염소를 포함하는 폐기물 또는 산업 부산물 (B)의 온도가 상기 중금속 (HM)을 포함하는 물질과의 혼합 시 100℃ 초과, 바람직하게는 150℃ 초과, 가장 바람직하게는 200℃ 초과인 것을 특징으로 하는, 방법.
[16] [1] 내지 [15] 중 어느 하나에 있어서, 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)의 비는, 조성물 (C)의 염소 함량이, 중금속 (HM)을 포함하는 물질 내 중금속 (HM)을 클로라이드로 화학양론적 전환시키는 데 필요한 양의 100% 내지 150%, 바람직하게는 100% 내지 130%, 가장 바람직하게는 100% 내지 110%인 것을 특징으로 하는, 방법.
[17] [1] 내지 [15] 중 어느 하나에 있어서, 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)의 비는, 조성물 (C)의 염소 함량이, 중금속 (HM)을 포함하는 물질 내 아연을 클로라이드로 화학양론적 전환시키는 데 필요한 양의 80% 내지 100%, 바람직하게는 90% 내지 99%, 가장 바람직하게는 90% 내지 95%인 것을 특징으로 하는, 방법.
[18] [1] 내지 [17] 중 어느 하나에 있어서, 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)은 물의 존재 하에 혼합되거나 배합되고, 2-50 질량%, 바람직하게는 5-30 질량%, 보다 바람직하게는 10-20 질량%의 물이 총 조성물 (C)에 존재하는 것을 특징으로 하는, 방법.
물은 조성물 (C)와 혼합되는 경우 또는 적절하다면 언제라도 첨가될 수 있다.
[19] [1] 내지 [18] 중 어느 하나에 있어서, 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)은 Ca2+ 이온을 포함하는 용액, 바람직하게는 Ca(OH)2 용액의 존재 하에 혼합되거나 배합되고, 이때, Ca2+ 이온을 포함하는 물의 양은, 조성물 (C) 내 Ca/S의 총 비가 1.2 초과, 바람직하게는 2.0 초과, 보다 바람직하게는 5 초과가 되는 양인 것을 특징으로 하는, 방법.
바람직한 가능성은, 조성물 (C)가 단계 b)의 열처리 전에 건조되는 것이다.
[20] [1] 내지 [19] 중 어느 하나에 있어서, 상기 열처리는 200 - 1500℃, 바람직하게는 300 - 1500℃, 보다 바람직하게는 300 - 1200℃, 가장 바람직하게는 500 - 900℃의 온도에서 수행되는 것을 특징으로 하는, 방법.
열처리에 보다 더 바람직한 온도는 500 - 850℃, 바람직하게는 600 - 700℃이다.
[21] [1] 내지 [20] 중 어느 하나에 있어서, 휘발된 물질(물을 배제함)의 양은 열처리에 투입되는 총 물질을 기준으로, 1 질량% 초과, 바람직하게는 2 질량% 초과, 가장 바람직하게는 5 질량% 초과인 것을 특징으로 하는, 방법.
휘발된 물질의 양의 평가는 증발된 상으로부터 수합된 물질의 중량의 결정에 의해 수행될 수 있다. 또 다른 옵션은 열처리 전의 건조 중량과 열처리 후의 건조 중량의 차이의 결정이다. 건조 중량의 결정을 위한 건조는 105℃에서 1시간 동안 수행된다.
[22] [1] 내지 [21] 중 어느 하나에 있어서, 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)의 질량비는, 조성물 (C) 내 Fe/Ca의 몰비가 0.8 - 3, 바람직하게는 0.9 - 1.8, 가장 바람직하게는 1.0 - 1.3이 되도록 선택되는 것을 특징으로 하는, 방법. 이는 칼슘 페리트(ferrite)가 열처리 공정 동안 발생될 수 있게 하고 열처리 후 수득되는 고체 물질을 철강 산업으로 재순환시키 위한 문을 연다.
[23] [1] 내지 [22] 중 어느 하나에 있어서, 상기 열처리가 비-산화적 분위기 하에 수행되는 것을 특징으로 하는, 방법.
[24] [1] 내지 [23] 중 어느 하나에 있어서, ZnCl2가 비-산화적 분위기 하에 500 - 700℃, 바람직하게는 600 - 680℃의 온도에서 열처리를 수행함으로써 증발되는 것을 특징으로 하는, 방법.
[25] [1] 내지 [19] 중 어느 하나에 있어서, 상기 열처리는 비-산화적 분위기 하에 1000 - 1200℃의 온도에서 수행되는 것을 특징으로 하는, 방법.
[26] [1]에 있어서, 염소를 포함하는 폐기물 또는 산업 부산물 (B)은 아연을 추가로 포함하고, 상기 방법은
a.
클로라이드, 바람직하게는 HCl 또는 FeCl2를 포함하는 용액을 공급하는 단계
b.
고로(blast furnace) 분진을 클로라이드를 포함하는 용액으로 통과시켜 고로 분진의 임의의 분획, 바람직하게는 미세 분획을 분리하고 수합하는 단계
c. 액체상으로부터 고체를 분리하는 단계
d. 고체 물질을 건조하고, 상기 고체 물질이 ZnCl2의 증발에 충분한 열처리를 받게 하는 단계
를 포함하는 것을 특징으로 하는, 방법.
[27] [1] 내지 [26] 중 어느 하나에 있어서, 아연 클로라이드의 용융점보다 높은 온도에서 기체상으로부터 상기 아연 클로라이드를 분리하고, 상기 아연 클로라이드를 액체로서 수득하는 것을 특징으로 하는, 방법.
[28] 금속성 Zn으로의 전해(electrolytic) 전환, ZnS 안료의 제조, ZnO의 제조, 또는 미량 영양소 비료의 제조를 위한, [1] 내지 [27] 중 어느 하나에 따른 방법에 의해 수득되는 ZnCl2의 용도.
청구된 발명은 또한, 염소를 포함하는 폐기물 또는 산업 부산물 (B)을 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합함으로써 수득 가능한 조성물 (C)을 제공하고, 이로써,
a)
Cl의 함량은 0.5-15 질량%, 바람직하게는 1-5 질량%, 가장 바람직하게는 1.5-3.5 질량%이며,
b)
Zn의 함량은 0.2-12 질량%, 바람직하게는 0.5-7 질량%, 가장 바람직하게는 1-3 질량%이며,
c)
Pb의 함량은 0.05-3 질량%, 바람직하게는 0.1-2 질량%, 가장 바람직하게는 0.2-0.7 질량%이고,
d)
Ca(CaO로서)의 함량은 10 질량% 초과, 바람직하게는 15 질량% 초과, 가장 바람직하게는 20 질량% 초과이다.
바람직한 구현예에서, 조성물 (C) 내 Fe의 함량은 1.5 질량% 초과, 바람직하게는 3.5 질량% 초과, 가장 바람직하게는 6 질량% 초과이며, 이는 열처리 후 수득되는 고체 물질을 더 매력적으로 만들 것이다.
나아가, 청구된 발명은 염소를 포함하는 폐기물 또는 산업 부산물 (B)을 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합하고 후속하여 열처리를 수행함으로써 수득 가능한 조성물 (C)의 열처리 후의 고체 물질을 제공하며, 여기서,
a)
Cl의 함량은 0-4 질량%, 바람직하게는 0.1-2.5 질량%, 가장 바람직하게는 0.2-1 질량%이며,
b)
Zn의 함량은 0-1.2 질량%, 바람직하게는 0-1 질량%, 가장 바람직하게는 0-0.5 질량%이며,
c)
Pb의 함량은 0-0.6 질량%, 바람직하게는 0-0.4 질량%, 가장 바람직하게는 0-0.2 질량%이고,
d)
Ca(CaO로서)의 함량은 10 질량% 초과, 바람직하게는 15 질량% 초과, 가장 바람직하게는 20 질량% 초과이다.
본 발명은 예를 들어, 시멘트 제조에서 증가된 함량의 염소를 갖는 저렴한 대체 연료의 증가된 사용을 가능하게 한다.
본 발명의 이점:
-
폐기물 또는 산업 부산물, 예를 들어 바이패스 분진 내 염소의 유의한 감소
-
염소의 감소는 염소의 더 많은 유입, 및 2차 원료에 대한 더 적은 비용을 가능하게 한다
-
중금속 클로라이드 화합물 (HMCC)의 열 증발 후 수득되는 고체 물질에서 중금속의 유의한 감소
-
산업적 용도에 가능한 열처리 후 수득되는 상기 고체 물질의 재순환
-
중금속 (HM)을 포함하는 물질은 추가의 이점을 제공할 수 있다: 열처리 후 수득되는 고체 물질의 재순환 시, 탄소를 연료로서 그리고 Fe를 원료(제강 분진에 의해 전달됨)로서 이용한다
-
중금속 클로라이드 화합물 (HMCC)로부터 가능한 중금속의 회수
-
소량의 Pb 불순물과 함께 Zn을 수득하는 옵션과 더불과, Zn 및 Pb의 열적 분리.
Zn 및/또는 Pb 및 클로라이드를 포함하는 시스템에 대해, 본 기술의 특징은 하기이다:
·
ZnCl2의 가시적 증발(즉, 가시적 연기(fume) 또는 매연(smoke))은 300℃에서 시작된다
·
약 650℃에서: 본질적으로 순수한 ZnCl2(>99% Zn; <1% Pb)의 증발
·
약 800℃에서: 낮은 수준까지의 Zn (및 Pb)의 제거
·
약 1100℃에서: Zn 및 Pb의 거의 완전한 제거
·
약 1100℃에서 수득된 생성물(미네랄 화합물 = "MiC")은 본질적으로 Zn 및 Pb가 없다
·
환원제가 필요하지 않다!(철 옥사이드는 철 옥사이드로 남아 있음)
·
FeCl2 또는 FeCl3의 유의한 증발이 없다
Waelz 공정("Walzprozess")과 비교하여, 본 발명의 방법은 환원 및 더 낮은 온도를 필요로 하지 않고, 유의하게 더 낮은 Zn 및 Pb 함량을 갖는 고체 생성물을 전달한다. 이는 더 양호한 유용성에 대한 문을 연다.
이들 특징으로 인해, 특정 공정에 대해 상이한 옵션이 존재한다:
a)
약 800℃의 온도에서 대부분의 Zn의 제거:
잔류 고체상에서 Zn의 농도는 상당히 (초기 값의 0.1 - 10%까지) 감소되며; 이는 철강 제조 공정으로의 재순환 또는 원치않는 요소인 Zn과 함께 사용하기 위한 문을 열어준다.
b)
약 1000 - 1100℃의 온도에서 거의 모든 Zn 및/또는 Pb의 제거:
잔류 고체상에서 Zn 및 Pb의 농도는 매우 낮은 수준(<<0.1% 또는 심지어 <200 ppm)까지 감소되며; 이는 철강 제조 공정으로의 재순환 또는 원치않는 요소인 Zn 및/또는 Pb와 함께 사용하기 위한 문을 열어준다.
예를 들어, 슬러지의 고로 (BF) 분진은 1100℃에서 클로라이드로 처리되어, Zn ~ 100 ppm 및 Pb ~ 20 ppm의 농도를 갖는 고체 잔류물을 초래하며(실시예 3 참조); 잔류 클로라이드는 후속 세척 단계에 의해 제거될 수 있다.
c)
약 650℃의 온도에서 본질적으로 순수한 ZnCl2 (>99% Zn)의 회수: 650℃에서, 증발된 생성물에서 Pb의 농도는 꽤 낮아서, 높은 Zn/Pb 비를 초래한다(도 4, 도 5a 및 도 5b와 함께 실시예 4 참조). 650℃에서 ZnCl2의 수합 후, 고체 잔류물 내 Zn 및 Pb의 농도는 제2 단계에서 더 높은 온도에서 최소화될 수 있다.
이는, 열 공정에 의한 낮은 농도의 Pb를 갖는 ZnCl2 농축물을 수득하고, Zn으로부터 Pb를 분리하기 위한 습식 처리를 피하는 문을 연다. 선택적으로, 습식 처리는 PbSO4의 침전에 의해 Pb 농도를 보다 더 최소화할 수 있다.
고체 잔류물은 철강 제조 공정으로 다시 재순환될 수 있다.
예를 들어, 전기 아크로(EAF) 분진은 650℃에서 후속 열처리에 의해 FeCl2 또는 HCl과 함께 혼합될 수 있다. 증발된 물질 내 Pb의 농도는 <1%(도 5의 데이터로부터 계산된 바와 같음)이다.
d)
Cl을 포함하는 물질, 예를 들어 산세 용액으로부터 Cl의 제거:
강철 산세로부터의 FeCl2 용액은 Zn 또는 Pb를 포함하는 물질, 예를 들어 BF 분진 또는 슬러지 또는 EAF 분진과 혼합함으로써 이용될 수 있다. 열처리는 ZnCl2 및 PbCl2를 증발시키고, 고체 잔류물은 철강 제조 공정으로 다시 재순환될 수 있다.
본 발명의 바람직한 구현예 및 이점은 하기를 포함한다:
·
열처리 동안 비-산화적 분위기
·
환원성 가스 분위기가 필요하지 않음: Fe 옥사이드를 환원시키는 것 없이 Zn의 제거
·
500 - 700℃, 바람직하게는 600 - 680℃의 온도에서 비-산화적 분위기 하에 열처리를 수행함으로써 ZnCl2를 특정하게 증발시켜 순수한 ZnCl2의 발생(표적 온도에서의 처리 시간은 0.5 - 2.5 h, 바람직하게는 1 - 2 h임)
·
약간 과량의 Cl (또는 과량이 아닌 Cl, 또는 심지어 <100%의 화학양론): 몰비 ([Zn] + [Pb]) / [Cl] <2, 바람직하게는 <1.3
·
Zn 및/또는 Pb를 포함하는 물질의 반응성에 따라, 클로라이드 공급원은 선택될 수 있다: FeCl2는, 클로라이드가 매우 일시적(fugitive)이지 않은 반면, HCl은 보다 양호한 반응성을 제공할 수 있다는 이점을 제공하고; 바이패스 분진은 시멘트 산업에서 적용에 더 양호한 상용성(compatibility)을 갖는 고체 물질(미네랄 물질)을 초래할 수 있다
·
Zn 및/또는 Pb의 양의 유의한 감소 및 동시에 열처리 후 Cl-무함유 물질의 발생
·
1000 - 1100℃의 온도에서 비-산화적 분위기에서 열처리를 수행함으로써 Zn 및 Pb가 없는(Zn< 200 ppm; Pb<50 ppm) 물질의 발생
·
구체적인 공정:
하기에 의한 BF 분진 (고로 분진)으로부터 Zn 및 Pb의 제거를 위한 공정:
a.
클로라이드를 포함하는 용액, 예를 들어 HCl 또는 FeCl2 용액 내로 BF 분진을 통과시키는 단계,
b.
과량의 물을 여과(변형된 BF 슬러지를 초래함)에 의해 제거하는 단계,
c.
선택적으로 건조하며 및/또는 펠렛화하는 단계, 및
d.
수득된 물질을 열처리하는 단계.
모든 Zn 또는 Pb가 ZnCl2 또는 PbCl2의 형태로 이용 가능한 것은 아닌 것으로 보인다. 800℃(즉, ZnCl2의 비점 이상)에서 더 긴 처리 후에도 일부 Zn은 고체층에 잔류한다. Zn을 ZnCl2로 완전히 전환시키기 위해서는 분명히 T ~ 1000-1100℃의 온도가 필요하다.
본 발명의 또 다른 구현예는 (약간) 하위화학량론적(understoichiometric) 양의 Cl을 갖는 혼합물을 제조하는 것을 포함한다. 이러한 제조는 ZnCl2로서 존재하는 대부분의 Zn의 증발을 가능하게 하며, 동시에 클로라이드 오염 없이 고체층 물질이 수득된다.
본 발명의 바람직한 구현예는, 클로라이드 이온, 특히 물 존재 하에 클로라이드 이온 형태의 염소를 포함하는 물질을 사용한다. 중금속 옥사이드(특히 ZnO 또는 PbO 또는 MexZnOy 형태의 보다 복잡한 물질로서, 이때, Me는 Zn 이외의 금속임)와 함께 물의 존재 하에 클로라이드 이온의 반응성은 HCl 가스 또는 결정질 클로라이드, 예컨대 CaCl2와 비교하여 유의하게 개선되는 것으로 보인다. 건조 물질의 배합물의 경우, 열처리 동안 중금속 클로라이드의 수율은 열처리 전에 소량의 물을 첨가함으로써 개선될 수 있다.
중간 단계에서(또는 소정의 시간 동안) 물의 존재 하에 클로라이드 이온의 존재는 열처리 전에 반응 혼합물을 건조한 후에도 열처리 동안 중금속 클로라이드의 수율을 개선할 수 있다.
ZnCl2 입자가 매우 미세하기 때문에 기체상으로부터 아연 클로라이드를 분리하는 것이 어려울 수 있다. 물을 통한 버블링도 기체상에서 분리되지 않은 ZnCl2 입자의 일부를 남긴다. 따라서, 본 발명의 일 구현예는 아연 클로라이드의 용융점 초과의 온도에서 기체상으로부터 ZnCl2를 분리하여 아연 클로라이드를 액체로서 수득하는 단계를 포함한다.
수득된 ZnCl2는 금속성 Zn으로의 전해 전환을 위해, Zns 안료의 제조를 위해, ZnO의 제조를 위한 배터리용 전해질로서, 또는 미량 영양소 비료로서 사용될 수 있다.
금속성 Zn으로의 전해 전환 또는 미량 영양소 비료로서의 사용을 위해, 황산과의 반응에 의한 ZnSO4로의 전환이 유리할 수 있다.
ZnCl2의 습식 처리는 또한, PbSO4의 침전 및 분리에 의한 Pb 오염의 감소를 가능하게 한다. 따라서, 10000 초과의 Zn/Pb 비가 달성될 수 있다.
정의:
염소를 포함하는 폐기물 또는 산업 부산물: 강철 산세 또는 TiO2 생산으로부터의 FeCl2 용액, 부산물 또는 금속 이온을 포함하는 HCl로서 수득된 HCl, 시멘트 산업으로부터의 바이패스 분진, PVC(특히 무기 충전제 포함), 언급된 임의의 물질을 포함하는 조성물이다.
임의의 다른 생성물과 조합하여 수득된 임의의 HCl은 상기 정의에 따른 산업 부산물, 즉 H2와 Cl2의 반응에 의해 수득되지 않은 임의의 HCl은 청구항 제1항의 의미에서 산업 부산물 또는 폐기물이다.
중금속 (HM)을 포함하는 물질: Zn 및/또는 Pb를 포함하는 고로 분진(BF 분진) 또는 슬러지, Zn 및/또는 Pb를 포함하는 전기 아크로 분진(EAF 분진), 중금속, 특히 Zn 및/또는 Pb를 포함하는 흡수에 사용되는 활성 탄소, 중금속의 중화로부터, 예를 들어 폐수 처리로부터 수득되는 슬러지, 언급된 임의의 물질을 포함하는 임의의 조성물이다.
비-산화적 분위기: <5 질량%의 산소 함량을 갖는 분위기; 상기 분위기는 질소, 비활성 기체, CO2, CO, H2 또는 이들의 혼합물로 구성될 수 있다.
산화적 분위기: >5%의 산소를 포함하는 분위기, 예를 들어 공기이다.
실시예
실시예 1:
35% 제철소 분진 및 65% 바이패스 분진의 건조 중량비로 시멘트 제조로부터의 바이패스 분진(BPD)과 함께 고로로부터 분진을 분리하여 수득된 혼합 BF 슬러지("Gichtgasschlamm")가 존재하였다. 머플로(muffle furnace)에서 열처리하기 전에 혼합물을 105℃에서 5시간 동안 건조하였다.
바이패스 분진의 클로라이드 함량은 6.4%였고, 제철소 분진의 Zn 및 Pb 함량은 각각 2.3% 및 0.5%였다.
수득된 조성물 (C)를 머플로의 도가니에서 900℃에서 90분 동안 열처리하였다.
열처리 후 도가니의 상부에서 많은 바늘형 결정이 발견되었다. 이와 대조적으로, 시멘트 제조에서 발생하는 개별 물질, 즉, 제철소 분진 및 바이패스 분진은 도가니에서 동일한 열처리로 결정 형성을 나타내지 않았다.
900℃에서의 열처리로 인한 조성물 (C)의 중량 손실은 16.66%인 반면, 개별 구성성분(둘 모두는 머플로에서 열처리하기 전에 105℃에서 5시간 동안 건조됨)으로부터의 계산된 중량 손실은 10.79%(BF 슬러지의 경우 24.10%, BPD의 경우 3.62%)였다.
5.87%의 혼합물의 중량 손실에 대해 "시너지 효과"가 존재하며, 이는 클로라이드 및 중금속이 접촉되면 증발이 촉진됨을 나타낸다.
실시예 2:
머플로로 일련의 실험을 수행하여 폐기물로부터의 중금속 제거 효율에 대한 공정 온도 및 산화적/비-산화적 조건의 영향을 연구하였다. 이를 위해, 시멘트 제조로부터 BF 슬러지 + HCl, BF 슬러지 + FeCl2, BF 슬러지 + 바이패스 분진(BPD), 및 전기 아크로 분진(EAFD) + BPD의 혼합물을 1:1, 5:1 및 10:1의 Cl/(Zn + Pb) 몰비를 사용하여 유리 비커에서 제조 하였다(표 1). 그 후, 소정의 양(4 내지 17 g)의 상기 혼합물을 실험을 위해 50 mL 커런덤(corundum) 도가니(정확도 ± 1mg)에서 칭량하였다.
중금속 제거에 대한 산화적/비-산화적 조건의 효과는 ~ 320 L/h의 플럭스(flux) 속도로 머플로를 공기(산화적 조건) 또는 아르곤(비-산화적 조건)으로 플러싱함으로써 조사되었다. 샘플을 삽입한 후, 머플로를 1000℃까지 가열하고, 공기 또는 아르곤으로 연속적으로 플러싱하였다. 아르곤의 경우, 머플로를 실온에서 (즉, 가열하기 전에) 60분 동안 아르곤으로 플러싱하여, 온도 증가 전에 비-산화적 조건을 확립하였다. 1000℃에서 180분의 체류 시간 동안 열처리한 후, 진행(run) 생성물을 갖는 도가니는 연속적인 가스 유동 하에 머플로에 상주하고, ~ 300℃까지 냉각되었다. 그 후에, 샘플을 실온까지 추가로 냉각시킨 후, 부위 분위기에서 노로부터 제거한 후에 수행하였다.
중금속 제거 효율에 대한 공정 온도의 영향을 특정 온도에서 머플로로부터 특정 샘플을 제거하는 것을 수반하는 실험에서 조사하였다. 이 실험에서, Cl/(Zn + Pb)의 몰비가 1인 BF 슬러지 + HCl의 혼합물 샘플 8개를 동시에 실온으로부터 최종 온도 1200℃까지 가열하였다. 500℃에서 100℃의 단계로, 샘플 후 샘플을 노에서 연속적으로 제거하고 공기 중에서 켄칭하여 주어진 온도 단계에서 물질의 벌크 조성을 고정시켰다. 아르곤 분위기에서 유사한 실험을 수행하는 것이 실용적이지 않은 것으로 밝혀졌으므로, 실시예 4에 나타낸 바와 같이 열중량 분석(TGA)을 사용하여 동등한 시간/온도 시리즈를 수행하였다.
각각의 실험 진행의 도가니를 칭량하고, 진행된 생성물을 막자사발과 막자를 사용하여 분쇄하였다. 각각의 실험으로부터의 분쇄된 생성물 및 분쇄된 유리체의 원소 질량 분율은 마이크로파-보조 총 분해(HNO3/HClO4/HF) 후 유도 결합 플라즈마 광 방출 분광법(ICP-OES)에 의해 결정되었다.
표 1: 비-산화적 조건 및 산화적 조건 하에 1000℃에서 열처리된 다양한 물질 혼합물들의 Zn 및 Pb 질량 분율.
| 유리체 | 생성물 | 제거 효율 | |||||||||
| Zn/Pb | Cl | 몰비 | T | t | Zn | Pb | Zn | Pb | Zn | Pb | |
| 공급원 | 공급원 | Cl/(Zn+Pb) | 가스 | ℃ | min | mg/kg | % | ||||
| BFS | HCl | 5:1 | Ar | 1000 | 180 | 24545 | 6793 | 176 | 38 | 99.3 | 99.4 |
| BFS | HCl | 10:1 | Ar | 1000 | 180 | 22013 | 6020 | 88 | 42 | 99.6 | 99.3 |
| BFS | FeCl2 | 5:1 | Ar | 1000 | 180 | 17848 | 4917 | 196 | 66 | 98.9 | 98.7 |
| BFS | FeCl2 | 10:1 | Ar | 1000 | 180 | 13517 | 3731 | 55 | 83 | 99.6 | 97.7 |
| BFS | BPD | 5:1 | Ar | 1000 | 180 | 8854 | 3398 | 327 | 197 | 96.3 | 94.2 |
| EAFD | BPD | 5:1 | Ar | 1000 | 180 | 18538 | 2123 | 11072 | 714 | 40.3 | 66.4 |
| BFS | HCl | 1.33:1 | Air | 1000 | 30 | 23636 | 6911 | 37104 | 1975 | -57.0† | 71.4 |
| BFS: BF 슬러지; EAFD: 전기-아크로 분진; BDP: 시멘트 분진으로부터의 바이패스 분진. T: 공정 온도; t: 체류 시간. †Zn에서 상대 증가는 열처리 동안 탄소의 연소(즉, 제거)로 인한 것임. |
|||||||||||
도 1은 출발 물질(유리체)의 Zn 및 Pb 농도와 비교하여 비-산화적 조건(생성물) 하에 1000℃에서 180분 동안 열처리된 다양한 물질 혼합물의 Zn 및 Pb 농도를 도시하고; 실험 조건에 대한 표 1을 참조한다.
도 2는 출발 물질(유리체)의 Zn 및 Pb 농도와 비교하여 산화적 조건, 즉 공기(생성물) 하에 1000℃에서 열처리된 Cl/(Zn + Pb)의 몰비 1을 갖는 BF 슬러지 + HCl 혼합물의 Zn 및 Pb 농도를 비교한 것이다. 유리체에 비해 생성물에서 Zn의 증가는 열처리 동안 탄소의 연소(즉, 제거)에 의한 것이며, 이는 상대 농화(enrichment)를 야기한다는 점을 주지한다.
도 1, 2, 3에서 아는 바와 같이, 가스 분위기의 영향은 놀랍게도 분명하다!
산화적 분위기(공기)에서, 공정 온도에 관계없이 ZnCl2의 유의한 증발은 검출되지 않은 반면(도 2; 표 1), 비-산화적 분위기(아르곤)에서 ZnCl2와 PbCl2의 유의한 증발이 검출되었다(도 1; 표 1).
순수한 ZnCl2가 안정적이고 이들 온도에서 증발해야 하기 때문에, ZnCl2로부터 ZnO로의 분해를 개시하는 촉매 효과가 있을 수 있다.
실시예 3:
415.7 g의 고로 슬러지 필터 케이크(BF 슬러지, "Gichtgasschlamm")를 42.1 g의 염산(37%의 HCl)과 혼합하였다. 더 나은 혼합 거동을 위해 60 mL의 물을 첨가하였다.
혼합물을 105℃에서 3시간 동안 건조하고, 수득된 제조물(유리체)을 회전 석영 가마에서 열처리하였다. 1100℃까지의 가열을 168분 이내에 수행하였고, 1100℃에서 가열을 34분 동안 수행하였다.
400 L/h의 속도로 석영 가마를 통해 N2를 통과시킴으로써 열처리하는 동안 비-산화적 분위기를 유지시켰다. N2 분위기를 실온까지 냉각하는 동안(~ 3 시간) 유지시켰다.
열처리 전과 후의 Zn 및 Pb 농도를 도 3에 도시한다: 알 수 있는 바와 같이, 99% 초과의 Zn 및 Pb가 열처리에 의해 제거된다.
실시예 4: 열중량 분석
기체상 분석을 통한 열중량 분석(TG) 조사를, 실리콘 카바이드 노가 장착된 Netzsch STA 443 F3 Jupiter 열 분석기를 사용하여 수행하였다. 30-40 mg의 BF 슬러지와 HCl의 혼합물(실시예 3의 "유리체")을 TG 샘플 홀더에 채우고 산화적 조건을 위한 합성 공기 또는 비-산화적 조건을 위한 아르곤으로 플러싱된 열 분석기에 넣었다. TG 샘플 홀더 내부의 샘플 혼합물을 5K/분의 속도를 사용하여 실리콘 카바이드 로에서 최대 온도 1200℃까지 가열하였다. 샘플의 중량을 시간이 지남에 따라 불활성 물질(코런덤)에 대해 영구적으로 결정하였고, 시스템의 배출-가스(off-gas)를 가열된 이송 라인(160℃까지 가열됨)을 통해 세척 플라스크(10 mL 질산 10%)로 연속적으로 유도하였으며, 이를 아연 및 납의 제거를 온도의 함수로서 조사하기 위해 10분마다(즉, 50℃ 온도 간격으로) 바꿔주었다. Pb 및 Zn의 농도를 실시예 2에서와 유사한 분석 루틴을 사용하여 ICP-OES(유도 결합 플라즈마 광 방출 분광법)에 의해 결정하였다. 소정의 온도에 상응하는 용액의 농도는 도 4 및 5에 제시된다.
도 4는 질산 용액 중 Zn 및 Pb 농도를 도시하며, 증발된 Zn 및 Pb의 양을 온도의 함수로서 나타낸다. Zn 및 Pb의 (상대) 농도는 주어진 온도에서 Zn 및 Pb의 (상대) 증발 강도를 나타낸다.
도 5a는 열처리 동안 수합된 질산 용액에 적분된 Zn 및 Pb 농도를 도시한다. 적분된 데이터는 모든 증분 분율을 표시된 온도까지 합산하는 것을 의미한다.
도 5b는 800℃까지의 온도 범위를 나타내는 도 5a의 부분 확대도이다.
도 5a 및 5b에 도시된 데이터로부터 알 수 있는 바와 같이, 650℃ 미만의 온도에서, 증발된 물질에서 PbCl2의 분율은 상당히 낮으며, 즉 증발된 물질은 거의 순수한 ZnCl2로 구성된다.
실시예 5:
BF 분진은 Zn + Pb의 총량이 Cl의 총량의 2배(몰 기준)와 거의 동일할 때까지 HCl 또는 FeCl2 용액에서 수합될 수 있다.
여과 또는 원심 분리(및 선택적으로 건조) 후, 비-산화적 분위기에서 1000-1100℃의 온도에서의 열처리는 99% 초과의 Zn 및 Pb를 증발시키기에 충분하다.
열처리 후 수득된 고체 물질(~ 30% FeO, ~ 40% C, ~ 10% SiO2 및 일부 CaO, Al2O3 및 MgO를 포함함)은 철강 공정으로 재순환되거나 시멘트 생산용 철 공급원 및 연료로서 사용될 수 있다.
Claims (16)
- 염소를 포함하는 폐기물 또는 산업 부산물 (B)을 정제하는 방법으로서,
상기 방법은
a) 염소를 포함하는 폐기물 또는 산업 부산물 (B)을, 중금속 (HM)을 포함하는 하나 이상의 물질과 배합하거나 혼합함으로써 조성물 (C)을 제조하는 단계
b) (C)의 열처리에 의해 (B) 및 (HM)을 반응시키는 단계
c) 증발된 중금속 클로라이드 화합물 (HMCC)을 분리하는 단계
d) 열처리 단계 후 고체 물질을 수득하는 단계
를 포함하는, 방법. - 제1항에 있어서,
상기 열처리 단계 후 수득된 고체 물질은 산업 공정으로, 바람직하게는 시멘트 제조 공정 또는 야금(metallurgical) 공정으로 재순환되는, 방법. - 제1항 또는 제2항에 있어서,
염소를 포함하는 폐기물 또는 산업 부산물 (B)은 1 내지 30 질량%, 바람직하게는 2 내지 20 질량%, 보다 바람직하게는 3 내지 15 질량%의 클로라이드를 포함하는, 시멘트 제조로부터의 분진, 바람직하게는 시멘트 분진으로부터의 바이패스(bypass) 분진인 것을 특징으로 하는, 방법. - 제1항 내지 제3항 중 어느 한 항에 있어서,
상기 중금속 (HM)을 포함하는 물질은 0.1 질량% 초과, 바람직하게는 0.5 질량% 초과, 보다 바람직하게는 2 질량% 초과, 가장 바람직하게는 20 질량% 초과의 Zn 및/또는 Pb를 포함하는 것을 특징으로 하는, 방법. - 제1항 내지 제4항 중 어느 한 항에 있어서,
상기 중금속 (HM)을 포함하는 물질은 제철소 분진, 바람직하게는 제철소로부터 분진을 분리함으로써 수득되는 슬러지 또는 필터 케이크("Gichtgassschlamm"), 전로강(electrosteel) 제조로부터 수득되는 분진 또는 사용된 활성 탄소를 포함하거나 이로 구성되는 것을 특징으로 하는, 방법. - 제1항 내지 제5항 중 어느 한 항에 있어서,
상기 염소를 포함하는 폐기물 또는 산업 부산물 (B)은 클로라이드 공정에 따른 TiO2의 제조로부터 수득되는 폐(waster) 금속 클로라이드, 일메나이트(ilmenite)로부터 합성 루틸(rutile)의 제조로부터 수득되는 폐 금속 클로라이드, 강철 산세(pickling)로부터 수득되는 폐 철 클로라이드, 또는 바람직하게는 Fe, Zn 및/또는 Pb와 같은 금속을 포함하는 폐 염산이거나 이를 포함하는 것을 특징으로 하는, 방법. - 제1항 내지 제6항 중 어느 한 항에 있어서,
상기 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)의 비는, 조성물 (C)의 염소 함량이, 중금속 (HM)을 포함하는 물질 내 중금속 (HM)을 클로라이드로 화학양론적 전환시키는 데 필요한 양의 100% 내지 150%, 바람직하게는 100% 내지 130%, 가장 바람직하게는 100% 내지 110%인 것을 특징으로 하는, 방법. - 제1항 내지 제6항 중 어느 한 항에 있어서,
상기 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)의 비는, 조성물 (C)의 염소 함량이, 중금속 (HM)을 포함하는 물질 내 아연을 클로라이드로 화학양론적 전환시키는 데 필요한 양의 80% 내지 100%, 바람직하게는 90% 내지 99%, 가장 바람직하게는 90% 내지 95%인 것을 특징으로 하는, 방법. - 제1항 내지 제8항 중 어느 한 항에 있어서,
상기 중금속 (HM)을 포함하는 물질 및 염소를 포함하는 폐기물 또는 산업 부산물 (B)은 물의 존재 하에 혼합되거나 배합되고, 2 내지 50 질량%, 바람직하게는 5 내지 30 질량%, 보다 바람직하게는 10 내지 20 질량%의 물이 총 조성물 (C)에 존재하는 것을 특징으로 하는, 방법. - 제9항에 있어서,
상기 열처리는 500℃ 내지 900℃, 바람직하게는 500℃ 내지 850℃, 보다 바람직하게는 600℃ 내지 700℃의 온도에서 수행되는 것을 특징으로 하는, 방법. - 제1항 내지 제10항 중 어느 한 항에 있어서,
상기 열처리는 비-산화적 분위기 하에 수행되는 것을 특징으로 하는, 방법. - 제1항 내지 제11항 중 어느 한 항에 있어서,
ZnCl2는 비-산화적 분위기 하에 500℃ 내지 700℃, 바람직하게는 600℃ 내지 680℃의 온도에서 열처리를 수행함으로써 증발되는 것을 특징으로 하는, 방법. - 제1항 내지 제9항 중 어느 한 항에 있어서,
상기 열처리는 비-산화적 분위기 하에 1000℃ 내지 1200℃의 온도에서 수행되는 것을 특징으로 하는, 방법. - 제1항에 있어서,
염소를 포함하는 폐기물 또는 산업 부산물 (B)은 아연을 추가로 포함하고, 상기 방법은
a. 클로라이드, 바람직하게는 HCl 또는 FeCl2를 포함하는 용액을 공급하는 단계
b. 고로(blast furnace) 분진을 클로라이드를 포함하는 용액으로 통과시켜 고로 분진의 임의의 분획, 바람직하게는 미세 분획을 분리하고 수합하는 단계
c. 액체상으로부터 고체를 분리하는 단계
d. 고체 물질을 건조하고, 상기 고체 물질이 ZnCl2의 증발에 충분한 열처리를 받게 하는 단계
e. 상기 열처리로부터 수득된 물질을 수합하는 단계
를 포함하는 것을 특징으로 하는, 방법. - 제1항 내지 제14항 중 어느 한 항에 있어서,
아연 클로라이드의 용융점보다 높은 온도에서 기체상으로부터 상기 아연 클로라이드를 분리하고, 상기 아연 클로라이드를 액체로서 수득하는 것을 특징으로 하는, 방법. - 금속성 Zn으로의 전해(electrolytic) 전환, ZnS 안료의 제조, ZnO의 제조, 또는 미량 영양소 비료의 제조를 위한, 제1항 내지 제15항 중 어느 한 항에 따른 방법에 의해 수득되는 ZnCl2의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17189174.0 | 2017-09-04 | ||
| EP17189174.0A EP3450412A1 (en) | 2017-09-04 | 2017-09-04 | Process for the purification of waste metal chlorides by thermal treatment |
| PCT/EP2018/073761 WO2019043261A1 (en) | 2017-09-04 | 2018-09-04 | PROCESS FOR PURIFYING WASTE OR INDUSTRIAL BY-PRODUCTS COMPRISING CHLORINE |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200053524A true KR20200053524A (ko) | 2020-05-18 |
Family
ID=59997029
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207009759A KR20200053524A (ko) | 2017-09-04 | 2018-09-04 | 염소를 포함하는 폐기물 또는 산업 부산물의 정제 방법 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US11938527B2 (ko) |
| EP (2) | EP3450412A1 (ko) |
| JP (1) | JP2020532425A (ko) |
| KR (1) | KR20200053524A (ko) |
| WO (1) | WO2019043261A1 (ko) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102020202575A1 (de) | 2020-02-28 | 2021-09-02 | Thyssenkrupp Steel Europe Ag | Nachhaltiges Wiederaufarbeitungsverfahren von Hüttenwerksstäuben und -schlämmen zur Herstellung von eisenhaltigen, schwermetallabgereicherten Sekundärrohstoffen unter Rückgewinnung von Blei und Zink |
| CN114618868B (zh) * | 2022-03-10 | 2023-02-17 | 华中科技大学 | 一种高氯灰渣中含氯组分的固定方法 |
| WO2024046656A1 (en) | 2022-09-01 | 2024-03-07 | Tata Steel Ijmuiden B.V. | Process for heavy metal removal from iron- and steelmaking flue dust |
| CN115626785B (zh) * | 2022-10-31 | 2023-10-31 | 北京工业大学 | 一种固定重金属锌的方法 |
| US11873233B1 (en) * | 2023-06-20 | 2024-01-16 | King Faisal University | Preparing magnetite and akaganéite nanoparticles from steel slag as a raw material for wastewater treatment |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06174383A (ja) * | 1992-05-08 | 1994-06-24 | Techno Toriito:Kk | 電気炉ダスト類の処理法 |
| GB9215034D0 (en) * | 1992-07-15 | 1992-08-26 | Fray Derek J | Treatment of polyvinylchloride |
| JP3553671B2 (ja) * | 1994-12-28 | 2004-08-11 | 同和鉱業株式会社 | 重金属含有廃棄物の処理方法 |
| JPH11503492A (ja) * | 1995-04-13 | 1999-03-26 | レフィスタ・リサイクリング・アクチェンゲゼルシャフト | 工業プロセス及び廃棄物焼却において生じる残留物の処理方法 |
| US5906671A (en) * | 1996-10-25 | 1999-05-25 | Agglo Inc. | Method for extraction of metals and non-metals from minerals, industrial by-products and waste materials |
| JP2000301103A (ja) * | 1999-04-21 | 2000-10-31 | Shinsei Dental Laboratory:Kk | 焼却灰または飛灰の無害化処理方法 |
| EP1064982B1 (de) * | 1999-07-02 | 2004-12-22 | CTU - Conzepte Technik Umwelt AG | Verfahren zum Entfernen von Metallen aus Reststoffen |
| JP5224490B2 (ja) * | 2000-06-19 | 2013-07-03 | モーミー リサーチ アンド エンジニアリング,インコーポレイティド | 炉からの煙塵の処理方法 |
| JP2003211127A (ja) * | 2002-01-29 | 2003-07-29 | Taiheiyo Cement Corp | 塩化物含有ダストの処理方法 |
| JP4525009B2 (ja) | 2003-07-11 | 2010-08-18 | 住友金属工業株式会社 | ロータリーキルンによる廃棄物処理方法 |
| JP5168992B2 (ja) * | 2007-04-12 | 2013-03-27 | 住友金属鉱山株式会社 | ニッケル精製工程から発生する鉄澱物の処理方法 |
| JP4948429B2 (ja) * | 2008-01-11 | 2012-06-06 | 太平洋セメント株式会社 | 金属類及び塩素を含有する可燃性廃棄物の処理システム |
| AT511410A1 (de) | 2011-04-21 | 2012-11-15 | Holcim Technology Ltd | Verfahren zur behandlung und verwertung von bypass-stäuben aus dem zementherstellungsprozess |
| JP2014172765A (ja) * | 2013-03-06 | 2014-09-22 | Toho Titanium Co Ltd | チタン含有原料の高品位化方法 |
-
2017
- 2017-09-04 EP EP17189174.0A patent/EP3450412A1/en not_active Withdrawn
-
2018
- 2018-09-04 JP JP2020514245A patent/JP2020532425A/ja active Pending
- 2018-09-04 WO PCT/EP2018/073761 patent/WO2019043261A1/en unknown
- 2018-09-04 US US16/641,966 patent/US11938527B2/en active Active
- 2018-09-04 EP EP18766183.0A patent/EP3679003A1/en active Pending
- 2018-09-04 KR KR1020207009759A patent/KR20200053524A/ko not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| EP3450412A1 (en) | 2019-03-06 |
| US11938527B2 (en) | 2024-03-26 |
| US20200222954A1 (en) | 2020-07-16 |
| JP2020532425A (ja) | 2020-11-12 |
| EP3679003A1 (en) | 2020-07-15 |
| WO2019043261A1 (en) | 2019-03-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20200053524A (ko) | 염소를 포함하는 폐기물 또는 산업 부산물의 정제 방법 | |
| US5667553A (en) | Methods for recycling electric arc furnace dust | |
| US8012437B2 (en) | Process for separating iron from other metals in iron containing feed stocks | |
| US4159310A (en) | Process for recovering aluminum and other metal values from fly ash | |
| KR101394521B1 (ko) | 전기로 제강분진의 처리방법 | |
| CN101341265A (zh) | 锌浸出残渣中有价金属的分离 | |
| JP3727232B2 (ja) | 亜鉛回収法 | |
| EP2875162A1 (en) | A method for the extraction of vanadiumpentoxide v2o5, from a source containing vanadium | |
| US6932853B2 (en) | Mechanical separation of volatile metals at high temperatures | |
| CA2182168C (en) | Process for treating solid waste containing volatilizable inorganic contaminants | |
| JPS5942059B2 (ja) | Zn含有物からZn分を回収する方法 | |
| JP2003147450A (ja) | 粗酸化亜鉛粉末の製造方法 | |
| US4288414A (en) | Process for chlorinating clays and bauxite | |
| JP2000016844A (ja) | ダイオキシンの熱分解方法および装置 | |
| JP7110128B2 (ja) | 洗煙排水中の水銀を除去する方法 | |
| US5411572A (en) | Method for utilizing smelter waste containing zinc and other valuable metals | |
| KR0138584B1 (ko) | 제강 분진의 처리방법. | |
| RU2205884C1 (ru) | Способ пирометаллургической переработки медьсодержащего сырья | |
| WO2024046656A1 (en) | Process for heavy metal removal from iron- and steelmaking flue dust | |
| JP2023515958A (ja) | 鉛と亜鉛を回収して、重金属を除去した鉄含有再生材料を生産するために、精錬所のダストおよびスラッジをリサイクルするための持続可能な方法 | |
| RU2588218C2 (ru) | Способ гидрометаллургической переработки цинксодержащих пылей металлургического производства | |
| JP2002332529A (ja) | 粗酸化亜鉛のフッ素除去方法 | |
| PL227662B1 (pl) | Sposób odseparowania metali obecnych w pyłach pochodzących z elektrycznych pieców łukowych. | |
| JP2009228066A (ja) | 焼結機煙灰からのカドミウムの浸出方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |