KR20180098131A - 액정 조성물 - Google Patents
액정 조성물 Download PDFInfo
- Publication number
- KR20180098131A KR20180098131A KR1020180010012A KR20180010012A KR20180098131A KR 20180098131 A KR20180098131 A KR 20180098131A KR 1020180010012 A KR1020180010012 A KR 1020180010012A KR 20180010012 A KR20180010012 A KR 20180010012A KR 20180098131 A KR20180098131 A KR 20180098131A
- Authority
- KR
- South Korea
- Prior art keywords
- formula
- liquid crystal
- carbon atoms
- chemical formula
- independently
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/42—Mixtures of liquid crystal compounds covered by two or more of the preceding groups C09K19/06 - C09K19/40
- C09K19/44—Mixtures of liquid crystal compounds covered by two or more of the preceding groups C09K19/06 - C09K19/40 containing compounds with benzene rings directly linked
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/12—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings at least two benzene rings directly linked, e.g. biphenyls
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/14—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a carbon chain
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3028—Cyclohexane rings in which at least two rings are linked by a carbon chain containing carbon to carbon single bonds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3048—Cyclohexane rings in which at least two rings are linked by a carbon chain containing carbon to carbon double bonds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3086—Cyclohexane rings in which at least two rings are linked by a chain containing nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3009—Cy-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/301—Cy-Cy-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3016—Cy-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3019—Cy-Cy-Ph-Ph
Landscapes
- Chemical & Material Sciences (AREA)
- Crystallography & Structural Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Liquid Crystal Substances (AREA)
Abstract
본 발명은 액정 조성물 및 액정 표시 장치에 관한 것이다. 본 발명의 액정 조성물은 고유전율 이방성, 및 고굴절률 이방성을 나타낼 수 있다. 이에 따라, 상기 액정 조성물을 이용하면 낮은 문턱 전압을 가지며 고속 응답이 가능하고 넓은 온도 범위에서 동작할 수 있는 액정 표시 장치를 제공할 수 있다.
Description
본 발명은 고유전율 이방성, 및 고굴절률 이방성을 가지는 액정 조성물에 관한 것이다.
액정 표시 장치(LCD)는 시계, 전자 계산기를 비롯하여 각종 전기 기기, 측정 기기, 자동차용 패널, 워드 프로세서, 전자 수첩, 프린터, 컴퓨터, 텔레비전 등에 사용되고 있다. 액정 표시 방식에는 대표적으로 TN(Twist nematic), STN(Super-twisted nematic), IPS(In-plane switching), FFS(Fringe field switching) 및 VA(Virtical alignment) 등이 있다.
이러한 액정 표시 장치에 사용되는 액정 재료는 저전압 구동 및 고속 응답이 가능하며, 넓은 온도 범위에서 동작 가능할 것이 요구된다. 구체적으로, 넓은 온도 범위에서 안정적으로 구동하기 위하여 액정 재료는 약 -20℃ 이하에서 안정적인 제반 물성을 나타내며(저온 안정성), 약 70℃ 이상의 투명점을 가질 것이 요구된다. 그리고, 저전압 구동 및 고속 응답을 위하여, 액정 재료는 유전율 이방성의 절대값이 크고, 회전 점도가 작으며, 적절한 탄성 계수(K11, K22, K33 평균값)를 가질 것이 요구된다.
이와 같은 액정 재료의 요구 물성은 1 내지 2 종류의 액정 화합물을 사용하여 만족시키는 것은 불가능하며, 통상적으로 7 내지 20 종류의 액정 화합물을 배합하여 충족시키고 있다.
한편, 상기 액정 표시 방식 중 수직 전계 모드(Virtical alignment,VA)의 액정 표시 장치는 범용의 IPS, TN이나 STN과 달리 유전율 이방성이 음(-)인 액정 재료를 사용한다는 특징을 갖는다. 그러나, 유전율 이방성이 음인 네가티브 액정 재료는 분자 측면에 극성 치환기가 존재하여 포지티브 액정 재료에 비하여 유전율 이방성을 조금만 변화시켜도 회전 점도가 크게 상승하는 문제가 있다. 이에 따라, 고속 응답이 가능한 VA형 액정 표시 장치를 제공하기 위하여 유전율 이방성이 음이며, 절대값이 크고, 점성이 낮은 액정 화합물의 개발이 요구되고 있다.
본 발명은 고유전율 이방성 및 고굴절률 이방성을 가지는 액정 조성물을 제공하기 위한 것이다.
또한, 본 발명은 상기 액정 조성물을 포함하는 액정 표시 장치를 제공하기 위한 것이다.
상기 과제를 해결하기 위하여, 본 발명은 적어도 하나의 하기 화학식 1로 표시되는 액정 화합물; 및 적어도 하나의 하기 화학식 2로 표시되는 액정 화합물을 포함하는 액정 조성물을 제공한다:
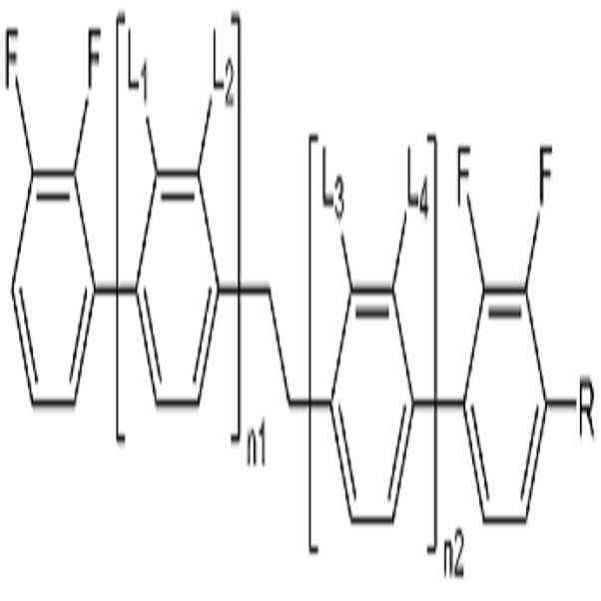
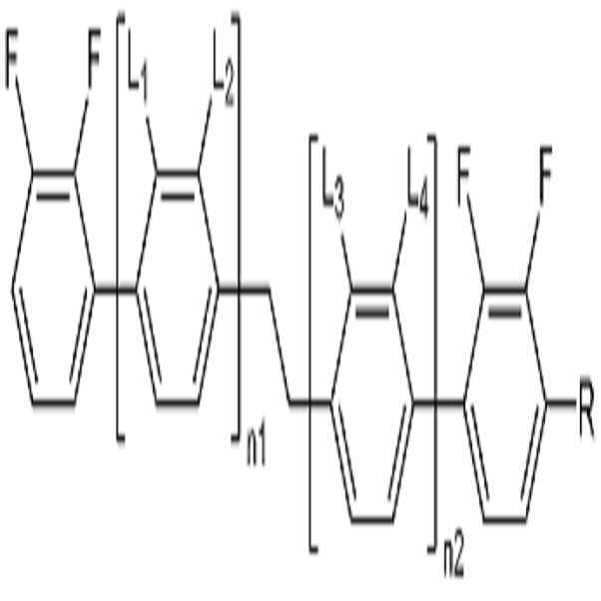
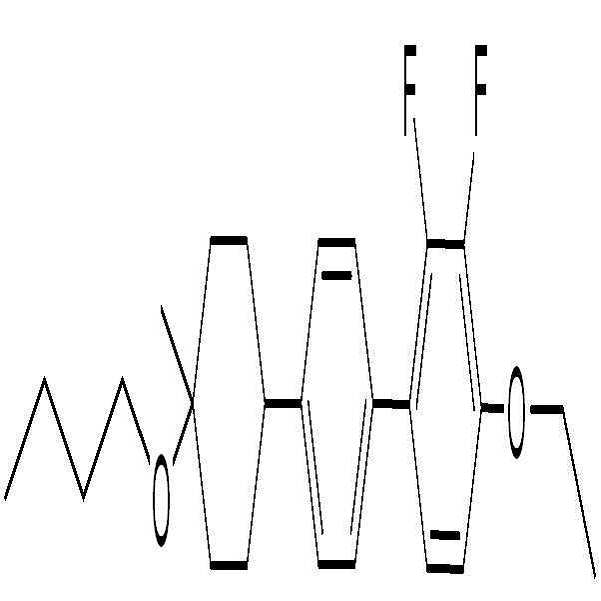
[화학식 1]
상기 화학식 1에서,
L1, L2, L3 및 L4는 각각 독립적으로 수소 또는 할로겐이고,
R은 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시이고, 및
n1 및 n2는 각각 독립적으로 0 내지 2의 정수이고, n1 및 n2의 합은 0 이상 2 이하이고,
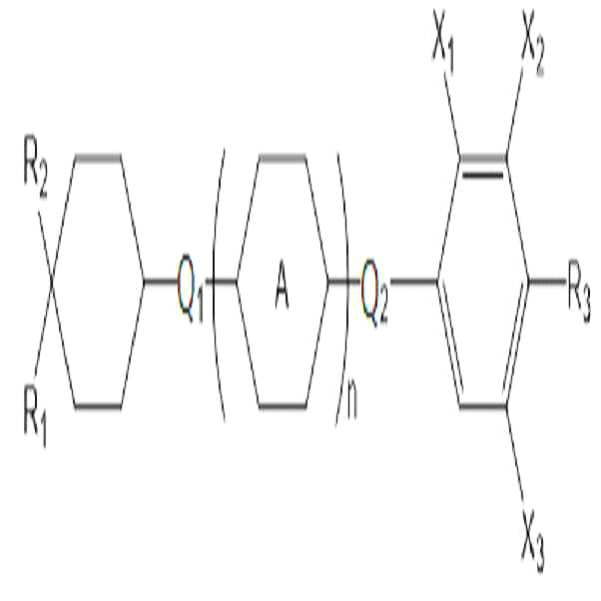
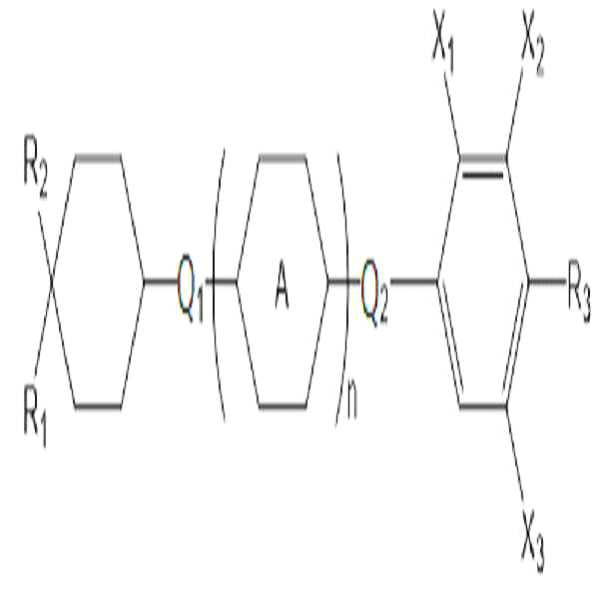
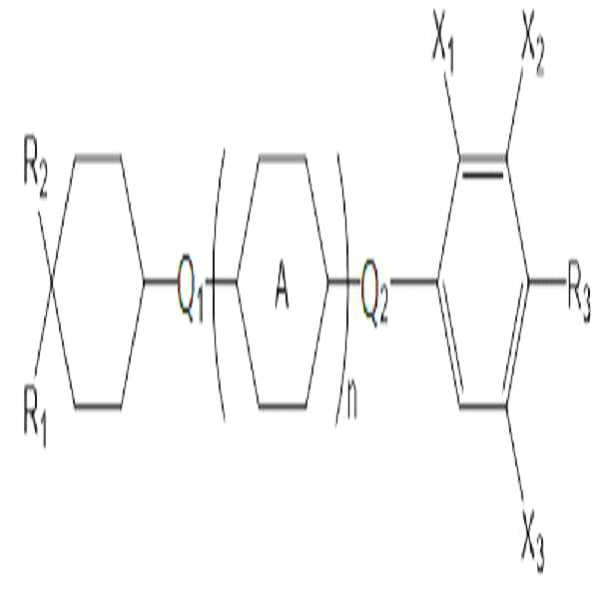
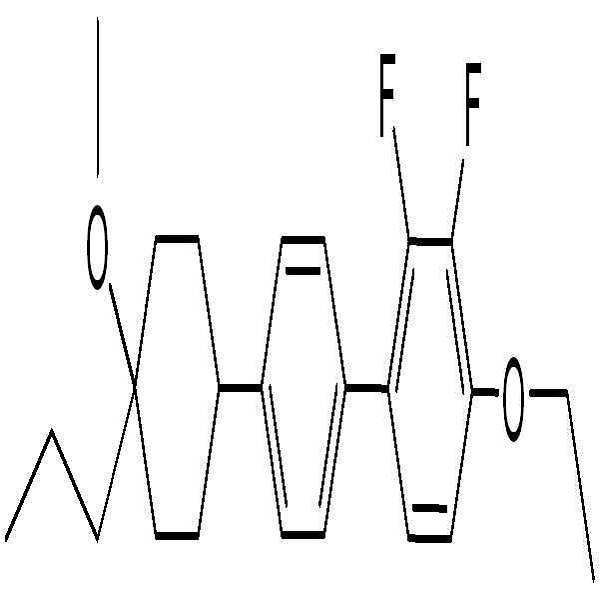
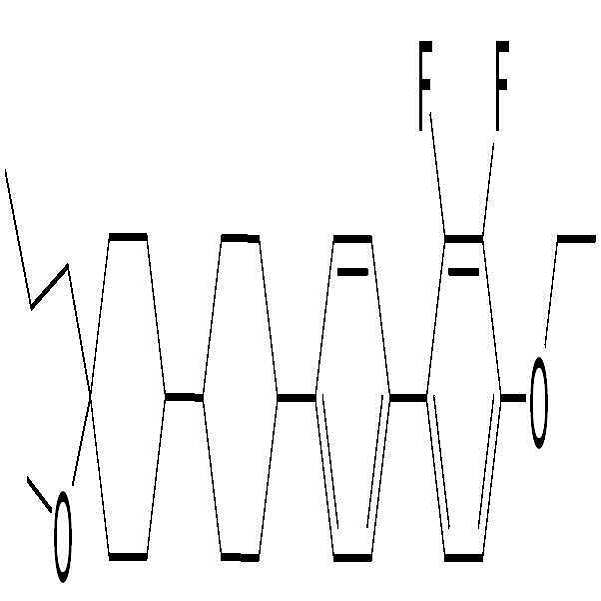
[화학식 2]
상기 화학식 2에서,
R1은 탄소수 2 내지 10의 알킬 또는 탄소수 1 내지 10의 알콕시이고,
R2는 탄소수 1 내지 10의 알킬 또는 탄소수 1 내지 10의 알콕시이고,
R3은 탄소수 1 내지 10의 알킬, 탄소수 1 내지 10의 알콕시, 또는 탄소수 2 내지 10의 알케닐이고,
고리 A는 사이클로헥실렌 또는 페닐렌이고,
Q1 및 Q2는 각각 독립적으로 단일 결합, -CH2O-, -OCH2-, -CH2CH2-, -CH=CH-, -C≡C-, -CH2CF2-, -CHFCHF-, -CF2CH2-, -CH2CHF-, -CHFCH2-, -CF2CF2-, -COO-, -OCO-, -CF2O-, -OCF2- 또는 -O-이고,
X1 내지 X3는 각각 독립적으로 수소, 할로겐, 또는 탄소수 1 내지 4의 할로알킬이고,
n은 0 내지 2의 정수이다.
또한, 본 발명은 상기 액정 조성물을 포함하는 액정 표시 장치를 제공한다.
본 발명의 일 구현예에 따른 액정 조성물은 높은 상전이온도를 가지며 충분한 굴절률 이방성 및 유전율 이방성을 나타낼 수 있다. 이에 따라, 상기 액정 조성물을 이용하면 낮은 문턱 전압을 가지며 고속 응답이 가능하고 넓은 온도 범위에서 동작할 수 있는 액정 표시 장치를 제공할 수 있다.
본 발명에 따른 액정 조성물은 고유전율 이방성, 고굴절률 이방성을 가지며, 따라서 다양한 액정 표시 장치에 적용될 수 있다. 비제한적인 예로, 수직 전계 모드(예를 들면, VA, MVA, PVA, PS-VA 등) 뿐 아니라, 수평 전계 모드(예를 들면, IPS, PLS, FFS, 등), TN 모드 등 다양한 모드의 액정 표시 장치에 최적화된 액정 조성물을 제공할 수 있다.
도 1은 일 구현예에 따른 액정 표시 장치의 구조를 모식적으로 나타낸 도면이다.
이하 발명의 구체적인 구현예에 따른 액정 조성물과 이를 포함하는 액정 표시 장치 등에 대해 설명하기로 한다.
본 발명의 일 구현예에 따른 액정 조성물은, 적어도 하나의 하기 화학식 1로 표시되는 액정 화합물; 및 적어도 하나의 하기 화학식 2로 표시되는 액정 화합물을 포함한다:
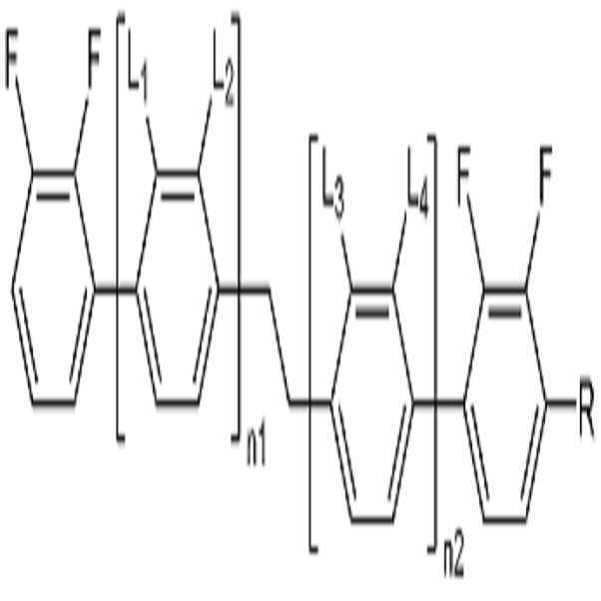
[화학식 1]
상기 화학식 1에서,
L1, L2, L3 및 L4는 각각 독립적으로 수소 또는 할로겐이고,
R은 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시이고, 및
n1 및 n2는 각각 독립적으로 0 내지 2의 정수이고, n1 및 n2의 합은 0 이상 2 이하이고,
[화학식 2]
상기 화학식 2에서,
R1은 탄소수 2 내지 10의 알킬 또는 탄소수 1 내지 10의 알콕시이고,
R2는 탄소수 1 내지 10의 알킬 또는 탄소수 1 내지 10의 알콕시이고,
R3은 탄소수 1 내지 10의 알킬, 탄소수 1 내지 10의 알콕시, 또는 탄소수 2 내지 10의 알케닐이고,
고리 A는 사이클로헥실렌 또는 페닐렌이고,
Q1 및 Q2는 각각 독립적으로 단일 결합, -CH2O-, -OCH2-, -CH2CH2-, -CH=CH-, -C≡C-, -CH2CF2-, -CHFCHF-, -CF2CH2-, -CH2CHF-, -CHFCH2-, -CF2CF2-, -COO-, -OCO-, -CF2O-, -OCF2- 또는 -O-이고,
X1 내지 X3는 각각 독립적으로 수소, 할로겐, 또는 탄소수 1 내지 4의 할로알킬이고,
n은 0 내지 2의 정수이다.
상기 화학식 1로 표시되는 액정 화합물은, 음의 유전율 이방성을 가지는 액정 화합물로서, 페닐기를 에틸렌(-CH2-CH2-)으로 연결함에 따라 액정의 점도를 낮출 수 있으며, 이에 따라 액정상을 최적화할 수 있다.
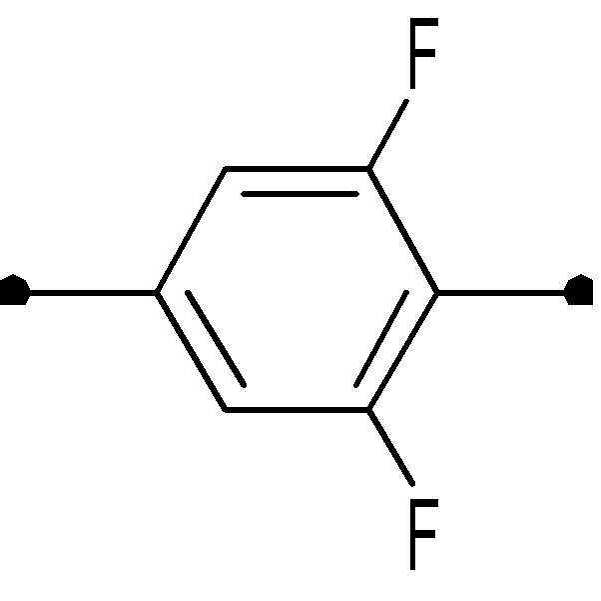
또한, 상기 화학식 1의 양말단은 2,3-디플루오로페닐기를 가지고, 적어도 하나의 말단에는 치환기로 알킬기를 가지지 않으며, 이러한 구조에 의하여 음의 유전율 이방성을 가질 수 있으며, 높은 유전율 값을 나타낼 수 있다. 또한, 상기 화학식 1의 액정 화합물은 벤젠 고리만으로 구성되어 있고, n1 및 n2에 따라 벤젠 고리의 개수를 조절하여 높은 굴절률 이방성 값을 가질 수 있으며, 따라서 액정 표시 장치의 빠른 응답 속도를 구현할 수 있다.
바람직하게는, 상기 L1, L2, L3 및 L4는 각각 독립적으로 수소 또는 플루오로이다. 또한 바람직하게는, 상기 L1 및 L2가 동일하다. 또한 바람직하게는, 상기 L3 및 L4가 동일하다. 예컨대, L1 및 L2가 모두 수소이거나, 또는 모두 플루오로일 수 있다. 또한 L3 및 L4가 모두 수소이거나, 또는 모두 플루오로일 수 있다. 또한, L1, L2, L3 및 L4가 모두 수소일 수 있다. 또한, L1, L2, L3 및 L4가 모두 플루오로일 수 있다.
또한 바람직하게는, R은 수소, 메틸, 에틸, 메톡시 또는 에톡시이다.
또한, n1 및 n2의 합이 0 이상 2 이하이므로, 상기 액정 화합물은 벤젠 고리를 2개, 3개 또는 4개를 가질 수 있다.
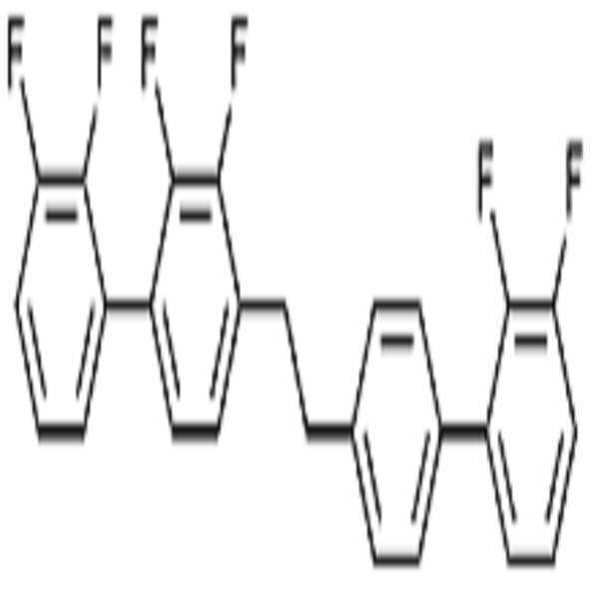
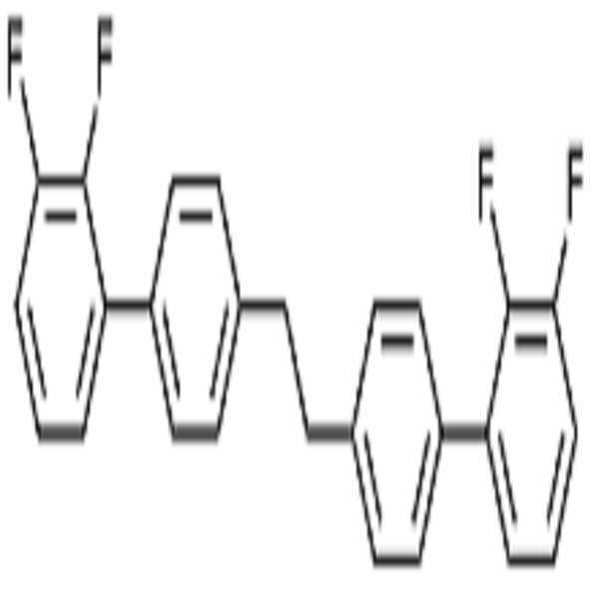
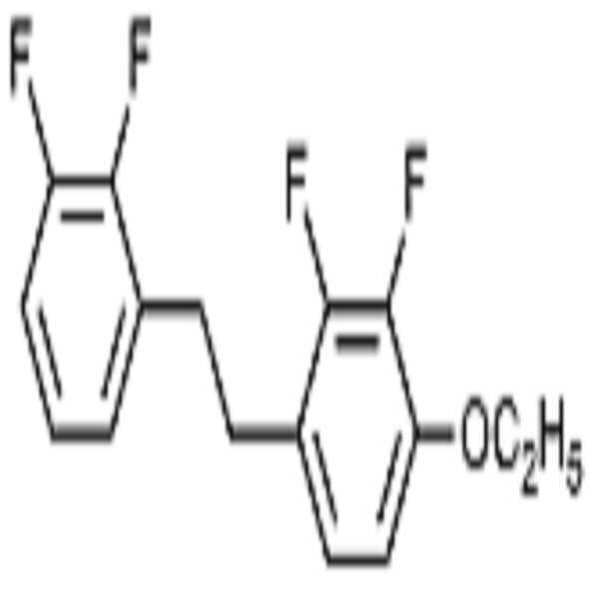
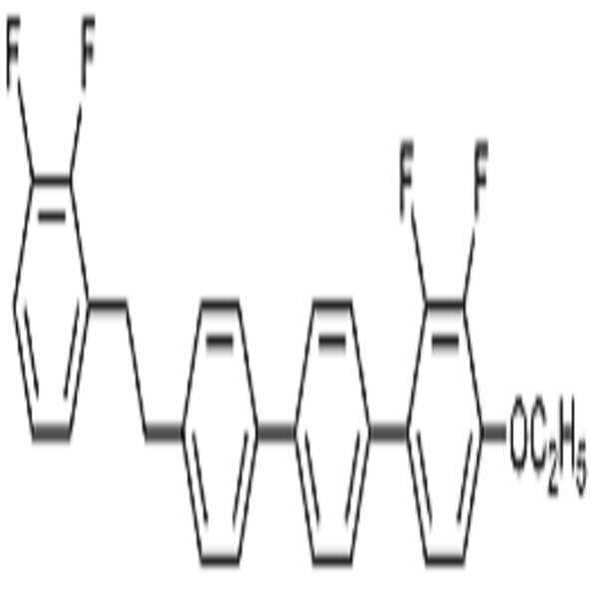
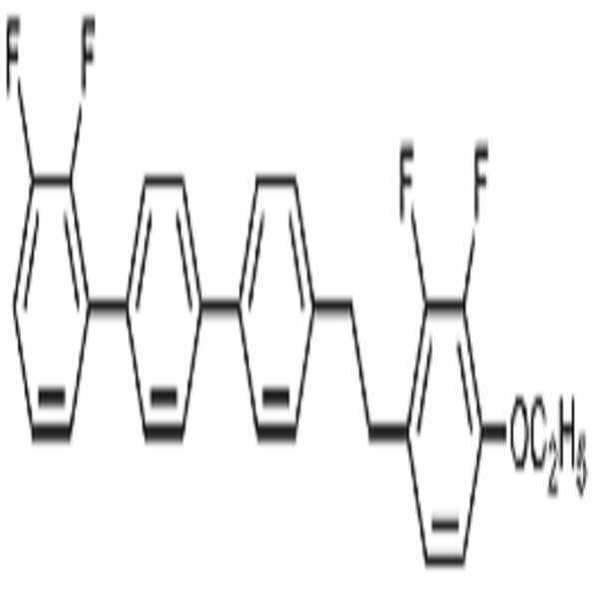
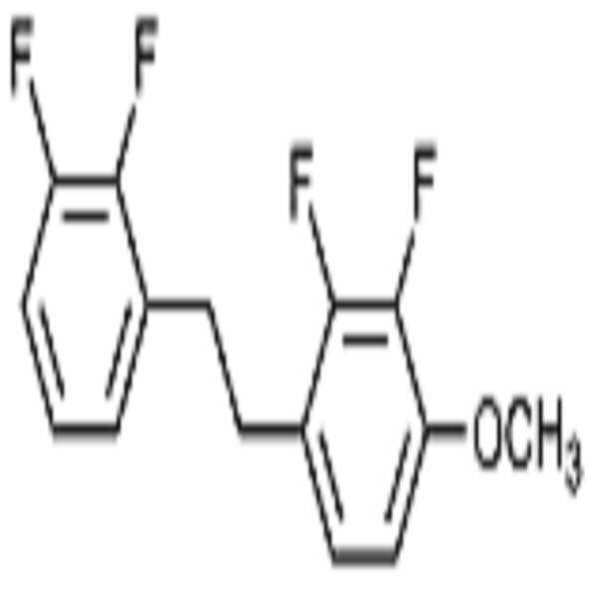
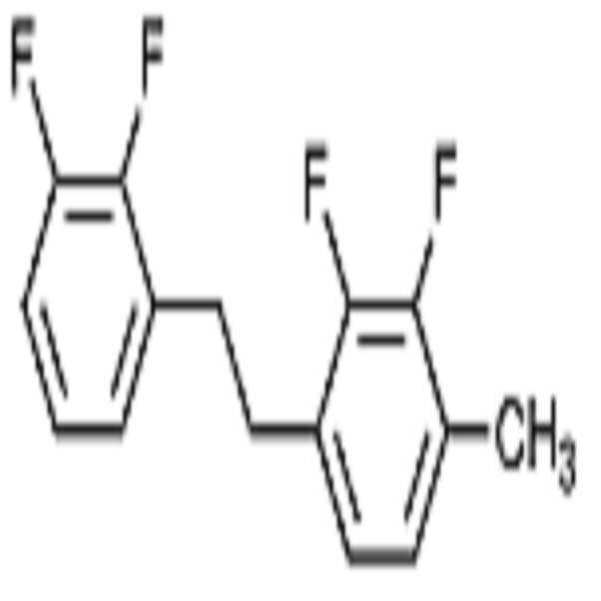
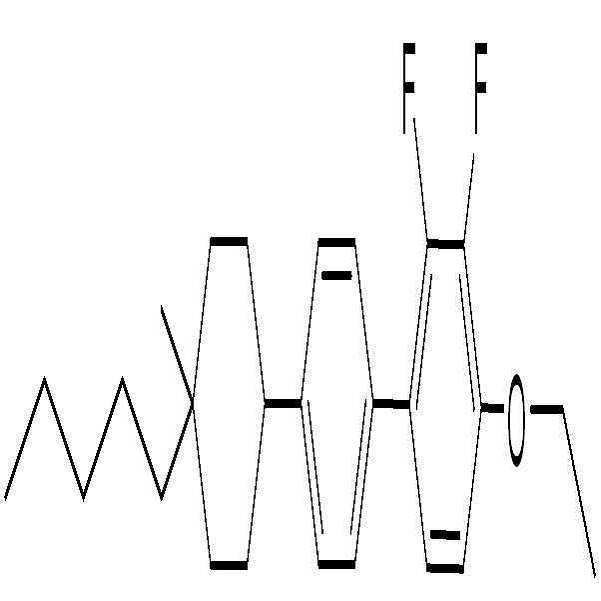
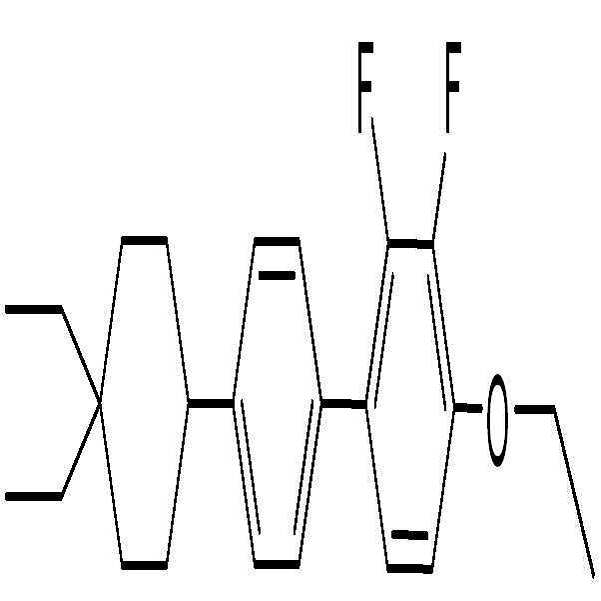
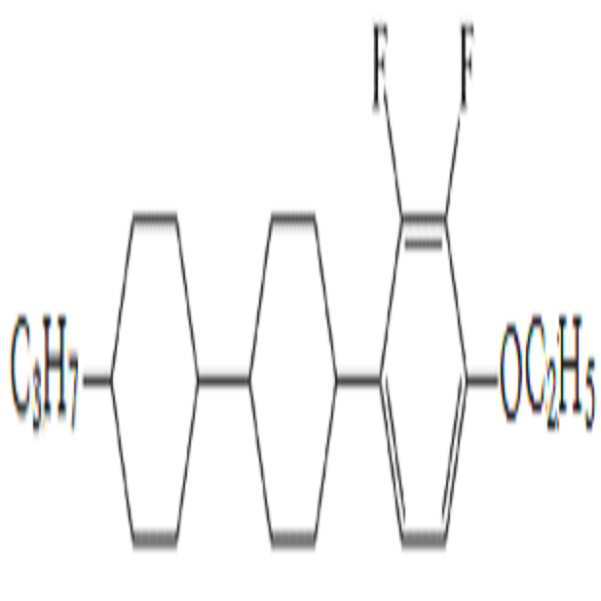
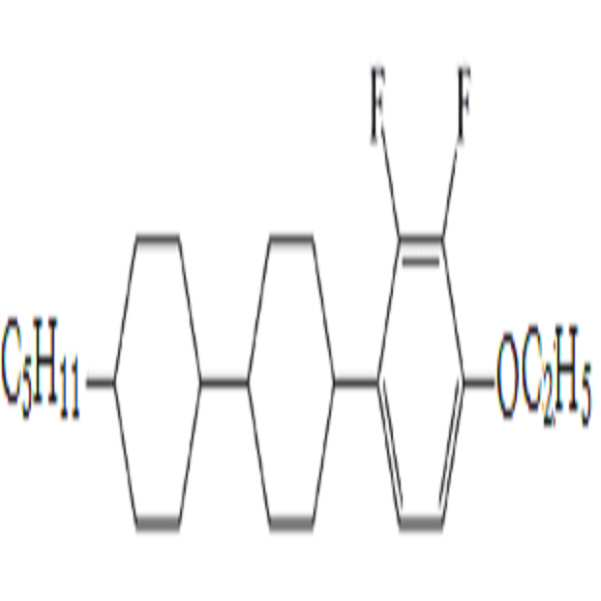
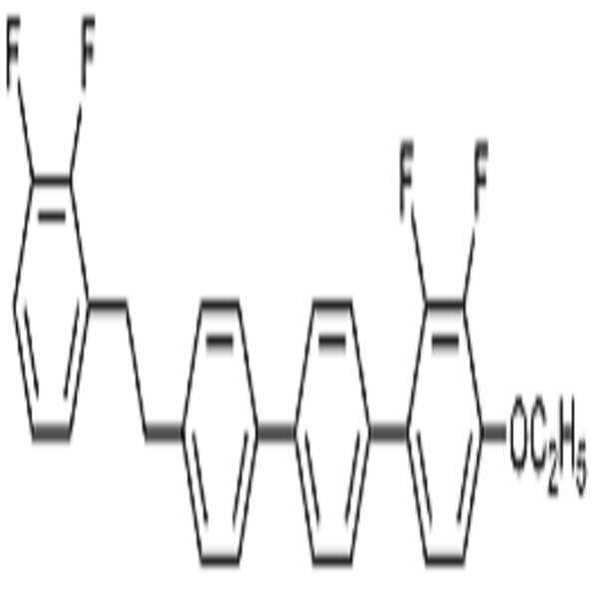
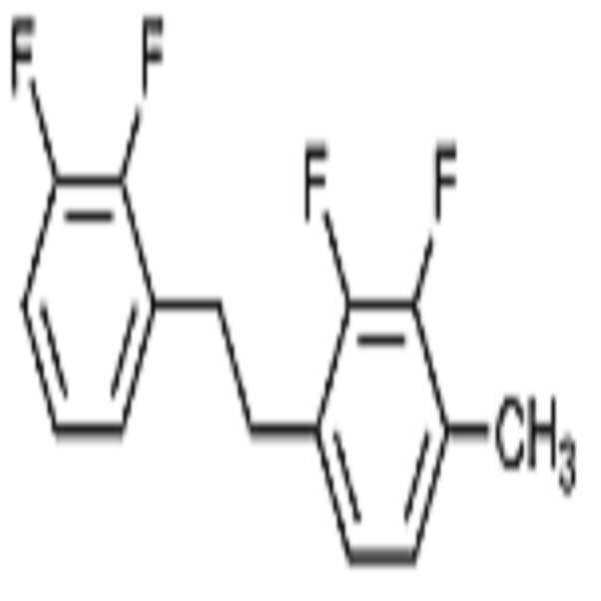
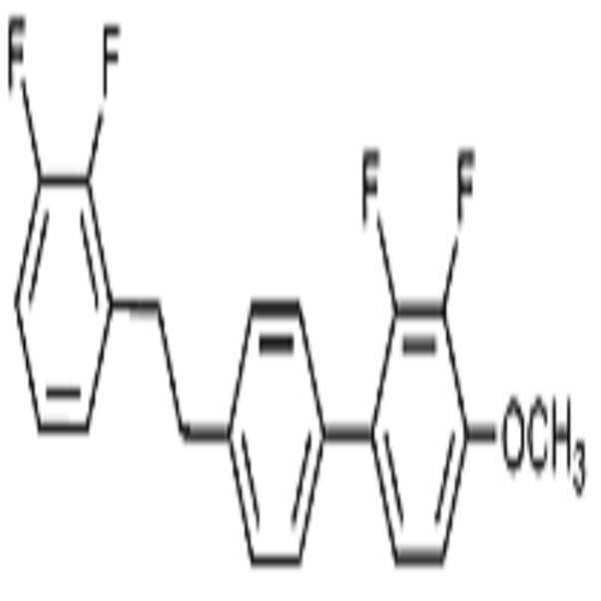
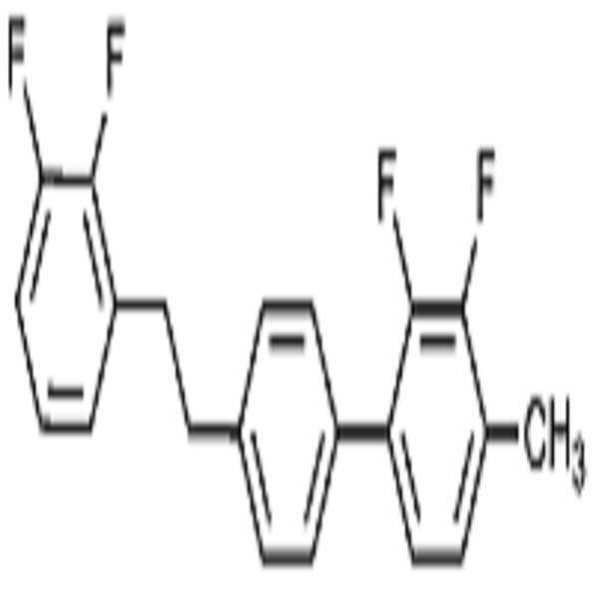
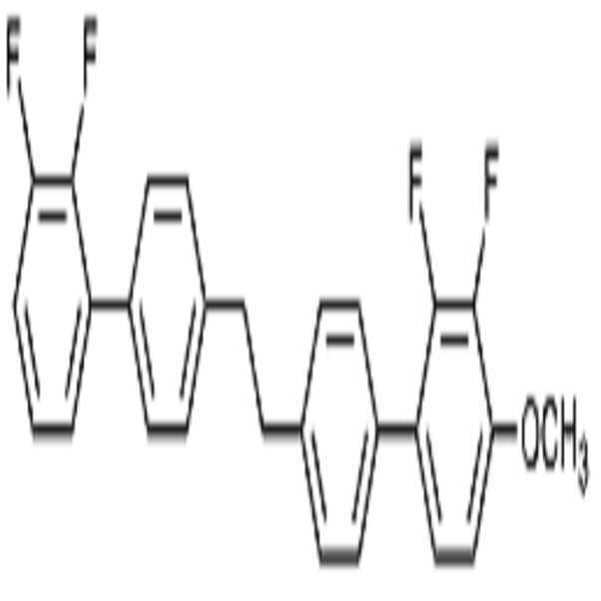
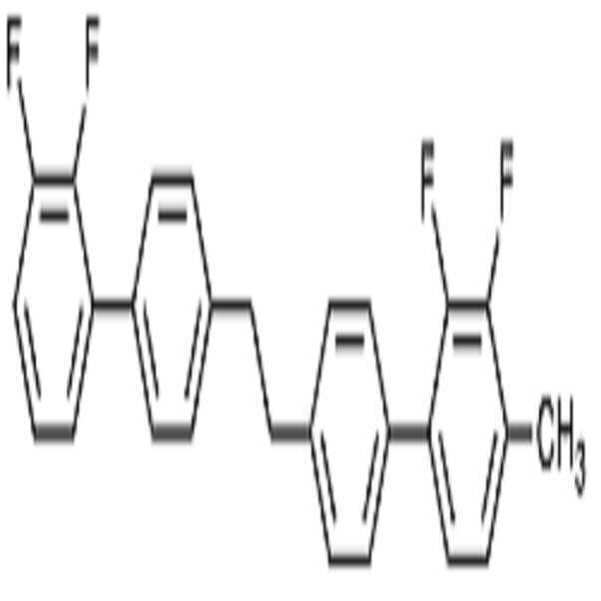
상기 화학식 1로 표시되는 액정 화합물의 대표적인 예는 하기 화학식 1-1 내지 1-17로 표시되는 화합물 중 하나 이상일 수 있으나, 본 발명이 이에 한정되는 것은 아니다.
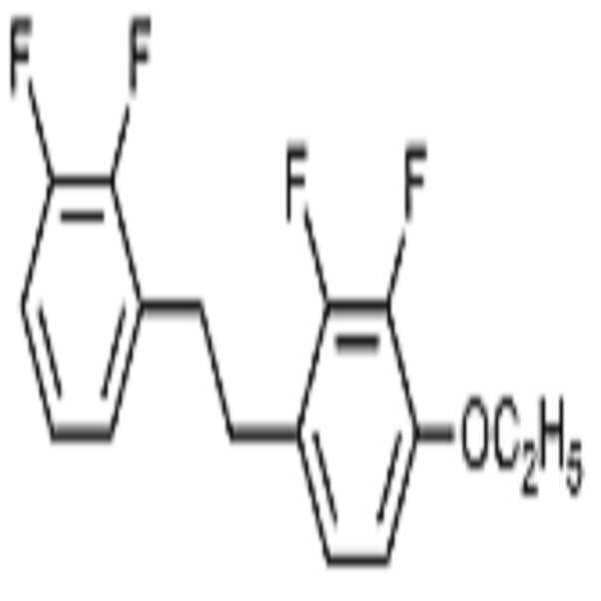
[화학식 1-1]
[화학식 1-2]
[화학식 1-3]
[화학식 1-4]
[화학식 1-5]
[화학식 1-6]
[화학식 1-7]
[화학식 1-8]
[화학식 1-9]
[화학식 1-10]
[화학식 1-11]
[화학식 1-12]
[화학식 1-13]
[화학식 1-14]
[화학식 1-15]
[화학식 1-16]
[화학식 1-17]
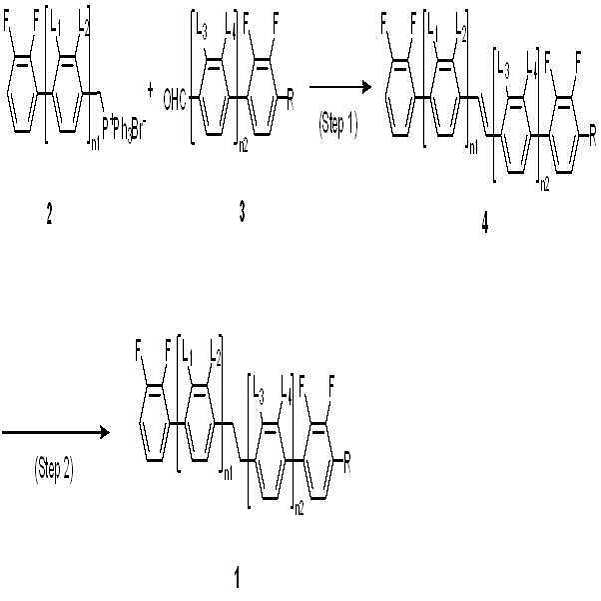
상기 화학식 1로 표시되는 액정 화합물은 하기 반응식 1과 같은 제조 방법에 의해 제조될 수 있으나, 본 발명이 이에 한정되는 것은 아니다.
[반응식 1]
상기 반응식 1에서, L1, L2, L3, L4, R, n1 및 n2는 앞서 화학식 1에서 정의한 바와 같다.
또한, 본 발명의 액정 조성물은 액정 조성물 전체 중량에 대하여 2 중량% 이상, 또는 3 중량% 이상, 또는 4 중량% 이상으로 상기 화학식 1로 표시되는 1종 이상의 액정 화합물을 포함할 수 있다. 상기 화학식 1로 표시되는 액정 화합물의 함량이 상기 범위 미만이면, 이로 인한 응답 속도의 향상 효과가 미미할 수 있다. 또한, 상기 액정 조성물은 액정 조성물 전체 중량에 대하여 20 중량% 이하, 15 중량% 이하, 10 중량% 이하, 또는 8 중량% 이하로 상기 화학식 1로 표시되는 1 종 이상의 액정 화합물을 포함할 수 있다. 상기 화학식 1로 표시되는 액정 화합물의 함량이 상기 범위를 초과하면, 액정 조성물의 상전이 온도가 크게 증가되어 저온 영역에서 액정상을 확보할 수 없다는 문제가 초래될 수 있다.
상기 화학식 2로 표시되는 액정 화합물은, 말단에 위치한 4,4-이치환사이클로헥실기의 치환기의 조절에 따라 액정의 점도 및 제반 물성이 조절될 수 있으며, 이에 따라 액정상이 최적화될 수 있다.
구체적으로, 말단의 사이클로헥실기의 4번 위치 치환기 중 하나가 알킬인 경우 다른 치환기의 탄소수가 감소할수록 높은 투명점 및 높은 굴절률 이방성 값을 나타낼 수 있다. 또한, 말단의 사이클로헥실기의 4번 위치 치환기 중 하나가 알콕시인 경우 다른 치환기의 탄소수가 증가할수록 높은 투명점, 높은 굴절률 이방성 값 및 높은 유전율 이방성 값을 나타낼 수 있다. 따라서, 상기 액정 화합물은 말단의 사이클로헥실기의 치환기가 고정된 경우에 비하여 2 개의 치환기를 조절함으로써 다양하게 요구되는 굴절률 이방성, 유전율 이방성 등의 물성 수치를 구현할 수 있다.
예를 들어, 상기 R1은 탄소수 2 내지 5의 알킬 또는 탄소수 1 내지 5의 알콕시일 수 있고, 상기 R2 및 R3는 각각 독립적으로 탄소수 1 내지 5의 알킬 또는 탄소수 1 내지 5의 알콕시일 수 있다.
구체적으로, 상기 R1은 탄소수 2 내지 5의 알킬이고, R2는 탄소수 1 내지 5의 알킬이거나; 상기 R1은 탄소수 2 내지 5의 알킬이고, R2는 탄소수 1 내지 5의 알콕시이거나; 또는 상기 R1은 탄소수 1 내지 5의 알콕시이고, R2는 탄소수 1 내지 5의 알킬일 수 있다. 예컨대, 상기 R1 및 R2는 모두 에틸일 수 있다.
다르게는, 상기 R1은 에틸, 프로필, 부틸, 또는 펜틸이고, R2는 메틸 또는 메톡시일 수 있다. 또한 다르게는, 상기 R1은 메톡시, 에톡시, 프로폭시, 부톡시, 또는 펜톡시이고, R2는 메틸일 수 있다.
이 때, 상기 R3은 메틸, 에틸, 메톡시, 에톡시, 비닐, 또는 1-프로페닐일 수 있다.
또한, 상기 Q1 및 Q2는 각각 단일 결합일 수 있다. 여기서, 단일 결합이라 함은 Q1 및 Q2로 표시되는 부분에 별도의 원자가 존재하지 않는 경우를 의미한다. 일 예로, 화학식 2에서 Q1이 단일 결합이고, 고리 A가 페닐렌인 경우, 사이클로헥산 고리는 벤젠 고리와 직접 연결되어 사이클로헥실 벤젠 구조를 형성할 수 있다.
또한, 상기 X1 내지 X3는 각각 독립적으로 수소, 할로겐, 또는 탄소수 1 또는 2의 할로알킬일 수 있다. 여기서, 할로알킬이라 함은, 하나 이상의 할로겐으로 치환된 알킬을 의미한다.
예를 들어, 상기 X1 내지 X3는 각각 독립적으로 수소, 플루오로, 또는 트리플루오로메틸일 수 있다. 예를 들어, 상기 X1 및 X2는 각각 플루오로이고, X3는 수소일 수 있다.
다르게는, 상기 X1 및 X3는 각각 수소이고, X2는 플루오로일 수 있다. 또한 다르게는, 상기 X1 및 X2는 각각 수소이고, X3는 플루오로일 수 있다. 또한 다르게는, 상기 X1은 수소이고, X2 및 X3는 각각 플루오로일 수 있다. 이 중, 음의 유전율 이방성 및 높은 유전율 값 구현 측면에서 상기 X1 및 X2는 각각 플루오로이고, X3는 수소일 수 있다.
또한 다르게는, 상기 X1 내지 X3는 모두 수소일 수 있다. 이 경우, 비극성 내지 중성(neutral)이면서 높은 굴절률 이방성을 갖는 액정 화합물이 구현될 수 있다.
또한, 상기 n은 0일 수 있고, 이 때 상기 액정 화합물은 2 개의 고리를 가질 수 있다. 또한 다르게는, 상기 n은 1일 수 있고, 이 때 상기 액정 화합물은 3 개의 고리를 가질 수 있다.
또한 다르게는, 상기 n은 2일 수 있고, 이 때 상기 액정 화합물은 4 개의 고리를 가질 수 있다.
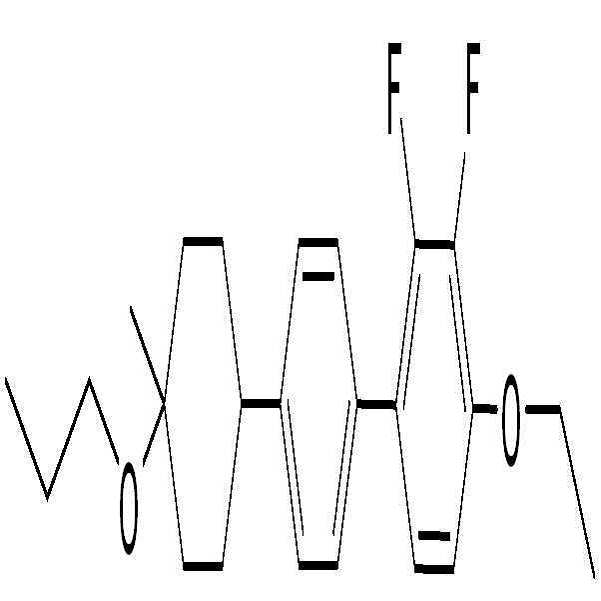
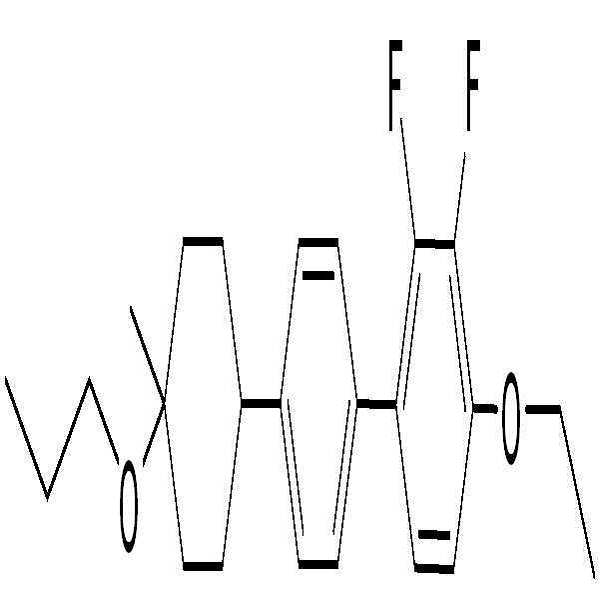
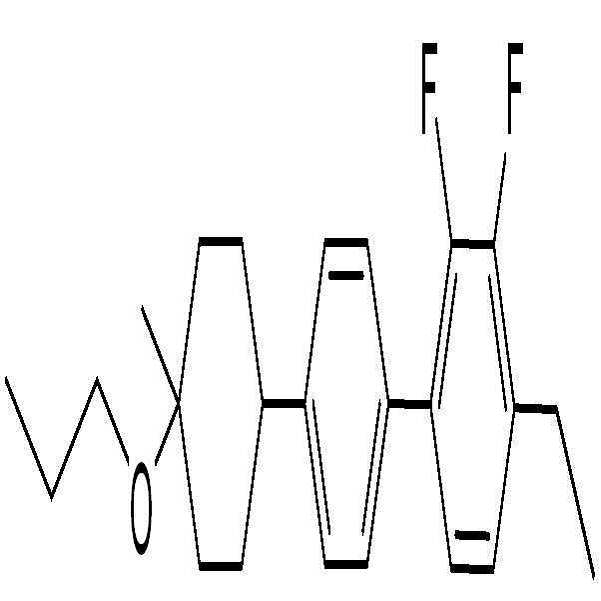
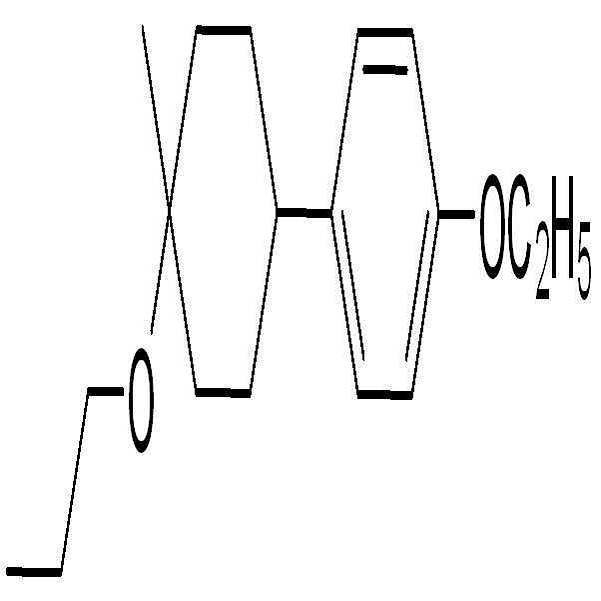
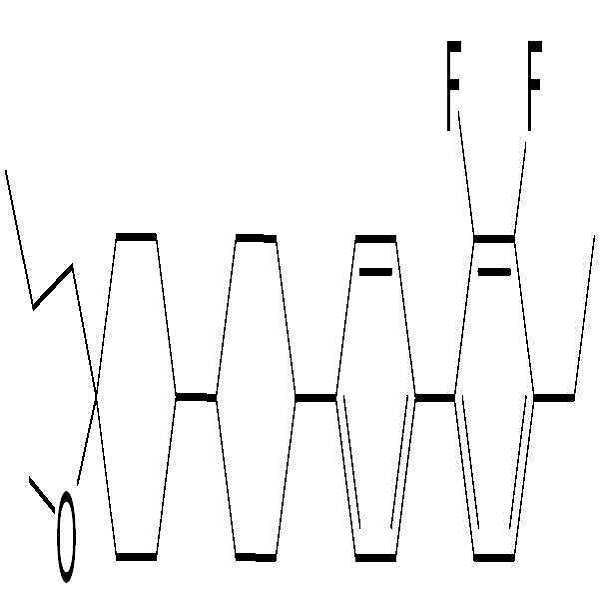
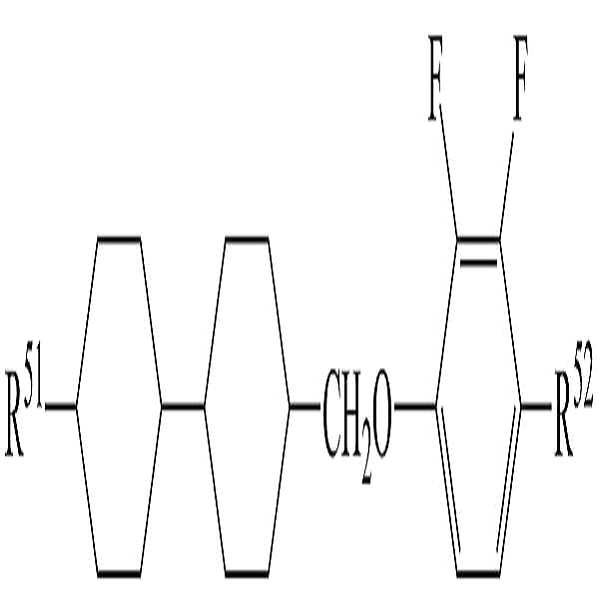
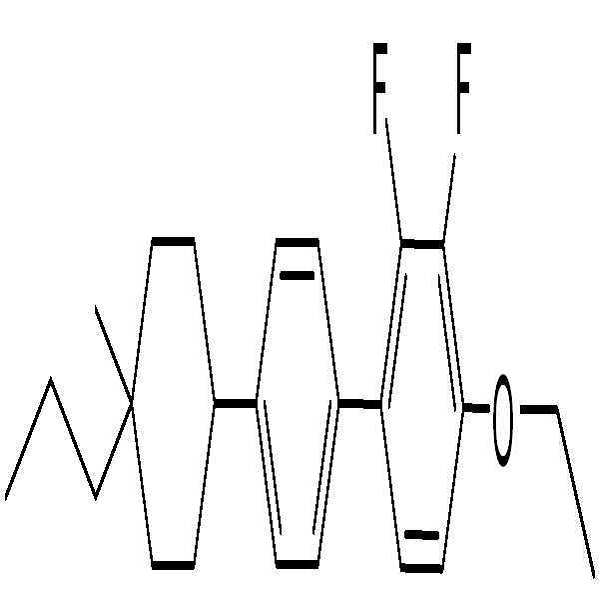
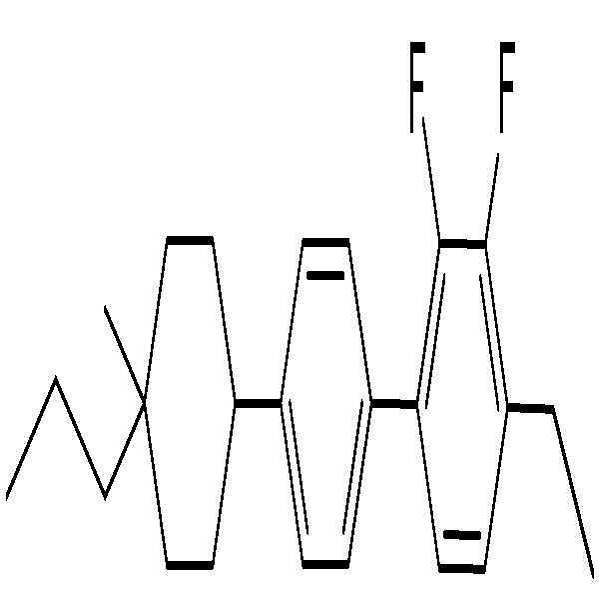
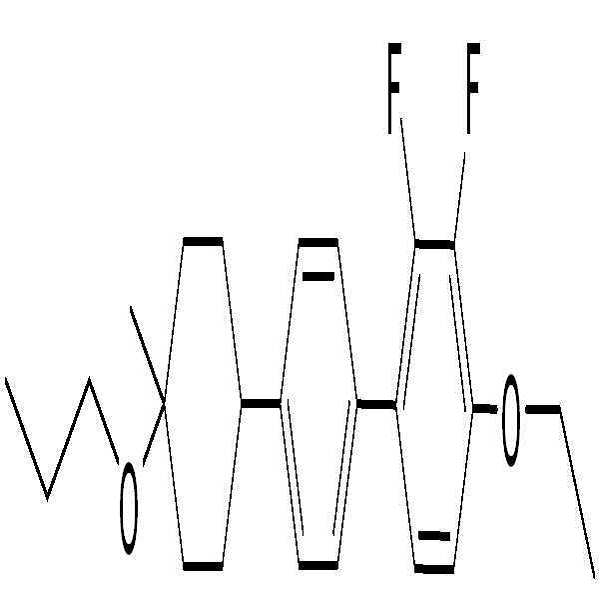
상기 화학식 2로 표시되는 액정 화합물의 대표적인 예는 하기 화학식 2-1 내지 2-20으로 표시되는 화합물 중 하나일 수 있으나, 본 발명이 이에 한정되는 것은 아니다.
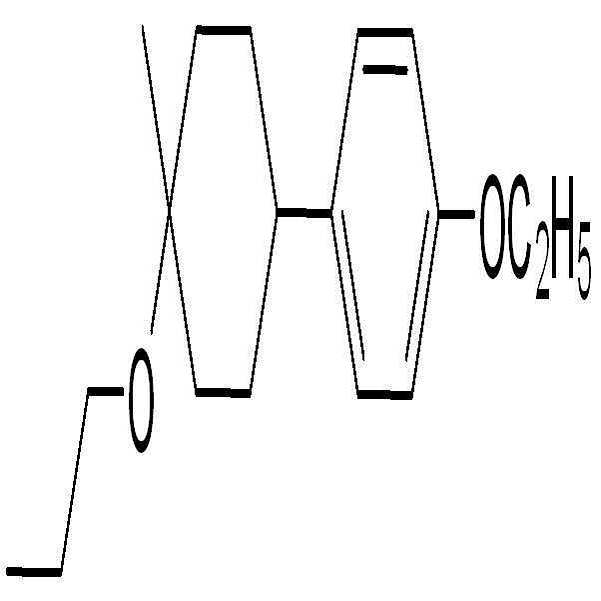
[화학식 2-1]
[화학식 2-2]
[화학식 2-3]
[화학식 2-4]
[화학식 2-5]
[화학식 2-6]
[화학식 2-7]
[화학식 2-8]
[화학식 2-9]
[화학식 2-10]
[화학식 2-11]
[화학식 2-12]
[화학식 2-13]
[화학식 2-14]
[화학식 2-15]
[화학식 2-16]
[화학식 2-17]
[화학식 2-18]
[화학식 2-19]
[화학식 2-20]
상기 화학식 2-1 내지 2-12, 2-19 및 2-20의 액정 화합물은 벤젠 고리에 2 개의 플루오로 원자를 함유하여 음의 유전율 이방성을 나타낼 수 있고, 상기 화학식 2-13 내지 2-18의 액정 화합물은 벤젠 고리에 수소 원자만을 함유하여 중성을 나타낼 수 있다.
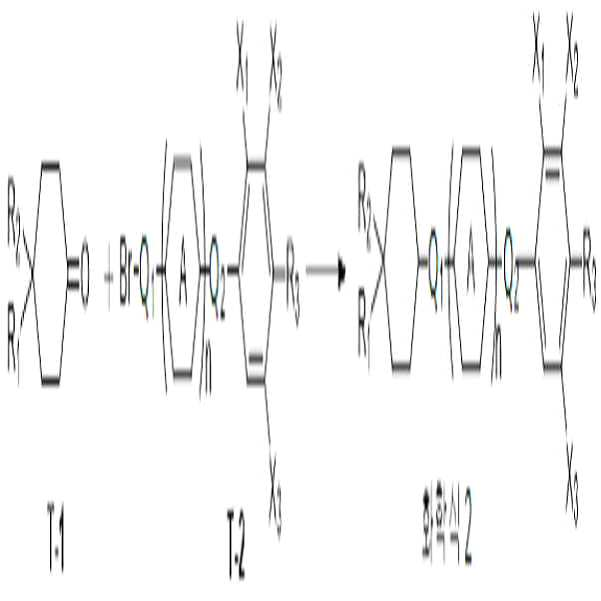
한편, 일 구현예에 따른 상기 화학식 2로 표시되는 액정 화합물은 하기 반응식 2와 같은 방법으로 제조될 수 있다.
[반응식 2]
상기 반응식 2에서, R1 내지 R3, A, Q1, Q2, X1 내지 X3 및 n은 앞서 화학식 2에서 정의한 바와 같다.
반응식 2를 참조하면, 상기 T-1으로 표시되는 4,4-이치환된 사이클로헥사논을 사용하여, 화학식 1로 표시되는 화합물의 말단에 4,4-이치환사이클로헥실기를 도입할 수 있다.
먼저, 하기 반응식 3 또는 4와 같은 방법으로 출발 물질인 상기 T-1으로 표시되는 화합물을 제조할 수 있다:
[반응식 3]
[반응식 4]
상기 반응식 3 및 4에서, R1 및 R2는 앞서 정의한 바와 같고, R4는 탄소수 1 내지 10의 알킬이다.
구체적으로, 화학식 2로 표시되는 화합물에 4,4-디알킬사이클로헥실기를 도입하기 위하여, 상기 반응식 3에 의해 T-1으로 표시되는 화합물을 제조할 수 있다. 상기 T-1-1로 표시되는 화합물을 제조하기 위해 염기로서 수소화나트륨을 사용할 수 있고, 상기 T-1로 표시되는 화합물을 제조하기 위해 아세트산을 사용할 수 있다.
다르게는, 화학식 2로 표시되는 화합물에 4-알킬-4-알콕시사이클로헥실기를 도입하기 위하여, 상기 반응식 4에 의해 T-1'로 표시되는 화합물을 제조할 수 있다. 여기서, R4O-는 R1을 나타내는 것으로, 이에 따라 R1으로 알콕시기를 도입할 수 있다. 또한, 본 명세서에서 도시하지 않으나, 반응식 4와 유사한 방법으로 R1에 알킬, R2에 알콕시기를 도입할 수도 있다.
이후, 상기 제조된 T-1으로 표시되는 화합물을 T-2로 표시되는 화합물과 반응시켜, 화학식 2로 표시되는 화합물을 제조할 수 있다.
상기 액정 조성물은 액정 조성물 전체 중량에 대하여 1 중량% 이상, 또는 2 중량% 이상, 또는 3 중량% 이상으로 상기 화학식 2로 표시되는 1종 이상의 액정 화합물을 포함할 수 있다. 상기 화학식 2로 표시되는 액정 화합물의 함량이 상기 범위 미만이면, 굴절률 이방성, 유전율 이방성 등의 물성 향상 효과를 발현하기 어려울 수 있다. 또한, 상기 액정 조성물은 액정 조성물 전체 중량에 대하여 15 중량% 이하, 10 중량% 이하, 7 중량% 이하로 상기 화학식 2로 표시되는 1 종 이상의 액정 화합물을 포함할 수 있다. 상기 화학식 2로 표시되는 액정 화합물의 함량이 상기 범위를 초과하면, 액정 조성물이 결정성을 나타내고 저온 안정성이 떨어질 수 있다.
본 발명의 액정 조성물은 상기 화학식 1 및 2의 액정 화합물을 함께 포함함으로써, 액정 조성물이 결정성을 나타낼 우려가 적으며 액정 조성물이 보다 높은 굴절률 및 유전율 특성을 나타낼 수 있다.
이에 따라, 본 발명의 액정 조성물은 굴절률 이방성(n)이 0.1100 이상, 또는 0.1110 이상으로 고굴절률 이방성을 나타낼 수 있다. 굴절률 이방성(n)의 상한값은 특별히 제한되지 않으나, 0.1200 이하, 또는 0.1180 이하일 수 있다.
또한, 본 발명의 액정 조성물은 유전율 이방성(△ε)이 -3.20 이하, 또는 -3.25 이하, 또는 -3.30 이하, 또는 -3.40 이하로 절대값이 큰 음의 유전율 이방성을 나타낼 수 있다. 유전율 이방성(△ε)의 하한값은 특별히 제한되지 않으나, -4.00 이상, 또는 -3.90 이상일 수 있다.
상기 액정 조성물은 화학식 1 및 2의 액정 화합물 외에도 액정 표시 장치의 제반 성능을 위하여 다양한 액정 화합물을 추가로 포함할 수 있다.
일례로, 상기 액정 조성물은 후술할 하기 화학식 3 내지 6으로 이루어진 군에서 선택되는 하나 이상의 액정 화합물을 추가로 포함할 수 있다.
상기 액정 조성물은 기존에 알려진 저점도의 액정 화합물을 추가로 포함할 수 있다. 이러한 저점도의 액정 화합물로는 하기 화학식 3으로 표시되는 액정 화합물 등을 사용할 수 있다.
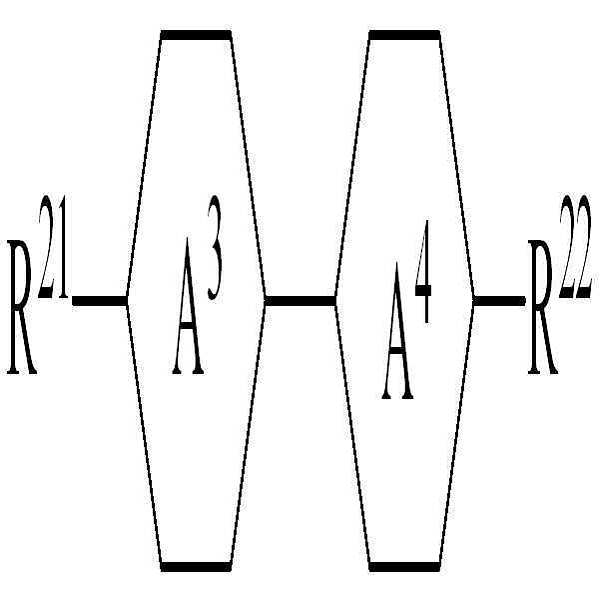
[화학식 3]
상기 화학식 3에서,
R21 및 R22는 각각 독립적으로 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A3 및 A4는 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌(tetrahydropyranylene) 또는 1,4-페닐렌이다.
상기 화학식 3으로 표시되는 액정 화합물로 하기 화학식 3-1 및 화학식 3-2로 표시되는 화합물로 이루어진 군에서 선택된 1종 이상의 액정 화합물을 사용할 수 있다. 이로 인하여 높은 비저항을 유지하면서 액정 조성물의 투명점, 회전 점도, 굴절률 이방성 및 유전율 이방성 등을 용이하게 조절할 수 있다.
[화학식 3-1]
[화학식 3-2]
상기 식들에서, R21 및 R22는 화학식 3에서 정의한 바와 동일하다.
보다 구체적으로, 상기 화학식 3-1 및 3-2에서, R21 및 R22는 각각 독립적으로 탄소수 1 내지 5의 알킬, 비닐(-CH=CH2), 또는 프로페닐(-CH=CH-CH3)일 수 있다.
일례로, 본 발명의 일 실시예에 따른 액정 조성물은 상기 화학식 3-1에서, R21은 탄소수 1 내지 5의 알킬이고 R22는 비닐 또는 프로페닐인 화합물들 중 어느 하나 이상을 포함할 수 있다.
일례로, 본 발명의 일 실시예에 따른 액정 조성물은 하기 화학식 3-1-1, 화학식 3-1-2, 또는 화학식 3-1-3의 화합물들 중 어느 하나 이상을 포함할 수 있다.
[화학식 3-1-1]
[화학식 3-1-2]
[화학식 3-1-3]
상기 액정 조성물은 액정 조성물 전체 중량에 대하여 약 10 중량% 이상, 또는 약 15 중량% 이상, 또는 약 20 중량% 이상이면서; 약 50 중량% 이하, 또는 약 40 중량% 이하, 또는 약 30 중량% 이하로 상기 화학식 3으로 표시되는 액정 화합물을 포함할 수 있다. 상기 화학식 3으로 표시되는 액정 화합물이 상기 범위로 포함됨에 따라, 최적화된 액정상의 구현이 가능하다.
다른 예로, 상기 액정 조성물은 기존에 알려진 액정 화합물로 상전이 온도가 높거나 고굴절률을 나타내는 액정 화합물을 추가로 포함할 수 있다. 이러한 액정 화합물로는 하기 화학식 4로 표시되는 액정 화합물 등을 사용할 수 있다.
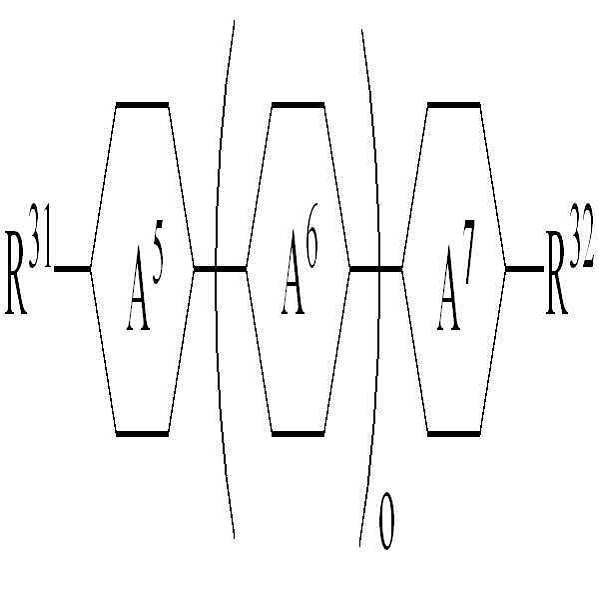
[화학식 4]
상기 화학식 4에서,
R31 및 R32는 각각 독립적으로 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A5 및 A7은 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌 또는 1,4-페닐렌이며,
고리 A6은 1,4-시클로헥실렌, 테트라하이드로피라닐렌, 1,4-페닐렌 또는 1 이상의 H가 할로겐으로 치환된 1,4-페닐렌이고,
o는 1 또는 2의 정수이고,
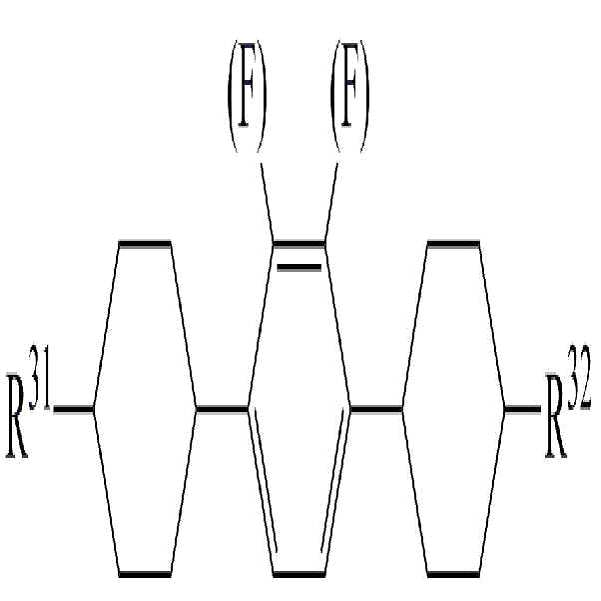
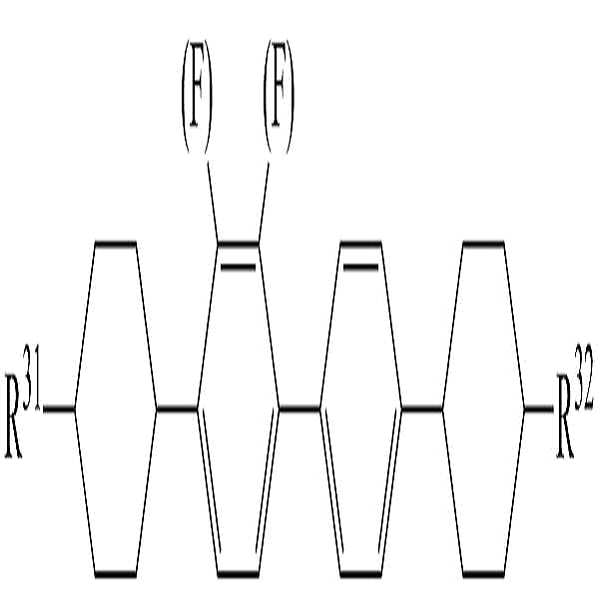
상기 화학식 4로 표시되는 액정 화합물로 하기 화학식 4-1 내지 4-8로 이루어진 군에서 선택된 1종 이상의 액정 화합물을 사용하여 높은 비저항을 유지하면서 액정 조성물의 투명점, 회전 점도, 굴절률 이방성 및 유전율 이방성 등을 용이하게 조절할 수 있다.
[화학식 4-1]
[화학식 4-2]
[화학식 4-3]
[화학식 4-4]
[화학식 4-5]
[화학식 4-6]
[화학식 4-7]
[화학식 4-8]
상기 화학식 4-1 내지 4-8에서, R31 및 R32는 화학식 4에서 정의한 바와 동일하다. 또한, 상기 화학식에서 둥근 괄호"( )"는 둥근 괄호 안에 기재된 치환기로 치환될 수 있음을 의미하는 것이다. 보다 구체적으로, -(F)는 그 부위에 수소 또는 불소가 결합될 수 있음을 의미한다.
보다 구체적으로, 상기 화학식 4-1 내지 4-3에서, R31 및 R32는 각각 독립적으로 탄소수 1 내지 5의 알킬일 수 있다.
일례로, 본 발명의 일 실시예에 따른 액정 조성물은 하기 화학식 4-2-1, 화학식 4-3-1, 또는 화학식 4-3-2의 화합물들 중 어느 하나 이상을 포함할 수 있다.
[화학식 4-2-1]
[화학식 4-3-1]
[화학식 4-3-2]
상기 액정 조성물은 액정 조성물 전체 중량에 대하여 약 5 중량% 이상, 또는 약 8 중량% 이상, 또는 약 10 중량% 이상이면서; 약 40 중량% 이하, 또는 약 25 중량% 이하, 또는 약 20 중량% 이하, 또는 약 15 중량% 이하로 상기 화학식 4로 표시되는 액정 화합물을 포함할 수 있다. 상기 화학식 4로 표시되는 액정 화합물이 상기 범위로 포함됨에 따라, 최적화된 액정상의 구현이 가능하다.
또 다른 예로, 상기 액정 조성물은 기존에 알려진 음의 유전율 액정 화합물을 추가로 포함할 수 있다. 이러한 음의 유전율 액정 화합물로는 하기 화학식 5로 표시되는 액정 화합물 등을 사용할 수 있다.
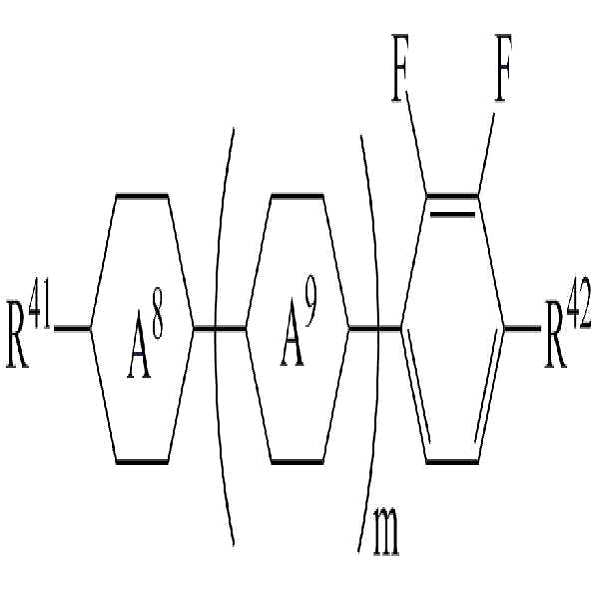
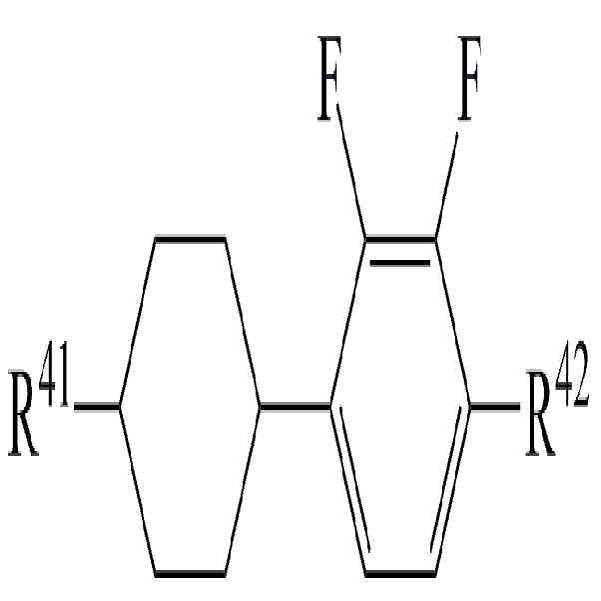
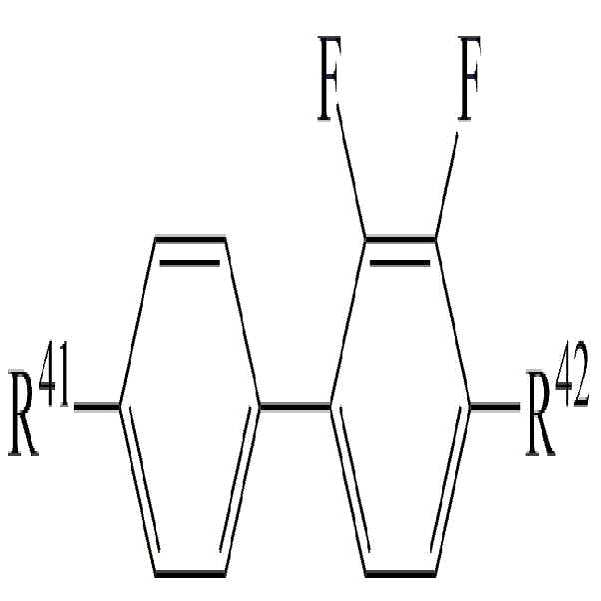
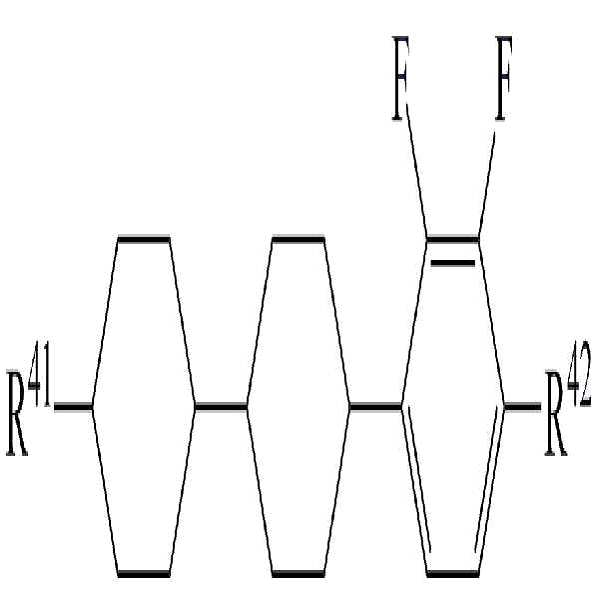
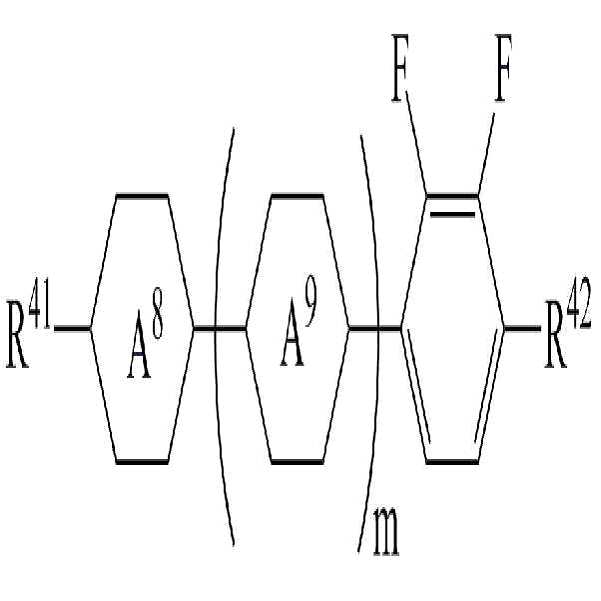
[화학식 5]
상기 화학식 5에서,
R41 및 R42는 각각 독립적으로 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A8 및 A9는 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌, 1,4-페닐렌 또는 1 이상의 H가 할로겐으로 치환된 1,4-페닐렌이며,
m은 0 내지 2의 정수이고.
상기 화학식 5로 표시되는 액정 화합물로 하기 화학식 5-1 내지 화학식 5-4로 이루어진 군에서 선택된 1종 이상의 액정 화합물을 사용하여 높은 비저항을 유지하면서 액정 조성물의 투명점, 회전 점도, 굴절률 이방성 및 유전율 이방성 등을 용이하게 조절할 수 있다.
일례로, 본 발명의 일 실시예에 따른 액정 조성물은 적어도 하나의 하기 화학식 5-1, 적어도 하나의 하기 화학식 5-2 및 적어도 하나의 하기 화학식 5-3을 포함할 수 있다.
[화학식 5-1]
[화학식 5-2]
[화학식 5-3]
[화학식 5-4]
상기 화학식 5-1 내지 5-4에서, R41 및 R42는 화학식 5에서 정의한 바와 동일하다.
보다 구체적으로, 상기 화학식 5-1 내지 5-3에서, R41 및 R42는 각각 독립적으로 탄소수 1 내지 5의 알킬 또는 탄소수 1 내지 3의 알콕시일 수 있다.
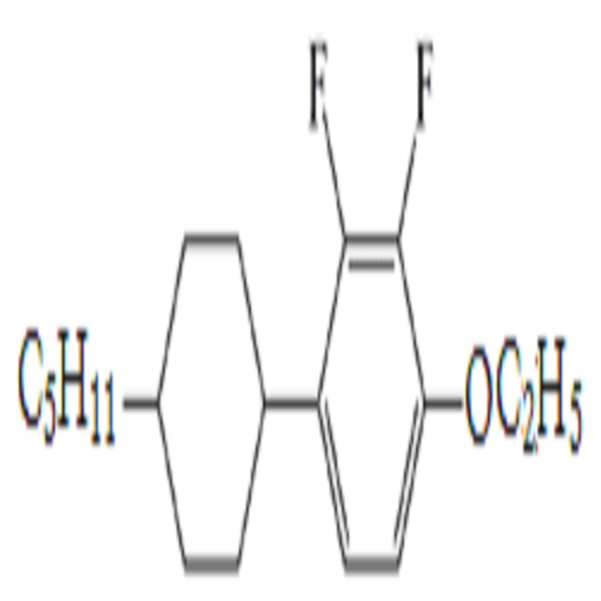
일례로, 본 발명의 일 실시예에 따른 액정 조성물은 하기 화학식 5-1-1, 화학식 5-1-2, 화학식 5-2-1, 화학식 5-3-1, 또는 화학식 5-3-2의 화합물들 중 어느 하나 이상을 포함할 수 있다.
[화학식 5-1-1]
[화학식 5-1-2]
[화학식 5-2-1]
[화학식 5-3-1]
[화학식 5-3-2]
상기 액정 조성물은 액정 조성물 전체 중량에 대하여 약 10 중량% 이상, 또는 약 20 중량% 이상, 또는 약 25 중량% 이상, 또는 약 30 중량% 이상이면서; 약 75 중량% 이하, 또는 약 70 중량% 이하, 또는 약 60 중량% 이하, 또는 약 50 중량% 이하로 상기 화학식 5로 표시되는 액정 화합물을 포함할 수 있다. 상기 화학식 5로 표시되는 액정 화합물이 상기 범위로 포함됨에 따라, 최적화된 액정상의 구현이 가능하다.
또 다른 예로, 상기 액정 조성물은 기존에 알려진 고유전율 액정 화합물을 추가로 포함할 수 있다. 이러한 액정 화합물로는 하기 화학식 6으로 표시되는 액정 화합물 등을 사용할 수 있다.
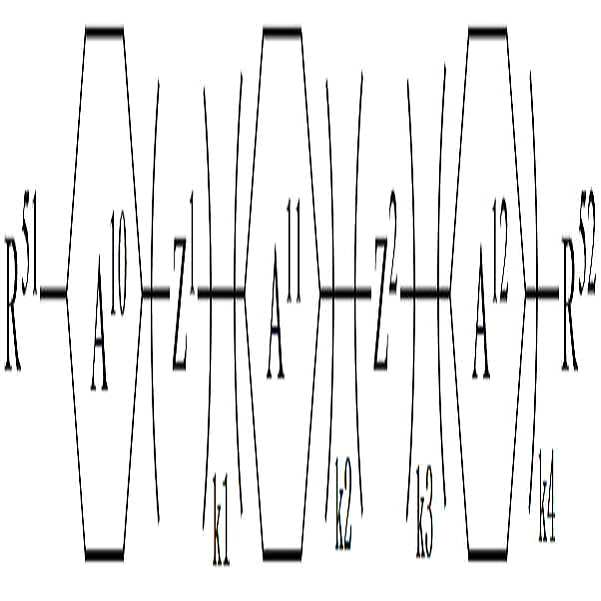
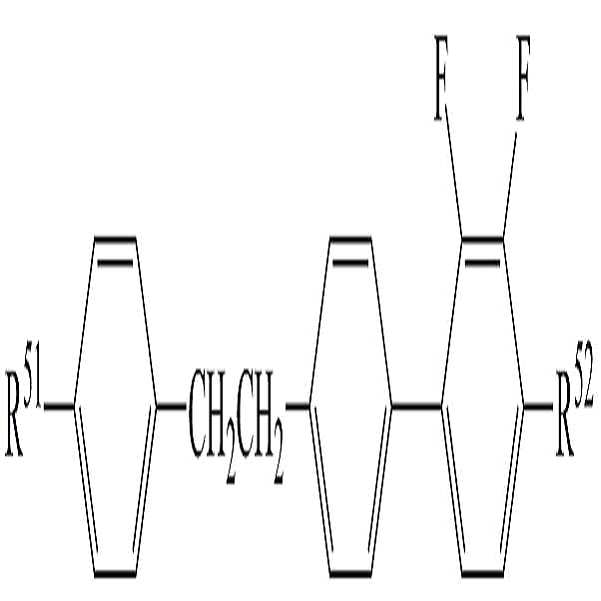
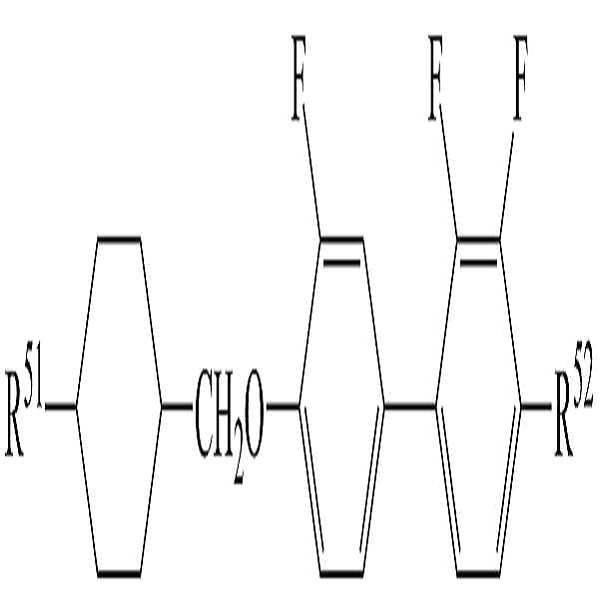
[화학식 6]
상기 화학식 6에서,
R51 및 R52는 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A10, A11 및 A12는 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌, 1,4-페닐렌 또는 1 이상의 H가 할로겐으로 치환된 1,4-페닐렌이며,
Z1 및 Z2는 각각 독립적으로 -CH2CH2-, -CH=CH-, -CH2O-, -OCH2-, -C≡C-, -CH2CF2-, -CHFCHF-, -CF2CH2-, -CH2CHF-, -CHFCH2-, -C2F4-, -O-, -COO-, -OCO-, -CF2O- 또는 -OCF2-이고,
k1 및 k3는 각각 독립적으로 0 또는 1이되, k1 및 k3의 합은 1 또는 2이고,
k2 및 k4는 각각 독립적으로 0 내지 2의 정수이다.
상기 화학식 6으로 표시되는 액정 화합물로 하기 화학식 6-1 내지 6-4로 이루어진 군에서 선택된 1종 이상의 액정 화합물을 사용하여 높은 비저항을 유지하면서 액정 조성물의 투명점, 회전 점도, 굴절률 이방성 및 유전율 이방성 등을 용이하게 조절할 수 있다.
[화학식 6-1]
[화학식 6-2]
[화학식 6-3]
[화학식 6-4]
상기 화학식 6-1 내지 6-4에서, R51 및 R52는 화학식 6에서 정의한 바와 동일하다.
특히, 상기 화학식 6의 액정 화합물로 상기 6-1로 표시되는 액정 화합물을 사용할 경우 보다 낮은 회전점도를 나타낼 수 있어 고속 응답용 액정 조성물 제공에 매우 유리하다.
상기 화학식 6의 화합물은 상술한 물성을 구현하기 위해 상기 액정 조성물은 액정 조성물 전체 중량에 대하여 약 0 중량% 이상, 또는 약 1 중량% 이상, 또는 약 3 중량% 이상이면서; 약 15 중량% 이하, 또는 약 12 중량% 이하, 또는 약 10 중량% 이하, 또는 약 8 중량% 이하로 포함될 수 있다.
상기 액정 조성물은 액정 조성물의 목적하는 용도 및 효과를 고려하여 상술한 화학식 3 내지 6의 액정 화합물 중 적어도 어느 한 종류 이상의 액정 화합물을 상기 화학식 1 및 2의 액정 화합물과 함께 포함하여 높은 음의 유전율 이방성을 나타내면서도 낮은 회전점도를 나타내는 액정 재료를 제공할 수 있다.
상기 액정 조성물은 액정 화합물 외에도 본 발명이 속하는 기술분야에서 통상적으로 사용하는 다양한 첨가제를 추가로 포함할 수 있다.
일례로, 상기 액정 조성물은 산화 방지제를 추가로 포함할 수 있다.
또한, 상기 액정 조성물은 반응성 메소젠을 추가로 포함할 수 있다. 이러한 반응성 메소젠은 액정상 거동을 나타내는 메소젠기와, 적어도 일측 말단에 광중합, 광가교 또는 광경화 가능한 불포화 작용기, 예를 들어, 비닐기, (메트)아크릴기 또는 에폭시기 등을 갖는 화합물로 정의될 수 있고, 이러한 정의를 충족하는 임의의 화합물을 반응성 메소젠으로서 포함할 수 있다. 일례로, 상기 반응성 메소젠으로, 액정 골격을 갖는 디아크릴레이트 단량체 또는 액정 골격을 갖는 디메타크릴레이트 단량체를 포함할 수 있다.
또한, 상기 액정 조성물은 UV 안정제를 추가로 포함할 수 있다. 사용가능한 UV 안정제의 종류는 특별히 제안되지 않지만 예를 들어 Hals (Hindered amine light stabilizer) 계열을 사용할 수 있다.
상기 산화 방지제 및/또는 UV 안정제는 전체 액정 조성물 중량에 대하여 약 1 내지 2,000ppm 혹은 약 200 내지 500ppm 로 사용될 수 있다.
또한, 본 발명은 상기 액정 조성물을 포함하는 액정 표시 장치를 제공한다.
본 발명의 액정 조성물은 AM-LCD (Active Matrix-LCD) 또는 PM-LCD (Passive Matrix-LCD)의 용도로 사용 가능하며, 비제한적인 예로 VA (Vertical alignment), MVA (Multi-domain VA), PVA (Patterned VA), PS-VA (polymer stabilized VA)와 같은 수직 전계 모드의 액정 표시 장치, 또는 PALC (plasma address liquid crystal), IPS (In-plane switching), FFS (Fringe field switching), PLS (Plane line switching), AH-IPS (advanced high-performance IPS), ADS (Advanced-super dimensional switching), PSA (Polymer sustained alignment)와 같은 수평 전계 모드의 액정 표시 장치, TN (Twist nematic), STN (Super-twisted nematic)과 같은 모드의 액정 표시 장치 등 다양한 모드의 액정 표시 장치에 사용 가능하다. 본 발명에 따른 액정 조성물은 높은 음의 유전율 이방성 및 고굴절률 이방성을 나타내어, 특히 네가티브 액정 재료를 사용하는 VA, MVA, PVA, PS-VA 모드 등의 액정 표시 장치의 우수한 제반 성능을 유지하면서 고속 응답을 실현할 수 있을 것으로 기대된다.
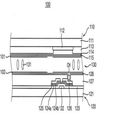
이러한 액정 표시 장치의 일 구현예에 따른 구조를 도 1에 나타내었다. 도 1을 참조하면, 액정 표시 장치(100)는 컬러필터 기판(110), 박막트랜지스터 기판(120) 및 상기 컬러필터 기판(110)과 상기 박막트랜지스터 기판(120) 사이에 개재된 액정층(130)을 포함한다. 상기 박막트랜지스터 기판(120) 상에는 복수의 화소 영역이 정의된다.
컬러필터 기판(110)은 상부 베이스 기판(111), 광차단층(112), 컬러필터(113), 상부 유기 절연막(114), 공통 전극(115) 및 상부 배향막(101)을 포함할 수 있다. 광차단층(112)은 상부 베이스 기판(111) 상에 형성되며, 광투과율이 낮은 불투명 물질, 예를 들어, 카본 블랙 등의 착색제를 포함할 수 있다.
컬러필터(113)는 상부 베이스 기판(111) 상에 형성되며, 광차단층(112)과 일부 중첩되도록, 또는 인접한 다른 컬러필터(113)와 일부 중첩되도록 형성될 수 있다. 상부 유기 절연막(114)은 광차단층(112)과 컬러필터(113)을 보호하며, 광차단층(112)와 컬러필터(113)으로 인하여 발생하는 단차를 보상하여 컬러필터 기판(110)의 표면을 평탄화한다.
공통 전극(115)은, 예를 들어, 인듐 주석 산화물(Indium Tin Oxide) 또는 인듐 아연 산화물(Indium Zinc oxide) 등으로 이루어질 수 있다. 공통 전극(115)에는 소정의 공통 전압이 인가된다. 상부 배향막(101)은 액정층(130)과 접촉하여 액정층(130)의 액정(131)을 소정의 방향으로 배향하거나 기울어지도록 한다.
박막트랜지스터 기판(120)은 복수의 박막트랜지스터를 포함한다. 구체적으로, 박막트랜지스터 기판(120)은 베이스 기판(121), 게이트 전극(122), 게이트 절연막(123), 채널층(124a), 오믹 콘택층(124b), 소스 전극(125), 드레인 전극(126), 하부 유기 절연막(127), 화소 전극(128), 및 하부 배향막(102)을 포함할 수 있다.
게이트 전극(122)은 베이스 기판(121) 위에 형성되며, 게이트 라인(미도시)으로부터 게이트 신호를 전달받는다. 게이트 절연막(123)은 상기 게이트 전극(122)을 커버한다.
채널층(124a)은 게이트 전극(122)과 중첩되도록 게이트 절연막(123) 위에 형성되며, 채널층(124a) 위에는 서로 이격된 한 쌍의 오믹 콘택층(124b)이 형성된다.
오믹 콘택층(124b) 위에는 소스 전극(125) 및 드레인 전극(126)이 형성된다. 소스 전극(125)과 드레인 전극(126)은 서로 이격되어 채널층(124a)의 일부를 노출시킨다. 드레인 전극(126)의 일부는 화소 전극(128)의 콘택홀(CH)을 통하여 화소 전극과 전기적으로 연결된다.
하부 유기 절연막(127)은 소스 전극(125), 드레인 전극(126) 및 노출된 채널층(124a)를 커버한다.
하부 유기 절연막(127) 위에는 화소 전극(128)이 형성된다. 하부 유기 절연막(127)은 박막트랜지스터 기판(120)의 표면을 평탄화한다.
하부 유기 절연막(127)에는 콘택홀(CH)이 형성되어, 이를 통하여 드레인 전극(126)과 화소 전극(128)이 전기적으로 연결된다.
하부 유기 절연막(127) 위에는 화소 전극(128)이 형성되고, 화소 전극(128) 위에 하부 배향막(102)이 형성된다. 화소 전극(128)에는 상기 드레인 전극(126)으로부터 전달된 소정의 데이터 전압이 인가된다.
상기 데이터 전압과 공통 전극(115)에 인가된 공통 전압의 전압차에 의해 전기장이 발생하고, 이로 인하여 액정층(130)의 액정(131)의 배열이 조절될 수 있다.
한편, 시야각 개선을 위해 각 화소는 복수의 도메인으로 분할되어 하나의 화소 영역 내에서 상기 액정 조성물은 서로 다른 둘 이상의 방향으로 배향될 수 있다. 각 화소를 복수의 도메인으로 분할하기 위하여 각 화소에는 돌기 등이 형성될 수 있으며, 화소 전극 및 공통 전극은 절개부를 포함할 수 있다.
상기 다른 일 구현예에 따른 액정 표시 장치는 액정층(130)에 상술한 는 액정 조성물을 주입하여 제공될 수 있다. 상기 액정 조성물에 관련된 내용은 전술하였으므로 구체적인 설명은 생략한다.
상기 다른 일 구현예에 따른 액정 표시 장치는 수직 전계 모드(예를 들면, VA, MVA, PVA, PS-VA 등)뿐 아니라 수평 전계 모드(예를 들면, IPS, PLS, FFS 등) 등 다양한 모드로 구현될 수 있다.
이하, 본 발명의 이해를 돕기 위하여 바람직한 실시예를 제시한다. 그러나 하기의 실시예는 본 발명을 보다 쉽게 이해하기 위하여 제공되는 것일 뿐, 이에 의해 본 발명의 내용이 한정되는 것은 아니다.
<
실시예
>
이하의 실시예, 비교예 및 실험예에 있어서, 액정 화합물의 표기는 하기 표 1과 같다.
실시예 및 비교예에서 사용되는 액정 화합물은 코드로 표시된다. 상기 코드는 액정 화합물의 중심그룹을 이루는 고리의 기호를 왼쪽부터 순차로 기재하고, 상기 중심그룹의 고리를 연결하는 연결그룹을 순서에 맞게 기재한 후, 말단그룹을 오른쪽에 기재하여 작성한다. 이때, 중심그룹의 고리와 중심그룹의 고리를 연결하는 연결그룹 사이에는 별도의 구분 표시가 없으나, 중심그룹과 말단그룹 사이는 "-"을 기재하여 구분하며, 양 말단그룹은 "."을 기재하여 구분한다. 물질의 개별적인 약식 기호(코드)는 하기 표 1에 정리하였다.
| 중심그룹 | 연결그룹 | 말단그룹 | |||||
| 구조 | 기호 | 구조 | 기호 | 구조 | 기호 | 구조 | 기호 |
| A | -CF2O- | X | -CnH2n +1 | n | OK | ||
| B | -CH2CH2- | N | -OCnH2n +1 | On | -OCF3 | OCF3 | |
| C | -COO- | L | V | -F | F | ||
| D | U1 | -CF3 | CF3 | ||||
| E | 3=2 | -C=N | CN | ||||
| F | W | ||||||
| I | |||||||
| Ia | |||||||
상기 표 1을 참고하면, 다음 코드는 하기 표시된 구조의 액정 화합물을 의미한다.
<액정 화합물의 제조>
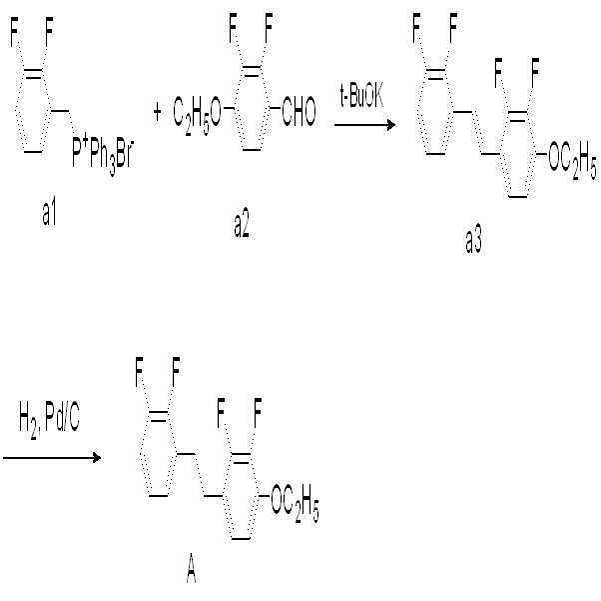
제조예
1 (
FNF
-H.O2)
브롬 염 화합물(화합물 a1, 40 mmol, 18.8g)을 무수 THF에 녹인 후 -30℃에서 교반하면서 포타슘 터셔리-부톡사이드(48.1 mmol, 5.4 g)를 서서히 가하고 30분 동안 교반하였다. -30℃에서 알데하이드 화합물(화합물 a2, 43.7 mmol, 8.13 g)을 THF에 녹여 적가하였다. -10℃로 온도를 올린 뒤 1시간 동안 교반한 후 반응 용기에 물과 톨루엔 1:1 용매를 넣어 반응을 종결시켰다. 유기 용매층을 추출하고 감압증류하여 생긴 고체를 컬럼 크로마토그래피를 통해 분리하여 에텐화합물 (화합물 a3, 60 %, 7.1 g)을 수득하였다. 수득한 에텐화합물(화학식 1-3, 24 mmol, 7.1 g)과 팔라듐/활성탄(10 wt.%, 1.5 g)을 THF와 메탄올 1:1 용매에 녹인 후 수소반응기에서 3시간 동안 반응시키고 여과하였다. 여과액을 농축한 후, 컬럼 크로마토 그래피를 통해 목적 화합물(화합물 A, 94 %, 6.7 g)을 수득하였다.
1H NMR (300 MHz, CDCl3): δ 7.01 (m, 2H), 6.87 (t, 1H), 6.75 (t, 1H), 6.63 (t, 1H), 4.11 (q, 2H), 2.95 (m, 4H), 1.45 (t, 3H); MS m/z 298 (M+); mp 55.9℃
제조예
2 (
FANAF
-H.O2)
브롬 염 화합물(화합물 b1, 20.2 mmol, 12.5 g)을 무수 THF에 녹인 후 -30℃에서 교반하면서 포타슘 터셔리-부톡사이드(25.4 mmol, 2.86 g)를 서서히 가하고 30분 동안 교반하였다. -30℃에서 알데하이드 화합물(화학식 b2, 23.1 mmol, 5.04 g)을 THF에 녹여 적가하였다. -10℃로 온도를 올린 뒤 1시간 동안 교반한 후 반응 용기에 물과 톨루엔 1:1 용매를 넣어 반응을 종결시켰다. 유기 용매층을 추출하고 감압증류하여 생긴 고체를 컬럼 크로마토그래피를 통해 분리하여 에텐화합물(화합물 5-3, 74 %, 7 g)을 수득하였다. 수득한 에텐화합물(화합물 b3, 15.6 mmol, 7 g)과 팔라듐/활성탄(10 wt.%, 1.75 g)을 THF와 메탄올 1:1 용매에 녹인 후 수소 반응기에서 3시간 동안 반응시키고 여과하였다. 여과액을 농축시킨 뒤 컬럼 크로마토그래피를 통해 목적 화합물(화합물 B, 81 %, 5.69 g)을 수득하였다.
1H NMR (300 MHz, CDCl3): δ 7.49 (d, 2H), 7.45 (d, 2H), 7.32 (t, 4H), 7.21 (m, 4H), 6.82 (t, 1H), 4.19 (q, 2H), 3.01 (m, 4H), 1.50 (t, 3H); MS m/z 450 (M+); mp 150℃
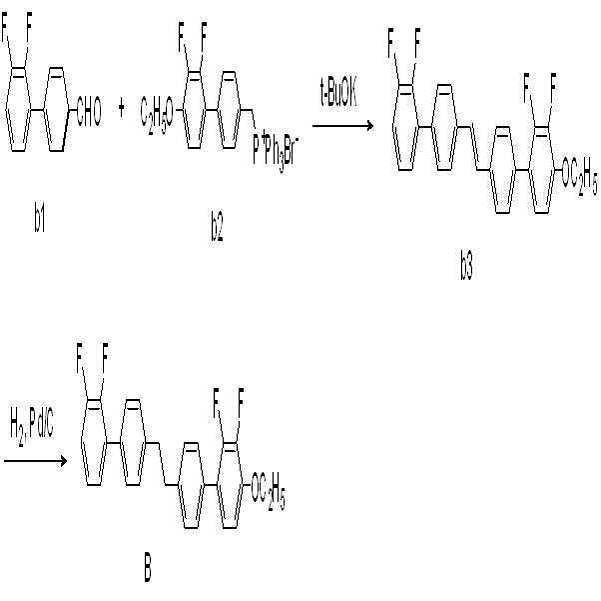
제조예
3 (
BAF
-
3.O1
-O2)
1) 화합물 12-2-1의 합성 (8-methoxy-8-propyl-1,4-dioxaspiro[4.5]decane)
화합물 (12-2) (8-propyl-1,4-dioxaspiro[4.5]decan-8-ol) (13.0 g, 65 mmol)을 톨루엔(260 mL, 20 mL/g)에 용해 시킨 뒤, -78 ℃ 및 질소조건 하에서 리튬디아이소프로필아민 (Lithium diisopropylamine, LDA) (48.7 mL, 97 mmol, 2.0M solution in THF)을 넣어준 후, 상온에서 30분 교반 후 화합물 11-1 (methyl 4-methylbenzene- sulfonate) (15.7 g, 84 mmol)을 반응 혼합물에 첨가하여, 환류(reflux) 조건하에 12 시간 동안 반응을 진행하였다. 반응 종료 후, 포화 암모늄클로라이드 용액을 첨가한 다음, 에틸아세테이트(EtOAc)를 사용하여 추출하고, 무수 Na2SO4 건조하여 유기층을 농축하였다. 농축된 반응물을 실리카 컬럼 크로마토그래피(Hexane:EtOAc = 5:1)를 이용하여, 분리 및 정제하여, 노란색의 액체 화합물 12-2-1 (8.5 g, 31% yield)을 얻었다.
1H NMR (CDCl3, Varian 400 MHz): δ 0.91 (3H, t, J = 7.6 Hz), 1.23-1.36 (4H, m), 1.39-1.54 (4H, m), 1.76-1.84 (4H, m), 3.13 (3H, s), 3.90-3.97 (4H, m)
2) 화합물 14-5의 합성 (4-methoxy-4-propylcyclohexanone)
화합물 (12-2-1) (8-methoxy-8-propyl-1,4-dioxaspiro[4.5]decane) (8.30 g, 39.0 mmol), 아세트산(80%, Acetic acid) (83.0 mL, 10 mL/g) 첨가 후, 60-70 ℃에서 3시간 교반 시킨다. 반응종료 후 포화 탄산수소나트륨 용액을 첨가 한 다음, 반응액을 에틸아세테이트(EtOAc)를 사용하여 추출하고, 무수 Na2SO4 건조하여 유기층을 농축하였다. 반응물을 컬럼 크로마토그래피(Hexane:EtOAc=5:1)으로 분리 및 정제하여, 노란색의 액체 화합물 14-5 (6.40 g, 97% yield)을 얻었다.
1H NMR (CDCl3, Varian 400 MHz): δ 0.94 (3H, t, J = 7.2Hz), 1.29-1.40 (2H, m), 1.47-1.51 (2H, m), 1.59-1.67 (2H, m), 2.09-2.21 (4H, m), 2.53-2.64 (2H, m) 3.23 (3H, s)
3) 화합물 16-1-1의 합성(4'-bromo-4-ethoxy-2,3-difluorobiphenyl)
제조예 1과 동일한 방법으로 화합물 16-1-1을 합성하였다.
4) 화합물 21-2의 합성 (1-(4'-ethoxy-2',3'-difluorobiphenyl-4-yl)-4-methoxy-4-propylcyclohexanol)
화합물 16-1-1 (4'-bromo-4-ethoxy-2,3-difluorobiphenyl) (11.8 g, 38.0 mmol)을 THF (120 mL, 10 mL/g)에 용해 시킨 뒤, -78 ℃에서 노말 부틸리튬 (n-BuLi)(35.0 mL, 56.0 mmol, 1.6M solution in Hexane)을 천천히 10분간 적가 후, 동일 온도에서 30분간 교반하였다. 화합물 14-5 (4-methoxy-4-propylcyclohexanone) (6.40 g, 38.0 mmol)을 THF (20.0 mL, 3.1 mL/g)에 용해시킨 후 10분간 천천히 적가 후, 천천히 상온으로 반응 온도를 증가시켜 12시간 동안 교반하였다. 반응 종료 후, 포화 암모늄클로라이드 용액을 첨가한 다음, 에틸아세테이트(EtOAc)를 사용하여 추출하고, 무수 Na2SO4 건조하여 유기층을 농축하였다. 농축된 반응물을 Hexane를 이용하여 재침전하여, 흰색의 고체 화합물 21-2 (8.40 g, 55% yield)을 얻었다.
1H-NMR (CDCl3, Varian 400 MHz): δ 0.93 (3H, t, J = 7.2 Hz), 1.30-1.39 (3H, m), 1.47-1.56 (3H, m), 1.70 (1H, s), 1.90-1.95 (4H, m), 2.02-2.10 (4H, m), 3.22 (3H, s), 4.16 (3H, q, J = 7.2 Hz), 6.78-6.82 (1H, m), 7.07-7.12 (1H, m), 7.50-7.52 (2H, m), 7.59(2H, d, J = 8.4 Hz)
5) 화합물 21-2-1의 합성 (4-ethoxy-2,3-difluoro-4'-(4-methoxy-4-propylcyclohex-1-enyl)biphenyl)
화합물 21-2 (1-(4'-ethoxy-2',3'-difluorobiphenyl-4-yl)-4-methoxy-4-propylcyclohexanol) (8.30 g, 21.0 mmol)을 톨루엔 (toluene)(83 mL, 10 mL/g)에 용해 시킨 뒤 파라-톨루엔설폰산 일수화물 (p-TsOH·H2O) (190 mg, 1.04 mmol)을 넣어 준 뒤, 65~70 ℃에서 2 시간 동안 반응을 진행하였다. 반응 완료 후, 포화 탄산수소나트륨 용액을 첨가한 다음, EtOAc를 사용하여 추출하고, 무수 Na2SO4 건조 한 후, 유기층을 농축하였다. 농축된 유기층을 실리카 컬럼 크로마토그래피 (Hexane:EtOAc = 5:1)를 이용하여 분리 및 정제를 통해 흰색의 고체 화합물 21-2-1 (5.10 g, 64% yield)을 얻었다.
1H-NMR (CDCl3, Varian 400 MHz): δ 0.95 (3H, t, J = 7.2 Hz), 1.35-1.44 (3H, m), 1.48 (3H, t, J = 6.8 Hz), 1.57-1.63 (1H, m), 1.70-1.77 (1H, m), 1.93-2.00 (1H, m), 2.20-2.26 (1H, m), 2.37-2.42 (2H, m), 2.54-2.62 (1H, m), 3.22 (3H, s), 4.16 (2H, q, J = 7.2 Hz), 6.08 (1H, s), 6.77-6.81 (1H, m), 7.07-7.12 (1H, m), 7.44-7.48 (4H, m)
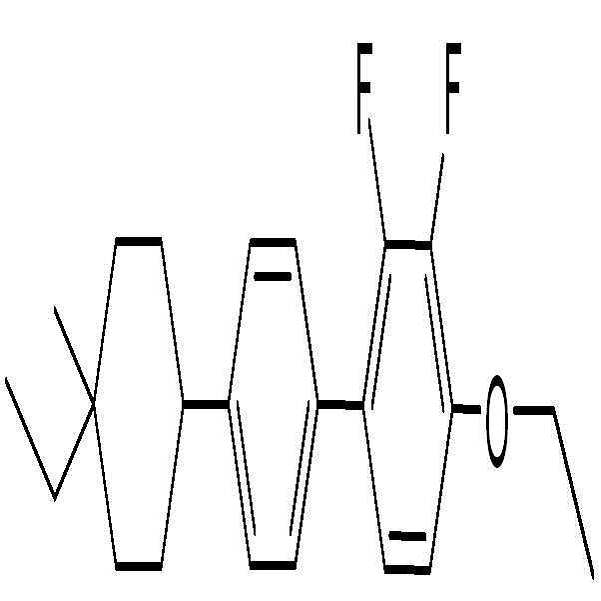
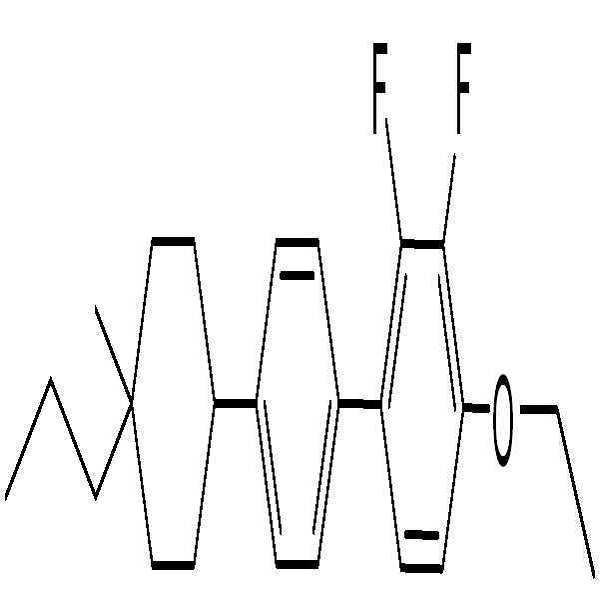
6) 화합물 BAF-3.O1-O2의 합성 (4-ethoxy-2,3-difluoro-4'-(4-methoxy-4-propylcyclohexyl)biphenyl)
화합물 21-2-1 (4-ethoxy-2,3-difluoro-4'-(4-methoxy-4-propylcyclohex-1-enyl)biphenyl) (5.16 g, 13.0 mmol)을 EtOAc (120 mL, 20 mL/g)에 용해 시킨 뒤, 팔라듐카본 (Pd/C) (260 mg, 5wt%, 10% on Palladium carbon) 첨가하여 수소화 반응기에서 0.8 MPa 압력조건 및 상온에서 4시간 반응을 진행하였다. 반응 완료 후, 셀라이트(Celite)와 에틸아세테이트(EtOAc)를 사용하여 감압여과하고 농축한 후, 실리카 컬럼 크로마토그래피 (Hexane:EtOAc = 10:1) 이용하여 분리 및 정제를 통해 흰색의 고체 화합물 BAF-3.O1-O2 (2.50 g, 48% yield)을 얻었다.
1H-NMR (CDCl3, Varian 400 MHz): δ 0.94 (3H, t, J = 7.2 Hz), 1.30-1.39 (4H, m), 1.41-1.45 (2H, m), 1.48 (3H, t, J = 6.8 Hz), 1.66-1.84 (4H, m), 1.97-1.99 (2H, m), 2.47-2.55 (1H, m), 3.17 (3H, s), 4.15 (2H, q, J = 7.2 Hz), 6.76-6.80 (1H, m), 7.06-7.11 (1H, m), 7.37 (2H, d, J = 8.0 Hz), 7.42-7.44 (2H, m)
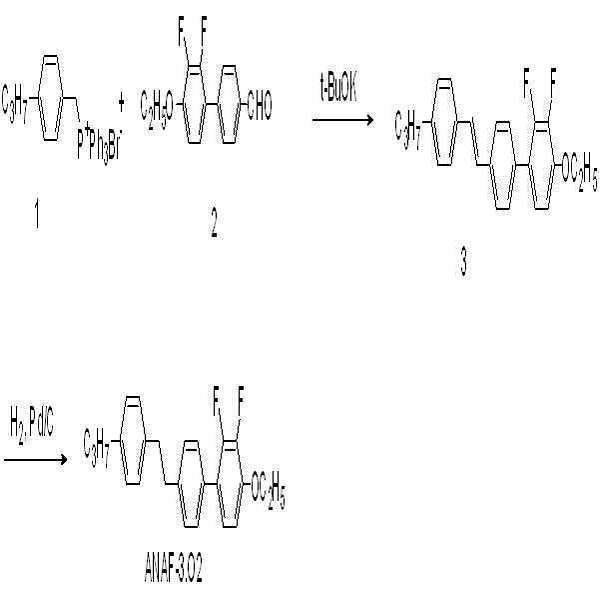
제조예
4 (
ANAF
-
3.O2
)
브롬 염 화합물(화합물 1, 20 mmol, 9.5 g)을 무수 THF에 녹인 후 -30℃에서 교반하면서 포타슘 터셔리-부톡사이드(24 mmol, 2.69 g)를 서서히 가하고 30분 동안 교반하였다. -30℃에서 알데하이드 화합물(화학식 2, 20 mmol, 5.24 g)을 THF에 녹여 적가하였다. -10℃로 온도를 올린 뒤 1시간 동안 교반한 후 반응 용기에 물과 톨루엔 1:1 용매를 넣어 반응을 종결시켰다. 유기 용매층을 추출하고 감압증류하여 생긴 고체를 컬럼 크로마토그래피를 통해 분리하여 에텐화합물(화합물 3, 80 %, 6.1 g)을 수득하였다. 수득한 에텐화합물(화합물 3, 16 mmol, 6.1 g)과 팔라듐/활성탄(10 wt.%, 1.75 g)을 THF와 메탄올 1:1 용매에 녹인 후 수소 반응기에서 3시간 동안 반응시키고 여과하였다. 여과액을 농축시킨 뒤 컬럼 크로마토그래피를 통해 목적 화합물(화합물 B, 81 %, 5.69 g)을 수득하였다.
1H NMR (300 MHz, CDCl3):δ 7.52 (m, 1H), 7.38 (m, 4H), 7.08-7.05 (m, 5H), 4.07 (q, 1H), 2.82 (s, 4H),2.61 (t, 2H), 1.64 (m, 2H), 1.34 (t, 3H), 0.94 (t, 3H); MS m/z 380 (M+); mp 105℃
<액정 조성물의 제조>
제조예에서 제조한 액정 화합물 중 일부를 사용하여, 하기 표 2 및 3과 같은 조성을 갖는 실시예 및 비교예의 액정 조성물을 제조하였다. 표 2 및 3에서 액정 화합물은 코드로 표시하였으며, 코드의 의미는 상기 표 1에 기재되어 있다. 하기 표 2 및 3에서 각 수치는 중량%를 의미한다.
| Code | 실시예 1 | 실시예 2 | 비교예 1 | 비교예 2 | 비교예 3 |
| BA-3.O1 | 5.2 | 4.7 | 4.0 | 5.7 | 5.0 |
| BA-3.O2 | 4.0 | 4.7 | 4.0 | 5.7 | 5.0 |
| BB-3.4 | 6.9 | 5.7 | 8.0 | 6.0 | 8.0 |
| BB-3.5 | - | - | - | 6.0 | |
| BB-3.U1 | 11.8 | 13.3 | 14.0 | 10.0 | 14.0 |
| BBA-3.1 | 2.3 | 2.8 | 3.5 | - | - |
| BAA-3.1 | 5.2 | 2.8 | 5.0 | 5.7 | 8.0 |
| BAA-3.2 | 6.6 | 6.6 | 6.5 | 8.0 | 8.0 |
| AF-3.O2 | 11.0 | 11.3 | 11.0 | 11.3 | 11.0 |
| BF-3.O2 | 13.2 | 13.2 | 13.0 | 12.3 | 11.0 |
| BF-5.O2 | 7.2 | 7.5 | 8.0 | 8.0 | 7.0 |
| BBF-3.O2 | 10.2 | 10.4 | 12.5 | 10.7 | 12.0 |
| BBF-5.O2 | 6. | 5.7 | 6.0 | 7.0 | 7.0 |
| ANAF-3.O2 | 4.6 | 5.7 | 4.5 | - | - |
| FANAF-H.O2 | 3.1 | 2.8 | - | 3.7 | - |
| BAF-3.O1-O2 | 2.7 | 2.8 | - | - | 4.0 |
| 합계 | 100.0 | 100.0 | 100.0 | 100.0 | 100.0 |
| Code | 실시예 3 | 실시예 4 | 실시예 5 | 실시예 6 | 비교예 4 | 비교예 5 |
| BB-3.4 | - | - | - | - | - | |
| BB-3.V | 17.7 | 19.0 | 18.0 | 18.0 | 20.5 | 18.4 |
| BB-3.U1 | 7.8 | 9.0 | 8.0 | 8.0 | 12.5 | 12.6 |
| BAA-3.1 | 6.1 | 4.5 | 4.5 | 4.0 | 5.5 | 5.0 |
| BAA-3.2 | 7.1 | 6.2 | 6.0 | 6.0 | 7.0 | 6.4 |
| AF-3.O2 | 13.0 | 11.4 | 9.5 | 11.0 | 7.0 | 10.7 |
| BF-3.O2 | 12.1 | 11.7 | 11.0 | 11.0 | 14.0 | 10.7 |
| BF-5.O2 | 7.8 | 7.3 | 7.5 | 7.0 | 8.0 | 7.2 |
| BBF-3.O2 | 12.1 | 11.6 | 12.0 | 12.0 | 15.5 | 11.2 |
| BBF-5.O2 | 8.7 | 7.6 | 7.0 | 7.0 | 7.6 | |
| ANAF-3.O2 | - | 7.3 | 7.5 | 7.0 | 7.0 | 5.8 |
| FNF-H.O2 | - | - | 1.5 | 1.5 | - | - |
| FANAF-H.O2 | 4.3 | 2.2 | 2.5 | 4.0 | 3.0 | - |
| BAF-3.O1-O2 | 3.3 | 2.2 | 5.0 | 3.5 | - | 4.4 |
| 합계 | 100.0 | 100.0 | 100.0 | 100.0 | 100.0 | 100.0 |
<
실험예
>
액정 조성물의 물성 평가
상기 제조예 및 비교 제조예에서 제조한 액정 조성물의 물성을 하기와 같은 방법으로 평가하였다.
(1) 상전이온도(TN-I)
상전이온도를 측정하고자 하는 액정 조성물을 스포이드로 슬라이드 글라스 위에 한 방울 떨어뜨린 후, 커버 글라스로 덮어 샘플을 제조하였다.
METTLER TOLEDO FP90 온도 조정기가 달린 기구에 상기 샘플을 넣고, FP82HT Hot stage로 온도를 3℃/min의 속도로 올리면서 샘플의 변화를 관찰하였다. 샘플이 네마틱 액정상에서 등방성 액체로 변화하는 지점의 온도를 기록하고, 이와 같은 작업을 3회 반복하여 평균값을 도출하였다. 그리고, 이 값을 액정 조성물의 네마틱 액정상에서 등방성 액체로의 상전이온도(TN-I)로 규정하였다.
(2) 굴절률 이방성(n)
액정 조성물의 굴절률 이방성은 20℃에서 589nm 파장의 광을 사용하여 접안경에 편광판을 장착한 아베 굴절계로 측정하였다. 주프리즘의 표면을 한 방향으로 러빙한 후, 측정 대상인 액정 조성물을 주프리즘에 적하하였다. 이후, 편광의 방향이 러빙의 방향과 평행할 때의 굴절률과 편광의 방향이 러빙의 방향과 수직일 때의 굴절률을 측정하였다. 상기 서로 다른 두 방향의 굴절률 중 보다 큰 굴절률을 ne (extraordinary), 보다 작은 굴절률을 no (ordinary)라 규정하고, 상기 ne에서 no를 뺀 값을 n로 규정하였다.
(3) 유전율 이방성(△ε)
액정 조성물의 유전율 이방성(△ε)은 하기와 같이 측정된 ε∥ 및 ε⊥를 식 1에 대입하여 계산하였다.
[식 1]
△ε= ε∥-ε⊥
① 유전율 ε∥ 의 측정: 2 장의 유리 기판의 ITO 패턴이 형성된 면에 수직 배향제를 도포하여 수직 배향막을 형성하였다. 이어서, 수직 배향막이 서로 마주보며 2 장의 유리 기판 사이의 간격(셀 갭)이 4㎛가 되도록 2 장의 유리 기판 중 어느 하나의 기판에 스페이서를 도포한 후 2 장의 유리 기판을 합착시켰다. 그리고, 이 소자에 측정 대상인 액정 조성물을 주입하고, 열 또는 자외선으로 경화시키는 접착제로 밀폐하였다. 이후, Agilent에서 제조한 4294A 장비에 사용하여, 이 소자의 20℃에서 유전율 ε∥ 을 측정하였다.
② 유전율 ε⊥ 의 측정: 2 장의 유리 기판의 ITO 패턴이 형성된 면에 수평 배향제를 도포하여 수평 배향막을 형성하였다. 이어서, 수평 배향막이 서로 마주보며 2 장의 유리 기판 사이의 간격(셀 갭)이 4㎛가 되도록 2 장의 유리 기판 중 어느 하나의 기판에 스페이서를 도포한 후 2 장의 유리 기판을 합착시켰다. 그리고, 이 소자에 측정 대상인 액정 조성물을 주입하고, 자외선으로 경화시키는 접착제로 밀폐하였다. 이후, Agilent에서 제조한 4294A 장비에 사용하여, 이 소자의 20℃에서 유전율 ε⊥ 을 측정하였다.
(4) 점도(η, 단위: mPa·s)
점도 측정을 위해 SCHOTT 사의 CT52 장비를 이용하였으며, 이에 2 mL의 부피에 대해 점도 측정이 가능한 capillary viscometer를 장착 후 측정하고자 하는 액정 조성물 2 mL를 주입하였다. 이후, 액정 조성물을 20℃에서 30 분간 안정화시킨 후 스포이드 루버를 사용하여 측정 부위까지 액정 조성물을 끌어 올렸다. 이어서, 액정 조성물이 흘러내리는 속도를 타이머를 통해 측정하고, 이를 통해 점도를 구하였다.
(5) 회전점도(γ, 단위: mPa·s)
2 장의 유리 기판의 ITO 패턴이 형성된 면에 수직 배향제를 도포하여 수직 배향막을 형성하였다. 이어서, 수직 배향막이 서로 마주보며 2 장의 유리 기판 사이의 간격(셀 갭)이 50㎛가 되도록 2 장의 유리 기판 중 어느 하나의 기판에 스페이서를 도포한 후 2 장의 유리 기판을 합착시켰다. 그리고, 이 소자에 액정 조성물을 주입하고, 자외선으로 경화시키는 접착제로 밀폐하였다. 이후, ESPEC Corp.에서 제조한 온도 controller(Model SU-241)를 장착한 Toyo Corp.의 Model 6254 장비를 사용하여, 이 소자의 20℃에서 회전점도를 측정하였다.
상기 결과를 하기 표 4 및 5에 나타내었다.
| 항목 | 실시예 1 | 실시예 2 | 비교예 1 | 비교예 2 | 비교예 3 |
| TN-I | 75.8 | 75.4 | 75.2 | 74.7 | 77.0 |
| Δn | 0.1152 | 0.1157 | 0.1081 | 0.1088 | 01080 |
| ne | 1.6032 | 1.6041 | 1.5947 | 1.5962 | 1.5950 |
| no | 1.4880 | 1.4884 | 1.4866 | 1.4873 | 1.4870 |
| △ε | -3.48 | -3.57 | -3.03 | -3.12 | -2.95 |
| η | 19.02 | 19.00 | 17.8 | 17.55 | 18.03 |
| γ | 139 | 138 | 113 | 118 | 126 |
| 항목 | 실시예 3 | 실시예 4 | 실시예 5 | 실시예 6 | 비교예 4 | 비교예 5 |
| TN-I | 79.0 | 76.10 | 76.1 | 76.2 | 75.3 | 77.1 |
| Δn | 0.1125 | 0.1123 | 0.1128 | 0.1150 | 0.1082 | 0.1092 |
| ne | 1.6006 | 1.5993 | 1.6008 | 1.6028 | 1.5942 | 1.5950 |
| no | 1.4881 | 1.4870 | 1.4880 | 1.4878 | 1.4860 | 1.4858 |
| △ε | -3.67 | -3.60 | -3.90 | -3.97 | -3.06 | -3.23 |
| η | 18.62 | 16.91 | 18.34 | 19.10 | 15.53 | 16.57 |
| γ | 129 | 122 | 130 | 137 | 111 | 113 |
상기 표 4 및 5를 참조하면, 실시예 1 내지 6의 경우 모두 0.1100 이상의 고굴절률 이방성 및 -3.20 이하의 음의 고유전율 이방성을 나타냄이 확인되었다.
따라서, 본 발명의 일 구현예에 따른 액정 조성물을 사용하면, 양호한 굴절률 이방성 및 유전율 이방성을 가지는 액정 조성물을 제공할 수 있어 액정 표시 장치의 응답 시간을 현저하게 향상시킬 수 있음이 기대된다.
100: 액정 표시 장치
110: 컬러필터 기판
112: 광차단층
120: 박막트랜지스터 기판
130: 액정층
131: 액정
111: 상부 베이스 기판
113: 컬러필터
114: 상부 유기 절연막
115: 공통 전극
101: 상부 배향막
121: 베이스 기판
122: 게이트 전극
123: 게이트 절연막
124a: 채널층:
124b: 오믹 콘택층
125: 소스 전극
126: 드레인 전극
127: 하부 유기 절연막
128: 화소 전극
102: 하부 배향막
110: 컬러필터 기판
112: 광차단층
120: 박막트랜지스터 기판
130: 액정층
131: 액정
111: 상부 베이스 기판
113: 컬러필터
114: 상부 유기 절연막
115: 공통 전극
101: 상부 배향막
121: 베이스 기판
122: 게이트 전극
123: 게이트 절연막
124a: 채널층:
124b: 오믹 콘택층
125: 소스 전극
126: 드레인 전극
127: 하부 유기 절연막
128: 화소 전극
102: 하부 배향막
Claims (17)
- 적어도 하나의 하기 화학식 1로 표시되는 액정 화합물; 및
적어도 하나의 하기 화학식 2로 표시되는 액정 화합물을 포함하는 액정 조성물:
[화학식 1]
상기 화학식 1에서,
L1, L2, L3 및 L4는 각각 독립적으로 수소 또는 할로겐이고,
R은 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시이고, 및
n1 및 n2는 각각 독립적으로 0 내지 2의 정수이고, n1 및 n2의 합은 0 이상 2 이하이고,
[화학식 2]
상기 화학식 2에서,
R1은 탄소수 2 내지 10의 알킬 또는 탄소수 1 내지 10의 알콕시이고,
R2는 탄소수 1 내지 10의 알킬 또는 탄소수 1 내지 10의 알콕시이고,
R3은 탄소수 1 내지 10의 알킬, 탄소수 1 내지 10의 알콕시, 또는 탄소수 2 내지 10의 알케닐이고,
고리 A는 사이클로헥실렌 또는 페닐렌이고,
Q1 및 Q2는 각각 독립적으로 단일 결합, -CH2O-, -OCH2-, -CH2CH2-, -CH=CH-, -C≡C-, -CH2CF2-, -CHFCHF-, -CF2CH2-, -CH2CHF-, -CHFCH2-, -CF2CF2-, -COO-, -OCO-, -CF2O-, -OCF2- 또는 -O-이고,
X1 내지 X3는 각각 독립적으로 수소, 할로겐, 또는 탄소수 1 내지 4의 할로알킬이고,
n은 0 내지 2의 정수이다.
- 제1항에 있어서,
상기 화학식 1의 L1, L2, L3 및 L4는 각각 독립적으로 수소 또는 플루오로인, 액정 조성물.
- 제2항에 있어서,
상기 화학식 1의 L1 과 L2가 동일하거나 L3 와 L4가 동일한, 액정 조성물.
- 제2항에 있어서,
상기 화학식 1의 L1 과 L2가 동일하고, L3 와 L4가 동일한, 액정 조성물.
- 제1항에 있어서,
상기 화학식 1의 R은 수소, 메틸, 에틸, 메톡시 또는 에톡시인, 액정 조성물.
- 제1항에 있어서,
상기 화학식 2의 R1은 탄소수 2 내지 5의 알킬이고, R2는 탄소수 1 내지 5의 알킬 또는 탄소수 1 내지 5의 알콕시이거나; 또는
R1은 탄소수 1 내지 5의 알콕시이고, R2는 탄소수 1 내지 5의 알킬인, 액정 조성물.
- 제1항에 있어서,
상기 화학식 2의 R3는 메틸, 에틸, 메톡시, 에톡시, 비닐, 또는 1-프로페닐인, 액정 조성물.
- 제1항에 있어서,
상기 화학식 2의 Q1 및 Q2는 각각 단일 결합인, 액정 조성물.
- 제1항에 있어서,
상기 화학식 2의 X1 내지 X3는 각각 독립적으로 수소, 플루오로 또는 트리플루오로메틸인, 액정 조성물.
- 제1항에 있어서,
하기 화학식 3 내지 6으로 이루어진 군에서 선택되는 하나 이상의 액정 화합물을 추가로 포함하는 액정 조성물:
[화학식 3]
상기 화학식 3에서,
R21 및 R22는 각각 독립적으로 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A3 및 A4는 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌(tetrahydropyranylene) 또는 1,4-페닐렌이고,
[화학식 4]
상기 화학식 4에서,
R31 및 R32는 각각 독립적으로 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A5 및 A7은 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌 또는 1,4-페닐렌이며,
고리 A6은 1,4-시클로헥실렌, 테트라하이드로피라닐렌, 1,4-페닐렌 또는 1 이상의 H가 할로겐으로 치환된 1,4-페닐렌이고,
o는 1 또는 2의 정수이고,
[화학식 5]
상기 화학식 5에서,
R41 및 R42는 각각 독립적으로 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A8 및 A9는 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌, 1,4-페닐렌 또는 1 이상의 H가 할로겐으로 치환된 1,4-페닐렌이며,
m은 0 내지 2의 정수이고,
[화학식 6]
상기 화학식 6에서,
R51 및 R52는 수소, 탄소수 1 내지 10의 알킬, 탄소수 2 내지 10의 알케닐 또는 탄소수 1 내지 10의 알콕시 중 어느 하나의 라디칼이거나, 혹은 상기 라디칼 중 1 이상의 H가 할로겐으로 치환되거나 또는 하나 이상의 산소 원자들이 직접 연결되지 않는 방식으로 -CH2-가 -C≡C-, -CH=CH-, -O-, -CO-O-, -O-CO- 또는 -O-CO-O-로 대체된 라디칼이고,
고리 A10, A11 및 A12는 각각 독립적으로 1,4-시클로헥실렌, 테트라하이드로피라닐렌, 1,4-페닐렌 또는 1 이상의 H가 할로겐으로 치환된 1,4-페닐렌이며,
Z1 및 Z2는 각각 독립적으로 -CH2CH2-, -CH=CH-, -CH2O-, -OCH2-, -C≡C-, -CH2CF2-, -CHFCHF-, -CF2CH2-, -CH2CHF-, -CHFCH2-, -C2F4-, -O-, -COO-, -OCO-, -CF2O- 또는 -OCF2-이고,
k1 및 k3는 각각 독립적으로 0 또는 1이되, k1 및 k3의 합은 1 또는 2이고,
k2 및 k4는 각각 독립적으로 0 내지 2의 정수이다.
- 제1항에 있어서,
상기 화학식 1의 액정 화합물은 상기 액성 조성물 전체 중량 대비 2 내지 20 중량%로 포함되고,
상기 화학식 2의 액정 화합물은 상기 액성 조성물 전체 중량 대비 1 내지 15 중량%로 포함되는, 액정 조성물.
- 제1항에 있어서,
산화 방지제 또는 UV 안정화제를 추가로 포함하는, 액정 조성물.
- 제1항에 있어서,
굴절률 이방성이 0.1100 이상이고, 유전율 이방성이 -3.20 이하인, 액정 조성물.
- 제1항 내지 제16항 중 어느 한 항의 액정 조성물을 포함하는, 액정 표시 장치.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020170024909 | 2017-02-24 | ||
| KR20170024909 | 2017-02-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180098131A true KR20180098131A (ko) | 2018-09-03 |
Family
ID=63375695
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020180010012A Withdrawn KR20180098131A (ko) | 2017-02-24 | 2018-01-26 | 액정 조성물 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20180098131A (ko) |
| CN (1) | CN108504364A (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112143508B (zh) * | 2020-10-09 | 2022-03-18 | 烟台显华科技集团股份有限公司 | 具有负介电各向异性的液晶化合物、液晶组合物及液晶显示器件 |
| CN115651669B (zh) * | 2022-11-14 | 2024-12-03 | 北京八亿时空液晶科技股份有限公司 | 一种负介电各向异性的液晶组合物及其应用 |
-
2018
- 2018-01-26 KR KR1020180010012A patent/KR20180098131A/ko not_active Withdrawn
- 2018-02-23 CN CN201810155812.1A patent/CN108504364A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN108504364A (zh) | 2018-09-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN105189701B (zh) | 液晶组合物与其用途及液晶显示元件 | |
| TWI475097B (zh) | 光等向性的液晶媒體與光元件 | |
| TWI431102B (zh) | 液晶組成物及液晶顯示元件 | |
| KR101431935B1 (ko) | 시클로헥산 화합물 및 그 화합물을 함유한 액정 조성물 | |
| KR20120093835A (ko) | 액정 조성물 및 액정 표시 소자 | |
| JP4662849B2 (ja) | パーフルオロアリルオキシ化合物及び該化合物を含有した液晶組成物 | |
| JP2014162752A (ja) | 化合物、液晶組成物、及び表示装置 | |
| KR102202251B1 (ko) | 액정 화합물, 액정 조성물 및 이를 포함하는 액정 표시 장치 | |
| JP4691893B2 (ja) | トリフルオロナフタレン誘導体を含有する液晶組成物と表示素子及び化合物。 | |
| TW201502254A (zh) | 液晶組成物及液晶顯示元件 | |
| KR20160123974A (ko) | 액정 표시 장치 및 이에 사용되는 액정 조성물 | |
| KR20180098131A (ko) | 액정 조성물 | |
| TWI464242B (zh) | 負介電異方性液晶化合物、液晶顯示器、與光電裝置 | |
| CN107001936B (zh) | 液晶化合物及包含它的液晶组合物 | |
| JP6115303B2 (ja) | 隣接基としてカルボニル基を有するフェノール化合物およびその用途 | |
| CN104788297B (zh) | 含有二氟亚甲氧基的液晶化合物及其组合物和应用 | |
| WO2017116075A1 (ko) | 액정 조성물 및 이를 포함하는 액정 표시 장치 | |
| KR20160136118A (ko) | 액정 화합물 및 이를 포함하는 액정 조성물 | |
| CN101747905B (zh) | 液晶化合物及包括此化合物的液晶组合物 | |
| KR102580896B1 (ko) | 중합성 화합물 및 이를 포함하는 액정 조성물 | |
| KR20180002542A (ko) | 액정 화합물 및 이를 포함하는 액정 조성물 | |
| KR101600391B1 (ko) | 내열성 액정 배향제, 액정 조성물 및 액정 표시 장치 | |
| JP2009263238A (ja) | 含フッ素液晶化合物、その製造方法および合成中間体、該含フッ素液晶化合物を含有する液晶組成物ならびに液晶電気光学素子 | |
| JP4573399B2 (ja) | ジフルオロベンゾニトリル化合物およびその中間体、製造方法、液晶組成物および液晶電気光学素子 | |
| JP6912056B2 (ja) | 液晶組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20180126 |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination |