KR20170027808A - 사이클로헥사논의 제조를 위한 방법 및 시스템 - Google Patents
사이클로헥사논의 제조를 위한 방법 및 시스템 Download PDFInfo
- Publication number
- KR20170027808A KR20170027808A KR1020177002642A KR20177002642A KR20170027808A KR 20170027808 A KR20170027808 A KR 20170027808A KR 1020177002642 A KR1020177002642 A KR 1020177002642A KR 20177002642 A KR20177002642 A KR 20177002642A KR 20170027808 A KR20170027808 A KR 20170027808A
- Authority
- KR
- South Korea
- Prior art keywords
- effluent
- cyclohexylbenzene
- phenol
- concentration
- hydrogenation
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/006—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by hydrogenation of aromatic hydroxy compounds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/14—Fractional distillation or use of a fractionation or rectification column
- B01D3/143—Fractional distillation or use of a fractionation or rectification column by two or more of a fractionation, separation or rectification step
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/24—Stationary reactors without moving elements inside
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/68—Purification; separation; Use of additives, e.g. for stabilisation
- C07C37/70—Purification; separation; Use of additives, e.g. for stabilisation by physical treatment
- C07C37/74—Purification; separation; Use of additives, e.g. for stabilisation by physical treatment by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C39/00—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring
- C07C39/02—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring monocyclic with no unsaturation outside the aromatic ring
- C07C39/04—Phenol
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/78—Separation; Purification; Stabilisation; Use of additives
- C07C45/81—Separation; Purification; Stabilisation; Use of additives by change in the physical state, e.g. crystallisation
- C07C45/82—Separation; Purification; Stabilisation; Use of additives by change in the physical state, e.g. crystallisation by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/78—Separation; Purification; Stabilisation; Use of additives
- C07C45/85—Separation; Purification; Stabilisation; Use of additives by treatment giving rise to a chemical modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/385—Saturated compounds containing a keto group being part of a ring
- C07C49/403—Saturated compounds containing a keto group being part of a ring of a six-membered ring
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/24—Stationary reactors without moving elements inside
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/582—Recycling of unreacted starting or intermediate materials
Abstract
적어도 일부의 혼합물을 수소화하는 단계 또는 장치 및 페놀/사이클로헥사논/사이클로헥실벤젠 혼합물을 증류하여 사이클로헥사논이 풍부한 유출물을 수득하는 단계 또는 장치를 포함하는, 페놀, 사이클로헥사논, 및 사이클로헥실벤젠을 포함하는 혼합물로부터 사이클로헥사논을 제조하기 위한 방법 및 시스템이 개시되어 있다.
Description
관련 출원에 대한 우선권 주장
본 출원은 2014년 8월 15일에 출원된 미국 가출원 일련번호 제62/037,794호 및 2014년 10월 13일에 출원된 유럽출원번호 제14188588.9호에 대해 우선권을 주장하며, 이의 개시내용은 그 전문이 본원에 참조로 포함되어 있다.
기술분야
본 발명은 사이클로헥사논의 제조를 위한 공정 및 시스템에 관한 것이다. 특히, 본 발명은 페놀 수소화에 의한 사이클로헥사논의 제조를 위한 공정 및 시스템에 관한 것이다. 본 발명은 예를 들면, 사이클로헥실벤젠 산화 및 사이클로헥실벤젠 하이드로퍼옥사이드 분해로부터 사이클로헥사논을 제조하는데 유용하다.
사이클로헥사논은 화학 산업에서 중요한 물질이고, 예를 들면, 페놀성 수지, 비스페놀 A, ε-카프로락탐, 아디프산, 및 가소제의 제조에서 널리 사용된다. 사이클로헥사논을 제조하기 위한 하나의 방법은 페놀의 수소화에 의한 것이다.
현재, 페놀의 제조를 위한 일반적인 경로는 호크 공정(Hock process)이다. 이는 제1 단계가 쿠멘을 제조하기 위한 벤젠의 프로필렌과의 알킬화, 이후 쿠멘의 상응하는 하이드로퍼옥사이드로의 산화, 및 이후 등몰 양의 페놀 및 아세톤을 제조하기 위한 하이드로퍼옥사이드의 분리를 수반하는 3단계 공정이다. 분리된 페놀 생성물은 이후 수소화 단계에 의해 사이클로헥사논으로 전환될 수 있다.
예를 들면, 미국특허 제6,037,513호로부터, 사이클로헥실벤젠은 MCM-22 유형의 분자체 및 팔라듐, 루테늄, 니켈, 코발트, 및 이들의 혼합물로부터의 하나 이상의 수소화 금속을 포함하는 이작용성 촉매의 존재 하에 벤젠을 수소와 접촉시켜 제조될 수 있다. 이 문헌은 생성된 사이클로헥실벤젠이 상응하는 하이드로퍼옥사이드로 산화될 수 있고, 이는 분해되어 페놀 및 사이클로헥사논의 분해 혼합물을 생성할 수 있고, 이는 결국 분리되어 순수한, 실질적으로 등몰의 페놀 및 사이클로헥사논 생성물을 수득할 있다. 페놀 및 사이클로헥사논을 공동제조하기 위한 이 사이클로헥실벤젠-기반 공정은 이러한 2개의 중요한 공업적 재료를 제조하는데 매우 효율적일 수 있다. 페놀보다 높은 상업적 가치의 사이클로헥사논이 얻어지는 경우, 본 공정에서 페놀보다 사이클로헥사논을 더 많이 제조하는 것이 매우 바람직하다. 이는 본 공정에서 일부 또는 모든 페놀을 사이클로헥사논으로 전환하기 위해 제조되는 순수 페놀 생성물을 이후 수소화함으로써 달성되는 한편, 보다 경제적인 공정 및 시스템이 더 바람직하다.
상기 사이클로헥실벤젠-기반 공정으로부터 페놀보다 더 많은 사이클로헥사논을 제조하는 하나의 해결책은 분해 혼합물로부터 수득된 페놀 및 사이클로헥사논을 함유하는 혼합물을 수소화하여 이에 포함된 적어도 일부의 페놀을 사이클로헥사논으로 전환시키는 것이다. 그러나, 페놀/사이클로헥사논 혼합물은 언제나 수소화 단계에서 비사이클로헥산로 전환될 수 있는 상당한 양의 사이클로헥실벤젠을 함유하고, 그리고 페놀/사이클로헥사논/사이클로헥실벤젠 혼합물의 수소화는 또한 사이클로헥사놀의 형성을 야기할 수 있고, 이 둘은 수율 손실을 야기할 수 있기 때문에, 이러한 방법은 해결과제를 가진다.
이와 같이, 페놀, 사이클로헥사논 및 사이클로헥실벤젠을 함유하는 혼합물로부터 사이클로헥사논을 제조하기 위한 개선된 방법 및/또는 시스템에 대한 필요성이 존재한다.
본 발명은 이러한 그리고 다른 필요성을 충족시킨다.
요약
고순도의 사이클로헥사논은 증류 및 수소화 단계의 다양한 조합에 의해 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 혼합물로부터 효과적으로 제조될 수 있다는 것이 밝혀졌다.
제1 양태에서, 본 개시물은 하기 단계를 포함하는 사이클로헥사논의 제조 방법에 관한 것이다:
(I) 제1 증류 컬럼으로 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 제1 혼합물을 공급하는 단계;
(II) 제1 증류 컬럼으로부터 하기를 수득하는 단계:
제1 혼합물보다 높은 농도의 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 제1 상부 유출물;
사이클로헥사논, 제1 혼합물보다 높은 농도의 페놀, 사이클로헥실벤젠 및 비사이클로헥산을 포함하는 제1 중간 유출물; 및
제1 혼합물보다 높은 농도의 사이클로헥실벤젠을 포함하는 제1 하부 유출물;
(III) 수소화 반응 구간으로 적어도 일부의 제1 중간 유출물 및 수소를 공급하는 단계로서, 여기서 페놀은 수소화 반응 조건으로 수소화 촉매의 존재 하에 수소와 반응하여, 제1 중간 유출물보다 높은 농도의 사이클로헥사논, 제1 중간 유출물보다 낮은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 수소화 반응 생성물을 수득하는 단계; 및
(IV) 적어도 일부의 수소화 반응 생성물을 제1 증류 컬럼으로 공급하는 단계.
본 개시물의 제2 양태는 사이클로헥사논을 제조하기 위한 제1 양태의 방법을 실시하도록 구성된 시스템에 관한 것으로, 상기 시스템은 하기를 포함한다:
(A) (i) 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 제1 혼합물을 공급받고; 그리고
(ii) 제1 혼합물보다 높은 농도의 사이클로헥사논을 포함하는 제1 상부 유출물;
사이클로헥사논, 제1 혼합물보다 높은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 제1 중간 유출물; 및
제1 혼합물보다 높은 농도의 사이클로헥실벤젠을 포함하는 제1 하부 유출물
을 제조하기 위해 구성된 제1 증류 컬럼;
(B) 적어도 일부의 제1 중간 유출물 및 수소를 공급받도록 구성된 수소화 반응 구간으로서, 여기서 페놀은 수소화 반응 조건으로 수소화 촉매의 존재 하에 수소와 반응하여, 제1 중간 유출물보다 높은 농도의 사이클로헥사논, 제1 중간 유출물보다 낮은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 수소화 반응 생성물을 제조하는 수소화 반응 구간; 및
(C) 적어도 일부의 수소화 반응 생성물을 제1 증류 컬럼으로 전달하도록 구성된 제1 유체 연통체(fluid communication).
도 1은 제1 분획화 컬럼(T1), 수소화 반응기(R1), 및 사이클로헥사논 정제 컬럼(T2)를 포함하는, 페놀, 사이클로헥사논 및 사이클로헥실벤젠을 포함하는 혼합물로부터 사이클로헥사논을 제조하기 위한, 본 개시물의 예시적인 방법/시스템을 나타내는 개략도이다.
도 2는 제1 분획화 컬럼(T1) 및 수소화 반응기(R1) 사이에 및/또는 그 내부에 변형된 유체 연통체를 포함하는 것을 제외하고, 도 1에 나타난 방법/시스템과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 3은 제1 분획화 컬럼(T1) 및 사이클로헥사논 정제 컬럼(T2) 사이에 및/또는 그 내부에 변형된 유체 연통체 및/또는 열전달 구조체를 포함하는 것을 제외하고, 도 1 및 2에 나타난 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 4는 수소화 반응이 주로 증기상에서 일어나는 관형 열 교환기-유형 수소화 반응기(R1)을 포함하는 것을 제외하고, 도 1 내지 도 3에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 5는 수소화 반응이 주로 액상에서 일어나는 일련으로 연결된 3개의 수소화 반응기(R3, R5, 및 R7)을 포함하는 것을 제외하고, 도 1 내지 도 4에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 6은 제1 분획화 컬럼(T1) 및 수소화 반응기(R1) 사이에 및/또는 그 내부에 변형된 유체 연통체를 포함하는 것을 제외하고, 도 1 내지 5에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 7은 수소화 반응기에서의 촉매 피독화를 감소시키거나 방지하기 위해 제1 분획화 컬럼(T1)으로 공급되는 페놀/사이클로헥사논/사이클로헥실벤젠 공급물로부터 적어도 일부의 경질 성분을 제거하도록 구성된 제1 분획화 컬럼(T1) 앞에 사이드 스트리퍼 컬럼(T4)를 포함하는 것을 제외하고, 도 1 내지 6에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 8은 수소화 반응기에서의 촉매 피독화를 감소시키거나 방지하기 위해 수소화 반응기로 공급되는 페놀/사이클로헥사논/사이클로헥실벤젠 공급물로부터 적어도 일부의 경질 성분을 제거하도록 구성된 제1 분획화 컬럼(T1) 뒤에 사이드 스트리퍼 컬럼(T5)를 포함하는 것을 제외하고, 도 1 내지 7에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 9는 최종 사이클로헥사논 생성물로부터 경질 성분의 양을 감소시키도록 구성된 사이클로헥사논 정제 컬럼(T2) 뒤에 사이드 스트리퍼 컬럼(T6)을 포함하는 것을 제외하고, 도 1 내지 8에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 2는 제1 분획화 컬럼(T1) 및 수소화 반응기(R1) 사이에 및/또는 그 내부에 변형된 유체 연통체를 포함하는 것을 제외하고, 도 1에 나타난 방법/시스템과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 3은 제1 분획화 컬럼(T1) 및 사이클로헥사논 정제 컬럼(T2) 사이에 및/또는 그 내부에 변형된 유체 연통체 및/또는 열전달 구조체를 포함하는 것을 제외하고, 도 1 및 2에 나타난 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 4는 수소화 반응이 주로 증기상에서 일어나는 관형 열 교환기-유형 수소화 반응기(R1)을 포함하는 것을 제외하고, 도 1 내지 도 3에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 5는 수소화 반응이 주로 액상에서 일어나는 일련으로 연결된 3개의 수소화 반응기(R3, R5, 및 R7)을 포함하는 것을 제외하고, 도 1 내지 도 4에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 6은 제1 분획화 컬럼(T1) 및 수소화 반응기(R1) 사이에 및/또는 그 내부에 변형된 유체 연통체를 포함하는 것을 제외하고, 도 1 내지 5에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 7은 수소화 반응기에서의 촉매 피독화를 감소시키거나 방지하기 위해 제1 분획화 컬럼(T1)으로 공급되는 페놀/사이클로헥사논/사이클로헥실벤젠 공급물로부터 적어도 일부의 경질 성분을 제거하도록 구성된 제1 분획화 컬럼(T1) 앞에 사이드 스트리퍼 컬럼(T4)를 포함하는 것을 제외하고, 도 1 내지 6에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 8은 수소화 반응기에서의 촉매 피독화를 감소시키거나 방지하기 위해 수소화 반응기로 공급되는 페놀/사이클로헥사논/사이클로헥실벤젠 공급물로부터 적어도 일부의 경질 성분을 제거하도록 구성된 제1 분획화 컬럼(T1) 뒤에 사이드 스트리퍼 컬럼(T5)를 포함하는 것을 제외하고, 도 1 내지 7에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
도 9는 최종 사이클로헥사논 생성물로부터 경질 성분의 양을 감소시키도록 구성된 사이클로헥사논 정제 컬럼(T2) 뒤에 사이드 스트리퍼 컬럼(T6)을 포함하는 것을 제외하고, 도 1 내지 8에 나타낸 것과 유사한 본 개시물의 일부의 예시적인 방법/시스템을 나타내는 개략도이다.
청구된 본 발명의 이해의 목적을 위해 본원에 적용된 바람직한 구현예 및 정의를 비롯하여 본 발명의 다양한 특정 구현예, 형태 및 예가 하기에 기술될 것이다. 하기 상세한 설명이 특정 바람직한 구현예를 기술하는 한편, 본 기술분야의 당업자는 이러한 구현예는 단지 예시적인 것이고, 본 발명이 다른 방식으로 실시될 수 있음을 이해할 것이다. 침해를 결정하기 위한 목적을 위해, 본 발명의 범위는 인용되는 것과 동등한 이의 등가물, 및 구성요소 또는 한정사항을 포함하는 임의의 하나 이상의 첨부된 청구항과 관련될 것이다. "본 발명"에 대한 임의의 참조는 청구항에 의해 정의된 본 발명의 필수적으로 전부는 아니나 하나 이상과 관련될 수 있다.
본 개시물에서, 공정은 하나 이상의 "단계"를 포함하는 것으로 기술된다. 각각의 단계는 연속적이거나 불연속적인 방식으로 공정에서의 일회 또는 복수회 실시될 수 있는 작동 또는 작업인 것으로 이해되어야 한다. 반대로 설명되거나 맥락에서 분명하게 달리 나타내지 않는 한, 공정에서의 각각의 단계는 다른 단계와 중복되거나 중복됨 없이 이들이 열거된 순서로 순차적으로, 또는 경우에 따라 임의의 다른 순서로 실시될 수 있다. 또한, 하나 이상 또는 심지어 모든 단계는 물질의 동일하거나 상이한 배치와 동시에 실시될 수 있다. 예를 들면, 연속식 공정에서, 공정에서의 제1 단계는 공정의 초기에 막 공급된 원재료와 관련하여 실시되는 한편, 제2 단계는 제1 단계의 초기에 공정에 공급된 원재료를 처리하여 생성된 중간체 물질과 관련하여 동시에 실시될 수 있다. 바람직하게는, 본 단계는 기재된 순서로 실시된다.
달리 나타내지 않는 한, 본 개시물에서 양을 나타내는 모든 수는 모든 경우에서 용어 "약"으로 변경되는 것으로 이해된다. 또한, 명세서 및 청구항에 사용되는 정확한 수치 값은 특정 구현예를 구성하는 것으로 이해되어야 한다. 실시예에서 데이터의 정확성을 보장하기 위해 노력이 이루어졌다. 그러나, 측정하는데 사용되는 기술 및 장비의 한계로 인해 임의의 측정된 데이터는 본래 특정 수준의 오차를 가지는 것으로 이해되어야 한다.
본원에 사용되는 바와 같이, 부정 관사 ("a" 또는 "an")는 반대로 상세되지 않거나 문맥에서 분명하게 달리 나타내지 않는 한, "하나 이상"을 의미하는 것이다. 따라서, "분획화 컬럼"을 사용하는 구현예는 반대로 상세되거나 문맥이 분명하게 단지 하나의 분획화 컬럼을 사용하는 것을 나타내지 않는 한, 1, 2개 또는 그 이상 분획화 컬럼을 사용하는 구현예를 포함한다. 마찬가지로, "C12+ 성분"은 단지 하나의 특정 C12+ 성분을 의미하는 것으로 상세되거나 문맥에 나타나지 않는 한, 1, 2개 또는 그 이상의 C12+ 성분을 포함하는 것으로 해석되어야 한다.
본원에 사용되는 바와 같이, "wt%"는 중량%를 의미하고, "vol%"는 부피%를 의미하고, "mol%"는 몰%를 의미하고, "ppm"은 백만분율을 의미하고, "ppm wt" 및 "wppm"은 중량 기준의 백만분율을 의미하는 것으로 상호교환적으로 사용된다. 본원에 사용되는 모든 "ppm"은 달리 상세되지 않는 한 중량 ppm이다. 본원의 모든 농도는 논의상 조성물의 총량 기준으로 표현된다. 따라서, 제1 공급 원료의 다양한 성분의 농도는 제1 공급 원료의 총 중량 기준으로 표현된다. 본원에 표현되는 모든 범위는 반대로 상세되거나 나타내지 않는 한, 2개의 특정 구현예의 두 종점을 포함할 것이다.
본 개시물에서, 컬럼의 말단(상부 또는 하부)에 "부근의" 위치는 컬럼의 말단(상부 또는 하부)로부터의 *Hc의 거리 내의 위치를 의미하고, Hc는 하부로부터 상부로의 컬럼의 높이이고, a1 ≤ a ≤ a2이고, 여기서 a1 및 a2는 a1 < a2이기만 한 경우에 독립적으로 0, 0.01, 0.02, 0.03, 0.04, 0.05, 0.06, 0.07, 0.08, 0.09, 0.10, 0.11, 0.12, 0.13, 0.14, 0.15, 0.16, 0.17, 0.18, 0.19, 0.20일 수 있다. 예를 들면, 컬럼의 말단의 부근의 위치는 최대 D 미터의 말단(상부 또는 하부)으로부터 절대 거리를 가질 수 있으며, D는 5.0, 4.5, 4.0, 3.5, 3.0, 2.5, 2.0, 1.5, 1.0, 0.8, 0.5, 0.4, 0.3, 0.2, 0.1, 또는 0일 수 있다.
본원에 사용되는 바와 같은 "상부 유출물"은 용기 예컨대 분획화 컬럼 또는 반응기의 가장 상부 또는 측면에 존재할 수 있으며, 이 위에 추가의 유출물이 있거나 없을 수 있다. 바람직하게는, 상부 유출물은 하나 이상의 공급물 위의 위치에서 인출된다. 본원에 사용되는 "하부 유출물"은 상부 유출물보다 낮은 위치에 존재하고, 이는 용기의 가장 하부 또는 측면에 존재할 수 있고, 측면인 경우 이보다 아래에 추가의 유출물이 있거나 없을 수 있다. 바람직하게는, 하부 유출물은 컬럼의 하부의 부근의 위치에서 인출된다. 바람직하게는, 하부 유출물은 하나 이상의 공급물 아래의 위치에서 인출된다. 본원에 사용되는 "중간 유출물"은 상부 유출물과 하부 유출물 사이의 유출물이다. 증류 컬럼 상의 "동일한 수준"은 컬럼의 총 높이의 5% 이하의 총 높이를 갖는 컬럼의 연속적인 세그먼트(continuous segment)를 의미한다.
본원 사용되는 원소 및 족의 명명법은 1998년 국제 순수 응용화학 연합(International Union of Pure and Applied Chemistry)에 의해 사용되는 주기율표에 따른다. 주기율표의 예는 문헌 [Advanced Inorganic Chemistry, 6th Edition, by F. Albert Cotton et al. (John Wiley & Sons, Inc., 1999)]의 앞면 커버의 내부 페이지에 나타나 있다.
본원에 사용되는 용어 "메틸사이클로펜타논"은 이들 2개의 이성질체 중 단지 하나만을 의미하는 것으로 분명하게 상세하거나 또는 이 경우를 문맥에서 분명하게 나타내지 않는 한, 이들 사이의 임의의 비율로, 두 이성질체 2-메틸사이클로펜타논 (CAS 등록번호 1120-72-5) 및 3-메틸사이클로펜타논 (CAS 등록번호 1757-42-2)을 포함한다. 본 공정의 다양한 단계의 조건 하에, 두 이성질체가 이성질화 반응이 진행되어 용기 예컨대 분획화 컬럼 내로 충전되기 바로 전에 원재료에서의 것과 상이한 이들 사이의 비를 생성할 수 있다는 것을 주지하여야 한다.
본원에 사용되는 일반 용어 "사이클로헥실벤젠" ("DiCHB")은 응집체에서, 이들 중 하나 또는 2개만을 의미하는 것으로 분명하게 상세하지 않는 한, 1,2-디사이클로헥실벤젠, 1,3-디사이클로헥실벤젠, 및 1,4-디사이클로헥실벤젠을 포함한다. 단일 형태로 사용되는 경우, 용어 사이클로헥실벤젠은 일치환된 사이클로헥실벤젠을 의미한다. 본원에 사용되는 용어 "C12"는 12개의 탄소 원자를 갖는 화합물을 의미하고, "C12+ 성분"은 12개 이상의 탄소 원자를 갖는 화합물을 의미한다. C12+ 성분의 예는 무엇보다도, 사이클로헥실벤젠, 비페닐, 비사이클로헥산, 메틸사이클로펜틸벤젠, 1,2-비페닐벤젠, 1,3-비페닐벤젠, 1,4-비페닐벤젠, 1,2,3-트리페닐벤젠, 1,2,4-트리페닐벤젠, 1,3,5-트리페닐벤젠, 및 이들 화합물로부터 유도되는 대응되는 산소화물 예컨대 알코올, 케톤, 산, 및 에스테르를 포함한다. 본원에 사용되는 용어 "C18"은 18개의 탄소 원자를 갖는 화합물을 의미하고, 용어 "C18+ 성분"은 18개 이상의 탄소 원자를 갖는 화합물을 의미한다. C18+ 성분의 예는, 무엇보다도, 디사이클로헥실벤젠 ("DiCHB", 상기 기재됨), 트리사이클로헥실벤젠 ("TriCH", 이의 모든 이성질체 포함, 1,2,3-트리사이클로헥실벤젠, 1,2,4-트리사이클로헥실벤젠, 1,3,5-트리사이클로헥실벤젠, 및 임의의 비율로의 이들의 2개 이상의 혼합물 포함)을 포함한다. 본원에 사용되는 용어 "C24"는 24개의 탄소 원자를 갖는 화합물을 의미한다.
본원에 사용되는 바와 같은 용어 "MCM-22 유형 물질" (또는 "MCM-22 유형의 물질" 또는 "MCM-22 유형의 분자체" 또는 "MCM-22 유형 제올라이트")는 하기 중 하나 이상을 포함한다:
단위 셀이 MWW 프레임워크 토폴로지(framework topology)를 갖는, 통상의 1급 결정성 빌딩 블록 단위 셀(common first degree crystalline building block unit cell)로 제조된 분자체. 단위 셀은 3차원 공간에 타일링(tiling)되는 경우 결정 구조를 정의하는 원자의 공간 배열이다. 이러한 결정 구조는 문헌 ["Atlas of Zeolite Framework Types," Fifth Edition, 2001]에 논의되어 있고, 이의 전체 내용은 참조로 포함되어 있음;
1개 이상의 단위 셀 두께의 층들인 통상의 2급 빌딩 블록으로 제조된 분자체로서, 여기서 1개 초과의 단위 셀 두께의 층은 하나 이상의 단위 셀 두께의 2개 이상의 단층을 적층하거나, 팩킹하거나, 또는 결합하여 제조되는 분자체. 이러한 2급 빌딩 블록의 적층은 규칙적 방식, 불규칙적 방식, 무작위 방식, 또는 이들의 임의의 조합일 수 있음; 및
MCM-22 유형의 분자체는 12.4±0.25, 6.9±0.15, 3.57±0.07, 및 3.42±0.07 옹스트롬에서 d-간격 최대치(d-spacing maxima)를 포함하는 X-선 회절 패턴을 갖는 분자체를 포함한다. 물질을 특성화하는데 사용되는 X-선 회절 데이터는 입사 방사선으로서 구리의 K-알파 이중선 및 수집 시스템으로서 신틸레이션 계수기 및 관련된 컴퓨터를 구비한 회절계를 사용하는 것과 같은 표준 기술에 의해 얻어진다.
MCM-22 유형의 물질은 MCM-22 (미국특허 제4,954,325호 기술됨), PSH-3 (미국특허 제4,439,409호에 기술됨), SSZ-25 (미국특허 제4,826,667호에 기술됨), ERB-1 (유럽특허 제0293032호에 기술됨), ITQ-1 (미국특허 제6,077,498호에 기술됨), ITQ-2 (국제특허출원번호 WO97/17290에 기술됨), MCM-36 (미국특허 제5,250,277호에 기술됨), MCM-49 (미국특허 제5,236,575호에 기술됨), MCM-56 (미국특허 제5,362,697호에 기술됨), 및 이들의 혼합물을 포함한다. 다른 분자체 예컨대 UZM-8 (미국특허 제6,756,030호에 기술됨)은 단독으로 또는 본 개시물의 목적을 위해서 MCM-22 유형 분자체와 함께 사용될 수 있다. 바람직하게는, 본 개시물의 촉매에 사용되는 분자체는 (a) MCM-49; (b) MCM-56; 및 (c) MCM-49 및 MCM-56, 예컨대 ITQ-2의 아이소타입으로부터 선택된다.
본원에 개시된 사이클로헥사논을 제조하기 위한 공정 및 시스템은 유리하게는 페놀, 사이클로헥사논 및 사이클로헥실벤젠을 포함하는 임의의 공급물 혼합물로부터 사이클로헥산논을 제조하기 위해 사용될 수 있다. 공급물이 임의의 공정 또는 공급원으로부터 유도될 수 있는 한편, 이는 바람직하게는 사이클로헥실벤젠 하이드로퍼옥사이드 및 사이클로헥실벤젠을 포함하는 혼합물의 산 분해(acid cleavage)로부터 수득되고, 이는 결국 바람직하게는 사이클로헥실벤젠의 호기성 산화로부터 수득되고, 이는 결국 바람직하게는 수득된 벤젠이다. 이러한 바람직한 공정의 단계들은 하기 상세하게 기술되어 있다.
사이클로헥실벤젠의
공급
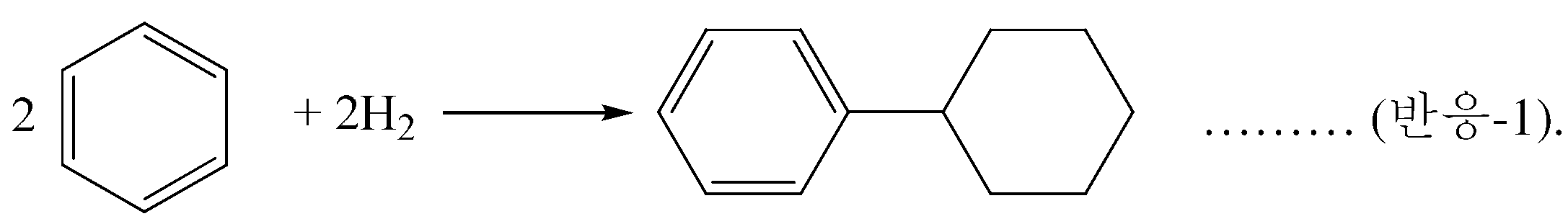
산화 단계로 공급되는 사이클로헥실벤젠은 제조되고 및/또는 벤젠으로부터 페놀 및 사이클로헥사논을 제조하기 위한 통합된 공정의 일부로서 재순환될 수 있다. 이러한 통합된 공정에서, 벤젠은 비페닐의 수소화가 후속되는 비페닐을 제조하기 위한 벤젠의 산화적 커플링을 포함하는 임의의 종래의 기술에 의해 초기에 사이클로헥실벤젠으로 전환된다. 그러나, 실제로, 사이클로헥실벤젠은 하이드로알킬화 촉매의 존재 하에 하이드로알킬화 조건으로 벤젠을 수소와 접촉시켜 제조되고, 이에 의해 벤젠은 하기 반응-1이 진행되어 사이클로헥실벤젠 (CHB)을 생성한다:
대안적으로, 사이클로헥실벤젠은 하기 반응-2에 따라 고형-산 촉매 예컨대 MCM-22 부류의 분자체의 존재 하에 사이클로헥센과의 벤젠의 직접 알킬화에 의해 제조될 수 있다;
미국특허 제6,730,625호 및 제7,579,511호, WO2009/13176, 및 WO2009/128984는 하이드로알킬화 촉매의 존재 하에 벤젠을 수소와 반응시켜 사이클로헥실벤젠을 제조하는 방법을 개시하고 있고, 이의 내용은 그 전문이 참조로 본원에 포함되어 있다.
하이드로알킬화 반응에 이용되는 촉매는 분자체, 예컨대 상기 기재된 MCM-22 유형 중 하나 및 수소화 금속을 포함하는 이작용성 촉매이다.
임의의 공지된 수소화 금속은 하이드로알킬화 촉매에서 이용될 수 있고, 이의 특정한, 비제한적인 적합한 예는 Pd, Pt, Rh, Ru, Ir, Ni, Zn, Sn, Co를 포함하고, Pd가 특히 유리하다. 바람직하게는, 촉매에 존재하는 수소화 금속의 양은 촉매의 총 중량의 0.05 wt% 내지 10.0 wt%, 예컨대 0.10 wt% 내지 5.0 wt%이다.
분자체 및 수소화 금속 이외, 하이드로알킬화 촉매는 하나 이상의 임의의 무기 산화물 지지체 물질 및/또는 결합제를 포함할 수 있다. 적합한 무기 산화물 지지체 물질(들)은 비제한적으로, 클레이, 비금속 산화물, 및/또는 금속 산화물을 포함한다. 이러한 지지체 물질의 특정한, 비제한적인 예는 SiO2, Al2O3, ZrO2, Y2O3, Gd2O3, SnO, SnO2, 및 이의 혼합물, 조합물 및 복합체를 포함한다.
하이드로알킬화 반응 (하이드로알킬화 반응 생성물 혼합물) 또는 알킬화 반응 (알킬화 반응 생성물 혼합물)로부터의 유출물은 일부의 폴리알킬화 벤젠, 예컨대 디사이클로헥실벤젠 (DiCHB), 트리사이클로헥실벤젠 (TriCHB), 메틸사이클로펜틸벤젠, 미반응된 벤젠, 사이클로헥산, 비사이클로헥산, 비페닐, 및 다른 오염물을 포함할 수 있다. 따라서, 통상적으로, 반응 이후, 하이드로알킬화 반응 생성물 혼합물은 증류에 의해 분리되어 C6 분획 함유 벤젠, 사이클로헥산, C12 분획 함유 사이클로헥실벤젠 및 메틸사이클로펜틸벤젠, 및 중질 분획 함유, 예를 들면, C18 예컨대 DiCHB 및 C24 예컨대 TriCHB를 수득한다. 미반응된 벤젠은 증류에 의해 회수되고, 하이드로알킬화 또는 알킬화 반응으로 재순환된다. 사이클로헥산은 일부의 잔류 벤젠이 있거나 없는, 그리고 공동-공급된 수소가 있거나 없는 탈수소화 반응기로 이송될 수 있고, 여기서 이는 벤젠 및 수소로 전환되고, 이는 하이드로알킬화/알킬화 단계로 재순환될 수 있다.
중질 분획의 양에 따라, 이는 (a) 추가의 벤젠과 함께 C18 예컨대 DiCHB 및 C24 예컨대 TriCHB를 트랜스알킬화하거나, 또는 (b) 원하는 모노알킬화된 종의 생산를 최대화하기 위해 C18 및 C24를 탈알킬화하는 것이 바람직하다.
추가의 벤젠을 사용한 트랜스알킬화는 바람직하게는 적합한 트랜스알킬화 촉매, 예컨대 MCM-22 유형, 제올라이트 베타, MCM-68 (예를 들면 미국특허 제6,049,018호), 제올라이트 Y, 제올라이트 USY, 및 모데나이트의 분자체 상에서 하이드로알킬화 반응기와 구별되는 트랜스알킬화 반응기에서 실시된다. 트랜스알킬화 반응은 바람직하게는 적어도 부분적으로 액상 조건으로 실시되고, 이는 적합하게는 100℃ 내지 300℃의 범위의 온도, 800 kPa 내지 3500 kPa의 범위의 압력, 총 공급물에 대한 1 hr-1 내지 10 hr-1의 중량 시간당 공간 속도(weight hourly space velocity), 및 1:1 내지 5:1의 범위의 벤젠/디사이클로헥실벤젠 중량비를 포함한다.
탈알킬화는 또한 바람직하게는 하이드로알킬화 반응기와 별개의 반응기, 예컨대 반응성 증류 유닛에서 산 촉매 예컨대 알루미노실리케이트, 알루미노포스페이트, 실리코알루미노포스페이트, 비결정성 실리카-알루미나, 산성 클레이, 혼합된 금속 산화물, 예컨대 WOx/ZrO2, 인산, 황산화 지르코니아 및 이들의 혼합물 상에서 약 150℃ 내지 약 500℃의 온도 및 15 내지 500 psig (200 내지 3550 kPa)의 범위의 압력으로 실시된다. 바람직하게는, 산 촉매는 FAU, AEL, AFI 및 MWW 부류의 하나 이상의 알루미노실리케이트, 알루미노포스페이트 또는 실리코알루미노포스페이트를 포함한다. 트랜스알킬화와 달리, 탈알킬화는 추가되는 벤젠 부재 하에 실시될 수 있고, 한편 벤젠이 탈알킬화 반응에 부가되어 코크스 형성을 감소시키는 것이 바람직하다. 이러한 경우, 탈알킬화 반응에 대한 공급물에서 벤젠 대 폴리알킬화된 방향족 화합물의 중량비는 0 내지 약 0.9, 예컨대 약 0.01 내지 약 0.5일 수 있다. 마찬가지로, 탈알킬화 반응이 부가되는 수소의 부재 하에 실시될 수 있지만, 수소는 바람직하게는 탈알킬화 반응기로 도입되어 코크스 환원을 보조할 수 있다. 적합한 수소 부가 속도는 탈알킬화 반응기에 대한 총 공급물에서 수소 대 폴리알킬화된 방향족 화합물의 몰비가 약 0.01 내지 약 10이 될 수 있는 것이다.
벤젠, C12 및 중질을 포함하는 트랜스알킬화 또는 탈알킬화 생성물 혼합물은 이후 분리되어, 이는 주로 벤젠을 포함하고, 하이드로알킬화/알킬화 단계로 재순환될 수 있는 C6 분획, 주로 사이클로헥실벤젠을 포함하는 C12 분획, 및 다시 트랜스알킬화/탈알킬화 반응에 가해지거나 폐기될 수 있는 중질 분획이 수득된다.
새롭게 제조되고 및/또는 재순환되는 사이클로헥실벤젠은 산화 단계로 공급되기 이전에 정제되어, 무엇보다도 적어도 일부의 메틸사이클로펜틸벤젠, 올레핀, 페놀, 산 등을 제거할 수 있다. 이러한 정제는, 예를 들면, 증류, 수소화, 가성용액 세척 등을 포함할 수 있다.
산화 단계에 대한 사이클로헥실벤젠 공급물은 공급물의 총 중량에 기초하여 하기 중 하나 이상을 함유할 수 있다: (i) 1 ppm 내지 1 wt%, 예컨대 10 ppm 내지 8000 ppm의 범위의 농도의 비사이클로헥산; (ii) 1 ppm 내지 1 wt%, 예컨대 10 ppm 내지 8000 ppm의 범위의 농도의 비페닐; (iii) 최대 5000 ppm, 예컨대 100 ppm 내지 1000 ppm의 농도의 물; 및 (iv) 1000 ppm 이하의 농도의 올레핀 또는 알켄 벤젠, 예컨대 페닐사이클로헥센.
사이클로헥실벤젠의
산화
산화 단계에서, 산화 공급물에 함유된 적어도 일부의 사이클로헥실벤젠은 하기 반응-3에 따라 사이클로헥실-1-페닐-1-하이드로퍼옥사이드, 원하는 하이드로퍼옥사이드로 전환된다:
예시적인 공정에서, 산화 단계는 산소-함유 가스, 예컨대 공기 및 다양한 공기의 유도체를 사이클로헥실벤젠을 포함하는 공급물과 접촉시킴으로써 달성될 수 있다. 예를 들면, 순수 O2, 불활성 가스 예컨대 N2로 희석된 O2, 순수 공기, 또는 다른 O2-함유 혼합물의 스트림은 산화 반응기에서 사이클로헥실벤젠-함유 공급물을 거쳐 펌핑된다.
산화는 촉매의 부재 또는 존재 하에 실시될 수 있다. 적합한 산화 촉매의 예는 하기 화학식 (FC-I), (FC-II), 또는 (FC-III)의 구조를 갖는 것을 포함한다:
식 중, A는 고리 구조에서 질소, 황, 또는 산소를 임의로 포함하고, 알킬, 알케닐, 할로겐, 또는 N-, S-, 또는 O-함유 기 또는 다른 기로 임의로 치환되는 고리를 나타내고;
X는 수소, 산소 무함유 라디칼, 하이드록실기, 또는 할로겐을 나타내고;
각 경우에서 동일하거나 상이하게, R1은 독립적으로 수소, N-, S-, 또는 O-함유 기, 또는 알킬, 알케닐, 할로겐, 또는 N-, S-, 또는 O-함유 기 또는 다른 기로 임의로 치환되는, 1 내지 20개의 탄소 원자를 갖는 선형 또는 분지형 비환식 알킬 또는 환식 알킬기를 나타내고; 및
m은 0, 1 또는 2이다.
산화 단계에 특히 적합한 촉매의 예는 하기 화학식 (FC-IV)으로 표시되는 것을 포함한다:
식 중, 각 경우에서 동일하거나 상이하게, R2는 독립적으로 수소, N-, S-, 또는 O-함유 기, 또는 1 내지 20개의 탄소 원자를 갖는 임의로 치환된 선형 또는 분지형 비환식 알킬 또는 환식 알킬기를 나타내고; 및
n은 0, 1, 2, 3, 또는 4이다.
산화 단계에 대해 상기 화학식 (FC-IV)를 갖는 하나의 특별히 적합한 촉매는 NHPI (N-하이드록시프탈이미드)이다. 예를 들면, 산화 단계에 대한 공급물은 공급물에서의 사이클로헥실벤젠의 중량 기준으로 10 내지 2500 ppm의 NHPI를 포함할 수 있다.
산화 촉매의 다른 비제한적인 예는 하기를 포함한다: 4-아미노-N-하이드록시프탈이미드, 3-아미노-N-하이드록시프탈이미드, 테트라브로모-N-하이드록시프탈이미드, 테트라클로로-N-하이드록시프탈이미드, N-하이드록시헤티미드 N-하이드록시히미미드, N-하이드록시트리멜리티미드, N-하이드록시벤젠-1,2,4-트리카르복시이미드, N,N'-디하이드록시(피로멜리트산 디이미드), N,N'-디하이드록시(벤조페논-3,3',4,4'-테트라카르복실산 디이미드), N-하이드록시말레이미드, 피리딘-2,3-디카르복시미드, N-하이드록시석시니미드, N-하이드록시(타르타르산 이미드), N-하이드록시-5-노보넨-2,3-디카르복시미드, 엑소-N-하이드록시-7-옥사비사이클로[2.2.1]헵트-5-엔-2,3-디카르복시미드, N-하이드록시-시스-사이클로헥산-1,2-디카르복시미드, N-하이드록시-시스-4-사이클로헥센-1,2 디카르복시미드, N-하이드록시나프탈이미드 나트륨염, N-하이드록시-o-벤젠디설폰이미드, 및 N,N',N''-트리하이드록시이소시아누르산.
이러한 산화 촉매는 단독으로 또는 자유 라디칼 개시제와 결합하여 사용될 수 있고, 추가로 액상 균일 촉매로서 사용될 수 있거나 또는 불균일 촉매를 제공하기 위해 고체 캐리어 상에 지지될 수 있다. 바람직하게는, N-하이드록시 치환된 환식 이미드 또는 N,N',N"-트리하이드록시이소시아누르산은 사이클로헥실벤젠 공급물의 0.0001 wt% 내지 15 wt%, 예컨대 0.001 wt% 내지 5 wt%의 양으로 이용된다.
산화 단계의 적합한 반응 조건의 비제한적인 예는 70℃ 내지 200℃, 예컨대 90℃ 내지 130℃의 범위의 온도, 및 50 kPa 내지 10,000 kPa의 범위의 압력을 포함한다. 염기성 완충제는 산화 과정에서 형성될 수 있는 산성 부산물과 반응하도록 부가될 수 있다. 또한, 수상은 산화 반응기로 주입될 수 있다. 반응은 회분식 또는 연속식 흐름 방식으로 일어날 수 있다.
산화 단계에 사용되는 반응기는 산화제, 예컨대 산소 분자에 의한 사이클로헥실벤젠의 산화를 가능하게 하는 임의의 유형의 반응기일 수 있다. 적합한 산화 반응기의 특히 유리한 예는 일정 체적의 반응 매체를 함유하고, 상기 매체를 통해 O2-함유 가스 스트림 (예컨대 공기)를 버블링시킬 수 있는 기포 컬럼 반응기(bubble column reactor)이다. 예를 들면, 산화 반응기는 대개 산소-함유 가스 스트림에 대한 배분기 유입구를 갖는 간단한 개방형 용기를 포함할 수 있다. 산화 반응기는 반응 매체의 일부를 인출하여 이를 적절한 냉각 장치를 통해 펌핑하고, 냉각된 부분을 반응기로 복귀시켜 반응에서 발생된 열을 관리하는 수단을 가질 수 있다. 대안적으로, 예를 들면, 냉각수에 의한 간접적 냉각을 공급하는 냉각 코일은 산화 반응기 내에서 작동되어 적어도 일부의 발생된 열을 제거할 수 있다. 대안적으로, 산화 반응기는 일련하여 그리고/또는 병렬적으로 복수개의 반응기를 포함할 수 있고, 각각은 상이한 조성을 갖는 반응 매체에서 산화 반응을 개선하도록 선택되는 동일하거나 상이한 조건에서 작동된다. 산화 반응기는 본 기술분야의 당업자에게 잘 알려진 회분식, 반회분식, 또는 연속식 유동 방식으로 작동될 수 있다.
산화 반응 생성물 혼합물의 조성
바람직하게는, 산화 반응기로부터 배출되는 산화 반응 생성물 혼합물은 산화 반응 생성물 혼합물의 총 중량 기준으로 Chp1 wt% 내지 Chp2 wt%의 범위의 농도의 사이클로헥실-1-페닐-1-하이드로퍼옥사이드를 함유하고, 상기 Chp1 및 Chp2는 독립적으로 Chp1 < Chp2인 경우에 한하여 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80일 수 있다. 바람직하게는, 산화 반응 생성물 혼합물에서의 사이클로헥실-1-페닐-1-하이드로퍼옥사이드의 농도는 산화 반응 생성물 혼합물의 적어도 20 중량%이다. 산화 반응 생성물 혼합물은 추가로 산화 반응 생성물 혼합물의 총 중량 기준으로 Cchb1 wt% 내지 Cchb2 wt%의 범위의 농도의 잔류 사이클로헥실벤젠을 포함할 수 있고, 상기 Cchb1 및 Cchb2는 독립적으로 Cchb1 < Cchb2인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95일 수 있다. 바람직하게는, 산화 반응 생성물 혼합물에서의 사이클로헥실벤젠의 농도는 65 중량% 이하의 산화 반응 생성물 혼합물이다.
또한, 산화 반응 생성물 혼합물은 사이클로헥실벤젠의 산화 반응의 부산물(들)로서, 또는 산화 단계에 공급되는 공급물에 함유될 수 있는 사이클로헥실벤젠 이외 산화성 성분(들)의 산화 반응 생성물로서 생성된 사이클로헥실-1페닐-1-하이드로퍼옥사이드 이외의 하나 이상의 하이드로퍼옥사이드, 예컨대 사이클로헥실-2-페닐-1-하이드로퍼옥사이드, 사이클로헥실-3-페닐-1-하이드로퍼옥사이드, 및 메틸사이클로펜틸벤젠 하이드로퍼옥사이드를 함유할 수 있다. 이러한 바람직하지 않은 하이드로퍼옥사이드는 Cu1 wt% 내지 Cu2 wt%의 총 농도로 존재하고, 상기 Cu1 및 Cu2는 독립적으로 Cu1 < Cu2인 경우에 한하여 0.1, 0.2, 0.3, 0.5, 0.7, 0.9, 1.0, 1.2, 1.4, 1.5, 1.6, 1.8, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 5.0, 6.0, 7.0, 8.0일 수 있다. 이는 원하는 전환율 및/또는 선택도로 분해 반응에서 페놀 및 사이클로헥사논으로 전환될 수 없고, 이는 전체 수율 손실을 야기하기 때문에 이들은 바람직하지 않다.
상기 주지한 바와 같이, 산화 반응 생성물 혼합물은 또한 산화 반응의 추가의 부산물로서 페놀을 함유할 수 있다. 산화 반응기(들)에서 배출되는 산화 반응 생성물 혼합물에서의 페놀 (CPh)의 농도는 CPh1 ppm 내지 CPh2 ppm의 범위일 수 있고, 상기 CPh1 및 CPh2는 독립적으로 CPh1 < CPh2인 경우에 한하여 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1500, 2000일 수 있다.
산화 반응 생성물 혼합물은 물을 함유할 수 있다. 산화 반응기로부터 배출되는 산화 반응 생성물 혼합물에서의 물의 농도는 산화 반응 생성물 혼합물의 총 중량 기준으로 C1a ppm 내지 C1b ppm의 범위일 수 있고, 상기 C1a 및 C1b는 독립적으로 C1a < C1b인 경우에 한하여 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 또는 5000일 수 있다.
산화 반응 생성물 혼합물은 임의의 촉매의 일부 또는 모두, 산화 단계로 공급되는 NHPI를 함유할 수 있다. 예를 들면, 산화 반응 생성물 혼합물은 10 내지 2500 중량ppm의 NHPI, 예컨대 100 내지 1500 중량ppm의 NHPI를 함유할 수 있다.
산화 반응 생성물 혼합물의 처리
본 개시물의 방법에서, 분해 단계에 공급되기 이전에, 적어도 일부의 산화 반응 생성물 혼합물이 분리될 수 있다. 분해 공정은 (i) 대다수의 사이클로헥실-1-페닐-1-하이드로퍼옥사이드 및 산화 반응 생성물 혼합물 일부의 다른 고비점 성분, 예컨대 산화 반응 생성물 혼합물 일부에 존재하는 경우의 다른 하이드로퍼옥사이드 및 NHPI 촉매를 포함하는 제1 분획; 및 (ii) 대부분의 사이클로헥실벤젠, 페놀, 존재하는 경우, 및 산화 반응 생성물 혼합물 일부의 다른 저비점 성분을 포함하는 제2 분획을 회수하기 위해 산화 반응 생성물 혼합물의 적어도 일부를 진공 증발시키는 것을 포함할 수 있다.
바람직하게는, 제1 분획에서, 사이클로헥실-1-페닐-1-하이드로퍼옥사이드의 농도는 Cc1 wt% 내지 Cc2 wt%의 범위일 수 있고, 사이클로헥실벤젠의 농도는 제1 분획의 총 중량에 기초하여 Cd1 wt% 내지 Cd2 wt의 범위일 수 있고, 상기 Cc1 및 Cc2는 독립적으로 Cc1 < Cc2인 경우에 한하여 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90일 수 있고, 그리고 Cd1 및 Cd2는 독립적으로 Cd1 < Cd2인 경우에 한하여 10, 15, 20, 25, 30, 35, 40, 45, 50일 수 있다.
유리하게는, 제2 분획에서, 사이클로헥실-1-페닐-1-하이드로퍼옥사이드의 농도는 Cc3 wt% 내지 Cc4 wt%의 범위일 수 있고, 사이클로헥실벤젠의 농도는 제2 분획의 총 중량 기준으로 Cd3 wt% 내지 Cd4 wt%의 범위일 수 있고, 상기 Cc3 및 Cc4는 독립적으로 Cc3 < Cc4인 경우에 한하여 0.01, 0.05, 0.10, 0.20, 0.40, 0.50, 0.60, 0.80, 1.00, 1.50, 2.00, 2.50, 3.00, 3.50, 4.00, 4.50, 5.00일 수 있고; 그리고 Cd3 및 Cd4는 독립적으로 Cd3 < Cd4인 경우에 한하며 90, 92, 94, 95, 96, 97, 98, 또는 심지어 99일 수 있다.
사이클로헥실벤젠 하이드로퍼옥사이드는 증가된 온도, 예를 들면, 150℃ 초과에서 분해되는 경향이 있고, 산화 반응 생성물 혼합물을 제1 및 제2 분획으로 분리하기 위한 진공 증발 단계는 상대적으로 저온, 예를 들면, 130℃ 이하, 또는 120℃ 이하, 또는 심지어 110℃ 이하에서 실시된다. 사이클로헥실벤젠은 고비점 (101 kPa에서 239℃)을 가진다. 이에 따라, 허용가능한 사이클로헥실벤젠-제거 온도에서, 사이클로헥실벤젠은 매우 낮은 증기압을 가지는 경향이 있다. 따라서, 바람직하게는, 산화 반응 생성물 혼합물로부터 유의미한 양의 사이클로헥실벤젠을 효과적으로 제거하기 위해, 산화 반응 생성물 혼합물은, 예를 들면, Pc1 kPa 내지 Pc2 kPa의 범위의 매우 낮은 절대압에 가해지고, 상기 Pc1 및 Pc2는 독립적으로 Pc1 < Pc2인 경우에 한하여 0.05, 0.10, 0.15, 0.20, 0.25, 0.26, 0.30, 0.35, 0.40, 0.45, 0.50, 0.60, 0.65, 0.70, 0.75, 0.80, 0.85, 0.90, 0.95, 1.00, 1.50, 2.00, 2.50, 3.00일 수 있다. 특히 유리하게는, Pc1 = 0.25, 그리고 Pc2 = 1.5이다.
산화 반응 생성물 혼합물을 제1 및 제2 분획으로 분리한 후, 제1 분획의 일부 또는 모두를 분해 단계로 직접적으로 이송시킬 수 있다. 제1 분획의 일부 또는 모두를 미반응된 이미드 산화 촉매의 결정화를 야기하도록 분해 단계로의 이동 전에 냉각될 수 있다. 이미드 결정은 이후 재사용을 위해 여과에 의해 또는 결정화를 실시하기 위해 사용되는 열 교환기 표면으로부터의 스크랩핑(scraping)에 의해 회수될 수 있다.
산화 반응 생성물 혼합물로부터 제조되는 제2 분획은 제2 분획에서의 사이클로헥실벤젠의 일부 또는 모두가 수소화로 재순환되기 이전에 그 내부의 페놀 수준을 감소시키기 위해 처리될 수 있다.
제2 분획의 처리는 염기가 페놀과 반응하여 수성 조성물에 잔류되는 페노에이트 종을 생성하게 하는 조건 하에 적어도 일부의 제2 분획을 염기를 포함하는 수성 조성물과 접촉시키는 것을 포함할 수 있다. 3 미만, 예컨대 2, 1, 0, 또는 -1의 pKb를 갖는 염기인 강염기가 바람직하게는 제2 분획의 처리시 이용된다. 특히 적합한 염기는 알칼리 금속 (예를 들면, LiOH, NaOH, KOH, RbOH)의 수산화물, 알칼리토 금속 (Mg(OH)2, Ca(OH)2, Sr(OH)2, Ba(OH)2)의 수산화물, 및 이들의 하나 이상의 혼합물을 포함한다. 페놀은 이러한 수산화물과 반응하여 전형적으로 페놀 자체보다 더 높은 수용성을 가지는 페노에이트를 형성할 수 있다. 특히 바람직한 염기는 비용 효용적이고, 제2 분획에서의 페놀과 반응하여 나트륨 페노에이트를 생성할 수 있는 NaOH이다. 수산화물이 염기로서 사용되는 경우, 대기에 존재하는 CO2와 수산화물의 반응으로 인해, 수성 조성물은 다양한 농도로 하나 이상의 대응되는 탄산염, 중탄산염, 또는 탄산염-수산화물 복합체를 포함할 수 있다는 것을 주지하여야 한다. 바람직하게는, 염기를 포함하는 수성 조성물은 적어도 8, 바람직하게는 적어도 10의 pH를 가진다.
제2 분획을 염기를 포함하는 수성 조성물과 접촉시키는 것은 페놀의 적어도 일부 및/또는 제2 분획로부터의 이의 유도체를 함유하는 수상 및 사이클로헥실벤젠을 함유하고, 제2 분획과 비교되는 바와 같은 페놀의 감소된 농도를 갖는 유기상을 생성한다. 바람직하게는, 유기상에서의 페놀 농도는 유기상의 총 중량 기준으로 CPh7 ppm 내지 CPh8 ppm의 범위이고, 상기 CPh7 및 CPh8은 독립적으로 CPh7 < CPh8인 경우에 한하여 0, 10, 20, 30, 40, 50, 100, 150, 200, 250일 수 있다.
이후, 유기상은 예를 들면 중력 하에 자발적으로 수상으로부터 분리될 수 있고, 이후 이는 유기상에 함유된 염기를 제거하기 위해, 물 세척 직후, 또는 더 바람직하게는 그 후에 제3 분획으로서 산화 단계에 재순환될 수 있다.
분해 반응(cleavage reaction)
분해 반응에서, 사이클로헥실-1-페닐-1-하이드로퍼옥사이드의 적어도 일부는 높은 선택도로 산 촉매의 존재 하에 하기 바람직한 반응-4에 따라 사이클로헥사논 및 페놀로 분해된다:
분해 생성물 혼합물은 산 촉매, 페놀, 사이클로헥사논, 사이클로헥실벤젠, 및 오염물을 포함할 수 있다.
산 촉매는 분해 반응 혼합물에서 적어도 부분적으로 가용성일 수 있고, 적어도 185℃의 온도에서 안정적이고, 사이클로헥실벤젠보다 더 낮은 휘발성(기준 비점보다 높음)을 가진다.
산 촉매는 바람직하게는, 비제한적으로, 브뢴스테드 산, 루이스 산, 설폰산, 과염소산, 인산, 염산, p-톨루엔 설폰산, 염화알루미늄, 올레움, 삼산화황, 염화제2철, 삼불화붕소, 이산화황, 및 삼산화황을 포함한다. 황산이 바람직한 산 촉매이다.
분해 반응은 바람직하게는 20℃ 내지 200℃, 또는 40℃ 내지 120℃의 범위의 온도, 및 1 내지 370 psig (적어도 7 kPa, 게이지 및 2,550 kPa 이하, 게이지), 또는 14.5 psig 내지 145 psig (100 kPa, 게이지 내지 1,000 kPa, 게이지)의 범위의 압력을 포함하는 분해 조건 하에 발생되어 이로써 분해 반응 혼합물이 분해 반응 과정에서 완전하게 또는 주로 액상으로 존재한다.
분해 반응 혼합물은 분해 반응 혼합물의 총 중량 기준으로 Cac1 ppm 내지 Cac2의 범위의 농도의 산 촉매를 함유할 수 있고, 상기 Cac1 및 Cac2는 독립적으로 Cac1 < Cac2이 경우에 한하여 10, 20, 30, 40, 50, 60, 80, 100, 150, 200, 250, 300, 350, 400, 450, 500, 600, 700, 800, 900, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 또는 심지어 5000일 수 있다. 바람직하게는, Cac1은 50이고, 그리고 Cac2는 200이다.
하이드로퍼옥사이드, 예컨대 사이클로헥실-1-페닐-1-하이드로퍼옥사이드, 및 편의상 모든 사이클로헥실-1-페닐-1-하이드로퍼옥사이드 및 다른 하이드로퍼옥사이드의 전환율은 분해 반응에서 예를 들면 적어도 AA wt%로 매우 높을 수 있고, 상기 AA는 90.0, 91.0, 92.0, 93.0, 94.0, 95.0, 96.0, 97.0, 98.0, 99.0, 99.5, 99.9, 또는 심지어 100일 수 있고, 백분율은 주어진 하이드로퍼옥사이드, 또는 분해 단계에 공급된 모든 하이드로퍼옥사이드의 중량에 기초한다. 이는 임의의 하이드로퍼옥사이드, 심지어 사이클로헥실-1-페닐-1-하이드로퍼옥사이드가 다운스트림 공정에서 오염물이 되기 때문에 바람직하다.
바람직하게는, 사이클로헥실-1-페닐-1-하이드로퍼옥사이드의 각각의 몰은 1몰의 페놀 및 1몰의 사이클로헥사논을 생성한다. 그러나, 부반응으로 인해, 페놀로의 분해 반응의 선택도는 Sph1% 내지 Sph2%의 범위일 수 있고, 사이클로헥사논에 대한 선택도는 Sch1% 내지 Sch2%의 범위일 수 있고, 상기 Sph1, Sph2, Sch1, 및 Sch2는 독립적으로 Sph1 < Sph2, 그리고 Sph1 < Sch2인 경우에 한하여 85, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 또는 심지어 99.5일 수 있다.
사이클로헥실벤젠 하이드로퍼옥사이드, 사이클로헥실벤젠 및 산화 반응 생성물 혼합물로부터 직접적으로 유래되는 다른 성분을 포함하는 분해 공급물 이외, 분해 반응 혼합물은 추가로 다른 부가된 물질, 예컨대 분해 촉매, 용매, 및 분해 반응의 하나 이상의 생성물, 예컨대 분해 생성물 혼합물, 또는 다운스트림 분리 단계로부터 재순환되는 페놀 및 사이클로헥사논을 포함할 수 있다. 따라서, 분해 반응기 내부의 분해 반응 혼합물은 분해 반응 혼합물의 총 중량 기준으로 (i) CPh9 wt% 내지 CPh10 wt%의 농도의 페놀로서, 상기 CPh9 및 CPh10이 독립적으로 CPh9 < CPh10인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 또는 80일 수 있는 페놀; (ii) Cch1 wt% 내지 Cch2 wt%의 농도의 사이클로헥사논으로서, 상기 Cch1 및 Cch2는 독립적으로 Cch1 < Cch2인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 또는 80일 수 있는 사이클로헥사논; 및 (iii) Cchb7 wt% 내지 Cchb8 wt%의 농도의 사이클로헥실벤젠으로서, 상기 Cchb7 및 Cchb8은 독립적으로 Cchb7 < Cchb8인 경우에 한하여 5, 8, 9, 10, 12, 14, 15, 18, 20, 22, 24, 25, 26, 28, 30, 35, 40, 45, 50, 55, 60, 65, 70일 수 있는 사이클로헥실벤젠을 포함할 수 있다.
분해 반응 (즉, 분해 반응기)을 실시하기 위해 사용되는 반응기는 본 기술분야의 당업자에게 공지된 임의의 유형의 반응기일 수 있다. 예를 들면, 분해 반응기는 대개 근-연속식 교반 탱크 반응기 방식(near-continuous stirred tank reactor mode)으로 작동되는 간단한 개방형 용기, 또는 근-플러그 흐름 반응식 방식(near-plug flow reactor mode)으로 작동되는 간단한 일정길이의 개방형 파이프일 수 있다. 분해 반응기는 연속적으로 복수의 반응기를 포함할 수 있고, 각각은 전환 반응의 일부를 수행하고, 경우에 따라 적절한 전환율 범위에서 분해 반응을 향상시키기 위해 선택되는 상이한 조건 및 상이한 방식으로 작동된다. 분해 반응기는 촉매적 증류 유닛(catalytic distillation unit)일 수 있다.
분해 반응기는 냉각 장치를 통해 내용물의 일부를 수송하고, 냉각된 부분을 분해 반응기로 복귀시키고, 이에 의해 분해 반응의 발열도(exothermicity)를 관리할 수 있도록 작동될 수 있다. 대안적으로, 반응기는 단열적으로 작동될 수 있다. 분해 반응기(들) 내에서 작동되는 냉각 코일은 발생된 열의 적어도 일부에 대해 사용될 수 있다.
분해 반응기로부터 배출되는 분해 생성물 혼합물은 분해 생성물 혼합물의 총 중량 기준으로 (i) CPh11 wt% 내지 CPh12 wt%의 농도의 페놀로서, 상기 CPh11 및 CPh12는 독립적으로 Ch11 < CPh12인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 또는 80일 수 있는 페놀; (ii) Cch3 wt% 내지 Cch4 wt%의 농도의 사이클로헥사논으로서, 상기 Cch3 및 Cch4는 독립적으로 Cch3 < Cch4인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 또는 80일 수 있는 사이클로헥사논; 및 (iii) Cchb9 wt% 내지 Cchb10 wt%의 농도의 사이클로헥실벤젠으로서, 상기 Cchb9 및 Cchb10은 독립적으로 Cchb9 < Cchb10인 경우에 한하여 5, 8, 9, 10, 12, 14, 15, 18, 20, 22, 24, 25, 26, 28, 30, 35, 40, 45, 50, 55, 60, 65, 70일 수 있는 사이클로헥실벤젠을 포함할 수 있다.
상기 논의된 바와 같이, 분해 생성물 혼합물은 하나 이상의 오염물을 포함할 수 있다. 본원에 개시된 구현예에서, 본 방법은 추가로 오염물의 적어도 일부를 산성 물질과 접촉시켜 오염물의 적어도 일부를 전환된 오염물로 전화시키고, 이에 의해 개질된 생성물 혼합물을 생성하는 단계를 포함한다. 오염물 처리 공정의 상세한 설명은 예를 들면, 국제특허출원 WO2012/036822A1에서 찾을 수 있고, 이의 관련 내용은 그 전문이 본원에 참조로 포함되어 있다.
분해 생성물 혼합물의 적어도 일부를 중화 반응에 가할 수 있다. 액체 산 예컨대 황산이 분해 촉매로 사용되는 경우, 분해 반응 생성물은 혼합물이 분리에 가해지기 이전에 염기, 예컨대 유기 아민 (예를 들면, 메틸아민, 에틸아민, 디아민 예컨대 메틸렌디아민, 프로필렌 디아민, 부틸렌 디아민, 펜틸렌 디아민, 헥실렌 디아민 등)으로 중화되어 산에 의한 장비 부식을 방지하는 것이 매우 바람직하다. 바람직하게는, 이에 따라 형성된 아민 설페이트염은 사이클로헥실벤젠의 것보다 높은 비점을 가진다.
분리 및 정제
일부의 중화된 분해 반응 생성물은 이후 증류와 같은 방법에 의해 분리될 수 있다. 일 예에서, 분해 반응기 뒤에 있는 제1 증류 컬럼에서, 아민염을 포함하는 중질 분획이 컬럼의 하부에서 얻어지고, 사이클로헥실벤젠을 포함하는 측면 분획(side fraction)이 중간 섹션에서 얻어지고, 사이클로헥사논, 페놀, 메틸사이클로펜타논, 및 물을 포함하는 상부 분획이 얻어진다.
분리된 사이클로헥실벤젠 분획은 이후 산화 단계에 전달되기 이전에 처리되고 및/또는 정제될 수 있다. 분해 생성물 혼합물로부터 분리된 사이클로헥실벤젠이 페놀 및/또는 올레핀 예컨대 사이클로헥세닐벤젠을 함유할 수 있기 때문에, 물질은 산화 생성물 혼합물의 제2 분획에 대해 상기 기재된 바와 같이 염기를 포함하는 수성 조성물로의 처리 및/또는 예를 들면 WO2011/100013A1에 개시된 바와 같은 수소화 단계에 가해질 수 있고, 이의 전체 내용은 본원에 참조로 포함되어 있다.
일 예에서, 페놀, 사이클로헥사논, 및 물을 포함하는 분획은 추가로 간단한 증류에 의해 분리되어 주로 사이클로헥사논 및 메틸사이클로펜타논을 포함하는 상부 분획 및 주로 페놀, 및 일부 사이클로헥사논을 포함하는 하부 스트림이 수득될 수 있다. 사이클로헥사논은 이들 둘 사여기서 형성된 공비혼합물로 인해 추출 용매를 사용하지 않고 페놀로부터 완전하게 분리될 수 없다. 따라서, 상부 분획은 별개의 컬럼에서 추가로 증류되어 바닥 근처에서 순수 사이클로헥사논 생성물 및 상부 부근에서 주로 필요한 경우 추가로 정제될 수 있고 이후 유용한 공업용 물질로서 사용되는 메틸사이클로펜타논을 포함하는 불순물 분획을 얻을 수 있다. 하부 분획은 추가로 예를 들면, 그 내용이 본원에 그 전문이 참조로 포함되어 있는, 공동 출원의 동시 계속 특허출원 WO2013/165656A1 및 WO2013/165659에 개시된 추출 용매 (예를 들면, 글리콜 예컨대 에틸렌 글리콜, 프로필렌 글리콜, 디에틸렌 글리콜, 트리에틸렌 글리콜 등)을 사용하는 추출 증류의 단계에 의해 분리될 수 있다. 사이클로헥사논을 포함하는 상부 분획 및 페놀 및 추출 용매를 포함하는 하부 분획이 수득될 수 있다. 후속 증류 컬럼에서, 하부 분획은 이후 분리되어 페놀 생성물을 포함하는 상부 분획 및 추출 용매를 포함하는 하부 분획을 얻을 수 있다.
분리 및 수소화
중화된 분해 유출물(분해 반응 생성물)의 적어도 일부, 바람직하게는 그 전부가, 분리될 수 있고, 이의 페놀-함유 분획은 수소화되어 본 발명에 따라 일부의 페놀이 사이클로헥사논으로 전환될 수 있다. 분리 및 수소화 공정 및/또는 시스템의 예는 첨부된 도면 및 하기 상세한 설명에 예시되어 있다.
개략적인 축척에 의하지 않는 도면에 나타난 상기 공정 및/또는 시스템은 단지 일반적 물질 및/또는 열 흐름 및 일반 작동 원리를 예시하기 위한 목적을 위한 것임을 이해하여야 한다. 예시 및 설명을 간소화하기 위해, 일부 통상적 구성요소, 예컨대 펌프, 밸브, 재비등기, 압력 조절기, 열 교환기, 재순환 루프, 응축기, 분리 드럼, 센서, 정류기, 필터, 분배기, 교반기, 모터 등은 도면에 나타나거나 본원에 기술되지 않는다. 본 기술분야의 당업자는 본원의 교시의 관점에서 적절한 경우 이들 구성요소를 부가할 수 있다.
도 1은 제1 분획화 컬럼(T1) (즉, 제1 증류 컬럼), 수소화 반응기(R1), 및 사이클로헥사논 정제 컬럼(T2) (즉, 제2 증류 컬럼)을 포함하는, 페놀, 사이클로헥사논 및 사이클로헥실벤젠을 포함하는 혼합물로부터 사이클로헥사논을 제조하기 위한 본 개시물의 예시적인 방법/시스템(101)을 나타내는 개략도이다. 페놀, 사이클로헥사논, 및 사이클로헥실벤젠을 포함하는 저장소(S1)으로부터의 공급물(103)은 제1 분획화 컬럼(T1)으로 공급된다.
공급물(103)은 임의의 방법으로 제조될 수 있다. 바람직한 방법은 산 촉매 예컨대 H2SO4 및 상기 기재된 바와 같은 사이클로헥실벤젠의 존재 하에 사이클로헥실벤젠 하이드로퍼옥사이드를 분해하는 것에 의한다. 공급물(103)은 추가로 사이클로헥실벤젠 이외 불순물 예컨대 경질 성분 예컨대 물, 메틸사이클로펜타논, 펜타날, 헥사날, 벤질산 등 및 중질 성분 예컨대 메틸사이클로펜틸벤젠, 비사이클로헥산, 아민을 분해 혼합물에 도입하여 사용된 액체 산 촉매를 중화시킴으로써 제조되는 유기 아민의 설페이트 (예컨대 1,6-헥사메틸렌디아민, 2-메틸-1,5-펜타메틸렌디아민, 에틸렌디아민, 프로필렌디아민, 디에틸렌트리아민 등)을 포함할 수 있다. 공급물(103)은 추가로 올레핀 예컨대 페닐사이클로헥센 이성질체, 하이드록실사이클로헥사논, 사이클로헥사논 등을 포함할 수 있다. 사이클로헥실벤젠 하이드로퍼옥사이드는 촉매 예컨대 상기 기재된 바와 같은 NHPI의 존재 하에 사이클로헥실벤젠 의 호기성 산화에 의해 제조될 수 있다. 사이클로헥실벤젠은 상기 기재된 바와 같이 수소화/알킬화 이작용성 촉매의 존재 하에 벤젠의 하이드로알킬화에 의해 제조될 수 있다.
이에 따라, 공급물(103)(제1 혼합물)은 이의 총 중량 기준으로 하기를 포함할 수 있다:
- x11 wt% 내지 x12 wt%의 범위의 Cxnone(FM1)의 농도의 사이클로헥사논으로서, 상기 x11 및 x12는 독립적으로 x11 < x12인 경우에 한하여 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 82, 84, 85, 86, 88, 또는 90일 수 있으며; 바람직하게는 20 wt% ≤ Cxnone(FM1) ≤ 30 wt%의 농도인 사이클로헥사논;
- x21 wt% 내지 x22 wt%의 범위의 Cphol(FM1)의 농도의 페놀로서, 상기 x21 및 x22는 독립적으로 x21 < x22인 경우에 한하여 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 82, 84, 85, 86, 88, 또는 90일 수 있으며; 바람직하게는 20 wt% ≤ Cphol(FM1) ≤ 30 wt%; 바람직하게는, 0.3 ≤ Cxnone(FM1)/Cphol(FM1) ≤ 2.0; 더 바람직하게는 0.5 ≤ Cxnone(FM1)/Cphol(FM1) ≤ 1.5; 보다 더 바람직하게는 0.8 ≤ Cxnone(FM1)/Cphol(FM1) ≤ 1.2의 농도인 페놀;
- x31 wt% 내지 x32 wt%의 범위의 Cchb(FM1)의 농도의 사이클로헥실벤젠으로서, 상기 x31 및 x32는 독립적으로 x31 < x32인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 32, 34, 35, 36, 38, 40, 42, 44, 45, 46, 48, 50, 52, 54, 55, 56, 58, 60, 62, 64, 65, 66, 68, 70, 72, 74, 75, 76, 77, 78, 79, 또는 80일 수 있으며; 바람직하게는 30 wt% ≤ Cchb(FM1) ≤ 60 wt%의 농도인 사이클로헥실벤젠; 및
- 제1 혼합물의 총 중량 기준으로 x41 wt% 내지 x42 wt%의 범위의 Cbch(FM1)의 농도의 비사이클로헥산으로서, 상기 x41 및 x42은 독립적으로, x41 < x42인 경우에 한하여, 0, 0.00001, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있으며; 바람직하게는, 0.001 wt% ≤ Cbch(FM1) ≤ 1 wt%의 농도인 비사이클로헥산.
제1 분획화 컬럼(T1)으로부터, 사이클로헥사논 및 경질 성분 예컨대 물, 메틸사이클로펜타논 등을 포함하는 제1 상부 유출물(105)은 컬럼(T1)의 상부 근처에서 제조된다. 유출물(105)은 이의 총 중량 기준으로 하기를 포함할 수 있다:
- Cxnone(UE1)의 농도의 사이클로헥사논으로서, 여기서 z11 wt% ≤ Cxnone(UE1) ≤ z12 wt%이고, 상기 z11 및 z12는 독립적으로 z11 < z12인 경우에 한하여 60, 65, 70, 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 99.5, 또는 99.9일 수 있으며; 바람직하게는 75 ≤ Cxnone(UE1) ≤ 95의 농도인 사이클로헥사논;
- Cphol(UE1)의 농도의 페놀로서, 여기서 z21 ≤ Cphol(UE1) ≤ z22이고, 상기 z21 및 z22는 독립적으로 z21 < z22인 경우에 한하여 0, 0.00001, 0.00005, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 또는 1일 수 있는 페놀;
- Cchb(UE1)의 농도의 사이클로헥실벤젠으로서, 여기서 y31 wt% ≤ Cchb(UE1) ≤ y32 wt%이고, 상기 y31 및 y32는 독립적으로 y31 < y32인 경우에 한하여, 0, 0.00001, 0.00005, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 또는 1일 수 있는 사이클로헥실벤젠;
- Cbch(UE1)의 농도의 비사이클로헥산으로서, 여기서 y41 wt% ≤ Cbch(UE1) ≤ y42 wt%이고, 상기 y41 및 y42는 독립적으로 y41 < y42인 경우에 한하여 0, 0.00001, 0.00005, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 또는 1일 수 있는 비사이클로헥산; 및
- Cxnol(UE1)의 농도의 사이클로헥사놀로서, 여기서 제1 상부 유출물의 총 중량 기준으로 x51 wt% ≤ Cxnol(UE1) ≤ x52 wt%, 바람직하게는 0.1 wt% ≤ Cxnol(UE1) ≤ 5.0 wt%이고, 상기 x51 및 x52는 독립적으로, x51 < x52인 경우에 한하여, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 5.0, 5.5, 6.0, 6.5, 7.0, 7.5, 8.0, 8.5, 9.0, 9.5, 또는 10일 수 있는 사이클로헥사놀.
제1 상부 유출물(105)은 이후 사이클로헥사논 정제 컬럼(T2)로 송부되고, 여기서 경질 성분 예컨대 물, 메틸사이클로펜타논 등을 포함하는 제3 상부 유출물(121)이 컬럼(T2)의 상부의 부근의 위치에서 생성되고, 이후 저장소(S5)로 전달된다. 본질적으로 순수한 사이클로헥사논을 포함하는 제2 상부 유출물(123)이 제조되어 저장소(S7)로 이송된다. 컬럼(T2)의 하부의 부근에서, 제2 하부 유출물(125)이 생성되어 저장소(S9)로 전달된다. 제2 하부 유출물은, 예를 들면, 사이클로헥사논 및 사이클로헥사놀 모두를 포함하는 KA 오일일 수 있다. 따라서, 제2 상부 유출물(123)은 이의 총 중량 기준으로 Cxnone(UE2)의 농도의 사이클로헥사논을 포함할 수 있고, 여기서 Cxnone(UE2) ≥ y11 wt%이고, 상기 y11은 95, 95.5, 96, 96.5, 97, 97.5, 98, 98.5, 99, 99.5, 99.8, 또는 99.9일 수 있다. 제2 하부 유출물(125)은 이의 총 중량 기준으로 Cxnol(LE2)의 농도의 사이클로헥사놀로서, 여기서 y51 wt% ≤ Cxnol(LE2) ≤ y52 wt%이고, 상기 y51 및 y52는 독립적으로 y51 < y52인 경우에 한하여 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 32, 34, 35, 36, 38, 40, 42, 44, 45, 46, 48, 50, 52, 54, 55, 56, 58, 60, 62, 64, 65, 66, 68, 70, 72, 74, 75, 76, 78, 또는 80일 수 있는 사이클로헥사놀; 및 Cxnone(LE2)의 농도의 사이클로헥사논으로서, 여기서 e11 wt% ≤ Cxnol(LE2) ≤ e12 wt%이고, 상기 e11 및 e12는 독립적으로 e11 < e22인 경우에 한하여 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 32, 34, 35, 36, 38, 40, 42, 44, 45, 46, 48, 50, 52, 54, 55, 56, 58, 60, 62, 64, 65, 66, 68, 70, 72, 74, 75, 76, 78, 또는 80일 수 있는 사이클로헥사논을 포함할 수 있다.
제1 분획화 컬럼(T1)으로부터 제조되는 제1 중간 유출물(107)은 공급물(103)에서의 것보다 더 높고, 제1 상부 유출물(105)에서의 것보다 높은 농도의 페놀 및 공급물(103) 및 제1 상부 유출물(105) 둘 모두에서의 것보다 낮은 농도의 사이클로헥사논, 바람직하게는 공급물(103)에서의 것보다 낮고, 제1 상부 유출물(105)에서의 것보다 높은 농도의 사이클로헥실벤젠, 및 하나 이상의 다른 불순물 예컨대 비사이클로헥산 및 사이클로헥사논을 포함한다. 따라서, 유출물(107)은 이의 총 중량 기준으로 하기를 포함할 수 있다:
- Cxnone(ME1)의 농도의 사이클로헥사논으로서, 여기서 a11 wt% ≤ Cxnone(ME1) ≤ a12 wt%이고, 상기 a11 및 a12는 독립적으로 a11 < a12인 경우에 한하여 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 35, 40, 45, 또는 50일 수 있는 사이클로헥사논;
- Cphol(ME1)의 농도의 페놀로서, 여기서 제1 중간 유출물의 총 중량 기준으로 a21 wt% ≤ Cphol(ME1) ≤ a22 wt%이고, 상기 a21 및 a22는 독립적으로 a21 < a22인 경우에 한하여, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80일 수 있으며, 페놀/사이클로헥사논 공비혼합물에서의 비에 근접되는 것으로, 바람직하게는, 1.0 ≤ Cphol(ME1)/Cxnone(ME1) ≤ 3.0, 더 바람직하게는, 2.0 ≤ Cphol(ME1)/Cxnone(ME1) ≤ 3.0의 농도인 페놀;
- Cchb(ME1)의 농도의 사이클로헥실벤젠으로서, 여기서 a31 wt% ≤ Cchb(ME1) ≤ a32 wt%이고, 상기 a31 및 a32는 독립적으로 a31 < a32인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있는 사이클로헥실벤젠;
- Cbch(ME1)의 농도의 비사이클로헥산으로서, 여기서 a41 wt% ≤ Cbch(ME1) ≤ a42 wt%이고, 상기 a41 및 a42는 독립적으로 a41 < a42인 경우에 한하여 0.001, 0.01, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있는 비사이클로헥산; 및
- Cxnol(ME1)의 농도의 사이클로헥사놀로서, 여기서 a51 wt% ≤ Cbch(ME1) ≤ a52 wt%이고, 상기 a51 및 a52는 독립적으로 a51 < a52인 경우에 한하여 0.01, 0.02, 0.04, 0.05, 0.06, 0.08, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있으며; 바람직하게는 0.01 wt% ≤ Cxnol(ME1) ≤ 5 wt%의 농도의 사이클로헥사놀.
유출물(107)은 수소화 반응기(R1)으로 전달되고, 여기서 이는 저장소(S3)로부터의 새로운 구성성분 수소 스트림(111) 및 재순환 수소(117)를 포함하는 수소 가스 공급물(112)과 혼합된다. 공급물(107)에 함유된 페놀 및 수소는 반응기(R1) 내부의 촉매층(113)의 존재 하에 서로 반응하여 사이클로헥사논을 생성한다. 반응기(R1) 내의 일부 사이클로헥사논은 또한 촉매층(113)의 존재 하에 수소와 반응하여 사이클로헥사놀을 생성한다. 도 1에 나타난 예시적인 공정에서, 과량의 수소는 반응기(R1)으로 공급된다.
수소화 반응은 수소화 촉매의 존재 하에 일어난다. 수소화 촉매는 지지체 물질 상에 지지되는 수소화 기능을 수행하는 수소화 금속을 포함할 수 있다. 수소화 금속은, 예를 들면, Fe, Co, Ni, Ru, Rh, Pd, Ag, Re, Os, Ir, 및 Pt, 및 이들의 하나 이상의 혼합물 및 조합물일 수 있다. 지지체 물질은 유리하게는 무기 물질, 예컨대 산화물, 유리, 세라믹, 분자체 등일 수 있다. 예를 들면, 지지체 물질은 활성 탄소, Al2O3, Ga2O3, SiO2, GeO2, SnO, SnO2, TiO2, ZrO2, Sc2O3, Y2O3, 알칼리 금속 산화물, 알칼리토 금속 산화물, 및 이의 혼합물, 조합물, 착물, 및 화합물일 수 있다. 수소화 금속의 농도는, 예를 들면, 촉매의 총 중량 기준으로 Cm1 wt% 내지 Cm2 wt%의 범위일 수 있고, 상기 Cm1 및 Cm2는 독립적으로 Cm1 < Cm2인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 5.0일 수 있다.
반응기(R1)로 공급되는 새로운 구성성분 수소(make-up hydrogen) 및 재순환된 수소를 포함하는 수소의 총량 및 수소화 반응 구간으로 공급되는 페놀의 총량은 바람직하게는 R(H2/phol)의 수소 대 페놀 몰비를 나타내고, 여기서 R1 ≤ R(H2/phol) ≤ R2이고, 상기 R1 및 R2는 독립적으로 R1 < R2인 경우에 한하여 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 5.0, 5.5, 6.0, 6.5, 7.0, 7.5, 8.0, 8.5, 9.0, 9.5, 또는 10일 수 있다. 한편, 더 높은 R(H2/phol) 비율은 페놀의 더 높은 전체 전환율을 야기할 수 있는 한편, 이는 또한 사이클로헥사논의 더 높은 전환율, 페놀의 사이클로헥사놀에 대한 더 높은 선택도, 및 사이클로헥실벤젠의 더 높은 전환율을 야기하는 경향이 있다. 따라서, 수소화 반응기(R1)에서, 비제한적으로 온도, 압력, 및 R(H2/phol) 비를 포함하는 반응 조건, 및 촉매는 페놀의 전체 전환율이 매우 높지 않도록 선택되는 것이 일반적으로 바람직하다는 것이 밝혀졌다.
반응기(R1)의 하부에서, 스트림(107)에서의 것보다 낮은 농도의 페놀, 스트림(107)에서의 것보다 높은 농도의 사이클로헥사논, 사이클로헥실벤젠, 비사이클로헥산, 및 과량의 수소를 포함하는 수소화 반응 생성물 스트림(115)이 취해진다. 스트림(115)은 이의 총 중량 기준으로 하기의 것을 포함할 수 있다:
- Cxnone(HRP)의 농도의 사이클로헥사논으로서, 여기서 b11 wt% ≤ Cxnone(HRP) ≤ b12 wt%이고, 상기 b11 및 b12는 독립적으로 b11 < b12인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90일 수 있는 사이클로헥사논;
- Cphol(HRP)의 농도의 페놀로서, 여기서 b21 wt% ≤ Cphol(HRP) ≤ b22 wt%이고, 상기 b21 및 b22는 독립적으로 b21 < b22인 경우에 한하여 1, 2, 5, 6, 8,10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 40, 50일 수 있는 페놀;
- Cchb(HRP)의 농도의 사이클로헥실벤젠으로서, 여기서 b31 wt% ≤ Cchb(HRP) ≤ b32 wt%이고, 상기 b31 및 b32는 독립적으로, b31 < b32인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30일 수 있는 사이클로헥실벤젠;
- Cbch(HRP)의 농도의 비사이클로헥산으로서, 여기서 b41 wt% ≤ Cbch(HRP) ≤ b42 wt%이고, 상기 b41 및 b42는 독립적으로 b41 < b42인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30일 수 있는 비사이클로헥산;
- Cxnol(HRP)의 농도의 사이클로헥사놀으로서, 여기서 b51 wt% ≤ Cxnol(HRP) ≤ b52 wt%이고, 상기 b51 및 b52는 독립적으로 b51 < b52인 경우에 한하여 0.01, 0.02, 0.04, 0.05, 0.06, 0.08, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10일 수 있는 사이클로헥사놀.
바람직하게는, 하기 카테고리 중 하나 이상이 수소화 반응 생성물 스트림(115)에서 충족된다:
- Ra31 ≤ Cchb(ME1)/Cchb(HRP) ≤ Ra32, 여기서 상기 Ra31 및 Ra32는 독립적으로 Ra31 < Ra32인 경우에 한하여 0.10, 0.20, 0.30, 0.40, 0.50, 0.60, 0.70, 0.75, 0.80, 0.85, 0.90, 0.92, 0.94, 0.95, 0.96, 0.98, 1.00, 1.02, 1.04, 1.05, 1.06, 1.08, 1.10, 1.15, 1.20, 1.25, 1.30, 1.35, 1.40, 1.50, 1.60, 1.70, 1.80, 1.90, 2.00, 3.00, 4.00, 5.00, 6.00, 7.00, 8.00, 9.00, 또는 10.0일 수 있으며; 더 바람직하게는, 0.80 ≤Cchb(ME1)/Cchb(HRP) ≤ 1.00이며, 이는 사이클로헥실벤젠 농도가 수소화 반응 구간에서 상당하게 감소되지 않는 것을 의미함;
- Ra41 ≤ Cbch(HRP)/Cbch(ME1) ≤ Ra42, 여기서 상기 Ra41 및 Ra42는 독립적으로 Ra41 < Ra42인 경우에 한하여 0.10, 0.20, 0.30, 0.40, 0.50, 0.60, 0.70, 0.75, 0.80, 0.85, 0.90, 0.92, 0.94, 0.95, 0.96, 0.98, 1.00, 1.02, 1.04, 1.05, 1.06, 1.08, 1.10, 1.15, 1.20, 1.25, 1.30, 1.35, 1.40, 1.50, 1.60, 1.70, 1.80, 1.90, 2.00, 3.00, 4.00, 5.00, 6.00, 7.00, 8.00, 9.00, 또는 10.0일 수 있으며, 바람직하게는, 1.0 ≤ Cbch(HRP)/Cbch(ME1) ≤ 1.5이며, 이는 비사이클로헥산 농도가 수소화 반응 구간에서 상당하게 증가되지 않는 것을 의미함; 및
- Ra51 ≤ Cxnol(HRP)/Cxnol(ME1) ≤ Ra52, 여기서 상기 Ra51 및 Ra52는 독립적으로, Ra51 < Ra52인 경우에 한하여, 0.10, 0.20, 0.30, 0.40, 0.50, 0.60, 0.70, 0.75, 0.80, 0.85, 0.90, 0.92, 0.94, 0.95, 0.96, 0.98, 1.00, 1.02, 1.04, 1.05, 1.06, 1.08, 1.10, 1.15, 1.20, 1.25, 1.30, 1.35, 1.40, 1.50, 1.60, 1.70, 1.80, 1.90, 2.00, 3.00, 4.00, 5.00, 6.00, 7.00, 8.00, 9.00, 또는 10.0일 수 있으며, 바람직하게는, 1.0 ≤ Cxnol(HRP)/Cxnol(ME1) ≤ 1.5이며, 이는 사이클로헥사놀 농도가 수소화 반응 구간에서 상당하게 증가되지 않는 것을 의미함.
스트림(115)는 분리 드럼(D1)으로 전달되고, 여기서 다수의 과량의 수소를 포함하는 증기상 및 액상이 수득된다. 증기상은 스트림(117)으로서 수소 공급원의 일부로서 반응기(R1)으로 재순환될 수 있고, 액상(119)은 컬럼(T1) 상의 하나 이상의 측면 위치에서 제1 분획화 컬럼(T1)으로 재순환되고, 이 위치 중 하나 이상은 제1 중간 유출물(107)이 취해지는 위치 위에 있으나, 제1 상부 유출물(105)이 취해지는 위치 아래에 있다.
제1 분획화 컬럼(T1)으로부터 수득되는 제1 하부 유출물(109)은 주로 중질 성분 예컨대 사이클로헥실벤젠, 비사이클로헥산, 상기 언급된 아민염, C18+, C12 산소화물, 및 C18+ 산소화물을 포함한다. 이 분획은 중질 증류 컬럼(T3)(제3 증류 컬럼)으로 전달되고, 이로부터 C31 wt%보다 높은 농도의 사이클로헥실벤젠을 함유하는 제3 상부 유출물(127) 및 하부 유출물(129)이 제조되고, 여기서 C31는 be 80, 82, 84, 85, 86, 88, 90, 92, 94, 95, 96, 98, 또는 99일 수 있다. 유출물(127)은 저장소(S11)으로 전달될 수 있고, 유출물(129)은 저장소(S13)으로 전달될 수 있다. 유출물(127)은 추가로 상당한 양으로 올레핀, 주로 페닐사이클로헥센 이성질체를 포함할 수 있다. 올레핀 농도를 감소시키기 위해 유출물(127)을 수소화시키고, 이후 수소화된 유출물(127)을 초기 단계 예컨대 사이클로헥실벤젠 산화로 재순환시켜 이의 적어도 일부를 사이클로헥실벤젠 하이드로퍼옥사이드로 전환시켜, 이에 의해 공정의 전체 수율을 개선하는 것이 바람직하다.
도 2는 제1 분획화 컬럼(T1) 및 수소화 반응기(R1) 사이의 및/또는 그 내에서 변형된 유체 연통체를 포함하는 것을 제외하고, 도 1에 나타낸 방법/시스템과 유사한 본 개시물의 예시적인 방법/시스템의 일부를 나타내는 개략도이다. 본 도면에서, 수소화 반응 생성물(115)은 도 1에 나타낸 예에서와 같이 잔류 수소를 포함한다. 유출물(115)은 우선 분리 드럼(D1)으로 전달되고, 여기서 수소-풍부 증기 스트림(117a)이 얻어지고, 압축기(118)에 의해 압축되고, 이후, 반응기(R1)에서의 새로운 구성성분 수소 스트림(111)과 함께 스트림(117b)으로서 반응기(R1)로 전달된다. 액체 스트림(119)가 분리 드럼(D1)으로부터 얻어지고, 이후 복수의 스트림(도 2에 나타난 바와 같은 2개의 재순환 스트림(119a 및 119b))으로 나누어지고, 컬럼(T1)의 측면 상의 2개의 상이한 위치로 재순환되고, 이중 하나는 제1 중간 유출물(107)이 취해지는 위치 아래(공급물(103)과 대략 동일한 수준으로 나타남)에 있고, 나머지 하나는 제1 중간 유출물(107)이 인출되는 위치 위에 있다. 도 1에 비교되는 수소화 반응기(R1) 및 분획화 컬럼(T1) 사이의 이러한 변형된 재순환 유체 연통체는 놀라운 장점을 가진다. 재순환 액체 스트림(119)가 단지 하나의 위치, 예컨대 제1 중간 유출물(107) 위의 위치에만 공급되는 경우, 비사이클로헥산은 스트림(107)에서의 사이클로헥실벤젠으로부터 반응기(R1)에서 연속적으로 생성되고, 이후 점차적으로 별개 상이 형성될 수 있는 높은 농도로 컬럼(T1)에 축적되고, 이는 컬럼(T1)에서의 효과적인 생성물 분리를 방해한다는 것을 발견하였다. 다른 한편, 재순환 스트림(119)가 (도 2에 나타낸 바와 같이) T1 상의 복수개의 위치에서 컬럼(T1)으로 다시 재순환되는 경우, T1 내부에서 별개의 비사이클로헥산 상을 형성할 가능성은 급격하게 감소되거나 없어진다.
도 3은 제1 분획화 컬럼(T1) 및 사이클로헥사논 정제 컬럼(T2) 사이의 및/또는 그 내부에 변형된 유체 연통체 및/또는 열 전달 구성을 포함하는 도 1 및 도 2에 나타난 것과 유사한 본 개시물의 예시적인 방법/시스템의 일부를 나타내는 개략도이다. 본 도면에서, 수소화 반응기(R1) 및 이의 주변 장비는 도시되지 않는다. 본 예에서, 컬럼(T1)으로부터 인출된 제1 중간 유출물(107)은 복수개의 스트림(나타낸 2개의 스트림(107a 및 107b))으로 나누어지고, 이 중 하나(107a)는 수소화 공급물로서 수소화 반응기(R1)(미도시됨)에 전달되고, 나머지 하나(107b)는 사이클로헥사논 정제 컬럼(T2)과 유체적 및 열적 연통되는 열 교환기(131)로 전달된다. 이러한 예에서, 컬럼(T2)로부터의 하부 스트림(125)(예를 들면, 사이클로헥사논 및 사이클로헥사놀의 혼합물을 포함함)은 하기 3개의 스트림으로 나누어진다: 열 교환기(131)을 통과하여 스트림(107b)에 의해 가열되는 스트림(135); 열 교환기(141)에 의해 가열되고, 이후 컬럼(T2)로 재순환되는 스트림(139); 및 펌프(147)를 통해 저장소(S9)로 전달되는 스트림(145). 스트림(107b)은 열 교환기(131)를 통과한 이후 더 냉각된 스트림(133)이 되고, 이는 이후 후속하여 하나 이상의 위치에서 제1 분획화 컬럼(T1)으로 재순환되고, 이 위치 중 하나 이상은 제1 중간 유출물(107)이 인출되는 위치보다 위에 위치한다. 도 3에 예시된 바와 같은 열 관리 도식은 본 개시물의 전체 방법 및 시스템의 에너지 효율을 상당하게 개선할 수 있다.
도 4는 관형 열 교환기-유형 수소화 반응기를 포함하는 것을 제외하고 도 1 - 3에 나타난 것과 유사한 본 개시물의 예시적인 방법/시스템의 일부를 나타내는 개략도이다. 이러한 도면은 수소화 반응기(R1)가 반응기(R1) 내부의 반응 매체에 존재하는 대다수의 페놀 및/또는 사이클로헥실벤젠이 증기상으로 존재하게 하는 수소화 조건 하에 작동되는 예를 예시하고 있다. 본 예에서, 제1 분획화 컬럼(T1)으로부터 취해지는 제1 중간 유출물(107)은 우선 수소 공급물(새로운 구성성분 수소 스트림(111) 및 재순환 수소 스트림(117b)을 포함함)과 조합되고, 열 교환기(151)에 의해 가열되고, 이후 튜브(157) 내부에 탑재된 수소화 촉매를 갖는 관형 열-교환기 유형 수소화 반응기(R1)으로 전달된다. 냉각 매체(159) 예컨대 저장소(S11)로부터 공급되는 냉각수의 스트림은 교환기/반응기(R1)의 쉘을 통과하고, 온난 스트림(161)으로서 반응기(R1)으로부터 배출되고, 이후 저장소(S13)으로 전달되어, 이에 의해 페놀 수소화 반응으로부터 배출되는 상당한 양의 열이 수송되어, 반응기(R1) 내부의 온도를 T1℃ 내지 T2 ℃의 범위로 그리고 반응기(R1) 내부의 절대 압력을 P1 kPa 내지 P2 kPa의 범위로 유지하게 하고, 여기서 상기 T1 및 T2는 독립적으로 T1 < T2인 경우에 한하여 140, 145,150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240, 250, 260, 270, 280, 290, 300일 수 있고, 상기 P1 및 P2는 독립적으로 P1 < P2인 경우에 한하여 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 350, 400일 수 있다. 바람직하게는 T2 = 240 및 P2 = 200이다. 증기상의 열 전달은 액상만큼 효율적이지 않고, 페놀 수소화 반응은 매우 발열성이고, 열 전달이 이러한 증기상 수소화 반응기에서 신중하게 관리되는 것이 매우 바람직하다.
도 5는 일련하여 연결된 3개의 고정층 수소화 반응기(R3, R5, 및 R7)를 포함하는 것을 제외하고, 도 1-4에 나타난 것과 유사한 본 개시물의 예시적인 방법/시스템의 일부를 나타내는 개략도이다. 본 도면은 수소화 반응기가 반응기(R3, R5, 및 R7) 내부의 반응 매체에 존재하는 대다수의 페놀 및/또는 사이클로헥실벤젠이 액상으로 존재하게 하는 수소화 조건 하에 작동되는 예를 예시하고 있다. 본 예에서, 제1 분획화 컬럼(T1)으로부터 취해지는 제1 중간 유출물(107)은 우선 수소 공급물(새로운 구성성분 수소 스트림(111) 및 재순환 수소 스트림(117b)를 포함함)과 조합되어 공급물 스트림(151)을 형성하고, 이후 열 교환기(153)에 의해 가열되고, 내부에 촉매층(167)을 갖는 제1 수소화 반응기(R3)로 스트림(155)로서 전달된다. 페놀의 일부는 반응기(R3)에서 사이클로헥사논으로 전환되고, 이는 반응 매체에서 온도를 상승시키는 적절한 양의 열을 방출한다. 반응기(R3)로부터 배출되는 유출물(169)은 이후 열 교환기(171)에 의해 냉각되고, 이후 내부에 촉매층(175)을 갖는 제2 고정층 반응기(R5)로 전달된다. 반응 매체에 함유되는 페놀의 일부는 반응기(R5)에서의 사이클로헥사논으로 전환되고, 이는 반응기(R5) 내부의 온도를 상승시키는 적절한 양의 열을 방출한다. 반응기(R5)로부터 배출되는 유출물(177)은 열 교환기(179)에 의해 냉각되고, 이후 내부에 촉매층(183)을 갖는 제3 고정층 수소화 반응기(R7)으로 전달된다. 반응 매체에 함유되는 페놀의 일부는 반응기(R7)에서의 사이클로헥사논으로 전환되고, 이는 반응기(R7) 내부의 온도를 상승시키는 적절한 양의 열을 방출한다. 반응기(R7)으로부터 배출되는 유출물(185)은 이후 열 교환기(179)에 의해 냉각되고, 드럼(D1)으로 전달되고, 여기서 증기상(117a) 및 액상(119)이 수득된다. 수소화 반응 구간에서의 복수개의 반응기를 사용하고, 각각의 반응기들 사여기서 및 그 뒤에서 열 교환기를 사용함으로써, 반응기(R3, R5, 및 R7) 내부의 온도는 각각 독립적으로 T3℃ 내지 T4℃의 범위로 유지되고, 반응기(R3, R5, 및 R7) 내부의 절대 압력은 각각 독립적으로 P3 kPa 내지 P4 kPa의 범위로 유지되고, 여기서 상기 T3 및 T4는 독립적으로 T3 < T4인 경우에 한하여 140, 145,150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240, 250, 260, 270, 280, 290, 300일 수 있고, 상기 P3 및 P4는 독립적으로 P3 < P4인 경우에 한하여 375, 400, 425, 450, 475, 500, 525, 550, 575, 600, 625, 650, 675, 700, 725, 750, 775, 800, 825, 850, 875, 900, 925, 950, 975, 1000, 1025, 1050, 1075, 1100, 1125, 1134, 1150, 1175, 1200일 수 있다. 바람직하게는 T4 = 240 및 P4 = 1134이다. 일반적으로 고온은 사이클로헥사논보다는 사이클로헥사놀의 제조에 선호된다. 따라서, 수소화는 220℃ 이하의 온도에서 실시되는 것이 매우 바람직하다.
도 6은 제1 분획화 컬럼(T1) 및 수소화 반응기(R1) 사여기서의 및/또는 그 내부에서의 변형된 유체 연통체를 포함하는 것을 제외하고 도 1-5에 나타난 방법/시스템과 유사한 본 개시물의 예시적인 방법/시스템의 일부를 나타내는 개략도이다. 본 도면에서, 제1 중간 유출물(107a) 및 제2 중간 유출물(107b)을 포함하는 2개의 중간 유출물이 제1 분획화 컬럼(T1)의 측면으로부터 인출된다. 2개의 유출물 (107a 및 107b)은 상이한 조성을 가지고, 이는 조합되어 공급물(107)을 형성하고, 이는 이후 수소 공급물 스트림(111 및 117b)과 조합되고, 수소화 반응기(들)로 전달된다. 상이한 위치에서 상이한 조성을 갖는 2개의 중간 유출물을 인출하는 것은 예상밖의 기술적 장점을 가진다. 단지 하나의 중간 유출물이 컬럼(T1) 상의 단일 위치로부터 인출되는 경우, 특정 바람직하지 않은 성분, 예컨대 하이드록시사이클로헥사논(들)이 컬럼(T1) 내에 축적될 수 있다. 하이드록시사이클로헥사논(들)이 탈수되어 사이클로헥사논을 형성할 수 있고, 이는 컬럼(T1) 내에 오염을 야기할 수 있는 것으로 여겨진다. 컬럼 상의 상이한 높이 위치에서 중간 유출물을 인출함으로써, 컬럼 내부에서의 이러한 바람직하지 않은 성분의 축적 및 오염의 가능성을 효과적으로 감소시킬 수 있다.
도 7은 수소화 반응기에서의 촉매 피독화를 감소시키거나 방지하기 위해 제1 분획화 컬럼(T1)으로 공급되는 페놀/사이클로헥사논/사이클로헥실벤젠 공급물로부터 경질 성분의 적어도 일부를 제거하도록 구성된 제1 분획화 컬럼(T1) 앞에 사이드 스트리퍼 컬럼(T4)을 포함하는 것을 제외하고, 도 1-6에 나타난 것과 유사한 본 개시물의 예시적인 방법/시스템의 일부를 나타내는 개략도이다. 수소화 반응 구간으로의 페놀/사이클로헥사논/사이클로헥실벤젠 공급물에 포함하는 경우, 특정 경질 성분(즉, 사이클로헥사논보다 낮은 기준 비점을 갖는 성분)은 탈수소화 촉매를 피독시킬 수 있고, 이는 촉매의 성능 및 수명의 조기 감소를 야기하는 것으로 여겨진다. 이와 같이, 본 도면에서, 페놀/사이클로헥사논/사이클로헥실벤젠 공급물(102)은 우선 컬럼(T1)보다 작은 사이드 스트리퍼(T4)로 공급되어, 경질 성분이 풍부하고, 페놀 및 사이클로헥실벤젠이 감소된 상부 유출물(105a) 및 경질 성분이 감소된 하부 유출물(103)을 수득한다. 상부 유출물(105a)은 이후 제1 분획화 컬럼(T1)으로부터 수득되는 제1 상부 유출물(105b)과 조합되어 스트림(105)을 형성하고, 이는 이후 사이클로헥사논 정제 컬럼(T2)으로 전달된다. 하부 유출물(103)은 이후 페놀/사이클로헥사논/사이클로헥실벤젠 공급물로서 제1 분획화 컬럼(T1)으로 전달된다. 소량의 상대적으로 저렴한 사이드 스트리퍼(T4)를 부가함으로써, 수소화 촉매를 피독화하는 경향이 있는 대다수의 경질 성분(예를 들면, C1-C6 유기산)을 제거할 수 있다.
도 8은 도 7의 구조의 대안을 나타낸다. 본 도면에서, 제1 분획화 컬럼(T1) 앞에 사이드 스트리퍼(T4)를 배치하는 것 대신에, 사이드 스트리퍼(T5)가 공급물로서 제1 중간 유출물(107)을 공급받는 컬럼(T1) 뒤에 배치되고, 유출물(107)이 인출되는 위치보다 높은 위치에서 컬럼(T1)으로 재순환되는, 수소화 촉매를 피독화하는 경향이 있는 경질 성분(예를 들면, C1-C6 유기산)이 풍부한 상부 유출물(193), 및 이러한 경질 성분이 감소되고, 수소 공급물(111 및 117b)과 함께 일부 또는 모든 페놀/사이클로헥사논/사이클로헥실벤젠 공급물(151)로서 수소화 반응기로 전달되는 하부 유출물(195)를 생성한다.
도 9는 최종 사이클로헥사논 생성물로부터 경질 성분의 양을 감소시키도록 구성된 사이클로헥사논 정제 컬럼(T2) 뒤에 사이드 스트리퍼 컬럼(T6)을 포함하는 도 1-8에 나타난 것과 유사한 본 개시물의 방법/시스템의 예시적인 일부를 나타내는 개략도이다. 본 도면에서, 주로 제1 분획화 컬럼(T1)으로부터 수득된 경질 성분 및 사이클로헥사논을 포함하는 제1 상부 유출물(105)은 사이클로헥사논 정제 컬럼(T2)로 전달되고, 여기서 하기와 같은 3개의 유출물이 수득된다: 경질 성분 예컨대 물 및 메틸사이클로펜타논이 풍부하고, 사이클로헥사논 및 사이클로헥사놀이 감소된 제2 상부 유출물(121), 사이클로헥사논이 풍부하고 경질 성분 및 사이클로헥사놀이 감소된 제2 중간 유출물(123), 및 사이클로헥사놀이 풍부한 제2 하부 유출물(125). 유출물(121)은 우선 열 교환기(197)에 의해 냉각되고, 분리 드럼(D2)으로 전달되어, 이후 컬럼(T2)로 재순환되는 액상(199), 및 열 교환기(203)에 의해 다시 냉각되는 증기상(201)을 수득하고, 다른 분리 드럼(D3)로 전달되어 스트림(205)로서 드럼(D2)로 부분적으로 재순환되고, 저장소로(S5)로 부분적으로 전달되는 액상 및 퍼징될 수 있는 증기상(206)을 수득한다. 유출물(123)은 사이드 스트리퍼(T6)로 전달되고, 여기서 하기 스트림이 생성된다: 저장소(S7)으로 전달되는 이의 하부 근처에서의 실질적으로 순수한 사이클로헥사논 스트림(211); 및 (123) 위의 위치에서 컬럼(T2)로 재순환되는 경질 스트림(209).
상기 모든 도면에서, 수소화 반응기로 전달되는 페놀/사이클로헥사논/사이클로헥실벤젠 공급물은 제1 분획화 컬럼(T1)으로부터의 하나 이상의 중간 유출물로부터 전반적으로 수득된다. 그러나, 부가적으로, 컬럼(T1)으로부터 수득되는 공급물 이상의 농도의 페놀을 포함하는 제2 페놀 공급물 스트림이 독립적으로 그리고 별도로 또는 컬럼(T1)으로부터 수득된 공급물 및/또는 수소 공급물과 조합한 이후에 수소화 반응기로 공급될 수 있다. 예를 들면, 제2 페놀 스트림은 이의 총 중량 기준으로 Cphol(f2) wt% 이상의 페놀 농도를 갖는 실질적으로 순수한 페놀을 포함할 수 있고, 여기서 Cphol(f2)는 예를 들면, 80, 82, 84, 85, 86, 88, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 99.5, 99.8, 또는 심지어 99.9일 수 있다.
사이클로헥사논
및 페놀의 용도
본원에 개시된 방법을 통해 제조된 사이클로헥사논은 예를 들면, 산화 반응에서 그리고 아디프산, 사이클로헥사논 수지, 사이클로헥사논 옥심, 카프로락탐, 및 나일론 예컨대 나일론-6 및 나일론-6,6의 제조시 활성제로서, 공업 용매로서 사용될 수 있다.
본원에 개시된 방법을 통해 제조된 페놀은 예를 들면, 페놀성 수지, 비스페놀 A, ε-카프로락탐, 아디프산, 및/또는 가소제를 제조하기 위해 사용될 수 있다.
본 발명이 특정 구현예를 참조하여 기술되고 예시되어 있는 한편, 본 기술분야의 당업자는 본 발명은 그 자체가 본원에 필수적으로 예시되지 않는 변형예에 제공될 수 있다는 것을 이해할 수 있을 것이다. 이러한 이유로, 이후 본 발명의 실제 범위를 결정하기 위한 목적을 위해 첨부된 청구항에 대해서만 참조가 이루어져야 한다.
본원에 인용된 모든 참조문헌의 내용은 그 전문이 참조로 포함되어 있다.
본 발명은 하나 이상의 하기 비제한적인 양태 및/또는 구현예를 포함한다.
E1. 하기 단계를 포함하는 사이클로헥사논의 제조 방법:
(I) Cxnone(FM1)의 농도의 사이클로헥사논, Cphol(FM1)의 농도의 페놀, 및 Cchb(FM1)의 농도의 사이클로헥실벤젠을 포함하는 제1 혼합물을 제1 증류 컬럼으로 공급하는 단계;
(II) 제1 증류 컬럼으로부터,
Cxnone(UE1)의 농도의 사이클로헥사논, Cphol(UE1)의 농도의 페놀 및 Cchb(UE1)의 농도의 사이클로헥실벤젠을 포함하는 제1 상부 유출물;
Cxnone(ME1)의 농도의 사이클로헥사논, Cphol(ME1)의 농도의 페놀, 및 Cchb(ME1)의 농도의 사이클로헥실벤젠, 및 Cbch(ME1)의 농도의 비사이클로헥산을 포함하는 제1 중간 유출물; 및
Cchb(LE1)의 농도의 사이클로헥실벤젠을 포함하는 제1 하부 유출물
을 수득하는 단계로서,
여기서,
Cxnone(UE1) > Cxnone(FM1);
Cphol(ME1) > Cphol(FM1); 및
Cchb(LE1) > Cchb(FM1)인 단계
(III) 적어도 일부의 제1 중간 유출물 및 수소를 수소화 반응 구간으로 공급하는 단계로서, 여기서 페놀이 수소화 반응 조건으로 수소화 촉매의 존재 하에 수소와 반응하여, Cxnone(HRP)의 농도의 사이클로헥사논, Cphol(HRP)의 농도의 페놀, Cchb(HRP)의 농도의 사이클로헥실벤젠, 및 Cbch(HRP)의 농도의 비사이클로헥산을 포함하는 수소화 반응 생성물을 수득하며, 여기서
Cxnone(HRP) > Cxnone(ME1); 및
Cphol(HRP) < Cphol(ME1)인 단계; 및
(IV) 적어도 일부의 수소화 반응 생성물을 제1 증류 컬럼으로 공급하는 단계.
E2. E1에 있어서, Cxnone(FM1)는 제1 혼합물의 총 중량 기준으로 x11 wt% 내지 x12 wt%의 범위이고, 여기서 상기 x11 및 x12는 독립적으로 x11 < x12인 경우에 한하여 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 82, 84, 85, 86, 88, 또는 90일 수 있는 방법.
E3. E1 또는 E2에 있어서, Cphol(FM1)이 제1 혼합물의 총 중량 기준으로 x21 wt% 내지 x22 wt%의 범위이고, 상기 x21 and x22는 독립적으로, x21 < x22인 경우에 한하여 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 82, 84, 85, 86, 88, 또는 90일 수 있는 방법.
E4. E1 내지 E3 중 어느 하나에 있어서, Cchb(FM1)이 제1 혼합물의 총 중량 기준으로 x31 wt% 내지 x32 wt%의 범위이고, 상기 x31 및 x32는 독립적으로 x31 < x32인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 32, 34, 35, 36, 38, 40, 42, 44, 45, 46, 48, 50, 52, 54, 55, 56, 58, 60, 62, 64, 65, 66, 68, 70, 72, 74, 또는 75일 수 있는 방법.
E5. E1 내지 E4 중 어느 하나에 있어서, 제1 혼합물은 제1 혼합물의 총 중량 기준으로 x41 wt% 내지 x42 wt%의 범위의 Cbch(FM1)의 농도의 비사이클로헥산을 더 포함하고, 상기 x41 및 x42는 독립적으로 x41 < x42인 경우에 한하여, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있는 방법.
E6. E1 내지 E5 중 어느 하나에 있어서, 제1 혼합물은 황산의 유기 아민염을 더 포함하는 방법.
E7. E1에 있어서, 제1 상부 유출물은 Cxnol(UE1)의 농도의 사이클로헥사놀을 더 포함하며, 본 방법은 하기 단계를 더 포함하는 방법:
(V) 적어도 일부의 제1 상부 유출물을 제2 증류 컬럼으로 공급하는 단계; 및
(VI) 제2 증류 컬럼으로부터,
Cxnone(UE2)의 농도의 사이클로헥사논을 포함하는 제2 상부 유출물; 및
Cxnone(LE2)의 농도의 사이클로헥사논 및 Cxnol(LE2)의 농도의 사이클로헥사놀을 포함하는 제2 하부 유출물을 수득하는 단계로서; 여기서,
Cxnone(UE2) > Cxnone(UE1) > Cxnone(LE2); 및
Cxnol(LE2) > Cxnol(UE1)인 단계.
E8. E7에 있어서, 제2 상부 유출물의 총 중량 기준으로 Cxnone(UE2) ≥ y11 wt%이고, 상기 y11은 95, 95.5, 96, 96.5, 97, 97.5, 98, 98.5, 99, 99.5, 99.8, 또는 99.9일 수 있는 방법.
E9. E7 또는 E8에 있어서, 제3 상부 유출물은 제2 상부 유출물 위의 위치에서 제2 증류 컬럼으로부터 수득되고, 제3 상부 유출물은 사이클로헥사논의 것보다 낮은 기준 비점을 갖는 성분을 포함하는 방법.
E10. E1 내지 E9 중 어느 하나에 있어서, 제1 상부 유출물의 총 중량 기준으로 z11 wt% ≤ Cxnone(UE1) ≤ z12 wt%이고, 상기 z11 및 z12는 독립적으로 z11 < z12인 경우에 한하여 60, 65, 70, 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99일 수 있는 방법.
E11. E1 내지 E10 중 어느 하나에 있어서, 제1 상부 유출물의 총 중량 기준으로 z21 ≤ Cphol(UE1) ≤ z22이고, 상기 z21 및 z22는 독립적으로 z21 < z22인 경우에 한하여 0.00001, 0.00005, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 또는 1일 수 있는 방법.
E12. E1 내지 E11 중 어느 하나에 있어서, 제1 상부 유출물의 총 중량 기준으로 y31 wt% ≤ Cchb(UE1) ≤ y32 wt%이고, 상기 y31 및 y32는 독립적으로 y31 < y32인 경우에 한하여 0.00001, 0.00005, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 또는 1일 수 있는 방법.
E13. E1 내지 E12 중 어느 하나에 있어서, 제1 상부 유출물은 Cbch(UE1)의 농도의 비사이클로헥산을 더 포함하고, 그리고 제1 상부 유출물의 총 중량 기준으로 y41 wt% ≤ Cbch(UE1) ≤ y42 wt%이고, 상기 y41 및 y42는 독립적으로 y41 < y42인 경우에 한하여, 0.00001, 0.00005, 0.0001, 0.0005, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 또는 1일 수 있는 방법.
E14. E7 내지 E13 중 어느 하나에 있어서, 제1 상부 유출물의 총 중량 기준으로 x51 wt% ≤ Cxnol(UE1) ≤ x52 wt%이고, 상기 x51 및 x52은 독립적으로 x51 < x52인 경우에 한하여, 0.001, 0.005, 0.01, 0.05, 0.1, 0.5, 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 5.0, 5.5, 6.0, 6.5, 7.0, 7.5, 8.0, 8.5, 9.0, 9.5, 또는 10일 수 있는 방법.
E15. E7 내지 E14 중 어느 하나에 있어서, 제2 하부 유출물의 총 중량 기준으로 y51 wt% ≤ Cxnol(LE2) ≤ y52 wt%이고, 상기 y51 및 y52는 독립적으로 y51 < y52인 경우에 한하여, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 32, 34, 35, 36, 38, 40, 42, 44, 45, 46, 48, 50, 52, 54, 55, 56, 58, 60, 62, 64, 65, 66, 68, 70, 72, 74, 75, 76, 78, 또는 80일 수 있는 방법.
E16. E1 내지 E15 중 어느 하나에 있어서, 제1 중간 유출물의 총 중량 기준으로 a11 wt% ≤ Cxnone(ME1) ≤ a12 wt%이고, 상기 a11 및 a12는 독립적으로 a11 < a12인 경우에 한하여, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30, 35, 40, 45, 또는 50일 수 있는 방법.
E17. E1 내지 E16 중 어느 하나에 있어서, 제1 중간 유출물의 총 중량 기준으로 a21 wt% ≤ Cphol(ME1) ≤ a22 wt%이고, 상기 a21 및 a22는 독립적으로 a21 < a22인 경우에 한하여, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 82, 84, 85, 86, 88, 또는 90일 수 있는 방법.
E18. E1 내지 E17 중 어느 하나에 있어서, 제1 중간 유출물의 총 중량 기준으로 a31 wt% ≤ Cchb(ME1) ≤ a32 wt%이고, 상기 a31 및 a32는 독립적으로 a31 < a32인 경우에 한하여, 0.001, 0.005, 0.01, 0.05, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있는 방법.
E19. E1 내지 E18 중 어느 하나에 있어서, 제1 중간 유출물의 총 중량 기준으로 a41wt% ≤ Cbch(ME1) ≤ a42 wt%이고, 상기 a41 및 a42는 독립적으로 a41 < a42인 경우에 한하여, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있는 방법.
E20. E1 내지 E19 중 어느 하나에 있어서, 제1 중간 유출물은 Cxnol(ME1)의 농도로 사이클로헥사놀을 더 포함하고, 제1 중간 유출물의 총 중량 기준으로 a51wt% ≤ Cbch(ME1) ≤ a52 wt%이고, 상기 a51 및 a52는 독립적으로 a51 < a52인 경우에 한하여, 0.01, 0.02, 0.04, 0.05, 0.06, 0.08, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 또는 30일 수 있는 방법.
E21. E1 내지 E20 중 어느 하나에 있어서, 제1 중간 유출물과는 별도의 제2 페놀-함유 스트림이 수소화 반응 구간으로 공급되는 방법.
E22. E21에 있어서, 제2 페놀-함유 스트림은 Cphol(FP)의 농도의 페놀을 포함하고, 제2 페놀-함유 스트림의 총 중량 기준으로 d21 wt% ≤ Cphol(FP) ≤ d22 wt%이고, 상기 d21 및 d22는 독립적으로 d21 < d22인 경우에 한하여, 50, 55, 60, 65, 70, 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 또는 100일 수 있는 방법.
E23. E1 내지 E22 중 어느 하나에 있어서, 수소 및 페놀은 R(H2/phol)의 수소 대 페놀 몰비로 수소화 반응 구간에 공급되고, R1 ≤ R(H2/phol) = R2이고, 상기 R1 및 R2는 독립적으로 R1 < R2인 경우에 한하여, 1.0, 1.5, 2.0, 2.5, 3.0, 3.5, 4.0, 4.5, 6.0, 6.5, 7.0, 7.5, 8.0, 8.5, 9.0, 9.5, 또는 10일 수 있는 방법.
E24. E1 내지 E23 중 어느 하나에 있어서, 수소화 반응 구간에서, 사이클로헥실벤젠의 C11% 이상은 액상으로 존재하고, 상기 C11은 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 96, 97, 98, 또는 99일 수 있는 방법.
E25. E1 내지 E24 중 어느 하나에 있어서, 수소화 반응 구간에서, 페놀의 C21% 이상은 액상으로 존재하고, 상기 C21은 60, 65, 70, 75, 80, 85, 90, 95, 96, 97, 98, 또는 99일 수 있는 방법.
E26. E24 또는 E25에 있어서, 수소화 반응 구간에서, 수소화 반응 조건은 T1℃ 내지 T2℃의 범위의 온도 및 P1 kPa 내지 P2 kPa의 범위의 절대 압력을 포함하고, 상기 T1 및 T2는 독립적으로 T1 ≤ T2인 경우에 한하여, 140, 145,150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240일 수 있고; 상기 P1 및 P2는 독립적으로 P1 ≤ P2인 경우에 한하여, 375, 400, 425, 450, 475, 500, 525, 550, 575, 600, 625, 650, 675, 700, 725, 750, 775, 800, 825, 850, 875, 900, 925, 950, 975, 1000, 1025, 1050, 1075, 1100, 1125, 1134, 1150, 1175, 1200일 수 있는 방법.
E27. E24 내지 E26 중 어느 하나에 있어서, 수소화 반응 구간은 연속하여 연결되는 복수개의 수소화 반응기를 포함하는 방법.
E28. E1 내지 E27 중 어느 하나에 있어서, 수소화 반응 구간에서, 사이클로헥실벤젠의 CA11% 이상은 증기상으로 존재하고, 상기 CA11는 90, 95, 96, 97, 98, 또는 99일 수 있는 방법.
E29. E28에 있어서, 수소화 반응 구간에서, CA21%의 페놀은 증기상으로 존재하고, 상기 CA21은 90, 95, 96, 97, 98, 또는 99일 수 있는 방법.
E30. E28 또는 E29에 있어서, 수소화 반응 구간에서, 수소화 반응 조건은 T1℃ 내지 T2℃의 범위의 온도 및 P1 kPa 내지 P2 kPa의 범위의 절대 압력을 포함하고, 상기 T1 및 T2는 독립적으로 T1 ≤ T2인 경우에 한하여, 140, 145,150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240일 수 있고; 상기 P1 및 P2는 독립적으로 P1 ≤ P2인 경우에 한하여, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200일 수 있는 방법.
E31. E1 내지 E30 중 어느 하나에 있어서, 수소화 반응 생성물의 총 중량 기준으로 b11 wt% ≤ Cxnone(HRP) ≤ b12 wt%이고, 상기 b11 및 b12는 독립적으로 b11 < b12인 경우에 한하여 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90일 수 있는 방법.
E32. E1 내지 E31 중 어느 하나에 있어서, 수소화 반응 생성물의 총 중량 기준으로 b21 wt% ≤ Cphol(HRP) ≤ b22 wt%이고, 상기 b21 및 b22는 독립적으로 b21 < b22인 경우에 한하여, 1, 2, 5, 6, 8,10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30일 수 있는 방법.
E33. E1 내지 E32 중 어느 하나에 있어서, 수소화 반응 생성물의 총 중량 기준으로 b31 wt% ≤ Cchb(HRP) ≤ b32 wt%이고, 상기 b31 및 b32는 독립적으로 b31 < b32인 경우에 한하여, 0.001, 0.005, 0.01, 0.05, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30일 수 있는 방법.
E34. E1 내지 E33 중 어느 하나에 있어서, 수소화 반응 생성물의 총 중량 기준으로 b41 wt% ≤ Cbch(HRP) ≤ b42 wt%이고, 상기 b41 및 b42는 독립적으로 b41 < b42인 경우에 한하여 0.001, 0.005, 0.01, 0.05, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10, 12, 14, 15, 16, 18, 20, 22, 24, 25, 26, 28, 30일 수 있는 방법.
E35. E1 내지 E34 중 어느 하나에 있어서, 수소화 반응 생성물은 추가로 Cxnol(HRP)의 농도의 사이클로헥사놀을 포함하고, 수소화 반응 생성물의 총 중량 기준으로 b51 wt% ≤ Cxnol(HRP) ≤ b52 wt%이고, 상기 b51 및 b52는 독립적으로 b51 < b52인 경우에 한하여, 0.01, 0.02, 0.04, 0.05, 0.06, 0.08, 0.1, 0.2, 0.4, 0.5, 0.6, 0.8, 1, 2, 4, 5, 6, 8, 10일 수 있는 방법.
E36. E1 내지 E35 중 어느 하나에 있어서, Ra31 ≤ Cchb(ME1)/Cchb(HRP) ≤ Ra32이고, 상기 Ra31 및 Ra32는 독립적으로 Ra31 < Ra32인 경우에 한하여, 0.10, 0.20, 0.30, 0.40, 0.50, 0.60, 0.70, 0.75, 0.80, 0.85, 0.90, 0.92, 0.94, 0.95, 0.96, 0.98, 1.00, 1.02, 1.04, 1.05, 1.06, 1.08, 1.10, 1.15, 1.20, 1.25, 1.30, 1.35, 1.40, 1.50, 1.60, 1.70, 1.80, 1.90, 2.00, 3.00, 4.00, 5.00, 6.00, 7.00, 8.00, 9.00, 또는 10.0일 수 있고; 더 바람직하게는, 0.80 ≤Cchb(ME1)/Cchb(HRP) ≤ 1.00인 방법.
E37. E1 내지 E36 중 어느 하나에 있어서, Ra41 ≤ Cbch(HRP)/Cbch(ME1) ≤ Ra42이고, 상기 Ra41 및 Ra42는 독립적으로 Ra41 < Ra42인 경우에 한하여, 0.10, 0.20, 0.30, 0.40, 0.50, 0.60, 0.70, 0.75, 0.80, 0.85, 0.90, 0.92, 0.94, 0.95, 0.96, 0.98, 1.00, 1.02, 1.04, 1.05, 1.06, 1.08, 1.10, 1.15, 1.20, 1.25, 1.30, 1.35, 1.40, 1.50, 1.60, 1.70, 1.80, 1.90, 2.00, 3.00, 4.00, 5.00, 6.00, 7.00, 8.00, 9.00, 또는 10.0일 수 있고; 바람직하게는, 1.00 ≤ Cbch(HRP)/Cbch(ME1) ≤ 1.50인 방법.
E38. E1 내지 E37 중 어느 하나에 있어서, Ra51 ≤ Cxnol(HRP)/Cxnol(ME1) ≤ Ra52이고, 상기 Ra51 및 Ra52는 독립적으로 Ra51 < Ra52인 경우에 한하여, 0.10, 0.20, 0.30, 0.40, 0.50, 0.60, 0.70, 0.75, 0.80, 0.85, 0.90, 0.92, 0.94, 0.95, 0.96, 0.98, 1.00, 1.02, 1.04, 1.05, 1.06, 1.08, 1.10, 1.15, 1.20, 1.25, 1.30, 1.35, 1.40, 1.50, 1.60, 1.70, 1.80, 1.90, 2.00, 3.00, 4.00, 5.00, 6.00, 7.00, 8.00, 9.00, 또는 10.0일 수 있고; 바람직하게는 1.00 ≤ Cxnol(HRP)/Cxnol(ME1) ≤ 1.50인 방법.
E39. E1 내지 E36 중 어느 하나에 있어서, 단계 (III) 이후,
(IIIA) 수소화 반응 생성물을 액체 스트림 및 증기 스트림으로 분리하는 단계; 및
(IIIB) 적어도 일부의 증기 스트림을 수소화 반응 구간으로 재순환시키는 단계
를 더 포함하고,
그리고 단계 (IV)는 적어도 일부의 액체 스트림을 제1 증류 컬럼으로 공급하는 것을 포함하는 방법.
E40. E39에 있어서, 적어도 일부의 액체 스트림을 제1 혼합물의 일부로서 증류 컬럼으로 공급하는 방법.
E41. E1 내지 E40 중 어느 하나에 있어서, 적어도 일부의 수소화 반응 생성물은 증류 컬럼으로 공급되는 제1 혼합물의 일부를 형성하는 방법.
E42. E1 내지 E41 중 어느 하나에 있어서,
수소화 반응 생성물은 복수개의 스트림으로 분리되고;
복수개의 스트림 중 하나 이상은 제1 중간 유출물이 인출되는 위치보다 높은 위치에서 제1 증류 컬럼으로 공급되고; 및
복수개의 스트림 중 하나 이상은 제1 중간 유출물이 인출되는 위치보다 낮은 위치에서 제1 증류 컬럼으로 공급되는 방법.
E43. E1 내지 E42 중 어느 하나에 있어서, 단계 (I)에서의 제1 혼합물은 하기를 포함하는 분해 공정에 의해 수득되는 방법:
(I-A) 1-페닐-1-사이클로헥산-하이드로퍼옥사이드 및 사이클로헥실벤젠을 포함하는 분해 공급물 혼합물을 분해 반응기에서의 산 촉매와 접촉시켜 분해 반응 생성물을 수득하는 단계.
E44. E43에 있어서, 단계 (I-A)에서, 산은 액체 산이고, 분해 공정은 하기 단계를 더 포함하는 방법:
(I-B) 염기성 물질을 분해 반응 생성물로 부가하여 제1 혼합물을 수득하는 단계.
E45. E44에 있어서, 염기성 물질은 유기 아민을 포함하는 방법.
E46. E43 내지 E45 중 어느 하나에 있어서, 분해 공급물 혼합물은 하기 단계에 의해 수득되는 방법:
(I-A-1) 하이드로알킬화 조건으로 하이드로알킬화 촉매의 존재 하에 벤젠을 수소와 접촉시켜 사이클로헥실벤젠을 포함하는 하이드로알킬화 생성물 혼합물을 생성하는 단계;
(I-A-2) 촉매의 존재 하에 사이클로헥실벤젠을 산소와 접촉시켜, 1-페닐-1-사이클로헥산-하이드로퍼옥사이드를 포함하는 산화 반응 생성물 혼합물을 생성하는 단계; 및
(I-A-3) 산화 반응 생성물 혼합물로부터의 분해 공급물 혼합물을 제공하는 단계.
E47. E1 내지 E46 중 어느 하나에 있어서, 하기 단계를 더 포함하는 방법:
(VII) 적어도 일부의 제1 하부 유출물을 제3 증류 컬럼으로 공급하는 단계; 및
(VIII) 제3 증류 컬럼으로부터,
Cchb(UE3)의 농도의 사이클로헥실벤젠을 포함하는 제3 상부 유출물; 및
사이클로헥실벤젠보다 높은 비점을 갖는 성분을 포함하는 제3 하부 유출물
을 수득하는 단계.
E48. E47에 있어서, 제3 상부 유출물의 총 중량 기준으로 Cchb(UE3) ≥ C31 wt%이고, 상기 C31은 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99일 수 있는 방법.
E49. E47 또는 E48에 있어서, 제3 상부 유출물은 제3 상부 유출물의 총 중량 기준으로 C12 중량ppm 이하의 농도의 페놀을 포함하고, 상기 C12는 1000, 800, 600, 500, 400, 200, 100, 80, 60, 50, 40, 20, 10, 8, 6, 5, 4, 2, 1일 수 있는 방법.
E50. E47 내지 E49 중 어느 하나에 있어서, 적어도 일부의 제3 상부 유출물은 단계 (I-A-2)로 재순환되는 방법.
EA1. 사이클로헥사논을 제조하기 위해 E1 내지 E5 중 어느 하나의 방법을 실시하기 위해 구성된 시스템으로서,
(A) (i) Cxnone(FM1)의 농도의 사이클로헥사논, Cphol(FM1)의 농도의 페놀, 및 Cchb(FM1)의 농도의 사이클로헥실벤젠을 포함하는 제1 혼합물을 공급받고; 및
(ii) Cxnone(UE1)의 농도의 사이클로헥사논, Cphol(UE1)의 농도의 페놀 및 Cchb(UE1)의 농도의 사이클로헥실벤젠을 포함하는 제1 상부 유출물;
Cxnone(ME1)의 농도의 사이클로헥사논, Cphol(ME1)의 농도의 페놀, 및 Cchb(ME1)의 농도의 사이클로헥실벤젠, 및 Cbch(ME1)의 농도의 비사이클로헥산을 포함하는 제1 중간 유출물; 및
Cchb(LE1)의 농도의 사이클로헥실벤젠을 포함하는 제1 하부 유출물
을 생성하도록 구성된 제1 증류 컬럼으로서,
여기서,
Cxnone(UE1) > Cxnone(FM1);
Cphol(ME1) > Cphol(FM1); 및
Cchb(LE1) > Cchb(FM1)인 제1 증류 컬럼;
(B) 적어도 일부의 제1 중간 유출물 및 수소를 공급받도록 구성된 수소화 반응 구간으로서, 여기서 페놀은 수소화 조건으로 수소화 촉매의 존재 하에 수소와 반응하여, Cxnone(HRP)의 농도의 사이클로헥사논, Cphol(HRP)의 농도의 페놀, Cchb(HRP)의 농도의 사이클로헥실벤젠, 및 Cbch(HRP)의 농도의 비사이클로헥산을 포함하는 수소화 반응 생성물을 생성하며, 여기서,
Cxnone(HRP) > Cxnone(ME1); 및
Cphol(HRP) < Cphol(ME1)인 수소화 반응 구간; 및
(C) 적어도 일부의 수소화 반응 생성물을 제1 증류 컬럼으로 전달하도록 구성된 제1 유체 연통체
를 포함하는 시스템.
EA2. EA1에 있어서, (D) (i) 적어도 일부의 제1 상부 유출물을 공급받고; 그리고 (ii) 하기의 것을 생성하도록 구성된 제2 증류 컬럼을 더 포함하는 시스템:
Cxnone(UE2)의 농도의 사이클로헥사논을 포함하는 제2 상부 유출물; 및
Cxnone(LE2)의 농도의 사이클로헥사논 및 Cxnol(LE2)의 농도의 사이클로헥사놀을 포함하는 제2 하부 유출물; 여기서
Cxnone(UE2) > Cxnone(UE1) > Cxnone(LE2); 및
Cxnol(LE2) > Cxnol(UE1)임.
EA3. EA2에 있어서, 제2 증류 컬럼은 추가로 제2 상부 유출물보다 높은 위치에서 사이클로헥사논의 것보다 낮은 기준 비점을 갖는 성분을 포함하는 제3 상부 유출물을 생성하도록 구성된 시스템.
EA4. EA1 내지 EA3 중 어느 하나에 있어서, 수소화 반응 구간은 추가로 제1 중간 유출물과는 별개의 제2 페놀-함유 스트림을 공급받도록 구성된 시스템.
EA5. EA1 내지 EA4 중 어느 하나에 있어서, 수소화 반응 구간은 연속하여 연결된 복수개의 수소화 반응기를 포함하는 시스템.
EA6. EA1 내지 EA5 중 어느 하나에 있어서,
(E) 적어도 일부의 수소화 반응 생성물을 공급받고, 공급받은 수소화 반응 생성물을 액체 스트림 및 증기 스트림으로 분리하도록 구성된 분리 드럼; 및
(F) 적어도 일부의 증기 스트림을 수소화 반응 구간으로 전달하도록 구성된 제2 유체 연통체
를 더 포함하고,
제1 유체 연통체는 적어도 일부의 액체 스트림을 제1 증류 컬럼으로 전달하는 시스템.
EA7. EA6에 있어서, 제1 증류 컬럼은 제1 증류 컬럼의 실질적으로 동일한 수준으로 액체 스트림 및 제1 혼합물을 공급받도록 구성되는 것인 시스템.
EA8. EA6 또는 EA7에 있어서, 제1 증류 컬럼은 제1 증류 컬럼의 동일한 위치에서 액체 스트림 및 제1 혼합물을 공급받도록 구성되는 것인 시스템.
EA9. EA1 내지 EA8 중 어느 하나에 있어서, 제1 유체 연통체는 수소화 반응 생성물이 복수개의 스트림으로 분리되고;
복수개의 스트림 중 하나 이상이 제1 중간 유출물이 인출되는 위치보다 높은 위치에서 제1 증류 컬럼으로 전달되고; 및
복수개의 스트림 중 하나 이상이 제1 중간 유출물이 인출되는 위치보다 낮은 위치에서 제1 증류 컬럼으로 공급되도록 구성되는 시스템.
EA10. EA1 내지 EA9 중 어느 하나에 있어서, 하기를 더 포함하는 것인 시스템:
(A-1) (i) 산 촉매 및 1-페닐-1-사이클로헥산-하이드로퍼옥사이드 및 사이클로헥실벤젠을 포함하는 분해 공급물을 공급받고, 그리고 (ii) 페놀, 사이클로헥사논, 및 사이클로헥실벤젠을 포함하는 분해 반응 생성물을 생성하도록 구성되는 분해 반응기; 및
(A-2) 제1 혼합물의 전구체 또는 제1 혼합물로서 적어도 일부의 분해 반응 생성물을 제1 증류 컬럼에 전달하도록 구성된 제3 유체 연통체.
EA11. EA10에 있어서, 산 촉매는 액체 산이고, 하기를 더 포함하는 것인 시스템:
(A-3) 염기성 물질을 분해 반응 생성물로 부가하여 제1 혼합물을 수득하도록 구성된 장치.
EA12. EA10 또는 EA11에 있어서, 하기를 더 포함하는 시스템:
(A-1a) 벤젠 및 수소를 공급받아 사이클로헥실벤젠을 포함하는 하이드로알킬화 생성물 혼합물을 생성하도록 구성된 하이드로알킬화 반응기;
(A-1b) 하이드로알킬화 생성물 혼합물로부터 적어도 일부의 사이클로헥실벤젠을 공급받아, 1-페닐-1-사이클로헥산-하이드로퍼옥사이드 및 사이클로헥실벤젠을 포함하는 산화 반응 혼합물을 생성하도록 구성된 산화 반응기; 및
(A-1c) 분해 공급물로서 적어도 일부의 산화 반응 혼합물을 분해 반응기로 전달하도록 구성된 제4 유체 연통체.
EA13. EA1 내지 EA12 중 어느 하나에 있어서, 하기를 더 포함하는 시스템:
(G) (i) 적어도 일부의 제1 하부 유출물을 공급받고; 그리고
(ii) Cchb(UE3)의 농도의 사이클로헥실벤젠을 포함하는 제3 상부 유출물; 및
사이클로헥실벤젠보다 높은 비점을 갖는 성분을 포함하는 제3 하부 유출물을 생성하도록 구성된 제3 증류 컬럼.
EA14. EA13에 있어서, 하기를 더 포함하는 시스템:
(H) 적어도 일부의 제3 상부 유출물을 산화 반응기로 전달하도록 구성된 제5 유체 연통체.
Claims (24)
- 사이클로헥사논의 제조 방법으로서,
(I) 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 제1 혼합물을 제1 증류 컬럼으로 공급하는 단계;
(II) 제 증류 컬럼으로부터,
제1 혼합물보다 높은 농도의 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 제1 상부 유출물;
사이클로헥사논, 제1 혼합물보다 높은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 제1 중간 유출물; 및
제1 혼합물보다 높은 농도의 사이클로헥실벤젠을 포함하는 제1 하부 유출물
을 수득하는 단계;
(III) 적어도 일부의 제1 중간 유출물 및 수소를 수소화 반응 구간으로 공급하는 단계로서, 여기서 페놀은 수소화 반응 조건으로 수소화 촉매의 존재 하에 수소와 반응하여, 제1 중간 유출물보다 높은 농도의 사이클로헥사논, 제1 중간 유출물보다 낮은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 수소화 반응 생성물을 수득하는 단계; 및
(IV) 적어도 일부의 수소화 반응 생성물을 제1 증류 컬럼으로 공급하는 단계
를 포함하는 사이클로헥사논의 제조 방법. - 제1항에 있어서, 하기 (i) 내지 (iii)의 조건 중 하나 이상이 충족되며, 하기 백분율은 제1 혼합물의 총 중량에 기초하는 것인 제조 방법:
(i) 제1 혼합물은 10 wt% 내지 90 wt%의 범위의 농도의 사이클로헥사논을 포함함;
(ii) 제1 혼합물은 10 wt% 내지 80 wt%의 범위의 농도의 페놀을 포함함; 및
(iii) 제1 혼합물은 0.001 wt% 내지 75 wt%의 범위의 농도의 사이클로헥실벤젠을 포함함. - 제1항 또는 제2항에 있어서, 제1 상부 유출물은 사이클로헥사놀을 더 포함하며, 상기 방법은,
(V) 적어도 일부의 제1 상부 유출물을 제2 증류 컬럼으로 공급하는 단계; 및
(VI) 제2 증류 컬럼으로부터,
제1 상부 유출물보다 높은 농도의 사이클로헥사논을 포함하는 제2 상부 유출물;
제2 상부 유출물 위의 위치에서의 제3 상부 유출물으로서, 사이클로헥사논의 것보다 더 낮은 기준 비점을 갖는 성분을 포함하는 제3 상부 유출물; 및
제1 상부 유출물보다 더 낮은 농도의 사이클로헥사논, 및 제1 상부 유출물보다 높은 농도의 사이클로헥사놀을 포함하는 제2 하부 유출물
을 수득하는 단계
를 더 포함하는 제조 방법. - 제3항에 있어서, 제2 상부 유출물은 제2 상부 유출물의 총 중량 기준으로 95 wt% 이상의 농도의 사이클로헥사논을 포함하는 제조 방법.
- 제3항 또는 제4항에 있어서, 제2 하부 유출물은 제2 하부 유출물의 총 중량 기준으로 10 wt% 내지 80 wt%의 범위의 농도의 사이클로헥사놀을 포함하는 제조 방법.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 하기 (i) 내지 (iv)의 조건 중 하나 이상이 충족되는 제조 방법:
(i) 제1 중간 유출물은 1 wt% 내지 50 wt%의 범위의 농도의 사이클로헥사논을 포함함;
(ii) 제1 중간 유출물은 10 wt% 내지 80 wt%의 범위의 농도의 페놀을 포함함;
(iii) 제1 중간 유출물은 0.001 wt% 내지 30 wt%의 범위의 농도의 사이클로헥실벤젠을 포함함; 및
(iv) 제1 중간 유출물은 0.001 wt% 내지 30 wt%의 범위의 농도의 비사이클로헥산을 포함함. - 제1항 내지 제6항 중 어느 한 항에 있어서, 제1 중간 유출물과는 별도의 제2 페놀-함유 스트림이 수소화 반응 구간으로 공급되고, 제2 페놀-함유 스트림은 제2 페놀-함유 스트림의 총 중량 기준으로 50 wt% 내지 100 wt%의 범위의 농도의 페놀을 포함하는 제조 방법.
- 제1항 내지 제7항 중 어느 한 항에 있어서, 수소 및 페놀은 1.0 내지 10의 범위의 수소 대 페놀 몰비로 수소화 반응 구간에 공급되는 제조 방법.
- 제1항 내지 제8항 중 어느 한 항에 있어서, 수소화 반응 구간에서, (i) 사이클로헥실벤젠의 50% 이상이 액상으로 존재하고; 및/또는 (ii) 페놀의 50% 이상이 액상으로 존재하는 것인 제조 방법.
- 제9항에 있어서, 수소화 반응 구간에서, 수소화 조건은 140℃ 내지 300℃의 범위의 온도 및 375 kPa 내지 1200 kPa의 범위의 절대 압력을 포함하는 제조 방법.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 수소화 반응 구간에서, (i) 존재하는 사이클로헥실벤젠의 90% 이상은 증기상으로 존재하고; 및/또는 (ii) 존재하는 페놀의 90% 이상은 증기상으로 존재하는 것인 제조 방법.
- 제11항에 있어서, 수소화 반응 구간에서, 수소화 반응 조건은 140℃ 내지 300℃의 범위의 온도 및 100 kPa 내지 400 kPa의 범위의 절대 압력을 포함하는 제조 방법.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 하기 (i) 내지 (iv)의 조건 중 하나 이상이 충족되며, 하기 백분율은 수소화 반응 생성물의 총 중량에 기초하는 것인 제조 방법:
(i) 수소화 반응 생성물은 20 wt% 내지 90 wt%의 범위의 농도의 사이클로헥사논을 포함함;
(ii) 수소화 반응 생성물은 1 wt% 내지 50 wt%의 범위의 농도의 페놀을 포함함;
(iii) 수소화 반응 생성물은 0.001 wt% 내지 30 wt%의 범위의 농도의 사이클로헥실벤젠을 포함함; 및
(iv) 수소화 반응 생성물은 0.001 wt% 내지 30 wt%의 범위의 농도의 비사이클로헥산을 포함함. - 제1항 내지 제13항 중 어느 한 항에 있어서, 수소화 반응 생성물은 수소화 반응 생성물의 총 중량 기준으로 0.01 wt% 내지 10 wt%의 범위의 농도의 사이클로헥사놀을 더 포함하는 제조 방법.
- 제1항 내지 제14항 중 어느 한 항에 있어서, 하기 (i) 내지 (iii)의 조건 중 하나 이상이 충족되며, 하기 농도는 각각 수소화 반응 생성물의 총 중량 또는 제1 중간 유출물의 총 중량에 기초하는 중량 백분율인 것인 제조 방법:
(i) 제1 중간 유출물에서의 사이클로헥실벤젠의 농도 대 수소화 반응 생성물에서의 사이클로헥실벤젠의 농도의 비는 0.10 내지 10의 범위임;
(ii) 수소화 반응 생성물에서의 비사이클로헥산의 농도 대 제1 중간 유출물에서의 비사이클로헥산의 농도의 비는 0.10 내지 10의 범위임; 및
(iii) 수소화 반응 생성물에서의 사이클로헥사놀의 농도 대 제1 중간 유출물에서의 사이클로헥사놀의 농도의 비는 0.10 내지 10임. - 제1항 내지 제15항 중 어느 한 항에 있어서, 단계 (III) 이후,
(IIIA) 수소화 반응 생성물을 액체 스트림 및 증기 스트림으로 분리하는 단계; 및
(IIIB) 적어도 일부의 증기 스트림을 수소화 반응 구간으로 재순환시키는 단계
를 더 포함하며,
단계 (IV)는 적어도 일부의 액체 스트림을 제1 증류 컬럼으로 공급하는 것을 포함하는 제조 방법. - 제1항 내지 제16항 중 어느 한 항에 있어서, 수소화 반응 생성물은 복수개의 스트림으로 분리되고;
복수개의 스트림 중 하나 이상은 제1 중간 유출물이 인출되는 위치보다 높은 위치에서 제1 증류 컬럼으로 공급되고; 및
복수개의 스트림 중 하나 이상은 제1 중간 유출물이 인출되는 위치보다 낮은 위치에서 제1 증류 컬럼으로 공급되는 제조 방법. - 제1항 내지 제17항 중 어느 한 항에 있어서, 단계 (I)에서의 제1 혼합물은 하기 단계를 포함하는 분해 공정에 의해 수득되는 것인 제조 방법:
(I-A) 분해 반응기에서 1-페닐-1-사이클로헥산-하이드로퍼옥사이드 및 사이클로헥실벤젠을 포함하는 분해 공급물 혼합물을 산 촉매와 접촉시켜 분해 반응 생성물을 수득하는 단계. - 제18항에 있어서, 단계 (I-A)에서, 산은 액체 산이고, 분해 공정은 하기 단계를 더 포함하는 것인 제조 방법:
(I-B) 염기성 물질을 분해 반응 생성물에 부가하여 제1 혼합물을 수득하는 단계. - 제19항에 있어서, 분해 공급물 혼합물이,
(I-A-1) 하이드로알킬화 조건으로 하이드로알킬화 촉매의 존재 하에 벤젠을 수소와 접촉시켜, 사이클로헥실벤젠을 포함하는 하이드로알킬화 생성물 혼합물을 생성하는 단계;
(I-A-2) 촉매의 존재 하에 사이클로헥실벤젠을 산소와 접촉시켜, 1-페닐-1-사이클로헥산-하이드로퍼옥사이드를 포함하는 산화 반응 생성물 혼합물을 생성하는 단계; 및
(I-A-3) 산화 반응 생성물 혼합물로부터의 분해 공급물 혼합물을 제공하는 단계
에 의해 수득되는 것인 제조 방법. - 제1항 내지 제20항 중 어느 한 항에 있어서,
(VII) 적어도 일부의 제1 하부 유출물을 제3 증류 컬럼으로 공급하는 단계; 및
(VIII) 제3 증류 컬럼으로부터,
사이클로헥실벤젠을 포함하는 제3 상부 유출물; 및
사이클로헥실벤젠보다 높은 비점을 갖는 성분을 포함하는 제3 하부 유출물
을 수득하는 단계
를 더 포함하는 제조 방법. - 제21항에 있어서, 제3 상부 유출물은 제3 상부 유출물의 총 중량 기준으로 90% 이상의 농도의 사이클로헥실벤젠을 포함하는 것인 제조 방법.
- 제21항 또는 제22항에 있어서, 적어도 일부의 제3 상부 유출물이 단계 (I-A-2)로 재순환되는 것인 제조 방법.
- 사이클로헥사논을 제조하기 위해 구성된 시스템으로서,
(A) (i) 사이클로헥사논, 페놀, 및 사이클로헥실벤젠을 포함하는 제1 혼합물을 공급받고; 및
(ii) 제1 혼합물보다 높은 농도의 사이클로헥사논을 포함하는 제1 상부 유출물;
사이클로헥사논, 제1 혼합물보다 높은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 제1 중간 유출물; 및
제1 혼합물보다 높은 농도의 사이클로헥실벤젠을 포함하는 제1 하부 유출물
을 제조하도록 구성된 제1 증류 컬럼;
(B) 적어도 일부의 제1 중간 유출물 및 수소를 공급받도록 구성된 수소화 반응 구간으로서, 여기서 페놀은 수소화 조건으로 수소화 촉매의 존재 하에 수소와 반응하여, 제1 중간 유출물보다 높은 농도의 사이클로헥사논, 제1 중간 유출물보다 낮은 농도의 페놀, 사이클로헥실벤젠, 및 비사이클로헥산을 포함하는 수소화 반응 생성물을 생성하는 수소화 반응 구간; 및
(C) 적어도 일부의 수소화 반응 생성물을 제1 증류 컬럼으로 전달하도록 구성된 제1 유체 연통체
를 포함하는 시스템.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462037794P | 2014-08-15 | 2014-08-15 | |
| US62/037,794 | 2014-08-15 | ||
| EP14188588 | 2014-10-13 | ||
| EP14188588.9 | 2014-10-13 | ||
| PCT/US2015/043475 WO2016025213A1 (en) | 2014-08-15 | 2015-08-03 | Process and system for making cyclohexanone |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170027808A true KR20170027808A (ko) | 2017-03-10 |
Family
ID=51844495
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177002642A KR20170027808A (ko) | 2014-08-15 | 2015-08-03 | 사이클로헥사논의 제조를 위한 방법 및 시스템 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US9926254B2 (ko) |
| EP (1) | EP3180303B1 (ko) |
| JP (1) | JP2017523199A (ko) |
| KR (1) | KR20170027808A (ko) |
| CN (1) | CN105367397B (ko) |
| SG (1) | SG11201700197XA (ko) |
| TW (1) | TWI593670B (ko) |
| WO (1) | WO2016025213A1 (ko) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9938220B2 (en) | 2014-08-15 | 2018-04-10 | Exxonmobil Chemical Patents Inc. | Process and system for making cyclohexanone |
| US9938219B2 (en) | 2014-08-15 | 2018-04-10 | Exxonmobil Chemical Patents Inc. | Process and system for making cyclohexanone |
| EP3180305A1 (en) | 2014-08-15 | 2017-06-21 | ExxonMobil Chemical Patents Inc. | Process and system for making cyclohexanone |
| KR20170031726A (ko) | 2014-08-15 | 2017-03-21 | 엑손모빌 케미칼 패턴츠 인코포레이티드 | 사이클로헥사논의 제조를 위한 방법 |
| WO2016053583A1 (en) | 2014-09-30 | 2016-04-07 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| US10233140B2 (en) * | 2014-09-30 | 2019-03-19 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| US20180186715A1 (en) | 2015-07-29 | 2018-07-05 | Exxonmobil Chemical Patents Inc. | Cyclohexanone Compositions and Processes for Making Such Compositions |
| WO2017023429A1 (en) | 2015-07-31 | 2017-02-09 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| US10259765B2 (en) | 2015-07-31 | 2019-04-16 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| BR112018013811A2 (pt) | 2016-01-06 | 2018-12-11 | Ecolab Usa Inc. | ?composição, método, e, uso de um concentrado de inibidor de parafina? |
| WO2017120287A1 (en) | 2016-01-06 | 2017-07-13 | Ecolab Usa Inc. | Temperature-stable paraffin inhibitor compositions |
| RU2742444C2 (ru) * | 2016-04-07 | 2021-02-05 | ЭКОЛАБ ЮЭсЭй ИНК. | Термостабильные композиции ингибиторов парафиноотложения |
| US10858575B2 (en) | 2017-06-02 | 2020-12-08 | Championx Usa Inc. | Temperature-stable corrosion inhibitor compositions and methods of use |
| WO2019005274A1 (en) * | 2017-06-28 | 2019-01-03 | Exxonmobil Chemical Patents Inc. | PROCESS FOR PRODUCTION OF CYCLOHEXANONE |
| US10941099B2 (en) | 2017-06-28 | 2021-03-09 | Exxonmobil Chemical Patents Inc. | Cyclohexanone-containing products and processes for making the same |
| WO2019005276A1 (en) * | 2017-06-28 | 2019-01-03 | Exxonmobil Chemical Patents Inc. | PRODUCTS CONTAINING CYCLOHEXANONE AND METHODS OF MAKING THE SAME |
Family Cites Families (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4169857A (en) * | 1978-10-05 | 1979-10-02 | Phillips Petroleum Company | Separation of cyclohexylbenzene-cyclohexanone-phenol-containing mixtures by hydrogenation and distillation |
| DE3117135A1 (de) | 1981-04-30 | 1982-11-18 | Bayer Ag, 5090 Leverkusen | Kristallines alumosilicat, verfahren zu dessen herstellung sowie dessen verwendung zur katalytischen umwandlung von methanol und/oder dimethylether in kohlenwasserstoffe |
| DD218092A1 (de) | 1983-09-30 | 1985-01-30 | Leuna Werke Veb | Verfahren zur herstellung von cyclohexanon und cyclohexanol |
| US4826667A (en) | 1986-01-29 | 1989-05-02 | Chevron Research Company | Zeolite SSZ-25 |
| US5233095A (en) | 1986-03-18 | 1993-08-03 | Catalytica, Inc. | Process for manufacture of resorcinol |
| US4954325A (en) | 1986-07-29 | 1990-09-04 | Mobil Oil Corp. | Composition of synthetic porous crystalline material, its synthesis and use |
| IT1205681B (it) | 1987-05-26 | 1989-03-31 | Eniricerche Spa | Materiale sintetico cristallino poroso contenente ossidi di silicio e boro |
| US5250277A (en) | 1991-01-11 | 1993-10-05 | Mobil Oil Corp. | Crystalline oxide material |
| US5236575A (en) | 1991-06-19 | 1993-08-17 | Mobil Oil Corp. | Synthetic porous crystalline mcm-49, its synthesis and use |
| US5362697A (en) | 1993-04-26 | 1994-11-08 | Mobil Oil Corp. | Synthetic layered MCM-56, its synthesis and use |
| ES2124154B1 (es) | 1995-11-08 | 1999-12-01 | Univ Politecnica De Valencia C | Metodo de preparaciion y propiedades cataliticas de un solido microporoso con alta superficie externa. |
| ES2105982B1 (es) | 1995-11-23 | 1998-07-01 | Consejo Superior Investigacion | Zeolita itq-1 |
| US8222459B2 (en) | 1997-06-13 | 2012-07-17 | Exxonmobil Chemical Patents Inc. | Process for producing cyclohexanone |
| US6037513A (en) | 1998-07-09 | 2000-03-14 | Mobil Oil Corporation | Hydroalkylation of aromatic hydrocarbons |
| US6049018A (en) | 1999-01-21 | 2000-04-11 | Mobil Corporation | Synthetic porous crystalline MCM-68, its synthesis and use |
| US6756030B1 (en) | 2003-03-21 | 2004-06-29 | Uop Llc | Crystalline aluminosilicate zeolitic composition: UZM-8 |
| WO2009025939A2 (en) | 2007-08-22 | 2009-02-26 | Exxonmobil Chemical Patents Inc. | Oxidation of hydrocarbons |
| WO2009058531A1 (en) | 2007-10-31 | 2009-05-07 | Exxonmobil Chemical Patents Inc. | Oxidation of hydrocarbons |
| US8658839B2 (en) | 2007-10-31 | 2014-02-25 | Exxonmobil Chemical Patents Inc. | Oxidation of hydrocarbons |
| EA016277B1 (ru) | 2007-12-20 | 2012-03-30 | ДСМ АйПи АССЕТС Б.В. | Способ получения циклогексанона с многократной постдистилляцией |
| CN101945845B (zh) | 2007-12-20 | 2013-09-18 | 帝斯曼知识产权资产管理有限公司 | 具有经改进的后蒸馏的环己酮生产方法 |
| JP2011506545A (ja) | 2007-12-20 | 2011-03-03 | ディーエスエム アイピー アセッツ ビー.ブイ. | 不純物の除去を伴うシクロヘキサノン生産プロセス |
| EP2297071B1 (en) | 2008-04-14 | 2016-03-30 | ExxonMobil Chemical Patents Inc. | Process for producing cyclohexylbenzene |
| JP5444327B2 (ja) | 2008-04-25 | 2014-03-19 | エクソンモービル・ケミカル・パテンツ・インク | フェノール及び/又はシクロヘキサノンの製造方法 |
| EP2303822A1 (en) | 2008-05-01 | 2011-04-06 | ExxonMobil Chemical Patents Inc. | Process for producing cyclohexanone |
| US7579511B1 (en) | 2008-10-10 | 2009-08-25 | Exxonmobil Research And Engineering Company | Process for making cyclohexylbenzene |
| US8884067B2 (en) | 2009-02-26 | 2014-11-11 | Exxonmobil Chemical Patents Inc. | Phenol and cyclohexanone mixtures |
| IT1395594B1 (it) | 2009-06-29 | 2012-10-16 | Polimeri Europa Spa | Processo per la preparazione di fenolo e cicloesanone |
| CN102695693A (zh) * | 2010-02-05 | 2012-09-26 | 埃克森美孚化学专利公司 | 脱氢方法 |
| US9242227B2 (en) * | 2010-02-05 | 2016-01-26 | Exxonmobil Chemical Patents Inc. | Dehydrogenation catalyst and process |
| US8658834B2 (en) | 2010-02-12 | 2014-02-25 | Exxonmobil Chemical Patents Inc. | Hydrogenation process |
| EP2616414A1 (en) | 2010-09-14 | 2013-07-24 | ExxonMobil Chemical Patents Inc. | Cyclohexylbenzene compositions |
| WO2012036819A1 (en) * | 2010-09-14 | 2012-03-22 | Exxonmobil Chemical Patents Inc. | Dehydrogenation process of cyclohexanone and phenol compositions |
| KR101748068B1 (ko) | 2010-09-14 | 2017-06-15 | 엑손모빌 케미칼 패턴츠 인코포레이티드 | 페놀의 제조 방법 |
| WO2013165659A1 (en) | 2012-05-02 | 2013-11-07 | Exxonmobil Chemical Patents Inc. | Process for producing phenol and cyclohexanone |
| CN104284876B (zh) | 2012-05-02 | 2017-03-08 | 埃克森美孚化学专利公司 | 用于分离包含苯酚和环己酮的混合物的方法 |
| EP2895454B1 (en) | 2012-09-14 | 2016-11-30 | ExxonMobil Chemical Patents Inc. | Process for separating methylcyclopentanone from cyclohexanone |
| CN104640827B (zh) | 2012-09-17 | 2016-11-09 | 埃克森美孚化学专利公司 | 由环己基苯生产苯酚和/或环己酮的方法 |
| US9475745B2 (en) | 2012-11-21 | 2016-10-25 | Exxonmobil Chemical Patents Inc. | Process for producing phenol |
| EP2964355B1 (en) | 2013-03-04 | 2017-03-22 | ExxonMobil Chemical Patents Inc. | System and process for making phenol and/or cyclohexanone |
| WO2014137623A1 (en) | 2013-03-04 | 2014-09-12 | Exxonmobil Chemical Patents Inc. | System and process for making phenol and/or cyclohexanone |
| US9938219B2 (en) | 2014-08-15 | 2018-04-10 | Exxonmobil Chemical Patents Inc. | Process and system for making cyclohexanone |
| US9938220B2 (en) | 2014-08-15 | 2018-04-10 | Exxonmobil Chemical Patents Inc. | Process and system for making cyclohexanone |
| KR20170031726A (ko) | 2014-08-15 | 2017-03-21 | 엑손모빌 케미칼 패턴츠 인코포레이티드 | 사이클로헥사논의 제조를 위한 방법 |
| EP3180305A1 (en) | 2014-08-15 | 2017-06-21 | ExxonMobil Chemical Patents Inc. | Process and system for making cyclohexanone |
| WO2016053583A1 (en) | 2014-09-30 | 2016-04-07 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| US10233140B2 (en) | 2014-09-30 | 2019-03-19 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| US20180186715A1 (en) | 2015-07-29 | 2018-07-05 | Exxonmobil Chemical Patents Inc. | Cyclohexanone Compositions and Processes for Making Such Compositions |
| US10259765B2 (en) | 2015-07-31 | 2019-04-16 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
| WO2017023429A1 (en) | 2015-07-31 | 2017-02-09 | Exxonmobil Chemical Patents Inc. | Process for making cyclohexanone |
-
2015
- 2015-08-03 WO PCT/US2015/043475 patent/WO2016025213A1/en active Application Filing
- 2015-08-03 SG SG11201700197XA patent/SG11201700197XA/en unknown
- 2015-08-03 JP JP2017505441A patent/JP2017523199A/ja active Pending
- 2015-08-03 US US15/319,827 patent/US9926254B2/en not_active Expired - Fee Related
- 2015-08-03 KR KR1020177002642A patent/KR20170027808A/ko active Search and Examination
- 2015-08-03 EP EP15749932.8A patent/EP3180303B1/en not_active Not-in-force
- 2015-08-04 TW TW104125221A patent/TWI593670B/zh not_active IP Right Cessation
- 2015-08-14 CN CN201510500257.8A patent/CN105367397B/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017523199A (ja) | 2017-08-17 |
| EP3180303A1 (en) | 2017-06-21 |
| CN105367397B (zh) | 2017-07-21 |
| WO2016025213A1 (en) | 2016-02-18 |
| TW201619111A (zh) | 2016-06-01 |
| US20170152201A1 (en) | 2017-06-01 |
| SG11201700197XA (en) | 2017-02-27 |
| EP3180303B1 (en) | 2018-07-18 |
| US9926254B2 (en) | 2018-03-27 |
| TWI593670B (zh) | 2017-08-01 |
| CN105367397A (zh) | 2016-03-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9926254B2 (en) | Process and system for making cyclohexanone | |
| TWI583663B (zh) | 製造環己酮之方法 | |
| TWI588125B (zh) | 環己酮之製法 | |
| EP3180302B1 (en) | Process for producing cyclohexanone | |
| EP3180304B1 (en) | Process for producing cyclohexanone | |
| TWI583665B (zh) | 製造環己酮之方法 | |
| TWI596085B (zh) | 製造環己酮之方法及系統 | |
| KR101745228B1 (ko) | 사이클로헥실벤젠을 제조하기 위한 시스템 및 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination |