KR20160078986A - 대상체의 기도로 효소를 투여하기 위한 조성물 및 방법 - Google Patents
대상체의 기도로 효소를 투여하기 위한 조성물 및 방법 Download PDFInfo
- Publication number
- KR20160078986A KR20160078986A KR1020167012122A KR20167012122A KR20160078986A KR 20160078986 A KR20160078986 A KR 20160078986A KR 1020167012122 A KR1020167012122 A KR 1020167012122A KR 20167012122 A KR20167012122 A KR 20167012122A KR 20160078986 A KR20160078986 A KR 20160078986A
- Authority
- KR
- South Korea
- Prior art keywords
- composition
- plasminogen activator
- solution
- subject
- scupa
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/48—Hydrolases (3) acting on peptide bonds (3.4)
- A61K38/49—Urokinase; Tissue plasminogen activator
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/0078—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy for inhalation via a nebulizer such as a jet nebulizer, ultrasonic nebulizer, e.g. in the form of aqueous drug solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/008—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy comprising drug dissolved or suspended in liquid propellant for inhalation via a pressurized metered dose inhaler [MDI]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y304/00—Hydrolases acting on peptide bonds, i.e. peptidases (3.4)
- C12Y304/21—Serine endopeptidases (3.4.21)
- C12Y304/21068—Tissue plasminogen activator (3.4.21.68), i.e. tPA
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/12—Aerosols; Foams
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y304/00—Hydrolases acting on peptide bonds, i.e. peptidases (3.4)
- C12Y304/21—Serine endopeptidases (3.4.21)
- C12Y304/21073—Serine endopeptidases (3.4.21) u-Plasminogen activator (3.4.21.73), i.e. urokinase
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Otolaryngology (AREA)
- Immunology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Biomedical Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
Abstract
대상체의 기도로 효소를 전달하기 위한 방법 및 조성물. 일부 측면에서, 효소, 예컨대 플라스미노겐 활성제를 포함하는 분무화된 조성물이 제공된다. 추가 측면에서 효소, 예컨대 플라스미노겐 활성제를 포함하는 퍼플루오로탄소 조성물이 제공된다. 조성물은, 일부 측면에서, 폐 감염 또는 급성 폐손상, 예컨대 흡입 연기로 유도된 급성 폐손상(ISALI)의 치료에 사용될 수 있다.
Description
본원은 미국 가특허 출원번호 61/899,739(2013년 11월 4일 출원)의 이점을 주장하며, 이것의 전체가 본원에 참고로 편입되었다.
1. 발명의 분야
본 발명은 일반적으로 분자생물학, 약물 전달 및 의약 분야에 관한 것이다. 더 상세하게는, 대상체의 호흡 계통에 치료적 효소 조성물을 전달하기 위한 조성물 및 방법에 관한 것이다.
2. 관련 기술의 설명
중증 화상을 입고 연기에 노출된 많은 환자들에게서 중증 형태의 ALI(급성폐손상), 소위 급성 호흡기 곤란증후군(ARDS)이 발병하는데, 이것은 30~40%의 사망률, 장기 입원 및 장기적 이환율과 관련이 있다. 흡입 연기(IS)로 유도된 ALI(ISALI)는 중증 기도폐색, 섬유성 기도 원주(casts) 또는 잔해, 및 폐포 피브린 침착을 특징으로 한다. 효과적이고 특이적인 ISALI 치료가 현재 부족한 상태이다.
화상은 연간 미국에서 1백만이 넘는 환자에게서 발생하고, ISALI는 민간 및 군사 부분에서 연간 수천의 연기-노출 환자에게서 발병한다(Enkhbaatar 등, 2004a). ISALI는 미국에서 연간 3000건 이상의 사망 및 17,000건의 화재-관련 손상에 기여하고, 인구 100,000명당 2~3명이라는 화재 관련 사망률에 기여하는데, 이것은 선진국에서 최고 수치 중 하나이다[Committee on injury and poison prevention (2000) Pediatrics 105:1355-1357]. 지지요법(supportive therapy)은 차선이고, 장기적이며 비싸다. 그 결과 유의미한 사망률 및 이환율을 초래한다. 기계적 환기를 비롯한 현 지지요법에도 불구하고, ISALI와 관련된 것을 비롯한 ARDS의 사망률은 30~40 퍼센트에 달한다(Phua 등,2009).
이와 같은 고려사항들 때문에, 새롭고 잠재적으로 더 효과적인 요법의 실험이 요구된다. ISALI는 중증 호흡기 손상, 장기 입원, 그리고 종종 기계적 환기의 필요성과 관련된다. ISALI의 장기적 합병증에는 기관지 반응성, 가속화된 폐섬유증 및 기관지 확장증이 포함된다. 모든 형태의 ALI 중에서, 특히 ISALI는 대기도에 형성되는 피브린 원주 및 폐포의 피브린을 비롯한 비정상적인 피브린 턴오버의 경향이 있다 (Enkhbaatar 등, 2004a). 기관지 원주는 기체 교환을 방해하여, 종종 기관지경 청소능을 요구하고, 폐확장 부전을 촉진한다. 분무화된 헤파린 및 N-아세틸시스테인이 임상적으로 사용되었으나, ISALI 환자에게 분무된 헤파린의 효능이 모든 무작위 또는 예상 사례가 제어된 임상시험에서 입증되지 않았고(Tuinman 등, 2012), 양을 대상으로 한 우리의 연구에서 실험했을 때 헤파린 단독으로 ISALI를 개선할 수 있음이 확인되지 않았다(Enkhbaatar 등, 2008a; Enkhbaatar 등, 2008b). 헤파린은 성립된 응혈을 없애지 못하며, 분무화된 헤파린은 ISALI에서 전신 응고장애를 개시할 수 있다(O'Donnell, 2012).
발명의 요약
본원에 대상체의 기도로 투여하기 위한 효소 용액의 제조 방법이 제공되는데, 여기서 상기 방법은 상기 효소 용액을 분무화하는 것을 포함한다(예를들면, 진동 메쉬 분무기 사용). 상기 효소는 조직 플라스미노겐 활성제일 수 있고, 이것은 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 및 조직 플라스미노겐 활성제(tPA)를 포함한다. 일부 구현예에서, 상기 진동 메쉬 분무기는 AERONEB®프로페셔널 분무기 또는 EZ 브리드 아토마이저(Breathe Atomizer)이다.
따라서, 일 구현예에서, 대상체의 기도로 투여하기 위한 효소 용액의 제조 방법이 제공되는데, 여기에는 상기 효소 용액을 분무화하여 분무화된 용액을 제공하는 것이 포함된다. 어떤 측면에서, 상기 효소는 플라스미노겐 활성제, 예컨대 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 또는 조직 플라스미노겐 활성제(tPA)일 수 있다. 어떤 측면에서, 상기 효소 용액을 분무화하는 것은 진동메쉬 분무기를 사용함으로써 이루어질 수 있다. 일부 측면에서, 상기 효소 용액을 분무화하는 것은 제트 분무기 또는 초음파 분무기의 사용은 포함하지 않는다. 어떤 측면에서, 상기 구현예의 효소 용액의 분무화는 충분한 분무화 에너지 및/또는 시간을 제공하여 중앙액적 크기가 약 2.5㎛ 내지 10㎛, 2.5㎛ 내지 8㎛, 또는 3.0㎛ 내지 6㎛인 분무화된 용액을 제공하는 단계를 포함할 수 있다. 일부 구체적 측면에서, 상기 효소 용액을 분무화하는 것은 동결건조된 효소 조성물을 획득하고, 상기 동결건조된 효소 조성물을 용액(예를 들면, 수용액)에 재구성하여 효소 용액을 제공하고, 상기 효소 용액을 분무화하는 것을 포함한다. 따라서, 추가 구현예에서, 상기 구현예의 방법에 따라 생산된 분무된 효소 용액이 제공된다.
또 다른 추가 구현예에서, scuPA 또는 tPA의 분무화된 용액을 포함하는 조성물이 제공된다. 일부 측면에서, 상기 구현예의 조성물 또는 효소 용액은 수용액일 수 있다. 어떤 측면에서, 상기 효소 용액은 생리적으로 허용가능한 염농도 및/또는 pH 완충제를 포함한다. 예를 들면, 효소 용액은 멸균된 염수용액 또는 포스페이트완충 염수(PBS)일 수 있다. 바람직한 측면에서, 상기 조성물 또는 효소 용액은 scuPA를 포함한다.
추가 구현예에서, 대상체를 치료하는 방법이 제공되는데, 이것은 분무된 효소 용액(예를 들면, tPA 및/또는 scuPA 효소 용액)을 이것을 필요로하는 대상체의 기도에 투여하는 것을 포함한다. 예를 들면, 상기 대상체에 급성 폐손상 또는 감염이 있을 수 있다. 또 다른 추가적 측면에서, 치료 대상체에 흡입연기로 유도된 급성 폐손상(ISALI), 화학적으로 유도된 폐손상, 플라스틱 기관지염, 중증천식 또는 급성호흡기곤란증후군(ARDS)이 있을 수 있다. 본 구현예에서, 상기 플라스미노겐 활성제가 분무기, 예컨대 진동 메쉬분무기(예를 들면, AERONEB® 프로페셔널 분무기또는 EZ 브리드 아토마이저)를 사용하여 분무된다. 당해기술의 숙련가는 상기 효소의 치료적으로 및 약제학적으로 허용가능한 용량을 전달하는 임의의 유형의 아토마이저, 예컨대 분무기가 본 구현예에 따른 사용에 적합함을 이해한다.
추가 구현예에서, 플라스미노겐 활성제 및 퍼플루오로탄소(예컨대, " 숨쉬는 액체")를 포함하는 조성물이 제공된다. 일부 측면에서, 상기 플라스미노겐 활성제는 scuPA 및/또는 tPA이다. 일부 측면에서, 상기 퍼플루오로탄소는 사이클로 알킬 그룹을 포함할 수 있다. 예를 들면, 상기 퍼플루오로탄소는 퍼플루오로데칼린 및/또는 퍼플루오로-옥틸브로마이드일 수 있다.
본 발명의 또 하나의 추가 구현예는 폐감염 또는 폐손상이 있는 대상체를 치료하기 위한 방법을 제공하는데, 상기 방법은 상기 대상체에게 플라스미노겐 활성제 및 퍼플루오로탄소를 포함하는 조성물의 치료적으로 효과적인 양을 투여하는 것을 포함한다. 일부 측면에서, 상기 플라스미노겐 활성제는 scuPA 또는 tPA이다. 어떤 측면에서, 상기 퍼플루오로탄소는 퍼플루오로데칼린 및/또는 퍼플루오로-옥틸브로마이드일 수 있다.
본 발명의 기타 목적, 특징 및 이점은 하기 상세한 설명에서 분명해질 것이다. 그러나, 하기 상세한 설명 및 구체적인 실시예들은, 본 발명의 바람직한 구현예를 나타내는 것이긴 하나, 하기의 상세한 설명에 의해 본 발명의 사상 및 범위 내에서 다양한 변화 및 수정이 당해분야의 숙련가에게 분명한 것이기 때문에, 단지 설명으로 제시된 것임이 이해되어야 한다.
하기 도면은 본 명세서의 일부를 형성하고, 본 발명의 어떤 측면을 추가로 입증하기 위해 포함된다. 본 발명은 본원에 제시된 특정 구현예의 상세한 설명과 함께 하나 이상의 이들 도면을 참고로 보다 잘 이해될 수 있다.
도 1은 블레오마이신으로 유도된 ALI가 있는 마우스에서 재조합 scuPA의 기관내 전달이 BAL uPA 활성을 증가시킴을 보여주는 그래프이다.
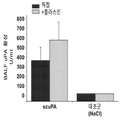
도 2는 분무화된 scuPA로의 양의 치료가 scuPA 치료 후 인간 uPA 항원과 관련된 검출가능한 uPA 활성을 제공하였음을 보여준다(선 3). uPA 항원 및 활성은 마찬가지로 scuPA로 치료된 동물에서 유래된 폐 균질물에서 발견되었다(선 4). 선 1: uPA 표준 및 선 2: 기준선 uPA 활성.
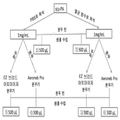
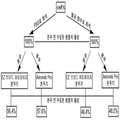
도 3은 몇개의 상이한 분무화된 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 제형을 제조하는 방법을 보여주는 도식이다.
도 4는 도 3에 따라 제조된 분무화된 scuPA 제형의 활성을 나타내는 도식이다.
도 5는 퍼플루오로데칼린(PFD) 또는 퍼플루오로-옥틸브로마이드(PFB)와 1회 혼합된 조직 플라스미노겐 활성제(tPA)의 활성을 보여주는 도식이다.
도 1은 블레오마이신으로 유도된 ALI가 있는 마우스에서 재조합 scuPA의 기관내 전달이 BAL uPA 활성을 증가시킴을 보여주는 그래프이다.
도 2는 분무화된 scuPA로의 양의 치료가 scuPA 치료 후 인간 uPA 항원과 관련된 검출가능한 uPA 활성을 제공하였음을 보여준다(선 3). uPA 항원 및 활성은 마찬가지로 scuPA로 치료된 동물에서 유래된 폐 균질물에서 발견되었다(선 4). 선 1: uPA 표준 및 선 2: 기준선 uPA 활성.
도 3은 몇개의 상이한 분무화된 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 제형을 제조하는 방법을 보여주는 도식이다.
도 4는 도 3에 따라 제조된 분무화된 scuPA 제형의 활성을 나타내는 도식이다.
도 5는 퍼플루오로데칼린(PFD) 또는 퍼플루오로-옥틸브로마이드(PFB)와 1회 혼합된 조직 플라스미노겐 활성제(tPA)의 활성을 보여주는 도식이다.
I. 본 발명
본원에 대상체의 기도에 투여하기 위한 효소 용액을 제조하는 방법이 제공되는데, 상기 방법은 분무기, 예컨대 진동 메쉬분무기를 사용하여 상기 효소 용액을 분무화하는 것을 포함한다. 진동 메쉬분무기를 사용하는 것과 같은 방법으로 효소를 분무화하면, 유의미한 효소 활성 수준을 유지하는 분무화된 조성물이 야기된다는 것은 본원에 상세히 명시된 본 연구의 놀라운 발견이다. 또한 본원에 분무화된 플라스미노겐 활성제의 치료적으로 효과적인 양을 기도를 통해 상기 대상체에게 투여함으로써, 대상체의 폐손상 및 감염, 예컨대 흡입연기로 유도된 급성폐손상(ISALI)을 치료하는 방법이 제공된다. 일부 경우에, 상기 플라스미노겐 활성제는 진동 메쉬분무기를 사용하여 분무된다. 추가로, 본원에 플라스미노겐 활성제 및 퍼플루오로탄소를 포함하는 조성물, 및 폐손상 및 감염(예를들면, ISALI)을 치료하기 위해 상기 플라스미노겐 활성제 /퍼플루오로탄소 조성물을 사용하는 방법이 제공된다. 일부 구현예에서, 상기 구현예에 따라 사용하기 위한 효소는 전구 효소이다. 추가 측면에서, 상기 효소는 플라스미노겐 활성제이다.
또 추가의 구현예에서, 본원에서 사용하기 위한 효소는 tPA 및 scuPA에서 선택된 플라스미노겐 활성제이다. 용어 "조직 플라스미노겐 활성제" 및 "tPA"는 상호 교환하여 사용되고, 본원에서 플라스미노겐의 플라스민으로의 전환에 관여될 수 있는 세린 프로테아제(일부 구현예에서, EC 3.4.21.68)를 가리킨다. 용어 "조직 플라스미노겐 활성제" 및 "tPA"에는 비제한적으로, 알테파아제, 레테플라제, 테넥테플라제 및 데스모테플라제을 비롯한 재조합 형태들이 포함됨이 이해되어야 한다. 용어 "조직 플라스미노겐 활성제" 및 "tPA"는 추가로 단일사슬 형태(sc-tPA), 2개 사슬 형태(ds-tPA) 및 이들의 혼합물을 포함한다. 일부 구현예에서, 상기 tPA는 인간 tPA 또는 인간에서 유도된 tPA이다. 용어 "단일사슬 우로키나제 플라스미노겐 활성제" 및 "scuPA"는 본원에서 우로키나제 세린 프로테아제의 전구 효소(일부 구현예에서, EC 3.4.21.73)를 가리키고, 여기서 세린 프로테아제는 플라스미노겐의 플라스민으로의 전환에 관여될 수 있다. "단일사슬 우로키나제 플라스미노겐 활성제" 또는 "scuPA"는 Lys158과 Ile159 사이의 단백분해 절단에 의해 활성화되어, 세린 프로테아제 효소를 형성하는 디설파이드 결합에 의해 연결된 2개의 사슬을 야기할 수 있다. 하기의 실시예 3 및 도 4는 진동 메쉬분무기를 사용한 scuPA의 분무화 및, 분무화의 선행기술 방법들과 비교하여, 분무화 후 달성된 놀랍게도 높은 효소 활성을 기술한다. 일부 구현예에서, 상기 진동 메쉬분무기는 AERONEB® 프로페셔널 분무기 또는 EZ 브리드 아토마이저이다.
용어 "효소 용액"은 본원에서 분무화에 적합한 효소를 함유하는 모든 액체 제형을 가리킨다. 일부 구현예에서, 상기 효소 용액은 본원에서 정의된 바와 같이 약제학적으로 허용가능한 캐리어 또는 부형제를 함유한다. 상기 효소 용액은 흡입 또는 당해분야의 숙련가에 공지된 임의의 다른 방법을 통해 대상체의 기도에 투여된다. 용어 "기도"는 본원에서 상부 기도, 호흡기 기도 및 폐를 비롯한 기도의 임의의 부분을 가리킨다. 상기 상부 기도에는 코 및 콧구멍, 입 및 목이 포함된다. 상기 호흡기 기도는 후두, 기관, 기관지 및 세기관지를 포함한다. 상기 폐는 호흡기 세기관지, 폐포관, 폐포낭 및 폐포를 포함한다.
또한 본원에 대상체의 흡입연기로 유도된 급성 폐손상(ISALI)을 치료하는 방법이 제공되는에, 상기 방법은 분무화된 플라스미노겐 활성제의 치료적으로 효과적인 양을 상기 대상체에게 기도를 통해 투여하는 것을 포함하고, 여기서 상기 플라스미노겐 활성제는 진동 메쉬분무기를 사용하여 분무된다. 일부 구현예에서, 상기 플라스미노겐 활성제는 tPA 및 scuPA에서 선택된다. 다른 또는 추가의 구현예에서, 상기 진동 메쉬분무기는 AERONEB® 프로페셔널 분무기 또는 EZ 브리드 아토마이저이다.
"ISALI 치료"는 장애 또는 병태, 예컨대 ISALI 질환의 하나 이상의 수반되는 증상을 부분적으로 또는 완전히 지연, 완화, 개선 또는 세기의 감소를 가리키고, 장애 또는 병태, 예컨대 ISALI 질환의 하나 이상의 원인을 완화, 개선 또는 방해하는 것을 가리킴이 이해되어야 한다. 본 발명에 따르면 치료는 방지차원으로, 예방 차원으로, 임시처방 차원으로 또는 치료차원으로 적용될 수 있다. 일부 예에서, 용어 "치료하다", "치료하는", "치료" 및 이들의 여러 가지 문법적 변형에는 상기 대상체의 치료 전과 비교하여, 또는 일반적인 또는 연구모집단에서 그와 같은 질환 또는 증상의 발생빈도와 비교하여, ISALI 질환과 관련된 병태 또는 증상을 부분적으로 또는 완전히 감소시키는 것이 포함된다. 일부 구현예에서, ISALI 질환에는 하기 중 하나 이상이 포함된다: 산소화 감소, 기도 폐색(중증 기도 폐색 포함), 섬유성 기도 원주 또는 잔해 및 폐포 피브린 침착. 따라서, ISALI 질환의 치료에는 산소화의 향상, 기도폐색의 감소, 섬유성 기도 원주 또는 잔해의 감소 및 폐포 피브린 침착의 감소 중 하나가 포함된다. 일부 구현예에서, ISALI 질환은 출혈의 발생 빈도의 감소로 치료된다.
추가로, 본원에 플라스미노겐 활성제 및 퍼플루오로탄소(PFC)를 포함하는 조성물이 제공된다. 일부 구현예에서, 본 조성물 중 상기 플라스미노겐 활성제는 tPA 및 scuPA에서 선택된다. 기타 또는 추가의 구현예에서, 본 조성물 중 PFC는 퍼플루오로데칼린, 퍼플루오로-1,3-디메틸사이클로헥산, FC-75, 퍼플루오로옥탄 및 퍼플루오로-옥틸브로마이드에서 선택된다. 일부 측면에서, PFC는 사이클로알킬 그룹, 예컨대 퍼플루오로데칼린, 퍼플루오로-1,3-디메틸사이클로헥산 또는 FC-75를 갖는 PFC 이거나 또는 이것을 포함한다. 상기 플라스미노겐 활성제 및 PFC가 어떤 비율로 또는 어떤 농도로든 존재할 수 있음이 이해되어야 한다. 일부 구현예에서, 본 조성물은 플라스미노겐 활성제를 PFC의 대략 0.005-0.040 mg/mL의 농도로 포함한다.
그 외 추가로, 대상체의 흡입연기로 유도된 급성 폐손상(ISALI)을 치료하는 방법이 제공되는데, 상기 방법은 플라스미노겐 활성제 및 PFC를 포함하는 조성물의 치료적으로 효과적인 양을 상기 대상체에게 투여하는 것을 포함한다. 실시예 4 및 도 5는 플라스미노겐 활성제, tPA가 퍼플루오로 탄소 혼합물에서 활성을 유지했음을 입증한다. 게다가, 상기 PFC 및 플라스미노겐 활성제는 부가적으로 폐포 피브린의 청소능 및 향상된 결과뿐만 아니라 기도 잔해 제거를 촉진하다. 특이적으로, 상기 PFC는 호흡기 기체 교환을 지원하면서 1) 기도 원주의 용해 및 이탈; 및 2) 기도 및 폐포잔해의 제거를 촉진하는 상기 플라스미노겐 활성제를 효과적으로 전달한다. 기계론적으로, PFC는 효과적으로 폐 용적을 동원한다. 상기 PFC 액체의 낮은 표면장력을 고려할 때, 상기 PFC는 폐를 통해, 잠재적으로 원주 및 기도벽 사이로 상기 플라스미노겐 활성제를 분산시킴으로써, 새로운 원주의 형성 속도는 늦추면서 형성 중인 원주를 부순다. 상기 PFC가 폐에서 기화되면서, 상기 플라스미노겐 활성제는 남아서 추가로 기도 원주 및 폐포 피브린을 용해하는 역할을 한다. PFC 현탁액의 재투여시, 상기 PFC 용적은 추가의 약물을 침착시킬 뿐만 아니라 원주 및 폐포 잔해를 제거한다. 상기 PFC가 압축이 불가능하기 때문에, 이것은 손상된 작은 기도에 삽입되어 개방하고, 그럼으로써 동원을 돕는다. 우리가 비록 어떤 기전에 구속되지 않으나, PFC와의 접촉은 또한, 사실상 모든 형태의 ALI에서 작은 기도 및 폐포에서 조직인자에 의해 개시되는, 응고의 감쇠를 통해 기저 상피를 보호할 수 있다. 인-라인(in-line) 흡인으로, 밀도가 더 낮은 잔해들이 비교적 밀도가 더 높은 PFC에서 부유하는데, 이것은 기도 피브린 원주 단편 및 잔해의 제거를 용이하게 한다.
따라서, 플라스미노겐 활성제 및 PFC 조성물을 투여하는 방법에 관한 일부 구현예에서, 상기 플라스미노겐 활성제는 tPA 및 scuPA에서 선택된다. 플라스미노겐 활성제 및 PFC 조성물을 투여하는 방법에 관한 다른 또는 추가의 구현예에서, 본 조성물 중 PFC는 퍼플루오로데칼린 및 퍼플루오로-옥틸브로마이드에서 선택된다.
또한 상기 전술한 내용은 본 발명의 바람직한 구현예에 관한 것으로, 본 발명의 범위에서 벗어나지 않는 한, 거기에 수 많은 변화가 이루어질 수 있음이 이해될 것이다. 본 발명은 추가로 하기 실시예에 의해 실증되는데, 이들은 어떤 식으로든 발명의 상기 범위을 제한하는 것으로 해석되어서는 안 된다. 반면, 본원의 설명을 읽은 후, 본 발명의 사상 및/또는 첨부된 청구항들의 범위에서 벗어나지 않으면서, 당해분야의 숙련가에게 스스로를 시사할 수 있는 다양한 기타 구현예, 변형 및 이들의 등가물에 의존할 수 있음이 명확히 이해되어야 한다. 본원에서 참조된 모든 특허들, 특허 출원 및 출판물은 그 전체가 다목적으로 참고로 편입되었다. 본 명세서 및 청구항에 사용된 용어 정의는 하기와 같다.
II.
정의
명세서 및 청구항에 사용된 바와 같이, 단수 형태 명사는 맥락이 명확히 다르게 지시하지 않는 한, 복수의 지시어를 포함한다. 예를 들면, 용어 "세포"는 이들의 혼합물을 비롯하여 복수의 세포들을 포함한다.
본 청구항에서 용어 "또는"의 사용은, 선택 만을 가리킨다거나 또는 상기 선택들이 상호배타적이라고 명백하게 명시하지 않는 한, 비록 개시내용이 오로지 선택 및 "및/또는"을 가리키는 정의를 뒷받침하더라도, "및/또는"을 의미하기 위해 사용된다. 본원에서 사용되는 "또 다른"은 최소한 두 번째 또는 그 이상을 의미할 수 있다.
본원에 전반적으로, 용어 "약"은 어떤 값이 상기 값을 측정하기 위해 활용된 장치 및 방법에 대한 본질적인 오차를 포함함을 가리키거나, 상기 연구 대상체에 존재하는 변형들을 가리키기 위해 사용된다.
용어 "투여하는"는 경구, 국소, 정맥내, 피하, 경피, 경피, 근육내, 관절내, 비경구, 세동맥내, 진피내, 뇌실내, 두개내, 복강내, 병소내, 비강내, 직장, 질, 흡입으로 또는 이식된 저장기에 의한 투여를 가리킨다. 용어 "비경구"는 피하, 정맥내, 근육내, 관절내, 활막내, 흉골내, 척추강내, 간내, 병소내 및 두개내 주사또는 주입 기술을 포함한다. 일부 구현예에서, 상기 투여는 분무화된 조성물의 흡입을 통해 이루어진다.
용어 "기도"는 본원에서 상부 기도, 호흡기 기도 및 폐를 비롯한 기도의 임의의 부분을 가리킨다. 상기 상부 기도는 코 및 콧구멍, 입 및 목을 포함한다. 상기 호흡기 기도는 후두, 기관, 기관지 및 세기관지를 포함한다. 상기 폐는 호흡기 세기관지, 폐포관, 폐포낭 및 폐포를 포함한다.
"조성물"은 활성제, 및 또 하나의 불활성(예를 들면, 검출가능한 제제 또는 표지) 또는 활성 화합물, 즉 조성물, 예컨대 아쥬반트의 조합물을 의미하는 것이다.
본원에서 사용된 바와 같이, 용어 "포함하는"은 상기 조성물 및 방법이 기타를 배제하지 않으면서 인용된 요소들을 포함하는 것을 의미하는 것이다. "본질적으로 ~으로 이루어진"이 조성물 및 방법을 정의하기 위해 사용될 경우, 상기 조합물에 모든 필수적인 유의성을 갖는 다른 요소들을 배제함을 뜻한다. 따라서, 본질적으로 본원에서 정의된 요소들로 이루어진 조성물은 상기 단리 및 정제 방법에 의한 미량의 오염물질 및 약제학적으로 허용가능한 캐리어, 예컨대 포스페이트완충 염수, 보존제 등을 배제하지는 않는다. "~로 이루어진"은 기타 성분의 미량 원소보다 많은 것과 본 발명의 조성물을 투여하기 위한 실질적인 방법 단계들을 배제함을 의미한다. 이들 이행 용어들 각각에 의해 정의된 구현예는 본 발명의 범위 내에 있다.
"대조군"은 비교를 위해 한 실험에서 사용되는 대안적인 개체 또는 샘플이다. 대조군은 "양성" 또는 "음성"일 수 있다. 치료를 목적으로 하는 "포유동물"은, 인간, 가축 및 농장 동물, 비인간 영장류 및 동물원, 스포츠용 또는 애완 동물, 예컨대, 개,말, 고양이, 소 등을 비롯한 포유동물로 분류된 모든 동물을 가리킨다.
본원에서 용어 "효소"는 특이적 생화학 반응의 촉매역할을 하는 하나 이상의 폴리펩타이드 또는 전구 효소를 가리킨다. 용어 "전구 효소"는 효소로 대사작용되는 생물학적 활성 물질을 가리킨다. 일 구현예에서, 상기 효소는 조직 플라스미노겐 활성제(tPA)이다. 다른 또는 추가의 구현예에서, 상기 효소는 전구 효소이고, 단일사슬 우로키나제 플라스미노겐 활성제(scuPA)이다.
본원에서 용어 "피브리놀리신"은 응혈의 용해를 촉진하는 여러 단백분해 효소 중 어떤 것을 가리킨다. 피브리놀리신에는, 비제한적으로, 플라스민, 조직 플라스미노겐 활성제(tPA, sc-tPA 및 dc-tPA), 우로키나제(uPA) 및 우로키나제 전구 효소(scuPA)가 포함된다.
용어 "동일성" 또는 "상동성"은, 서열을 배열하고 간격을 도입한 후, 필요하면 전체 서열에 대한 최대 퍼센트 동일성을 달성하기 위해, 그러나 상기 서열동일성의 일부로서 모든 보존적 치환을 고려하지 않고, 후보서열 중, 상기 서열과 비교되는 상응하는 서열의 잔기와 동일한 아미노산 잔기의 백분율을 의미하는 것으로 해석되어야 한다. N- 또는 C-말단 확대 또는 삽입 모두 동일성 또는 상동성을 감소시키는 것으로 해석되어서는 안 된다. 상기 정렬을 위한 방법 및 컴퓨터 프로그램은 당해기술에 공지되어 있다. 서열 동일성은 서열분석 소프트웨어를 사용하여 측정될 수 있다.
본원에서 용어 "흡입연기로 유도된 급성 폐손상" 및 "ISALI"는 상호 교환하여 사용되며, 연기흡입에 의해 야기된 급성 폐손상(ALI)의 형태를 가리킨다. ALI는 또한 일명 "가벼운 ARDS"라 일컬어진다. ALI는 대상체에서 하기 조건들 중 하나가 발견되는 경우로 정의될 수 있다: 1) 가슴 x-선 상의 양측성 폐 침투물, 2) 임상적으로 명시된 바와 같이 우심카테터로 측정 시, 폐모세관 쐐기압력< 18 mmHg(2.4 kPa), 및3) PaO2/FiO2 <300 mmHg(40 kPa). 일부 구현예에서, ISALI의 치료에는 하기 병태들 중 하나 이상의 치료가 포함된다: 산소화 감소, 기도폐색(중증 기도폐색 포함), 섬유성 기도 원주 또는 잔해 및 폐포 피브린 침착.
용어 "분무화하는", "분무화된" 및 기타 문법적 변형들은 본원에서 액체를 작은 에어로졸 액적으로 전환하는 과정을 가리킨다. 일부 구현예에서, 상기 에어로졸 액적은 중앙 직경이 대략 2~10㎛이다. 일부 구현예에서, 상기 에어로졸 액적은 중앙 직경이 대략 2~4㎛이다.
용어 "퍼플루오로탄소" 및 "PFC"는 본원에서 상호 교환하여 사용되고, 주로 탄소 및 불소를 함유하는 유기불소 화합물을 가리킨다. 용어 "퍼플루오로탄소"가 탄소 및 불소 이외에 분자를 함유하고, 통상적으로 플루오로탄소라 불리는 크게 플루오르화된 분자를 포함하는 것을 의미함이 이해되어야 한다. 퍼플루오로탄소의 예에는, 비제한적으로, 퍼플루오로데칼린, 퍼플루오로-옥틸브로마이드, FC 77, PF 5060 및 Rimar 101이 포함된다. 본 발명에 따라 사용된 PFC들은 기체 용해도, 밀도 및 표면장력과 관련하여 유사한 물리화학 특성을 공유하지만, 죽은조직 제거술에서 기도 원주의 가시화 및 이동도에 영향을 미칠 수 있는 방사선-불투명 및 동점도(kinematic viscosity)와 관련하여 차이가 있을 수 있다. 열거된 각각의 퍼플루오로탄소에는 모든 관련 이성질체, 예컨대 입체이성질체, 거울상이성질체 및 부분 입체이성질체가 포함된다.
용어 "플라스미노겐 활성제"는 플라스미노겐을 플라스민으로 전환시키는 세린 프로테아제 폴리펩타이드를 가리키고, 여기에는 비제한적으로, tPA, uPA (2개 사슬또 는 활성 형태) 및 본원에서 정의된 전구 효소 scuPA가 포함된다.
"약제학적 조성물"은 활성제와, 상기 조성물을 시험관내, 생체내 또는 생체외 진단 또는 치료용으로 적합하게 만드는 불활성 또는 활성 캐리어의 조합물을 포함한 것이다.
본원에서 사용된 바와 같이, 용어 "약제학적으로 허용가능한 캐리어" 또는 "부형제"에는 표준 약제학적 캐리어, 예컨대 포스페이트완충 염수 용액, 염수(멸균 염수 포함) 물, 에멀젼(예컨대 기름/물 또는 물/기름 에멀젼 중 어떤 것을 아우르는데, 여기서 "기름"은 약제학적으로 허용가능한 에멀젼의 물 불혼화성 상) 및 다양한 유형의 습윤제가 포함된다. 상기 조성물에는 또한 안정제 및 보존제가 포함된다. 캐리어, 안정제 및 아쥬반트의 자세한 예는 Martin, REMINGTON'S PHARM. SCI., 15th Ed. (Mack Publ. Co., Easton (1975)) 참조.
용어 "약제학적으로 허용가능한 염"은 모든 산 또는 염기 부가염을 가리키는 것으로, 이들의 반대이온은 이들의 상기 염의 약제학적 용량으로 투여된 상기 대상체에 비독성이다. 약제학적으로 허용가능한 염의 구체적인 예는 당해분야의 숙련가에게 공지되어 있다.
용어 "약제학적으로 효과적인 양", "치료적으로 효과적인 양", 또는 "치료적으로 효과적인 용량"은 연구자, 수의사, 의사 또는 기타 임상의에 의해 추구되는, 조직, 시스템, 동물 또는 인간의 생물학적 또는 의료반응을 야기시키는, ACPD 조성물과 같은 화합물의 양을 가리킨다.
용어 "폴리펩타이드"는 가장 넓은 의미로 사용되어 둘 이상의 서브유닛 아미노산, 아미노산 유사체 또는 펩타이드 모사체의 화합물을 가리킨다. 상기 서브유닛은 펩타이드 결합에 의해 연결될 수 있다. 또 다른 구현예에서, 상기 서브유닛은 기타 결합, 예를 들면 에스테르, 에테르 등의 결합에 의해 연결될 수 있다. 본원에서 사용된 바와 같이, 용어 "아미노산"은 천연 및/또는 비천연 또는 합성 아미노산을 가리키는 것으로, 여기에는 글리신 및 D 또는 L 광학이성질체 및 아미노산유사체 및 펩타이드모사체가 포함된다. 3개 이상의 아미노산으로 이루어진 펩타이드는, 상기 펩타이드사슬이 짧은 경우, 통상적으로 올리고펩타이드로 일컬어진다. 상기 펩타이드 사슬이 긴 경우, 상기 펩타이드는 통상적으로 폴리펩타이드 또는 단백질이라 불린다.
폴리뉴클레오타이드 또는 폴리뉴클레오타이드 영역(또는 폴리펩타이드 또는 폴리펩타이드 영역)은 또 하나의 서열에 대해 어떤 백분율(예를 들면, 80%, 85%, 90% 또는 95%)의 "서열 동일성" 또는 "상동성"을 갖는데, 이것은 정렬된 경우, 상기 두 개의 서열을 비교할 때, 상기 백분율만큼의 염기(또는 아미노산)가 동일함을 뜻한다. 이와 같은 정렬 및 퍼센트 상동성 또는 서열 동일성은 당해기술에 공지된 소프트웨어프로그램, 예를 들면 CURRENT PROTOCOLS IN MOLECULAR BIOLOGY (F. M. Ausubel et al., eds., 1987) 보충물 30, 섹션 7.7.18, 표 7.7.1에 기술된 것을 사용하여 측정될 수 있다. 바람직하게는, 디폴트 파라미터가 정렬에 사용된다. 바람직한 정렬 프로그램은 디폴트 파라미터를 사용하는 BLAST이다. 특히, 바람직한 프로그램은 하기 디폴트 파라미터를 사용하는 BLASTN 및 BLASTP이다: 유전자암호=표준; 필터=없음; 가닥=양쪽; 컷오프=60; 예상=10; 매트릭스=BLOSUM62; 설명=50 서열; 분류수단=HIGH SCORE; 데이타베이스=중복 안 됨, 유전자은행+EMBL+DDBJ+PDB+유전자은행 CDS 번역+Swiss단백질+SPupdate+PIR.
본원에서 사용된 용어 "예방하다", "예방하는", "예방" 및 이들의 문법적 변형들은 장애 또는 병태 및/또는 이것의 수반되는 증상들 중 하나 이상의 개시 또는 재발을 부분적으로 또는 완전히 지연시키거나 불가능하게 하는 방법, 또는 대상체가 장애 또는 병태를 얻거나 다시 얻지 않게 차단하는 방법, 또는 대상체가 장애 또는 병태, 또는 이것의 수반되는 증상들 중 하나 이상을 얻거나 또는 다시 얻을 위험을 감소시키는 방법을 가리킨다.
용어 "대상체"는 본원에서 동물, 예컨대 비제한적으로, 영장류(예를 들면, 인간), 소, 양, 염소, 말, 개, 고양이, 토끼, 랫트, 마우스 등을 포함하는 포유동물을 포함하는 것으로 정의된다. 바람직한 구현예에서, 상기 대상체는 인간이다.
용어 "약제학적으로 효과적인 양", "치료적으로 효과적인 양", 또는 "치료적으로 효과적인 용량"은 연구자, 수의사, 의사 또는 기타 임상의에 의해 추구되는, 조직, 시스템, 동물 또는 인간의 생물학적 또는 의료반응을 야기시키는, tPA 및/또는 scuPA 조성물과 같은 화합물의 양을 가리킨다.
용어 "단일사슬 우로키나제 플라스미노겐 활성제" 및 "scuPA"는 상호교환하여 사용되고, 본원에서 우로키나제 세린 프로테아제 폴리펩타이드의 전구 효소(이때 세린 프로테아제는 플라스미노겐의 플라스민으로의 전환에 관여할 수 있음)(일부 구현예에서, EC 3.4.21.73), 또는 본원에 참고로 편입된 미국특허번호 7,332,469에 기재된 전구 효소를 가리킨다. 상기 "단일사슬 우로키나제 플라스미노겐 활성제" 및 "scuPA"는 Lys158 및 Ile159 사이의 단백분해 절단에 의해 활성화되어, 결과적으로 세린 프로테아제 효소를 형성하는, 디설파이드 결합으로 연결된 2개의 사슬을 야기할 수 있다. scuPA 동족체 또한 본 발명에 포함됨이 이해되어야 한다. 용어 "scuPA 동족체"는 본원에서 EC 3.4.21.73으로서 확인된 우로키나제 세린 프로테아제 폴리펩타이드의 전구 효소의 동족체, 오쏘로그 및 파라로그, 그리고 EC 3.4.21.73으로서 확인된 우로키나제 세린 프로테아제 폴리펩타이드의 전구 효소와 70%보다 큰 상동성을 갖는 다른 서열, 또는 미국특허번호 7,332,469에 기재된 전구 효소를 가리킨다.
"대상체", "개체" 또는 "환자"는 본원에서 상호교환되어 사용되고, 이들은 척추동물, 바람직하게는 포유동물, 더 바람직하게는 인간을 가리킨다. 포유동물에는 비제한적으로, 쥣과, 유인원, 인간, 농장동물, 스포츠용 동물 및 애완동물이 포함된다.
용어 "치료적으로 효과적인 양"은, 투여됐을 때, 치료대상인 ISALI 비정상의 발병을 방지하거나, 또는 이것의 증상들 중 하나 이상을 얼마간 완화하기에 충분한, tPA 및/또는 scuPA 조성물과 같은 화합물의 양을 포함한다. 상기 치료적으로 효과적인 양은 상기 화합물, 예컨대 tPA 및/또는 scuPA 조성물, 상기 장애 또는 병태 및 그것의 중증도, 투여 경로, 투여 시간, 배출 속도, 약물 배합, 치료 의사의 판단, 복용형태 및, 치료대상인 대상체의 연령, 체중, 일반적인 건강, 성별 및/또는 식습관에 따라 달라진다.
용어 "조직 플라스미노겐 활성제" 및 "tPA"는 상호교환하여 사용되고, 본원에서 플라스미노겐의 플라스민으로의 전환에 관여할 수 있는 세린 프로테아제(일부 구현예에서, EC 3.4.21.68)를 가리킨다. 용어 "조직 플라스미노겐 활성제" 및 "tPA"에는 비제한적으로, 알테파아제, 레테플라제, 테넥테플라제 및 데스모테플라제를 비롯한 재조합 형태들이 포함됨이 이해되어야 한다. 용어 "조직 플라스미노겐 활성제" 및 "tPA"는 추가로 단일사슬 형태(sc-tPA), 상기 2개 사슬 형태(ds-tPA) 및 이들의 혼합물을 포함한다. 일부 구현예에서, 상기 tPA는 인간 tPA 또는 인간에서 유도된 tPA이다. 또한 tPA 동족체가 본 발명에 포함됨이 이해되어야 한다. 용어 "tPA 동족체"는 EC 3.4.21.68로 확인된 조직 플라스미노겐 활성제 폴리펩타이드의 동족체, 오쏘로그 및 파라로그, 그리고 EC 3.4.21.68로 확인된 조직 플라스미노겐 활성제 폴리펩타이드와 70%보다 큰 상동성을 갖는 다른 서열을 가리킨다. 일부 구현예에서, 상기 tPA는 단일사슬 형태, 예컨대 ALTEPASETM 형태이다.
본원에서 사용되는 용어 "치료하다", "치료하는", "치료" 및 이들의 문법적 변형에는 장애 또는 병태, 예컨대 ISALI 질환의 수반되는 증상들 중 하나 이상을 부분적으로 또는 완전히 지연, 완화, 개선, 또는 이들의 세기를 감소시키는 것, 및/또는 장애 또는 병태, 예컨대 ISALI 질환의 하나 이상의 원인을 완화, 개선 또는 방해하는 것이 포함된다. 본 발명에 따른 치료는 방지차원으로, 예방 차원으로, 임시처방 차원으로 또는 치료 차원으로 적용될 수 있다. 일부 예에서, 용어 "치료하다", "치료하는", "치료" 및 이들의 문법적 변형에는, 상기 대상체의 치료 이전과 비교하여, 또는 일반적인 또는 연구모집단에서 그와 같은 질환 또는 증상의 발생빈도와 비교하여, ISALI 질환과 관련된 병태 또는 증상을 부분적으로 또는 완전히 감소시키는 것이 포함된다. 일부 구현예에서, ISALI 질환에는 하기 중 하나 이상이 포함된다: 산소화 감소, 기도폐색(중증 기도폐색 포함), 섬유성 기도 원주 또는 잔해 및 폐포 피브린 침착. 일부 구현예에서, ISALI 질환은 출혈의 발생빈도 감소로 치료된다.
용어 "진동 메쉬분무기"는 본원에서 미세-입자, 저-속도 에어로졸를 생성하기 위해 다수의 구멍(개구판)이 있는 함께 진동메쉬 또는 판을 사용하는 일반적인 원리로 작동하는 모든 분무기를 가리킨다. 일부 분무기는 1000 내지 7000개 구멍이 있는 메쉬/막을 함유할 수 있고, 상기 메쉬/막은 액체저장기의 상부에서 진동한다(참고,예를 들면, U.S. 특허 공보 20090134235 및 Waldrep and Dhand 2008, 각각은 참고로 본원에 편입되었다). 일부 구현예에서, 상기 진동 메쉬분무기는 AERONEB® 프로페셔널 분무기, Omron MICROAIR®, Pari EFLOW® 또는 EZ 브리드 아토마이저이다. 일부 측면에서, 진동 메쉬분무기는 진동주파수가 약 50~250kHz, 75~200kHz, 100~150kHz 또는 약 120kHz이다. 이들 장치는 폐에 에어로졸을 전달하는 효율이 높고, 이들 장치에 잔존하는 액체의 용적은 최소인데, 플라스미노겐 활성제와 같이 값비싸고 강력한 화합물에 이로운 요인이다.
III.
실시예
하기 실시예들은 본 발명의 바람직한 구현예들을 실증하기 위해 포함되었다. 하기 실시예들에 개시된 기법들은 본 발명의 실행 시 제대로 기능을 하는 본 발명가에 의해 발견된 기법들이며, 따라서 본 실행을 위한 바람직한 방법들을 구성하는 것으로 간주될 수 있음을 당해분야의 숙련가들에 의해 인정되어야 한다. 그러나, 당해기술의 숙련가는, 본 개시 내용에 비추어, 개시된 특정구현예에 수많은 변형이 이루어질 수 있으며, 그럼에도 본 발명의 사상 및 범위에서 벗어나지 않으면서 유사한 결과를 획득할 수 있음을 이해해야할 것이다.
실시예
1 -
블레오마이신으로
유도된 ALI가 있는 마우스에서 재조합
scuPA
의 기관내 전달이 BAL uPA 활성을 증가시킨다
0일째에 C57/B6 마우스에서 2.5U/kg 블레오마이신으로 ALI를 유도하였다(n=10 동물/그룹). 매일 상기 마우스에 마이크로분무기를 통해(100㎕) 한 마리 당 25,000 U; 167 ㎍의 재조합 인간 scuPA를 투여하였다. 7일째, scuPA의 마지막 마이크로분무기를 투여하고 4 시간 후, BAL을 수득하였다. 아미드분해 기질 S-2444(직접적으로 + 5 시간 동안 1mU/ml 플라스민으로 배양한 후)를 사용하여 uPA 활성을 측정하였다. 상기 결과는 도 1에 나타내었다. 플라스민 치료 후 uPA 활성의 증분은 상기 분무된 scuPA의 일부가 폐포 내벽액에 온전히 남아 있고, 체내에서 플라스민에 의한 활성화를 위해 여전히 이용가능함을 시사하였다. 폐 또는 전신 출혈이 발생하지 않았다. 이들 데이타는 분무화된 scuPA가 외상-유도된 AL에서 세척 섬유소 용해 활성을 증가시키고 내성이 좋음을 보여주는 이전의 보고(Munster 등, 2002)의 내용들을 확인해준다. 또한 조사 결과는 scuPA의 내구성 섬유소 용해 활성(분무주입 4시간 후, 실질적인 증가)이 ALI가 있는 폐에서 발생되었음을 보여준다.
실시예
2 -
분무화된
scuPA
가 기도 원주를 용해하고,
ISALI
가 있는 양의
BAL
에서 검출가능하다
양에게 분무화된 scuPA를 투여하였다(ISALI의 유도 4시간 후, 투여1회 당 2mg 시작, 4시간 마다 48시간 동안). 기도 원주 부하(폐색 스코어 12)가 4 시간마다 분무화된 tPA 4mg을 투여한 양의 범위에 속하였다(비히클 중 20.7을 ISALI가 있는 양에게 투여한 경우와 비교)(Enkhbaatar 등,2004b). 도 2에 나타낸 바와 같이, 양의 BAL(기관지폐포 세척)에는 형광측정 분석에 의한 검출가능한 기준선 uPA 활성이 없었으나(선 2), scuPA 투여 후 인간 uPA 항원과 관련된 검출가능한 uPA 활성이 있었고(선 3), uPA 항원 및 활성은 마찬가지로 scuPA-투여 동물에서 유래된 폐 균질물에서 발견되었다(선 4). 선 1: uPA 표준.
실시예
3 -
분무화된
scuPA
가 기도 원주를 용해하고,
ISALI
가 있는 양의 BAL에서 검출가능하다
또한 생리적으로 완충된 염수 또는 정상 식염수 중 하나에 용해시키고, 이어서 두 가지 유형의 진동 메쉬분무기, EZ 브리드 아토마이저 및 AeroNeb 프로 분무기를 사용하여 분무화한, scuPA를 1mg/mL 함유하는 scuPA 용액에 대한 연구를 수행하였다. scuPA는 두 가지 액체 캐리어에서 쉽게 용해되었다. 분무화 전과 후의 scuPA의 활성이 분무화 조건(예를 들면, 용액 형성, 상기 분무기에서 분무화 공정에서의 전단 및 온도)에 의해 영향을 받지 않음을 확인하였다. 또한, scuPA 용액에 대한 중앙 기하학적 입자크기가, 좁고 허용가능한 크기 분포를 갖는 3~4 마이크론임을 확인하였다. 재료, 방법 및 결과가 하기에 제공되었고, 절차의 도식은 도 3에 제공하였다.
포스페이트
완충 염수 및 멸균 염수 제제:
상기 포스페이트 완충 염수(DPBS, Lot 14190-250, Gibco)을 Biostore at UT-Austin에서 구매하였다. PBS의 조성은 표 1에 나타내었다.
상기 PBS의 pH는 7.3±0.1이었다. 멸균 염수는 B.Braun Medical Inc(Lot J1H573)에서 구매하였다. 두 가지 제제를 주위 실온에서 보관하였고, 과도한 열을 받지 않게 하였다.
장치 도입:
실험을 위해 EZ 브리드 아토마이저 분무기 및 AeroNeb 프로 분무기를 사용하였다. Aeroneb® 프로페셔널 분무기 시스템(진동 메쉬, Aerogen, Galway)은 다중 환자 사용을 위해 휴대가 쉬운 의료기기다. Aeroneb®은 일반적인 용도의 분무기와 함께 사용하는 것이 승인된 흡입용 의사-처방약을 에어로졸화하기 위한 것이다. EZ 브리드 아토마이저(진동 메쉬, Nephron Pharmaceuticals Corporation, USA)은 액체 약물을 에어로졸 형태로 공기 중에 분사하여, 사람이 들여마시도록 의도된 장치이다. 이들 장치는 기계적 환기 또는 기타 양압 숨쉬기 보조를 받거나 또는 받지 않는 환자에 의해 사용될 수 있다.
Scu
-PA 용액 제제:
8개 바이알(각각 scu-PA 3.5mg /mL 함유)을 수득하여 -80℃에서 보관하였다. 두 종류의 scu-PA 용액을 만들기 위해, 하기의 방식으로 용액을 제조하였다:
A.
scu-PA 바이알이 용액으로 용융될 때까지 실온에(20℃-25℃) 두었다. 6mL 주사기를 사용하여, 상기 바이알에서 용액 2mL를 취해 새로운 10mL 바이알에 옮겼다.
B.
21-게이지바늘이 부착된 6mL 주사기를 사용하여, 멸균된 포스페이트완충 염수(또는 멸균 염수) 3mL를 하나의 바이알에 주입하였다. 모든 scu-PA 용액이 균일해질 때까지 상기 내용물을 수작업으로 진탕하였다. 이어서, 상기 용액을 멸균된 포스페이트 완충 염수(또는 멸균 염수)로 최종농도 1mg/mL으로 희석하였다.
기하학적 입자-크기분포(
PSD
) 실험:
두 가지 분무기에 샘플로 두 가지 종류의 scu-PA(농도 1mg/mL)를 5mL씩 로딩하고, 별도로 공시험 대조군으로서 순수 염수 및 순수 PBS를 로딩하였다(총 8개 샘플). Malvern Spraytec을 사용하여, 기하학적 입자-크기 분포(PSD)를 측정하였다. 표준분무화 절차를 5회 수행하였다; 1회당 5초 동안 지속하였다. 모든 측정은 주위실온, 기압 및 습도에서 이루어졌다.
추가 연구를 위해 분무기에서 수집된 샘플:
10 초 후, 분무화 절차를 시작하여, 에어로졸 발생이 안정화될 때까지 수행하고, 그후 분무화된 출력 scu-PA의 500㎕ 샘플(총 4개 샘플)을 수집하여, 이어서 -80℃의 냉장고에서 동결시켰다. 표 2에 나타낸 바와 같이 6개 샘플을 제조하였다.
결과:
표 3은 샘플의 기하학적 입자-크기 분포(PSD) 정보(n=5)를 나타내고, 도 4는 분무화 이후 각 샘플의 활성을 나타낸다.
이들 결과를 기반으로, scuPA 용액을 최상의 분무기를 식별하는데 초점을 맞춰 분무화을 위해 최적화하였다. 분무기 투여에 대해 연구되는 기타 파라미터에는 처리 파라미터(예를 들면, scuPA 활성을 위한 최적의 용액 조성물, 공기역학적 특성(예컨대, 미세입자 분획), 대량 중앙공기 역학적 직경 및 총방출된 용량)의 효과, 분무화 중 scuPA 활성에 미치는 온도효과(예를 들면, 상이한 분무기 기전 유형을 사용) 및 scuPA 활성에 미치는 액체의 전단 효과(예를 들면, 원자화 압력, 초음파 진동, 메쉬 크기)를 확인하는 것이 포함된다.
실시예
4- PFC 중 tPA 현탁액은 안정적이고 tPA 활성을 보존한다
도 5는 PFC 중 tPA의 현탁액이 안정적이고, tPA 활성이 보존됨을 보여준다. 이들 연구의 경우, 10mL 주사기와 21 게이지바늘을 사용하여, 37℃에서 50 분 대기시간 동안 기관내 튜브(7mm 성인 기관 내 튜브)를 통해 tPA/PFC 현탁액(0.22mg/mL로 만든 tPA-PFC 현탁액 18mL)을 주입하였다. 상기 tPA가 적절히 습윤되었으며, PFCs에서 덩어리가 작은 입자로 잘게 부서졌음에 주목하였다. tPA 투여에 대해 연구되는 기타 파라미터에는 처리 파라미터(예를 들면, 상기 tPA의 입자 크기 감소, 상기 PFC의 점도, 수득된 tPA-PFC 현탁액, 상기 tPA-PFC 현탁액의 고형물함량 및 상기 tPA 활성에 대한 기관지 내시경 중 이것이 투여에 미치는 효과)의 효과를 확인하는 것이 포함된다. 상기 scuPA-PFC 개입의 제형을 분석하기 위해 동일한 접근법을 사용하였다.
PFC 및 피브리놀리신은 부가적으로 폐포 피브린의 청소 및 향상된 결과뿐만 아니라 기도잔해 제거를 증진시켰다. 특이적으로, 상기 PFC는 호흡기 기체 교환을 지원하면서 1) 상기 기도 원주의 용해 및 이탈; 및 2) 기도 및 폐포 잔해의 제거를 촉진하는 피브리놀리신을 효과적으로 전달한다. 기계론적으로, PFC는 효과적으로 폐 용적을 동원한다. PFC 액체의 낮은 표면장력을 감안할 때, PFC는 폐를 통해, 잠재적으로 원주 및 기도벽 사이로 피브리놀리신을 분산시킴으로써, 새로운 원주의 형성 속도를 늦추면서 형성되는 원주를 부순다. 상기 PFC가 폐에서 기화되면서, 상기 피브리놀리신은 잔존하여 추가로 기도 원주 및 폐포 피브린을 용해시키는 역할을 한다. PFC 현탁액의 재투여시, 상기 PFC 용적은 추가의 약물을 침착시킬 뿐만 아니라, 원주 및 폐포 잔해를 제거한다. 상기 PFC가 압축이 불가능하기 때문에, 이것은 손상된 작은 기도에 삽입되어 개방하고, 그럼으로써 동원을 돕는다. PFC와의 접촉은 또한 사실상 모든 형태의 ALI에서 작은기도 및 폐포의 조직인자에 의해 개시되는, 응고의 감쇠를 통해 기저상피를 보호할 수 있다. 인-라인(in-line) 흡인으로, 밀도가 더 낮은 잔해가 비교적 밀도가 더 높은 PFC 중에 부유하고, 이것은 기도 피브린 원주 단편 및 잔해의 제거를 용이하게 한다.
***
본원에 개시되고 청구된 모든 방법은 본 개시내용에 비추어 과도한 실험 과정 없이 이루어지고 실행될 수 있다. 본 발명의 조성물 및 방법이 바람직한 구현예의 측면에서 기재되었으나, 본 발명의 개념, 사상 및 범위에서 벗어나지 않으면서, 본원에 기재된 방법, 기재된 방법의 단계들 또는 단계들의 순서에 변화가 적용될 수 있음은 당해분야의 숙련가들에게 명백할 것이다. 더 구체적으로, 화학적으로 그리고 생리적으로 관련된 어떤 제제들이 본원에 기술된 제제로 치환되어 동일한 또는 유사한 결과가 달성될 수 있음이 명백할 것이다. 당해분야의 숙련가에게 명백한 모든 그와 같은 유사한 대체물 및 변형은 첨부된 청구항들에 의해 정의된 바와 같이, 본 발명의 사상, 범위 및 개념 내에 속하는 것으로 간주된다.
참조문헌
하기 참조문헌들은, 본원에 명시된 내용에 예시적 절차 또는 기타 세부 보충 사항들을 제공하는 범위에서, 특이적으로 본원에 참고로 편입되었다.
Claims (55)
- 대상체의 기도에 투여하기 위한 효소 용액의 제조 방법으로서,
상기 효소 용액을 분무화하여 분무화된 용액을 제공하는 단계를 포함하는, 방법. - 청구항 1에 있어서, 상기 효소가 플라스미노겐 활성제인, 방법.
- 청구항 2에 있어서, 상기 플라스미노겐 활성제가 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 또는 조직 플라스미노겐 활성제(tPA)인, 방법.
- 청구항 2에 있어서, 상기 플라스미노겐 활성제가 scuPA인, 방법.
- 청구항 1에 있어서, 상기 효소 용액을 분무화하는 것이 진동 메쉬분무기의 사용에 의해 이루어지는, 방법.
- 청구항 5에 있어서, 상기 진동 메쉬분무기가 AERONEB® 프로페셔널 분무기 또는 EZ 브리드 아토마이저인, 방법.
- 청구항 5에 있어서, 상기 분무화하는 것이 제트 분무기 또는 초음파 분무기의 사용을 포함하지 않는, 방법.
- 청구항 1에 있어서, 상기 효소 용액이 수용액인, 방법.
- 청구항 8에 있어서, 상기 효소 용액이 생리적으로 허용가능한 염농도를 포함하는, 방법.
- 청구항 8에 있어서, 상기 효소 용액이 pH 완충제를 포함하는, 방법.
- 청구항 8에 있어서, 상기 효소 용액이 포스페이트완충 염수(PBS)인, 방법.
- 청구항 8에 있어서, 상기 효소 용액이 scuPA를 포함하는, 방법.
- 청구항 1에 있어서, 상기 효소 용액을 분무화하는 것은:
(i) 동결건조된 효소 조성물 획득하는 것;
(ii) 상기 동결건조된 효소 조성물을 수용액에 재구성하여 효소 용액을 제공하는 것; 및
(iii) 상기 효소 용액을 분무화하는 것을 포함하는, 방법. - 청구항 1에 있어서, 상기 효소 용액을 분무화하는 것이 충분한 분무화 에너지 및/또는 시간을 제공하여 중앙액적 크기가 약 2.5㎛ 내지 10㎛인 분무화된 용액을 제공하는 것을 포함하는, 방법.
- 청구항 14에 있어서, 상기 효소 용액을 분무화하는 것이 충분한 분무화 에너지 및/또는 시간을 제공하여 중앙액적 크기가 약 2.5㎛ 내지 8㎛인 분무화된 용액을 제공하는 것을 포함하는, 방법.
- 청구항 15에 있어서, 상기 효소 용액을 분무화하는 것이 충분한 분무화 에너지 및/또는 시간을 제공하여 중앙액적 크기가 약 3.0㎛ 내지 6㎛인 분무화된 용액을 제공하는 것을 포함하는, 방법.
- 청구항 1 내지 16 중 어느 한 청구항의 방법에 의해 생산된 분무화된 효소 용액.
- 청구항 1 내지 16 중 어느 한 청구항에 있어서, 상기 분무화된 용액을 이를 필요로 하는 대상체의 기도에 투여하는 단계를 추가로 포함하는, 방법.
- 청구항 18에 있어서, 상기 대상체에 급성 폐손상 또는 감염이 있는, 방법.
- 청구항 19에 있어서, 화학적으로 유도된 폐손상이 있는 대상체의 기도에 상기 분무화된 용액을 투여하는 단계를 추가로 포함하는, 방법.
- 청구항 19에 있어서, 플라스틱 기관지염, 천식 또는 급성 호흡기 곤란 증후군(ARDS)이 있는 대상체의 기도에 상기 분무화된 용액을 투여하는 단계를 추가로 포함하는, 방법.
- 청구항 19에 있어서, 흡입연기로 유도된 급성 폐손상(ISALI)이 있는 대상체에 상기 분무화된 용액을 투여하는 단계를 추가로 포함하는, 방법.
- 대상체의 흡입연기로 유도된 급성 폐손상(ISALI)을 치료하는 방법으로서,
기도를 통해 상기 대상체에게 분무화된 플라스미노겐 활성제 조성물의 치료적으로 효과적인 양을 투여하는 단계를 포함하고,
상기 플라스미노겐 활성제가 진동 메쉬분무기를 사용하여 분무되는, 방법. - 청구항 23에 있어서, 상기 플라스미노겐 활성제가 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 또는 조직 플라스미노겐 활성제(tPA)인, 방법.
- 청구항 23에 있어서, 상기 플라스미노겐 활성제가 scuPA인, 방법.
- 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 또는 조직 플라스미노겐 활성제(tPA)의 분무화된 용액을 포함하는, 조성물.
- 청구항 26에 있어서, 상기 용액이 수용액인, 조성물.
- 청구항 27에 있어서, 상기 용액이 생리적으로 허용가능한 염농도를 포함하는, 조성물.
- 청구항 27에 있어서, 상기 용액이 pH 완충제를 포함하는, 조성물.
- 청구항 29에 있어서, 상기 용액이 포스페이트완충 염수(PBS)인, 조성물.
- 청구항 26에 있어서, scuPA를 포함하는, 조성물.
- 청구항 26에 있어서, 상기 분무화된 용액의 중앙 입자크기가 약 2.5㎛ 내지 10㎛인, 조성물.
- 청구항 26에 있어서, 상기 분무화된 용액의 중앙 입자크기가 약 2.5㎛ 내지 8㎛인, 조성물.
- 청구항 26에 있어서, 상기 분무화된 용액의 중앙 입자크기가 약 3.0㎛ 내지 6㎛인, 조성물.
- 급성 폐손상 또는 폐감염의 치료에 사용하기 위한 조성물로서,
청구항 26 내지 34 중 어느 한 청구항의 분무화된 용액을 포함하는, 조성물. - 청구항 35에 있어서, 화학적으로 유도된 폐손상, 플라스틱 기관지염, 천식, 급성호흡기곤란 증후군(ARDS) 또는 흡입연기로 유도된 급성 폐손상(ISALI)의 치료에 사용하기 위한, 조성물.
- 흡입연기로 유도된 급성폐손상(ISALI)의 치료에 사용하기 위한 조성물로, 청구항 26 내지 34 중 어느 한 청구항의 분무화된 용액을 포함하는, 조성물.
- 플라스미노겐 활성제 및 퍼플루오로탄소를 포함하는, 조성물.
- 청구항 38에 있어서, 상기 플라스미노겐 활성제가 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 또는 조직 플라스미노겐 활성제(tPA)인, 조성물.
- 청구항 38에 있어서, 상기 플라스미노겐 활성제가 scuPA인, 조성물.
- 청구항 38에 있어서, 상기 퍼플루오로탄소가 사이클로알킬그룹을 포함하는, 조성물.
- 청구항 38에 있어서, 상기 퍼플루오로탄소가 퍼플루오로데칼린 및 퍼플루오로-옥틸브로마이드에서 선택되는, 조성물.
- 청구항 38에 있어서, 상기 퍼플루오로탄소가 퍼플루오로데칼린을 포함하는, 조성물.
- 급성 폐손상 또는 감염의 치료에 사용하기 위한 조성물로, 청구항 38 내지 43 중 어느 한 청구항의 조성물을 포함하는, 조성물.
- 청구항 44에 있어서, 화학적으로 유도된 폐손상, 플라스틱 기관지염, 천식, 급성호흡기 곤란증후군(ARDS) 또는 흡입연기로 유도된 급성폐손상(ISALI)의 치료에 사용하기 위한 조성물.
- 흡입연기로 유도된 급성 폐손상(ISALI)의 치료에 사용하기 위한 조성물로, 청구항 38 내지 43 중 어느 한 청구항의 조성물을 포함하는, 조성물.
- 폐감염 또는 폐손상이 있는 대상체를 치료하는 방법으로서,
청구항 38 내지 43 중 어느 한 청구항의 조성물의 효과적인 양을 상기 대상체의 기도에 투여하는 단계를 포함하는, 방법. - 청구항 47에 있어서, 상기 대상체에 화학적으로 유도된 폐손상이 있는, 방법.
- 청구항 48에 있어서, 상기 대상체에 플라스틱 기관지염, 급성 호흡기 곤란증후군(ARDS) 또는 흡입연기로 유도된 급성폐손상(ISALI)이 있는, 방법.
- 흡입연기로 유도된 급성 폐손상(ISALI)이 있는 대상체를 치료하기 위한 방법으로서,
청구항 38 내지 43 중 어느 한 청구항의 조성물의 효과적인 양을 상기 대상체의 기도에 투여하는 단계를 포함하는, 방법. - 대상체의 흡입연기로 유도된 급성폐손상(ISALI)을 치료하는 방법으로서,
플라스미노겐 활성제 및 퍼플루오로탄소를 포함하는 조성물의 치료적으로 효과적인 양을 상기 대상체에게 투여하는 단계를 포함하는, 방법. - 청구항 51에 있어서, 상기 플라스미노겐 활성제가 단일사슬 우로키나제 플라스미노겐 활성제(scuPA) 또는 조직 플라스미노겐 활성제(tPA)인, 방법.
- 청구항 51에 있어서, 상기 플라스미노겐 활성제가 scuPA인, 방법.
- 청구항 51에 있어서, 상기 퍼플루오로탄소가 퍼플루오로데칼린 및 퍼플루오로-옥틸브로마이드에서 선택되는, 방법.
- 청구항 54에 있어서, 상기 퍼플루오로탄소가 퍼플루오로데칼린을 포함하는, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361899739P | 2013-11-04 | 2013-11-04 | |
| US61/899,739 | 2013-11-04 | ||
| PCT/US2014/063784 WO2015066664A2 (en) | 2013-11-04 | 2014-11-04 | Compositions and methods for administration of an enzyme to a subject's airway |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20160078986A true KR20160078986A (ko) | 2016-07-05 |
Family
ID=53005414
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020167012122A KR20160078986A (ko) | 2013-11-04 | 2014-11-04 | 대상체의 기도로 효소를 투여하기 위한 조성물 및 방법 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US20160279209A1 (ko) |
| EP (1) | EP3065705A4 (ko) |
| JP (1) | JP2016535782A (ko) |
| KR (1) | KR20160078986A (ko) |
| CN (1) | CN105764488A (ko) |
| AU (1) | AU2014341862A1 (ko) |
| CA (1) | CA2928759A1 (ko) |
| CL (1) | CL2016001062A1 (ko) |
| MX (1) | MX2016005720A (ko) |
| PE (1) | PE20160789A1 (ko) |
| WO (1) | WO2015066664A2 (ko) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2875853T3 (es) | 2013-03-15 | 2021-11-11 | Univ Texas | Método de tratar fibrosis |
| AU2019339260A1 (en) | 2018-09-10 | 2021-03-25 | Lung Therapeutics, Inc. | Modified peptide fragments of Cav-1 protein and the use thereof in the treatment of fibrosis |
| WO2021180068A1 (zh) * | 2020-03-09 | 2021-09-16 | 泰伦基国际有限公司 | 一种治疗2019新型冠状病毒引发疾病的方法和药物 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4790305A (en) * | 1986-06-23 | 1988-12-13 | The Johns Hopkins University | Medication delivery system |
| EP0266032A1 (en) | 1986-08-29 | 1988-05-04 | Beecham Group Plc | Modified fibrinolytic enzyme |
| US5302390A (en) | 1987-07-01 | 1994-04-12 | Beecham Group Plc | Hybrid proteins of human plasminogen and human t-PA, pharmaceutical compositions and methods of treatment |
| US5531219A (en) * | 1994-11-04 | 1996-07-02 | Alliance Pharmaceutical Corp. | Use of liquid fluorocarbons to facilitate pulmonary drug delivery |
| WO1998006426A1 (en) * | 1996-08-14 | 1998-02-19 | Gram Joergen Brodersen | Use of a plasminogen activator for the treatment of pulmonary disorders |
| US20030113271A1 (en) * | 1997-01-29 | 2003-06-19 | University Technology Corporation | Formulations for pulmonary delivery |
| JP2005518274A (ja) * | 2001-12-21 | 2005-06-23 | エンバイロスクラブ テクノロジーズ コーポレイション | マンガン酸化物の前処理および再生 |
| MXPA05007466A (es) * | 2003-01-09 | 2006-03-08 | Arizeke Pharmaceuticals Inc | Metodos para el tratamiento de enfermedades pulmonares. |
| US20050169908A1 (en) | 2004-01-23 | 2005-08-04 | Kazunori Murakami | Use of aerosolized antithrombin to treat acute lung injury |
| US20060198940A1 (en) | 2005-03-04 | 2006-09-07 | Mcmorrow David | Method of producing particles utilizing a vibrating mesh nebulizer for coating a medical appliance, a system for producing particles, and a medical appliance |
| US20070157931A1 (en) | 2005-07-11 | 2007-07-12 | Richard Parker | System and method for optimized delivery of an aerosol to the respiratory tract |
| EP1962869B1 (en) * | 2005-12-21 | 2013-03-20 | SolAeroMed Inc. | Treatment of respiratory diseases |
| SI22865A (sl) | 2008-09-25 | 2010-03-31 | Univerza@V@Ljubljani | Peptid uroaktivin kot aktivator encima urokinaze |
| CA2744555A1 (en) * | 2008-11-26 | 2010-06-03 | Five Prime Therapeutics, Inc. | Compositions and methods for regulating collagen and smooth muscle actin expression by serpine2 |
| DE102009031274A1 (de) * | 2009-06-30 | 2011-01-13 | Justus-Liebig-Universität Giessen | Liposomen zur pulmonalen Applikation |
| US20140205658A1 (en) * | 2011-08-29 | 2014-07-24 | Trifoilium Aps | Compositions and methods for treating or preventing radiation- or chemotherapy-induced pulmonary dysfunction |
-
2014
- 2014-11-04 CA CA2928759A patent/CA2928759A1/en not_active Abandoned
- 2014-11-04 US US15/034,019 patent/US20160279209A1/en not_active Abandoned
- 2014-11-04 WO PCT/US2014/063784 patent/WO2015066664A2/en active Application Filing
- 2014-11-04 PE PE2016000563A patent/PE20160789A1/es not_active Application Discontinuation
- 2014-11-04 JP JP2016552448A patent/JP2016535782A/ja active Pending
- 2014-11-04 KR KR1020167012122A patent/KR20160078986A/ko not_active Application Discontinuation
- 2014-11-04 EP EP14857307.4A patent/EP3065705A4/en not_active Withdrawn
- 2014-11-04 CN CN201480060878.2A patent/CN105764488A/zh active Pending
- 2014-11-04 AU AU2014341862A patent/AU2014341862A1/en not_active Abandoned
- 2014-11-04 MX MX2016005720A patent/MX2016005720A/es unknown
-
2016
- 2016-05-03 CL CL2016001062A patent/CL2016001062A1/es unknown
-
2019
- 2019-01-28 US US16/259,112 patent/US11033611B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN105764488A (zh) | 2016-07-13 |
| US20190255157A1 (en) | 2019-08-22 |
| AU2014341862A1 (en) | 2016-05-19 |
| MX2016005720A (es) | 2016-11-25 |
| CL2016001062A1 (es) | 2017-01-13 |
| CA2928759A1 (en) | 2015-05-07 |
| EP3065705A4 (en) | 2017-10-18 |
| US11033611B2 (en) | 2021-06-15 |
| EP3065705A2 (en) | 2016-09-14 |
| JP2016535782A (ja) | 2016-11-17 |
| PE20160789A1 (es) | 2016-08-17 |
| WO2015066664A3 (en) | 2015-09-17 |
| US20160279209A1 (en) | 2016-09-29 |
| WO2015066664A2 (en) | 2015-05-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2792682T3 (es) | Métodos para el tratamiento de enfermedades pulmonares con estabilizadores de mastocitos | |
| US8709496B2 (en) | Use of deuterium oxide for the treatment of virus-based diseases of the respiratory tract | |
| US11033611B2 (en) | Compositions and methods for administration of an enzyme to a subject's airway | |
| JP6397984B2 (ja) | 乾燥粉末ペプチド医薬 | |
| JP5970465B2 (ja) | ペプチドおよびウイルス・ノイラミニダーゼ阻害剤を含んでなる組成物 | |
| WO2022009081A1 (en) | Drug for use against the novel coronavirus disease, covid-19 | |
| US20220160814A1 (en) | Compositions and methods for protecting type 2 alveolar epithelial cells (aec2) | |
| WO2021228875A1 (en) | Treatment of respiratory viral infections | |
| US20180140547A1 (en) | Compositions and methods for administration of an enzyme to a subject's airway | |
| KR102664833B1 (ko) | 나파모스타트 또는 카모스타트를 포함하는 흡입용 제제 | |
| TWI788779B (zh) | 一種治療病毒性肺炎的方法和藥物 | |
| US20240009227A1 (en) | Use of a heparin composition in the treatment of viral lung diseases, acute and/or chronic lung diseases by soft mist inhaler or vibration mesh technology nebulizer through inhalation route | |
| WO2022140817A1 (en) | Anti-viral proteases and methods of use | |
| WO2021188334A1 (en) | Use of st266 to treat severe systemic inflammation and post-acute covid-19 syndrome | |
| CA3173121A1 (en) | Methods and compositions for treating infections | |
| US20220168360A1 (en) | Compositions, devices, and methods for treating respiratory disorders | |
| Vanbever | Optimization of dry powder aerosols for systemic drug delivery | |
| Abdalaziz et al. | Formulation strategy for hydroxychloroquine as inhaler dosage from as a potential for COVID-19 treatment |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |