KR20140109509A - 펩타이드의 지속 방출 전달을 위한 의약 조성물 - Google Patents
펩타이드의 지속 방출 전달을 위한 의약 조성물 Download PDFInfo
- Publication number
- KR20140109509A KR20140109509A KR1020147023622A KR20147023622A KR20140109509A KR 20140109509 A KR20140109509 A KR 20140109509A KR 1020147023622 A KR1020147023622 A KR 1020147023622A KR 20147023622 A KR20147023622 A KR 20147023622A KR 20140109509 A KR20140109509 A KR 20140109509A
- Authority
- KR
- South Korea
- Prior art keywords
- peptide
- polymer
- group
- peptides
- octreotide
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1808—Epidermal growth factor [EGF] urogastrone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/2278—Vasoactive intestinal peptide [VIP]; Related peptides (e.g. Exendin)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/25—Growth hormone-releasing factor [GH-RF] (Somatoliberin)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/26—Glucagons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/29—Parathyroid hormone (parathormone); Parathyroid hormone-related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/47—Hydrolases (3) acting on glycosyl compounds (3.2), e.g. cellulases, lactases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/34—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyesters, polyamino acids, polysiloxanes, polyphosphazines, copolymers of polyalkylene glycol or poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/542—Carboxylic acids, e.g. a fatty acid or an amino acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/543—Lipids, e.g. triglycerides; Polyamines, e.g. spermine or spermidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
Abstract
본 발명은 생체적합성이며, 비수용성이고, 생체분해성을 갖는 폴리머의 유효량과 하나 이상의 친지성 또는 양친성 모이어티에 의해 공유적으로 변형된 치료용 펩타이드의 유효량이 생체적합성이고 수용성인 유기 용매 중에 용해 또는 분산되어 있는 형태로 포함된 액상의 의약 조성물을 투여함으로써, 체내에서 현장(in situ)로 고상의 생체분해성 임플란트를 형성하는 방법을 제공하다.
Description
관련 출원
본 출원은 2006년 7월 11일자로 출원된 미국 가특허출원 제 60/830,011호의 우선권 주장 출원으로서, 상기 출원의 내용은 본 출원 발명에 참고로 통합된다.
본 출원 명세서 전반에 걸쳐, 여러가지 문헌이 인용된다. 이들 문헌의 개시 내용 역시 본 출원에 참고로 통합시켜 본 발명이 속한 기술 분야의 기술 수준을 보다 완벽하게 설명하고자 한다.
1. 발명의 분야
본 발명은 치료용 펩타이드의 조절적 방출 전달 분야 및 하나 이상의 친지성 또는 양친성 분자에 의해 공유적으로 변형된 치료용 펩타이드의 조절적 방출 전달에 유용한 조성물 및 방법에 관한 것이다.
2. 관련 기술에 관한 설명
펩타이드, 또는 달리 올리고펩타이드, 폴리펩타이드 및 단백질은 치료제로서 널리 사용되어 왔다. 펩타이드들은 재조합 DNA 기술에 의해 간편하게 생산될 수 있으며 또는 잘 알려진 펩타이드 합성 기술에 의해 합성될 수도 있다. 그러나, 많은 펩타이드들은 효소에 의해 분해되기 쉽고 생체내 순환 반감기가 대단히 짧다. 따라서, 대부분의 펩타이드 약품은 주사에 의해, 일반적으로 하루에 수차례에 걸쳐 투여되어 왔다. 따라서, 안전성, 효능 및 환자의 편리성을 개선시키기 위해 연장되니 기간 동안 조절적인 방식으로 이러한 펩타이드를 전달할 수 있다면 매우 바람직할 것이다.
생체분해성(biodegradable) 폴리머는 치료용 펩타이드를 지속적으로 전달하는데 사용되어 왔다. 이러한 펩타이드는 일반적으로 폴리머 조성물에 혼입되어 막대형, 웨이퍼형 및 미립자와 같은 목적하는 형태로 체외에서 만들어진다. 이렇게 만들어진 고상 조성물은 절개 또는 주사에 의해 체내로 삽입될 수 있다. 별법으로 그리고 바람직하게는, 이러한 폴리머 조성물 중 몇가지는 액상 폴리머 조성물로서 체내에 주사되어 임플란트를 현장(in situ) 형성할 수 있다. 약물을 조절적인 방식으로 전달하기 위하여, 임플란트를 현장(in situ) 형성하기 위한 주사가능한 액상 생체분해성 폴리머 조성물은 여러 특허 문헌에 설명되어 있다. 다음의 인용 문헌들은 이 분야의 대표적인 문헌인 것으로 믿어지며 본 발명에 그 내용이 참고로 통합되었다: 미국 특허 6,565,874; 6,528,080; RE37, 950; 6,461,631; 6,395,293; 6,355,657; 6,261,583; 6,143,314; 5,990,194; 5,945,115; 5,792,469; 5,780,044; 5,759,563; 5,744,153; 5,739,176; 5,736,152; 5,733,950; 5,702,716; 5,681,873; 5,599,552; 5,487,897; 5,340,849; 5,324,519; 5,278,202; 5,278,201; 및 4,938,763. 여기에 설명된 바와 같이, 생물활성 제제는 생체적합성 유기 용매 중의 생체분해성 폴리머 용액에 용해 또는 분산되어 액상 조성물을 형성한다. 액상 조성물이 체내로 주사되면, 용매가 주변의 수성 환경 내로 소산되어 폴리머가 침전됨으로 해서 고상 또는 겔상의 데포(depot)를 형성하고 이로부터 생물활성 물질이 폴리머가 분해됨에 따라 장기간 방출되게 된다. 이러한 전달계의 사용은 진전된 전립선암을 치료하기 위한 류프롤라이드 아세테이트 (EligardTM)을 전달하기 위해 예시되었다. 몇건의 성공에도 불구하고, 이러한 방법은 이러한 접근법에 의해 효과적으로 전달되었을 수 있는 다수의 펩타이드에 있어서는 전적으로 만족스럽지는 못하였다.
많은 치료용 펩타이드의 경우, 폴리(DL-락타이드-코-글리콜라이드)의 마이크로스피어에 봉입된 펩타이드의 아실화 및/또는 분해가 방출 프로세스 중에 관찰되어 왔다. 예컨대, 문헌 [Na DH , Youn YS , Lee SD , Son MO , Kim WA , DeLuca PP , Lee KC. J Control Release . 2003; 92(3):291-9]참조. 펩타이드 상의 친핵성 작용기들은 생체분해성 폴리머와 반응할 수 있을 뿐만 아니라, 생체분해성 폴리머의 분해를 촉매할 수도 있다. 또한 아실화 및/또는 분해는 고체 상태에서 있을 때보다 폴리머 용액 중에서 훨씬 신속하게 일어난다는 것 역시 밝혀졌다. 예컨대, 카르복실 말단기를 갖는 50/50 폴리(DL-락타이드-코-글리콜라이드)와 옥트레오타이드 아세테이트를 NMP 중에서 혼합하자, 24시간 이내에 80%를 상회하는 옥트레오타이드가 아실화 및/또는 분해되었다. 이 펩타이드와 폴리머 또는 그의 분해 산물 간의 상호반응/반응은 포뮬레이션 도중, 보관 도중 및 투여 중에 일어날 수 있다. 따라서, 포뮬레이션의 안정성을 유지하기 위해, 펩타이드를 별도의 시린지에 공급하는 한편, 나머지 성분들은 다른 시린지에 밀봉한다. 시린지 내의 내용물은 사용 직전에 혼합시킨다. 그러나, 폴리머 포뮬레이션의 점성으로 인해, 최종 사용자에게는 종종 두가지 별개의 시린지들의 내용물을 한데 혼합하는 것이 어렵다. 최종 사용자들에 의해 제조된 포뮬레이션의 균질성은 크게 변할 수 있고, 오염 역시도 발생할 수 있기 때문에, 치료의 품질도 크게 저하될 가능성이 있다. 뿐만 아니라, 주사가능한 액상 폴리머 포뮬레이션으로부터 고상 임플랜트를 현장(in situ) 형성하는 것은 느린 프로세스이다. 일반적으로 용매의 소산(dissipation)/확산(diffusion) 프로세스는 몇시간 내지 며칠이 걸릴 수 있고 심지어는 사용되는 용매에 따라 더 오래 걸릴수도 있다. 이 기간 동안, 유기 용매가 존재하면 펩타이드와 폴리머 또는 그의 분해 산물 간의 상호반응/반응이 촉진될 수 있다.
또한, 임플란트가 형성되는 동안, 응집 폴리머 조성물로부터 펩타이드가 확산되는 속도는, 후속적으로 형성되는 고상 임플란트로부터 일어나는 방출 속도보다 훨씬 빠를 수 있다. 임플란트가 형성되는 동안 펩타이드의 이와 같은 최초의 "분출(burst)" 방출로 인하여, 치료적 펩타이드는 대량으로 유실되거나 방출될 수 있다. 펩타이드가 특히 독성을 갖는 것이거나 치료 범위(therapeutic window)가 좁은 것일 경우에는, 이러한 최초의 방출 또는 분출로 인해 독성 부작용이 야기되거나 인접한 조직에 따기 손상이 가해질 염려가 있다. 따라서, 고상 임플란트의 이러한 더딘 형성 프로세스와 생물활성 물질 및/또는 부형제의 불안정성으로 인하여, 치료용 펩타이드의 서방형 전달에 이러한 유형의 포뮬레이션을 사용하는 것이 매우 심각한 장애 요인이 된다.
지방산과 같은 친지성 분자로 펩타이드를 공유적으로 변형(covalent modification) 시키면 알부민에 대한 결합을 통한 생체내 순환 반감기를 증가시킴으로써 치료 효능이 증진되는 것으로 설명되어 왔다 [[EP0708179-A2, EP0699686-A2, US 6268343, Knudsen LB, Nielsen PF, Huusfeldt PO, Johansen NL, Madsen K, Pedersen FZ, Thogersen H, Wilken M, Agerso H. Potent derivatives of glucagon-like peptide-1 with pharmacokinetic properties suitable for once daily administration. J Med Chem. 2000, 43(9):1664-9; Kurtzhals P, Havelund S, Jonassen I, Kiehr B, Larsen UD, Ribel U, Markussen J. Albumin binding of insulins acylated with fatty acids: characterization of the ligand-protein interaction and correlation between binding affinity and timing of the insulin effect in vivo. Biochem J. 1995;312 (3):725-31, 및 이들 문헌에 인용된 다른 참조 문헌들]. 비록 친지적으로 변형된 펩타이드들은 천연 펩타이드에 비해 생체내에서 연장된 활성을 나타내기는 하지만, 변형된 펩타이드의 혈장 체류 시간은 알부민에 대한 그의 결합 친화도에 의해 제한을 받는다. 한가지 성공적인 사례는 아실화 인슐린 (Detemir)인데, 이것은 순환 반감기가 10.2 ± 1.2 시간이다. [Havelund S, Plum A, Ribel U, Jonassen I, Voelund A, Markussen J and Kurtzhals P, Pharmaceutical Research, 2004; 21 (8), 1498-1504]. 이 생성물은 I형 당뇨병 환자들을 치료하기 위한 주사제로 승인되었다. 그러나, 이 물질 역시 환자들에게 매일 투여되어야 한다.
따라서, 특정 펩타이드, 특히 장기간 동안 지속적으로 방출될 필요가 있는 펩타이드의 전달 속도를 훨씬 용이하게 조절할 수 있는, 안정한 조성물이 여전히 절실히 요구되는 실정이다.
발명의 개요
놀랍게도, 하나 이상의 친지성 및/또는 양친성 분자에 의해 공유적으로 변형된 펩타이드를 생체분해성 폴리머와 함께 조성시킴으로써, 컨쥬게이트되지 않은(non-conjugated) 펩타이드에 비하여 안정성과 지속 방출 프로파일을 크게 향상시킬 수 있는 것으로 밝혀졌다. 친지성 및/또는 양친성으로 변형된 펩타이드는 제조 과정, 보관 과정 및 후속적인 생체내 방출 과정에서, 조절되지 않은 무작위적인 펩타이드의 아실화 및 분해를 방지하여 줄 뿐만 아니라, 펩타이드의 원치 않는 최초의 분출 방출량도 감소시킬 수 있다. 이러한 전달 시스템은 더 높은 농도의 치료용 펩타이드를 생체분해성 폴리머 전달 시스템 내로 안전하게 혼입시킬 수 있게 해준다. 이러한 제품의 효능 역시 개선되는데, 이는 온전한 활성 펩타이드가 훨씬 더 높은 비율로 서방형 전달 시스템 내에 남아있기 때문에 포뮬레이션 도중, 보관시, 투여시 및 후속적인 생체내 방출시, 분해에 의한 손실이 일어나지 않기 때문이다.
따라서, 본 발명은 치료용 펩타이드를 조절적이고도 서서히 방출시키기 위한 신규한 약학적 포뮬레이션을 제공한다. 본 발명의 조성물은 (a) 하나 이상의 친지성 분자(들)과 공유적으로 컨쥬게이트된 펩타이드; (b) 생체분해성 폴리머; 및 (c) 약학적으로 허용가능한 유기 용매를 포함하여 이루어진다. 여기서 상기 펩타이드는 하나 이상의 친지성 분자(들)과 공유적으로 컨쥬게이트되어 있되, 이렇게 컨쥬게이트된 펩타이드는, 컨쥬게이트되지 않은 펩타이드의 생물학적 활성을 전부 또는 거의 유지하는 한편, 시험관내 및 생체내 양쪽 모두에서, 컨쥬게이트되지 않은 펩타이드에 비하여 상대적으로 생체분해성 폴리머와의 반응에 대한 화학적 내성이 더 증강된 방식으로 컨쥬게이트되어 있다. 이어서, 친지적으로 변형된 (lipophilically modified) 펩타이드는 약학적으로 허용가능한 유기 용매를 이용하여 생체분해성 폴리머 용액에서 용해 또는 분산시킴으로써 조성된다. 본 발명의 포뮬레이션은 포뮬레이션 도중, 보관시, 투여시 및 후속적인 방출시 펩타이드의 안정성을 증강시켜 줄 뿐만 아니라, 초기 분출 레벨은 더 낮춰주는 한편, 연장된 기간 동안 방출 프로파일을 향상시켜준다.
또 다른 측면에서, 본 발명은 (a) 하나 이상의 양친성 모이어티와 공유적으로 컨쥬게이트된 펩타이드; (b) 생체분해성 폴리머; 및 (c) 약학적으로 허용가능한 유기 용매를 포함하는 조성물을 제공한다. 여기서 상기 펩타이드는 하나 이상의 양친성 분자(들)과 공유적으로 컨쥬게이트되어 있되, 이렇게 컨쥬게이트된 펩타이드는, 컨쥬게이트되지 않은 펩타이드의 생물학적 활성을 전부 또는 거의 유지하는 한편, 시험관내 및 생체내 양쪽 모두에서, 컨쥬게이트되지 않은 펩타이드에 비하여 상대적으로 생체분해성 폴리머와의 반응에 대한 화학적 내성이 더 증강된 방식으로 컨쥬게이트되어 있다. 이어서, 양친성으로 변형된 (amphiphilically modified) 펩타이드는 약학적으로 허용가능한 유기 용매를 이용하여 생체분해성 폴리머 용액에서 용해 또는 분산시킴으로써 조성된다. 본 발명의 포뮬레이션은 포뮬레이션 도중, 보관시, 투여시 및 후속적인 방출시 펩타이드의 안정성을 증강시켜 줄 뿐만 아니라, 초기 분출 레벨은 더 낮춰주는 한편, 연장된 기간 동안 방출 프로파일을 향상시켜준다. 이와 같이 컨쥬게이트된 펩타이드는 또한, 이 펩타이드의 친핵성 기에 의해 폴리머의 촉매 분해를 감소시켜준다.
본 발명의 각각의 조성물은 주사기를 이용하여 주사될 수 있도록 플루이드로서 이동하는, 점성 또는 비점성 액체, 겔 또는 반고체일 수 있다. 각각의 조성물은 시험관내에서 이식가능한 폴리머 매트릭스로서 형성될 수 있으며, 또는 별법으로 겔 또는 고형 임플란트 형태로서 현장(in situ) 형성될 수 있다. 본 발명의 조성물은 주사 및/또는 피하, 근육내, 복강내 또는 피내 이식(implantation)에 의해 투여될 수 있다. 대상자에게 투여되는 경우, 이러한 펩타이드의 조절적 방출은 임플란트의 조성에 따라 원하는 기간만큼 지속될 수 있다. 생체분해성 폴리머 및 다른 부형제의 선택에 따라, 펩타이드의 지속 방출 기간을 수주일에서 1년까지 조절할 수 있다.
본 발명을 특징짓는 여러가지 신규한 특징들은 본 명세서에 첨부되어 본 명세서의 일부를 구성하는 특허청구범위에 특히 잘 표현되어 있다. 본 발명을 더욱 쉽게 이해할 수 있도록, 그 작동상의 장점 및 이를 사용함으로써 달성되는 특수한 목적들을 첨부된 도면 및 발명의 상세한 설명에 상세히 기술하였으나, 이러한 설명과 도면은 본 발명의 바람직한 구체예를 설명하기 위한 것일 뿐 본 발명의 범위가 이에 한정되는 것은 아니다.
도 1은 mPEG350 중 RG503H 용액의 포뮬레이션으로부터의 리소자임 및 팔미트산 아실화 리소자임의 시험관내 방출 프로필을 도시한 도면이다.
도 2는 mPEG350 중 RG503H 용액의 포뮬레이션으로부터의 그렐린 및 탈아실화 그렐린의 시험관내 방출 프로필을 도시한 도면이다.
도 3은 NMP 중 DLPLG85/15 (IV 0.28) 용액의 포뮬레이션으로부터의 옥트레오타이드의 시험관내 방출 프로필을 도시한 도면이다.
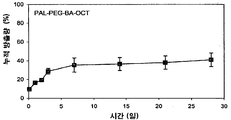
도 4는 NMP 중 DLPLG85/15 (IV 0.28) 용액의 포뮬레이션으로부터의 변형된 옥트레오타이드 (Pal-PEG-BA-OCT)의 시험관내 방출 프로필을 도시한 도면이다.
도 2는 mPEG350 중 RG503H 용액의 포뮬레이션으로부터의 그렐린 및 탈아실화 그렐린의 시험관내 방출 프로필을 도시한 도면이다.
도 3은 NMP 중 DLPLG85/15 (IV 0.28) 용액의 포뮬레이션으로부터의 옥트레오타이드의 시험관내 방출 프로필을 도시한 도면이다.
도 4는 NMP 중 DLPLG85/15 (IV 0.28) 용액의 포뮬레이션으로부터의 변형된 옥트레오타이드 (Pal-PEG-BA-OCT)의 시험관내 방출 프로필을 도시한 도면이다.
본 발명은 펩타이드를 조절적으로 방출시키는 전달 시스템을 형성하기 위한 주사가능한 생체분해성 액상 폴리머 조성물을 제공한다. 본 발명은 또한 이의 제조 방법과 사용 방법도 제공한다.
본 발명의 조성물은 (a) 하나 이상의 친지성 분자와 바람직하게는 공유적으로 컨쥬게이트된 펩타이드; (b) 약학적으로 허용가능한 비수용성 생체분해성 폴리머; 및 (c) 약학적으로 허용가능한 유기 용매를 포함하여 이루어진다. 상기 펩타이드는 하나 이상의 친지성 분자(들)과 공유적으로 컨쥬게이트되어 있되, 이렇게 컨쥬게이트된 펩타이드는, 컨쥬게이트되지 않은 펩타이드의 생물학적 활성을 전부 또는 거의 유지하는 한편, 시험관내 및 생체내 양쪽 모두에서, 컨쥬게이트되지 않은 펩타이드에 비하여 상대적으로 생체분해성 폴리머와의 반응에 대한 화학적 내성이 더 증강된 방식으로 컨쥬게이트되어 있다. 이어서, 친지적으로 변형된 펩타이드는 약학적으로 허용가능한 유기 용매를 이용하여 생체분해성 폴리머 용액에서 용해 또는 분산시킴으로써 조성된다. 본 발명의 포뮬레이션은 포뮬레이션 도중, 보관시, 투여시 및 후속적인 방출시 펩타이드의 안정성을 증강시켜 줄 뿐만 아니라, 초기 분출 레벨은 더 낮춰주는 한편, 연장된 기간 동안 방출 프로파일을 향상시켜준다.
또 다른 측면에서, 본 발명은 (a) 하나 이상의 양친성 분자와 공유적으로 컨쥬게이트된 펩타이드; (b) 약학적으로 허용가능한, 비수용성 생체분해성 폴리머; 및 (c) 약학적으로 허용가능한 유기 용매를 포함하는 조성물을 제공한다. 여기서 상기 펩타이드는 하나 이상의 양친성 분자(들)과 공유적으로 컨쥬게이트되어 있되, 이렇게 컨쥬게이트된 펩타이드는, 컨쥬게이트되지 않은 펩타이드의 생물학적 활성을 전부 또는 거의 유지하는 한편, 시험관내 및 생체내 양쪽 모두에서, 컨쥬게이트되지 않은 펩타이드에 비하여 상대적으로 생체분해성 폴리머와의 반응에 대한 화학적 내성이 더 증강된 방식으로 컨쥬게이트되어 있다. 이어서, 양친성으로 변형된 펩타이드는 약학적으로 허용가능한 유기 용매를 이용하여 생체분해성 폴리머 용액에서 용해 또는 분산시킴으로써 조성된다. 본 발명의 포뮬레이션은 포뮬레이션 도중, 보관시, 투여시 및 후속적인 방출시 펩타이드의 안정성을 증강시켜 줄 뿐만 아니라, 초기 분출 레벨은 더 낮춰주는 한편, 연장된 기간 동안 방출 프로파일을 향상시켜준다. 이와 같이 컨쥬게이트된 펩타이드는 또한, 이 펩타이드의 친핵성 기에 의해 폴리머의 촉매 분해를 감소시켜준다.
본 명세서에서, "a", "an", 및 "one" 등의 용어는 "하나 이상" 또는 "적어도 하나"의 의미로 해석되는 것으로 한다.
"펩타이드"라는 용어는 "폴리펩타이드"와 "단백질"과 동의적으로 사용된다. 펩타이드가 지닐 수 있는 치료적 특징의 예로는 항대사성, 항진균성, 항염, 항종양, 항감염, 항생, 영양, 아고니스트 및 안타고니스트 특성 등을 들 수 있으나 이에 한정되지 않는다.
더욱 구체적으로, 본 발명의 펩타이드는 친지성 또는 양친성 분자(들)에 의해 공유적으로 변형될 수 있다. 이 펩타이드는 바람직하게는 하나 이상의 변형가능한 작용기들을 함유하는 것이 좋다. 본 발명의 포뮬레이션을 조제하는데 유용한 펩타이드로는 옥시토신, 바소프레신, 부신피질자극 호르몬(ACTH), 상피 성장 인자 (EGF), 혈소판 유래 성장 인자 (PDFG), 프롤락틴, 호르몬, 예컨대, 황체형성 호르몬, 황체형성호르몬분비호르몬 (LHRH), LHRH 아고니스트, LHRH 안타고니스트, 성장호르몬, 성장호르몬 방출인자, 인슐린, 에리쓰로포이에틴, 소마토스타틴, 글루카곤, 인터류킨, 인터페론-알파, 인터페론-베타, 인터페론-감마, 가스트린, 테트라가스트린, 펜타가스트린, 우로가스트론, 세크레틴, 칼시토닌, 엔케팔린, 엔도르핀, 안지오텐신, 갑상선자극호르몬분비호르몬 (TRH), 종양괴사인자 (TNF), 부갑상선 호르몬 (PTH), 신경성장인자 (NGF), 과립구-콜로니 형성 자극인자 (G-CSF), 과립구 마크로파지-콜로니 자극인자 (GM-CSF), 마크로파지-콜로니 자극인자 (M-CSF), 헤파리나제, 혈관내피성장인자 (VEG-F), 골형태형성 단백질 (BMP), hANP, 글루카곤-유사 펩타이드 (GLP-1), 엑세나타이드, 펩타이드 YY (PYY), 그렐린, 레닌, 브래디키닌, 바시트라신, 폴리믹신, 콜리스틴, 티로시딘, 그라미시딘, 사이클로스포린, 효소, 사이토카인, 항체, 백신, 항생제, 항체, 당단백질, 난포자극 호르몬, 키오토르핀,타프트신, 티모포이에틴, 티모신, 티모스티뮬린, 흉선 체액 인자, 혈청 흉선 인자, 콜로니 자극 인자, 모틸린, 봄베신, 디노르핀, 뉴로텐신, 세룰레인, 우로키나제, 칼리크레인, 물질 P 유사체 및 안타고니스트, 안지오텐신 II, 혈액 응고 인자 VII 및 IX, 리소자임, 그라미시딘, 멜라노사이트 자극 호르몬, 갑상선 호르몬 분비 호르몬, 갑상선 자극 호르몬, 판크레오지민, 콜레시스토키닌, 인간 태반 락토겐, 인간 융모막 고나도트로핀, 단백질 합성 자극 펩타이드, 위 억제 펩타이드, 혈과작용성 장 펩타이드, 혈소판 유래 성장인자, 색소 호르몬, 소마토메딘, 융모막 고나도트로핀, 시상하부 분비 호르몬, 항이뇨 호르몬, 갑상선 자극 호르몬, 비팔린 및 프롤락틴을 들 수 있으나 이에 한정되지 않는다.
본 명세서에서, "친지성 모이어티(lipophilic moiety)"라는 용어는 친지 특성을 갖는 한편 20℃에서 물에 대한 용해도가 5 mg/ml 미만, 바람직하게는 0.5 mg/ml 미만인 모이어티를 가리킨다. 이러한 친지성 모이어티는 일반적으로 C3 -39-알킬, C3 -39-알케닐, C3 -39-알카디에닐, 토코페롤 및 스테로이드계 잔기 중에서 선택된다. "C3 -39-알킬", "C3 -39-알케닐" 및 "C3 -39-알카디에닐"이라는 용어는 직쇄 및 분지상, 바람직하게는 직쇄상의, 포화, 일불포화(monounsaturated) 및 이불포화된(di-unsaturatd) 탄소 원자 3-39개의 탄화수소를 모두 포괄한다.
펩타이드에 대한 친지성 모이어티의 공유 컨쥬게이션에 의해, 천연 펩타이드에 비해 개선된 치료 효과를 갖는 친지적으로 변형된 펩타이드를 얻을 수 있다. 이것은 일반적으로 친지성 분자 중의 산 또는 다른 반응성 기와 펩타이드 중의 아민기와 같은 작용기와의 반응에 의해 행해질 수 있다. 별법으로, 펩타이드와 친지성 분자 간의 컨쥬게이션은 브릿지, 스페이서, 또는 연결 모이어티 (linkage moiety)와 같이 분해성 또는 비분해성인 부가적인 모이어티를 통해 수행할 수도 있다. 이에 관한 예가 종래 기술 문헌에 개시되어 있다 [예컨대, 지방산-아실화 인슐린은 일본 특허 출원 1,254,699호에 설명되어 있다. 또한, Hashimoto, M., et al., Pharmaceutical Research, 6:171-176 (1989), and Lindsay, D. G., et al., Biochemical J., 121:737-745 (1971) 참조]. 지방산-아실화 인슐린 및 지방 아실화되니 인슐린 유사체, 및 이들의 합성 방법에 대한 추가적인 개시 내용은 미국 특허5,693,609, WO95/07931, 미국 특허 5,750,497, 및 WO96/29342에서 찾아볼 수 있다. 아실화 펩타이드의 또 다른 예는 WO98/08871, WO98/08872, 및 WO99/43708에서 찾아볼 수 있다. 이들 개시 내용은 친지적으로 변형된 펩타이드에 대하여 설명하고 있으며 이들의 제조 방법도 설명하고 있다.
본 명세서에서, "양친성 모이어티"라는 용어는 친지성 및 친수성 특성을 두가지 모두 갖는 한편, 물과 친지성 용매 두가지 모두에 가용성인 모이어티를 가리킨다. 본 발명에서 사용되는 양친성 분자는 친지성 모이어티와 친수성 모이어티로 구성된다. 친지성 모이어티는 좋기로는 천연의 지방산 또는 알킬 사슬이며 상기 설명된 것들이다. 친수성 모이어티는 폴리에틸렌 글리콜, 폴리비닐피롤리돈, 슈가 등에서 선택된다. 친수성 모이어티는 바람직하게는 1000개 미만의 에틸렌 글리콜 유닛을 갖는 폴리에틸렌 글리콜 (PEG)인 것이 좋다. 친지성 모이어티 및 친수성 모이어티의 크기와 조성은 소망되는 양친성을 획득할 수 있도록 적절히 조정될 수 있다.
본 명세서에서, "컨쥬게이트되다", "연결되다", "결합되다" 등등의 용어가 본 발명의 펩타이드 및 기타 변형된 펩타이드의 다른 성분들과 연관되어 사용될 경우, 이들 용어는 특정된 모이어티가 다른 모이어티에, 바람직하게는 공유적으로, 링커, 브릿지, 스페이서 등을 통해 결합되어 있음을 의미한다.
본 명세서에서, "링커", "브릿지", "스페이서" 등의 용어는 예컨대 친지서어 모이어티를 치료용 펩타이드에 바람직하게는 공유적으로 연결시켜주는 원자 또는 원자단을 가리킨다.
공유적 컨쥬게이션을 수행하기 위해, 치료용 펩타이드는 하나 이상의 적절한 작용기를 가질 수 있으며, 또는 친지성 또는 양친성 모이어티에 대한 공유 커플링을 위해 하나 이상의 적절한 작용기를 포함하도록 변형될 수 있다. 적절한 작용기로는 다음을 예시할 수 있다: 히드록실기, 아미노기 (일차 아미노기 또는 이차 아미노기), 티올기, 및 카르복실기. 본 발명의 친지성 모이어티 또는 양친성 모이어티는 하나 이상의 적절한 작용기를 갖거나 또는 펩타이드에 대한 공유 커플링을 위하여 하나 이상의 적절한 작용기를 포함하도록 변형될 수 있다. 적절한 작용기에는 예컨대 다음 기가 포함된다: 히드록실기, 아미노기 (일차 아미노기 또는 이차 아미노기), 티올기, 카르복실기, 알데히드기, 이소시아네이토기, 설폰산기, 황산기, 인산기, 포스폰산기, 알릴릭 할라이드기, 벤질릭 할라이드기, 치환 된 벤질릭 할라이드기 및 옥시라닐기.
치료용 펩타이드는 에스테르기, 아미드기, 2차 또는 3차 아민기, 카바메이트기, 설포네이트기, 설페이트기, 포스페이트기, 포스포네이트기, 또는 에테르기를 통해 하나 이상의 친지성 모이어티에 직접 또는 간접적으로 커플링될 수 있다.
본 발명의 일 구체예에서, 팔미트산을 N-히드록시숙신이미드로 활성화시킨 다음 옥타펩타이드인 옥트레오타이드 상의 아민기와 반응시켜 팔미틸 친지성 모이어티와 펩타이드 사이의 아미드 링커를 통해 컨쥬게이트를 형성시켰다. 옥트레오타이드 상에는 일차 아민기가 두개 있다. 두개의 아민기는 반응 조건을 조정함으로써 두개 모두 동시에 컨쥬게이트될 수도 있고 또는 오직 하나의 아민기만 선택적으로 컨쥬게이트시킨 다음 분리시킬 수도 있다.
*또 다른 구체예에서는 알데히드 말단기를 갖는 친지성 화합물인 디캐널(decanal)을 옥트레오타이드 상의 아민기와 반응시켜 2차 아민 결합을 통하여 컨쥬게이트를 형성시켰다. 두개의 아민기 모두 동시에 컨쥬게이트될 수도 있고 또는 반응 조건을 조정하여 하나의 아민기만을 컨쥬게이션시킨 다음 분리할 수도 있다.
또 다른 구체예에서는, 팔미트산을 리소자임에 그의 6개 아민기를 통해 몇가지 비율로 컨쥬게이트시켰다. 팔미트산 대 리소자임의 비율이 6 미만이면, 리소자임 상의 컨쥬게이션 위치는 각각의 아민기의 반응성에 따라 무작위적으로 달라진다.
또 다른 구체예에서, 그렐린은 그의 히드록실기를 통해 n-옥타노일 모이어티에 의해 아실화된 펩타이드이다. 그렐린은 성장호르몬 분비를 촉진하여, 비만증을 증가시키는 위의 펩타이드이다. 이것은 뇌의 뇌하수체샘과 시상하부에 존재하는, 이전에 클론된 성장 호르몬 분비 수용체에 대하여 최초로 동정된 천연 리간드이다.
친지성 모이어티는 먼저 친수성 모이어티에 공유적으로 커플링되어 양친성 분자를 형성할 수 있다. 본 발명의 양친성 분자는 하나 이상의 적절한 작용기를 갖거나, 또는 펩타이드에 공유적으로 커플링되기 위한 하나 이상의 적절한 작용기를 갖도록 변형될 수 있다. 이러한 적절한 작용기는 히드록실기, 아미노기 (일차 아미노기 또는 이차 아미노기), 티올기, 카르복실기, 알데히드기, 이소시아네이토기, 설폰산기, 황산기, 인산기, 포스폰산기, 알릴릭 할라이드기, 벤질릭 할라이드기, 치환된 벤질릭 할라이드기 및 옥시라닐기 중에서 선택된다.
치료용 펩타이드는 에스테르기, 아미드기, 이차 또는 삼차 아민기, 카바메이트기, 설포네이트기, 설페이트기, 포스페이트기, 포스포네이트기 또는 에테르기르르 통해 하나 이상의 양친성 모이어티와 직간접적으로 커플링될 수 있다.
바람직하게는 치료용 펩타이드는 (a) 친수성 모이어티 및 (b) 친지성 모이어티를 포함하는 하나 이상의 양친성 분자에 공유적으로 컨쥬게이트되며, 여기서 상기 양친성 분자의 균형잡힌 친지성 및 친수성 특성으로 인해 컨쥬게이트는 체액이나 수용액에서 적절한 용해도를 갖게 된다.
더욱 바람직하게는, 치료용 펩타이드는 (a) 선형 폴리에틸렌 글리콜 모이어티 및 (b) 친지성 모이어티를 포함하는 하나 이상의 양친성 분자에 공유적으로 컨쥬게이트되는 것이 좋고, 여기서 상기 치료용 펩타이드, 폴리에틸렌 글리콜 및 친지성 모이어티는 친지성 환경이나 세포막과의 상호작용에 이용될 수 있도록 친지성 모이어티를 외부에 갖도록 공간적으로 배치되어 있다. 이러한 양친성 변형된 펩타이드는 시험관내 및 생체내 모두에서 생체분해성 폴리머와의 반응에 대해, 컨쥬게이트되지 않은 펩타이드보다 증강된 화학적 내성을 갖는다.
바람직하게는, 양친성 분자는 다음의 구조식을 갖는 것이 좋다: L-S-(OC2H4)mOH (화학식 1), 식 중, L은 바람직하게는 C3 -39-알킬, C3 -39-알케닐, C3 -39-알카디에닐, 토코페롤 및 스테로이드 잔기 중에서 선택되는 친지성 모이어티이고, S는 에스테르기, 아미드기, 2차 또는 3차 아민기, 카바메이트기, 설포네이트기, 설페이트기, 포스페이트기, 포스포네이트기 또는 에테르 기 중에서 선택된 링커이다.
일 구체예에서, 탄소 원자 16개의 알킬기를 에테르 결합을 통해 폴리에틸렌 글리콜 분자에 공유적으로 커플링시켰다. 얻어진 양친성 분자는 하나의 히드록실기를 가지며, 이것은 펩타이드 상의 적절한 작용기와 반응하도록 활성화 또는 유도화시킬 수 있다. 본 발명의 일 구체예에서, 양친성 분자를 유도화시켜 알데히드 말단기를 갖도록 할 수 있다. 이어서, 이 양친성 분자를 옥트레오타이드 상의 아민기와 반응시킴으로써 옥트레오타이드에 공유적으로 컨쥬게이트시킨 다음 NaCNBH3와 환원 반응시킨다. 옥트레오타이드 상의 2개의 아민기는 반응 조건을 조정함으로써 두개 모두는 동시에 컨쥬게이트될 수도 있고 또는 오직 하나의 아민기만을 선택적으로 컨쥬게이트시킨 다음 분리할 수도 있다. 컨쥬게이트는 컨쥬게이트되지 않은 옥트레오타이드의 전하 특성을 변화시키지 않는 2차 아민을 통해 형성되었다. 이 특성은 상기 펩타이드의 활성을 유지하는 데 유용할 수 있다.
또 다른 구체예에서, 양친성 분자인 모노팔미틸 폴리(에틸렌 글리콜) (Mn ~ 1124)를 4-니트로페닐 클로로포르메이트를 이용하여 활성화시켰다. 이어서 양친성 분자를 옥트레오타이드 상의 아민기와의 반응을 통해 옥트레오타이드에 공유적으로 컨쥬게이트시켰다. 옥트레오타이드 상의 2개의 아민기는 반응 조건을 조정함으로써두개 모두 동시에 컨쥬게이트될 수도 있고 또는 오직 하나의 아민기만을 선택적으로 컨쥬게이트시킨 다음 분리할 수도 있다.
하나 이상의 친지성 또는 양친성 모이어티에 의해 공유적으로 변형된 펩타이드는 예컨대, 이 변형된 펩타이드의 약학적으로 허용가능한 염 및 착화합물을 포함한다. 변형은 펩타이드 상의 한군데 이상의 위치에서 일어날 수 있다. 이러한 펩타이드에는 또한, 예컨대 위치-특이적으로 변형된 펩타이드와, 단일 위치 및 복수개의 위치에서 변형된 펩타이드들의 혼합물도 포함된다.
"약학적으로 허용가능한 염"이라 함은 하나 이상의 약학적으로 허용가능한, 비독성 양이온 또는 음이온과 펩타이드에 있는 하나 이상의 하전된 기들 간에 형성된 염을 의미한다. 예컨대 유기염 및 무기염의 예로는 염산, 황산, 설폰산, 타르타르산, 푸마르산, 브롬화수소산, 글리콜산, 시트르산, 말레산, 인산, 숙신산, 아세트산, 질산, 벤조산, 아스코르브산, p-톨루엔설폰한, 벤젠설폰산, 나프탈렌설폰산, 프로피온산, 카르본산 등 또는 암모늄, 소듐, 포타슘, 칼슘 또는 마그네슘을 들 수 있다.
"생체분해성 비수용성 폴리머"라는 용어는 생체적합성 (즉, 약학적으로 허용가능한)이면서 생체분해성인, 생체내에서 사용될 수 있는 합성 또는 천연 폴리머를 가리킨다. 이 용어는 또한 37℃에서 물 또는 체액에 불용성이거나 불용성으로 되는 폴리머도 포괄한다. 이들 폴리머는 필요에 따라 기술 분야의 공지 기술을 이용함으로써 정제시켜 모노머와 올리고머를 제거할 수 있다 (예컨대, 미국 특허 4,728,721; 미국 특허 출원 2004/0228833). 이러한 폴리머의 비제한적인 예로는 폴리락타이드, 폴리글리콜라이드, 폴리카프로락톤, 폴리디옥산온, 폴리카보네이트, 폴리히드록시부티레이트, 폴리알킬렌 옥살레이트, 폴리안하이드라이드, 폴리아미드, 폴리에스테르아미드, 폴리우레탄, 폴리아세탈, 폴리오르토카보네이트, 폴리포스파젠, 폴리히드록시발레레이트, 폴리알킬렌 숙시네이트 및 폴리오르토에스테르, 및 이들의 코폴리머, 블록 코폴리머, 분지상 코폴리머, 터폴리머 및 조합(combination)과 혼합물을 들 수 있다.
폴리머의 적절한 분자량은 본 발명이 속한 기술 분야의 당업자라면 용이하게 결정할 수 있을 것이다. 분자량을 측정하기 위하여 고려될 수 있는 인자에는 바람직한 폴리머 분해 속도, 기계적 강도 및 용매 중 폴리머의 용해 속도가 포함된다. 일반적으로, 폴리머 분자량의 적절한 범위는 약 2,000 달톤 내지 약 150,000 달톤이며 다분산도(polydispersity)는 1.1 내지 2.8으로서, 이에 따라 특히 폴리머의 용도가 적절히 선택된다.
본 발명에 따라, 치료용 펩타이드의 약학적 포뮬레이션은, 분산되거나 용해된 친지성 또는 양친성으로 변형된 펩타이드를 함유하는 약학적으로 허용가능한 용매 중에 폴리머의 주사용 용액 또는 현탁액 형태로서 조제된다. 펩타이드를 친지성 또는 양친성 분자와 공유적으로 커플링시킴으로서, 펩타이드 내의 몇몇 반응성 기들이 보호되어 용액 중의 폴리머와 상호반응할 수 없게 된다. 따라서, 본 발명의 조성물 중 폴리머 및 펩타이드의 안정성은 펩타이드의 이러한 공유적 변형에 의해 향상된다.
따라서, 본 발명은 (a) 생체적합성, 비수용성 생체분해성 폴리머 및 하나 이상의 친지성 또는 양친성 모이어티에 의해 공유적으로 변형된 치료용 펩타이드를 생체적합성의 수용성 유기 용매에 용해 또는 분산시켜 조성물을 형성하는 단계 ( 여기서 상기 유기 용매는 신체 조직 내로 들어가게 되면 체액 내로 소산 또는 확산될 수 있는 것이다) (b) 상기 조성물을 체내의 임플란트 부위 내로 투여하여, 유기 용매를 체액 내로 소산 또는 확산시키고, 폴리머를 응고 또는 고형화시켜 생체분해성 고체 임플랜트를 생산하는 단계를 포함하는, 대상자 체내에서 고상의 생체분해성 임플란트를 현장(in situ) 형성하는 방법을 제공한다.
또한, 본 발명은 유효량의 생체적합성, 비수용성, 생체분해성 폴리머와 하나 이상의 친지성 또는 양친성 모이어티에 의해 공유적으로 변형된 유효량의 펩타이드가, 유효량의 생체적합성의 수용성 유기 용매 중에 용해 또는 분산된 상태로 포함되어 있는, 체내에서 생체분해성 임플란트를 현장(in situ) 형성하기 위한 의약 조성물을 제공하며; 여기서 상기 용매는 체액 내로 소산되거나 확산될 수 있는 것이고 상기 폴리머는 체액과 접촉시 응고 또는 고화될 수 있는 것이다.
적절한 펩타이드 및 친지성 또는 양친성 분자들은 상기 정의한 바와 같다. 컨쥬게이트 중에서 펩타이드 대 친지성 또는 양친성 분자의 몰 비율은 펩타이드의 성질에 따라 1:1 내지 1:10이다.
적당한 생체분해성 폴리머는 그 폴리머가 37℃의 체액이나 수성 매질에서 불용성이거나 불용성으로 되기만 하는 것이면, 어느 것이든 사용할 수 있다. 적절한 생체분해성 폴리머는 상기 정의한 바와 같다.
조성물 중에 존재하는 생체분해성 폴리머의 종류, 분자량 및 양은 조절 방출되는 임플란트로부터 펩타이드가 방출되는 시간에 용향을 미친다. 본 발명이 속하는 분야의 숙련가라면 일상적인 실험을 통하여 조절 방출되는 임플란트의 목적하는 특성을 얻기 위하여, 조성물 중에 존재하는 생체분해성 폴리머의 종류, 분자량 및 양을 선택할 수 있다.
약학적으로 허용가능한 유기 용매에는 N-메틸-2-피롤리돈, N,N-디메틸포름아미드, 디메틸 설폭사이드, 프로필렌 카보네이트, 카프로락탐, 트리아세틴, 벤질 벤조에이트, 벤질 알코올, 에틸 락테이트, 글리세릴 트리아세테이트, 시트르산의 에스테르, 폴리에틸렌 글리콜류, 알콕시폴리에틸렌 글리콜 및 폴리에틸렌 글리콜 아세테이트, 또는 이들의 조합이 포함되나 이에 한정되지 않는다.
생체분해성 폴리머의 유기 용매에 요구되는 조건은 이들이 약학적으로 허용가능하여야 하고 체액이나 수성 매질에 혼화되어 분산가능하여야 한다는 것이다. 적절한 유기 용매는, 액상 조성물이 응고 또는 고화하여 현장(in situ)에서 임플란트를 형성할 수 있도록, 체액 내로 확산될 수 있는 것이어야 한다. 단일 및/또는 혼합 용매를 사용할 수 있고, 이러한 용매의 적합성 여부는 통상적인 실험에 의해 용이하게 검정할 수 있다.
본 발명의 의약 조성물은 일반적으로 펩타이드를 0.1 내지 40% w/v의 양으로 함유한다. 일반적으로, 약물의 최적 부하량은 목적하는 방출 기간과 펩타이드의 효능에 따라 달라진다.
효능이 낮은 펩타이드인 경우, 그리고 장기간 방출을 요하는 경우, 더 많은 양으로 혼입시켜야 함은 자명하다.
본 발명의 주사가능한 액상 조성물의 점도는 사용되는 유기 용매 및 폴리머의 분자량에 따라 결정된다. 예컨대, 폴리(락타이드-코-글리콜라이드)가 사용될 경우, NMP 중의 폴리에스테르 용액은 mPEG350에서 보다 더 낮은 점도를 갖는다. 일반적으로, 동일한 용매가 사용될 경우, 폴리머의 분자량과 농도가 더 높을수록, 점도도 더 높아진다. 바람직하게는 용액 중 폴리머의 농도가 70 중량% 미만인 것이 좋다. 더욱 구체적으로, 용액 중 폴리머의 농도는 20 내지 60 중량%인 것이 좋다.
친지성 또는 양친성으로 변형된 펩타이드가 이러한 현장(in situ) 형성 임플란트로부터 방출되는 것은, 모노리스(monolithic) 폴리머 기구로부터 약물을 방출시키는 경우와 유사한 일반 법칙에 따른다. 친지성 또는 양친성으로 변형된 펩타이드의 방출은 임플란트의 크기와 형상, 임플란트 내의 친지성 또는 양친성 변형된 펩타이드의 로딩량, 특정 폴리머 및 친지성 또는 양친성 변형된 펩타이드와 관련된 투과도 인자, 및 폴리머의 분해도에 의해 영향을 받을 수 있다. 전달하고자 선택된 변형된 펩타이드의 양에 따라, 당업자들은 전술한 변수들을 조정함으로써 목적하는 방출 속도와 방출 기간을 달성할 수 있다.
주사가능한 조성물의 투여량은 일반적으로 조절적으로 방출되는 임플란트의 목적하는 특성에 따라 달라진다. 예컨대, 주사가능한 용액 조성물의 양은 조절 방출되는 임플란트로부터 펩타이드가 방출되는 기간에 영향을 미칠 수 있다.
본 발명에 따라, 친지성 또는 양친성으로 변형된 펩타이드를 함유하는 조성물은 펩타이드가 지속적 및 조절적으로 방출될 것이 요망되는 대상자에게 투여될 수 있다. 본 명세서에서, "대상자"라는 용어는 온혈동물, 바람직하게는 포유동물, 가장 바람직하게는 인간을 포함하는 것으로 의도된다.
본 명세서에서 "투여되다"라는 용어는 조성물(에컨대, 약학적 포뮬레이션)의 전달을 위한 적당한 경로, 예컨대, 주사 및/또는 피하, 근육내, 복강내 또는 피내 이식, 및 점막 내 투여에 의한 전달 경로 에 의해, 대상자 체내의 목적하는 부위로 조성물을 분산, 전달 또는 적용함으로써, 치료용 펩타이드에 의해 다양한 의학적 질환을 치료하기 위하여, 공지의 변수에 기초하여 필요량의 펩타이드를 제공하는 것을 의미한다.
본 명세서에서 "조절 방출 전달, 지속 방출 전달"이라는 의미는 예컨대, 투여 후 일정 기간, 바람직하게는 적어도 며칠에서 수주일 또는 몇개월 동안 생체내에서 치료용 펩타이드를 지속적으로 전달하는 것을 포함한다. 펩타이드를, 조절 방출, 지속 방출 전달되는지 여부는 예컨대 해당 약제의 치료 효과가 일정 기간 지속되는지에 의해 입증가능하다 (예컨대, 옥트레오타이드의 경우, 펩타이드의 지속적 전달은 일정 기간에 걸친 GH의 지속적 감소에 의해 입증된다). 또한, 약제의 지속 전달은 생체내에서 일정 기간 동안 약제가 존재하는지를 검출함으로써 입증할 수 있다.
본 발명의 액상의 의약 조성물에 대해 청구범위에 제시된 다양한 구체예들은 이러한 조성물을 조제하기 위한 본 발명의 방법 및 고상 임플란트를 형성하기 위한 본 발명의 방법에도 적용된다.
실시예
다음의 실시예들은 본 발명의 조성물과 방법을 설명하기 위해 제공된다. 다음의 실시예들은 어디까지나 설명 목적을 위해 개시되는 것으로서, 본 발명의 범위가 이에 한정되는 것은 아니며, 단지 유용한 약물 전달 시스템을 만드는 방법을 설명하기 위해 개시되는 것일 뿐이다.
실시예
1.
팔미토일
-
옥트레오타이드(PAL-OCT)의
제조
100 μL 트리에틸아민(TEA)르르 함유하는 1 mL의 무수 DMSO에 50 mg의 옥트레오타이드 아세테이트를 용해시켰다. 40.2 mg의 팔미트산 N-히드록시숙신이미드 에스테르 (Mw 353.50)를 3 mL 무수 DMSO에 용해시키고 펩타이드 용액에 첨가하였다. 실온에서 3시간 동안 반응을 진행시켰다. 혼합물을 디에틸에테르에 부어 팔미토일화 옥트레오타이드를 침전시켰다. 이 침전물을 디에틸에테르로 2회 세척하고 진공 건조시켰다. 얻어진 아실화 펩타이드는 백색 분말 형태였다.
실시예
2.
팔미토일
-
옥트레오타이드
(
PAL
-
OCT
)의 제조
50 mg의 옥트레오타이드 아세테이트를 100 μL TEA를 함유하는 1000 μL의 무수 DMSO에 용해시켰다. 17.1 mg의 팔미트산 N-히드록시숙신이미드 에스테르 (Mw 353.50)를 3 mL 무수 DMSO에 용해시키고 직접 주입에 의해 펩타이드 용액에 첨가하였다. 실온에서 밤새 반응시켰다. 혼합물을 디에틸에테르에 부어 팔미토일화된 옥트레오타이드를 침전시켰다. 이 침전물을 디에틸에테르로 2회 세척한 다음 진공 하에 건조시켰다. 얻어진 아실화 펩타이드는 백색 분말 형태였다.
실시예
3.
데칸올
-
옥트레오타이드
(
DCL
-
OCT
)의 제조
50 mg의 옥트레오타이드를 pH 5의 0.1 M 아세테이트 완충액 중 2 mL의 20 mM 소듐 시아노보로하이드라이드 (Mw 62.84, NaCNBH3) (2.51 mg) 용액에 용해시켰다13.7 mg의 Decanal (Mw 156.27) (OCT:DCL = 1:2)을 직접 주입에 의해 펩타이드 용액에 첨가하였다. 4℃에서 밤새 반응시켰다. 이 혼합물을 원심분리시켰다. 침전된PAL-OCT를 동결 건조시켰다.
실시예
4.
팔미토일
-
리소자임
(
PAL
-
Lyz
, 3:1)의 제조
302 mg의 리소자임 (Mw 14,500)을 200 μL TEA를 함유하는 1000 μL의 무수 DMSO에 용해시켰다. 18.25 mg의 팔미트산 N-히드록시숙신이미드 에스테르 (Mw 353.50)를 3 mL 무수 DMSO에 용해시키고 직접 주입에 의해 단백질 용액에 첨가하였다. 실온에서 밤새도록 반응을 진행시켰다. The PAL-Lyz을 디에틸에테르에서 침전시키고, 유기 용매를 제거한 후 최종 생성물을 동결 건조시켰다.
실시예
5. 주사가능한
폴리머
포뮬레이션으로부터의
팔미토일
-
리소자임의
방출
폴리머를 mPEG350에 적절히 용해시킴으로써 40% PLGA RG503H를 제조하였다. 이어서, 팔미토일-리소자임 및 리소자임을 각각 약 7%씩 농도로 폴리머 용액과 혼합하였다. 얻어진 포뮬레이션을 완전히 혼합하여 균질한 포뮬레이션을 얻었다.
주사가능한 폴리머 용액으로부터 리소자임 및 팔미토일화된 리소자임의 시험관내 방출: 37℃에서 포뮬레이션 현탁액 (약 100 mg)을 pH 7.4의 3 mL 인산염 완충액 염수 용액 내로 0.1% 아지드나트륨과 함께 주입하였다. 선택된 시점에서 리시빙 플루이드(receiving fluid)를 신선한 완충 용액으로 대체하고, 제거된 완충 용액을 pH 7.4에서 PB로 적절히 희석한 다음 280 nm에서 UV 분광광도계에 의해 표준 곡선에 대해 약물 농도를 분석하였다. 도 1은 아실화된 리소자임과 천연 리소자임 두가지 모두의 누적 방출 프로파일을 도시한 것이다. 천연 리소자임은 아실화된 리소자임에 비해 초기에 훨씬 더 많이 방출되는 것으로 나타났다.
실시예
6.
팔미토일
-
리소자임
(
PAL
-
Lyz
, 5:1)의 제조
50 mg의 리소자임 (Mw 14,500)을 물에 용해시키고 pH를 9.58로 조정하였다. 이 용액을 동결 건조시켰다. 이어서 건조시킨 분말을 3 mL DMSO에 용해시켰다. 이어서, 322 μL의 20 mg/mL 무수 DMSO 중 팔미트산 N-히드록시숙신이미드 에스테르 (Mw 353.50) 용액을 직접 주입에 의해 단백질 용액에 첨가하였다. 4℃에서 밤새 반응을 진행시켰다. PAL-Lyz을 디에틸에테르에서 침전시키고 유기 용매를 제거한 뒤 최종 생성물을 동결 건조 시켰다.
실시예
7.
팔미토일
-
리소자임
(
PAL
-
Lyz
, 13:1)의 제조
50 mg의 리소자임 (Mw 14,500)을 물에 용해시키고 pH를 9.58로 조정하였다. 이 용액을 동결 건조시켰다. 이어서 건조시킨 분말을 3 mL DMSO에 용해시켰다. 이어서, 799 μL의 20 mg/mL 무수 DMSO 중 팔미트산 N-히드록시숙신이미드 에스테르 (Mw 353.50) 용액을 직접 주입에 의해 단백질 용액에 첨가하였다. 4℃에서 밤새 반응을 진행시켰다. PAL-Lyz을 디에틸에테르에서 침전시키고 유기 용매를 제거한 뒤 최종 생성물을 동결 건조 시켰다.
실시예
8.
팔미토일
-
리소자임
(
PAL
-
Lyz
)의 제조
2% 데옥시콜레이트 (DOC)를 함유하는 PBS (pH 8.0) 중 PAL-NHS에 리소자임을 첨가하였다. 혼합물을 37℃에서 6시간 동안 인큐베이션시킨다. 혼합물을 원심분리하여 미반응 PAL-NHS을 제거한다. 생성물을 0.15% DOC를 함유하는 PBS에 대해 48 시간 동안 투석한다(PAL-NHS:Lyso=15:1).
실시예
9. 주사가능한
폴리머
포뮬레이션으로부터의
그렐린의
방출
폴리머를 mPEG350에 적절히 용해시킴으로써, 40% PLGA RG503H를 제조하였다. 이어서 그렐린 (Human, Rat 1-5) 및 탈아실화된 그렐린 (Des-n-Octanoyl-[Ser]3-ghrelin (Human, Rat 1-5))을 각각 6%씩 폴리머 용액과 혼합하였다. 얻어진 포뮬레이션을 완전히 혼합하여 균질한 포뮬레이션을 얻었다.
37℃에서 이 포뮬레이션 현탁액 (약 100 mg)을 pH 7.4의 3 mL 인산염 완충액 염수 용액 내로 0.1% 아지드나트륨과 함께 주입하였다. 선택된 시점에서 리시빙 플루이드를 신선한 완충 용액으로 대체하고, 제거된 완충 용액을 pH 7.4에서 PB로 적절히 희석한 다음 야물 농도를 상응하는 표준 곡선을 이용하여 HPLC에 의해 분석하였다. 도 2는 그렐린과 탈아실화된 그렐린의 PBS에서의 누적 방출 프로파일을 도시한 것이다. 탈아실화된 그렐린은 시험된 2주일 동안 훨씬 빨리 방출되는 것으로 나타났다. 친지성 모이어티를 갖는 그렐린은 방출 속도가 훨씬 느렸다.
실시예
10.
모노팔미틸
폴리
(에틸렌 글리콜)-
부티르알데히드
,
디에틸
아세탈
의 제조
모노팔미틸 폴리(에틸렌 글리콜) (평균 Mn ~1124) (5.0 g, 4.45 mmoles) 및 톨루엔 (75 mL)을 감압 하에 톨루엔을 증류시킴으로써 공비 건조시켰다. 건조된 모노팔미틸 폴리(에틸렌 글리콜)을 무수 톨루엔 (50 mL)에 용해시키고 여기에 THF (4.0 ml, 6.6 mmoles) 및 4-클로로부티르알데히드 디에틸 아세탈 (0.96 g, 5.3 mmoles, MW 180.67) 중 3차-부톡사이드 칼륨의 20% (w/w) 용액을 첨가하였다. 이 혼합물을 아르곤 분위기 하, 100-105℃에서 밤새 교반하였다. 실온으로 냉각한 뒤, 이 혼합물을 여과하고 0-5℃에서 150 ml 에틸 에테르에 첨가하였다. 침전된 생성물을 여과하고 감압 하에 건조시켰다.
실시예
11. N-말단
아민기에서의
옥트레오타이드와
모노팔미틸
폴리(에틸렌
글리콜)의
컨쥬게이션
(
PAL
-
PEG
-
BA
-
OCT
)
전형적인 제조 방법으로서, 201.6 mg의 모노팔미틸 폴리(에틸렌 글리콜)-부티르알데히드, 디에틸 아세탈 (PAL-PEG-BADA)을 10 mL의 0.1 M 인산 (pH 2.1)에 용해시키고 얻어진 용액을 50℃에서 1시간 동안 가열한 다음 실온으로 냉각시켰다. 용액의 pH를 1N NaOH를 이용하여 5.5로 조정하고, 얻어진 용액을 3.5 mL의 0.1 M 인산나트륨 완충액 (pH 5.5) 중 195.3 mg의 옥트레오타이드 용액에 첨가하였다. 1시간 후, 18.9 mg의 NaCNBH3 를 첨가하여 20 mM로 농축시켰다. 실온에서 밤새도록 계속 반응시켰다. 이어서, 반응 혼합물을 MW 컷오프가 2000 달톤인 막을 이용하여 투석하거나 또는 C-18 컬럼을 갖는 예비 HPLC 상에 로딩시켰다. 정제된 컨쥬게이트된 옥트레오타이드는 주로 하나의 일차 아민(라이신)과 하나의 2차 아민 (N-말단)을 갖는 단일 화합물이었다.
실시예
12. 액상
폴리머
조성물 중에서의
생체분해성
폴리머와
펩타이드의
시험관내
방출 및 안정성
락타이드 대 글리콜라이드의 비율이 85/15이고 다분산도가 1.5 (DLPLG85/15, IV: 0.28)인 폴리(DL-락타이드-코-글리콜라이드) (PLGA)를 N-메틸-2-피로리돈 (NMP)에 용해시켜 50 중량% 용액을 얻었다. 펩타이드를 NMP 중 PLGA 용액과 혼합하여 다음 표 1에 도시된 비율로 균질한 주사용 조성물을 얻었다.
각각의 포뮬레이션으로부터 일정액을 채취하여 37℃에서 0.1% 아지드나트륨을 함유하는 pH 7.4의 인산염 완추액 중에서의 시험관내 방출 시험을 행하고 나머지 포뮬레이션을 이용하여 실온에서 펩타이드와 폴리머의 경시적 안정성을 모니터링하였다. 시점은 0.125, 1, 2, 5, 7, 14, 21, 및 28일이었다. 샘플 중 펩타이드의 순도는 HPLC에 의해 측정하였다. 폴리머의 분자량은 분자량이 공지인 폴리스티렌 표준품을 이용하여 겔 투과 크로마토그래피 (GPC)에 의해 측정하였다.
종래기술에 의하면, 펩타이드 상에 친핵성 기가 존재하면 조성물의 생체분해성 폴리머와 펩타이드 사이에 상호반응이 일어날 수 있다. 펩타이드 상의 친핵성 기는 생체분해성 폴리머와 반응하여 아실화 산물을 형성하고 생체분해성 폴리머의 분해를 촉매할 수 있다. 옥트레오타이드와 폴리(DL-락타이드-코-글리콜라이드)가 특히 NMP와 같은 유기 용매에서 결합될 경우, 옥트레오타이드가 아실화하여 폴리머가 급속히 분해된다는 것은 익히 알려져 있다. 본 발명에서 옥트레오타이드의 N-말단 컨쥬게이션은 하나의 일차 아민, 하나의 이차아민 및 하나의 C-말단 카르복실산기를 함유하며 옥트레오타이드 자체와 유사하게, 폴리머와 상호반응 및/또는 반응하리라고 예상된다. 그러나, 예기치 않게도, 본 발명의 공유적으로 컨쥬게이트된 옥트레오타이드는 아실화 반응을 방지하여 변형되지 않은 옥트레오타이드에 비해 폴리머의 분해 속도를 현저히 감소시킨 것으로 밝혀졌다. 종래기술에 따른 설명과 표 2에 나타낸 바와 같이, 옥트레오타이드를 NMP 중 폴리(DL-락타이드-코-글리콜라이드) 용액과 혼합하자, 옥트레오타이드는 실온에서 24시간 이내에 80% 넘게 아실화되고 7일 후에는 거의 완전히 반응하였다. 그러나, 공유적으로 컨쥬게이트된 옥트레오타이드는 동일한 조건에서 56일이 경과한 후에 조차 안정하게 유지되었다. 표 3에 나타낸 바와 같이, 옥트레오타이드를 함유하는 포뮬레이션 중 폴리머의 분자량은 실온에서 급속히 감소하였다. 21일 후, 폴리머의 분자량은 50%까지 감소되었다. 그러나, 공유적으로 컨쥬게이트된 옥트레오타이드를 함유하는 포뮬레이션 중의 폴리머의 경우에는, 본래 분자량의 90%가 유지되었다.
종래 기술에 개시된 바와 같이, 포뮬레이션 중의 생물학적 활성제제와 부형제의 안정성을 유지시키기 위해서, 예컨대 시판되는 류프롤라이드 포뮬레이션 Eligard의 경우와 같이, 생물학적 활성제제는 일반적으로 포뮬레이션의 다른 성분들과 격리되어 포장된다. 이어서 사용 직전에 모든 성분들을 한데 혼합시킨다. 이러한 조제물은 유통 보관 중 펩타이드와 생체분해성 폴리머 간의 상호반응을 방지시킬 수는 있지만, 이들이 혼합된 후에도 상호반응을 방지시켜주지는 않는다. 펩타이드와 폴리머 간의 상호반응은 투여 중에도, 그리고 시험관내 또는 생체내에서 방출되는 동안에도 일어날 수 있다.
제조 후 각각의 포뮬레이션으로부터 일정액을 채취하여 37℃에서, 0.1% 아지드나트륨을 함유하는 pH 7.4의 인산염 완충액 중에서 시험관내 방출 시험을 수행하자, 놀랍게도 혼합 도중 및 시험관내에서의 후속적인 방출시에 옥트레오타이드와 폴리머 간에 상호반응이 일어난 것으로 밝혀졌다. 도 3에 도시된 바와 같이, 방출 매질 중에 검출된 옥트레오타이드의 약 30%는 3시간 이내에 폴리머와 반응하거나 분해되었다. 또한 방출 매질 중에 검출된 옥트레오타이드의 50% 이상은 28일 후에 분해되거나 아실화되었다. 28일 후, 폴리머 매트릭스를 아세토니트릴에 용해시키고 폴리머를 물을 이용하여 침전시켰다. HPLC에 의해 옥트레오타이드를 분석하였다. 폴리머 매트릭스 중에 잔류하는 옥트레오타이드의 50% 이상 역시 아실화된 것으로 밝혀졌다. 이러한 옥트레오타이드의 분해 및/또는 아실화는 천연옥트레오타이드의 이용성을 현저히 감소시키는 것으로서 바람직하지 못한 유독한 부산물이 생성될 수 있다. 따라서 펩타이드와 폴리머 간의 이러한 상호반응을 방지하는 것이 매우 요망된다.
도 4는 공유적으로 컨쥬게이트된 옥트레오타이드 Pal-PEG-BA-OCT의 시험관내 방출 프로파일을 도시한 도면이다. 비록 변형된 옥트레오타이드는 변형되지 않은 옥트레오타이드과 유사한 양의 친핵성기를 함유하지만, 놀랍게도, 변형된 옥트레오타이드는 28일이 지난 후에도 방출 매질과 폴리머 매트릭스 중에서 전혀 분해되지 않은 것으로 밝혀졌다. 이 결과는 펩타이드를 모노팔미틸 폴리(에틸렌 그리콜)과 같은 양친성 모이어티로 공유적으로 컨쥬게이션시킴으로써 펩타이드와 생체분해성 폴리머 사이의 상호반응 및/또는 반응을 현저히 감소시키거나 방지할 수 있음을 가리키는 것이다.
실시예
13. 4-
니트로페닐
클로로포르메이트(NPC)로
활성화시킨
모노팔미틸
폴리(에틸렌 글리콜)의
제조
모노팔미틸 폴리(에틸렌 글리콜) (평균 Mn ~1124) (10.0 g, 8.9 mmoles) 및 벤젠 (100 mL)의 혼합물을 감압 하에서 50 mL 벤젠을 증류시킴으로서 공비 건조시켰다. 이 반응 혼합물을 30℃로 냉각한 다음, 아르곤 분위기 하에 무수 피리딘 (0.809 mL, 10 mmol)과 4-니트로페닐 클로로포르메이트 (2.015 g, 10.0 mmoles)를 첨가하였다. 첨가 완료 후, 반응물을 45℃에서 2시간 동안 교반한 다음 실온에서 밤새 교반하였다.
이어서 반응 혼합물을 여과한 다음, 진공 증류시킴으로써 여액으로부터 용매를 제거하였다. 잔사를 2-프로판올로부터 재결정화시켜 8.2 g의 생성물 (PAL-PEG-NPC)을 수득하였다.
실시예
14.
옥트레오타이드와
모노팔미틸
폴리(에틸렌 글리콜)과의
컨쥬게
이션
(
PAL
-
PEG
-
OCT
)
236.5 mg의 PAL-PEG-NPC를 10 mL의 50 mM 붕산나트륨 완충액 (pH 9) 중 239 mg의 옥트레오타이드 용액에 첨가하였다. 이 용액을 밤새도록 자석 교반기로 지속적으로 교반하였다. 최종 용액을 MW 컷오프가 2000인 막을 이용하여 투석하였다. 투석된 용액을 동결 건조시키고 HPLC에 의해 분석하였다. 분석 결과 변형된 펩타이드는 단일 위치 및 복수개 위치에서 컨쥬게이트된 옥트레오타이드의 혼합물인 것으로 나타났다.
이제까지 상기한 실시예로서 개시된 몇몇 구체예를 들어 본 발명을 설명하였으나 본 발명의 범위가 이들 실시예로 국한되는 것은 아니며, 본 발명은 첨부된 특허 청구범위에 규정된 보호 범위 내에서 다양한 방식으로 변형이 가능하다.
Claims (3)
- 치료용 폴리펩타이드를 조절적으로 방출시키기 위한 액상 폴리머 의약 조성물로서,
(a) 약학적으로 허용가능한, 비수용성 생체분해성 폴리머;
(b) 상기 생체분해성 폴리머를 용해시키는, 약학적으로 허용가능한 유기 용매; 및
(c) 하나 이상의 친지성 모이어티와 컨쥬게이트된 치료용 폴리펩타이드를 를 포함하여 이루어지며, 상기 조성물은 점성이 있는 주사가능한 액상 형태이며, 대상의 체 내에서 유기 용매를 소산 또는 분산시킴으로써 조절 방출 임플란트를 형성할 수 있고, 상기 조성물은 친지성 모이어티에 치료용 펩타이드가 컨쥬게이트 되지 않은 조성물에 비해 시험관 내 안정성이 더 높고 초기 분출 방출량은 더 적은 것인 액상 폴리머 의약 조성물. - 제1항에 있어서, 상기 폴리펩타이드는 효소, 사이토카인, 항체, 백신, 항생제 및 당단백질로부터 선택되는 것인 액상 폴리머 의약 조성물.
- 제2항에 있어서, 상기 폴리펩타이드는 콜로니 자극 인자인 것인 액상 폴리머 의약 조성물.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US83001106P | 2006-07-11 | 2006-07-11 | |
| US60/830,011 | 2006-07-11 | ||
| PCT/US2007/015770 WO2008008363A1 (en) | 2006-07-11 | 2007-07-11 | Pharmaceutical compositions for sustained release delivery of peptides |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020097002817A Division KR101466933B1 (ko) | 2006-07-11 | 2007-07-11 | 펩타이드의 지속 방출 전달을 위한 의약 조성물 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140109509A true KR20140109509A (ko) | 2014-09-15 |
Family
ID=38923538
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020097002817A KR101466933B1 (ko) | 2006-07-11 | 2007-07-11 | 펩타이드의 지속 방출 전달을 위한 의약 조성물 |
| KR1020147023622A KR20140109509A (ko) | 2006-07-11 | 2007-07-11 | 펩타이드의 지속 방출 전달을 위한 의약 조성물 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020097002817A KR101466933B1 (ko) | 2006-07-11 | 2007-07-11 | 펩타이드의 지속 방출 전달을 위한 의약 조성물 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US8206735B2 (ko) |
| EP (1) | EP2054073B1 (ko) |
| JP (1) | JP5231412B2 (ko) |
| KR (2) | KR101466933B1 (ko) |
| CN (1) | CN101511380B (ko) |
| BR (1) | BRPI0715469A2 (ko) |
| CA (1) | CA2657911C (ko) |
| DK (1) | DK2054073T3 (ko) |
| ES (1) | ES2531679T3 (ko) |
| HK (1) | HK1131751A1 (ko) |
| MX (1) | MX2009000434A (ko) |
| RU (1) | RU2456018C2 (ko) |
| WO (1) | WO2008008363A1 (ko) |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7731947B2 (en) | 2003-11-17 | 2010-06-08 | Intarcia Therapeutics, Inc. | Composition and dosage form comprising an interferon particle formulation and suspending vehicle |
| US11246913B2 (en) | 2005-02-03 | 2022-02-15 | Intarcia Therapeutics, Inc. | Suspension formulation comprising an insulinotropic peptide |
| US8299025B2 (en) | 2005-02-03 | 2012-10-30 | Intarcia Therapeutics, Inc. | Suspension formulations of insulinotropic peptides and uses thereof |
| KR101200728B1 (ko) | 2006-08-09 | 2012-11-13 | 인타르시아 세라퓨틱스 인코포레이티드 | 삼투성 전달 시스템 및 피스톤 조립체 |
| US20090081276A1 (en) * | 2007-08-13 | 2009-03-26 | Eben Alsberg | Bioresorbable implant composition |
| AU2008306218A1 (en) | 2007-09-11 | 2009-04-09 | Mondobiotech Laboratories Ag | Use of a peptide as a therapeutic agent |
| JP5718058B2 (ja) * | 2008-02-08 | 2015-05-13 | キューピーエス リミテッド ライアビリティ カンパニー | タンパク質又はペプチドの徐放送達用組成物 |
| EP2240155B1 (en) | 2008-02-13 | 2012-06-06 | Intarcia Therapeutics, Inc | Devices, formulations, and methods for delivery of multiple beneficial agents |
| DK2957292T3 (en) | 2008-03-27 | 2018-01-22 | Clinuvel Pharmaceuticals Ltd | VITILIGOTERAPHY |
| CA2653866A1 (en) * | 2008-07-03 | 2010-01-03 | Induce Biologics Inc. | Use of immobilized antagonists for enhancing growth factor containing bioimplant effectiveness |
| HUE035862T2 (en) * | 2009-09-28 | 2018-05-28 | Intarcia Therapeutics Inc | Rapid development and / or completion of substantially steady-state drug delivery |
| IE20100174A1 (en) * | 2010-03-25 | 2012-02-29 | Trinity College Dublin | Transdermal administration of peptides |
| US9364518B2 (en) | 2010-06-24 | 2016-06-14 | Torrent Pharmaceuticals Limited | Pharmaceutical composition containing goserelin for in-situ implant |
| US20120208755A1 (en) | 2011-02-16 | 2012-08-16 | Intarcia Therapeutics, Inc. | Compositions, Devices and Methods of Use Thereof for the Treatment of Cancers |
| CN102796165B (zh) * | 2011-05-24 | 2014-02-26 | 首都医科大学 | 京都酚逆序列修饰的脂肪胺/醇衍生物及其制备方法和应用 |
| MX352907B (es) | 2013-03-15 | 2017-12-13 | Heron Therapeutics Inc | Composiciones de un poliortoéster y un solvente aprótico. |
| WO2015032981A1 (en) * | 2013-09-09 | 2015-03-12 | Lek Pharmaceuticals D.D. | Erythropoietin conjugates having oral bioavailability |
| JP6564369B2 (ja) | 2013-12-09 | 2019-08-21 | デュレクト コーポレイション | 薬学的活性剤複合体、ポリマー複合体、ならびにこれらを伴う組成物及び方法 |
| US9889085B1 (en) | 2014-09-30 | 2018-02-13 | Intarcia Therapeutics, Inc. | Therapeutic methods for the treatment of diabetes and related conditions for patients with high baseline HbA1c |
| US20160106804A1 (en) * | 2014-10-15 | 2016-04-21 | Yuhua Li | Pharmaceutical composition with improved stability |
| WO2016059592A1 (en) * | 2014-10-16 | 2016-04-21 | Piramal Enterprises Limited | Stable injectable composition of peptide drugs and process for its preparation |
| EP3206706A4 (en) * | 2014-10-16 | 2018-05-30 | Piramal Enterprises Limited | Stable injectable composition of pharmaceutically active agents and process for its preparation |
| US20160151511A1 (en) | 2014-12-02 | 2016-06-02 | Antriabio, Inc. | Proteins and protein conjugates with increased hydrophobicity |
| EP3302354B1 (en) | 2015-06-03 | 2023-10-04 | i2o Therapeutics, Inc. | Implant placement systems |
| CA2988500A1 (en) * | 2015-06-12 | 2016-12-15 | Novo Nordisk A/S | Selective pyy compounds and uses thereof |
| AU2016328958B2 (en) | 2015-09-21 | 2022-04-21 | Teva Pharmaceuticals International Gmbh | Sustained release olanzapine formulations |
| BR112018073511A2 (pt) | 2016-05-16 | 2019-03-26 | Intarcia Therapeutics, Inc. | polipeptídeos seletivos do receptor de glucagon e métodos de uso dos mesmos |
| USD840030S1 (en) | 2016-06-02 | 2019-02-05 | Intarcia Therapeutics, Inc. | Implant placement guide |
| USD860451S1 (en) | 2016-06-02 | 2019-09-17 | Intarcia Therapeutics, Inc. | Implant removal tool |
| CN107753953B (zh) * | 2016-08-18 | 2021-06-08 | 江苏众红生物工程创药研究院有限公司 | 聚乙二醇化激肽原酶的制剂及其应用 |
| US11174288B2 (en) | 2016-12-06 | 2021-11-16 | Northeastern University | Heparin-binding cationic peptide self-assembling peptide amphiphiles useful against drug-resistant bacteria |
| CN110225762A (zh) | 2017-01-03 | 2019-09-10 | 因塔西亚制药公司 | 包括glp-1受体激动剂的连续施用和药物的共同施用的方法 |
| EP3600258A1 (en) | 2017-03-20 | 2020-02-05 | Teva Pharmaceuticals International GmbH | Sustained release olanzapine formulaitons |
| MX2020014160A (es) * | 2018-06-25 | 2021-03-09 | Titan Pharmaceuticals Inc | Implantes para liberacion de sustancias farmaceuticas lipofilicas o anfifilicas. |
| US20210309763A1 (en) * | 2018-07-31 | 2021-10-07 | Lemonex Inc. | Polypeptide delivery composition |
| CN109908407A (zh) * | 2019-03-14 | 2019-06-21 | 西南交通大学 | 具有一氧化氮储存性能的功能薄膜材料及其制备方法 |
| US20220152017A1 (en) * | 2019-03-29 | 2022-05-19 | Allegheny Singer Research Institute | Covalent Modification and Controlled Delivery of Mu Opioid Receptor Antagonists |
| CN113368041B (zh) * | 2020-07-17 | 2023-01-03 | 丽珠医药集团股份有限公司 | 药物组合物、缓释制剂及其制备方法 |
| EP4277661A1 (en) | 2021-01-18 | 2023-11-22 | Anton Frenkel | Pharmaceutical dosage form |
| BR102021001712A2 (pt) * | 2021-01-29 | 2022-08-16 | Edson Luiz Peracchi | Implante subcutâneo reabsorvível de longa duração com liberação prolongada de substância farmacologicamente ativa pré-concentrada em polímero para tratamento da diabetes mellitus tipo 2 e processo |
| CA3227324A1 (en) | 2021-07-06 | 2023-01-12 | Mark Hasleton | Treatment of serotonin reuptake inhibitor withdrawal syndrome |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2551756B2 (ja) * | 1985-05-07 | 1996-11-06 | 武田薬品工業株式会社 | ポリオキシカルボン酸エステルおよびその製造法 |
| JPH01254699A (ja) | 1988-04-05 | 1989-10-11 | Kodama Kk | インスリン誘導体及びその用途 |
| US4938763B1 (en) | 1988-10-03 | 1995-07-04 | Atrix Lab Inc | Biodegradable in-situ forming implants and method of producing the same |
| US5702716A (en) | 1988-10-03 | 1997-12-30 | Atrix Laboratories, Inc. | Polymeric compositions useful as controlled release implants |
| US5487897A (en) * | 1989-07-24 | 1996-01-30 | Atrix Laboratories, Inc. | Biodegradable implant precursor |
| US5324519A (en) * | 1989-07-24 | 1994-06-28 | Atrix Laboratories, Inc. | Biodegradable polymer composition |
| USRE37950E1 (en) * | 1990-04-24 | 2002-12-31 | Atrix Laboratories | Biogradable in-situ forming implants and methods of producing the same |
| AU2605592A (en) * | 1991-10-15 | 1993-04-22 | Atrix Laboratories, Inc. | Polymeric compositions useful as controlled release implants |
| EP0560014A1 (en) * | 1992-03-12 | 1993-09-15 | Atrix Laboratories, Inc. | Biodegradable film dressing and method for its formation |
| CA2171424C (en) | 1993-09-17 | 2002-06-04 | Svend Havelund | Acylated insulin |
| US5681873A (en) * | 1993-10-14 | 1997-10-28 | Atrix Laboratories, Inc. | Biodegradable polymeric composition |
| DE69534780T2 (de) * | 1994-04-08 | 2006-10-05 | Qlt Usa Inc., Fort Collins | Flüssige Zusammensetzungen zur Arzneistoffabgabe |
| US5552771A (en) | 1994-06-10 | 1996-09-03 | Leyden; Roger J. | Retractable sensor for an alarm system |
| US5512549A (en) | 1994-10-18 | 1996-04-30 | Eli Lilly And Company | Glucagon-like insulinotropic peptide analogs, compositions, and methods of use |
| US5693609A (en) * | 1994-11-17 | 1997-12-02 | Eli Lilly And Company | Acylated insulin analogs |
| US5869602A (en) | 1995-03-17 | 1999-02-09 | Novo Nordisk A/S | Peptide derivatives |
| US5736152A (en) * | 1995-10-27 | 1998-04-07 | Atrix Laboratories, Inc. | Non-polymeric sustained release delivery system |
| AU4112497A (en) * | 1996-08-30 | 1998-03-19 | Novo Nordisk A/S | Glp-2 derivatives |
| DK0944648T3 (da) | 1996-08-30 | 2007-07-02 | Novo Nordisk As | GLP-1 derivater |
| US20020012942A1 (en) * | 1998-01-22 | 2002-01-31 | Regents Of The University Of Minnesota | Polypeptides with a4 integrin subunit related activity |
| EP1056775B1 (en) | 1998-02-27 | 2010-04-28 | Novo Nordisk A/S | Glp-1 derivatives of glp-1 and exendin with protracted profile of action |
| US6261583B1 (en) * | 1998-07-28 | 2001-07-17 | Atrix Laboratories, Inc. | Moldable solid delivery system |
| US6143314A (en) * | 1998-10-28 | 2000-11-07 | Atrix Laboratories, Inc. | Controlled release liquid delivery compositions with low initial drug burst |
| US6565874B1 (en) * | 1998-10-28 | 2003-05-20 | Atrix Laboratories | Polymeric delivery formulations of leuprolide with improved efficacy |
| US6355657B1 (en) * | 1998-12-30 | 2002-03-12 | Atrix Laboratories, Inc. | System for percutaneous delivery of opioid analgesics |
| US7544486B2 (en) * | 2003-02-07 | 2009-06-09 | The Regents Of The University Of California | Nell peptide expression systems and bone formation activity of nell peptide |
| US6461631B1 (en) * | 1999-11-16 | 2002-10-08 | Atrix Laboratories, Inc. | Biodegradable polymer composition |
| US7060675B2 (en) * | 2001-02-15 | 2006-06-13 | Nobex Corporation | Methods of treating diabetes mellitus |
| US6858580B2 (en) * | 2001-06-04 | 2005-02-22 | Nobex Corporation | Mixtures of drug-oligomer conjugates comprising polyalkylene glycol, uses thereof, and methods of making same |
| WO2004035754A2 (en) * | 2002-10-17 | 2004-04-29 | Alkermes Controlled Therapeutics, Inc. Ii | Microencapsulation and sustained release of biologically active polypeptides |
| US20080193997A1 (en) * | 2004-08-24 | 2008-08-14 | Kenji Kangawa | Liquid Preparation of Physiologically Active Peptide |
| AU2005304435B8 (en) * | 2004-11-10 | 2011-06-23 | Tolmar Therapeutics, Inc. | A stabilized polymeric delivery system |
-
2007
- 2007-07-11 ES ES07810318.1T patent/ES2531679T3/es active Active
- 2007-07-11 JP JP2009519503A patent/JP5231412B2/ja active Active
- 2007-07-11 WO PCT/US2007/015770 patent/WO2008008363A1/en active Application Filing
- 2007-07-11 KR KR1020097002817A patent/KR101466933B1/ko active IP Right Grant
- 2007-07-11 DK DK07810318T patent/DK2054073T3/da active
- 2007-07-11 CN CN2007800288591A patent/CN101511380B/zh not_active Expired - Fee Related
- 2007-07-11 MX MX2009000434A patent/MX2009000434A/es active IP Right Grant
- 2007-07-11 EP EP07810318.1A patent/EP2054073B1/en active Active
- 2007-07-11 US US11/827,260 patent/US8206735B2/en active Active
- 2007-07-11 CA CA2657911A patent/CA2657911C/en not_active Expired - Fee Related
- 2007-07-11 KR KR1020147023622A patent/KR20140109509A/ko not_active Application Discontinuation
- 2007-07-11 BR BRPI0715469-0A patent/BRPI0715469A2/pt not_active Application Discontinuation
- 2007-07-11 RU RU2009103210/15A patent/RU2456018C2/ru not_active IP Right Cessation
-
2009
- 2009-12-08 HK HK09111477.0A patent/HK1131751A1/xx not_active IP Right Cessation
-
2012
- 2012-05-25 US US13/480,544 patent/US8840915B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CA2657911A1 (en) | 2008-01-17 |
| ES2531679T3 (es) | 2015-03-18 |
| WO2008008363A1 (en) | 2008-01-17 |
| KR101466933B1 (ko) | 2014-12-01 |
| RU2009103210A (ru) | 2010-08-20 |
| CN101511380A (zh) | 2009-08-19 |
| CA2657911C (en) | 2012-02-21 |
| MX2009000434A (es) | 2009-01-29 |
| EP2054073A1 (en) | 2009-05-06 |
| CN101511380B (zh) | 2012-12-12 |
| EP2054073A4 (en) | 2010-06-23 |
| US20080020016A1 (en) | 2008-01-24 |
| HK1131751A1 (en) | 2010-02-05 |
| KR20090043510A (ko) | 2009-05-06 |
| DK2054073T3 (da) | 2015-03-02 |
| BRPI0715469A2 (pt) | 2013-03-12 |
| RU2456018C2 (ru) | 2012-07-20 |
| US20120237476A1 (en) | 2012-09-20 |
| US8206735B2 (en) | 2012-06-26 |
| JP2009543776A (ja) | 2009-12-10 |
| JP5231412B2 (ja) | 2013-07-10 |
| EP2054073B1 (en) | 2014-11-26 |
| US8840915B2 (en) | 2014-09-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101466933B1 (ko) | 펩타이드의 지속 방출 전달을 위한 의약 조성물 | |
| US10646572B2 (en) | Pharmaceutical compositions with enhanced stability | |
| JP5718058B2 (ja) | タンパク質又はペプチドの徐放送達用組成物 | |
| KR101231856B1 (ko) | 생물학적 활성 화합물의 제어 방출 전달용 약학 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |