KR20100074196A - 친수성 및/또는 친지성 분자를 캡슐화하기 위한 수계-코어 지질 나노캡슐 - Google Patents
친수성 및/또는 친지성 분자를 캡슐화하기 위한 수계-코어 지질 나노캡슐 Download PDFInfo
- Publication number
- KR20100074196A KR20100074196A KR1020107008347A KR20107008347A KR20100074196A KR 20100074196 A KR20100074196 A KR 20100074196A KR 1020107008347 A KR1020107008347 A KR 1020107008347A KR 20107008347 A KR20107008347 A KR 20107008347A KR 20100074196 A KR20100074196 A KR 20100074196A
- Authority
- KR
- South Korea
- Prior art keywords
- oil
- water
- surfactant
- emulsion
- composition
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/513—Organic macromolecular compounds; Dendrimers
- A61K9/5146—Organic macromolecular compounds; Dendrimers obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyamines, polyanhydrides
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23P—SHAPING OR WORKING OF FOODSTUFFS, NOT FULLY COVERED BY A SINGLE OTHER SUBCLASS
- A23P10/00—Shaping or working of foodstuffs characterised by the products
- A23P10/30—Encapsulation of particles, e.g. foodstuff additives
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23P—SHAPING OR WORKING OF FOODSTUFFS, NOT FULLY COVERED BY A SINGLE OTHER SUBCLASS
- A23P10/00—Shaping or working of foodstuffs characterised by the products
- A23P10/30—Encapsulation of particles, e.g. foodstuff additives
- A23P10/35—Encapsulation of particles, e.g. foodstuff additives with oils, lipids, monoglycerides or diglycerides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/11—Encapsulated compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/87—Polyurethanes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
- A61K9/1075—Microemulsions or submicron emulsions; Preconcentrates or solids thereof; Micelles, e.g. made of phospholipids or block copolymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J13/00—Colloid chemistry, e.g. the production of colloidal materials or their solutions, not otherwise provided for; Making microcapsules or microballoons
- B01J13/02—Making microcapsules or microballoons
- B01J13/06—Making microcapsules or microballoons by phase separation
- B01J13/14—Polymerisation; cross-linking
- B01J13/16—Interfacial polymerisation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/41—Particular ingredients further characterized by their size
- A61K2800/412—Microsized, i.e. having sizes between 0.1 and 100 microns
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/41—Particular ingredients further characterized by their size
- A61K2800/413—Nanosized, i.e. having sizes below 100 nm
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Polymers & Plastics (AREA)
- Dispersion Chemistry (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biophysics (AREA)
- Birds (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Optics & Photonics (AREA)
- Dermatology (AREA)
- Nanotechnology (AREA)
- Biomedical Technology (AREA)
- Physics & Mathematics (AREA)
- Manufacturing Of Micro-Capsules (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Colloid Chemistry (AREA)
Abstract
본 발명은 오일 상; 상기 오일 상 중에, 수계 액적(droplet), 또는 수계 코어와 폴리머 쉘 또는 양친성 물질로 구성된 쉘을 포함하는 나노캡슐(NC); 및 계면활성제를 포함하는, 직경이 20 내지 500 nm 범위인 입자(P)를 수계 상에 포함하는 조성물에 관한 것이다. 상기 조성물은 특히 친수성 및/또는 친지성 물질의 캡슐화에 유용하다.
Description
본 발명은 수계 코어 지질 나노캡슐을 포함하는 신규한 조성물, 이의 제조 방법 및 친수성 및/또는 친지성 분자의 캡슐화를 위한 이의 용도에 관한 것이다.
나노캡슐(NC)은, 전반적으로 코어가 약물의 액체 저장소로서 작용하고, 쉘이 보호막으로서 작용하는, 코어-쉘 구조를 가지는 콜로이드 물질로 설명된다. NC 시스템은 과거 수년간 약물의 잠재적인 운반체로서 매우 유망하고, 치료 및 진단 용도로서, 예컨대 조영제로서 매우 흥미로운 콜로이드인 것으로 알려져 있다. 기존의 나노구 및 나노입자 등의 이러한 약물 운반체의 가장 우수한 장점은, (i) 나노입자 코어에 대한 최적화된 약물 용해성으로 인해, 약물 캡슐화 효율이 우수하며; (ii) 폴리머 나노구에 비해 폴리머의 함량이 현저히 적으며; 및 (iii) 캡슐화되는 약물이 NC 코어 내부에 '보호'되어 약물이 분해되지 않도록 보호하는 것이다.
액체 코어를 구성하고 있는 물질의 성질에 따라, 기본적으로 상이한 2종의 NC, 즉, 오일- 또는 수계-코어 나노입자가 형성되며, 이 둘다 연속 수상에 분산되어 있다. 실제, 전자의 형태(오일-코어 NC)는 벌크 수 상(water bulk phase)에서의 더욱 용이한 제형화로 인해 가장 많이 접하게 되는 시스템이며, 일반적으로 수중유 나노에멀젼 시스템에서부터 인 시츄(in situ) 계면 폴리머 쉘 합성 또는 미리 형성된 폴리머의 나노침전이 있다.
그러나, 이러한 오일-코어 NC 시스템은 친지성 물질을 캡슐화하는데만 사용할 수 있어, 친수성 물질을 캡슐화하기 위해, 벌크 수계 상에 분산된 수계-코어 나노캡슐을 제조하는데 과거 수년간 (현 연구와 같이) 수많은 노력들이 이루어져 왔다. 이러한 면에서, 역으로 정교하게 분산된 에멀젼(Lambert, G. et al., 2000; Lambert, G. et al., 2000) 또는 유중수 마이크로에멀젼(Hillaireau, H. et al., 2006)의 계면 중합에서부터 지질 간의 인 시츄 중합에 의한 리포좀의 안정화와 수계-코어 폴리머로좀(polymerosome)) 나노구조를 형성하는 단계로 구성된 대안적인 공정까지의 다양한 전략들이 실행되어 왔다(Ruysschaert T. et al., 2006; Gomes, J. F. P. d. S. et al., 2006).
나노-어셈블리의 제조 방법, 유중수 나노-에멀젼 주형으로부터 특히 저-에너지 방법에 의해 제조되는, 수계-코어 저장소 나노캡슐의 형성 방법 및 나노캡슐 쉘인 오일 저장소로 또한 구성되는 신규한 다중 기능성 물질의 제조 방법을 개발하였다.
이들 수계 코어 나노캡슐은 친수성 또는 친지성 물질, 특히 취성(fragile) 약물의 캡슐화와 전달에 특히 유용하다. 나아가, 이것은 수계 코어내 친수성 물질의 캡슐화와 지질 쉘내 친지성 물질의 캡슐화를 동시에 고수율로 실시할 수 있는 특별한 이점을 제공한다.
이에, 본 발명의 제1 측면은 입자(P) 직경이 20 내지 500 nm 범위인 입자를 수계 상에 포함하는 조성물의 제조 방법에 관한 것으로, 상기 입자는
- 오일 상;
- 상기 오일 상 중에,
- 수계 액적(droplet) 또는
- 하기 성분을 포함하는 나노캡슐(NC):
- 수계 코어, 및
- 폴리머 쉘 또는 양친성 물질로 구성된 쉘;
및
-계면활성제를 포함하며,
상기 방법은,
i) 액적의 평균 유체 역학 직경이 10 내지 400 nm이고, 연속 상에 2종의 오일, 휘발성 오일(O1) 및 비휘발성 오일(O2)을 포함하고 있으며, 휘발성 오일(O1)은 물 보다 휘발성이 높으며, 비휘발성 오일(O2)은 물 보다 휘발성이 낮은, 유중수(w/o) 에멀젼(E1)을 제조하는 단계;
ii) 선택적으로, 상기 에멀젼(E1)의 연속 상에 용해되며 물과 접촉하였을 때 중합되는 단량체를 첨가하거나, 또는 양친성 물질을 첨가하여, 수계 쉘-코어 나노캡슐(NC)을 형성하는 단계; 및
iii) 수 상을 첨가하고, 휘발성 오일(O1)을 제거함으로써, 원하는 조성물을 제조하는 단계를 포함한다.
본원에서, "평균 직경"이라는 용어는 측정한 모든 측정가능한 입자의 크기 값의 합을 측정한 전체 입자의 수로 나눈 것이다.
본 발명에서, 에멀젼 E1의 액적의 "유체 역학 직경"(또한, 본원에서는 "나노에멀젼"이라고도 함)은 동적 광 산란(Dynamic Light Scattering)을 기초로 한 방법에 따라 에멀젼상에서 수행한 입자 크기 측정에 의해 결정된다.
입자(P)의 직경은 투과 전자 현미경(TEM) 및/또는 Cryo-TEM으로 수행한 입자 크기 측정에 의해 결정된다.
단계 i)
유중수(w/o) 에멀젼(E1)은 연속상으로서 2종의 오일 (O1) 및 (O2)의 혼합물과 계면활성제를 포함한다. 이것은, 특히 고압 호모게나이저 또는 초음파발생기와 같은 고-전단 장치를 사용하는 이른바 고에너지 방법, 및 자발적인 에멀젼화(또는 용매 확산) 및 상 반전 온도(PIT) 방법과 같은 저에너지 방법 등의, 당업계에 공지된 임의의 통상적인 기법에 따라 제조할 수 있다.
그 중에서도, 저에너지 방법, 보다 구체적으로는 PIT 방법은 캡슐화할 취약 분자가 가공 중에 분해되는 것을 방지할 수 있지 때문에, 약물의 캡슐화에 특히 바람직하다.
PIT 방법은 Shinoda 및 Saito (Shinoda, K. et al., 1968; Shinoda, K. et al., 1969)가 30년 전에 도입한 유기 용매-무첨가 방법(organic solvent-free method)으로, 근본적으로 수중유 에멀젼의 제조에 대한 것이다. 이 방법은 혼합되지 않는 2가지 상에 대해, 온도에 따라 바뀌는 변화되는 고유 용해성을 나타내는, 열에 민감한 비이온성 계면활성제를 이용하여, 수/오일 에멀젼을 안정화시키는 방법이다. 이러한 방식으로, 전체 마크로-에멀젼은, 고정된 조성에서 점진적인 온도 변화가 가해질 때, 전이성 상 반전(transitional phase inversion)을 겪게 된다. 그런 다음, 유중수(w/o) 에멀젼은 온도가 상승하면 수중유(o/w) 에멀젼이 될 것이며, 온도가 감소하면 반대가 될 것이다. 상 반전 온도(PIT)에서, 물과 오일에 대한 계면활성제의 친화성은 균형을 이루어, 나노 크기의 구조를 가진 2개의 연속 마이크로에멀젼이 확립되게 된다. 여기서, 오일/물 에멀젼의 제조에 적용되어, 동적으로 안정적인 나노에멀젼 액적을 형성하는 비가역적인 공정으로 사용되는 'PIT 방법'은, PIT에서 신속한 냉각 및/또는 갑작스러운 물 희석을 수행함으로써, 그러한 2중 연속적인 나노미터형 네트워크를 갑작스럽게 해체시킨다.
본 발명자들은 오일 연속상 중의 나노에멀젼을 제조하기 위해, 변형되고 개질된, PIT 방법을 기초로 한 방법들을 최근에 개발하였다. 주로, 이러한 방법은, (i1) 대략 PIT에서의 온도 사이클링 단계, 및 (i2) 전이성 마이크로에멀젼 구조를 해체시켜 즉시 나노에멀젼을 제조하기 위한 갑작스러운 희석 단계로 나누어진다. 그래서, 이 단계가 o/w 나노에멀젼을 만들기 위해 물 희석에 의해 통상적으로 수행되면, 전이성 마이크로에멀젼은 오일로 갑자기 희석되며, w/o 나노에멀젼이 형성되게 된다.
따라서, 바람직한 구현예에서, (w/o) 에멀젼(E1)은 PIT 방법에 따라 제조되며, 온도가 상 반전 온도(PIT) 보다 높을 경우 물 보다 비휘발성 오일(O2)에 더 잘 용해되고, 온도가 PIT 보다 낮을 경우에는 비휘발성 오일(O2) 보다 물에 더 잘 용해되는 계면활성제(S1)를 포함한다.
보다 구체적으로는, 유중수(w/o) 에멀젼(E1)은 아래 단계를 포함하는 방법에 따라 제조된다:
i1) 대략 PIT에서의 온도 사이클링을 수행함으로써, 비휘발성 오일(O2), 물 및 계면활성제(S1)를 포함하는 3성분 혼합물로부터 나노구조의 이중 연속 시스템(bicontinuous system)을 제조하는 단계;
i2) 휘발성 오일(O1)을 첨가하여, 액적이 10 내지 400 nm의 범위의 유체 역학 평균 직경을 가진, w/o 에멀젼을 제조하는 단계; 및
i3) 선택적으로, 추가량의 계면활성제(S2)를 첨가하는 단계.
본원에서, 용어 "휘발성 오일"은 물 보다 휘발성이 높으며, 끓는점이 물 보다 낮고, 특히 50℃ 이하, 바람직하게는 25℃ 내지 50℃의 범위인, 오일을 의미한다. 단계 i)에 따라 나노에멀젼을 제조하는데 적합한 휘발성 오일의 예는, 특히 i) 이소펜탄(Bp = 28℃) 또는 펜탄(Bp = 36℃)이다.
본원에서, 용어 "비휘발성 오일"은 물 보다 휘발성이 낮으며, 끓는 점이 물 보다 높고, 바람직하게는 150℃ 보다 높은, 오일을 의미한다.
비휘발성 오일(O2)은 약학적으로 허용가능한 것이 바람직하다.
본원에서, "약학적으로 허용가능한"은 확실한 의학적 판단 범위내에서 과도한 독성, 자극, 알레르기 반응 또는 적정한 이점/위험도 비에 상응하는 다른 합병증 문제 없이, 인간 및 동물의 조직과의 접촉에 적합한, 그러한 오일을 의미한다.
바람직하게는, 비휘발성 오일(O2)은 페트롤륨으로부터 수득되는 포화 탄화수소 혼합물을 의미하는 표준화된 명칭의 소위 '라이트 미네랄 오일(light mineral oil)'이며, 유리하게는 약학적으로 허용가능하다.
바람직하게는, O1/O2의 체적비는 1 보다 크고, 특히 3 보다 크며, 보다 구체적으로는 5보다 크다.
바람직하게는, 계면활성제(S1)의 상 반전 온도(PIT)는 50℃ 보다 낮다.
바람직하게는, 계면활성제(S1)는 비이온성이다. 바람직하게는, 폴리옥시에틸렌 모이어티를 포함하며, 특히 폴리옥시에틸렌 C6-C18 지방산 에스테르, 예컨대 POE-300-스테아레이트이다.
라이트 미네랄 오일(O2), 물 및 POE-300-스테아레이트(S1)로 구성된 3성분 혼합물에서, 100 x 물/(물 + 오일) 중량비는 바람직하게는 30 내지 90의 범위이고, 및/또는 계면활성제(S1) 양은 3성분 혼합물 전체 중량 대비 5 내지 15 중량%이며, 바람직하게는 8 내지 13 중량%이다.
단계 i1)
w/o 나노에멀젼(E1)의 제조에 적용되는 PIT 방법의 i1) 단계에서, 3성분 혼합물{물/비휘발성 오일(O2)/계면활성제(S1)}은 나노구조의 이중 연속 시스템으로 구조화되며, 이는 열역학적으로 동역학적으로 매우 안정적인 중간 단계이다.
본원에서, 용어 "나노구조의 이중 연속 시스템"은, 오일 상과 수 상이 상호 연결된 연속 도메인에 존재하고 계면활성제가 그 계면에 위치하는 것을 의미한다. 또한, 이러한 나노구조의 이중 연속 시스템은 "윈저(Winsor) IV 이중 연속 마이크로에멀젼"이라고도 한다.
온도 사이클링은, 온도를 PIT 보다 높게, 특히 최대 30℃ 높게 승온시킨 다음 PIT 보다 낮게 냉각시키는 것으로 구성된다. 이를 위해, PIT는 바람직하게는 70℃ 보다 높지 않다. 이러한 온도 사이클링은 이중 연속 시스템의 안정화를 형성 및 유도할 수 있게 해준다. 나아가, 본 발명자들은 사이클 수와 더불어 액적의 직경과 다분산 지수(PDI: polydispersity index)를 낮춘다는 측면에서, 수득되는 나노에멀젼(E1)의 품질이 향상됨을 확인하였다.
온도 사이클링의 가열 및 냉각 속도는 중요하지 않으며, 넓은 범위내에서 다양할 수 있다. 실제, 나노에멀젼 E1을 형성하는데 필요한 사이클의 수에만 영향을 나타낼 뿐이다. 예컨대, 가열 및 냉각 속도를 dT/dt = ± 1.5 ℃/min로 하는 경우, 6회, 심지어 3회 사이클만으도로 다분산 지수가 낮은 나노에멀젼 E1을 수득하기에 충분할 수 있다.
온도 사이클링은 선택한 사이클 수로 이루어지며, 수득되는 이중 연속 시스템은 거의 PIT 온도에서, 바람직하게는 적절한 교반 하에 안정화된다.
양친성 물질로 구성된 쉘을 포함하는 나노캡슐을 가진 조성물의 제조에, 이러한 방법을 적용하였을 때, 이러한 양친성 물질은 다른 예로 단계 ii) 대신 단계 i1)의 개시시에 첨가될 수 있음을 유의하여야 한다.
단계 i2)
그 후, 단계 i2)에서, 소정의 온도에서 반투명의 푸른빛이 도는 이중 연속 시스템을 휘발성 오일 O1로 갑자기 희석하면, w/o 나노에멀젼 E1이 즉시 비가역적으로 제조된다. 연속 상은 실제 휘발성 오일 O1과 비휘발성 오일 O2의 혼합물이다.
희석 단계 동안의 이중 연속 시스템의 교반과 교반 속도는 나노-액적 형성 메카니즘에 영향을 미치지 않지만, 중앙 부분의 균질화를 향상시키고 균질화를 확보할 수 있게 하여, 특히 다분산 지수가 낮은 나노에멀젼을 수득할 수 있음을, 유념하여야 한다.
본 발명의 방법에서, 휘발성 오일 O1은 바람직하게는 펜탄 또는 이소펜탄 등의 물 보다 점성이 낮은 물질이다.
일반적으로, O1는 이중 연속 시스템 체적의 2배에 해당되는 체적 이상으로 첨가하여 w/o 나노에멀젼(E1)을 제조한다.
이러한 휘발성 오일 O1은, 점성이 물보다 상대적으로 낮아, 보다 신속하게 서로 연결된 이중 연속 도메인 모두에 침투하여, 따라서 유중수 에멀젼(E1)을 만들게 될 것이다.
단계 i3)
본 발명에 따른 PIT 방법은 또한 단계 i3)에서 계면활성제(S2)의 추가량을 첨가하는 것을 포함할 수 있다. 실제, 나노에멀젼 연속 오일 상 내부에 추가적인 계면활성제의 첨가는 비가역적으로 현탁물을 안정화시키는 결과를 초래하여, 즉 액적의 응집화를 방지하는 것으로 관찰되었다.
바람직하게는, 액적의 우수한 안정성을 확보하기 위한, 추가량의 계면활성제(S2)는 계면활성제 총량의 30 중량% 내지 40 중량%이다.
계면활성제 분자(S2)는 수계 액적을 둘러싸 피복함으로써, 이의 입체적인 안정성을 유도하는 것으로 추측된다.
추가적인 계면활성제(S2)는 단계 i1)에서 사용되는 (S1)과 동일하거나 다를 수 있다.
바람직하게는, 계면활성제(S2)는 수 상 보다 오일 상에 더 잘 용해된다. 계면활성제(S2)는 특히 POE 300 스테아레이트와 같은 폴리옥시에틸렌 지방산일 수 있다.
단계
ii
)
단계 i)을 종료한 후 형성된 에멀젼(E1)의 수계 액적은 선택적으로 단계 iii) 전에 "셀"에 의해 강화될 수 있다.
본 발명의 내용에서, "쉘"은 수계 액적을 둘러싸고 있으며, 수계 액적 안정성을 강화시킬 수 있는 층을 의미한다.
따라서, 방법의 선택 단계 ii)에서, 에멀젼(E1) 액적의 계면은 폴리머의 2차 구조 네트워크 또는 양친성 물질에 의해 보강된다.
바람직한 측면에서, 에멀젼(E1)의 액적은 폴리머에 의해 강화된다.
바람직한 구현예에서, 단량체는 수 상과 반응하여 계면의 중합을 개시하며, 오일 상에 용해되고, 즉 수 상 보다 오일 상에 더 잘 용해되고, 및/또는 계면활성제(들) (S1) 및/또는 (S2) 또는 에멀젼 E1에 존재하는 임의의 다른 화합물과는 반응하지 않는다.
바람직하게는, 단량체는 2개의 디이소시아네이트(-N=C=O) 기를 포함한다. 단량체의 예로서, 톨릴렌-2,4-디이소시아네이트(TDI), 이소포론 디이소시아네이트 또는 4,4-메틸-비스(페닐이소시아네이트)를 들 수 있다. 가장 바람직하게는, 단량체는 톨릴렌-2,4-디이소시아네이트(TDI)이다.
이론에 결부시키고자 하는 것은 아니며, 물 액적과의 접촉시, 단량체 분자의 이소시아네이트 관능기는 아민기가 되어, 물 보다 반응성이 높아져, 선호적으로 다른 이소시아네이트 단량체와 반응하여 폴리유레아를 형성하게 된다. 따라서, 화학 반응은 단계적인 중합이며, 물과 오일(단량체 저장소) 둘다와 접촉하여 연속적으로 되는 생장에 폴리유레아 체인이 필요하기 때문에, 폴리머 쉘의 제조되는 두께는 분자 범위에서 유익하며, 그리드(grid)형의 계면 네트워크가 형성되게 된다.
이롭게는, 폴리머 "그리드" 밀도는 단량체 농도에 따라 변경될 수 있다. 단량체 함량이 높을수록 형성되는 폴리머는 "그리드"에 가까워진다. 따라서, 친수성 분자의 캡슐화를 위해서는, 저농도의 단량체가 더 작은 크기의 캡슐화에 요구될 것이다.
바람직하게는, 에멀젼(E1)의 오일 상의 단량체 농도는 0.05 mg.L-1 보다 높고, 특히 0.5 mg.L-1 보다 높으며, 특히 0.6 내지 0.8 mg.L-1의 범위이다.
다른 구체적인 구현예에서, 에멀젼(E1)의 액적은 양친성 물질에 의해 강화된다.
양친성 물질은, 특히 계면활성제, 합성 또는 생물학적 폴리머를 포함한다.
본원에서, 용어 "생물학적 폴리머"는 단량체 유닛 30개 이상, 전형적으로 개별 단량체 단위 최대 100개로 구성되는, 천연에서 발견되는 분자를 의미하는 것으로 이해된다. 단량체 유닛은 특히 당(sugar), 아미노산 및 뉴클레오티드일 수 있다.
본 발명의 내용에서, 용어 "생물학적 폴리머"는 또한 단량체 유닛 30개 또는 그 이하로 포함하는 "바이오-올리고머"를 포함한다.
생물학적 폴리머의 예로는, 펩타이드, 단백질(전체(globular) 또는 섬유성), 예컨대 콜라겐(아미노산 단량체), 다당류, 예컨대 셀룰로스, 알기네이트 또는 키틴(당 단량체), 핵산, 예컨대 RNA 및 DNA(뉴클레오티드 단량체)를 들 수 있다
본원에서, 용어 "합성 폴리머"는 동일하거나 상이할 수 있는 최대 천개의 개별 단량체 유닛으로 전형적으로 구성된 거대 분자를 의미한다. 즉, 용어 "합성 폴리머"는 동형폴리머 또는 공중합체를 포함한다. 본 발명의 내용에서, 합성 폴리머는 계면활성제를 포함할 수 있다.
바람직하게는, 양친성 물질은 계면활성제 S4, 특히 비이온성 계면활성제이다.
바람직하게는, 계면활성제는 친수성 친지성 밸런스(HKB)가 10 이상이다.
바람직하게는, 계면활성제 S4는 폴리소르베이트, 가장 바람직하게는 폴리소르베이트 80이다.
단계
iii
)
본 단계에서, 선택 단계 ii)에서 수득되는 시스템은 휘발성 오일 O1과 비휘발성 오일 O2의 혼합물에 분산된 폴리머 쉘 수계 코어의 나노캡슐(NC)를 포함한다. 다른 구현예에서, 단계 ii)에서 수득되는 시스템은 양친성 물질로 구성된 쉘을 가진 수계 코어 나노캡슐(NC)을 포함한다.
다른 구현예에서, 본 단계에서, 시스템은 휘발성 오일 O1과 비휘발성 오일 O2의 혼합물에 분산된 에멀젼(E1)의 수계 액적을 포함한다.
단계 iii)에서, 입자(P)의 조성물은, 단계 ii) 또는 i)에서 수득되는 분산물에 이의 부피에 바람직하게는 4 내지 5배의 물을 첨가하고, 바람직하게는 동시에 휘발성 오일 O1을 특히 O1의 끓는점 보다 높은 온도, 바람직하게는 (E1)의 끓는점에서 20℃ 높게 승온하여 증발을 통해 제거함으로써, 수득한다.
임의의 이론에 결부시키고자 하는 것은 아니며, 지질 쉘-수계 코어의 입자(P) 형성을 설명해줄 수 있는 가설은, 특히 증발을 통해 휘발성 오일을 제거하는 에너지가, 특히 구체적으로는, 휘발성 오일의 양이 매우 적어지면, 시스템의 우수한 균질화를 가능하게 한다는 것이다. 비휘발성 오일 O2은 오일 상에 처음에 존재하는 나노캡슐(NC) 상에 분포되어 있어, 소형의 수계 코어-지질 쉘 입자(P)가 수득된다. 따라서, 입자(P)의 크기는 비휘발성 오일(O2)의 잔류량에 따라 유용하게 조절할 수 있다.
또한, 휘발성 오일 O1이 증발되면, 오일 상의 부피가 감소되면, 오일 상에 용해되는 계면활성제(S1)는, 점차 오일 상에서, 특히 O2에서 결정화되는 것으로 관찰되었다. 마지막으로, 고체 계면활성제(S1)는 액적을 둘러싸고 있는 오일 상에 봉입되어, 폴리머 쉘 또는 양친성 물질(NC)에 의해 선택적으로 보호된 수계 코어를 싸고 있는, 비정질 고체 계면활성제 및 오일(O2)을 포함하는 매트릭시얼(matricial) 지질 쉘을 형성하게 된다.
단계
iv
)
바람직한 측면에서, 본 발명의 방법은 수 상에 친수성 계면활성제(S3)를 첨가하는 단계 iv)를 더 포함한다. 이러한 부가적인 단계는 실제 유익하게 수득되는 입자(P)를 안정화시키고 이의 응집을 방지하도록 한다
본원에서, "친수성 계면활성제"는 "친수성 친지성 밸런스"(HLB)가 12 보다 높은, 보다 구체적으로는 14 보다 높은 계면활성제를 의미한다.
적합한 친수성 계면활성제(S3)의 예로, POE 660 하이드록시스테아레이트(Solutol HS15®)를 들 수 있으며, 이의 HLB는 14 내지 16일 수 있다.
다른 구현예에서, 상기 방법은 또한 단계 iii)에서 수득한 조성물을 물로 더욱 희석하는 추가적인 단계를 포함할 수 있다.
친수성 및/또는
친지성
물질의 캡슐화
본 발명에 따른 방법에 의해 수득가능한 입자(P)는, 친수성 또는 친지성 물질 또는 이 두가지를 병합할 수 있다.
친수성 및 친지성 물질은 특히 약제, 진단제, 화장료, 수의학 제품, 식물 위생 제품 또는 가공 식품 중에서 선택할 수 있다.
친수성 물질은, 방법의 단계 i)에서, 보다 구체적으로는 나노구조의 이중 연속 시스템을 제조하도록 의도한 수 상에 투입할 수 있다.
바람직하게는, 친수성 물질을 포함하는 수용액은, 단계 i1)에 따른 이중 연속 시스템을 형성한 후, 단계 i2)에 따라 휘발성 오일 O1을 첨가하기 전에, 첨가한다. 즉, 3성분 혼합물(비휘발성 오일(O2)/물/계면활성제(S1)}을 이중 연속 시스템으로 만드는 온도 처리는, 캡슐화시킬 친수성 물질에 이롭게 작용하진 않는다.
첨가되는 수용액의 부피는 바람직하게는 이중 연속 시스템의 부피에 비해 매우 작으며, 특히 1 내지 5 부피%일 수 있다. 따라서, 이러한 농축된 용액은 이중 연속 시스템의 수계 파트에 매우 신속하게 혼입될 것이며, 단계 i2)에 따라 휘발성 오일 O1로 희석한 후 나노에멀젼 E1으로 동일하게 제조될 것이다.
친지성 물질과 관련하여, 이는 계면 중합 단계 ii) 후 및 단계 iii) 전에 첨가하는 것이 바람직하다. 이로 인해, 휘발성 오일의 증발이 완료된 후, 친지성 물질이 입자(P)의 오일 상에 동등하게 분배된다.
다른 측면에서, 본 발명은 입자(P) 직경이 20 내지 500 nm 범위인 입자를 수계 상에 포함하는 조성물에 관한 것으로서, 상기 입자는
- 오일 상;
- 상기 오일 상 중에
- 수계 액적(droplet) 또는
- 하기 성분을 포함하는 나노캡슐(NC)
- 수계 코어, 및
- 폴리머 쉘 또는 양친성 물질로 구성된 쉘;
및
-계면활성제를 포함한다.
본 조성물은 본 발명의 방법에 따라 수득가능하다.
본 발명의 일 측면에서, 입자(P)에는, 오일 상에, 선택적으로 친수성 물질을 포함하는 수계 액적이 포함되어 있다. 이러한 구현예는 특히 고분자량의 다양한 친수성 물질을 캡슐화하는데 특히 적합하다.
이러한 친수성 물질의 예로는 특히 단백질, 플라스미드, 항체, 다당류가 있다.
다른 측면에서, 입자(P)에는 오일 상에, 수계 코어와 쉘을 포함하는 나노캡슐(NC)이 포함되어 있다.
일 측면에서, 나노캡슐(NC)은 양친성 물질로 구성된 쉘을 포함한다.
바람직한 측면에서, 나노캡슐(NC)은 폴리머 쉘을 포함한다.
바람직하게는, 폴리머 쉘은 폴리유레아로 구성된다.
바람직하게는, 입자(P)의 나노캡슐(NC)의 직경은, 투과 전자 현미경(TEM) 및/또는 Cryo-TEM으로 측정한 입자 크기에 따르면, 10 내지 400 nm, 특히 약 50 nm이다.
바람직하게는, 수계 코어에는 친수성 물질이 포함된다.
바람직하게는, 오일 상에는 친지성 물질이 포함된다.
유익하게는, 본 발명에 따른 조성물은 다분산 지수가 0.5 미만, 특히 약 0.1 미만인 것이 특징적이다.
다른 측면에서, 본 발명은 하기 단계를 포함하는 방법으로 수득가능한 유중수(w/o) 에멀젼(E1)에 관한 것이다:
i1) 대략 PIT에서 온도 사이클링을 수행함으로써, 비휘발성 오일(O2), 물 및 계면활성제(S1)를 포함하는 3성분 혼합물로부터 나노구조의 이중 연속 시스템(bicontinuous system)을 제조하는 단계;
i2) 휘발성 오일(O1)을 첨가하여, 액적이 10 내지 400 nm 범위의 유체 역학 평균 직경을 가진, w/o 에멀젼을 제조하는 단계; 및
i3) 선택적으로, 추가량의 계면활성제(S2)를 첨가하는 단계로서,
상기 비휘발성 오일(O2)은 파라핀 오일이고, 휘발성 오일(O1)은 펜탄 또는 이소펜탄이다.
또다른 측면에서, 본 발명은
- 연속 상으로서, 휘발성 오일인 이소펜탄 또는 펜탄 및 비휘발성 오일인 파라핀 오일;
- 불연속 상으로서 물; 및
- 계면활성제(S1)를 포함하는, 유중수(w/o) 에멀젼(E1)에 관한 것이다.
바람직하게는, 계면활성제(S1)는 폴리옥시에틸렌 모이어티를 포함한다.
이러한 에멀젼(E1)은 안정성이 우수하여, 본 발명에 따라 입자(P)의 안정적인 조성물의 제조가 가능하다는 점에서 특히 유익하다.
또다른 측면에서, 본 발명은 친수성 및/또는 친지성 물질의 캡슐화를 위한 본 발명에 따른 입자(P)의 조성물의 용도에 관한 것이다.
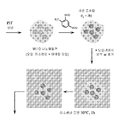
도 1: 본 발명에 따른 입자(P)의 조성물 제조 방법에 대한 개략도. 중축합 시간, tp는 2시간으로 고정하였다.
도 2: 본 발명에 따른 입자(P)의 조성물의 희석(1/10) 샘플의 네거티브 염색 기법(염료: 우라닐 아세테이트)과 조합된 TEM.
도 3 (a) (b), (c): 본 발명에 따른 입자(P)의 조성물의 희석(1/10) 샘플의 Cryo-TEM 및 (a), (b), (c)에 기재한 경로에 따른 전자 강도의 상세 내용.
도 4 및 5: 친수성 분자의 캡슐화 수율에 대한 제형 파라미터의 영향
도 4: 제형화에 대한 첨가한 단량체의 양 효과, 메틸렌 블루(MB) 및 BSA-FITC 간에 비교하며, 중축합 시간 tp는 2시간으로 고정됨.
도 5: 단량체를 3가지의 양 0.07, 0.22 및 0.44 mg·mL- 1으로 사용하였을 때, MB에 대한 tp의 영향. 화살표는 입자(P) 제조의 전과정의 선택 시간을 나타낸다.
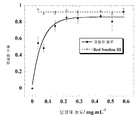
도 6: 친수성(메틸렌 블루(MB)) 및 친지성(레드 수단(RS)) 분자의 동시 캡슐화하는 캡슐화 수율에 대한 단량체의 양 효과. 중축합 시간 tp는 2시간으로 고정된다.
도 7: 클로르하이드레이트 독소루비신(DOX)의 캡슐화 수율에 대한 단량체의 양 효과.
도 8: 입자(P)에서의 독소루비신 클로르하이드레이트의 방출 속도.
도 2: 본 발명에 따른 입자(P)의 조성물의 희석(1/10) 샘플의 네거티브 염색 기법(염료: 우라닐 아세테이트)과 조합된 TEM.
도 3 (a) (b), (c): 본 발명에 따른 입자(P)의 조성물의 희석(1/10) 샘플의 Cryo-TEM 및 (a), (b), (c)에 기재한 경로에 따른 전자 강도의 상세 내용.
도 4 및 5: 친수성 분자의 캡슐화 수율에 대한 제형 파라미터의 영향
도 4: 제형화에 대한 첨가한 단량체의 양 효과, 메틸렌 블루(MB) 및 BSA-FITC 간에 비교하며, 중축합 시간 tp는 2시간으로 고정됨.
도 5: 단량체를 3가지의 양 0.07, 0.22 및 0.44 mg·mL- 1으로 사용하였을 때, MB에 대한 tp의 영향. 화살표는 입자(P) 제조의 전과정의 선택 시간을 나타낸다.
도 6: 친수성(메틸렌 블루(MB)) 및 친지성(레드 수단(RS)) 분자의 동시 캡슐화하는 캡슐화 수율에 대한 단량체의 양 효과. 중축합 시간 tp는 2시간으로 고정된다.
도 7: 클로르하이드레이트 독소루비신(DOX)의 캡슐화 수율에 대한 단량체의 양 효과.
도 8: 입자(P)에서의 독소루비신 클로르하이드레이트의 방출 속도.
실시예
1. 재료 및 방법
1.1. 재료
테크니컬 그레이드의 폴리에톡시된 계면활성제 C18E6은 Stearinerie-Dubois (Boulogne, France)로부터 친절하게 제공받았다. 이는 푸아송-계 에틸렌 옥사이드(EO) 분포가 약 6인 전형적인 상업 제품이다. 이것은 다소 친지성의 양친성이며, 즉 EO 수치가 낮으며, '라이트 미네랄 오일' 및 물 + 전해질(NaMl)로 구성된 에멀젼을 안정화시킬 것이다. 라이트 미네랄 오일은 Cooper (Melun, France)에서 구입하였으며, 이는 페트롤륨으로부터 수득되는 포화 탄화수소를 의미하는 표준 명칭이다. 초순수수(ultrapure water)는 MilliQ® 여과 시스템(Millipore, Saint-Quentin-en-Yvelines, France)에 의해 수득하고, 소듐 클로라이드는 Prolabo (Fontenay-sous-Bois, France)에서 구입하였다. 마지막으로, 매우 유동적이며 휘발성인 비극성(apolar) 상을 제2 오일로 사용하였고, 또한 과정의 중요 물질로서 사용하였다: 이소펜탄(2-메틸부탄)은 Riedel-de-Han (Germany)사에서 구입하였고, 이것은 25℃에서의 절대 점성, η은 0.35 mPa·s이고, 끓는점은 Bis . p = 28℃이다.
메틸렌 블루(MB), 소 혈청 알부민 - 플루오레세인 이소티아시아네이트 표지물(BSA-FITC), 레드 수단(RS)은 시그마에서 구입하였다.
1.2. 입자(P) 조성물의 제조
입자(P)의 조성물은 하기 성분(표 1)을 기초로 일반적인 공정에 따라 제조하였다.
| 마이크로에멀젼 제조 | 양 |
| NaCl | 0.8 g |
| MilliQ 물 | 26.88 g |
| 파라핀 오일 | 40.32 g |
| POE 300 스테아레이트 | 7.46 g |
| 나노에멀젼 제조( E 1 ) | |
| POE 300 스테아레이트 | 0.4 g |
| 이소펜탄 | 30 ml |
| 계면 중축합 | |
| 톨릴렌-2,4-디이소시아네이트 | 이소펜탄 중의 0.7 mg/L |
| 증발 | |
| MilliQ 물 | 20 ml |
1.2.1. 유중수 나노에멀젼(E1)의 제조
'라이트 미네랄 오일' 및 MilliQ 물(100 x 물/(물+오일) 중량비: WOR = 40) + NaCl(수 중의 농도: 0.51 M)를, PEO 단쇄가 있는 비이온성 폴리에톡시화된(PEO) 계면활성제(PEO-300 스테아레이트, 10 wt.%)에 의해 안정화하였다. PEO-300 스테아레이트는 이러한 "라이트 미네랄 오일"에 자유롭게 용해되지만 물에는 용해되지 않는다(Yu, C. D., 1994).
이 시스템은 온도에 따라 결정적으로 에멀젼 상 반전이 될 수 있다(Salager, J. L. et al., 2004; Anton, N. et al., 2007). 이러한 현상, 제형 및 조성물 파라미터의 영향 뿐만 아니라 이러한 3성분 시스템의 특정화는 이전 연구들에서 심도깊에 연구되었다(Anton, N. et al., 2007). 따라서, 시스템이 에멀젼 상 반전 온도(PIT)에서 정확하게 유지되었을 때, 이중 연속 마이크로에멀젼(Winsor IV-like)은 자발적으로 나노미터 규모로 구조화된 푸른빛이 도는 반투명 형상을 나타내게 된다(Kahlweit, M. et al., 1985; Forster, T. et al., 1995; Morales, D. et al., 2003; Izquierdo, P. et al., 2004). 다음으로, 전이성 마이크로에멀젼을 '구조화'하기 위해, 다수의 온도 사이클과 더불어 나노미터-규모의 네트워크의 정교성을 점차적으로 증가시키면서, 온도 사이클링 처리를 PIT 부근 온도(35 < T < 60℃)에서 수행한다.
마지막 단계로, PIT에서 나노미터의 이중 연속 시스템을 갑자기 물 보다 유동성이 큰 다른 오일(이소펜탄)로 희석한다. 유중수 나노에멀젼이 즉각적으로 제조되며, 이는 전형적으로 액적의 유체 역학 직경 ~ 40 nm을 나타내며 매우 만족스러운 다분산 지수 ~0.05(Nano ZS Malvern 장치를 이용하여 수행한 측정)를 나타낸다. 이러한 w/o 나노에멀젼의 탈안정화 메카니즘은, 액적간의 상호작용 프로파일이 일반적으로 딥 프라이머리 미니멈(deep primary minimum)을 보이는, 역위된 에멀젼의 전형적인 콜로이드 응집 과정을 따르는 것으로 확인되었다.
나아가, 확립된 나노에멀젼을 수득한 후, 나노에멀젼의 연속 오일 상 내부에 다른 계면활성제(또한, POE-300 스테아레이트)를 첨가하여, 비가역적으로 현탁액을 안정화시키고, 즉 응집 과정을 방지한다. 실제, 액적의 우수한 안정성을 확보하기 위해, 계면활성제의 총 양의 ~35 중량%에 해당되는 계면활성제를 첨가한다. 비이온성 계면활성제 분자는 수계 액적을 둘러싸고 피복함으로써, 이들 사이의 입체적 안정성을 유도하는 것으로 추측된다.
1.2.2. 계면 중축합
계면 중축합 단계는 이차원의 폴리유레아 필름을 w/o 나노에멀젼 주형 상에 피복함으로서 이루어지는 단계적 과정이다. 선택한 단량체에 의해 만족되는 기준은, (i) 연속 오일 혼합물(이소펜탄 + 미네랄 오일)에 대한 자유 용해성, 및 (ii) 분산된 수계 상과의 우수한 반응성이다. 도 1을 참조하면, 톨릴렌-2,4-디이소시아네이트(TDI)를 본 구현예에서 선택하였다. 이러한 방식으로, 수 액적과 접촉하는 단량체 분자의 이소시아네이트 관능기가 아민기가 되고, 그런 후 물 보다 반응성이 높아지게 되어 다른 TDI 분자와 선호적으로 반응하게 될 것이다.
따라서, 화학 반응은 단계적인 중합이고, 폴리유레아 체인이 물과 오일(단량체 저장소) 둘다와 접촉하면서 연속적으로 성장하는데 필요하므로, 제조되는 폴리머 쉘의 두께는 분자 범위내일 것이며, 그리드(캡슐화 수율과 관련한 하기 결과에 의해 뒷받침되는 개념임)로서 짐작할 수 있는 계면 네트워크를 형성하게 될 것이다. 단량체와, 캡슐화될 분자의 잠재적인 NH2 기 사이의 반응이, 폴리머 필름의 형성을 방해하지 않을 것으로 생각된다. 캡슐화 수율에 있어 중축합 시간, tp의 효과는 하기에 나타내었으며, 궁극적으로 제형 최적화를 위해 2시간으로 고정하였다.
1.2.3. 나노캡슐(NC)의 제조
본 단계에서, 실험 시스템은 그리드-형 구조를 나타낼 것으로 예상되는 폴리유레아 이차원 필름에 의해 둘러싸여 있으며, 이소펜탄(PIT 희석 유래) 및 미네랄 오일(초기 에멀젼)의 벌크 오일 혼합물에 분산되어 있는, 수계 나노-액적으로 구성된다. 또한, 아직까지 반응하지 않은 일부 단량체 분자가 오일에 존재할 가능성을 고려해야 한다.
그래서, 수계 코어의 나노캡슐의 제조(도 1 참조)는, 간략하게, (i) 외부 상이 될 추가적인 수 상을 첨가하고, 동시에 (ii) 이소펜탄의 끓는점(Bis.p = 28℃) 보다 상당히 높게 고정된 온도, 예컨대 50℃에서 한시간 동안 보일러에서 증발시켜 이소펜탄 상을 제거함으로써 달성한다.
그로 인해, 이러한 증발 단계에 제공되는 에너지는 휘발성 오일의 신속한 제거 뿐만 아니라 오일의 전체 부피를 감소시키면서 즉각적인 액적 응집을 방지하는 샘플의 적합한 균질화를 부여할 수 있게 해준다. 수계 액적은 비극성 상에 동등하게 분포될 가능성이 있어, 수중에 별개의 콜로이드 물질의 제조를 유도할 수 있다. 이러한 방식에서, 비휘발성 미네랄 오일이 비극성 상에 존재하기 때문에, 이소펜탄 증발이 완료되었을 때, 최종적으로 새롭게-형성된 콜로이드 입자 상에 분배되게 된다. 더욱이, 사용한 PEO 비이온성 계면활성제는 오일이 증발됨에 따라 전체적으로 물에 난용성이 되기 때문에, 즉, 오일 부피가 감소되기 때문에, 양친성 물질은 오일 중에 점차적으로 결정화될 것이다. 최종적으로, 고체 계면활성제는 액적을 둘러싸고 있는 제조되는 미네랄 오일에 봉입될 것이며, 그래서 폴리머 필름에 의해 보호되어 있는 수계 코어를 싸고 있는 미네랄 오일과, 양친성 고체 계면활성제로 구성된 매트릭시얼 리피드 쉘(matricial lipid shell)이 형성되게 된다(도 1에 기술된 구조). 이러한 캡슐 구조는 아래 전자 현미경 실험에 의해 뒷받침되며, 또한 친수성 및 친지성 분자를 동시에 캡슐화하는 우수한 능력에 의해 뒷받침된다. 마지막으로, 자유 단량체가 오일 중에 남아있을 가능성과 관련하여, 이것은 형성된 폴리머 막과 접촉하거나(말단 NH2기에 의해) 또는 외부 수 상과 접촉하여 명백하게 중화(또한 미네랄 오일에 봉입되었기에)된 것으로 보인다.
1.2.4. 나노캡슐(NC)의 특정화
현미경 관찰
투사 전자 현미경( TEM ). 각각의 수계 분산물의 샘플 한방울을 탄소 코팅된 TEM 구리 그리드(Quantifoil, Germany)에 먼저 넣고, 공기 건조시켰다. 그런 후, 샘플을 우라닐 아세테이트(Merck, Germany)로 네거티브 염색하였다. 이를 위해, 샘플-코팅된 TEM 그리드에 우라닐 아세테이트 수용액(2 wt.%) 한 방울과 증류수 한 방울을 차례대로 처리하였다. 그 후, 그리드를 전자 현미경에 넣기 전에 공기 건조하였다. 샘플은 80 kV에서 작동하는 JEOL JEM-1230 TEM을 이용하여 검경하였다.
Cryo - TEM. cryo-TEM 관찰용 샘플을 글로우-방전(glow-discharged) 홈이 있는 형태의 탄소-코팅 그리드(Ted Pella Inc., USA) 상에 수계 현탁액 한방울이 있는, 크리오플러지(cryoplunge) cryo-고정기(Gatan, USA)를 이용하여 준비하였다. 그 후, 샘플이 포함된 용액 한 방울을 지지 탄소 필름에서 구멍 횡단 두께가 약 50-500 nm인 액체 박층에 블롯팅하여, TEM 그리드를 준비하였다. 액체 필름은, 그리드를 액체 질소로 냉각시킨 액체 에탄에 신속하게 담구어 유리질화하였다. 유리질화된 샘플을, cryotransfert system (Gatan, USA)을 이용하여 현미경에 삽입하고 액체 질소로 냉각시킨 Gatan 910 샘플 홀더(Gatan, USA) 위에 두었다. 그런 다음, 투명 얼음에 보존시키고, 지지 탄소 기질에서 구멍을 관통하면서 현탁된 샘플로부터 TEM 이미지를 수득하였다. 샘플은 저용량(10e·A2 보다 낮은) 조건에서 -178℃에서, LaB6 필라멘트가 장착되어 있으며, 80 kv에서 작동하는 JEM 1230 'Cryo' 현미경(Jeol, Japan)을 이용하여 관찰하였다. 모든 현미경 사진은 Gatan 1.35 K x1, 04 K x12 bit ES500W Erlangshen CCD 카메라로 기록하였다.
표면 전위 측정
나노캡슐 표면 전위의 이미지로서, η 전위를 Nano ZS (Malvern Instruments)를 이용하여 측정하였다. 스몰루초스키의 모델 링킹 전기영동 이동성(Smoluchowski's model linking electrophoretic mobility) 및 η 전위를 사용하였다. 헬륨-네온 레이저 4 mW를 633 nm에서 작동시켰고, 분산 각도는 25℃의 불변 온도에서 173°로 고정하였다. 그러나, 연질 입자 분석 모델을 통한 표면 특성의 깊이 연구(H. Ohshima, et al., 2006)에서, 캡슐화된 물질이 대상의 표면 전위에 영향을 미치지 않는 것으로 확인되었다. 캡슐화되 물질은 쉘 구조의 역할을 하지 않는 것으로 나타났다.
1.2.5 친수성 및 친지성 모델 분자의 병합
도 1의 전체 제조 공정과 관련하여, 친수성 및 친지성 물질의 병합은 여러가지 방법에 의해 수행될 것으로 보인다.
(i) 친수성 물질은, 궁극적으로 w/o 나노에멀젼 물 액적에 분배되어야 하며, 마크로-에멀젼 조제물의 수 상에 포함된 출발 물질로부터 적절하게 행해질 수 있다. 다른 더욱 효과적인 방법은, 온도 사이클링 후에 그리고 이소펜탄 희석 전에, 고농축된 수용액을 소량(2 % (v./v.) 미만) PIT로 유지시킨 마이크로에멀젼에 주입하는 것으로 구성된다. (여전히) 교반한 마이크로에멀젼에 주입한 액적은 매우 신속하게 이중 연속 네트워크의 수계 파트에 혼입된다. 오일 희석의 결과로, 나노에멀젼이 바로 형성되고, 주입한 친수성 분자는 오일내에 매우 균질하게 분산될 수 있게 된다. 오리지날 방식을 통한 친수성 물질의 병합은, 궁극적으로 온도 사이클링 처리시 가능성 있는 공정 중의 분자의 분해를 방지한다. 친수성 모델 분자는 매우 다양한 분자 중량을 가진 것으로 선택하였다: 첫번째는 불안정한 염료, 메틸렌 블루(MB)이며, 두번째는 단백질, 소 혈청 알부민 플루오레세인 이소티오시아네이트 표지물(BSA-FITC)이고, 마지막은 플루오레센트 화합물, 독소루비신 클로르하이드레이트(DOX)이며, 이것은 항암제이다.
(ii) 한편, 친지성 물질을, 선택한 중합 시간 이후에(단량체와의 상호작용 가능성을 최대한 방지하기 위해), 그리고 이소펜탄 증발 단계 전에, 나노에멀젼의 오일 상에 도입하였다. 그로 인해, 이소펜탄 증발이 완료된 후, 첨가된 친지성 물질은 잔류 미네랄 오일에 봉입된 액적 상에 균등하게 분배될 것이며, 즉 비정질 오일/비이온성 계면활성제 매트릭스에 포획될 것이다. 마지막으로, 이는 잔류 미네랄 오일 위치의 마커로서 보이며, 현저한 캡슐화 수율의 결정은 제안된 다중 기능의 수/오일 구조를 뒷받침하여야 한다. 또한, 친지성 모델 분자는 염료, 레드 수단 III(RS)이다. 본원에서, 친수성 및 친지성 물질을 함유하는 나노캡슐의 제형화 과정은 매우 낮은 에너지만 필요로하는 방법(대개 '저에너지' 방법)으로 간주될 수 있다는 점에서 매우 중요하다. 그래서, 캡슐화된 분자는 에멀젼화 공정 및 장치(예, 고압 호모게나이저 또는 초음파발생기)가 필요하지 않으며, 심지어 온도 사이클링이 필요하지 않다. 캡슐화되는 취성 분자가, 공정 중에 분해될 가능성을 방지한다.
모든 정량 측정은 다음의 비간접 방법으로 수행하였으며, 원심분리(30 min, 14500 rpm)에 의해 나노캡슐을 외부 물과 분리한 후, 동결 건조하여(RP2V, SGD, Le Coudray Saint-Germer, France), 남아있는 나노캡슐의 파괴 가능성으로부터 안전하게 하였다(또한, 정량 측정 과정에서 이의 추가적인 광 흡수를 방지함). 다음으로, 동결 건조한 샘플을 디클로로메탄(DCM)에 용해하고, 외부 물에 존재하는 DOX를 제외한 여러가지 병합 물질을 스펙트로포토미터 UV-visible Uvikon 922 스펙트로포토미터(Bio-Tek Koutron instruments, Saint-Quentin-en-Yvelines, France)를 이용하게 간단하게 정량하였다. DOX는 스펙트로플루오르미터(Fluoroskan Ascent FL, type 374, Thermo Electron Corporation, Finland)를 이용하여 정량하였다. 밴드-패스 필터를 통한 여기 및 방사 광은 각각 485 nm 및 550 nm이다.
1.2.6. 입자(P)에서의 독소루비신 방출율
약물 방출 속도를 설정하기 위해(도 8 참조), DOX-주입된 입자(P)가 함유된 막 제조한 현탁물 2 mL을 15 kDa 투석막(Spectra/Por® Membranes, Fisher Bioblock Scientific, Illkirch, France)에 넣고, 시그마 사의 포스페이트 완충 염수(PBS, pH 7,4) 40 mL을 첨가하였다. 플랙을 약하게 기계적으로 암조건(보일러, Julabo SW22, JULABO Labortechnik GmbH, Seelbach, Germany) 및 37℃에서 교반하였다. 다음으로, 지정된 시간 대에 방출 매질 500 ㎕를 취하여, DOX 농도를 스펙트로플루오르미터로 전술한 바와 같이 측정하였다. 취합한 부피는 "싱크(sink)" 실험 조건을 부여하기 위한 신선한 PBS 동일 부피로 체계적으로 교체하였다.
2. 결과
2.1 나노캡슐의 특정화
수계 코어 나노캡슐의 네거티브 염색한 TEM 사진은 도 2에 나타내며, Cryo-TEM 사진은 도 3에 나타낸다. 이들 2가지의 보완적인 실험 기법으로부터, 보완적인 정보가 도출되었고, 궁극적으로 도 1에 제시된 구조와 매우 일치되었다. 먼저 주목할 사항은 액적의 크기인데, 이는 약 50 nm이며, 측정한 w/o 나노에멀젼 크기와 최종적으로 일치된다(- 오일 + 계면활성제 쉘 두께). 또한, 이론적인 오일/계면활성제 쉘 두께는 나노캡슐을 형성하고 있는 물질, 그 각각의 알고 있는 특성 및 나노캡슐의 추출되는 구조를 보일 것이라는 예상만 고려하여 접근한 것으로, 그 결과 두께는 약 7.5 nm이었다. 이러한 계산 결과는 도 2에 나타낸 코어/쉘 특성에 의해 뒷받침되는 것으로 보인다.
또한, 이들 전자 현미경 사진에서 캡슐의 단분산성은 비교적 우수한 것으로 보이며, 분산 및 그러한 제형화 과정에서의 상대적인 우수성이 입증된다. 물론, 콜로이드 물질의 수계 코어를 가진 캡슐 구조가 도 2에 제시되어 있는데, 이러한 물질은 진공 설정 단계에 따른 측정시에 파열될 가능성이 있기 때문이다. 구멍은 (친수성) 염색제로 덮여, 나노캡슐 내부에 대조 스팟을 형성한다.
대조적으로, 도 3(a), (b), (c)의 Cryo-TEM 사진에서는 온전한 나노캡슐이 보이며, 마찬가지로 입자의 가운데와 가장자리 간의 대비 차이로 인해 캡슐 구조가 보인다. 실제, 유기 물질(species)과 물 간의 차이는 염색제 없이도 이러한 사항을 이해할 수 있을 만큼 충분하게 대비된다. 마지막으로, 도 3에 기술된 전자 밀도에 대한 내용과 관련하여, 특정 쉘 텍스처는 유기 물질이 나노캡슐 쉘에 랜덤 분포(및 폴리머 배열)되어 있음을 나타낸다. 도 1에 나타낸 그리드 형 구조와 제안된 메카니즘은 역시 일치된다.
2.2 안정성
미립자 나노캡슐 구조로 인해, 쉘 프래임워크를 구성하는 폴리머의 존재는, 사용한 계면활성제가 친지성 부분과 관련있는 단쇄 PEO를 가지고 있고 또한 대부분 오일 쉘에서 결정화되기 때문에, 입체 오리진 만큼의 높은 정전기의 반발력(repulsive contributions force)은 매우 낮은 것으로 보인다. 막 제조된 나노캡슐은 매우 우수한 단분산성(Nano ZS Malvern, 적합한 희석 조건)을 보일 뿐만 아니라 다분산 지수도 비교적 양호하여 0.1 보다 낮다. 그 후, 농축된 NC 현탁물은 명백하게 수 중에서의 콜로이드 응집 과정을 통해 빠르게 불안정하게 되어, 약 1달 보관한 후, 크림형의 NC 농축물이 관찰된다. 실제, 충분히 크면(> 1 ㎛), 클러스터는 중력을 받게 된다. 반면, 이러한 과정은 샘플을 단순히 희석(예, 1/100)함으로써 현저하게 단축되며, 현탁물은 수개월간 안정적인 것으로 보인다.
2.3 친수성 및/또는
친지성
분자의 고효율의 나노캡슐화
연속적인 수계 상에 분산되어 있는 나노캡슐 자체에 친수성 물질을 캡슐화하고자 하는 실제 노력 덕분에, 일차 결과는 선택한 친수성 종, 메틸렌 블루 및 BSA-FITC를 그러한 콜로이드로 캡슐화할 수 있는 범위에 관한 것일 것이다. 나노에멀젼 제조 단계에서, 분자의 혼입과 캡슐 수율을 결정하기 위한 분자의 정량화는 전술한 공정 다음에 실시한다. 그에 따른, 제형화 파라미터, 제형에 도입된 단량체의 양 및 중합 시간 tp가 캡슐화 수율에 미치는 효과는 도 4에 나타낸다.
따라서, 최적화된 중축합 시간을 tp = 2시간으로 고정하여, 도 4에서는 캡슐화 수율에 있어 w/p 나노에멀젼에 투입되는 단량체의 양적 효과를 여러가지 친수성 분자 MB 및 BSA-FITC 둘다에서 비교한다. 즉, 수율이 0(null)으로 추측되고 내부의 물이 전체적으로 외부 물쪽으로 흘러나오는, 단량체가 없을 때 캡슐화가 불가능한 것에서부터, 단량체의 최고 함량에서 매우 만족스러운 수율을 수득하는 결과에 있어, 매우 유사한 경향이 나타난다. BM 및 BSA-FITC 둘다에서 수득되는 안정 수준(plateaus)은 약 0.9로 매우 유사하지만, 2종의 분자 간에 존재하는 쉬프트(shift)에 매우 흥미로운 포인트가 보인다. 실제, 소량의 염료에 비해, 더 적은 양의 단량체에 거대 단백질이 유지된다. BSA-FITC의 경우 안정 수준은 이미 약 0.05 mg/mL에서 수득되었으며, MB의 경우에는 0.5 mg/mL 범위이며, 이는 단량체 농도와 폴리머 '그리드' 밀도 사이의 관련성이 존재함을 시사하하는 것일 수 있으며, 단량체 함량이 많을수록 형성된 폴리머는 '그리드'에 가까워진다. 궁극적으로, 중축합 반응은 폴리머 파이버가 그리드형 네트워크를 형성하면서 합생(intergrowth)하는 이차원적인 막을 형성할 뿐이기 때문에, 이러한 결과는 상기에서 제시한 나노캡슐 구조와 일관된다. 여기에서, 이소펜탄이 증발되는 동안, 제공되는 에너지는 캡슐화된 분자의 일부가 외부 물쪽으로 새어나가게 유도할 것이며, 마찬가지로, 이러한 흐름은 폴리머 그리드 밀도가 증가할수록 감소된다. 또한, MB 및 BSA-FITC에서 관찰되는 차이로부터, 캡슐화된 분자의 분자량 역시 공정에 중요한 것으로 보인다. 가장 큰 분자는 그 보다 작은 분자에 비해 폴리머 네트워크에 의해 쉽게 정지되며, 결국 유사한 캡슐화 수율(~ 0.5 mg/mL)에 도달하게 된다.
도 5는 단량체를 3가지 선택 첨가량으로 하여, MB의 캡슐화 수율에 대한 중축합 시간 tp의 영향을 나타낸다. tp는 나노에멀젼에 단량체 첨가한 다음 부터 이소펜탄 증발 단계까지의 지연 시간에 해당된다. 그 시간 동안 샘플은 500 rpm으로 매우 약하게 교반한다. 공정에서 고정 시간(tp = 2시간)은, 임의의 안정화가 각각의 경우에서와 유사하게 신속하게(1시간 미만) 수득되는 것으로 명백하게 보이기 때문에, 최종적으로 본원에서 입증되었다. 또한, 단량체가 오일 박층에 봉입되는(및 내부 물, 폴리머 쉘 또는 외부 물 중 어느 하나와 접촉하도록 가해지는) 이소펜탄 증발 단계 때문에, 모든 TDI 분자는 결국은 폴리유레아 네트워크와 반응하여 연결되도록 압박을 받게 것이다. 이런 점에서, 짧은 tp, 그래서 합성되는 동량의 폴리머에 대해 주어지는 캡슐화 수율 차이는, 나노캡슐 구조내 비-균등적으로 분포된 폴리머에 의한 것일 것이다. 이러한 강제된 중축합(단기 tp 동안의)이 내부 물이 오일을 통과하여 방출됨으로써 캡슐에 폴리머 구멍을 만들 수 있다는 생각을 더욱 뒷받침한다.
현재 친수성 및 친지성 성분의 동시 캡슐화와 관련하여, 동일한 나노캡슐 내부에 메틸렌 블루 및 레드 수단 III을 혼입하는 실험을 수행하였고, 도 6에 나타내었다. 전술한 바와 같이, 캡슐화 수율을 제형에 첨가한 단량체의 양에 따라 측정하였고, 최적화된 중축합 시간은 2시간으로 선택하였다. 마찬가지로, NC 구조에 대해 이전에 제시된 바와 같이, MB는 내부 물에 있고, RS는 오일의 주변 쉘에 있다. 물론, 메틸렌 블루 곡선은 나노캡슐 단독인 도 4에 나타낸 그래프와 매우 유사한 양상을 보인다. 현재의 레드 수단 III는, 단량체의 양이 캡슐화 수율에 영향을 미치지 않는 것으로 명확하게 보이며, 궁극적으로 친지성 분자가 계면 중축합 이후에 오일 상에 첨가되기 때문에, 공정과 일치된다. 그 결과, RS는 오일/비정질 계면활성제 쉘에 봉입되며, 매우 높은 캡슐화 수율, 약 0.92를 나타낸다.
종합하면, 본 발명은 폴리머의 내부 프래임워크에 독특한 영향을 나타내는 친지성 물질을 캡슐화하는 흥미로운 능력을 보일 뿐만 아니라, 친수성(MB) 및 친지성(RS) 모델 분자를 동시에 캡슐화하는 유의한 능력이 있다. 이러한 다중 기능 특성은, 자신의 구조에 액체 물과 오일 저장소를 포함하고 있고, 마찬가지로 콜로이드 범위의 크기를 가지고 있기 때문에, 비교적 독창적으로 보인다.
본 발명의 다른 측면은, 제형 변수에 따른 DOX 캡슐화 수율의 추적을 다루고 있다. 그래서, 철저한 연구를 통해, 2가지의 파라미터만 캡슐화 수율에 유의한 영향을 미치는 것으로 확인되었다: 단량체의 함량과 중축합 시간(tp). tp가 약 1-1.5 시간을 초과하면 수율은 신속하게 안정 수준에 도달하여, 단량체 농도에서 tp = 2시간으로 고정하였다.
한편, DOX 캡슐화 수율에 대한 단량체의 양 영향은 도 7에 나타낸 전형적인 전개를 보인다. 이러한 양상은 나노캡슐 구조와 균질적인 쉘(구멍 없음)의 형성이 단량체의 농도, 즉 액적 계면에서의 폴리머 치밀성(compactness)과 밀접하게 연결되어 있음을 나타낸다. 이러한 결과는, 캡슐화 수율과 폴리머의 전체 양 사이의 절충을 행함으로써 공정을 최적화할 수 있게 해준다.
이후에, 수계-코어 나노캡슐의 방출 양상을 생리 조건에서 조사하였고, 결과는 도 8에 나타낸다. 도 8에서는 쉘 투과성 및 DOX 방출 메카니즘에 대한 정보 뿐만 아닐라 수계-콩 나노캡슐의 구조 특성에 대한 정보도 제공할 것이다. 결국, DOX가 캡슐에 효과적으로 캡슐화되며, 시간에 따라 모두 방출될 수 있다는 것을 입증한다(곡선 피트에 의해 최대 ~100%). 우선, 방출 프로파일이 지수 함수(R= 0.992)에 잘 들어맞는, 지수 양상(exponential behavior)을 보인다는 것에 주목한다.
2.4. 임의의 캡슐화된 활성 성분이 없는 입자(P)의 세포독성
상기 1.2에 따라 제조한, 임의의 캡슐화된 활성 성분이 없는 입자(P)(이하 NCB라 함)의 세포 독성을 NIH/3T3 세포(마우스의 Mus musculus의 섬유모세포)에서 평가하였다. 입자(P)를 다양한 농도의 입자에 4, 24, 48 또는 72 시간 노출시켰다. 세포 생존율은 MTT 테스트로 결정하였다. 결과는 하기 표와 도 9에 나타낸다. 현저한 독성은 최대 1/1000 희석에서도 나타나지 않았다.
| 평균 | 대조군 | DMSO | NCB 1/10 | NCB 1/100 | NCB 1/1000 | NCB 1/10000 |
| 4H | 100,00 | 46,75 | 24,98 | 90,40 | 86,12 | 92,79 |
| 24H | 100,00 | 10,22 | 9,20 | 40,06 | 84,58 | 102,73 |
| 48H | 100,00 | 4,79 | 5,91 | 35,16 | 72,94 | 83,45 |
| 72H | 100,00 | 5,00 | 6,00 | 51,00 | 98,00 | 111,00 |
| 편차 | 대조군 | DMSO | 1/10 NCB | NCB 1/100 | NCB 1/1000 | NCB 1/10000 |
| 4H | 11,91 | 9,03 | 5,17 | 1,18 | 10,13 | 6,84 |
| 24H | 4,03 | 2,60 | 3,83 | 5,22 | 17,10 | 23,07 |
| 48H | 22,70 | 1,35 | 2,60 | 13,79 | 11,25 | 12,55 |
| 72H | 2,05 | 0,64 | 0,21 | 11,91 | 2,64 | 1,79 |
2.5. 양친성 물질로서 TweenTM 80으로 구성된 쉘을 포함하는 나노캡슐(NC) 함유성 입자(P) 조성물의 제조
조성물을 전술한(1.2.1 및 1.2.3 참조) 일반적인 방법에 따라 하기 성분으로 제조하였다.
| 마이크로에멀젼 제조 | 양 |
| NaCl | 0.08 g |
| MilliQ 물 | 2.6 g |
| 파라핀 오일 | 4 g |
| POE 300 스테아레이트 | 0.74 g |
| 트윈TM 80 | 0.124 g |
| 나노에멀젼(E1) 제조 | |
| POE 300 스테아레이트 | 0.4 g |
| 이소펜탄 | 30 mL |
| 증발 | |
| MilliQ 물 | 20 mL |
교반(500 rpm) 하에, 35 내지 60℃에서 3회 온도 사이클을 수행하였다. 3번째 사이클의 냉각 단계 동안에, 이소펜탄과 POE 스테아레이트를 첨가하여 안정적인 (w/o) 나노에멀젼을 제조함으로써, 시스템을 50℃에서 희석하였다.
그런 후, 50℃에서 milliQ 물에 수득한 나노에멀젼을 첨가한 다음 약 1시간 이소펜탄을 증발시켜, 나노캡슐을 만들었다.
수득되는 조성물의 경시적인 안정성을, 입자(P)의 크기 및 제타 전위의 전개를 모니터링함으로써(입자 측정기(nanosizer) ZS, 1.2.4 부분 참조) 평가하였다.
그 결과, 시간(1개월) 대비 입자 및 제타 전위의 수치가 일정한, 우수한 입자 안정성이 확인되었다.
2.6. 단량체의 존재 또는 부재시의 친수성 항암제(독소루비신)의 캡슐화 수율 비교(수계 액적에 의한 캡슐화)
상기에 기술된 일반적인 방법(1.2.1 및 1.2.3 참조)에 따라, 하기 성분들로 조성물을 제조하였다.
| 마이크로에멀젼 제조 | 양 |
| NaCl | 0.08 g |
| MilliQ 물 | 2.6 g |
| 파라핀 오일 | 4 g |
| POE 300 스테아레이트 | 0.74 g |
| 나노에멀젼 제조(E1) | |
| POE 300 스테아레이트 | 0.4 g |
| 이소펜탄 | 30 mL |
| 증발 | |
| MilliQ 물 | 20 mL |
교반(500 rpm) 하에, 35 내지 60℃에서 3회 온도 사이클을 수행하여, 마이크로에멀젼을 만들었다. 그 후, 마이크로에멀젼을 39℃에서 안정화하였다.
독소루비신 수용액(4.18 mg/ml) 50 ㎕를 마이크로에멀젼에 연속 첨가하고, 이소펜탄으로 희석한 후 독소루비신이 주입된 w/o 나노에멀젼을 만들었다.
이 나노에멀젼의 일부를 톨릴렌 2,4-디이소시아네이트(상기 1.2.2 참조)와 계면 중합하였고, 나머지는 중합하지 않았다.
그 후, 수득한 나노에멀젼을 50℃에서 milliQ 물에 첨가하여 나노캡슐을 제조한 다음, 약 1시간 동안 이소펜탄 증발을 수행하였다.
이들 2가지 나노에멀젼의 수계 나노캡슐 또는 수계 액적의 크기는 130 nm (입자측정기 ZS로 측정함)이었다.
폴리머 나노캡슐내에 캡슐화된 독소루비신의 수율은 70%이었고, 수계 액적은 30%였다.
이러한 결과는, 폴리머 나노캡슐로 수득되는 캡슐화 수율에 비해 낮지만, 수계 액적이 독소루비신을 캡슐화할 수 있음을 입증하는 것이다.
참고문헌
Hillaireau, H.; Le Doan, T.; Besnard, M.; Chacun, H.; Janin, J.; Couvreur, P., Int. J. Pharm. 2006, 324, 37-42.
Ruysschaert, T.; Paquereau, L.; Winterhalter, M.; Fournier, D., Nano Lett. 2006, 6,2755-2757.
Gomes, J. F. P. d. S.; Sonnen, A. F.-P.; Kronenberger, A.; Fritz, J.; Coelho, M. A. N.; Fournier, D.; Fournier-Noel, C.; Mauzac, M.; Winterhalter, M. Langmuir, 2006, 22, 7755-7759.
Yu, C. D., Handbook of Pharmaceutical Excipients, second edition; The Pharmaceutical Press: London, 1994.
Salager, J. L.; Forgiarini, A.; Marquez, L.; Pena, A.; Pizzino, A.; Rodriguez, M.; Rondon-Gonzalez, M., Adv. Colloid Interface Sci. 2004, 108-109, 259-272.
Anton, N.; Saulnier, P.; Beduneau, A.; Benoit, J. P., J. Phys. Chem. B 2007, 111, 3651-3657.
Shinoda, K.; Saito, H. J. Colloid Interface Sci. 1968, 26, 70-74.
Shinoda, K.; Saito, H. J. Colloid Interface Sci. 1969, 30, 258-263.
Kahlweit, M.; Strey, R.; Firman, P.; Haase, D. Langmuir 1985, 1, 281-288.
Forster, T.; von Rybinski, W.; Wadle, A. Adv. Colloid Interface Sci. 1995, 58, 119-149.
Morales, D.; Gutierrez, J. M.; Garcia-Celma, M. J.; Solans, C. Langmuir 2003, 19, 7196-7200.
Izquierdo, P.; Esquena, J.; Tadros, T. F.; Dederen, J. C.; Feng, J.; Garcia-Celma, M. J.; Azemar, N.; Solans, C. Langmuir 2004, 20, 6594-6598.
Ohshima, H., Electrophoresis of soft particles: Analytic approximations, Electrophoresis 27 (2006) 526-533.
Claims (29)
- 직경이 20 내지 500 nm 범위인 입자(P)를 수계 상에 포함하는 조성물로서,
상기 입자는
- 오일 상;
- 상기 오일 상 중에
- 수계 액적(droplet) 또는
- 하기 성분을 포함하는 나노캡슐(NC)
- 수계 코어, 및
- 폴리머 쉘 또는 양친성 물질로 구성된 쉘;
및
-계면활성제를 포함하는, 조성물. - 제1항에 있어서, 상기 나노캡슐(NC)이 양친성 물질로 구성된 쉘을 포함하는 것을 특징으로 하는 조성물.
- 제2항에 있어서, 상기 양친성 물질이 계면활성제(S4)인 것을 특징으로 하는 조성물.
- 제3항에 있어서, 상기 계면활성제(S4)가 비이온성 계면활성제인 것을 특징으로 하는 조성물.
- 제4항에 있어서, 상기 계면활성제(S4)의 친수성 친지성 밸런스(HLB: Hydrophilic Lipophilic Balance)가 10 이상인 것을 특징으로 하는 조성물.
- 제5항에 있어서, 상기 계면활성제(S4)가 폴리소르베이트인 것을 특징으로 하는 조성물.
- 제1항에 있어서, 상기 나노캡슐(NC)이 폴리머 쉘을 포함하는 것을 특징으로 하는 조성물.
- 제7항에 있어서, 상기 폴리머 쉘이 폴리유레아로 구성된 것을 특징으로 하는 조성물.
- 제1항 내지 제8항 중 어느 한항에 있어서, 상기 나노캡슐 또는 수계 액적의 직경이 10 내지 400 nm 범위인 것을 특징으로 하는 조성물.
- 제1항 내지 제9항 중 어느 한항에 있어서, 상기 수계 코어 또는 수계 액적이 친수성 물질을 포함하는 것을 특징으로 하는 조성물.
- 제1항 내지 제10항 중 어느 한항에 있어서, 상기 오일 상이 친지성 물질을 포함하는 것을 특징으로 하는 조성물.
- 제1항 내지 제11항 중 어느 한항에 따른 조성물의 제조 방법으로서,
상기 방법은
i) 액적의 평균 유체 역학 직경(hydrodynamic diameter)이 10 내지 400 nm이고, 연속상에 2종의 오일, 휘발성 오일(O1) 및 비휘발성 오일(O2)을 포함하며, 휘발성 오일(O1)은 물 보다 휘발성이 높으며, 비휘발성 오일(O2)은 물 보다 휘발성이 낮은, 유중수(w/o) 에멀젼(E1)을 제조하는 단계;
ii) 선택적으로, 상기 에멀젼(E1)의 연속 상에 용해되며 물과 접촉하였을 때 중합되는 단량체를 첨가하거나, 또는 양친성 물질을 첨가하여, 수계 코어-쉘 나노캡슐(NC)을 제조하는 단계; 및
iii) 수 상을 첨가하고, 휘발성 오일(O1)을 제거함으로써, 제1항 내지 제11항 중 어느 한항에 따른 조성물을 제조하는 단계를 포함하는 것을 특징으로 하는 제조 방법. - 제12항에 있어서, 상기 에멀젼(E1)이 상 반전 온도(PIT: phase inversion temperature) 보다 높은 온도에서는 물 보다 비휘발성 오일(O2)에 더 잘 용해되고, PIT 보다 낮은 온도에서는 비휘발성 오일(O2) 보다 물에 더 잘 용해되는 계면활성제(S1)를 포함하며,
상기 유중수(w/o) 에멀젼(E1)이,
i1) 대략 PIT에서 온도 사이클링을 수행함으로써, 비휘발성 오일(O2), 물 및 계면활성제(S1)를 포함하는 혼합물로부터 나노구조의 이중 연속 시스템(bicontinuous system)을 제조하는 단계;
i2) 휘발성 오일(O1)을 첨가하여, 액적이 10 내지 400 nm 범위의 유체 역학 평균 직경을 가진, w/o 에멀젼(E1)을 제조하는 단계; 및
i3) 선택적으로, 추가량의 계면활성제(S2)를 첨가하는 단계를 포함하는 방법에 따라 제조되는 것을 특징으로 하는 제조 방법. - 제13항에 있어서, 친수성 물질을 포함하는 수용액을 단계 i2) 전에 첨가하여 나노구조의 이중 연속 시스템을 제조하는 것을 특징으로 하는 제조 방법.
- 제13항 또는 제14항에 있어서, 상기 계면활성제(S1)가 폴리옥시에틸렌 모이어티를 포함하는 것을 특징으로 하는 제조 방법.
- 제15항에 있어서, 상기 계면활성제(S1)가 폴리옥시에틸렌 C6-C18 지방산 에스테르인 것을 특징으로 하는 제조 방법.
- 제16항에 있어서, 상기 계면활성제(S1)가 POE-300 스테아레이트인 것을 특징으로 하는 제조 방법.
- 제12항 내지 제17항 중 어느 한항에 있어서, 상기 비휘발성 오일(O2)이 라이트 미네랄 오일(light mineral oil)인 것을 특징으로 하는 제조 방법.
- 제12항 내지 제18항 중 어느 한항에 있어서, 상기 휘발성 오일(O1)이 펜탄 또는 이소펜탄인 것을 특징으로 하는 제조 방법.
- 제13항 내지 제19항 중 어느 한항에 있어서, 상기 추가량의 계면활성제(S2)가 계면활성제의 총량의 30 중량% 내지 40 중량%인 것을 특징으로 하는 제조 방법.
- 제12항 내지 제20항 중 어느 한항에 있어서, 상기 단량체가 2개의 디이소시아네이트 기를 포함하는 것을 특징으로 하는 제조 방법.
- 제21항에 있어서, 상기 단량체가 톨릴렌-2,4-디이소시아네이트, 이소포론 디이소시아네이트 또는 4,4-메틸-비스(페닐-이소시아네이트) 중에서 선택되는 것을 특징으로 하는 제조 방법.
- 제12항 내지 제22항 중 어느 한항에 있어서, 친지성 물질을 중합 단계 ii) 후에, 단계 iii) 전에 첨가하는 것을 특징으로 하는 제조 방법.
- 제12항 내지 제23항 중 어느 한항에 있어서, 상기 친수성 및 친지성 물질이 약제, 진단제, 화장료, 수의학 제품, 식물 위생 제품 또는 가공 식품 중에서 선택되는 것을 특징으로 하는 제조 방법.
- 제12항 내지 제24항 중 어느 한항에 있어서, 단계 iii) 이후에 수 상에 친수성 계면활성제(S3)를 첨가하는 단계 iv)를 더 포함하는 것을 특징으로 하는 제조 방법.
- 유중수(w/o) 에멀젼으로서,
i1) 대략 PIT에서 온도 사이클링을 수행함으로써, 비휘발성 오일(O2), 물 및 계면활성제(S1)를 포함하는 혼합물로부터 나노구조의 이중 연속 시스템(bicontinuous system)을 제조하는 단계;
i2) 휘발성 오일(O1)을 첨가하여, 액적이 10 내지 400 nm 범위의 유체 역학 평균 직경을 가진, w/o 에멀젼(E1)을 제조하는 단계; 및
i3) 선택적으로, 추가량의 계면활성제(S2)를 첨가하는 단계를 포함하는 방법에 따라 제조되며,
상기 비휘발성 오일(O2)이 파라핀 오일이고, 상기 휘발성 오일(O1)이 펜탄 또는 이소펜탄인 것을 특징으로 하는 유중수(w/o) 에멀젼. - - 불연속 상으로서, 휘발성 오일인 이소펜탄 또는 펜탄과 비휘발성 오일인 파라핀 오일;
- 불연속 상으로서, 물; 및
- 계면활성제(S1)를 포함하는, 유중수(w/o) 에멀젼. - 제26항 또는 제27항에 있어서, 상기 계면활성제가 폴리옥시에틸렌 모이어티를 포함하는 것을 특징으로 하는 유중수(w/o) 에멀젼.
- 친수성 및/또는 친지성 물질의 캡슐화를 위한, 제1항 내지 제11항 중 어느 한항에 따른 조성물의 용도.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07291109A EP2039352A1 (en) | 2007-09-18 | 2007-09-18 | Aqueous-core lipid nanocapsules for encapsulating hydrophilic and/or lipophilic molecules |
| EP07291109.2 | 2007-09-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20100074196A true KR20100074196A (ko) | 2010-07-01 |
Family
ID=38785137
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107008347A KR20100074196A (ko) | 2007-09-18 | 2008-09-18 | 친수성 및/또는 친지성 분자를 캡슐화하기 위한 수계-코어 지질 나노캡슐 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9522121B2 (ko) |
| EP (2) | EP2039352A1 (ko) |
| JP (2) | JP5989964B2 (ko) |
| KR (1) | KR20100074196A (ko) |
| CN (2) | CN101842088B (ko) |
| CA (1) | CA2699802A1 (ko) |
| WO (1) | WO2009037310A2 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9175152B2 (en) | 2012-06-25 | 2015-11-03 | Lg Chem, Ltd. | Emulsion composition for manufacturing polyalkylene carbonate product and resin product using the same |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9393315B2 (en) | 2011-06-08 | 2016-07-19 | Nitto Denko Corporation | Compounds for targeting drug delivery and enhancing siRNA activity |
| FR2950253B1 (fr) * | 2009-09-24 | 2011-09-23 | Ethypharm Sa | Nanocapsules lipidiques, procede de preparation et utilisation comme medicament |
| JP4834775B2 (ja) | 2010-03-04 | 2011-12-14 | 株式会社 資生堂 | 日焼け止め用組成物 |
| US10196637B2 (en) | 2011-06-08 | 2019-02-05 | Nitto Denko Corporation | Retinoid-lipid drug carrier |
| CN102441355B (zh) * | 2011-08-29 | 2013-10-30 | 华南理工大学 | 一种嵌段离聚体水相自组装纳米胶囊及其制备方法 |
| US20130251855A1 (en) * | 2012-03-21 | 2013-09-26 | Pepsico, Inc. | Aqueous product comprising oil-containing microcapsules and method for the manufacture thereof |
| JP6412676B2 (ja) * | 2013-03-12 | 2018-10-24 | セファロン、インク. | ナノ粒子及びナノ粒子製剤 |
| JP6377913B2 (ja) * | 2013-04-16 | 2018-08-22 | 積水化学工業株式会社 | マイクロカプセルの製造方法及びマイクロカプセル |
| TWI482782B (zh) | 2013-05-31 | 2015-05-01 | Univ Nat Chiao Tung | 架接抗體之雙乳化核殼奈米結構 |
| CN103271406B (zh) * | 2013-06-08 | 2014-07-16 | 吉林大学 | 一种复合型两亲性芯材微胶囊冲剂及其制备方法 |
| FR3008900B1 (fr) * | 2013-07-25 | 2018-03-30 | Centre Nat Rech Scient | Nanoparticules lipidiques multicompartimentees |
| GB2520371B (en) * | 2014-05-01 | 2016-09-14 | Frito Lay Trading Co Gmbh | Snack food seasoning |
| GB2520370B (en) | 2014-05-01 | 2016-09-14 | Frito Lay Trading Co Gmbh | Snack food seasoning |
| CA2946807A1 (en) * | 2014-05-30 | 2015-12-03 | AbbVie Deutschland GmbH & Co. KG | Highly drug-loaded poly(alkyl 2-cyanoacrylate) nanocapsules |
| JP6572598B2 (ja) * | 2015-04-02 | 2019-09-11 | 日本製鉄株式会社 | ナノ粒子の粒径測定方法 |
| US10053616B2 (en) * | 2015-04-09 | 2018-08-21 | Saudi Arabian Oil Company | Encapsulated nanocompositions for increasing hydrocarbon recovery |
| KR102692648B1 (ko) * | 2015-12-04 | 2024-08-06 | (주)아모레퍼시픽 | 변성 단백질 수상 분산입자를 포함하는 화장료 조성물 및 이의 제조방법 |
| CN106942771A (zh) * | 2017-04-06 | 2017-07-14 | 贝因美婴童食品股份有限公司 | 一种用于制备营养品的胶囊 |
| CN112368562A (zh) * | 2018-07-11 | 2021-02-12 | 香港大学 | 用于液滴的连续和定量收集的自动微流控系统 |
| FR3092833B1 (fr) | 2019-02-18 | 2021-07-16 | Commissariat Energie Atomique | Procede de fabrication de nanoparticules hybrides metal/polymere a faible distribution de tailles par polymerisation en mini-emulsion |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9414318D0 (en) * | 1994-07-15 | 1994-09-07 | Dowelanco Ltd | Preparation of aqueous emulsions |
| FR2725369B1 (fr) * | 1994-10-07 | 1997-01-03 | Oreal | Composition cosmetique ou dermatologique constituee d'une emulsion huile dans eau a base de globules huileux pourvus d'un enrobage cristal liquide lamellaire |
| DE19630176C2 (de) * | 1996-07-26 | 2000-11-02 | Babor Gmbh & Co Dr | Kosmetische und pharmazeutische Mittel, gebildet durch eine nach dem Phaseninversionsverfahren erzeugte W/O/W-Emulsion |
| CA2338031C (en) * | 1998-07-17 | 2006-12-05 | Sankaram Bhima Mantripragada | Biodegradable compositions for the controlled release of encapsulated substances |
| FR2805761B1 (fr) * | 2000-03-02 | 2002-08-30 | Mainelab | Nanocapsules lipidiques, procede de preparation et utilisation comme medicament |
| GB0009735D0 (en) * | 2000-04-19 | 2000-06-07 | Zeneca Ltd | Formulation |
| US20020155084A1 (en) * | 2000-06-02 | 2002-10-24 | The Regents Of The University Of The Michigan | Nanoemulsion formulations |
| AU2003220670A1 (en) | 2002-04-05 | 2003-10-27 | University Of Florida | Oil-filled nanocapsules from microemulsions utilizing cross-linkable surfactants |
| AU2003288902A1 (en) * | 2002-09-06 | 2004-04-08 | Genteric, Inc. | Microcapsules and methods of use |
| WO2004112695A2 (en) * | 2003-05-20 | 2004-12-29 | Erimos Pharmaceutical Llc | Methods and compositions for delivery of catecholic butanes for treatment of obesity |
| CN1460468A (zh) * | 2003-06-05 | 2003-12-10 | 浙江大学 | 改进的包埋蛋白类药物和疫苗的高分子微球的制备方法 |
| WO2005003543A1 (en) * | 2003-07-02 | 2005-01-13 | Tiax Llc | Free piston stirling engine control |
| CN100402109C (zh) * | 2003-08-01 | 2008-07-16 | 卡拉科科学公司 | 经颅电刺激设备和方法 |
| JP4747534B2 (ja) * | 2003-09-01 | 2011-08-17 | 大正製薬株式会社 | W/o/w型複合エマルション |
| DE10351644A1 (de) * | 2003-11-05 | 2005-06-09 | Bayer Technology Services Gmbh | Verfahren zur Herstellung von lagerstabilen multiplen Emulsionen |
| US20070154560A1 (en) * | 2003-12-24 | 2007-07-05 | Mg Pharmacy Inc. | Process for producing microsphere and apparatus for producing the same |
| JP2005263647A (ja) * | 2004-03-16 | 2005-09-29 | Konica Minolta Medical & Graphic Inc | エマルション粒子含有造影剤 |
| US20110135734A1 (en) * | 2004-04-20 | 2011-06-09 | Yissum Research Development Company Of The Hebrew University Of Jerusalem | Method For the Preparation of Nanoparticles From Nanoemulsions |
| US8211415B2 (en) * | 2004-10-13 | 2012-07-03 | L'oreal | Easily removable waterproof cosmetic care and/or makeup composition comprising at least one latex or pseudolatex |
| US8029709B2 (en) * | 2004-10-29 | 2011-10-04 | The University Of Cincinnati | Liquid core capsules and methods of synthesis thereof through interfacial polymerization |
| AU2006316507B2 (en) * | 2005-11-22 | 2012-11-01 | Nestec S.A. | Oil-in-water emulsion and its use for the delivery of functionality |
| EP2026771B1 (en) * | 2006-01-23 | 2009-10-21 | Yissum Research Development Company Of The Hebrew University Of Jerusalem | Microspheres comprising nanocapsules containing a lipophilic drug |
| CN100999656A (zh) * | 2006-12-22 | 2007-07-18 | 华南理工大学 | 潜热型纳米流体传热工质及其制备方法 |
-
2007
- 2007-09-18 EP EP07291109A patent/EP2039352A1/en not_active Ceased
-
2008
- 2008-09-18 WO PCT/EP2008/062435 patent/WO2009037310A2/en active Application Filing
- 2008-09-18 CN CN200880114087.8A patent/CN101842088B/zh not_active Expired - Fee Related
- 2008-09-18 US US12/678,868 patent/US9522121B2/en not_active Expired - Fee Related
- 2008-09-18 CA CA2699802A patent/CA2699802A1/en not_active Abandoned
- 2008-09-18 CN CN201410049011.9A patent/CN103800304A/zh active Pending
- 2008-09-18 KR KR1020107008347A patent/KR20100074196A/ko not_active Application Discontinuation
- 2008-09-18 JP JP2010525348A patent/JP5989964B2/ja not_active Expired - Fee Related
- 2008-09-18 EP EP08804375A patent/EP2187877A2/en not_active Withdrawn
-
2014
- 2014-07-11 JP JP2014143421A patent/JP2014221802A/ja active Pending
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9175152B2 (en) | 2012-06-25 | 2015-11-03 | Lg Chem, Ltd. | Emulsion composition for manufacturing polyalkylene carbonate product and resin product using the same |
| US9382419B2 (en) | 2012-06-25 | 2016-07-05 | Lg Chem, Ltd. | Polyalkylene carbonate molded product manufactured by using an emulsion composition |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009037310A2 (en) | 2009-03-26 |
| US20100297247A1 (en) | 2010-11-25 |
| CA2699802A1 (en) | 2009-03-26 |
| WO2009037310A3 (en) | 2010-02-18 |
| CN101842088B (zh) | 2014-03-12 |
| CN101842088A (zh) | 2010-09-22 |
| JP5989964B2 (ja) | 2016-09-07 |
| JP2010539221A (ja) | 2010-12-16 |
| CN103800304A (zh) | 2014-05-21 |
| US9522121B2 (en) | 2016-12-20 |
| JP2014221802A (ja) | 2014-11-27 |
| EP2039352A1 (en) | 2009-03-25 |
| EP2187877A2 (en) | 2010-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20100074196A (ko) | 친수성 및/또는 친지성 분자를 캡슐화하기 위한 수계-코어 지질 나노캡슐 | |
| Ching et al. | Alginate gel particles–A review of production techniques and physical properties | |
| Astete et al. | Synthesis and characterization of PLGA nanoparticles | |
| Rodríguez et al. | Current encapsulation strategies for bioactive oils: From alimentary to pharmaceutical perspectives | |
| Morikawa et al. | The use of an efficient microfluidic mixing system for generating stabilized polymeric nanoparticles for controlled drug release | |
| Tsai et al. | Liposomal microencapsulation using the conventional methods and novel supercritical fluid processes | |
| Elzayat et al. | Nanoemulsions for synthesis of biomedical nanocarriers | |
| Quintanilla-Carvajal et al. | Nanoencapsulation: a new trend in food engineering processing | |
| Liu et al. | Preparation of uniform-sized multiple emulsions and micro/nano particulates for drug delivery by membrane emulsification | |
| Romero et al. | Synthesis of organic nanoparticles | |
| Panigrahi et al. | Nanoencapsulation strategies for lipid-soluble vitamins | |
| JP5741442B2 (ja) | リポソームの製造方法 | |
| Imbrogno et al. | Polycaprolactone multicore-matrix particle for the simultaneous encapsulation of hydrophilic and hydrophobic compounds produced by membrane emulsification and solvent diffusion processes | |
| PL229276B1 (pl) | Nanokapsuła do przenoszenia związku lipofilowego i sposób jej wytwarzania | |
| Leena et al. | Nanoencapsulation of nutraceutical ingredients | |
| Adamczak et al. | Preparation of the squalene-based capsules by membrane emulsification method and polyelectrolyte multilayer adsorption | |
| JP5494054B2 (ja) | 二段階乳化によるリポソーム製造方法 | |
| Gonçalves et al. | Development of multicore hybrid particles for drug delivery through the precipitation of CO2 saturated emulsions | |
| Vauthier et al. | Processing and scale-up of polymeric nanoparticles | |
| Zimmermann et al. | Production of nanostructured systems: Main and innovative techniques | |
| Chountoulesi et al. | Studying the properties of polymer-lipid nanostructures: The role of the host lipid | |
| Montasser et al. | The effect of monomers on the formulation of polymeric nanocapsules based on polyureas and polyamides | |
| Kondiah et al. | Nanotechnological paradigms for neurodegenerative disease interventions | |
| Rabanel et al. | Nanostructured nanoparticles for improved drug delivery | |
| Baghbanbashi et al. | Recent advances in drug delivery applications of aqueous two-phase systems |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| N231 | Notification of change of applicant | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| J201 | Request for trial against refusal decision | ||
| AMND | Amendment | ||
| E902 | Notification of reason for refusal | ||
| B601 | Maintenance of original decision after re-examination before a trial | ||
| J301 | Trial decision |
Free format text: TRIAL NUMBER: 2015101006228; TRIAL DECISION FOR APPEAL AGAINST DECISION TO DECLINE REFUSAL REQUESTED 20151022 Effective date: 20171124 |