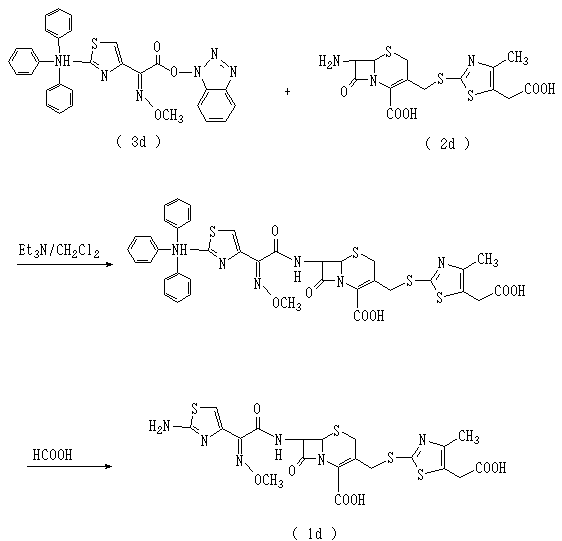KR100229175B1 - 세펨 유도체의 제조방법 - Google Patents
세펨 유도체의 제조방법 Download PDFInfo
- Publication number
- KR100229175B1 KR100229175B1 KR1019970040067A KR19970040067A KR100229175B1 KR 100229175 B1 KR100229175 B1 KR 100229175B1 KR 1019970040067 A KR1019970040067 A KR 1019970040067A KR 19970040067 A KR19970040067 A KR 19970040067A KR 100229175 B1 KR100229175 B1 KR 100229175B1
- Authority
- KR
- South Korea
- Prior art keywords
- reaction
- formula
- maem
- represented
- yield
- Prior art date
Links
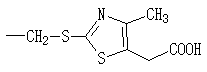
- ZMFOTRMQXVYXKU-UHFFFAOYSA-N CCSc1nc(C)c(CC(O)=O)[s]1 Chemical compound CCSc1nc(C)c(CC(O)=O)[s]1 ZMFOTRMQXVYXKU-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D501/00—Heterocyclic compounds containing 5-thia-1-azabicyclo [4.2.0] octane ring systems, i.e. compounds containing a ring system of the formula:, e.g. cephalosporins; Such ring systems being further condensed, e.g. 2,3-condensed with an oxygen-, nitrogen- or sulfur-containing hetero ring
- C07D501/02—Preparation
- C07D501/04—Preparation from compounds already containing the ring or condensed ring systems, e.g. by dehydrogenation of the ring, by introduction, elimination or modification of substituents
- C07D501/06—Acylation of 7-aminocephalosporanic acid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D501/00—Heterocyclic compounds containing 5-thia-1-azabicyclo [4.2.0] octane ring systems, i.e. compounds containing a ring system of the formula:, e.g. cephalosporins; Such ring systems being further condensed, e.g. 2,3-condensed with an oxygen-, nitrogen- or sulfur-containing hetero ring
- C07D501/14—Compounds having a nitrogen atom directly attached in position 7
- C07D501/16—Compounds having a nitrogen atom directly attached in position 7 with a double bond between positions 2 and 3
- C07D501/20—7-Acylaminocephalosporanic or substituted 7-acylaminocephalosporanic acids in which the acyl radicals are derived from carboxylic acids
- C07D501/24—7-Acylaminocephalosporanic or substituted 7-acylaminocephalosporanic acids in which the acyl radicals are derived from carboxylic acids with hydrocarbon radicals, substituted by hetero atoms or hetero rings, attached in position 3
- C07D501/26—Methylene radicals, substituted by oxygen atoms; Lactones thereof with the 2-carboxyl group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D501/00—Heterocyclic compounds containing 5-thia-1-azabicyclo [4.2.0] octane ring systems, i.e. compounds containing a ring system of the formula:, e.g. cephalosporins; Such ring systems being further condensed, e.g. 2,3-condensed with an oxygen-, nitrogen- or sulfur-containing hetero ring
- C07D501/14—Compounds having a nitrogen atom directly attached in position 7
- C07D501/16—Compounds having a nitrogen atom directly attached in position 7 with a double bond between positions 2 and 3
- C07D501/20—7-Acylaminocephalosporanic or substituted 7-acylaminocephalosporanic acids in which the acyl radicals are derived from carboxylic acids
- C07D501/24—7-Acylaminocephalosporanic or substituted 7-acylaminocephalosporanic acids in which the acyl radicals are derived from carboxylic acids with hydrocarbon radicals, substituted by hetero atoms or hetero rings, attached in position 3
- C07D501/48—Methylene radicals, substituted by hetero rings
- C07D501/56—Methylene radicals, substituted by hetero rings with the 7-amino radical acylated by carboxylic acids containing hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Cephalosporin Compounds (AREA)
Abstract
Description
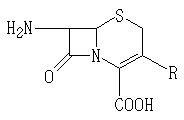
본 발명은 세펨 유도체의 제조방법에 관한 것으로서, 더욱 상세하게는 다음 화학식 2로 표시되는 7-아미노-3-세펨-4-카르복실산 유도체(이하, "7-ACA 중간체"라 함)와 2-머캅토벤조티아졸-2-(2-아미노티아졸-4-일)-2-신-메톡시이미노아세테이트(이하, "MAEM"이라 함)를 특정 반응용매 및 염기조건하에서 반응시킨 다음, 유기산으로 처리하는 1단계반응(one-step reaction)으로 다음 화학식 1로 표시되는 세펨 유도체를 제조하는 방법에 관한 것이다.
화학식 1
화학식 2
상기 화학식 1로 표시되는 세펨 유도체는 공지의 화합물로서 베타 락타마제에 안정하고, 그람 양성 및 그람 음성 박테리아에 대하여 광범위한 항균력을 나타내므로 주사용 항생제로서 널리 이용되고 있다. 일반적으로 주사제로 제조하기 위해서는 상기 화학식 1로 표시되는 세펨 유도체를 유기용매중에서 트리에틸아민으로 용해시킨 후 나트륨 화합물인 소디움 아세테이트 또는 소디움-2-에틸 헥사노에이트를 반응시켜 나트륨염으로 전환한다.
상기 화학식 1로 표시되는 세펨 유도체 또는 이들의 나트륨염의 제조방법에 대해서는 미국특허 제4,152,432호, 미국특허 제4,278,793호, 미국특허 제4,327,210호, 미국특허 제4,427,674호 및 유럽특허 제95-5088호에 공지되어 있다.
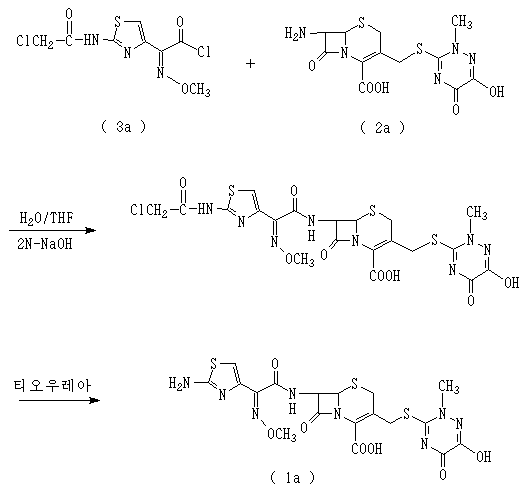
예컨대 미국특허 제4,327,210호에는 다음 화학식 1a로 표시되는 세프트리악손을 제조하는 방법이 개시되어 있는 바, 이를 간략히 나타내면 다음 반응식 1과 같다.
상기 반응식 1에서 사용되고 있는 화학식 3a로 표시되는 화합물의 경우, 클로로아세틸 클로라이드를 아미노 보호기로 도입하는 과정, PCl5를 이용하여 산 클로라이드를 제조하는 과정 등 복잡한 제조과정과 다루기 힘든 시약을 사용하여 제조하고 있으며, 또한 보호기로 도입된 클로로아세틸 클로라이드를 제거하기 위한 별도의 공정이 추가되어야 하는 등 공업적인 생산에 적용하기에는 많은 문제가 있었다.
미국특허 제4,152,432호에는 다음 화학식 1b로 표시되는 세포탁심을 제조하는 방법이 개시되어 있는 바, 이를 간략히 나타내면 다음 반응식 2와 같다.
상기 반응식 2에서도 역시 제조방법이 복잡한 화학식 3a로 표시되는 화합물을 사용하고 있어 상기에서와 같이 공업적인 생산에 적용하기에는 많은 문제가 있었다.
또한, 유럽특허 제95-5088호에도 다음 화학식 1b로 표시되는 세포탁심을 제조하는 방법이 개시되어 있는 바, 이를 간략히 나타내면 다음 반응식 3과 같다.
상기 제조방법에서는 반응용매로서 H2O와 아세톤의 혼합용매를 사용하고, 반응후에는 반응용매중에서 결정화하여 80 ~ 85%의 수율로 세포탁심을 얻고 있다. 그러나, 이러한 제조방법은 아실화 반응시 고농도로 반응을 수행하기 때문에 불순물의 제거가 용이하지 않으며, H2O와 아세톤의 혼합용매의 농도를 묽게할 경우 수율저하의 문제가 있다.
미국특허 제4,427,674호에는 다음 화학식 1c로 표시되는 세프티족심을 제조하는 방법이 개시되어 있는 바, 이를 간략히 나타내면 다음 반응식 4와 같다.
상기 제조방법에서는 화학식 2c로 표시되는 화합물을 실릴 보호기의 도입과정 및 보호기 이탈과정이 필요하고, 또 반응물질로 사용하는 화학식 3c로 표시되는 화합물이 매우 불안정화하여 취급이 어려운 단점이 있어 이를 공업적으로 적용하는데는 많은 문제가 있다.
그리고, 미국특허 제4,278,793호에는 다음 화학식 1d로 표시되는 세포디짐을 제조하는 방법이 개시되어 있는 바, 이를 간략히 나타내면 다음 반응식 5와 같다.
상기 제조방법은 출발물질로 사용되는 화학식 3d로 표시되는 화합물을 제조하기 위해 보호기 도입과정 및 보호기 이탈반응이 필요하고, 반응시간도 6시간 이상의 장시간이 소요되며, 제조공정이 매우 복잡하고 수율도 적어 경제성이 떨어지므로 이를 공업적인 생산에 적용하기에는 많은 문제가 있다.
본 발명에서는 7-아미노-3-세펨-4-카르복실산 유도체(7-ACA 중간체)에의 보호기 도입과정을 생략하고 디클로로메탄(CH2Cl2)에 알콜 또는 알콜과 물의 혼합물이 혼합되어 있는 혼합용액을 반응용매로 사용하고 3차아민염기 존재하에서 2-머캅토벤조티아졸-2-(2-아미노티아졸-4-일)-2-신-메톡시이미노아세테이트(MAEM)와 반응시킨 후에 곧바로 유기산을 투입하는 1단계반응(one-step reaction)에 의해 화학식 1로 표시되는 세펨 유도체를 제조함으로써 본 발명을 완성하였다.
따라서, 본 발명은 종래발명에서의 실릴 보호기 도입과정을 생략하고 특정 반응조건하에서 7-ACA 중간체와 MAEM의 반응용액을 직접 반응시키고, 또한 반응 중간체의 분리과정 없이 주사제로 유용한 세펨 유도체를 1단계반응으로 합성하는 개선된 제조방법을 제공하는데 그 목적이 있다.
본 발명은 디클로로메탄(CH2Cl2)/알콜 또는 디클로로메탄(CH2Cl2)/알콜/물의 혼합용매 및 3차아민염기 존재하에서 다음 화학식 2로 표시되는 7-ACA 중간체와 다음 화학식 3b로 표시되는 MAEM을 직접 반응시킨 다음 유기산으로 처리하여 다음 화학식 1로 표시되는 세펨 유도체를 제조하는 방법을 그 특징으로 한다.
화학식 1
화학식 2
상기 화학식들에서 R은 상기에서 정의한 바와 같다.
이와같은 본 발명을 더욱 상세히 설명하면 다음과 같다.
본 발명은 특정 반응용매 및 3차아민염기를 사용하므로써 7-ACT에의 보호기 도입과정을 생략하면서, 7-ACA 중간체와 MAEM을 반응시킨 후 유기산을 투입하여 1단계반응(one-step reaction)으로 화학식 1로 표시되는 세펨유도체를 제조하는 방법에 관한 것이다.
특히, 본 발명에서는 반응용매로서 디클로로메탄/알콜 또는 디클로로메탄/알콜/물의 혼합용매를 사용하는 바, 디클로로메탄과 같은 단일 비극성유기용매를 사용하게 되면 반응물의 용해도 저하로 반응이 제대로 진행되지 못하는 문제가 있고, 알콜 또는 물과 같은 단일 극성용매를 사용하게 되면 반응물 뿐만 아니라 불순물의 용해도가 높아 목적물의 순도가 저하되는 문제가 있다. 또한, 반응용매로서 물을 함께 사용할 경우, 물의 함량이 지나치게 많으면 목적물의 순도향상을 위하여 과량의 유기용매가 사용되어야 하므로 경제적으로 바람직하지 못하다.
그러나, 본 발명에서는 비극성 유기용매로서 디클로로메탄을 사용하고 극성용매로서 알콜 또는 알콜과 물의 혼합물을 적당량 함께 사용하므로써 제조 공정시간을 단축시키고 반응물의 용해도를 증가시키며 불순물은 유기용매를 사용한 추출에 의해 용이하게 제거될 수 있어서 목적물의 순도를 높이게 된다.
이러한 혼합용매의 배합비율에 있어서, 디클로로메탄에 대하여 극성용매(알콜 또는 알콜과 물의 혼합물)는 100 : 8 ~ 12(v/v)로 사용하는 데, 극성용매의 사용량이 적으면 반응물의 용해도가 떨어져 반응시간이 오래 소요되는 문제가 있고, 과량 사용하게 되면 부반응으로 인하여 목적물의 순도 및 수율이 저하되는 문제가 있다. 또한, 알콜과 물의 배합비에 있어서, 알콜에 대하여 물은 100 : 70(v/v) 미만으로 사용하는 것이 바람직하며, 알콜에 대한 물의 사용량이 이보다 과량이면 반응물의 용해도는 증가하나 부반응이 생길 수 있다.
본 발명에 따른 세펨 유도체의 제조과정을 간략히 나타내면 다음 반응식 6과 같다.
상기 반응식에서 R은 상기에서 정의 한바와 같다.
먼저 화학식 2로 표시되는 7-ACA 중간체와 화학식 3b로 표시되는 MAEM을 반응시키며, MAEM은 화학식 2로 표시되는 7-ACA 중간체 1 몰에 대하여 대략 1 몰비로 사용한다.
이때의 반응용매는 상기에서 설명한 바와 같은 디클로로메탄/알콜 또는 디클로로메탄/알콜/물의 혼합용매를 사용한다. 알콜으로는 탄소원자수 1 ~ 5의 알콜 예를들면 메탄올, 에탄올, n-프로판올, 이소프로판올, 부탄올, 펜탄올 등을 사용한다. 반응온도는 -50 ~ 100℃, 바람직하기로는 -10 ~ 10℃를 유지하는 것이다.
또한, 상기 반응은 3차아민염기 존재하에서 수행되는데 3차아민은 3차알킬아민 화합물으로서, 예를들면 트리메틸아민, 트리에틸아민을 사용할 수 있다.
상기 화학식 2로 표시되는 7-ACA 중간체와 화학식 3b로 표시되는 MAEM의 반응이 완료되면, 여기에 유기산을 투입하여 본 발명에서 목적으로 하는 세펨 유도체를 제조한다. 이때, 유기산으로는 p-톨루엔술폰산(p-TsOH), 벤젠술폰산, 메탄술폰산 등을 사용한다. 반응온도는 -50 ~ 100℃, 바람직하기로는 10 ~ 25℃를 유지하는 것이다.
상기에서 설명한 바와 같이 본 발명의 제조방법은 특정 반응조건 설정으로 인하여 반응물질로 사용되는 화학식 2로 표시되는 7-ACA 중간체에의 보호기 도입과정을 생략할 수 있고, 짧은 반응시간내에 높은 제조수율로 목적으로 하는 화학식 1로 표시되는 세펨 유도체를 제조할 수 있다.
이와 같은 본 발명을 실시예에 의거하여 더욱 상세히 설명하겠는 바, 본 발명이 실시예에 한정되는 것은 아니다.
실시예 1
7-아미노-3-[(2,5-디히드로-6-히드록시-2-메틸-5-옥소-1,2,4-트리아진-3-일)티오메틸-3-세펨-4-카르복실산(화학식 2a; 185.2g)와 2-머캅토벤조티아졸-2-(2-아미노티아졸-4-일)-2-신-메톡시이미노아세테이트(MAEM; 174.8g)를 디클로로메탄(1750 ㎖)에 현탁시켰다. 여기에 H2O(148.2 ㎖)와 메탄올(205 ㎖)을 가하고, 0℃로 냉각한 다음 트리에틸아민(138.6 ㎖)를 서서히 적가하였다. 10℃에서 4시간동안 반응시킨 후, 반응이 완료되면 p-TsOH·H2O(204.5 g)을 적가하여 결정이 석출되면 1시간동안 교반하였다. 석출된 결정을 여과하고 아세톤(850 ㎖)으로 세척한 후 40℃에서 3시간동안 진공감압건조하여 세프트리악손(258.6g, 수율 93.5%)을 얻었다.
IR 스펙트럼(KBr) : 1780(β-락탐카보닐) ㎝-1
1H-NMR(D2O/NaHCO3, ppm): δ3.62(s, 3H, N-CH3), 3.95(s, 3H, -OCH3), 4.21(d, 2H, -SCH2-), 5.17(d, 1H, C6-H), 5.72(d, 1H, C7-H), 6.95(s, 1H, 티아졸-H)
실시예 2
상기 실시예 1과 동일한 방법으로 제조하되, 다만 화학식 2a와 MAEM의 반응에서 메탄올(205 ㎖) 대신에 에탄올(205 ㎖)을 사용하여 세프트리악손(261.4g, 수율 94.5%)을 얻었다.
실시예 3
상기 실시예 1과 동일한 방법으로 제조하되, 다만 화학식 2a와 MAEM의 반응에서 메탄올(205 ㎖) 대신에 이소프로판올(205 ㎖)을 사용하여 세프트리악손(266.1g, 수율 96.2%)을 얻었다.
실시예 4
상기 실시예 1과 동일한 방법으로 제조하되, 다만 화학식 2a와 MAEM의 반응에서 메탄올(205 ㎖) 대신에 n-프로판올(205 ㎖)을 사용하여 세프트리악손(265g, 수율 95.8%)을 얻었다.
실시예 5
상기 실시예 1과 동일한 방법으로 제조하되, 다만 p-TsOH·H2O(204.5g) 대신에 벤젠술폰산(175g)을 적가하여 세프트리악손(257.5g, 수율 93.1%)을 얻었다.
실시예 6
7-아미노-3-아세톡시메틸-3-세펨-4-카르복실산 유도체(화학식 2b; 213.8g)와 2-머캅토벤조티아졸-2-(2-아미노티아졸-4-일)-2-신-메톡시이미노아세테이트(MAEM; 275.2g)를 디클로로메탄(2500 ㎖)에 현탁시켰다. 여기에 H2O(149.7 ㎖)와 메탄올(427.6 ㎖)을 가하고, 0℃로 냉각한 다음 트리에틸아민(167.5 ㎖)를 서서히 적가하였다. 10℃에서 4시간동안 반응시킨 후, 반응이 완료되면 p-TsOH·H2O(175 g)을 적가하여 결정이 석출되면 1시간동안 교반하였다. 석출된 결정을 여과하고 아세톤(950 ㎖)으로 세척한 후 40℃에서 3시간동안 진공감압건조하여 세포탁심(339.7g, 수율 95%)을 얻었다.
IR 스펙트럼(KBr) : 1780(β-락탐카보닐) ㎝-1
1H-NMR(D2O/NaHCO3, ppm): δ3.53(d, 2H, C2-H), 4.02(s, 3H, -OCH3), 4.84(d, 2H, -SCH2-), 5.2(d, 1H, C6-H), 5.83(d, 1H, C7-H), 6.97(s, 1H, 티아졸-H)
실시예 7
상기 실시예 6과 동일한 방법으로 제조하되, 다만 화학식 2b와 MAEM의 반응에서 메탄올(427.6 ㎖) 대신에 에탄올(427.6 ㎖)을 사용하여 세포탁심(340.4g, 수율 95.2%)을 얻었다.
실시예 8
상기 실시예 6과 동일한 방법으로 제조하되, 다만 화학식 2b와 MAEM의 반응에서 메탄올(427.6 ㎖) 대신에 이소프로판올(427.6 ㎖)을 사용하여 세포탁심(346.9g, 수율 97%)을 얻었다.
실시예 9
상기 실시예 6과 동일한 방법으로 제조하되, 다만 화학식 2b와 MAEM의 반응에서 메탄올(427.6 ㎖) 대신에 n-프로판올(427.6 ㎖)을 사용하여 세포탁심(345.1g, 수율 96.5%)을 얻었다.
실시예 10
상기 실시예 6과 동일한 방법으로 제조하되, 다만 p-TsOH·H2O(175g) 대신에 벤젠술폰산(135g)을 적가하여 세포탁심(330g, 수율 92.3%)을 얻었다.
실시예 11
7-아미노-3-세펨-4-카르복실산(화학식 2c; 175.6g)와 2-머캅토벤조티아졸-2-(2-아미노티아졸-4-일)-2-신-메톡시이미노아세테이트(MAEM; 307.2g)를 디클로로메탄(1830 ㎖)에 현탁시켰다. 여기에 H2O(114.2 ㎖)와 메탄올(351.2 ㎖)을 가하고, 0℃로 냉각한 다음 트리에틸아민(134.5 ㎖)를 서서히 적가하였다. 10℃에서 4시간동안 반응시킨 후, 반응이 완료되면 p-TsOH·H2O(168.5 g)을 적가하여 결정이 석출되면 1시간동안 교반하였다. 석출된 결정을 여과하고 아세톤(690 ㎖)으로 세척한 후 40℃에서 2시간동안 진공감압건조하여 세포티족심(314.3g, 수율 93.5%)을 얻었다.
IR 스펙트럼(KBr) : 1780(β-락탐카보닐) ㎝-1
1H-NMR(DMSO-d6, ppm): δ3.84(s, 3H), 5.12(d, 1H), 5.84(dd, 1H), 6.52(s, 1H), 6.76(s, 1H)
실시예 12
상기 실시예 11과 동일한 방법으로 제조하되, 다만 화학식 2c와 MAEM의 반응에서 메탄올(351.2 ㎖) 대신에 에탄올(351.2 ㎖)을 사용하여 세프티족심(313.3g, 수율 93.2%)을 얻었다.
실시예 13
상기 실시예 11과 동일한 방법으로 제조하되, 다만 화학식 2c와 MAEM의 반응에서 메탄올(351.2 ㎖) 대신에 이소프로판올(351.2 ㎖)을 사용하여 세프티족심(319.9g, 수율 95.2%)을 얻었다.
실시예 14
상기 실시예 11과 동일한 방법으로 제조하되, 다만 화학식 2c와 MAEM의 반응에서 메탄올(351.2 ㎖) 대신에 n-프로판올(351.2 ㎖)을 사용하여 세프티족심(318.6g, 수율 94.8%)을 얻었다.
실시예 15
상기 실시예 11과 동일한 방법으로 제조하되, 다만 p-TsOH·H2O(168.5g) 대신에 벤젠술폰산(134.5g)을 적가하여 세프티족심(307.6g, 수율 91.5%)을 얻었다.
실시예 16
7-아미노-3-[(5-카르복시메틸-4-메틸티아졸-2-일)티오메틸]-3-세펨-4-카르복실산(화학식 2d; 156.8g)와 2-머캅토벤조티아졸-2-(2-아미노티아졸-4-일)-2-신-메톡시이미노아세테이트(MAEM; 136.9g)를 디클로로메탄(1750 ㎖)에 현탁시켰다. 여기에 H2O(125.4 ㎖)와 메탄올(305 ㎖)을 가하고, 0℃로 냉각한 다음 트리에틸아민(115.3 ㎖)를 서서히 적가하였다. 10℃에서 4시간동안 반응시킨 후, 반응이 완료되면 p-TsOH·H2O(172.5 g)을 적가하여 결정이 석출되면 1시간동안 교반하였다. 석출된 결정을 여과하고 아세톤(950 ㎖)으로 세척한 후 40℃에서 3시간동안 진공감압건조하여 세포디짐(212.6g, 수율 93.1%)을 얻었다.
IR 스펙트럼(KBr) : 1780(β-락탐카보닐) ㎝-1
1H-NMR(DMSO-d6, ppm): δ2.2(s, 3H, CH3), 3.75(s, 2H, CH2), 3.85(s, 3H, -OCH3), 5.1(d, 1H, C6-H), 5.75(dd, 1H, C7-H), 6.7(s, 1H, 티아졸 -H)
실시예 17
상기 실시예 16과 동일한 방법으로 제조하되, 다만 화학식 2d와 MAEM의 반응에서 메탄올(305 ㎖) 대신에 에탄올(305 ㎖)을 사용하여 세포디짐(213.5g, 수율 93.5%)을 얻었다.
실시예 18
상기 실시예 16과 동일한 방법으로 제조하되, 다만 화학식 2d와 MAEM의 반응에서 메탄올(305 ㎖) 대신에 이소프로판올(305 ㎖)을 사용하여 세포디짐(218.7g, 수율 95.8%)을 얻었다.
실시예 19
상기 실시예 16과 동일한 방법으로 제조하되, 다만 화학식 2d와 MAEM의 반응에서 메탄올(305 ㎖) 대신에 n-프로판올(305 ㎖)을 사용하여 세포디짐(217.6g, 수율 95.3%)을 얻었다.
실시예 20
상기 실시예 22와 동일한 방법으로 제조하되, 다만 p-TsOH·H2O(172.5g) 대신에 벤젠술폰산(141g)을 적가하여 세포디짐(208.5g, 수율 91.3%)을 얻었다.
본 발명은 7-ACA 중간체와 MAEM을 특정 용매 및 3차아민염기 존재하에서 직접 반응시킨 후에 물층에 곧바로 유기산을 투입하여 주사제로 유용한 세펨 유도체를 제조하는 바, 특정 반응조건 설정으로 7-ACA 중간체에의 보호기 도입과정이 생략되며 제조수율이 높고 및 반응시간이 짧아 공업적으로 매우 유리한 효과를 갖는다.
Claims (3)
- 제 1 항에 있어서, 상기 3차아민염기로는 트리에틸아민을 사용하는 것을 특징으로 하는 세펨 유도체의 제조방법.
- 제 1 항에 있어서, 상기 유기산으로는 p-톨루엔술폰산(p-TsOH) 또는 벤젠술폰산을 사용하는 것을 특징으로 하는 세펨 유도체의 제조방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1019970040067A KR100229175B1 (ko) | 1997-08-22 | 1997-08-22 | 세펨 유도체의 제조방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1019970040067A KR100229175B1 (ko) | 1997-08-22 | 1997-08-22 | 세펨 유도체의 제조방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR19990017228A KR19990017228A (ko) | 1999-03-15 |
| KR100229175B1 true KR100229175B1 (ko) | 1999-11-01 |
Family
ID=19518133
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1019970040067A KR100229175B1 (ko) | 1997-08-22 | 1997-08-22 | 세펨 유도체의 제조방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR100229175B1 (ko) |
-
1997
- 1997-08-22 KR KR1019970040067A patent/KR100229175B1/ko not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| KR19990017228A (ko) | 1999-03-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20010005907A (ko) | 세프디니르의 결정성 아민 염 | |
| US5831086A (en) | Production of cefotaxime and new sodium salts | |
| KR20190055481A (ko) | 고순도 일라프라졸 결정형 b의 제조방법 | |
| KR100229175B1 (ko) | 세펨 유도체의 제조방법 | |
| KR100343434B1 (ko) | 7-아미노-3-메톡시메틸-3-세펨-4-카복실산의 제조방법 | |
| KR100537595B1 (ko) | Gm-95 물질의 제조 방법 | |
| RO109651B1 (ro) | Procedeu pentru preparea unui antibiotic cefepim dihidroclorura hidrat | |
| KR20010087055A (ko) | 신규한 티아졸 화합물 및 그의 제조 방법 | |
| RO109652B1 (ro) | Procedeu pentru prepararea unui antibiotic cefepim dihidroclorura hidrat | |
| KR20010005943A (ko) | 0-(3-아미노-2-히드록시-프로필)-히드록심산할라이드의 제조방법 | |
| FR2481280A1 (fr) | Procede de preparation de derives de 2-guanidinothiazole, nouveaux produits ainsi obtenus et leur utilisation comme agents contre les ulceres d'estomac | |
| CA1204435A (en) | Preparation of penicillin and cephalosporin compounds and novel intermediates useful therein | |
| US4237280A (en) | Intermediate for cephalosporin type compound | |
| KR970004047B1 (ko) | 세펨 화합물의 신규한 제조방법 | |
| KR100477763B1 (ko) | 세파트리진 프로필렌글리콜 중간체의 신규한 제조방법 | |
| KR101170192B1 (ko) | 1,2-벤즈이속사졸-3-메탄술폰아미드의 원-포트 제조방법 | |
| KR100502390B1 (ko) | 세팔로스포린산 유도체의 제조방법 | |
| KR100841044B1 (ko) | 세팔로스포린 화합물의 제조 방법 | |
| KR100388108B1 (ko) | 세팔로스포린계 항생제 중간체 신규 제조방법 | |
| KR960011778B1 (ko) | 신규한 결정성 세팔로스포린 유도체의 제조방법 | |
| KR0174432B1 (ko) | 신규한 결정성 세프디니르 중간체 및 그의 제조방법 | |
| HUT59687A (en) | Process for producing 7-amino-3-methoxy-methyl-ceph-3-eme-4-carboxylic acid | |
| US4147876A (en) | Easily hydrolyzable esters of 4-(2-carboxyethyl)phenyl trans-4-aminomethylcyclohexanecarboxylate and process of use | |
| KR0174431B1 (ko) | 세프디니르의 제조방법 | |
| KR100192616B1 (ko) | 7-[1-(1h)-테트라졸일아세트아미도]-3-[2-(5-메틸1,3,4-티아디아졸일)티오메틸]-3-세펨-4-카르복실산의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20020814 Year of fee payment: 4 |
|
| LAPS | Lapse due to unpaid annual fee |