JP7679384B2 - 抗炎症特性を有するカルボン酸誘導体 - Google Patents
抗炎症特性を有するカルボン酸誘導体 Download PDFInfo
- Publication number
- JP7679384B2 JP7679384B2 JP2022538727A JP2022538727A JP7679384B2 JP 7679384 B2 JP7679384 B2 JP 7679384B2 JP 2022538727 A JP2022538727 A JP 2022538727A JP 2022538727 A JP2022538727 A JP 2022538727A JP 7679384 B2 JP7679384 B2 JP 7679384B2
- Authority
- JP
- Japan
- Prior art keywords
- methyl
- acrylic acid
- oxadiazol
- phenyl
- mmol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D271/00—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms
- C07D271/02—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms not condensed with other rings
- C07D271/06—1,2,4-Oxadiazoles; Hydrogenated 1,2,4-oxadiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4245—Oxadiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/02—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings
- C07D263/30—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D263/32—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/22—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
- C07D277/24—Radicals substituted by oxygen atoms
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Rheumatology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pain & Pain Management (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Epidemiology (AREA)
- Transplantation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pyridine Compounds (AREA)
Description
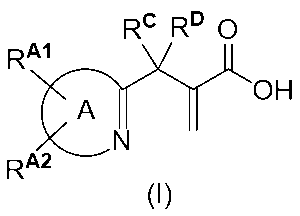
または
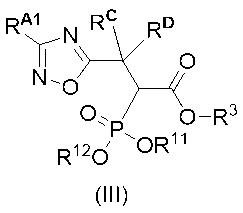
RA1が、C1-10アルキル、C2-10アルケニル、C2-10アルキニル、-(CH2)0-6-C3-10シクロアルキル、-(CH2)0-6-C5-10スピロシクロアルキル、-(CH2)0-6-アリール、およびO-アリールからなる群から選択され、
RA1が、任意にハロ、C1-6アルキル、C1-6ハロアルキル、ヒドロキシ、シアノ、OG1、S(O)0-2G1、SF5、(CH2)0-3C3-7シクロアルキル、および5~7員ヘテロシクリルからなる群から選択される1つ以上の置換基で置換され、C3-7シクロアルキルおよび5~7員ヘテロシクリルが、任意にハロ、C1-3アルキル、およびC1-3ハロアルキルから選択される1つ以上の基で置換され、同じ炭素原子と結合する2つのアルキル基が、任意に連結して、C3-7シクロアルキル環を形成し、C3-10シクロアルキル基が、任意にフェニル環に縮合し、フェニル環が、任意に1つ以上のハロ原子で置換されるか、
またはRA1が、任意にC1-2ハロアルキル、C1-2ハロアルコキシ、もしくは1つ以上のハロ原子で置換される1つのフェニル環で任意に置換され、
G1が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、または(CH2)0-1フェニルであり、G1が、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
RA2が、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、ヒドロキシ、シアノ、ニトロ、NR1R2、OG2、およびS(O)0-2G2からなる群から選択され、
G2が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
R1およびR2が独立して、HまたはC1-2アルキルであるか、または一緒になって、R1およびR2が組み合わされて、5~7員複素環を形成し得、
またはRA2が、非存在であり、
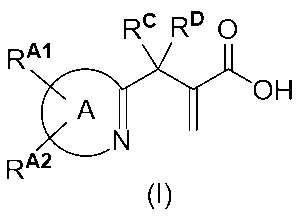
RCおよびRDが各々独立して、H、C1-2アルキル、ヒドロキシ、フルオロ、またはC1-2アルコキシであるか、またはRCおよびRDが結合して、C3-5シクロアルキル環を形成し得、
式(I)の化合物中の
あるいはその薬学的に許容される塩および/または溶媒和物が提供される。
式(I)の化合物に関して本明細書に記載の実施形態および選択は、本発明の薬学的組成物、使用する化合物、使用および方法の態様に等しく適用される。
または
RA1が、C1-10アルキル、C2-10アルケニル、C2-10アルキニル、-(CH2)0-6-C3-10シクロアルキル、-(CH2)0-6-C5-10スピロシクロアルキル、および-(CH2)0-6-アリールからなる群から選択され、RA1が、任意にハロ、C1-6アルキル、C1-6ハロアルキル、ヒドロキシ、シアノ、OG1、S(O)0-2G1、SF5、およびC3-7シクロアルキルからなる群から選択される1つ以上の置換基で置換され、C3-7シクロアルキルが、任意にハロ、C1-3アルキル、およびC1-3ハロアルキルから選択される1つ以上の基で置換され、同じ炭素原子と結合する2つのアルキル基が、任意に連結して、C3-7シクロアルキル環を形成するか、またはRA1が、任意にC1-2ハロアルキル、C1-2ハロアルコキシ、もしくは1つ以上のハロ原子で置換される1つのフェニル環で任意に置換され、
G1が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、または(CH2)0-1フェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
RA2が、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、ヒドロキシ、シアノ、ニトロ、NR1R2、OG2、およびS(O)0-2G2からなる群から選択され、
G2が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
R1およびR2が独立して、HまたはC1-2アルキルであるか、または一緒になって、R1およびR2が組み合わされて、5~7員複素環を形成し得、
またはRA2が、非存在であり、
RCおよびRDが各々独立して、H、C1-2アルキル、ヒドロキシ、フルオロ、またはC1-2アルコキシであり、
基RA1およびRA2の炭素原子の総数が、それらの任意の置換基を含んで一緒に、6~14であり、
あるいはその薬学的に許容される塩および/または溶媒和物が提供される。
または
RA1が、C1-10アルキル、C2-10アルケニル、C2-10アルキニル、-(CH2)0-6-C3-10シクロアルキル、-(CH2)0-6-C5-10スピロシクロアルキル、および-(CH2)0-6-アリールからなる群から選択され、RA1が、任意にハロ、C1-6アルキル、C1-6ハロアルキル、ヒドロキシ、シアノ、OG1、およびS(O)0-2G1からなる群から選択される1つ以上の置換基で置換され、同じ炭素原子と結合する2つのアルキル基が、任意に連結して、C3-7シクロアルキル環を形成するか、またはRA1が、任意にC1-2ハロアルキル、C1-2ハロアルコキシ、もしくは1つ以上のハロ原子で置換される1つのフェニル環で任意に置換され、
G1が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
RA2が、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、ヒドロキシ、シアノ、ニトロ、NR1R2、OG2、およびS(O)0-2G2からなる群から選択され、
G2が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
R1およびR2が独立して、HまたはC1-2アルキルであるか、または一緒になって、R1およびR2が組み合わされて、5~7員複素環を形成し得、
またはRA2が、非存在であり、
RCおよびRDが各々独立して、H、C1-2アルキル、ヒドロキシ、またはフルオロであり、
基RA1およびRA2の炭素原子の総数が、それらの任意の置換基を含んで一緒に、6~14であり、
あるいはその薬学的に許容される塩および/または溶媒和物が提供される。
または
RA1が、C1-10アルキル、C2-10アルケニル、C2-10アルキニル、-(CH2)1-6-C3-10シクロアルキル、-(CH2)0-6-C5-10スピロシクロアルキル、および-(CH2)0-6-アリールからなる群から選択され、RA1が、任意にハロ、C1-6アルキル、C1-6ハロアルキル、ヒドロキシ、シアノ、OG1、およびS(O)0-2G1からなる群から選択される1つ以上の置換基で置換され、同じ炭素原子と結合する2つのアルキル基が、任意に連結して、C3-7シクロアルキル環を形成し、
G1が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
RA2が、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、ヒドロキシ、シアノ、ニトロ、NR1R2、OG2、およびS(O)0-2G2からなる群から選択され、
G2が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
R1およびR2が独立して、HまたはC1-2アルキルであり、
またはRA2が、非存在であり、
RCおよびRDが各々独立して、H、C1-2アルキル、ヒドロキシ、またはフルオロであり、
基RA1およびRA2の炭素原子の総数が、それらの任意の置換基を含んで一緒に、6~12であり、
あるいはその薬学的に許容される塩および/または溶媒和物である。
または
RA1が、C1-10アルキル、C2-10アルケニル、C2-10アルキニル、-(CH2)0-6-C3-10シクロアルキル、-(CH2)0-6-C5-10スピロシクロアルキル、および-(CH2)0-6-アリールからなる群から選択され、RA1が、任意にハロ、C1-6アルキル、C1-6ハロアルキル、ヒドロキシ、シアノ、OG1、およびS(O)0-2G1からなる群から選択される1つ以上の置換基で置換され、
G1が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
RA2が、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、ヒドロキシ、シアノ、ニトロ、NR1R2、OG2、およびS(O)0-2G2からなる群から選択され、
G2が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
R1およびR2が独立して、HまたはC1-2アルキルであり、
またはRA2が、非存在であり、
RCおよびRDが各々独立して、H、C1-2アルキル、ヒドロキシ、またはフルオロであり、
基RA1およびRA2の炭素原子の総数が、それらの任意の置換基を含んで一緒に、6~12であり、
あるいはその薬学的に許容される塩および/または溶媒和物が提供される。
式中、A、RA1、RA2、RC、およびRDが、本明細書の他の場所で定義されるとおりである。この構造中の炭素-炭素二重結合は、「エキソ」と称される。
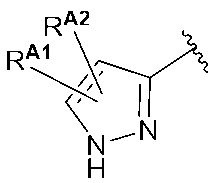
式中、A、RA1、RA2、およびRCが、本明細書の他の場所で定義されるとおりである。この構造中の炭素-炭素二重結合は、「エンド」と称される。
2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチル-1,3,4-オキサジアゾール-2-イル)メチル)アクリル酸、および
2-((5-オクチル-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
2-((3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-クロロフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-ヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
2-((3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((1-オクチル-1H-1,2,4-トリアゾール-3-イル)メチル)アクリル酸、
2-((3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチル-1,3,4-チアジアゾール-2-イル)メチル)アクリル酸、
2-((4-オクチルチアゾール-2-イル)メチル)アクリル酸、
2-((4-オクチルオキサゾール-2-イル)メチル)アクリル酸、
(R)-2-((3-(オクタン-2-イル1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(S)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-ノニル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチルチアゾール-2-イル)メチル)アクリル酸、
2-((3-ウンデシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチルオキサゾール-2-イル)メチル)アクリル酸、
2-((3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、および
2-((3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
2-((3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((4-(4-ブチルフェニル)オキサゾール-2-イル)メチル)アクリル酸、
2-((5-オクチルイソオキサゾール-3-イル)メチル)アクリル酸、
2-((4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)メチル)アクリル酸、
2-((4-オクチルピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩、
2-((5-オクチルピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩、
2-((5-オクチルピリミジン-2-イル)メチル)アクリル酸、
2-((5-オクチルピラジン-2-イル)メチル)アクリル酸、
2-((6-オクチルピリダジン-3-イル)メチル)アクリル酸、
2-((5-メチル-4-オクチルオキサゾール-2-イル)メチル)アクリル酸、
2-(ヒドロキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)メチル)アクリル酸、
2-(メトキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロプロポキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、および
2-((3-(1-(4-シクロペンチルフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
2-((3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((4,5-ジブチルオキサゾール-2-イル)メチル)アクリル酸、
2,2-((3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2,2-((3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((4-(4-ブチルベンジル)オキサゾール-2-イル)メチル)アクリル酸、
2-((3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-プロポキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロブチルフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
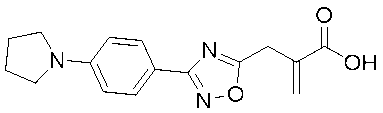
2-((3-(4-(ピロリジン-1-イル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
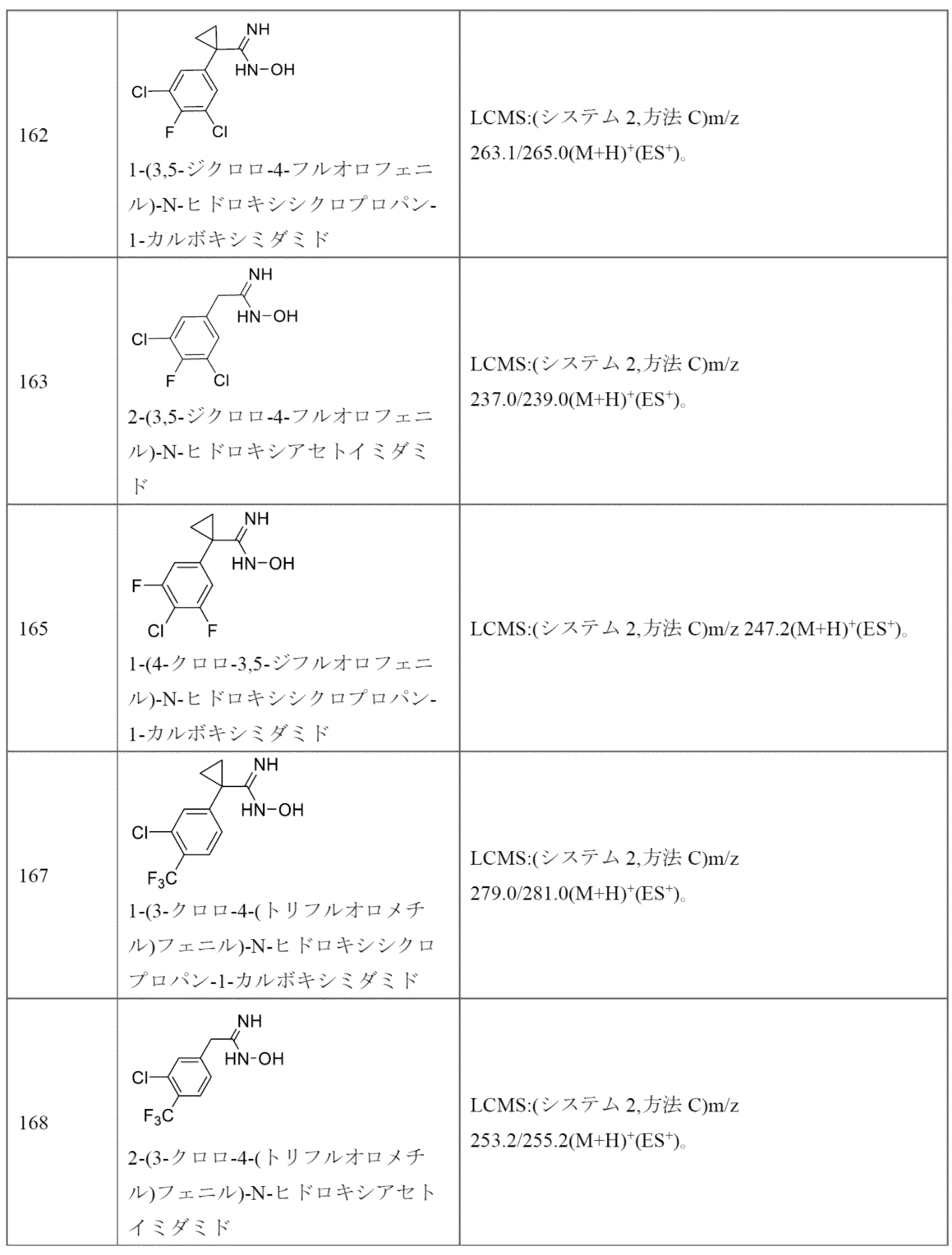
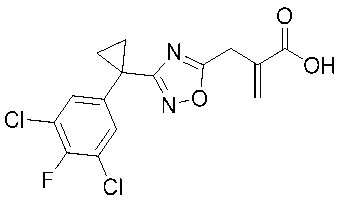
2-((3-(1-(3,5-ジクロロ-4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3,5-ジクロロ-4-フルオロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロ-3,5-ジフルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロ-4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
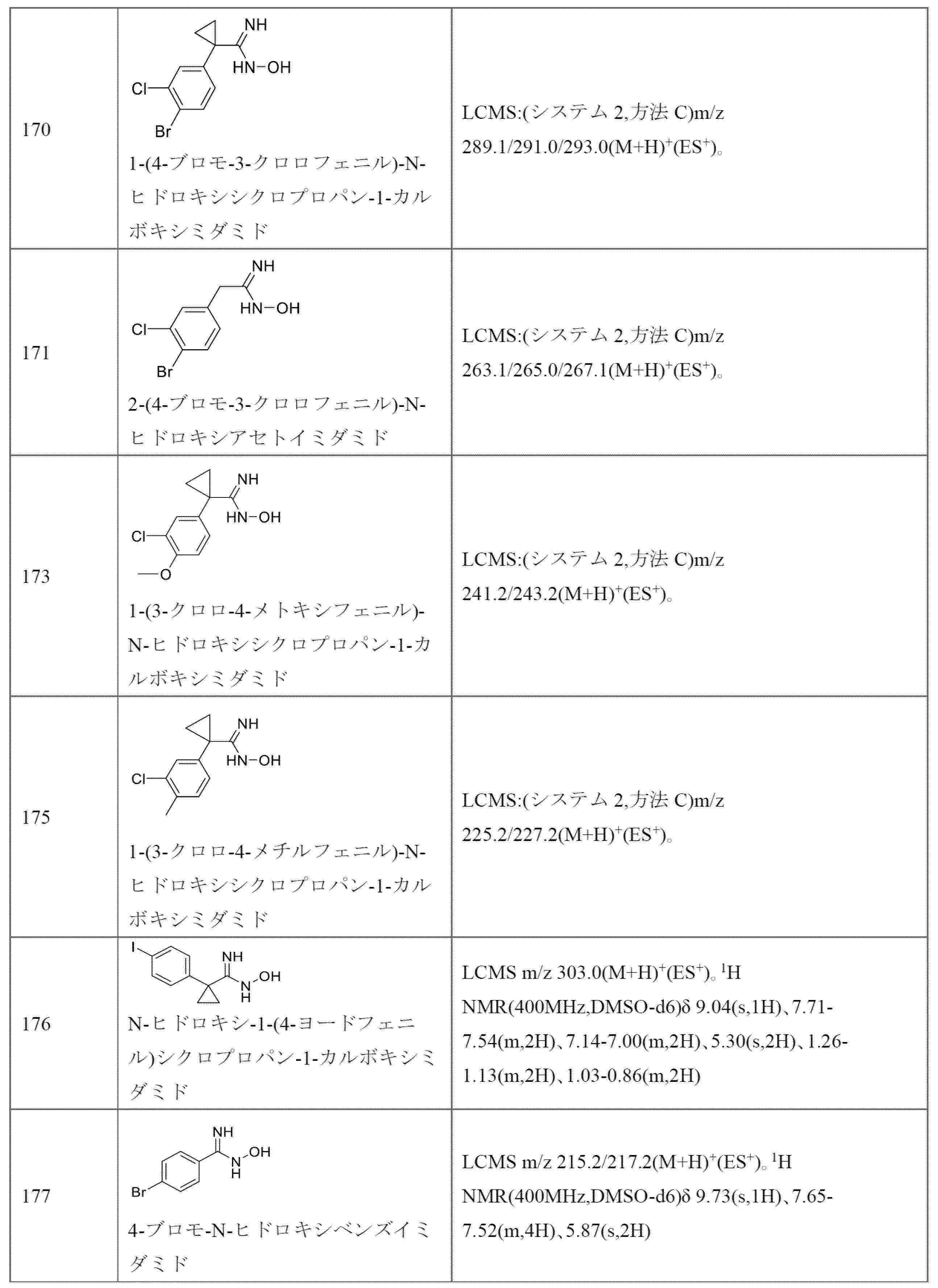
2-((3-(1-(4-ブロモ-3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブロモ-3-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロ-4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロ-4-メチルフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-シクロペンチルオキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(R)-2-((3-(4-(sec-ブトキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(S)-2-((3-(4-(sec-ブトキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(4,4,4-トリフルオロブトキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1-プロピルシクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4,6-ジクロロ-2,3-ジヒドロ-1H-インデン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-プロポキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((3-クロロ-4-メチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-クロロフェニル)フルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
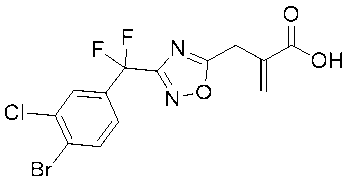
2-((3-((4-ブロモ-3-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-((トリフルオロメチル)チオ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)アクリル酸、
3-メチル-2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタン酸、
2-((3-(1-(4-((トリフルオロメチル)スルフィニル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-((トリフルオロメチル)チオ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(3-メトキシプロポキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
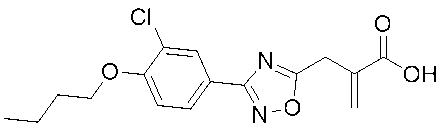
2-((3-(4-ブトキシ-3-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3-(トリフルオロメチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3,5-ジフルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-メトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-クロロ-3,5-ジフルオロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-メチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(E)-2-メチル-3-(3-オクチル-1,2,4-オキサジアゾール-5-イル)アクリル酸、
(E)-3-(3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)-2-メチルアクリル酸、
(E)-3-(3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-メチルアクリル酸、
(E)-2-メチル-3-(3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)アクリル酸、
(E)-2-メチル-3-(3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)アクリル酸、
2-((6-(4-クロロベンジル)ピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩、
2-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)アクリル酸、
2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタン酸、
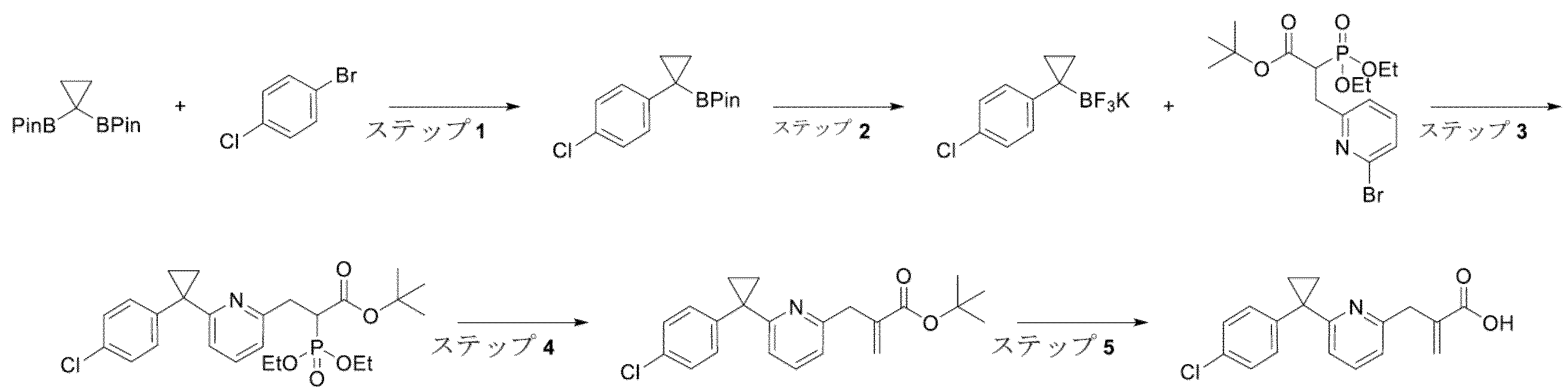
2-((6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)メチル)アクリル酸、および
2-((3-(1-(4-ブロモ-3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、および
2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、および
2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
あるいはその薬学的に許容される塩および/または溶媒和物からなる群から選択される。
式中、
ホルムアルデヒドまたはその同等物と反応させることを含み、
式中、
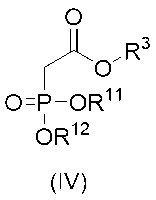
式(IV)の化合物、
式中、
式(VII)の化合物、
式中、RA1、RC、RD、R3、R11、およびR12が、本明細書の他の場所で定義される、プロセスが提供される。
Cs2CO3などの塩基と反応させることを含み、
式中、RA1、RC、RD、R3、R11、およびR12が、本明細書の他の場所で定義される、プロセスが提供される。
式中、X、RA1、RC、RD、R3、R11、およびR12が、本明細書の他の場所で定義される、プロセスが提供される。
式中、RA1およびRA2が、本明細書の他の場所で定義され、Pが、パラ-メトキシベンジルなどのカルボン酸保護基である、プロセスが提供される。
金属触媒、例えば、パラジウム触媒の存在下で一酸化炭素と反応させ、続いて加水分解し(例えば、塩基性加水分解、例えば、水性K2CO3、その後の酸性化)、式(I)の化合物を得ることを含み、
式中、RA1が、本明細書の他の場所で定義される、プロセスが提供される。
式中、RA1およびRA2が、本明細書の他の場所で定義され、Pが、パラ-メトキシベンジルなどのカルボン酸保護基である、化合物、またはその塩が提供される。
5-(クロロメチル)-3-オクチル-1,2,4-オキサジアゾール、
5-(クロロメチル)-3-ヘプチル-1,2,4-オキサジアゾール、
5-(クロロメチル)-3-(オクタン-2-イル)-1,2,4-オキサジアゾール、
5-(クロロメチル)-3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール、
5-(クロロメチル)-3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール、および
9,9,9-トリフルオロノナンニトリルからなる群から選択される化合物、
あるいはその塩、例えば、その薬学的に許容される塩および/または溶媒和物が提供される。
あるいはその塩、例えば、その薬学的に許容される塩および/または溶媒和物が提供される。
あるいはその塩、例えば、その薬学的に許容される塩および/または溶媒和物が提供される。
あるいはその塩、例えば、その薬学的に許容される塩および/または溶媒和物が提供される。
式の化合物(I)は、特に炎症性疾患もしくは望ましくない免疫応答に関連する疾患の治療または予防のための治療に使用される。以下の生物学的実施例1に示されるように、実施例1の式(I)の化合物は、より低いIC50値によって示されるように、4-オクチルイタコネートおよび2-(2-クロロベンジル)アクリル酸よりも効果的にサイトカイン放出を減少させた。この化合物はまた、NRF2を4-オクチルイタコネートおよび2-(2-クロロベンジル)アクリル酸よりも強力かつ高い効力で活性化すると同時に、マウスおよびヒト凍結保存肝細胞の両方で改善された安定性を示す。式(I)の他の例示的な化合物は、より低いIC50値によって示されるように、4-オクチルイタコネートおよび2-(2-クロロベンジル)アクリル酸よりも効果的にサイトカイン放出を減少させ、および/またはNRF2を4-オクチルイタコネートおよび2-(2-クロロベンジル)アクリル酸よりも強力かつ高い効力で活性化すると同時に、マウスおよびヒト凍結保存肝細胞の両方で改善された安定性を示す。サイトカインは、それらを標的とする抗体によってもたらされる治療上の利益によって証明されるように、炎症および免疫性疾患の重要なメディエーターである。
式の化合物(I)は通常、薬学的組成物として投与される。したがって、一実施形態では、式(I)の化合物および1つ以上の薬学的に許容される希釈剤または担体を含む薬学的組成物が提供される。
●細胞からのサイトカイン、例えば、IL-1βおよび/またはIL-6の放出を阻害するための低いIC50値、
●酵素NQO1またはNRF2経路を活性化するための低いEC50および/または高いEmax値、
●改善された代謝安定性および/または増強した最大応答、
●改善された薬物動態、特に増強された肝細胞安定性の結果を介した減少した用量および投薬頻度、
●改善された経口全身バイオアベイラビリティ、
●減少した静脈内投与後の血漿クリアランス、
●例えば、血漿および/または肝細胞における改善された安定性によって示されるような、改善された代謝安定性、
●増加した細胞透過性、
●増強された水溶解度、
●例えば、経口DMFによって引き起こされる紅潮および/または胃腸の副作用を制限することによる(Hunt T.et al.,2015;WO2014/152494A1、参照により本明細書に組み込まれる)、あるいはHCA2活性を減少または排除することによる、良好な耐容性、
●関連する治療用量での低い傷害性、
●システインプロテオームの異なる標的化をもたらし(van der Reest J.et al.,2018)、したがって、遺伝子活性化に対する効果を変更する、様々な求電子性に起因する明確な抗炎症プロファイル、
●グルタチオン-節約作用、
●オンコメタボライトフマル酸の回避(Kulkarni R.A.et al.,2019)、
●改善された物理的形状(固体)またはより高い融点。
NMRスペクトルは、BBFO 5mmプローブを備えたBruker 400MHz Avance III分光計、またはBruker 5mm SmartProbeTMを備えたBruker 500MHz Avance III HD分光計を使用して記録した。スペクトルは、特に明記されていない限り、298Kで測定し、溶媒共鳴を基準にして参照した。化学シフトは、100万分の1で報告した。データをBruker TopSpinソフトウェアを使用して取得した。
DSCデータは、45位試料ホルダを備えたPerkinElmer Pyris 6000 DSCで収集した。機器は、認定インジウムを使用してエネルギーおよび温度の校正について検証した。予め定義した量の試料の0.5~3.0mgをピンホール化アルミニウムパンに入れ、20℃.分-1で30~350℃に加熱するか、または実験指示に応じて変化させた。20ml分-1での乾窒素のパージを試料上で維持した。機器制御、データ取得、および分析は、Pyrisソフトウェアv11.1.1改訂Hを用いて実施した。
TGAデータは、20位オートサンプラを備えたPerkinElmer Pyris 1 TGAで収集した。機器は、認定重量および認定AlumelおよびPerkalloyを使用して温度について校正した。予め定義した量の1~5mgの試料を、あらかじめ風袋引きされたアルミニウムルツボに負荷し、周囲温度から400℃まで20℃.分-1で加熱した。試料上で20℃.分-1の窒素パージを維持した。機器制御、データ取得、および分析は、Pyrisソフトウェアv11.1.1改訂Hを用いて実施した。
X線粉末回折パターンは、CuKα放射線(45kV、40mA)、θ-θゴニオメータ、集束鏡、発散スリット(1/2’’)、入射および発散ビームの両方でのソラースリット(4mm)、ならびにPIXcel検出器を使用してPANalytical回折計で収集した。データ収集に使用したソフトウェアは、X’Pert Data Collectorバージョン2.2fであり、データは、X’Pert Data Viewerバージョン1.2dを使用して提示した。XRPDパターンは、PANalytical X’Pert PROを使用して、周囲条件下で透過フォイル試料ステージ(ポリイミド-カプトン、厚さ12.7μmのフィルム)を介して周囲条件下で取得した。データ収集範囲は2.994~35°2θであり、連続スキャン速度は0.202004°s-1であった。
特に明記しない限り、すべての反応物を攪拌した。
Tert-ブチルジエチルホスホノアセテート(1当量)を、NMP(0.6M)中の水素化ナトリウム(鉱油中60重量%分散、1.1当量)の溶液に0℃で滴下して加えた。反応物を室温に温め、2時間撹拌した。NMP(1.3M)中のクロロメチル-ヘテロアレーン(1.1当量)の溶液を滴下して加え、混合物を60℃に2時間加熱した。混合物を室温に冷却し、水に注ぎ、EtOAc(3回)で抽出した。合わせた有機抽出物をブラインで洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
水素化ナトリウム(鉱油中60%分散、1.5当量)を、THF(0.6M)中のtert-ブチルジエチルホスホノアセテート(1.4当量)の溶液に0℃で少しずつ加えた。混合物を室温に温め、1時間撹拌した。別に、ヨウ化ナトリウム(1.1当量)を、THF(1.8M)中のクロロメチルヘテロアレーン(1当量)に室温で加えた。混合物を1時間撹拌し、次にホスホノアセテートおよび水素化ナトリウムの混合物に加えた。反応物を70℃に加熱し、3時間撹拌し、次に室温に冷却した後、EtOAcと水との間に分配した。相を分離し、水相をEtOAc(2回)で抽出した。合わせた有機相をブラインで洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
水素化ナトリウム(1.3当量)を、THF(0.67M)中のtert-ブチルジエチルホスホノアセテート(1.3当量)の溶液に0℃で少しずつ加えた。混合物を室温に温め、1時間撹拌した。溶液を、THF(0.7M)中のクロロメチル-ヘテロアレーン(1当量)およびヨウ化ナトリウム(1.1当量)の混合物に室温で滴下して加えた。反応物を室温で2時間撹拌し、次に水を加え、混合物を濃縮してTHFを除去した。混合物を水およびEtOAcで希釈した。相を分離し、水相をEtOAcで抽出し、次に合わせた有機相をブラインで洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
鉱油中の水素化ナトリウム懸濁液(60重量%、1.2当量)を、THF(0.36M)中のtert-ブチル2-(ジエトキシホスホリル)アセテート(1.1当量)の溶液に0℃で加え、混合物を0℃で0.5時間撹拌した。次に、クロロメチルヘテロアレーン(1当量)を加え、混合物を室温で一晩撹拌した。混合物を、飽和水性NH4Cl溶液でクエンチし、EtOAc(3回)で抽出した。合わせた有機相をブラインで洗浄し、乾燥させ(Na2SO4)、濾過し、減圧下で濃縮した。残留物をフラッシュカラムクロマトグラフィーにより精製して、必要な生成物を得た。
水素化ナトリウム(鉱油中の60%重量分散、1当量)を、THF(0.2M)中のホスホネート(1当量)の溶液に0℃で加えた。10分後、パラホルムアルデヒド(3当量)を加え、次に反応物を室温に温め、45分間撹拌した。反応物を飽和水性NaHCO3でクエンチし、混合物をEtOAc(3回)で抽出した。合わせた有機抽出物をブラインで洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
パラホルムアルデヒド(1.1~2.5当量)を、THF(0.15M)中のホスホネート(1当量)および炭酸カリウム(1.2~2当量)の混合物に加えた。混合物を65℃に加熱し、4時間撹拌した後、室温に冷却し、水(150mL)に注いだ。相を分離し、水相をEtOAc(2回)で抽出した。合わせた有機相をブラインで洗浄し、乾燥させ(MgSO4)、濃縮し、次に粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
水中のホルムアルデヒド溶液(37重量%、2~30当量)を、THF(0.1~0.5M)中のホスホネート(1当量)および炭酸カリウム(2~3当量)の混合物に加えた。混合物を室温で2~5時間撹拌した後、EtOAc(3回)またはMTBE(3回)で抽出した。合わせた有機相をブラインで洗浄し、乾燥させ(Na2SO4)、濃縮し、次に粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
TFA(10~350当量)を、DCM中のtert-ブチルエステル(1当量)の溶液に加えた(最終濃度を30~50%v/v TFAにするため)。混合物を、室温で1~16時間撹拌した後、濃縮し、トルエン(2回)と共蒸発させた。粗生成物をシリカゲルでのクロマトグラフィーまたは分取HPLCにより精製して、必要な化合物を得た。
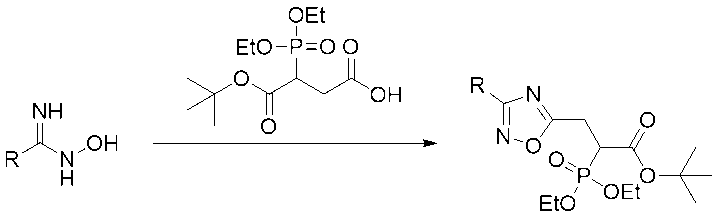
HATU(1.2~1.5当量)およびアミドキシム(1~1.5当量)を、ジメチルホルムアミド(0.2M)中の4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(1当量)およびDIPEA(5当量)の溶液に加えた。混合物を室温で1時間撹拌し、次に90℃に2時間加熱した。混合物を室温に冷却し、水で希釈し、EtOAc(3回)で抽出した。合わせた有機相を1M HCl(200mL)、ブライン(200mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
トリエチルアミン(2.0~4.0当量)を、EtOAcまたはジメチルホルムアミド(0.4~0.8M)中のアミドキシム(1.0~1.3当量)および4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(1当量)の懸濁液に室温で加えた。T3Pの溶液(EtOAcまたはジメチルホルムアミド中50重量%、2.0~2.5当量)を、0℃または室温で20分間にわたって滴下して加えた。混合物を80℃に加熱し、17時間撹拌した。混合物を室温に冷却し、ブラインおよび1M HClで希釈し、EtOAc(3回)で抽出した。合わせた有機相を1M HCl(水性)(3回)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
トリエチルアミン(2~3当量)を、EtOAcまたはジメチルホルムアミド(0.4M)中のアミドキシム(1当量)および4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(1当量)の懸濁液に室温で加えた。T3Pの溶液(EtOAcまたはジメチルホルムアミド中50重量%、2.0~2.5当量)を室温で滴下して加えた。混合物を室温で1時間撹拌し、水で希釈し、EtOAc(3回)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。残留物をTHF(0.2M)中に入れ、炭酸セシウム(2当量)を加えた。混合物を70℃に加熱し、1~5時間撹拌して、室温に冷却し、水で希釈して、EtOAc(3回)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィーにより精製して、必要な化合物を得た。
重炭酸ナトリウム(11.8g、141mmol)を、イソプロパノール(100mL)中のヒドロキシルアミンハイドロクロライド(5.88g、85mmol)の懸濁液に加えた。混合物を室温で10分間撹拌し、次にノナンニトリル(10mL、57mmol)を加え、混合物を12時間加熱還流した後、室温に冷却した。混合物を濾過し、真空で濃縮して、N-ヒドロキシノナニイミダミド(9.74g、52.0mmol、92%純度)を白色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 8.67(s,1H)、5.31(s,2H)、2.03-1.87(m,2H)、1.58-1.43(m,2H)、1.39-1.17(m,10H)、0.90-0.83(m,3H)。(主要な互変異性体割り当て)LCMS m/z 173.2(M+H)+(ES+)。
クロロアセチルクロリド(3.8mL、48mmol)を、DCM(100mL)中のN-ヒドロキシノナニミダミド(7.5g、44mmol)およびトリエチルアミン(6.9mL、50mmol)の溶液に0℃で10分間滴下して加えた。混合物を室温に温め、2時間撹拌し、次にEtOAc(100mL)で希釈し、水(150mL)で洗浄した。有機相をブライン(150mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。残留物をトルエン(100mL)中に入れ、120℃に3時間加熱し、次に室温に冷却し、15時間撹拌した。反応混合物を濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、表題化合物(6.79g、44mmol)を淡黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 5.07(s,2H)、2.72(t,J=7.4Hz,2H)、1.73-1.50(m,2H)、1.41-1.21(m,10H)、0.90-0.82(m,3H)。LCMS m/z 231.0/233.0(M+H)+(ES+)。
エタノール(50mL)中のエチルノナノエート(10mL、46mmol)およびヒドラジン水和物(50%、5.8mL、92mmol)の混合物を加熱して、一晩還流させた。混合物を室温に冷却し、濃縮した。残留物をトルエン(20mL)と共蒸発させ、次にMTBE(50mL)中に懸濁した。固体を濾過により単離し、MTBE(2×20mL)で洗浄して、ノナンヒドラジド(4.9g、28mmol)を無色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 8.89(s,1H)、4.09(br.s,2H)、1.99(t,J=7.4Hz,2H)、1.63-1.41(m,2H)、1.24(s,10H)、0.94-0.75(m,3H)。LCMS m/z 173.6(M+H)+(ES+)。
ノナンヒドラジド(1.00g、5.8mmol)、2-クロロ酢酸(0.55g、5.8mmol)、およびオキシ塩化リン(4mL、43mmol)の懸濁液を、80℃まで2時間加熱した。混合物を室温に冷却し、濃縮した。残留物をトルエン(2×15mL)で蒸発させ、次に温水(45℃)中に入れ、EtOAc(3×15mL)で抽出した。合わせた有機抽出物をブライン(20mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、表題化合物(0.861g、3.54mmol)を淡いピンク色の油として得た。1H NMR(400MHz,DMSO-d6)δ 5.02(s,2H)、2.88(t,J=7.4Hz,2H)、1.75-1.61(m,2H)、1.34-1.22(m,10H)、0.90-0.82(m,3H)。LCMS m/z 231.0/233.0(M+H)+(ES+)。
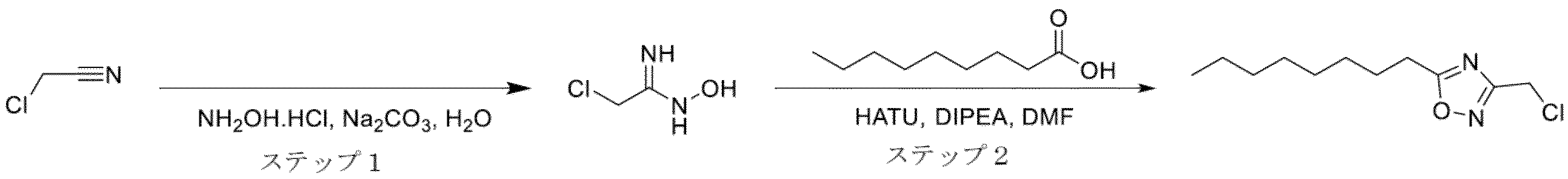
炭酸ナトリウム(7.02g、66.2mmolを、水(30mL)中の2-クロロアセトニトリル(8.4mL、132mmol)およびヒドロキシルアミンハイドロクロライド(9.20g、132mmol)の混合物に、内部温度が30℃を超えないように少しずつ加えた。反応混合物を30℃で15分間撹拌し、次にEtOAc(3×20mL)で抽出した。合わせた有機抽出物を乾燥させ(Na2SO4)、濃縮して、2-クロロ-N-ヒドロキシアセトイミダミド(8.0g、67mmol)をオレンジ色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 9.43(s,1H)、5.62(s,2H)、4.01(s,2H)。
HATU(17.5g、46.1mmol)を、ジメチルホルムアミド(50mL)中の2-クロロ-N-ヒドロキシアセトイミダミド(5.0g、46mmol)、ノナン酸(8.0mL、46mmol)、およびDIPEA(16mL、92mmol)の溶液に0℃で加えた。反応物を室温に温め、5時間撹拌した後、水(250mL)に注ぎ、EtOAc(3×30mL)で抽出した。合わせた有機抽出物をブライン(2x40mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。残留物をジメチルホルムアミド(50mL)に再溶解し、16時間撹拌して120℃に加熱した。混合物を室温に冷却し、水(250mL)に注いだ後、EtOAc(3×50mL)で抽出した。合わせた有機抽出物をブライン(2x100mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、表題化合物(3.18g、11.0mmol、80%純度)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.85(s,2H)、2.95(t,J=7.5Hz,2H)、1.78-1.68(m,2H)、1.35-1.21(m,10H)、0.88-0.84(m,3H)。LCMS m/z 231.0/233.0(M+H)+(ES+)。
水素化ナトリウム(鉱油中60重量%分散、2.05g、51.1mmol)を、ジメチルホルムアミド(25mL)中のメチル1H-1,2,4-トリアゾール-3-カルボキシレート(5.00g、39.3mmol)の溶液に0℃で少しずつ加えた。混合物を30分間撹拌した後、1-ヨードオクタン(9.92g、7.46mL、41.3mmol)を0℃で10分間にわたって滴下して加えた。反応物を室温に温め、16時間撹拌した。反応混合物を水(100mL)に注ぎ、EtOAc(3×30mL)で抽出した。合わせた有機層を水(50mL)、ブライン(50mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、メチル1-オクチル-1H-1,2,4-トリアゾール-3-カルボキシレート(3.83g、16mmol)を白色の固体として得た。LCMS m/z 240.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.70(s,1H)、4.24(t,J=7.0Hz,2H)、3.84(s,3H)、1.87-1.73(m,2H)、1.35-1.13(m,10H)、0.91-0.80(m,3H)。
水素化ホウ素ナトリウム(3.03g、80.0mmol)を、エタノール(60mL)およびTHF(60mL)中のメチル1-オクチル-1H-1,2,4-トリアゾール-3-カルボキシレート(3.83g、16.0mmol)および塩化リチウム(3.39g、80.0mmol)の懸濁液に室温で加えた。混合物を18時間撹拌し、次に飽和水性NH4Cl(50mL)でクエンチした。混合物を30分間撹拌し、次に相を分離し、水相を酢酸エチル(3×25mL)で抽出した。合わせた有機層をブライン(50mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、(1-オクチル-1H-1,2,4-トリアゾール-3-イル)メタノール(2.22g、10mmol)を白色の固体として得た。LCMS m/z 212.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.39(s,1H)、5.18(s,1H)、4.40(s,2H)、4.10(t,J=7.0Hz,2H)、1.80-1.68(m,2H)、1.33-1.16(m,10H)、0.92-0.78(m,3H)。
塩化チオニル(20mL、273mmol)を、(1-オクチル-1H-1,2,4-トリアゾール-3-イル)メタノール(2.22g、10mmol)に慎重に加えた。得られた溶液を80℃に1.5時間加熱した。混合物を濃縮し、残留物をDCM(50mL)中に溶解し、飽和NaHCO3(2×25mL)、水(25mL)、およびブライン(25mL)で洗浄した。次に、有機層を乾燥させ(Na2SO4)、濃縮して、3-(クロロメチル)-1-オクチル-1H-1,2,4-トリアゾール(2.40g、10mmol)を得、これを精製せずに使用した。LCMS m/z 230.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.51(s,1H)、4.70(s,2H)、4.14(t,J=7.0Hz,2H)、1.80-1.71(m,2H)、1.29-1.19(m,10H)、0.89-0.81(m,3H)。
塩化チオニル(9.1mL、125mmol)を、DCM(33mL)中の2-(4-ブチルフェニル)酢酸(2.00g、10.4mmol)の溶液に0℃で加えた。反応混合物を2時間加熱還流し、次に室温に冷却した。混合物を濃縮し、残留物をトルエン(2x10mL)と共蒸発させた。残留物をTHF(14mL)中に溶解し、0℃に冷却し、水酸化アンモニウム(19.2mL、28重量%、135mmol)の溶液を10分間にわたって滴下して加えた。混合物を室温に温め、さらに2時間撹拌した。次に、混合物をDCM(3×25mL)で抽出し、合わせた有機層を乾燥させ(相分離器)、濃縮し、2-(4-ブチルフェニル)アセトアミド(1.90g、8.9mmol、90%純度)をオフホワイトの固体として得た。LCMS m/z 192.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.41(s,1H)、7.16(d,J=8.1Hz,2H)、7.10(d,J=8.1Hz,2H)、6.83(s,1H)、3.31(s,2H)、2.57-2.51(m,2H)、1.59-1.47(m,2H)、1.37-1.21(m,2H)、0.89(t,J=7.3Hz,3H)。
TFAA(5.5mL、40mmol)を、1,4-ジオキサン(20mL)中の2-(4-ブチルフェニル)アセトアミド(1.90g、9.93mmol)およびトリエチルアミン(5.5mL、40mmol)の溶液に0℃で滴下して加えた。反応物を室温に加温させ、16時間撹拌した。反応混合物を濃縮し、水(30mL)に注ぎ、次にEtOAc(3×25mL)で抽出した。合わせた有機層をブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-(4-ブチルフェニル)アセトニトリル(1.75g、9.85mmol)を褐色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 7.28-7.18(m,4H)、3.98(s,2H)、2.61-2.53(m,2H)、1.59-1.49(m,2H)、1.36-1.22(m,2H)、0.89(t,J=7.4Hz,3H)。
水素化ナトリウム(鉱油中の60重量%分散、9.00g、225mmol)を、THF(500mL)中のtert-ブチル2-(ジエトキシホスホリル)アセテート(50mL、213mmol)の溶液に0℃で少しずつ加えた。混合物を15分間撹拌した後、エチルブロモアセテート(23mL、210mmol)を滴下して加えた。混合物を1時間撹拌し、次に飽和水性NH4Cl(100mL)でクエンチし、EtOAc(3×100mL)で抽出した。合わせた有機相をブライン(300mL)で洗浄し、乾燥させ(MgSO4)、濃縮し、1-(tert-ブチル)4-エチル2-(ジエトキシホスホリル)スクシナート(77.1g、182mmol、80%純度)を無色の油として得た。LCMS m/z 361.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.13-4.01(m,6H)、3.28(ddd,J=23.8,11.3,3.9Hz,1H)、2.78(ddd,J=17.2,11.3,8.2Hz,1H)、2.64(ddd,J=17.1,8.5,4.0Hz,1H)、1.40(s,9H)、1.28-1.21(m,6H)、1.18(t,J=7.1Hz,3H)。
水酸化ナトリウム水溶液(1M、250mL、250mmol)を、THF(250mL)中の1-(tert-ブチル)4-エチル2-(ジエトキシホスホリル)スクシナート(77.1g、182mmol、80%純度)の溶液に加えた。混合物を室温で16時間撹拌した。混合物を部分的に約250mLに濃縮し、次にEtOAc(3×100mL)で抽出した。水相を濃HClでpH1に酸性化し、EtOAc(3×100mL)で抽出した。合わせた有機相をブライン(250mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。残留物をヘキサン(300mL)で粉砕し、得られた固体を濾過により収集し、4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(53.00g、0.15mmol、90%純度)を白色の固体として得た。LCMS m/z 333.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.44(s,1H)、4.11-3.99(m,4H)、3.22(ddd,J=23.7,11.5,3.7Hz,1H)、2.73(ddd,J=17.3,11.5,7.6Hz,1H)、2.56(ddd,J=17.3,8.6,3.7Hz,1H)、1.40(s,9H)、1.25(dt,J=8.3,7.0Hz,6H)。31P NMR(162MHz,DMSO-d6)δ 21.88。
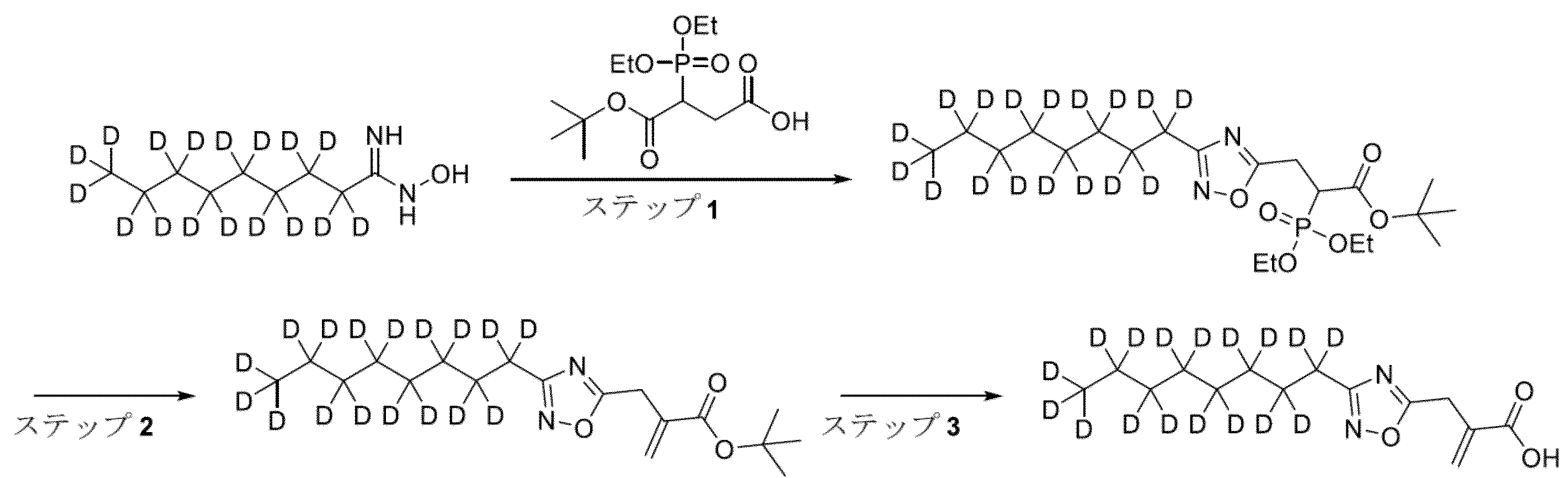
0℃でDCM(20mL)中のノナン-d17酸(1.00g、5.70mmol)の撹拌溶液を、塩化チオニル(2.1mL、29ミリモル)で滴下して処理した。混合物を0℃で15分間、次に40℃で3時間撹拌した。反応混合物を濃縮し、次にトルエン(2x10mL)と共蒸発させた。残留物をTHF(10mL)中に入れ、0℃に冷却し、水酸化アンモニウム(28%水性、8.0mL 57mmol)で滴下して処理した。反応混合物を室温に温め、16時間撹拌した。混合物を部分的に濃縮し、DCM(3x10mL)で抽出した。合わせた有機抽出物を乾燥させ(相分離器)、濃縮して、ノナンアミド-d17(844mg、4.84mmol)を白色の固体として得、これをさらに精製することなく次のステップで使用した。LCMS m/z 175.3(M+H)+(ES+)。
0℃で1,4-ジオキサン(10mL)中のノナンアミド-d17(844mg、4.84mmol)およびトリエチルアミン(2.7mL、19mmol)の撹拌懸濁液を、TFAA(2.0mL、14mmol)で滴下して処理した。得られた溶液を室温まで温め、18時間撹拌した。反応混合物を濃縮し、残留物を水(20mL)に注ぎ、EtOAc(20mL)で抽出した。相を分離し、水相をEtOAc(3x20mL)で抽出した。合わせた有機抽出物をブライン(40mL)で洗浄し、乾燥させ(相分離器)、濃縮し、ノナンニトリル-d17(1.2g)を黄色の油として得、これを定量的収率を仮定して、さらに精製または分析することなく次のステップで使用した。
IPA(10mL)中のヒドロキシルアミンハイドロクロライド(685mg、9.76mmol)の懸濁液を、重炭酸ナトリウム(1.24g、14.8mmol)で処理し、15分間撹拌した。IPA(5mL)中のノナンニトリル-d17(約1.2g、4.84mmol[仮定])の溶液を滴下し、次に反応混合物を85℃で18時間撹拌した。反応混合物を室温に冷却し、濾過し、EtOAc(50mL)で洗浄した。濾液を真空中で濃縮して、N-ヒドロキシノナニイミダミド-d17(1.37g、4.84mmol[仮定])を黄色の油として得、これを定量的収率を仮定して、さらに精製することなく次のステップで使用した。LCMS m/z 190.3(M+H)+(ES+)。
p-TsCl(8.1g、42mmol)を、ピリジン(11mL)中の(S)-オクタン-2-オール(5.0g、38mmol)の混合物に-5℃で少しずつ加えた。混合物を室温に温め、18時間撹拌した。混合物を氷でクエンチし、次に水(100mL)を加えた。混合物をEtOAc(3×100mL)で抽出した。合わせた有機層を10%クエン酸(3x100mL)、水(100mL)で洗浄し、乾燥(MgSO4)させ、濃縮し、(S)-オクタン-2-イル4-メチルベンゼンスルホネート(9.86g、33mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.84-7.73(m,2H)、7.48(d,J=8.0Hz,2H)、4.63-4.46(m,1H)、2.42(s,3H)、1.56-1.37(m,2H)、1.25-0.95(m,11H)、0.83(t,J=7.1Hz,3H)。
シアン化ナトリウム(1.78g、36.2mmol)を、DMSO(50mL)中の(S)-オクタン-2-イル4-メチルベンゼンスルホネート(9.86g、33mmol)の溶液に50℃で加えた。混合物を50℃で18時間撹拌し、室温に冷却した。水(500mL)を加え、相を分離し、水相をDCM(3x100mL)で抽出した。合わせた有機相をブライン(3x100mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、(R)-2-メチルオクタニトリル(3.47g、22mmol)を透明な無色の油として得た。1H NMR(400MHz,CDCl3)δ 2.67-2.53(m,1H)、1.70-1.12(m,13H)、0.97-0.81(m,3H)。1H NMR(400MHz,DMSO-d6)δ 7.84-7.73(m,2H)、7.48(d,J=8.0Hz,2H)、4.63-4.46(m,1H)、2.42(s,3H)、1.56-1.37(m,2H)、1.25-0.95(m,11H)、0.83(t,J=7.1Hz,3H)。
シアン化ナトリウム(0.84g、17.2mmol)を、DMSO(24mL)中の8-ブロモオクタン-1-オール(3.00g、14.4mmol)の溶液に室温で加えた。混合物を室温で18時間撹拌し、次に水(50mL)で希釈し、EtOAc(2x100mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、9-ヒドロキシノナンニトリル(1.45g、9.1mmol)を半透明の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.32(t,J=5.2Hz,1H)、3.38(td,J=6.5,5.1Hz,2H)、2.48(t,J=7.1Hz,2H)、1.61-1.48(m,2H)、1.47-1.21(m,10H)。
DMP(5.54g、13.1mmol)を、DCM(14mL)中の9-ヒドロキシノナンニトリル(1.45g、9.1mmol)の溶液に0℃で少しずつ加えた。反応混合物を室温に温め、45分間撹拌した。反応混合物を飽和Na2S2O3(15mL)でクエンチした。有機層を飽和水性NaHCO3(15mL)で洗浄した。水層をDCM(3x30mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、9-オキソペンタンニトリルを得、これをDCM(35mL)で直接希釈し、次に0℃に冷却した。三フッ化ジエチルアミノ硫黄(2.46mL、18.6mmol)を滴下して加えた。混合物を室温に温め、16時間撹拌した。反応混合物を飽和水性NaHCO3でpH7までクエンチした。水相をDCM(3x30mL)で抽出した。合わせた有機抽出物を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、9,9-ジフルオロノナンニトリル(0.490g、2.5mmol、90%純度)を黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 6.05(tt,J=56.9,4.5Hz,1H)、2.48(t,J=7.1Hz,2H)、1.89-1.69(m,2H)、1.61-1.48(m,2H)、1.46-1.18(m,8H)。
イソプロピルマグネシウムクロリド(THF中2M、33mL、66mmol)を、THF(150mL)中のtert-ブチル(2-(メトキシ(メチル)アミノ)-2-オキソエチル)カルバメート(14.5g、66mmol)の懸濁液に0℃で滴下して加えた。オクチルマグネシウムブロミド(THF中2M、42mL、84mmol)を滴下して加えた。混合物を室温に温め、16時間撹拌した。反応混合物を0℃に冷却し、1M HCl(100mL)でクエンチした。相を分離し、水層をEtOAc(2×100mL)で抽出した。合わせた有機相をブライン(2x100mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルのクロマトグラフィー(0~40%MTBE/イソヘキサン)により精製して、tert-ブチル(2-オキソデシル)カルバメート(16.5g、55mmol、90%純度)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.02(t,J=5.9Hz,1H)、3.72(d,J=5.9Hz,2H)、2.37(t,J=7.3Hz,2H)、1.49-1.41(m,2H)、1.39(s,9H)、1.27-1.19(m,10H)、0.93-0.80(m,3H)。
HCl(1,4-ジオキサン中4M、46mL、0.18mol)を、1,4-ジオキサン中のtert-ブチル(2-オキソデシル)カルバメート(16.5g、56mmol、90%純度)の溶液に0℃で滴下して加えた。反応物を18時間室温で撹拌した。HCl(1,4-ジオキサン中4M、18mL、72mmol)を加え、混合物を室温でさらに2時間撹拌した。混合物を濃縮して、1-アミノデカン-2-オンハイドロクロライド(13.0g、53mmol、85%純度)を淡褐色の固体として得、これをさらに精製することなく使用した。1H NMR(400MHz,DMSO-d6)δ 7.98(s,3H)、3.91(s,2H)、2.53-2.48(m,2H)、1.55-1.46(m,2H)、1.34-1.15(m,10H)、0.95-0.75(m,3H)。
THF(20mL)中の1-ブロモ-4-(1-(トリフルオロメチル)シクロプロピル)ベンゼン(1.00g、3.77mmol)およびPd-170(50mg、75μmol)の溶液を、窒素で10分間脱気した。(2-(tert-ブトキシ)-2-オキソエチル)亜鉛(II)ブロミド(THF中0.45M、9.2mL)の溶液を滴下して加えた。反応物を室温で1.5時間撹拌し、次に75℃に加熱し、16時間撹拌した。反応物を室温に冷却し、水(20mL)に注いだ。相を分離し、水層をEtOAc(3×20mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(4-(1-(トリフルオロメチル)シクロプロピル)フェニル)アセテート(0.653g、2.2mmol)を透明な黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.41(d,J=8.0Hz,2H)、7.31-7.20(m,2H)、3.57(s,2H)、1.41(s,9H)、1.35-1.30(m,2H)、1.14-1.08(m,2H)。
tert-ブチル2-(4-(1-(トリフルオロメチル)シクロプロピル)フェニル)アセテート(0.653g、2.2mmol)およびギ酸(4.1mL、109mmol)の混合物を、室温で16時間撹拌した。混合物を濃縮し、残留物をトルエン(2x10mL)と共蒸発させて、2-(4-(1-(トリフルオロメチル)シクロプロピル)フェニル)酢酸(0.625g、2.1mmol、84%純度)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 12.37(s,1H)、7.40(d,J=8.0Hz,2H)、7.28(d,J=7.9Hz,2H)、3.58(s,2H)、1.36-1.29(m,2H)、1.14-1.07(m,2H)。
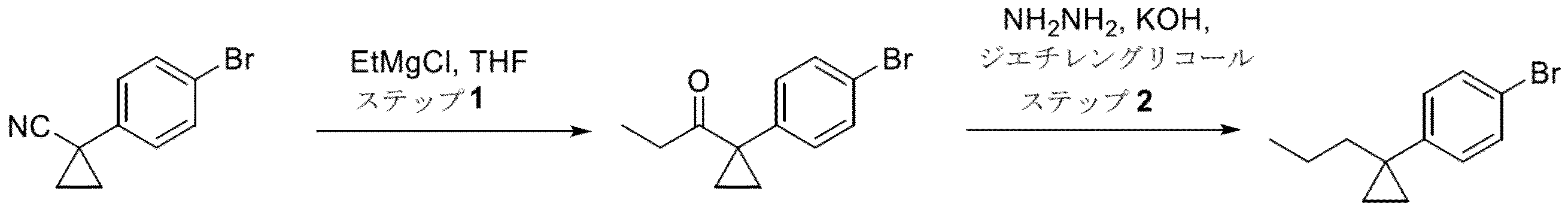
エチルマグネシウムクロリドの溶液(THF中2M、14mL、28mmol)を、THF(40mL)中の1-(4-ブロモフェニル)シクロプロパン-1-カルボニトリル(5.0g、22.5mmol)の溶液に室温で滴下して加えた。次に、混合物を70℃で4時間撹拌し、室温に冷却し、飽和NH4Cl(75mL)に注いだ。希H2SO4(1M、15mL)を加え、混合物を10分間撹拌し、次にEtOAc(3×30mL)で抽出した。合わせた有機層をブラインで洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、1-(1-(4-ブロモフェニル)シクロプロピル)プロパン-1-オン(4.61g、18.2mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.57-7.51(m,2H)、7.39-7.32(m,2H)、2.25(q,J=7.1Hz,2H)、1.50-1.42(m,2H)、1.17-1.10(m,2H)、0.82(t,J=7.1Hz,3H)。
ジエチレングリコール(35mL)中の1-(1-(4-ブロモフェニル)シクロプロピル)プロパン-1-オン(4.61g 18.2mmol)、ヒドラジン水和物(2.7mL、54.6mmol)、および水酸化カリウム(3.07g、54.6mmol)の溶液を、200℃に3時間加熱した。混合物を室温に冷却し、水(100mL)に注いだ。混合物をEtOAc(3×50mL)で抽出し、合わせた有機層をブライン(100mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、1-ブロモ-4-(1-プロピルシクロプロピル)ベンゼン(3.73g、15mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.48-7.42(m,2H)、7.25-7.19(m,2H)、1.55-1.49(m,2H)、1.26-1.15(m,2H)、0.81(t,J=7.4Hz,3H)、0.75-0.71(m,2H)、0.71-0.66(m,2H)。
MeCN(20ml)中の1,1,1-トリフルオロ-4-ヨードブタン(2.7mL、21mmol)およびトリフェニルホスフィン(5.50g、21mmol)の混合物を、18時間加熱還流した。混合物を室温に冷却し、濃縮した。残留物をトルエン(15ml)に懸濁し、85℃で10分間撹拌した。混合物を室温に冷却し、沈殿物を濾過により収集した。固体をトルエン(2×20mL)で洗浄して、トリフェニル(4,4,4-トリフルオロブチル)ホスホニウムヨージド(10.5g、19mmol、90%純度)を白色の固体として得た。LCMS m/z 373.0(M-I)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.94-7.80(m,9H)、7.80-7.68(m,6H)、4.15-4.00(m,2H)、2.79-2.64(m,2H)、2.05-1.83(m,2H)。
炭酸カリウム(4.66g、33.7mmol)を、IPA(100mL)中の4-ブロモベンズアルデヒド(3.40g、18.3mmol)およびトリフェニル(4,4,4-トリフルオロブチル)ホスホニウムヨージド(10.2g、18.3mmol、90%純度)の溶液に加えた。混合物を80℃に加熱し、17時間撹拌した。混合物を室温に冷却し、濃縮した。得られた固体をDCM(100mL)中に懸濁し、濾過し、濾液を濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%DCM/イソヘキサン)により精製して、(E)-1-ブロモ-4-(5,5,5-トリフルオロペント-1-エン-1-イル)ベンゼン(4.81g、16mmol)を透明な無色の油として異性体の83:17混合物として得た。1H NMR(400MHz,DMSO-d6)δ 7.54-7.48(m,2H)、7.39-7.31(m,2H)、6.53-6.47(m,1H)、6.36-6.31(m,1H)、2.49-2.37(m,4H)[(E)-異性体に対応するデータ]。
EtOH(75mL)中の(E)-1-ブロモ-4-(5,5,5-トリフルオロペント-1-エン-1-イル)ベンゼン(4.81g、16mmol)、および1%Pt/C(50重量%、950mg)の懸濁液を、水素雰囲気(1バール)下で、室温で2時間撹拌した。混合物を濾過して濃縮した。粗生成物をシリカゲル(100%イソ-ヘキサン)でのクロマトグラフィーにより精製して、1-ブロモ-4-(5,5,5-トリフルオロペンチル)ベンゼン(4.33g、14mmol、90%純度)を透明な無色の液体としてを得た。1H NMR(400MHz,DMSO-d6)δ 7.50-7.44(m,2H)、7.20-7.15(m,2H)、2.59(t,J=7.6Hz,2H)、2.36-2.18(m,2H)、1.69-1.55(m,2H)、1.54-1.43(m,2H)。
炭酸カリウム(5.70g、41.2mmol)を、IPA(100mL)中の4-ブロモベンズアルデヒド(4.05g、21.9mmol)およびトリフェニル(シクロプロピルメチル)ホスホニウムヨージド(9.72g、21.9mmol)の溶液に加えた。混合物を80℃に加熱し、17時間撹拌した。混合物を室温に冷却し、濃縮した。得られた固体をDCM(100mL)中に懸濁し、濾過し、濾液を濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%DCM/イソヘキサン)により精製して、(E)-1-ブロモ-4-(2-シクロプロピルビニル)ベンゼン(4.28g、18mmol)を白色の固体として異性体の76:24混合物として得た。1H NMR(400MHz,DMSO-d6)δ 7.49-7.42(m,2H)、7.33-7.26(m,2H)、6.44(d,J=15.9Hz,1H)、5.89(dd,J=15.9,9.1Hz,1H)、1.63-1.46(m,1H)、0.87-0.74(m,2H)、0.58-0.46(m,2H)[(E)-異性体に対応するデータ]。
EtOH(60mL)中の(E)-1-ブロモ-4-(2-シクロプロピルビニル)ベンゼン(4.28g、18mmol)および1%Pt/C(50重量%、800mg)の懸濁液を、水素雰囲気下(1バール)下で、室温で6時間撹拌した。混合物を濾過して濃縮した。粗生成物をシリカゲル(100%イソ-ヘキサン)でのクロマトグラフィーにより精製して、1-ブロモ-4-(2-シクロプロピルエチル)ベンゼン(4.46g、12mmol、61%純度)を透明な無色の液体としてを得た。1H NMR(400MHz,DMSO-d6)δ 7.49-7.39(m,2H)、7.22-7.13(m,2H)、2.68-2.58(m,2H)、1.49-1.44(m,1H)、0.90-0.81(m,1H)、0.72-0.59(m,1H)、0.43-0.29(m,2H)、0.09--0.03(m,2H)。
エチルクロロホルメート(8.1mL、85mmol)を、THF(200mL)中の4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(25.0g、80.6mmol)、およびトリエチルアミン(12.0mL、86mmol)の溶液に0℃で滴下して加えた。混合物を30分間撹拌し、次にさらにトリエチルアミン(3.0mL、22mmol)およびエチルクロロホルメート(2.0mL、21mmol)を加えた。1時間後、アンモニア(30%水性、25mL、0.39mol)を滴下して加えた。混合物を室温で1時間撹拌し、次に約50mLに濃縮した。混合物を水(300mL)で希釈し、EtOAc(5x200mL)で抽出した。合わせた有機相を飽和水性NH4Cl(400mL)、ブライン(400mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。残留物をMTBE(200mL)で粉砕し、得られた固体を濾過により単離して、tert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-オキソブタノエート(10.66g、34mmol)を白色の固体として得た。LCMS m/z 254.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.41(s,1H)、6.89(s,1H)、4.10-3.97(m,4H)、3.21(ddd,J=23.3,11.5,3.4Hz,1H)、2.69(ddd,J=16.3,11.5,7.2Hz,1H)、2.39(ddd,J=16.4,9.6,3.4Hz,1H)、1.38(s,9H)、1.24(q,J=7.2Hz,6H)。31P NMR(162MHz,DMSO-d6)δ 23.19。
無水トリフルオロ酢酸(17.9mL、129mmol)を、1,4-ジオキサン(100mL)中のtert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-オキソブタノエート(12.85g、41.6mmol)およびトリエチルアミン(18.0mL、129mmol)の撹拌溶液に0℃で少しずつ加えた。反応物を室温に加温させ、60時間撹拌した。反応混合物を水(100mL)でクエンチし、混合物を部分的に濃縮した。混合物をEtOAc(2×150mL)で抽出した。合わせた有機抽出物をブライン(200mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-シアノ-2-(ジエトキシホスホリル)プロパノエート(6.63g、22mmol)を褐色の油として得た。LCMS m/z 236.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.14-4.03(m,4H)、3.59(ddd,J=23.8,8.1,5.9Hz,1H)、2.90-2.75(m,2H)、1.44(s,9H)、1.29-1.22(m,6H)。
2-プロパノール(45mL)中のヒドロキシルアミンハイドロクロライド(2.30g、33.1mmol)および重炭酸ナトリウム(2.78g、33.1mmol)の混合物を15分間撹拌した後、tert-ブチル3-シアノ-2-(ジエトキシホスホリル)プロパノエート(6.63g、22.1mmol)を加え、混合物を還流下で18時間撹拌した。反応混合物を室温に冷却し、濾過した。濾液を濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~20%MeOH/DCM)により精製して、tert-ブチル2-(ジエトキシホスホリル)-4-(ヒドロキシアミノ)-4-イミノブタノエート(4.83g、15mmol)をワックス状の淡緑色の固体として得た。LCMS m/z 325.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.93(s,1H)、5.40(s,2H)、4.10-3.96(m,4H)、3.25(ddd,J=23.0,11.8,3.1Hz,1H)、2.57(ddd,J=15.9,11.7,6.8Hz,1H)、2.37(ddd,J=15.9,10.2,3.1Hz,1H)、1.38(s,9H)、1.24(q,J=7.0Hz,6H)。
エチル2-(4-ブロモフェニル)-2,2-ジフルオロアセテート(3.5g、13mmol)およびアンモニア(メタノール中7M、20mL、0.92mol)の混合物を、室温で16時間撹拌した。混合物を濃縮して、2-(4-ブロモフェニル)-2,2-ジフルオロアセトアミド(3.0g、10mmol、90%純度)を淡黄色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 8.38(s,br.1H)、8.05(s,br.1H)、7.80-7.70(m,2H)、7.57-7.47(m,2H)。
TFAA(1.2mL、8.6mmol)を、THF(30mL)中の2-(4-ブロモフェニル)-2,2-ジフルオロアセトアミド(2.0g、7.2mmol、90%純度)およびピリジン(1.7mL、22mmol)の溶液に0℃で滴下して加えた。混合物を0℃で1時間撹拌し、次に室温に温め、さらに20分間撹拌した。混合物を水(80mL)中に注ぎ、EtOAc(3x80mL)で抽出した。合わせた有機層を乾燥させ(MgSO4)、濃縮し、2-(4-ブロモフェニル)-2,2-ジフルオロアセトニトリル(1.9g、7.2mmol、90%純度)を透明な淡いオレンジ色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.93-7.84(m,2H)、7.82-7.73(m,2H)。
1-ヨード-4-(トリフルオロメチル)ベンゼン(8.0mL、54.4mmol)およびエチル2-ブロモ-2,2-ジフルオロアセテート(7.0mL、54.4mmol)を、DMSO(100mL)中の銅(8.99g、142mmol)の懸濁液に加えた。混合物を60℃に加熱し、18時間撹拌した。混合物を室温に冷却し、飽和水性NH4Cl(200mL)およびEtOAc(200mL)に注いだ。混合物を濾過し、相を分離した。水相をEtOAc(2×100mL)で抽出した。合わせた有機相をブライン(200mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、エチル2,2-ジフルオロ-2-(4-(トリフルオロメチル)フェニル)アセテート(13.17g、45mmol、92%純度)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.95(d,J=8.2Hz,2H)、7.85(d,J=8.2Hz,2H)、4.32(q,J=7.1Hz,2H)、1.23(t,J=7.1Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-61.64,-102.28。
エチル2,2-ジフルオロ-2-(4-(トリフルオロメチル)フェニル)アセテート(8.00g、29.8mmol)から、中間体128、ステップ1で記載した手順に従って調製し、2,2-ジフルオロ-2-(4-(トリフルオロメチル)フェニル)アセトアミド(5.25g、22mmol)を白色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 8.47(br.s,1H)、8.12(br.s,1H)、7.93(d,J=8.2Hz,2H)、7.82(d,J=8.2Hz,2H)。19F NMR(376MHz,DMSO-d6)δ-61.49,-102.79。
2,2-ジフルオロ-2-(4-(トリフルオロメチル)フェニル)アセトアミド(5.25g、22mmol)から、中間体128、ステップ2で記載した手順に従って調製し、2,2-ジフルオロ-2-(4-(トリフルオロメチル)フェニル)アセトニトリル(3.35g、15mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 8.07(d,J=8.7Hz,2H)、8.04(d,J=8.8Hz,2H)。19F NMR(376MHz,DMSO-d6)δ-61.90,-83.33。
THF(20mL)中の1-ブロモ-4-(1,1-ジフルオロペンチル)ベンゼン(1.00g、3.80mmol)およびPd-170(51mg、76μmol)の溶液を、窒素で10分間スパージングした。(2-エトキシ-2-オキソエチル)亜鉛(II)ブロミド(THF中0.34M、25mL、8.4mmol)を滴下して加えた。混合物を75℃に加熱し、16時間撹拌し、次に室温に冷却し、水(20mL)に注いだ。混合物を分離し、水層をEtOAc(3×20mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、エチル2-(4-(1,1-ジフルオロペンチル)フェニル)アセテート(0.651g、2.4mmol)を透明な黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.46(d,J=8.2Hz,2H)、7.37(d,J=8.1Hz,2H)、4.09(q,J=7.1Hz,2H)、3.73(s,2H)、2.26-2.10(m,2H)、1.34-1.25(m,4H)、1.18(t,J=7.1Hz,3H)、0.87-0.81(m,3H)。19F NMR(376MHz,DMSO-d6)δ-92.45。
大きなBiotageマイクロ波バイアルにエチル2-(4-(1,1-ジフルオロペンチル)フェニル)アセテート(0.65g、2.4mmol)およびアンモニア(MeOH中7M、6.9mL、48mmol)を負荷した。バイアルを密封し、75℃で16時間加熱した。混合物を室温に冷却し、濃縮した。容器にアンモニア(MeOH中7M、6.9mL、48mmol)を再負荷し、75℃で16時間加熱した。混合物を濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、2-(4-(1,1-ジフルオロペンチル)フェニル)アセトアミド(0.471g、1.9mmol)を白色の固体として得た。LCMS m/z 242.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.50(s,1H)、7.43(d,J=8.3Hz,2H)、7.35(d,J=8.0Hz,2H)、6.91(s,1H)、3.42(s,2H)、2.25-2.09(m,2H)、1.35-1.25(m,4H)、0.88-0.81(m,3H)。19F NMR(376MHz,DMSO-d6)δ-92.25。
2-(4-(1,1-ジフルオロペンチル)フェニル)アセトアミド(0.471g、1.9mmol)から、中間体62、ステップ2で記載した手順に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%、0~10%EtOAc/イソヘキサン)により精製して、2-(4-(1,1-ジフルオロペンチル)フェニル)アセトニトリル(0.394g、1.7mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.54(d,J=8.3Hz,2H)、7.46(d,J=8.1Hz,2H)、4.11(s,2H)、2.26-2.10(m,2H)、1.34-1.22(m,4H)、0.90-0.80(m,3H)。19F NMR(376MHz,DMSO-d6)δ-92.67。
鉱油中のNaH懸濁液(60重量%、16g、408mmol)を、THF(340mL)中のヘキサ-5-イン-1-オール(40g、408mmol)の溶液に0℃で加え、混合物を発泡が静まるまで撹拌した。テトラブチルアンモニウムヨージド(12.6g、34mmol)およびベンジルブロミド(58.2g、340mmol)を加え、混合物を室温で18時間撹拌した。飽和水性NH4Cl溶液を加え、反応混合物をEt2Oで抽出した。合わせた有機相をブラインで洗浄し、MgSO4で乾燥させ、濾過し、濾液を減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(120gシリカ、10~20%EtOAc/石油エーテル)により精製して、((ヘキサ-5-イン-1-イルオキシ)メチル)ベンゼン(70g、372mmol、91%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 189.4(M+H)+(ES+)。
ジメチルホルムアミド(540mL)中のCuI(15.2g、79.8mmol)、K2CO3(36g、266mmol)、およびN,N,N’,N’-テトラメチルエチレンジアミン(9.4g、79.8mmol)の混合物を室温で、乾燥空気雰囲気下で15分間激しく撹拌した。TMSCF3(15.2g、106mmol)を加え、得られた深緑色の混合物をさらに5分間撹拌し、次に0℃に冷却した。次に0℃に予め冷却したジメチルホルムアミド(540mL)中の((ヘキサ-5-イン-1-イルオキシ)メチル)ベンゼン(10g、53.2mmol)およびTMSCF3(15.2g、106mmol)の溶液を一度に少しずつ加えた。0℃で30分後、反応混合物を室温に温め、乾燥空気雰囲気下で24時間撹拌した。次に水を加え、混合物をEt 2 Oで抽出した。合わせた有機相を水およびブラインで洗浄し、次にMgSO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(120gシリカ、10~20%EtOAc/石油エーテル)により精製して、(((7,7,7-トリフルオロヘプト-5-イン-1-イル)オキシ)メチル)ベンゼン(6.8g、26.5mmol、50%)を淡黄色の油として得た。LCMS:(システム2,方法A)m/z 274.4(M+NH4)+(ES+)。
THF(13.5mL)およびH2O(1.5mL)の混合物中の(((7,7,7-トリフルオロヘプト-5-イン-1-イル)オキシ)メチル)ベンゼン(2.5g、9.8mmol)の溶液に、JohnPhos AuCl(CAS:854045-93-5)(265mg、0.5mmol)および銀トリフルオロメタンスルホネート(128mg、0.5mmol)を加え、バイアルをアルミホイルで包み、70℃に加熱した。18時間後、反応混合物を室温に冷却し、飽和水性NaHCO3溶液で希釈し、DCM(3回)で抽出した。合わせた有機相をNa2SO4で乾燥させ、濾過し、減圧下で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、10~30%EtOAc/石油エーテル)により精製して、7-(ベンジルオキシ)-1,1,1-トリフルオロヘプタン-3-オン(2.0g、7.3mmol、75%)を淡黄色の油として得た。LCMS:(システム2,方法A)m/z 275.3(M+H)+(ES+)。
DCE(60mL)中の7-(ベンジルオキシ)-1,1,1-トリフルオロヘプタン-3-オン(6.0g、21.9mmol)およびDAST(50g、313mmol)の溶液を、50℃で一晩撹拌した。反応混合物を氷(50mL)に注ぎ、DCM(3×20mL)で抽出した。合わせた有機層を水(50mL)およびブライン(50mL)で洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(80gシリカ、10~40%EtOAc/石油エーテル)により精製して、(((5,5,7,7,7-ペンタフルオロヘプチル)オキシ)メチル)ベンゼン(5.5g、18.6mmol、85%)を淡黄色の油として得た。1H NMR(400MHz,CDCl3)δ:7.39-7.25(m,5H)、4.50(s,2H)、3.49(t,J=5.9Hz,2H)、2.81-2.62(m,2H)、2.07-1.88(m,2H)、1.73-1.57(m,4H)。19F NMR(376MHz,CDCl3)δ:-61.93(t,J=8.9Hz)、-95.16(q,J=8.9Hz)。
MeOH(50mL)中の(((5,5,7,7,7-ペンタフルオロヘプチル)オキシ)メチル)ベンゼン(7.0g、23.6mmol)の溶液に、5%Pd(OH)2/C触媒(水中50重量%、3.5g)およびAcOH(0.5mL)を加え、反応混合物をH2雰囲気下で、60℃で一晩撹拌した。反応混合物をセライトを通して濾過し、濾液を減圧下、40℃で濃縮し、5,5,7,7,7-ペンタフルオロヘプタン-1-オール(4.8g、23.3mmol、98%)を淡黄色の油として得、これを次のステップで直接使用した。
ジクロロメタン(80mL)中の5,5,7,7,7-ペンタフルオロヘプタン-1-オール(4.8g、23.3mmol)の溶液に、デス・マーチンペルヨージナン(14.8g、35mmol)を加え、反応混合物を室温で30分間撹拌した。混合物を水性Na2S2O3(100mL)でクエンチし、ジクロロメタン(50mL)で希釈し、分離した。水相をジクロロメタン(2x50mL)で抽出し、合わせた有機相を水(2x60mL)およびブラインで洗浄し、MgSO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(40gシリカ、10~50%EtOAc/石油エーテル)により精製して、5,5,7,7,7-ペンタフルオロヘプタナール(3.6g、17.6mmol、75%)を淡黄色の油として得た。1H NMR(400MHz,CDCl3)δ:9.78(s,1H)、2.83-2.65(m,2H)、2.60-2.51(m,2H)、2.08-1.92(m,2H)、1.92-1.82(m,2H)。
THF中のカリウムtert-ブトキシド溶液(20重量%、15.0g、26.4mmol)を、テトラヒドロフラン(50mL)中のジエチルシアノメチルホスホネート(4.7g、26.4mmol)の溶液に0℃で滴下して加えた。反応混合物を室温に30分間温め、次に0℃に冷却し、テトラヒドロフラン(40mL)中の5,5,7,7,7-ペンタフルオロヘプタナール(3.6g、17.6mmol)の溶液を加えた。反応混合物を室温に温め、一晩撹拌した。混合物を水でクエンチし、EtOAcで抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(40gシリカ、10~40%EtOAc/石油エーテル)により精製して、7,7,9,9,9-ペンタフルオロノン-2-エンニトリル(3.5g、15.4mmol、88%)を淡黄色の油として得た。1H NMR(400MHz,CDCl3)δ:6.75-6.63(m,0.4H)、6.52-6.41(m,0.6H)、5.43-5.32(m,1H)、2.83-2.64(m,2H)、2.55-2.45(m,1H)、2.36-2.25(m,1H)、2.08-1.89(m,2H)、1.79-1.66(m,2H)。E/Z異性体の混合物。
EtOAc(30mL)中の7,7,9,9,9-ペンタフルオロノン-2-エンニトリル(3.5g、15.4mmol)および20%Pd/C(水中50重量%、700mg)の混合物を、H2の雰囲気下で、室温で一晩撹拌した。反応混合物をセライトを通して濾過し、濾液を減圧下、40℃で濃縮し、7,7,9,9,9-ペンタフルオロノナンニトリル(3.1g、13.5mmol、88%)を淡黄色の油として得た。1H NMR(400MHz,CDCl3)δ:2.82-2.64(m,2H)、2.37(t,J=7.0Hz,2H)、2.06-1.89(m,2H)、1.75-1.65(m,2H)、1.64-1.47(m,4H)。19F NMR(376MHz,CDCl3)δ:-61.97(t,J=8.9Hz)、-95.23(q,J=8.9Hz)。
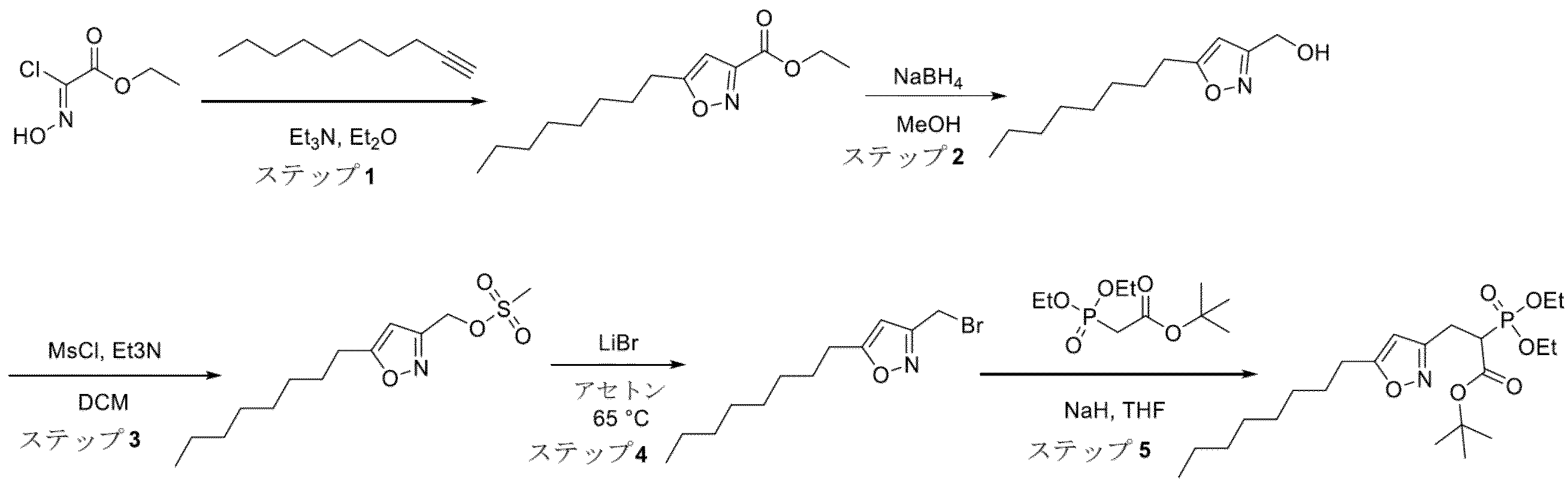
0℃でのEt2O(25mL)中のエチル2-クロロ-2-(ヒドロキシイミノ)アセテート(2.00g、13.2mmol)およびデカ-1-イン(5.48g、39.7mmol)の溶液に、トリエチルアミン(1.79mL、13.2mmol)を加え、反応混合物を0℃で30分間、次に室温で12時間撹拌した。反応物を水(40mL)でクエンチし、相を分離し、水相を酢酸エチル(2x30mL)で抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下35℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(1:50~1:10 EtOAc/石油エーテル)により精製して、エチル5-オクチルイソオキサゾール-3-カルボキシレート(3g、11.8mmol、90%)を淡黄色の油として得た。LCMS:(システム2,方法B)m/z 286.3(M+H)+(ES+)。
0℃でのMeOH(30mL)中のエチル5-オクチルイソオキサゾール-3-カルボキシレート(3g、11.8mmol)の溶液に、NaBH4(887mg、23.7mmol)を加え、混合物を室温で1時間撹拌した。混合物を水(20mL)でクエンチし、濃縮してメタノールを除去し、残留物を酢酸エチル(4x10mL)で抽出した。合わせた有機相をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下30℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(40gシリカ、0~30%MTBE/石油エーテル)により精製して、(5-オクチルイソオキサゾール-3-イル)メタノール(2g、9.47mmol、80%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 212.4(M+H)+(ES+)。
0℃でのDCM(10mL)中の(5-オクチルイソオキサゾール-3-イル)メタノール(750mg、3.6mmol)およびトリエチルアミン(1mL、7.2mmol)の溶液に、メタンスルホニルクロリド(0.41mL、5.4mmol)を加え、反応混合物を室温で1.5時間撹拌した。混合物を減圧下30℃で濃縮して、粗(5-オクチルイソオキサゾール-3-イル)メチルメタンスルホネート(878mg、3.0mmol、84%)を淡黄色の油として得、これを次のステップで直接使用した。LCMS:(システム2,方法C)m/z 290.2(M+H)+(ES+)。
アセトン(10mL)中の(5-オクチルイソオキサゾール-3-イル)メチルメタンスルホネート(878mg、3.0mmol)の溶液に、LiBr(779mg、9.0mmol)を加え、混合物を65℃で2時間撹拌した。混合物を水(20mL)でクエンチし、酢酸エチル(4x10mL)で抽出した。合わせた有機相をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(25gシリカ、0~30%MTBE/石油エーテル)により精製して、3-(ブロモメチル)-5-オクチルイソオキサゾール(600mg、2.2mmol、73%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 274.2/276.2(M+H)+(ES+)。
0℃でのTHF(15mL)中のtert-ブチル2-(ジエトキシホスホリル)アセテート(55mg、2.2mmol)の溶液に、鉱油中のNaH懸濁液(60重量%、96mg、2.4mmol)を加え、混合物を0℃で0.5時間撹拌した。次に、0℃でのTHF(5mL)中の3-(ブロモメチル)-5-オクチルイソオキサゾール(600mg、2.2mmol)の溶液を加え、反応混合物を室温で16時間撹拌した。混合物を水(20mL)でクエンチし、相を分離し、水相を酢酸エチル(4x10mL)で抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(25gシリカ、0~80%MTBE/石油エーテル)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチルイソオキサゾール-3-イル)プロパノエート(500mg、1.1mmol、50%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 446.2(M+H)+(ES+)。
EtOH(15mL)およびH2O(15mL)中の1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボニトリル(3.00g、14.2mmol)およびKOH(2.38g、42.6mmol)溶液を、100℃で16時間撹拌した。混合物を減圧下で、35℃で濃縮し、残留物をEtOAc(2×20mL)で洗浄した。希水性HCl(1M)を使用して水層をpH=4に調整し、次にEtOAc(2×20mL)で抽出した。合わせた有機抽出物をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下35℃で濃縮し、1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボン酸(3.2g、13.9mmol、94%)を黄色の油として得、これを次のステップで直接使用した。1H NMR(400MHz,DMSO-d6)δ:12.50(br,1H)、7.66(d,J=8.1Hz,2H)、7.55(d,J=8.0Hz,2H)、1.49(q,J=4.0Hz,2H)、1.20(q,J=4.0Hz,2H)。
0℃でのジメチルホルムアミド(70mL)中の1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボン酸(3.2g、13.9mmol)、N,O-ジメチルヒドロキシルアミンハイドロクロライド(4.07g、41.7mmol)、およびHATU(10.56g、27.8mmol)の溶液に、Et3N(9.83g、97.3mmol)を加えた。反応混合物を室温で2時間撹拌し、次に飽和水性NH4Cl溶液でクエンチし、EtOAc(2×100mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下35℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(20~33%EtOAc/石油エーテル)により精製して、N-メトキシ-N-メチル-1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボキサミド(3.5g、12.8mmol、92%)を無色の油として得た。LCMS:(システム2,方法C)m/z 274.2(M+H)+(ES+)。
0℃でのTHF(55mL)中のN-メトキシ-N-メチル-1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボキサミド(3.00g、11.0mmol)の混合物に、ジエチルエーテル中のメチルマグネシウムブロミド溶液(3M、5.1mL、15.3mmol)を加え、反応混合物を室温で16時間撹拌した。反応混合物を飽和水性NH4Cl溶液(50mL)でクエンチし、EtOAc(2×50mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下30℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(25gシリカ、0~10%MTBE/石油エーテル)により精製して、1-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)エタン-1-オン(2.5g、11.0mmol、99%)を無色の油として得た。LCMS:(システム2,方法C)m/z 229.3(M+Na)+(ES+)。
室温でのMeOH(50mL)中の1-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)エタン-1-オン(2.2g、9.64mmol)の溶液に、Br2(2.31g、14.46mmol)を滴下して加え、反応混合物を室温で16時間撹拌した。反応混合物を飽和水性NaHCO3を使用してpH=7に調整し、次に減圧下30℃で濃縮してMeOHを除去した。残留水性混合物をEtOAc(2×50mL)で抽出し、合わせた有機相をNa2SO4で乾燥させ、濾過し、減圧下35℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(40gシリカ、0~10%MTBE/石油エーテル)により精製して、2-ブロモ-1-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)エタン-1-オン(1.4g、4.56mmol、47%)を白色の固体として得た。1H NMR(400MHz,DMSO-d6)δ:7.72(d,J=8.0Hz,2H)、7.67(d,J=8.2Hz,2H)、4.22(s,2H)、1.65(q,J=4.1Hz,2H,1.35(q,J=4.2Hz,2H)。
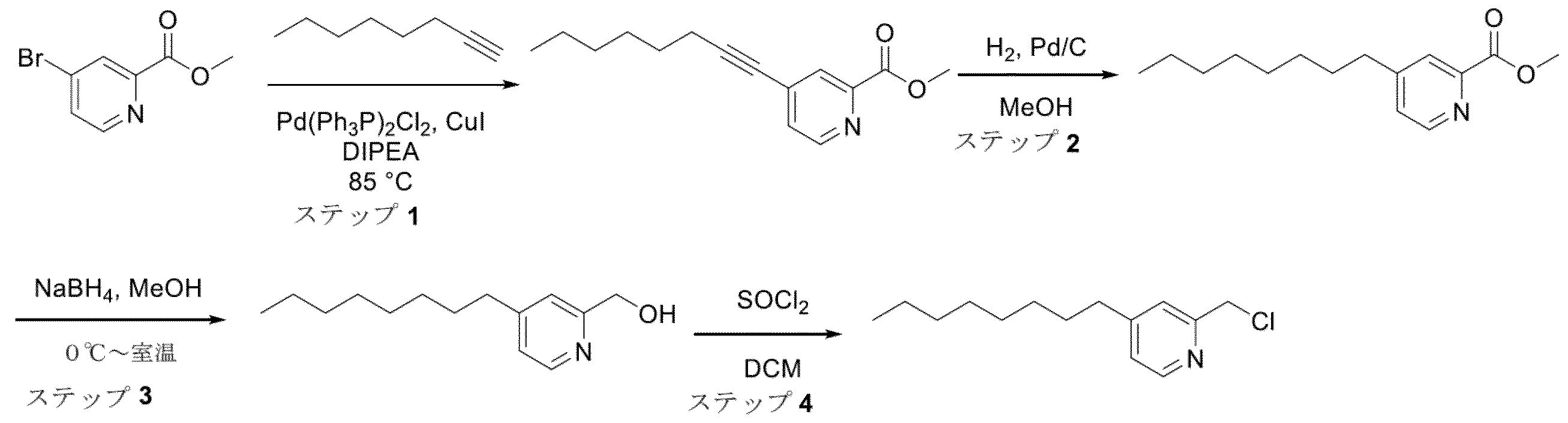
DIPEA(65mL)中のメチル4-ブロモピコリネート(2.80g、13.0mmol)、オクタ-1-イン(5.70g、51.8mmol)、Pd(PPh3)2Cl2(0.92g、1.30mmol)、およびCuI(492mg、2.60mmol)の混合物を、85℃で3時間撹拌した。混合物を室温に冷却し、濾過して、濾液を水(60mL)で希釈し、酢酸エチル(3x50mL)で抽出した。合わせた有機層を希水性HCl溶液(0.5M、3×30mL)、水(2×30mL)、およびブラインで洗浄し、Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(120gシリカ、0~30%EtOAc/石油エーテル)により精製して、メチル4-(オクタ-1-イン-1-イル)ピコリネート(2.40g、9.78mmol、75%)を暗色の油として得た。LCMS:(システム2,方法C)m/z 246.4(M+H)+(ES+)。
MeOH(20mL)中のメチル4-(オクタ-1-イン-1-イル)ピコリネート(2.40g、9.78mmol)およびPd/C触媒(10重量%、240mg)の混合物を、H2の雰囲気下で、室温で12時間撹拌した。混合物を濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~30%EtOAc/石油エーテル)により精製して、メチル4-オクチルピコリネート(2.20g、8.82mmol、90%)を褐色の油として得た。LCMS:(システム2,方法C)m/z 250.4(M+H)+(ES+)。
0℃でのMeOH(44mL)中のメチル4-オクチルピコリネート(2.20g、8.82mmol)の溶液に、NaBH4(3.35g、88.2mmol)を加え、得られた混合物を室温で12時間撹拌し、反応混合物を水(40mL)でクエンチし、減圧下40℃で濃縮して、MeOHを除去した。水性残留物を酢酸エチル(3x40mL)で抽出し、合わせた有機相をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(40gシリカ、0~30%EtOAc/石油エーテル)により精製して、(4-オクチルピリジン-2-イル)メタノール(1.20g、5.42mmol、61%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 222.4(M+H)+(ES+)。
室温でのDCM(27mL)中の(4-オクチルピリジン-2-イル)メタノール(1.20g、5.42mmol)の溶液に、SOCl2(1.90g、16.3mmol)を加え、反応混合物を室温で3時間撹拌した。次に、溶媒を減圧下30℃で除去し、残留物をH2O(10mL)で希釈し、希水性HCl(2M)を使用してpH=4に調整し、MTBE(3×10mL)で抽出した。合わせた有機層をH2O(2×2mL)およびブラインで洗浄し、Na2SO4で乾燥させ、濾過し、減圧下30℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(20gシリカ、0~30%MTBE/石油エーテル)により精製して、2-(クロロメチル)-4-オクチルピリジン(1.30g、5.42mmol、100%)を褐色の油として得た。LCMS:(システム2,方法C)m/z 240.4/242.4(M+H)+(ES+)。1H NMR(400MHz,CDCl3)δ:8.44(d,J=5.1Hz,1H)、7.28(s,1H)、7.05(dd,J=5.1,1.7Hz,1H)、4.65(s,2H)、2.62(t,J=7.8Hz,2H)、1.68-1.57(m,2H)、1.37-1.20(m,10H)、0.88(t,J=6.8Hz,3H)。
0℃でのTHF(10mL)中の3,5-ジクロロ-4-フルオロ安息香酸(9.00g、43.1mmol)の溶液に、THF中のBH3.Me2S錯体の溶液(2M、130mL、260mmol)を加え、反応混合物を室温で12時間撹拌した。反応混合物をMeOH(20mL)でクエンチし、減圧下30℃で濃縮して、残留物をMTBE(30mL)および水で希釈した。相を分離し、水相をMTBE(3x30mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~40%MTBE/石油エーテル)により精製して、(3,5-ジクロロ-4-フルオロフェニル)メタノール(8.00g、41.0mmol、95%)を無色の油として得た。1H NMR(400MHz,CDCl3)δ:7.32(d,J=6.2Hz,2H)、4.64(s,2H)。1つの交換可能なプロトンは観察されない。
0℃でのDCM(100mL)中の(3,5-ジクロロ-4-フルオロフェニル)メタノール(8.00g、41.0mmol)の溶液に、SOCl2(24.2g、205mmol)を加え、反応混合物を室温で2.5時間撹拌した。混合物を水(40mL)でクエンチし、相を分離し、水相をDCM(4x30mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~5%MTBE/石油エーテル)により精製して、1,3-ジクロロ-5-(クロロメチル)-2-フルオロベンゼン(7.60g、35.6mmol、87%)を淡黄色の油として得た。1H NMR(400MHz,CDCl3)δ:7.35(d,J=6.1Hz,2H)、4.48(s,2H)。
MeCN(80mL)中の1,3-ジクロロ-5-(クロロメチル)-2-フルオロベンゼン(7.20g、33.7mmol)、TMSCN(5.00g、50.6mmol)、K2CO3(7.00g、50.6mmol)、およびKF(2.90g、50.6mmol)の混合物を、80℃で12時間撹拌した。混合物を減圧下40℃で濃縮し、残留物をDCM(30mL)および水(20mL)で希釈し、相を分離し、水層をDCM(3×30mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~20%MTBE/石油エーテル)により精製して、2-(3,5-ジクロロ-4-フルオロフェニル)アセトニトリル(3.20g、15.7mmol、46%)を黄色の固体として得た。1H NMR(400MHz,CDCl3)δ:7.31(d,J=6.0Hz,2H)、3.71(s,2H)。
0℃でのTHF(10mL)中の2-(3,5-ジクロロ-4-フルオロフェニル)アセトニトリル(1.00g、4.90mmol)の溶液に、鉱油中の水素化ナトリウム懸濁液(60重量%、431mg、10.8mmol)を加え、混合物を0℃で30分間撹拌した。1,2-ジブロモエタン(1.00g、5.39mmol)を加え、得られた懸濁液を室温で16時間撹拌した。混合物を飽和水性NH4Cl(10mL)でクエンチし、相を分離し、水相をMTBE(3×20mL)で抽出した。合わせた有機層をH2O(2×20mL)およびブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(25gシリカ、0~20%MTBE/石油エーテル)により精製して、1-(3,5-ジクロロ-4-フルオロフェニル)シクロプロパン-1-カルボニトリル(800mg、3.48mmol、71%)を白色の固体として得た。1H NMR(400MHz,CDCl3)δ:7.25(d,J=6.2Hz,2H),1.80-1.74(m,2H)、1.43-1.36(m,2H)。
次に、室温に冷却した。混合物をEtOH(1mL)でクエンチし、次にブライン(50mL)で希釈し、EtOAc(3×50mL)で抽出した。合わせた有機層を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、4-シクロブトキシベンゾニトリル(0.74g、3.8mmol、90%純度)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.80-7.68(m,2H)、7.05-6.98(m,2H)、4.84-4.72(m,1H)、2.49-2.39(m,2H)、2.11-1.98(m,2H)、1.86-1.73(m,1H)、1.71-1.58(m,1H)。
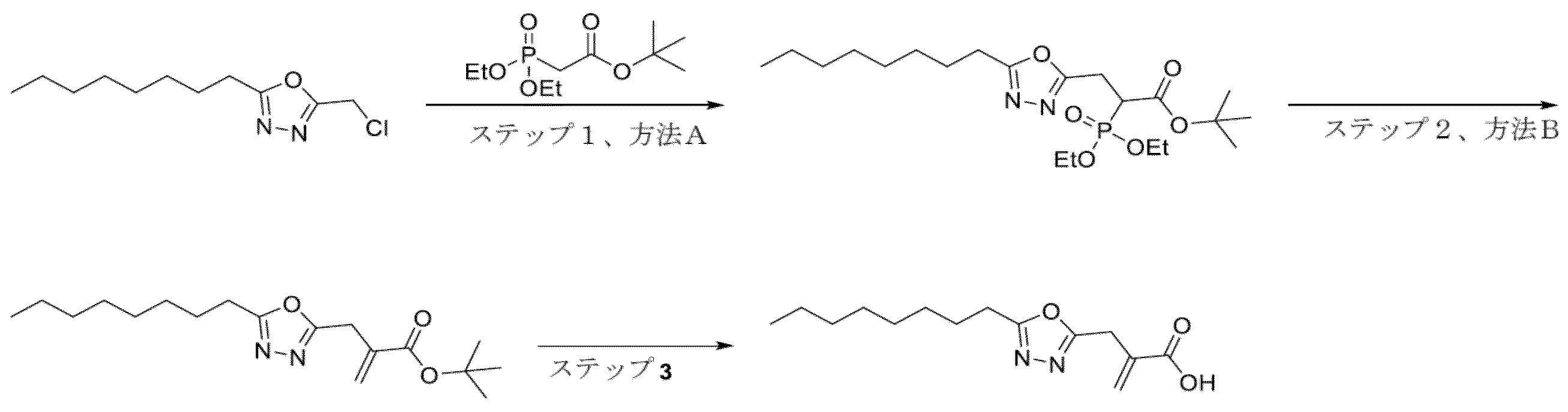
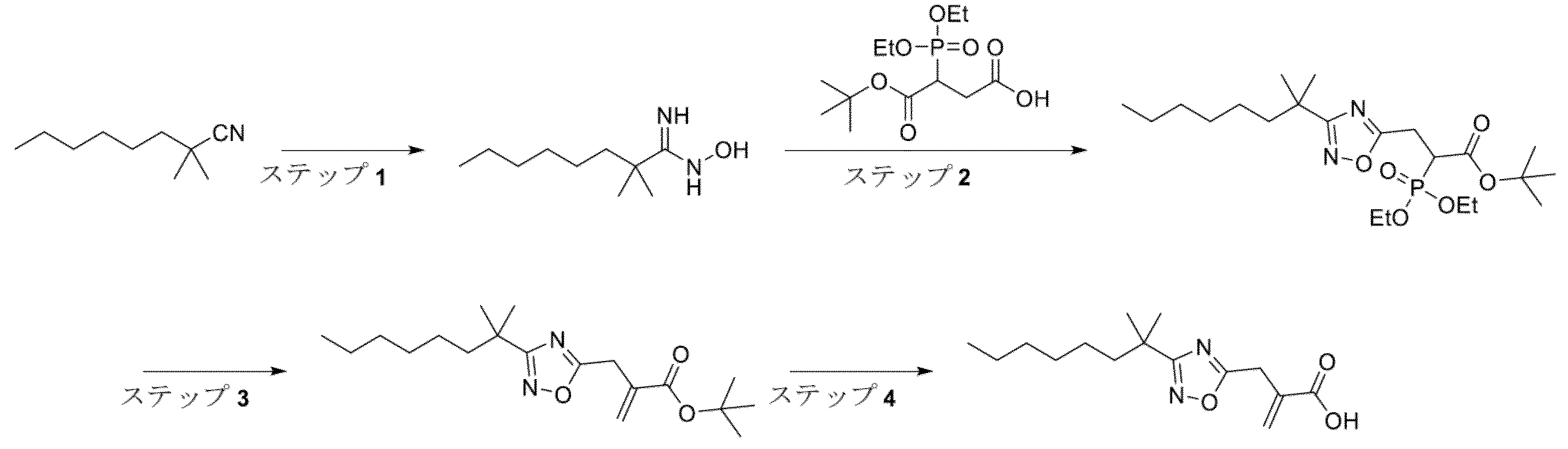
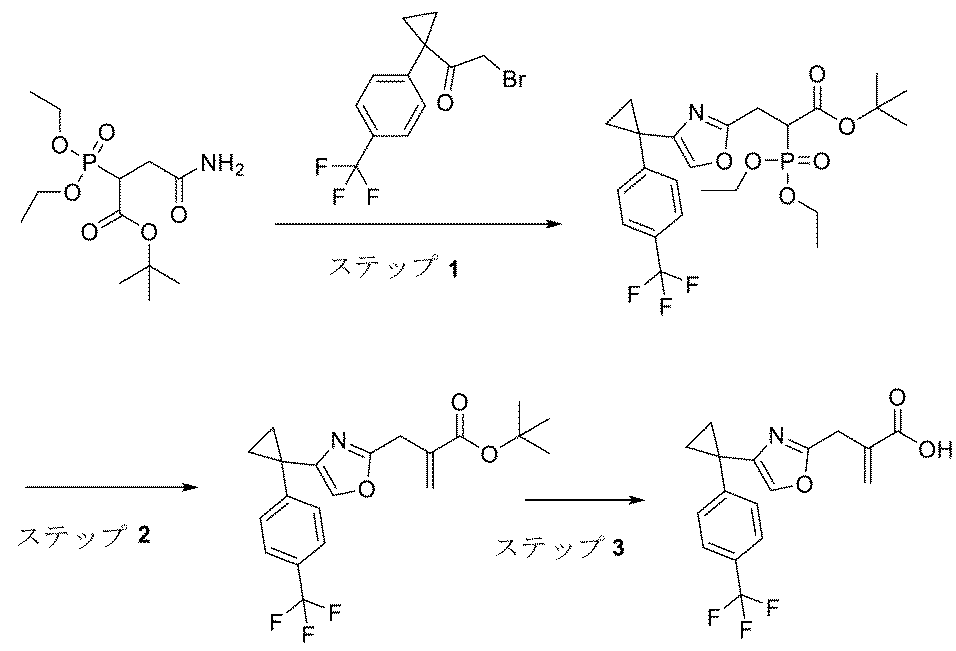
5-(クロロメチル)-3-オクチル-1,2,4-オキサジアゾール(中間体1、0.60g、2.6mmol)から、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-オクチル-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.413g、0.92mmol)を黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.15-4.04(m,4H)、3.56(ddd,J=23.4,11.1,4.4Hz,1H)、3.41-3.32(m,1H)、3.28-3.17(m,1H)、2.64(t,J=7.4Hz,2H)、1.71-1.55(m,2H)、1.37(s,9H)、1.32-1.19(m,16H)、0.90-0.82(m,3H)。LCMS m/z 469.3(M+Na)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-オクチル-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.413g、0.93mmol)から、一般的な手順A、ステップ2、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.105g、0.322mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.3Hz,1H)、5.93-5.86(m,1H)、3.91(s,2H)、2.64(t,J=7.3Hz,2H)、1.68-1.57(m,2H)、1.34(s,9H)、1.28-1.21(m,10H)、0.91-0.78(m,3H)。LCMS m/z 323.2(M+H)+(ES+)。
tert-ブチル2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.105g、0.33mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、表題化合物(0.059g、0.22mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(d,J=1.2Hz,1H)、5.94-5.83(m,1H)、3.91(s,2H)、2.64(t,J=7.5Hz,2H)、1.66-1.56(m,2H)、1.33-1.19(m,10H)、0.90-0.81(m,3H)。LCMS m/z 267.2(M+H)+(ES+)。
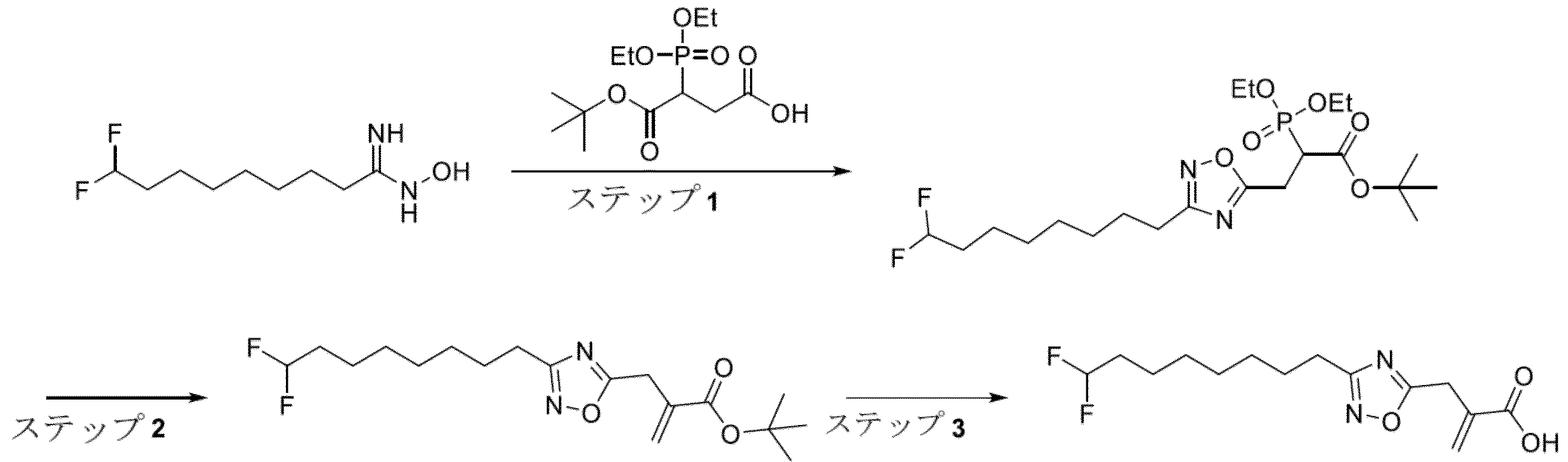
イソプロパノール(420mL)中のヒドロキシルアミンハイドロクロライド(72.9g、1.05mol)の溶液に、NaHCO3(150g、1.78mol)を一度に少しずつ加えた。混合物を室温で10分間撹拌し、次にノナンニトリル(73.0g、524mmol)を混合物に一度に少しずつ加えた。混合物を85℃に加熱し、12時間撹拌した。混合物を濾過し、濾過ケーキをイソプロパノール(2x200mL)で洗浄した。濾液を減圧下45℃で濃縮して、粗N-ヒドロキシノナニミダミド(80g、464mmol、89%)を白色の固体として得た。粗生成物をさらに精製することなく次のステップで直接使用した。1H NMR(400MHz,DMSO-d6)δ:8.65(s,1H)、5.27(s,2H)、1.92(t,J=7.2Hz,2H)、1.51-1.40(m,2H)、1.31-1.19(m,10H)、0.86(t,J=6.0Hz,3H)。
5つの反応物を並行して実施した。THF(3L)中のtert-ブチル2-(ジエトキシホスホリル)アセテート(300g、1.19mol)の溶液に、鉱油中のNaH懸濁液(60重量%、50.4g、1.26mol)を0℃で少しずつ加えた。混合物を0℃で0.5時間撹拌し、次にエチルブロモアセテート(179g、1.07mol)を、内部温度が10℃を下回るように保つような速度で混合物に滴下して加えた。混合物を10℃で1時間撹拌し、次に0~10℃で一度に少しずつ水性NH4Cl溶液(2L)に注いだ。反応の5つのバッチを合わせ、合わせた混合物を酢酸エチル(3×2L)で抽出した。合わせた有機層をブライン(500mL)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下45℃で濃縮し、1-(tert-ブチル)4-エチル2-(ジエトキシホスホリル)スクシナート(1.80kg、5.32mol、89%粗製)を無色の油として得た。粗生成物をさらに精製することなく次のステップで直接使用した。1H NMR(400MHz,DMSO-d6)δ:4.12-3.98(m,6H)、3.34-3.21(m,1H)、2.84-2.71(m,1H)、2.68-2.57(m,1H)、1.40(s,9H)、1.29-1.14(m,9H)。
4つの反応物を並行して実施した。テトラヒドロフラン(1.48L)中の1-(tert-ブチル)4-エチル2-(ジエトキシホスホリル)スクシナート(300g、887mmol)の溶液に、水性NaOH溶液(1M、1.21L、1.21mmol)を一度に少しずつ加えた。混合物を室温で12時間撹拌した。4つの反応物を後処理のために組み合わせた。反応混合物を減圧下45℃で濃縮してテトラヒドロフランを除去し、残留物を酢酸エチル(2×500mL)で抽出した。水相のpHを濃水性HCl(12M)で1に調整し、水相を酢酸エチル(3×2L)で抽出した。合わせた有機層をブライン(5L)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下45℃で濃縮した。粗生成物をイソプロピルエーテル(1.1L)で粉砕し、室温で30分間撹拌した。懸濁液を濾過し、フィルタケーキをイソプロピルエーテル(2x300mL)で洗浄し、真空下で乾燥させ、4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(840g、2.70mmol、76%)を白色の固体として得た。1H NMR(400MHz,CDCl3)δ:10.04(br.s,1H)、4.22-4.08(m,4H)、3.43-3.29(m,1H)、3.08-2.94(m,1H)、2.85-2.73(m,1H)、1.45(s,9H)、1.37-1.27(m,6H)。
THF(600mL)中の4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(100g、322mmol)の溶液に、4-メチルモルホリン(32.6g、322mmol)を室温で一度に少しずつ加えた。混合物を-15℃に冷却し、クロロギ酸エチル(35.0g、322mmol)を、内部温度を-15~-10℃に保つような速度で混合物に滴下して加えた。混合物を-15~-10℃で2時間撹拌し、次にN-ヒドロキシノナニミダミド(55.5g、322mmol)およびトリエチルアミン(54.5g、538mmol)を-15~-10℃で滴下して加えた。混合物を室温で12時間撹拌し、次に室温で希水性HCl(1M、500mL)を加えることによりクエンチした。混合物を酢酸エチル(3×500mL)で抽出し、合わせた有機層をブライン(500mL)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下45℃で濃縮して、褐色の油を得た。粗生成物をシリカでのフラッシュカラムクロマトグラフィー(5~100%酢酸エチル/n-ヘプタン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-4-((1-(ヒドロキシアミノ)ノニリデン)アミノ)-4-オキソブタノエート(140g、301mmol、94%)を黄色の油として得た。LCMS m/z 465.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:6.35(s,1H)、4.12-3.98(m,4H)、3.45-3.33(m,1H)、2.97-2.83(m,1H)、2.79-2.66(m,1H)、2.06-1.95(m,2H)、1.57-1.44(m,2H)、1.39(s,9H)、1.31-1.19(m,16H)、0.89-0.81(m,3H)。1つの交換可能なプロトンは観察されない。
THF(840mL)中のtert-ブチル2-(ジエトキシホスホリル)-4-((1-(ヒドロキシアミノ)ノニリデン)アミノ)-4-オキソブタノエート(140g、301mmol)の溶液に、Cs2CO3(196g、603mmol)を室温で一度に少しずつ加えた。混合物を70℃で3時間撹拌し、次に室温で水(1L)を加えることによりクエンチした。混合物を酢酸エチル(3×1L)で抽出し、合わせた有機層をブライン(500mL)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下45℃で濃縮して、褐色の油を得た。粗生成物をシリカでのフラッシュカラムクロマトグラフィー(5~100%酢酸エチル/n-ヘプタン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-オクチル-1,2,4-オキサジアゾール-5-イル)プロパノエート(109g、244mmol、81%)を黄色の油として得た。LCMS m/z 469.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:4.14-4.04(m,4H)、3.60-3.48(m,1H)、3.39-3.28(m,1H)、3.27-3.17(m,1H)、2.62(t,J=7.6Hz,2H)、1.66-1.55(m,2H)、1.36(s,9H)、1.29-1.20(m,16H)、0.87-0.82(m,3H)。
THF(600mL)中のtert-ブチル2-(ジエトキシホスホリル)-3-(3-オクチル-1,2,4-オキサジアゾール-5-イル)プロパノエート(100g、192mmol)の溶液に、K2CO3(79.9g、578mmol)およびパラホルムアルデヒド(3.30g、193mmol)を室温で一度に少しずつ加えた。混合物を65℃で12時間撹拌し、次に混合物を減圧下45℃で濃縮して、粗生成物を得た。粗生成物をシリカでのフラッシュカラムクロマトグラフィー(5~100%酢酸エチル/n-ヘプタン)により精製して、tert-ブチル2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(48g、149mmol、61%)を黄色の油として得た。LCMS m/z 323.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:6.22(s,1H)、5.89(d,J=1.2Hz,1H)、3.90(s,2H)、2.63(t,J=7.2Hz,2H)、1.67-1.55(m,2H)、1.34(s,9H)、1.31-1.18(m,10H)、0.85(t,J=7.2Hz,3H)。
DCM(160mL)中のtert-ブチル2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(48g、149mmol)の溶液に、TFA(170g、1.49mol)を少しずつ加えた。混合物を室温で12時間撹拌し、次に減圧下45℃で濃縮した。残留物を分取HPLC(カラム:Phenomenex Luna C18 10μm 100x250mm;溶媒系:MeCN/(0.1%TFA/水)勾配:40~70%MeCN)により精製して、生成物を得、真空下、室温で凍結乾燥した。依然としていくらかのMeCNを含む生成物をMTBE(100mL)と3回共蒸発させ、次に減圧下45℃で3時間濃縮し、2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(28g、105mmol、69%)を黄色の油として得た。LCMS m/z 267.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.8(s,1H)、6.27(s,1H)、5.90(d,J=0.8Hz,1H)、3.90(s,2H)、2.67-2.60(m,2H)、1.66-1.56(m,2H)、1.32-1.18(m,10H)、0.85(t,J=6.8Hz,3H)。
実施例1(38.4mg、1モル当量)をバイアルに負荷し、ACN(400μL)中に溶解した。トロメタミン(17.5mg、0.99モル当量)を溶液に負荷し、300rpmで2時間周囲温度で撹拌した。得られた溶液を窒素流動下で蒸発させて、固体を得た。これは、XRPD、DSC、TGA、および1H NMRによって分析した。m.p.122℃.1H NMR(400MHz,DMSO-d6)δ 5.88(s,1H)、5.23(s,1H)、3.73(s,2H)、3.45(s,6H)、2.59(t,J=7.4Hz,2H)、1.63-1.53(m,2H)、1.27-1.12(m,10H)、0.80(t,J=6.6Hz,3H)。6つの交換可能なプロトンは観察されない。
2-(クロロメチル)-5-オクチル-1,3,4-オキサジアゾール(中間体2、0.86g、3.7mmol)から、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,3,4-オキサジアゾール-2-イル)プロパノエート(1.23g、1.1mmol、40%純度)を黄色の油として得た。LCMS m/z 469.3(M+Na)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,3,4-オキサジアゾール-2-イル)プロパノエート(1.23g、1.1mmol、40%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((5-オクチル-1,3,4-オキサジアゾール-2-イル)メチル)アクリレート(0.197g、0.60mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 6.20(d,J=1.1Hz,1H)、5.87-5.79(m,1H)、3.86-3.76(m,2H)、2.80(t,J=7.4Hz,2H)、1.70-1.57(m,2H)、1.38(s,9H)、1.34-1.20(m,10H)、0.93-0.80(m,3H)。LCMS m/z 323.2(M+H)+(ES+)。
tert-ブチル2-((5-オクチル-1,3,4-オキサジアゾール-2-イル)メチル)アクリレート(0.197g、0.60mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、表題化合物(0.132g、0.49mmol)を白色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 12.78(s,1H)、6.25(d,J=1.1Hz,1H)、5.86-5.80(m,1H)、3.83(s,2H)、2.80(t,J=7.5Hz,2H)、1.71-1.60(m,2H)、1.34-1.23(m,10H)、0.90-0.83(m,3H)。LCMS m/z 267.1(M+H)+(ES+)。
3-(クロロメチル)-5-オクチル-1,2,4-オキサジアゾール(中間体3、3.18g、13.8mmol)から、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,2,4-オキサジアゾール-3-イル)プロパノエート(3.70g、7.3mmol、88%純度)を黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.14-4.03(m,4H)、3.42-3.33(m,1H)、3.24-3.12(m,1H)、3.07-2.98(m,1H)、2.89(t,J=7.4Hz,2H)、1.73-1.65(m,2H)、1.36(s,9H)、1.29-1.22(m,16H)、0.89-0.83(m,3H)。LCMS m/z 469.3(M+Na)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,2,4-オキサジアゾール-3-イル)プロパノエート(3.70g、7.3mmol、88%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((5-オクチル-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(1.75g、5.4mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 6.16(d,J=1.3Hz,1H)、5.78-5.70(m,1H)、3.68(s,2H)、2.88(t,J=7.4Hz,2H)、1.74-1.64(m,2H)、1.38(s,9H)、1.34-1.19(m,10H)、0.89-0.81(m,3H)。LCMS m/z 267.2(M-tBu+H)+(ES+)。
tert-ブチル2-((5-オクチル-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(1.65g、5.12mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、表題化合物(1.32g、4.9mmol)を淡黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 12.57(s,1H)、6.22(d,J=1.3Hz,1H)、5.75(d,J=1.5Hz,1H)、3.68(s,2H)、2.88(t,J=7.5Hz,2H)、1.78-1.59(m,2H)、1.37-1.18(m,10H)、0.93-0.78(m,3H)。LCMS m/z 267.1(M+H)+(ES+)。
3-(4-クロロベンジル)-5-(クロロメチル)-1,2,4-オキサジアゾール(中間体5、5.65g、23.2mmol)から、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(7.27g、9.0mmol、57%純度)を黄色の油として得た。LCMS m/z 481.2/483.3(M+Na)+(ES+)。
tert-ブチル3-(3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(7.27g、9.0mmol、57%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.468g、1.40mmol)を無色の油として得た。LCMS m/z 279.1/281.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.42-7.35(m,2H)、7.35-7.26(m,2H)、6.21(d,J=1.2Hz,1H)、5.94-5.84(m,1H)、4.06(s,2H)、3.91(s,2H)、1.25(s,9H)。
tert-ブチル2-((3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.468g、1.40mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.265g、0.94mmol)を無色のガムとして得た。LCMS m/z 279.5/281.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、7.44-7.35(m,2H)、7.35-7.28(m,2H)、6.27(d,J=1.2Hz,1H)、5.95-5.87(m,1H)、4.08(s,2H)、3.91(s,2H)。
反応物を室温を上回るように加熱しなかったことを除いて、5-(クロロメチル)-3-(4-クロロフェネチル)-1,2,4-オキサジアゾール(中間体6、2.11g、8.21mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,3,4-オキサジアゾール-2-イル)プロパノエート(1.87g、1.7mmol、44%純度)を黄色の油として得た。LCMS m/z 495.1/497.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.35-7.20(m,4H)、4.15-4.01(m,4H)、3.64-3.49(m,1H)、3.41-3.32(m,1H)、3.29-3.19(m,1H)、2.98-2.96(m,4H)、1.37(s,9H)、1.27-1.22(m,6H)。
tert-ブチル3-(3-(4-クロロフェネチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.87g、1.7mmol、44%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-ペンチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.413g、1.2mmol)を黄色の油として得た。LCMS m/z 293.1/295.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.36-7.29(m,2H)、7.29-7.22(m,2H)、6.24(d,J=1.2Hz,1H)、5.92-5.85(m,1H)、3.92(s,2H)、2.97(s,4H)、1.34(s,9H)。
tert-ブチル2-((3-(4-クロロフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.41g、1.40mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-(4-クロロフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.275g、0.93mmol)を無色のガムとして得た。LCMS m/z 293.1/295.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,1H)、7.37-7.28(m,2H)、7.27-7.19(m,2H)、6.29(d,J=1.3Hz,1H)、5.97-5.86(m,1H)、3.92(s,2H)、2.97(m,4H)。
5-(クロロメチル)-3-ヘプチル-1,2,4-オキサジアゾール(中間体4、7.00g、31mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~70%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-ヘプチル-1,2,4-オキサジアゾール-5-イル)プロパノエート(5.84g、13mmol)を無色の油として得た。LCMS m/z 455.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.05(m,4H)、3.56(ddd,J=23.3,11.1,4.4Hz,1H)、3.40-3.29(m,1H)、3.23(ddd,J=16.8,8.6,4.3Hz,1H)、2.64(t,J=7.3Hz,2H)、1.68-1.56(m,2H)、1.37(s,9H)、1.31-1.20(m,14H)、0.90-0.83(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-ヘプチル-1,2,4-オキサジアゾール-5-イル)プロパノエート(5.84g、13.5mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-ヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(3.42g、11mmol)を無色の油として得た。LCMS m/z 253.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、3.91(s,2H)、2.64(t,J=7.4Hz,2H)、1.62(s,2H)、1.34(s,9H)、1.30-1.21(m,8H)、0.89-0.82(m,3H)。
tert-ブチル2-((3-ヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.00g、3.24mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-ヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.746g、2.9mmol)を無色のガムとして得た。LCMS m/z 253.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.79(br.s,1H)、6.28(d,J=1.2Hz,1H)、5.92(d,J=1.2Hz,1H)、3.91(s,2H)、2.65(t,J=7.5Hz,2H)、1.71-1.54(m,2H)、1.35-1.19(m,8H)、0.95-0.78(m,3H)。
5-(クロロメチル)-3-(4-クロロフェニル)-1,2,4-オキサジアゾール(中間体7、4.00g、17mmol)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%MeCN/水0.1%ギ酸)により精製して、tert-ブチル3-(3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(3.06g、6.2mmol、90%純度)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 8.03-7.95(m,2H)、7.71-7.62(m,2H)、4.17-4.05(m,4H)、3.75-3.61(m,1H)、3.53-3.34(m,2H)、1.38(s,9H)、1.27(q,J=6.8Hz,6H)。LCMS m/z 445.1(M+H)+(ES+)。
tert-ブチル3-(3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(3.06g、6.2mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をRP Flash C18(5~75%MeCN/水0.1%ギ酸)でのクロマトグラフィー、次にシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.89mmol)を透透明な無色の油として得た。LCMS m/z 265.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.04-7.94(m,2H)、7.69-7.60(m,2H)、6.29(d,J=1.2Hz,1H)、6.03-5.95(m,1H)、4.05(s,2H)、1.34(s,9H)。
tert-ブチル2-((3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.89mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をRP Flash C18(5~75%MeCN/水0.1%ギ酸)でのクロマトグラフィーにより精製して、2-((3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.232g、0.83mmol)を白色の固体として得た。LCMS m/z 265.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.88(s,br.1H)、8.07-7.91(m,2H)、7.70-7.56(m,2H)、6.33(d,J=1.2Hz,1H)、6.07-5.90(m,1H)、4.04(s,2H)。
5-(クロロメチル)-3-(オクタン-2-イル)-1,2,4-オキサジアゾール(中間体8、1.16g、4.78mmol)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.62g、1.2mmol、90%純度)を無色の油として得た。LCMS m/z 469.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.14-4.03(m,4H)、3.63-3.47(m,1H)、3.40-3.32(m,1H)、3.28-3.16(m,1H)、2.94-2.82(m,1H)、1.68-1.44(m,2H)、1.37(s,9H)、1.32-1.08(m,17H)、0.84(t,J=6.8Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.62g、1.2mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.36g、1.1mmol)を無色の油として得た。LCMS m/z 267.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.25-6.21(m,1H)、5.92-5.88(m,1H)、3.92(s,2H)、2.97-2.81(m,1H)、1.69-1.45(m,2H)、1.34(s,9H)、1.29-1.09(m,11H)、0.90-0.80(m,3H)。
tert-ブチル2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.38g、1.1mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.32g、1.1mmol)を無色の油として得た。LCMS m/z 267.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,br.1H)、6.30-6.26(m,1H)、5.92-5.88(m,1H)、3.91(s,2H)、3.02-2.81(m,1H)、1.69-1.57(m,1H)、1.57-1.46(m,1H)、1.33-1.06(m,11H)、0.91-0.79(m,3H)。
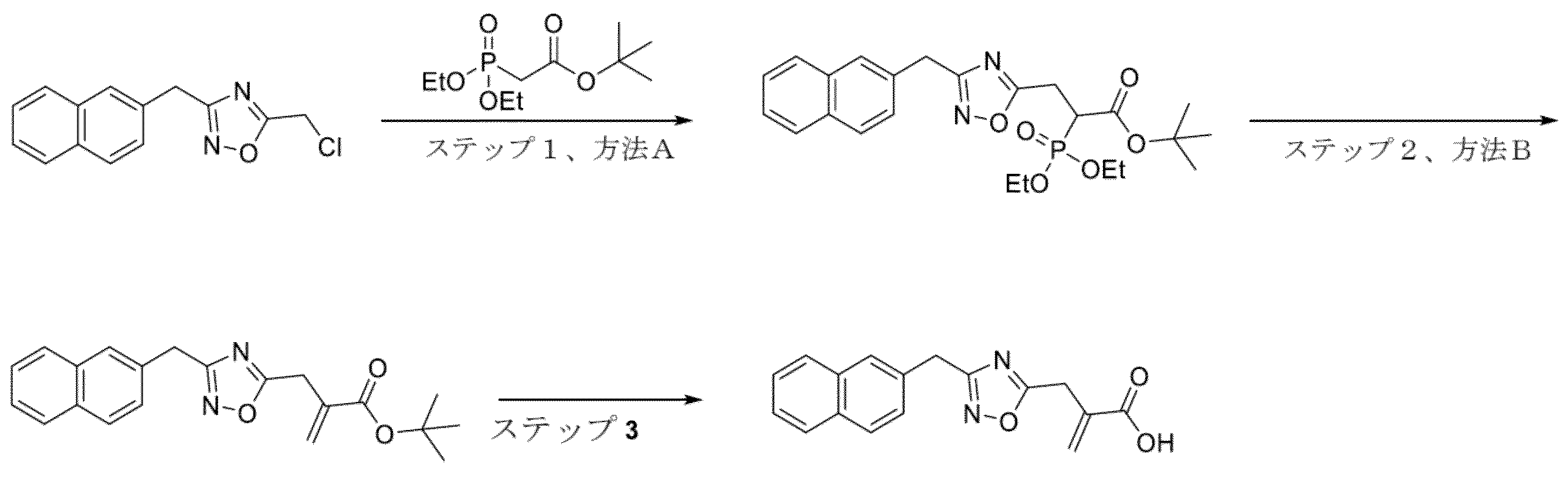
5-(クロロメチル)-3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール(中間体9、1.00g、3.7mmol)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.01g、1.8mmol、84%純度)をオレンジ色の油として得た。LCMS m/z 497.3(M+Na)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.01g、1.8mmol、84%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.85mmol)を淡黄色の油として得た。LCMS m/z 295.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.92-7.83(m,3H)、7.81(d,J=1.7Hz,1H)、7.54-7.45(m,2H)、7.42(dd,J=8.5,1.8Hz,1H)、6.20(d,J=1.3Hz,1H)、5.88(t,J=1.2Hz,1H)、4.22(s,2H)、3.91(s,2H)、1.20(s,9H)。
tert-ブチル2-((3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.85mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(180mg、0.58mmol)を白色の固体として得た。LCMS m/z 295.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.93-7.84(m,3H)、7.80(d,J=1.7Hz,1H)、7.54-7.46(m,2H)、7.43(dd,J=8.5,1.8Hz,1H)、6.26(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、4.23(s,2H)、3.91(s,2H)。
Tert-ブチル2-(ジエトキシホスホリル)アセテート(1.92mL、8.17mmol)を、DME(20mL)中の5-(クロロメチル)-3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール(中間体10、2.00g、7.43mmol)および炭酸セシウム(2.66g、8.17mmol)の懸濁液に室温で加えた。反応物を80℃に加熱し、18時間撹拌した。ヨウ化カリウム(123mg、0.74mmolを加え、80℃で1時間撹拌を続けた。混合物を室温に冷却し、水(50mL)に注ぎ、EtOAc(3x25mL)で抽出した。合わせた有機層をブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~60%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.12g、1.6mmol、71%純度)を黄色の油として得た。LCMS m/z 507.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.40(s,4H)、4.15-3.99(m,4H)、3.52(ddd,J=23.3,10.9,4.4Hz,1H)、3.37-3.28(m,1H)、3.20(ddd,J=16.8,8.8,4.4Hz,1H)、1.56-1.37(m,4H)、1.36(s,9H)、1.25(q,J=6.8Hz,6H)。
tert-ブチル3-(3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.12g、1.6mmol、71%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(396mg、1.1mmol)を無色の油として得た。LCMS m/z 305.1/307.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.40(s,4H)、6.21(d,J=1.2Hz,1H)、5.88(d,J=1.3Hz,1H)、3.89(s,2H)、1.50-1.41(m,2H)、1.41-1.34(m,2H)、1.33(s,9H)。
tert-ブチル2-((3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.394g、1.1mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~60%EtOAc/イソヘキサン)により精製して、2-((3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(206mg、0.67mmol)を無色のガムとして得た。LCMS m/z 305.1/307.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.60-7.27(m,4H)、6.27(d,J=1.2Hz,1H)、5.90(d,J=1.2Hz,1H)、3.89(s,2H)、1.51-1.34(m,4H)。
反応物を室温を上回るように加熱しなかったことを除いて、5-(クロロメチル)-3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール(中間体11、4.30g、15.1mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~60%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(4.30g、1.7mmol、44%純度)を黄色の油として得た。LCMS m/z 523.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.21-3.90(m,4H)、3.69-3.48(m,1H)、3.39-3.30(m,1H)、3.23(ddd,J=16.8,8.7,4.4Hz,1H)、2.69-2.60(m,2H)、2.29-2.13(m,2H)、1.68-1.55(m,2H)、1.50-1.42(m,2H)、1.41-1.14(m,21H)
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(4.30g、8.59mmol)から、一般的な手順A、ステップ2、方法Bに従って調製し、粗生成物をシリカゲルでのクロマトグラフィー(0~30%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.84g、4.6mmol)を透明な無色の油として得た。LCMS m/z 321.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.92-5.86(m,1H)、3.91(s,2H)、2.65(t,J=7.4Hz,2H)、2.29-2.12(m,2H)、1.69-1.57(m,2H)、1.49-1.41(m,2H)、1.36-1.28(m,15H)。
tert-ブチル2-((3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.84g、4.89mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%EtOAc/イソヘキサン)により精製して、2-((3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(1.39g、4.33mmol)を透明な無色の油として得た。LCMS m/z 321.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、6.30-6.25(m,1H)、5.94-5.87(m,1H)、3.91(s,2H)、2.65(t,J=7.5Hz,2H)、2.30-2.15(m,2H)、1.68-1.56(m,2H)、1.51-1.40(m,2H)、1.37-1.25(m,6H)。19F NMR(376MHz,DMSO-d6)δ-64.76。
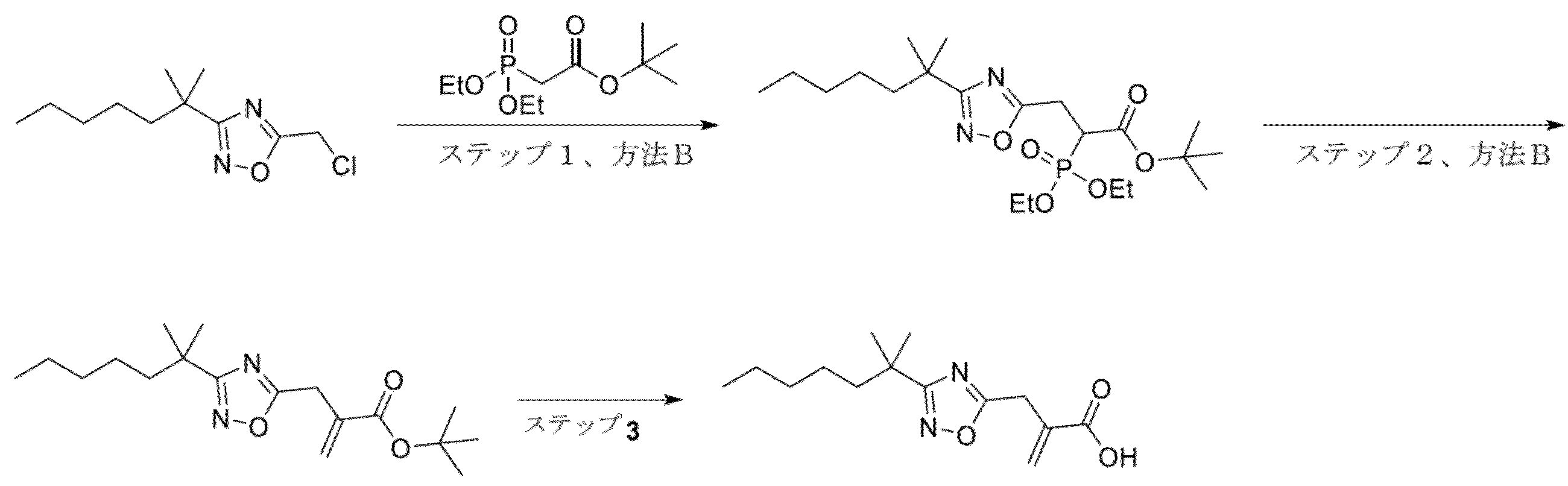
ヨウ化ナトリウムを使用せず、反応物を室温を上回るように加熱しなかったことを除いて、5-(クロロメチル)-3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール(0.60g、2.5mmol)から、一般的な手順A、ステップ1、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.55g、1.1mmol、90%純度)を黄色の油として得た。LCMS m/z 447.4(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.03(m,4H)、3.54(ddd,J=23.3,11.1,4.3Hz,1H)、3.40-3.32(m,1H)、3.31-3.17(m,1H)、1.60-1.52(m,2H)、1.37(s,10H)、1.31-1.12(m,16H)、1.08(ddd,J=13.8,7.5,5.3Hz,1H)、0.82(t,J=7.0Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.55g、1.1mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.93mmol)を無色の油として得た。LCMS m/z 267.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.22(d,J=1.3Hz,1H)、5.89(q,J=1.3Hz,1H)、3.90(s,2H)、1.60-1.52(m,2H)、1.34(s,9H)、1.27-1.12(m,10H)、1.11-1.01(m,2H)、0.81(t,J=7.0Hz,3H)。
tert-ブチル2-((3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.93mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.16g、0.57mmol)を白色のワックス状の固体として得た。LCMS m/z 267.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.78(s,1H)、6.27(d,J=1.2Hz,1H)、5.88(q,J=1.3Hz,1H)、3.90(s,2H)、1.61-1.50(m,2H)、1.28-1.11(m,10H)、1.11-1.00(m,2H)、0.81(t,J=7.0Hz,3H)。
3-(クロロメチル)-1-オクチル-1H-1,2,4-トリアゾール(2.40g、10.4mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(1-オクチル-1H-1,2,4-トリアゾール-3-イル)プロパノエート(3.72g、5.4mmol、65%純度)をオレンジ色の油として得た。LCMS m/z 466.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.36(s,1H)、4.10-4.03(m,6H)、3.39-3.29(m,1H)、3.13(ddd,J=15.5,11.8,7.1Hz,1H)、2.92(ddd,J=15.5,9.6,3.3Hz,1H)、1.74-1.69(m,2H)、1.33(s,9H)、1.27-1.21(m,16H)、0.86-0.83(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(1-オクチル-1H-1,2,4-トリアゾール-3-イル)プロパノエート(3.72g、5.4mmol、65%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((1-オクチル-1H-1,2,4-トリアゾール-3-イル)メチル)アクリレート(1.60g、4.98mmol)を無色の油として得た。LCMS m/z 344.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.36(s,1H)、6.05(d,J=1.6Hz,1H)、5.61-5.49(m,1H)、4.07(t,J=6.9Hz,2H)、3.57(s,2H)、1.80-1.63(m,2H)、1.37(s,9H)、1.30-1.14(m,10H)、0.88-0.82(m,3H)。
tert-ブチル2-((1-オクチル-1H-1,2,4-トリアゾール-3-イル)メチル)アクリレート(1.60g、4.98mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((1-オクチル-1H-1,2,4-トリアゾール-3-イル)メチル)アクリル酸(1.17g、4.40mmol)を無色の油として得た。LCMS m/z 266.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.48(s,1H)、8.37(s,1H)、6.12(d,J=1.6Hz,1H)、5.53(q,J=1.6Hz,1H)、4.08(t,J=7.0Hz,2H)、3.57(s,2H)、1.73(p,J=7.1Hz,2H)、1.31-1.15(m,10H)、0.85(t,J=6.8Hz,3H)。
5-(クロロメチル)-3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール(5.00g、18.0mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~60%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(2.74g、3.1mmol、55%純度)をオレンジ色の油として得た。LCMS m/z 437.1/439.1(M-tBu+H)+(ES+)。
tert-ブチル3-(3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(2.74g、3.1mmol、55%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.39g、0.80mmol、76%純度)を無色の油として得た。LCMS m/z 315.6(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.62-7.54(m,2H)、7.29(dd,J=8.2,2.1Hz,1H)、6.21(s,1H)、5.89(s,1H)、4.10(s,2H)、3.91(s,2H)、1.23(s,9H)。
tert-ブチル2-((3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.39g、0.80mmol、76%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(239.91mg、0.76mmol)を無色の油として得た。LCMS m/z 314.8(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,1H)、7.65-7.54(m,2H)、7.29(dd,J=8.3,2.1Hz,1H)、6.28(s,1H)、5.92(s,1H)、4.12(s,2H)、3.92(s,2H)。
3-(4-(tert-ブチル)ベンジル)-5-(クロロメチル)-1,2,4-オキサジアゾール(2.33g、6.51mmol、74%純度)から、一般的な手順A、ステップ1、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.0g、2.0mmol)をオレンジ色の油として得た。LCMS m/z 503.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.35-7.29(m,2H)、7.22-7.15(m,2H)、4.12-4.01(m,5H)、3.98(d,J=1.6Hz,2H)、3.54(ddd,J=23.4,10.9,4.5Hz,1H)、3.22(ddd,J=16.8,8.7,4.5Hz,1H)、1.30-1.20(m,24H)。
tert-ブチル3-(3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.0g、2.1mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.58mmol、69%純度)を淡黄色の油として得た。LCMS m/z 300.8(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.33-7.30(m,2H)、7.21-7.17(m,2H)、6.21(d,J=1.2Hz,1H)、5.88(q,J=1.3Hz,1H)、3.98(s,2H)、3.90(d,J=1.0Hz,2H)、1.25(s,9H)、1.24(s,9H)。
tert-ブチル2-((3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.30g、0.58mmol、69%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(Waters X-Select Prep-C18、5μm、30x100mmカラム、水中40~70%MeCN 0.1%ギ酸)により精製して、2-((3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(100mg、0.33mmol)を粘着性の黄色の油として得た。LCMS m/z 300.8(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.40-7.28(m,2H)、7.25-7.14(m,2H)、6.26(d,J=1.2Hz,1H)、5.90(d,J=1.4Hz,1H)、4.00(s,2H)、3.90(d,J=1.0Hz,2H)、1.26(s,9H)。
ヨウ化ナトリウムを使用していないことを除いて、5-(クロロメチル)-3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール(4.18g、9.2mmol、61%純度)から、一般的な手順A、ステップ1、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.0g、2.0mmol)をオレンジ色の油として得た。LCMS m/z 503.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.35-7.29(m,2H)、7.22-7.15(m,2H)、4.12-4.01(m,5H)、3.98(d,J=1.6Hz,2H)、3.54(ddd,J=23.4,10.9,4.5Hz,1H)、3.22(ddd,J=16.8,8.7,4.5Hz,1H)、1.30-1.20(m,24H)。
tert-ブチル3-(3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.0g、2.0mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.61g、1.6mmol)を無色の油として得た。LCMS m/z 313.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.52(t,J=2.0Hz,1H)、7.38(d,J=2.0Hz,2H)、6.22(d,J=1.2Hz,1H)、5.90(q,J=1.3Hz,1H)、4.13(s,2H)、3.93(d,J=1.1Hz,2H)、1.25(s,9H)。
tert-ブチル2-((3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(610mg、1.57mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(230mg、0.71mmol)を淡黄色の油として得た。LCMS m/z 313.5/315.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.52(t,J=1.9Hz,1H)、7.39(d,J=1.9Hz,2H)、6.28(d,J=1.2Hz,1H)、5.93(q,J=1.2Hz,1H)、4.14(s,2H)、3.93(d,J=1.2Hz,2H)。
反応物を60℃に加熱したことを除いて、5-(クロロメチル)-3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール(2.74g、8.53mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.754g、1.3mmol、90%純度)を無色の油として得た。LCMS m/z 558.9(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.17-3.95(m,4H)、3.55(ddd,J=23.3,11.0,4.4Hz,1H)、3.42-3.28(m,2H)、3.22(ddd,J=16.8,8.6,4.4Hz,1H)、2.65(t,J=7.4Hz,2H)、2.15(tq,J=16.2,7.8Hz,2H)、1.68-1.55(m,2H)、1.48(p,J=7.6,6.8Hz,14H)、1.29-1.19(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.754g、1.3mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.326g、0.78mmol)を無色の油として得た。LCMS m/z 357.6(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(s,1H)、5.90(s,1H)、3.91(s,2H)、2.66(t,J=7.4Hz,2H)、2.27-2.07(m,2H)、1.63(p,J=7.4Hz,2H)、1.55-1.43(m,3H)、1.43-1.27(m,12H)。
tert-ブチル2-((3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.326g、0.78mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.188g、0.52mmol)を無色の油として得た。LCMS m/z 357.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(s,1H)、5.91(s,1H)、3.91(s,2H)、2.66(t,J=7.5Hz,2H)、2.17(tt,J=19.3,7.8Hz,2H)、1.64(p,J=7.4Hz,2H)、1.56-1.44(m,2H)、1.44-1.27(m,4H)。
ヨウ化ナトリウムを使用していないことを除いて、3-(4-ブチルフェニル)-5-(クロロメチル)-1,2,4-オキサジアゾール(2.80g、7.37mmol、66%純度)から、一般的な手順A、ステップ1、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.72g、3.5mmol)を黄色の油として得た。LCMS m/z 489.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.92-7.85(m,2H)、7.41-7.35(m,2H)、4.11(qdd,J=7.9,6.6,5.0Hz,4H)、3.67(ddd,J=23.4,10.8,4.6Hz,1H)、3.52-3.33(m,2H)、2.69-2.62(m,2H)、1.64-1.53(m,2H)、1.38(s,9H)、1.27(q,J=6.9Hz,8H)、0.91(t,J=7.3Hz,3H)。
tert-ブチル3-(3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.72g、3.5mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.0g、2.8mmol)を淡黄色の油として得た。LCMS m/z 287.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.92-7.86(m,2H)、7.42-7.34(m,2H)、6.28(d,J=1.2Hz,1H)、5.97(q,J=1.3Hz,1H)、4.03(s,2H)、2.69-2.61(m,2H)、1.63-1.53(m,2H)、1.34(m,11H)、0.91(t,J=7.3Hz,3H)。
tert-ブチル2-((3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.0g、2.8mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(775mg、2.7mmol)を白色の固体として得た。LCMS m/z 286.7(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.94-7.83(m,2H)、7.41-7.34(m,2H)、6.33(d,J=1.2Hz,1H)、6.00(d,J=1.3Hz,1H)、4.02(s,2H)、2.69-2.61(m,2H)、1.64-1.53(m,2H)、1.32(h,J=7.4Hz,2H)、0.90(t,J=7.4Hz,3H)。
反応物を60℃に加熱したことを除いて、3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-5-(クロロメチル)-1,2,4-オキサジアゾール(1.52g、1当量、4.76mmol)から、一般的な手順A、ステップ1、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.529g、0.89mmol、90%純度)を無色の油として得た。LCMS m/z 559.5(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.71-7.56(m,4H)、7.55-7.47(m,2H)、7.42-7.32(m,2H)、4.14-3.96(m,6H)、3.55(ddd,J=23.3,10.9,4.5Hz,1H)、3.42-3.18(m,2H)、1.31-1.18(m,15H)。
3-(3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.529g、0.89mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.178g、0.39mmol、91%純度)を無色の油として得た。LCMS m/z 355.6(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.70-7.64(m,2H)、7.64-7.58(m,2H)、7.54-7.48(m,2H)、7.41-7.35(m,2H)、6.22(s,1H)、5.89(s,1H)、4.10(s,2H)、3.91(s,2H)、1.25(s,9H)。
tert-ブチル2-((3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.178g、0.39mmol、91%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(72mg、0.20mmol)を淡黄色の油として得た。LCMS m/z 355.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.72-7.66(m,2H)、7.66-7.58(m,2H)、7.54-7.48(m,2H)、7.42-7.34(m,2H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.3Hz,1H)、4.11(s,2H)、3.92(s,2H)。
ヨウ化ナトリウムを使用していないことを除いて、3-(4-ブチルベンジル)-5-(クロロメチル)-1,2,4-オキサジアゾール(1.10g、3.9mmol)から、一般的な手順A、ステップ1、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.85g、1.8mmol)を無色の油として得た。LCMS m/z 481.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.16(d,J=8.2Hz,2H)、7.11(d,J=8.2Hz,2H)、4.13-4.01(m,4H)、3.98(s,2H)、3.64-3.46(m,1H)、3.31-3.27(m,1H)、3.27-3.16(m,1H)、2.56-2.53(m,2H)、1.58-1.45(m,2H)、1.28(s,9H)、1.26-1.18(m,8H)、0.88(t,J=7.3Hz,3H)。
3-(3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.85g、1.8mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/シクロヘキサン)により精製して、tert-ブチル2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.62g、1.74mmol)を無色の油として得た。LCMS m/z 301.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.17(d,J=8.0Hz,2H)、7.11(d,J=8.1Hz,2H)、6.23-6.19(m,1H)、5.90-5.86(m,1H)、3.99(s,2H)、3.90(s,2H)、2.57-2.52(m,2H)、1.59-1.46(m,2H)、1.33-1.26(m,2H)、1.25(s,9H)、0.88(t,J=7.3Hz,3H)。
tert-ブチル2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.62g、1.74mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/ヘプタン)により精製して、2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.523g、1.72mmol)を白色の固体として得た。LCMS m/z 301.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,br.1H)、7.17(d,J=8.2Hz,2H)、7.13(d,J=8.1Hz,2H)、6.29-6.25(m,1H)、5.93-5.89(m,1H)、4.00(s,2H)、3.90(s,2H)、2.57-2.53(m,2H)、1.57-1.47(m,2H)、1.34-1.23(m,2H)、0.89(t,J=7.3Hz,3H)。
ヨウ化ナトリウムを使用していないことを除いて、5-(クロロメチル)-3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール(2.24g、7.41mmol、89%純度)から、一般的な手順A、ステップ1、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.60g、3.3mmol)を粘着性の黄色の油として得た。LCMS m/z 501.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.43-7.39(m,1H)、7.40-7.32(m,3H)、4.14-3.99(m,4H)、3.53(ddd,J=23.3,10.9,4.4Hz,1H)、3.38-3.27(m,1H)、3.21(ddd,J=16.8,8.9,4.5Hz,1H)、1.54-1.39(m,4H)、1.36(s,9H)、1.29-1.21(m,6H)。
tert-ブチル3-(3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.60g、3.3mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/シクロヘキサン)により精製して、tert-ブチル2-((3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.88g、2.3mmol)を無色の油として得た。LCMS m/z 383.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.44-7.41(m,1H)、7.41-7.32(m,3H)、6.22(d,J=1.1Hz,1H)、5.89(q,J=1.3Hz,1H)、3.90(s,2H)、1.48-1.39(m,4H)、1.34(s,9H)。
tert-ブチル2-((3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.88g、2.3mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/ヘプタン)により精製して、2-((3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(670mg、2.1mmol)を無色のガムとして得た。LCMS m/z 305.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.46-7.43(m,1H)、7.40-7.33(m,3H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.2Hz,1H)、3.89(s,2H)、1.51-1.38(m,4H)。
N-ヒドロキシ-1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボキシミダミド(1.12g、1.5当量、4.59mmol)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.532g、0.93mmol、91%純度)を無色の油として得た。LCMS m/z 541.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.69(dd,J=11.6,8.1Hz,2H)、7.57(dd,J=18.7,8.0Hz,2H)、4.14-3.99(m,4H)、3.52(ddd,J=23.3,10.9,4.4Hz,1H)、3.39-3.26(m,1H)、3.20(ddd,J=16.8,8.9,4.4Hz,1H)、1.57-1.14(m,19H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.532g、0.93mmol、91%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.107g、0.27mmol)を無色の油として得た。LCMS m/z 339.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.70(d,J=8.1Hz,2H)、7.60(d,J=8.1Hz,2H)、6.21(s,1H)、5.88(s,1H)、3.90(s,2H)、1.56-1.39(m,4H)、1.32(s,9H)。
tert-ブチル2-((3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.107g、0.27mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(70mg、0.20mmol)を無色の油として得た。LCMS m/z 339.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.71(d,J=8.2Hz,2H)、7.61(d,J=8.1Hz,2H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.3Hz,1H)、3.90(s,2H)、1.58-1.39(m,4H)。
N-ヒドロキシ-4-ペンチルベンズイミダミド(0.95g、1.5当量、4.6mmol)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.509g、1.0mmol)を無色の油として得た。LCMS m/z 503.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.93-7.84(m,2H)、7.43-7.34(m,2H)、4.18-4.04(m,4H)、3.67(ddd,J=23.4,10.8,4.6Hz,1H)、3.52-3.27(m,2H)、2.65(t,J=7.7Hz,2H)、1.61(p,J=7.5Hz,2H)、1.38(s,9H)、1.34-1.22(m,10H)、0.88(t,J=7.1Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.509g、1.0mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.268g、0.74mmol)を無色の油として得た。LCMS m/z 301.5(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.93-7.86(m,2H)、7.42-7.35(m,2H)、6.28(d,J=1.2Hz,1H)、5.97(d,J=1.3Hz,1H)、4.03(s,2H)、2.66(t,J=7.8Hz,2H)、1.60(p,J=7.4Hz,2H)、1.40-1.22(m,13H)、0.87(t,J=6.9Hz,3H)。
tert-ブチル2-((3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.268g、0.74mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(185mg、0.61mmol)を無色の油として得た。LCMS m/z 301.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.87(s,1H)、7.95-7.84(m,2H)、7.44-7.32(m,2H)、6.33(d,J=1.2Hz,1H)、6.00(s,1H)、4.02(d,J=1.1Hz,2H)、2.65(t,J=7.6Hz,2H)、1.70-1.52(m,2H)、1.41-1.19(m,4H)、0.87(t,J=6.9Hz,3H)。
1-(2-クロロフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(729mg、2.77mmol、80%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.43g、0.84mmol)を透明な無色のガムとして得た。LCMS m/z 485.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.55-7.43(m,2H)、7.41-7.29(m,2H)、4.14-4.01(m,4H)、3.59-3.45(m,1H)、3.36-3.13(m,2H)、1.66-1.50(m,2H)、1.43-1.39(m,2H)、1.37(s,9H)、1.30-1.20(m,6H)。
tert-ブチル3-(3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.43g、0.84mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.300g、0.79mmol)を透明な無色の油として得た。LCMS m/z 305.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.56-7.44(m,2H)、7.41-7.32(m,2H)、6.24-6.19(m,1H)、5.90-5.86(m,1H)、3.89(s,2H)、1.61-1.54(m,2H)、1.44-1.37(m,2H)、1.34(s,9H)。
tert-ブチル2-((3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.300g、0.79mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.225g、0.70mmol)を無色のガムとして得た。LCMS m/z 305.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,br.1H)、7.56-7.50(m,1H)、7.49-7.43(m,1H)、7.41-7.30(m,2H)、6.28-6.23(m,1H)、5.91-5.86(m,1H)、3.89(s,2H)、1.66-1.51(m,2H)、1.47-1.28(m,2H)。
1-(4-クロロフェニル)-N-ヒドロキシシクロブタン-1-カルボキシミダミド(596mg、1当量、2.18mmol、82%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(602mg、0.72mmol、60%純度)を透明な無色の油として得た。LCMS m/z 520.5(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.41-7.36(m,2H)、7.32-7.26(m,2H)、4.10-4.00(m,4H)、3.52(ddd,J=23.3,10.9,4.6Hz,1H)、3.38-3.17(m,2H)、2.80-2.57(m,4H)、2.09-1.86(m,2H)、1.27(s,9H)、1.25-1.20(m,6H)。
tert-ブチル3-(3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(602mg、0.72mmol、60%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(250mg、0.64mmol)を無色の油として得た。LCMS m/z 319.2/321.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.41-7.35(m,2H)、7.33-7.26(m,2H)、6.21(d,J=1.3Hz,1H)、5.87(d,J=1.3Hz,1H)、3.90(s,2H)、2.80-2.71(m,2H)、2.68-2.57(m,2H)、2.09-1.85(m,2H)、1.20(s,9H)。
tert-ブチル2-((3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(250mg、0.64mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~60%EtOAc/イソヘキサン)により精製して、2-((3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(164mg、0.50mmol)を粘着性の無色のガムとして得た。LCMS m/z 319.1/321.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.44-7.36(m,2H)、7.34-7.27(m,2H)、6.26(d,J=1.2Hz,1H)、5.88(d,J=1.3Hz,1H)、3.90(s,2H)、2.81-2.70(m,2H)、2.68-2.56(m,2H)、2.09-1.98(m,1H)、1.97-1.83(m,1H)。
IPA(20mL)中のヒドロキシルアミンハイドロクロライド(1.22g、17.6mmol)および重炭酸ナトリウム(1.48g、17.6mmol)の混合物を、15分間撹拌した。2,2-ジメチルオクタニトリル(2.50g、14.7mmol、90%純度)を加え、混合物を85℃に加熱し、22時間撹拌した。混合物を室温に冷却し、濾過し、IPA(3x20mL)で洗浄した。濾液を濃縮して、N-ヒドロキシ-2,2-ジメチルオクタニミダミド(2.70g、14mmol)を粘着性のオレンジ色の油として得、これを次のステップで直接使用した。
粗N-ヒドロキシ-2,2-ジメチルオクタニミダミド(1.44g、7.35mmol)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.92g、2.1mmol、50%純度)を淡褐色の油として得た。LCMS m/z 483.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-3.99(m,4H)、3.54(ddd,J=23.3,11.1,4.3Hz,1H)、3.40-3.28(m,1H)、3.23(ddd,J=16.7,8.7,4.3Hz,1H)、1.40(t,J=7.0Hz,3H)、1.37(s,9H)、1.29-1.16(m,10H)、1.03(s,6H)、0.88-0.81(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.92g、2.1mmol、50%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(504mg、1.5mmol)を無色の油として得た。LCMS m/z 337.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.89(d,J=1.4Hz,1H)、3.91(s,2H)、1.61-1.53(m,2H)、1.34(s,9H)、1.25(s,6H)、1.23-1.13(m,6H)、1.13-1.01(m,2H)、0.83(t,J=6.9Hz,3H)。
tert-ブチル2-((3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(504mg、1.5mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(405mg、1.4mmol)を黄色の油として得た。LCMS m/z 281.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.67(s,1H)、6.27(d,J=1.2Hz,1H)、5.88(d,J=1.3Hz,1H)、3.90(s,2H)、1.61-1.50(m,2H)、1.30-1.10(m,12H)、1.10-0.99(m,2H)、0.83(t,J=6.8Hz,3H)。
3-ブチル-N-ヒドロキシベンズイミダミド(728mg、1.1当量、3.37mmol、89%)純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~85%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.65g、1.3mmol、90%純度)を透明な無色のガムとして得た。LCMS m/z 411.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.85-7.73(m,2H)、7.54-7.37(m,2H)、4.18-4.07(m,4H)、3.76-3.59(m,1H)、3.53-3.38(m,2H)、2.72-2.61(m,2H)、1.65-1.52(m,2H)、1.40(s,9H)、1.36-1.21(m,8H)、0.91(t,J=7.3Hz,3H)。
tert-ブチル3-(3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.65g、1.3mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.400g、1.1mmol)を透明な無色の油として得た。LCMS m/z 287.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.84-7.76(m,2H)、7.53-7.37(m,2H)、6.31-6.25(m,1H)、6.00-5.93(m,1H)、4.04(s,2H)、2.73-2.61(m,2H)、1.64-1.52(m,2H)、1.38-1.26(m,11H)、0.91(t,J=7.3Hz,3H)。
tert-ブチル2-((3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.400g、1.1mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(190mg、0.66mmol)を白色の固体として得た。LCMS m/z 287.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.87(s,1H)、7.82-7.75(m,2H)、7.49-7.38(m,2H)、6.33(d,J=1.2Hz,1H)、6.00(d,J=1.3Hz,1H)、4.03(s,2H)、2.71-2.60(m,2H)、1.63-1.51(m,2H)、1.38-1.25(m,2H)、0.90(t,J=7.4Hz,3H)。
N-ヒドロキシ-2-(4-ペンチルフェニル)アセトイミダミド(780mg、1.05当量、3.22mmol、91%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.27g、0.52mmol)を透明な淡褐色のガムとして得た。LCMS m/z 495(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.18-7.14(m,2H)、7.13-7.09(m,2H)、4.13-4.01(m,4H)、3.98(s,2H)、3.61-3.48(m,1H)、3.32-3.16(m,4H)、1.60-1.49(m,2H)、1.28(s,9H)、1.26-1.19(m,10H)、0.85(t,J=6.9Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.27g、0.52mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.12g、0.31mmol)を透明な無色の油として得た。LCMS m/z 315.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.17(d,J=8.1Hz,2H)、7.11(d,J=8.2Hz,2H)、6.25-6.16(m,1H)、5.92-5.81(m,1H)、3.99(s,2H)、3.90(s,2H)、2.56-2.52(m,2H)、1.60-1.46(m,2H)、1.34-1.18(m,13H)、0.85(t,J=7.0Hz,3H)。
tert-ブチル2-((3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.12g、0.31mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(50mg、0.16mmol)を黄色の油として得た。LCMS m/z 315.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.17(d,J=8.1Hz,2H)、7.13(d,J=8.0Hz,2H)、6.26(s,1H)、5.90(d,J=1.4Hz,1H)、4.00(s,2H)、3.90(s,2H)、2.54(d,J=7.7Hz,2H)、1.54(p,J=7.4Hz,2H)、1.28(dddd,J=14.9,9.3,6.8,2.1Hz,4H)、0.86(t,J=6.9Hz,3H)。
2-(3-ブチルフェニル)-N-ヒドロキシアセトイミダミド(2.66g、1当量、11.2mmol、87%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.68g、2.9mmol、84%純度)を濃いオレンジ色の油として得た。LCMS m/z 503.3(M+Na)+(ES+)。
tert-ブチル3-(3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.68g、2.9mmol、84%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.98g、2.6mmol)を黄色の油として得た。LCMS m/z 300.7(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.20(t,J=7.5Hz,1H)、7.07(td,J=7.9,1.9Hz,3H)、6.21(d,J=1.3Hz,1H)、5.88(t,J=1.3Hz,1H)、4.00(s,2H)、3.90(s,2H)、2.54(d,J=7.6Hz,2H)、1.52(tt,J=8.3,6.5Hz,2H)、1.32-1.26(m,2H)、1.25(s,9H)、0.89(t,J=7.3Hz,3H)。
tert-ブチル2-((3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.98g、2.6mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(700mg、2.2mmol)を粘着性の黄色の油として得た。LCMS m/z 301.6(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.21(t,J=7.5Hz,1H)、7.10(d,J=1.8Hz,1H)、7.09-7.02(m,2H)、6.27(d,J=1.2Hz,1H)、5.90(d,J=1.4Hz,1H)、4.01(s,2H)、3.91(s,2H)、2.54(t,J=7.7Hz,2H)、1.53(tt,J=7.9,6.4Hz,2H)、1.30(h,J=7.3Hz,2H)、0.89(t,J=7.3Hz,3H)。
2-(4-クロロフェニル)-N-ヒドロキシ-2-メチルプロパニイミダミド(0.98g、4.6mmol)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.320g、0.65mmol)を無色の油として得た。LCMS m/z 509.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.39-7.33(m,2H)、7.32-7.25(m,2H)、4.15-3.98(m,4H)、3.51(ddd,J=23.3,10.9,4.4Hz,1H)、3.40-3.27(m,1H)、3.22(ddd,J=16.8,8.7,4.4Hz,1H)、1.65(d,J=3.7Hz,6H)、1.28(s,9H)、1.26-1.20(m,6H)。
tert-ブチル3-(3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.320g、0.65mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.133g、0.36mmol)を無色の油として得た。LCMS m/z 307.5(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.40-7.26(m,4H)、6.20(s,1H)、5.87(s,1H)、3.90(s,2H)、1.66(s,6H)、1.27(s,9H)。
tert-ブチル2-((3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.133g、0.36mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(78mg、0.25mmol)を無色の油として得た。LCMS m/z 307.5(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,br.1H)、7.56-7.50(m,1H)、7.49-7.43(m,1H)、7.41-7.30(m,2H)、6.28-6.23(m,1H)、5.91-5.86(m,1H)、3.89(s,2H)、1.66-1.51(m,2H)、1.47-1.28(m,2H)。
8,8-ジフルオロ-N-ヒドロキシノナニミダミド(1.06g、5.07mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.28g、2.6mmol)を透明な黄色の油として得た。LCMS m/z 505.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.02(m,4H)、3.56(ddd,J=23.3,11.1,4.4Hz,1H)、3.39-3.33(m,1H)、3.23(ddd,J=16.8,8.6,4.4Hz,1H)、2.65(t,J=7.4Hz,2H)、1.90-1.76(m,2H)、1.66-1.46(m,5H)、1.43-1.19(m,21H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.28g、2.6mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~20%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.650g、1.8mmol)を透明な無色の油として得た。LCMS m/z 303.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.3Hz,1H)、5.96-5.83(m,1H)、3.91(s,2H)、2.65(t,J=7.4Hz,2H)、1.90-1.76(m,2H)、1.67-1.51(m,5H)、1.34(s,15H)。
tert-ブチル2-((3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.650g、1.8mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.479g、1.6mmol、86%、98%純度)を透明な無色の油として得た。LCMS m/z 303.6(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(d,J=1.2Hz,1H)、5.91(d,J=1.4Hz,1H)、3.91(s,2H)、2.65(t,J=7.5Hz,2H)、1.92-1.75(m,2H)、1.70-1.51(m,5H)、1.44-1.25(m,6H)。
2-シクロヘキシル-N-ヒドロキシアセトイミダミド(553mg、2.90mmol、82%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(356mg、0.78mmol、94%純度)を淡褐色の油として得た。LCMS m/z 431.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ .67(m,1H)、4.17-4.01(m,4H)、3.56(m,1H)、3.41-3.17(m,2H)、2.53(s,1H)、1.72-1.54(m,6H)、1.41(t,J=7.1Hz,1H)、1.37(s,9H)、1.26(m,6H)、1.19-1.08(m,2H)、1.03-0.91(m,2H)。
tert-ブチル3-(3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(356mg、0.78mmol、94%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(125mg、0.39mmol)を無色の油として得た。LCMS m/z 251.1(M-tBu+H)+(ES+)。1H NMR(400MHz,CD3OD)δ 6.34(s,1H)、5.86(s,1H)、3.90(s,2H)、2.58(d,J=6.9Hz,2H)、1.77-1.65(m,6H)、1.43(s,9H)、1.35-1.17(m,3H)、1.09-0.97(m,2H)。
tert-ブチル2-((3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(125mg、0.39mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(55.6mg、0.20mmol)を透明な無色の油として得た。LCMS m/z 251.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(br.s,1H)、6.27(s,1H)、5.91(s,1H)、3.91(s,2H)、3.32(br.s,1H)、2.53(d,J=6.8Hz,2H)、1.75-1.55(m,5H)、1.31-1.07(m,3H)、1.04-0.89(m,2H)。
4-(4-クロロフェニル)-N-ヒドロキシブタニイミダミド(1.00g、1当量、3.71mmol、79%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.73g、1.5mmol)を透明なオレンジ色の油として得た。LCMS m/z 487.1/489.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.37-7.30(m,2H)、7.25-7.19(m,2H)、4.14-3.99(m,5H)、3.40-3.17(m,2H)、2.67-2.57(m,4H)、1.95-1.84(m,2H)、1.34(s,9H)、1.29-1.19(m,6H)。
tert-ブチル3-(3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.73g、1.5mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.345g、0.92mmol)を淡黄色の油として得た。LCMS m/z 307.0/309.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.37-7.29(m,2H)、7.26-7.19(m,2H)、6.22(d,J=1.2Hz,1H)、5.89(d,J=1.3Hz,1H)、3.91(s,2H)、2.69-2.57(m,4H)、1.97-1.85(m,2H)、1.33(s,9H)。
tert-ブチル2-((3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.345g、0.92mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.23g、0.74mmol)を透明な無色の油として得た。LCMS m/z 307.0/309.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.38-7.29(m,2H)、7.27-7.18(m,2H)、6.27(d,J=1.3Hz,1H)、5.91(d,J=1.3Hz,1H)、3.90(s,2H)、2.65(t,J=7.4Hz,2H)、2.60(t,J=7.6Hz,2H)、1.91(p,J=7.5Hz,2H)。
N-ヒドロキシノナニミダミド-d17(0.917g、1当量、4.84mmol)から、一般的な手順B、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)プロパノエート(145mg、0.30mmol)を透明なオレンジ色の油として得た。LCMS m/z 464.4(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.14-4.03(m,4H)、3.55(ddd,J=23.3,11.1,4.3Hz,1H)、3.39-3.32(m,1H)、3.22(ddd,J=16.8,8.6,4.4Hz,1H)、1.36(s,9H)、1.29-1.21(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)プロパノエート(145mg、0.30mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(21mg、0.6mmol)を淡黄色の油として得た。LCMS m/z 284.2(M-tBu+H)+(ES+)。1H NMR(400MHz,CDCl3)δ 6.35(d,J=0.9Hz,1H)、5.70(d,J=1.0Hz,1H)、3.84(d,J=0.6Hz,2H)、1.44(s,9H)。
tert-ブチル2-((3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(21mg、0.6mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(3.5mg、12μmol、21%、100%純度)を透明な無色の油として得た。LCMS m/z 284.2(M+H)+(ES+)。1H NMR(400MHz,CDCl3)δ 6.54(s,1H)、5.93(d,J=1.3Hz,1H)、3.90(dd,J=1.4,0.7Hz,2H)。1つの交換可能なプロトンは観察されない。
N-ヒドロキシノン-8-イニミダミド(1.00g、5.35mmol、90%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.68g、1.4mmol、90%純度)を濃いオレンジ色の油として得た。LCMS m/z 465.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.03(m,4H)、3.63-3.50(m,2H)、3.29-3.12(m,1H)、2.73(t,J=2.6Hz,1H)、2.64(t,J=7.3Hz,2H)、2.14(td,J=6.8,2.6Hz,2H)、1.68-1.57(m,2H)、1.45-1.39(m,4H)、1.37(s,9H)、1.29-1.21(m,8H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.68g、1.4mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.22g、0.62mmol、90%純度)を黄色の油として得た。LCMS m/z 262.9(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.90(d,J=1.2Hz,1H)、3.91(s,2H)、2.73(t,J=2.7Hz,1H)、2.65(t,J=7.4Hz,2H)、2.14(td,J=6.8,2.6Hz,2H)、1.63(p,J=7.4Hz,2H)、1.47-1.20(m,15H)。
tert-ブチル2-((3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.22g、0.62mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(171mg、0.63mmol)を粘着性の黄色の油として得た。LCMS m/z 267.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、6.28(d,J=1.2Hz,1H)、5.92(d,J=1.4Hz,1H)、3.91(s,2H)、2.74(t,J=2.7Hz,1H)、2.65(t,J=7.4Hz,2H)、2.14(td,J=6.8,2.6Hz,2H)、1.63(p,J=7.5Hz,2H)、1.48-1.13(m,6H)。
N-ヒドロキシ-3-(4-プロピルフェニル)プロパニミダミド(0.72g、1当量、2.7mmol、78%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.35g、0.60mmol、83%純度)を濃いオレンジ色の油として得た。LCMS m/z 503.27(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.12-7.06(m,4H)、4.14-4.04(m,4H)、3.63-3.55(m,1H)、3.42-3.33(m,1H)、3.29-3.14(m,1H)、2.98-2.86(m,4H)、1.61-1.50(m,2H)、1.38(s,9H)、1.30-1.22(m,8H)、0.88(t,J=7.3Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.35g、0.60mmol、83%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(80mg、0.22mmol)を黄色の油として得た。LCMS m/z 357.4(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.12(d,J=8.2Hz,2H)、7.08(d,J=8.1Hz,2H)、6.24(d,J=1.3Hz,1H)、5.89(q,J=1.2Hz,1H)、3.92(s,2H)、2.94(q,J=3.6Hz,4H)、2.52-2.51(m,2H)、1.60-1.49(m,2H)、1.35(s,9H)、0.88(t,J=7.3Hz,3H)。
tert-ブチル2-((3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(80mg、0.22mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(52mg、0.16mmol)を粘着性の黄色の油として得た。LCMS m/z 301.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.14-7.05(m,4H)、6.29(d,J=1.3Hz,1H)、5.91(d,J=1.4Hz,1H)、3.92(s,2H)、2.93(d,J=3.2Hz,4H)、2.53-2.51(m,2H)、1.55(dt,J=14.7,7.4Hz,2H)、0.88(t,J=7.3Hz,3H)。
N-エチル-N’-(3-ジメチルアミノプロピル)カルボジイミドハイドロクロライド(0.371g、1.93mmol)を、DCM(8mL)中の4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(0.50g、1.61mmol)、ノナンヒドラジド(0.333g、1.93mmol)、DMAP(39mg、0.3mmol)、およびDIPEA(0.56mL、3.2mmol)の混合物に加えた。混合物を室温で3.5日間撹拌し、次に飽和水性NH4Cl(20mL)で希釈し、相を分離した。水相をDCM(2x10mL)で抽出した。合わせた有機相をブライン(20mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル2-(ジエトキシホスホリル)-4-(2-ノナノイルヒドラジニル)-4-オキソブタノエート(0.658g、1.1mmol、80%純度)を、放置すると固化する透明な無色の油として得た。LCMS m/z 487.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 9.83(s,1H)、9.72(s,1H)、4.15-3.97(m,4H)、3.28-3.16(m,1H)、2.76(ddd,J=16.3,11.5,6.8Hz,1H)、2.49-2.41(m,1H)、2.09(t,J=7.3Hz,2H)、1.56-1.45(m,2H)、1.39(s,9H)、1.33-1.18(m,16H)、0.93-0.80(m,3H)。
THF(10mL)中のtert-ブチル2-(ジエトキシホスホリル)-4-(2-ノナノイルヒドラジニル)-4-オキソブタノエート(0.658g、1.1mmol、80%純度)およびローソン試薬(0.550g、1.36mmol)の混合物を60℃で1時間、次に室温で36時間撹拌した。混合物を濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,3,4-チアジアゾール-2-イル)プロパノエート(450mg、0.78mmol、80%純度)を黄色の油として得た。LCMS m/z 463.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.16-4.02(m,4H)、3.60-3.48(m,2H)、3.47-3.30(m,1H)、3.03(t,J=7.4Hz,2H)、1.73-1.61(m,2H)、1.35(s,9H)、1.32-1.20(m,16H)、0.88-0.83(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチル-1,3,4-チアジアゾール-2-イル)プロパノエート(450mg、0.78mmol、80%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~40%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((5-オクチル-1,3,4-チアジアゾール-2-イル)メチル)アクリレート(175mg、0.52mmol)を無色の油として得た。LCMS m/z 339.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.17(d,J=1.3Hz,1H)、5.84(d,J=1.3Hz,1H)、4.01(s,2H)、3.02(t,J=7.4Hz,2H)、1.72-1.62(m,2H)、1.38(s,9H)、1.34-1.19(m,10H)、0.89-0.82(m,3H)。
tert-ブチル2-((5-オクチル-1,3,4-チアジアゾール-2-イル)メチル)アクリレート(175mg、0.52mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((5-オクチル-1,3,4-チアジアゾール-2-イル)メチル)アクリル酸(71mg、0.25mmol)を無色の油として得た。LCMS m/z 283.5(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、6.22(s,1H)、5.86(s,1H)、4.01(s,2H)、3.01(t,J=7.5Hz,2H)、1.68(p,J=7.5Hz,2H)、1.36-1.16(m,10H)、0.86(t,J=7.0Hz,3H)。
ジメチルホルムアミド(10mL)中の4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(2.00g、6.45mmol)、アンモニウムクロリド(517mg、9.67mmol)、およびDIPEA(1.7mL、9.67mmol)の混合物を、室温で15分間撹拌した。HATU(2.94g、7.73mmol)を加え、混合物を室温で30分間撹拌し、次に水(100mL)に注ぎ、EtOAc(3x50mL)で抽出した。合わせた有機層を水(25mL)、ブライン(25mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、次にシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)によりさらに精製して、tert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-オキソブタノエート(1.63g、5.2mmol)を白色の固体として得た。LCMS m/z 332.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.42(s,1H)、6.90(s,1H)、4.10-3.96(m,4H)、3.22(ddd,J=23.3,11.5,3.4Hz,1H)、2.69(ddd,J=16.4,11.4,7.2Hz,1H)、2.40(ddd,J=16.4,9.5,3.4Hz,1H)、1.39(s,9H)、1.28-1.22(m,6H)。
ローソン試薬(549mg、1.36mmol)を、1,4-ジオキサン(3mL)中のtert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-オキソブタノエート(0.70g、2.26mmol)の溶液に60℃で加えた。混合物を60℃で2時間撹拌し、室温に冷却し、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-チオキソブタノエート(0.621g、1.8mmol、92%純度)を濃い黄色のガムとして得た。LCMS m/z 348.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 9.53(s,1H)、9.36(s,1H)、4.12-3.98(m,4H)、3.83-3.66(m,1H)、3.08(ddd,J=16.0,11.5,6.5Hz,1H)、2.60(ddd,J=16.0,9.8,3.3Hz,1H)、1.39(s,9H)、1.31-1.21(m,6H)。
EtOH(19mL)中のtert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-チオキソブタノエート(0.621g、1.8mmol、92%純度)および1-ブロモデカン-2-オン(792mg、2.86mmol、85%純度)の溶液を、80℃に20分間加熱した。混合物を室温に冷却し、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(4-オクチルチアゾール-2-イル)プロパノエート(0.602g、1.0mmol、80%純度)を透明なオレンジ色の油として得た。LCMS m/z 462.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.14(s,1H)、4.14-4.03(m,4H)、3.50-3.41(m,2H)、3.32-3.23(m,1H)、2.62(t,J=7.5Hz,2H)、1.65-1.55(m,2H)、1.34(s,9H)、1.29-1.21(m,16H)、0.89-0.82(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(4-オクチルチアゾール-2-イル)プロパノエート(0.602g、1.0mmol、80%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((4-オクチルチアゾール-2-イル)メチル)アクリレート(0.275g、0.77mmol、94%純度)を透明な無色の油として得た。LCMS m/z 338.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.10(s,1H)、6.14(d,J=1.5Hz,1H)、5.79-5.73(m,1H)、3.90(d,J=1.1Hz,2H)、2.66-2.59(m,2H)、1.65-1.54(m,2H)、1.37(s,9H)、1.32-1.19(m,10H)、0.89-0.82(m,3H)。
tert-ブチル2-((4-オクチルチアゾール-2-イル)メチル)アクリレート(0.275g、0.77mmol、94%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((4-オクチルチアゾール-2-イル)メチル)アクリル酸(110mg、0.37mmol)を透明な黄色の油として得た。LCMS m/z 282.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.69(br s,1H)、7.10(s,1H)、6.21(d,J=1.5Hz,1H)、5.79(d,J=1.4Hz,1H)、3.89(d,J=1.0Hz,2H)、2.63(t,J=7.6Hz,2H)、1.60(t,J=7.5Hz,2H)、1.32-1.19(m,10H)、0.88-0.80(m,3H)。
銀トリフルオロメタンスルホネート(136mg、0.53mmol)を、EtOAc(2mL)中の1-ブロモデカン-2-オン(100mg、0.43mmol)およびtert-ブチル4-アミノ-2-(ジエトキシホスホリル)-4-オキソブタノエート(164mg、0.53mmol)の懸濁液に室温で加えた。混合物を暗所で、室温で16時間撹拌し、次にブライン(4mL)で希釈し、室温で3時間撹拌した。混合物を濾過し、濾液をEtOAc(3×5mL)で抽出した。合わせた有機層を乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(4-オクチルオキサゾール-2-イル)プロパノエート(0.030g、56μmol、83%純度)を透明な無色の油として得た。LCMS m/446.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.69(s,1H)、4.12-4.05(m,4H)、3.41(ddd,J=22.8,11.5,3.9Hz,1H)、3.17(ddd,J=16.3,11.5,8.3Hz,1H)、3.03(ddd,J=16.4,8.8,3.9Hz,1H)、2.39-2.32(m,2H)、1.55-1.45(m,2H)、1.36(s,9H)、1.27-1.23(m,16H)、0.87-0.84(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(4-オクチルオキサゾール-2-イル)プロパノエート(142mg、0.32mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((4-オクチルオキサゾール-2-イル)メチル)アクリレート(0.053g、0.12mmol、75%純度)を淡黄色の油として得た。LCMS m/z 266.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.68(t,J=1.1Hz,1H)、6.13(d,J=1.4Hz,1H)、5.74-5.68(m,1H)、3.68(s,2H)、2.41-2.33(m,2H)、1.55-1.48(m,2H)、1.35(s,9H)、1.27-1.24(m,10H)、0.87-0.85(m,3H)。
tert-ブチル2-((4-オクチルオキサゾール-2-イル)メチル)アクリレート(0.053g、0.12mmol、75%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((4-オクチルオキサゾール-2-イル)メチル)アクリル酸(0.020g、75μmol)を透明な無色の油として得た。LCMS m/z 266.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.66(s,1H)、7.67(d,J=1.3Hz,1H)、6.19(d,J=1.4Hz,1H)、5.71(d,J=1.6Hz,1H)、3.69(s,2H)、2.38(t,J=7.5Hz,2H)、1.58-1.46(m,2H)、1.31-1.21(m,10H)、0.90-0.81(m,3H)。
(R)-N-ヒドロキシ-2-メチルオクタニミダミド(1.46g、7.20mmol、85%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-((R)-オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.79g、2.8mmol、70%純度)を透明な淡黄色の油として得た。LCMS m/z 469.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.18-4.01(m,4H)、3.63-3.46(m,1H)、3.42-3.33(m,1H)、3.28-3.16(m,1H)、2.97-2.82(m,1H)、1.65-1.49(m,2H)、1.37(s,9H)、1.30-1.15(m,17H)、0.84(t,J=6.7Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-((R)-オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.79g、2.8mmol、70%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、tert-ブチル(R)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.0g、2.8mmol、90%純度)を透明な無色の油として得た。LCMS m/z 267.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.29-6.18(m,1H)、5.97-5.84(m,1H)、3.92(s,2H)、2.99-2.78(m,1H)、1.70-1.45(m,2H)、1.34(s,9H)、1.29-1.09(m,11H)、0.84(t,J=6.8Hz,3H)。
tert-ブチル(R)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.0g、2.8mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~35%MTBE/イソヘキサン)により精製して、(R)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.696g、2.5mmol)を透明な無色の油として得た。LCMS m/z 267.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,br.1H)、6.37-6.19(m,1H)、5.98-5.81(m,1H)、3.91(s,2H)、3.03-2.76(m,1H)、1.75-1.41(m,2H)、1.34-1.01(m,11H)、0.85(t,J=6.7Hz,3H)。
3-(4-エチルフェニル)-N-ヒドロキシプロパニイミダミド(1.10g、5.03mmol、85%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.55g、1.1mmol、94%純度)を濃いオレンジ色の油として得た。LCMS m/z 489.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.11(s,4H)、4.15-4.05(m,4H)、3.58(ddd,J=23.3,10.9,4.2Hz,1H)、3.42-3.33(m,1H)、3.24(ddd,J=16.9,8.8,4.4Hz,1H)、2.98-2.87(m,4H)、2.55(q,J=7.6Hz,2H)、1.38(s,9H)、1.30-1.22(m,6H)、1.15(t,J=7.6Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.55g、1.1mmol、94%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.28g、0.65mmol、79%純度)を黄色の油として得た。LCMS m/z 287.5(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.15-7.07(m,4H)、6.24(d,J=1.3Hz,1H)、5.92-5.86(m,1H)、3.92(s,2H)、2.94(q,J=3.3Hz,4H)、2.55(q,J=7.7Hz,2H)、1.35(s,9H)、1.15(t,J=7.6Hz,3H)。
tert-ブチル2-((3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.28g、0.65mmol、79%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をHPLC(Waters XSelect CSHカラムC18、5μm 30x100mm、水中40~70%MeCN 0.1%ギ酸)により精製して、2-((3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(80mg、0.28mmol)を白色の固体として得た。LCMS m/z 286.9(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.11(d,J=1.2Hz,4H)、6.28(d,J=1.3Hz,1H)、5.90(d,J=1.6Hz,1H)、3.92(s,2H)、2.93(s,4H)、2.55(q,J=7.6Hz,2H)、1.15(t,J=7.6Hz,3H)。
N-ヒドロキシ-2-(4-(トリフルオロメチル)フェニル)アセトイミダミド(0.60g、2.5mmol、90%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.28g、0.54mmol)を濃いオレンジ色の油として得た。LCMS m/z 515.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.68(d,J=8.0Hz,2H)、7.51(d,J=8.0Hz,2H)、4.18(d,J=3.5Hz,2H)、4.11-3.96(m,4H)、3.53(ddd,J=23.4,10.9,4.5Hz,1H)、3.39-3.13(m,2H)、1.27-1.19(m,15H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.28g、0.54mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(130mg、0.35mmol)を黄色の油として得た。LCMS m/z 313.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.69(d,J=8.0Hz,2H)、7.53(d,J=8.0Hz,2H)、6.21(d,J=1.3Hz,1H)、5.89(d,J=1.3Hz,1H)、4.18(s,2H)、3.91(s,2H)、1.22(s,9H)。
tert-ブチル2-((3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(130mg、0.35mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサンにより精製して、2-((3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(110mg、0.35mmol)を無色の油として得た。(3135-108)。LCMS m/z 313.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.70(d,J=8.0Hz,2H)、7.52(d,J=7.9Hz,2H)、6.27(d,J=1.3Hz,1H)、5.92(d,J=1.5Hz,1H)、4.20(s,2H)、3.92(s,2H)。
(S)-N-ヒドロキシ-2-メチルオクタニミダミド(1.63g、8.04mmol、85%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-((S)-オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.85g、2.9mmol、71%純度)を透明な淡黄色の油として得た。LCMS m/z 469.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.20-3.99(m,4H)、3.63-3.46(m,1H)、3.40-3.34(m,1H)、3.28-3.15(m,1H)、2.96-2.83(m,1H)、1.67-1.50(m,2H)、1.37(s,9H)、1.31-1.14(m,17H)、0.84(t,J=6.7Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-((S)-オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.85g、2.9mmol、71%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、tert-ブチル(S)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.98g、2.9mmol)を透明な無色の油として得た。LCMS m/z 267.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.28-6.19(m,1H)、5.95-5.84(m,1H)、3.92(s,2H)、2.97-2.81(m,1H)、1.70-1.46(m,2H)、1.34(s,9H)、1.28-1.10(m,11H)、0.84(t,J=6.8Hz,3H)。
tert-ブチル(S)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.98g、2.9mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~35%MTBE/イソヘキサン)により精製して、(S)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.612g、2.2mmol)を透明な無色の油として得た。LCMS m/z 267.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、6.28(d,J=1.2Hz,1H)、5.90(q,J=1.3Hz,1H)、3.91(d,J=1.0Hz,2H)、2.95-2.81(m,1H)、1.68-1.59(m,1H)、1.52(ddt,J=14.6,12.8,5.5Hz,1H)、1.33-1.11(m,11H)、0.85(t,J=6.9Hz,3H)。
1-(4-フルオロフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(1.42g、6.58mmol、90%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(2.27g、4.4mmol、90%純度)を透明な淡黄色の油として得た。LCMS m/z 491.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.47-7.32(m,2H)、7.23-7.09(m,2H)、4.17-3.95(m,4H)、3.61-3.43(m,1H)、3.32-3.25(m,1H)、3.25-3.12(m,1H)、1.53-1.30(m,13H)、1.25(q,J=6.7Hz,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(2.27g、4.4mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.55g、1.5mmol)を透明な無色の油として得た。LCMS m/z 289.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.50-7.35(m,2H)、7.24-7.10(m,2H)、6.21(s,1H)、5.92-5.84(m,1H)、3.89(s,2H)、1.49-1.40(m,2H)、1.39-1.27(m,11H)。
tert-ブチル2-((3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.55g、1.5mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~35%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.430g、1.4mmol)を透明な無色の濃厚な油として得た。LCMS m/z 289.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.48-7.38(m,2H)、7.20-7.11(m,2H)、6.27(d,J=1.2Hz,1H)、5.90(q,J=1.3Hz,1H)、3.88(s,2H)、1.51-1.43(m,2H)、1.40-1.31(m,2H)。
N-ヒドロキシ-1-(4-メトキシフェニル)シクロプロパン-1-カルボキシミダミド(0.90g、2.7mmol、63%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(235mg、0.32mmol、65%純度)を濃いオレンジ色の油として得た。LCMS m/z 481.1(M+H)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(235mg、0.32mmol、65%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(60mg、0.16mmol)を黄色の油として得た。LCMS m/z 301.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.32-7.26(m,2H)、6.92-6.86(m,2H)、6.21(d,J=1.2Hz,1H)、5.87(d,J=1.5Hz,1H)、3.88(s,2H)、3.75(s,3H)、1.40(q,J=4.2,3.6Hz,2H)、1.34(s,9H)、1.30(q,J=4.8,4.3Hz,2H)。
tert-ブチル2-((3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(60mg、0.16mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(35mg、0.12mmol)を白色の固体として得た。LCMS m/z 301.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.33-7.26(m,2H)、6.93-6.84(m,2H)、6.26(d,J=1.2Hz,1H)、5.89(d,J=1.5Hz,1H)、3.87(s,2H)、3.75(s,3H)、1.45-1.38(m,2H)、1.32-1.27(m,2H)。
N-ヒドロキシ-2-(4-(トリフルオロメトキシ)フェニル)アセトイミダミド(1.17g、5.0mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.25g、2.2mmol、90%純度)を褐色の油として得た。LCMS m/z 531.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.41(d,J=9.0Hz,2H)、7.31(d,J=8.1Hz,2H)、4.16-3.99(m,6H)、3.54(ddd,J=23.4,10.9,4.5Hz,1H)、3.41-3.16(m,2H)、1.31-1.17(m,15H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.25g、2.2mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.605g、1.5mmol)を無色の油として得た。LCMS m/z 329.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.42(d,J=8.6Hz,2H)、7.31(d,J=8.2Hz,2H)、6.21(s,1H)、5.89(s,1H)、4.10(s,2H)、3.91(s,2H)、1.22(s,9H)。
tert-ブチル2-((3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.605g、1.5mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.405g、1.2mmol)を無色の油として得た。LCMS m/z 329.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.41(d,J=8.2Hz,2H)、7.32(d,J=8.2Hz,2H)、6.27(s,1H)、5.91(s,1H)、4.12(s,2H)、3.91(s,2H)。
8,8,9-トリフルオロ-N-ヒドロキシノナニミダミド(1.28g、5.66mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.02g、1.9mmol、92%純度)を褐色の油として得た。LCMS m/z 523.2(M+Na)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.02g、1.9mmol、92%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.516g、1.3mmol、93%純度)を無色の油として得た。LCMS m/z 321.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(s,1H)、5.90(s,1H)、4.64(dt,J=45.9,13.2Hz,2H)、3.91(s,2H)、2.65(t,J=7.4Hz,2H)、1.99-1.81(m,2H)、1.63(p,J=7.3Hz,2H)、1.49-1.22(m,15H)。
tert-ブチル2-((3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.516g、1.3mmol、93%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.315g、0.97mmol、71%、99%純度)を無色の油として得た。LCMS m/z 321.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(s,1H)、5.92(s,1H)、4.64(dt,J=46.0,13.2Hz,2H)、3.91(s,2H)、2.66(t,J=7.5Hz,2H)、2.00-1.83(m,2H)、1.64(p,J=7.3Hz,2H)、1.51-1.24(m,6H)。
8N-ヒドロキシ-2-(4-(1-(トリフルオロメチル)シクロプロピル)フェニル)アセトイミダミド(0.320g、1.24mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.350g、0.65mmol)を淡黄色の油として得た。LCMS m/z 555.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.40(d,J=8.0Hz,2H)、7.29(d,J=8.1Hz,2H)、4.11-4.00(m,6H)、3.54(ddd,J=23.4,10.9,4.5Hz,1H)、3.38-3.32(m,1H)、3.23(ddd,J=16.9,8.7,4.5Hz,1H)、1.35-1.29(m,2H)、1.28-1.19(m,15H)、1.10-1.04(m,2H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.350g、0.65mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.226g、0.55mmol)を透明な無色の油として得た。LCMS m/z 353.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.40(d,J=8.0Hz,2H)、7.29(d,J=8.1Hz,2H)、6.21(d,J=1.3Hz,1H)、5.92-5.84(m,1H)、4.05(s,2H)、3.90(s,2H)、1.35-1.29(m,2H)、1.23(s,9H)、1.10-1.05(m,2H)。
tert-ブチル2-((3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.226g、0.55mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.164g、0.46mmol、89%、99%純度)を透明な無色の油として得た。LCMS m/z 353.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,1H)、7.41(d,J=7.9Hz,2H)、7.29(d,J=8.1Hz,2H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.4Hz,1H)、4.07(s,2H)、3.91(s,2H)、1.36-1.28(m,2H)、1.14-1.07(m,2H)。
N-ヒドロキシ-1-(4-(トリフルオロメトキシ)フェニル)シクロプロパン-1-カルボキシミダミド(0.971g、3.73mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.088g、1.6mmol、77%純度)を褐色の油として得た。LCMS m/z 535.2(M+H)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.088g、1.6mmol、77%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.539g、1.3mmol)を無色の油として得た。LCMS m/z 355.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.51(d,J=8.1Hz,2H)、7.34(d,J=8.1Hz,2H)、6.21(s,1H)、5.89(s,1H)、3.90(s,2H)、1.59-1.23(m,13H)。
tert-ブチル2-((3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.539g、1.3mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(371mg、1.0mmol)を無色の油として得た。LCMS m/z 355.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.95-12.70(m,1H)、7.61-7.45(m,2H)、7.42-7.26(m,2H)、6.27(s,1H)、5.91(s,1H)、3.89(s,2H)、1.52-1.35(m,4H)。
1-(4-ブロモフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(1.29g、4.30mmol、85%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.80g、3.1mmol、90%純度)を白色の固体として得た。LCMS m/z 551.1/553.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.59-7.48(m,2H)、7.40-7.25(m,2H)、4.15-3.97(m,4H)、3.60-3.43(m,1H)、3.32-3.26(m,1H)、3.25-3.11(m,1H)、1.53-1.31(m,13H)、1.25(q,J=6.8Hz,6H)。
tert-ブチル3-(3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.80g、3.1mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.71g、1.7mmol)を透明な無色の油として得た。LCMS m/z 349.1/351.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.58-7.48(m,2H)、7.39-7.27(m,2H)、6.24-6.19(m,1H)、5.90-5.84(m,1H)、3.89(s,2H)、1.47-1.42(m,2H)、1.41-1.35(m,2H)、1.33(s,9H)。
tert-ブチル2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.71g、1.7mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~35%MTBE/イソヘキサン)により精製して、次に分取HPLC(Waters XSelect CSH C18 OBD分取カラム、130Å、5μm、30mmX100mmカラム、水中35~65%MeCN 0.1%ギ酸)によりさらに精製して、2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.447g、1.2mmol)を白色の固体として得た。LCMS m/z 349.1/351.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.57-7.51(m,2H)、7.38-7.32(m,2H)、6.26(d,J=1.2Hz,1H)、5.88(q,J=1.3Hz,1H)、3.88(d,J=1.0Hz,2H)、1.48-1.43(m,2H)、1.39-1.34(m,2H)。
2-(4-ブトキシフェニル)-N-ヒドロキシアセトイミダミド(2.0g、7.9mmol、88%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.4g、2.3mmol、81%純度)を濃いオレンジ色の油として得た。LCMS m/z 519.2(M+Na)+(ES+)。
tert-ブチル3-(3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.4g、2.3mmol、81%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(400mg、1.0mmol)を黄色の油として得た。LCMS m/z 317.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.20-7.13(m,2H)、6.87-6.82(m,2H)、6.21(d,J=1.3Hz,1H)、5.88(d,J=1.4Hz,1H)、3.95(s,2H)、3.90(s,2H)、1.72-1.62(m,2H)、1.49-1.33(m,4H)、1.26(s,9H)、0.92(t,J=7.4Hz,3H)。
tert-ブチル2-((3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(400mg、1.0mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(150mg、0.45mmol)を粘着性のオレンジ色の油として得た。LCMS m/z 317.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、7.21-7.13(m,2H)、6.89-6.82(m,2H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.4Hz,1H)、3.97(s,2H)、3.93(t,J=6.5Hz,2H)、3.90(s,2H)、1.74-1.62(m,2H)、1.43(h,J=7.4Hz,2H)、0.93(t,J=7.4Hz,3H)。
1-(4-クロロ-3-フルオロフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(2.00g、7.0mmol、80%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.50g、0.86mmol、87%純度)を濃いオレンジ色の油として得た。LCMS m/z 503.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.56(t,J=8.2Hz,1H)、7.42(dd,J=10.5,2.1Hz,1H)、7.24(ddd,J=8.4,2.1,0.8Hz,1H)、4.13-4.05(m,4H)、3.63-3.47(m,1H)、3.38-3.27(m,1H)、3.25-3.16(m,1H)、1.43-1.40(m,2H)、1.35(s,9H)、1.29-1.21(m,8H)。
tert-ブチル3-(3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.50g、0.86mmol、87%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.21g、0.53mmol)を黄色の油として得た。LCMS m/z 379.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.56(t,J=8.2Hz,1H)、7.43(dd,J=10.5,2.1Hz,1H)、7.25(ddd,J=8.3,2.1,0.8Hz,1H)、6.22(d,J=1.2Hz,1H)、5.89(q,J=1.2Hz,1H)、3.92-3.87(m,2H)、1.46(dq,J=6.3,2.6,2.1Hz,4H)、1.34(s,9H)。
tert-ブチル2-((3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.21g、0.53mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(150mg、0.46mmol)を黄色の油として得た。LCMS m/z 323.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,1H)、7.56(t,J=8.2Hz,1H)、7.46(dd,J=10.6,2.1Hz,1H)、7.26(dt,J=8.3,1.4Hz,1H)、6.27(d,J=1.2Hz,1H)、5.91(q,J=1.3Hz,1H)、3.90(s,2H)、1.52-1.46(m,2H)、1.46-1.40(m,2H)。
N-ヒドロキシデカニミダミド(2.50g、8.05mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-ノニル-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.70g、1.4mmol、90%純度)を濃いオレンジ色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.14-4.05(m,4H)、3.56(ddd,J=23.5,11.3,4.3Hz,1H)、3.38-3.33(m,1H)、3.23(ddd,J=16.8,8.6,4.3Hz,1H)、2.64(t,J=7.3Hz,2H)、1.66-1.56(m,2H)、1.37(s,9H)、1.27-1.20(m,18H)、0.86(t,J=6.7Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-ノニル-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.70g、1.4mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-ノニル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.20g、0.52mmol、87%純度)を黄色の油として得た。LCMS m/z 281.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.90(q,J=1.2Hz,1H)、3.91(d,J=1.1Hz,2H)、2.64(t,J=7.4Hz,2H)、1.61(p,J=7.0Hz,2H)、1.34(s,9H)、1.29-1.20(m,12H)、0.89-0.80(m,3H)。
tert-ブチル2-((3-ノニル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.20g、0.52mmol、87%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、2-((3-ノニル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(25mg、88μmol)を無色の油として得た。LCMS m/z 281.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.3Hz,1H)、3.90(s,2H)、2.64(t,J=7.5Hz,2H)、1.62(p,J=7.3Hz,2H)、1.33-1.18(m,12H)、0.91-0.82(m,3H)。
8,8,8-トリフルオロ-N-ヒドロキシ-2-メチルオクタニミダミド(1.70g、6.3mmol、84%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.20g、0.40mmol)を濃いオレンジ色の油として得た。LCMS m/z 523.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.00(m,4H)、3.56(ddd,J=23.4,11.1,4.4Hz,1H)、3.39-3.33(m,1H)、3.23(ddd,J=16.8,8.5,4.4Hz,1H)、2.91(dt,J=7.8,6.4Hz,1H)、2.79(t,J=6.2Hz,1H)、2.28-2.12(m,3H)、1.66-1.39(m,4H)、1.38-1.35(m,9H)、1.29-1.22(m,7H)、1.23-1.16(m,4H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.20g、0.40mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(80mg、0.21mmol)を黄色の油として得た。LCMS m/z 321.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.3Hz,1H)、5.90(q,J=1.3Hz,1H)、3.92(d,J=1.1Hz,2H)、2.95-2.87(m,1H)、2.25-2.14(m,2H)、1.67-1.58(m,1H)、1.57-1.50(m,1H)、1.47-1.39(m,3H)、1.34(s,9H)、1.32-1.23(m,3H)、1.20(d,J=7.0Hz,3H)。19F NMR(471MHz,DMSO-d6)δ-64.82。
tert-ブチル2-((3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(80mg、0.21mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(45mg、0.14mmol)を黄色の油として得た。LCMS m/z 321.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、6.27(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、3.91(s,2H)、2.96-2.85(m,1H)、2.28-2.11(m,2H)、1.71-1.59(m,1H)、1.58-1.49(m,1H)、1.49-1.38(m,2H)、1.38-1.26(m,2H)、1.26-1.13(m,5H)。
1-ヒドロキシベンゾトリアゾール水和物(1.04g、6.82mmol)およびN-(3-ジメチルアミノプロピル)-N’-エチルカルボジイミドハイドロクロライド(1.31g、6.82mmol)を、ジメチルホルムアミド(9mL)中の4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(0.347g、1.12mmol)の溶液に室温で加えた。混合物を室温で45分間撹拌した後に、ジメチルホルムアミド(7mL)中の1-アミノデカン-2-オンハイドロクロライド(1.28g、6.15mmol)の溶液を滴下して加えた。トリエチルアミン(0.86mL、6.15mmol)を滴下して加え、混合物を室温で16時間撹拌した。反応物を1M HCl(50mL)に注ぎ、EtOAc(3×25mL)で抽出した。合わせた有機層を飽和水性NaHCO3(30mL)、ブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル2-(ジエトキシホスホリル)-4-オキソ-4-((2-オキソデシル)アミノ)ブタノエート(560mg、1.1mmol、90%純度)を濃い黄色のガムとして得た。LCMS m/z 464.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.30(t,J=5.7Hz,1H)、4.10-4.00(m,4H)、3.88(d,J=5.6Hz,2H)、3.23(ddd,J=23.4,11.5,3.4Hz,1H)、2.85-2.73(m,1H)、2.54-2.52(m,1H)、2.42-2.35(m,2H)、1.46-1.41(m,2H)、1.38(s,9H)、1.28-1.23(m,16H)、0.86(s,3H)。
ローソン試薬(78mg、0.19mmol)を、THF(2mL)中のtert-ブチル2-(ジエトキシホスホリル)-4-オキソ-4-((2-オキソデシル)アミノ)ブタノエート(0.15g、0.32mmol)の溶液に加えた。混合物を70℃に2時間加熱した。さらなるローソン試薬(65mg、0.16mmol)を加え、温度を70℃に1時間維持した。さらなるローソン試薬(39mg、0.1mmol)を加え、反応物を70℃で16時間加熱した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチルチアゾール-2-イル)プロパノエート(0.174g、0.22mmol、59%純度)を淡黄色の油として得た。LCMS m/z 462.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.37(s,1H)、4.13-4.05(m,4H)、3.87-3.81(m,2H)、3.46-3.41(m,1H)、2.76(t,J=7.3Hz,2H)、1.58-1.53(m,2H)、1.33(s,9H)、1.27-1.24(m,16H)、0.87-0.85(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチルチアゾール-2-イル)プロパノエート(0.174g、0.22mmol、59%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((5-オクチルチアゾール-2-イル)メチル)アクリレート(61mg、0.14mmol、77%純度)を透明な無色の油として得た。LCMS m/z 282.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.37(d,J=1.0Hz,1H)、6.14(d,J=1.5Hz,1H)、5.79-5.73(m,1H)、3.90-3.84(m,2H)、2.76(t,J=7.4,1.0Hz,2H)、1.60-1.50(m,2H)、1.37(s,9H)、1.29-1.22(m,10H)、0.86-0.83(m,3H)。
tert-ブチル2-((5-オクチルチアゾール-2-イル)メチル)アクリレート(61mg、0.14mmol、77%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((5-オクチルチアゾール-2-イル)メチル)アクリル酸(30mg、0.11mmol)を黄色の油として得た。LCMS m/z 282.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.68(s,1H)、7.42-7.31(m,1H)、6.20(d,J=1.5Hz,1H)、5.79(d,J=1.4Hz,1H)、3.88(s,2H)、2.79-2.71(m,2H)、1.61-1.50(m,2H)、1.35-1.21(m,10H)、0.90-0.81(m,3H)。
N-ヒドロキシドデカニミダミド(1.09g、5.1mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-ウンデシル-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.00g、2.0mmol)を褐色の油として得た。LCMS m/z 489.5(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.16-4.00(m,4H)、3.55(ddd,J=23.3,11.1,4.3Hz,1H)、3.40-3.16(m,2H)、2.63(t,J=7.3Hz,2H)、1.66-1.54(m,2H)、1.36(s,9H)、1.32-1.16(m,22H)、0.90-0.81(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-ウンデシル-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.00g、2.0mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-ウンデシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.526g、1.4mmol)を無色の油として得た。LCMS m/z 309.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、3.91(s,2H)、2.64(t,J=7.3Hz,2H)、1.62(t,J=7.3Hz,2H)、1.34(s,9H)、1.31-1.18(m,16H)、0.92-0.80(m,3H)。
tert-ブチル2-((3-ウンデシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.526g、1.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-ウンデシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(318mg、1.0mmol)を無色の油として得た。LCMS m/z 309.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(s,1H)、5.91(s,1H)、3.91(s,2H)、2.64(t,J=7.5Hz,2H)、1.61(p,J=7.2Hz,2H)、1.35-1.17(m,16H)、0.86(t,J=6.9,6.2Hz,3H)。
N-ヒドロキシノン-4-イニミダミド(1.283g、7.63mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.71g、3.8mmol)を褐色の油として得た。LCMS m/z 443.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.17-4.00(m,4H)、3.54(ddd,J=23.3,11.1,4.2Hz,1H)、3.42-3.29(m,1H)、3.23(ddd,J=16.8,8.8,4.3Hz,1H)、2.80(t,J=7.1Hz,2H)、2.56-2.46(m,2H)、2.12-2.01(m,2H)、1.43-1.20(m,19H)、0.84(t,J=7.0Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.71g、3.8mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.498g、1.5mmol)を無色の油として得た。LCMS m/z 263.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.24(d,J=1.2Hz,1H)、5.89(d,J=1.3Hz,1H)、3.92(s,2H)、2.81(t,J=7.1Hz,2H)、2.57-2.47(m,2H)、2.11-2.04(m,2H)、1.39-1.26(m,13H)、0.84(t,J=7.1Hz,3H)。
tert-ブチル2-((3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.498g、1.5mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(325mg、1.2mmol)を無色の油として得た。LCMS m/z 263.6(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、6.28(s,1H)、5.91(s,1H)、3.92(s,2H)、2.82(t,J=7.2Hz,2H)、2.59-2.44(m,2H)、2.15-2.02(m,2H)、1.42-1.22(m,4H)、0.84(t,J=7.1Hz,3H)。
9,9-ジフルオロ-N-ヒドロキシノナニミダミド(0.40g、1.92mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(400mg、0.79mmol)を褐色の油として得た。LCMS m/z 483.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.04(tt,J=56.9,4.5Hz,1H)、4.15-4.02(m,4H)、3.55(ddd,J=23.3,11.0,4.4Hz,1H)、3.40-3.28(m,1H)、3.22(ddd,J=16.8,8.6,4.4Hz,1H)、2.64(t,J=7.4Hz,2H)、1.87-1.68(m,2H)、1.68-1.57(m,2H)、1.42-1.20(m,23H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(400mg、0.79mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.155g、0.39mmol、90%純度)を無色の油として得た。LCMS m/z 303.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(s,1H)、6.21-5.87(m,2H)、3.91(s,2H)、2.65(t,J=7.4Hz,2H)、1.88-1.69(m,2H)、1.63(q,J=7.1Hz,2H)、1.41-1.22(m,17H)。
tert-ブチル2-((3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.155g、0.39mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(91mg、0.30mmol)を無色の油として得た。LCMS m/z 302.9(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(s,1H)、6.22-5.87(m,2H)、3.91(s,2H)、2.65(t,J=7.5Hz,2H)、1.89-1.69(m,2H)、1.64(p,J=7.2Hz,2H)、1.44-1.19(m,8H)。
バージェス試薬(1.19g、5.00mmol)を、THF(7mL)中のtert-ブチル2-(ジエトキシホスホリル)-4-オキソ-4-((2-オキソデシル)アミノ)ブタノエート(0.772g、1.67mmol)の溶液に加えた。混合物を75℃に1時間加熱し、次に室温に冷却し、飽和水性NaHCO3(20mL)でクエンチした。混合物をEtOAc(3×20mL)で抽出し、合わせた有機層をブライン(50mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチルオキサゾール-2-イル)プロパノエート(0.344g、0.65mmol、84%純度)を透明なオレンジ色の油として得た。LCMS m/z 446.4(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.73(t,J=1.2Hz,1H)、4.14-3.99(m,4H)、3.44-3.36(m,1H)、3.17(ddd,J=16.1,11.4,8.1Hz,1H)、3.02(ddd,J=16.2,9.2,3.8Hz,1H)、2.62-2.55(m,2H)、1.59-1.50(m,2H)、1.36(s,9H)、1.30-1.21(m,16H)、0.89-0.83(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチルオキサゾール-2-イル)プロパノエート(0.344g、0.65mmol、84%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((5-オクチルオキサゾール-2-イル)メチル)アクリレート(0.184g、0.54mmol)を透明な無色の油として得た。LCMS m/z 322.4(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.73(t,J=1.1Hz,1H)、6.13(d,J=1.4Hz,1H)、5.73-5.67(m,1H)、3.68(s,2H)、2.58(t,J=7.4Hz,2H)、1.59-1.49(m,2H)、1.37(s,9H)、1.31-1.21(m,10H)、0.88-0.84(m,3H)。
tert-ブチル2-((5-オクチルオキサゾール-2-イル)メチル)アクリレート(0.184g、0.54mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、tert-ブチル2-((5-オクチルオキサゾール-2-イル)メチル)アクリル酸(0.127g、0.47mmol、83%、99%純度)を透明なオレンジ色の油として得た。LCMS m/z 266.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.64(s,1H)、6.72(t,J=1.2Hz,1H)、6.19(d,J=1.4Hz,1H)、5.71-5.67(m,1H)、3.68(s,2H)、2.62-2.55(m,2H)、1.59-1.49(m,2H)、1.32-1.21(m,10H)、0.89-0.83(m,3H)。
10,10,10-トリフルオロ-N-ヒドロキシデカニミダミド(4.52g、11.6mmol、60%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.30g、0.58mmol)をオレンジ色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.15-4.05(m,4H)、3.63-3.49(m,1H)、3.40-3.34(m,1H)、3.28-3.14(m,1H)、2.64(t,J=7.4Hz,2H)、2.29-2.14(m,2H)、1.62(s,2H)、1.48(s,2H)、1.40-1.36(m,10H)、1.34-1.22(m,13H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.30g、0.58mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.11g、0.27mmol)を黄色の油として得た。LCMS m/z 335.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.3Hz,1H)、5.90(d,J=1.2Hz,1H)、3.91(s,2H)、2.65(t,J=7.3Hz,2H)、2.29-2.14(m,2H)、1.67-1.57(m,2H)、1.53-1.39(m,2H)、1.34(s,9H)、1.32-1.25(m,8H)。
tert-ブチル2-((3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.11g、0.27mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、2-((3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(15mg、43μmol)を黄色の油として得た。LCMS m/z 335.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.86(s,1H)、6.26(d,J=1.3Hz,1H)、5.93-5.81(m,1H)、3.90(s,2H)、2.65(t,J=7.5Hz,2H)、2.30-2.14(m,2H)、1.71-1.53(m,2H)、1.53-1.41(m,3H)、1.40-1.21(m,7H)。
4-ブトキシ-N-ヒドロキシベンズイミダミド(1.00g、4.8mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.496g、3.0mmol、62%、96%純度)を褐色の油として得た。LCMS m/z 505.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.94-7.86(m,2H)、7.14-7.06(m,2H)、4.18-4.00(m,6H)、3.66(ddd,J=23.3,10.8,4.6Hz,1H)、3.51-3.26(m,2H)、1.78-1.66(m,2H)、1.52-1.34(m,11H)、1.27(q,J=6.8Hz,6H)、0.95(t,J=7.4Hz,3H)。
tert-ブチル3-(3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.70g、1.2mmol、86%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.20g、0.53mmol)を黄色の油として得た。LCMS m/z 303.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.93-7.87(m,2H)、7.12-7.06(m,2H)、6.28(d,J=1.2Hz,1H)、5.96(q,J=1.3Hz,1H)、4.05(t,J=6.5Hz,2H)、4.01(s,2H)、1.77-1.68(m,2H)、1.51-1.40(m,2H)、1.34(s,9H)、0.95(t,J=7.4Hz,3H)。
tert-ブチル2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.20g、0.53mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(95mg、0.31mmol)を白色の固体として得た。LCMS m/z 303.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.90(s,1H)、7.96-7.84(m,2H)、7.12-7.04(m,2H)、6.31(d,J=1.3Hz,1H)、5.97(s,1H)、4.05(t,J=6.5Hz,2H)、4.00(s,2H)、1.78-1.68(m,2H)、1.51-1.40(m,2H)、0.95(t,J=7.4Hz,3H)。
N-ヒドロキシジスピロ[3.1.36.14]デカン-2-カルボキシミダミド(0.263g、1.4mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.326g、0.69mmol)を淡黄色の油として得た。LCMS m/z 491.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.03(m,4H)、3.63-3.50(m,1H)、3.51-3.41(m,1H)、3.38-3.32(m,1H)、3.22(ddd,J=16.8,8.6,4.4Hz,1H)、2.34-2.26(m,2H)、2.23-2.15(m,2H)、2.11(s,2H)、1.97-1.85(m,6H)、1.80-1.72(m,2H)、1.38(s,9H)、1.30-1.22(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.326g、0.69mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.206g、0.60mmol)を透明な無色の油として得た。LCMS m/z 289.4(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、3.91(s,2H)、3.46(p,J=8.4Hz,1H)、2.34-2.25(m,2H)、2.23-2.15(m,2H)、2.11(s,2H)、1.98-1.84(m,6H)、1.81-1.71(m,2H)、1.34(s,9H)。
tert-ブチル2-((3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.206g、0.60mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)によって精製して、2-((3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.13g、0.45mmol)を無色の油として得た。LCMS m/z 289.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、6.28(d,J=1.2Hz,1H)、5.91(d,J=1.2Hz,1H)、3.90(s,2H)、3.46(p,J=8.5Hz,1H)、2.34-2.24(m,2H)、2.24-2.16(m,2H)、2.11(s,2H)、1.97-1.85(m,6H)、1.81-1.71(m,2H)。
5-(クロロメチル)-3-シクロオクチル-1,2,4-オキサジアゾール(1.85g、7.3mmol、90%純度)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル3-(3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.42g、2.9mmol、90%純度)を無色の油として得た。LCMS m/z 445.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.17-3.99(m,4H)、3.63-3.44(m,1H)、3.30(s,2H)、3.02-2.91(m,1H)、1.95-1.82(m,2H)、1.82-1.44(m,12H)、1.37(s,9H)、1.26(q,J=6.8Hz,6H)。
tert-ブチル3-(3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.42g、2.9mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)、次にRP Flash C18でのクロマトグラフィー(5~80%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル2-((3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.78g、2.2mmol、90%純度)を無色の油として得た。LCMS m/z 265.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(s,1H)、5.91-5.88(m,1H)、3.91(s,2H)、3.02-2.92(m,1H)、1.94-1.82(m,2H)、1.81-1.45(m,12H)、1.34(s,9H)。
tert-ブチル2-((3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.78g、2.2mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物を、RP Flash C18(5~75%MeCN/水0.1%ギ酸)でのクロマトグラフィーによって精製して、2-((3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.600g、2.2mmol)を無色のガムとして得た。LCMS m/z 265.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、6.27(s,1H)、5.92-5.89(m,1H)、3.90(s,2H)、3.07-2.87(m,1H)、1.96-1.83(m,2H)、1.81-1.46(m,12H)。
5-(クロロメチル)-3-シクロヘキシル-1,2,4-オキサジアゾール(6.80g、30.5mmol、90%純度)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(5.7g、12mmol、90%純度)を無色の油として得た。LCMS m/z 417.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.18-3.96(m,4H)、3.64-3.47(m,1H)、3.37-3.32(m,1H)、3.28-3.18(m,1H)、2.81-2.70(m,1H)、1.95-1.82(m,2H)、1.78-1.59(m,2H)、1.36(s,15H)、1.26(q,J=6.8Hz,6H)。
tert-ブチル3-(3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(5.7g、12mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(3.66g、12mmol)を無色の油として得た。LCMS m/z 237.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.27-6.18(m,1H)、5.91-5.87(m,1H)、3.91(s,2H)、2.81-2.70(m,1H)、1.94-1.83(m,2H)、1.79-1.60(m,2H)、1.52-1.21(m,15H)。
tert-ブチル2-((3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(3.66g、12mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(2.64g、11mmol)を無色の油として得た。LCMS m/z 237.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(br.s,1H)、6.29-6.26(m,1H)、5.93-5.90(m,1H)、3.91(s,2H)、2.83-2.69(m,1H)、1.97-1.83(m,2H)、1.78-1.59(m,3H)、1.54-1.19(m,5H)。
5-(クロロメチル)-3-シクロヘプチル-1,2,4-オキサジアゾール(5.0g、21mmol、90%純度)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(4.6g、9.6mmol、90%純度)を無色の油として得た。LCMS m/z 431.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.05(m,4H)、3.63-3.48(m,1H)、3.41-3.32(m,1H)、3.27-3.17(m,1H)、3.02-2.90(m,1H)、1.97-1.87(m,2H)、1.76-1.44(m,10H)、1.37(s,9H)、1.31-1.22(m,6H)。
tert-ブチル3-(3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(4.6g、9.6mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(2.44g、7.6mmol)を無色の油として得た。LCMS m/z 251.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.27-6.18(m,1H)、5.93-5.83(m,1H)、3.91(s,2H)、3.03-2.88(m,1H)、1.98-1.87(m,2H)、1.76-1.44(m,10H)、1.33(s,9H)。
tert-ブチル2-((3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(2.44g、7.6mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(1.92g、7.3mmol)を無色の油として得た。LCMS m/z 251.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(br.s,1H)、6.36-6.18(m,1H)、5.97-5.85(m,1H)、3.90(s,2H)、3.04-2.85(m,1H)、2.04-1.85(m,2H)、1.82-1.39(m,10H)。
3-(アダマンタン-1-イル)-5-(クロロメチル)-1,2,4-オキサジアゾール(5.32g、18.9mmol、90%純度)から、NMPの代わりにTHFを使用して、一般的な手順A、ステップ1、方法Aに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(4.34g、7.9mmol、85%純度)を透明な淡黄色の油として得た。LCMS m/z 491.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.03(m,4H)、3.63-3.48(m,1H)、3.38-3.32(m,1H)、3.28-3.16(m,1H)、2.07-2.01(m,3H)、1.95-1.86(m,6H)、1.80-1.66(m,6H)、1.37(s,9H)、1.30-1.21(m,6H)。
tert-ブチル3-(3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(4.34g、7.9mmol、85%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(2.60g、6.8mmol、90%純度)を無色の油として得た。LCMS m/z 289.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(s,1H)、5.91-5.88(m,1H)、3.91(s,2H)、2.06-2.00(m,3H)、1.93-1.88(m,6H)、1.79-1.67(m,6H)、1.33(s,9H)。
tert-ブチル2-((3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(2.60g、6.8mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)によって精製して、2-((3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.37g、1.3mmol)を白色の固体として得た。LCMS m/z 289.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(br.s,1H)、6.30-6.24(m,1H)、5.93-5.87(m,1H)、3.91(s,2H)、2.07-1.99(m,3H)、1.95-1.85(m,6H)、1.80-1.66(m,6H)。
1-(3,5-ジクロロフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(2.00g、8.2mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.00g、1.7mmol、87%純度)を黄色の油として得た。LCMS m/z 540.6(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.56(t,J=1.9Hz,1H)、7.43(d,J=1.9Hz,2H)、4.13-4.05(m,4H)、3.53(ddd,J=23.3,10.9,4.4Hz,1H)、3.34-3.27(m,1H)、3.26-3.17(m,1H)、1.53-1.47(m,2H)、1.36(s,9H)、1.29-1.22(m,8H)。
tert-ブチル3-(3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.00g、1.7mmol、87%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-((3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.44g、1.0mmol、91%純度)を無色の油として得た。LCMS m/z 341.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.56(t,J=1.9Hz,1H)、7.44(d,J=1.9Hz,2H)、6.22(d,J=1.2Hz,1H)、5.89(q,J=1.3Hz,1H)、3.91(s,2H)、1.49(t,J=2.5Hz,2H)、1.46(t,J=2.4Hz,2H)、1.34(s,9H)。
tert-ブチル2-((3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.44g、1.0mmol、91%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(215mg、0.63mmol、99%純度)を白色の固体として得た。LCMS m/z 338.8/341.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.56(t,J=1.9Hz,1H)、7.46(d,J=1.9Hz,2H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.3Hz,1H)、3.90(s,2H)、1.48(s,4H)。
N-ヒドロキシ-7-メチルオクタニミダミド(1.70g、9.9mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.10g、2.0mmol、80%純度)を黄色の油として得た。LCMS m/z 469.0(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.06(m,4H)、3.56(ddd,J=23.4,11.1,4.4Hz,1H)、3.39-3.33(m,1H)、3.23(ddd,J=16.8,8.6,4.4Hz,1H)、2.64(t,J=7.3Hz,2H)、1.62(td,J=7.5,7.1,2.6Hz,2H)、1.55-1.44(m,1H)、1.37(s,9H)、1.26(q,J=6.8Hz,10H)、1.16-1.08(m,2H)、0.85(d,J=6.6Hz,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.10g、2.0mmol、80%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(300mg、0.78mmol、84%純度)を黄色の油として得た。LCMS m/z 266.9(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.23(d,J=1.3Hz,1H)、5.90(q,J=1.3Hz,1H)、3.91(d,J=1.0Hz,2H)、2.64(t,J=7.3Hz,2H)、1.67-1.57(m,2H)、1.54-1.45(m,1H)、1.34(s,9H)、1.26(p,J=3.4Hz,4H)、1.15-1.07(m,2H)、0.84(d,J=6.6Hz,6H)。
tert-ブチル2-((3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(300mg、0.78mmol、84%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.14g、0.50mmol)を黄色の油として得た。LCMS m/z 267.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.79(s,1H)、6.28(d,J=1.2Hz,1H)、5.91(d,J=1.3Hz,1H)、3.91(s,2H)、2.65(t,J=7.4Hz,2H)、1.63(p,J=7.2Hz,2H)、1.56-1.44(m,1H)、1.33-1.21(m,4H)、1.19-1.08(m,2H)、0.85(d,J=6.6Hz,6H)。
N-ヒドロキシ-2-(4-ネオペンチルフェニル)アセトイミダミド(1.40g、6.35mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.70g、1.4mmol)を濃いオレンジ色の油として得た。LCMS m/z 516.9(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.17(d,J=7.7Hz,2H)、7.09-7.01(m,2H)、4.07(dd,J=12.7,5.5Hz,4H)、4.00(t,J=2.9Hz,2H)、3.93(dt,J=15.2,7.3Hz,1H)、3.55(ddd,J=23.3,10.9,4.5Hz,1H)、3.39-3.16(m,1H)、2.43(s,2H)、1.40(s,9H)、1.27-1.22(m,6H)、0.85(s,9H)。
3-(3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.70g、1.4mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.20g、0.51mmol)を黄色の油として得た。LCMS m/z 393.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.20-7.15(m,2H)、7.08-7.03(m,2H)、6.21(d,J=1.2Hz,1H)、5.89(q,J=1.3Hz,1H)、4.00(s,2H)、3.91(d,J=1.0Hz,2H)、2.43(s,2H)、1.25(s,9H)、0.85(s,9H)。
tert-ブチル2-((3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.20g、0.51mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.12g、0.36mmol)を黄色の油として得た。LCMS m/z 315.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、7.20-7.13(m,2H)、7.11-7.04(m,2H)、6.27(d,J=1.2Hz,1H)、5.91(q,J=1.3Hz,1H)、4.02(s,2H)、3.91(d,J=1.0Hz,2H)、2.44(s,2H)、0.86(s,9H)。
N-ヒドロキシ-2-(4-プロピルフェニル)アセトイミダミド(1.00g、3.59mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.21g、0.42mmol)をオレンジ色の油として得た。LCMS m/z 489.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.17(d,J=8.1Hz,2H)、7.12(d,J=8.2Hz,2H)、4.11-4.03(m,4H)、3.99(s,2H)、3.54(ddd,J=23.3,10.9,4.5Hz,1H)、3.38-3.33(m,1H)、3.22(ddd,J=16.8,8.8,4.5Hz,1H)、2.57-2.51(m,2H)、1.61-1.50(m,2H)、1.29(s,9H)、1.23(t,J=7.0Hz,6H)、0.88(t,J=7.3Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.21g、0.42mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(90mg、0.24mmol、90%純度)を粘着性の黄色の油として得た。LCMS m/z 287.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.17(d,J=8.1Hz,2H)、7.12(d,J=8.2Hz,2H)、6.21(d,J=1.3Hz,1H)、5.88(q,J=1.2Hz,1H)、3.99(s,2H)、3.90(s,2H)、2.54-2.47(m,2H)、1.61-1.52(m,2H)、1.25(s,9H)、0.90-0.83(m,3H)。
tert-ブチル2-((3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(90mg、0.24mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(55mg、0.19mmol)を黄色の油として得た。LCMS m/z 287.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.17(d,J=8.2Hz,2H)、7.13(d,J=8.2Hz,2H)、6.27(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、4.00(s,2H)、3.91(s,2H)、2.55-2.52(m,2H)、1.64-1.50(m,2H)、0.88(t,J=7.3Hz,3H)。
4-(1,1-ジフルオロプロピル)-N-ヒドロキシベンズイミダミド(0.90g、3.8mmol、90%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.10g、2.1mmol)を濃い黄色の油として得た。LCMS m/z 511.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.10(d,J=8.1Hz,2H)、7.75-7.70(m,2H)、4.18-4.07(m,4H)、3.69(ddd,J=23.4,10.7,4.7Hz,1H)、3.54-3.35(m,2H)、2.26(tq,J=16.9,7.5Hz,2H)、1.39(s,9H)、1.31-1.23(m,6H)、0.93(t,J=7.4Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.10g、2.1mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-((3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.68g、1.8mmol)を無色の油として得た。LCMS m/z 309.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.10(d,J=8.3Hz,2H)、7.71(d,J=8.4Hz,2H)、6.30(d,J=1.2Hz,1H)、5.99(q,J=1.2Hz,1H)、4.07(s,2H)、2.34-2.17(m,2H)、1.34(s,9H)、0.93(t,J=7.4Hz,3H)。
tert-ブチル2-((3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.68g、1.8mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、2-((3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.47g、1.5mmol)を白色の固体として得た。LCMS m/z 309.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.89(s,1H)、8.10(d,J=8.2Hz,2H)、7.71(d,J=8.3Hz,2H)、6.34(d,J=1.2Hz,1H)、6.02(d,J=1.4Hz,1H)、4.06(s,2H)、2.25(ddt,J=24.2,16.8,7.5Hz,2H)、0.93(t,J=7.4Hz,3H)。
N-ヒドロキシ-4-(1-プロピルシクロプロピル)ベンズイミダミド(1.00g、4.1mmol、90%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.30g、2.4mmol、90%純度)を濃いオレンジ色の油として得た。LCMS m/z 493.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.89(d,J=8.3Hz,2H)、7.44(d,J=8.5Hz,2H)、4.17-4.06(m,4H)、3.66(ddd,J=23.4,10.8,4.6Hz,1H)、3.51-3.39(m,2H)、1.63-1.55(m,2H)、1.37(s,10H)、1.31-1.22(m,7H)、0.87-0.79(m,5H)、0.78-0.72(m,2H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.30g、2.4mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-((3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.56g、1.4mmol)を無色の油として得た。LCMS m/z 313.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.92-7.86(m,2H)、7.45-7.41(m,2H)、6.28(d,J=1.2Hz,1H)、5.97(q,J=1.3Hz,1H)、4.03(s,2H)、1.62-1.56(m,2H)、1.34(s,9H)、1.30-1.20(m,2H)、0.87-0.79(m,5H)、0.79-0.72(m,2H)。
tert-ブチル2-((3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.56g、1.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.47g、1.5mmol)を黄色の油として得た。LCMS m/z 313.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.87(s,1H)、7.89(d,J=8.0Hz,2H)、7.43(d,J=8.0Hz,2H)、6.33(s,1H)、6.00(s,1H)、4.02(s,2H)、1.64-1.52(m,2H)、1.25(p,J=7.6Hz,2H)、0.87-0.78(m,5H)、0.78-0.72(m,2H)。
N-ヒドロキシ-4-(3,3,3-トリフルオロプロピル)ベンズイミダミド(0.42g、1.8mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.55g、1.1mmol)を粘着性の黄色の油として得た。LCMS m/z 529.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.95-7.89(m,2H)、7.54-7.48(m,2H)、4.18-4.07(m,4H)、3.68(ddd,J=23.4,10.8,4.6Hz,1H)、3.52-3.33(m,2H)、2.96-2.88(m,2H)、2.74-2.58(m,2H)、1.38(s,9H)、1.32-1.23(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.55g、1.1mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-((3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.38g、0.94mmol)を無色の油として得た。LCMS m/z 327.5(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.95-7.88(m,2H)、7.52-7.46(m,2H)、6.29(d,J=1.1Hz,1H)、5.98(q,J=1.2Hz,1H)、4.05-4.03(m,2H)、2.95-2.87(m,2H)、2.73-2.58(m,2H)、1.34(s,9H)。
tert-ブチル2-((3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.38g、0.94mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(255mg、0.77mmol)を白色の固体として得た。LCMS m/z 327.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.89(s,1H)、7.97-7.89(m,2H)、7.56-7.43(m,2H)、6.33(d,J=1.2Hz,1H)、6.00(d,J=1.3Hz,1H)、4.03(s,2H)、2.99-2.86(m,2H)、2.74-2.57(m,2H)。
2-(4-クロロフェニル)-2,2-ジフルオロ-N-ヒドロキシアセトイミダミド(1.11g、5.1mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.592g、0.67mmol、56%純度)を褐色がかった固体として得た。LCMS m/z 517.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.65(s,4H)、4.14-4.00(m,4H)、3.64(ddd,J=23.4,10.6,4.8Hz,1H)、3.52-3.27(m,2H)、1.30(s,9H)、1.28-1.20(m,6H)。
tert-ブチル3-(3-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.592g、0.67mmol、56%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.045g、0.14mmol)を白色の固体として得た。LCMS m/z 313.9(M-tBu-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 7.65(s,4H)、6.27(s,1H)、5.96(s,1H)、4.05(s,2H)、1.24(s,9H)。
tert-ブチル2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.072g、0.17mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(255mg、0.77mmol)を白色の固体として得た。LCMS m/z 313.4(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.91(s,1H)、7.65(s,4H)、6.31(s,1H)、5.98(s,1H)、4.04(s,2H)。
N-ヒドロキシ-4-(5,5,5-トリフルオロペンチル)ベンズイミダミド(1.30g、4.3mmol、86%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.23g、2.3mmol)を緑色の油として得た。LCMS m/z 557.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.94-7.87(m,2H)、7.45-7.36(m,2H)、4.20-4.07(m,4H)、3.67(ddd,J=23.3,10.8,4.6Hz,1H)、3.51-3.33(m,2H)、2.69(t,J=7.6Hz,2H)、2.37-2.21(m,2H)、1.69(p,J=7.7Hz,2H)、1.58-1.46(m,2H)、1.38(s,9H)、1.32-1.22(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.23g、2.3mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-((3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.86g、1.9mmol、90%純度)を無色の油として得た。LCMS m/z 433.0(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.93-7.88(m,2H)、7.42-7.37(m,2H)、6.28(d,J=1.2Hz,1H)、5.97(d,J=1.3Hz,1H)、4.03(s,2H)、2.69(t,J=7.7Hz,2H)、2.38-2.21(m,2H)、1.68(p,J=7.6Hz,2H)、1.57-1.46(m,2H)、1.34(s,9H)。
tert-ブチル2-((3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.86g、1.9mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、2-((3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(488mg、1.3mmol)を白色の固体として得た。LCMS m/z 355.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.88(s,1H)、7.94-7.87(m,2H)、7.43-7.36(m,2H)、6.33(d,J=1.2Hz,1H)、6.00(d,J=1.3Hz,1H)、4.02(s,2H)、2.69(t,J=7.6Hz,2H)、2.38-2.20(m,2H)、1.75-1.62(m,2H)、1.57-1.44(m,2H)。
4-(2-シクロプロピルエチル)-N-ヒドロキシベンズイミダミド(1.05g、4.0mmol、78%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.80g、2.9mmol、77%純度)を黄色の油として得た。LCMS m/z 501.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.89(d,J=7.9Hz,2H)、7.43-7.38(m,2H)、4.17-4.07(m,4H)、3.67(ddd,J=23.3,10.8,4.6Hz,1H)、3.51-3.33(m,2H)、2.74(t,J=6.6Hz,2H)、1.51(q,J=7.5Hz,2H)、1.39(s,9H)、1.32-1.23(m,6H),0.77-0.64(m,1H)、0.44-0.35(m,2H)、0.08-0.01(m,2H)。
tert-ブチル3-(3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.80g、2.9mmol、77%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)によって精製して、tert-ブチル2-((3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.82g、1.9mmol、84%純度)を無色の油として得た。LCMS m/z 377.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.94-7.84(m,2H)、7.42-7.37(m,2H)、6.28(d,J=1.2Hz,1H)、5.97(q,J=1.3Hz,1H)、4.03(s,2H)、2.78-2.70(m,2H)、1.54-1.46(m,2H)、1.34(s,9H)、0.76-0.65(m,1H)、0.44-0.36(m,2H)、0.09-0.02(m,2H)。
tert-ブチル2-((3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.82g、1.9mmol、84%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(Waters X-Select Prep-C18、5μm、30x100mmカラム、水中45~75%MeCN 0.1%ギ酸)により精製して、2-((3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸を黄色のガラスとして得た。LCMS m/z 296.7(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.88(s,1H)、7.94-7.82(m,2H)、7.43-7.33(m,2H)、6.32(d,J=1.2Hz,1H)、5.99(d,J=1.3Hz,1H)、4.01(s,2H)、2.78-2.68(m,2H)、1.57-1.43(m,2H)、0.75-0.61(m,1H)、0.44-0.33(m,2H)、0.11-0.00(m,2H)。
N-ヒドロキシ-1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロパン-1-カルボキシミダミド(0.97g、3.0mmol)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.34g、2.0mmol、85%純度)を透明な無色のガムとして得た。LCMS m/z 521.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.91-7.82(m,2H)、7.59(d,J=8.4Hz,2H)、4.15-3.92(m,4H)、3.61-3.44(m,1H)、3.39-3.33(m,1H)、3.24-3.14(m,1H)、1.58-1.42(m,4H)、1.33(s,9H)、1.30-1.18(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.34g、2.0mmol、85%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.60g、1.2mmol、90%純度)を透明な無色の油として得た。LCMS m/z 396(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.91-7.84(m,2H)、7.61(d,J=8.4Hz,2H)、6.23-6.19(m,1H)、5.91-5.86(m,1H)、3.90(s,2H)、1.55-1.42(m,4H)、1.32(s,9H)。
tert-ブチル2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.60g、1.2mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.44g、1.0mmol)を白色の固体として得た。LCMS m/z 397.5(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.94-7.75(m,2H)、7.61(d,J=8.4Hz,2H)、6.29-6.22(m,1H)、5.95-5.84(m,1H)、3.90(s,2H)、1.62-1.38(m,4H)。
1-(4-(ジフルオロメトキシ)フェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(1.27g、4.61mmol、88%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.36g、2.5mmol)を透明な無色の油として得た。LCMS m/z 460.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.48-7.36(m,2H)、7.27-6.99(m,3H)、4.14-4.01(m,4H)、3.60-3.42(m,1H)、3.31(s,1H)、3.25-3.13(m,1H)、1.53-1.37(m,4H)、1.35(s,9H)、1.29-1.21(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.36g、2.5mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.98g、2.4mmol)を透明な無色の油として得た。LCMS m/z 337.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.47-7.36(m,2H)、7.28-6.99(m,3H)、6.25-6.16(m,1H)、5.92-5.85(m,1H)、3.88(s,2H)、1.47-1.40(m,2H)、1.38-1.34(m,2H)、1.33(s,9H)。
tert-ブチル2-((3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.98g、2.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.76g、2.1mmol)を淡いオレンジ色のガムとして得た。LCMS m/z 337.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.48-7.39(m,2H)、7.29-6.99(m,3H)、6.33-6.20(m,1H)、5.97-5.81(m,1H)、3.88(s,2H)、1.49-1.42(m,2H)、1.39-1.32(m,2H)。
4-(1,1-ジフルオロペンチル)-N-ヒドロキシベンズイミダミド(0.33g、1.26mmol、92%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.430g、0.82mmol)を淡黄色の油として得た。LCMS m/z 539.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.08(d,J=8.2Hz,2H)、7.72(d,J=8.3Hz,2H)、4.17-4.06(m,4H)、3.68(ddd,J=23.4,10.7,4.6Hz,1H)、3.53-3.32(m,2H)、2.31-2.16(m,2H)、1.38(s,9H)、1.35-1.22(m,10H)、0.88-0.81(m,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.430g、0.82mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.292g、0.73mmol)を透明な無色の油として得た。LCMS m/z 337.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.09(d,J=8.1Hz,2H)、7.75-7.65(m,2H)、6.29(d,J=1.2Hz,1H)、6.02-5.95(m,1H)、4.06(s,2H)、2.30-2.15(m,2H)、1.37-1.26(m,13H)、0.90-0.80(m,3H)。
ギ酸(1.4mL)中のtert-ブチル2-((3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.292g、0.73mmol)を18時間撹拌し、次に濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製し、次にシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により再精製して、2-((3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.170g、0.50mmol)を白色の固体として得た。LCMS m/z 335.2(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.88(s,1H)、8.09(d,J=8.4Hz,2H)、7.75-7.67(m,2H)、6.34(d,J=1.2Hz,1H)、6.06-5.97(m,1H)、4.05(s,2H)、2.31-2.14(m,2H)、1.31(h,J=3.7Hz,4H)、0.90-0.79(m,3H)。19F NMR(376MHz,DMSO-d6)δ-93.47。
1-(4-ブトキシフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(0.262g、0.86mmol、81%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.291g、0.41mmol、74%純度)を淡黄色の油として得た。LCMS m/z 523.4(M +H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.28-7.23(m,2H)、6.90-6.86(m,2H)、4.12-4.03(m,4H)、3.97-3.93(m,2H)、3.51(ddd,J=23.3,10.9,4.4Hz,1H)、3.30-3.24(m,1H)、3.18(ddd,J=16.8,8.8,4.5Hz,1H)、1.72-1.66(m,2H)、1.46-1.40(m,3H)、1.35(s,9H)、1.32-1.20(m,9H)、0.95-0.91(m,3H)。
tert-ブチル3-(3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.291g、0.41mmol、74%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.143g、0.36mmol)を透明な無色の油として得た。LCMS m/z 343.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.29-7.20(m,2H)、6.90-6.81(m,2H)、6.20(d,J=1.2Hz,1H)、5.90-5.83(m,1H)、3.95(t,J=6.4Hz,2H)、3.87(s,2H)、1.73-1.63(m,2H)、1.47-1.36(m,4H)、1.33(s,9H)、1.30(s,2H)、0.93(t,J=7.4Hz,3H)。
tert-ブチル2-((3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.143g、0.36mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製し、次にシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により再精製して、2-((3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.066g、0.19mmol)を白色の固体として得た。LCMS m/z 343.7(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.33-7.23(m,2H)、6.91-6.83(m,2H)、6.25(d,J=1.2Hz,1H)、5.92-5.84(m,1H)、3.95(t,J=6.5Hz,2H)、3.86(s,2H)、1.73-1.64(m,2H)、1.48-1.37(m,4H)、1.31-1.26(m,2H)、0.93(t,J=7.4Hz,3H)。
N-ヒドロキシ-2-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)アセトイミダミド(2.31g、7.55mmol、87%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(2.24g、4.1mmol)を淡黄色の油として得た。LCMS m/z 541.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.41-7.33(m,2H)、7.28-7.18(m,2H)、6.79(tt,J=51.9,3.1Hz,1H)、4.10-4.00(m,6H)、3.54(ddd,J=23.4,10.9,4.5Hz,1H)、3.40-3.17(m,2H)、1.30-1.15(m,15H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(2.24g、4.1mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.20g、2.9mmol)を透明な無色の油として得た。LCMS m/z 361.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.43-7.35(m,2H)、7.26-7.18(m,2H)、6.79(tt,J=51.9,3.1Hz,1H)、6.23-6.18(m,1H)、5.91-5.86(m,1H)、4.08(s,2H)、3.91(s,2H)、1.22(s,9H)。
tert-ブチル2-((3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.20g、2.9mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(847mg、2.3mmol)を無色の油として得た。LCMS m/z 359.2(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.42-7.34(m,2H)、7.23(d,J=8.6Hz,2H)、6.79(tt,J=51.9,3.1Hz,1H)、6.27(d,J=1.3Hz,1H)、5.91(d,J=1.3Hz,1H)、4.10(s,2H)、3.91(s,2H)。19F NMR(376MHz,DMSO-d6)δ-87.41(t,J=5.9Hz)、-137.71(t,J=5.9Hz)。
N-ヒドロキシ-1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロパン-1-カルボキシミダミド(0.878g、2.37mmol、79%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(860mg、1.35mmol、89%純度)を淡黄色の油として得た。LCMS m/z 567.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.51-7.43(m,2H)、7.28-7.20(m,2H)、6.99-6.63(m,1H)、4.14-4.05(m,2H)、4.09-3.98(m,2H)、3.52(ddd,J=23.3,10.9,4.4Hz,1H)、3.38-3.14(m,2H)、1.53-1.37(m,2H)、1.40(s,2H)、1.35(s,9H)、1.25(dd,J=7.1,6.0Hz,4H)、1.25-1.13(m,2H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(860mg、1.35mmol、89%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(357mg、0.78mmol)を透明な無色の油として得た。LCMS m/z 387.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.52-7.44(m,2H)、7.28-7.21(m,2H)、6.97-6.62(m,1H)、6.23-6.18(m,1H)、5.91-5.85(m,1H)、3.89(s,2H)、1.49-1.42(m,2H)、1.42-1.35(m,2H)、1.32(s,9H)。
tert-ブチル2-((3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(357mg、0.78mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(268mg、0.67mmol)を白色の固体として得た。LCMS m/z 385.2(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.53-7.45(m,2H)、7.28-7.21(m,2H)、6.81(t,J=3.1Hz,1H)、6.26(d,J=1.2Hz,1H)、5.89(d,J=1.3Hz,1H)、3.88(s,2H)、1.51-1.42(m,2H)、1.44-1.35(m,2H)。19F NMR(376MHz,DMSO-d6)δ-87.39(t,J=5.9Hz)、-137.70(t,J=5.9Hz)。
ヘプチルマグネシウムブロミド(THF中1M、50mL、50mmol)を、THF(30mL)中のジエチルオキサレート(8.8mL、65mmol)の溶液に-78°で滴下して加えた。混合物を室温に温め、2時間撹拌した。混合物を飽和水性NH4Cl(20mL)でクエンチした。混合物をEtOAc(3×60mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、エチル2-オキソノナノエート(6.89g、31mmol、90%純度)をわずかに黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.22(q,J=7.1Hz,2H)、2.79(t,J=7.2Hz,2H)、1.49(p,J=7.2Hz,2H)、1.36-1.20(m,11H)、0.92-0.79(m,3H)。
DAST(6.4mL、48.1mmol)を、エチル2-オキソノナノエート(6.89g、31mmol、90%純度)に0℃で滴下して加えた。混合物を室温に温め、16時間撹拌した。混合物をDCM(50mL)で希釈し、飽和水性NaHCO3でpH7までクエンチした。水相をDCM(3x80mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、エチル2,2-ジフルオロノナノエート(5.12g、21mmol、90%純度)を黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 4.30(q,J=7.1Hz,2H)、2.17-1.99(m,2H)、1.46-1.17(m,13H)、0.91-0.81(m,3H)。
水酸化リチウム一水和物(1.18g、27.6mmol)を、0℃で水(3.8mL)およびEtOH(0.4mL)中のエチル2,2-ジフルオロノナノエート(5.12g、21mmol、90%純度)の溶液に5分間にわたって加えた。混合物を室温に温め、次に50℃まで2時間加熱した。混合物を1M HClでpH1に酸性化し、MTBE(3×20mL)で抽出した。合わせた有機層を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(40gカートリッジ、0~50%EtOAc/イソヘキサン)により精製して、2,2-ジフルオロノナン酸(1.061g、4.9mmol、90%純度)をわずかに黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 14.55(s,1H)、2.12-1.93(m,2H)、1.53-1.14(m,10H)、0.96-0.78(m,3H)。
T3P(EtOAc中50重量%、5.3mL、10.3mmol)を、ジメチルホルムアミド(6mL)中の2,2-ジフルオロノナン酸(800mg、4.13mmol)、tert-ブチル2-(ジエトキシホスホリル)-4-(ヒドロキシアミノ)-4-イミノブタノエート(1.49g、4.13mmol、90%純度)、およびトリエチルアミン(1.7mL、12.4mmol)の混合物に室温で滴下して加えた。混合物を80℃に加熱し、16時間撹拌した。混合物を室温に冷却し、1M HCl(25mL)で希釈し、EtOAc(3×20mL)で抽出した。合わせた有機相をブライン(3x80mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)プロパノエート(0.316g、0.64mmol)を褐色の油として得た。LCMS m/z 505.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.17-4.03(m,4H)、3.47(ddd,J=22.9,10.9,4.2Hz,1H)、3.38-3.25(m,1H)、3.18(ddd,J=16.1,9.4,4.2Hz,1H)、2.47-2.30(m,2H)、1.49-1.16(m,25H)、0.86(t,J=7.0Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)プロパノエート(0.316g、0.64mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.104g、0.29mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 6.22(s,1H)、5.86(s,1H)、3.84(s,2H)、2.48-2.30(m,2H)、1.49-1.16(m,19H)、0.86(t,J=6.9Hz,3H)。
tert-ブチル2-((5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.104g、0.29mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(57mg、0.19mmol)を無色の油として得た。LCMS m/z 301.3(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.78(s,1H)、6.26(s,1H)、5.84(s,1H)、3.82(s,2H)、2.47-2.29(m,2H)、1.51-1.37(m,2H)、1.37-1.16(m,8H)、0.86(t,J=7.2Hz,3H)。
T3P(EtOAc中50重量%、4.2mL、7.1mmol)を、EtOAc(20mL)中の2-(4-クロロフェニル)-2,2-ジフルオロ酢酸(730mg、3.54mmol)、tert-ブチル2-(ジエトキシホスホリル)-4-(ヒドロキシアミノ)-4-イミノブタノエート(1.26g、3.54mmol、91%純度)、およびトリエチルアミン(1.0mL、7.1mmol)の混合物に滴下して加えた。混合物を室温で18時間撹拌し、次に水(50mL)で希釈し、EtOAc(3x50mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.41g、0.79mmol)を透明な無色のガムとして得た。LCMS m/z 517.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.75-7.63(m,4H)、4.13-3.99(m,4H)、3.52-3.36(m,1H)、3.30-3.22(m,1H)、3.22-3.11(m,1H)、1.30(s,9H)、1.27-1.17(m,6H)。
tert-ブチル3-(5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.41g、0.79mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.250g、0.61mmol、90%純度)を透明な無色の油として得た。LCMS m/z 313.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.77-7.59(m,4H)、6.25-6.14(m,1H)、5.88-5.77(m,1H)、3.82(s,2H)、1.29(s,9H)。
tert-ブチル2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.250g、0.61mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(0.20g、0.6mmol)を白色の固体として得た。LCMS m/z 313.0(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.78(s,1H)、7.79-7.57(m,4H)、6.33-6.17(m,1H)、5.92-5.73(m,1H)、3.81(s,2H)。
2-(4-ブロモフェニル)-2,2-ジフルオロ酢酸(888mg、3.54mmol)から、実施例84、ステップ1と同様の手順を使用して調整した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.435g、0.77mmol)を透明な無色のガムとして得た。LCMS m/z 561.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.87-7.79(m,2H)、7.67-7.59(m,2H)、4.14-3.97(m,4H)、3.52-3.36(m,1H)、3.29-3.22(m,1H)、3.21-3.10(m,1H)、1.30(s,9H)、1.26-1.20(m,6H)。
tert-ブチル3-(5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.435g、0.77mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.15g、0.32mmol、89%純度)を透明な無色の油として得た。LCMS m/z 357.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.91-7.75(m,2H)、7.70-7.58(m,2H)、6.24-6.14(m,1H)、5.88-5.77(m,1H)、3.82(s,2H)、1.29(s,9H)。
tert-ブチル2-((5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.15g、0.32mmol、89%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(0.090g、0.24mmol)を透明な無色のガムとして得た。LCMS m/z 357.0/359.0(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.78(s,1H)、7.89-7.76(m,2H)、7.73-7.53(m,2H)、6.32-6.12(m,1H)、5.92-5.76(m,1H)、3.81(s,2H)。
N-ヒドロキシ-1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロパン-1-カルボキシミダミド(2.82g、9.9mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(3.04g、5.4mmol)を淡黄色の油として得た。LCMS m/z 551.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.72-7.64(m,2H)、7.56-7.48(m,2H)、4.14-3.98(m,4H)、3.53(ddd,J=23.4,10.9,4.4Hz,1H)、3.37-3.27(m,1H)、3.21(ddd,J=16.9,8.9,4.4Hz,1H)、1.54-1.43(m,4H)、1.35(s,9H)、1.24(d,J=7.0Hz,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(3.04g、5.4mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.03g、2.4mmol)を透明な無色のガムとして得た。LCMS m/z 371.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.72-7.65(m,2H)、7.58-7.49(m,2H)、6.23-6.19(m,1H)、5.91-5.86(m,1H)、3.90(s,2H)、1.52-1.40(m,4H)、1.33(s,9H)。
tert-ブチル2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.03g、2.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)によって精製して、2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(815mg、2.2mmol)を無色のガムとして得た。LCMS m/z 371.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、7.72-7.65(m,2H)、7.57-7.50(m,2H)、6.26(d,J=1.2Hz,1H)、5.89(d,J=1.3Hz,1H)、3.89(s,2H)、1.50(td,J=5.7,2.1Hz,2H)、1.44(td,J=5.7,2.0Hz,2H)。19F NMR(376MHz,DMSO-d6)δ-42.00。
7,7,9,9,9-ペンタフルオロ-N-ヒドロキシノナニミダミド(3.46g、9.24mmol、70%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(3.18g、5.7mmol)を淡黄色の油として得た。LCMS m/z 481.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.15-4.02(m,4H)、3.55(ddd,J=23.4,11.1,4.4Hz,1H)、3.41-3.12(m,2H)、2.65(t,J=7.3Hz,2H)、2.01-1.83(m,2H)、1.69-1.58(m,2H)、1.54-1.40(m,2H)、1.36(s,9H)、1.35-1.29(m,2H)、1.25(q,J=6.8Hz,6H)[2つのプロトンはDMSO-d6ピークによって不明瞭である]。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(3.18g、5.7mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、tert-ブチル2-((3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.87g、4.4mmol)を透明な無色の油として得た。LCMS m/z 430.3(M+NH4)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 6.22(d,J=1.2Hz,1H)、5.92-5.86(m,1H)、3.91(d,J=1.1Hz,2H)、3.30-3.12(m,2H)、2.66(t,J=7.4Hz,2H)、2.00-1.84(m,2H)、1.70-1.58(m,2H)、1.52-1.38(m,2H)、1.34(s,11H)。
tert-ブチル2-((3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.87g、4.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-((3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(1.22g、3.4mmol)を無色の油として得た。LCMS m/z 357.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.80(s,1H)、6.27(d,J=1.2Hz,1H)、5.91(d,J=1.3Hz,1H)、3.93-3.88(m,2H)、3.29-3.16(m,2H)、2.66(t,J=7.5Hz,2H)、2.02-1.84(m,2H)、1.65(p,J=7.5Hz,2H)、1.51-1.39(m,2H)、1.39-1.27(m,2H)。19F NMR(376MHz,DMSO-d6)δ-60.23,-96.59。
メタノール(25mL)中のエチル2,2-ジフルオロノナノエート(1.00g、4.50mmol)およびアンモニア(メタノール中7M、5mL、0.2mol)の混合物を、室温で16時間撹拌した。混合物を濃縮して、2,2-ジフルオロノナンアミド(0.88g、4.0mmol、88%純度)を白色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 8.05(s,1H)、7.84(s,1H)、2.06-1.90(m,2H)、1.38-1.22(m,10H)、0.90-0.81(m,3H)。
TFAA(2.5mL、18mmol)を、1,4-ジオキサン(10mL)中の2,2-ジフルオロノナンアミド(0.88g、4.0mmol、88%純度)およびトリエチルアミン(2.5mL、18mmol)の溶液に0℃で滴下して加えた。混合物を室温に温め、16時間撹拌した。混合物を氷水(20mL)に注ぎ、EtOAc(3x15mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%EtOAc/イソヘキサン)により精製して、2,2-ジフルオロノナンニトリル(0.297g、1.7mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 2.46-2.31(m,2H)、1.53-1.43(m,2H)、1.40-1.20(m,8H)、0.90-0.82(m,3H)。19F NMR(376MHz,DMSO-d6)δ-88.52。
2,2-ジフルオロノナンニトリル(0.297g、1.7mmol)から、中間体23で記載した手順に従って調製し、2,2-ジフルオロ-N-ヒドロキシノナニミダミド(0.210g、0.95mmol、94%純度)を白色の固体として得た。LCMS m/z 209.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 9.78(s,1H)、5.75(s,2H)、2.10-1.95(m,2H)、1.44-1.34(m,2H)、1.31-1.23(m,8H)、0.89-0.81(m,3H)。19F NMR(376MHz,DMSO-d6)δ-98.44。
2,2-ジフルオロ-N-ヒドロキシノナニミダミド(0.210g、0.95mmol、94%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.193g、0.40mmol)を無色の油として得た。LCMS m/z 505.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 4.16-4.02(m,4H)、3.65(ddd,J=23.5,10.7,4.8Hz,1H)、3.51-3.33(m,2H)、2.34-2.19(m,2H)、1.41-1.18(m,25H)、0.89-0.81(m,3H)。19F NMR(376MHz,DMSO-d6)δ-97.06(d,J=267.3Hz)、-97.94(d,J=267.3Hz)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.193g、0.40mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.0767g、0.21mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 6.28(d,J=1.1Hz,1H)、6.01-5.93(m,1H)、4.06(s,2H)、2.36-2.20(m,2H)、1.32(m,19H)、0.89-0.81(m,3H)。19F NMR(376MHz,DMSO-d6)δ-97.46。
tert-ブチル2-((3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.0767g、0.21mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、2-((3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.0485g、0.16mmol)を白色の固体として得た。LCMS m/z 303.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 1 2.92(s,1H)、6.31(d,J=1.2Hz,1H)、5.98(d,J=1.4Hz,1H)、4.04(s,2H)、2.37-2.20(m,2H)、1.44-1.35(m,2H)、1.34-1.19(m,8H)、0.91-0.81(m,3H)。19F NMR(376MHz,DMSO-d6)δ-97.48。
T3P(EtOAc中50重量%、1.9mL、3.2mmol)を、EtOAc(10mL)中のtert-ブチル2-(ジエトキシホスホリル)-4-(ヒドロキシアミノ)-4-イミノブタノエート(500mg、1.54mmol)、1-(4-ブロモフェニル)シクロプロパン-1-カルボン酸(372mg、1.54mmol)、およびトリエチルアミン(0.7mL、5.0mmol)の溶液に滴下して加えた。混合物を室温で1時間撹拌し、次に50℃に加熱し、1時間撹拌した。混合物をEtOAc(20mL)で希釈し、水(50mL)およびブライン(50mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。残留物をTHF(20mL)中に入れ、炭酸セシウム(1.51g、4.63mmol)を加えた。混合物を70℃に加熱し、1時間撹拌して、次に室温に冷却し、水(20mL)に注ぎ、EtOAc(3x15mL)で抽出した。合わせた有機層をブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(5-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.164g、0.26mmol、84%純度)を透明な無色の油として得た。LCMS m/z 529.2/531.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.60-7.55(m,2H)、7.41-7.36(m,2H)、4.09-4.04(m,4H)、3.30-3.22(m,1H)、3.12(ddd,J=16.0,11.1,8.5Hz,1H)、2.97(ddd,J=16.0,9.7,3.9Hz,1H)、1.70-1.64(m,2H)、1.60-1.56(m,2H)、1.33(s,9H)、1.26-1.22(m,6H。
tert-ブチル3-(5-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.164g、0.26mmol、84%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~40%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(80mg、0.20mmol)を無色の油として得た。LCMS m/z 349.3/351.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.60-7.54(m,2H)、7.42-7.36(m,2H)、6.12(d,J=1.3Hz,1H)、5.71(d,J=1.3Hz,1H)、3.62(s,2H)、1.71-1.64(m,2H)、1.59-1.51(m,2H)、1.36(s,9H)。
tert-ブチル2-((5-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(80mg、0.20mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により精製して、2-((5-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(28mg、0.08mmol)を無色の固体として得た。LCMS m/z 349.1/351.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.66(s,1H)、7.61-7.51(m,2H)、7.44-7.37(m,2H)、6.19(d,J=1.3Hz,1H)、5.72(d,J=1.4Hz,1H)、3.62(s,2H)、1.70-1.62(m,2H)、1.62-1.51(m,2H)。
2-(4-ブロモフェニル)-2,2-ジフルオロ-N-ヒドロキシアセトイミダミド(2.4g、7.7mmol、85%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.66g、2.8mmol、90%純度)を淡褐色のガムとして得た。LCMS m/z 483.1/485.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.82-7.72(m,2H)、7.60-7.51(m,2H)、4.13-4.00(m,4H)、3.71-3.55(m,1H)、3.51-3.34(m,2H)、1.29(s,9H)、1.26-1.20(m,6H)。
tert-ブチル3-(3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.800g、1.34mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.200g、0.43mmol、90%純度)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.78(d,J=8.5Hz,2H)、7.61-7.51(m,2H)、6.29-6.20(m,1H)、5.98-5.91(m,1H)、4.04(s,2H)、1.23(s,9H)。
tert-ブチル2-((3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.200g、0.43mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.15g、0.39mmol)を白色の固体として得た。LCMS m/z 357.0/359.0(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.91(s,br.1H)、7.87-7.68(m,2H)、7.66-7.50(m,2H)、6.36-6.21(m,1H)、6.04-5.87(m,1H)、4.04(s,2H)。
トルエン(12mL)中のtert-ブチル3-(3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.800g、1.34mmol、90%純度)、ブチルボロン酸(520mg、5.10mmol)、および炭酸カリウム(810mg、5.86mmol)の混合物を、窒素で10分間スパージングして、次にPd(PPh3)4(0.166g、0.14mol)を加えた。混合物を100℃で1.5時間撹拌し、次に室温に冷却し、セライトで濾過し、EtOAc(3×40mL)で洗浄した。濾液を濃縮した。粗生成物をRP Flash C18でのクロマトグラフィー(5~100%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.37g、0.68mmol)を淡褐色の油として得た。LCMS m/z 461.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.49(d,J=8.3Hz,2H)、7.36(d,J=8.1Hz,2H)、4.15-3.94(m,4H)、3.71-3.55(m,1H)、3.52-3.33(m,2H)、2.63(t,J=7.7Hz,2H)、1.62-1.49(m,2H)、1.29(s,9H)、1.26-1.16(m,6H)、0.89(t,J=7.3Hz,3H)[2つのプロトンは分解されていない]。
tert-ブチル3-(3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.37g、0.68mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.16g、0.38mmol、92%純度)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.49(d,J=8.2Hz,2H)、7.36(d,J=8.0Hz,2H)、6.31-6.21(m,1H)、6.01-5.90(m,1H)、4.04(s,2H)、2.63(t,J=7.7Hz,2H)、1.61-1.46(m,2H)、1.34-1.25(m,2H)、1.23(s,9H)、0.89(t,J=7.3Hz,3H)。
tert-ブチル2-((3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.16g、0.38mmol、92%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(90mg、0.25mmol)を淡褐色のガムとして得た。LCMS m/z 335.0(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.91(s,br.1H)、7.53-7.44(m,2H)、7.37(d,J=8.0Hz,2H)、6.35-6.24(m,1H)、6.03-5.90(m,1H)、4.03(s,2H)、2.64(t,J=7.7Hz,2H)、1.65-1.46(m,2H)、1.38-1.23(m,2H)、0.89(t,J=7.4Hz,3H)。
2,2-ジフルオロ-N-ヒドロキシ-2-(4-(トリフルオロメチル)フェニル)アセトイミダミド(1.0g、3.54mmol、90%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(352mg、0.63mmol)を黄色の油として得た。LCMS m/z 473.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.96(d,J=8.3Hz,2H)、7.87(d,J=8.3Hz,2H)、4.12-4.01(m,4H)、3.63(ddd,J=23.4,10.6,4.7Hz,1H)、3.46(dd,J=16.9,10.0Hz,1H)、3.41-3.32(m,1H)、1.26(s,9H)、1.25-1.20(m,6H)。19F NMR(376MHz,DMSO-d6)δ-61.69,-95.52.31P NMR(162MHz,DMSO-d6)δ 19.90。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(352mg、0.63mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~40%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(179mg、0.44mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.95(d,J=8.3Hz,2H)、7.88(d,J=8.3Hz,2H)、6.26(d,J=1.1Hz,1H)、5.96(d,J=1.2Hz,1H)、4.05(s,2H)、1.20(s,9H)。19F NMR(376MHz,DMSO-d6)δ-61.69,-96.06。
tert-ブチル2-((3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(179mg、0.44mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(122mg、0.35mmol)を紫色の油として得た。LCMS m/z 347.1(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.92(s,1H)、7.96(d,J=8.3Hz,2H)、7.88(d,J=8.3Hz,2H)、6.31(d,J=1.1Hz,1H)、5.99(d,J=1.2Hz,1H)、4.05(s,2H)。19F NMR(376MHz,DMSO-d6)δ-61.63,-94.72。
2-(4-(1,1-ジフルオロペンチル)フェニル)-N-ヒドロキシアセトイミダミド(347mg、1.26mmol、93%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(432mg、0.66mmol、81%純度)を淡黄色の油として得た。LCMS m/z 553.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.44(d,J=8.2Hz,2H)、7.37(d,J=8.1Hz,2H)、4.12-3.99(m,6H)、3.53(ddd,J=23.3,10.9,4.5Hz,1H)、3.39-3.32(m,1H)、3.23(ddd,J=16.9,8.8,4.6Hz,1H)、2.24-2.09(m,2H)、1.33-1.18(m,19H)、0.89-0.79(m,3H)。19F NMR(376MHz,DMSO-d6)δ-92.44。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(432mg、0.66mmol、81%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.280g、0.69mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.45(d,J=8.3Hz,2H)、7.39(d,J=8.1Hz,2H)、6.21(d,J=1.2Hz,1H)、5.91-5.84(m,1H)、4.10(s,2H)、3.90(s,2H)、2.24-2.09(m,2H)、1.33-1.25(m,4H)、1.22(s,9H)、0.87-0.80(m,3H)。19F NMR(376MHz,DMSO-d6)δ-92.43。
tert-ブチル2-((3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.280g、0.69mmol)から、実施例79、ステップ3で記載した手順に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.168g、0.47mmol)を白色の固体として得た。LCMS m/z 349.2(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.82(s,1H)、7.46(d,J=8.3Hz,2H)、7.38(d,J=8.1Hz,2H)、6.26(d,J=1.2Hz,1H)、5.90(d,J=1.4Hz,1H)、4.12(s,2H)、3.91(s,2H)、2.26-2.10(m,2H)、1.35-1.24(m,4H)、0.90-0.79(m,3H)。19F NMR(376MHz,DMSO-d6)δ-92.49。
2,2-ジフルオロ-N-ヒドロキシ-2-(4-(トリフルオロメトキシ)フェニル)アセトイミダミド(1.00g、3.33mmol、90%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(427mg、0.78mmol)を黄色の油として得た。LCMS m/z 489.4(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.81-7.75(m,2H)、7.61-7.52(m,2H)、4.15-4.02(m,4H)、3.63(ddd,J=23.5,10.6,4.8Hz,1H)、3.46(dd,J=16.9,10.2Hz,1H)、3.41-3.33(m,1H)、1.28(s,9H)、1.26-1.19(m,6H)。19F NMR(376MHz,DMSO-d6)δ-56.80,-94.10.31P NMR(162MHz,DMSO-d6)δ 19.93。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(427mg、0.78mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(242mg、0.57mmol)を無色の油として得た。LCMS m/z 363.2(M-tBu-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 7.79(d,J=8.8Hz,2H)、7.60-7.53(m,2H)、6.26(d,J=1.1Hz,1H)、5.96(d,J=1.3Hz,1H)、4.05(s,2H)、1.21(s,9H)。
tert-ブチル2-((3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(242mg、0.57mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(155mg、0.41mmol)を紫色の油として得た。LCMS m/z 363.2(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.91(s,1H)、7.95-7.68(m,2H)、7.68-7.49(m,2H)、6.31(d,J=1.1Hz,1H)、5.99(q,J=1.2Hz,1H)、4.05(s,2H)。19F NMR(376MHz,DMSO-d6)δ-56.77,-93.40。
EDC(430mg、2.24mmol)を、DCM(10mL)中の2-(4-ブチルフェニル)酢酸(316mg、1.65mmol)、tert-ブチル2-(ジエトキシホスホリル)-4-(ヒドロキシアミノ)-4-イミノブタノエート(0.50g、1.50mmol)、およびDMAP(18mg、0.15mmol)の混合物に加えた。混合物を室温で2.5時間撹拌した。混合物を水(40mL)で希釈し、DCM(3x20mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濾過して、濃縮した。残留物をTHF(10mL)中に入れ、Cs2CO3(0.93g、2.8mmol)を加え、混合物を室温で18時間撹拌した。混合物を水(40mL)で希釈し、EtOAc(3x30mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.45g、0.89mmol)を淡褐色のガムとして得た。LCMS m/z 503.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.25-7.08(m,4H)、4.26(s,2H)、4.14-3.95(m,4H)、3.42-3.34(m,1H)、3.25-3.10(m,1H)、3.07-2.93(m,1H)、2.58-2.52(m,2H)、1.57-1.47(m,2H)、1.30(s,9H)、1.28-1.19(m,6H)、0.88(t,J=7.3Hz,3H)。2つのプロトンは分解されていない。
tert-ブチル3-(5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.45g、0.89mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(231mg、0.64mmol)を無色の油として得た。LCMS m/z 301.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.20(d,J=8.1Hz,2H)、7.15(d,J=8.1Hz,2H)、6.15(d,J=1.3Hz,1H)、5.75(q,J=1.3Hz,1H)、4.26(s,2H)、3.67(s,2H)、2.57-2.52(m,2H)、1.57-1.46(m,2H)、1.32(s,9H)、1.31-1.23(m,2H)、0.88(t,J=7.3Hz,3H)。
tert-ブチル2-((5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(231mg、0.64mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(163mg、0.54mmol)を紫色の油として得た。LCMS m/z 301.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.68(s,1H)、7.21(d,J=8.2Hz,2H)、7.16(d,J=8.2Hz,2H)、6.21(d,J=1.3Hz,1H)、5.75(d,J=1.3Hz,1H)、4.26(s,2H)、3.67(s,2H)、2.60-2.52(m,2H)、1.59-1.47(m,2H)、1.35-1.23(m,2H)、0.88(t,J=7.3Hz,3H)。
4-ブトキシ安息香酸(383mg、1.97mmol)から、実施例95、ステップ1で記載した手順に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.15g、0.25mmol、80%純度)を透明な淡褐色のガムとして得た。LCMS m/z 427.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.72(s,1H)、8.03-7.98(m,2H)、7.17-7.11(m,2H)、6.24(d,J=1.3Hz,1H)、5.81(s,1H)、4.08(t,J=6.5Hz,2H)、3.75(s,2H)、1.77-1.68(m,2H)、1.51-1.39(m,2H)、0.94(t,J=7.4Hz,3H)。
tert-ブチル3-(5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)-2-(ジエトキシホスホリル)プロパノエート(0.15g、0.25mmol、80%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(82mg、0.22mmol)を無色の油として得た。LCMS m/z 303.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.05-7.97(m,2H)、7.22-7.11(m,2H)、6.19(d,J=1.3Hz,1H)、5.81(q,J=1.3Hz,1H)、4.08(t,J=6.5Hz,2H)、3.76(s,2H)、1.78-1.67(m,2H)、1.50-1.40(m,2H)、1.38(s,9H)、0.94(t,J=7.4Hz,3H)。
tert-ブチル2-((5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(82mg、0.22mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(50mg、0.16mmol)を白色の固体として得た。LCMS m/z 303.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.72(s,1H)、8.03-7.98(m,2H)、7.17-7.11(m,2H)、6.24(d,J=1.3Hz,1H)、5.81(s,1H)、4.08(t,J=6.5Hz,2H)、3.75(s,2H)、1.77-1.68(m,2H)、1.51-1.39(m,2H)、0.94(t,J=7.4Hz,3H)。
2,2-ジフルオロ-2-(4-(トリフルオロメチル)フェニル)酢酸(389mg、1.62mmol)から、実施例84、ステップ1と同様の手順を使用して調整した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)プロパノエート(187mg、0.33mmol、93%純度)を淡黄色の油として得た。LCMS m/z 551.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.00(d,J=8.5Hz,2H)、7.95(d,J=8.6Hz,2H)、4.12-3.99(m,4H)、3.43(ddd,J=22.8,10.8,4.1Hz,1H)、3.33-3.23(m,1H)、3.16(ddd,J=16.1,9.5,4.2Hz,1H)、1.27(s,9H)、1.26-1.19(m,6H)。19F NMR(376MHz,DMSO-d6)δ-61.75,-94.21(d,J=6.4Hz)。31P NMR(162MHz,DMSO-d6)δ 20.49。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)プロパノエート(187mg、0.33mmol、93%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(112mg、0.27mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.99(d,J=8.9Hz,2H)、7.95(d,J=8.7Hz,2H)、6.19(d,J=1.2Hz,1H)、5.83(d,J=1.3Hz,1H)、3.82(d,J=1.1Hz,2H)、1.27(s,9H)。19F NMR(376MHz,DMSO-d6)δ-61.74,-94.46。
tert-ブチル2-((5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(112mg、0.27mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(61mg、0.17mmol)を無色の油として得た。LCMS m/z 347.1(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.78(s,1H)、8.00(d,J=8.7Hz,2H)、7.96(d,J=8.7Hz,2H)、6.25(d,J=1.2Hz,1H)、5.84(q,J=1.3Hz,1H)、3.81(s,2H)。19F NMR(376MHz,DMSO-d6)δ-61.69,-93.67。
4-(1,1-ジフルオロブチル)-N-ヒドロキシベンズイミダミド(0.361g、1.53mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.567g、1.1mmol)を淡黄色の油として得た。LCMS m/z 525.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.08(d,J=8.2Hz,2H)、7.72(d,J=8.3Hz,2H)、4.18-4.05(m,4H)、3.69(ddd,J=23.4,10.7,4.7Hz,1H)、3.53-3.42(m,1H)、3.37(ddd,J=16.8,8.9,4.7Hz,1H)、2.29-2.14(m,2H)、1.41-1.32(m,11H)、1.30-1.22(m,6H)、0.91(t,J=7.4Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-93.44。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.567g、1.1mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/ヘキサン)により精製して、tert-ブチル2-((3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.368g、0.92mmol)を透明な無色の油として得た。LCMS m/z 323.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.09(d,J=8.1Hz,2H)、7.71(d,J=8.3Hz,2H)、6.29(d,J=1.3Hz,1H)、6.00-5.96(m,1H)、4.06(s,2H)、2.29-2.14(m,2H)、1.42-1.30(m,11H)、0.91(t,J=7.4Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-93.44。
tert-ブチル2-((3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.368g、0.92mmol)から、実施例79、ステップ3で記載した手順に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製し、次にシリカゲルでのクロマトグラフィー(0~10%MeOH/DCM)により再精製して、2-((3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.233g、0.72mmol)を白色の固体として得た。LCMS m/z 323.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.89(s,1H)、8.09(d,J=8.2Hz,2H)、7.70(d,J=8.3Hz,2H)、6.33(d,J=1.2Hz,1H)、6.01(d,J=1.3Hz,1H)、4.05(s,2H)、2.31-2.13(m,2H)、1.43-1.30(m,2H)、0.90(t,J=7.4Hz,3H)。19F NMR(376MHz,DMSO-d6)δ-93.43。
1-(4-(トリフルオロメトキシ)フェニル)シクロプロパン-1-カルボン酸(405mg、1.65mmol)から、実施例95、ステップ1で記載した手順に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)プロパノエート(0.31g、0.46mmol、80%純度)を淡黄色のガムとして得た。LCMS m/z 557.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.61-7.52(m,2H)、7.42-7.32(m,2H)、4.12-3.99(m,4H)、3.29-3.21(m,1H)、3.19-3.04(m,1H)、3.04-2.91(m,1H)、1.74-1.57(m,4H)、1.33(s,9H)、1.28-1.16(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)プロパノエート(0.31g、0.46mmol、80%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.17g、0.36mmol、88%純度)を透明な無色の油として得た。LCMS m/z 355.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.64-7.50(m,2H)、7.42-7.31(m,2H)、6.17-6.06(m,1H)、5.75-5.67(m,1H)、3.62(s,2H)、1.73-1.65(m,2H)、1.62-1.55(m,2H)、1.36(s,9H)。
tert-ブチル2-((5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリレート(0.17g、0.36mmol、88%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-((5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸(0.112g、0.30mmol)を透明な無色のガムとして得た。LCMS m/z 355.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.67(s,1H)、7.64-7.51(m,2H)、7.42-7.29(m,2H)、6.23-6.15(m,1H)、5.77-5.64(m,1H)、3.62(s,2H)、1.75-1.66(m,2H)、1.63-1.53(m,2H)。
4-(ベンジルオキシ)-N-ヒドロキシベンズイミダミド(5.97g、24.6mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、0~100%MTBE/イソヘキサンを得)、tert-ブチル3-(3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(8.30g、16mmol)を褐色の油として得た。LCMS m/z 461.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.95-7.88(m,2H)、7.52-7.45(m,2H)、7.45-7.38(m,2H)、7.38-7.30(m,1H)、7.25-7.13(m,2H)、5.19(s,2H)、4.17-4.06(m,4H)、3.65(ddd,J=23.4,10.8,4.6Hz,1H)、3.43(ddd,J=16.8,10.8,9.7Hz,1H)、3.36-3.27(m,1H)、1.38(s,9H)、1.30-1.23(m,6H)。
tert-ブチル3-(3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(0.300g、0.58mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.176g、0.44mmol)を透明な無色の油として得た。LCMS m/z 337.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.97-7.87(m,2H)、7.51-7.31(m,5H)、7.23-7.14(m,2H)、6.27(d,J=1.2Hz,1H)、6.00-5.91(m,1H)、5.19(s,2H)、4.01(s,2H)、1.33(s,9H)。
tert-ブチル2-((3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.176g、0.44mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.0956g、0.28mmol)を白色の固体として得た。LCMS m/z 337.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.84(s,1H)、12.85(s,1H)、7.96-7.89(m,2H)、7.50-7.45(m,2H)、7.44-7.38(m,2H)、7.37-7.32(m,1H)、7.21-7.15(m,2H)、6.32(d,J=1.2Hz,1H)、6.03-5.95(m,1H)、5.19(s,2H)、4.00(s,2H)。
2-ブロモ-1-(4-ブチルフェニル)エタン-1-オン(906mg、3.55mmol)を使用して、実施例39、ステップ1に従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、0~20%MTBE/石油エーテル)により精製して、tert-ブチル3-(4-(4-ブチルフェニル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(230mg、0.49mmol、15%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 466.3(M+H)+(ES+)。
tert-ブチル3-(4-(4-ブチルフェニル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(230mg、0.49mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(10%MTBE/石油エーテル)により精製して、tert-ブチル2-((4-(4-ブチルフェニル)オキサゾール-2-イル)メチル)アクリレート(160mg、0.47mmol、95%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 254.3(M+H)+(ES+)。
tert-ブチル2-((4-(4-ブチルフェニル)オキサゾール-2-イル)メチル)アクリレート(160mg、0.47mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.1%TFA/水);勾配:50~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((4-(4-ブチルフェニル)オキサゾール-2-イル)メチル)アクリル酸(88mg、0.31mmol、65%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 286.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.70(br,1H)、8.44(s,1H)、7.63(d,J=8.2Hz,2H)、7.22(d,J=8.2Hz,2H)、6.24(s,1H)、5.81(d,J=1.4Hz,1H)、3.80(s,2H)、2.58(t,J=7.7Hz,2H)、1.61-1.49(m,2H)、1.36-1.24(m,2H)、0.89(t,J=7.3Hz,3H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(5-オクチルイソオキサゾール-3-イル)プロパノエート(500mg、1.1mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、0~30%MTBE/石油エーテル)により精製して、tert-ブチル2-((5-オクチルイソオキサゾール-3-イル)メチル)アクリレート(300mg、0.93mmol、85%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 344.3(M+Na)+(ES+)。
tert-ブチル2-((5-オクチルイソオキサゾール-3-イル)メチル)アクリレート(200mg、0.62mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.05%TFA/水);勾配:45~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下40℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((5-オクチルイソオキサゾール-3-イル)メチル)アクリル酸(94mg、0.35mmol、56%)を得た。LCMS:(システム2,方法B)m/z 266.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.65(br,1H)、6.16(s,1H)、6.06(s,1H)、5.67(d,J=1.5Hz,1H)、3.55(s,2H)、2.68(t,J=7.5Hz,2H)、1.64-1.53(m,2H)、1.32-1.18(m,10H)、0.85(t,J=6.8Hz,3H)。
2-ブロモ-1-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)エタン-1-オン(1.0g、3.26mmol)を使用して、実施例39、ステップ1に従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、0~80%MTBE/石油エーテル)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)プロパノエート(300mg、0.58mmol、17%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 518.2(M+H)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)プロパノエート(300mg、0.58mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、0~20%MTBE/石油エーテル)により精製して、tert-ブチル2-((4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)メチル)アクリレート(180mg、0.46mmol、79%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 394.2(M+H)+(ES+)。
tert-ブチル2-((4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)メチル)アクリレート(180mg、0.46mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.05%TFA/水);勾配:40~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)メチル)アクリル酸(127mg、0.38mmol、82%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 338.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.69(br,1H)、7.66(d,J=8.1Hz,2H)、7.53(s,1H)、7.50(d,J=8.1Hz,2H)、6.19(d,J=1.3Hz,1H)、5.73(d,J=1.4Hz,1H)、3.70(s,2H)、1.34-1.27(m,2H)、1.27-1.19(m,2H)。
2-(クロロメチル)-4-オクチルピリジン(1.3g、5.42mmol)から、一般的な手順A、ステップ1、方法Dに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(80gシリカ、0~40%MTBE/石油エーテル)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(4-オクチルピリジン-2-イル)プロパノエート(1.20g、2.63mmol、49%)を褐色の油として得た。LCMS:(システム2,方法B)m/z 456.3(M+H)+(ES+)。
tert-ブチル2-(ジエトキシホスホリル)-3-(4-オクチルピリジン-2-イル)プロパノエート(0.70g、1.54mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、0~20%MTBE/石油エーテル)により精製して、tert-ブチル2-((4-オクチルピリジン-2-イル)メチル)アクリレート(200mg、0.60mmol、39%)を無色の油として得た。LCMS:(システム2,方法C)m/z 332.4(M+H)+(ES+)。
tert-ブチル2-((4-オクチルピリジン-2-イル)メチル)アクリレート(180mg、0.54mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.1%TFA/水);勾配:50~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下35℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((4-オクチルピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩(112mg、0.29mmol、54%)を無色の油として得た。LCMS:(システム2,方法B)m/z 276.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.95(br,1H)、8.45(d,J=5.3Hz,1H)、7.28(s,2H)、6.19(s,1H)、5.65(s,1H)、3.76(s,2H)、2.63(t,J=7.7Hz,2H)、1.62-1.51(m,2H)、1.32-1.18(m,10H)、0.85(t,J=6.7Hz,3H)。1つの交換可能なプロトンは観察されない。
CHCl3(4mL)中のtert-ブチル2-((4-オクチルオキサゾール-2-イル)メチル)アクリレート(100mg、0.31mmol)、およびNBS(109mg、0.62mmol)の混合物を室温で1時間撹拌し、還流で0.5時間加熱した。反応混合物をH 2 O(5mL)で希釈し、相を分離し、水層をDCM(3×5mL)で抽出した。合わせた有機層をH2O(2×5mL)およびブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下35℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(25gシリカ、0~30%MTBE/石油エーテル)により精製して、tert-ブチル2-((5-ブロモ-4-オクチルオキサゾール-2-イル)メチル)アクリレート(100mg、0.25mmol、80%)を無色の油として得た。LCMS:(システム2,方法C)m/z 400.2/402.2(M+H)+(ES+)。1H NMR(400MHz,CDCl3)δ:6.28(d,J=1.0Hz,1H)、5.61(q,J=1.3Hz,1H)、3.71(s,2H)、2.40(t,J=7.6Hz,2H)、1.57(s,2H)、1.45(s,9H)、1.34-1.19(m,10H)、0.87(t,J=6.8Hz,3H)。
ジメチルホルムアミド(5mL)中のジエチルエーテル(2M、2mL、4.0mmol)中のtert-ブチル2-((5-ブロモ-4-オクチルオキサゾール-2-イル)メチル)アクリレート(100mg、0.25mmol)、Pd(PPh3)2Cl2(526mg、0.75mmol)、およびCH3ZnCl溶液の混合物を、80℃で12時間撹拌した。反応混合物をH2O(5mL)で希釈し、EtOAc(3×5mL)で抽出した。合わせた有機層をH2O(2×5mL)およびブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下35℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(25gシリカ、0~30%MTBE/石油エーテル)により精製して、tert-ブチル2-((5-メチル-4-オクチルオキサゾール-2-イル)メチル)アクリレート(42mg、0.13mmol、50%)を無色の油として得た。LCMS:(システム2,方法C)m/z 336.4(M+H)+(ES+)。
tert-ブチル2-((5-メチル-4-オクチルオキサゾール-2-イル)メチル)アクリレート(42mg、0.13mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.1%TFA/水);勾配:45~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下35℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((5-メチル-4-オクチルオキサゾール-2-イル)メチル)アクリル酸(19mg、0.07mmol、52%)を無色の油として得た。LCMS:(システム2,方法B)m/z 280.2(M+H)+(ES+)。1H NMR(400MHz,CDCl3)δ:6.42(s,1H)、5.74(s,1H)、3.74(s,2H)、2.38(t,J=7.6Hz,2H)、2.20(s,3H)、1.61-1.50(m,2H)、1.34-1.18(m,10H)、0.87(t,J=6.7Hz,3H)。1つの交換可能なプロトンは観察されない。
室温でのEtOAc(65mL)中のN-ヒドロキシノナニミダミド(13.28g、77.1mmol)、アクリル酸(5.56g、77.2mmol)、およびトリエチルアミン(23.4g、231mmol)の溶液に、EtOAc中のT3Pの溶液(50重量%、123g、193mmol)を加えた。得られた混合物を80℃で一晩撹拌した。混合物を水(100mL)でクエンチし、分離し、水相をEtOAc(3x65mL)で抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(120gシリカ、5%MTBE/石油エーテル)により精製して、3-オクチル-5-ビニル-1,2,4-オキサジアゾール(6.90g、33.1mmol、43%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 209.4(M+H)+(ES+)。
室温でのアセトン(128mL)および水(69mL)中の3-オクチル-5-ビニル-1,2,4-オキサジアゾール(6.90g、33.1mmol)およびK2OsO4(0.55g、1.65mmol)の溶液に、NaIO4(21.26g、99.4mmol)を加え、得られた混合物を室温で一晩撹拌した。混合物を水(50mL)で希釈し、減圧下で濃縮してアセトンを除去した。水性残留物をEtOAc(3×100mL)で抽出し、合わせた有機相をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(80gシリカ、45%MTBE/石油エーテル)により精製して、3-オクチル-1,2,4-オキサジアゾール-5-カルバルデヒド(6.24g、29.7mmol、89%)を白色の固体として得た。LCMS:(システム2,方法C)m/z 211.3(M+H)+(ES+)。
DMSO(60mL)中の3-オクチル-1,2,4-オキサジアゾール-5-カルバルデヒド(6.00g、28.5mmol)、メチルアクリレート(3.69g、42.9mmol)、DABCO(1.60g、14.3mmol)、および分子篩(6.00g)の混合物を、室温で3時間撹拌した。反応混合物を濾過し、濾液を水(300mL)に注ぎ、混合物をEtOAc(3×300mL)で抽出した。合わせた有機相をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(80gシリカ、45%MTBE/石油エーテル)により精製して、メチル2-(ヒドロキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.35g、4.55mmol、16%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 297.2(M+H)+(ES+)。
水中のLiOH溶液(2M、0.3mL、0.6mmol)を、THF(0.9mL)中のメチル2-(ヒドロキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(184mg、0.62mmol)の溶液に加え、得られた混合物を室温で0.5時間撹拌した。混合物を希水性HCl(0.5M)を使用してpH=6に調整し、EtOAc(3×300mL)で抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10 μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.1%TFA/水);勾配:35~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下40℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-(ヒドロキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(34mg、0.12mmol、19%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 283.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.83(br,1H)、6.70(br,1H)、6.36(s,1H)、6.11(s,1H)、5.59(s,1H)、2.66(t,J=7.5Hz,2H)、1.68-1.55(m,2H)、1.34-1.16(m,10H)、0.85(t,J=6.9Hz,3H)。
0℃でのTHF(132mL)中の4-クロロベンズアルデヒド(3.70g、26.3mmol)の溶液に、THF中のペンチルマグネシウムブロミドの溶液(1M、31.6mL、31.6mmol)を加え、反応混合物を室温で16時間撹拌した。反応混合物を飽和水性NH4Cl溶液(100mL)でクエンチし、EtOAc(2×100mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下30℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~10%MTBE/石油エーテル)により精製して、1-(4-クロロフェニル)ヘキサン-1-オール(4.2g、19.7mmol、75%)を黄色の油として得た。1H NMR(400MHz,CDCl3)δ:7.29(q,J=8.6Hz,4H)、4.64(dd,J=7.5,5.8Hz,1H)、1.81-1.71(m,1H)、1.70-1.59(m,1H)、1.45-1.33(m,1H)、1.33-1.19(m,5H)、0.92-0.81(m,3H)。1つの交換可能なプロトンは観察されない。
DCM(100mL)中の1-(4-クロロフェニル)ヘキサン-1-オール(4.2g、19.7mmol)およびMnO2(6.87g、79.0mmol)の混合物を、40℃で16時間撹拌した。混合物を濾過し、濾液を減圧下35℃で濃縮し、1-(4-クロロフェニル)ヘキサン-1-オン(3.80g、18.0mmol、91%)を黄色の油として得、これを次のステップで直接使用した。1H NMR(400MHz,CDCl3)δ:7.89(d,J=8.6Hz,2H)、7.43(d,J=8.5Hz,2H)、2.93(t,J=7.4Hz,2H)、1.78-1.67(m,2H)、1.42-1.29(m,4H)、0.91(t,J=6.9Hz,3H)。
室温でのMeOH(35mL)中の1-(4-クロロフェニル)ヘキサン-1-オン(1.50g、7.12mmol)の溶液に、Br2(1.46g、9.26mmol)を滴下して加え、反応混合物を室温で16時間撹拌した。反応混合物を飽和水性NaHCO3でpH=7に調整し、混合物を減圧下35℃で濃縮してMeOHを除去した。残留水層をEtOAc(2×40mL)で抽出し、合わせた有機層をNa2SO4で乾燥させ、濾過し、減圧下35℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(40gシリカ、0~10%MTBE/石油エーテル)により精製して、2-ブロモ-1-(4-クロロフェニル)ヘキサン-1-オン(1.40g、4.83mmol、68%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 289.1/291.1(M+H)+(ES+)。
混合物を室温ではなく50℃で16時間撹拌したことを除いて、2-ブロモ-1-(4-クロロフェニル)ヘキサン-1-オン(1.37g、4.73mmol)を使用して、実施例39、ステップ1に従って調製した。反応混合物を濾過し、濾液を減圧下35℃で濃縮した。残留物を逆相フラッシュクロマトグラフィーにより精製して、粗3-(5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパン酸(200mg、0.45mmol、9%)を淡黄色の油として得、これを次のステップで直接使用した。LCMS:(システム2,方法C)m/z 444.2(M+H)+(ES+)。
0℃でのジメチルホルムアミド(3mL)中の3-(5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパン酸(200mg、0.45mmol)、およびK2CO3(93mg、0.68mmol)の混合物に、PMBCl(85mg、0.54mmol)を加え、反応混合物を室温で16時間撹拌した。反応混合物を水でクエンチし、EtOAcで抽出した。合わせた有機層を水および飽和水性NH4Clで洗浄し、次にNa2SO4で乾燥させ、濾過した。濾液を減圧下30℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(12gシリカ、0~40%MTBE/石油エーテル)によって精製して、4-メトキシベンジル3-(5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(70mg、0.12mmol、2%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 564.0(M+H)+(ES+)。
4-メトキシベンジル3-(5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(70mg、0.12mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(10%MTBE/石油エーテル)により精製して、4-メトキシベンジル2-((5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)メチル)アクリレート(34mg、0.077mmol、64%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 440.0(M+H)+(ES+)。
4-メトキシベンジル2-((5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)メチル)アクリレート(34mg、0.077mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.05%TFA/水);勾配:45~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)メチル)アクリル酸(16mg、0.050mmol、65%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 320.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.71(s,1H)、7.63(d,J=8.7Hz,2H)、7.48(d,J=8.6Hz,2H)、6.21(s,1H)、5.77(s,1H)、3.74(s,2H)、2.85(t,J=7.5Hz,2H)、1.65-1.54(m,2H)、1.38-1.26(m,2H)、0.87(t,J=7.4Hz,3H)。
DCM(3.1mL)中のメチル2-(ヒドロキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(300mg、1.01mmol)の溶液に、メチルヨージド(860mg、6.06mmol)およびAg2O(470mg、2.03mmol)を加えた。混合物をN2雰囲気下、室温で16時間撹拌した。混合物をセライトのプラグを通して濾過し、残留物をDCMで洗浄した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(8gシリカ、15%EtOAc/石油エーテル)により精製して、メチル2-(メトキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(126mg、0.41mmol、41%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 311.2(M+H)+(ES+)。
THF(2.4mL)中のメチル2-(メトキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(224mg、0.72mmol)の溶液に、水中のLiOH溶液(2M、0.8mL、1.6mmol)を加え、得られた混合物を室温で2時間撹拌した。混合物を希水性HCl(0.5M)を使用してpH=6に調整し、次にEtOAc(3×30mL)で抽出した。合わせた有機相をブラインで洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10 μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.1%TFA/水);勾配:55~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下40℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-(メトキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(33mg、0.11mmol、15%)を黄色の油として得た。LCMS:(システム2,方法B)m/z 297.2(M+H)+(ES+)。1H NMR(400MHz,CDCl3)δ:6.70(s,1H)、6.30(s,1H)、5.36(s,1H)、3.50(s,3H)、2.74(t,J=7.7Hz,2H)、1.80-1.68(m,2H)、1.40-1.18(m,10H)、0.87(t,J=6.7Hz,3H)。1つの交換可能なプロトンは観察されない。
1-(4-シクロブトキシフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(1.30g、5.28mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(50gシリカ、20~40%EtOAC/石油エーテル)により精製して、tert-ブチル3-(3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(2.20g、4.23mmol、80%)を無色の油として得た。LCMS:(システム2,方法C)m/z 521.1(M+H)+(ES+)。
tert-ブチル3-(3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(2.20g、4.23mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、0~20%MTBE/石油エーテル)により精製して、tert-ブチル2-((3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.20g、3.03mmol、72%)を無色の油として得た。LCMS:(システム2,方法C)m/z 379.3(M+H)+(ES+)。
tert-ブチル2-((3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.40g、1.01mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.2%ギ酸/水);勾配:70~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(233mg、0.68mmol、68%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 341.0(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.81(br,1H)、7.29-7.23(m,2H)、6.81-6.74(m,2H)、6.26(d,J=1.2Hz,1H)、5.89(d,J=1.3Hz,1H)、4.72-4.61(m,1H)、3.86(s,2H)、2.47-2.37(m,2H)、2.08-1.95(m,2H)、1.83-1.71(m,1H)、1.70-1.56(m,1H)、1.42-1.35(m,2H)、1.31-1.24(m,2H)。
2-(4-シクロペンチルフェニル)-N-ヒドロキシアセトイミダミド(420mg、1.92mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、20~40%EtOAC/石油エーテル)により精製して、tert-ブチル3-(3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(400mg、0.81mmol、42%)を無色の油として得た。LCMS:(システム2,方法C)m/z 493.2(M+H)+(ES+)。
tert-ブチル3-(3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(400mg、0.81mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、0~20%MTBE/石油エーテル)により精製して、tert-ブチル2-((3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(180mg、0.49mmol、60%)を無色の油として得た。LCMS:(システム2,方法C)m/z 369.3(M+H)+(ES+)。
tert-ブチル2-((3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(180mg、0.49mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.2%ギ酸/水);勾配:55~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(105mg、0.34mmol、69%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 313.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.80(br,1H)、7.22-7.13(m,4H)、6.26(s,1H)、5.90(s,1H)、3.99(s,2H)、3.89(s,2H)、2.96-2.86(m,1H)、2.03-1.91(m,2H)、1.81-1.68(m,2H)、1.68-1.55(m,2H)、1.55-1.41(m,2H)。
HATU(1.23g、3.24mmol)を、ジメチルホルムアミド(10mL)中の1-(4-ヨードフェニル)-N-ヒドロキシシクロプロパン-1-カルボキシミダミド(0.825g、2.70mmol)、4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(0.923g、2.97mmol)、およびトリエチルアミン(1.13mL、8.11mmol)の混合物に加えた。混合物を室温で1時間撹拌し、次に飽和水性NaHCO3(100mL)を加えた。混合物をEtOAc(3×80mL)で抽出し、合わせた有機相をブライン(3×100mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。残留物をTHF(20mL)中に入れ、Cs2CO3(1.76g、5.39mmol)を加えた。混合物を70℃に加熱し、3時間撹拌して、次に室温に冷却し、水(40mL)で希釈し、DCM(3x20mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.52g、2.5mmol)を白色の固体として得た。LCMS m/z 599.2(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.78-7.61(m,2H)、7.24-7.07(m,2H)、4.16-3.96(m,4H)、3.61-3.40(m,1H)、3.30-3.24(m,1H)、3.24-3.12(m,1H)、1.53-1.36(m,4H)、1.35(s,9H)、1.30-1.17(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.52g、2.5mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.99g、2.0mmol、90%純度)を透明な無色の油として得た。LCMS m/z 397.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.77-7.62(m,2H)、7.23-7.13(m,2H)、6.24-6.16(m,1H)、5.93-5.82(m,1H)、3.88(s,2H)、1.46-1.40(m,2H)、1.39-1.34(m,2H)、1.33(s,9H)。
tert-ブチル2-((3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.99g、2.0mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~30%MTBE/イソヘキサン)により精製して、2-((3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.574g、1.4mmol)を淡褐色の固体として得た。LCMS m/z 3971(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.81(s,1H)、7.79-7.56(m,2H)、7.28-7.12(m,2H)、6.31-6.17(m,1H)、5.97-5.79(m,1H)、3.88(s,2H)、1.48-1.41(m,2H)、1.39-1.31(m,2H)。
4-ブロモ-N-ヒドロキシベンズイミダミド(1.90g、8.0mmol、90%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.37g、2.5mmol、90%純度)を透明な無色の油として得た。LCMS m/z 433.2/435.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.95-7.86(m,2H)、7.84-7.75(m,2H)、4.18-4.02(m,4H)、3.76-3.58(m,1H)、3.53-3.34(m,2H)、1.37(s,9H)、1.26(q,J=6.8Hz,6H)。
tert-ブチル3-(3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.37g、2.5mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~20%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.84g、2.1mmol、90%純度)を透明な無色の油として得た。LCMS m/z 309.2/311.2(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.96-7.88(m,2H)、7.83-7.72(m,2H)、6.33-6.23(m,1H)、6.00-5.93(m,1H)、4.04(s,2H)、1.33(s,9H)。
tert-ブチル2-((3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.84g、2.1mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~40%MTBE/イソヘキサン)により精製して、2-((3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.522g、1.6mmol)を白色の固体として得た。LCMS m/z 307.4/309.4(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.88(s,1H)、7.95-7.88(m,2H)、7.81-7.73(m,2H)、6.35-6.29(m,1H)、6.03-5.98(m,1H)、4.04(s,2H)。
4-ヨード-N-ヒドロキシベンズイミダミド(1.3g、4.5mmol、90%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.17g、2.1mmol、94%純度)を透明な無色の油として得た。LCMS m/z 480.8(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.00-7.90(m,2H)、7.80-7.67(m,2H)、4.21-4.02(m,4H)、3.77-3.58(m,1H)、3.53-3.34(m,2H)、1.37(s,9H)、1.31-1.19(m,6H)。
tert-ブチル3-(3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.17g、2.1mmol、94%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~10%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.68g、1.5mmol、90%純度)を透明な無色の油として得た。LCMS m/z 357.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.00-7.89(m,2H)、7.83-7.70(m,2H)、6.32-6.22(m,1H)、6.02-5.89(m,1H)、4.04(s,2H)、1.32(s,9H)。
tert-ブチル2-((3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.68g、1.5mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.411g、1.1mmol)を白色の固体として得た。LCMS m/z 354.8(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.87(s,1H)、7.99-7.88(m,2H)、7.81-7.69(m,2H)、6.38-6.25(m,1H)、6.06-5.93(m,1H)、4.03(s,2H)。
2,2-ジフルオロ-N-ヒドロキシ-2-(4-ヨードフェニル)アセトイミダミド(4.9g、13mmol、80%純度)から、一般的な手順B、方法Aに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.92g、2.6mmol、79%純度)を透明な淡黄色の油として得た。LCMS m/z 531.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.99-7.89(m,2H)、7.45-7.33(m,2H)、4.14-3.99(m,4H)、3.71-3.54(m,1H)、3.52-3.33(m,2H)、1.29(s,9H)、1.26-1.19(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.92g、2.6mmol、79%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~10%MTBE/イソヘキサン)、続いてRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル2-((3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.50g、1mmol)を無色のガムとして得た。1H NMR(400MHz,DMSO-d6)δ 8.02-7.84(m,2H)、7.47-7.32(m,2H)、6.30-6.21(m,1H)、6.00-5.90(m,1H)、4.04(s,2H)、1.23(s,9H)。
tert-ブチル2-((3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.50g、1mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.326g、0.79mmol)を白色の固体として得た。LCMS m/z 405.1(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.90(s,1H)、8.01-7.88(m,2H)、7.45-7.33(m,2H)、6.37-6.24(m,1H)、6.04-5.87(m,1H)、4.04(s,2H)。
N-ヒドロキシ-4-(ペンタフルオロ-λ6-スルファネイル)ベンズイミダミド(1.05g、4.0mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.35g、2.5mmol)を淡黄色の油として得た。LCMS m/z 537.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.20(d,J=8.7Hz,2H)、8.16-8.11(m,2H)、4.17-4.06(m,4H)、3.70(ddd,J=23.4,10.7,4.7Hz,1H)、3.56-3.44(m,1H)、3.39(ddd,J=16.9,8.9,4.7Hz,1H)、1.38(s,9H)、1.29-1.22(m,6H)。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.35g、2.5mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.858g、2.1mmol)を透明な無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 8.21(d,J=8.9Hz,2H)、8.14-8.09(m,2H)、6.30(d,J=1.2Hz,1H)、6.02-5.97(m,1H)、4.08(d,J=1.0Hz,2H)、1.33(s,9H)。
tert-ブチル2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.858g、2.1mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.560g、1.6mmol)を白色の固体として得た。LCMS m/z 355.0(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.89(s,1H)、8.25-8.17(m,2H)、8.14-8.07(m,2H)、6.34(d,J=1.2Hz,1H)、6.07-5.99(m,1H)、4.07(s,2H)。
DCM(100mL)中の(E)-デカ-5-エン(1.4g、10mmol)の混合物に、0℃でm-CPBA(3.5g、20ミリモル)を加え、反応混合物を0℃で3時間撹拌した。反応混合物を希水性NaS2O3(100mL)でクエンチし、DCM(2x100mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下30℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~10%MTBE/石油エーテル)により精製して、(トランス)-2,3-ジブチルオキシラン(1.3g、8.3mmol、83%)を黄色の油として得た。1H NMR(400MHz,CDCl3)δ:2.65(t,J=4.9Hz,2H)、1.60-1.20(m,12H)、0.99-0.80(m,6H)。
THF(10mL)中の(トランス)-2,3-ジブチルオキシラン(1.3g、8.3mmol)および水性HBr(40重量%、5mL)の溶液を、室温で16時間撹拌した。混合物を減圧下35℃で濃縮して、粗(トランス)-6-ブロモデカン-5-オール(1.6g、6.7mmol、81%)を黄色の油として得、これを次のステップで直接使用した。1H NMR(400MHz,CDCl3)δ:4.22-4.12(m,1H)、3.74-3.63(m,1H)、1.94(d,J=6.5Hz,1H)、1.90-1.70(m,2H)、1.66-1.45(m,4H)1.45-1.18(m,6H)、0.92(t,J=7.0Hz 6H)。
DCM(40mL)中の(トランス)-6-ブロモデカン-5-オール(1.6g、6.7mmol)の溶液に、デス・マーチン試薬(4.3g、10.2mmol)を室温で加え、反応混合物を室温で30分間撹拌した。反応混合物を希水性Na2CO3(50mL)でクエンチし、MTBE(2×50mL)で抽出した。合わせた有機層をブラインで洗浄し、無水Na2SO4で乾燥させ、濾過し、減圧下30℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(1.4gシリカ、0~10%MTBE/石油エーテル)により精製して、6-ブロモデカン-5-オン(1.4g、6.0mmol、87%)を黄色の油として得た。1H NMR(400MHz,CDCl3)δ:4.23(dd,J=8.1,6.5Hz,1H)、2.77-2.56(m,2H)、2.07-1.84(m,2H)、1.70-1.53(m,2H)、1.50-1.21(m,6H)、0.99-0.81(m,6H)。
6-ブロモデカン-5-オン(0.70g、3.0mmol)を使用して、実施例109、ステップ4に従って調製した。粗生成物を逆相フラッシュクロマトグラフィーにより精製して、粗3-(4,5-ジブチルオキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパン酸(200mg、0.51mmol、17%)を淡黄色の油として得、これを次のステップで直接使用した。LCMS:(システム2,方法C)m/z 390.2(M+H)+(ES+)。
3-(4,5-ジブチルオキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパン酸(200mg、0.51mmol)を使用して、実施例109、ステップ5に従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(12gシリカ、0~40%MTBE/石油エーテル)により精製して、4-メトキシベンジル3-(4,5-ジブチルオキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(230mg、0.45mmol、88%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 510.2(M+H)+(ES+)。
3-(4,5-ジブチルオキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(230mg、0.45mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(10%MTBE/石油エーテル)により精製して、4-メトキシベンジル2-((4,5-ジブチルオキサゾール-2-イル)メチル)アクリレート(90mg、0.23mmol、52%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 386.2(M+H)+(ES+)。
4-メトキシベンジル2-((4,5-ジブチルオキサゾール-2-イル)メチル)アクリレート(90mg、0.23mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.1%TFA/水);勾配:45~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((4,5-ジブチルオキサゾール-2-イル)メチル)アクリル酸(28mg、0.11mmol、45%)を淡黄色の油として得た。LCMS:(システム2,方法B)m/z 266.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.64(br,1H)、6.17(s,1H)、5.66(d,J=1.5Hz,1H)、3.63(s,2H)、2.57-2.51(m,2H)、2.31(t,J=7.4Hz,2H)、1.53-1.40(m,4H)、1.32-1.18(m,4H)。0.86(t,J=7.4Hz,6H)。
2,2-ジフルオロ-N-ヒドロキシ-2-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)アセトイミダミド(2.00g、5.32mmol、83%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.964g、1.6mmol)を褐色の油として得た。LCMS m/z 531.1(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 8.16-8.10(m,2H)、7.89(d,J=8.6Hz,2H)、4.06(dddd,J=12.0,9.5,7.7,6.0Hz,4H)、3.62(ddd,J=23.5,10.6,4.7Hz,1H)、3.51-3.42(m,1H)、3.42-3.32(m,1H)、1.25(s,9H)、1.24-1.19(m,6H)。19F NMR(376MHz,DMSO)δ-95.88(d,J=16.8Hz)。31P NMR(162MHz,DMSO)δ 19.88。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(0.964g、1.6mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(488mg、1.0mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 8.16-8.10(m,2H)、7.90(d,J=8.5Hz,2H)、6.26(d,J=1.1Hz,1H)、5.96(d,J=1.2Hz,1H)、4.05(s,2H)、1.19(s,9H)。19F NMR(376MHz,DMSO)δ-96.51。
tert-ブチル2-((3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(488mg、1.0mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(367mg、0.88mmol)を濃い無色のガムとして得た。LCMS m/z 404.3(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.90(s,1H)、8.13(d,J=8.9Hz,2H)、7.90(d,J=8.6Hz,2H)、6.31(d,J=1.1Hz,1H)、5.99(d,J=1.3Hz,1H)、4.05(s,2H)。19F NMR(376MHz,DMSO)δ-94.93。
2,2-ジフルオロ-2-(4-フルオロフェニル)-N-ヒドロキシアセトイミダミド(2.14g、8.91mmol、85%純度)から、一般的な手順B、方法Cに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.748g、3.2mmol、88%純度)を褐色の油として得た。LCMS m/z 423.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.72-7.64(m,2H)、7.45-7.37(m,2H)、4.13-4.03(m,4H)、3.63(ddd,J=23.4,10.6,4.8Hz,1H)、3.46(dd,J=16.9,10.2Hz,1H)、3.42-3.33(m,1H)、1.30(s,9H)、1.25-1.20(m,6H)。19F NMR(376MHz,DMSO)δ-93.08(dd,J=13.2,3.0Hz)、-108.82。31P NMR(162MHz,DMSO)δ 19.95。
tert-ブチル2-(ジエトキシホスホリル)-3-(3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)プロパノエート(1.748g、3.2mmol、88%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(812mg、2.7mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.72-7.65(m,2H)、7.40(t,J=8.8Hz,2H)、6.26(d,J=1.1Hz,1H)、5.96(d,J=1.2Hz,1H)、4.05(d,J=1.1Hz,2H)、1.24(s,9H)。19F NMR(376MHz,DMSO)δ-93.59(d,J=3.0Hz)、-108.85。
tert-ブチル2-((3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(812mg、2.7mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(508mg、1.7mmol)を白色の固体として得た。LCMS m/z 297.5(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.90(s,1H)、7.88-7.59(m,2H)、7.40(t,J=8.8Hz,2H)、6.31(d,J=1.1Hz,1H)、5.99(d,J=1.2Hz,1H)、4.04(s,2H)。19F NMR(376MHz,DMSO)δ-92.57(d,J=3.2Hz)、-108.75。
-10℃での乾燥ジエチルエーテル(28mL)中の4-ブチルフェノール(3.00g、20.0mmol)およびEt3N(2.23g、22.0mmol)の溶液に、乾燥ジエチルエーテル(6mL)中のシアンブロミド(2.34g、22.1mmol)の溶液を滴下して加えた。次に、混合物を-10℃で1.5時間激しく撹拌した。混合物を濾過し、濾過残留物を追加の乾燥ジエチルエーテルで洗浄した。濾液を水およびブラインで洗浄し、Na2SOで乾燥させ、減圧下35℃で濃縮した。残留物をフラッシュカラムクロマトグラフィーにより精製して、1-ブチル-4-シアナトベンゼン(3.10g、17.7mmol、89%)を白色の固体として得た。LCMS:(システム2,方法C)m/z 176.4(M+H)+(ES+)。
MeOH(15mL)中の1-ブチル-4-シアナトベンゼン(3.00g、17.1mmol)の溶液に、ヒドロキシルアミンハイドロクロライド(2.39g、34.4mmol)を加えた。懸濁液を0℃に冷却し、DIPEA(4.44g、34.4mmol)をゆっくりと滴下して加えた。次に、反応混合物を室温に温め、30分間撹拌した。反応混合物を水性HCl(2M、30mL)で希釈し、酢酸エチル(3×25mL)で洗浄した。水層を水性NaOH(2M)でpH=8に塩基性化し、次にEtOAc(3×25mL)で抽出した。合わせた有機抽出物をブライン(50mL)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮して、4-ブチルフェニルヒドロキシカルバミミデート(1.10g、5.28mmol、31%)を黄色の固体として得た。LCMS:(システム2,方法C)m/z 209.4(M+H)+(ES+)。
4-ブチルフェニルヒドロキシカルバミミデート(1.10g、5.28mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(50%EtOAc/石油エーテル)により精製して、tert-ブチル3-(3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.13g、2.34mmol、44%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 483.2(M+H)+(ES+)。
tert-ブチル3-(3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(400mg、0.83mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、45%EtOAc/石油エーテル)により精製して、tert-ブチル2-((3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(230mg、0.64mmol、77%)を黄色の固体として得た。LCMS:(システム2,方法C)m/z 359.3(M+H)+,381.2(M+Na)+(ES+)。
tert-ブチル2-((3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(230mg、0.64mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.2%ギ酸/水);勾配:55~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(130mg、0.43mmol、67%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 303.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.90(br,1H)、7.30-7.16(m,4H)、6.29(s,1H)、5.96(d,J=1.3Hz,1H)、3.91(s,2H)、2.59(t,J=7.7Hz,2H)、1.60-1.49(m,2H)、1.37-1.24(m,2H)、0.90(t,J=7.3Hz,3H)。
DCM(80mL)中の2-(4-ブチルフェニル)酢酸(4.70g、24.5mmol)およびオキサリルクロリド(1.55g、122.3mmol)の混合物を、0℃で1時間撹拌した。反応混合物を減圧下35℃で濃縮して、粗2-(4-ブチルフェニル)アセチルクロリド(5.14g、24.4mmol、100%)を淡黄色の油として得た。粗生成物を次のステップに直接使用した。LCMS:(システム2,方法C)m/z 207.4(in-situ methyl ester formation+H)+(ES+)。
0℃でのDCM(80mL)中のN,O-ジメチルヒドロキシルアミンハイドロクロライド(2.38g、24.4mmol)およびトリエチルアミン(17.2g、171mmol)の溶液に、2-(4-ブチルフェニル)アセチルクロリドを加え、得られた淡黄色の混合物を室温で12時間撹拌した。混合物を水(40mL)でクエンチし、相を分離し、有機層をDCM(2x30mL)で抽出した。合わせた有機層を水で洗浄し、Na2SO4で乾燥させ、濾過した。濾液を減圧下40℃で濃縮し、残留物をフラッシュカラムクロマトグラフィー(80gシリカ、20%MTBE/石油エーテル)により精製して、2-(4-ブチルフェニル)-N-メトキシ-N-メチルアセトアミド(3.90g、16.6mmol、68%)を無色の油として得た。LCMS:(システム2,方法C)m/z 236.4(M+H)+(ES+)。
0℃でのTHF(40mL)中の2-(4-ブチルフェニル)-N-メトキシ-N-メチルアセトアミド(3.90g、16.6mmol)の溶液に、ジエチルエーテル中のMeMgBrの溶液(2M、20.7mL、41.4mmol)を加え、反応混合物を室温で3時間撹拌した。反応混合物を飽和水性NH4Cl(20mL)でクエンチし、相を分離し、有機層をMTBE(3×30mL)で抽出した。合わせた有機層をH2O(2x20mL)およびブラインで洗浄し、Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~20%MTBE/石油エーテル)により精製して、1-(4-ブチルフェニル)プロパン-2-オン(2.20g、11.6mmol、69%)を無色の油として得た。LCMS:(システム2,方法C)m/z 191.4(M+H)+(ES+)。
MeOH(38mL)中の1-(4-ブチルフェニル)プロパン-2-オン(2.20g、11.6mmol)およびブロミド(5.11g、11.6mmol)の溶液を25℃で6時間撹拌した。反応混合物を希水性K2CO3(3M、20mL)でクエンチし、次に減圧下30℃で濃縮して揮発性物質を除去した。水性残留物をEtOAc(3×30mL)で抽出し、合わせた有機層を希水性K2CO3(3M、2×20mL)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。淡いオレンジ色の残留物をTHF(20mL)および希水性硫酸(1M、30mL)の混合物中に溶解し、70℃で3時間撹拌した。次に、混合物を減圧下40℃で濃縮し、水性残留物をEtOAc(3×25mL)で抽出した。合わせた有機層を希水性K2CO3(3M、2×20mL)およびブライン(2×20mL)で洗浄し、Na2SO4で乾燥させ、濾過し、減圧下40℃で濃縮した。残留物をフラッシュカラムクロマトグラフィー(80gシリカ、0~4%MTBE/石油エーテル)によって精製して、1-ブロモ-3-(4-ブチルフェニル)プロパン-2-オン(700mg、2.60mmol、22%)を淡黄色の油として得た。1H NMR(400MHz,CDCl3)δ:7.19-7.11(m,4H)、3.91(s,2H)、3.91(s,2H)、2.64-2.54(m,2H)、1.64-1.52(m,2H)、1.41-1.28(m,2H)、0.92(t,J=7.3Hz,3H)。
1-ブロモ-3-(4-ブチルフェニル)プロパン-2-オン(700mg、2.60mmol)を使用して、実施例109、ステップ4に従って調製した。混合物を濾過し、濾液を希HCl(0.5M、20mL)で希釈した。相を分離し、水層をEtOAc(3×20mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、濾過し、濾液を40℃で濃縮した。残留物を逆相カラムクロマトグラフィー(120g C18シリカ;流量:40mL/分;30~50%MeCN/(10mMギ酸/水);収集波長:214nm)によって精製した。収集した画分を減圧下40℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、3-(4-(4-ブチルベンジル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパン酸(270mg、0.64mmol、24%)を無色の油として得た。LCMS:(システム2,方法C)m/z 424.2(M+H)+(ES+)。
3-(4-(4-ブチルベンジル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパン酸(270mg、0.64mmol)を使用して、実施例109、ステップ5に従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(50~90%MTBE/石油エーテル)により精製して、4-メトキシベンジル3-(4-(4-ブチルベンジル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(175mg、0.32mmol、50%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 544.2(M+H)+(ES+)。
4-メトキシベンジル3-(4-(4-ブチルベンジル)オキサゾール-2-イル)-2-(ジエトキシホスホリル)プロパノエート(175mg、0.32mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(25gシリカ、0~20%MTBE/石油エーテル)により精製して、4-メトキシベンジル2-((4-(4-ブチルベンジル)オキサゾール-2-イル)メチル)アクリレート(125mg、0.30mmol、92%)を無色の油として得た。LCMS:(システム2,方法C)m/z 420.2(M+H)+(ES+)。
4-メトキシベンジル2-((4-(4-ブチルベンジル)オキサゾール-2-イル)メチル)アクリレート(125mg、0.30mmolmmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.2%ギ酸/水);勾配:57~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下35℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((4-(4-ブチルベンジル)オキサゾール-2-イル)メチル)アクリル酸(50mg、0.17mmol、56%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 300.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.67(br,1H)、7.67(s,1H)、7.15-7.06(m,4H)、6.18(s,1H)、5.72(d,J=1.5Hz,1H)、3.71(s,2H)、3.68(s,2H)、2.56-2.50(m,2H)、1.57-1.46(m,2H)、1.35-1.22(m,2H)、0.88(t,J=7.3Hz,3H)。
2-(4-シクロブチルフェニル)-N-ヒドロキシアセトイミダミド(中間体153、500mg、2.45mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、40%EtOAc/石油エーテル)により精製して、tert-ブチル3-(3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(760mg、1.59mmol、65%)を無色の油として得た。LCMS:(システム2,方法C)m/z 479.2(M+H)+(ES+)。
tert-ブチル3-(3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(760mg、1.59mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、0~30%MTBE/石油エーテル)により精製して、tert-ブチル2-((3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(480mg、1.35mmol、85%)を淡黄色の油として得た。LCMS:(システム2,方法C)m/z 355.3(M+H)+,377.2(M+Na)+(ES+)。
tert-ブチル2-((3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(480mg、1.35mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.2%ギ酸/水);勾配:50~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下40℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(307mg、1.03mmol、76%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 299.1(M+H)+,321.1(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.80(br,1H)、7.22-7.13(m,4H)、6.26(d,J=1.2Hz,1H)、5.90(d,J=1.3Hz,1H)、4.00(s,2H)、3.90(s,2H)、3.54-3.41(m,1H)、2.32-2.19(m,2H)、2.13-1.87(m,3H)、1.85-1.72(m,1H)。
4-ブトキシ-3-フルオロ-N-ヒドロキシベンズイミダミド(中間体155、400mg、1.77mmol)から、一般的な手順B、方法Bに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、40%EtOAc/石油エーテル)により精製して、tert-ブチル3-(3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(400mg、0.80mmol、45%)を黄色の固体として得た。LCMS:(システム2,方法C)m/z 501.2(M+H)+(ES+)。
tert-ブチル3-(3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(400mg、0.80mmol)から、一般的な手順A、ステップ2、方法Cに従って調製した。粗生成物をフラッシュカラムクロマトグラフィー(40gシリカ、0~20%MTBE/石油エーテル)により精製して、tert-ブチル2-((3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(290mg、0.77mmol、96%)を黄色の油として得た。LCMS:(システム2,方法C)m/z 377.2(M+H)+(ES+)。
tert-ブチル2-((3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(290mg、0.77mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物を分取HPLC(カラム:Waters X-Bridge C18 OBD 10μm 19x250mm;流量:20mL/分;溶媒系:MeCN/(0.2%ギ酸/水);勾配:53~95%MeCN;収集波長:214nm)によって精製した。画分を減圧下30℃で濃縮してMeCNを除去し、残留物を凍結乾燥して、2-((3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(180mg、0.56mmol、73%)を白色の固体として得た。LCMS:(システム2,方法B)m/z 321.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ:12.86(br,1H)、7.80-7.67(m,2H)、7.34(t,J=8.6Hz,1H)、6.32(s,1H)、6.00(d,J=1.3Hz,1H)、4.13(t,J=6.5Hz,2H)、4.01(s,2H)、1.80-1.68(m,2H)、1.51-1.38(m,2H)、0.94(t,J=7.4Hz,3H)。
4-シクロブトキシ-N-ヒドロキシベンズイミダミド(0.81g、3.5mmol、90%純度)から、一般的な手順B、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.04g、1.9mmol、90%純度)を透明な無色のガムとして得た。LCMS m/z 425.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.92-7.81(m,2H)、7.07-6.93(m,2H)、4.84-4.67(m,1H)、4.17-4.02(m,4H)、3.74-3.54(m,1H)、3.51-3.36(m,1H)、3.34-3.31(m,1H)、2.46-2.40(m,2H)、2.16-1.96(m,2H)、1.86-1.73(m,1H)、1.73-1.57(m,1H)、1.37(s,9H)、1.30-1.19(m,6H)。
tert-ブチル3-(3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.04g、1.9mmol、90%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.59g、1.5mmol、90%純度)を透明な無色の油として得た。LCMS m/z 301.3(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.92-7.82(m,2H)、7.04-6.93(m,2H)、6.32-6.22(m,1H)、6.03-5.90(m,1H)、4.85-4.67(m,1H)、4.00(s,2H)、2.48-2.40(m,2H)、2.13-1.99(m,2H)、1.86-1.74(m,1H)、1.73-1.59(m,1H)、1.33(s,9H)。
tert-ブチル2-((3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.59g、1.5mmol、90%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.441g、1.4mmol)を白色の固体として得た。LCMS m/z 301.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.85(s,1H)、7.96-7.77(m,2H)、7.06-6.92(m,2H)、6.36-6.25(m,1H)、6.04-5.90(m,1H)、4.88-4.65(m,1H)、4.00(s,2H)、2.48-2.40(m,2H)、2.13-1.98(m,2H)、1.88-1.74(m,1H)、1.72-1.58(m,1H)。
HATU(2.85g、7.50mmol)を、DCM(30mL)中の2-(3-クロロ-4-メトキシフェニル)-2,2-ジフルオロ-N-ヒドロキシアセトイミダミド(1.74g、6.25mmol、90%純度)、4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(2.13g、6.87mmol)、およびトリエチルアミン(2.6mL、18.7mmol)の混合物に加えた。混合物を室温で2時間撹拌し、次に1M HCl(50mL)で希釈し、DCM(2×40mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。残留物をTHF(40mL)中に入れ、炭酸セシウム(4.7g、14mmol)を加えた。反応物を70℃に加熱し、3時間撹拌した。混合物を室温に冷却し、1M HCl(50mL)でクエンチし、EtOAc(3×40mL)で抽出した。合わせた有機相を乾燥させ(MgSO4)、濃縮した。粗生成物をRP Flash C18でのクロマトグラフィー(5~75%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル3-(3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.63g、2.1mmol、69%純度)を褐色のガムとして得た。LCMS m/z 547.3(M+Na)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.61(d,J=2.3Hz,1H)、7.56(dd,J=8.7,2.4Hz,1H)、7.31(d,J=8.7Hz,1H)、4.14-3.99(m,4H)、3.92(s,3H)、3.71-3.55(m,1H)、3.52-3.33(m,2H)、1.30(s,9H)、1.27-1.18(m,6H)。
tert-ブチル3-(3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(1.63g、2.1mmol、69%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~25%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.83g、1.8mmol、87%純度)を透明な無色のガムとして得た。1H NMR(400MHz,DMSO-d6)δ 7.62(d,J=2.3Hz,1H)、7.60-7.55(m,1H)、7.31(d,J=8.7Hz,1H)、6.30-6.17(m,1H)、6.00-5.91(m,1H)、4.05(s,2H)、3.92(s,3H)、1.24(s,9H)。
tert-ブチル2-((3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(0.83g、1.8mmol、87%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-((3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(0.53g、1.5mmol)を淡黄色のガムとして得た。LCMS m/z 343.3(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.87(s,1H)、7.65(d,J=2.3Hz,1H)、7.57(dd,J=8.7,2.4Hz,1H)、7.31(d,J=8.7Hz,1H)、6.33-6.28(m,1H)、6.02-5.95(m,1H)、4.04(s,2H)、3.93(s,3H)。
HATU(2.30g、6.04mmol)を、DCM(25mL)中の2-(3,5-ジクロロ-4-フルオロフェニル)-2,2-ジフルオロ-N-ヒドロキシアセトイミダミド(1.50g、5.49mmol)、4-(tert-ブトキシ)-3-(ジエトキシホスホリル)-4-オキソブタン酸(1.70g、5.49mmol)、およびDIPEA(2.1mL、12mmol)の混合物に室温で加えた。混合物を1時間撹拌し、次に水(50mL)で希釈した。相を分離し、水相をEtOAc(2x25mL)で抽出した。合わせた有機相を飽和水性NaHCO3(50mL)、1M HCl(50mL)、およびブライン(50mL)で洗浄し、次に乾燥させ(MgSO4)、濃縮した。残留物をTHF(25mL)中に入れ、炭酸セシウム(2.15g、6.59mmol)を加えた。混合物を60℃に加熱し、1時間撹拌し、次に室温に冷却し、16時間撹拌した。混合物を濃縮した。残留物をEtOAc(50mL)と水(50mL)との間で分配した。相を分離し、水相をEtOAc(25mL)で抽出した。合わせた有機相を飽和水性NaHCO3(50mL)、1M HCl(50mL)、およびブライン(50mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(2.055g、3.6mmol)をオレンジの油として得た。LCMS m/z 491.0/493.0(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.91(d,J=6.2Hz,2H)、4.12-4.04(m,4H)、3.64(ddd,J=23.4,10.7,4.6Hz,1H)、3.53-3.44(m,1H)、3.36(ddd,J=17.1,9.1,4.6Hz,1H)、1.31(s,9H)、1.28-1.21(m,6H)。19F NMR(376MHz,DMSO)δ-93.49(d,J=2.7Hz)、-112.02.31P NMR(162MHz,DMSO)δ 19.94。
tert-ブチル3-(3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)-2-(ジエトキシホスホリル)プロパノエート(2.055g、3.6mmol)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.052g、2.4mmol)を黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.93(dd,J=6.1,0.8Hz,2H)、6.27(d,J=1.1Hz,1H)、5.97(d,J=1.2Hz,1H)、4.06(s,2H)、1.26(s,9H)。19F NMR(376MHz,DMSO)δ-93.91(d,J=2.8Hz)、-112.03。
tert-ブチル2-((3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリレート(1.052g、2.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、2-((3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸(690mg、1.9mmol)を濃い無色のガムとして得た。LCMS m/z 365.1/367.1(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.91(s,1H)、7.95(d,J=6.2Hz,2H)、6.32(d,J=1.0Hz,1H)、6.01(d,J=1.3Hz,1H)、4.06(s,2H)。
水酸化ナトリウム(4M水性、40mL、160mmol)を、EtOH(10mL)中のエチル1-アセチルシクロプロパン-1-カルボキシレート(5.00g、32mmol)の溶液に0℃で加えた。混合物を室温に温め、16時間撹拌した。混合物を部分的に濃縮し、MTBE(3x25mL)で抽出した。次に、水層を濃HClでpH約2に酸性化し、DCM(3×25mL)で抽出した。合わせた有機層をブライン(50mL)で洗浄し、乾燥させ(Na2SO4)、濃縮して、1-アセチルシクロプロパン-1-カルボン酸(3.62g、28mmol、87%、99%純度)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 12.86(s,1H)、2.36(s,3H)、1.36-1.28(m,4H)。
T3P(EtOAc中50重量%、11.8mL、20mmol)を、EtOAc(4mL)中のN-ヒドロキシ-1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボキシミダミド(2.00g、7.94mmol)、1-アセチルシクロプロパン-1-カルボン酸(1.02g、7.94mmol)、およびトリエチルアミン(3.3mL、24mmol)の溶液に室温で滴下して加えた。混合物を80℃に加熱し、18時間撹拌した。混合物を室温に冷却し、氷水(50mL)に注ぎ、次にEtOAc(3x20mL)で抽出した。合わせた有機層を飽和NaHCO3(2x25mL)、ブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/ヘキサン)により精製して、1-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)エタン-1-オン(1.09g、2.6mmol、80%純度)を淡黄色の油として得た。LCMS:m/z 337.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.73-7.69(m,2H)、7.66-7.61(m,2H)、2.24(s,3H)、1.76-1.72(m,2H)、1.63-1.59(m,2H)、1.59-1.55(m,2H)、1.50-1.45(m,2H)。
LDA(2M THF/ヘプタン/エチルベンゼン、1.68mL、3.35mmol)を、THF(15mL)中の1-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)エタン-1-オン(1.08g、3.19mmol)の溶液に-20℃で滴下して加えた。混合物を-20℃で30分間撹拌した後、THF(2mL)中のN-フェニル-ビス(トリフルオロメタンスルホンイミド)(1.25g、3.51mmol)の溶液を滴下して加えた。反応物を-10℃に温め、2時間撹拌した。飽和水性NH4Cl(20mL)を加え、混合物をEtOAc(3x20mL)で抽出した。合わせた有機層をブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮して、粗1-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)ビニルトリフルオロメタンスルホネート(2.28g)を琥珀色の固体として得、それを分析/精製なしで次のステップで使用した。
トリフェニルホスフィン(168mg、641μmol)およびパラジウム(II)アセテート(72mg、320μmol)を、ジメチルホルムアミド(7.5mL)中の粗1-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)ビニルトリフルオロメタンスルホネート(1.50g)の溶液に加えた。ギ酸(0.2mL、5.1mmol)およびトリエチルアミン(0.9mL、6.4mmol)を加えた。混合物を、CO(3バール)の雰囲気下、室温で18時間、室温で撹拌した。混合物を10%水性K2CO3(30mL)に注ぎ、MTBE(3x15mL)で抽出した。次に、水層を濃HClでpH約2に酸性化し、MTBE(3×15mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、濾過し、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)アクリル酸(21mg、59μmol)をオフホワイトの固体として得た。LCMS:m/z 365.4(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.76(s,1H)、7.69(d,J=8.2Hz,2H)、7.58(d,J=8.1Hz,2H)、6.32(s,1H)、5.93(s,1H)、1.54-1.45(m,4H)、1.45-1.36(m,4H)。19F NMR(376MHz,DMSO)δ-60.95。
(4-クロロフェニル)マグネシウムブロミド(MeTHF中1M、73mL、73mmol)を、THF(200mL)中のメチル6-ホルミルピコリネート(10.0g、60.6mmol)の懸濁液に-78℃で滴下して加えた。混合物を室温に温め、60時間撹拌した。混合物を飽和水性NH4Cl(10mL)でクエンチし、次に水(200mL)で希釈した。相を分離し、水相をEtOAc(2x100mL)で抽出した。合わせた有機相をブライン(200mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、メチル6-((4-クロロフェニル)(ヒドロキシ)メチル)ピコリネート(6.34g、22mmol)を黄色の油として得た。LCMS m/z 278.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.99(t,J=7.7Hz,1H)、7.92(dd,J=7.7,1.2Hz,1H)、7.79(dd,J=7.8,1.2Hz,1H)、7.44-7.39(m,2H)、7.39-7.34(m,2H)、6.35(d,J=4.2Hz,1H)、5.78(d,J=4.2Hz,1H)、3.87(s,3H)。
三臭化リン(0.50mL、5.4mmol)を、THF(15mL)中のメチル6-((4-クロロフェニル)(ヒドロキシ)メチル)ピコリネート(0.50g、1.8mmol)の溶液に加えた。混合物を室温で20分間撹拌し、次に80℃に加熱し、3時間撹拌し、次に室温に冷却し、18時間撹拌した。混合物を氷浴で冷却し、水(20mL)でクエンチし、次に固体Na2CO3で塩基性化した。相を分離し、水相をEtOAc(3x50mL)で抽出した。合わせた有機相をブライン(50mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)によって精製して、メチル6-(4-クロロベンジル)ピコリネート(260mg、0.98mmol)を無色の油として得た。LCMS m/z 262.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.96-7.87(m,2H)、7.52(dd,J=6.4,2.4Hz,1H)、7.39-7.33(m,2H)、7.32-7.26(m,2H)、4.17(s,2H)、3.87(s,3H)。
リチウムアルミニウムヒドリド(ジエチルエーテル中4M、1.2mL、4.8mmol)を、THF(25mL)中のメチル6-(4-クロロベンジル)ピコリネート(1.23g、4.70mmol)の溶液に0℃で滴下して加えた。混合物を1時間撹拌した。硫酸ナトリウム十水和物を、発泡が止まるまで少しずつ加えた。混合物を撹拌し、得られた懸濁液を濾過し、EtOAc(50mL)で洗浄した。濾液を乾燥させ(MgSO4)、濃縮して、(6-(4-クロロベンジル)ピリジン-2-イル)メタノール(1.128g、4.3mmol、90%純度)を黄色の油として得た。LCMS m/z 234.2/236.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.70(t,J=7.7Hz,1H)、7.38-7.24(m,5H)、7.10(dd,J=7.6,1.0Hz,1H)、5.35(t,J=5.9Hz,1H)、4.52(d,J=5.9Hz,2H)、4.04(s,2H)。
チオニルクロリド(0.80mL、11mmol)を、DCM(20mL)中の(6-(4-クロロベンジル)ピリジン-2-イル)メタノール(1.128g、4.3mmol、90%純度)の溶液に加えた。混合物を室温で2時間撹拌した。混合物を水(50mL)でクエンチし、固体K2CO3で塩基性化した。相を分離し、水相をEtOAc(2x50mL)で抽出した。合わせた有機相をブライン(50mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%EtOAc/イソヘキサン)により精製して、2-(4-クロロベンジル)-6-(クロロメチル)ピリジン(0.880g、3.4mmol)を黄色の油として得た。LCMS m/z 240.3/242.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.76(t,J=7.7Hz,1H)、7.38(dd,J=7.8,1.0Hz,1H)、7.37-7.32(m,2H)、7.32-7.27(m,2H)、7.23(dd,J=7.8,1.0Hz,1H)、4.74(s,2H)、4.08(s,2H)。
Tert-ブチル2-(ジエトキシホスホリル)アセテート(0.32mL、1.4mmol)を、THF(5mL)中の水素化ナトリウム(55mg、60重量%、1.4mmol)の懸濁液に0℃で滴下して加えた。混合物を30分間撹拌し、次にTHF(2mL)中の2-(4-クロロベンジル)-6-(クロロメチル)ピリジン(300mg、1.14mmol)の溶液を加えた。混合物を室温に温め、16時間撹拌した。ヨウ化ナトリウム(171mg、1.14mmol)を加え、混合物をさらに24時間撹拌した。混合物を飽和水性NH4Cl(2mL)でクエンチし、水(20mL)で希釈した。混合物をEtOAc(3×15mL)で抽出した。合わせた有機相をブライン(20mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、tert-ブチル3-(6-(4-クロロベンジル)ピリジン-2-イル)-2-(ジエトキシホスホリル)プロパノエート(366mg、0.47mmol、60%純度)を黄色の油として得た。LCMS m/z 468.3/470.3(M+H)+(ES+)。
tert-ブチル3-(6-(4-クロロベンジル)ピリジン-2-イル)-2-(ジエトキシホスホリル)プロパノエート(366mg、0.47mmol、60%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-((6-(4-クロロベンジル)ピリジン-2-イル)メチル)アクリレート(145mg、0.37mmol、88%純度)を無色の油として得た。LCMS m/z 344.3/346.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.63(t,J=7.7Hz,1H)、7.35-7.29(m,2H)、7.27(d,J=8.5Hz,2H)、7.08(d,J=7.6Hz,1H)、7.03(d,J=7.7Hz,1H)、6.08(d,J=1.7Hz,1H)、5.53(d,J=1.6Hz,1H)、4.01(s,2H)、3.69(s,2H)、1.30(s,9H)。
tert-ブチル2-((6-(4-クロロベンジル)ピリジン-2-イル)メチル)アクリレート(145mg、0.37mmol、88%純度)から、一般的な手順A、ステップ3に従って調製して、2-((6-(4-クロロベンジル)ピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩(139mg、0.34mmol)を粘着性の褐色の油として得た。LCMS m/z 288.2/290.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 13.05(br.s,2H)、8.06(t,J=7.9Hz,1H)、7.48-7.30(m,6H)、6.25(s,1H)、5.72(s,1H)、4.24(s,2H)、3.87(s,2H)。
HATU(3.29g、8.66mmol)を、DCM(35mL)中の2,2-ジフルオロ-N-ヒドロキシ-2-(4-(トリフルオロメチル)フェニル)アセトイミダミド(2.00g、7.87mmol)、1-アセチルシクロプロパン-1-カルボン酸(1.01g、7.87mmol)、およびDIPEA(3.0mL、17.3mmol)の混合物を室温で加えた。混合物を1時間撹拌し、次に水(50mL)で希釈した。相を分離し、水相をEtOAc(2x25mL)で抽出した。合わせた有機相を飽和水性NaHCO3(50mL)、1M HCl(50mL)、およびブライン(50mL)で洗浄し、次に乾燥させ(MgSO4)、濃縮した。残留物をTHF(35mL)中に入れ、炭酸セシウム(3.08g、9.44mmol)を加えた。混合物を60℃に加熱し、1時間撹拌し、次に室温に冷却し、水(60mL)に注いだ。混合物をEtOAc(3×25mL)で抽出した。合わせた有機相を1M HCl(50mL)、ブライン(50mL)で洗浄し、乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%EtOAc/イソヘキサン)により精製して、1-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)エタン-1-オン(1.79g、5.1mmol)をオレンジ色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.97(d,J=8.4Hz,2H)、7.92(d,J=8.4Hz,2H)、2.26(s,3H)、1.88-1.79(m,2H)、1.79-1.71(m,2H)。19F NMR(376MHz,DMSO)δ-61.61,-94.17。
LDA(2M THF/ヘプタン/エチルベンゼン、1.5mL、3.0mmol)を、THF(11mL)中の1-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)エタン-1-オン(0.984g、2.84mmol)の溶液に-20℃で滴下して加えた。混合物を-20℃で30分間撹拌した後、N-フェニル-ビス(トリフルオロメタンスルホンイミド)(1.12g、3.13mmol)を少しずつ加えた。反応物を-10℃に温め、2時間撹拌した。飽和水性NH4Cl(20mL)を加え、混合物をEtOAc(3x20mL)で抽出した。合わせた有機層をブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%DCM/イソヘキサン)により精製して、1-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)ビニルトリフルオロメタンスルホネート(0.183g、0.31mmol、80%純度)を淡黄色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.98-7.94(m,2H)、7.91-7.87(m,2H)、5.82(d,J=4.7Hz,1H)、5.63(d,J=4.8Hz,1H)、1.84-1.82(m,2H)、1.80-1.75(m,2H)。
トリフェニルホスフィン(20mg、80μmol)およびパラジウム(II)アセテート(9mg、40μmol)を、ジメチルホルムアミド(2mL)中の1-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)ビニルトリフルオロメタンスルホネート(0.183g、0.31mmol、80%純度)の溶液に加えた。ギ酸(23μL、610μmol)およびトリエチルアミン(107μL、765μmol)を加えた。混合物を、CO(2バール)の雰囲気下、室温で18時間、室温で撹拌した。混合物を10%水性K2CO3(30mL)に注ぎ、MTBE(3x15mL)で抽出した。次に、水層を濃HClでpH約2に酸性化し、MTBE(3×15mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、濾過し、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)アクリル酸(36mg、95μmol)をオフホワイトの固体として得た。LCMS:m/z 373.1(M-H)-(ES-)。1H NMR(400MHz,DMSO-d6)δ 12.87(s,1H)、7.95(d,J=8.3Hz,2H)、7.87(d,J=8.3Hz,2H)、6.39(s,1H)、6.02(s,1H)、1.67-1.58(m,2H)、1.58-1.48(m,2H)。19F NMR(376MHz,DMSO)δ-61.61,-94.33。
2-クロロプロパノイルクロリド(1.75mL、18.0mmol)を、DCM(80mL)中のN-ヒドロキシ-1-(4-(トリフルオロメチル)フェニル)シクロプロパン-1-カルボキシミダミド(4.00g、16.4mmol)およびトリエチルアミン(2.6mL、18.8mmol)の溶液に0℃で滴下して加えた。混合物を室温に温め、2時間撹拌した。水(50mL)を加えた。有機層を分離し、濃縮された相分離器に通した。残留物をトルエン(80mL)中に溶解し、混合物を120℃に3時間加熱し、次に室温に冷却し、16時間撹拌した。混合物を濃縮し、粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、5-(1-クロロエチル)-3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール(3.76g、12mmol)を無色の油として得た。1H NMR(400MHz,DMSO-d6)δ 7.72(d,J=8.2Hz,2H)、7.64(d,J=8.2Hz,2H)、5.60(q,J=6.9Hz,1H)、1.83(d,J=6.9Hz,3H)、1.61-1.54(m,2H)、1.54-1.47(m,2H)。
ヨウ化ナトリウム(1.04g、6.95mmol)を、THF(8mL)中の5-(1-クロロエチル)-3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール(2.00g、6.31mmol)の溶液に室温で加えた。混合物を室温で1時間撹拌した。別に、水素化ナトリウム(60重量%、8.2mmol)を、THF(13mL)中のtert-ブチル2-(ジエトキシホスホリル)アセテート(1.9mL、8.2mmol)の溶液に0℃で加えた。混合物を0℃で10分間撹拌し、次に室温に温め、1時間撹拌した。得られた溶液を最初の混合物に滴下して加えた。次に混合物を60℃に加熱し、16時間撹拌した。混合物を室温に冷却し、水(40mL)に注ぎ、次にEtOAc(3x25mL)で抽出した。合わせた有機層をブライン(50mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタノエート(1.76g、3.2mmol)を無色の油として得た。LCMS:m/z 533.3(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.71(d,J=8.2Hz,2H)、7.62-7.56(m,2H)、4.12-3.93(m,4H)、3.71-3.57(m,1H)、3.45-3.34(m,1H)、1.52-1.37(m,11H)、1.29-1.16(m,11H)。19F NMR(376MHz,DMSO-d6)δ-60.99,-61.00.31P NMR(162MHz,DMSO-d6)δ 19.62,19.34。
水性ホルムアルデヒド(37重量%、0.68mL、9.2mmol)を、ジメチルホルムアミド(0.7mL)中のtert-ブチル2-(ジエトキシホスホリル)-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタノエート(1.00g、1.88mmol)および炭酸カリウム(566mg、4.09mmol)の懸濁液に室温で加えた。混合物を室温で30分間撹拌し、次に水(15mL)に注いだ。混合物をEtOAc(3×15mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、乾燥させ(Na2SO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、tert-ブチル2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタノエート(579mg、1.4mmol)を無色の油として得た。LCMS:m/z 353.4(M-tBu+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.71(d,J=8.2Hz,2H)、7.60(d,J=8.1Hz,2H)、6.23(s,1H)、5.82(s,1H)、4.20(q,J=7.1Hz,1H)、1.52-1.48(m,2H)、1.48-1.42(m,5H)、1.31(s,9H)。
tert-ブチル2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタノエート(579mg、1.4mmol)から、一般的な手順A、ステップ3に従って調製した。粗生成物をシリカゲルでのクロマトグラフィー(0~50%MTBE/イソヘキサン)により精製して、2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタン酸(331mg、0.93mmol)を無色のガムとして得た。LCMS m/z 353.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.83(s,1H)、7.70(d,J=8.2Hz,2H)、7.60(d,J=8.1Hz,2H)、6.28(s,1H)、5.82(s,1H)、4.22(q,J=7.1Hz,1H)、1.54-1.49(m,2H)、1.48-1.42(m,5H)。19F NMR(376MHz,DMSO-d6)δ-60.96。
フラスコに、2,2’-(シクロプロパン-1,1-ジイル)ビス(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン)(0.925g、3.15mmol)、cataCXium A Pd G3(115mg、0.16mmol)、1-ブロモ-4-クロロベンゼン(1.20g、6.29mmol)、Cs2CO3(3.08g、9.44mmol)、1,4-ジオキサン(75mL)、および水(7.5mL)を負荷した。得られた混合物を、窒素で15分間スパージングした。混合物を100℃に24時間加熱し、次に室温に冷却した。ブライン(100mL)を加え、混合物をEtOAc(3x80mL)で抽出した。合わせた有機層を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~5%MTBE/イソヘキサン)により精製して、2-(1-(4-クロロフェニル)シクロプロピル)-4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン(0.469g、1.6mmol)を淡黄色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 7.35-7.14(m,4H)、1.16(s,12H)、1.07-0.95(m,2H)、0.92-0.79(m,2H)。
メタノール(15mL)中の2-(1-(4-クロロフェニル)シクロプロピル)-4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン(0.495g、1.78mmol)およびフッ化水素カリウム(833mg、10.7mmol)の混合物を、80℃で5時間撹拌した。混合物を室温に冷却し、濃縮した。残留物を50%MTBE/イソヘキサン(20mL)で粉砕し、得られた沈殿物を濾過により収集し、50%MTBE/イソヘキサン(2×20mL)で濯いだ。固体を熱したアセトニトリル(30mL)に溶解し、濾過し、MeCN(2x20mL)で洗浄した。濾液を濃縮して、カリウム(1-(4-クロロフェニル)シクロプロピル)トリフルオロボレート(0.355g、1.1mmol、80%純度)を淡いピンク色の固体として得た。1H NMR(400MHz,DMSO-d6)δ 7.20-7.13(m,2H)、7.11-7.04(m,2H)、0.57-0.40(m,2H)、0.20-0.08(m,2H)。
フラスコに、カリウム(1-(4-クロロフェニル)シクロプロピル)トリフルオロボレート(0.355g、1.1mmol、80%純度)、cataCXium A Pd G3(37mg、0.05mmol)、tert-ブチル3-(6-ブロモピリジン-2-イル)-2-(ジエトキシホスホリル)プロパノエート(958mg、2.04mmol、90%純度)、Cs2CO3(998mg、3.06mmol)、トルエン(15.0mL)、および水(1.5mL)を負荷した。得られた混合物を、窒素で5分間スパージングした。混合物を95℃に24時間加熱し、次に室温に冷却した。ブライン(50mL)を加え、水相をEtOAc(3x40mL)で抽出した。合わせた有機層を乾燥させ(MgSO4)、濃縮した。粗生成物をシリカゲルでのクロマトグラフィー(0~100%MTBE/イソヘキサン)により精製して、tert-ブチル3-(6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)-2-(ジエトキシホスホリル)プロパノエート(0.090g、0.13mmol、70%純度)を淡褐色のガムとして得た。LCMS m/z 494.1/496.1(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.48(t,J=7.7Hz,1H)、7.44-7.40(m,2H)、7.37-7.31(m,2H)、7.05(d,J=7.6Hz,1H)、6.58(d,J=7.8Hz,1H)、4.17-3.99(m,4H)、3.69-3.52(m,1H)、3.29-3.18(m,1H)、3.10-3.01(m,1H)、1.65-1.47(m,2H)、1.29(s,9H)、1.28-1.23(m,6H)、1.23-1.20(m,2H)。
tert-ブチル3-(6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)-2-(ジエトキシホスホリル)プロパノエート(0.090g、0.13mmol、70%純度)から、一般的な手順A、ステップ2、方法Bに従って調製した。粗生成物をRP Flash C18でのクロマトグラフィー(5~90%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))により精製して、tert-ブチル2-((6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)メチル)アクリレート(0.039g、84μmol、80%純度)を淡褐色のガムとして得た。LCMS m/z 370.4/372.4(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 7.48(t,J=7.8Hz,1H)、7.44-7.39(m,2H)、7.38-7.32(m,2H)、6.96(d,J=7.6Hz,1H)、6.58(d,J=7.8Hz,1H)、6.10-6.04(m,1H)、5.58-5.52(m,1H)、3.68(s,2H)、1.53-1.46(m,2H)、1.34(s,9H)、1.21-1.15(m,2H)。
tert-ブチル2-((6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)メチル)アクリレート(0.039g、84μmol、80%純度)から、一般的な手順A、ステップ3に従って調製した。粗生成物をRP Flash C18(5~75%MeCN/(水中0.1%ギ酸))でのクロマトグラフィーにより精製して、2-((6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)メチル)アクリル酸(0.021g、57μmol、88%純度)を褐色の固体として得た。LCMS m/z 314.2/316.2(M+H)+(ES+)。1H NMR(400MHz,DMSO-d6)δ 12.48(s,1H)、7.47(t,J=7.8Hz,1H)、7.44-7.33(m,4H)、6.97(d,J=7.6Hz,1H)、6.56(d,J=7.8Hz,1H)、6.14-6.10(m,1H)、5.61-5.46(m,1H)、3.69(s,2H)、1.57-1.47(m,2H)、1.21-1.16(m,2H)。
THP-1からのIL-1βサイトカイン出力に対する阻害効果の測定
式(I)の化合物のサイトカイン阻害プロファイルを、分化THP-1細胞アッセイで決定した。すべてのアッセイは、特に明記されていない限り、10%ウシ胎児血清(FBS;Gibco)、1%ペニシリン-ストレプトマイシン、および1%ピルビン酸ナトリウムを補充したRPMI-1640増殖培地(Gibco)中で実施した。IL-1βサイトカイン阻害アッセイは、以下に記載されるように、分化THP-1細胞のバックグラウンドで実施した。記載されるすべての試薬は、特に明記されていない限り、Sigma-Aldrichからである。化合物を10mM DMSOストックとして調製した。
THP-1細胞は、適切な増殖培地で最大80%のコンフルエントまで懸濁液として増殖させた。細胞を回収し、懸濁して、適切な濃度のホルボール12-ミリステート13-アセテート(PMA)で72時間(37℃/5%CO2)処理した。
DiscoverX PathHunter NRF2転座キットでの抗炎症性転写因子NRF2に対する化合物活性化効果の測定
NRF2(核因子赤芽球2関連因子2)を活性化する目的の標的に対する式(I)の化合物の効力および有効性を、PathHunter NRF2転座キット(DiscoverX)を使用して決定した。NRF2転座アッセイは、酵素断片相補性を利用して、Keap1-NRF2タンパク質複合体の活性化と、それに続くNRF2の核への転座を決定する、操作された組換え細胞株を使用して実施した。酵素活性は、PKタグ付きNRF2の核への移行時に機能性酵素が形成された後に消費される化学発光基質を使用して定量化した。
U2OS PathHunter eXpress細胞を、プレーティング前に凍結から解凍した。プレーティング後、U2OS細胞を市販のキット提供細胞培地で24時間インキュベートした(37℃/5%CO2)。
解凍した凍結保存肝細胞(生存率>70%)は、固有クリアランス(Clint;血流および細胞結合の非存在下での肝臓からの化合物の除去の尺度)の計算を介して化合物の代謝安定性を決定するために使用したクリアランスデータは、薬物の半減期および経口バイオアベイラビリティを予測するためにインビボデータと組み合わせて使用できるため、インビトロ作業にとって特に重要である。
本明細書で引用される以下の刊行物は、参照によりその全体が本明細書に組み込まれる。
Ackermann et al.Proc.Soc.Exp.Bio.Med.1949,72(1),1-9.
Andersen J.L.et al.Nat.Commun.2018,9,4344.
Angiari S.and O’Neill L.A.Cell Res.2018,28,613-615.
Bagavant G.et al.Indian J.Pharm.Sci.1994,56,80-85.
Bambouskova M.et al.Nature 2018,556,501-504.
Blewett M.M.et al.Sci.Sign.2016,9(445),rs10;6.
Brennan M.S.et al.PLoS One 2015,10,e0120254.
Bruck J.et al.Exp.Dermatol.2018,27,611-624.
Cocco M.et al.J.Med.Chem.2014,57,10366-10382.
Cocco M.et al.J.Med.Chem.2017,60,3656-3671.
Cordes T.et al.J.Biol.Chem.2016,291,14274-14284.
Cordes T.et al.Mol.Metab.2020,32,122-135.
Daly R.et al.medRxiv 2019,19001594;doi:https://doi.org/10.1101/19001594.
Daniels B.P.et al.Immunity 2019,50(1),64-76.e4.
Dibbert S.et al.Arch.Dermatol.Res.2013,305,447-451.
ElAzzouny M.et al.J.Biol.Chem.2017,292,4766-4769.
Gillard G.O.et al.J.Neuroimmunol.2015,283,74-85.
Gu L.et al.Immunol.Cell Biol.2020,98(3),229-241.
Hanke T.et al.Pharmacol.Therapeut.2016,157,163-187.
Hunt T.et al.Consortium of Multiple Sclerosis Centers 2015 Annual Meeting,27-30 May 2015,Indianapolis,IN,USA:Poster DX37.
Kobayashi E.H.et al.Nat.Commun.2016,7,11624.
Kornberg M.D.et al.Science 2018,360,449-453.
Kulkarni R.A.et al.Nat.Chem.Biol.2019,15,391-400.
Lampropoulou V.et al.Cell Metab.2016,24,158-166.
Lehmann J.C.U.et al.J.Invest.Dermatol.2007,127,835-845.
Liao S.-T.et al.Nat.Commun.2019,10(1),5091.
Liu H.et al.Cell Commun.Signal.2018,16,81.
McGuire V.A.et al.Sci.Rep.2016,6,31159.
Michelucci A.et al.Proc.Natl.Acad.Sci.USA 2013,110,7820-7825.
Mills E.A.et al.Front.Neurol.2018,9,5.
Mills E.L.et al.Cell 2016,167,457-470.
Mills E.L.et al.Nature 2018,556,113-117.
Mrowietz U.et al.Trends Pharmacol.Sci.2018,39,1-12.
Muller S.et al.J.Dermatol.Sci.2017,87,246-251.
Murphy M.P.and O’Neill L.A.J.Cell 2018,174,780-784.
O’Neill L.A.J.and Artyomov M.N.Nat.Rev.Immunol.2019 273-281.
Olagnier D.et al.Nat.Commun.2018,9,3506.
Schmidt T.J.et al.Bioorg.Med.Chem.2007,15,333-342.
Shan Q.et al.Biochem.Biophys.Res.Commun.2019,517,538-544.
Straub R.H.and Schradin C.Evol.Med.Public Health 2016,1,37-51S.
Straub R.H.and Cutolo M.Rheumatology 2016,55(Suppl.2),ii6-ii14.
Sun X.et al.,FASEB J.2019,33,12929-12940.
Tang C.et al.Cell Physiol.Biochem.2018,51,979-990.
Tang C.et al.Biochem.Biophys.Res.Commun.2019,508,921-927.
Tang H.et al.Biochem.Biophys.Res.Commun.2008,375,562-565.
Tian et al.Eur.J.Pharmacol.2020,873,172989.
van der Reest J.et al.Nat.Commun.2018,9,1581.
von Glehn F.et al.Mult.Scler.Relat.Disord.2018,23,46-50.
Yi F.et al.Hepatology 2020,873,172989.
Yu X.-H.et al.Immunol.Cell Biol.2019,97,134-141.
Zhang D.et al.Int.Immunopharmacol.2019,77,105924.
Zhang S.et al.Bioorg.Med.Chem.2012,20,6073-6079.
Zhao C.et al.Microb.Pathogen.2019,133,103541.
Zhao G.et al.Biochem.Biophys.Res.Commun.2014,448,303-307.
特許および特許出願を含む、本出願で言及されるすべての参考文献は、可能な限り最大限に参照することにより本明細書に組み込まれる。
Claims (17)
- 式(I)の化合物であって、
または
RA1が、C1-10アルキル、C2-10アルケニル、C2-10アルキニル、-(CH2)0-6-C3-10シクロアルキル、-(CH2)0-6-C5-10スピロシクロアルキル、-(CH2)0-6-アリール、およびO-アリールからなる群から選択され、
RA1が、任意にハロ、C1-6アルキル、C1-6ハロアルキル、ヒドロキシ、シアノ、OG1、S(O)0-2G1、SF5、(CH2)0-3C3-7シクロアルキル、および5~7員ヘテロシクリルからなる群から選択される1つ以上の置換基で置換され、前記C3-7シクロアルキルおよび前記5~7員ヘテロシクリルが、任意にハロ、C1-3アルキル、およびC1-3ハロアルキルから選択される1つ以上の基で置換され、同じ炭素原子と結合する2つのアルキル基が、任意に連結して、C3-7シクロアルキル環を形成し、C3-10シクロアルキル基が、任意にフェニル環に縮合し、前記フェニル環が、任意に1つ以上のハロ原子で置換されるか、またはRA1が、任意にC1-2ハロアルキル、C1-2ハロアルコキシ、もしくは1つ以上のハロ原子で置換される1つのフェニル環で任意に置換され、
G1が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、または(CH2)0-1フェニルであり、G1が、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
RA2が、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、ヒドロキシ、シアノ、ニトロ、NR1R2、OG2、およびS(O)0-2G2からなる群から選択され、
G2が、C1-6アルキル、C3-7シクロアルキル、C1-6ハロアルキル、またはフェニルであり、それが、任意にハロ、C1-2アルキル、C1-2ハロアルキル、ヒドロキシ、シアノ、ニトロ、C1-2アルコキシ、およびC1-2ハロアルコキシからなる群から選択される1つ以上の置換基で置換され、
R1およびR2が独立して、HまたはC1-2アルキルであるか、または一緒になって、R1およびR2が組み合わされて、5~7員複素環を形成し得、
またはRA2が、非存在であり、
RCおよびRDが各々独立して、H、C1-2アルキル、ヒドロキシ、フルオロ、またはC1-2アルコキシであるか、またはRCおよびRDが連結して、C3-5シクロアルキル環を形成し得、
基RA1およびRA2の炭素原子の総数が、それらの任意の置換基を含んで一緒に、6~14であり、
あるいはその薬学的に許容される塩および/または溶媒和物。 - RA1が、-(CH2)0-2-フェニルであり、ここで、RA1が、1つのOG1基で置換され、G1が、C1-6アルキルである、請求項1~3のいずれか一項に記載の化合物、あるいはその薬学的に許容される塩および/または溶媒和物。
- RA2が、非存在であり、RCが、Hであり、そして、RDが、Hである、請求項1~4のいずれか一項に記載の化合物、あるいはその薬学的に許容される塩および/または溶媒和物。
- 2-((3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチル-1,3,4-オキサジアゾール-2-イル)メチル)アクリル酸、
2-((5-オクチル-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(4-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-クロロフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-ヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ナフタレン-2-イルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(8,8,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(2-メチルヘプタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((1-オクチル-1H-1,2,4-トリアゾール-3-イル)メチル)アクリル酸、
2-((3-(3,4-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(tert-ブチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3,5-ジクロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(7,7,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4’-クロロ-[1,1’-ビフェニル]-4-イル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ペンチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(2-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロフェニル)シクロブチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(2-メチルオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-ブチルフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(2-(4-クロロフェニル)プロパン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(7,7-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(シクロヘキシルメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-(4-クロロフェニル)プロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクチル-d17)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクタ-7-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-プロピルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチル-1,3,4-チアジアゾール-2-イル)メチル)アクリル酸、
2-((4-オクチルチアゾール-2-イル)メチル)アクリル酸、
2-((4-オクチルオキサゾール-2-イル)メチル)アクリル酸、
(R)-2-((3-(オクタン-2-イル1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-エチルフェネチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(S)-2-((3-(オクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(トリフルオロメトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(7,7,8-トリフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1-(トリフルオロメチル)シクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロ-3-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-ノニル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(8,8,8-トリフルオロオクタン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチルチアゾール-2-イル)メチル)アクリル酸、
2-((3-ウンデシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(オクタ-3-イン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(8,8-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-オクチルオキサゾール-2-イル)メチル)アクリル酸、
2-((3-(9,9,9-トリフルオロノニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジスピロ[3.1.36.14]デカン-2-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-シクロオクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-シクロヘキシル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-シクロヘプチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(アダマンタン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(6-メチルヘプチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ネオペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-プロピルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1-プロピルシクロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(3,3,3-トリフルオロプロピル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(5,5,5-トリフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(2-シクロプロピルエチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(ジフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロペンチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1,2,2-テトラフルオロエトキシ)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-(1,1,2,2-テトラフルオロエトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(6,6,8,8,8-ペンタフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1,1-ジフルオロオクチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-((4-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-((4-ブロモフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-ブチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロペンチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-(トリフルオロメトキシ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-(4-ブチルベンジル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((5-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(4-(1,1-ジフルオロブチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-(1-(4-(トリフルオロメトキシ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-3-イル)メチル)アクリル酸、
2-((3-(4-(ベンジルオキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((4-(4-ブチルフェニル)オキサゾール-2-イル)メチル)アクリル酸、
2-((5-オクチルイソオキサゾール-3-イル)メチル)アクリル酸、
2-((4-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)オキサゾール-2-イル)メチル)アクリル酸、
2-((4-オクチルピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩、
2-((5-オクチルピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩、
2-((5-オクチルピリミジン-2-イル)メチル)アクリル酸、
2-((5-オクチルピラジン-2-イル)メチル)アクリル酸、
2-((6-オクチルピリダジン-3-イル)メチル)アクリル酸、
2-((5-メチル-4-オクチルオキサゾール-2-イル)メチル)アクリル酸、
2-(ヒドロキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((5-ブチル-4-(4-クロロフェニル)オキサゾール-2-イル)メチル)アクリル酸、
2-(メトキシ(3-オクチル-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロブトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-シクロペンチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロプロポキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロペンチルフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ヨードフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブロモフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ヨードフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-ヨードフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((4,5-ジブチルオキサゾール-2-イル)メチル)アクリル酸、
2,2-((3-(ジフルオロ(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2,2-((3-(ジフルオロ(4-フルオロフェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブチルフェノキシ)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((4-(4-ブチルベンジル)オキサゾール-2-イル)メチル)アクリル酸、
2-((3-(4-シクロブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3-フルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-プロポキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-シクロブチルフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(ピロリジン-1-イル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3,5-ジクロロ-4-フルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3,5-ジクロロ-4-フルオロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-クロロ-3,5-ジフルオロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロ-4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-(トリフルオロメチル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(4-ブロモ-3-クロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブロモ-3-クロロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロ-4-メトキシフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(1-(3-クロロ-4-メチルフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-シクロブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-シクロペンチルオキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(R)-2-((3-(4-(sec-ブトキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
(S)-2-((3-(4-(sec-ブトキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(4,4,4-トリフルオロブトキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(1-プロピルシクロプロピル)ベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4,6-ジクロロ-2,3-ジヒドロ-1H-インデン-1-イル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-プロポキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((3-クロロ-4-メトキシフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((3-クロロ-4-メチルフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-クロロフェニル)フルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((3,5-ジクロロ-4-フルオロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-((4-ブロモ-3-クロロフェニル)ジフルオロメチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(ジフルオロ(4-((トリフルオロメチル)チオ)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-(1-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)アクリル酸、
3-メチル-2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタン酸、
2-((3-(1-(4-((トリフルオロメチル)スルフィニル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-((トリフルオロメチル)チオ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-(3-メトキシプロポキシ)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3-クロロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3-(トリフルオロメチル)フェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-ブトキシ-3,5-ジフルオロフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-メトキシベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(4-クロロ-3,5-ジフルオロベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((3-(3-クロロ-4-メチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
2-((6-(4-クロロベンジル)ピリジン-2-イル)メチル)アクリル酸トリフルオロ酢酸塩、
2-(1-(3-(ジフルオロ(4-(トリフルオロメチル)フェニル)メチル)-1,2,4-オキサジアゾール-5-イル)シクロプロピル)アクリル酸、
2-メチレン-3-(3-(1-(4-(トリフルオロメチル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)ブタン酸、
2-((6-(1-(4-クロロフェニル)シクロプロピル)ピリジン-2-イル)メチル)アクリル酸、および
2-((3-(1-(4-ブロモ-3,5-ジクロロフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸、
からなる群から選択される、請求項1に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。 - 2-((3-(4-ブチルベンジル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸である、請求項5に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
- 2-((3-(1-(4-ブロモフェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸である、請求項5に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
- 2-((3-(4-ブトキシフェニル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸である、請求項5に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
- 2-((3-(1-(4-((トリフルオロメチル)チオ)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸である、請求項5に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
- 2-((3-(1-(4-(ペンタフルオロ-λ6-スルファネイル)フェニル)シクロプロピル)-1,2,4-オキサジアゾール-5-イル)メチル)アクリル酸である、請求項5に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
- 請求項1~11のいずれか一項に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物を含む、薬剤として使用するための、薬学的組成物。
- 炎症性疾患もしくは望ましくない免疫応答に関連する疾患の治療または予防に使用するための、請求項1~11のいずれか一項に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物を含む、薬学的組成物。
- 前記炎症性疾患または望ましくない免疫応答に関連する疾患が、乾癬(慢性プラーク、紅皮症、膿疱性、滴状、逆および爪変異を含む)、喘息、慢性閉塞性肺疾患(COPD、慢性気管支炎および肺気腫を含む)、心不全(左心室不全を含む)、心筋梗塞、狭心症、他のアテローム性動脈硬化症および/またはアテローム血栓症関連障害(末梢血管疾患および虚血性脳卒中を含む)、ミトコンドリアおよび神経変性疾患、自己免疫腫瘍随伴性網膜症、移植拒絶反応(抗体媒介型およびT細胞媒介型を含む)、多発性硬化症、横断性脊髄炎、虚血再灌流傷害、AGE誘発性のゲノム損傷、炎症性腸疾患、原発性硬化性胆管炎(PSC)、PSC-自己免疫性肝炎重複症候群、非アルコール性脂肪性肝疾患(非アルコール性脂肪性肝炎)、リウマチ性、環状肉芽腫、皮膚エリテマトーデス(CLE)、全身性エリテマトーデス(SLE)、ループス腎炎、薬剤誘導性ループス、自己免疫性心筋炎または心筋心膜炎、ドレスラー症候群、巨細胞性心筋炎、心膜切開後症候群、薬剤性過敏症症候群(過敏性心筋炎を含む)、湿疹、サルコイドーシス、結節性紅斑、急性散在性脳脊髄炎(ADEM)、視神経脊髄炎スペクトラム障害、MOG(ミエリンオリゴデンドロサイト糖タンパク質)抗体関連障害(MOG-EMを含む)、視神経炎、CLIPPERS(ステロイドに反応する橋血管周囲の増強を伴う慢性リンパ球性炎症)、びまん性脊髄破砕性硬化症、アジソン病、円形脱毛症、強直性脊椎炎、他の脊椎関節炎(乾癬、炎症性腸疾患、反応性関節炎または若年発症型に関連する末梢脊椎関節炎を含む)、抗リン脂質抗体症候群、自己免疫性溶血性貧血、自己免疫性肝炎、自己免疫性内耳疾患、類天疱瘡(水疱性類天疱瘡、粘膜類天疱瘡、瘢痕性類天疱瘡、妊娠性類天疱瘡または類天疱瘡、眼性瘢痕性類天疱瘡を含む)、線状IgA病、ベーチェット病、セリアック病、シャーガス病、皮膚筋炎、I型糖尿病、子宮内膜症、グッドパスチャー症候群、グレーブス病、ギランバレー症候群およびそのサブタイプ(急性炎症性脱髄性多発神経障害、AIDP、急性運動軸索ニューロパシー(AMAN)、急性運動および感覚軸索ニューロパシー(AMSAN)、咽頭-頸部-腕神経叢変異体、ミラーフィッシャー変異体およびビッカースタッフ脳幹脳炎を含む)、進行性炎症性ニューロパシー、橋本病、化膿性汗腺炎、封入体筋炎、壊死性ミオパチー、川崎病、IgA腎症、ヘノッホシェーンライン紫斑病、特発性血小板減少性紫斑病、血栓性血小板減少性紫斑病(TTP)、エヴァンス症候群、間質性膀胱炎、混合性結合組織病、未分化結合組織病、モルフィア、重症筋無力症(MuSK抗体陽性および血清陰性変異体を含む)、ナルコレプシー、神経筋緊張症、尋常性天疱瘡、悪性貧血、乾癬性関節炎、多発性筋炎、原発性胆汁性胆管炎(原発性胆汁性肝硬変としても知られる)、関節リウマチ、パリンドローム性リウマチ、統合失調症、自己免疫(髄膜)脳炎症候群、強皮症、シェーグレン症候群、全身硬直症候群、リウマチ性多発筋痛、巨細胞性動脈炎(側頭動脈炎)、高安動脈炎、結節性多発動脈炎、川崎病、多発血管炎性肉芽腫症(GPA;以前はウェゲナー肉芽腫症として知られていた)、多発血管炎を伴う好酸球性肉芽腫症(EGPA;以前はチャーグ-ストラウス症候群として知られていた)、顕微鏡的多発動脈炎/多発血管炎、低補体性蕁麻疹性血管炎、過敏性血管炎、クリオグロブリン血症、閉塞性血栓血管炎(バージャー病)、血管炎、白血球破砕性血管炎、白斑、急性散在性脳脊髄炎、副腎白質ジストロフィー、アレキサンダー病、アルパー病、バロ同心硬化症またはマールブルグ病、特発性器質化肺炎(以前は、肺炎を組織化する閉塞性気管支炎として知られていた)、カナバン病、中枢神経系血管炎症候群、シャルコー・マリー・トゥース病、中枢神経系髄鞘形成不全を伴う小児運動失調、慢性炎症性脱髄性多発神経障害(CIDP)、糖尿病性網膜症、グロボイド細胞白質ジストロフィー(クラッベ病)、移植片対宿主病(GVHD)(急性および慢性形態、ならびに腸GVHDを含む)、C型肝炎(HCV)感染または合併症、単純ヘルペスウイルス感染または合併症、ヒト免疫不全ウイルス(HIV)感染または合併症、扁平苔癬、平山病、嚢胞性線維症、肺動脈性肺高血圧症(PAH、特発性PAHを含む)、肺サルコイドーシス、特発性肺線維症、小児喘息、アトピー性皮膚炎、アレルギー性皮膚炎、接触性皮膚炎、アレルギー性鼻炎、鼻炎、副鼻腔炎、結膜炎、アレルギー性結膜炎、乾性角結膜炎、ドライアイ、眼球乾燥症、緑内障、黄斑浮腫、糖尿病性黄斑浮腫、網膜中心静脈閉塞症(CRVO)、黄斑変性症(乾性および/または湿性加齢性黄斑変性症、AMDを含む)、術後白内障炎症、ブドウ膜炎(後部、前部、中間および汎ブドウ膜炎を含む)、虹彩毛様体炎、強膜炎、角膜移植片および角膜細胞移植片拒絶反応、グルテン感受性腸症(セリアック病)、疱疹状皮膚炎、好酸球性食道炎、アカラシア、自己免疫性自律神経失調症、自己免疫性脳脊髄炎、自己免疫性食道炎、自己免疫性精巣炎、自己免疫性膵炎、大動脈炎および血管周囲炎、自己免疫性網膜症、自己免疫性蕁麻疹、ベーチェット病、(特発性)キャッスルマン病、コーガン症候群、IgG4関連疾患、後腹膜線維症、全身性若年性特発性関節炎(スティル病)を含む若年性特発性関節炎、成人発症スティル病、木質結膜炎、ムーレン潰瘍、急性痘瘡状苔癬状粃糠疹(PLEVA、ムッハ・ハーベルマン病としても知られる)、多巣性運動ニューロパシー(MMN)、小児急性発症神経精神症候群(PANS)(連鎖球菌感染症(PANDAS)に関連する小児自己免疫性神経精神障害を含む)、傍腫瘍性症候群(傍腫瘍性小脳変性症、ランバート・イートン筋麻酔症候群、辺縁系脳炎、脳幹脳炎、眼球クローヌス・ミオクローヌス運動失調、抗NMDA受容体脳炎、胸腺腫関連多臓器自己免疫を含む)、静脈周囲脳脊髄炎、反射性交感神経性ジストロフィー、再発性多発性軟骨炎、精子および精巣自己免疫、スザック症候群、トロサハント症候群、フォークト・小柳・原田症候群、抗シンテターゼ症候群、自己免疫性腸症、免疫調節不全多発性内分泌障害腸症X連鎖(IPEX)、顕微鏡的大腸炎、自己免疫性リンパ増殖症候群(ALPS)、自己免疫性多内分泌腺症-カンジダ症-外胚葉性ジストロフィー症候群(APEX)、痛風、偽痛風、アミロイド(AAまたは続発性アミロイドーシスを含む)、好酸球性筋膜炎(シュルマン症候群)、プロゲステロン過敏症(プロゲステロン皮膚炎を含む)、家族性地中海熱(FMF)、腫瘍壊死因子(TNF)受容体関連周期性発熱症候群(TRAPS)、周期性発熱を伴う高免疫グロブリン血症D(HIDS)、PAPA(化膿性関節炎、壊疽性膿皮症、重度嚢胞性痒疹)症候群、インターロイキン1受容体アンタゴニスト(DIRA)の欠乏、インターロイキン36受容体アンタゴニスト(DITRA)の欠乏、クリオピリン関連周期症候群(CAPS)(家族性寒冷自己炎症症候群[FCAS]、マックルウェルズ症候群、新生児期発症多臓器炎症性疾患[NOMID]を含む)、NLRP12関連自己炎症性疾患(NLRP12AD)、周期性熱アフタ性口内炎(PFAPA)、脂肪異栄養症および高温を伴う慢性非定型好中球性皮膚症(CANDLE)、マジード症候群、ブラウ症候群(若年性全身性肉芽腫症としても知られる)、マクロファージ活性化症候群、慢性再発性多発性骨髄炎(CRMO)、家族性寒冷自己炎症症候群、変異型アデノシンデアミナーゼ2および単一遺伝子性インターフェロン症(アイカルディ・グティエール症候群、脳白質ジストロフィーを伴う網膜血管障害、脊椎軟骨異形成症、乳児期に発症するSTING[インターフェロン遺伝子の刺激因子]関連血管障害、プロテアソーム関連自己炎症症候群、家族性凍瘡、遺伝性対側性色異常症を含む)、シュニッツラー症候群;家族性円柱腫症、先天性B細胞リンパ球増加症、OTULIN関連自己炎症性症候群、2型糖尿病、インスリン抵抗性およびメタボリックシンドローム(肥満関連の炎症を含む)、アテローム性動脈硬化症、および、腎炎症性疾患、からなる群から選択される疾患であるか、またはそれに関連する、請求項13に記載の薬学的組成物。
- さらなる治療剤であって、コルチコステロイド(糖質コルチコイド)、レチノイド、アントラリン、ビタミンD類似体、カルシニューリン阻害剤、シクロスポリン、チオプリン、メトトレキサート、抗TNFα剤、ホスホジエステラーゼ-4(PDE4)阻害剤、抗IL-17剤、抗IL12/IL-23剤、抗IL-23剤、JAK(ヤヌスキナーゼ)阻害剤、静脈内免疫グロブリン(IVIG)、シクロホスファミド、抗CD20 B細胞枯渇剤、アントラサイクリン類似体、クラドリビン、スフィンゴシン1-リン酸受容体修飾因子またはスフィンゴシン類似体、インターフェロンベータ製剤(インターフェロンベータ1b/1aを含む)、グラチラマー、抗CD52標的剤、レフルノミド、テリフルノミド、金化合物、ラキニモド、カリウムチャネル遮断剤、ミコフェノール酸、ミコフェノール酸モフェチル、プリン類縁物質、mTOR(ラパマイシンの機械的標的)経路阻害剤、抗胸腺細胞グロブリン(ATG)、IL-2受容体(CD25)阻害剤、抗IL-6受容体または抗IL-6剤、ブルトン型チロシンキナーゼ(BTK)阻害剤、チロシンキナーゼ阻害剤、ウルソデオキシコール酸、ヒドロキシクロロキン、クロロキン、B細胞活性化因子(BAFF、BLyS、Bリンパ球刺激剤としても知られる)阻害剤、汎阻害剤を含むPI3K阻害剤、またはアイソフォームを含むp110δおよび/もしくはp110γを標的とする阻害剤、インターフェロンα受容体阻害剤、T細胞共刺激遮断剤、サリドマイドおよびその誘導体、ダプソン、クロファジミン、ロイコトリエンアンタゴニスト、テオフィリン、抗IL-5剤、長時間作用型ムスカリン剤、リルゾール、フリーラジカルスカベンジャー、プロテアソーム阻害剤、C5に指向するものを含む補体カスケード阻害剤、免疫吸着剤、抗胸腺細胞グロブリン、5-アミノサリチル酸およびその誘導体、α4β1および/またはα4β7インテグリンを標的とするものを含む抗インテグリン剤、抗CD11-α剤、サリチラートを含む非ステロイド性抗炎症剤(NSAID)、オキシカム、フェナメート、選択的または比較性選択的COX-2阻害剤、コルヒチン、IL-4受容体阻害剤、IL-1β阻害剤、クロラムブシル、免疫調節特性および/またはNRF2を調節する能力を有する特定の抗生物質、ペントキシフィリン、ウルソデオキシコール酸、オベチコール酸、フィブラート、嚢胞性線維症膜コンダクタンス(CFTR)制御因子、VEGF(血管内皮増殖因子)阻害剤、ピルフェニドン、およびミゾリビン、から選択される治療剤と組み合わせて使用するための、請求項12~14のいずれか一項に記載の薬学的組成物。
- 式(I)の化合物あるいはその薬学的に許容される塩および/または溶媒和物が、式(I)の化合物である、請求項1~11のいずれか一項に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
- 式(I)の化合物あるいはその薬学的に許容される塩および/または溶媒和物が、式(I)の化合物の薬学的に許容される塩である、請求項1~11のいずれか一項に記載の化合物あるいはその薬学的に許容される塩および/または溶媒和物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2025077120A JP2025131581A (ja) | 2019-12-23 | 2025-05-07 | 抗炎症特性を有するカルボン酸誘導体 |
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19219531 | 2019-12-23 | ||
| EP19219531.1 | 2019-12-23 | ||
| EP20162545 | 2020-03-11 | ||
| EP20162545.6 | 2020-03-11 | ||
| EP20189623.0 | 2020-08-05 | ||
| EP20189623 | 2020-08-05 | ||
| EP20205768 | 2020-11-04 | ||
| EP20205768.3 | 2020-11-04 | ||
| PCT/GB2020/053357 WO2021130492A1 (en) | 2019-12-23 | 2020-12-23 | Carboxy derivatives with antiinflammatory properties |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025077120A Division JP2025131581A (ja) | 2019-12-23 | 2025-05-07 | 抗炎症特性を有するカルボン酸誘導体 |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| JP2023508142A JP2023508142A (ja) | 2023-03-01 |
| JPWO2021130492A5 JPWO2021130492A5 (ja) | 2023-12-22 |
| JP2023508142A5 JP2023508142A5 (ja) | 2023-12-22 |
| JP7679384B2 true JP7679384B2 (ja) | 2025-05-19 |
Family
ID=74104118
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022538727A Active JP7679384B2 (ja) | 2019-12-23 | 2020-12-23 | 抗炎症特性を有するカルボン酸誘導体 |
| JP2025077120A Pending JP2025131581A (ja) | 2019-12-23 | 2025-05-07 | 抗炎症特性を有するカルボン酸誘導体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025077120A Pending JP2025131581A (ja) | 2019-12-23 | 2025-05-07 | 抗炎症特性を有するカルボン酸誘導体 |
Country Status (30)
| Country | Link |
|---|---|
| US (1) | US20230219907A1 (ja) |
| EP (2) | EP4442319A3 (ja) |
| JP (2) | JP7679384B2 (ja) |
| KR (1) | KR20220119425A (ja) |
| CN (1) | CN115066418B (ja) |
| AU (1) | AU2020412853A1 (ja) |
| BR (1) | BR112022011933A2 (ja) |
| CA (2) | CA3161424C (ja) |
| CL (1) | CL2022001722A1 (ja) |
| CO (1) | CO2022008652A2 (ja) |
| CR (1) | CR20220300A (ja) |
| DK (1) | DK4081511T3 (ja) |
| EC (1) | ECSP22049370A (ja) |
| ES (1) | ES2987014T3 (ja) |
| FI (1) | FI4081511T3 (ja) |
| HR (1) | HRP20241378T1 (ja) |
| HU (1) | HUE068571T2 (ja) |
| IL (1) | IL293982B2 (ja) |
| JO (1) | JOP20220162A1 (ja) |
| LT (1) | LT4081511T (ja) |
| MA (1) | MA58170B1 (ja) |
| MD (1) | MD4081511T2 (ja) |
| MX (1) | MX2022007846A (ja) |
| PE (1) | PE20221584A1 (ja) |
| PH (1) | PH12022551546A1 (ja) |
| PL (1) | PL4081511T4 (ja) |
| RS (1) | RS66019B1 (ja) |
| SI (1) | SI4081511T1 (ja) |
| TW (1) | TWI891696B (ja) |
| WO (1) | WO2021130492A1 (ja) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MA55795A (fr) | 2019-04-30 | 2022-03-09 | Sitryx Therapeutics Ltd | Dérivés d'acide itaconique et leurs utilisations dans le traitement d'une maladie inflammatoire ou d'une maladie associée à une réponse immunitaire indésirable |
| IL322315A (en) | 2019-05-14 | 2025-09-01 | Provention Bio Inc | Methods and preparations for preventing type 1 diabetes |
| AU2021287998B2 (en) | 2020-06-11 | 2026-03-12 | Benaroya Research Institute At Virginia Mason | Methods and compositions for preventing type 1 diabetes |
| WO2022029438A1 (en) | 2020-08-05 | 2022-02-10 | Sitryx Therapeutics Limited | Alpha,beta unsaturated methacrylic esters with anti-inflammatory properties |
| WO2022229617A1 (en) * | 2021-04-26 | 2022-11-03 | Sitryx Therapeutics Limited | 2-methylene-4-oxo-butanoic acid drivatives for the treatment of inflammation |
| US12565529B2 (en) | 2021-05-24 | 2026-03-03 | Provention Bio, Inc. | Methods for treating type 1 diabetes |
| WO2022269251A1 (en) * | 2021-06-22 | 2022-12-29 | Sitryx Therapeutics Limited | Acrylamide derivatives useful as anti-inflammatory agents |
| CN113499453B (zh) * | 2021-07-20 | 2022-10-21 | 徐州医科大学 | 自噬抑制及抗炎联合温合光热诊疗剂及其制备方法与应用 |
| US20240360067A1 (en) | 2021-08-11 | 2024-10-31 | Sitryx Therapeutics Limited | Derivatives of itaconic acid and their use as anti-inflammatory agents |
| CN119968366A (zh) | 2022-06-22 | 2025-05-09 | 西特瑞治疗有限公司 | 噁二唑衍生物、其制备方法及其在治疗炎性疾病中的用途 |
| WO2024089421A1 (en) | 2022-10-25 | 2024-05-02 | Sitryx Therapeutics Limited | Tetrazole derivatives |
| JP2025541281A (ja) | 2022-12-15 | 2025-12-18 | シトリクス・セラピューティクス・リミテッド | 炎症性疾患若しくは望ましくない免疫応答に関連する疾患の治療又は予防に使用するための置換ピリジン |
| KR102864655B1 (ko) * | 2023-01-19 | 2025-09-29 | 대한민국 | 뎅기바이러스 감염에 의한 질환의 예방 또는 치료용 약학적 조성물 |
| CN115819186B (zh) * | 2023-02-14 | 2023-05-16 | 广东银珠医药科技有限公司 | 一种3,5-二氯苯甲醇的新型制备方法 |
| CN117205194A (zh) * | 2023-05-10 | 2023-12-12 | 苏州大学 | 衣康酸或其衍生物在制备预防或治疗急性移植物抗宿主病药物中的应用 |
| CN116725998A (zh) * | 2023-07-20 | 2023-09-12 | 中国科学技术大学 | 特立氟胺在抑制nlrp3炎症小体活化中的应用 |
| CN118812769B (zh) * | 2024-07-02 | 2025-09-26 | 南京工业大学 | 一种衣康酰肼诱导的Janus结构聚合物表皮贴片电极及其制备方法 |
| CN119792264B (zh) * | 2025-03-14 | 2025-06-10 | 华中科技大学同济医学院附属同济医院 | 丁酰肼在制备预防或治疗copd的药物中的应用 |
| CN120585811B (zh) * | 2025-08-07 | 2026-01-06 | 华南理工大学 | 4-辛基衣康酸在制备改善肺动脉高压的药物中的应用 |
| CN121668151A (zh) * | 2026-02-11 | 2026-03-17 | 武汉大学人民医院(湖北省人民医院) | 衣康酸类化合物在制备治疗视网膜动脉阻塞药物中的用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103923105A (zh) | 2014-04-17 | 2014-07-16 | 北京大学 | 2-中氮茚甲酰胺类化合物及其制备和用途 |
| WO2014152263A1 (en) | 2013-03-15 | 2014-09-25 | Karyopharm Therapeutics Inc. | Exo olefin-containing nuclear transport modulators and uses thereof |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995011235A1 (en) * | 1993-10-20 | 1995-04-27 | The Upjohn Company | Pyrimidinones as antiarthritic and anti-inflammatories |
| US6566384B1 (en) * | 1996-08-07 | 2003-05-20 | Darwin Discovery Ltd. | Hydroxamic and carboxylic acid derivatives having MMP and TNF inhibitory activity |
| TW201206429A (en) * | 2010-07-08 | 2012-02-16 | Merck Serono Sa | Substituted oxadiazole derivatives |
| PE20140421A1 (es) * | 2010-12-06 | 2014-04-26 | Glaxo Group Ltd | COMPUESTOS DERIVADOS DE PIRIMIDINONA COMO INHIBIDORES DE Lp-PLA2 |
| BR112015022854A2 (pt) | 2013-03-14 | 2017-07-18 | Alkermes Pharma Ireland Ltd | pró-farmacos de fumaratos e uso do mesmo no tratamento de várias doenças |
| AU2014290368B2 (en) * | 2013-07-18 | 2019-07-11 | Baylor College Of Medicine | Methods and compositions for treatment of muscle wasting, muscle weakness, and/or cachexia |
| EP3416634A4 (en) | 2016-02-15 | 2019-10-09 | Artyomov, Maxim | IMMUNOMODULATORY AGENTS AND METHOD FOR USE THEREOF |
| EP3668497A4 (en) | 2017-08-14 | 2021-04-28 | Washington University | Methods and compositions for the treatment of diseases associated with cancer, inflammation, or immune response |
| US20200377510A1 (en) * | 2019-05-30 | 2020-12-03 | Auransa Inc. | Derivatives of piperlongumine and uses thereof |
| CN110731955B (zh) | 2019-10-28 | 2023-05-02 | 中山大学 | 衣康酸二甲酯在预防和治疗溃疡性结肠炎及其癌变中的应用 |
-
2020
- 2020-12-23 JP JP2022538727A patent/JP7679384B2/ja active Active
- 2020-12-23 MD MDE20221214T patent/MD4081511T2/ro unknown
- 2020-12-23 PH PH1/2022/551546A patent/PH12022551546A1/en unknown
- 2020-12-23 EP EP24183456.3A patent/EP4442319A3/en not_active Withdrawn
- 2020-12-23 BR BR112022011933A patent/BR112022011933A2/pt unknown
- 2020-12-23 HU HUE20830293A patent/HUE068571T2/hu unknown
- 2020-12-23 AU AU2020412853A patent/AU2020412853A1/en active Pending
- 2020-12-23 CA CA3161424A patent/CA3161424C/en active Active
- 2020-12-23 CA CA3280359A patent/CA3280359A1/en active Pending
- 2020-12-23 PE PE2022001159A patent/PE20221584A1/es unknown
- 2020-12-23 CR CR20220300A patent/CR20220300A/es unknown
- 2020-12-23 ES ES20830293T patent/ES2987014T3/es active Active
- 2020-12-23 HR HRP20241378TT patent/HRP20241378T1/hr unknown
- 2020-12-23 CN CN202080083315.0A patent/CN115066418B/zh active Active
- 2020-12-23 KR KR1020227024819A patent/KR20220119425A/ko active Pending
- 2020-12-23 DK DK20830293.5T patent/DK4081511T3/da active
- 2020-12-23 IL IL293982A patent/IL293982B2/en unknown
- 2020-12-23 EP EP20830293.5A patent/EP4081511B3/en active Active
- 2020-12-23 US US17/787,870 patent/US20230219907A1/en active Pending
- 2020-12-23 MA MA58170A patent/MA58170B1/fr unknown
- 2020-12-23 PL PL20830293.5T patent/PL4081511T4/pl unknown
- 2020-12-23 WO PCT/GB2020/053357 patent/WO2021130492A1/en not_active Ceased
- 2020-12-23 MX MX2022007846A patent/MX2022007846A/es unknown
- 2020-12-23 SI SI202030480T patent/SI4081511T1/sl unknown
- 2020-12-23 RS RS20241087A patent/RS66019B1/sr unknown
- 2020-12-23 TW TW109145642A patent/TWI891696B/zh active
- 2020-12-23 LT LTEPPCT/GB2020/053357T patent/LT4081511T/lt unknown
- 2020-12-23 FI FIEP20830293.5T patent/FI4081511T3/fi active
-
2022
- 2022-06-21 EC ECSENADI202249370A patent/ECSP22049370A/es unknown
- 2022-06-21 JO JOP/2022/0162A patent/JOP20220162A1/ar unknown
- 2022-06-21 CO CONC2022/0008652A patent/CO2022008652A2/es unknown
- 2022-06-22 CL CL2022001722A patent/CL2022001722A1/es unknown
-
2025
- 2025-05-07 JP JP2025077120A patent/JP2025131581A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014152263A1 (en) | 2013-03-15 | 2014-09-25 | Karyopharm Therapeutics Inc. | Exo olefin-containing nuclear transport modulators and uses thereof |
| CN103923105A (zh) | 2014-04-17 | 2014-07-16 | 北京大学 | 2-中氮茚甲酰胺类化合物及其制备和用途 |
Non-Patent Citations (2)
| Title |
|---|
| Bioorganic & Medicinal Chemistry Letters,2015年,Vol. 25, No. 13,p. 2664-2667 |
| Journal of Medicinal Chemistry,2014年,Vol. 57, No. 24,p. 10366-10382 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7679384B2 (ja) | 抗炎症特性を有するカルボン酸誘導体 | |
| US12459908B2 (en) | Alpha, beta unsaturated methacrylic esters with anti-inflammatory properties | |
| KR20220002952A (ko) | 이타콘산 유도체, 및 염증성 질환 또는 바람직하지 않은 면역반응과 관련된 질환의 치료에서의 이의 용도 | |
| WO2022038365A9 (en) | Fumarate derivatives and their medical use | |
| WO2022090723A1 (en) | Itaconic acid derivatives | |
| WO2022090724A1 (en) | Novel compounds | |
| EP4237402A1 (en) | Novel compounds | |
| EP4359390A1 (en) | Acrylamide derivatives useful as anti-inflammatory agents | |
| KR20250136325A (ko) | 염증성 질환 또는 바람직하지 않은 면역 반응과 연관된 질환을 치료 또는 예방하는 데 사용하기 위한 치환된 피리딘 | |
| KR20250033235A (ko) | 옥사디아졸 유도체, 그의 제조 방법 및 염증성 질환의 치료에 있어서의 그의 용도 | |
| EA048584B1 (ru) | Карбоксипроизводные с противовоспалительными свойствами | |
| HK40083255A (en) | Carboxy derivatives with antiinflammatory properties | |
| HK40083255B (en) | Carboxy derivatives with antiinflammatory properties |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231214 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231214 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20240315 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20241121 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241126 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250225 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250408 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250507 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7679384 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |