JP7646972B2 - 乳酸菌由来のアンジオテンシン変換酵素阻害剤 - Google Patents
乳酸菌由来のアンジオテンシン変換酵素阻害剤 Download PDFInfo
- Publication number
- JP7646972B2 JP7646972B2 JP2021081054A JP2021081054A JP7646972B2 JP 7646972 B2 JP7646972 B2 JP 7646972B2 JP 2021081054 A JP2021081054 A JP 2021081054A JP 2021081054 A JP2021081054 A JP 2021081054A JP 7646972 B2 JP7646972 B2 JP 7646972B2
- Authority
- JP
- Japan
- Prior art keywords
- strain
- lactic acid
- acid bacteria
- cells
- angiotensin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Landscapes
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Cosmetics (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
このようにACEは、昇圧ペプチド(アンジオテンシンII)を産生すると共に、一方では降圧ペプチド(ブラジキニン)を分解、不活性化するので、結果として血圧を上昇させる作用を示す。すなわち、ACEを阻害することにより血圧の上昇を抑制することが出来るため、ACE阻害物質は有効な経口血圧降下剤として、各種開発研究がなされている。
一方で、最近では、皮膚に発現したACEをACE阻害物質で阻害することにより、皮膚の光老化が抑制されることが報告され(非特許文献1)、それを利用したしわ改善組成物が提案されている(例えば、特許文献1等)。
ある種の乳酸菌はプロバイオティクス(適量の経口摂取により宿主の健康維持に寄与する微生物)として知られ、様々な効用が報告されている。一方で、乳酸菌体成分を用いた外用剤の報告(非特許文献2)も見られる。乳酸菌に対する消費者のイメージは良く、加えて、合成物質でなく、微生物由来とすることにより、安価で調製が可能である新しい化粧品素材の開発に向けて、安全性の高い乳酸菌体由来のACE阻害物質の開発が求められている。
これまでに、ある種の乳酸菌について、乳の発酵に伴いACE阻害作用を示すペプチドが生産されることが報告されている(例えば、特許文献2等)。これらの機能性ペプチドの産生には、菌株のタンパク質分解能が影響を与え、有効なペプチドの種、量を産生する乳酸菌は限られており、同活性が低いものは、ACE阻害活性を示す乳酸菌のスクリーニングの対象から外れていた。
乳酸菌は現在44属に分かれており、安全性が低い属もある。このうち、高い安全性が確認されているラクトコッカス属乳酸菌由来の、菌株のタンパク質分解能に関係がない、ACE阻害剤に関する、新たな提案が望まれている。菌株のタンパク質分解能に関係がないものからスクリーニングすることにより、スクリーニングできる菌株数が増え、有効な菌株が見つけやすくなる可能性がある。また、タンパク質分解能は菌株のタンパク質分解酵素の活性に左右されることが多いが、同酵素活性を増大させるには遺伝子組み換えなどの方法を用いるしかない。
1.ラクトコッカス・ラクティスN7株(受託番号:FERM P-18217)の生菌体、死菌体及び抽出物から選択される1種以上を含有する、アンジオテンシン変換酵素阻害剤。
2.1.記載のアンジオテンシン変換酵素阻害剤を有効成分とする、皮膚の老化阻害組成物。
3.1.記載のアンジオテンシン変換酵素阻害剤を有効成分とする、しわ改善組成物。
4.ラクトコッカス・ラクティスN7株(受託番号:FERM P-18217)を、特定の炭素源下において培養する及び/又は熱処理することを特徴とする、アンジオテンシン変換酵素阻害活性を増大させる方法。
本発明はラクトコッカス・ラクティスN7株の生菌体、死菌体及び抽出物から選択される1種以上を含有する、ACE阻害剤を提供するものである。
ラクトコッカス・ラクティスN7株の正式名称は、ラクトコッカス・ラクティス・サブスピーシーズ・ラクティス・バイオバラエティー・ジアセチラクティスN7株で、独立行政法人 製品評価技術基盤機構 特許微生物寄託センターに寄託されており、その受託番号は、FERM P-18217である。
本発明における乳酸菌N7株は、国立研究開発法人 農業・食品産業技術総合研究機構 畜産研究部門内 畜産物研究領域が有する乳酸菌ライブラリーに保存されていた菌株の中から、ACE阻害活性が極めて高い菌株として選抜されたものである。
後述する実施例において詳細に説明するものの、本発明における乳酸菌N7株のACE阻害活性は、紫外線UV-B照射による正常ヒト表皮角化細胞の生存率の減少抑制効果を有すること(非特許文献3)を、本発明者らが確認した乳酸菌H61株と比較しても、1.7倍程度高いことからも、その有用性は極めて高いものと考えられる。
本発明における乳酸菌N7株の培養条件は、特に制限がなく、従来公知の条件下において培養することができる。
培養培地としては、ラクトコッカス属に属する乳酸菌が資化可能な炭素源、窒素源又は無機塩類などの必要な栄養源を加えた培地を挙げることができる。乳酸菌が生育できる培地であれば、天然培地、合成培地のいずれを用いてもよく、当業者であれば使用する適切な公知の培地を適宜選ぶことができる。炭素源としてはグルコース、ラクトース、ガラクトース、フルクトース、トレハロース、スクロース、マンノース、廃糖蜜などを使用することができ、窒素源としては肉エキス、ペプトン、イーストエキストラクト、カゼイン加水分解物、ホエータンパク質加水分解物、大豆タンパク質加水分解物などを使用することができる。また無機塩類としては、リン酸塩、ナトリウム、カリウム、マグネシウムなどを用いることができる。乳酸菌の培養に適した培地としては、例えばM17培地(グルコース添加)、MRS液体培地、GYP培地、TYG培地、GAM培地、獣乳、脱脂乳、乳性ホエーなどが挙げられ、中でも、MRS培地が好適である。
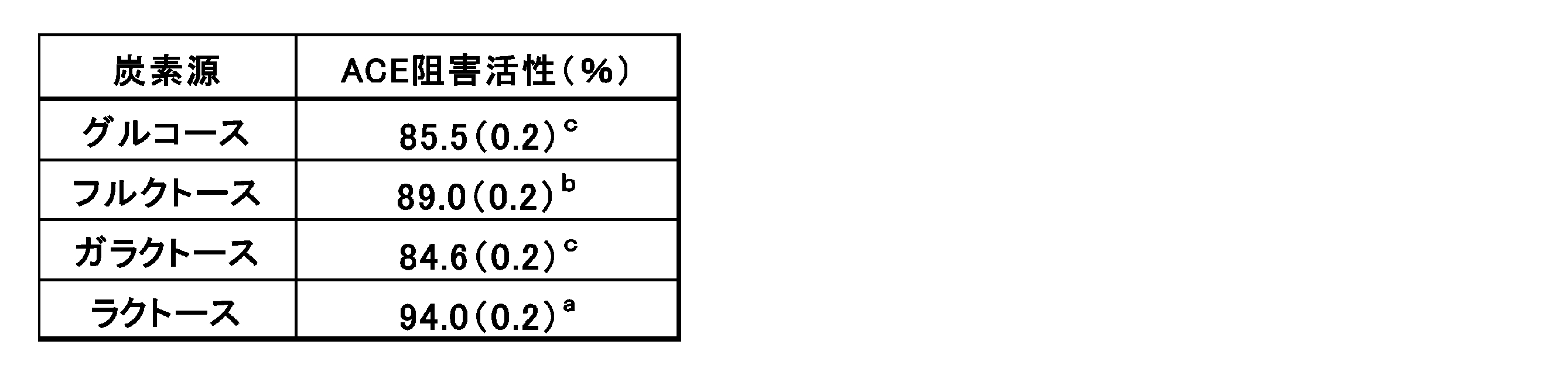
本発明における乳酸菌N7株は、乳酸菌の培養に一般的に使用されるMRS培地(炭素源はグルコース)において別の糖源に代替して培養することにより、ACE阻害活性を向上させ得ることができ、中でも、ラクトース、フルクトースを添加した培地で培養することにより、グルコースを添加した場合よりも、ACE阻害活性が向上することが後述する実施例により確認されている。
培地のpHは特に制限されないものの、通常pH5~7、好ましくはpH6~7の範囲を挙げることができる。なお、培地や培養装置は100℃以下の低温で殺菌して利用することができる。
培養温度は、乳酸菌N7株の生育温度の範囲、好ましくは最適生育温度の範囲に設定すればよく、例えば4℃~40℃の範囲を挙げることができ、好ましくは25~30℃程度である。培養時間は、制限はされないものの、例えば1~2日程度を挙げることができる。
培養に際して、酸素は特に遮断する必要も供給する必要もない。培養の形式は、静置培養、振とう培養、タンク培養などが挙げられる。
本発明における乳酸菌N7株は、培養後加熱処理した菌体のACE阻害活性が、生菌体のACE阻害活性よりも大きく向上することも後述する実験例により確認されている。
ここで、加熱処理とは、例えば菌体水懸濁液をブロックヒーターや湯浴に入れ、一定時間、保温することをいう。加熱処理に適した温度としては、95℃、100℃、121℃が挙げられるが、これに限定されない。
本発明における抽出物とは、水などの溶媒に懸濁した菌体部分を遠心分離により沈殿させた後の上清をいう。水に懸濁した菌体を加熱処理後にそのまま遠心分離したものは、「熱水抽出物」、加熱していない水に菌体を懸濁して、そのまま遠心分離を行った後の上清は「水抽出物」と呼称するが、いずれも本発明の抽出物に含まれる。
実施例において、実際に使用しているのはすべて抽出物であるが、抽出物に含まれるものは、もともと菌体の中にあるものなので、生菌体、死菌体にもACE阻害効果を有する物質が含まれていると考える。
菌体のACE阻害活性には菌体の糖タンパク質が関わっていると考えられ、糖成分は熱水で抽出されることから、生菌よりも関与成分の抽出量が多くなると考えられる。
(1)試験検体
乳酸菌N7株、H61株それぞれを、MRS培地(Becton, Dickinson and Company, Sparks, MD, USA)において30℃で一晩培養した後、5000g、10分間の条件で遠心分離を行って集菌し、菌体を0.85%塩化ナトリウム溶液で2回洗浄後、水に懸濁させて、121℃で15分間加熱処理をした。このサンプルを凍結乾燥して、産業的に汎用される死菌体凍結乾燥菌体末を調製し、ACE阻害活性測定用の試験検体とした。
試験検体をそれぞれ2mg採取し水に懸濁した。この死菌体水懸濁液を13000g、10分間の条件で遠心分離を行い、得られた上清(死菌体水抽出物)を水で10倍希釈したものを実施例1と同じACE阻害活性試験に供した。
(2)試験方法
ACE阻害活性はACE阻害活性測定キット(DOJINDO LABORATORIES, Kumamoto)を用い、キットのプロトコルに従って測定した。
1.96ウェルのマイクロプレートに、20μLのサンプルをサンプルウェル、ブランク1およびブランク2のウェルに加える。
2.キットに含まれる反応基質20μLをそれぞれのウェルに添加する。
3.20μLの水をブランク2のウェルに加える。
4.20μLの酵素反応液をサンプルウェルとブランク1のウェルに加える。
5.プレートにシールを貼り、37℃の恒温槽で1時間保温する。
6.200μLの指示液をそれぞれのウェルに加える。
7.プレートを室温で10分間保温する。
8.マイクロプレートリーダー(BIO-RAD Model 3550 Microplate Reader (Hercules, CA)で450nmの吸光度を測定する。
[ACE阻害活性の算出式]
ACE阻害活性(%)=[(Ablank1-Asample)/(Ablank1-Ablank2)]×100
Ablank1:水の吸光度(450nm)
Ablank2:反応基質の吸光度
Asample:菌サンプルの吸光度
試験結果を図1に示す。
図1に示すように、本発明における乳酸菌N7株のACE阻害活性は54.3%である一方で、乳酸菌H61株は32.8%であった。すなわち、乳酸菌N7株のACE阻害活性は、乳酸菌H61株のACE阻害活性より1.7倍程度高いことが明らかとなった。
乳酸菌H61株は、紫外線UV-B照射による正常ヒト表皮角化細胞の生存率の減少抑制効果を有することを本発明者らが確認したことからも、N7株には光老化に対し、有益な効果をもつことが期待された。
上記のとおり、本発明における乳酸菌N7株は、高いACE阻害活性を有することが確認された。
乳酸菌N7株について、一晩培養したMRS培養液を0.5%(v/v)でMRS培地に接種し、30℃で一晩培養した菌体(定常期)、5.5時間培養した菌体(対数期)、37℃で一晩培養した菌体を、集菌後、それぞれ水で3回洗浄後、水に懸濁して、100mg/mL(湿菌体重量 w/v)とした。この菌体水懸濁液を95℃で15分間加熱処理を行い、13000g、10分間の条件で遠心分離を行い、上清(熱水抽出物)について、実施例1に記載したACE阻害活性試験を行い、ACE阻害活性算出式に従い、ACE阻害活性(%)を算出した。
(1)試験方法
炭水化物(グルコース)を含まないMRS培地(C free MRS)を調製した。
このMRS培地(C free MRS)は、1%プロテオースペプトン、0.5%酵母エキス、0.1%Tween80、0.2%クエン酸アンモニウム、0.5%酢酸ナトリウム、0.01%硫酸マグネシウム、0.005%硫酸マンガン、及び0.2%リン酸二カリウムを含有する(pH6.5)。
グルコース、フルクトース、ラクトース、ガラクトースの10%溶液をそれぞれ作製し、フィルター(0.2μm、株式会社アドバンス製)で濾過し滅菌した。この溶液を、上記MRS培地に最終濃度が0.5%(v/v)になるように添加した。N7株を10%スキムミルクで一晩培養し、その1白金耳を0.85%塩化ナトリウム溶液に懸濁した菌液をそれぞれの培地に、0.5%濃度(v/v)で接種し、一晩培養した。培養菌体を集菌後、水で3回洗浄後、水に懸濁して、100mg/mL(湿菌体重量 w/v)とした。この菌体水懸濁液を95℃で15分間加熱処理を行い、13000g、10分間の条件で遠心分離を行い、上清(熱水抽出物)について、実施例1に記載したACE阻害活性試験を行い、ACE阻害活性算出式に従い、ACE阻害活性(%)を算出した。
(1)試験検体
乳酸菌N7株を、MRS培地において30℃で一晩培養した後、集菌し、菌体を水で3回洗浄後、水に懸濁させて、121℃で15分間加熱処理をした。この菌体水懸濁液を13000g、10分間の条件で遠心分離を行い、上清(熱水抽出物)を採取し、凍結乾燥したものを試験検体とした。
(2)試験方法
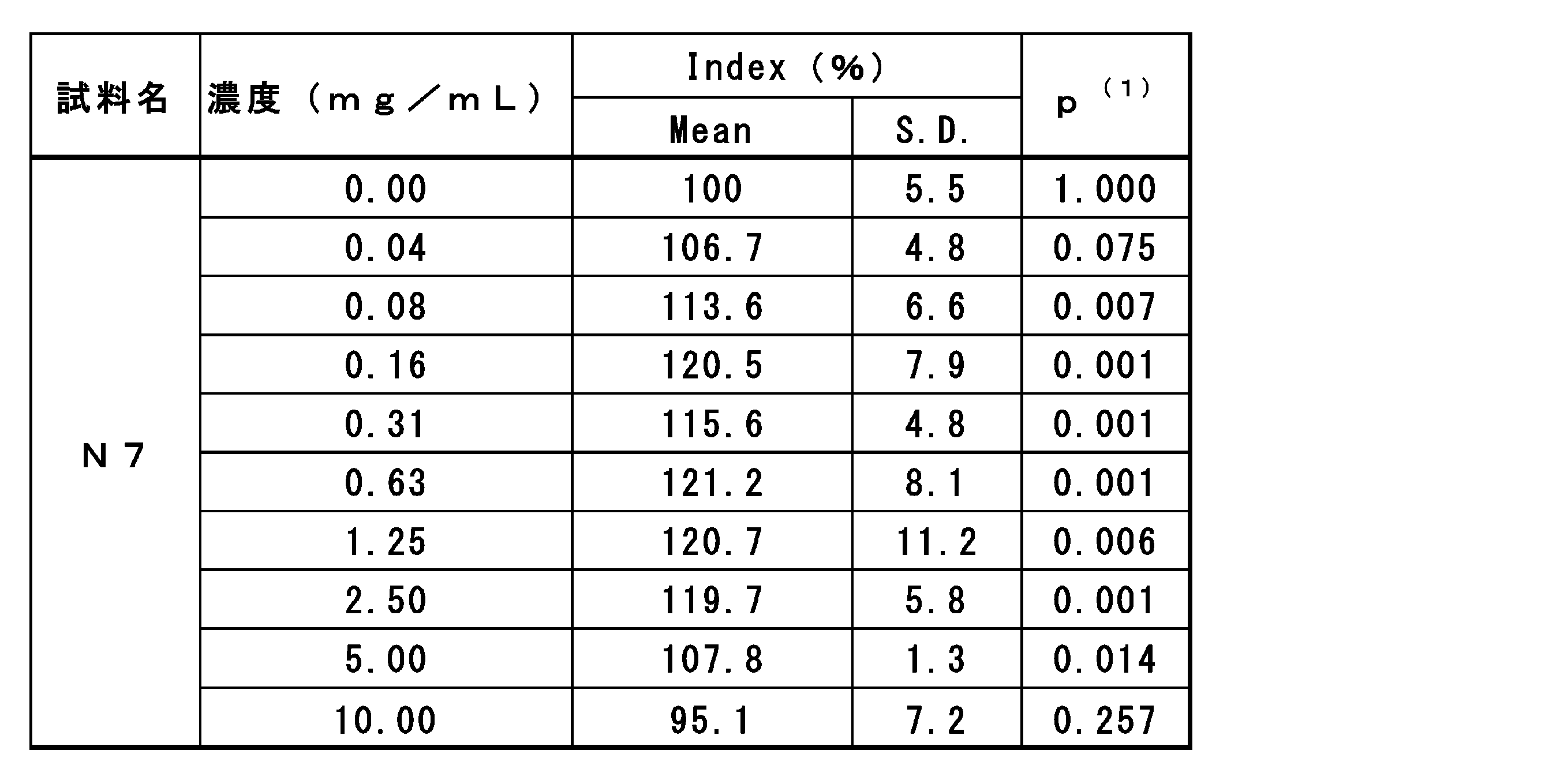
正常ヒト真皮線維芽細胞を、DMEM培地(5%FBS)を用いて、1.0×104cells/wellの細胞密度で48穴プレートに播種した。24時間培養後、上述の試験検体を、下記表3記載の濃度で含有するDMEM培地(5%FBS)に交換し、72時間培養した。培養後、細胞をトリプシン処理にて回収した後、フローサイトメトリーを用いて細胞数をカウントした。測定値について、Student‐t検定を用いて有意差検定を行った。
また、乳酸菌N7株熱水抽出物を0.04~5mg/mLを添加しても、正常ヒト真皮線維芽細胞の生存には影響がないことが明らかとなった。
(1)老化誘導した細胞の調製
正常ヒト真皮線維芽細胞に用時調整した600μmol/Lの過酸化水素を含有するDMEM(0%FBS)を添加して37℃で1時間培養した。1時間培養後、過酸化水素含有DMEM(0%FBS)を除去し、DMEM培地(10%FBS)を添加した。この操作を4日間繰り返した後、DMEM培地(10%FBS)で3日間培養した。ここで得られた細胞を老化誘導細胞とした。
老化誘導細胞の老化判定はSA-β-Gal染色にて行った。
すなわち、老化誘導細胞及び非老化誘導細胞を、5×104cells/wellの細胞密度にて48穴プレートに播種した。24時間培養した後、3%ホルムアルデヒドを含有するPBSにて固定した。1mg/mLのX-Galを含有するpH6の反応液(40mmol/Lクエン酸/リン酸ナトリウム、0.5mmol/Lフェロシアン化カリウム、5mmol/Lフェリシアン化カリウム、150mmol/L塩化ナトリウム、2mmol/L塩化マグネシウム)に交換し、16時間培養した。
培養後、顕微鏡観察を行い、非老化誘導細胞と老化誘導細胞で、老化マーカーであるSA-β-Gal染色強度を比較し、老化誘導細胞において非老化誘導細胞よりも染色強度の増加を確認した。
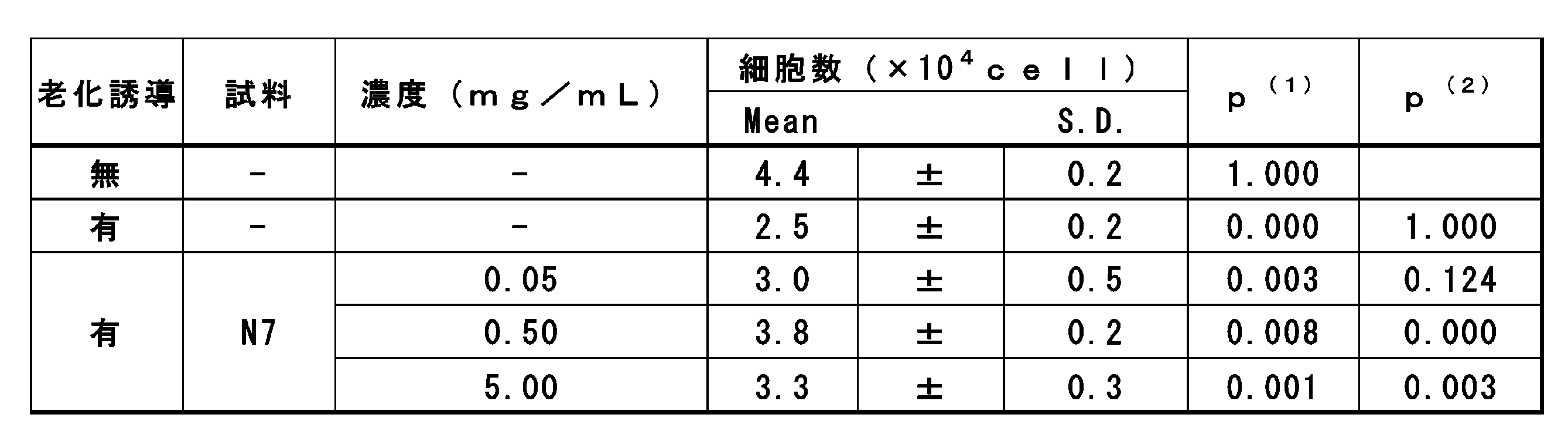
老化誘導細胞及び非老化誘導細胞を、DMEM培地(5%FBS)を用いて、1.0×104cells/wellの細胞密度で48穴プレートに播種した。24時間培養後、老化誘導細胞群では、乳酸菌N7株の菌体を121℃、15分で加熱処理後、遠心分離を行った熱水抽出試験検体を、下記表4記載の濃度で含有するDMEM培地(5%FBS)に交換し、72時間培養した。非老化誘導細胞では、試験検体を含有しないDMEM培地(5%FBS)に交換し、72時間培養した。培養後、細胞をトリプシン処理にて回収した後、フローサイトメトリーを用いて細胞数をカウントした。Student‐t検定を用いて有意差検定を行った。結果を表4に示す。
表4に示すとおり、老化誘導細胞は、非老化誘導細胞に比べて、細胞数が有意に減少した。正常ヒト真皮線維芽老化誘導細胞に乳酸菌N7株の菌体熱水抽出物を0.5~5.0mg/mLの範囲で添加すると、未添加の場合よりも細胞数が有意に増加し、細胞増殖能が増加することが確認された。
Claims (4)
- ラクトコッカス・ラクティスN7株(寄託番号:FERM P-18217)の生菌体、死菌体及び抽出物から選択される1種以上を含有する、アンジオテンシン変換酵素阻害剤。
- 請求項1記載のアンジオテンシン変換酵素阻害剤を有効成分とする、皮膚の老化阻害組成物。
- 請求項1記載のアンジオテンシン変換酵素阻害剤を有効成分とする、しわ改善組成物。
- ラクトコッカス・ラクティスN7株(寄託番号:FERM P-18217)を、グルコース、フルクトース、ガラクトース及びラクトースから選択される1種以上の炭素源下において培養する及び/又は熱処理することを特徴とする、アンジオテンシン変換酵素阻害活性を増大させる方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021081054A JP7646972B2 (ja) | 2021-05-12 | 2021-05-12 | 乳酸菌由来のアンジオテンシン変換酵素阻害剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021081054A JP7646972B2 (ja) | 2021-05-12 | 2021-05-12 | 乳酸菌由来のアンジオテンシン変換酵素阻害剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022174972A JP2022174972A (ja) | 2022-11-25 |
| JP7646972B2 true JP7646972B2 (ja) | 2025-03-18 |
Family
ID=84144916
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021081054A Active JP7646972B2 (ja) | 2021-05-12 | 2021-05-12 | 乳酸菌由来のアンジオテンシン変換酵素阻害剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7646972B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023086469A (ja) * | 2021-12-10 | 2023-06-22 | 株式会社ニコリオ | 線維芽細胞増殖促進用組成物、飲食品及び製造方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010143885A (ja) | 2008-12-22 | 2010-07-01 | Asahi Breweries Ltd | 乳酸菌およびそれらを用いた飲食物又は化粧品 |
| JP2011148734A (ja) | 2010-01-21 | 2011-08-04 | Shiseido Co Ltd | シワ処理におけるアンジオテンシン変換酵素阻害物質および/またはアンジオテンシンiiレセプター阻害物質の使用 |
| JP2015145357A (ja) | 2014-02-04 | 2015-08-13 | 株式会社東書エステート | 微粒子化した乳酸菌(ラクトコッカス・ラクティス・サブスピーシーズクレモリスh−61株)を有効成分として含有する降圧剤並びにこれを含有する薬剤及び食品 |
-
2021
- 2021-05-12 JP JP2021081054A patent/JP7646972B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010143885A (ja) | 2008-12-22 | 2010-07-01 | Asahi Breweries Ltd | 乳酸菌およびそれらを用いた飲食物又は化粧品 |
| JP2011148734A (ja) | 2010-01-21 | 2011-08-04 | Shiseido Co Ltd | シワ処理におけるアンジオテンシン変換酵素阻害物質および/またはアンジオテンシンiiレセプター阻害物質の使用 |
| JP2015145357A (ja) | 2014-02-04 | 2015-08-13 | 株式会社東書エステート | 微粒子化した乳酸菌(ラクトコッカス・ラクティス・サブスピーシーズクレモリスh−61株)を有効成分として含有する降圧剤並びにこれを含有する薬剤及び食品 |
Non-Patent Citations (1)
| Title |
|---|
| Appl. Environ. Microbiol.,2008年,Vol.74, No.2,pp. 424-436 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022174972A (ja) | 2022-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Aguilar-Toalá et al. | Assessment of multifunctional activity of bioactive peptides derived from fermented milk by specific Lactobacillus plantarum strains | |
| CN113773999B (zh) | 副干酪乳杆菌发酵滤液、制备方法及其应用 | |
| Nwamaioha et al. | A selective medium for the enumeration and differentiation of Lactobacillus delbrueckii ssp. bulgaricus | |
| EP0154549A2 (en) | Anticariogenic or antiperiodontitic agent | |
| CN111826300A (zh) | 动物双歧杆菌乳亚种gfc-b09菌株及包含其的化妆品组合物 | |
| CN113956993B (zh) | 一株具有缓解人角质形成细胞氧化损伤作用的副干酪乳杆菌 | |
| CN113930361A (zh) | 一种副干酪乳杆菌的发酵培养基及其应用 | |
| CN113088473B (zh) | 一株具有缓解HaCaT细胞氧化损伤作用的动物双歧杆菌 | |
| CN115093985A (zh) | 一种乳双歧杆菌及其发酵方法和应用 | |
| CN105296541A (zh) | 燕麦发酵液及其制备方法与作为化妆品原料的应用 | |
| KR102133689B1 (ko) | 용암해수 유래 미네랄과 더마바이오틱스 유래 뉴클레오티드의 결합체 제조방법 및 이를 이용한 기능성 더마바이오틱스 화장품 조성물 | |
| CN113604395A (zh) | 一株可发酵石斛且其发酵液可改善皮肤质量的植物乳杆菌 | |
| JP7646972B2 (ja) | 乳酸菌由来のアンジオテンシン変換酵素阻害剤 | |
| CN118620784A (zh) | 一株鼠李糖乳杆菌lthink-0088及其在美白、祛皱化妆品中的应用 | |
| Noori et al. | Growth optimization of Lactobacillus plantarum T5jq301796. 1, an Iranian indigenous probiotic in lab scale fermenter | |
| CN116904332B (zh) | 一株具有良好抗氧化效果的痤疮丙酸杆菌及其应用 | |
| US12128074B2 (en) | External agent for hair growth or hair loss prevention | |
| KR20110135477A (ko) | 항산화 및 미백 효능을 갖는 효모 발효액 및 이의 제조 방법 | |
| Marranzini et al. | Effect of threonine and glycine concentrations on threonine aldolase activity of yogurt microorganisms during growth in a modified milk prepared by ultrafiltration | |
| CN118755646B (zh) | 一种具有抗氧化、抗衰老、抗光老化作用的植物乳植杆菌mh95及其应用 | |
| JP2004149442A (ja) | 化粧料 | |
| JP3533427B2 (ja) | 化粧料 | |
| CN114317617A (zh) | 具有抗皱功效的三重益生菌发酵复合物制备方法及其应用 | |
| JPH0515366A (ja) | 乳酸菌およびビフイズス菌の増殖促進剤 | |
| JP3684205B2 (ja) | ラクトコッカス・ラクチスcbt−19及びこれを利用した抗菌培養液の分離濃縮物の製造方法並びにこれを包含する化粧料組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240202 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20250107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250109 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250128 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250210 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7646972 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |