JP7635237B2 - 4-[[(7-アミノピラゾロ[1,5-a]ピリミジン-5-イル)アミノ]メチル]ピペリジン-3-オール化合物及びそれらの治療的使用 - Google Patents
4-[[(7-アミノピラゾロ[1,5-a]ピリミジン-5-イル)アミノ]メチル]ピペリジン-3-オール化合物及びそれらの治療的使用 Download PDFInfo
- Publication number
- JP7635237B2 JP7635237B2 JP2022536538A JP2022536538A JP7635237B2 JP 7635237 B2 JP7635237 B2 JP 7635237B2 JP 2022536538 A JP2022536538 A JP 2022536538A JP 2022536538 A JP2022536538 A JP 2022536538A JP 7635237 B2 JP7635237 B2 JP 7635237B2
- Authority
- JP
- Japan
- Prior art keywords
- mmol
- methyl
- amino
- pyrimidin
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/138—Aryloxyalkylamines, e.g. propranolol, tamoxifen, phenoxybenzamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
- A61K31/282—Platinum compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4166—1,3-Diazoles having oxo groups directly attached to the heterocyclic ring, e.g. phenytoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4196—1,2,4-Triazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/513—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim having oxo groups directly attached to the heterocyclic ring, e.g. cytosine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/565—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol
- A61K31/568—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol substituted in positions 10 and 13 by a chain having at least one carbon atom, e.g. androstanes, e.g. testosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/565—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol
- A61K31/568—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol substituted in positions 10 and 13 by a chain having at least one carbon atom, e.g. androstanes, e.g. testosterone
- A61K31/5685—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol substituted in positions 10 and 13 by a chain having at least one carbon atom, e.g. androstanes, e.g. testosterone having an oxo group in position 17, e.g. androsterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/664—Amides of phosphorus acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/704—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin attached to a condensed carbocyclic ring system, e.g. sennosides, thiocolchicosides, escin, daunorubicin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Oncology (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Mycology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biomedical Technology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Microbiology (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
本出願は、2019年12月16日に出願された英国(GB)特許出願番号第1918541.2号に関連しており、該出願の内容は、参照によりその全体が本明細書に援用される。
サイクリン依存性プロテインキナーゼ(CDK)は、21個のセリン/スレオニンプロテインキナーゼのファミリーの触媒サブユニットであり(例えば、Malumbres et al., 2009を参照)、それらのうちのいくつかは、成長段階を通じた細胞の進行、DNA複製及び有糸分裂を制御する(例えば、Pines, 1995;Morgan, 1995を参照)。細胞周期の異なる段階を通しての適切な進行と、細胞周期の次の段階への移行には、特定のCDKの活性化が必要とされる。
Bondke et al., 2015は、CDK阻害剤としての特定のピラゾロ[1,5-a]ピリミジン-5,7-ジアミン化合物について記載しており、例えば、以下の化合物(当該文献中PPDA-001と呼ばれる):
本明細書中に記載されるH-APPAMP化合物は、強力なCDK12及び/又はCDK13阻害剤であり、これらはまた、例えば、CDK7と比較してCDK12及び/又はCDK13に対して高選択的でもある。
本発明の一態様は、本明細書中に記載される特定の4-[[(7-アミノピラゾロ[1,5-a]ピリミジン-5-イル)アミノ]メチル]ピペリジン-3-オール化合物(本明細書中「H-APPAMP化合物」と呼ばれる)に関する。
化合物
本発明の一態様は、ピラゾロ[1,5-a]ピリミジン-5,7-ジアミン(「PPDA」)に関連する特定の化合物:
(a) 7位における置換アミノ基(本明細書中-NH-L7-R7として示される);及び
(b) 3位におけるアルキル基又はシクロアルキル基(本明細書中-R3として示される)。
(式中、
-R7は、正確に1、2又は3個の環ヘテロ原子を有する縮合二環式C8-10ヘテロアリール基であり、各環ヘテロ原子はN、S又はOであり;
且つ-R7は、
場合により、炭素上で、1個以上の基-RSCにより置換されており;
場合により、存在する場合は第二級窒素上で、基-RSNにより置換されており;
ここで:
各-RSCは、独立して:
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)OH、-C(=O)ORTT、
-OC(=O)RTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、
-NHC(=O)RTT、-NRTNC(=O)RTT、
-NHC(=O)NH2、-NHC(=O)NHRTT、-NHC(=O)NRTT 2、-NHC(=O)RTM、
-NRTNC(=O)NH2、-NRTNC(=O)NHRTT、-NRTNC(=O)NRTT 2、-NRTNC(=O)RTM、
-NHC(=O)ORTT、-NRTNC(=O)ORTT、
-OC(=O)NH2、-OC(=O)NHRTT、-OC(=O)NRTT 2、-OC(=O)RTM、
-C(=O)RTT、
-SRTT、-S(=O)RTT、-S(=O)2RTT、
-S(=O)NH2、-S(=O)NHRTT、-S(=O)NRTT 2、-S(=O)RTM、
-S(=O)2NH2、-S(=O)2NHRTT、-S(=O)2NRTT 2、-S(=O)2RTM、
-NHS(=O)2RTT、-NRTNS(=O)2RTT、
-CN、又は-NO2
であり、
各-RSNは、独立して:
-RTT、
-LT-OH、-LT-ORTT、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)RTT、
-C(=O)ORTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、又は
-S(=O)2RTT
であり、
各-LT-は、独立して、直鎖又は分岐鎖の飽和C1-4アルキレンであり;
各-RTTは、独立して、-RTT1、-RTT2、-LTT-RTT2、-RTT3、又は-LTT-RTT3であり;
各-RTT1は、独立して、直鎖又は分岐鎖の飽和C1-6アルキルであり、場合により、-F、-OH、及び-ORTTTから選択される1個以上の基で置換されており;
各-RTT2は、飽和C3-6シクロアルキルであり、場合により、-F、-RTTT、-OH、及び-ORTTTから選択される1個以上の基で置換されており;
各-RTT3は、独立して、フェニル又はナフチルであり、場合により、-F、-Cl、-Br、-I、-RTTT、OH、-ORTTT、-OCF3、-NH2、-NHRTTT、及び-NRTTT 2から選択される1個以上の基で置換されており;
各-LTT-は、独立して、直鎖又は分岐鎖の飽和C1-4アルキレンであり;
各-RTNは、直鎖又は分岐鎖の飽和C1-4アルキル、フェニル又はベンジルであり;
各-RTMは、独立して、アゼチジノ、ピロリジノ、ピペリジノ、ピペラジノ、モルホリノ、アゼパノ、又はジアゼパノであり;
場合により、炭素上で、-RTMM、-C(=O)RTMM、-S(=O)2RTMM、-F、-NH2、-NHRTMM、-NRTMM 2、-OH、及び-ORTMMから選択される1個以上の基により置換されており;
場合により、存在する場合は第二級窒素上で、-RTMM、-C(=O)RTMM、-C(=O)ORTMM、及び-S(=O)2RTMMから選択される基により置換されており;
各-RTTTは、独立して、直鎖又は分岐鎖の飽和C1-4アルキル、フェニル又はベンジルであり;
各-RTMMは、独立して、直鎖又は分岐鎖の飽和C1-4アルキル、フェニル又はベンジルであり;
またここで
-L7-は、独立して、直鎖又は分岐鎖の飽和C1-3アルキレンであり、場合により、-F、-OH、及び-OMeから選択される1個以上の基で置換されており;
-R3は、独立して、-R3A又は-R3Bであり;
-R3Aは、独立して、直鎖又は分岐鎖の飽和C1-6アルキルであり、場合により、-F、-OH、及び-OMeから選択される1個以上の基で置換されており;
-R3Bは、独立して、飽和C3-7シクロアルキルであり、場合により、-F、-OH、及び-OMeから選択される1個以上の基で置換されている)。
「C9-10ヘテロアリール」、「C3-7ヘテロシクリル」などの用語における添字「Cx-y」は、炭素原子又はヘテロ原子(例えば、場合によりN、O、S)であり得る環原子の数を指す。例えば、ピリジルは、C6ヘテロアリール基の一例であり、ピペリジノは、C6ヘテロシクリル基の一例である。
(2) -R7が、正確に1、2又は3個の環ヘテロ原子を有する縮合二環式C9-10ヘテロアリール基であり、各環ヘテロ原子がNである、(1)に記載の化合物。
(3) -R7が、正確に1、2又は3個の環ヘテロ原子を有する縮合二環式C9ヘテロアリール基であり、各環ヘテロ原子がNである、(1)に記載の化合物。
(33) -R7が、正確に1、2又は3個の環ヘテロ原子を有する縮合二環式C8ヘテロアリール基であり、各環ヘテロ原子がN、S又はOである、(1)に記載の化合物。
(48) -R7が、正確に1、2又は3個の環ヘテロ原子を有する縮合二環式C10ヘテロアリール基であり、各環ヘテロ原子がNである、(1)に記載の化合物。
(58) -R7が、-R7の環炭素原子(例えば、-R7の非架橋環炭素原子)を介して-L7-に結合している、(1)~(57)のいずれか1つに記載の化合物。
(60) 各-RSCが、存在する場合、独立して:
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)OH、-C(=O)ORTT、
-OC(=O)RTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、
-NHC(=O)RTT、
-NHC(=O)NH2、-NHC(=O)NHRTT、-NHC(=O)NRTT 2、-NHC(=O)RTM、
-NHC(=O)ORTT、
-OC(=O)NH2、-OC(=O)NHRTT、-OC(=O)NRTT 2、-OC(=O)RTM、
-C(=O)RTT、
-S(=O)2RTT、
-S(=O)2NH2、-S(=O)2NHRTT、-S(=O)2NRTT 2、-S(=O)2RTM、
-NHS(=O)2RTT、
-CN、又は-NO2
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)OH、-C(=O)ORTT、
-OC(=O)RTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、
-NHC(=O)RTT、
-C(=O)RTT、
-S(=O)2NH2、-S(=O)2NHRTT、-S(=O)2NRTT 2、-S(=O)2RTM、
-NHS(=O)2RTT、
-CN、又は-NO2
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)OH、-C(=O)ORTT、
-OC(=O)RTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、
-NHC(=O)RTT、
-C(=O)RTT、
-S(=O)2NH2、-S(=O)2NHRTT、-S(=O)2NRTT 2、-S(=O)2RTM、
-NHS(=O)2RTT、
-CN、又は-NO2
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、又は-LT-RTM
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、又は-OCHF2
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-CF3、-CHF2、-OCF3、又は-OCHF2
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT、
-F、-Cl、-Br、又は-I
である、(1)~(59)のいずれか1つに記載の化合物。
-RTT
である、(1)~(59)のいずれか1つに記載の化合物。
(68) 各-RSNが、存在する場合、独立して:
-RTT、
-C(=O)RTT、
-C(=O)ORTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、又は
-S(=O)2RTT
である、(1)~(67)のいずれか1つに記載の化合物。
-RTT、
-C(=O)RTT、又は
-C(=O)ORTT
である、(1)~(67)のいずれか1つに記載の化合物。
-RTT
である、(1)~(67)のいずれか1つに記載の化合物。
(75) 各-RTTが、存在する場合、独立して、-RTT1、-RTT2、-RTT3、又は-LTT-RTT3である、(1)~(74)のいずれか1つに記載の化合物。
(78) 各-RTT1が、存在する場合、独立して、直鎖又は分岐鎖の飽和C1-6アルキルである、(1)~(77)のいずれか1つに記載の化合物。
(84) 各-RTT2が、存在する場合、飽和C3-6シクロアルキルであり、場合により、-F、-OH、及び-ORTTTから選択される1個以上の基で置換されている、(1)~(83)のいずれか1つに記載の化合物。
(88) 各-RTT3が、存在する場合、フェニルであり、場合により、-F、-Cl、-Br、-I、-RTTT、OH、-ORTTT、-OCF3、-NH2、-NHRTTT、及び-NRTTT 2から選択される1個以上の基で置換されている、(1)~(87)のいずれか1つに記載の化合物。
(92) 各-LTT-が、存在する場合、独立して、直鎖又は分岐鎖の飽和C1-3アルキレンである、(1)~(91)のいずれか1つに記載の化合物。
(96) 各-RTNが、存在する場合、独立して、直鎖又は分岐鎖の飽和C1-4アルキルである、(1)~(95)のいずれか1つに記載の化合物。
(98) 各-RTMが、存在する場合、独立して、アゼチジノ、ピロリジノ、ピペリジノ、ピペラジノ、モルホリノ、アゼパノ、又はジアゼパノであり:
場合により、炭素上で、-RTMM、-F、-OH、及び-ORTMMから選択される1個以上の基により置換されており;
場合により、存在する場合は第二級窒素上で、-RTMM、-C(=O)RTMM、及び-C(=O)ORTMMから選択される基により置換されている、
(1)~(97)のいずれか1つに記載の化合物。
場合により、炭素上で、-RTMM、-F、-OH、及び-ORTMMから選択される1個以上の基により置換されており;
場合により、存在する場合は第二級窒素上で、-RTMM、-C(=O)RTMM、及び-C(=O)ORTMMから選択される基により置換されている、(1)~(97)のいずれか1つに記載の化合物。
場合により、炭素上で、-RTMMから選択される1個以上の基により置換されており;
場合により、存在する場合は第二級窒素上で、-RTMM、-C(=O)RTMM、及び-C(=O)ORTMMから選択される基により置換されている、
(1)~(97)のいずれか1つに記載の化合物。
場合により、炭素上で、-RTMMから選択される1個以上の基により置換されており、
場合により、存在する場合は第二級窒素上で、-RTMMから選択される基により置換されている、
(1)~(97)のいずれか1つに記載の化合物。
(102) 各-RTTTが、存在する場合、独立して、直鎖又は分岐鎖の飽和C1-4アルキルである、(1)~(101)のいずれか1つに記載の化合物。
(104) 各-RTMMが、存在する場合、独立して、直鎖又は分岐鎖の飽和C1-4アルキルである、(1)~(103)のいずれか1つに記載の化合物。
(106) -L7-が、独立して、直鎖又は分岐鎖の飽和C1-3アルキレンである、(1)~(105)のいずれか1つに記載の化合物。
(113) -R3が-R3Aである、(1)~(112)のいずれか1つに記載の化合物。
(115) -R3Aが、存在する場合、独立して、直鎖又は分岐鎖の飽和C1-6アルキルである、(1)~(114)のいずれか1つに記載の化合物。
(122) -R3Bが、存在する場合、飽和C3-7シクロアルキルである、(1)~(121)のいずれか1つに記載の化合物。
(127)
-R7が、独立して:
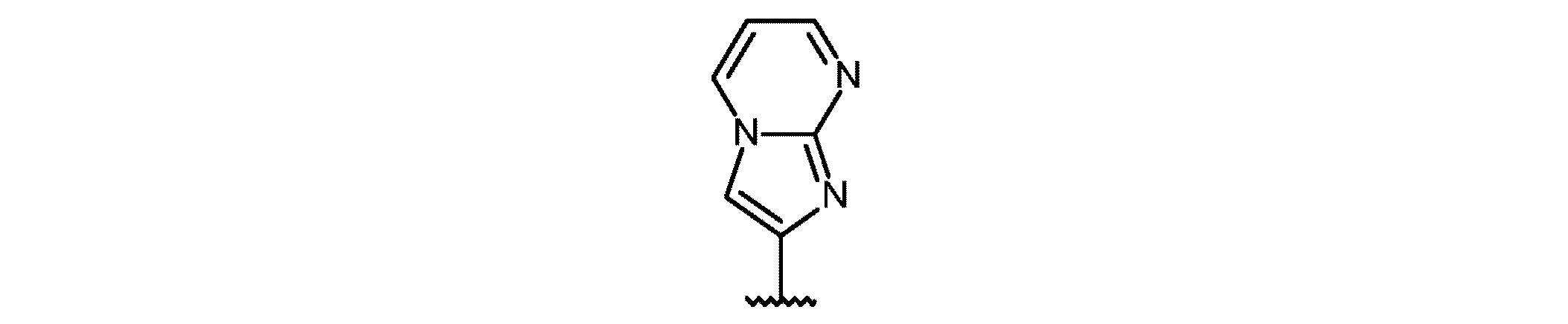
イミダゾ[1,2-a]ピリジニル;
イミダゾ[1,2-a]ピリミジニル;
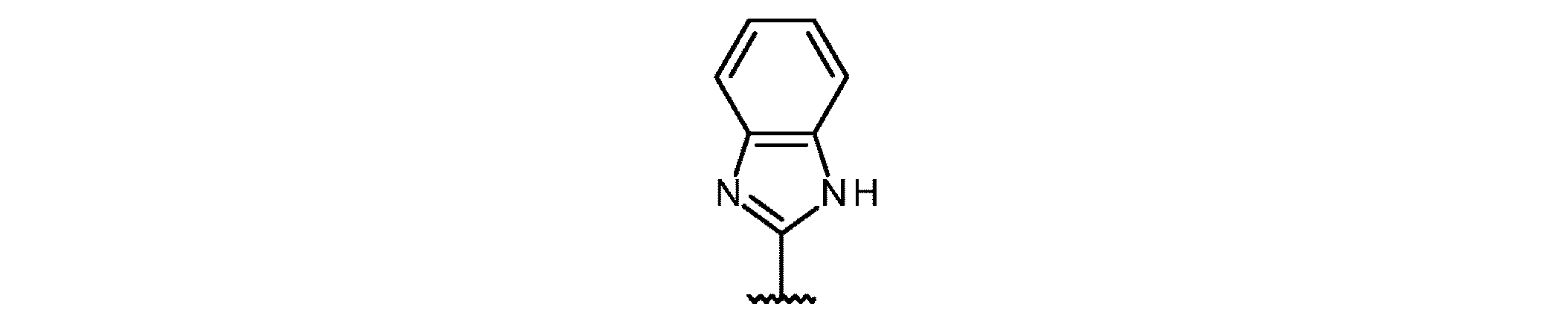
ベンズイミダゾリル;
イミダゾ[2,1-b]チアゾリル;
イミダゾ[1,2-b]ピリダジニル;
[1,2,4]トリアゾロ[1,5-a]ピリジニル;
キノリニル;又は
ベンゾフラニル
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が、-CH2-又は-CH(CH3)-であり;
-R3が、-R3A又は-R3Bであり;
-R3Aが-iPrであり;
-R3Bがシクロプロピルである、
(1)に記載の化合物。
-R7が、独立して:
2-イミダゾ[1,2-a]ピリジニル;
3-イミダゾ[1,2-a]ピリジニル;
2-イミダゾ[1,2-a]ピリミジニル;
2-ベンズイミダゾリル;
5-ベンズイミダゾリル;
6-イミダゾ[2,1-b]チアゾリル;
2-イミダゾ[1,2-b]ピリダジニル;
2-[1,2,4]トリアゾロ[1,5-a]ピリジニル;
2-キノリニル;
3-キノリニル;又は
2-ベンゾフラニル
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が、-CH2-又は-CH(CH3)-であり;
-R3が、-R3A又は-R3Bであり;
-R3Aが-iPrであり;
-R3Bがシクロプロピルである、
(1)に記載の化合物。
-R7が、独立して:
イミダゾ[1,2-a]ピリジニル;又は
イミダゾ[1,2-a]ピリミジニル;
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が、-CH2-又は-CH(CH3)-であり;
-R3が、-R3A又は-R3Bであり;
-R3Aが-iPrであり;
-R3Bがシクロプロピルである、
(1)に記載の化合物。
-R7が、独立して:
2-イミダゾ[1,2-a]ピリジニル;
2-イミダゾ[1,2-a]ピリミジニル
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が、-CH2-又は-CH(CH3)-であり;
-R3が、-R3A又は-R3Bであり;
-R3Aが-iPrであり;
-R3Bがシクロプロピルである、
(1)に記載の化合物。
-R7が、独立して:
イミダゾ[1,2-a]ピリジニル;
イミダゾ[1,2-a]ピリミジニル;
ベンズイミダゾリル;又は
イミダゾ[2,1-b]チアゾリル
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が-CH2-であり;
-R3が-R3Aであり;
-R3Aが-iPrである、
(1)に記載の化合物。
-R7が、独立して:
イミダゾ[1,2-a]ピリジニル;
イミダゾ[1,2-a]ピリミジニル;又は
ベンズイミダゾリル;
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が-CH2-であり;
-R3が-R3Aであり;
-R3Aが-iPrである、
(1)に記載の化合物。
-R7が、独立して:
3-イミダゾ[1,2-a]ピリジニル;
2-イミダゾ[1,2-a]ピリジニル;
2-イミダゾ[1,2-a]ピリミジニル;
2-ベンズイミダゾリル;
5-ベンズイミダゾリル;又は
イミダゾ[2,1-b]チアゾール-6-イル;
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が-CH2-であり;
-R3が-R3Aであり;
-R3Aが-iPrである、
(1)に記載の化合物。
-R7が、独立して:
3-イミダゾ[1,2-a]ピリジニル;
2-イミダゾ[1,2-a]ピリジニル;
2-イミダゾ[1,2-a]ピリミジニル;
2-ベンズイミダゾリル;又は
5-ベンズイミダゾリル;
であり、場合により本明細書中に記載されているとおりに置換されており;
-L7-が-CH2-であり;
-R3が-R3Aであり;
-R3Aが-iPrである、
(1)に記載の化合物。
(135) 以下の式の化合物、並びにその薬学的に許容される塩、水和物及び溶媒和物から選択される、(1)に記載の化合物。
明確性のために別個の実施形態の文脈で記載されている本発明の特定の特徴は、単一の実施形態として組み合わせて提供することも可能であることが理解される。逆に、簡潔さのために、単一の実施形態の文脈で記載されている本発明の様々な特徴は、別々に、又は任意の好適なサブコンビネーションで提供することもできる。可変要素(例えば、-R7、-L3-、-R3等)によって表される化学基に関する実施形態の全ての組み合わせは、本発明により具体的に包含され、それぞれの及び全ての組み合わせは、このような組み合わせが、安定化合物(すなわち、単離し、特性決定し、生物学的活性について試験することができる化合物)である化合物を包含する程度まで、個別に且つ明確に開示されていたかのように本明細書中で開示される。この文脈において、当業者であれば、基(例えば置換基)の特定の組み合わせが、容易に合成することができない、及び/又は化学的に不安定な化合物を生じさせ得ることを容易に理解する。さらに、このような可変要素について記載している実施形態において列挙されている化学基の全てのサブコンビネーションもまた、本発明により具体的に包含され、本明細書において、それぞれの及び全てのこのような化学基のサブコンビネーションが、本明細書中で正確にあたかも個別に且つ明確に開示されていたかのように開示されている。
本発明の一態様は、実質的に精製された形態及び/又は混入物が実質的に存在していない形態の、本明細書中に記載されるH-APPAMP化合物に関する。
特定の化合物は、1種以上の特定の幾何形態、光学形態、エナンチオマー形態、ジアステレオ異性体形態、エピマー形態、アトロピック(atropic)形態、立体異性体形態、互変異性体形態、立体配座形態又はアノマー形態、例えば、限定するものではないが、cis-及びtrans-形;E-及びZ-形;c-、t-、及びr-形;endo-及びexo-形;R-、S-、及びmeso-形;D-及びL-形;d-及びl-形;(+及び(-)形;ケト-、エノール-及びエノラート-形;syn-及びanti-形;シンクリナル-及びアンチクリナル-形;α-及びβ-形;アキシアル及びエカトリアル形;舟-、いす-、ねじれ-、エンベロープ-及び半いす-形;ならびにそれらの組合せなどで存在し得、本明細書中以降、総称的に「異性体」(又は「異性体形態」)と呼ぶ。
対応する化合物の塩、例えば薬学的に許容される塩を調製し、精製し、及び/又は取り扱うことが、好都合であるか又は望ましい場合がある。薬学的に許容される塩の例は、Berge et aL、1977, “Pharmaceutically Acceptable Salts,” J. Pharm. Sci., Vol. 66, pp. 1-19において考察されている。
化合物の対応する溶媒和物を調製し、精製し、及び/又は取り扱うことが好都合であるか又は望ましい場合があり得る。本明細書中で「溶媒和物」という用語は、溶質(例えば、化合物、化合物の塩)と溶媒の複合体を指す従来の意味で使用される。溶媒が水である場合、溶媒和物を好都合に水和物と呼ぶことが可能であり、例えば一水和物、二水和物、三水和物等と呼ぶことができる。
化合物を化学的保護形態で調製し、精製し、及び/又は取り扱うことが好都合であるか又は望ましくあり得る。本明細書中で「化学的保護形態」という用語は従来の化学的な意味で使用され、1個以上の反応性官能基が、特定の条件(例えば、pH、温度、放射線、溶媒など)下での望ましくない化学反応から保護されている化合物に関する。実際に、周知の化学的方法を利用して、保護されない場合は特定の条件下で反応性である官能基を可逆的に非反応性にする。化学的保護形態においては、1個以上の反応性官能基は、被保護基又は保護基(あるいは、被マスク基若しくはマスキング基、又は被ブロック基若しくはブロッキング基)の形態である。反応性官能基を保護することにより、被保護基に影響を及ぼすことなく、他の無保護の反応性官能基が関わる反応を行うことが可能であり;通常は後続のステップで、分子の残りの部分に実質的に影響を及ぼすことなく、上記の保護基を除去するか、又はマスキング基を変換することができる。例えば、Protective Groups in Organic Synthesis (T. Green 及び P. Wuts;第4版;John Wiley 及び-Sons, 2006)を参照のこと。
化合物をプロドラッグの形態で調製し、精製し、及び/又は取り扱うことが好都合であるか又は望ましい場合がある。本明細書中で使用される用語「プロドラッグ」は、in vivoで所望の活性化合物を生成する化合物に関する。典型的には、プロドラッグは不活性であるか、又は所望の活性化合物よりも活性が低いが、有利な取り扱い特性、投与特性又は代謝特性を提供することができる。
本発明の一態様は、本明細書中に記載されるH-APPAMP化合物と、薬学的に許容できる担体、希釈剤又は賦形剤とを含む組成物(例えば、医薬組成物)に関する。
本明細書中に記載されるH-APPAMP化合物は、例えば、増殖性障害の治療(「抗増殖剤」として)、がんの治療(「抗がん剤」として)、ウイルス感染症の治療(「抗ウイルス剤」として)、神経変性疾患の治療(「抗神経変性剤」として)等において有用である。
本発明の一態様は、in vitro又はin vivoでCDK(例えばCDK12及び/又はCDK13)機能(例えば、細胞における機能)を阻害する方法であって、前記細胞と、有効量の本明細書中に記載されるH-APPAMP化合物とを接触させることを含む、上記方法に関する。
本明細書中に記載されるH-APPAMP化合物は、例えば(a) 細胞増殖を制御する(例えば、阻害する)か;(b) 細胞周期の進行を阻害するか;(c) アポトーシスを促進するか;又は(d) これらのうちの1種以上の組合せを行う。
本発明の別の態様は、療法による人体又は動物体の治療方法における使用のための、本明細書中に記載されるH-APPAMP化合物に関し、例えば、本明細書中に記載される障害(例えば、疾患)の治療方法を使用するための化合物に関する。
本発明の別の態様は、例えば、本明細書中に記載される障害(例えば、疾患)の治療方法において使用するための、例えば治療方法の使用のための医薬の製造における、本明細書中に記載されるH-APPAMP化合物の使用に関する。
本発明の別の態様は、治療方法、例えば本明細書中に記載される障害(例えば、疾患)の治療方法であって、治療を必要とする対象に、治療有効量の本明細書中に記載されるH-APPAMP化合物を、好ましくは医薬組成物の形態で投与することを含む、上記方法に関する。
一実施形態(例えば、療法における使用のための実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、CDK、とりわけCDK12及び/又はCDK13に関連する障害(例えば、疾患);CDK、とりわけCDK12及び/又はCDK13の不適切な活性により生じる障害(例えば、疾患);CDK変異、とりわけCDK12及び/又はCDK13変異に関連する障害(例えば、疾患):CDK過剰発現、とりわけCDK12及び/又はCDK13過剰発現に関連する障害(例えば、疾患);CDK、とりわけCDK12及び/又はCDK13の上流経路活性化に関連する障害(例えば、疾患);CDK、とりわけCDK12及び/又はCDK13の阻害(例えば、選択的阻害)により寛解する障害(例えば疾患)の治療である。
一実施形態(例えば、療法における使用のための実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、増殖性障害;がん;ウイルス感染症(例えば、HIV);神経変性障害(例えば、アルツハイマー病、パーキンソン病);虚血;腎疾患;心血管障害(例えば、アテローム性動脈硬化症);又は自己免疫障害(例えば、関節リウマチ)の治療である。
一実施形態(例えば、療法における使用のための実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、増殖性障害の治療である。
一実施形態(例えば、療法における使用の実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、がんの治療である。
(1) がん腫、例えば、重層扁平上皮(扁平上皮がん)から生じる腫瘍、及び臓器又は腺(腺がん)内に生じる腫瘍など。
例としては、乳房、結腸、肺、前立腺、卵巣が挙げられる。
軟骨肉腫(軟骨);平滑筋肉腫(平滑筋);横紋筋肉腫(骨格筋);中皮肉腫及び中皮腫(体腔の膜裏層);線維肉腫(線維組織);血管肉腫及び血管内皮腫(血管);脂肪肉腫(脂肪組織);グリオーマ及び星状細胞腫(脳で見出された神経原性結合組織);粘液肉腫(原始胚結合組織);間葉腫及び混合性中胚葉性腫瘍(混合性結合組織型)。
一実施形態(例えば、療法における使用の実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、例えばBRCA1、BRCA2、ATM、ATR、BAP1、CDK12、CDK13、CHK1、CHK2、FANCA、FANCC、FANCD2、FANCE、FANCF、FANCI、PALB2、NBS1、WRN、RAD51B、RAD51C、RAD51D、MRE11A、BLM、BRIP1などの、DNA修復に関わるタンパク質の遺伝子における低発現、欠損及び/又は変異を有する患者における障害(例えば、疾患)の治療である。この患者としては、例えば、腫瘍が「BRCAness」を呈するがん患者などが挙げられる(例えば、Lord et al., 2019を参照)。
一実施形態(例えば、療法における使用のための実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療はウイルス感染症の治療である。
(グループI:) dsDNAウイルス、例えばアデノウイルス、ヘルペスウイルス、ポックスウイルス;
(グループII:) ssDNAウイルス、例えばパルボウイルス;
(グループIII:) dsRNAウイルス、例えばレオウイルス;
(グループIV:) (+)ssRNAウイルス、例えばピコルナウイルス、トガウイルス;
(グループV:) (-)ssRNAウイルス、例えばオルソミクソウイルス、ラブドウイルス;
(グループVI:) ssRNA-RTウイルス、例えばレトロウイルス;又は
(グループVII:) dsDNA-RTウイルス、例えばヘパドナウイルス
によるウイルス感染症の治療である。
一実施形態(例えば、療法における使用のための実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、自己免疫障害の治療である。
一実施形態(例えば、療法における使用のための実施形態、医薬の製造における使用の実施形態、治療方法の実施形態)において、治療は、細胞内の翻訳機能不全により引き起こされる障害の治療である。
本明細書において障害の治療の文脈において使用される場合、「治療」という用語は、一般的に、いくつかの所望の治療効果、例えば障害の進行の阻害が達成されるヒト又は動物(例えば、獣医学的適用における)の治療に関し、例えば、進行の速度の低下、進行の速度の停止、障害の症状の緩和、障害の寛解、及び障害の治癒が挙げられる。予防的手段(すなわち、予防)としての治療も含まれる。例えば、未だ障害を発症していないが、障害を発症するリスクを有する患者での使用が、「治療」という用語に包含される。
「治療」という用語は、2つ以上の治療又は療法を、例えば逐次的に又は同時に組み合わせた併用治療及び併用療法を含む。例えば、本明細書に記載される化合物は、例えば他の薬剤と組み合わせて、併用療法で使用することもできる。治療及び療法の例としては、化学療法(例えば薬物、抗体(例えば、免疫療法として)、プロドラッグ(例えば、光線力学的療法、GDEPT、ADEPT等として)などの活性薬剤の投与);外科手術;放射線療法;光線力学的療法;遺伝子療法;及び食事制限が挙げられる。
アロマターゼ阻害剤、例えばエキセメスタン(アロマシンとしても知られる)、レトロゾール(フェマーラとしても知られる)、アナストロゾール(アリミデックスとしても知られる)等;
抗エストロゲン剤、例えばフェソロデックス(フルベストラント及びICI182780としても知られる)、タモキシフェン(ノルバデックスとしても知られる)、ヒドロキシタモキシフェン等;
抗アンドロゲン剤、例えば、前立腺がんの治療において使用される抗アンドロゲン剤、例えば、フルタミド、エンザルタミド、アパルタミド、ビカルタミド、ニルタミド等;
Her2遮断薬、例えばハーセプチン、ペルツズマブ、ラパチニブ等;
細胞傷害性化学療法剤、例えば、タキサン(例えば、タキソールとしても知られるパクリタキセル;タキソテールとしても知られるドセタキセル)、シクロホスファミド、代謝拮抗薬(例えば、カルボプラチン、カペシタビン、ゲムシタビン、ドキソルビシン、エピルビシン、5-フルオロウラシル等)。
免疫系を刺激する薬剤、例えば、Toll様受容体(TLR1-13)アゴニスト、インターフェロン遺伝子の刺激剤(STING)アゴニスト等;
チェックポイント阻害剤、例えば、PD1、PD1L、CTLA4の阻害剤等、例えば、ペムブロリズマブ、アテゾリズマブ、イピリムマブ等;
DNA修復阻害剤、例えば、PARP阻害剤、例えば、オラパリブ、ニラパリブ等。
本明細書中に記載されるH-APPAMP化合物は、CDK(例えばCDK12及び/又はCDK13)を阻害するための細胞培養液添加剤として使用することもできる。
本発明の一態様は、(a) 本明細書中に記載されるH-APPAMP化合物、又は本明細書中に記載されるH-APPAMP化合物を含む組成物、例えば、好ましくは好適な容器中で及び/又は好適なパッケージを用いて提供されるもの;並びに(b) 使用についての説明書、例えば上記の化合物又は組成物の投与方法についての書面による説明書を含むキットに関する。
H-APPAMP化合物又はそのH-APPAMP化合物を含む医薬組成物は、全身投与/末梢投与又は局所投与のいずれであっても(すなわち、所望の作用部位において)、任意の好都合な投与経路で対象に投与することができる。
対象/患者は、脊索動物、脊椎動物、哺乳動物、有胎盤哺乳動物、有袋類(例えば、カンガルー、ウォンバット)、齧歯類(例えば、モルモット、ハムスター、ラット、マウス)、ネズミ科動物(例えば、マウス)、ウサギ目動物(例えば、ウサギ)、鳥類(例えば、トリ)、イヌ科動物(例えば、イヌ)、ネコ科動物(例えば、ネコ)、ウマ科動物(例えば、ウマ)、イノシシ科動物(porcine)(例えば、ブタ(pig))、ヒツジ科動物(ovine)(例えば、ヒツジ(sheep))、ウシ科動物(例えば、ウシ)、霊長類、サル(simian)(例えば、サル(monkey)又は類人猿(ape))、サル(monkey)(例えば、マーモセット、ヒヒ)、類人猿(ape)(例えば、ゴリラ、チンパンジー、オランウータン、テナガザル)、又はヒトであり得る。
H-APPAMP化合物は単独で投与することも可能であるが、少なくとも1種の本明細書中に記載されるH-APPAMP化合物を、当業者に周知の1種以上の他の薬学的に許容される成分、例えば薬学的に許容される担体、希釈剤、賦形剤、アジュバント、充填剤、緩衝剤、防腐剤、抗酸化剤、滑沢剤、安定剤、可溶化剤、界面活性剤(例えば、湿潤剤)、マスキング剤、着色剤、香味剤及び甘味剤などと共に含む医薬製剤(例えば、組成物、調剤薬、医薬)として提供することが好ましい。製剤は、他の活性薬剤、例えば、他の治療剤又は予防剤をさらに含み得る。
H-APPAMP化合物、及びH-APPAMP化合物を含む組成物の適切な用量が患者間で異なり得ることは当業者に理解されよう。最適用量の決定は、一般的に、任意のリスク又は有害な副作用に対する治療上の利益のレベルのバランスをとることを含む。選択される用量レベルは、様々な要因、例えば、特定のH-APPAMP化合物の活性、投与経路、投与の時間、H-APPAMP化合物の排出速度、治療期間、組み合わせて使用される他の薬物、化合物及び/又は物質、障害の重症度、ならびに患者の種、性別、年齢、体重、状態、一般的健康状態及び既往歴などによって決まる。H-APPAMP化合物の量及び投与経路は、最終的には医師、獣医師又は臨床医の裁量量に委ねられるものであるが、一般的には、用量は、作用部位で、実質的に有害な又は悪影響のある副作用を引き起こすことなく所望の効果を達成する局所濃度が得られるように選択される。
略語
aq:水性;
Boc:tert-ブトキシカルボニル;
Boc2O:ジ-tert-ブチルジカーボネート;
br:ブロード;
ca.:約;
d:ダブレット;
tBuXPhos-Pd-G3:[(2-ジ-tert-ブチルホスフィノ-2',4',6'-トリイソプロピル-1,1'-ビフェニル)-2-(2'-アミノ-1,1'-ビフェニル)]パラジウム(II)メタンスルホネート;
DCM:ジクロロメタン;
DCE:1,2-ジクロロエタン;
ジオキサン:1,4-ジオキサン;
DIPEA:ジイソプロピルエチルアミン;
DMAP:4-(ジメチルアミノ)ピリジン;
EtOAc:酢酸エチル;
EtOH:エタノール;
h:時間;
HPLC:高速液体クロマトグラフィー;
IPA:イソプロパノール;
LCMS:液体クロマトグラフィー - 質量分析;
LiHMDS:リチウムヘキサメチルジシラジド;
m:マルチプレット;
M:モル、分子イオン;
mCPBA:3-クロロ過安息香酸;
MeCN:アセトニトリル;
MeOH:メタノール;
min:分;
MS:質量分析;
NCS:N-クロロスクシンイミド;
NIS:N-ヨードスクシンイミド;
NMR:核磁気共鳴;
PdCl2(dppf) DCM:[1,1'-ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)、ジクロロメタンとの錯体;
q:カルテット;
RT:室温(約20℃);
RT:保持時間;
s:シングレット、固体;
SCX:強カチオン交換;
t:トリプレット;
TBME:tert-ブチルメチルエーテル;
TFA:トリフルオロ酢酸;
THF:テトラヒドロフラン;
UPLC/MS:超高速液体クロマトグラフィー 質量分析。
H-APPAMP化合物の化学合成のための方法は、本明細書中に記載されている。これらの及び/又は他の周知の方法は、代替的な又は改善されたH-APPAMP化合物の合成方法を提供するために公知の方法で改変及び/又は適合され得る。
スキーム1
スキーム2
スキーム3
スキーム4
以下の実施例は単に本発明を説明するために提供されるものであり、本明細書に記載される本発明の範囲を限定することを意図するものではない。
全ての出発物質及び溶媒は、商業的供給源から得たか、又は文献の引用に従って調製した。別段の指示がない限り、反応混合物を磁気撹拌した。
方法1 - LCMS酸性4分法:
カラム:Waters X-Select CSH C18, 2.5μm、4.6x30mm
検出: 別段の指示がない限り、254nmのUV
MSイオン化:エレクトロスプレー
溶媒A:水/0.1%ギ酸
溶媒B:MeCN/0.1%ギ酸
カラム:Waters X-Bridge BEH C18, 2.5μm、4.6x30mm
溶媒A:水/10mM重炭酸アンモニウム
溶媒B:MeCN
(他のパラメータは方法1と同じ)
カラム:Waters Acquity CSH C18(2.1x30mm)
検出:Waters Acquity PDA検出器 210~400nm
MSイオン化:エレクトロスプレー
溶媒A:水/0.1%ギ酸
溶媒B:MeCN/0.1%ギ酸
カラム:Waters Acquity BEH C18カラム(2.1x30mm)
検出:Waters Acquity PDA検出器 210~400nm
MSイオン化:エレクトロスプレー
溶媒A:水/10mM重炭酸アンモニウム
溶媒B:MeCN
(他のパラメータは方法3と同じ)
カラム:Waters Acquity BEH C18カラム(2.1x30mm)
検出:Waters Acquity PDA検出器 210~400nm
MSイオン化:エレクトロスプレー
溶媒A:水/10mM 水酸化アンモニウム
溶媒B:MeCN
(他のパラメータは方法3と同じ)
カラム:Waters Acquity BEH C18カラム(2.1x30mm)
検出:Waters Acquity PDA検出器 210~400nm
MSイオン化:エレクトロスプレー
溶媒A:水/10mM重炭酸アンモニウム
溶媒B:MeCN
(3R,4R)-4-(((7-((イミダゾ[1,2-a]ピリジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-003)
5-クロロ-N-(イミダゾ[1,2-a]ピリジン-2-イルメチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン
イミダゾ[1,2-a]ピリジン-2-イルメタンアミン、2HCl(0.175g、0.80mmol)を、EtOH(10mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(0.122g、0.53mmol)及びDIPEA(0.74mL、4.24mmol)の溶液に添加した。反応混合物を90℃で6時間加熱した。反応混合物を真空中で濃縮し、残渣をEtOAc(50mL)と水(50mL)に分配した。水性層をEtOAc(3x50mL)で抽出し、合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮し、表題化合物(0.160g、0.42mmol、収率80%、純度90%)を白色の固体として得た。
UPLC/MS (方法4):m/z 341 (M+H)+, RT 1.38分。
tert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(イミダゾ[1,2-a]ピリジン-2-イルメチル)カルバメート
BOC無水物(0.14mL、0.61mmol)を、THF(10mL)中の5-クロロ-N-(イミダゾ[1,2-a]ピリジン-2-イルメチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(0.160g、0.47mmol)及びDMAP(0.011g、0.09mmol)の溶液に添加した。反応混合物を室温で16時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)と水(30mL)に分配した。水性層をDCM(2x10mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(80gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(0.170g、0.37mmol、収率78%、純度95%)をクリーム色の固体として得た。
UPLC/MS (方法4):m/z 441 (M+H)+, RT 1.73分。
tert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(イミダゾ[1,2-a]ピリジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート
THF(3mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(イミダゾ[1,2-a]ピリジン-2-イルメチル)カルバメート(0.150g、0.34mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(0.094g、0.41mmol)及びtBuBrettPhos Pd G3 (0.029g、0.03mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.51mL、0.51mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1時間加熱した。反応を水(5mL)でクエンチし、EtOAc(3x10mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(0.075g、0.12mmol、収率34%、純度98%)を白色の固体として得た。
UPLC/MS (方法4):m/z 635 (M+H)+, RT 1.65分。
(3R,4R)-4-(((7-((イミダゾ[1,2-a]ピリジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
塩化水素(ジオキサン中4M)(0.44mL、1.77mmol)を、DCM(10mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(イミダゾ[1,2-a]ピリジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(0.075g、0.12mmol)の溶液に添加した。反応混合物を室温で16時間撹拌し、真空中で濃縮した。残渣をMeOH(5mL)中に希釈し、SCXカートリッジ上にロードし、MeOH(約5mL)で洗浄し、MeOH中0.7Mアンモニア(約5mL)で溶出した。このアンモニア性メタノール溶液を減圧下で濃縮した。カラムクロマトグラフィーにより精製し(4gカートリッジ、0~10%MeOH(0.7M NH3含有)/DCM)、表題化合物(0.030g、0.07mmol、収率57%、純度95%)を透明なガラス状固体として得た。
UPLC/MS (方法4):m/z 435 (M+H)+, RT 0.96分。
1H NMR (500 MHz, DMSO-d6) δ 8.50 - 8.46 (m, 1H), 7.78 (s, 1H), 7.65 (t, J = 6.3 Hz, 1H), 7.63 (s, 1H), 7.50 (d, J = 9.1 Hz, 1H), 7.24 - 7.16 (m, 1H), 6.85 (td, J = 6.8, 1.2 Hz, 1H), 6.76 - 6.70 (m, 1H), 5.35 - 5.30 (m, 1H), 5.28 (s, 1H), 4.56 (d, J = 5.9 Hz, 2H), 4.12 - 4.05 (m, 1H), 3.60 - 3.48 (m, 1H), 3.17 (d, J = 4.2 Hz, 1H), 3.06 - 2.99 (m, 1H), 2.98 - 2.92 (m, 1H), 2.92 (dd, J = 11.6, 4.8 Hz, 1H), 2.81 - 2.74 (m, 1H), 2.30 (td, J = 12.2, 2.7 Hz, 1H), 2.16 (dd, J = 11.6, 9.9 Hz, 1H), 1.58 - 1.51 (m, 1H), 1.38 - 1.28 (m, 1H), 1.23 (t, J = 6.5 Hz, 6H), 1.19 - 1.10 (m, 1H)。
(3R,4R)-4-(((7-((イミダゾ[1,2-a]ピリミジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-002)
5-クロロ-N-(イミダゾ[1,2-a]ピリミジン-2-イルメチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン
イミダゾ[1,2-a]ピリミジン-2-イルメタンアミン、2HCl(5.04g、22.82mmol)を、EtOH(80mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(3.50g、15.21mmol)及びDIPEA(21.3mL、122.0mmol)の溶液に添加した。反応混合物を90℃で5時間加熱した。反応混合物を真空中で濃縮し、残渣をEtOAc(50mL)と水(50mL)に分配した。水性層をEtOAc(3x50mL)で抽出し、合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮し、表題化合物(5.10g、14.62mmol、収率96%、純度98%)を白色の固体として得た。
UPLC/MS (方法3):m/z 342 (M+H)+, RT 1.06分。
tert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(イミダゾ[1,2-a]ピリミジン-2-イルメチル)カルバメート
BOC無水物(3.2mL、13.69mmol)を、THF(10mL)中の5-クロロ-N-(イミダゾ[1,2-a]ピリミジン-2-イルメチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(3.60g、10.53mmol)及びDMAP(0.26g、2.11mmol)の溶液に添加した。反応混合物を室温で16時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)と水(30mL)に分配した。水性層をDCM(2x30mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(80gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(4g、8.60mmol、収率82%、純度95%)をクリーム色の固体として得た。
UPLC/MS (方法3):m/z 442 (M+H)+, RT 1.44分。
tert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(イミダゾ[1,2-a]ピリミジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート
THF(30mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(イミダゾ[1,2-a]ピリミジン-2-イルメチル)カルバメート(3.19、7.22mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(1.75g、7.58mmol)及びtBuBrettPhos Pd G3 (0.62g、0.72mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(10.8mL、10.8mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1時間加熱した。反応を水(50mL)でクエンチし、EtOAc(3x30mL)で抽出し、合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(80gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(2.10g、3.24mmol、収率44%、純度98%)をオレンジ色の固体として得た。
UPLC/MS (方法4):m/z 636 (M+H)+, RT 1.50分。
(3R,4R)-4-(((7-((イミダゾ[1,2-a]ピリミジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
塩化水素(ジオキサン中4M)(12.4mL、49.5mmol)を、DCM(10mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(イミダゾ[1,2-a]ピリミジン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(2.10g、3.30mmol)の懸濁液に添加した。反応混合物を室温で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7Mアンモニア(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、黄色の固体を得た。カラムクロマトグラフィー(24gカートリッジ、0~20%MeOH(0.7M NH3含有)/DCM)でさらに精製し、黄色の固体を得た。固体をDCM(20mL)及びMeOH(約1mL)中に溶解した。ジエチルエーテル(100mL)を添加した。褐色の固体が形成し、これを濾過により回収し、表題化合物(0.700g、1.56mmol、収率47%、純度98%)を得た。
UPLC/MS (方法4):m/z 436 (M+H)+, RT 0.85分。
1H NMR (500 MHz, DMSO-d6) δ 8.89 (dd, J = 6.8, 2.1 Hz, 1H), 8.49 (dd, J = 4.1, 2.0 Hz, 1H), 7.78 - 7.72 (m, 2H), 7.64 (s, 1H), 7.02 (dd, J = 6.7, 4.1 Hz, 1H), 6.76 (d, J = 5.0 Hz, 1H), 5.47 (s, 1H), 5.27 (s, 1H), 4.60 (d, J = 6.0 Hz, 2H), 3.58 - 3.48 (m, 1H), 3.45 - 3.25 (m, 2H), 3.25 - 3.19 (m, 1H), 3.14 - 3.07 (m, 1H), 3.00 - 2.95 (m, 1H), 2.85 (d, J = 12.2 Hz, 1H), 2.39 (td, J = 12.3, 2.9 Hz, 1H), 2.25 (d, J = 11.0 Hz, 1H), 1.63 - 1.57 (m, 1H), 1.37 (d, J = 11.7 Hz, 1H), 1.24 (t, J = 6.5 Hz, 6H), 1.21 - 1.17 (m, 1H)。
(3R,4R)-4-(((3-イソプロピル-7-(((1-メチル-1H-ベンゾ[d]イミダゾール-5-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-006)
5-クロロ-3-イソプロピル-7-(メチルチオ)ピラゾロ[1,5-a]ピリミジン
THF(100mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(8.00g、34.8mmol)の溶液を-5℃に冷却し、ナトリウムチオメトキシド(2.44g、34.8mmol)を添加した。反応混合物を室温に温め、一晩撹拌した。反応混合物をEtOAc(400mL)で希釈し、飽和NaHCO3水溶液(500mL)で洗浄した。水性層をEtOAc(260mL)で抽出し、合わせた有機層をブライン(160mL)で洗浄し、MgSO4で乾燥させ、真空中で濃縮した。カラムクロマトグラフィー(40gカートリッジ、0~20%EtOAc/イソヘキサン)により精製し、表題化合物(6.00g、24.6mmol、収率71%、純度99%)を淡黄色の油状物として得、これを静置して固化した。
LCMS (方法1):m/z 242 (M+H)+, RT 2.40分。
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルチオ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート
THF(10mL)中の5-クロロ-3-イソプロピル-7-(メチルチオ)ピラゾロ[1,5-a]ピリミジン(1.70g、7.03mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(1.62g、7.03mmol)及びtBuBrettPhos Pd G3 (300mg、0.35mmol)の溶液を、5分間脱気した。LiHMDS(THF中1M)(7.8mL、7.74mmol)を添加し、混合物をさらに5分間脱気した。反応混合物を60℃に加熱し、0.5時間撹拌した。溶媒を蒸発させ、残渣をEtOAcに再溶解し、1:1の水/ブライン(50mL)で洗浄し、水性層をEtOAc(3x50mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、濾過し、溶媒を蒸発させた。カラムクロマトグラフィー(80gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(2.30g、5.12mmol、収率66%、純度97%)を黄色の固体として得た。
LCMS (方法1):m/z 436 (M+H)+, RT 2.25分。
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルチオ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(1.70g、3.90mmol)を、DCM(30mL)中に溶解した。この溶液を0℃に冷却し、mCPBA(1.35g、5.85mmol)を一回で添加した。反応混合物を0℃で1時間撹拌した。反応混合物をDCM(30mL)の添加により後処理し、飽和NaHCO3水溶液(2x30mL)で洗浄した。水性層をDCM(3x20mL)で抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、溶媒を蒸発させて、表題化合物(1.50g、3.16mmol、収率81%、純度95%)を得た。
UPLC/MS (方法4):m/z 452 (M+H)+, RT 1.43分。
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((1-メチル-1H-ベンゾ[d]イミダゾール-5-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート
ジオキサン(0.5mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(90mg、0.149mmol)を、ジオキサン(0.5mL)中の(1-メチル-1H-ベンゾ[d]イミダゾール-5-イル)メタンアミン(72mg、0.448mmol)及びDIPEA(0.25mL、1.431mmol)の溶液に添加した。結果として得られた混合物を、100℃で3日間加熱した。反応混合物を室温に冷却し、真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~100%EtOAc/イソヘキサン、その後0~5%MeOH/DCM)により精製し、表題化合物(28mg、0.046mmol、収率31%、純度90%)を淡黄色のガラス状物として得た。
UPLC/MS (方法4):m/z 549 (M+H)+, RT 1.44分。
(3R,4R)-4-(((3-イソプロピル-7-(((1-メチル-1H-ベンゾ[d]イミダゾール-5-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((1-メチル-1H-ベンゾ[d]イミダゾール-5-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(28mg、0.051mmol)を、DCM(0.5mL)中のTFA(50μL、0.649mmol)の混合物で処理した。結果として得られた混合物を3時間撹拌した。この混合物を濃縮し、次いでEtOAc(5mL)と飽和NaHCO3水溶液(3mL)に分配し、相を分離した。有機相を水(2mL)とブライン(2mL)で洗浄し、MgSO4で乾燥させ、濾過して真空中で濃縮し、表題化合物(10mg、0.021mmol、収率41%、純度95%)を白色の粉末として得た。
UPLC/MS (方法4):m/z 449 (M+H)+, RT 0.97分。
1H NMR (500 MHz, DMSO-d6) δ 8.14 (s, 1H), 7.88 (t, J = 6.5 Hz, 1H), 7.65 - 7.62 (m, 2H), 7.51 (d, J = 8.3 Hz, 1H), 7.31 (dd, J = 8.3, 1.6 Hz, 1H), 6.73 - 6.66 (m, 1H), 5.35 - 5.29 (m, 1H), 5.22 (s, 1H), 4.53 (d, J = 6.4 Hz, 2H), 3.81 (s, 3H), 3.57 - 3.47 (m, 1H), 3.19 - 3.12 (m, 1H), 3.05 - 2.96 (m, 1H), 2.96 - 2.91 (m, 1H), 2.89 (dd, J = 12.0, 4.3 Hz, 1H), 2.79 - 2.73 (m, 1H), 2.34 - 2.25 (m, 1H), 2.15 (dd, J = 11.6, 10.0 Hz, 1H), 1.55 - 1.49 (m, 1H), 1.34 - 1.27 (m, 1H), 1.22 (t, J = 7.0 Hz, 6H), 1.15 - 1.07 (m, 1H), 1H under water.
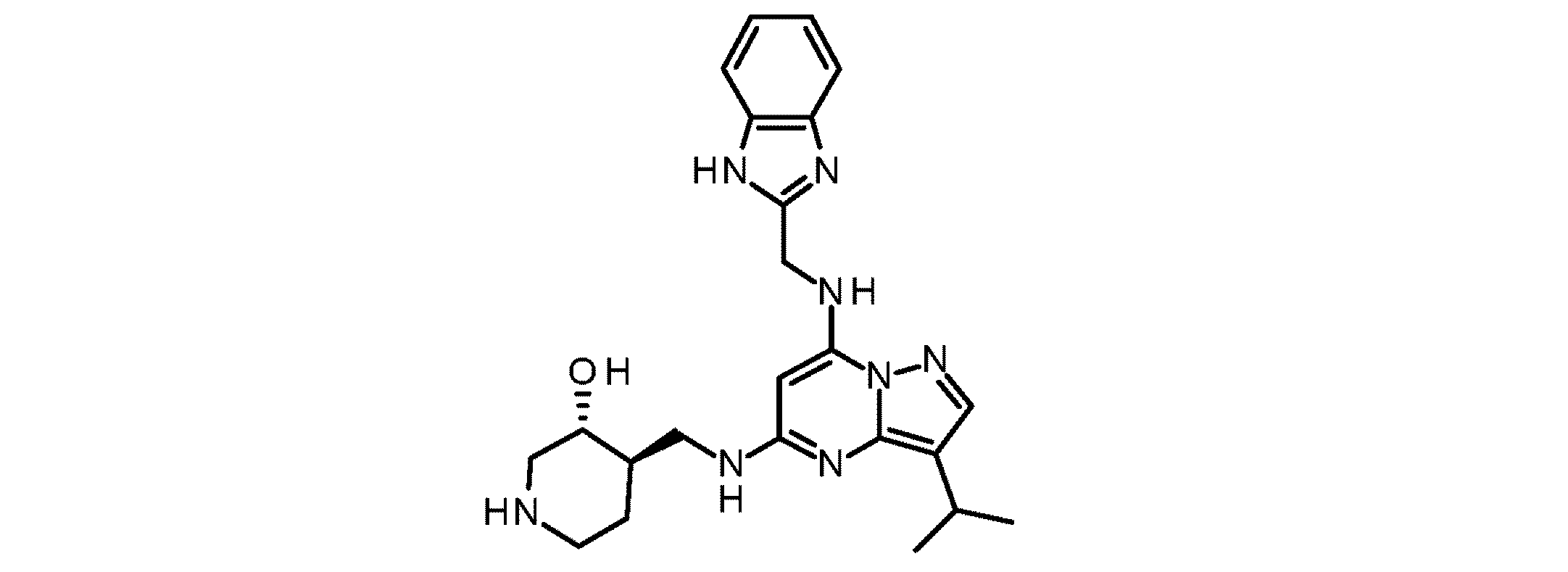
(3R,4R)-4-(((7-(((1 H-ベンゾ[d]イミダゾール-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-005)
ジオキサン(1mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(純度80%)(0.467g、0.827mmol)及び(1H-ベンゾ[d]イミダゾール-2-イル)メタンアミン(0.146g、0.993mmol)を、105℃に16時間加熱した。反応混合物を室温に冷却し、真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~20%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(26mg、0.041mmol、収率5%、純度85%)を茶色の固体として得た。
UPLC/MS (方法4):m/z 535 (M+H)+, RT 1.45分。
(3R,4R)-4-(((7-(((1H-ベンゾ[d]イミダゾール-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
塩化水素(ジオキサン中4M)(0.15mL、0.61mmol)を、DCM(10mL)中のtert-ブチル(3R,4R)-4-(((7-(((1H-ベンゾ[d]イミダゾール-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(30mg、0.040mmol)の溶液に添加した。反応物を16時間撹拌し、真空中で濃縮した。残渣をMeOH(5mL)中に希釈し、SCXカートリッジ上にロードし、MeOH(3xカラム体積)で洗浄し、MeOH中0.7Mアンモニア(3xカラム体積)で溶出した。アンモニア性メタノール溶液を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~20%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(5mg、10.9μmol、収率27%、純度95%)を黄色の固体として得た。
UPLC/MS (方法4と同じ方法であるが、ラン長は10分間であった):m/z 435 (M+H)+, RT 3.87分。
1H NMR (500 MHz, DMSO-d6) δ 12.30 (s, 1H), 7.71 (t, J = 6.2 Hz, 1H), 7.66 (s, 1H), 7.55 (s, 1H), 7.44 (s, 1H), 7.14 (dd, J = 6.1, 3.0 Hz, 2H), 6.81 - 6.71 (m, 1H), 5.29 (s, 1H), 5.22 (s, 1H), 4.69 (d, J = 5.8 Hz, 2H), 3.59 - 3.44 (m, 1H), 3.23 - 3.14 (m, 2H), 3.06 - 2.99 (m, 1H), 2.96 (p, J = 6.9 Hz, 1H), 2.89 (dd, J = 11.7, 4.6 Hz, 1H), 2.79 - 2.73 (m, 1H), 2.32 - 2.24 (m, 1H), 2.15 (dd, J = 11.6, 9.9 Hz, 1H), 1.53 (dd, J = 13.0, 3.4 Hz, 1H), 1.32 (s, 1H), 1.24 (t, J = 6.5 Hz, 6H), 1.18 - 1.07 (m, 1H)。
(3R,4R)-4-(((3-イソプロピル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-004)
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート
ジオキサン(0.5mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(0.100g、0.221mmol)及び(8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(0.107g、0.666mmol)を、105℃に4日間加熱した。反応混合物を室温に冷却し、濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(48mg、0.041mmol、収率38%、純度95%)をオレンジ色のガラス状固体として得た。
UPLC/MS (方法1):m/z 549 (M+H)+, RT 1.32分。
(3R,4R)-4-(((3-イソプロピル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
塩化水素(ジオキサン中4M)(0.40mL、1.51mmol)を、ジオキサン(3mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(48mg、0.083mmol)の懸濁液に添加した。反応混合物を40℃で4時間撹拌した。溶媒を真空中で除去した。残渣をMeOH(1mL)中に希釈し、SCXカートリッジ上にロードし、MeOH(約5mL)で洗浄し、MeOH中0.7Mアンモニア(約5mL)で溶出した。アンモニア性メタノール溶液を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(24mg、0.052mmol、収率63%、純度98%)を褐色のガラス状固体として得た。
LCMS (方法2):m/z 449 (M+H)+, RT 1.67分。
1H NMR (400 MHz, DMSO-d6) δ 8.32 (dt, J = 6.8, 1.1 Hz, 1H), 7.74 (s, 1H), 7.66 (t, J = 6.2 Hz, 1H), 7.63 (s, 1H), 7.01 (dt, J = 6.8, 1.2 Hz, 1H), 6.75 (t, J = 6.8 Hz, 1H), 6.72 - 6.68 (m, 1H), 5.35 - 5.29 (m, 1H), 5.27 (s, 1H), 4.57 (d, J = 6.1 Hz, 2H), 3.59 - 3.46 (m, 1H), 3.24 - 3.14 (m, 1H), 3.08 - 2.99 (m, 1H), 2.96 (p, J = 6.8 Hz, 1H), 2.90 (dd, J = 11.9, 4.3 Hz, 1H), 2.82 - 2.73 (m, 1H), 2.47 (s, 3H), 2.35 - 2.26 (m, 1H), 2.16 (dd, J = 11.6, 9.9 Hz, 1H), 1.59 - 1.51 (m, 1H), 1.39 - 1.28 (m, 1H), 1.23 (dd, J = 6.9, 4.8 Hz, 6H), 1.20 - 1.08 (m, 1H), 1H under water.
(3R,4R)-4-(((3-イソプロピル-7-(((5-メチルイミダゾ[1,2-a]ピリジン-3-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-001)
(3R,4R)-4-(((3-イソプロピル-7-(((5-メチルイミダゾ[1,2-a]ピリジン-3-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
ステップ4:ジオキサン(0.5mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(0.100g、0.221mmol)及び(8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(0.107g、0.666mmol)を、105℃に4日間加熱した。反応混合物を室温に冷却し、濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH(0.7M NH3含有)/DCM)により精製し、対応するBoc中間体(40mg)を得た。
LCMS (方法2):m/z 449 (M+H)+, RT 1.64分。
1H NMR (500 MHz, DMSO-d6) δ 7.61 (s, 1H), 7.58 (t, J = 5.3 Hz, 1H), 7.51 (s, 1H), 7.40 (d, J = 9.0 Hz, 1H), 7.13 (dd, J = 9.0, 6.8 Hz, 1H), 6.81 - 6.74 (m, 1H), 6.68 (d, J = 6.9 Hz, 1H), 5.42 (s, 1H), 5.31 (s, 1H), 4.96 (d, J = 5.0 Hz, 2H), 3.60 - 3.49 (m, 1H), 3.28 - 3.21 (m, 1H), 3.11 - 3.03 (m, 1H), 2.98 - 2.91 (m, 2H), 2.89 (s, 3H), 2.84 - 2.79 (m, 1H), 2.38 - 2.31 (m, 1H), 2.23 - 2.16 (m, 1H), 1.64 - 1.57 (m, 1H), 1.42 - 1.32 (m, 1H), 1.23 (dd, J = 6.9, 5.2 Hz, 6H), 1.20 - 1.13 (m, 1H), 1H under water.
(3R,4R)-4-[[[3-イソプロピル-7-[(3-メチルイミダゾ[2,1-b]チアゾール-6-イル)メチルアミノ]ピラゾロ[1,5-a]ピリミジン-5-イル]アミノ]メチル]ピペリジン-3-オール
(H-APPAMP-007)
エタノール(2mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(80.0mg、0.145mmol)、(3-メチルイミダゾ[2,1-b]チアゾール-6-イル)メタンアミン、2HCl、水和物(74.9mg、0.290mmol)及びDIPEA(0.228mL、1.305mmol)を、マイクロ波照射下に140℃で4時間加熱した。反応混合物を室温に冷却し、濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%MeOH(0.7M NH3含有)/DCM)により精製し、その後逆相C18クロマトグラフィー(4gカートリッジ、15~75%MeCN/10mM重炭酸アンモニウム)により精製し、表題化合物(40mg、0.071mmol、収率49%、純度97%)を褐色の固体として得た。
UPLC/MS (方法4):m/z 555 (M+H)+, RT 0.52分。
塩化水素(ジオキサン中4M)(0.169mL、0.676mmol)を、ジオキサン(2mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((3-メチルイミダゾ[2,1-b]チアゾール-6-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(25mg、0.045mmol)の溶液に添加した。反応混合物を35℃で1時間撹拌した。溶媒を蒸発させた。残渣をMeOH(1mL)中に希釈し、SCXカートリッジ上にロードし、MeOH(約5mL)で洗浄し、MeOH中0.7Mアンモニア(約5mL)で溶出した。アンモニア性メタノール溶液を減圧下で濃縮し、表題化合物(18mg、0.038mmol、収率84%、純度96%)を、Et2O中でトリチュレーションしその後真空下に50℃で一晩乾燥させた後で、褐色の固体として得た。
UPLC/MS (方法4):m/z 455 (M+H)+, RT 1.03分。
1H NMR (500 MHz, DMSO-d6) δ 7.62 (s, 1H), 7.59 (s, 1H), 7.49 (t, J = 6.1 Hz, 1H), 6.85 (q, J = 1.3 Hz, 1H), 6.79 - 6.73 (m, 1H), 5.38 - 5.35 (m, 1H), 5.35 (s, 1H), 4.47 - 4.43 (m, 2H), 3.25 - 3.19 (m, 1H), 3.10 - 3.02 (m, 1H), 2.98 - 2.90 (m, 2H), 2.85 - 2.79 (m, 2H), 2.36 (d, J = 1.3 Hz, 3H), 2.35 - 2.30 (m, 1H), 2.23 - 2.16 (m, 1H), 1.63 - 1.56 (m, 1H), 1.40 - 1.32 (m, 1H), 1.23 (dd, J = 6.9, 6.0 Hz, 6H), 1.21 - 1.13 (m, 1H), 1H under water.
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((7-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート
(H-APPAMP-008)
UPLC/MS (方法3):m/z 549 (M+H)+, RT 0.84分。
1,4-ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((7-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(67mg、0.122mmol)の溶液を、HCl(1,4-ジオキサン中4M)(458μL、1.832mmol)で処理した。反応混合物を室温で一晩撹拌し、濃縮乾固した。カラムクロマトグラフィー(4gカートリッジ、0~15%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(32mg、0.068mmol、収率55%、純度95%)を、真空下に50℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法4):m/z 449 (M+H)+, RT 1.08分。
1H NMR (500 MHz, DMSO-d6) δ 8.93 - 8.82 (m, 1H), 8.65 - 8.52 (m, 1H), 8.32 (s, 1H), 7.73 (s, 1H), 7.67 (s, 1H), 7.44 (d, J = 9.2 Hz, 1H), 7.13 (d, J = 9.3 Hz, 1H), 6.99 - 6.86 (m, 1H), 6.12 - 6.03 (m, 1H), 5.27 (s, 1H), 4.56 (d, J = 6.0 Hz, 2H), 3.60 - 3.50 (m, 1H), 3.47 - 3.39 (m, 1H), 3.25 - 3.13 (m, 2H), 3.01 - 2.92 (m, 1H), 2.84 - 2.72 (m, 1H), 2.66 - 2.59 (m, 1H), 2.53 - 2.52 (m, 1H), 2.26 (s, 3H), 1.85 - 1.76 (m, 1H), 1.68 - 1.56 (m, 1H), 1.52 - 1.41 (m, 1H), 1.24 (t, J = 6.6 Hz, 6H)。
(3R,4R)-4-(((3-イソプロピル-7-(((7-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-009)
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(80mg、0.145mmol)を、EtOH(2.0mL)中の(7-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、2HCl(102mg、0.435mmol)及びDIPEA(0.228mL、1.305mmol)の溶液に添加した。結果として得られた混合物を、マイクロ波照射下に140℃で3.5時間加熱した。反応混合物を室温に冷却し、真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(60mg、0.093mmol、収率64%、純度85%)を茶色の油状物として得た。
UPLC/MS (方法3):m/z 549 (M+H)+, RT 0.83分。
1,4-ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((6-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(60mg、0.104mmol)の溶液を、HCl(1,4-ジオキサン中4M)(0.390mL、1.558mmol)で処理した。反応混合物を室温で一晩撹拌し、濃縮乾固した。カラムクロマトグラフィー(4gカートリッジ、0~15%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(33mg、0.070mmol、収率67%、純度95%)を、真空下に50℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法4):m/z 449 (M+H)+, RT 1.07分。
1H NMR (500 MHz, DMSO-d6) δ 8.36 (d, J = 6.9 Hz, 1H), 7.68 (s, 1H), 7.67 - 7.65 (m, 1H), 7.64 (s, 1H), 7.30 - 7.25 (m, 1H), 6.82 - 6.76 (m, 1H), 6.70 (dd, J = 7.0, 1.7 Hz, 1H), 5.61 - 5.55 (m, 1H), 5.27 (s, 1H), 4.53 (d, J = 5.9 Hz, 2H), 3.62 - 3.51 (m, 1H), 3.25 - 3.20 (m, 1H), 3.19 - 3.12 (m, 1H), 3.01 (dd, J = 11.6, 4.4 Hz, 1H), 2.99 - 2.93 (m, 1H), 2.92 - 2.87 (m, 1H), 2.47 - 2.42 (m, 1H), 2.33 (s, 3H), 2.32 - 2.26 (m, 1H), 1.67 - 1.61 (m, 1H), 1.46 - 1.38 (m, 1H), 1.30 - 1.26 (m, 1H), 1.24 (t, J = 6.6 Hz, 6H). 1H under water.
(3R,4R)-4-(((3-イソプロピル-7-(((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-010)
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(80mg、0.145mmol)を、EtOH(2.0mL)中の(5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、2HCl(102mg、0.435mmol)及びDIPEA(0.228mL、1.305mmol)の溶液に添加した。結果として得られた混合物を、マイクロ波照射下に140℃で4時間加熱した。反応混合物を室温に冷却し、真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(85mg、0.116mmol、収率80%、純度75%)を茶色の油状物として得た。
UPLC/MS (方法4):m/z 549 (M+H)+, RT 1.50分。
1,4-ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(85mg、0.116mmol)の溶液を、HCl(1,4-ジオキサン中4M)(0.436mL、1.743mmol)で処理した。反応混合物を室温で一晩撹拌し、濃縮乾固した。RPフラッシュC18上のカラムクロマトグラフィー(4gカートリッジ、15~50%MeCN/10mM重炭酸アンモニウム)により精製し、表題化合物(12mg、0.025mmol、収率21%、純度93%)を、真空下に50℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法4):m/z 449 (M+H)+, RT 1.07分。
1H NMR (500 MHz, DMSO-d6) δ 7.67 (s, 1H), 7.63 (s, 1H), 7.58 (t, J = 6.1 Hz, 1H), 7.43 (dd, J = 8.9, 1.2 Hz, 1H), 7.21 (dd, J = 9.0, 6.8 Hz, 1H), 6.79 - 6.75 (m, 2H), 5.44 - 5.37 (m, 1H), 5.33 (s, 1H), 4.59 (d, J = 5.9 Hz, 2H), 3.61- 3.49 (m, 1H), 3.25 - 3.19 (m, 1H), 3.11 - 3.05 (m, 1H), 2.99 - 2.92 (m, 2H), 2.87 - 2.81 (m, 1H), 2.56 (s, 3H), 2.40 - 2.33 (m, 1H), 2.26 - 2.20 (m, 1H), 1.64 - 1.57 (m, 1H), 1.42 - 1.34 (m, 1H), 1.24 (dd, J = 6.9, 6.0 Hz, 6H), 1.21 - 1.15 (m, 1H). 1H under water.
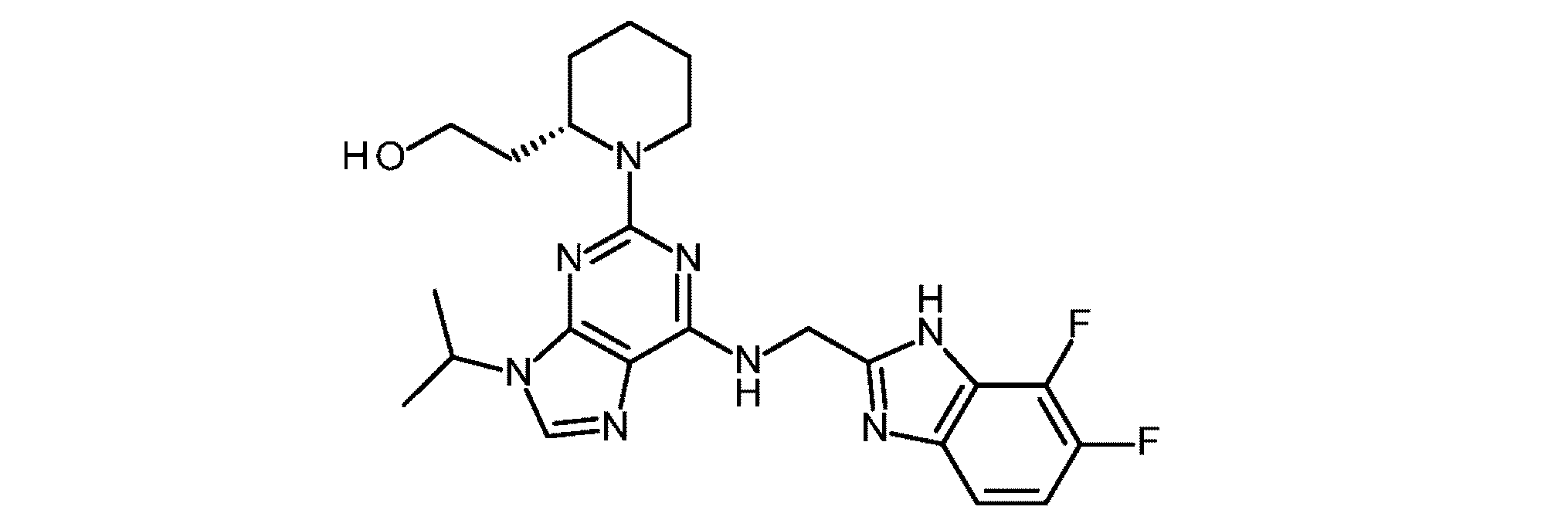
(3R,4R)-4-(((7-(((6-フルオロイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-011)
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(60mg、0.109mmol)を、EtOH(4.0mL)中の(6-フルオロイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(53.9mg、0.326mmol)及びDIPEA(0.171mL、0.979mmol)の溶液に添加した。結果として得られた混合物を、マイクロ波照射下に140℃で4時間加熱し、濃縮乾固し、NMP(3.0mL)に再溶解した。結果として得られた混合物を、マイクロ波照射下に160℃で4時間加熱した。粗油状物を、SCX(2g - MeOH(15mL)で洗浄し、0.7M NH3含有MeOH(15mL)で溶出した)を通して濾過し、茶色の油状物を得た。カラム(4gカートリッジ(乾燥ロード)、0~10%MeOH(0.7M NH3含有)/DCM、次いで100%MeOH(0.7M NH3含有))により精製し、その後RPフラッシュC18上のカラムクロマトグラフィー(4gカートリッジ、15~75%MeCN/10mM重炭酸アンモニウム)により精製し、表題化合物(5mg、9.94μmol、収率9%、純度90%)を、Et2Oからの沈殿後に褐色の固体として得た。
UPLC/MS (方法4):m/z 453 (M+H)+, RT 1.01分。
1H NMR (500 MHz, DMSO-d6) δ 8.69 (dd, J = 4.7, 2.5 Hz, 1H), 7.79 (s, 1H), 7.68 (t, J = 6.2 Hz, 1H), 7.63 (s, 1H), 7.57 (dd, J = 10.0, 5.3 Hz, 1H), 7.30 (ddd, J = 10.2, 8.4, 2.5 Hz, 1H), 6.75 - 6.68 (m, 1H), 5.30 - 5.27 (m, 1H), 5.26 (s, 1H), 4.56 (d, J = 6.1 Hz, 2H), 3.60 - 3.47 (m, 1H), 3.23 - 3.15 (m, 1H), 3.07 - 2.99 (m, 1H), 2.98 - 2.92 (m, 1H), 2.89 (dd, J = 11.4, 4.5 Hz, 1H), 2.82 - 2.73 (m, 1H), 2.33 - 2.23 (m, 1H), 2.14 (dd, J = 11.7, 9.9 Hz, 1H), 1.58 - 1.51 (m, 1H), 1.37 - 1.27 (m, 1H), 1.23 (t, J = 6.5 Hz, 6H), 1.19 - 1.11 (m, 1H). 1H under water.
(3R,4R)-4-(((7-(((6-クロロイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-012)
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(60mg、0.109mmol)を、EtOH(4mL)中の(6-クロロイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(59.3mg、0.326mmol)及びDIPEA(0.171mL、0.979mmol)の溶液に添加した。結果として得られた混合物を、マイクロ波照射下に140℃で4時間加熱し、濃縮乾固し、NMP(3mL)に再溶解した。結果として得られた混合物を、マイクロ波照射下に160℃で4時間加熱した。粗油状物を、SCX(2g - MeOH(15mL)で洗浄し、0.7M NH3含有MeOH(15mL)で溶出した)を通して濾過し、茶色の油状物を得た。RPフラッシュC18上のカラムクロマトグラフィー(4gカートリッジ、35~100%MeCN/10mM重炭酸アンモニウム)により精製し、表題化合物(32mg、42μmol、収率38%、純度75%)を茶色の油状物として得た。
UPLC/MS (方法4):m/z 569 (M+H)+, RT 1.55分。
1,4-ジオキサン(2mL)中のtert-ブチル(3R,4R)-4-(((7-(((6-クロロイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(32mg、0.045mmol)の溶液を、HCl(1,4-ジオキサン中4M)(0.169mL、0.675mmol)で処理した。反応混合物を室温で一晩撹拌し、濃縮乾固した。粗油状物を、SCX(2g - MeOH(15mL)で洗浄し、0.7M NH3含有MeOH(15mL)で溶出した)を通して濾過し、茶色の油状物を得た。カラム(4gカートリッジ(乾燥ロード)、0~20%MeOH(0.7M NH3含有)/DCM)により精製し、その後RPフラッシュC18上のカラムクロマトグラフィー(4gカートリッジ、35~100%MeCN/10mM重炭酸アンモニウム)により精製し、表題化合物(10mg、0.020mmol、収率44%、純度92%)を、Et2Oから沈殿させ、次いで真空下に50℃で一晩乾燥させた後に、褐色の固体として得た。
UPLC/MS (方法4):m/z 469 (M+H)+, RT 1.08分。
1H NMR (500 MHz, DMSO-d6) δ 8.76 (d, J = 2.1 Hz, 1H), 7.77 (s, 1H), 7.69 (t, J = 6.3 Hz, 1H), 7.63 (s, 1H), 7.55 (d, J = 9.6 Hz, 1H), 7.26 (dd, J = 9.6, 2.1 Hz, 1H), 6.76 - 6.68 (m, 1H), 5.32 - 5.27 (m, 1H), 5.25 (s, 1H), 4.56 (d, J = 6.1 Hz, 2H), 3.60 - 3.47 (m, 1H), 3.24 - 3.16 (m, 1H), 3.05 - 2.98 (m, 1H), 2.98 - 2.91 (m, 1H), 2.91 - 2.87 (m, 1H), 2.80 - 2.73 (m, 1H), 2.33 - 2.24 (m, 1H), 2.18 - 2.11 (m, 1H), 1.58 - 1.50 (m, 1H), 1.39 - 1.27 (m, 1H), 1.26 - 1.21 (m, 6H), 1.18 - 1.09 (m, 1H). 1H under water.
(3R,4R)-4-(((7-(((8-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-013)
tert-ブチル(3R,4R)-3-ヒドロキシ-4-(((3-イソプロピル-7-(メチルスルフィニル)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-1-カルボキシレート(120mg、99重量%、0.22mmol)を、NMP(2mL)中の(8-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、酢酸(0.11g、0.43mmol)及びDIPEA(0.19mL、1.1mmol)の溶液に添加した。結果として得られた混合物を、マイクロ波照射下に140℃で4時間、次いで160℃で4時間加熱した。粗油状物を、SCX(4g - MeOH(30mL)で洗浄し、0.7M NH3含有MeOH(30mL)で溶出)を通して濾過し、茶色の油状物を得た。カラム(4gカートリッジ(乾燥ロード)、0~15%MeOH(0.7M NH3含有)/DCM)により精製し、表題化合物(42mg、67μmol、収率31%、純度92%)を茶色の油状物として得た。
UPLC/MS (方法4):m/z 575 (M+H)+, RT 1.58分。
1,4-ジオキサン(0.25mL)中のtert-ブチル(3R,4R)-4-(((7-(((8-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(23mg、37μmol)を、HCl(1,4-ジオキサン中4M)(0.14mL、0.55mmol)で処理した。反応混合物を35℃で1時間撹拌し、濃縮乾固した。粗油状物を、SCX(4g - MeOH(30mL)で洗浄し、0.7M NH3含有MeOH(30mL)で溶出した)を通して精製し、表題化合物(17mg、34μmol、収率92%、純度95%)を、Et2Oから沈殿させ、次いで真空下に50℃で一晩乾燥させた後、茶色の固体として得た。
UPLC/MS (方法4):m/z 475 (M+H)+, RT 1.14分。
1H NMR (500 MHz, DMSO-d6) δ 8.30 - 8.23 (m, 1H), 7.74 (s, 1H), 7.67 (t,J= 6.2 Hz, 1H), 7.64 (s, 1H), 6.74 - 6.69 (m, 3H), 5.36 - 5.30 (m, 1H), 5.28 (s, 1H), 4.58 (d,J = 5.9 Hz, 2H), 3.59 - 3.49 (m, 1H), 3.23 - 3.16 (m, 1H), 3.08 - 3.00 (m, 1H), 2.99 - 2.92 (m, 1H), 2.91 (dd,J = 11.8, 4.9 Hz, 1H), 2.81 - 2.75 (m, 1H), 2.48 - 2.43 (m, 1H), 2.35 - 2.26 (m, 1H), 2.16 (dd,J = 11.7, 9.9 Hz, 1H), 1.59 - 1.52 (m, 1H), 1.39 - 1.29 (m, 1H), 1.24 (dd,J = 6.9, 5.9 Hz, 6H), 1.20 - 1.11 (m, 1H), 1.04 - 0.98 (m, 2H), 0.98 - 0.92 (m, 2H). 1H under water.
(8-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、AcOH
水(2.5mL)中のリン酸三カリウム(755mg、3.55mmol)の溶液を、1,4-ジオキサン(10mL)中の8-ブロモイミダゾ[1,2-a]ピリジン-2-カルボアルデヒド(200mg、0.889mmol)及びシクロプロピルボロン酸(229mg、2.67mmol)の溶液に添加した。N2を、反応混合物を通して10分間バブリングし、次いでPdCl2(dppf)(65.0mg、0.089mmol)を添加した。N2を、反応混合物を通してさらに5分間バブリングし、その後100℃で3時間加熱した。室温で、水(20mL)及びEtOAc(40mL)を添加した。層を分離し、水性層をEtOAc(3x15mL)で抽出した。合わせた有機層を相分離器を通して濾過し、濃縮した。カラム(12gカートリッジ(乾燥ロード)、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(141mg、0.750mmol、収率71%、純度99%)を黄色の固体として得た。
EtOH(3.5mL)中の8-シクロプロピルイミダゾ[1,2-a]ピリジン-2-カルボアルデヒド(130mg、698μmol)、ヒドロキシルアミン塩酸塩(121mg、1.75mmol)及びピリジン(0.14mL、1.75mmol)の溶液を、80℃で2時間撹拌した。室温で、沈殿物を濾過により回収し、EtOH(2x2mL)ですすいだ。固体を真空下でさらに乾燥させて、8-シクロプロピルイミダゾ[1,2-a]ピリジン-2-カルボアルデヒドオキシム(135mg)を褐色の固体として得、これをAcOH(3mL)に溶解した。溶液を0℃で冷却し、次いで酢酸ナトリウム(11.0mg、134μmol)及び亜鉛粉末(658mg、10.1mmol)を添加した。反応混合物を室温で一晩撹拌した後、セライトを通して濾過し、DCM(20mL)及びMeOH(20mL)ですすいだ。濾液を濃縮乾固し、油状物を得た。SCX(10g - MeOH(50mL)で洗浄し、0.7M NH3含有MeOH(50mL)で溶出した)を通して濾過し、表題化合物(164mg、663μmol、収率99%、純度95%)をわずかに黄色の油状物として得た。
1H NMR (500 MHz, DMSO-d6)は生成物の構造と一致していた。
(3R,4R)-4-(((3-イソプロピル-7-((キノリン-2-イルメチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-014)
キノリン-2-イルメタンアミン(165mg、1.04mmol)を、EtOH(3.3mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(200mg、0.869mmol)及びDIPEA(908μL、5.21mmol)の溶液に添加した。反応混合物を一晩加熱還流した。反応混合物を真空中で濃縮し、オレンジ色の固体を得た。カラム(12gカートリッジ、DCM)により精製し、表題化合物(240mg、0.67mmol、収率78%、純度99%)をオレンジ色の固体として得た。
1H NMR (500 MHz, DMSO-d6)は生成物の構造と一致していた。
BOC無水物(193mg、886.1μmol)を、THF(13.6mL)中の5-クロロ-3-イソプロピル-N-(キノリン-2-イルメチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(240mg、681.6μmol)及びDMAP(17mg、136.3μmol)の溶液に添加した。反応混合物を60℃で1.5時間撹拌した。反応混合物を減圧下で濃縮し、次いでDCM(15mL)中に希釈し、ブライン(3x10mL)で洗浄した。合わせた有機層を相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~2.5%MeOH/DCM)により精製し、表題化合物(317mg、0.67mmol、収率98%、純度95%)をオレンジ色の油状物として得た。
UPLC/MS (方法6):m/z 453 (M+H)+, RT 0.92分。
THF(2.1mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(キノリン-2-イルメチル)カルバメート(115mg、0.25mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(63mg、0.27mmol)及びtBuBrettPhos Pd G3(21mg、25μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.37mL、0.37mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1時間加熱した。反応を水(5mL)でクエンチし、EtOAc(3x5mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(130mg、0.19mmol、収率77%、純度95%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 646 (M+H)+, RT 1.85分。
塩化水素(1,4-ジオキサン中4M)(0.88mL、3.5mmol)を、1,4-ジオキサン(1mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(キノリン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(120mg、0.18mmol)の懸濁液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(66mg、0.14mmol、収率81%、純度97%)を、Et2Oから沈殿させて真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法4):m/z 446 (M+H)+, RT 1.18分。
1H NMR (500 MHz, DMSO-d6) δ 8.35 (d,J = 8.5 Hz, 1H), 8.04 - 7.99 (m, 2H), 7.97 (dd,J = 8.2, 1.4 Hz, 1H), 7.81 - 7.74 (m, 1H), 7.68 (s, 1H), 7.62 - 7.57 (m, 1H), 7.53 (d,J= 8.5 Hz, 1H), 6.75 - 6.68 (m, 1H), 5.29 - 5.23 (m, 1H), 5.19 (s, 1H), 4.73 (d,J = 6.0 Hz, 2H), 3.56 - 3.44 (m, 1H), 3.21 - 3.14 (m, 1H), 3.05 - 2.98 (m, 1H), 2.99 - 2.92 (m, 1H), 2.88 (dd,J = 11.5, 4.5 Hz, 1H), 2.78 - 2.72 (m, 1H), 2.31 - 2.23 (m, 1H), 2.17 - 2.11 (m, 1H), 1.55 - 1.49 (m, 1H), 1.36 - 1.27 (m, 1H), 1.27 - 1.22 (m, 6H), 1.16 - 1.11 (m, 1H). 1H under water.
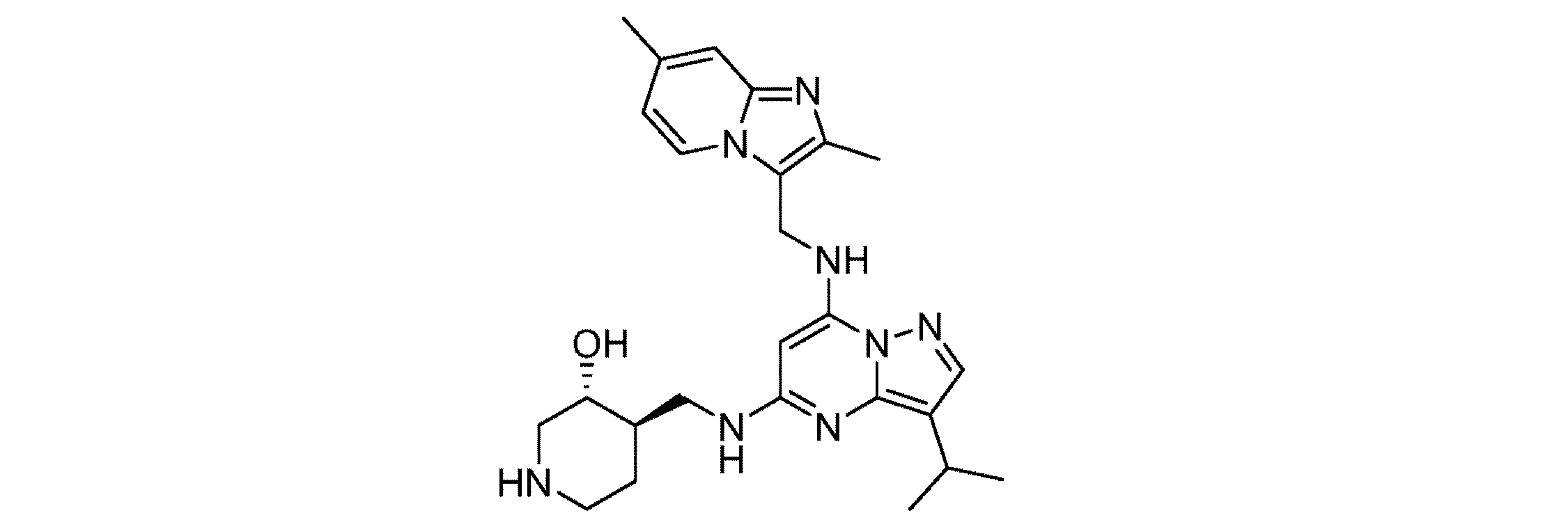
(3R,4R)-4-(((7-(((2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-015)
(2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メタンアミン(171mg、0.976mmol)を、EtOH(3.2mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(187mg、0.813mmol)及びDIPEA(0.85mL、4.874mmol)の溶液に添加した。反応混合物を、一晩加熱還流した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、イソヘキサン中0~100%EtOAc)により精製し、表題化合物(233mg、0.57mmol、収率70%、純度90%)を、オフホワイト色の固体として得た。
UPLC/MS (方法6):m/z 369 (M+H)+, RT 0.73分。
BOC無水物(179mg、819μmol)を、THF(12.6mL)中の5-クロロ-N-((2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(233mg、0.63mmol)及びDMAP(15.4mg、126μmol)の溶液に添加した。反応混合物を60℃で16分間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(15mL)と水(10mL)に分配した。有機層をブライン(2x10mL)で洗浄し、相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~4%MeOH/DCM)により精製し、表題化合物(249mg、0.50mmol、収率79%、純度94%)を淡黄色の固体として得た。
UPLC/MS (方法6):m/z 469 (M+H)+, RT 0.84分。
THF(2.5mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メチル)カルバメート(120mg、0.256mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(64.9mg、0.282mmol)及びtBuBrettPhos Pd G3(21.9mg、0.0256mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.33mL、333μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に4.5時間加熱した。室温で、反応混合物をセライトを通して濾過し、EtOAc(15mL)ですすいだ。濾液を水で希釈し、この水性(aqueous)をEtOAc(3x20mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~80%(1:3 EtOH/EtOAc)/イソヘキサン)により精製し、表題化合物(89mg、0.10mmol、収率39%、純度75%)を、茶色の油状物として得た。
UPLC/MS (方法4):m/z 663 (M+H)+, RT 1.75分。
塩化水素(1,4-ジオキサン中4M)(0.66mL、2.62mmol)を、1,4-ジオキサン(10mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(87mg、0.131mmol)の懸濁液に添加した。反応混合物を35℃で2.5時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(60mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(40mg、83mmol、収率63%、純度95%)を、Et2Oから沈殿させて真空下に40℃で一晩乾燥させた後、淡黄色の固体として得た。
UPLC/MS (方法4):m/z 463 (M+H)+, RT 1.05分。
1H NMR (500 MHz, DMSO-d6) δ 8.51 (d, J = 7.0 Hz, 1H), 7.80 (t, J = 5.4 Hz, 1H), 7.59 (s, 1H), 7.21 (s, 1H), 6.85 - 6.79 (m, 1H), 6.75 (dd, J = 7.0, 1.7 Hz, 1H), 5.33 - 5.28 (m, 1H), 5.17 (s, 1H), 4.73 (d, J = 5.1 Hz, 2H), 3.61 - 3.48 (m, 1H), 3.23 - 3.16 (m, 1H), 3.06 - 2.98 (m, 1H), 2.95 - 2.86 (m, 2H), 2.84 - 2.76 (m, 1H), 2.48 (s, 3H), 2.33 - 2.30 (m, 4H), 2.19 - 2.12 (m, 1H), 1.61 - 1.53 (m, 1H), 1.39 - 1.32 (m, 1H), 1.22 - 1.18 (m, 6H), 1.19 - 1.12 (m, 1H). 1H under water.
(2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メタンアミン
EtOH(14.8mL)中の2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-カルボアルデヒド(0.525g、3.01mmol)、ヒドロキシルアミン塩酸塩(0.524g、7.54mmol)及びピリジン(0.61mL、7.54mmol)の溶液を、80℃で2時間撹拌した。反応混合物を減圧下で濃縮し、次いでAcOH(10.5mL)に再溶解した。この溶液を0℃で冷却し、次いで酢酸ナトリウム(50mg、604μmol)及び亜鉛粉末(2.96g、45.3mmol)を添加した。反応混合物を室温で一晩撹拌した後、セライトを通して濾過し、DCM(100mL)ですすいだ。濾液を濃縮乾固し、油状物を得た。SCX(14g - MeOH(100mL)で洗浄し、0.7M NH3含有MeOH(100mL)で溶出した)を通して濾過し、表題化合物(2,7-ジメチルイミダゾ[1,2-a]ピリジン-3-イル)メタンアミン(0.259g、1.33mmol、収率44%、純度90%)を白色の固体として得た。
UPLC/MS (方法6):m/z 176 (M+H)+, RT 0.42分。
(3R,4R)-4-(((7-((イミダゾ[1,2-a]ピリジン-3-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-016)
イミダゾ[1,2-a]ピリジン-3-イルメタンアミン、2HCl(115mg、522μmol)を、EtOH(1.5mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(100mg、435μmol)及びDIPEA(0.38mL、2.17mmol)の溶液に添加した。反応混合物を一晩加熱還流した。反応混合物を真空中で濃縮した。
1H NMR (500 MHz, DMSO-d6)は生成物の構造と一致していた。
BOC無水物(97mg、442μmol)を、THF(2mL)中の5-クロロ-N-(イミダゾ[1,2-a]ピリジン-3-イルメチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(137mg、402μmol)及びDMAP(5mg、40.2μmol)の溶液に添加した。反応混合物を室温で3時間撹拌した。反応混合物を減圧下で濃縮した。
UPLC/MS (方法4):m/z 441 (M+H)+, RT 1.71分。
THF(3.3mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(イミダゾ[1,2-a]ピリジン-3-イルメチル)カルバメート(167mg、379μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(96.0mg、417μmol)及びtBuBrettPhos Pd G3(32.4mg、37.9μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(492μL、492μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応を水(15mL)でクエンチし、EtOAc(3x15mL)で抽出した。合わせた有機層を相分離器を通して濾過し、減圧下で濃縮した。
UPLC/MS (方法4):m/z 635 (M+H)+, RT 1.64分。
塩化水素(1,4-ジオキサン中4M)(0.88mL、3.53mmol)を、1,4-ジオキサン(0.5mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(イミダゾ[1,2-a]ピリジン-3-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(112mg、176μmol)の溶液に添加した。反応混合物を35で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物を0.7M NH3含有MeOH(40mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(57mg、0.13mmol、収率73%、純度98%)を、Et2Oからの沈殿後に白色の固体として得た。
UPLC/MS (方法4):m/z 435 (M+H)+, RT 0.97分。
1H NMR (500 MHz, DMSO-d6) δ 8.48 (dd,J = 6.8, 1.2 Hz, 1H), 7.78 (s, 1H), 7.65 (t,J = 6.1 Hz, 1H), 7.63 (s, 1H), 7.50 (d,J = 9.1 Hz, 1H), 7.24 - 7.18 (m, 1H), 6.85 (td,J = 6.7, 1.2 Hz, 1H), 6.75 - 6.69 (m, 1H), 5.33 - 5.29 (m, 1H), 5.28 (s, 1H), 4.56 (d,J = 6.0 Hz, 2H), 3.60 - 3.47 (m, 1H), 3.22 - 3.15 (m, 1H), 3.06 - 2.99 (m, 1H), 2.99 - 2.92 (m, 1H), 2.90 (dd,J = 11.6, 4.5 Hz, 1H), 2.81 - 2.74 (m, 1H), 2.33 - 2.25 (m, 1H), 2.15 (dd,J = 11.6, 9.9 Hz, 1H), 1.57 - 1.51 (m, 1H), 1.38 - 1.28 (m, 1H), 1.23 (t,J = 6.5 Hz, 6H), 1.19 - 1.10 (m, 1H). 1H under water.
(3R,4R)-4-(((3-イソプロピル-7-(((3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-017)
(3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(105mg、652μmol)を、EtOH(3.2mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(150mg、652μmol)及びDIPEA(0.85mL、4.89)の溶液に添加した。反応混合物を、80℃で一晩加熱した。反応混合物を、真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(130mg、0.31mmol、収率48%、純度85%)を黄色の固体として得た。
UPLC/MS (方法4):m/z 355 (M+H)+, RT 1.48分。
BOC無水物(32mg、0.15mmol)を、THF(1.2mL)中の5-クロロ-3-イソプロピル-N-((3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(44mg、0.12mmol)及びDMAP(3mg、25μmol)の溶液に添加した。反応混合物を室温で2時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~100%EtOAc/イソヘキサン)による精製N2により、表題化合物(51mg、0.11mmol、収率89%、純度99%)を白色の固体として得た。
UPLC/MS (方法4):m/z 455 (M+H)+, RT 1.80分。
THF(1.9mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(88mg、0.19mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(49mg、0.21mmol)及び tBuBrettPhos Pd G3(17mg、19μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.25mL、0.25mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1.5時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン、次いで0~100%(1:3 EtOH/EtOAc)/イソヘキサン)により精製し、表題化合物(140mg、0.18mmol、収率95%、純度85%)を茶色の油状物として得た。
UPLC/MS (方法4):m/z 649 (M+H)+, RT 1.69分。
塩化水素(ジオキサン中4M)(1.02mL、4.10mmol)を、ジオキサン(1.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(140mg、205μmol)の懸濁液に添加した。反応混合物を35℃で1.5時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(30mg、60μmol、32%、純度95%)を、Et2Oから沈殿させて真空下に40℃で一晩乾燥させた後、クリーム色の固体として得た。
UPLC/MS (方法4):m/z 449 (M+H)+, RT 1.02分。
1H NMR (400 MHz, DMSO-d6) δ 8.23 (d,J = 6.9 Hz, 1H), 7.61 (s, 1H), 7.53 - 7.49 (m, 1H), 7.44 (t,J = 5.8 Hz, 1H), 7.26 - 7.17 (m, 1H), 6.93 (td,J = 6.8, 1.2 Hz, 1H), 6.80 - 6.74 (m, 1H), 5.39 (s, 1H), 5.35 - 5.31 (m, 1H), 4.55 (d,J = 5.7 Hz, 2H), 3.61 - 3.47 (m, 1H), 3.24 - 3.15 (m, 1H), 3.08 - 2.99 (m, 1H), 2.99 - 2.86 (m, 2H), 2.82 - 2.74 (m, 1H), 2.35 - 2.24 (m, 1H), 2.16 (dd,J = 11.6, 9.9 Hz, 1H), 1.61 - 1.52 (m, 1H), 1.40 - 1.29 (m, 1H), 1.22 (dd,J = 6.9, 5.0 Hz, 6H), 1.19 - 1.13 (m, 1H)。4Hは見えない。
3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
(3-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
EtOH(5.0mL)中の3-メチルイミダゾ[1,2-a]ピリジン-2-カルボアルデヒド(500mg、3.12mmol)、ヒドロキシルアミン塩酸塩(542mg、7.80mmol)及びピリジン(0.63mL、7.80mmol)の懸濁液を、80℃で2時間撹拌した。反応混合物を減圧下で濃縮し、次いでAcOH(5.0mL)に再溶解した。溶液を0℃で冷却し、次いで酢酸ナトリウム(51mg、616μmol)及び亜鉛粉末(2.02g、30.8mmol)を添加した。反応混合物を室温で一晩撹拌した後、セライトを通して濾過し、DCM(50mL)及びMeOH(50mL)ですすいだ。濾液を濃縮乾固し、油状物を得た。SCX(14g - MeOH(50mL)で洗浄し、0.7M NH3含有MeOH(50mL)で溶出した)を通して濾過し、表題化合物(371mg、2.2mmol、収率71%、純度95%)を白色の固体として得た。
DMSO-d6中の1H NMRは生成物の構造と一致していた。
(3R,4R)-4-(((7-((イミダゾ[1,2-a]ピリジン-2-イルメチル-d2)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-018)
イミダゾ[1,2-a]ピリジン-2-イルメタン-d2-アミン(102mg、684μmol)を、EtOH(7.0mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(157mg、684μmol)及びDIPEA(0.89mL、893μmol)の溶液に添加した。反応混合物を80℃で一晩加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(180mg、0.50mmol、収率73%、純度95%)を白色の固体として得た。
UPLC/MS (方法4):m/z 345 (M+H)+, RT 1.36分。
BOC無水物(131mg、599μmol)を、THF(5.0mL)中の5-クロロ-N-(イミダゾ[1,2-a]ピリジン-2-イルメチル-d2)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(180mg、499μmol)及びDMAP(12mg、99.8μmol)の溶液に添加した。反応混合物を室温で2時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(184mg、0.36mmol、収率72%、純度87%)を白色の固体として得た。
UPLC/MS (方法4):m/z 445 (M+H)+, RT 1.72分。
THF(1.9mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(イミダゾ[1,2-a]ピリジン-2-イルメチル-d2)カルバメート(184mg、415μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(105mg、457μmol)及びtBuBrettPhos Pd G3(35.5mg、41.5μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(540μL、540μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1.5時間加熱した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(236mg、0.33mmol、収率80%、純度90%)を白色の固体として得た。
UPLC/MS (方法4):m/z 637 (M+H)+, RT 1.64分。
塩化水素(ジオキサン中4M)(0.79mL、3.14mmol)を、ジオキサン(1.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(イミダゾ[1,2-a]ピリジン-2-イルメチル-d2)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(100mg、157μmol)の懸濁液に添加した。反応混合物を35℃で4時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(61mg、0.13mmol、収率85%、純度95%)を、Et2Oから沈殿させて真空下に40℃で一晩乾燥させた後、白色の固体として得た。
UPLC/MS (方法4):m/z 437 (M+H)+, RT 1.03分。
1H NMR (400 MHz, DMSO-d6) δ 8.48 (dt,J = 6.8, 1.3 Hz, 1H), 7.78 (s, 1H), 7.63 (s, 2H), 7.50 (d,J = 9.1 Hz, 1H), 7.20 (m, 1H), 6.85 (td,J = 6.8, 1.2 Hz, 1H), 6.76 - 6.68 (m, 1H), 5.29 (m, 2H), 3.60 - 3.48 (m, 1H), 3.23 - 3.13 (m, 1H), 3.07 - 2.85 (m, 3H), 2.80 - 2.72 (m, 1H), 2.34 - 2.23 (m, 1H), 2.14 (dd,J = 11.5, 10.0 Hz, 1H), 1.58 - 1.49 (m, 1H), 1.37 - 1.27 (m, 1H), 1.23 (dd,J = 6.9, 4.9 Hz, 6H), 1.19 - 1.11 (m, 1H). 1H under water.
イミダゾ[1,2-a]ピリジン-2-イルメタン-d2-アミン
重水素化リチウムアルミニウム(88mg、2.10mmol)を、THF(21mL)中のエチルイミダゾ[1,2-a]ピリジン-2-カルボキシレート(400mg、2.10mmol)の溶液に0℃で添加した。混合物を0℃で15分間撹拌し、次いで水(0.1mL)を添加し、その後2M NaOH水溶液(0.1mL)、次いで水(0.3mL)を添加した。溶液を室温に温め、15分間撹拌し、その後無水MgSO4を添加し、混合物をさらに15分間撹拌した。混合物を減圧下で濃縮した。
UPLC/MS (方法4):m/z 151 (M+H)+, RT 0.47分。
塩化チオニル(205μL、2.81mmol)を、DCM(14mL)中のイミダゾ[1,2-a]ピリジン-2-イルメタン-d2-オール(211mg、1.40mmol)の溶液に0℃で滴下添加した。混合物を0℃で2時間撹拌し、次いで減圧下で濃縮乾固し、表題化合物(278mg、1.3mmol、収率92%、純度95%)をクリーム色の固体として得た。
UPLC/MS (方法3):m/z 169 (M+H)+, RT 0.16分。
DMF(14mL)中の2-(クロロメチル-d2)イミダゾ[1,2-a]ピリジン、HCl(278mg、1.36mmol)及びDIPEA(708μL、4.07mmol)の溶液を、アジ化ナトリウム(132mg、2.03mmol)で処理した。混合物を60℃に加熱し、2時間撹拌した。混合物を室温に冷却し、水(100mL)で希釈した。TBME(3x25mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、減圧下で濃縮した。クロマトグラフィー(12gカートリッジ、0~100%(3:1 EtOAc/EtOH)/イソヘキサン)による精製により、表題化合物(150mg、0.66mmol、収率49%、純度77%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 176 (M+H)+, RT 0.77分。
2-(アジドメチル-d2)イミダゾ[1,2-a]ピリジン(150mg、659μmol)及びトリフェニルホスフィン(208mg、791μmol)を、THF(8.0mL)及び水(0.8mL)に溶解した。混合物を50℃に加熱し、1時間撹拌した後、溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(102mg、0.65mmol、収率99%、純度95%)を白色の固体として得た。
DMSO-d6中の1H NMRは、生成物の構造と一致していた。
(3R,4R)-4-(((7-((1-(イミダゾ[1,2-a]ピリジン-2-イル)エチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-019)
1-(イミダゾ[1,2-a]ピリジン-2-イル)エタン-1-アミン(133mg、782μmol)を、EtOH(3.0mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(100mg、435μmol)及びDIPEA(0.38mL、2.17mmol)の溶液に添加した。反応混合物を90℃で1時間加熱した。反応混合物を真空中で濃縮した。
UPLC/MS (方法4):m/z 355 (M+H)+, RT 1.47分。
BOC無水物(136mg、623μmol)を、THF(2.5mL)中の5-クロロ-N-(1-(イミダゾ[1,2-a]ピリジン-2-イル)エチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(158mg、445μmol)及びDMAP(5.4mg、44.5μmol)の溶液に添加した。反応混合物を50℃で一晩撹拌した。さらなるBOC無水物(136mg、623μmol)を添加し、反応混合物を50℃で3時間撹拌した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(171mg、0.36mmol、収率80%、純度95%)を黄色の油状物として得た。
UPLC/MS (方法3):m/z 455 (M+H)+, RT 1.79分。
THF(3.2mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(1-(イミダゾ[1,2-a]ピリジン-2-イル)エチル)カルバメート(171mg、376μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(95mg、413μmol)及びtBuBrettPhos Pd G3 (32mg、37.6μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.49mL、489μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。室温で、水(15mL)及びEtOAc(25mL)を添加した。層を分離し、水性層をEtOAc(2x15mL)で抽出した。合わせた有機層を相分離器を通して濾過し、濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(168mg、0.24mmol、収率64%、純度93%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 649 (M+H)+, RT 1.68分。
塩化水素(ジオキサン中4M)(1.17mL、4.69mmol)を、ジオキサン(1.2mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(1-(イミダゾ[1,2-a]ピリジン-2-イル)エチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(160mg、234μmol)の溶液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(40mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(70mg、0.15mmol、収率63%、純度95%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法4):m/z 449 (M+H)+, RT 1.02分。
1H NMR (400 MHz, DMSO-d6) δ 8.49 (d,J = 6.8 Hz, 1H), 7.80 (d,J = 4.9 Hz, 1H), 7.62 (s, 1H), 7.52 (d,J = 9.1 Hz, 1H), 7.26 - 7.18 (m, 1H), 7.13 (d,J = 7.8 Hz, 1H), 6.85 (t,J = 6.7 Hz, 1H), 6.76 - 6.68 (m, 1H), 5.32 (d,J = 2.0 Hz, 1H), 5.31 - 5.23 (m, 1H), 4.87 - 4.81 (m, 1H), 3.60 - 3.43 (m, 1H), 3.27 - 3.17 (m, 1H), 3.08 - 2.98 (m, 1H), 2.99 - 2.86 (m, 2H), 2.82 - 2.73 (m, 1H), 2.35 - 2.25 (m, 1H), 2.16 (td,J = 10.8, 4.3 Hz, 1H), 1.66 (d,J = 6.6 Hz, 3H), 1.60 - 1.51 (m, 1H), 1.40 - 1.28 (m, 1H), 1.26 - 1.20 (m, 6H), 1.18 - 1.12 (m, 1H). 1H under water.
1-(イミダゾ[1,2-a]ピリジン-2-イル)エタン-1-アミン
臭化メチルマグネシウム(Et2O中3M)(1.71mL、5.13mmol)を、THF(10mL)中のイミダゾ[1,2-a]ピリジン-2-カルボアルデヒド(0.500g、3.42mmol)の溶液に-10℃で添加した。混合物をゆっくりと室温に温め、一晩撹拌した。水(50mL)を添加し、水性層をEtOAc(3x50mL)で抽出した。合わせた有機層を回収し、硫酸ナトリウムで乾燥させ、濾過して真空中で濃縮して、表題(350mg、2.1mmol、収率61%、純度96%)を白色の固体として得た。
UPLC/MS (方法3):m/z 163 (M+H)+, RT 0.15分。
塩化チオニル(675μL、9.25mmol)を、DCE(5.0mL)中の1-(イミダゾ[1,2-a]ピリジン-2-イル)エタン-1-オール(300mg、1.85mmol)の溶液に、室温で滴下添加した。混合物を45℃で3時間撹拌し、次いで減圧下で濃縮乾固し、表題化合物(300mg、1.4mmol、収率74%、純度82%)を無色の油状物として得た。
UPLC/MS (方法3):m/z 181 (M+H)+, RT 0.15分。
DMF(14mL)中の2-(1-クロロエチル)イミダゾ[1,2-a]ピリジン、HCl(200mg、921μmol)及びDIPEA(390μL、2.76mmol)の溶液を、アジ化ナトリウム(90mg、1.38mmol)で処理した。混合物を60℃に加熱し、6時間撹拌した。この混合物を室温に冷却し、水(40mL)及びブライン(60mL)で希釈した。TBME(3x50mL)及びEtOAc(50mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。クロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)による精製により、表題化合物(190mg、0.81mmol、収率88%、純度80%)を茶色の油状物として得た。
UPLC/MS (方法4):m/z 188 (M+H)+, RT 0.90分。
2-(1-アジドエチル)イミダゾ[1,2-a]ピリジン(190mg、913μmol)及びトリフェニルホスフィン(287mg、1.10mmol)を、THF(4.5mL)及び水(0.5mL)に溶解した。混合物を室温で1時間撹拌し、次いで50℃で1時間撹拌した後、溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(144mg、0.85mmol、収率93%、純度95%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 162 (M+H)+, RT 0.48分。
(3R,4R)-4-(((7-((ベンゾフラン-2-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-020)
ベンゾフラン-2-イルメタンアミン塩酸塩(100mg、0.547mmol)を、EtOH(1.9mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(105mg、0.456mmol)及びDIPEA(0.48mL、2.74mmol)の溶液に添加した。反応混合物を90℃で一晩加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~30%EtOAc/ヘプタン)による精製により、表題化合物(157mg、0.42mmol、収率91%、純度90%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 341 (M+H)+, RT 1.82分。
BOC無水物(109mg、0.498mmol)を、THF(8.0mL)中のN-(ベンゾフラン-2-イルメチル)-5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(157g、0.415mmol)及びDMAP(10mg、83μmol)の溶液に添加した。反応混合物を65℃で2時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(15mL)と水(30mL)に分配した。水性層をDCM(2x30mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~20%EtOAc/イソヘキサン)により精製し、表題化合物(164mg、0.37mmol、収率89%、純度99%)をクリーム色の固体として得た。
UPLC/MS (方法4):m/z 385 (M+H-tBu)+, RT 2.10分。
THF(3.6mL)中のtert-ブチル(ベンゾフラン-2-イルメチル)(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)カルバメート(164mg、0.372mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(94mg、0.409mmol)及び tBuBrettPhos Pd G3 (31.8mg、37.2μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.48mL、0.48mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。室温で、混合物をセライトを通して濾過し、EtOAc(15mL)ですすいだ。濾液を水(15mL)で洗浄し、水性層をEtOAc(3x20mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)による精製により、表題化合物(235mg、0.33mmol、収率89、純度90%)をオレンジ色の固体として得た。
UPLC/MS (方法4):m/z 635 (M+H)+, RT 1.96分。
塩化水素(ジオキサン中4M)(2.0mL、8.0mmol)を、ジオキサン(2.5mL)中のtert-ブチル(3R,4R)-4-(((7-((ベンゾフラン-2-イルメチル)(tert-ブトキシカルボニル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(233mg、0.367mmol)の懸濁液に添加した。反応混合物を35℃で2時間撹拌し、次いで、さらなる塩化水素(ジオキサン中4M)(0.92mL、3.67mmol)を添加した。反応混合物を35℃で2.5時間撹拌し、次いで真空中で濃縮した。
UPLC/MS (方法4):m/z 435 (M+H)+, RT 1.37分。
1H NMR (400 MHz, DMSO-d6) δ 7.81 (t, J = 6.3 Hz, 1H), 7.63 (s, 1H), 7.58 (dd, J = 7.5, 1.6 Hz, 1H), 7.53 (d, J = 8.0 Hz, 1H), 7.30 - 7.17 (m, 2H), 6.78 (s, 1H), 6.74 (t, J = 6.1 Hz, 1H), 5.37 (s, 1H), 5.28 - 5.20 (m, 1H), 4.62 (d, J = 6.1 Hz, 2H), 3.56 - 3.45 (m, 1H), 3.27 - 3.17 (m, 1H), 3.08 - 2.98 (m, 1H), 2.98 - 2.87 (m, 2H), 2.82 - 2.72 (m, 1H), 2.36 - 2.23 (m, 1H), 2.15 (dd, J = 11.5, 10.0 Hz, 1H), 1.62 - 1.52 (m, 1H), 1.39 - 1.29 (m, 1H), 1.23 (dd, J = 6.9, 4.7 Hz, 6H), 1.18 - 1.09 (m, 1H). 1H under water.
(3R,4R)-4-(((3-イソプロピル-7-((キノリン-3-イルメチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール (H-APPAMP-021)
キノリン-3-イルメタンアミン二塩酸塩(121mg、0.522mmol)を、EtOH(2.0mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(100mg、0.435mmol)及びDIPEA(0.68mL、3.92mmol)の溶液に添加した。反応混合物を90℃で一晩加熱した。反応混合物を真空中で濃縮し、残渣をDCM(20mL)と飽和NaHCO3水溶液(10mL)に分配した。有機層を飽和NaHCO3水溶液(3x10mL)で洗浄し、相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(80gカートリッジ、0~30%EtOAc/イソヘキサン)により精製することにより、表題化合物(109mg、0.29mmol、収率66%、純度93%)を黄色の固体として得た。
UPLC/MS (方法3):m/z 352 (M+H)+, RT 1.56分。
BOC無水物(80mg、0.368mmol)を、THF(6.0mL)中の5-クロロ-3-イソプロピル-N-(キノリン-3-イルメチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(108mg、0.307mmol)及びDMAP(7.5mg、61.4μmol)の溶液に添加した。反応混合物を65℃で2.5時間撹拌した。さらなるBOC無水物(34mg、0.154mmol)を添加し、反応混合物を65℃で1.5時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(15mL)と水(30mL)に分配した。水性層をDCM(2x30mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(143mg、0.29mmol、収率94%、純度91%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 452 (M+H)+, RT 1.91分。
THF(3.0mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)(キノリン-3-イルメチル)カルバメート(139mg、0.308mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(78mg、0.339mmol)及びtBuBrettPhos Pd G3(26.3mg、30.8μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(399μL、0.399mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1.5時間加熱した。
UPLC/MS (方法4):m/z 646 (M+H)+, RT 1.80分。
塩化水素(ジオキサン中4M)(0.90mL、3.60mmol)を、ジオキサン(2.6mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)(キノリン-3-イルメチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(116mg、0.18mmol)の懸濁液に添加した。反応混合物を35℃で3時間撹拌した。さらなる塩化水素(ジオキサン中4M)(0.23mL、0.90mmol)を添加し、反応混合物を35℃で1時間撹拌し、次いで真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(20mL)で洗浄し、生成物をMeOH中0.7M NH3(60mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(51mg、0.11mmol、収率71%、純度99%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法3):m/z 446 (M+H)+, RT 0.67分。
1H NMR (400 MHz, DMSO-d6) δ 8.96 (d,J = 2.2 Hz, 1H), 8.24 (s, 1H), 8.07 - 7.99 (m, 2H), 7.99 - 7.95 (m, 1H), 7.80 - 7.71 (m, 1H), 7.66 (s, 1H), 7.60 (ddd,J = 1.2, 6.8, 8.1 Hz, 1H), 6.66 (t,J = 6.1 Hz, 1H), 5.23 (s, 2H), 4.68 (d,J = 6.2 Hz, 2H), 3.59 - 3.41 (m, 1H), 3.22 - 3.13 (m, 1H), 3.05 - 2.84 (m, 3H), 2.79 - 2.70 (m, 1H), 2.30 - 2.21 (m, 1H), 2.18 - 2.05 (m, 1H), 1.59 - 1.46 (m, 1H), 1.37 - 1.26 (m, 1H), 1.23 (dd,J = 5.3, 6.9 Hz, 6H), 1.17 - 1.04 (m, 1H). 1H under water.
(3R,4R)-4-(((3-シクロプロピル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-022)
(8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、2HCl(101mg、0.432mmol)を、EtOH(2.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(83.0mg、0.364mmol)及びDIPEA(0.57mL、3.28mmol)の溶液に添加した。反応混合物を65℃で1時間加熱した。反応混合物を真空中で濃縮し、残渣をDCM(20mL)で希釈し、次いで溶液を飽和NaHCO3水溶液(20mL)で洗浄した後、ブライン(20mL)で洗浄した。有機層を相分離器を通して濾過し、減圧下で濃縮し、表題化合物(129mg、0.36mmol、収率99%、純度99%)をオフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 353 (M+H)+, RT 1.37分。
BOC無水物(94.50mg、0.433mmol)を、THF(10mL)中の5-クロロ-3-シクロプロピル-N-((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(128.6mg、0.361mmol)及びDMAP(8.8mg、0.072mmol)の溶液に添加した。反応混合物を65℃で3時間撹拌し、次いで、さらなるBOC無水物(94.50mg、0.433mmol)。反応混合物を65℃で1時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)で希釈した。この溶液を水(15mL)で洗浄し、次いでブライン(15mL)で洗浄した。有機層を相分離器を通して濾過し、次いで減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/ヘプタン)により精製し、表題化合物(150mg、0.33mmol、収率91%、純度99%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 452 (M+H)+, RT 1.73分。
THF(3.2mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(150.2mg、0.332mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(84.02mg、0.3645mmol)及びtBuBrettPhos Pd G3(28.33mg、0.033mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.37g、0.431mL、431.1μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1.5時間加熱した。室温で、反応混合物をセライトを通して濾過し、EtOAc(15mL)で洗浄した。濾液を水で希釈し、水性層をEtOAc(3x20mL)で抽出し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%(3:1 EtOAc/EtOH)/イソヘキサン)により精製し、表題化合物を(221mg、0.30mmol、収率92%、純度89%)をベージュ色の固体として得た。
UPLC/MS (方法5):m/z 647 (M+H)+, RT 1.62分。
TFA(0.6mL)を、DCM(2.4mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(77mg、0.115mmol)の懸濁液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(42mg、90μmol、収率78%、純度95%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、白色の固体として得た。
UPLC/MS (方法5):m/z 447 (M+H)+, RT 1.09分。
1H NMR (400 MHz, DMSO-d6) δ 8.32 (d,J = 6.7 Hz, 1H), 7.73 (s, 1H), 7.64 (t,J = 6.1 Hz, 1H), 7.52 (s, 1H), 7.01 (dt,J = 6.9, 1.3 Hz, 1H), 6.78 - 6.69 (m, 2H), 5.36 - 5.30 (m, 1H), 5.27 (s, 1H), 4.56 (d,J = 5.8 Hz, 2H), 3.57 - 3.46 (m, 1H), 3.25 - 3.15 (m, 1H), 3.10 - 2.97 (m, 1H), 2.91 (dd,J = 11.6, 4.5 Hz, 1H), 2.83 - 2.73 (m, 1H), 2.47 (s, 3H), 2.35 - 2.24 (m, 1H), 2.20 - 2.12 (m, 1H), 1.78 - 1.67 (m, 1H), 1.61 - 1.51 (m, 1H), 1.40 - 1.26 (m, 1H), 1.22 - 1.11 (m, 1H), 0.79 - 0.73 (m, 2H), 0.70 - 0.59 (m, 2H). 1H under water.
(3R,4R)-4-(((3-イソプロピル-7-(((3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-023)
(3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(139mg、646μmol)を、EtOH(6.0mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(149mg、646μmol)及びDIPEA(0.84mL、4.84mmol)の溶液に添加した。反応混合物を60℃で3時間加熱した。反応混合物を真空中で濃縮した。室温で水(50mL)を添加し、混合物をDCM(3x25mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、減圧下で濃縮し、表題化合物(246mg、487μmol、収率76%、純度81%)を白色の固体として得た。
UPLC/MS (方法4):m/z 409 (M+H)+, RT 0.83分。
BOC無水物(158mg、166μL、722μmol)を、THF(6.0mL)中の5-クロロ-3-イソプロピル-N-((3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(246mg、602μmol)及びDMAP(14.7mg、120μmol)の溶液に添加した。反応混合物を室温で3時間撹拌した。
UPLC/MS(方法4):m/z 509 (M+H)+, RT 1.99分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(100mg、196μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(45.3mg、196μmol)及びtBuBrettPhos Pd G3(16.8mg、19.6μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(255μL、255μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に3時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、次いでカラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製した後、RPフラッシュC18 (12gカートリッジ、5~100%MeCN/10mM重炭酸アンモニウム)上でさらに精製し、表題化合物(68mg、92μmol、収率47%、純度95%)を白色の固体として得た。
UPLC/MS (方法5):m/z 704 (M+H)+, RT 0.85分。
TFA(0.6mL)を、DCM(2.4mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(68mg、96.8μmol)の溶液に添加した。反応混合物を室温で6時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(20mL)で洗浄し、生成物をMeOH中0.7M NH3(20mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(20mg、39μmol、収率40%、純度98%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、白色の固体として得た。
UPLC/MS (方法3):m/z 504 (M+H)+, RT 0.78分。
1H NMR (400 MHz, DMSO-d6) δ 8.52 (d,J = 6.9 Hz, 1H), 7.83 - 7.78 (m, 1H), 7.64 (s, 1H), 7.55 (m, 1H), 7.49 (t,J = 5.7 Hz, 1H), 7.20 (m, 1H), 6.78 - 6.70 (m, 1H), 5.31 (s, 1H), 5.29 - 5.20 (m, 1H), 4.72 (d,J = 5.3 Hz, 2H), 3.59 - 3.47 (m, 1H), 3.25 - 3.19 (m, 1H), 3.08 - 2.87 (m, 3H), 2.81 - 2.74 (m, 1H), 2.34 - 2.25 (m, 1H), 2.15 (dd,J = 11.6, 9.9 Hz, 1H), 1.60 - 1.53 (m, 1H), 1.40 - 1.29 (m, 1H), 1.24 (dd,J = 6.9, 4.3 Hz, 6H), 1.21 - 1.12 (m, 1H). 1H under water.
(3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
N2下で、トリフルオロメチルトリメチルシラン(1.50g、1.6mL、10.5mmol)を、MeCN(15mL)中のエチルイミダゾ[1,2-a]ピリジン-2-カルボキシレート(500mg、2.63mmol)、ヨードベンゼンジアセテート(1.69g、5.26mmol)及びフッ化セシウム(1.60g、10.5mmol)の混合物に添加した。反応混合物を30℃に3時間加熱し、次いで減圧下で濃縮乾固した。カラム(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(203mg、680μmol、収率26%、純度87%)を白色の固体として得た。
UPLC/MS (方法5):m/z 259 (M+H)+, RT 1.17分。
LiAlH4(THF中2M)(0.393mL、786μmol)を、THF(8.0mL)中のエチル3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-カルボキシレート(203mg、786μmol)の溶液に、0℃で添加した。反応混合物を室温に温め、1時間撹拌した。0℃において、飽和NH4Cl水溶液(10mL)及び水(10mL)を添加した。水性層をDCM(3x20mL)で抽出し、合わせた有機層をMgSO4で乾燥させ、濾過し、減圧下で濃縮した。カラム(12gカートリッジ、0~100%(3:1 EtOAc/EtOH)/イソヘキサン)により精製し、表題化合物(102mg、0.45mmol、収率58%、純度96%)を白色の固体として得た。
UPLC/MS (方法5):m/z 217 (M+H)+, RT 0.81分。
塩化チオニル(203μL、2.78mmol)を、DCM(5.0mL)中の(3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタノール(250mg、1.11mmol)の溶液に、0℃で滴下添加した。
UPLC/MS (方法5):m/z 235 (M-OH)+, RT 1.19分。
DMF(4.0mL)中の2-(クロロメチル)-3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-1-イウムクロリド(250mg、922μmol)及びDIPEA(0.48mL、2.77mmol)の溶液を、アジ化ナトリウム(90mg、1.38mmol)で処理した。混合物を50℃に加熱し、2時間撹拌した。混合物を室温に冷却し、水(10mL)及びブライン(10mL)で希釈した。DCM(3x20mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、減圧下で濃縮した。カラム(12gカートリッジ、0~100%EtOAc/シクロヘキサン)により精製し、表題化合物(209mg、0.75mmol、収率81%、純度86%)を無色の油状物として得た。
UPLC/MS (方法3):m/z 242 (M+H)+, RT 1.20分。
2-(アジドメチル)-3-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン(209mg、780μmol)及びトリフェニルホスフィン(245mg、936μmol)を、ジオキサン(4.0mL)及び水(0.4mL)に溶解した。混合物を50℃で一晩撹拌し、その後溶媒を真空中で除去した。
UPLC/MS (方法5):m/z 216 (M+H)+, RT 0.82分。
(3R,4R)-4-(((7-(((3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-024)
(3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(52mg、0.22mmol)を、EtOH(2.2mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(61mg、0.27mmol)及びDIPEA(0.29mL、1.70mmol)の溶液に添加した。反応混合物を60℃で18時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~50%(3:1 EtOAc/EtOH)/イソヘキサン)により精製し、表題化合物(74mg、155μmol、収率70%、純度80%)をピンク色の固体として得た。
UPLC/MS (方法5):m/z 381 (M+H)+, RT 1.63分。
BOC無水物(51mg、0.23mmol)を、THF(1.9mL)中の5-クロロ-N-((3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(74mg、155μmol)及びDMAP(5mg、40μmol)の溶液に添加した。反応混合物を室温で3時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(74mg、154μmol、収率99%、純度99%)を白色の固体として得た。
UPLC/MS (方法5):m/z 783 (M+H)+, RT 1.89分。
THF(3.0mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(74.0mg、0.154mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(40.0mg、0.170mm0l)及びtBuBrettPhos Pd G3(13.9 mh、0.015mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.200mL、0.200mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に16時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、その後RPフラッシュC18(4gカートリッジ、15~100%MeCN/10mM重炭酸アンモニウム)上でさらに精製し、表題化合物(60mg、89μmol、収率58%、純度99%)を白色の固体として得た。
UPLC/MS (方法5):m/z 675 (M+H)+, RT 1.77分。
TFA(0.3mL)を、DCM(1.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(60mg、89μmol)の溶液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。
UPLC/MS (方法5):m/z 475 (M+H)+, RT 1.25分。
1H NMR (400 MHz, DMSO-d6) δ 8.43 (d,J = 6.8 Hz, 1H), 7.61 (s, 1H), 7.54 (d, J = 9.1, 1H), 7.26 (m, 2H), 6.98 (td,J = 6.8, 1.2 Hz, 1H), 6.85 - 6.76 (m, 1H), 5.43 - 5.36 (m, 2H), 4.58 (d,J = 5.1 Hz, 2H), 3.61 - 3.51 (m, 1H), 3.27 - 3.20 (m, 1H), 3.14 - 3.06 (m, 1H), 3.00 - 2.90 (m, 2H), 2.88 - 2.79 (m, 1H), 2.41 - 2,31 (m, 1H), 2.26 - 2.17 (m, 1H), 1.96 - 1.87 (m, 1H), 1.65 - 1.57 (m, 1H), 1.44 - 1.34 (m, 1H), 1.28 - 1.17 (m, 7H), 1.15 - 1.08 (m, 2H), 0.74 - 0.67 (m, 2H). 1H under water.
(3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン合成
水(4.0mL)中のリン酸三カリウム(1.56g、7.35mmol)の溶液を、ジオキサン(20mL)中の3-ヨードイミダゾ[1,2-a]ピリジン-2-カルボアルデヒド(500mg、1.84mmol)、シクロプロパンボロン酸(474mg、5.51mmol)及びPdCl2(dppf)-CH2Cl2付加物(300mg、368μmol)の溶液に添加した。N2を、反応混合物を通して10分間バブリングし、次いで反応混合物を80℃で20時間加熱した。室温で、混合物をセライトを通して濾過し、DCM(25mL)ですすいだ。水(50mL)を濾液に添加し、層を分離し、水性層をDCM(2x25mL)で抽出した。合わせた有機画分をMgSO4で乾燥させ、真空中で濃縮した。カラム(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(111mg、513μmol、収率28%、純度90%)を白色の固体として得た。
UPLC/MS (方法5):m/z 187 (M+H)+, RT 0.80分。
(S)-2-メチルプロパン-2-スルフィンアミド(86.7mg、715μmol)、次いでチタニウム(IV)プロパン-2-オレート(0.53mL、1.79mmol)を、DCM(6.0mL)中の3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-カルボアルデヒド(111mg、596μmol)の溶液に0℃で添加した。反応混合物を40℃で18時間撹拌した。ブライン(50mL)及びセライトを、反応混合物に撹拌しながら添加した。混合物を、セライトのパッドを通して充填し(filled)、DCM(100mL)で洗浄した。有機層を濾液から回収し、水性層をDCM(2x25mL)でさらに抽出した。合わせた有機層をMgSO4で乾燥させ、次いで減圧下で濃縮した。カラム(12gカートリッジ、0~100%(3:1 EtOAc/EtOH)/シクロヘキサン)により精製し、表題化合物(139mg、0.39mmol、収率65%、純度81%)を黄色の油状物として得た。
UPLC/MS (方法5):m/z 290 (M+H)+, RT 1.08分。
水素化ホウ素ナトリウム(18mg、476μmol)を、MeOH(2.4mL)中のS,E)-N-((3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチレン)-2-メチルプロパン-2-スルフィンアミド(139mg、389μmol)の溶液に、0℃で添加した。反応物を室温に温め、1時間撹拌した。水(30mL)及びDCM(25mL)を添加した。層を分離し、水性層をDCM(2x25mL)でさらに抽出した。合わせた有機層を相分離器を通して濾過し、減圧下で濃縮し、表題化合物(139mg、382μmol、収率98%、純度80%)をピンク色の固体として得た。
UPLC/MS (方法4):m/z 292 (M-OH)+, RT 1.05分。
塩化水素(MeOH中1.25M)(0.9mL、1.14mmol)を、MeOH(1.0mL)中の(S)-N-((3-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)-2-メチルプロパン-2-スルフィンアミド(139mg、382μmol)の溶液に添加した。反応物を室温で2時間撹拌し、次いで、さらなる塩化水素(MeOH中1.25M)(0.9mL、1.14mmol)及び混合物を1時間撹拌した後、減圧下で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(20mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(53mg、226μmol、収率59%、純度80%)を黄色の油状物として得た。
DMSO-d6中の1H NMRは、生成物の構造と一致していた。
(3R,4R)-4-(((3-シクロプロピル-7-(((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-025)
(5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、2HCl(111mg、0.474mmol)を、EtOH(1.5mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(90mg、0.395mmol)及びDIPEA(0.62mL、3.55mmol)の溶液に添加した。反応混合物を65℃で1.5時間加熱した。反応混合物を真空中で濃縮した。残渣をDCM(15mL)中で希釈し、飽和NaHCO3水溶液(15mL)及びブライン(15mL)で洗浄した。有機層を相分離器を通して濾過し、減圧下で濃縮し、表題化合物(118mg、0.33mmol、収率83%、純度98%)を灰色の固体として得た。
UPLC/MS (方法3):m/z 353 (M+H)+, RT 1.36分。
BOC無水物(87mg、0.398mmol)を、THF(6.5mL)中の5-クロロ-3-シクロプロピル-N-((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(117.0mg、331.6mmol)及びDMAP(8.1mg、66μmol)の溶液に添加した。反応混合物を65℃で1時間撹拌し、次いでBOC無水物(87mg、0.398mmol)及びDMAP(8.1mg、66μmol)を再充填し、65℃で1時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(15mL)中で希釈した。有機層をブライン(3x10mL)で洗浄し、相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(135mg、0.29mmol、収率87%、純度97%)を緑色の固体として得た。
UPLC/MS (方法3):m/z 453 (M+H)+, RT 1.71分。
THF(2.9mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(136mg、0.30mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(83mg、360μmol)及びtBuBrettPhos Pd G3(26mg、30μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.39mL、390μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。室温で、混合物をセライトを通して濾過し、EtOAc(15mL)で洗浄した。濾液を水(10mL)で分配し、水性層をEtOAc(3x20mL)で再抽出した。合わせた有機層をブライン(10mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(163mg、0.22mmol、収率74%、純度88%)を茶色の油状物として得た。
UPLC/MS (方法3):m/z 647 (M+H)+, RT 1.22分。
TFA(0.5mL)を、DCM(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(163mg、252μmol)の溶液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(60mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(81mg、0.18mmol、収率71%、純度98%)を、Et2Oからトリチュレーションし、真空下に40℃で一晩乾燥させた後、ベージュ色の固体として得た。
UPLC/MS (方法5):m/z 447 (M+H)+, RT 1.42分。
1H NMR (400 MHz, DMSO-d6) δ 7.66 (s, 1H), 7.56 (t,J = 6.0 Hz, 1H), 7.51 (s, 1H), 7.42 (d,J = 9.0 Hz, 1H), 7.21 (dd,J = 9.1, 6.8 Hz, 1H), 6.79 - 6.73 (m, 2H), 5.44 - 5.37 (m, 1H), 5.32 (s, 1H), 4.57 (d,J = 5.9 Hz, 2H), 3.58 - 3.46 (m, 1H), 3.26 - 3.17 (m, 1H), 3.12 - 3.03 (m, 1H), 2.94 (dd,J = 11.5, 4.5 Hz, 1H), 2.87 - 2.78 (m, 1H), 2.55 (s, 3H), 2.40 - 2.31 (m, 1H), 2.27 - 2.16 (m, 1H), 1.76 - 1.67 (m, 1H), 1.63 - 1.55 (m, 1H), 1.42 - 1.32 (m, 1H), 1.25 - 1.11 (m, 1H), 0.80 - 0.71 (m, 2H), 0.69 - 0.58 (m, 2H). 1H under water.
(3R,4R)-4-(((3-エチル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-026)
(8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、HCl(96.1mg、486μmol)を、EtOH(2.0mL)中の5,7-ジクロロ-3-エチルピラゾロ[1,5-a]ピリミジン(100mg、463μmol)及びDIPEA(0.56mL、3.24mmol)の溶液に添加した。反応混合物を50℃で18時間加熱した。反応混合物を真空中で濃縮した。
UPLC/MS (方法5):m/z 341 (M+H)+, RT 1.22分。
BOC無水物(98mg、451μmol)を、THF(4.0mL)中の5-クロロ-3-エチル-N-((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(128mg、376μmol)及びDMAP(9mg、75μmol)の溶液に添加した。反応混合物を室温で18時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%(3:1 EtOAc/EtOH)/イソヘキサン)により精製し、表題化合物(138mg、0.30mmol、収率80%、純度96%)を褐色の固体として得た。
UPLC/MS (方法5):m/z 441 (M+H)+, RT 1.61分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-エチルピラゾロ[1,5-a]ピリミジン-7-イル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(138mg、300μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(83mg、361μmol)及びtBuBrettPhos Pd G3(0.62g、0.72mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(391μL、391μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に18時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(141mg、222μmol、収率74%、純度98%)を白色の固体として得た。
UPLC/MS (方法3):m/z 635 (M+H)+, RT 1.62分。
TFA(0.5mL)を、ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-エチルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(140mg、221μmol)の溶液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(71mg、160μmol、収率73%、純度98%)を得た。
UPLC/MS (方法5):m/z 435 (M+H)+, RT 1.02分。
1H NMR (400 MHz, DMSO-d6) δ 8.32 (d, J = 6.5 Hz, 1H), 7.74 (s, 1H), 7.69 - 7.63 (m, 2H), 7.01 (dt,J = 6.9, 1.3 Hz, 1H), 6.71 - 6.79 (m, 2H), 5.46 - 5.37 (m, 1H), 5.27 (s, 1H), 4.57 (d,J = 6.0 Hz, 2H), 3.49 - 3.60 (m, 1H), 3.11 - 3.20 (m, 1H), 3.06 - 2.95 (m, 1H), 2.89 (dd,J = 11.5, 4.6 Hz, 1H), 2.81 - 2.73 (m, 1H), 2.47 (s, 3H), 2.24 - 2.34 (m, 1H), 2.19 - 2.10 (m, 1H), 1.57 - 1.48 (m, 1H), 1.36 - 1.25 (m, 1H), 1.11 - 1.20 (m, 4H)。DMSO下で1CH2. 1H under water.
(3R,4R)-4-(((3-シクロプロピル-7-(((5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-027)
(5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(64mg、0.34mmol)を、EtOH(3.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(86mg、0.38mmol)及びDIPEA(0.42mL、2.4mmol)の溶液に添加した。反応混合物を50℃で20時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(105mg、0.27mmol、収率78%、純度94%)を褐色の固体として得た。
UPLC/MS (方法5):m/z 369 (M+H)+, RT 1.35分。
BOC無水物(70mg、321μmol)を、THF(3.0mL)中の5-クロロ-3-シクロプロピル-N-((5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(105mg、268μmol)及びDMAP(6.5mg、54μmol)の溶液に添加した。反応混合物を室温で1時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(120mg、256μmol、収率95%、純度99%)を白色の固体として得た。
UPLC/MS (方法5):m/z 469 (M+H)+, RT 0.81分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(140mg、299μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(83mg、358μmol)及びtBuBrettPhos Pd G3(25mg、29.9μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(388μL、388μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に18時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(167mg、0.21mmol、収率69%、純度82%)を白色の固体として得た。
UPLC/MS (方法5):m/z 663 (M+H)+, RT 1.61分。
塩化水素(ジオキサン中4M)(1.04mL、4.16mmol)を、ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(168mg、208μmol)の溶液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(62mg、0.13mmol、収率61%、純度95%)を得た。
UPLC/MS (方法5):m/z 463 (M+H)+, RT 1.04分。
1H NMR (400 MHz, DMSO-d6) δ 7.61 (t,J = 6.1 Hz, 1H), 7.56 (s, 1H), 7.52 (s, 1H), 7.29 (dd,J = 9.0, 7.5 Hz, 1H), 7.15 (d,J = 9.0 Hz, 1H), 6.77 - 6.71 (m, 1H), 6.34 (d,J = 7.4 Hz, 1H), 5.36 - 5.32 (m, 1H), 5.30 (s, 1H), 4.55 (d,J = 5.9 Hz, 2H), 4.06 (s, 3H), 3.57 - 3.49 (m, 1H), 3.26 - 3.15 (m, 1H), 3.09 - 2.99 (m, 1H), 2.92 (dd,J = 11.5, 4.6 Hz, 1H), 2.83 - 2.76 (m, 1H), 2.36 - 2.26 (m, 1H), 2.17 (dd,J = 11.6, 9.9 Hz, 1H), 1.78 - 1.66 (m, 1H), 1.61 - 1.53 (m, 1H), 1.36 - 1.29 (m, 1H), 1.22 - 1.11 (m, 1H), 0.82 - 0.72 (m, 2H), 0.76 - 0.59 (m, 2H). 1H under water.
(5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
IPA(2.0mL)及び水(2.0mL)中の6-メトキシピリジン-2-アミン(400mg、3.22mmol)及びエチル3-ブロモ-2-オキソプロパノエート(0.81mL、6.44mmol)を、マイクロ波照射下に80℃で1時間加熱した。反応混合物を水(50mL)で希釈し、DCM(3x25mL)で抽出した。合わせた有機画分をMgSO4で乾燥させ、濾過し、次いで真空下で濃縮した。カラムクロマトグラフィー(40gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(280mg、1.3mmol、収率39%、純度99%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 221 (M+H)+, RT 0.93分。
水素化ホウ素リチウム(THF中2M)(0.63mL、1.26mmol)を、THF(6.0mL)中のエチル5-メトキシイミダゾ[1,2-a]ピリジン-2-カルボキシレート(280mg、1.26mmol)の溶液に0℃で添加した。反応混合物を一晩室温に温めた。0℃において、水(5mL)、飽和NH4Cl水溶液(10mL)を添加した。水性層(aqueous)をDCM(3x20mL)で抽出し、合わせた有機層をMgSO4で乾燥させ、濾過して減圧下で濃縮した。カラム(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(120mg、0.61mmol、収率49%、純度91%)を白色の固体として得た。
UPLC/MS (方法5):m/z 179 (M+H)+, RT 0.62分。
塩化チオニル(112μL、1.53mmol)を、DCM(7.0mL)中の(5-メトキシイミダゾ[1,2-a]ピリジン-2-イル)メタノール(120mg、613μmol)の溶液に、0℃で滴下添加した。混合物を0℃で2時間撹拌した。減圧下で濃縮乾固し、表題化合物(142mg、0.60mmol、収率98%、純度99%)をオフホワイト色の固体として得た。
DMSO-d6中の1H NMRは生成物の構造と一致していた。
DMF(3.0mL)中の2-(クロロメチル)-5-メトキシイミダゾ[1,2-a]ピリジン、HCl(142mg、597μmol)及びDIPEA(0.31mL、1.79mmol)の溶液を、アジ化ナトリウム(58mg、0.90mmol)で処理した。混合物を50℃に加熱し、2時間撹拌した。混合物を室温に冷却し、水(10mL)及びブライン(10mL)で希釈し、その後TBME(3x20mL)で抽出し、次いでEtOAc(3x20mL)で抽出した。合わせた有機層をブライン(4x20mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラム(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(91mg、0.37mmol、収率62%、純度83%)を白色の固体として得た。
UPLC/MS (方法5):m/z 205 (M+H)+, RT 0.94分。
2-(アジドメチル)-5-メトキシイミダゾ[1,2-a]ピリジン(91mg、0.45mmol)及びトリフェニルホスフィン(0.14g、0.54mmol)を、THF(1.8mL)及び水(0.2mL)に溶解した。混合物を室温で一晩撹拌した後、溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(64mg、0.34mmol、収率77%、純度95%)を白色の固体として得た。
UPLC/MS (方法5):m/z 178 (M+H)+, RT 0.64分。
(3R,4R)-4-(((3-シクロプロピル-7-(((6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-028)
(6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メタンアミン(130mg、691μmol)を、EtOH(3.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(158mg、691μmol)及びDIPEA(0.84mL、4.83mmol)の溶液に添加した。反応混合物を50℃で2時間加熱した。反応混合物を真空中で濃縮し、表題化合物(449mg、0.69mmol、収率99%、純度58%)を茶色の固体として得た。
UPLC/MS (方法5):m/z 380 (M+H)+, RT 1.45分。
BOC無水物(129mg、592μmol)を、THF(5.0mL)中の5-クロロ-3-シクロプロピル-N-((6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(206mg、494μmol)及びDMAP(12.1mg、99μmol)の溶液に添加した。反応混合物を室温で3時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(231mg、0.46mmol、収率93%、純度95%)を茶色の固体として得た。
UPLC/MS (方法5):m/z 480 (M+H)+, RT 1.83分。
THF(5.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メチル)カルバメート(254mg、529μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(146mg、635μmol)及びtBuBrettPhos Pd G3(45mg、52.9μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(688μL、688μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に72時間加熱した。反応物を減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(230mg、0.32mmol、収率61%、純度94%)を茶色の固体として得た。
UPLC/MS (方法4):m/z 674 (M+H)+, RT 1.72分。
塩化水素(ジオキサン中4M)(1.71mL、6.83mmol)を、ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(230mg、341μmol)の溶液に添加した。反応混合物を35℃で4時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(10mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(145mg、0.30mmol、収率87%、純度97%)を、Et2Oからトリチュレーションし、真空下に40℃で一晩乾燥させた後で得た。
UPLC/MS (方法5):m/z 475 (M+H)+, RT 1.14分。
1H NMR (400 MHz, DMSO-d6) δ 7.98 (s, 1H), 7.92 (d,J = 9.4 Hz, 1H), 7.61 (t,J = 6.1 Hz, 1H), 7.51 (s, 1H), 7.08 (d,J = 9.4 Hz, 1H), 6.77 (t,J = 6.0 Hz, 1H), 5.47 - 5.42 (m, 1H), 5.30 (s, 1H), 4.55 (d,J = 5.9 Hz, 2H), 3.59 - 3.47 (m, 1H), 3.28 - 3.20 (m, 1H), 3.20 - 3.05 (m, 1H), 2.97 (dd,J = 11.6, 4.5 Hz, 1H), 2.90 - 2.82 (m, 1H), 2.44 - 2.34 (m, 1H), 2.25 (dd,J = 11.6, 10.0 Hz, 1H), 2.21 - 2.11 (m, 1H), 1.77 - 1.66 (m, 1H), 1.65 - 1.57 (m, 1H), 1.48 - 1.30 (m, 1H), 1.49 - 1.11 (m, 1H), 1.11 - 1.01 (m, 2H), 1.01 - 0.92 (m, 2H), 0.81 - 0.72 (m, 2H), 0.72 - 0.59 (m, 2H). 1H under water.
(6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メタンアミン
ジオキサン(10mL)中のエチル6-クロロイミダゾ[1,2-b]ピリダジン-2-カルボキシレート(400mg、1.77mmol)、フッ化セシウム(1.21g、7.98mmol)、PdCl2(dtbpf)(116mg、177μmol)、シクロプロピルボロン酸(685mg、7.98mmol)の混合物を、N2で10分間脱気した。次いで、混合物を60℃に5.5時間加熱し、その後減圧下で濃縮乾固した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(400mg、1.6mmol、収率93%、純度95%)を黄色の固体として得た。
UPLC/MS (方法3):m/z 232 (M+H)+, RT 1.13分。
水素化ジイソブチルアルミニウム(DCM中1M)(4.32mL、4.32mmol)を、THF(20mL)中のエチル6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-カルボキシレート(400mg、1.73mmol)の溶液に-10℃で添加した。反応混合物を室温に温め、2時間撹拌した。0℃において、MeOH(10mL)、その後水(10mL)及び1M HCl水溶液(10mL)を添加した。混合物を30分間勢いよく撹拌し、酢酸エチル(3x35mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、相分離器を通して濾過し、真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(220mg、1.10mmol、収率66%、純度98%)を茶色の油状物として得た。
UPLC/MS (方法3):m/z 190 (M+H)+, RT 0.44分。
塩化チオニル(434μL、5.95mmol)を、DCE(5.0mL)中の(6-シクロプロピルイミダゾ[1,2-b]ピリダジン-2-イル)メタノール(225mg、1.19mmol)の溶液に添加した。反応混合物を45℃で1時間撹拌した。減圧下で濃縮乾固し、表題化合物(290mg、1.1mmol、収率95%、純度95%)を緑色の固体として得た。
UPLC/MS (方法5):m/z 209 (M+H)+, RT 1.00分。
DMF(5.0mL)中の2-(クロロメチル)-6-シクロプロピルイミダゾ[1,2-b]ピリダジン、HCl(290mg、1.19mmol)及びDIPEA(0.62mL、3.56mmol)の溶液を、アジ化ナトリウム(116mg、1.78mmol)で処理した。混合物を50℃に加熱し、2時間撹拌した。混合物を室温に冷却し、減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(155mg、0.67mmol、収率57%、純度93%)を無色の油状物として得た。
UPLC/MS (方法5):m/z 216 (M+H)+, RT 1.10分。
2-(アジドメチル)-6-シクロプロピルイミダゾ[1,2-b]ピリダジン(155mg、673μmol)及びトリフェニルホスフィン(212mg、807μmol)を、THF(3.6mL)及び水(0.4mL)に溶解した。混合物を室温で一晩撹拌し、その後溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(130mg、0.66mmol、収率98%、純度95%)を白色の固体として得た。
UPLC/MS (方法5):m/z 189 (M+H)+, RT 0.76分。
(3R,4R)-4-(((3-シクロブチル-7-(((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-029)
(8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン、2HCl(1.98g、8.47mmol)を、EtOH(38mL)中の5,7-ジクロロ-3-ヨードピラゾロ[1,5-a]ピリミジン(2.80g、8.47mmol)及びDIPEA(4.4mL、25.4mmol)の溶液に添加した。反応混合物を85℃で一晩加熱した。室温で、沈殿した固体を濾過により回収し、EtOH(100mL)ですすいで、表題化合物(3.57g、8.03mmol、収率94%、純度98%)をベージュ色の固体として得た。
UPLC/MS (方法5):m/z 439 (M+H)+, RT 1.77分。
BOC無水物(1.74g、7.99mmol)を、THF(23mL)及びDMF(23mL)中の5-クロロ-3-ヨード-N-((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(2.92g、6.66mmol)及びDMAP(81mg、0.66mmol)の溶液に添加した。反応混合物を50℃で1.5時間撹拌した。室温で水(20mL)を添加し、結果として得られた固体を濾過により回収し、その後水(25mL)及びTBME(25mL)ですすぎ、表題化合物(3.1g, 5.68mmol、収率85%、純度99%)を、真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 539 (M+H)+, RT 2.24分。
無水NMP(11mL)中のtert-ブチル(5-クロロ-3-ヨードピラゾロ[1,5-a]ピリミジン-7-イル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(1.00g、1.86mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(1.71g、7.42mmol)及びDIPEA(1.29mL、7.42mmol))の溶液を、N2で脱気し、次いで110℃で2時間加熱した。反応混合物を0℃で冷却し、水(30mL)を添加した。固体を濾過により回収し、さらなる水(10mL)ですすぎ、その後減圧下に40℃で乾燥させて、表題化合物(1.28g、1.6mmol、収率87%、純度92%)を淡色の固体として得た。
UPLC/MS (方法5):m/z 733 (M+H)+, RT 2.06分。
N2下に、臭化シクロブチル亜鉛(II)(THF中0.38M)(文献の手順に従って調製した)(3.59mL、1.37mmol)を、THF(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-ヨードピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(200mg、273μmol)、XPhos Pd G3(8mg、9.28μmol)の溶液に滴下添加した。反応混合物を室温で18時間撹拌し、次いで水(10mL)でクエンチし、DCM(3x10mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、濾過し、その後減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、その後RP分取HPLC(25~100%MeCN/水中0.1%NH3)によりさらに精製し、表題化合物(19mg、29μmol、収率11%、純度99%)を白色の固体として得た。
UPLC/MS (方法3):m/z 662 (M+H)+, RT 1.34分。
TFA(0.10mL)を、DCM(0.4mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((8-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロブチルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(19mg、29μmol)の溶液に添加した。反応混合物を室温で16時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(10mg、21μmol、収率72%、純度95%)を得た。
UPLC/MS (方法5):m/z 461 (M+H)+, RT 1.82分。
1H NMR (400 MHz, DMSO-d6) δ 8.32 (d,J = 6.7 Hz, 1H), 7.75 (d,J = 4.9 Hz, 2H), 7.66 (t,J = 6.2 Hz, 1H), 7.02 (dt,J = 6.8, 1.2 Hz, 1H), 6.78 - 6.69 (m, 2H), 5.32 - 5.25 (m, 2H), 4.58 (d,J = 6.0 Hz, 2H), 3.59 - 3.42 (m, 2H), 3.24 - 3.14 (m, 1H), 3.07 - 2.96 (m, 1H), 2.90 (dd,J = 11.5, 4.5 Hz, 1H), 2.82 - 2.72 (m, 1H), 2.48 (s, 3H), 2.34 - 2.11 (m, 6H), 1.97 - 1.78 (m, 2H), 1.59 - 1.50 (m, 1H), 1.38 - 1.28 (m, 1H), 1.21 - 1.07 (m, 1H). 1H under water.
(3R,4R)-4-(((3-シクロプロピル-7-(((5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-030)
(5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(90mg、481μμmol)を、EtOH(3.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(110mg、481μmol)及びDIPEA(0.59mL、3.36mmol)の溶液に添加した。反応混合物を50℃で5時間加熱した。反応混合物を真空中で濃縮し、表題化合物(325mg、0.48mmol、収率99%、純度56%)を黄色の液体として得た。
UPLC/MS (方法5):m/z 379 (M+H)+, RT 1.48分。
BOC無水物(126mg、0.58mmol)を、THF(5.0mL)中の5-クロロ-3-シクロプロピル-N-((5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(325mg、0.48mmol)及びDMAP(12mg、96μmol)の溶液に添加した。反応混合物を室温で72時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(145mg、0.29mmol、収率60%、純度96%)を茶色の固体として得た。
UPLC/MS (方法5):m/z 479 (M+H)+, RT 1.80分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(145mg、303μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(83.7mg、363μmol)及びtBuBrettPhos Pd G3(25.9mg、30.3μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.39mL、394μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に18時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、その後RPフラッシュC18(24gカートリッジ、10~100%(MeCN中0.1%ギ酸)/(水中0.1%ギ酸))上でさらに精製し、表題化合物(83mg、0.12mmol、収率39%、純度97%)を白色の固体として得た。
UPLC/MS (方法5):m/z 673 (M+H)+, RT 1.70分。
TFA(0.5mL)を、DCM(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(83mg、0.12mmol)の溶液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(49mg、0.10mmol、収率81%、純度96%)を得た。
UPLC/MS (方法5):m/z 473 (M+H)+, RT 1.16分。
1H NMR (400 MHz, DMSO-d6) δ 7.91 (s, 1H), 7.57 (t,J = 6.0 Hz, 1H), 7.52 (s, 1H), 7.43 (d,J = 9.0 Hz, 1H), 7.20 (dd,J = 9.0, 7.0 Hz, 1H), 6.79 - 6.74 (m, 1H), 6.69 - 6.64 (m, 1H), 5.36 (s, 1H), 5.34 - 5.29 (m, 1H), 4.60 (d,J = 5.8 Hz, 2H), 3.59 - 3.47 (m, 1H), 3.26 - 3.19 (m, 1H), 3.10 - 3.00 (m, 1H), 2.91 (dd,J = 11.5, 4.5 Hz, 1H), 2.84 - 2.75 (m, 1H), 2.36 - 2.26 (m, 1H), 2.22 - 2.12 (m, 2H), 1.77 - 1.68 (m, 1H), 1.63 - 1.53 (m, 1H), 1.40 - 1.29 (m, 1H), 1.22 - 1.10 (m, 1H), 1.10 - 1.03 (m, 2H), 0.82 - 0.73 (m, 4H), 0.71 - 0.61 (m, 2H). 1H under water.
(5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
ジオキサン(10.0mL)中のエチル5-ブロモイミダゾ[1,2-a]ピリジン-2-カルボキシレート(500mg、1.86mmol)、フッ化セシウム(564mg、3.72mmol)、PdCl2(dtbpf)(121mg、186μmol)、シクロプロピルボロン酸(319mg、3.72mmol)の混合物を、N2で10分間脱気した。次いで、混合物を90℃に一晩加熱した。室温で、反応混合物をセライトのショートパッドを通して濾過し、20%MeOH/DCM(20mL)ですすぎ、濾液を減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(440mg、1.7mmol、収率93%、純度90%)を茶色の油状物として得た。
UPLC/MS (方法3):m/z 231 (M+H)+, RT 0.86分。
2-(クロロメチル)-5-シクロプロピルイミダゾ[1,2-a]ピリジン、HCl
水素化ホウ素リチウム(THF中2M)(860μL、1.72mmol)を、THF(8.0mL)中のエチル5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-カルボキシレート(440mg、1.72mmol)の溶液に0℃で添加した。反応混合物を室温に温め、次いで20時間撹拌した。0℃において、MeOH(5mL)、その後水(5mL)及び1M HCl水溶液(5mL)を添加した。混合物を30分間勢いよく撹拌し、酢酸エチル(3x15mL)で抽出した。合わせた有機層をブライン(15mL)で洗浄し、MgSO4で乾燥させ、真空中で濃縮して粗アルコール中間体(5-シクロプロピルイミダゾ[1,2-a]ピリジン-2-イル)メタノール(235mg、1.25mmol)を得、これを乾燥DCE(5.0mL)に再溶解した。塩化チオニル(455μL、6.24mmol)を添加し、反応混合物を45℃で1時間撹拌した。減圧下で濃縮乾固し、表題化合物(260mg、1.00mmol、収率55%、純度96%)を黄色の液体として得た。
UPLC/MS (方法3):m/z 207 (M+H)+, RT 0.52分。
DMF(6.0mL)中の2-(クロロメチル)-5-シクロプロピルイミダゾ[1,2-a]ピリジン、HCl(260mg、1.21mmol)及びDIPEA(0.63mL、3.62mmol)の溶液を、アジ化ナトリウム(118mg、1.81mmol)で処理した。混合物を50℃に加熱し、3時間撹拌した。混合物を室温に冷却し、減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(218mg、0.97mmol、収率80%、純度95%)を無色の油状物として得た。
UPLC/MS (方法6):m/z 214 (M+H)+, RT 0.63分。
2-(アジドメチル)-5-シクロプロピルイミダゾ[1,2-a]ピリジン(218mg、971μmol)及びトリフェニルホスフィン(255mg、971μmol)を、THF(3.6mL)及び水(0.4mL)に溶解した。混合物を室温で一晩撹拌した後、溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(90mg、0.46mmol、収率48%、純度96%)を白色の固体として得た。
UPLC/MS (方法5):m/z 188 (M+H)+, RT 0.83分。
(3R,4R)-4-(((3-エチル-7-(((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-031)
(5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(100mg、620μmol)を、EtOH(3.0mL)中の5,7-ジクロロ-3-エチルピラゾロ[1,5-a]ピリミジン(122mg、564μmol)及びDIPEA(0.69mL、3.95mmol)の溶液に添加した。反応混合物を50℃で2.5時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(70mg、0.20mmol、収率35%、純度97%)を白色の固体として得た。
UPLC/MS (方法5):m/z 341 (M+H)+, RT 1.33分。
BOC無水物(52mg、0.24mmol)を、THF(2.0mL)中の5-クロロ-3-エチル-N-((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(70mg、0.20mmol)及びDMAP(4.9mg、40μmol)の溶液に添加した。反応混合物を室温で18時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(83mg、0.16mmol、収率82%、純度87%)を褐色の固体として得た。
UPLC/MS (方法5):m/z 441 (M+H)+, RT 1.69分。
THF(3.0mL)中のtert-ブチル(5-クロロ-3-エチルピラゾロ[1,5-a]ピリミジン-7-イル)((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(166mg、376μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(83.0mg、314μmol)及びtBuBrettPhos Pd G3(26.8mg、31.4μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(408μL、408μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2.5時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(61mg、91μmol、収率29%、純度95%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 635 (M+H)+, RT 1.63分。
TFA(0.4mL)を、DCM(1.6mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-メチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-エチルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(61mg、91μmol)の懸濁液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(26mg、57μmol、収率62%、純度95%)をオフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 435 (M+H)+, RT 1.03分。
1H NMR (400 MHz, DMSO-d6) δ 7.67 (s, 1H), 7.64 (s, 1H), 7.58 (t,J = 6.0 Hz, 1H), 7.43 (d,J = 9.1 Hz, 1H), 7.21 (dd,J = 9.1, 6.8 Hz, 1H), 6.80 - 6.73 (m, 2H), 5.49 - 5.42 (m, 1H), 5.34 (s, 1H), 4.59 (d,J = 5.7 Hz, 2H), 3.62 - 3.50 (m, 1H), 3.22 - 3.13 (m, 1H), 3.08 - 2.98 (m, 1H), 2.91 (dd,J = 11.7, 4.5 Hz, 1H), 2.84 - 2.75 (m, 1H), 2.56 (s, 3H), 2.51 - 2.44 (m, 2H), 2.36 - 2.26 (m, 1H), 2.17 (dd,J = 11.6, 9.9 Hz, 1H), 1.61 - 1.52 (m, 1H), 1.38 - 1.28 (m, 1H), 1.21 - 1.13 (m, 4H). 1H under water.
(3R,4R)-4-(((3-シクロプロピル-7-(((5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-032)
(5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(66mg、0.38mmol)を、EtOH(2.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(86mg、0.38mmol)及びDIPEA(0.46mL、2.6mmol)の溶液に添加した。反応混合物を50℃で16時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(108mg、0.28mmol、収率74%、純度95%)を黄色の油状物として得た。
UPLC/MS (方法5):m/z 367 (M+H)+, RT 1.44分。
BOC無水物(82.0mg、376μmol)を、THF(2.0mL)中の5-クロロ-3-シクロプロピル-N-((5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(106mg、289μmol)及びDMAP(1.9mg、57.8μmol)の溶液に添加した。反応混合物を室温で3時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(148mg、0.29mmol、収率99%、純度90%)を白色の固体として得た。
UPLC/MS (方法5):m/z 467 (M+H)+, RT 1.78分。
THF(2.3mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(130mg、278μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(76.9mg、334μmol)及びtBuBrettPhos Pd G3(35.7mg、41.8μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(418μL、418μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、その後カラムクロマトグラフィー(4gカートリッジ、0~100%EtOAc/イソヘキサン、次いで0~5%(0.7M NH3/MeOH)/DCM)でさらに精製し、表題化合物(140mg、0.19mmol、収率68%、純度90%)を茶色の固体として得た。
UPLC/MS (方法4):m/z 661 (M+H)+, RT 1.68分。
塩化水素(ジオキサン中4M)(953μL、3.81mmol)を、ジオキサン(1.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(140mg、191μmol)の懸濁液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(40mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(67mg、0.14mmol、収率72%、純度95%)を、真空下に50℃で一晩乾燥させた後、ベージュ色の固体として得た。
UPLC/MS (方法4):m/z 461 (M+H)+, RT 1.17分。
1H NMR (400 MHz, DMSO-d6) δ 7.56 (s, 1H), 7.53 - 7.47 (m, 2H), 7.19 (s, 1H), 6.74 (t,J = 6.1 Hz, 1H), 6.61 (s, 1H), 5.35 - 5.29 (m, 2H), 4.54 (d,J = 5.8 Hz, 2H), 3.61 - 3.46 (m, 1H), 3.25 - 3.17 (m, 1H), 3.08 - 2.99 (m, 1H), 2.90 (dd,J = 11.7, 4.5 Hz, 1H), 2.81 - 2.74 (m, 1H), 2.36 - 2.31 (m, 3H), 2.30 - 2.25 (m, 1H), 2.15 (dd, J = 11.6, 9.9 Hz, 1H), 1.79 - 1.66 (m, 1H), 1.60 - 1.53 (m, 1H), 1.32 (s, 1H), 1.11 - 1.15 (m, 1H), 0.80 - 0.71 (m, 2H), 0.69 - 0.58 (m, 2H)。DMSO下で3H. 1H under water.
(5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
水素化ジイソブチルアルミニウム(ヘキサン中1M)(3.44mL、3.44mmol)を、THF(8.0mL)中のエチル5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-カルボキシレート(300mg、1.37mmol)の溶液に0℃で添加した。反応混合物を室温に温め、18時間撹拌し、次いでMeOH(10mL)、その後水(10mL)及び1M HCl水溶液(10mL)を添加した。混合物を30分間勢いよく撹拌し、酢酸エチル(3x25mL)で抽出した。合わせた有機層をブライン(15mL)で洗浄し、MgSO4で乾燥させ、真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(93mg、0.51mmol、収率37%、純度98%)を茶色の固体として得た。
UPLC/MS (方法5):m/z 177 (M+H)+, RT 0.77分。
塩化チオニル(96μL、1.32mmol)を、DCM(2.5mL)中の(5,7-ジメチルイミダゾ[1,2-a]ピリジン-2-イル)メタノール(93.0mg、528μmol)の溶液に0℃で滴下添加した。混合物を室温で1時間撹拌した。減圧下で濃縮乾固し、表題化合物(132mg、0.52mmol、収率98%、純度91%)を黄色の固体として得た。
DMSO-d6中の1H NMRは、生成物の構造と一致していた。
DMF(3.0mL)中の2-(クロロメチル)-5,7-ジメチルイミダゾ[1,2-a]ピリジン(132mg、617μmol)及びDIPEA(322μL、1.85mmol)の溶液を、アジ化ナトリウム(40mg、617μmol)で処理した。混合物を50℃に加熱し、3時間撹拌した。混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(117mg、0.38mmol、収率61%、純度65%)を無色の油状物として得た。
UPLC/MS (方法5):m/z 202 (M+H)+, RT 0.46分。
2-(アジドメチル)-5,7-ジメチルイミダゾ[1,2-a]ピリジン(117mg、378μmol)及びトリフェニルホスフィン(119mg、454μmol)を、THF(1.8mL)及び水(0.2mL)に溶解した。混合物を50℃で16時間撹拌し、その後溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(66mg、377μmol、収率99%、純度99%)を褐色の固体として得た。
UPLC/MS (方法5):m/z 176 (M+H)+, RT 0.79分。
(3R,4R)-4-(((7-(((8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-033)
(8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(175mg、701μmol)を、EtOH(10mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(145mg、637μmol)及びDIPEA(666μL、3.82mmol)の溶液に添加した。反応混合物を50℃で5時間加熱した。反応混合物を真空中で濃縮し、表題化合物(290mg、0.58mmol、収率91%、純度88%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 441 (M+H)+, RT 1.61分。
NMP(1.5mL)中の5-クロロ-N-((8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(130mg、295μmol)、tert-ブチル(3R,4R)-4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(271mg、1.18mmol)及びDIPEA(232μL、1.33mmol)の溶液を、マイクロ波照射下に150℃で5時間加熱した。室温で、水を添加した。結果として得られた固体を濾過により回収し、表題化合物(175mg、0.19mmol、65%、純度69%)を黄色の固体として得た。
UPLC/MS (方法3):m/z 535 (M-Boc)+, RT 1.09分。
塩化水素(ジオキサン中4M)(1.29mL、5.16mmol)を、ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(164mg、258μmol)の懸濁液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(10mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮した。RP分取HPLC(25~100%MeCN/水中0.1%ギ酸)によるさらなる精製により、表題化合物(84mg、0.15mmol、収率60%、純度98%)をオフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 535 (M+H)+, RT 1.27分。
1H NMR (400 MHz, DMSO-d6) δ 9.18 (t,J = 1.5 Hz, 1H), 8.00 (s, 1H), 7.85 - 7.77 (m, 2H), 7.54 (s, 1H), 6.72 (t,J = 5.9 Hz, 1H), 5.34 - 5.28 (m, 1H), 5.25 (s, 1H), 4.63 (d,J = 6.1 Hz, 2H), 3.59 - 3.47 (m, 1H), 3.27 - 3.18 (m, 1H), 3.11 - 3.01 (m, 1H), 2.93 (dd,J = 11.6, 4.5 Hz, 1H), 2.84 - 2.77 (m, 1H), 2.36 - 2.26 (m, 1H), 2.18 (dd,J = 11.6, 9.9 Hz, 1H), 1.79 - 1.67 (m, 1H), 1.62 - 1.53 (m, 1H), 1.38 - 1.29 (m, 1H), 1.26 - 1.07 (m, 1H), 0.83 - 0.73 (m, 2H), 0.77 - 0.60 (m, 2H). 1H under water.
(8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
水素化ジイソブチルアルミニウム(ヘキサン中1M)(18.8mL、18.8mmol)を、THF(40mL)中のエチル8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-カルボキシレート(2.20g、7.52mmol)の溶液に-40℃で添加した。反応混合物を0℃に温め、0℃で2時間撹拌し、次いでMeOH(10mL)、その後水(10mL)及び1M HCl水溶液(10mL)を添加した。混合物を30分間勢いよく撹拌し、酢酸エチル(3x25mL)で抽出した。合わせた有機層をブライン(15mL)で洗浄し、MgSO4で乾燥させ、真空中で濃縮し、表題化合物(1.80g、6.9mmol、収率92%、純度96%)を白色の固体として得た。
UPLC/MS (方法5):m/z 251 (M+H)+, RT 0.94分。
塩化チオニル(2.6mL、36mmol)を、DCE(20mL)中の(8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタノール(1.8g、7.2mmol)の溶液に滴下添加した。混合物を45℃で3時間撹拌した。減圧下で濃縮乾固し、表題化合物(2.0g、6.7mmol、収率93%、純度90%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 269 (M+H)+, RT 1.25分。
DMF(30mL)中の8-クロロ-2-(クロロメチル)-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン(2.00g, 6.69mmol)及びDIPEA(3.5mL、20.1mmol)の溶液を、アジ化ナトリウム(652mg、10.0mmol)で処理した。混合物を60℃に加熱し、6時間撹拌した。混合物を室温に冷却し、水(40mL)及びブライン(60mL)で希釈した後、TBME(4x50mL)で抽出し、次いでEtOAc(50mL)で抽出した。合わせた有機層をブライン(4x20mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%TBME/イソヘキサン)により精製し、表題化合物(1.80g、6.2mmol、収率93%、純度95%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 276 (M+H)+, RT 1.27分。
2-(アジドメチル)-8-クロロ-6-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン(1.8g、6.5mmol)、トリフェニルホスフィン(2.1g、7.8mmol)を、THF(36mL)及び水(4.0mL)に溶解した。混合物を室温で一晩撹拌した後、溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(150mL)で洗浄し、生成物をMeOH中0.7M NH3(100mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(1.32g、5.0mmol、収率77%、純度95%)を白色の固体として得た。
UPLC/MS (方法5):m/z 250 (M+H)+, RT 0.92分。
(3R,4R)-4-(((3-エチル-7-(((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-034)
(5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(106mg、444μmol)を、EtOH(1.6mL)中の5,7-ジクロロ-3-エチルピラゾロ[1,5-a]ピリミジン(80mg、370μmol)及びDIPEA(387μL、2.22mmol)の溶液に添加した。反応混合物を65℃で5時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(136mg、0.34mmol、収率91%、純度98%)をオレンジ色の固体として得た。
UPLC/MS (方法3):m/z 395 (M+H)+, RT 1.51分。
BOC無水物(36.8mg、169μmol)を、THF(6.8mL)中の5-クロロ-3-エチル-N-((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(136mg、338μmol)及びDMAP(8.3mg、67.5μmol)の溶液に添加した。反応混合物を65℃で2時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)と水(10mL)に分配した。水性層をDCM(2x10mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(159mg、0.29mmol、収率86%、純度90%)を黄色の油状物として得た。
UPLC/MS (方法5):m/z 495 (M+H)+, RT 1.88分。
THF(3.2mL)中のtert-ブチル(5-クロロ-3-エチルピラゾロ[1,5-a]ピリミジン-7-イル)((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(159mg、0.321mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(91.0mg、0.395mmol)及びtBuBrettPhos Pd G3(28mg、32.9μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(395μL、395μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応を水(20mL)でクエンチし、EtOAc(3x20mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~5%MeOH/DCM)により精製し、その後RPフラッシュC18(24gカートリッジ、30~100%MeCN/10mM重炭酸アンモニウム)上でさらに精製し、表題化合物(153mg、0.18mmol、収率55%、純度80%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 689 (M+H)+, RT 1.77分。
塩化水素(ジオキサン中4M)(900μL、3.6mmol)を、ジオキサン(2.3mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-エチルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(155mg、0.180mmol)の懸濁液に添加した。反応混合物を、40℃ RTで2時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(80mL)で洗浄し、生成物をMeOH中0.7M NH3(100mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(89mg、0.18mmol、収率99%、純度98%)を得た。
UPLC/MS (方法3):m/z 489 (M+H)+, RT 0.70分。
1H NMR (400 MHz, DMSO-d6) δ 7.95 - 7.87 (m, 2H), 7.68 - 7.60 (m, 2H), 7.57 (d,J = 7.1 Hz, 1H), 7.41 (dd,J = 7.1, 9.2 Hz, 1H), 6.77 (t,J = 5.9 Hz, 1H), 5.41 - 5.36 (m, 1H), 5.35 (s, 1H), 4.62 (d,J = 6.3 Hz, 2H), 3.60 - 3.47 (m, 1H), 3.23 - 3.14 (m, 1H), 3.06 - 2.96 (m, 1H), 2.90 (dd,J = 4.5, 11.4 Hz, 1H), 2.82 - 2.73 (m, 1H), 2.48 - 2.44 (m, 2H), 2.36 - 2.26 (m, 1H), 2.15 (dd,J = 9.9, 11.6 Hz, 1H), 1.60 - 1.50 (m, 1H), 1.42 - 1.27 (m, 1H), 1.17 (t,J = 7.5 Hz, 3H), 1.16 - 1.09 (m, 1H). 1H under water.
(3R,4R)-4-(((3-シクロプロピル-7-(((7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-035)
(7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(90mg、0.30mmol)を、EtOH(2.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(95mg、0.42mmol)及びDIPEA(0.69mL、3.9mmol)の溶液に添加した。反応混合物を50℃で2時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、10%MeOH/DCM)により精製し、表題化合物(79mg、0.16mmol、収率54%、純度84%)をベージュ色の固体として得た。
UPLC/MS (方法5):m/z 407 (M+H)+, RT 1.51分。
BOC無水物(35mg、0.16mmol)を、THF(2.0mL)中の5-クロロ-3-シクロプロピル-N-((7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(55mg、0.14mmol)及びDMAP(3.3mg、27μmol)の溶液に添加した。反応混合物を室温で16時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(57mg、0.10mmol、収率74%、純度89%)を黄色のガム状として得た。
UPLC/MS (方法5):m/z 507 (M+H)+, RT 1.84分。
THF(1.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(55mg、0.11mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(27mg、0.12mmol)及びtBuBrettPhos Pd G3(9.3mg、11.3μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.14mL、0.14mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に3時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(53mg、73μmol、収率67%、純度96%)を白色の固体として得た。
UPLC/MS (方法5):m/z 701 (M+H)+, RT 1.72分。
TFA(0.20mL)を、DCM(0.80mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(50mg、71μmol)の溶液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(20mL)で洗浄し、生成物をMeOH中0.7M NH3(20mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(23mg、44μmol、収率61%、純度95%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、オフホワイト色の固体とした。
UPLC/MS (方法5):m/z 501 (M+H)+, RT 1.21分。
1H NMR (400 MHz, DMSO-d6) δ 8.70 (d,J = 7.1 Hz, 1H), 7.99 (s, 2H), 7.73 (t,J = 6.2 Hz, 1H), 7.52 (s, 1H), 7.15 (dd,J = 7.2, 1.9 Hz, 1H), 6.73 - 6.68 (m, 1H), 5.33 - 5.27 (m, 1H), 5.25 (s, 1H), 4.62 (d,J = 6.1 Hz, 2H), 3.56 - 3.44 (m, 1H), 3.25 - 3.15 (m, 1H), 3.08 - 2.97 (m, 1H), 2.90 (dd,J = 11.7, 4.5 Hz, 1H), 2.82 - 2.73 (m, 1H), 2 2.34 - 2.25 (m, 1H), 2.21 - 2.09 (m, 1H), 1.78 - 1.66 (m, 1H), 1.59 - 1.51 (m, 1H), 1.37 - 1.27 (m, 1H), 1.19 - 1.05 (m, 1H), 0.79 - 0.74 (m, 2H), 0.70 - 0.60 (m, 2H). 1H under water.
(7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
エタノール(0.60mL)中の4-(トリフルオロメチル)ピリジン-2-アミン(200mg、1.23mmol)、2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(366mg、1.23mmol)、及び重炭酸ナトリウム(104mg、1.23mmol)をマイクロ波照射下で80℃に1時間加熱した。次いで、混合物を減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(348mg、0.80mmol、収率65%、純度79%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 364 (M+H)+, RT 1.02分。
ヒドラジン(水中35重量%)(250μL、2.79mmol)を、EtOH(4.0mL)中の2-(((7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバモイル)安息香酸(348mg、105μmol)の懸濁液に添加した。この懸濁液を65℃で3時間撹拌した。混合物を真空中で濃縮し、次いで1M HCl水溶液(20mL)で希釈し、白色の固体を濾過除去し、1M HCl水溶液(2x20mL)で洗浄し、その後合わせた水性層を固体NaHCO3で塩基性化し、EtOAc(3x20mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、濾過し、次いで真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、茶色の油状物としての表題化合物(90mg、0.31mmol、収率38%、純度73%)とした。
UPLC/MS (方法5):m/z 216 (M+H)+, RT 0.82分。
(3R,4R)-4-(((3-シクロプロピル-7-(((5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-036)
(5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メタンアミン(155mg、786μmol)を、EtOH(10mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(163mg、715μmol)及びDIPEA(0.12mL、715μmol)溶液に添加した。反応混合物を90℃で3時間加熱した。反応混合物を真空中で濃縮し、残渣をMeCN中でトリチュレーションし、表題化合物(170mg、0.43mmol、収率61%、純度99%)を白色の固体として得た。
UPLC/MS (方法3):m/z 389 (M+H)+, RT 1.52分。
BOC無水物(180mg、823μmol)を、DMF(5.0mL)中の5-クロロ-3-シクロプロピル-N-((5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(160mg、412μmol)及びDMAP(10.1mg、82.3μmol)の溶液に添加した。反応混合物を60℃で2時間撹拌した。反応混合物をEtOAc(20mL)と水(20mL)に分配した。水性層をEtOAc(2x20mL)で抽出し、合わせた有機層をブライン(2x20mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(190mg、0.25mmol、収率60%、純度64%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 488 (M+H)+, RT 1.83分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メチル)カルバメート(190mg、249μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(68.7mg、298μmol)及びtBuBrettPhos Pd G3(21.3mg、24.9μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(323μL、323μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に18時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(103mg、0.13mmol、収率50%、純度83%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 684 (M+H)+, RT 1.73分。
塩化水素(ジオキサン中4M)(626μL、2.50mmol)を、ジオキサン(2.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(103mg、125μmol)の溶液に添加した。反応混合物を35℃で4時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(10mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(28mg、54μmol、収率43%、純度93%)を得た。
UPLC/MS (方法3):m/z 484 (M+H)+, RT 0.72分。
1H NMR (400 MHz, DMSO-d6) δ 7.79 - 7.70 (m, 2H), 7.66 (dd,J = 11.1, 7.4 Hz, 1H), 7.53 (s, 1H), 6.84 - 6.73 (m, 1H), 5.38 (s, 1H), 5.28 - 5.20 (m, 1H), 4.73 (d,J = 5.5 Hz, 2H), 3.83 (s, 3H), 3.55 - 3.44 (m, 1H), 3.27 - 3.16 (m, 1H), 3.08 - 3.00 (m, 1H), 2.95 - 2.86 (m, 1H), 2.81 - 2.74 (m, 1H), 2.33 - 2.23 (m, 1H), 2.19 - 2.09 (m, 1H), 2.03 - 1.83 (m, 1H), 1.77 - 1.66 (m, 1H), 1.61 - 1.53 (m, 1H), 1.20 - 1.10 (m, 1H), 0.79 - 0.73 (m, 2H), 0.67 - 0.63 (m, 2H). 1H under water.
(5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メタンアミン
1-[ビス(ジメチルアミノ)メチレン]-1H-1,2,3-トリアゾロ[4,5-b]ピリジニウム3-オキシドヘキサフルオロホスフェート(HATU)(3.96g、10.4mmol)を、THF(25mL)中の4,5-ジフルオロベンゼン-1,2-ジアミン(2.00g、13.9mmol)、2-(1,3-ジオキソイソインドリン-2-イル)酢酸(1.42g、6.94mmol)及びDIPEA(3.6mL、20.8mmol)の溶液に添加した。反応混合物を50℃で72時間撹拌した。室温で、EtOAc(25mL)及び水(10mL)を添加した。結果として得られた固体を濾過により回収し、次いでMeCN中でトリチュレーションし、表題化合物(1.81g、5.4mmol、収率78%、純度99%)をオフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 332 (M+H)+, RT 1.46分。
AcOH(15mL)中のN-(2-アミノ-4,5-ジフルオロフェニル)-2-(1,3-ジオキソイソインドリン-2-イル)アセトアミド(1.81g、5.46mmol)の溶液を、60℃で3時間撹拌した。反応混合物を濃縮乾固し、トルエン(2x10mL)と一緒に2回共蒸発させ、次いでMeCNでトリチュレーションし、表題化合物(1.56g、4.9mmol、収率90%、純度99%)をオフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 314 (M+H)+, RT 1.47分。
2-((5,6-ジフルオロ-1H-ベンゾ[d]イミダゾール-2-イル)メチル)イソインドリン-1,3-ジオン(600mg、1.92mmol)を、DMF(15mL)中のヨードメタン(179μL、2.87mmol)及びK2CO3(529mg、3.83mmol)の溶液に0℃で添加した。反応混合物を0℃で5分間撹拌し、次いで室温において一晩撹拌し、その後結果として得られた固体を濾過により回収し、水(2.0mL)、次いでMeCN(2.0mL)で洗浄し、表題化合物(610mg、1.7mmol、収率88%、純度90%)を灰色の固体として得た。
UPLC/MS (方法5):m/z 328 (M+H)+, RT 1.21分。
ヒドラジン水和物(259μL、5.33mmol)を、EtOH(10mL)中の2-((5,6-ジフルオロ-1-メチル-1H-ベンゾ[d]イミダゾール-2-イル)メチル)イソインドリン-1,3-ジオン(600mg、1.52mmol)の溶液に添加した。懸濁液を65℃で一晩撹拌した。室温で懸濁液を濾過し、固体をIPA(5.0mL)で洗浄した。濾液を減圧下で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(10mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(300mg、1.40mmol、収率89%、純度89%)を白色の固体として得た。
UPLC/MS (方法5):m/z 199 (M+H)+, RT 0.78分。
(3R,4R)-4-(((3-シクロプロピル-7-(((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-037)
(5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(106mg、0.443mmol)を、EtOH(1.6mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(86mg、0.377mmol)及びDIPEA(390μL、2.24mmol)の溶液に添加した。反応混合物を65℃で2時間加熱し、次いで真空中で濃縮した。
UPLC/MS (方法3):m/z 407 (M+H)+, RT 1.54分。
BOC無水物(97.8mg、0.448mmol)を、THF(7.5mL)中の5-クロロ-3-シクロプロピル-N-((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(185mg、0.373mmol)及びDMAP(9.1mg、74.6μmol)の溶液に添加した。反応混合物を65℃で2時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)と水(30mL)に分配した。水性層をDCM(2x30mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、Na2SO4で乾燥させて、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(167mg、0.32mmol、収率87%、純度98%)をオレンジ色の油状物として得た。
UPLC/MS (方法3):m/z 507 (M+H)+, RT 1.87分。
THF(3.2mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(167mg、0.329mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(91mg、0.395mmol)及びtBuBrettPhos Pd G3(28mg、0.0329mmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(395μL、0.395mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応を水(10mL)でクエンチし、EtOAc(3x10mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(80gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(177mg、0.16mmol、収率49%、純度64%)をオレンジ色の固体として得た。
UPLC/MS (方法3):m/z 701 (M+H)+, RT 1.76分。
塩化水素(ジオキサン中4M)(0.80mL、3.20mmol)を、ジオキサン(2.2mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(175mg、160μmol)の懸濁液に添加した。反応混合物を40℃で3時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、黄色の固体を得た。分取HPLC(20~100%MeCN/水中0.1%NH3)によるさらなる精製により、表題化合物(41mg、79μmol、収率50%、純度98%)を白色の固体として得た。
UPLC/MS (方法5):m/z 501 (M+H)+, RT 1.20分。
1H NMR (400 MHz, DMSO-d6) δ 7.91 (d, J = 9.3 Hz, 2H), 7.61 (t, J = 6.2 Hz, 1H), 7.57 (d, J = 7.1 Hz, 1H), 7.51 (s, 1H), 7.44 - 7.35 (m, 1H), 6.74 (t, J = 6.1 Hz, 1H), 5.35 (s, 1H), 5.26 (s, 1H), 4.61 (d, J = 6.0 Hz, 2H), 3.50 (s, 1H), 3.27 - 3.18 (m, 1H), 3.10 - 2.95 (m, 1H), 2.90 (dd, J = 11.6, 4.5 Hz, 1H), 2.82 - 2.74 (m, 2H), 2.36 - 2.23 (m, 1H), 2.20 - 2.10 (m, 1H), 1.77 - 1.65 (m, 1H), 1.60 - 1.51 (m, 1H), 1.40 - 1.24 (m, 1H), 1.19 - 1.07 (m, 1H), 0.80 - 0.71 (m, 2H), 0.71 - 0.53 (m, 2H)。
(5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
IPA(5.8mL)及び水(5.8mL)中の6-(トリフルオロメチル)ピリジン-2-アミン(1.00g、6.17mmol)及びエチル3-ブロモ-2-オキソプロパノエート(1.6mL、12.3mmol)を、マイクロ波照射下に80℃で1時間加熱した。反応混合物を真空下で濃縮した。カラム(80gカートリッジ、0~5%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(1.24g、4.32mmol、収率67%、純度90%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 259 (M+H)+, RT 1.13分。
水素化ジイソブチルアルミニウム(ヘキサン中1M)(11mL、11.0mmol)を、THF(9.0mL)中のエチル5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-カルボキシレート(860mg、2.99mmol)の溶液に-40℃で添加した。反応混合物を一晩室温に温めた。0℃において、MeOH(5.0mL)、その後水(5.0mL)及び1M HCl水溶液(5.0mL)を添加した。混合物を30分間勢いよく撹拌し、酢酸エチル(3x15mL)で抽出した。合わせた有機層をブライン(15mL)で洗浄し、MgSO4で乾燥させ、真空中で濃縮し、表題化合物(453mg、2.0mmol、収率57%、純度95%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 217 (M+H)+, RT 0.82分。
塩化チオニル(363μL、4.98mmol)を、DCM(8.5mL)中の(5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタノール(453mg、1.99mmol)の溶液に0℃で滴下添加した。
UPLC/MS (方法3):m/z 271 (M+H)+, RT 1.14分。
DMF(8.0mL)中の2-(クロロメチル)-5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン、HCl(494mg、1.73mmol)及びDIPEA(1.9mL、11mmol)の溶液を、アジ化ナトリウム(176mg、2.71mmol)で処理した。混合物を60℃に加熱し、2.5時間撹拌した。混合物を室温に冷却し、水(10mL)及びブライン(10mL)で希釈した。TBME(3x20mL)で抽出し、次いでEtOAc(3x20mL)で抽出した。合わせた有機層をブライン(4x20mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮し、表題化合物(383mg、1.5mmol、収率89%、純度97%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 242 (M+H)+, RT 1.12分。
2-(アジドメチル)-5-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン(383.5mg、1.54mmol)、トリフェニルホスフィン(486mg、1.85mmol)を、THF(8.0mL)及び水(0.90mL)に溶解した。混合物を室温で一晩撹拌した後、溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(150mL)で洗浄し、生成物をMeOH中0.7M NH3(100mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物 (336mg、1.4mmol、収率91%、純度90%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 216 (M+H)+, RT 0.82分。
(3R,4R)-4-(((7-(((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-エチルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-038)
(6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(125mg、0.333mmol)を、EtOH(1.1mL)中の5,7-ジクロロ-3-エチルピラゾロ[1,5-a]ピリミジン(60.1mg、0.278mmol)及びDIPEA(291μL、1.67mmol)の溶液に添加した。反応混合物を80℃で3時間加熱し、次いで真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(103.6mg、0.23mmol、収率82%、純度96%)を淡ベージュ色の固体として得た。
UPLC/MS (方法5):m/z 435 (M+H)+, RT 1.67分。
BOC無水物(60.8mg、279μmol)を、THF(4.6mL)中の5-クロロ-N-((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)-3-エチルピラゾロ[1,5-a]ピリミジン-7-アミン(103mg、232μmol)及びDMAP(5.6mg、46.4μmol)の溶液に添加した。反応混合物を65℃で2.5時間撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)と水(30mL)に分配した。水性層をDCM(2x30mL)で抽出し、合わせた有機層をブライン(30mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(116mg、0.20mmol、収率88%、純度94%)をオレンジ色の油状物として得た。
UPLC/MS (方法3):m/z 535 (M+H)+, RT 2.01分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-エチルピラゾロ[1,5-a]ピリミジン-7-イル)((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(115mg、202μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(60.5mg、263μmol)及びtBuBrettPhos Pd G3((25.9mg、30.3μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.26mL、263μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応を水(50mL)でクエンチし、EtOAc(3x30mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(53mg、71μmol、収率35%、純度98%)をベージュ色の固体として得た。
UPLC/MS (方法5):m/z 729 (M+H)+, RT 1.84分。
TFA(0.40mL)を、DCM(1.6mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-エチルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(53mg、73μmol)の溶液に添加した。反応混合物を室温で一晩撹拌し、次いで真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(30mg、54μmol、収率75%、純度96%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、ベージュ色の固体として得た。
UPLC/MS (方法5):m/z 529 (M+H)+, RT 1.34分。
1H NMR (400 MHz, DMSO-d6) δ 8.55 (s, 1H), 7.78 (s, 1H), 7.76 (t,J = 6.4 Hz, 1H), 7.66 (s, 1H), 7.46 (s, 1H), 6.74 (t,J = 5.7 Hz, 1H), 5.53 - 5.40 (m, 1H), 5.24 (s, 1H), 4.59 (d, J = 6.0 Hz, 2H), 3.60 - 3.48 (m, 1H), 3.22 - 3.12 (m, 1H), 3.10 - 2.97 (m, 1H), 2.92 (dd,J = 4.5, 11.7 Hz, 1H), 2.84 - 2.76 (m, 1H), 2.48 - 2.44 (m, 2H), 2.39 - 2.28 (m, 1H), 2.24 - 2.13 (m, 1H), 2.04 - 1.96 (m, 1H), 1.62 - 1.50 (m, 1H), 1.38 - 1.28 (m, 1H), 1.18 (t,J = 7.5 Hz, 3H), 1.25 - 1.12 (m, 1H), 0.98 - 0.89 (m, 2H), 0.78 - 0.67 (m, 2H). 1H under water.
(3R,4R)-4-(((3-シクロプロピル-7-(((5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-039)
(5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(60mg、0.26mmol)を、EtOH(1.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(50mg、0.22mmol)及びDIPEA(0.19mL、1.1mmol)の溶液に添加した。反応混合物を65℃で1時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(90mg、0.20mmol、収率93%、純度95%)をベージュ色の固体として得た。
UPLC/MS (方法5):m/z 421 (M+H)+, RT 1.59分。
BOC無水物(70mg、0.32mmol)を、THF(2.0mL)中の5-クロロ-3-シクロプロピル-N-((5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(90mg、0.21mmol)及びDMAP(1.4mg、43μmol)の溶液に添加した。反応混合物を室温で16時間撹拌し、次いで減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(105mg、0.19mmol、収率90%、純度95%)を黄色の泡状物として得た。
DMSO-d6中の1H NMRは生成物の構造と一致していた。
THF(1.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(100mg、192μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(53mg、230μmol)及びtBuBrettPhos Pd G3(24.6mg、28.8μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(230μL、230μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応混合物を減圧下で濃縮した。
UPLC/MS (方法5):m/z 715 (M+H)+, RT 1.79分。
TFA(0.2mL)を、DCM(0.80mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(77mg、0.11mmol)の溶液に添加した。反応混合物を室温で16時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(20mL)で洗浄し、生成物をMeOH中0.7M NH3(20mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(30mg、57μmol、収率52%、純度97%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 515 (M+H)+, RT 1.27分。
1H NMR (400 MHz, DMSO-d6) δ 7.90 (s, 1H), 7.88 (s, 1H), 7.64 (t,J = 6.0 Hz, 1H), 7.51 (s, 1H), 7.10 (s, 1H), 6.71 (t,J = 5.8 Hz, 1H), 5.31 - 5.27 (m, 2H), 4.63 (d,J = 5.9 Hz, 2H), 3.56 - 3.45 (m, 1H), 3.25 - 3.16 (m, 1H), 3.08 - 2.97 (m, 1H), 2.90 (dd,J = 11.5, 4.5 Hz, 1H), 2.81 - 2.73 (m, 1H), 2.65 (s, 3H), 2.34 - 2.24 (m, 1H), 2.15 (dd,J = 11.6, 9.9 Hz, 1H), 1.77 - 1.67 (m, 1H), 1.59 - 1.50 (m, 1H), 1.38 - 1.27 (m, 1H), 1.20 - 1.11 (m, 1H), 0.80 - 0.72 (m, 2H), 0.70 - 0.59 (m, 2H). 1H under water.
(5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
水(3.0mL)中のCs2CO3(2.50g、7.63mmol)の溶液を、1,4-ジオキサン(7.0mL)中の6-クロロ-4-(トリフルオロメチル)ピリジン-2-アミン(500mg、2.54mmol)、2,4,6-トリメチル-1,3,5,2,4,6-トリオキサトリボリナン(1.4mL、10.2mmol)及びPdCl2(dppf)-CH2Cl2付加物(208mg、254μmol)の溶液に添加した。N2を、反応混合物を通して10分間バブリングし、次いで反応混合物を100℃で1時間加熱した。混合物を真空中で濃縮した。カラム(24gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(352mg、1.8mmol、69%、純度88%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 177 (M+H)+, RT 1.06分。
エタノール(6.4mL)中の6-メチル-4-(トリフルオロメチル)ピリジン-2-アミン(238mg、1.28mmol)及び2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(471mg、1.67mmol)を、マイクロ波照射下に80℃で2時間加熱した。混合物を0℃に冷却し、MeOH(3.0mL)を添加し、固体を濾過により回収し、MeOH(2x1.0mL)ですすいで、表題化合物(301mg、0.82mmol、収率64%、純度98%)を白色の固体として得た。
DMSO-d6中の1H NMRは、生成物の構造と一致していた。
ヒドラジン水和物(78μL、1.61mmol)を、EtOH(4.0mL)中の2-((5-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)イソインドリン-1,3-ジオン(381mg、1.01mmol)の懸濁液に添加した。懸濁液を65℃で1時間撹拌した。室温で懸濁液を濾過し、固体をIPA(5.0mL)で洗浄した。濾液を減圧下で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(10mL)で洗浄し、生成物をMeOH中0.7M NH3(10mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(128mg、0.53mmol、収率53%、純度95%)を白色の固体として得た。
UPLC/MS (方法5):m/z 230 (M+H)+, RT 0.93分。
(3R,4R)-4-(((3-シクロプロピル-7-(((6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-040)
(6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(80mg、0.35mmol)を、EtOH(10mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(72mg、0.31mmol)及びDIPEA(0.36mL、2.1mmol)の溶液に添加した。反応混合物を50℃で5時間加熱した。反応混合物を真空中で濃縮し、表題化合物(65mg、0.15mmol、収率43%、純度98%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 421 (M+H)+, RT 1.61分。
BOC無水物(51mg、0.23mmol)を、THF(5.0mL)中の5-クロロ-3-シクロプロピル-N-((6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(65mg、0.15mmol)及びDMAP(1.9mg、15.0μmol)の溶液に添加した。反応混合物を35℃で2時間撹拌した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(70mg、0.13mmol、収率83%、純度95%)をベージュ色の固体として得た。
UPLC/MS (方法5):m/z 521 (M+H)+, RT 1.92分。
THF(2.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(70mg、0.13mmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(37mg、0.16mmol)及びtBuBrettPhos Pd G3(11mg、13μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(0.17mL、0.17mmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に18時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(4gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(65mg、86μmol、収率64%、純度95%)を白色の固体として得た。
UPLC/MS (方法5):m/z 715 (M+H)+, RT 1.79分。
TFA(0.20mL)を、DCM(0.80mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(46mg、64μmol)の溶液に添加した。反応混合物を室温で16時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(20mL)で洗浄し、生成物をMeOH中0.7M NH3(20mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(24mg、46μmol、収率71%、純度98%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、黄色の固体として得た。
UPLC/MS (方法5):m/z 515 (M+H)+, RT 1.28分。
1H NMR (400 MHz, DMSO-d6) δ 8.54 (s, 1H), 7.93 (s, 1H), 7.88 (s, 1H), 7.70 (t,J = 6.2 Hz, 1H), 7.52 (s, 1H), 6.71 (t,J = 6.4 Hz, 1H), 5.31 (s, 1H), 5.24 (s, 1H), 4.59 (d,J = 6.0 Hz, 2H), 3.56 - 3.44 (m, 1H), 3.24 - 3.15 (m, 1H), 3.08 - 2.97 (m, 1H), 2.90 (dd,J = 11.6, 4.5 Hz, 1H), 2.81 - 2.73 (m, 1H), 2.36 - 2.23 (m, 4H), 2.15 (dd,J = 11.6, 9.9 Hz, 1H), 1.76 - 1.65 (m, 1H), 1.59 - 1.50 (m, 1H), 1.37 - 1.26 (m, 1H), 1.19 - 1.11 (m, 1H), 0.80 - 0.73 (m, 2H), 0.70 - 0.59 (m, 2H). 1H under water.
(5-メチル-6-(トリフルオロメチル)-3aH-インドール-2-イル)メタンアミン
水(3.0mL)中のリン酸三カリウム(2.64g、12.45mmol)の溶液を、ジオキサン(30mL)中の5-ブロモ-4-(トリフルオロメチル)ピリジン-2-アミン(1.00g、4.15mmol)、2,4,6-トリメチル-1,3,5,2,4,6-トリオキサトリボリナン(1.03g、8.30mmol)及び(2-ジシクロヘキシルホスフィノ-2',6'-ジメトキシビフェニル)[2-(2'-アミノ-1,1'-ビフェニル)]パラジウム(II)メタンスルホネート(291mg、332μmol)の溶液に添加した。N2を、反応混合物を通して10分間バブリングし、次いで反応混合物を60℃で4時間加熱した。混合物を真空中で濃縮した。カラム(80gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)により精製し、表題化合物(800mg、3.9mmol、収率93%、純度85%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 177 (M+H)+, RT 1.05分。
エタノール(20mL)中の5-メチル-4-(トリフルオロメチル)ピリジン-2-アミン(800mg、4.54mmol)、エチル3-ブロモ-2-オキソプロパノエート(1.1mL、9.08mmol)及び重炭酸ナトリウム(382mg、4.54mmol)を、80℃で一晩加熱した。反応物を真空下で濃縮した。カラム(40gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(535mg、1.7mmol、収率37%、純度85%)を黄色ガム状物として得た。
UPLC/MS (方法5):m/z 273 (M+H)+, RT 1.22分。
水素化ジイソブチルアルミニウム(ヘキサン中1M)(4.0mL、4.03mmol)を、THF(10mL)中のエチル6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-カルボキシレート(530mg、1.75mmol)の溶液に-40℃で添加した。反応混合物を2時間かけて0℃に温め、この温度で2時間撹拌した。0℃において、MeOH(10mL)、その後水(10mL)及び1M HCl水溶液(10mL)を添加した。混合物を20分間勢いよく撹拌し、酢酸エチル(3x35mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、相分離器を通過させ、真空中で濃縮した。カラム(24gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(200mg、0.83mmol、収率48%、純度96%)を白色固体として得た。
UPLC/MS (方法5):m/z 231 (M+H)+, RT 0.94分。
塩化チオニル(317μL、4.34mmol)を、DCE(5.0mL)中の(6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタノール(200mg、869μmol)の溶液に室温で滴下添加した。混合物を45℃で2時間撹拌し、次いで減圧下で濃縮乾固し、表題化合物(215mg、0.80mmol、収率92%、純度92%)を黄色の油状物として得た。
UPLC/MS (方法5):m/z 249 (M+H)+, RT 1.24分。
DMF(5.0mL)中の2-(クロロメチル)-6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン(215mg、865μmol)及びDIPEA(452μL、2.59mmol)の溶液を、アジ化ナトリウム(84mg、1.30mmol)で処理した。混合物を60℃に加熱し、6時間撹拌した。混合物を室温に冷却し、水(100mL)で希釈した。TBME(3x25mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、減圧下で濃縮した。クロマトグラフィー(12gカートリッジ、0~100%TBME/イソヘキサン)による精製により、表題化合物(200mg、0.76mmol、収率88%、純度97%)を茶色の油状物として得た。
UPLC/MS (方法5):m/z 256 (M+H)+, RT 1.26分。
2-(アジドメチル)-6-メチル-7-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン(200mg、784μmol)、トリフェニルホスフィン(247mg、940μmol)を、THF(4.5mL)及び水(0.50mL)に溶解した。混合物を室温で20時間撹拌し、その後溶媒を真空中で除去した。
UPLC/MS (方法5):m/z 230 (M+H)+, RT 0.94分。
(3R,4R)-4-(((3-シクロプロピル-7-(((5-イソプロポキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-041)
(5-イソプロポキシイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(92.0mg、448μmol)を、EtOH(4.0mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(102mg、448μmol)及びDIPEA(547μL、3.14mmol)の溶液に添加した。反応混合物を50℃で72時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(115mg、0.28mmol、収率63%、純度97%)を白色の固体として得た。
1H NMRは、生成物構造と一致する。
BOC無水物(74mg、337μmol)を、THF(3.0mL)中の5-クロロ-3-シクロプロピル-N-((5-イソプロポキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(115mg、281μmol)及びDMAP(6.9mg、56.2μmol)の溶液に添加した。反応混合物を室温で16時間撹拌した。反応混合物を減圧下で濃縮した。
UPLC/MS (方法5):m/z 497 (M+H)+, RT 1.85分。
THF(2.5mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5-イソプロポキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(115mg、231μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(64mg、278μmol)及びtBuBrettPhos Pd G3(19.8mg、23.1μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(301μL、1モル、301μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に3時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、その後RPフラッシュC18(24gカートリッジ、20~80%MeCN/10mM重炭酸アンモニウム)上でさらに精製し、表題化合物(120mg、0.16mmol、収率68%、純度90%)を白色の固体として得た。
UPLC/MS (方法5):m/z 692 (M+H)+, RT 1.75分。
UPLC/MS (方法5):m/z 492 (M+H)+, RT 1.23分。
1H NMR (400 MHz, DMSO-d6) δ 7.59 (t,J = 6.1 Hz, 1H), 7.53 (s, 1H), 7.51 (s, 1H)., 7.26 (dd,J = 9.0, 7.5 Hz, 1H), 7.11 (d,J= 8.9 Hz, 1H), 6.75 (t,J = 6.0 Hz, 1H), 6.37 (d,J = 7.5 Hz, 1H), 5.33 - 5.27 (m, 2H), 4.92 (hept,J = 6.1 Hz, 1H), 4.53 (d,J = 6.0 Hz, 2H), 3.56 - 3.46 (m, 1H), 3.25 - 3.18 (m, 1H), 3.08 - 2.97 (m, 1H), 2.91 (dd,J = 11.6, 4.5 Hz, 1H), 2.81 - 2.73 (m, 1H), 2.36 - 2.23 (m, 1H), 2.16 (dd,J = 11.5, 9.9 Hz, 1H), 1.76 - 1.66 (m, 1H), 1.60 - 1.52 (m, 1H), 1.39 (d,J = 6.0 Hz, 6H), 1.36 - 1.27 (m, 1H), 1.21 - 1.06 (m, 1H), 0.80 - 0.71 (m, 2H), 0.71 - 0.59 (m, 2H). 1H under water.
(5-イソプロポキシイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
6-フルオロピリジン-2-アミン(500mg、4.46mmol)、水酸化ナトリウム(446mg、11.1mmol)及びIPA(3.4mL、44mmol)を、マイクロ波照射下に150℃で5分間加熱した。混合物を水(100mL)で希釈し、DCM(3x30mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、濾過して真空中で濃縮し、表題化合物(510mg、3.2mmol、収率71%、純度95%)を無色の油状物として得た。
UPLC/MS (方法5):m/z 153 (M+H)+, RT 0.80分。
エタノール(10mL)中の6-イソプロポキシピリジン-2-アミン(300mg、1.97mmol)、2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(556mg、1.97mmol)、重炭酸ナトリウム(166mg、1.97mmol)を、マイクロ波照射下に80℃で1時間加熱した。
UPLC/MS (方法5):m/z 336 (M+H)+, RT 1.30分。
2-((5-イソプロポキシイミダゾ[1,2-a]ピリジン-2-イル)メチル)イソインドリン-1,3-ジオン(190mg、567μmol)、ヒドラジン(水中35重量%)(178μL、1.98mmol)及びエタノール(4.0mL)を65℃で2時間撹拌した。反応物を、2N NaOH水溶液(15mL)、水(15mL)及びDCM(15mL)で希釈した。層を分離し、水性層をDCM(2x15mL)で抽出して、次いで真空中で濃縮し、表題化合物(94mg、0.41mmol、収率73%、純度90%)を黄色の固体として得た。
DMSO-d6中の1H NMRは生成物の構造と一致していた。
(3R,4R)-4-(((3-シクロプロピル-7-(((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-042)
(6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(127mg、479μmol)を、EtOH(1.6mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(91.0mg、399μmol)及びDIPEA(417μL、2.39mmol)の溶液に添加した。反応混合物を60℃で一晩加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)による精製により、表題化合物(170mg、0.37mmol、収率92%、純度97%)をオフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 447 (M+H)+, RT 1.63分。
BOC無水物(124mg、568μmol)を、THF(7.5mL)中の5-クロロ-3-シクロプロピル-N-((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(170mg、369μmol)及びDMAP(9.3mg、75.9μmol)の溶液に添加した。反応混合物を65℃で1時間撹拌した。
UPLC/MS (方法5):m/z 547(M+H)+, RT 1.98分。
THF(3.3mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(192mg、330μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(91mg、396μmol)及びtBuBrettPhos Pd G3(28.2mg、33.0μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(396μL、396μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1時間加熱した。反応を水(50mL)でクエンチし、EtOAc(3x30mL)で抽出した。合わせた有機層をNa2SO4で乾燥させ、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製して固体を得、これをRPフラッシュC18(24gカートリッジ、30~100%MeCN/10mM重炭酸アンモニウム)上でさらに精製し、表題化合物(136mg、0.18mmol、収率54%、純度97%)を黄色固体として得た。
UPLC/MS (方法5):m/z 741 (M+H)+, RT 1.84分。
塩化水素(ジオキサン中4M)(884μL、3.54mmol)を、ジオキサン(2.2mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(135mg、177μmol)の懸濁液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(30mL)で洗浄し、生成物をMeOH中0.7M NH3(30mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(65mg、0.12mmol、収率67%、純度98%)を、Et2Oからトリチュレーションし、真空下に40℃で一晩乾燥させた後、白色固体として得た。
UPLC/MS (方法5):m/z 541 (M+H)+, RT 1.32分。
1H NMR (400 MHz, DMSO-d6) δ 8.55 (s, 1H), 7.77 (s, 1H), 7.72 (t,J = 6.3 Hz, 1H), 7.53 (s, 1H), 7.46 (s, 1H), 6.70 (t,J = 6.1 Hz, 1H), 5.32 - 5.26 (m, 1H), 5.25 (s, 1H), 4.59 (d,J = 6.2 Hz, 2H), 3.56 - 3.46 (m, 1H), 3.25 - 3.15 (m, 1H), 3.08 - 2.98 (m, 1H), 2.90 (dd,J = 4.5, 11.7 Hz, 1H), 2.82 - 2.73 (m, 1H), 2.35 - 2.28 (m, 1H), 2.21 - 2.09 (m, 1H), 2.06 - 1.95 (m, 1H), 1.76 - 1.68 (m, 1H), 1.59 - 1.50 (m, 1H), 1.37 - 1.26 (m, 1H), 1.21 - 1.04 (m, 1H), 0.99 - 0.90 (m, 2H), 0.80 - 0.69 (m, 4H), 0.71 - 0.58 (m, 2H). 1H under water.
(6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
水(3.8mL)中のリン酸三カリウム(3.96g、18.7mmol)の溶液を、ジオキサン(15mL)中の5-ブロモ-3-(トリフルオロメチル)ピリジン-2-アミン(1.50g、6.22mmol)、シクロプロピルボロン酸(1.60g、18.7mmol)、酢酸パラジウム(II)(210mg、934μmol)及びトリシクロヘキシルホスファン(524mg、1.87mmol)の溶液に添加した。N2を、反応混合物を通して10分間バブリングし、次いで反応混合物を100℃で加熱し、一晩撹拌した。反応混合物をEtOAc(10mL)で希釈し、セライトを通して濾過し、EtOAc(100mL)ですすいだ。濾液を減圧下で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮した。カラム(40gカートリッジ、0~10%(0.7M NH3/MeOH)/DCM)によりさらに精製し、表題化合物(1.015g、4.9mmol、収率78%、純度97%)をオレンジ色の固体として得た。
UPLC/MS (方法3):m/z 203 (M+H)+, RT 0.94分。
エタノール(5.0mL)中の5-シクロプロピル-3-(トリフルオロメチル)ピリジン-2-アミン(204mg、1.01mmol)及び2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(285mg、1.01mmol)を、マイクロ波照射下に80℃で2.5時間加熱した。重炭酸ナトリウム(42mg、505μmol)を添加し、反応混合物をマイクロ波照射下に80℃で1時間加熱した。2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(85mg、303μmol)を添加し、反応混合物をマイクロ波照射下に80℃で1時間加熱した。結果として得られた固体を濾過により回収し、水(2x3.0mL)ですすいだ。湿潤固体をDCM(10mL)に溶解し、混合物を相分離器を通して濾過した。濾液を濃縮し、表題化合物(256mg、0.63mmol、収率63%、純度95%)を茶色の固体として得た。
UPLC/MS (方法5):m/z 386 (M+H)+, RT 1.47分。
ヒドラジン水和物(50μL、1.01mmol)を、EtOH(3.0mL)中の2-((6-シクロプロピル-8-(トリフルオロメチル)イミダゾ[1,2-a]ピリジン-2-イル)メチル)イソインドリン-1,3-ジオン(255mg、0.629mmol)の懸濁液に添加した。懸濁液を65℃で4時間撹拌した。
UPLC/MS (方法5):m/z 256 (M+H)+, RT 1.01分。
(3R,4R)-4-(((7-(((5,7-ジメチルイミダゾ[1,2-a]ピリミジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-043)
水酸化アンモニウム(28%水溶液)(10mL、71.9mmol)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(1.0g、4.35mmol)の混合物を、85℃で一晩撹拌した。室温で、結果として得られた固体を濾過により回収し、水(3x5mL)ですすいだ。固体をTBME(20mL)に溶解し、相分離器を通して濾過した。濾液を真空中で濃縮し、表題化合物(900mg、4.06mmol、収率93%、純度95%)をオフホワイト色の固体として得た。
DMSO-d6中の1H NMRは、生成物の構造と一致していた。
BOC無水物(570mg、2.61mmol)を、DCM(12mL)中の5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(500mg、2.37mmol)及びDMAP(29mg、0.24mmol)の溶液に添加した。反応混合物を室温で一晩撹拌した。反応混合物を減圧下で濃縮し、残渣をDCM(20mL)と水(20mL)に分配した。水性層をDCM(2x15mL)で抽出し、合わせた有機層を相分離器を通して濾過し、次いで減圧下で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(600mg、1.8mmol、収率77%、純度95%)を白色の固体として得た。
無水DMF(3.5mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)カルバメート(200mg、0.64mmol)、2-(クロロメチル)-5,7-ジメチルイミダゾ[1,2-a]ピリミジン(164mg、0.84mmol)及びK2CO3(178mg、1.29mmol)の混合物を、70℃で一晩撹拌した。室温で、EtOAc(20mL)、水(20mL)及びブライン(20mL)を添加した。層を分離し、次いで水性層をEtOAc(3x30mL)で抽出した。合わせた有機層をブライン(3x30mL)で洗浄し、Na2SO4で乾燥させ、減圧下で濃縮した。
UPLC/MS (方法6):m/z 470 (M+H)+, RT 0.80分。
THF(1.7mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((5,7-ジメチルイミダゾ[1,2-a]ピリミジン-2-イル)メチル)カルバメート(96mg、200μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(52mg、220μmol)及びtBuBrettPhos Pd G3(17mg、28.1μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(270μL、270μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。室温で、水(15mL)及びEtOAc(25mL)を添加した。層を分離し、水性層をEtOAc(2x15mL)で抽出した。合わせた有機層を相分離器を通して濾過し、減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%(3:1 EtOAc/EtOH)/イソヘキサン)により精製し、表題化合物(92mg、140μmol、収率66%、純度98%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 664 (M+H)+, RT 1.61分。
塩化水素(ジオキサン中4M)(0.69mL、2.8mmol)を、ジオキサン(0.5mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((5,7-ジメチルイミダゾ[1,2-a]ピリミジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(92mg、0.14mmol)の溶液に添加した。反応混合物を35℃で1時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(40mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(58mg、120μmol、収率86%、純度95%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法4):m/z 464 (M+H)+, RT 0.94分。
1H NMR (500 MHz, DMSO-d6) δ 7.63 (s, 1H), 7.62 - 7.57 (m, 2H), 6.84 (d,J = 1.1 Hz, 1H), 6.77 - 6.71 (m, 1H), 5.37 (s, 1H), 5.31 (s, 1H), 4.57 (d,J = 5.7 Hz, 2H), 3.58 - 3.49 (m, 1H), 3.23 - 3.17 (m, 1H), 3.09 - 3.01 (m, 1H), 2.98 - 2.90 (m, 2H), 2.83 - 2.77 (m, 1H), 2.57 (s, 3H), 2.48 (s, 3H), 2.36 - 2.29 (m, 1H), 2.19 (t,J = 10.8 Hz, 1H), 1.60 - 1.54 (m, 1H), 1.39 - 1.31 (m, 1H), 1.25 - 1.21 (m, 6H), 1.20 - 1.13 (m, 1H). 1H under water.
(3R,4R)-4-(((7-(((7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-044)
(7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メタンアミン(95mg、0.45mmol)を、EtOH(4.0mL)中の5,7-ジクロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン(130mg、0.55mmol)及びDIPEA(0.55mL、3.2mmol)の溶液に添加した。反応混合物を50℃で16時間加熱した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(138mg、0.29mmol、収率64%、純度81%)を黄色の油状物として得た。
UPLC/MS (方法4):m/z 382 (M+H)+, RT 1.57分。
BOC無水物(77mg、351μmol)を、THF(3.0mL)中の5-クロロ-N-((7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メチル)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-アミン(138mg、293μmol)及びDMAP(7.2mg、59μmol)の溶液に添加した。反応混合物を室温で18時間撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(154mg、281μmol、収率96%、純度88%)を黄色の油状物として得た。
UPLC/MS (方法3):m/z 482 (M+H)+, RT 1.87分。
THF(3.0mL)中のtert-ブチル(5-クロロ-3-イソプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メチル)カルバメート(154mg、281μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(71.2mg、309μmol)及びtBuBrettPhos Pd G3(24.0mg、28.1μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(366μL、366μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に2時間加熱した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(139mg、187μmol、収率67%、純度91%)を黄色の固体として得た。
UPLC/MS (方法4):m/z 676 (M+H)+, RT 2.23分。
TFA(0.5mL)を、DCM(1.5mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メチル)アミノ)-3-イソプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(139mg、187μmol)の溶液に添加した。反応混合物を室温で18時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(50mL)で洗浄し、生成物をMeOH中0.7M NH3(50mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(75mg、150μmol、収率80%、純度95%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、褐色の固体として得た。
UPLC/MS (方法3):m/z 476 (M+H)+, RT 0.73分。
1H NMR (400 MHz, DMSO-d6) δ 8.74 (d,J = 7.1 Hz, 1H), 7.67 - 7.58 (m, 2H), 7.47 (d,J = 1.8 Hz, 1H), 6.87 (dd,J = 7.1, 1.9 Hz, 1H), 6.74 (t,J = 6.0 Hz, 1H), 5.35 - 5.27 (m, 1H), 5.25 (s, 1H), 4.66 (d,J = 6.2 Hz, 2H), 3.58 - 3.46 (m, 1H), 3.24 - 3.16 (m, 1H), 3.09 - 3.00 (m, 1H), 3.00 - 2.89 (m, 2H), 2.82 - 2.74 (m, 1H), 2.37 - 2.27 (m, 1H), 2.17 (dd,J = 11.7, 9.9 Hz, 1H), 2.13 - 2.05 (m, 1H), 1.61 - 1.51 (m, 1H), 1.40 - 1.29 (m, 1H), 1.24 (dd,J = 6.9, 4.8 Hz, 6H), 1.21 - 1.12 (m, 1H), 1.11 - 1.02 (m, 2H), 0.88 - 0.82 (m, 2H). 1H under water.
(7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メタンアミン
ジオキサン(15mL)中のエチル7-ブロモ-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-カルボキシレート(400mg、1.48mmol)、フッ化セシウム(675mg、4.44mmol)及びシクロプロピルボロン酸(382mg、4.44mmol)の混合物を、N2で10分間スパージした。PdCl2(dppf)-CH2Cl2付加物(242mg、296μmol)を添加し、N2を、反応混合物を通してさらに10分間バブリングし、その後50℃で16時間加熱した。混合物をセライトを通して濾過し、濾液を水(100mL)で希釈し、次いでEtOAc(3x50mL)で抽出した。合わせた有機層をMgSO4で乾燥させ、真空中で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(274mg、1.1mmol、収率75%、純度94%)を黄色の固体として得た。
UPLC/MS (方法4):m/z 232 (M+H)+, RT 1.00分。
THF(5.0mL)中のエチル7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-カルボキシレート(274mg、1.11mmol)及びNaBH4(42.1mg、1.11mmol)の混合物を、50℃に加熱して17時間撹拌した。混合物をMeOH(5mL)でクエンチし、10分間撹拌した。飽和NH4Cl水溶液(aq)(5mL)を添加し、次いで混合物を飽和NaHCO3水溶液(20mL)及び水(20mL)で希釈した。この水溶液(aq.)をDCM(3x20mL)で抽出し、その後、合わせた有機層をMgSO4で乾燥させ、真空中で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(134mg、0.67mmol、収率60%、純度95%)を白色の固体として得た。
UPLC/MS (方法4):m/z 190 (M+H)+, RT 0.70分。
塩化チオニル(129μL、1.77mmol)を、DCM(7.0mL)中の(7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-2-イル)メタノール(134mg、0.71mmol)の溶液に滴下添加した。混合物を0℃で2時間撹拌した。減圧下で濃縮乾固し、表題化合物(172mg、0.63mmol、収率90%、純度90%)を白色の固体として得た。
UPLC/MS (方法3):m/z 208 (M+H)+, RT 0.60分。
DMF(3.5mL)中の2-(クロロメチル)-7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン-1-イウムクロリド(174mg、641μmol)及びDIPEA(335μL、1.92mmol)の溶液を、アジ化ナトリウム(63mg、962mmol)で処理した。混合物を50℃に加熱し、3時間撹拌した。混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(122mg、540μmol、収率84%、純度95%)を無色の油状物として得た。
UPLC/MS (方法4):m/z 215 (M+H)+, RT 1.01分。
2-(アジドメチル)-7-シクロプロピル-[1,2,4]トリアゾロ[1,5-a]ピリジン(122mg、569μmol)及びトリフェニルホスフィン(179mg、683μmol)を、THF(5.0mL)及び水(0.6mL)に溶解した。混合物を40℃で2時間撹拌し、その後溶媒を真空中で除去した。残渣をSCXのカラム上にロードした。カラムをMeOH(40mL)で洗浄し、生成物をMeOH中0.7M NH3(40mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(95mg、0.45mmol、収率80%、純度90%)を白色の固体として得た。
UPLC/MS (方法4):m/z 189 (M+H)+, RT 0.71分。
(3R,4R)-4-(((3-シクロプロピル-7-(((7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)ピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)ピペリジン-3-オール
(H-APPAMP-045)
(7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン(371mg、332μmol)を、EtOH(2.7mL)中の5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(75mg、329μmol)及びDIPEA(0.46mL、2.63mmol)の溶液に添加した。反応混合物を65℃で1.5時間加熱した。さらなる5,7-ジクロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン(25mg、110μmol)をさらに65℃で1.5時間撹拌した。反応混合物を真空中で濃縮した。カラムクロマトグラフィー(24gカートリッジ、0~100%EtOAc/イソヘキサン)により精製し、表題化合物(155mg、0.36mmol、収率82%、純度96%)をオレンジ色のガム状物として得た。
UPLC/MS (方法5):m/z 415 (M+H)+, RT 1.58分。
BOC無水物(144mg、660μmol)を、THF(8.6mL)中の5-クロロ-3-シクロプロピル-N-((7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メチル)ピラゾロ[1,5-a]ピリミジン-7-アミン(155mg、362μmol)及びDMAP(11mg、90μmol)の溶液に添加した。反応混合物を65℃で一晩撹拌した。反応混合物を減圧下で濃縮した。カラムクロマトグラフィー(12gカートリッジ、0~10%MeOH/DCM)により精製し、表題化合物(157mg、301μmol、収率82%、純度98%)を黄色の固体として得た。
UPLC/MS (方法5):m/z 515 (M+H)+, RT 1.88分。
THF(3.0mL)中のtert-ブチル(5-クロロ-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-7-イル)((7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メチル)カルバメート(156mg、303μmol)、(3R,4R)-tert-ブチル4-(アミノメチル)-3-ヒドロキシピペリジン-1-カルボキシレート(91mg、394μmol)及びtBuBrettPhos Pd G3(52mg、61μmol)の溶液を、N2で10分間脱気した。LiHMDS(THF中1M)(370μL、370μmol)を、バブリングN2下に一回で添加した。バブリングを停止し、反応混合物を60℃に1.5時間加熱した。
UPLC/MS (方法5):m/z 709 (M+H)+, RT 1.75分。
HCl(ジオキサン中4M)(0.58mL、2.31mmol)を、ジオキサン(1.0mL)中のtert-ブチル(3R,4R)-4-(((7-((tert-ブトキシカルボニル)((7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メチル)アミノ)-3-シクロプロピルピラゾロ[1,5-a]ピリミジン-5-イル)アミノ)メチル)-3-ヒドロキシピペリジン-1-カルボキシレート(109mg、154μmol)の溶液に添加した。反応混合物を35℃で2時間撹拌し、真空中で濃縮した。残渣をSCXのカラム上にロードした。カラムをMeOH(20mL)で洗浄し、生成物をMeOH中0.7M NH3(20mL)で溶出した。アンモニア性メタノール溶液を真空中で濃縮し、表題化合物(61mg、110μmol、収率74%、純度95%)を、Et2Oからトリチュレーションして真空下に40℃で一晩乾燥させた後、オフホワイト色の固体として得た。
UPLC/MS (方法5):m/z 509 (M+H)+, RT 1.29分。
1H NMR (400 MHz, DMSO-d6) δ 8.55 (dd,J = 7.2, 0.9 Hz, 1H), 7.83 - 7.76 (m, 4H), 7.65 (t,J = 6.2 Hz, 1H), 7.52 (s, 1H), 7.52 - 7.47 (m, 2H), 7.43 - 7.38 (m, 1H), 7.26 (dd,J = 7.1, 1.9 Hz, 1H), 6.77 - 6.71 (m, 2H), 5.37 - 5.31 (m, 1H), 5.29 (s, 1H), 4.58 (d,J = 6.0 Hz, 2H), 3.58 - 3.47 (m, 1H), 3.24 - 3.16 (m, 1H), 3.09 - 2.99 (m, 1H), 2.91 (dd,J = 11.6, 4.5 Hz, 1H), 2.82 - 2.74 (m, 1H), 2.35 - 2.25 (m, 1H), 2.16 (dd,J = 11.6, 10.0 Hz, 1H), 1.78 - 1.68 (m, 1H), 1.60 - 1.51 (m, 1H), 1.37 - 1.28 (m, 1H), 1.21 - 1.11 (m, 1H), 0.81 - 0.72 (m, 2H), 0.71 - 0.60 (m, 2H). 1H under water.
(7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メタンアミン
エタノール(15mL)中の4-フェニル-2-ピリジンアミン(300μL、2.00mmol)、2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(564mg、2.00mmol)及び炭酸ナトリウム(212mg、2.00mmol)の混合物を、マイクロ波照射下に80℃で2時間加熱した。さらなる2-(3-ブロモ-2-オキソプロピル)イソインドリン-1,3-ジオン(226mg、800μmol)及び炭酸ナトリウム(85mg、800μmol)を添加し、反応混合物をマイクロ波照射下に80℃で1時間加熱した。0℃において、水(20mL)を添加した。結果として得られた固体を濾過により回収し、水(5mL)ですすいだ。固体をDCM(50mL)に溶解し、次いで溶液を相分離器を通して濾過し、濾液を減圧下で濃縮し、固体を得た。Et2O(5x5mL)中でトリチュレーションし、表題化合物(470mg、1.1mmol、収率53%、純度79%)を緑色の固体として得た。
UPLC/MS (方法3):m/z 354 (M+H)+, RT 0.90分。
ヒドラジン水和物(85μL、1.7mmol)を、EtOH(5.2mL)中の2-((7-フェニルイミダゾ[1,2-a]ピリジン-2-イル)メチル)イソインドリン-1,3-ジオン(470mg、1.05mmol)の懸濁液に添加した。この懸濁液を65℃で一晩撹拌した。さらなるヒドラジン水和物(26μL、525μmol)を添加し、混合物を65℃で2時間撹拌した。懸濁液を濾過し、固体をEtOH(15mL)で洗浄した。濾液を減圧下で濃縮した。冷(0℃)TBME(2x5mL)中でトリチュレーションし、表題化合物(371mg、0.33mmol、収率32%、純度20%)を茶色の固体として得た。
UPLC/MS (方法3):m/z 224 (M+H)+, RT 0.47分。
IC 50 アッセイ
材料及び溶液:
- HEPES-NaOH(Sigma、H-3375)
- オルトバナジン酸ナトリウム(Sigma、S-6508)
- DTT (Sigma、D-0632)
- MgCl2 (M-3634)
- MnCl2 (VWR、1.05927.1000)
- PEG-20000 (SERVA、33138)
- ATP (Sigma、A-7699)
- [γ-33P]-ATP (Hartmann Analytic、FF301T)
- H3PO4 (VWR、1.00563.1000)
- NaCl (Merck、1.06404)
- ヒトCDK12 wt/CycK (ProQinase、1483-1484-1 - ロット2)
- RBER-IRStide (ProQinase、0863-0000-1 - ロット036)
- 96ウェルFlashPlates(商標)(PerkinElmer、SMP200)
- ヒトCDK12 wt/CycK(ProQinase、1483-1484-1 - ロット2)
- RBER-IRStide (ProQinase、0863-0000-1 - ロット036)
- ヒトCDK7/CycH/MAT1 (ProQinase、0366-0360-4 - ロット2)。
- RBER-CHKtide (ProQinase、0581-0000-5 - ロット106)。
2つのプロテインキナーゼ(CDK12/CDK7)のキナーゼ活性を測定するため、放射性プロテインキナーゼアッセイ(33PanQinase(登録商標)活性アッセイ)を使用した。全てのキナーゼアッセイは、PerkinElmer社(米国マサチューセッツ州、ボストン)製の96ウェルFlashPlates (商標)中で、50μLの反応容量で行った。
- 20μLのアッセイバッファー(標準バッファー)
- 5μLのATP溶液(H2O中)
- 5μLの試験化合物(10%DMSO中)
- 10μLの基質/10μLの酵素溶液(プレミックス)
- 70mM HEPES-NaOH (pH7.5);
- オルトバナジン酸ナトリウム(3μM);
- PEG-20000 (50μg/mL);
- DTT (1.2mM);
- MgCl2 (3mM);
- MnCl2 (3mM);
- 精製ヒトCDK7/CycH/MAT1 (3.3nM - ロット02);
- RBER-CHKtide基質 (40μg/mL - ロット106);
- ATP (3μM);
- [γ-33P]-ATP (1ウェル当たり約8x105cpm);及び
- DMSOの最終濃度が10%w/wであるような適切な濃度の試験化合物。
- 70mM HEPES-NaOH (pH7.5);
- オルトバナジン酸ナトリウム(3μM);
- PEG-20000 (50μg/mL);
- DTT (1.2mM);
- MgCl2 (3mM);
- MnCl2 (3mM);
- 精製ヒトCDK12wt/CycK(14.7nM - ロット02);
- RBER-IRStide基質(40μg/mL - ロット036);
- ATP(0.3μM);
- [γ-33P]-ATP (1ウェル当たり約8 x 105cpm);及び
- DMSOの最終濃度が10%w/wであるような適切な濃度の試験化合物。
A673細胞を、10μMプロテアソーム阻害剤MG132(Sigma Aldrich社)又はNAE(NEDD8活性化酵素)阻害剤MLN4942(Cell Signalling Technologies社)の存在下又は不存在下で1μM化合物と共に2時間インキュベートした。細胞を、冷リン酸緩衝生理食塩水(PBS、Sigma Aldrich社)で2x洗浄し、続いて溶解バッファーを氷上で15分間添加し、その後回収して遠心分離した。
H-APPAMP化合物を、上記の生物学的方法を用いて評価した。
本発明は例えば以下の態様を含む。
[項1]
以下の式の化合物:
(式中、
-R7は、正確に1、2又は3個の環ヘテロ原子を有する縮合二環式C8-10ヘテロアリール基であり、各環ヘテロ原子はN、S又はOであり;
且つ-R7は、
場合により、炭素上で、1個以上の基-RSCにより置換されており;
場合により、存在する場合は第二級窒素上で、基-RSNにより置換されており;
ここで:
各-RSCは、独立して:
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)OH、-C(=O)ORTT、
-OC(=O)RTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、
-NHC(=O)RTT、-NRTNC(=O)RTT、
-NHC(=O)NH2、-NHC(=O)NHRTT、-NHC(=O)NRTT 2、-NHC(=O)RTM、
-NRTNC(=O)NH2、-NRTNC(=O)NHRTT、-NRTNC(=O)NRTT 2、-NRTNC(=O)RTM、
-NHC(=O)ORTT、-NRTNC(=O)ORTT、
-OC(=O)NH2、-OC(=O)NHRTT、-OC(=O)NRTT 2、-OC(=O)RTM、
-C(=O)RTT、
-SRTT、-S(=O)RTT、-S(=O)2RTT、
-S(=O)NH2、-S(=O)NHRTT、-S(=O)NRTT 2、-S(=O)RTM、
-S(=O)2NH2、-S(=O)2NHRTT、-S(=O)2NRTT 2、-S(=O)2RTM、
-NHS(=O)2RTT、-NRTNS(=O)2RTT、
-CN、又は-NO2
であり、
各-RSNは、独立して:
-RTT、
-LT-OH、-LT-ORTT、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)RTT、
-C(=O)ORTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、又は
-S(=O)2RTT
であり、
各-LT-は、独立して、直鎖又は分岐鎖の飽和C1-4アルキレンであり;
各-RTTは、独立して、-RTT1、-RTT2、-LTT-RTT2、-RTT3、又は-LTT-RTT3であり;
各-RTT1は、独立して、直鎖又は分岐鎖の飽和C1-6アルキルであり、場合により、-F、-OH、及び-ORTTTから選択される1個以上の基で置換されており;
各-RTT2は、飽和C3-6シクロアルキルであり、場合により、-F、-RTTT、-OH、及び-ORTTTから選択される1個以上の基で置換されており;
各-RTT3は、独立して、フェニル又はナフチルであり、場合により、-F、-Cl、-Br、-I、-RTTT、OH、-ORTTT、-OCF3、-NH2、-NHRTTT、及び-NRTTT 2から選択される1個以上の基で置換されており;
各-LTT-は、独立して、直鎖又は分岐鎖の飽和C1-4アルキレンであり;
各-RTNは、直鎖又は分岐鎖の飽和C1-4アルキル、フェニル又はベンジルであり;
各-RTMは、独立して、アゼチジノ、ピロリジノ、ピペリジノ、ピペラジノ、モルホリノ、アゼパノ、又はジアゼパノであり、
場合により、炭素上で、-RTMM、-C(=O)RTMM、-S(=O)2RTMM、-F、-NH2、-NHRTMM、-NRTMM 2、-OH、及び-ORTMMから選択される1個以上の基により置換されており、
場合により、存在する場合は第二級窒素上で、-RTMM、-C(=O)RTMM、-C(=O)ORTMM、及び-S(=O)2RTMMから選択される基により置換されており;
各-RTTTは、独立して、直鎖又は分岐鎖の飽和C1-4アルキル、フェニル又はベンジルであり;
各-RTMMは、独立して、直鎖又は分岐鎖の飽和C1-4アルキル、フェニル又はベンジルであり;
またここで
-L7-は、独立して、直鎖又は分岐鎖の飽和C1-3アルキレンであり、場合により、-F、-OH、及び-OMeから選択される1個以上の基で置換されており;
-R3は、独立して、-R3A又は-R3Bであり;
-R3Aは、独立して、直鎖又は分岐鎖の飽和C1-6アルキルであり、場合により、-F、-OH、及び-OMeから選択される1個以上の基で置換されており;
-R3Bは、独立して、飽和C3-7シクロアルキルであり、場合により、-F、-OH、及び-OMeから選択される1個以上の基で置換されている)。
[項2]
-R7が、正確に、1、2又は3個の環ヘテロ原子を有する縮合二環式C9-10ヘテロアリール基であり、各環ヘテロ原子がNである、項1に記載の化合物。
[項3]
-R7が、正確に、1、2又は3個の環ヘテロ原子を有する縮合二環式C9ヘテロアリール基であり、各環ヘテロ原子がNである、項1に記載の化合物。
[項4]
-R7が、独立して、イミダゾ[1,2-a]ピリジニル、イミダゾ[1,2-a]ピリミジニル、ベンズイミダゾリル、イミダゾ[1,2-b]ピリダジニル、又は[1,2,4]トリアゾロ[1,5-a]ピリジニルである、項1に記載の化合物。
[項5]
-R7が、イミダゾ[1,2-a]ピリジニルである、項1に記載の化合物。
[項6]
-R7が、独立して、2-イミダゾ[1,2-a]ピリジニル、又は3-イミダゾ[1,2-a]ピリジニルである、項1に記載の化合物。
[項7]
-R7が、2-イミダゾ[1,2-a]ピリジニルである、項1に記載の化合物。
[項8]
-R7が、イミダゾ[1,2-a]ピリミジニルである、項1に記載の化合物。
[項9]
-R7が、2-イミダゾ[1,2-a]ピリミジニルである、項1に記載の化合物。
[項10]
-R7がベンゾフラニルである、項1に記載の化合物。
[項11]
-R7が、イミダゾ[2,1-b]チアゾリルである、項1に記載の化合物。
[項12]
-R7がキノリニルである、項1に記載の化合物。
[項13]
各-RSCが、存在する場合、独立して:
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-LT-OH、-LT-ORTT、
-CF3、-CHF2、-OCF3、-OCHF2、
-NH2、-NHRTT、-NRTT 2、-RTM、
-LT-NH2、-LT-NHRTT、-LT-NRTT 2、-LT-RTM、
-C(=O)OH、-C(=O)ORTT、
-OC(=O)RTT、
-C(=O)NH2、-C(=O)NHRTT、-C(=O)NRTT 2、-C(=O)RTM、
-NHC(=O)RTT、
-C(=O)RTT、
-S(=O)2NH2、-S(=O)2NHRTT、-S(=O)2NRTT 2、-S(=O)2RTM、
-NHS(=O)2RTT、
-CN、又はNO2
である、項1~12のいずれか1項に記載の化合物。
[項14]
各-RSCが、存在する場合、独立して:
-RTT、
-F、-Cl、-Br、-I、
-OH、-ORTT、
-CF3、-CHF2、-OCF3、又は-OCHF2
である、項1~12のいずれか1項に記載の化合物。
[項15]
各-RSNが、存在する場合、独立して
-RTT、
-C(=O)RTT、又は
-C(=O)ORTT
である、項1~14のいずれか1項に記載の化合物。
[項16]
各-RSNが、存在する場合、-RTTである、項1~14のいずれか1項に記載の化合物。
[項17]
各-LT-が、存在する場合、-CH2-である、項1~16のいずれか1項に記載の化合物。
[項18]
各-RTTが、存在する場合、-RTT1である、項1~17のいずれか1項に記載の化合物。
[項19]
各-RTT1が、存在する場合、独立して、-Me、-Et、-nPr、-iPr、-nBu、-sBu、-iBu、又は-tBuである、項1~18のいずれか1項に記載の化合物。
[項20]
各-RTT1が、存在する場合、-Meである、項1~18のいずれか1項に記載の化合物。
[項21]
各-RTT2が、存在する場合、独立して、シクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである、項1~20のいずれか1項に記載の化合物。
[項22]
各-RTT2が、存在する場合、シクロプロピルである、項1~20のいずれか1項に記載の化合物。
[項23]
各-RTT3が、存在する場合、フェニルであり、場合により、-F、-Cl、-Br、-I、-RTTT、OH、-ORTTT及び-OCF3から選択される1個以上の基で置換されている、項1~22のいずれか1項に記載の化合物。
[項24]
各-LTT-が、存在する場合、独立して、-CH2-、-CH2CH2-、又は-CH2CH2CH2-である、項1~23のいずれか1項に記載の化合物。
[項25]
各-RTNが、存在する場合、-Meである、項1~24のいずれか1項に記載の化合物。
[項26]
各-RTMが、存在する場合、独立して、ピロリジノ、ピペリジノ、ピペラジノ、又はモルホリノであり、
場合により、炭素上で、-RTMMから選択される1個以上の基により置換されており、
場合により、存在する場合は第二級窒素上で、-RTMM、-C(=O)RTMM、及び-C(=O)ORTMMから選択される基により置換されている、
項1~25のいずれか1項に記載の化合物。
[項27]
各-RTTTが、存在する場合、-Meである、項1~26のいずれか1項に記載の化合物。
[項28]
各-RTMMが、存在する場合、-Meである、項1~27のいずれか1項に記載の化合物。
[項29]
-L7-が、独立して、-CH2-、-CH(CH3)-、-C(CH3)2-、又は-CH(CH2CH3)-である、項1~28のいずれか1項に記載の化合物。
[項30]
-L7-が、-CH2-である、項1~28のいずれか1項に記載の化合物。
[項31]
-R3が、-R3Aである、項1~30のいずれか1項に記載の化合物。
[項32]
-R3が、-R3Bである、項1~31のいずれか1項に記載の化合物。
[項33]
-R3Aが、存在する場合、独立して、-Me、-Et、-nPr、又は-iPrである、項1~32のいずれか1項に記載の化合物。
[項34]
-R3Aが、存在する場合、-iPrである、項1~32のいずれか1項に記載の化合物。
[項35]
-R3Bが、存在する場合、独立して、シクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである、項1~34のいずれか1項に記載の化合物。
[項36]
-R3Bが、存在する場合、独立して、シクロプロピル又はシクロブチルである、項1~34のいずれか1項に記載の化合物。
[項37]
以下の式の化合物:
H-APPAMP-001~H-APPAMP-045
並びにその薬学的に許容される塩、水和物及び溶媒和物から選択される、項1に記載の化合物。
[項38]
項1~37のいずれか1項に記載の化合物、及び薬学的に許容される担体若しくは希釈剤を含む組成物。
[項39]
項1~37のいずれか1項に記載の化合物と、薬学的に許容される担体若しくは希釈剤とを混合するステップを含む、組成物の調製方法。
[項40]
In vitro又はin vivoで、細胞におけるサイクリン依存性プロテインキナーゼ(CDK)(例えばCDK12及び/又はCDK13)機能を阻害する方法であって、前記細胞と、有効量の項1~37のいずれか1項に記載の化合物とを接触させることを含む、前記方法。
[項41]
In vitro又はin vivoで、細胞増殖(例えば、細胞の増殖)を制御する(例えば阻害する)か、細胞周期の進行を阻害するか、アポトーシスを促進するか、又はこれらのうちの1つ以上の組み合わせを行う方法であって、細胞と、有効量の項1~37のいずれか1項に記載の化合物とを接触させることを含む、前記方法。
[項42]
療法による人体又は動物体の治療方法における使用のための、項1~37のいずれか1項に記載の化合物。
[項43]
障害の治療方法における使用のための、項1~37のいずれか1項に記載の化合物。
[項44]
障害の治療方法における使用のための医薬の製造における、項1~37のいずれか1項に記載の化合物の使用。
[項45]
治療を必要とする対象に、治療有効量の項1~37のいずれか1項に記載の化合物を投与することを含む、障害の治療方法。
[項46]
前記障害が、サイクリン依存性プロテインキナーゼ(CDK)(例えばCDK12及び/又はCDK13)に関連する障害;CDK(例えばCDK12及び/又はCDK13)の不適切な活性により生じる障害;CDK(例えばCDK12及び/又はCDK13)変異に関連する障害;CDK(例えばCDK12及び/又はCDK13)過剰発現に関連する障害;CDK(例えばCDK12及び/又はCDK13)の上流経路活性化に関連する障害;又はCDK(例えばCDK12及び/又はCDK13)の阻害により寛解する障害である、項43に記載の使用のための化合物、項44に記載の使用、又は項45に記載の方法。
[項47]
前記障害が、増殖性障害;がん;ウイルス感染症(例えば、HIV);神経変性障害(例えばアルツハイマー病、パーキンソン病);虚血;腎疾患;心血管障害(例えばアテローム性動脈硬化症);自己免疫障害(例えば、関節リウマチ、全身性エリテマトーデス、乾癬、シェーグレン症候群);又は細胞内の翻訳機能不全により引き起こされる障害(例えば、筋ジストロフィー、筋強直性ジストロフィー、筋萎縮性側索硬化症、脊髄性筋萎縮症、脆弱X症候群)である、項43に記載の使用のための化合物、項44に記載の使用、又は項45に記載の方法。
[項48]
前記障害が増殖性障害である、項43に記載の使用のための化合物、項44に記載の使用、又は項45に記載の方法。
[項49]
前記障害ががんである、項43に記載の使用のための化合物、項44に記載の使用、又は項45に記載の方法。
[項50]
前記治療が、アロマターゼ阻害剤であるさらなる活性薬剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項51]
前記アロマターゼ阻害剤が、エキセメスタン(アロマシンとしても知られる)、レトロゾール(フェマーラとしても知られる)、又はアナストロゾール(アリミデックスとしても知られる)である、項50に記載の使用のための化合物、項50に記載の使用、又は項50に記載の方法。
[項52]
前記障害が、乳がん(例えば、前記アロマターゼ阻害剤に耐性のある乳がん)である、項50若しくは51に記載の使用のための化合物、項50若しくは51に記載の使用、又は項50若しくは51に記載の方法。
[項53]
前記治療が、抗エストロゲン剤であるさらなる活性薬剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項54]
抗エストロゲン剤が、フェソロデックス(フルベストラント及びICI182780としても知られる)、タモキシフェン(ノルバデックスとしても知られる)、又はヒドロキシタモキシフェンである、項53に記載の使用のための化合物、項53に記載の使用、又は項53に記載の方法。
[項55]
前記障害が、乳がん(例えば、前記抗エストロゲン剤に耐性のある乳がん)である、項53若しくは54に記載の使用のための化合物、項53若しくは54に記載の使用、又は項53若しくは54に記載の方法。
[項56]
前記治療が、抗アンドロゲン剤であるさらなる活性薬剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項57]
抗アンドロゲン剤が、フルタミド、エンザルタミド、アパルタミド、ビカルタミド、又はニルタミドである、項56に記載の使用のための化合物、項56に記載の使用、又は項56に記載の方法。
[項58]
前記治療が、Her2遮断薬であるさらなる活性薬剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項59]
Her2遮断薬が、ハーセプチン、ペルツズマブ又はラパチニブである、項58に記載の使用のための化合物、項58に記載の使用、又は項58に記載の方法。
[項60]
前記治療が、さらなる細胞傷害性化学療法剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項61]
前記細胞傷害性化学療法剤が、タキサン(例えば、タクソールとしても知られるパクリタキセル;タキソテールとしても知られるドセタキセル)、シクロホスファミド、又は代謝拮抗薬(例えば、カルボプラチン、カペシタビン、ゲムシタビン、ドキソルビシン、エピルビシン、5-フルオロウラシル等)である、項60に記載の使用のための化合物、項60に記載の使用、又は項60に記載の方法。
[項62]
前記治療が、免疫系を刺激する薬剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項63]
前記治療が、チェックポイント阻害剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
[項64]
前記治療が、DNA修復阻害剤による治療(例えば、同時治療又は逐次治療)をさらに含む、項43及び47~49のいずれか1項に記載の使用のための化合物、項44及び47~49のいずれか1項に記載の使用、又は項45~49のいずれか1項に記載の方法。
Claims (18)
- 以下の式の化合物:
(式中、
-R7 は、2-イミダゾ[1,2-a]ピリジニルであり、場合により、炭素上で、1個以上の基-RSCにより置換されており;
各-RSCは、独立して:
-RTT、
-F、-Cl、-Br、-I、
-OH、-OR TT 、
-CF 3 、-CHF2、-OCF3、又は-OCHF 2
であり、
各-RTTは、独立して、-R TT1 又は-R TT2 であり;
各-RTT1は、独立して、直鎖又は分岐鎖の飽和C1-6アルキルであり;
各-RTT2は、飽和C3-6シクロアルキルであり;
-L 7 -は、-CH 2 -であり;
-R3は、飽和C 3-7 シクロアルキルである)。 - 各-R TT1 が、存在する場合、独立して、-Me、-Et、-nPr、-iPr、-nBu、-sBu、-iBu、又は-tBuである、請求項1に記載の化合物。
- 各-R TT1 が、存在する場合、-Meである、請求項1に記載の化合物。
- 各-R TT2 が、存在する場合、独立して、シクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである、請求項1~3のいずれか1項に記載の化合物。
- 各-R TT2 が、存在する場合、シクロプロピルである、請求項1~3のいずれか1項に記載の化合物。
- R 3 が、独立して、シクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである、請求項1~5のいずれか1項に記載の化合物。
- R 3 が、独立して、シクロプロピル又はシクロブチルである、請求項1~5のいずれか1項に記載の化合物。
- R 3 が、シクロプロピルである、請求項1~5のいずれか1項に記載の化合物。
- 請求項1~9のいずれか1項に記載の化合物又はその薬学的に許容される塩若しくは溶媒和物、及び薬学的に許容される担体若しくは希釈剤を含む医薬組成物。
- 請求項1~9のいずれか1項に記載の化合物又はその薬学的に許容される塩若しくは溶媒和物と、薬学的に許容される担体若しくは希釈剤とを混合するステップを含む、医薬組成物の調製方法。
- In vitroで、細胞におけるサイクリン依存性プロテインキナーゼ(CDK)機能を阻害する方法であって、前記細胞と、有効量の請求項1~9のいずれか1項に記載の化合物又はその薬学的に許容される塩若しくは溶媒和物とを接触させることを含む、前記方法。
- In vitroで、細胞増殖を阻害するか、細胞周期の進行を阻害するか、アポトーシスを促進するか、又はこれらのうちの1つ以上の組み合わせを行う方法であって、細胞と、有効量の請求項1~9のいずれか1項に記載の化合物又はその薬学的に許容される塩若しくは溶媒和物とを接触させることを含む、前記方法。
- 請求項1~9のいずれか1項に記載の化合物又はその薬学的に許容される塩若しくは溶媒和物を含む、療法による人体又は動物体の治療方法における使用のための組成物。
- 請求項1~9のいずれか1項に記載の化合物又はその薬学的に許容される塩若しくは溶媒和物を含む、障害の治療方法における使用のための組成物であって、
前記障害が、増殖性障害;がん;ウイルス感染症;神経変性障害;虚血;腎疾患;心血管障害;自己免疫障害;又は細胞内の翻訳機能不全により引き起こされる障害である、前記組成物。 - 前記障害ががんである、請求項15に記載の組成物。
- 前記治療が、
アロマターゼ阻害剤、
抗エストロゲン剤、
抗アンドロゲン剤、
Her2遮断薬、
さらなる細胞傷害性化学療法剤、
免疫系を刺激する薬剤、
チェックポイント阻害剤、又は
DNA修復阻害剤
であるさらなる活性薬剤による治療をさらに含む、請求項16に記載の組成物。 - 前記アロマターゼ阻害剤が、エキセメスタン、レトロゾール、又はアナストロゾールであり、
前記抗エストロゲン剤が、フェソロデックス、タモキシフェン、又はヒドロキシタモキシフェンであり、
前記抗アンドロゲン剤が、フルタミド、エンザルタミド、アパルタミド、ビカルタミド、又はニルタミドであり、
前記Her2遮断薬が、ハーセプチン、ペルツズマブ又はラパチニブであり、
前記細胞傷害性化学療法剤が、パクリタキセル、ドセタキセル、シクロホスファミド、カルボプラチン、カペシタビン、ゲムシタビン、ドキソルビシン、エピルビシン、又は5-フルオロウラシルである、請求項17に記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1918541.2A GB201918541D0 (en) | 2019-12-16 | 2019-12-16 | Therapeutic compounds and their use |
| GB1918541.2 | 2019-12-16 | ||
| PCT/EP2020/086419 WO2021122745A1 (en) | 2019-12-16 | 2020-12-16 | 4-[[(7-aminopyrazolo[1,5-a]pyrimidin-5-yl)amino]methyl]piperidin-3-ol compounds and their therapeutic use |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2023505734A JP2023505734A (ja) | 2023-02-10 |
| JPWO2021122745A5 JPWO2021122745A5 (ja) | 2023-11-13 |
| JP7635237B2 true JP7635237B2 (ja) | 2025-02-25 |
Family
ID=69186648
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022536538A Active JP7635237B2 (ja) | 2019-12-16 | 2020-12-16 | 4-[[(7-アミノピラゾロ[1,5-a]ピリミジン-5-イル)アミノ]メチル]ピペリジン-3-オール化合物及びそれらの治療的使用 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US12473303B2 (ja) |
| EP (1) | EP4077330A1 (ja) |
| JP (1) | JP7635237B2 (ja) |
| CN (1) | CN114929708B (ja) |
| AU (1) | AU2020406056A1 (ja) |
| CA (1) | CA3159835A1 (ja) |
| GB (1) | GB201918541D0 (ja) |
| WO (1) | WO2021122745A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113387947B (zh) * | 2021-07-12 | 2022-07-01 | 中国科学院成都生物研究所 | 调节雌激素受体合成活性的吡唑并吡啶衍生物 |
| WO2023107705A1 (en) | 2021-12-10 | 2023-06-15 | Incyte Corporation | Bicyclic amines as cdk12 inhibitors |
| CN120712267A (zh) * | 2023-02-21 | 2025-09-26 | 杭州德睿智药科技有限公司 | 作为CDKs抑制剂的新型并杂环类新化合物及其应用 |
| WO2025110815A1 (ko) * | 2023-11-24 | 2025-05-30 | 아이리드비엠에스 주식회사 | CDK 억제제로서 이미다조[1,2-b]피리다진 계열의 신규 화합물 및 이의 용도 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017506250A (ja) | 2014-02-21 | 2017-03-02 | キャンサー・リサーチ・テクノロジー・リミテッド | Cdk阻害剤としてのピラゾロ[1,5‐a]ピリミジン‐5,7‐ジアミン化合物及びその治療用途 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE60043397D1 (de) | 1999-12-28 | 2010-01-07 | Pharmacopeia Inc | Cytokine, insbesondere tnf-alpha, hemmer |
| EP1537116B1 (en) | 2002-09-04 | 2010-06-02 | Schering Corporation | Pyrazolopyrimidines suitable for the treatment of cancer diseases |
| JP2006516573A (ja) | 2003-01-31 | 2006-07-06 | メルク エンド カムパニー インコーポレーテッド | 糖尿病の治療および予防のためのジペプチジルペプチダーゼ阻害薬としての3−アミノ−4−フェニルブタン酸誘導体 |
| CA2516824A1 (en) | 2003-02-28 | 2004-09-10 | Teijin Pharma Limited | Pyrazolo[1,5-a]pyrimidine derivatives |
| EP1608652A1 (en) | 2003-03-31 | 2005-12-28 | Vernalis (Cambridge) Limited | Pyrazolopyrimidine compounds and their use in medicine |
| JO2478B1 (en) | 2003-06-19 | 2009-01-20 | جانسين فارماسوتيكا ان. في. | (Aminomethyl) -biperidine benzamides as 5 HT4 antagonists |
| AU2008261027A1 (en) | 2007-06-05 | 2008-12-11 | Emory University | Selective inhibitors for cyclin-dependent kinases |
| US8591943B2 (en) | 2009-04-09 | 2013-11-26 | Merck Sharp & Dohme Corp. | Pyrazolo[1,5-a]pyrimidine derivatives as mTOR inhibitors |
| PL2509602T3 (pl) | 2009-12-04 | 2017-08-31 | Senhwa Biosciences, Inc. | Pirazolopirymidyny i podobne heterocykle jako inhibitory ck2 |
| WO2012059932A1 (en) | 2010-11-01 | 2012-05-10 | Aurigene Discovery Technologies Limited | 2, 4 -diaminopyrimidine derivatives as protein kinase inhibitors |
| EP2634189A1 (en) * | 2012-03-01 | 2013-09-04 | Lead Discovery Center GmbH | Pyrazolo-triazine derivatives as selective cyclin-dependent kinase inhibitors |
| EP2634190A1 (en) * | 2012-03-01 | 2013-09-04 | Lead Discovery Center GmbH | Pyrazolo-triazine derivatives as selective cyclin-dependent kinase inhinitors |
| US20200197392A1 (en) | 2017-08-15 | 2020-06-25 | The Brigham & Women's Hospital, Inc. | Compositions and methods for treating tuberous sclerosis complex |
| GB201715194D0 (en) | 2017-09-20 | 2017-11-01 | Carrick Therapeutics Ltd | Compounds and their therapeutic use |
| WO2019144149A2 (en) | 2018-01-22 | 2019-07-25 | Fred Hutchinson Cancer Research Center | Treatment methods for pancreatic tumors associated with the worst prognosis |
| CN112313235A (zh) | 2018-04-11 | 2021-02-02 | 奎利恩特有限公司 | 作为周期蛋白依赖性激酶的选择性抑制剂的吡唑并-三嗪和/或吡唑并-嘧啶衍生物 |
| AU2019250504B2 (en) * | 2018-04-11 | 2023-05-18 | Lead Discovery Center Gmbh | Pharmaceutically active pyrazolo-triazine and/or pyrazolo-pyrimidine derivatives |
| WO2019217421A1 (en) | 2018-05-08 | 2019-11-14 | The Scripps Research Institute | Small molecule inhibitors of cdk12/cdk13 |
-
2019
- 2019-12-16 GB GBGB1918541.2A patent/GB201918541D0/en not_active Ceased
-
2020
- 2020-12-16 WO PCT/EP2020/086419 patent/WO2021122745A1/en not_active Ceased
- 2020-12-16 US US17/785,511 patent/US12473303B2/en active Active
- 2020-12-16 CA CA3159835A patent/CA3159835A1/en active Pending
- 2020-12-16 JP JP2022536538A patent/JP7635237B2/ja active Active
- 2020-12-16 EP EP20841892.1A patent/EP4077330A1/en active Pending
- 2020-12-16 CN CN202080086870.9A patent/CN114929708B/zh active Active
- 2020-12-16 AU AU2020406056A patent/AU2020406056A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017506250A (ja) | 2014-02-21 | 2017-03-02 | キャンサー・リサーチ・テクノロジー・リミテッド | Cdk阻害剤としてのピラゾロ[1,5‐a]ピリミジン‐5,7‐ジアミン化合物及びその治療用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| US12473303B2 (en) | 2025-11-18 |
| US20230144197A1 (en) | 2023-05-11 |
| WO2021122745A1 (en) | 2021-06-24 |
| CA3159835A1 (en) | 2021-06-24 |
| EP4077330A1 (en) | 2022-10-26 |
| JP2023505734A (ja) | 2023-02-10 |
| CN114929708B (zh) | 2025-02-18 |
| GB201918541D0 (en) | 2020-01-29 |
| CN114929708A (zh) | 2022-08-19 |
| AU2020406056A1 (en) | 2022-06-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7635237B2 (ja) | 4-[[(7-アミノピラゾロ[1,5-a]ピリミジン-5-イル)アミノ]メチル]ピペリジン-3-オール化合物及びそれらの治療的使用 | |
| JP7029388B2 (ja) | 抗がん活性を有するmdm2-p53相互作用のイソインドリノン阻害剤 | |
| CN114948963A (zh) | 蛋白激酶抑制剂苯并内酰胺化合物 | |
| EP3380474B1 (en) | Janus kinases inhibitors, compositions thereof and use thereof | |
| JP7806100B2 (ja) | CDK阻害剤としての置換ピラゾロ[1,5-a]ピリミジン-7-アミン化合物及びその治療的使用 | |
| TW201722914A (zh) | 醫藥化合物 | |
| TW201838981A (zh) | 嘧啶基-吡啶氧基-萘基化合物以及治療ire1相關之疾病及病症的方法 | |
| CN113508115A (zh) | 吡啶并嘧啶酮和蝶啶酮化合物作为需要酶i(ire i α)的内切核糖核酸酶肌醇的抑制剂用于治疗癌症疾病 | |
| WO2022216680A1 (en) | Nek7 inhibitors | |
| TW201446767A (zh) | 作為磷脂肌醇3-激酶抑製劑之吡咯並三嗪衍生物 | |
| CN112739420A (zh) | 苯氧基-吡啶基-嘧啶化合物及使用方法 | |
| US11731943B2 (en) | Therapeutic compounds, compositions and methods of use thereof | |
| CN110272425A (zh) | 吡啶酰基八氢吡咯并[3,4-c]吡咯衍生物及其用途 | |
| CN117597346A (zh) | Nek7抑制剂 | |
| HK40113584A (zh) | 作为细胞周期蛋白依赖性激酶抑制剂的2-氨基-吡啶或2-氨基-嘧啶衍生物 | |
| HK40098888A (zh) | 通过缀合btk抑制剂与e3连接酶配体降解布鲁顿氏酪氨酸激酶(btk)及其使用方法 | |
| HK40098888B (zh) | 通过缀合btk抑制剂与e3连接酶配体降解布鲁顿氏酪氨酸激酶(btk)及其使用方法 | |
| HK40010369B (zh) | 为jak抑制剂的5-氯-2-二氟甲氧基苯基吡唑并嘧啶化合物 | |
| HK40051446A (en) | Phenoxy-pyridyl-pyrimidine compounds and methods of use | |
| HK40017188B (zh) | Pd-1/pd-l1 抑制剂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20220727 |
|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7426 Effective date: 20220727 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231102 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231102 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240919 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240924 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241218 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20241218 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250212 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7635237 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |