JP7608822B2 - 抗原検出システム、抗原検出キット、及び抗原検出方法 - Google Patents
抗原検出システム、抗原検出キット、及び抗原検出方法 Download PDFInfo
- Publication number
- JP7608822B2 JP7608822B2 JP2020214818A JP2020214818A JP7608822B2 JP 7608822 B2 JP7608822 B2 JP 7608822B2 JP 2020214818 A JP2020214818 A JP 2020214818A JP 2020214818 A JP2020214818 A JP 2020214818A JP 7608822 B2 JP7608822 B2 JP 7608822B2
- Authority
- JP
- Japan
- Prior art keywords
- antigen
- enzyme
- unit
- labeled antibody
- detection
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
酵素標識抗体を含んでいてもよい導入ユニットと、
前記酵素標識抗体と反応する抗原アナログが固定された精製ユニットと、
前記酵素標識抗体の酵素と反応する基質が固定された反応ユニットと、
電気信号の増減を検出する検出ユニットとを有する、抗原検出システム。
[2] 前記反応ユニットと前記検出ユニットが同一流路上に存在するものである、[1]に記載の抗原検出システム。
[3] 前記導入ユニットと精製ユニットと前記反応ユニットと前記検出ユニットがこの順に試料液が移動できるように構成されている、[1]または[2]に記載の抗原検出システム。
[4] 前記酵素標識抗体の酵素が、加水分解酵素、及び酸化還元酵素からなる群から選択される少なくとも1種である、[1]~[3]のいずれかに記載の抗原検出システム。
[5] 前記精製ユニットにおいて抗原アナログを固定する担持体が、メンブレンフィルター、イムノクロマトメンブレン、不織布、ろ紙、メッシュ、及び担体微粒子からなる群から選択される少なくとも1種である、[1]~[4]のいずれかに記載の抗原検出システム。
[6] 前記検出ユニットが、少なくとも作用極及び対極を備える電極を有する、[1]~[5]のいずれかに記載の抗原検出システム。
[7] 支持体に固定された[1]~[6]のいずれかに記載の抗原検出システムと、酵素標識抗体とを含む、抗原検出キット。
[8]
[1]~[7]のいずれかに記載の抗原検出システムを用いる抗原検出方法であって、
(1)検出対象物である抗原を含有する試料と酵素標識抗体とを接触させて被検試料を得る第1工程、
(2)第1工程で得られた被検試料と精製ユニットとを接触させて未反応の酵素標識抗体を精製ユニットに捕捉させ、精製試料を得る第2工程、
(3)精製試料と反応ユニットとを接触させて、酵素標識抗体の酵素と基質とを反応させる第3工程、及び
(4)第3工程の反応生成物と検出ユニットとを接触させて生じる電気信号を検出する第4工程
を含む、抗原検出方法。
抗原検出システムは、試料中の検出対象である抗原と、酵素標識抗体とを特異的に結合させて、その結合体中の標識酵素と反応した基質量を測定することにより、検出対象の抗原量を測定することが可能な免疫測定システムであって、以下の四つのユニットを有し、それぞれの部位を順に試料液が移動できるように構成されている。ここで試料液とは、抗原検出システムを移動する全ての液体を包括して指すものとする。
第一の部位は、試料と酵素標識抗体が投入される“導入ユニット”で、第二の部位は、被験試料中の遊離の酵素標識抗体を捕捉する“精製ユニット”で、第三の部位は、標識酵素が基質と反応する“反応ユニット”で、第四の部位は、電流を電極で検出する“検出ユニット”で、以上、四つのユニットから構成されている。
導入ユニットには、いくつかの機能を持たせることができる。一つには、予め酵素標識抗体と混合した被検試料や、まだ酵素標識抗体を混合していない試料を本システムに導入する機能である。その場合、下流に設置する精製ユニット,反応ユニット,検出ユニットは各々の機能は独立していてもよいし、各機能を任意に組み合わせたユニットでもよい。
精製ユニットは、被検試料に含まれる抗原と結合していない遊離の酵素標識抗体を取り除く部位である。抗原と結合していない遊離の酵素標識抗体が存在したまま基質に接触すると、抗原と結合していなくても標識酵素が基質と反応するため、ノイズ発生の原因となり抗原濃度を正確に測定できない。精製ユニットには所定量の抗原アナログが予め固定化されているので、精製ユニットに展開供給される試料液中の遊離の酵素標識抗体を捕捉することができる。
反応ユニットは、抗原と結合している酵素標識抗体を基質と反応させて電極活性物質を生成する部位である。酵素標識抗体と結合した抗原量に比例して生成した電極活性物質が電極上で酸化されるときの電流を検出することにより、抗原を高感度で測定することが可能となる。反応ユニットは後述の検出ユニットと同じ空間に存在してもよい。
検出ユニットは、作用極と対極、または作用極と対極と参照極とからなる電極間に定電圧を印加して電流を測定する測定部を備える。
前記電極としては、電極として機能することができる材料、大きさ及び形状であれば特に限定されることはなく、どのようなものでも用いることができる。電極として、例えば、グラファイト、カーボン、カーボンファブリック、金、白金、銀、銅、アルミニウム等の金属又は合金、SnO2、In2O3、WO3、TiO2等導電性酸化物等の単層又は2以上の積層構造が挙げられる。この電極は、導電材料片を基板上に貼り付けるか、一部を埋設するなどして形成してもよいし、導電剤ペーストを用いたスクリーン印刷法等の印刷法や蒸着、スパッタリングを用いて形成してもよい。
酵素標識抗体を使って電気特性を測定する工程について、詳述する。本発明の酵素標識抗体としては、基質との反応において、ニコチンアミドアデニンジヌクレオチド(NAD)やフラビンアデニンジヌクレオチド(FAD)などの補酵素を必要とするもの、必要としないものの両方とも利用可能で、基質との反応の程度を電気的手法で検出できるものを用いる。電気的手法で検出できるものとしては、酵素反応により分解されると電気化学的に活性化される基質を用いたり、補酵素の共存下で補酵素によって還元される電子伝達物質を用いて当該活性化基質や当該電子伝達物質の電気化学的応答を測定することができるものであればよい。
本発明における試料とは、一般的な臨床検査等における検査対象物を指す。具体的な試料としては、血液(全血、血漿、血清)、リンパ液、唾液、尿、大便、汗、粘液、涙、随液、鼻汁、頸部又は膣の分泌液、精液、胸膜液、羊水、腹水、中耳液、関節液、胃吸引液、組織・細胞等の抽出液や破砕液等の生体液の他、食品、土壌、植物の抽出液や破砕液等の溶液や、河川水、温泉水、飲料水、汚染水等を含むほとんど全ての液体試料が用いられる。本発明では、検出対象物に対して1種類の抗体しか必要としないため、複数のモノクローナル抗体が結合できるような分子量の大きい物質だけでなく、1つのモノクローナル抗体しか結合できない低分子物質(ハプテン)も検出対象物となりうる。
本発明における抗原検出システムで用いる抗原アナログとしては、標識抗体と抗原抗体反応で特異的に結合して結合体を形成するものであれば、その種類は特に限定されない。例えば、カドミウム,ダイオキシンなどの化合物、ウィルスタンパク、ステロイドなどの各種生体分子、低分子抗体、アプタマーなども利用できる。本発明において抗原アナログは抗原検出システムの精製ユニットに固定化される。よって抗原アナログは保存安定性の高いものが好ましい。具体的には、免疫グロブリンA/IgAやクロモグラニンA/CgA等のストレスマーカー、抗炎症サイトカイン等の炎症マーカー等が挙げられる。
酵素標識抗体は、例えばペルオキシダーゼやアルカリフォスファターゼなど、用いる基質と反応する酵素を予め標識した市販の酵素標識抗体試薬が利用できる。また、市販の酵素標識キットを使い、自前の酵素標識抗体を作製してもよい。その場合、アルカリフォスファターゼなどの酵素は、あらかじめスクシンイミジルエステル基やマレイミド基で活性化されており、標的の抗体分子と混合するだけで、標識する抗体分子のアミノ基やチオール基に酵素の標識が簡便にできるキットを使うことができる。例えば、ペルオキシダーゼの場合、同仁化学研究所社製のPeroxidase Labeling Kit-NH2 (製品番号LK11)やPeroxidase Labeling Kit-SH(製品番号LK09)が、アルカリフォスファターゼの場合、Alkaline Phosphatase Labeling Kit-NH2 (製品番号LK12)やAlkaline Phosphatase Labeling Kit-SH(製品番号LK13)を用いると簡便に酵素標識が可能である。
本発明における抗原検出システムの形態としては、例えば、テストストリップ、バイオマーカー検出チップ等、が挙げられる。
支持体の素材としては軽量で廃棄が容易な樹脂であればよく、例えばアクリル、ポリカーボネイト、ポリプロピレン、ポリスチレンなどが望ましい。
抗原検出キットは、少なくとも酵素標識抗体の溶液、または酵素標識抗体を含む導入ユニット、並びに抗原アナログが固定された精製ユニット、基質が固定された反応ユニット、電極を有する検出ユニット、及び吸収ユニットを備える抗原検出システムを含む。抗原検出システムが固定された支持体をさらに含んでもよい。
・メンブレン:イムノクロマト用ニトロセルロースメンブレン(Immunopore RP)、(GEヘルスケア社製,コード番号 78356403)
・抗原アナログ結合フィルター用メンブレン:セルロース混合エステルタイプ メンブレンフィルター、(アドバンテック東洋社製,製品番号A500A090C)
・吸収パッド:イムノクロマト用吸収パッド(CF4)、(GEヘルスケア社製,コード番号8114-2250)
・アルカリフォスファターゼ標識抗イムノグロブリンA抗体:Goat Anti-Human IgA alpha chain (Alkaline Phosphatase) preadsorbed、 (アブカム社製,ab98551)
・イムノグロブリンA抗原:Native Human IgA protein、(アブカム社製,ab91025)
・p-アミノフェニルリン酸(pAPP):4-Aminophenylphosphate Monosodium、(CAS番号.52331-30-3),(エルケーティー ラボラトリーズ/LKT Laboratories社製,製品番号A5030)
・リン酸緩衝生理食塩水(PBS):137mmol/l NaCl, 8.1mmol/l Na2HPO4,2.68mmol/l KCl, 1.47mmol/l KH2PO4 pH7.4
・トリス緩衝生理食塩水(TBS):150mmol/l NaCl, 20mmol/l Tris, pH7.4とpH8.0に調整
・ウシ血清アルブミン(BSA):Bovine Serum Albumin、(CAS番号.9048-46-8)、(シグマ・アルドリッチ社製,カタログ番号A4503)
・ブロッキング試薬:SuperBlock (TBS) Blocking Buffer, (サーモフィシャーサイエンティフィック社製/Thermo Fisher Scientific K.K.,製品番号37535)
・界面活性剤:ポリオキシエチレン(20)ソルビタンモノラウレート,ツイーン(TM)20相当品、(CAS番号.9005-64-5),(和光純薬社製,製品コード番号 167-11515)
・塩化カリウム(KCl):(CAS番号.7447-40-7)、(和光純薬社製,製品番号169-03542)
・作用電極:ポリエチレンナフタレート(PEN)フィルム、帝人デュポンフィルム社製のPENフィルムQ51-A4-188μmの基板上に膜厚50nmで金を真空蒸着した電極 (図3)。
・参照電極:参照電極用銀塩化銀インク(ビー・エイ・エス社製、カタログ番号011464)、作用電極上に参照電極用銀塩化銀インクを滴下し、60℃の乾燥機にて2時間乾燥したもの(図3)。
・電極おさえ:ポリジメチルシロキサン(Polydimethylsiloxane)、東レ・ダウコーニング社製シリコーン・ポッティング材のSILPOTTM 184を使用したシリコン樹脂製シート。樹脂製シートは、SILPOTTM 184の主剤と硬化剤を20:1で混合し、75℃の加温しながら真空ポンプで脱泡後に、樹脂液を5mm×10mm×1mmの型に流し込み、厚みが均一になるように広げ、75℃で1時間静置したもの。
・計測装置:ALS/CH Instruments 電気化学アナライザー ALS704E、ビー・エイ・エス社製。
以下の、ブロッキング工程、基質を保持する工程、抗原アナログを固定する工程、検出器具を組み立てる工程、検出対象の抗原と酵素標識抗体を接触させる工程、メンブレンの電気特性を測定する工程を実施例における電気化学的な生体物質の検出方法とした。
GEヘルスケア社製のイムノクロマト用メンブレン(Immunopore RP)を長さ50mm、幅5mmに裁断した。非特異吸着を抑制するために、ブロッキングバッファーとして、サーモフィシャーサイエンティフィック社製のSuperBlock (TBS) Blocking Buffer溶液(製品番号37535)に界面活性剤のポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を 0.5パーセント添加したメンブレンブロッキングバッファーを調製した。このブロッキングバッファーに裁断したイムノクロマト用メンブレンを浸漬し、プレートミキサー(タイテック社、卓上小型振とう機 マイルドミキサー PR-36)で揺らしながら60分間ブロッキングバッファー中に浸漬してブロッキング処理を施した。
界面活性剤のポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を 0.5パーセント添加した20mM TBS-T(pH8.0)の洗浄液を調製した。この洗浄液に裁断したイムノクロマト用メンブレンを浸漬し、プレートミキサー(タイテック社、卓上小型振とう機 マイルドミキサー PR-36)で揺らしながら30分間メンブレンを洗浄処理した。洗浄液から取り出したメンブレンを4℃の冷蔵庫内にて1晩静置した。
アルカリフォスファターゼの基質であるp-アミノフェニルリン酸(pAPP)を精製水で溶解して100mMのpAPP溶液を調製した。予めブロッキング処理を施したメンブレンの端から20mmのところに、100mM pAPP溶液を2μL滴下し、37℃で2時間静置して基質をメンブレンに保持した。その後、基質を保持したメンブレンは4℃にて使用まで保管した。この基質液を滴下する操作は、メンブレンをブロッキング液に浸漬する前であっても、浸漬した後でもよいが、浸漬後のほうがより高い電気化学シグナルを得ることができるので好ましい。また、基質液を滴下した後は、低温下でそのまま保管してもよいが、滴下した基質を十分乾かす必要がある。
検出対象の抗原と反応しない遊離のアルカリフォスファターゼ標識抗イムノグロブリンA抗体を捕捉するために、以下の方法で予め抗原アナログとしてイムノグロブリンA抗原を裁断したメンブレンフィルターや流路のイムノクロマトメンブレン上に固定した。
メンブレンフィルターに固定する方法では、メンブレンフィルターにセルロース混合エステルタイプ メンブレンフィルター(アドバンテック東洋社,製品番号A500A090C)を使い、5mm×7mmに裁断し、その上に100ng/mLのBSAを含むPBSにて1mg/mLに調整したイムノグロブリンA抗原(Native Human IgA protein、(アブカム社製,ab91025)2μLを4か所、計8μLを滴下した。なお、実施例では、イムノグロブリンA抗原を結合したメンブレンフィルターは、特に非特異吸着を抑制するブロッキング処理を施さなかったが、非特異吸着をさらに抑制したい場合は、適当なブロッキング剤を使いブロッキング処理を施してもよい。また、イムノグロブリンA抗原を結合するメンブレンフィルターには、セルロース混合エステルタイプ以外にも、液体の通過に適当な細孔サイズを有しタンパク分子を結合できるようなPVDFメンブレンや、タンパク分子を結合できるようなビーズ粒子などを充填したカラム等も使用できる。
(1)検出用金電極の作製
図3に示した電極配線を有する検出用金電極は、真空蒸着装置を使ってポリエチレンナフタレート(PEN)フィルム(帝人デュポンフィルム社製、PENフィルムQ51-A4- 188μm)の基板上に50nmの膜厚で金を蒸着した。さらに、図3に示す部位に電極の3配線の内の真中の配線上で、図3にて示すイムノクロマト用メンブレンの流路と接する部分の中央部付近に参照電極用銀塩化銀インク(ビー・エイ・エス社製、カタログ番号 011464)を塗布し、60℃で2時間乾燥した。
シリコン樹脂には、ポリジメチルシロキサン(Polydimethylsiloxane)(東レ・ダウコーニング社製シリコーン・ポッティング材のSILPOT(登録商標) 184)を使用した。SILPOT(登録商標) 184の主剤と硬化剤を20:1で混合し、75℃に加温しながら真空ポンプで脱泡した後に、調製した樹脂液を5mm×10mm×1mmの型に流し込み、厚みが均一になるように広げた。さらに75℃で1時間静置した後に、型から取り出してシリコン樹脂製シートを作製した。
イムノクロマト用吸収パッド(CF4)(GEヘルスケア社製,コード番号8114-2250)を14.7mm×17mmに裁断した。
図1と図2に示したような構成で、アクリル製イムノクロマト用筐体6の上に、予め準備した基質保持イムノクロマトメンブレン2,抗原アナログ結合フィルター7,参照電極用インクを塗布した検出用金電極3,吸水パッド4,基質保持イムノクロマトメンブレン2と検出用金電極3を確実に接触させるためのシリコン樹脂製シート(5mm×10mm×1mm)8を電極裏に、それぞれ装着して本検出器具とした。
抗原アナログ結合フィルターを設置する場所として、実施例1に示す検出器具の試料注入口1の近傍でイムノクロマトメンブレンと接するように配置した。また、実施例2では、イムノクロマトメンブレン端から13mmの位置に抗原アナログを滴下したものを用いる場合は、抗原アナログ結合フィルター7が不要になる。その他、フィルターメンブレンの装着が可能なフィルターホルダーを使用して、試料注入口1に接する部分に設置する場合や、予め試料の前処理工程用の治具としても使用できる。
0.1パーセントのBSAと0.05パーセントのポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を含むTBS(pH8.0)で、試験濃度に調整したイムノグロブリンA抗原溶液11μL と、同じく0.1パーセントのBSAと0.05パーセントのポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を含むTBS(pH8.0)で10μg/mLに調整したアルカリフォスファターゼ標識抗イムノグロブリンA抗体溶液 11μLと、予めTBS(pH8.0)425μLと1M KCl 25μLと精製水50μLを混合したサンプル調製用の溶液22μLとをマイクロチューブ内で混合した試料を各実施例の試験液とした。
図1と図2に示す検出用金電極3の端子と計測装置のALS/CH Instruments 電気化学アナライザー ALS704E(ビー・エイ・エス社)をコネクターケーブルで接続した。
アンペロメトリーi-tテクニックの測定パラメータ:
初期電位(V)=0.15
サンプル間隔(Sec) =0.1
測定時間(Sec) =2e+3
静止時間(Sec) =0
感度(A/V)=1e-6
電流(A)×時間(S)=電荷(C) ・・・式1
試験液中に含まれるイムノグロブリンA抗原の各試験濃度について得られた電荷量を図4に示した。
前述の本実施例における電気化学的な生体物質の検出方法において、未反応のアルカリフォスファターゼ標識抗イムノグロブリンA抗体を捕捉するために、予めイムノグロブリンA抗原をセルロース混合エステル膜に固定した抗原結合フィルターを使用した。
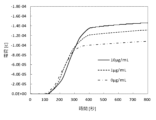
また、0.1パーセントのBSAと0.05パーセントのポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を含むTBS(pH8.0)で、試験濃度が0,1,10,100μg/mLになるように調整したイムノグロブリンA抗原溶液11μL と、同じく0.1パーセントのBSAと0.05パーセントのポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を含むTBS(pH8.0)で10μg/mLに調整したアルカリフォスファターゼ標識抗イムノグロブリンA抗体溶液 11μLと、予めTBS(pH8.0)425μLと1M KCl 25μLと精製水50μLを混合したサンプル調製用の溶液22μLとをマイクロチューブ内で混合した試験液として、本検出器具を使用して電気化学アナライザーで電気化学的に発生した電流値を計測し、式1にて求めた積算値/一定時間に検出できた電荷量(クーロン・C)を図4に示す。図4のように、本発明の電気化学的な生体物質の検出方法においては、0.1μg/mLから100μg/mLの濃度まで検出が可能であり、検出された電荷値(クーロン・C)より、イムノグロブリンA抗原の有無を確認することができ、さらにその濃度も求めることができた。
前述の本実施例における電気化学的な生体物質の検出方法において、未反応のアルカリフォスファターゼ標識抗イムノグロブリンA抗体を捕捉するために、予めイムノグロブリンA抗原を裁断したイムノクロマトメンブレン上で試料注入口側のメンブレンの端から13mmの位置に滴下し、界面活性剤のポリオキシエチレン(20)ソルビタンモノラウレート(ツイーン20相当品)を0.5パーセント添加したサーモフィシャーサイエンティフィック社Super Block溶液にてブロッキング処理を施し、さらにアルカリフォスファターゼの基質であるp-アミノフェニルリン酸(pAPP)をメンブレンの端から23mmのところに滴下したイムノクロマトメンブレンを使用した。また、検出目的のイムノグロブリンA抗原と、アルカリフォスファターゼを標識した抗イムノグロブリンA抗体 10μg/mLと、リン酸緩衝生理食塩水を混合して作られる被検体試験液は実施例1と同じである。図5のように、抗イムノグロブリンA抗原濃度を0,1,10μg/mLでの電荷(クーロン・C)からイムノグロブリンA抗原の有無を確認することができ、さらにその濃度も求めることができた。
実施例1および2で使用した試薬・部材の他に、ミリポア社製のイムノクロマト用ニトロセルロースメンブレン(HF120)や、そのイムノクロマト用メンブレンに固定化する抗原捕捉用抗体として、一次抗体の抗イムノグロブリンA抗体:Anti-Human IgA 抗体 [3B7] (アブカム社製,ab7400)を使用した。
アンペロメトリー(i-t)モードの測定パラメータ:
初期電位(V)=0.15
サンプル間隔(Sec) =0.1
測定時間(Sec) =400
静止時間(Sec) =0
測定値のスケール =1
感度(A/V)=1e-6
Claims (7)
- 抗原と反応する酵素標識抗体を用いる抗原検出システムであって、
酵素標識抗体を含んでいてもよい導入ユニットと、
前記酵素標識抗体と反応する抗原アナログが固定された精製ユニットと、
前記酵素標識抗体の酵素と反応する基質が固定された反応ユニットと、
電気信号の増減を検出する検出ユニットとを有し、
前記抗原アナログと前記基質が一つの担持体上に固定されており、
前記検出ユニットが、作用極及び対極を備える電極を有する、抗原検出システム。 - 前記反応ユニットと前記検出ユニットが同一流路上に存在するものである、請求項1に記載の抗原検出システム。
- 前記導入ユニットと精製ユニットと前記反応ユニットと前記検出ユニットがこの順に試料液が移動できるように構成されている、請求項1または2に記載の抗原検出システム。
- 前記酵素標識抗体の酵素が、加水分解酵素、酸化還元酵素からなる群から選択される少なくとも1種である、請求項1~3のいずれか1項に記載の抗原検出システム。
- 前記精製ユニットにおいて抗原アナログを固定する担持体が、メンブレンフィルター、イムノクロマトメンブレン、不織布、ろ紙、メッシュ、及び担体微粒子からなる群から選択される少なくとも1種である、請求項1~4のいずれか1項に記載の抗原検出システム。
- 支持体に固定された請求項1~5のいずれか1項に記載の抗原検出システムと、酵素標識抗体とを含む、抗原検出キット。
- 請求項1~6のいずれか1項に記載の抗原検出システムを用いる抗原検出方法であって、
(1)抗原を含有する試料と酵素標識抗体とを接触させて被検試料を得る第1工程、
(2)第1工程で得られた被検試料と精製ユニットとを接触させて未反応の酵素標識抗体を精製ユニットに捕捉させ、精製試料を得る第2工程、
(3)精製試料と反応ユニットとを接触させて酵素標識抗体と基質とを反応させる第3工程、及び
(4)第3工程の反応生成物と検出ユニットとを接触させて生じる電気信号を検出する第4工程
を含む、抗原検出方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020214818A JP7608822B2 (ja) | 2020-12-24 | 2020-12-24 | 抗原検出システム、抗原検出キット、及び抗原検出方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020214818A JP7608822B2 (ja) | 2020-12-24 | 2020-12-24 | 抗原検出システム、抗原検出キット、及び抗原検出方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022100694A JP2022100694A (ja) | 2022-07-06 |
| JP7608822B2 true JP7608822B2 (ja) | 2025-01-07 |
Family
ID=82271255
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020214818A Active JP7608822B2 (ja) | 2020-12-24 | 2020-12-24 | 抗原検出システム、抗原検出キット、及び抗原検出方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7608822B2 (ja) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000155122A (ja) | 1998-11-18 | 2000-06-06 | Toyota Central Res & Dev Lab Inc | 微小酸素電極を利用した特異的結合対測定方法 |
| JP2003294680A (ja) | 2002-03-29 | 2003-10-15 | Techno Medica Co Ltd | 電気化学式バイオセンサー |
| JP2007064827A (ja) | 2005-08-31 | 2007-03-15 | Rohm Co Ltd | バイオチップ及び免疫分析方法 |
| JP5097557B2 (ja) | 2005-12-22 | 2012-12-12 | ローム株式会社 | 免疫測定装置及び方法 |
-
2020
- 2020-12-24 JP JP2020214818A patent/JP7608822B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000155122A (ja) | 1998-11-18 | 2000-06-06 | Toyota Central Res & Dev Lab Inc | 微小酸素電極を利用した特異的結合対測定方法 |
| JP2003294680A (ja) | 2002-03-29 | 2003-10-15 | Techno Medica Co Ltd | 電気化学式バイオセンサー |
| JP2007064827A (ja) | 2005-08-31 | 2007-03-15 | Rohm Co Ltd | バイオチップ及び免疫分析方法 |
| JP5097557B2 (ja) | 2005-12-22 | 2012-12-12 | ローム株式会社 | 免疫測定装置及び方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022100694A (ja) | 2022-07-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2930426B2 (ja) | 一又は複数種の競合イムノアッセイを実施するための器具 | |
| JP4040110B2 (ja) | 膜ベースでの検定のための分析装置 | |
| Lin et al. | A nanoparticle label/immunochromatographic electrochemical biosensor for rapid and sensitive detection of prostate-specific antigen | |
| EP0306772B1 (en) | Lateral flow chromatographic binding assay device | |
| US4956302A (en) | Lateral flow chromatographic binding assay device | |
| JP3214854B2 (ja) | カード上での微量分析 | |
| US4746631A (en) | Immunoassay method, device, and test kit | |
| KR101481189B1 (ko) | 분석 장치에의 지시약 고정 | |
| US5435970A (en) | Device for analysis for constituents in biological fluids | |
| JP2504923B2 (ja) | 免疫学的測定方法 | |
| KR101002031B1 (ko) | 직접 면역센서 평가 방법 및 장치 | |
| EP0121385A1 (en) | Conductimetric bioassay techniques | |
| KR101644144B1 (ko) | 향상된 면역분석 센서 | |
| JP4379588B2 (ja) | 高密度リポタンパク質アッセイのデバイスおよび方法 | |
| US20030045001A1 (en) | Immunochromatographic test strip with arcuate sample application zone for ease-of-use in the field | |
| JPS61142463A (ja) | クロマトグラフイ−用装置 | |
| KR890010559A (ko) | 크로마토그래피 결합분석 장치 및 방법 | |
| CA2519402A1 (en) | Adhered membranes retaining porosity and biological activity in assay device for measuring serum cholesterol associated with high-density lipoproteins | |
| US20020164811A1 (en) | Novel method for measurement of glycated hemoglobin by a rapid strip test procedure | |
| JPS63180857A (ja) | 診断装置、その製造方法と使用方法 | |
| CN106796224B (zh) | 测试带组件 | |
| JP3859027B2 (ja) | 乳頭分泌液中の特定物質の測定方法 | |
| JPH10185920A (ja) | アッセイ装置およびそれを用いるアッセイ方法 | |
| US4181501A (en) | Method and apparatus for measuring antibody levels | |
| JP7608822B2 (ja) | 抗原検出システム、抗原検出キット、及び抗原検出方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20210415 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231026 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240419 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240430 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240627 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240820 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241119 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241202 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7608822 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |