JP7586868B2 - 重水素化jak阻害剤による脱毛障害の処置 - Google Patents
重水素化jak阻害剤による脱毛障害の処置 Download PDFInfo
- Publication number
- JP7586868B2 JP7586868B2 JP2022147751A JP2022147751A JP7586868B2 JP 7586868 B2 JP7586868 B2 JP 7586868B2 JP 2022147751 A JP2022147751 A JP 2022147751A JP 2022147751 A JP2022147751 A JP 2022147751A JP 7586868 B2 JP7586868 B2 JP 7586868B2
- Authority
- JP
- Japan
- Prior art keywords
- compound
- day
- pharma
- administered
- acceptable salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2027—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Inorganic Chemistry (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
本出願は、2016年5月4日に出願された米国仮出願第62/331,827号明細書、2016年5月19日に出願された同第62/338,869号明細書、2016年11月7日に出願された同第62/418,774号明細書、2016年11月8日に出願された同第62/419,237号明細書、2016年12月14日に出願された同第62/434,404号明細書、2017年3月2日に出願された同第62/466,358号明細書および2017年5月1日に出願された同第62/492,758号明細書の利益を主張する。上記出願の教示全体が参照により本明細書に組み込まれる。
[1]哺乳動物対象の脱毛障害を処置する方法であって、前記対象に、1日当たり4mg~50mgの範囲の量の、下記構造式:
で表される化合物またはその薬学的に許容される塩を投与することを含む方法。
[2]前記脱毛障害は円形脱毛症である、[1]に記載の方法。
[3]前記対象に、約5mg/日、約10mg/日、約20mg/日、約30mg/日、約40mg/日または約50mg/日の化合物(I)またはその薬学的に許容される塩を投与することを含む[1]または[2]に記載の方法。
[4]前記対象に、約8mg/日、約12mg/日、約16mg/日または約24mg/日の化合物(I)またはその薬学的に許容される塩を投与することを含む[1]~[3]のいずれか一項に記載の方法。
[5]前記化合物を経口投与する、[1]~[4]のいずれか一項に記載の方法。
[6]前記化合物を錠剤である医薬製剤で投与する、[1]~[5]のいずれか一項に記載の方法。
[7]前記化合物を1日当たり1回投与する、[1]~[6]のいずれか一項に記載の方法。
[8]前記化合物を1日当たり2回投与する、[1]~[6]のいずれか一項に記載の方法。
[9]化合物(I)において、重水素に指定されていないあらゆる原子は、この原子の天然の同位体存在度で存在する、[1]~[8]のいずれか一項に記載の方法。
[10]薬学的に許容される担体または希釈剤と、4~50mgの、下記構造式:
で表される化合物またはその薬学的に許容される塩を含む医薬組成物。
[11]約5mg、約10mg、約20mg、約30mg、約40mgまたは約50mgの化合物(I)またはその薬学的に許容される塩を含む[10]に記載の医薬組成物。
[12]前記医薬組成物は経口投与に適している、[10]または[11]に記載の医薬組成物。
[13]前記組成物は錠剤である、[10]または[11]に記載の医薬組成物。
[14]前記組成物を1日当たり1回投与する、[10]~[13]のいずれか一項に記載の医薬組成物。
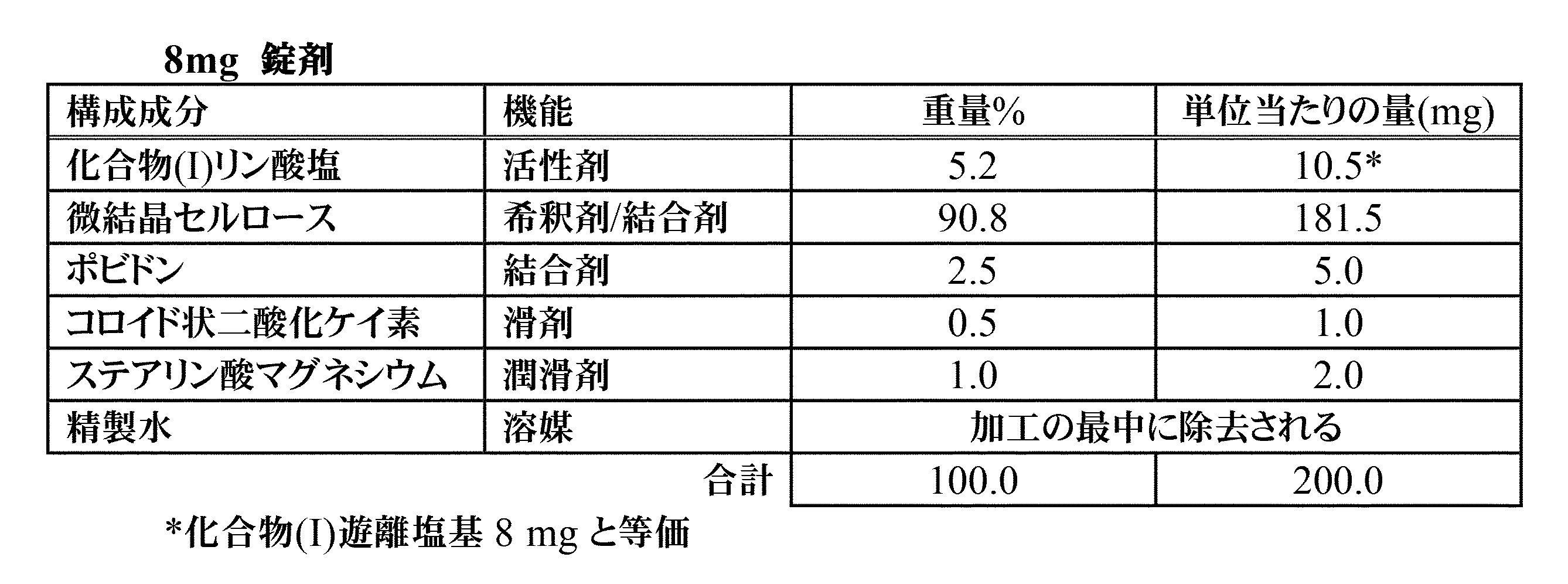
[15]前記組成物は、
(i)約5.2重量%の化合物(I)リン酸塩、
(ii)約90.8重量%の微結晶セルロース、
(iii)約2.5重量%のポビドン、
(iv)約0.5重量%のコロイド状二酸化ケイ素、および
(v)約1.0重量%のステアリン酸マグネシウム
を含む錠剤である、[10]に記載の医薬組成物。
[16]前記組成物は、約10.5mgの化合物(I)リン酸塩を含む200mg錠剤である、[15]に記載の医薬組成物。
[17]前記組成物は、
(i)約5.3重量%の化合物(I)リン酸塩、
(ii)約88.2重量%の微結晶セルロース、
(iii)約5.0重量%のポビドン、
(iv)約0.5重量%のコロイド状二酸化ケイ素、および
(v)約1.0重量%のステアリン酸マグネシウム
を含む錠剤である、[10]に記載の医薬組成物。
[18]前記組成物は、約10.6mgの化合物(I)リン酸塩を含む200mg錠剤である、[17]に記載の医薬組成物。
[19]前記組成物は、
(i)約10.6重量%の化合物(I)リン酸塩、
(ii)約82.9重量%の微結晶セルロース、
(iii)約5.0重量%のポビドン、
(iv)約0.5重量%のコロイド状二酸化ケイ素、および
(v)約1.0重量%のステアリン酸マグネシウム
を含む錠剤である、[10]に記載の医薬組成物。
[20]前記組成物は、約21.1mgの化合物(I)リン酸塩を含む200mg錠剤である、[19]に記載の医薬組成物。
[21]哺乳動物対象の脱毛障害を処置する方法であって、前記対象に、約4mgの、下記構造式:
で表される化合物またはその薬学的に許容される塩を1日当たり2回投与することを含む方法。
[22]化合物(I)を約5.3mgのリン酸塩として1日当たり2回投与する、[21]に記載の方法。
[23]哺乳動物対象の脱毛障害を処置する方法であって、前記対象に、約8mgの、下記構造式:
で表される化合物またはその薬学的に許容される塩を1日当たり2回投与することを含む方法。
[24]化合物(I)を約10.5mgのリン酸塩として1日当たり2回投与する[23]に記載の方法。
[25]哺乳動物対象の脱毛障害を処置する方法であって、前記対象に、約12mgの、下記構造式:
で表される化合物またはその薬学的に許容される塩を1日当たり2回投与することを含む方法。
[26]化合物(I)を約15.8mgのリン酸塩として1日当たり2回投与する、[25]に記載の方法。
[27]哺乳動物対象の脱毛障害を処置する方法であって、前記対象に、約16mgの、下記構造式:
で表される化合物またはその薬学的に許容される塩を1日当たり2回投与することを含む方法。
[28]化合物(I)を約21.1mgのリン酸塩として1日当たり2回投与する、[27]に記載の方法。
[29]前記脱毛障害は円形脱毛症である、[21]~[28]のいずれか一項に記載の方法。
[30]前記化合物を経口投与する、[21]~[29]のいずれか一項に記載の方法。
[31]前記化合物を錠剤である医薬製剤で投与する、[21]~[30]のいずれか一項に記載の方法。
用語「処置する」は、疾患(例えば、本明細書で詳述されている疾患または障害)の発症または進行を低減すること、抑制すること、減弱させること、減少させること、停止させることもしくは安定化させること、この疾患の重症度を低下させること、またはこの疾患と関連する症状を改善することを意味する。例えば、脱毛障害の処置として、毛の再成長、さらなる脱毛の予防、または脱毛速度の低下が挙げられる。
材料および方法:
材料:CYP3A4スーパーソーム(商標)をCorning Gentestから入手した。β-ニコチンアミドアデニンジヌクレオチドホスフェート、還元型(NADPH)、塩化マグネシウム(MgCl2)およびジメチルスルホキシド(DMSO)をSigma-Aldrichから購入した。重水素化試験化合物をConcert Pharmaceuticalsから供給された。
インビトロでのt1/2=0.693/k
k=-[残存する親の%(ln)対インキュベーション時間の直線回帰の傾き]
Microsoft Excel Softwareを使用してデータ解析を実施した。
材料:ヒト肝臓ミクロソーム(20mg/mL)をXenotech,LLC(Lenexa,KS)から入手した。β-ニコチンアミドアデニンジヌクレオチドホスフェート、還元型(NADPH)、塩化マグネシウム(MgCl2)およびジメチルスルホキシド(DMSO)をSigma-Aldrichから購入した。重水素化試験化合物をConcert Pharmaceuticalsから供給された。
インビトロでのt1/2=0.693/k
k=-[残存する親の%(ln)対インキュベーション時間の直線回帰の傾き]
Microsoft Excel Softwareを使用してデータ解析を実施した。
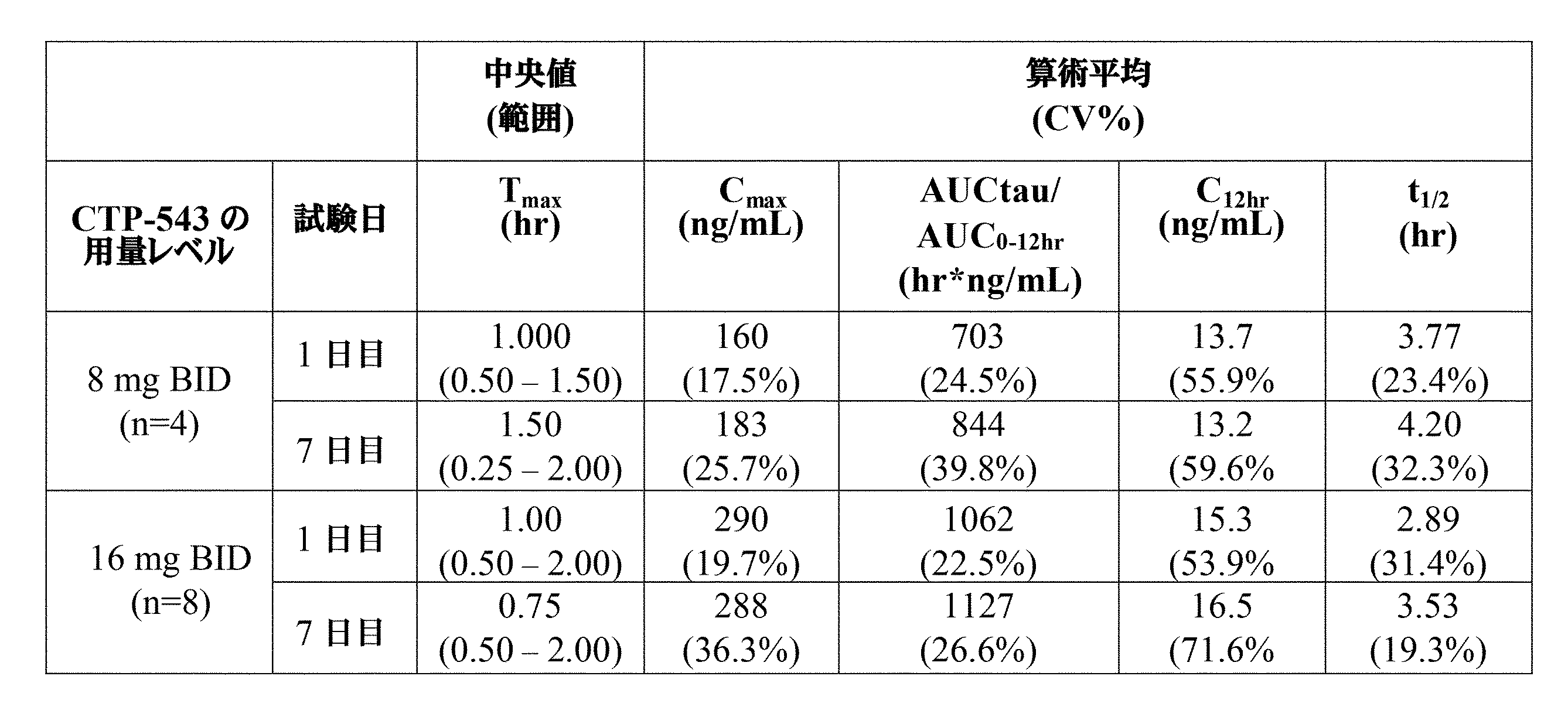
単回漸増用量(SAD)試験:健康なボランティに、絶食条件下で化合物(I)またはプラセボの用量を投与した。この試験の目的は、リン酸塩としての化合物(I)8mg、16mg、32mgまたは48mg(例えば、化合物(I)リン酸塩10.5mgは化合物(I)遊離塩基8mgと等価である)の単回用量の薬物動態を評価することであった。各用量群に関して、6例の対象に化合物(I)を投与し、2例の対象にプラセボを投与した。この試験の設計を図1Aに示す。化合物(I)の代謝産物を分析した。化合物(I)の用量をカプセル中粉末としての化合物(I)リン酸塩として投与し、水と共に投与した。予備的結果を図1Bおよび図1Cに示す。
Claims (26)
- 前記脱毛障害は全身性脱毛症である、請求項1に記載の医薬製剤。
- 前記脱毛障害は完全脱毛症である、請求項1に記載の医薬製剤。
- 前記方法は、前記対象に、約4mgの化合物(I)またはその薬学的に許容される塩を含む医薬製剤を1日当たり2回投与することを含む請求項1~3のいずれか一項に記載の医薬製剤。
- 前記化合物を経口投与する、および/または
前記化合物を錠剤である医薬製剤で投与する、請求項1~4のいずれか一項に記載の医薬製剤。 - 前記化合物を1日当たり1回投与する、請求項1~3のいずれか一項に記載の医薬製剤。
- 前記化合物を1日当たり2回投与する、請求項1~3のいずれか一項に記載の医薬製剤。
- 化合物(I)において、重水素に指定されていないあらゆる原子は、この原子の天然の同位体存在度で存在する、請求項1~7のいずれか一項に記載の医薬製剤。
- 化合物(I)が、1日当たり2回、約5.3mgのリン酸塩として投与される、請求項4に記載の医薬製剤。
- 前記化合物を経口投与する、および/または
前記化合物を錠剤である医薬製剤で投与する、請求項9に記載の医薬製剤。 - 前記脱毛障害は全身性脱毛症である、請求項11に記載の医薬組成物。
- 前記脱毛障害は完全脱毛症である、請求項11に記載の医薬組成物。
- 前記医薬組成物は経口投与に適している、請求項11~13のいずれか一項に記載の医薬組成物。
- 前記組成物は錠剤である、請求項11~14のいずれか一項に記載の医薬組成物。
- 前記組成物は、カプセル剤である、請求項11~14のいずれか一項に記載の医薬組成物。
- 前記組成物を1日当たり1回8mgの前記化合物として投与する、請求項11~16のいずれか一項に記載の医薬組成物。
- 前記組成物を1日当たり2回4mgの前記化合物として投与する、請求項11~16のいずれか一項に記載の医薬組成物。
- 前記組成物は、
(i)約2.6重量%の化合物(I)リン酸塩、
(ii)約90.9重量%の微結晶セルロース、
(iii)約5.0重量%のポビドン、
(iv)約0.5重量%のコロイド状二酸化ケイ素、および
(v)約1.0重量%のステアリン酸マグネシウム
を含む錠剤である、請求項11~13のいずれか一項に記載の医薬組成物。 - 前記組成物は、約5.3mgの化合物(I)リン酸塩を含む200mg錠剤である、請求項19に記載の医薬組成物。
- 重水素と特に指定された化合物(I)の各位置は、少なくとも90%の重水素の組込みを有する、請求項11~20のいずれか一項に記載の医薬組成物。
- 重水素と特に指定された化合物(I)の各位置は、少なくとも95%の重水素の組込みを有する、請求項11~20のいずれか一項に記載の医薬組成物。
- 重水素と特に指定された化合物(I)の各位置は、少なくとも97%の重水素の組込みを有する、請求項11~20のいずれか一項に記載の医薬組成物。
- 重水素と特に指定された化合物(I)の各位置は、少なくとも90%の重水素の組込みを有する、請求項1~10のいずれか一項に記載の医薬製剤。
- 重水素と特に指定された化合物(I)の各位置は、少なくとも95%の重水素の組込みを有する、請求項1~10のいずれか一項に記載の医薬製剤。
- 重水素と特に指定された化合物(I)の各位置は、少なくとも97%の重水素の組込みを有する、請求項1~10のいずれか一項に記載の医薬製剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024195175A JP2025026895A (ja) | 2016-05-04 | 2024-11-07 | 重水素化jak阻害剤による脱毛障害の処置 |
Applications Claiming Priority (16)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662331827P | 2016-05-04 | 2016-05-04 | |
| US62/331,827 | 2016-05-04 | ||
| US201662338869P | 2016-05-19 | 2016-05-19 | |
| US62/338,869 | 2016-05-19 | ||
| US201662418774P | 2016-11-07 | 2016-11-07 | |
| US62/418,774 | 2016-11-07 | ||
| US201662419237P | 2016-11-08 | 2016-11-08 | |
| US62/419,237 | 2016-11-08 | ||
| US201662434404P | 2016-12-14 | 2016-12-14 | |
| US62/434,404 | 2016-12-14 | ||
| US201762466358P | 2017-03-02 | 2017-03-02 | |
| US62/466,358 | 2017-03-02 | ||
| US201762492758P | 2017-05-01 | 2017-05-01 | |
| US62/492,758 | 2017-05-01 | ||
| JP2018557837A JP7145080B2 (ja) | 2016-05-04 | 2017-05-04 | 重水素化jak阻害剤による脱毛障害の処置 |
| PCT/US2017/031142 WO2017192905A1 (en) | 2016-05-04 | 2017-05-04 | Treatment of hair loss disorders with deuterated jak inhibitors |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018557837A Division JP7145080B2 (ja) | 2016-05-04 | 2017-05-04 | 重水素化jak阻害剤による脱毛障害の処置 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024195175A Division JP2025026895A (ja) | 2016-05-04 | 2024-11-07 | 重水素化jak阻害剤による脱毛障害の処置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022171838A JP2022171838A (ja) | 2022-11-11 |
| JP7586868B2 true JP7586868B2 (ja) | 2024-11-19 |
Family
ID=60203616
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018557837A Active JP7145080B2 (ja) | 2016-05-04 | 2017-05-04 | 重水素化jak阻害剤による脱毛障害の処置 |
| JP2022147751A Active JP7586868B2 (ja) | 2016-05-04 | 2022-09-16 | 重水素化jak阻害剤による脱毛障害の処置 |
| JP2024195175A Pending JP2025026895A (ja) | 2016-05-04 | 2024-11-07 | 重水素化jak阻害剤による脱毛障害の処置 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018557837A Active JP7145080B2 (ja) | 2016-05-04 | 2017-05-04 | 重水素化jak阻害剤による脱毛障害の処置 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024195175A Pending JP2025026895A (ja) | 2016-05-04 | 2024-11-07 | 重水素化jak阻害剤による脱毛障害の処置 |
Country Status (21)
| Country | Link |
|---|---|
| US (3) | US10561659B2 (ja) |
| EP (2) | EP4424367A3 (ja) |
| JP (3) | JP7145080B2 (ja) |
| KR (3) | KR20250070139A (ja) |
| CN (1) | CN109069493A (ja) |
| AU (3) | AU2017261286B2 (ja) |
| BR (1) | BR112018072339A2 (ja) |
| CA (1) | CA3022519A1 (ja) |
| DK (1) | DK3452039T3 (ja) |
| ES (1) | ES2988629T3 (ja) |
| FI (1) | FI3452039T3 (ja) |
| HR (1) | HRP20241345T1 (ja) |
| HU (1) | HUE068643T2 (ja) |
| LT (1) | LT3452039T (ja) |
| MX (6) | MX388054B (ja) |
| PL (1) | PL3452039T3 (ja) |
| PT (1) | PT3452039T (ja) |
| RS (1) | RS66006B1 (ja) |
| SI (1) | SI3452039T1 (ja) |
| SM (1) | SMT202400389T1 (ja) |
| WO (1) | WO2017192905A1 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HRP20241345T1 (hr) | 2016-05-04 | 2024-12-20 | Sun Pharmaceutical Industries, Inc. | Liječenje poremećaja gubitka kose deuteriranim inhibitorima jak |
| CN113906032A (zh) * | 2019-02-06 | 2022-01-07 | 康塞特医药品有限公司 | 用于制备对映异构体富集的jak抑制剂的方法 |
| WO2021236139A1 (en) | 2020-05-21 | 2021-11-25 | Concert Pharmaceuticals, Inc. | Novel deuterated jak inhibitor and uses thereof |
| EP4236956A1 (en) * | 2020-10-28 | 2023-09-06 | Sun Pharmaceutical Industries, Inc. | Regimens for the treatment of hair loss disorders with deuterated jak inhibitors |
| CN116916927A (zh) * | 2020-10-28 | 2023-10-20 | 太阳医药工业公司 | 用于用氘化jak抑制剂治疗脱发症的方案 |
| CN112402615A (zh) * | 2020-11-11 | 2021-02-26 | 长沙晶易医药科技有限公司 | 一种用于治疗斑秃的复方外用制剂及其制备方法 |
| AU2022328272A1 (en) | 2021-08-11 | 2024-02-22 | Sun Pharmaceutical Industries, Inc. | Treatment of hair loss disorders with deuterated jak inhibitors |
| WO2023018954A1 (en) | 2021-08-12 | 2023-02-16 | Concert Pharmaceuticals, Inc. | Treatment of jak-inhibition-responsive disorders with prodrugs of jak inhibitors |
| US20250275977A1 (en) | 2022-05-04 | 2025-09-04 | Sun Pharmaceutical Industries, Inc. | Dosage regimens for treatment with deuterated jak inhibitors |
| US12364699B2 (en) * | 2023-10-10 | 2025-07-22 | Sun Pharmaceuticals Industries, Inc. | Method of treating hair loss disorders |
| US12247034B1 (en) * | 2024-04-19 | 2025-03-11 | Sun Pharmaceutical Industries, Inc. | Crystalline form of deuruxolitinib phosphate |
| US20260021047A1 (en) * | 2024-07-19 | 2026-01-22 | Sun Pharmaceutical Industries, Inc. | Oral formulations of deuruxolitinib |
| US20260027120A1 (en) * | 2024-07-25 | 2026-01-29 | Sun Pharmaceutical Industries, Inc. | Methods of treatment of jak inhibition responsive conditions with deuterated jak inhibitors |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014500249A (ja) | 2010-11-02 | 2014-01-09 | ザ トラスティース オブ コロンビア ユニバーシティ インザ シティ オブ ニューヨーク | 脱毛症の治療方法 |
| JP2015117185A (ja) | 2013-12-17 | 2015-06-25 | コンサート ファーマシューティカルズ インコーポレイテッド | ルキソリチニブの重水素化誘導体 |
| US20150239896A1 (en) | 2012-06-15 | 2015-08-27 | Concert Pharmaceuticals, Inc. | Deuterated Derivatives of Ruxolitinib |
| JP2015537030A (ja) | 2012-11-15 | 2015-12-24 | インサイト・コーポレイションIncyte Corporation | ルキソリチニブの徐放性投薬形態 |
| JP7145080B2 (ja) | 2016-05-04 | 2022-09-30 | コンサート ファーマシューティカルズ インコーポレイテッド | 重水素化jak阻害剤による脱毛障害の処置 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9925962D0 (en) | 1999-11-02 | 1999-12-29 | Novartis Ag | Organic compounds |
| BR0209325A (pt) | 2001-05-03 | 2004-07-20 | Hoffmann La Roche | Forma de dosagem farmacêutica de mesilato de nelfinavir amorfo |
| BRPI0516170A (pt) | 2004-09-29 | 2008-08-26 | Cordis Corp | formas de dosagens farmacêuticas estáveis e amorfas de compostos de rapamicina |
| TWI630207B (zh) | 2005-12-13 | 2018-07-21 | 英塞特控股公司 | 作為傑納斯激酶(JANUS KINASE)抑制劑之經雜芳基取代之吡咯并〔2,3-b〕吡啶及吡咯并〔2,3-b〕嘧啶 |
| LT1993360T (lt) | 2005-12-28 | 2017-06-12 | Vertex Pharmaceuticals Incorporated | N-[2,4-bis(1,1-dimetiletil)-5-hidroksifenil]-1,4-dihidro-4-oksochinolin-3-karboksamido kieta forma |
| CL2008001709A1 (es) | 2007-06-13 | 2008-11-03 | Incyte Corp | Compuestos derivados de pirrolo [2,3-b]pirimidina, moduladores de quinasas jak; composicion farmaceutica; y uso en el tratamiento de enfermedades tales como cancer, psoriasis, artritis reumatoide, entre otras. |
| TWI665200B (zh) | 2009-01-15 | 2019-07-11 | 英塞特公司 | 製造jak抑制劑之方法及相關中間化合物 |
| US9198911B2 (en) | 2010-11-02 | 2015-12-01 | The Trustees Of Columbia University In The City Of New York | Methods for treating hair loss disorders |
| PL2830662T3 (pl) | 2012-03-29 | 2019-02-28 | The Trustees Of Columbia University In The City Of New York | Sposoby leczenia zaburzeń utraty włosów |
| BR112015001839A2 (pt) * | 2012-07-30 | 2017-07-04 | Concert Pharmaceuticals Inc | ibrutinibe deuterado |
| CN110229159B (zh) * | 2013-12-18 | 2021-08-24 | 康塞特医药品有限公司 | 卢索替尼的氘代衍生物 |
| WO2015120110A2 (en) * | 2014-02-07 | 2015-08-13 | Auspex Pharmaceuticals, Inc. | Novel pharmaceutical formulations |
-
2017
- 2017-05-04 HR HRP20241345TT patent/HRP20241345T1/hr unknown
- 2017-05-04 KR KR1020257015799A patent/KR20250070139A/ko active Pending
- 2017-05-04 WO PCT/US2017/031142 patent/WO2017192905A1/en not_active Ceased
- 2017-05-04 EP EP24175652.7A patent/EP4424367A3/en active Pending
- 2017-05-04 HU HUE17793380A patent/HUE068643T2/hu unknown
- 2017-05-04 RS RS20241081A patent/RS66006B1/sr unknown
- 2017-05-04 LT LTEPPCT/US2017/031142T patent/LT3452039T/lt unknown
- 2017-05-04 SM SM20240389T patent/SMT202400389T1/it unknown
- 2017-05-04 PL PL17793380.1T patent/PL3452039T3/pl unknown
- 2017-05-04 FI FIEP17793380.1T patent/FI3452039T3/fi active
- 2017-05-04 SI SI201731552T patent/SI3452039T1/sl unknown
- 2017-05-04 KR KR1020237019001A patent/KR102810262B1/ko active Active
- 2017-05-04 CA CA3022519A patent/CA3022519A1/en active Pending
- 2017-05-04 AU AU2017261286A patent/AU2017261286B2/en active Active
- 2017-05-04 ES ES17793380T patent/ES2988629T3/es active Active
- 2017-05-04 CN CN201780027427.2A patent/CN109069493A/zh active Pending
- 2017-05-04 US US16/098,338 patent/US10561659B2/en active Active
- 2017-05-04 PT PT177933801T patent/PT3452039T/pt unknown
- 2017-05-04 DK DK17793380.1T patent/DK3452039T3/da active
- 2017-05-04 EP EP17793380.1A patent/EP3452039B1/en active Active
- 2017-05-04 KR KR1020187034867A patent/KR20190003711A/ko not_active Ceased
- 2017-05-04 MX MX2018013347A patent/MX388054B/es unknown
- 2017-05-04 BR BR112018072339-8A patent/BR112018072339A2/pt not_active Application Discontinuation
- 2017-05-04 JP JP2018557837A patent/JP7145080B2/ja active Active
-
2018
- 2018-10-31 MX MX2023002324A patent/MX2023002324A/es unknown
- 2018-10-31 MX MX2023002323A patent/MX2023002323A/es unknown
- 2018-10-31 MX MX2023002321A patent/MX2023002321A/es unknown
- 2018-10-31 MX MX2021014175A patent/MX2021014175A/es unknown
- 2018-10-31 MX MX2023002325A patent/MX2023002325A/es unknown
-
2019
- 2019-12-05 US US16/704,402 patent/US12076323B2/en active Active
-
2022
- 2022-09-16 JP JP2022147751A patent/JP7586868B2/ja active Active
-
2023
- 2023-02-24 AU AU2023201112A patent/AU2023201112B2/en active Active
-
2024
- 2024-06-26 US US18/755,253 patent/US20240423986A1/en active Pending
- 2024-11-07 JP JP2024195175A patent/JP2025026895A/ja active Pending
-
2025
- 2025-08-06 AU AU2025213576A patent/AU2025213576A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014500249A (ja) | 2010-11-02 | 2014-01-09 | ザ トラスティース オブ コロンビア ユニバーシティ インザ シティ オブ ニューヨーク | 脱毛症の治療方法 |
| US20150239896A1 (en) | 2012-06-15 | 2015-08-27 | Concert Pharmaceuticals, Inc. | Deuterated Derivatives of Ruxolitinib |
| JP2015537030A (ja) | 2012-11-15 | 2015-12-24 | インサイト・コーポレイションIncyte Corporation | ルキソリチニブの徐放性投薬形態 |
| JP2015117185A (ja) | 2013-12-17 | 2015-06-25 | コンサート ファーマシューティカルズ インコーポレイテッド | ルキソリチニブの重水素化誘導体 |
| JP7145080B2 (ja) | 2016-05-04 | 2022-09-30 | コンサート ファーマシューティカルズ インコーポレイテッド | 重水素化jak阻害剤による脱毛障害の処置 |
Non-Patent Citations (3)
| Title |
|---|
| J. Am. Acad. Dermatol.,2016年,Vol.74, No.2,p.1-5(p.370-371) |
| JAMA Dermatology,2016年,Vol.152, No.4,p.490-491 |
| Nat. Med.,2014年,Vol.20, No.9,p.1-17(p.1043-1049) |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7586868B2 (ja) | 重水素化jak阻害剤による脱毛障害の処置 | |
| JP2024531188A (ja) | 重水素化jak阻害剤による脱毛障害の治療 | |
| US20230390292A1 (en) | Regimens for the treatment of hair loss disorders with deuterated jak inhibitors | |
| HK40112813A (en) | Treatment of hair loss disorders with deuterated jak inhibitors | |
| HK40002100A (en) | Treatment of hair loss disorders with deuterated jak inhibitors | |
| US20250275977A1 (en) | Dosage regimens for treatment with deuterated jak inhibitors | |
| OA21444A (en) | Regimens For The Treatment Of Hair Loss Disorders With Deuterated Jak Inhibitors. | |
| OA22110A (en) | Dosage Regimens For Treatment With Deuterated Jak Inhibitors. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221013 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230829 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231113 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20231117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240229 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240513 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240809 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241011 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241107 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7586868 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |