JP7578043B2 - 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 - Google Patents
細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 Download PDFInfo
- Publication number
- JP7578043B2 JP7578043B2 JP2021058006A JP2021058006A JP7578043B2 JP 7578043 B2 JP7578043 B2 JP 7578043B2 JP 2021058006 A JP2021058006 A JP 2021058006A JP 2021058006 A JP2021058006 A JP 2021058006A JP 7578043 B2 JP7578043 B2 JP 7578043B2
- Authority
- JP
- Japan
- Prior art keywords
- cell culture
- region
- hydrophilic
- cell
- culture component
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Immobilizing And Processing Of Enzymes And Microorganisms (AREA)
Description
しかし、本発明者らの検討によれば、特許文献1の細胞培養部材には、培養細胞の接着領域を限定しながら、培養細胞の配向性を制御する点で改善の余地がある。加えて、細胞シート形成用の細胞培養部材には製造時の工業的な量産性も求められる。
本発明は、培養細胞の配向性と接着領域を制御でき、工業的な量産性に優れる細胞シート形成用の細胞培養部材;及びその製造方法;前記細胞シート形成用の細胞培養部材を備えた培養容器;前記細胞シート形成用の細胞培養部材を用いる培養細胞の生産方法;並びに前記細胞シート形成用の細胞培養部材を備えた細胞培養部材付き培養細胞を提供する。
[1] 基材を有する細胞培養部材であって;前記基材の表面に、親水性領域と疎水性領域とが形成され;前記疎水性領域が、前記基材の厚み方向で前記親水性領域に対して相対的に高低差を設けた位置にあり;前記疎水性領域の少なくとも一部に、複数の凸部又は複数の凹部を含む微細凹凸構造領域が形成され;前記細胞培養部材を平面視した際の前記親水性領域の面積と前記疎水性領域の面積との面積和に対する前記疎水性領域の面積の比が、0.02~0.95である、細胞シート形成用の細胞培養部材。
[2] 前記親水性領域と前記疎水性領域との間の高低差が、100nm~10μmである、[1]の細胞シート形成用の細胞培養部材。
[3] 前記複数の凸部の平均高さ又は前記複数の凹部の平均深さが、100nm以上である、[1]又は[2]の細胞シート形成用の細胞培養部材。
[4] 基材を有する細胞培養部材であって;前記基材の表面に、親水性領域と疎水性領域とが形成され;前記疎水性領域の少なくとも一部に、複数の凸部又は複数の凹部を含む微細凹凸構造領域が形成され;前記複数の凸部の平均高さ又は前記複数の凹部の平均深さが、100nm以上であり;前記細胞培養部材を平面視した際の前記親水性領域の面積と前記疎水性領域の面積との面積和に対する前記疎水性領域の面積の比が、0.02~0.95である、細胞シート形成用の細胞培養部材。
[5] 前記親水性領域と前記疎水性領域との間の高低差の絶対値が、0~10μmである、[4]の細胞シート形成用の細胞培養部材。
[6] 前記親水性領域には、親水性コーティング層が設けられている、[1]~[5]のいずれかの細胞シート形成用の細胞培養部材。
[7] 前記親水性領域及び前記疎水性領域の両方に、親水性コーティング層が設けられている、[1]~[6]のいずれかの細胞シート形成用の細胞培養部材。
[8] 前記複数の凸部の平均高さ又は前記複数の凹部の平均深さが、前記親水性コーティング層の厚みより大きい、[1]~[7]のいずれかの細胞シート形成用の細胞培養部材。
[9] 前記疎水性領域の前記微細凹凸構造領域の前記複数の凸部の間の凹部に、又は前記複数の凹部の底部に、親水性層が形成されている、[1]~[8]のいずれかの細胞シート形成用の細胞培養部材。
[10] 前記基材が、ポリエチレンテレフタラート、トリアセチルセルロース、ポリカーボネート、シクロオレフィンポリマー、シクロオレフィンコポリマー、アクリル樹脂、ポリスチレン及びジメチルポリシロキサンからなる群から選ばれる少なくとも1種以上の樹脂を含む、[1]~[9]のいずれかの細胞シート形成用の細胞培養部材。
[11] 基材を有する細胞培養部材の製造方法であって;前記基材の表面に、親水性領域と前記親水性領域より前記基材の厚み方向で相対的に高低差を設けた位置にある疎水性領域とを形成し、かつ、前記疎水性領域に複数の凸部又は複数の凹部を含む微細凹凸構造領域を形成し;次いで、前記表面の全体に親水性付与液を塗布することを特徴とする、細胞シート形成用の細胞培養部材の製造方法。
[12] 前記親水性領域と前記疎水性領域との間の高低差を前記基材の厚み方向で100nm~10μmとする、[11]の細胞シート形成用の細胞培養部材の製造方法。
[13] 前記複数の凸部の平均高さ又は前記複数の凹部の平均深さを100nm以上とする、[11]又は[12]の細胞シート形成用の細胞培養部材の製造方法。
[14] 基材を有する細胞培養部材の製造方法であって;前記基材の表面を、親水性領域と疎水性領域とに区分して、平均高さが100nm以上である複数の凸部又は平均深さが100nm以上である複数の凹部を含む微細凹凸構造領域を前記疎水性領域に形成し;次いで、前記表面の全体に親水性付与液を塗布することを特徴とする、細胞シート形成用の細胞培養部材の製造方法。
[15] 前記親水性領域と前記疎水性領域との間の高低差の絶対値を前記基材の厚み方向で0~10μmとする、[14]の細胞シート形成用の細胞培養部材の製造方法。
[16] [1]~[10]のいずれかの細胞シート形成用の細胞培養部材を備えた、培養容器。
[17] [1]~[10]のいずれかの細胞シート形成用の細胞培養部材を用いて細胞を培養し、次いで、前記細胞シート形成用の細胞培養部材から培養細胞を剥離する、培養細胞の生産方法。
[18] [1]~[10]いずれかの細胞シート形成用の細胞培養部材と;前記細胞培養部材に付着した細胞と;を備えた、細胞培養部材付き培養細胞。
以下、一実施形態に係る細胞シート形成用の細胞培養部材について説明する。以下、本明細書において「一実施形態に係る細胞シート形成用の細胞培養部材」を単に「一実施形態に係る細胞培養部材」と記載する。
基材の全体的な形状は培養細胞、培養細胞の用途に応じて変更してもよい。例えば、培養細胞シートを製造する場合、基材の全体的な形状はシート状が好ましい。全体的な形状がシート状である基材は「シート状基材」と称されることがある。
この親水性、疎水性の表面性状の違いにより、親水性領域と疎水性領域とで細胞の接着性に差異が生じる。したがって、一実施形態に係る細胞培養部材によれば、疎水性領域に細胞を選択的に集合させることができ、疎水性領域にて培養細胞を接着させて接着領域と配向性を制御できる。
一実施形態において、疎水性の基材の表面に微細凹凸構造を形成すると、その表面の接触角は、元の平坦な基材の接触角より大きくなり、さらに疎水性を示すように変化する場合がある。この場合、微細凹凸構造が形成された表面領域を疎水性領域とし、元の平坦な表面領域を親水性領域とする。
親水性材料は、水酸基、カルボニル基、カルボキシ基等の親水性官能基を有するものであれば特に限定されない。例えば、リン脂質類似構造を持つMPCポリマー等の生体適合性ポリマーが挙げられる。細胞毒性が低く、細胞の非特異的接着を抑制できることから、生体適合性ポリマーが好ましい。生体適合性ポリマーの種類は特に限定されないが、例えば、ジメチルポリシロキサン(PDMS)、ポリエチレングリコール(PEG)、オリゴエチレングリコール(OED)、2-メタクリロイルオキシエチルホスホリルコリン(MPC)、ポリ(MPC-co-ブチルメタクリレート)(PMB)、ポリ(MPC-co-ドデシルメタクリレート)(PMD)等が挙げられる。
親水性材料として、PREVELEX(登録商標、日産化学社製)、LIPIDURE(登録商標、日油社製)、RX-6-GBシリーズ、RX-6-GAシリーズ(登録商標、日本触媒社製)等の市販品を使用してもよい。
親水性領域に設けられる親水性コーティング層の厚みは、0.005~0.500μmが好ましく、0.005~0.300μmがより好ましく、0.010~0.100μmがさらに好ましい。親水性コーティング層の厚みが前記数値範囲の下限値以上であると、親水性領域が充分な親水性を示しやすい。親水性コーティング層の厚みが前記数値範囲の上限値以下であると、生産コストを低減しやすい。
比(S2/(S1+S2))が前記上限値以下であるため、親水性領域、疎水性領域の間で細胞に対する接着性の差異が生じ、培養細胞の配向性と接着領域の制御が可能となる。
一実施形態に係る細胞培養部材において、親水性領域が2以上存在する場合、各親水性領域の面積の総和を面積S1とする。また、疎水性領域が2以上存在する場合、各疎水性領域の面積の総和を面積S2とする。
また、親水性領域及び疎水性領域の数は特に限定されない。親水性領域及び疎水性領域は少なくとも1以上それぞれ形成されていればよい。
複数の凸部及び複数の凹部を含む微細凹凸構造(いわゆるモスアイ構造)は、培養時に細胞を支える構造となり得る。そのため微細凹凸構造は、細胞外マトリクスのように細胞の足場として機能し得る。したがって、微細凹凸構造領域は疎水性領域の中でも相対的に高い細胞接着性を示し得る。
疎水性領域の一部に微細凹凸構造領域が形成されている場合には、微細凹凸構造領域の有無によって細胞に対する接着性の差異が疎水性領域の中でも生じ得る。この場合、疎水性領域の中でも微細凹凸構造領域に細胞をさらに選択的に集合させやすくなり、培養細胞の接着領域や配向性の制御がさらに容易となる。
前記平均ピッチが前記数値範囲の下限値以上であると、微細凹凸構造領域を形成しやすく、工業的な量産性がよくなる。前記平均ピッチが前記数値範囲の上限値以下であると、微細凹凸構造領域に対する細胞の接着性がさらによくなる。
親水性層は親水性材料の層である。親水性材料の詳細及び好ましい態様は、親水性コーティング層について説明した内容と同様である。親水性層における親水性材料は親水性コーティング層の親水性材料と同一の材料でもよく、異なる材料でもよい。親水性層における親水性材料が親水性コーティング層の親水性材料と同一であると、工業的な量産性がさらに優れる。
一実施形態に係る細胞培養部材においては、基材の表面に少なくとも1以上の親水性領域と少なくとも1以上の疎水性領域が形成され、当該疎水性領域の少なくとも一部に微細凹凸構造領域が形成されている。そのため、親水性領域と比較して疎水性領域に細胞が相対的に接着しやすく、疎水性領域の中でも微細凹凸構造領域に細胞がさらに接着しやすい。また、疎水性領域の面積の比(S2/(S1+S2))が充分に大きいから、疎水性領域における培養細胞の接着性がよくなり、疎水性領域を細胞の接着領域とすることができる。
加えて、疎水性領域の面積の比(S2/(S1+S2))が過度に大きすぎないから、親水性領域、疎水性領域、微細凹凸構造領域の間で細胞に対する接着性の差異が充分に生じる。
したがって、一実施形態に係る細胞培養部材によれば、培養細胞の配向性と接着領域を制御できる。
第1実施形態に係る細胞培養部材(P1):疎水性領域が基材の厚み方向で親水性領域に対して相対的に高低差を設けた位置にある細胞培養部材。
第2実施形態に係る細胞培養部材(P2):微細凹凸構造領域における複数の凸部の平均高さ又は複数の凹部の平均深さが100nm以上である細胞培養部材。
第1実施形態に係る細胞培養部材(P1)において、疎水性領域は基材の厚み方向で親水性領域より相対的に高低差を設けた位置にある。ここで、疎水性領域の高さ位置は、微細凹凸構造領域の基底面の高さ位置とする。したがって、細胞培養部材(P1)においては、微細凹凸構造領域の基底面が親水性領域の表面より基材の厚み方向で高い位置又は低い位置にある。
したがって、親水性領域及び疎水性領域の形成に際し、親水性付与液を基材の表面の全面に塗工するという一体的な処理が可能となる。その結果、親水性付与液を特定の領域のみに選択塗布する必要性がなくなり、細胞培養部材の生産性が向上し、工業的な量産性が向上する。
一方、複数の凸部の平均高さ又は複数の凹部の平均深さが前記数値範囲の上限値以下であると、微細凹凸構造領域に対する細胞の接着性がさらによくなる。
前記アスペクト比が前記数値範囲の下限値以上であると、微細凹凸構造領域に対する細胞の接着性がさらによくなる。前記アスペクト比が前記数値範囲の上限値以下であると、微細凹凸構造領域を形成しやすく、工業的な量産性がさらによくなる。
第2実施形態に係る細胞培養部材(P2)において、微細凹凸構造領域における複数の凸部の平均高さ又は複数の凹部の平均深さは100nm以上である。
細胞培養部材(P2)においては、微細凹凸構造領域の存在により、製造時に基材の表面の全体に親水性付与液を塗布した後に、親水性付与液は疎水性領域の表面に留まりにくく、親水性領域へと容易に流出する。
加えて、細胞培養部材(P2)において、微細凹凸構造領域における複数の凸部の平均高さ又は複数の凹部の平均深さが100nm以上である。そのため、塗布層の親水性付与液が疎水性領域の微細凹凸構造の高い位置から低い位置に流出することで、複数の凸部の頂部又は複数の凹部の基底面において親水性付与液の塗布層の厚さが薄くなり、細胞が接着しやすくなる。
したがって、親水性領域及び疎水性領域の形成に際し、親水性付与液を基材の表面の全面に塗工するという一体的な処理が可能となる。その結果、細胞培養部材の生産性が向上し、工業的な量産性が優れる。
細胞培養部材(P2)においても、複数の凸部の平均高さ又は複数の凹部の平均深さは細胞培養部材(P1)と同様にして求められる。また、細胞培養部材(P2)における複数の凸部又は複数の凹部のアスペクト比の詳細及び好ましい態様も、細胞培養部材(P1)と同様である。
以下、一実施形態に係る細胞培養部材について実施形態例を例示して適宜図面を参照しながら説明する。ただし、一実施形態に係る細胞培養部材は、以下の実施形態例に限定されない。
図1~図14における寸法比は、説明の便宜上のものであり、実際のものとは異なったものである。また、以下の図面において、同一の構成については同じ符号を用いて示し、重複する構成について説明を省略することがある。
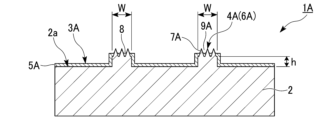
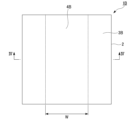
図1は、細胞培養部材の一例を模式的に示す拡大平面図である。図2は、図1のII-II断面図である。
図1、図2に示す細胞培養部材1Aにおいては、基材2の表面2aに親水性領域3Aと疎水性領域4Aとが形成されている。
親水性コーティング層5Aの厚みは、0.005~0.500μmが好ましく、0.005~0.300μmがより好ましく、0.010~0.100μmがさらに好ましい。
微細凹凸構造領域6Aは複数の円錐形状の凸部7Aを含む。微細凹凸構造領域6Aの複数の凸部7Aの間の凹部9Aには、親水性層8が形成されている。
その結果、親水性付与液の塗布層は複数の凸部7Aの頂部ではより薄い膜を形成している。その後、親水性付与液が複数の凸部7Aの間の凹部9Aを部分的に満たした状態で固化すると、疎水性の複数の凸部7Aの頂部と凸部7Aの間の凹部9Aでは厚さの異なる親水化層8が形成される。
親水性層8の厚みは複数の凸部7Aの平均高さより小さい。
微細凹凸構造領域6Aにおいては、複数の凸部7A及び複数の凹部9Aの上側の1/2~1/3には親水性層が付着していない場合もある。また、凸部7Aの側面は親水性層8によって薄く被覆され、凹部9Aの底部に近づくほど、親水性層8が厚くなる。
親水性層8の厚みは複数の凸部7Aの平均高さに対して80%以下が好ましく、50%以下が望ましい。親水性層8の厚みは、凹部9Aにおける最大厚みとする。
加えて細胞培養部材1Aにおいては、培養細胞が帯状の微細凹凸構造領域6Aの凸部7の表面に集まりやすい。そのため培養細胞の配向性を帯状に制御できる。
したがって、親水性領域3A及び疎水性領域4Aの形成に際し、親水性付与液を基材2の表面2aの全面に塗工するという一体的な処理が可能となる。その結果、生産性が向上するから、細胞培養部材1Aは工業的な量産性に優れる。
細胞培養部材1Aにおいて「高低差h」とは、親水性領域3Aにおける基材2の表面2aと疎水性領域4Aにおける微細凹凸構造領域6Aの基底面との間の高さの差とする。
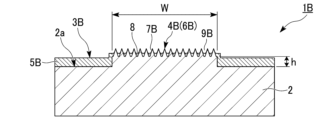
図3は、細胞培養部材の一例を模式的に示す拡大平面図である。図4は、図3のIV-IV断面図である。
図3、4に示す細胞培養部材1Bにおいては、基材2の表面2aに親水性領域3Bと疎水性領域4Bとが形成されている。疎水性領域4Bの外側にそれぞれ親水性領域3Bが形成されている。細胞培養部材1Bにおいて「高低差h」とは、親水性領域3Bにおける基材2の表面2aと疎水性領域4Bにおける微細凹凸構造領域6Bの基底面との間の高さの差とする。
加えて、疎水性領域4Bが基材2の厚み方向で親水性領域3Bより高い位置にあり、疎水性領域4Bには微細凹凸構造領域6Bが形成されているから、製造時に基材の表面の全体に親水性付与液を塗布した後に、親水性付与液が疎水性領域4Bから親水性領域3Bに移行する。
したがって、親水性領域3B及び疎水性領域4Bの形成に際し、親水性付与液を基材2の表面2aの全面に塗工するという一体的な処理が可能となる。その結果、生産性が向上するから、細胞培養部材1Bは工業的な量産性に優れる。
図5は、細胞培養部材の一例を模式的に示す拡大平面図である。図6は、図5のVI-VI断面図である。
図5、図6に示す細胞培養部材1Cは、以下の3点で細胞培養部材1Bと相違し、その他の点では細胞培養部材1Bと共通の構成を備える。
・疎水性領域4Cが、基材2の表面2aより基材2の厚み方向で低い位置にある点。
・微細凹凸構造領域6Cの複数の凸部7Cの平均高さ又は複数の凹部9Cの平均深さが、100nm以上である点。
・親水性コーティング層5Cの厚みが、親水性コーティング層5B(図4)の厚みより小さい点。
細胞培養部材1Cにおいて「高低差h」とは、親水性領域3Cにおける基材2の表面2aと疎水性領域4Cにおける微細凹凸構造領域6Cの基底面との間の高さの差とする。
図7は、細胞培養部材の一例を模式的に示す拡大平面図である。図8は、図7のVIII-VIII断面図である。図7、図8に示す細胞培養部材1Dは、以下の2点で細胞培養部材1Bと相違し、その他の点では細胞培養部材1Bと共通する構成を備える。
・親水性領域3Dに微細凹凸構造領域6Dが形成されている点。
細胞培養部材1Dにおいても、細胞培養部材1Bと同様の作用効果が得られる。
細胞培養部材1Dにおいて「高低差h」とは、親水性領域3Dにおける微細凹凸構造領域6Dの基底面と疎水性領域4Bにおける微細凹凸構造領域6Bの基底面との間の高さの差とする。
図9は、細胞培養部材の一例を模式的に示す拡大平面図である。図10は、図9のX-X断面図である。
図9、図10に示す細胞培養部材1Eは、以下の2点で細胞培養部材1Aと相違し、その他の点では細胞培養部材1Aと共通の構成を備える。
・凹型の微細凹凸構造領域6Eが形成されている点。
・微細凹凸構造領域6Eの複数の凹部9Eの間に親水性層8が形成されている点。
細胞培養部材1Eにおいても、細胞培養部材1Aと同様の作用効果が得られる。
図11は、細胞培養部材の一例を模式的に示す拡大平面図である。図12は、図11のXII-XII断面図である。
図11、図12に示す細胞培養部材1Fは、以下の2点で細胞培養部材1Bと相違し、その他の点では細胞培養部材1Bと共通の構成を備える。
・凹型の微細凹凸構造領域6Fが形成されている点。
・微細凹凸構造領域6Fの複数の凹部9Fの間に親水性層8が形成されている点。
細胞培養部材1Fにおいても、細胞培養部材1Bと同様の作用効果が得られる。
図13は、細胞培養部材の一例を模式的に示す拡大平面図である。図14は、図13のXIV-XIV断面図である。
図13、図14に示す細胞培養部材1Gは、以下の2点で細胞培養部材1Dと相違し、その他の点では細胞培養部材1Dと共通の構成を備える。
・凹型の微細凹凸構造領域6Gが形成されている点。
・微細凹凸構造領域6Gの複数の凹部9の間に親水性層8が形成されている点。
細胞培養部材1Gにおいても、細胞培養部材1Dと同様の作用効果が得られる。
以下、一実施形態に係る細胞培養部材について説明する。
一実施形態に係る細胞培養部材の製造方法は、基材を有する細胞培養部材の製造方法である。基材の詳細及び好ましい態様は一実施形態に係る細胞培養部材の項で説明した内容と同様である。
親水性付与液は親水性材料を少なくとも含む液体である。親水性付与液は基材の表面に親水性を付与できる範囲内であれば、親水性材料以外の成分をさらに含んでもよい。親水性材料の詳細は、一実施形態に係る細胞培養部材の項で説明した内容と同様である。
親水性付与液の塗布後には自然乾燥で親水性付与液を乾燥してもよく、加熱乾燥で親水性付与液を乾燥してもよく、乾燥方法は特に限定されない。
第1実施形態に係る細胞培養部材の製造方法:基材の表面に、親水性領域と親水性領域より基材の厚み方向で高低差を設けた位置にある疎水性領域とを形成し、かつ、疎水性領域に複数の凸部又は複数の凹部を含む微細凹凸構造領域を形成し;次いで、基材の表面の全体に親水性付与液を塗布することを特徴とする細胞培養部材(Q1)の製造方法。
第2実施形態に係る細胞培養部材の製造方法:基材の表面を、親水性領域と疎水性領域とに区分して、疎水性領域に平均高さが100nm以上である複数の凸部を含む微細凹凸構造領域を形成し;次いで、基材の表面の全体に親水性付与液を塗布することを特徴とする、細胞培養部材(Q2)の製造方法。
第1実施形態に係る細胞培養部材の製造方法では、基材の表面に、親水性領域と親水性領域より基材の厚み方向で相対的に高低差を設けた位置にある疎水性領域とを形成し、かつ、疎水性領域に複数の凸部又は複数の凹部を含む微細凹凸構造領域を形成する。そのため、基材の表面の全体に親水性付与液を塗布した後に、親水性付与液が厚み方向で高い位置の領域から低い位置の領域に移行する。
したがって、親水性領域及び疎水性領域の形成に際し、親水性付与液を基材の表面の全面に塗工するという一体的な処理が可能となる。その結果、細胞培養部材の生産性が向上し、工業的な量産性が優れる。
一方、複数の凸部の平均高さを前記数値範囲の上限値以下にすると、細胞培養部材(Q1)を細胞培養に使用した際に微細凹凸構造領域に対する細胞の接着性がさらによくなる。
原版(X1)の作製には、例えば、特開2009-034630号公報に記載のコロイダルシリカからなる単粒子膜エッチングマスクを用いてもよい。当該単粒子膜エッチングマスクを用いた気相エッチングによって基材に微細凹凸構造を均一にかつ高精度で形成できる。
金属層の形成方法としては、例えば、無電解メッキ又は金属蒸着によって金属層を原版(X1)の表面に設け、電解メッキによって金属層の厚さを増加させる方法が挙げられる。ただし、金属層の形成方法はこの方法に何ら限定されない。
また、金属層の材質は特に限定されない。例えば、ニッケル、銅、金、銀、白金、チタン、コバルト、錫、亜鉛、クロム、金コバルト合金、金ニッケル合金、はんだ、銅/ニッケル/クロム合金、錫ニッケル合金、ニッケルパラジウム合金、ニッケル/コバルト/りん合金等が挙げられる。
第2実施形態に係る細胞培養部材の製造方法では、基材の表面を、親水性領域と疎水性領域とに区分して、平均高さが100nm以上である複数の凸部又は平均深さが100nm以上である複数の凹部を含む微細凹凸構造領域を疎水性領域に形成する。
したがって、親水性領域及び疎水性領域の形成に際し、親水性付与液を基材の表面の全面に塗工するという一体的な処理が可能となる。その結果、細胞培養部材の生産性が向上し、工業的な量産性が優れる。
第2実施形態に係る細胞培養部材の製造方法においては、複数の凸部の平均高さ又は複数の凹部の平均深さを100nm以上とするのが好ましく200nm~2μmがより好ましく、400nm~1μmとするのがさらに好ましい。
原版(X2)の作製方法の詳細は複数の凸部の平均高さ又は複数の凹部の平均深さを100nm以上とする点以外は原版(X1)について説明した内容と同様である。
細胞培養部材(Q1)をモールドとして使用することで、細胞培養部材(Q1)の表面形状及び表面構造を反転させて基材に転写して、基材の表面を親水性領域と疎水性領域とに区分できる。この場合、原版(X2)、モールド(Y2)の作製を省略し得る点で工業的な量産性に有利である。
その他、モールド(Y2)の作製方法、使用方法はモールド(Y1)について説明した内容と同様である。
ただし、細胞培養部材(P1)は第1実施形態に係る細胞培養部材の製造方法で好適に製造され得る。また、細胞培養部材(P2)は第2実施形態に係る細胞培養部材の製造方法で好適に製造され得る。細胞培養部材(P1)、細胞培養部材(P2)を製造する場合においては、原版の作製時に面積の比(S2/(S1+S2))を0.02~0.95の範囲内とすればよい。
以下の本明細書の説明において「一実施形態に係る細胞培養部材」とは、少なくとも細胞培養部材(P1)、細胞培養部材(P2)、細胞培養部材(Q1)、細胞培養部材(Q2)を包含する。
一実施形態に係る培養容器は一実施形態に係る細胞培養部材を備えるため、培養細胞の配向性を制御でき、工業的な量産性にも優れる。
培養容器として、例えば、細胞を含む培養液を収容する容器本体の内壁面に細胞培養部材を備えたものが挙げられる。容器本体の内壁面は、培養液と接触し得る面であれば特に限定されず、容器本体の底面でもよく、容器本体の内側の側面でもよい。細胞培養部材は接着剤を介して容器本体の内壁面に設けられていてもよい。
培養プレートのウェルの数は、特に限定されず、培養細胞の用途、使用する分析装置等に応じて設定される。ウェルの平面視の形状は特に限定されない。例えば、真円、楕円、三角形、正方形、長方形、五角形等が挙げられる。ウェルの底面の形状も特に限定されない。平底、丸底、凹凸等が挙げられる。
金属材料としては、ステンレス、銅、鉄、ニッケル、アルミ、チタン、金、銀、白金等が挙げられる。
無機材料としては、各種無機混合物からなるガラス、酸化ケイ素(石英ガラス)、酸化アルミ、酸化チタン、酸化ジルコニウム、酸化鉄、窒化ケイ素等が挙げられる。
一実施形態に係る培養細胞の生産方法では、一実施形態に係る細胞培養部材を用いて、細胞を培養し、次いで、細胞培養部材から培養細胞を剥離する。培養細胞の生産方法では上述の一実施形態に係る細胞培養部材を用いて培養するため、疎水性領域に細胞が集まりやすく、培養細胞の配向性を制御できる。
細胞は特に限定されない。生体内で配向性、形態に基づいた機能を発現し得るものが好適に選択され得る。例えば、筋芽細胞、線維芽細胞、心筋細胞、神経細胞、血管内皮細胞、肝細胞、骨芽細胞、軟骨細胞が挙げられる。
細胞としてiPS細胞等の幹細胞、幹細胞から分化した分化細胞、腫瘍細胞を用いてもよい。
細胞、幹細胞、分化細胞、腫瘍細胞の動物種は特に限定されない。例えば、ヒト、ブタ、マウス、ラット、ウサギ、モルモット、ハムスター、ウシ、ウマ、ネコ、イヌ、ヒツジ、ヤギ等の哺乳類が挙げられる。
コンフルエントになった培養細胞を剥離する際には細胞剥離剤を使用してもよい。細胞剥離剤は、細胞培養に一般的に使用される剥離剤であれば、特に限定されない。
一実施形態に係る細胞培養部材付き培養細胞は、一実施形態に係る細胞培養部材と;細胞培養部材の疎水性領域に付着した培養細胞と;を備える。
一実施形態に係る細胞培養部材付き培養細胞は、上述の細胞培養部材を用いて、細胞が細胞培養部材の表面に付着した状態で培養することで生産したものである。そのため、細胞接着領域や配向性が制御された培養細胞が細胞培養部材の表面に付着し得る。
細胞の種類は特に限定されない。培養細胞の生産方法の項で例示したものと同様の細胞が挙げられる。
特開2009-034630号公報に記載の方法でコロイダルシリカからなる単粒子膜エッチングマスクを一般的なフォトリソグラフィー法を利用したストライプパターン(幅10μm、高さ1μm、フォトレジスト層が10μm間隔で配列)付きSiウェハ上に作製した。この単粒子膜エッチングマスクを用いた気相エッチング法によって微細凹凸構造をSi基板に形成し、残ったフォトレジストを除去することで、複数の平坦部(親水性領域となる)と複数の凸部集合体部(疎水性領域となる)を交互にストライプ状に配列させた凸型のSi製表面微細構造原版(1)を作製した。凸型のSi製表面微細構造原版(1)において、ストライプ状の配列の距離は、平坦部の短軸方向が10μm、凸部集合体部の短軸方向が10μmであった。また、疎水性領域となる凸部集合体部の面積の比(S2/(S1+S2))は0.5であった。また、微細凹凸構造には略円錐形状の複数の凸部が含まれ、複数の凸部の平均ピッチが600nmであり、複数の凸部の平均高さが500nmであった。疎水性領域は親水性領域より低い位置にあり、高低差は、550nmであった。
続いて、凸型のSi製表面微細構造原版(1)から凹型のNi製電鋳スタンパー(1)を作製した。その後、凹型のNi製電鋳スタンパー(1)を用いて、熱ナノインプリント法によって、厚さ150μmのポリスチレンシート表面に載置部となる凸構造を転写し、凸型の樹脂転写部材(1)を作製した。具体的には、厚さ150μmのポリスチレンシートの表面に、凹型のNi製電鋳スタンパー(1)の構造面を対向させ、ナノインプリント装置加圧部にセットした。その状態で昇温を開始し、130℃で5分間、4MPaの加圧を行った。5分間経過後、加圧部を室温まで冷却した後に、凹型のNi製電鋳スタンパー(1)をポリスチレンシートの表面から離型した。
得られた凸型の樹脂転写部材(1)にUVオゾン法により親水化処理を行った後に、PREVELEX AP1(登録商標、日産化学社製)をコーティングし、親水性領域に平均厚み5nmの親水性コーティング層が設けられた実施例1の凸型の細胞培養部材を得た。
実施例1で作製した凸型のSi製表面微細構造原版(1)から熱ナノインプリント法によって、厚さ188μmのシクロオレフィンポリマーフィルム表面に載置部となる凸構造を転写し、凹型の樹脂原版(1)を作製した。凹型の樹脂原版(1)から凸型のNi製電鋳スタンパー(1R)を作製した。その後、凸型のNi製電鋳スタンパー(1R)を用いた以外は、実施例1と同様の作製方法によって実施例2の凹型の細胞培養部材を作製した。
特開2009-034630号公報に記載の方法でコロイダルシリカからなる単粒子膜エッチングマスクを一般的なフォトリソグラフィー法を利用したストライプパターン(幅10μm、高さ1μm、フォトレジスト層が5μm間隔で配列)付きSiウェハ上に作製した。この単粒子膜エッチングマスクを用いた気相エッチング法によって微細凹凸構造をSi基板に形成し、残ったフォトレジストを除去することで、複数の平坦部(親水性領域となる)と複数の凸部集合体部(疎水性領域となる)を交互にストライプ状に配列させた凸型のSi製表面微細構造原版(2)を作製した。凸型のSi製表面微細構造原版(2)において、ストライプ状の配列の距離は、平坦部の短軸方向が10μmであり、凸部集合体部の短軸方向が5μmであった。また、疎水性領域となる凸部集合体部の面積の比(S2/(S1+S2))は0.33であった。また、微細凹凸構造には略円錐形状の複数の凸部が含まれ、複数の凸部の平均ピッチが600nmであり、複数の凸部の平均高さ500nmであった。疎水性領域は親水性領域より低い位置にあり、高低差は、550nmであった。
続いて、凸型のSi製表面微細構造原版(2)から凹型のNi製電鋳スタンパー(2)を作製した。その後、凹型のNi製電鋳スタンパー(2)を用いて、実施例1と同様の作製方法によって、実施例3の凸型の細胞培養部材を作製した。
実施例3で作製した凸型のSi製表面微細構造原版(2)から実施例2と同様の方法で、厚さ188μmのシクロオレフィンポリマーフィルムからなる凹型の樹脂原版(2)を作製した。凹型の樹脂原版(2)から凸型のNi製電鋳スタンパー(2R)を作製した。その後、凸型のNi製電鋳スタンパー(2R)を用いた以外は、実施例1と同様の作製方法によって実施例4の凹型の細胞培養部材を作製した。
特開2009-034630号公報に記載の方法でコロイダルシリカからなる単粒子膜エッチングマスクを一般的なフォトリソグラフィー法を利用したストライプパターン(幅10μm、高さ1μmのフォトレジスト層が10μm間隔で配列)付きSiウェハ上に作製した。この単粒子膜エッチングマスクを用いた気相エッチング法によって微細凹凸構造をSi基板に形成し、実施例1とは異なり、微細凹凸構造が形成されたフォトレジストを除去せずそのまま使用した。形状の異なる2数類の凸部集合体部を交互にストライプ状に配列させた凸型のSi製表面微細構造原版(3)を作製した。凸型のSi製表面微細構造原版(3)において、ストライプ状の配列の距離は、平坦部の短軸方向が10μm、凸部集合体部の短軸方向が10μmであった。また、フォトレジストからなる微細凹凸構造には略円錐形状の複数の凸部が含まれ、複数の凸部の平均ピッチが600nmであり、複数の凸部の平均高さが300nmであり、Siからなる微細凹凸構造には略円錐形状の複数の凸部が含まれ、複数の凸部の平均ピッチが600nmであり、複数の凸部の平均高さが500nmであり、あった。2数類の凸部集合体部の高低差は、800nmであった。
続いて、凸型のSi製表面微細構造原版(3)から凹型のNi製電鋳スタンパー(3)を作製した。その後、凹型のNi製電鋳スタンパー(3)を用いて、平均厚み300nmの親水性コーティング層を設けた以外、実施例1と同様の作製方法によって、実施例5の凸型の細胞培養部材を作製した。また、疎水性領域となる凸部集合体部の面積の比(S2/(S1+S2))は0.5であった。
実施例5で作製した凸型のSi製表面微細構造原版(3)から実施例2と同様の方法で、厚さ188μmのシクロオレフィンポリマーフィルムからなる凹型の樹脂原版(2)を作製した。凹型の樹脂原版(3)から凸型のNi製電鋳スタンパー(3R)を作製した。その後、凸型のNi製電鋳スタンパー(3R)を用いた以外は、実施例5と同様の作製方法によって実施例6の凹型の細胞培養部材を作製した。
実施例1~6の細胞培養基材を使用し、マウス由来の筋芽細胞(C2C12細胞)の培養を行った。前培養として、細胞培養用フラスコ(25cm2)を使用し、FBS(ウシ胎児血清)10%を添加したDMEM(ダルベッコ改変イーグル培地)を用いてC2C12細胞を37℃、5%CO2雰囲気下にて培養した。
細胞の回収はトリプシンを用いた。血球計算版を用いて細胞数を計測した後、7.6×104細胞/mlの濃度の細胞懸濁液を調製した。
細胞培養用マルチウェルプレート(24孔)の底面に、10mm角に裁断した実施例1~6の基材を設置した。リン酸緩衝生理食塩水で細胞培養部材を洗浄後、調製した細胞懸濁液を0.5mlずつ分注し、細胞を播種した。細胞を播種したマルチウェルプレートは37℃、5%CO2雰囲気下で48時間培養した。
さらに、細胞が付着した細胞培養部材をパラホルムアルデヒドで固定し、ファロイジンを用いてアクチンを、DAPIを用いて細胞核を染色し、オールインワン蛍光顕微鏡(BZ-X800、キーエンス社)により2次元画像を取得した。いずれの細胞培養部材においても、培養細胞が微細凹凸構造領域に接着し、培養細胞は各微細凹凸構造に沿ってストライプ状に伸長した。一方、平坦な親水性領域の表面には培養細胞がほとんど接着しなかった。図15に実施例1の2次元画像を示す。
実施例1~6の細胞培養基材によれば、微細凹凸構造領域に特異的にC2C12細胞が接着して培養細胞の配向性を制御できることを確認した。
実施例1~6の細胞培養部材を使用し、ヒト臍帯静脈内皮細胞(HUVEC)の培養を行った。細胞と専用培地はScienCell Research Laboratories社から購入した。
ヒト臍帯静脈内皮細胞は、フィブロネクチンでコーティングした細胞培養用フラスコ(25cm2)を使用し、専用培地を用いて37℃、5%CO2雰囲気下にて培養した。コンフルエントになるまで2日毎に培地交換を行った。細胞の回収はトリプシンを用いた。血球計算版を用いて細胞数を計測した後、2.8×104細胞/mlの濃度の細胞懸濁液を調製した。
細胞培養用マルチウェルプレート(24孔)の底面に、10mm角に裁断した実施例1~6の基材を設置し、フィブロネクチンのコーティングを1時間行った。フィブロネクチンを除去し、滅菌水で基材シートを洗浄後、調製した細胞懸濁液を0.5mlずつ分注し、細胞を播種した。細胞を播種したマルチウェルプレートは37℃、5%CO2雰囲気下で4日間培養した。いずれの細胞培養部材においても、培養細胞が微細凹凸構造領域に接着し、培養細胞は各微細凹凸構造に沿ってストライプ状に伸長した。一方、平坦な親水性領域の表面には培養細胞がほとんど接着しなかった。
実施例1~6の細胞培養基材によれば、微細凹凸構造領域に特異的にヒト臍帯静脈内皮細胞が接着して培養細胞の配向性を制御できることを確認した。
Claims (11)
- 基材を有する細胞培養部材であって、
前記基材の表面に、親水性領域と疎水性領域とが形成され、
前記疎水性領域が、前記基材の厚み方向で前記親水性領域に対して相対的に高低差を設けた位置にあり、
前記親水性領域は、全面が親水性コーティング層で覆われた領域であり、
前記疎水性領域は、複数の凸部又は複数の凹部を含む微細凹凸構造とされ、かつ少なくとも前記複数の凸部の頂部又は前記複数の凹部の間の凸部の頂部が親水性コーティング層で覆われていない領域であり、
前記細胞培養部材を平面視した際の前記親水性領域の面積と前記疎水性領域の面積との面積和に対する前記疎水性領域の面積の比が、0.02~0.95である、細胞シート形成用の細胞培養部材。 - 前記親水性領域に加えて、前記疎水性領域の前記凸部の頂部又は前記複数の凹部の間の凸部の頂部以外が親水性コーティング層で覆われている、請求項1に記載の細胞シート形成用の細胞培養部材。
- 前記複数の凸部の平均高さ又は前記複数の凹部の平均深さが、前記親水性コーティング層の厚みより大きい、請求項1又は2に記載の細胞シート形成用の細胞培養部材。
- 前記疎水性領域が、前記基材の厚み方向で前記親水性領域に対して相対的に高い位置にある、請求項1~3のいずれか一項に記載の細胞シート形成用の細胞培養部材。
- 前記基材が、ポリエチレンテレフタラート、トリアセチルセルロース、ポリカーボネート、シクロオレフィンポリマー、シクロオレフィンコポリマー、アクリル樹脂、ポリスチレン及びジメチルポリシロキサンからなる群から選ばれる少なくとも1種以上の樹脂を含む、請求項1~4のいずれか一項に記載の細胞シート形成用の細胞培養部材。
- 基材を有する細胞培養部材の製造方法であって、
前記基材の表面に、親水性領域と前記親水性領域より前記基材の厚み方向で相対的に高低差を設けた位置にある疎水性領域とを形成し、かつ、前記疎水性領域に複数の凸部又は複数の凹部を含む微細凹凸構造領域を形成し、
次いで、前記表面の全体に親水性付与液を塗布することにより、前記複数の凸部の頂部又は前記複数の凹部の間の凸部の頂部を除いて親水性コーティング層を形成することを特徴とする、細胞シート形成用の細胞培養部材の製造方法。 - 前記疎水性領域に形成した複数の凸部の平均高さ又は前記複数の凹部の平均深さより小さい厚みで、前記親水性付与液を、前記表面の全体に塗布する、請求項6に記載の細胞シート形成用の細胞培養部材の製造方法。
- 前記疎水性領域を、前記基材の厚み方向で前記親水性領域に対して相対的に高い位置に形成する、請求項6又は7に記載の細胞シート形成用の細胞培養部材の製造方法。
- 請求項1~5のいずれか一項に記載の細胞シート形成用の細胞培養部材を備えた、培養容器。
- 請求項1~5のいずれか一項に記載の細胞シート形成用の細胞培養部材を用いて細胞を培養し、次いで、前記細胞培養部材から培養細胞を剥離する、培養細胞の生産方法。
- 請求項1~5のいずれか一項に記載の細胞シート形成用の細胞培養部材と、
前記細胞培養部材に付着した細胞と、
を備えた、細胞培養部材付き培養細胞。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021058006A JP7578043B2 (ja) | 2021-03-30 | 2021-03-30 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
| JP2024144087A JP2024152967A (ja) | 2021-03-30 | 2024-08-26 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021058006A JP7578043B2 (ja) | 2021-03-30 | 2021-03-30 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024144087A Division JP2024152967A (ja) | 2021-03-30 | 2024-08-26 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022154799A JP2022154799A (ja) | 2022-10-13 |
| JP7578043B2 true JP7578043B2 (ja) | 2024-11-06 |
Family
ID=83557362
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021058006A Active JP7578043B2 (ja) | 2021-03-30 | 2021-03-30 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
| JP2024144087A Pending JP2024152967A (ja) | 2021-03-30 | 2024-08-26 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024144087A Pending JP2024152967A (ja) | 2021-03-30 | 2024-08-26 | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 |
Country Status (1)
| Country | Link |
|---|---|
| JP (2) | JP7578043B2 (ja) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006325532A (ja) | 2005-05-30 | 2006-12-07 | Hitachi Ltd | 細胞培養容器,細胞培養容器の製造方法、及び培養細胞 |
| JP2010119304A (ja) | 2008-11-17 | 2010-06-03 | Dainippon Printing Co Ltd | 配向制御された細胞パターンの回収ツール |
| JP2013099272A (ja) | 2011-11-08 | 2013-05-23 | Dainippon Printing Co Ltd | 細胞培養基材の製造方法、細胞培養基材、およびそれを用いた細胞シートの製造方法 |
| JP2016067314A (ja) | 2014-09-30 | 2016-05-09 | セイコーエプソン株式会社 | 細胞培養用基体の製造方法 |
| JP2019037220A (ja) | 2017-08-23 | 2019-03-14 | 王子ホールディングス株式会社 | 細胞シート形成部材、細胞シート形成部材の製造方法、および、細胞シートの製造方法 |
| WO2020158482A1 (ja) | 2019-01-28 | 2020-08-06 | 王子ホールディングス株式会社 | 細胞シート形成部材、細胞シート形成部材の製造方法、および、細胞シートの製造方法 |
| WO2020158481A1 (ja) | 2019-01-28 | 2020-08-06 | 王子ホールディングス株式会社 | 細胞シートの製造方法および細胞シート |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6451134B2 (ja) * | 2014-08-04 | 2019-01-16 | 大日本印刷株式会社 | 細胞担持用基板およびその製造方法 |
-
2021
- 2021-03-30 JP JP2021058006A patent/JP7578043B2/ja active Active
-
2024
- 2024-08-26 JP JP2024144087A patent/JP2024152967A/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006325532A (ja) | 2005-05-30 | 2006-12-07 | Hitachi Ltd | 細胞培養容器,細胞培養容器の製造方法、及び培養細胞 |
| JP2010119304A (ja) | 2008-11-17 | 2010-06-03 | Dainippon Printing Co Ltd | 配向制御された細胞パターンの回収ツール |
| JP2013099272A (ja) | 2011-11-08 | 2013-05-23 | Dainippon Printing Co Ltd | 細胞培養基材の製造方法、細胞培養基材、およびそれを用いた細胞シートの製造方法 |
| JP2016067314A (ja) | 2014-09-30 | 2016-05-09 | セイコーエプソン株式会社 | 細胞培養用基体の製造方法 |
| JP2019037220A (ja) | 2017-08-23 | 2019-03-14 | 王子ホールディングス株式会社 | 細胞シート形成部材、細胞シート形成部材の製造方法、および、細胞シートの製造方法 |
| WO2020158482A1 (ja) | 2019-01-28 | 2020-08-06 | 王子ホールディングス株式会社 | 細胞シート形成部材、細胞シート形成部材の製造方法、および、細胞シートの製造方法 |
| WO2020158481A1 (ja) | 2019-01-28 | 2020-08-06 | 王子ホールディングス株式会社 | 細胞シートの製造方法および細胞シート |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2024152967A (ja) | 2024-10-25 |
| JP2022154799A (ja) | 2022-10-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Yao et al. | Cell–material interactions revealed via material techniques of surface patterning | |
| Jeon et al. | A mini‐review: cell response to microscale, nanoscale, and hierarchical patterning of surface structure | |
| Nakanishi et al. | Recent advances in cell micropatterning techniques for bioanalytical and biomedical sciences | |
| CN201080483Y (zh) | 细胞培养容器 | |
| TWI810202B (zh) | 細胞層片形成構件、細胞層片形成構件的製造方法、及細胞層片的製造方法 | |
| JP6021802B2 (ja) | 培養方法及び薬物スクリーニング方法 | |
| US20140141503A1 (en) | Cell culture substrate having uniform surface coating | |
| KR20140125662A (ko) | 세포배양 기판 | |
| US20130029422A1 (en) | Composite Substrate for 3D Cell Culture | |
| Pardo-Figuerez et al. | Controlled arrangement of neuronal cells on surfaces functionalized with micropatterned polymer brushes | |
| US20250333674A1 (en) | Cell sheet-forming member, method for producing cell sheet-forming member, and method for producing cell sheet | |
| US9290735B2 (en) | Mammary gland epithelial cell culture | |
| JP7222404B2 (ja) | 細胞シート形成部材、細胞シート形成部材の製造方法、および、細胞シートの製造方法 | |
| JP7192892B2 (ja) | 細胞シートの製造方法 | |
| JP7578043B2 (ja) | 細胞シート形成用の細胞培養部材、細胞シート形成用の細胞培養部材の製造方法、培養容器、培養細胞の生産方法、細胞培養部材付き培養細胞 | |
| JP2015164406A (ja) | ライフサイエンス用容器 | |
| JP7813435B2 (ja) | 細胞塊形成部材、培養容器、培養細胞の生産方法、細胞塊形成部材付き培養細胞 | |
| JP7180698B2 (ja) | 細胞シート形成部材、基材、および、細胞シート形成部材の製造方法 | |
| Coutinho et al. | Micro-and nanotechnology in tissue engineering | |
| Sung et al. | Integrated circuit-based biofabrication with common biomaterials for probing cellular biomechanics | |
| Xie | Brain-on-a-chip integrated neuronal networks | |
| Xu et al. | Contact printing of arrayed microstructures | |
| JP7472689B2 (ja) | 細胞培養部材の製造方法、細胞培養部材、細胞培養部材の製造用原型の製造方法、および細胞培養部材の製造用原型 | |
| JP2025094534A (ja) | 腫瘍細胞塊付細胞培養基材、並びにこれを用いた腫瘍細胞の悪性度の評価方法および被験物質の評価方法 | |
| Jang et al. | MICROPATTERNED POLYMER STRUCTURES FOR CELL AND TISSUE ENGINEERING |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230616 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240522 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240625 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240826 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240924 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241007 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7578043 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |