JP7300552B2 - 縮合環ピリミジンアミノ化合物、その調製方法、医薬組成物及び使用 - Google Patents
縮合環ピリミジンアミノ化合物、その調製方法、医薬組成物及び使用 Download PDFInfo
- Publication number
- JP7300552B2 JP7300552B2 JP2022503815A JP2022503815A JP7300552B2 JP 7300552 B2 JP7300552 B2 JP 7300552B2 JP 2022503815 A JP2022503815 A JP 2022503815A JP 2022503815 A JP2022503815 A JP 2022503815A JP 7300552 B2 JP7300552 B2 JP 7300552B2
- Authority
- JP
- Japan
- Prior art keywords
- substituted
- unsubstituted
- chr
- alkyl
- heteroatoms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
- C07D239/72—Quinazolines; Hydrogenated quinazolines
- C07D239/78—Quinazolines; Hydrogenated quinazolines with hetero atoms directly attached in position 2
- C07D239/84—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Rheumatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Immunology (AREA)
- Physical Education & Sports Medicine (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
本発明は、生物医学の技術分野に属し、縮合環ピリミジンアミノ化合物、その調製方法、医薬組成物及び使用に関する。
R3は未置換若しくはR3-1に置換されたC6-10アリール、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリール、未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキル、又は、未置換若しくはR3-4に置換されたC6-10アリール縮合「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~8員の」ヘテロシクロアルキルであり、
R3-1及びR3-2は独立して重水素、ヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR3-1-2に置換されたC3-10シクロアルキル、未置換若しくはR3-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、未置換若しくはR3-1-4に置換されたC6-10アリール、又は、未置換若しくはR3-1-5に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~6員の」ヘテロアリールであり、
R3-3及びR3-4は独立して水素又は1つ又は複数のハロゲンに置換されたC1-6アルキルであり、
R3-1-1~R3-1-5は独立してヒドロキシ、シアノ、ハロゲン、C1-6アルキル、C3-10シクロアルキル、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1は、ヒドロキシ、
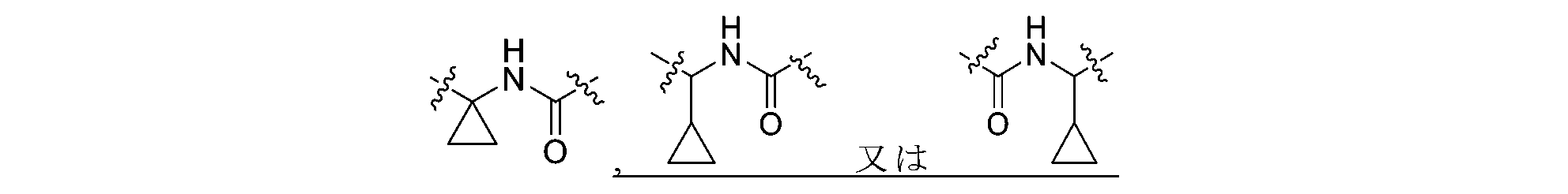
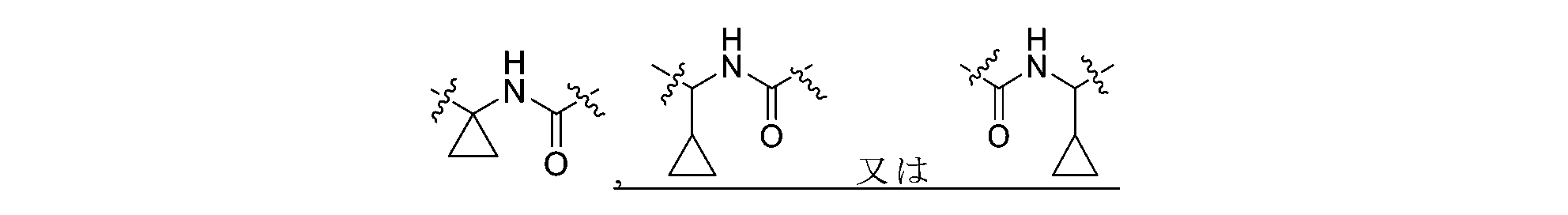
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がメチル又はエチルである場合、R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、R1は水素、C1-10アルキル、C1-6ハロアルキル、未置換若しくはR1-1に置換されたC6-10アリール、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリール、未置換若しくはR1-3に置換されたヘテロシクロアルキル、未置換若しくはR1-4に置換されたヘテロシクロアルキル-C1-6アルキル、未置換若しくはR1-5に置換されたC3-7シクロアルキル、未置換若しくはR1-6に置換されたC3-7シクロアルキル-C1-6アルキル、未置換若しくはR1-7に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個であり、炭素原子の数が1~6個である」C1-6ヘテロアルキルであり、前記ヘテロシクロアルキルは「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
Lの左端は
R4-1~R4-8は独立して水素、C1-4アルキル、「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~2個であり、炭素原子の数が1~4個である」C1-4ヘテロアルキル、C3-6シクロアルキル、「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~2個である3~7員の」ヘテロシクロアルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
R1-1及びR1-2は独立して重水素、未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又はNR1-1-4R1-1-5であり、
R1-1-1~R1-1-5は独立してヒドロキシ、C1-6アルキル、C3-10シクロアルキル、又は、「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R1-3~R1-7は独立してハロゲン、ヒドロキシ、C6-10アリール、C1-6アルキル、C1-6ハロアルキル、C1-3アルコキシ、C1-4アシルオキシ-C1-3アルキル又はC1-3ヒドロキシアルキルである。
例えば、
例えば、
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-2-NH-CO-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-2-NH-CO-であり、
R4-2は水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2はイソプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリール、又は、未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-3は水素又は1個又は複数個のハロゲンに置換されたC1-6アルキルであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらが連結する炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらが連結する炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリール、又は、未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-3は水素又は1つ又は複数のハロゲンに置換されたC1-6アルキルであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2はイソプロピル又はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2はイソプロピル又はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R4-1~R4-6は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R4-1~R4-6は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、未置換若しくはR1-1-2に置換されたC3-10シクロアルキルであり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-又は-CHR4-5-NH-CO-NH-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-CHR4-3-、-CHR4-5-NH-CO-NH-又は-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである。
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたフェニルである。
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたフェニルである。
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである。
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンである。
R3-1-1-1はC1-4アルキルである。
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである。
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである。
R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5である。
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5である。
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルである。
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルである。
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルである。
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-である。
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-である。
R2がメチル又はエチルである場合、Lは-CHR4-2-NH-CO-である。
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-である。
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-である。
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-2-NH-CO-である。
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
R4-1~R4-6は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
R4-2は水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して重水素、ヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR3-1-2に置換されたC3-10シクロアルキル、未置換若しくはR3-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、未置換若しくはR3-1-4に置換されたC6-10アリール、又は、未置換若しくはR3-1-5に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~6員の」ヘテロアリールであり、
R3-1-1~R3-1-5は独立してヒドロキシ、シアノ、ハロゲン、C1-6アルキル、C3-10シクロアルキル、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はヒドロキシ、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がメチル又はエチルである場合、R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、R1は水素、C1-10アルキル、C1-6ハロアルキル、未置換若しくはR1-1に置換されたC6-10アリール、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリール、未置換若しくはR1-3に置換されたヘテロシクロアルキル、未置換若しくはR1-4に置換されたヘテロシクロアルキル-C1-6アルキル、未置換若しくはR1-5に置換されたC3-7シクロアルキル、未置換若しくはR1-6に置換されたC3-7シクロアルキル-C1-6アルキル、未置換若しくはR1-7に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個であり、炭素原子の数が1~6個である」C1-6ヘテロアルキルであり、前記ヘテロシクロアルキルは「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
Lの左端は
R4-1~R4-8は独立して水素、C1-4アルキル、「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~2個であり、炭素原子の数が1~4個である」C1-4ヘテロアルキル、C3-6シクロアルキル、「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~2個である3~7員の」ヘテロシクロアルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
R1-1及びR1-2は独立して重水素、未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又はNR1-1-4R1-1-5であり、
R1-1-1~R1-1-5は独立してヒドロキシ、C1-6アルキル、C3-10シクロアルキル、又は、「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R1-3~R1-7は独立してハロゲン、ヒドロキシ、C6-10アリール、C1-6アルキル、C1-6ハロアルキル、C1-3アルコキシ、C1-4アシルオキシ-C1-3アルキル又はC1-3ヒドロキシアルキルである。
例えば、
例えば、
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-2-NH-CO-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-2-NH-CO-であり、
R4-2は水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2はイソプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらが連結する炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2はイソプロピル又はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R4-1~R4-6は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである。
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたフェニルである。
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたフェニルである。
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンである。
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである。
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである。
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5である。
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルである。
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルである。
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-である。
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-である。
R2がメチル又はエチルである場合、Lは-CHR4-2-NH-CO-である。
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-である。
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-である。
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-2-NH-CO-である。
R2はシクロプロピルである。
R2はイソプロピルである。
R4-1~R4-8は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する。
R4-1~R4-6は独立して水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
R4-2は水素、未置換若しくはR4-1-1に置換されたC1-4アルキルである。
用語「立体異性体」とは、空間内の分子内の原子のさまざまな配置によって生成される異性体を指し、シス-トランス異性体、エナンチオマー、及び立体配座異性体に分類することができ、また、エナンチオマーとジアステレオマーの2つの種類に分類することもできる。前記シス-トランス異性体とは、二重結合又は環を形成する炭素原子の単結合が自由に回転できないことによって引き起こされる異性体であり、例えば、シス-2-ブテンやトランス-2-ブテンがある。エナンチオマーとは、互いに実像と鏡像であり、重ね合わせることができない立体異性体を指し、例えば、L-乳酸やD-乳酸がある。立体配座異性体とは、単結合の回転によって生じる立体異性体を指し、例えば、いす形のシクロヘキサンやボート形のシクロヘキサンがある。
(1)本発明の縮合環ピリミジンアミノ化合物は、DDRs、特にDDR2に対して良好な阻害活性を有する。
(2)本発明の化合物は、肺の炎症及び肺線維症に対して良好な治療効果を有する。
(3)さらに、本発明の化合物は、キナーゼに対して良好な選択性を有し、副作用の発生を低減することができる。
2-アミノ-5-ブロモ安息香酸(10g、46.3mmol)を秤量し、80mlの乾燥テトラヒドロフランに溶解し、氷浴条件下で、1Mボランテトラヒドロフラン溶液(231ml)を、定圧滴下漏斗を使用して反応液にゆっくりと滴下した。滴下完了後、室温まで冷却し、一晩撹拌した。反応終了後、反応液に水を注意深く滴下してクエンチングさせ、酢酸エチルで抽出し、水と飽和塩化ナトリウム溶液で洗浄し、無水硫酸ナトリウムで乾燥し、濾過し、溶剤を蒸発乾固して、9gの白色固体を得た。収率96%。
中間体(2-アミノ-5-ブロモフェニル)メタノール(9g、44.54mmol)、二酸化マンガン(27g、312mmol)を100mlのジクロロメタンに秤量し、室温で6時間撹拌し、反応完了後、濾過により二酸化マンガンを除去した。ケーキをジクロロメタンで洗浄し、濾液を合わせ、溶剤を蒸発乾固させて、7.2gの黄褐色の固体を得た。収率80%。
2-アミノ-5-ブロモベンズアルデヒド(3.7g、18.5mmol)と尿素(16.6g、277mmol)を丸底フラスコに秤量し、油浴で180℃に加熱し、固体が溶解した後、5時間撹拌し、室温まで冷却し、水を加えて撹拌し、この時点で固体が析出し、吸引濾過し、水で洗浄し、乾燥させて淡黄色の固体4gを得て、これを次のステップに直接に投入した。収率96%。
前のステップで得られた中間体を丸底フラスコに直接に入れ、25mlのオキシ塩化リンを加えた。反応液を110℃の油浴に入れ、6時間加熱還流し、反応終了後、室温まで冷却し、反応系に氷水を注意深く加えて反応をクエンチし、飽和炭酸ナトリウム溶液で中和し、pH値を8~9に調節し、酢酸エチルで3回抽出し、無水硫酸ナトリウムで乾燥し、濾過し、溶剤を蒸発乾固させ、粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、白い固体2gを得た。収率46%。
前のステップで得られた中間体(250mg、1.03mmol)を丸底フラスコに秤量し、1-メチル-1H-ピラゾール-4-アミン(122.65mg、1.23mmol)、トリフルオロ酢酸(265mg、2.05mmol)を加え、30mlのイソプロパノールに溶解した。反応液を85℃の油浴で4時間加熱した。原料が完全に消失した後、反応液に水を加えて反応をクエンチし、酢酸エチルで3回抽出し、無水硫酸ナトリウムで乾燥し、濾過し、蒸発乾固させて、黄色の固体である粗生成物を得、これをジクロロメタンでスラリー化して精製することにより、黄色の固体240mgを得た。収率88%。
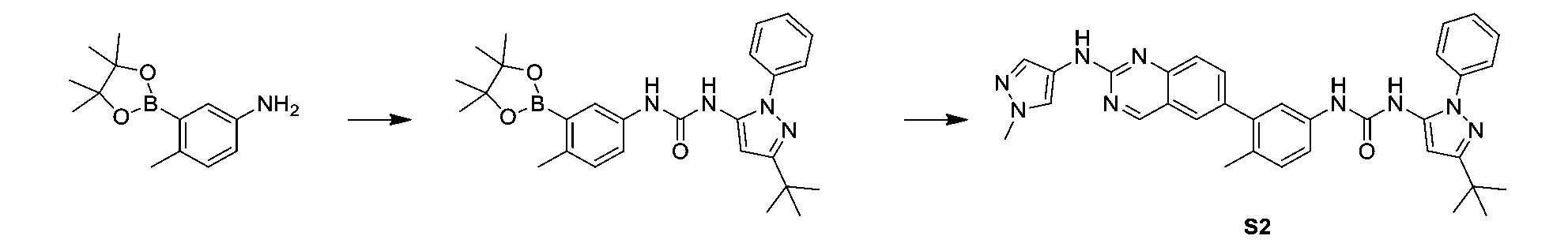
化合物3-ブロモ-4-メチルアニリン(10g、53.75mmol)をシュレンクボトルに秤量し、80ml乾燥ジメチルスルホキシドに溶解し、ビス(ピナコラト)ジボロン(17.74g、69.87mmol)、酢酸カリウム(15.82g、161.25mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(1.32g、1.61mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系を室温に冷却した後、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥させ、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、褐色の固体(10.6g)を得た。収率84.6%。
中間体4-メチル-3-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)アニリン(10g、42.9mmol)を乾燥テトラヒドロフランに溶解し、その中に3-(トリフルオロメチル)フェニルイソシアナート(8.0g、42.9mmol)をゆっくりと滴下し、室温で3時間撹拌し、白色の固体を析出させ、反応完了後、吸引濾過して白色の固体(14g)を得た。収率77%。
化合物6-ブロモ-N-(1-メチル-1H-ピラゾール-4-イル)キナゾリン-2-アミン(200mg、0.657mmol)をシュレンクボトルに秤量し、16mlのジオキサンと4mlの水に溶解し、1-(4-メチル-3-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)フェニル)-3-(3-(トリフルオロメチル)フェニル)ウレア(304mg、0.723mmol)、炭酸カリウム(182mg、1.32mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(16mg、0.020mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系を室温に冷却した後、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥し、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、黄色の固体(260mg)を得た。収率76%。
トリホスゲン(84mg、0.283mmol)を秤量してジクロロメタンに溶解し、3-(tert-ブチル)-1-フェニル-1H-ピラゾール-5-アミン(184.71mg、0.858mmol)を氷浴下で反応液にゆっくりと加え、30分間反応させた後、300μLのDIPEA、4-メチル-3-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)アニリン(200mg、0.858mmol)を反応液に加え、室温で6時間撹拌し、白色の固体を析出させ、反応完了後、吸引濾過により白色の固体を得、ケーキをジエチルエーテルで洗浄した。収率86%。
化合物6-ブロモ-N-(1-メチル-1H-ピラゾール-4-イル)キナゾリン-2-アミン(200mg、0.657mmol)をシュレンクボトルに秤量し、16mlのジオキサンと4mlの水に溶解し、1-(3-(tert-ブチル)-1-フェニル-1H-ピラゾール-5-イル)-3-(4-メチル-3-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)フェニル)ウレア(312mg、0.657mmol)、炭酸カリウム(182mg、1.32mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(16mg、0.020mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系を室温に冷却した後、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥させ、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、黄色の固体(283mg)を得た。収率75%。
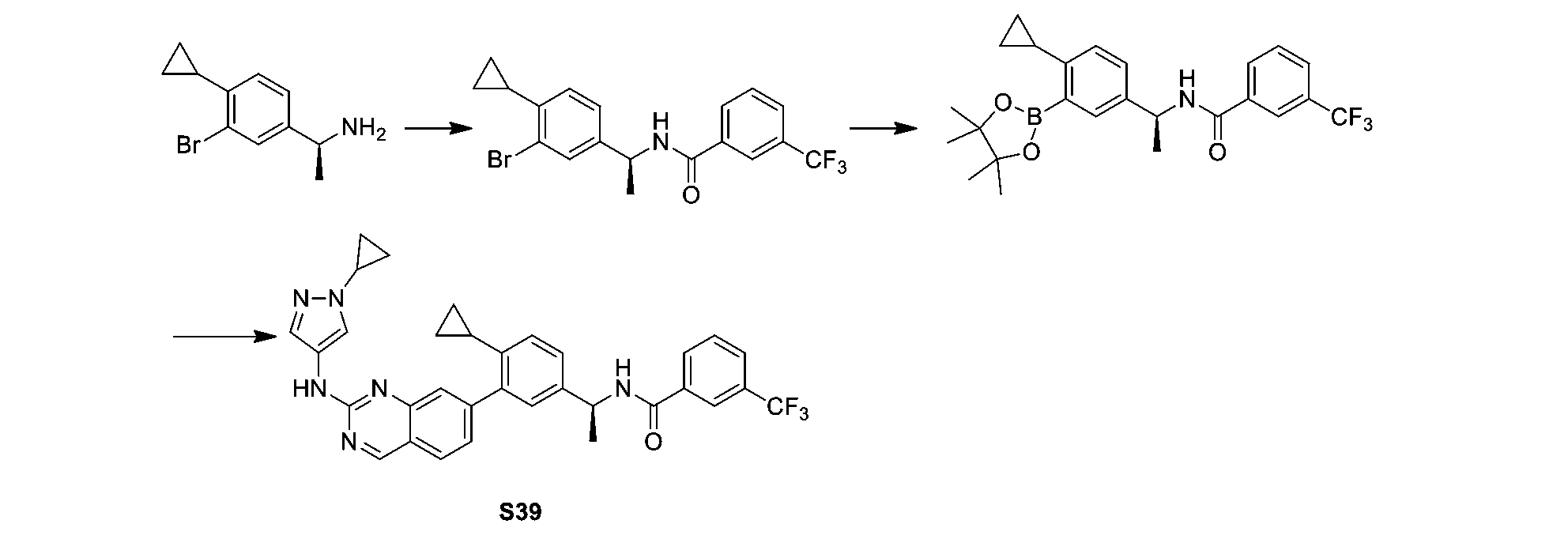
3-ブロモ-4-メチルアセトフェノン(5g、23.47mmol)を100mlの無水メタノールに溶解し、2gの4Aモレキュラーシーブをそれに加えた。固体酢酸アンモニウム(18g、234.7mmol)を秤量し、無水エタノールにバッチで加えた。室温で2時間撹拌した後、シアノ水素化ホウ素ナトリウム(4.42g、70.4mmol)を氷浴条件下でゆっくりと加えた。添加後、室温で48時間撹拌し、原料が完全に反応した後、溶剤メタノールを減圧下で蒸留除去し、酢酸エチルで抽出し、水で洗浄して過剰の固体を除去し、有機相を収集し、無水硫酸ナトリウムで乾燥させ、減圧下で蒸留して、酢酸エチルを除去した。得られた油状物をジエチルエーテルの塩酸溶液に加えて超音波処理し、この時点で大量の白色固体を析出させ、吸引濾過し、ケーキを無水ジエチルエーテルで洗浄して、合計4.8gの白色固体を得た。収率81.7%。
中間体1-(3-ブロモ-4-メチルフェニル)エタン-1-アミン塩酸塩(3g、11.97mmol)、HATU(5g、11.97mmol)及びDIPEA(4.64g、35.92mmol)を丸底フラスコに秤量し、50mlの無水N,N-ジメチルホルムアミドをそれに加え、室温で30分間撹拌した後、3-トリフルオロメチル安息香酸(2.3g、11.97mmol)を反応液に滴下した。反応液を室温で4時間撹拌し続け、反応が完了した後、飽和食塩水を反応液に加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥し、濾過し、溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計4gの黄色の油状液体を得た。収率86.5%。
中間体N-(1-(3-ブロモ-4-メチルフェニル)エチル)-3-(トリフルオロメチル)ベンズアミド(3g、7.77mmol)をシュレンクボトルに秤量し、30mlの乾燥ジメチルスルホキシドに溶解し、ビス(ピナコラト)ジボロン(2.17g、8.54mmol)、酢酸カリウム(2.29g、23.30mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(189mg、0.23mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系を室温に冷却した後、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥させ、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計3gの白色固体を得た。収率89%。
化合物6-ブロモ-N-(1-メチル-1H-ピラゾール-4-イル)キナゾリン-2-アミン(140mg、0.462mmol)をシュレンクボトルに秤量し、20mlのジオキサンと4mlの水に溶解し、N-(1-(4-メチル-3-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)フェニル)エチル)-3-(トリフルオロメチル)ベンズアミド(200mg、0.462mmol)、炭酸カリウム(138mg、0.923mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(15mg、0.015mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系を室温に冷却した後、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥させ、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計150mgの黄色の固体を得た。収率77%。
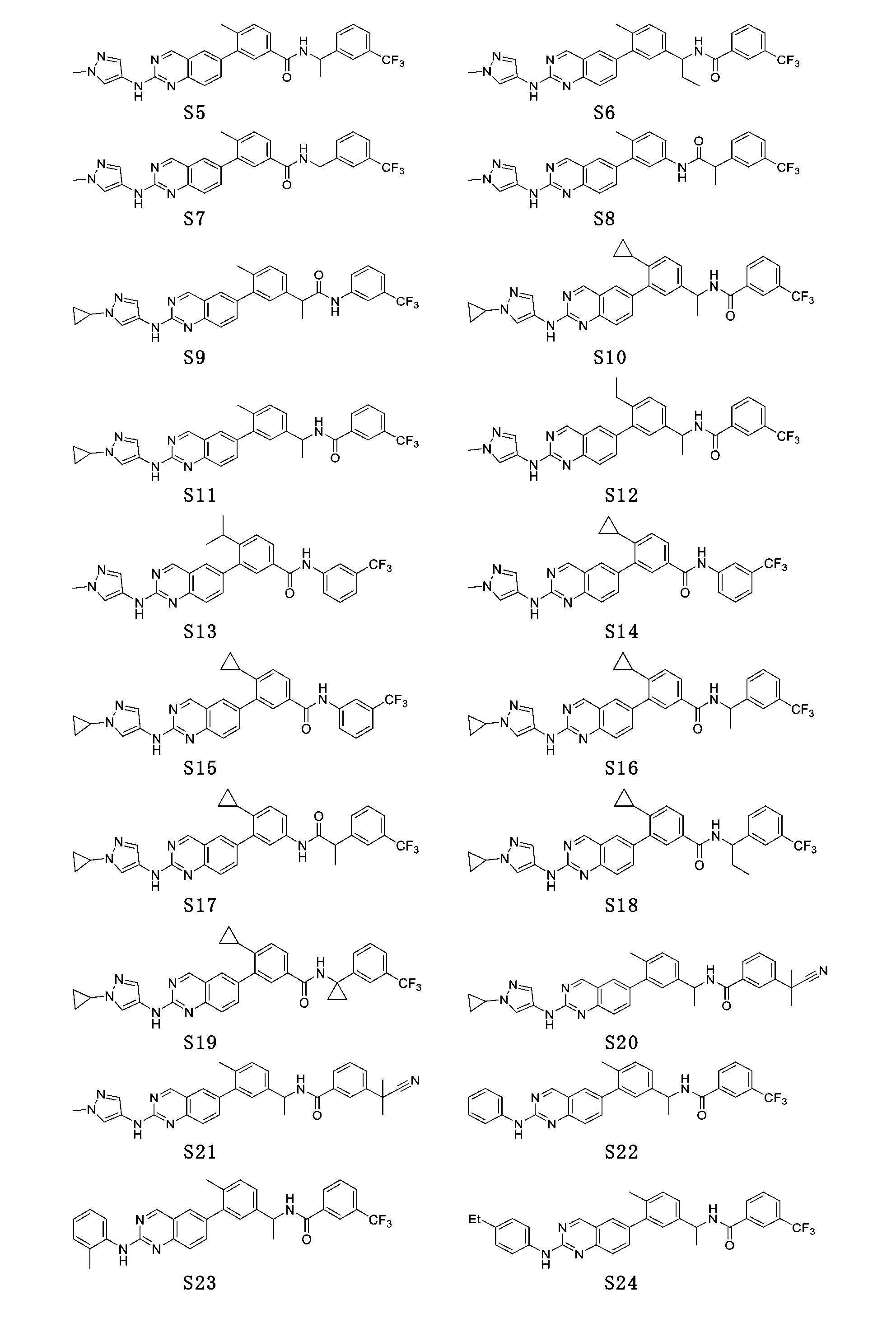
4-メチル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)-N-(1-(3-(トリフルオロメチル)フェニル)エチル)ベンズアミド(S5)
N-(1-(4-メチル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)フェニル)プロピル)-3-(トリフルオロメチル)ベンズアミド(S6)
N-(4-メチル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)フェニル)-2-(3-(トリフルオロメチル)フェニル)プロピオンアミド(S8)
2-ブロモ-4-(ブロモメチル)-1-メチルベンゼン(5g,、18.94mmol)を30mlの無水アセトニトリルに溶解し、それに18-クラウンエーテル-6(15g、56.83mmol)を加え、シアン化カリウム(1.36g、20.84mmol)をゆっくりと加え、室温で6時間撹拌した後、原料が完全に反応するまで待ち、酢酸エチル及び水で3回抽出し、有機相を収集し、無水硫酸ナトリウムで乾燥し、減圧下で蒸留して酢酸エチルを除去した。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計2gの無色の油状液体を得た。収率50%。
中間体2-(3-ブロモ-4-メチルフェニル)アセトニトリル(1g、4.76mmol)を10mlの無水DMFに溶解し、水素化ナトリウム(60%、209mg、5.24mmol)を氷浴条件下でゆっくりと加え、氷浴条件下で30分間撹拌した後、ヨウ化メチル(675mg、4.76mmol)を反応液に滴下した。約5時間の反応後、原料が完全に反応するまで待ち、酢酸エチルと水で3回抽出し、有機相を集めて無水硫酸ナトリウムで乾燥し、減圧蒸留により酢酸エチルを除去した。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計700mgの黄色の油状液体を得た。収率66%。
中間体2-(3-ブロモ-4-メチルフェニル)プロピオニトリル(500mg、2.23mmol)を20mlの4N水酸化ナトリウム溶液に溶解し、125℃で6時間撹拌した後、黄色の油状懸濁物が完全に消失した後、酢酸エチル及び水で抽出し、有機相を捨てて水層を保留し、水層を塩酸でPH=2~3に酸性化し、酢酸エチルで抽出し、有機相を集め、無水硫酸ナトリウムで乾燥し、減圧蒸留により酢酸エチルを除去した。無色の油状液体400mgを得た。収率74%。
中間体2-(3-ブロモ-4-メチルフェニル)プロピオン酸(300mg、1.23mmol)、HATU(516mg、1.36mmol)及びDIPEA(319mg、2.47mmol)を丸底フラスコに秤量し、これに15mlの無水N,N-ジメチルホルムアミドを加えた。室温で30分間撹拌した後、m-アミノトリフルオロトルエン(199mg、1.23mmol)を反応液に滴下した。反応液を室温で4時間撹拌し、反応物が完全に反応した後、飽和食塩水を反応液に加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥し、濾過し、溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計400mgの黄色の油状液体を得た。収率84%。
中間体2-(3-ブロモ-4-メチルフェニル)-N-(3-(トリフルオロメチル)フェニル)プロピオンアミド(300mg、0.777mmol)をシュレンクボトルに秤量し、10mlの乾燥ジメチルスルホキシドに溶解し、ビス(ピナコラト)ジボロン(217mg、0.854mmol)、酢酸カリウム(229mg、2.33mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(19mg、0.02mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系を室温に冷却し、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥させ、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計270mgの白色固体を得た。収率80%。
中間体6-ブロモ-N-(1-シクロプロピル-1H-ピラゾール-4-イル)キナゾリン-2-アミン(136mg、0.446mmol、原料が異なることを除いて、合成方法は実施例1と同じである)をシュレンクボトルに秤量し、20mlのジオキサンと4mlの水に溶解し、中間体2-(4-メチル-3-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)フェニル)-N-(3-(トリフルオロメチル)フェニル)プロピオンアミド(200mg、0.446mmol)、炭酸カリウム(123mg、0.892mmol)、[1,1’-ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン錯体(11mg、0.014mmol)をそれぞれに加え、真空ポンプ及びアルゴンバルーンによってガス交換を行い、反応系内の空気を除去し、3回の交換処理の後、アルゴンバルーンで保護し、80℃の油浴に置いて3時間反応させた。反応完了後、反応系が室温に冷却するまで待ち、飽和食塩水を加え、酢酸エチルで3回抽出し、有機層を無水硫酸ナトリウムで乾燥させ、濾過し、そして溶剤を蒸発乾固させた。粗生成物をシリカゲルカラムクロマトグラフィーにより精製して、合計175mgの黄色の固体を得た。収率77%。
その合成方法は実施例4を参照した。
その合成方法は実施例4を参照した。
上記の表から、実施例13でキラル合成された化合物S11-A’、S11-B’は、それぞれ実施例11で分割により得られた化合物S11-A及びS11-Bと同じ配置を有することを分かった。
その合成方法は実施例4を参照した。
4-イソプロピル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)-N-(3-(トリフルオロメチル)フェニル)ベンズアミド(S13)
4-シクロプロピル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)-N-(3-(トリフルオロメチル)フェニル)ベンズアミド(S14)
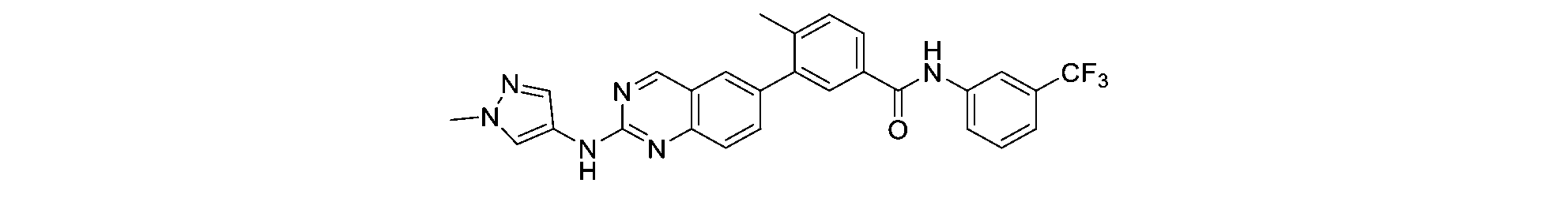
4-シクロプロピル-3-(2-((1-シクロプロピル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)-N-(3-(トリフルオロメチル)フェニル)ベンズアミド(S15)
4-シクロプロピル-3-(2-((1-シクロプロピル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)-N-(1-(3-(トリフルオロメチル)フェニル)エチル)ベンズアミド(S16)
N-(4-シクロプロピル-3-(2-((1-シクロプロピル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)フェニル)-2-(3-(トリフルオロメチル)フェニル)プロピオンアミド(S17)
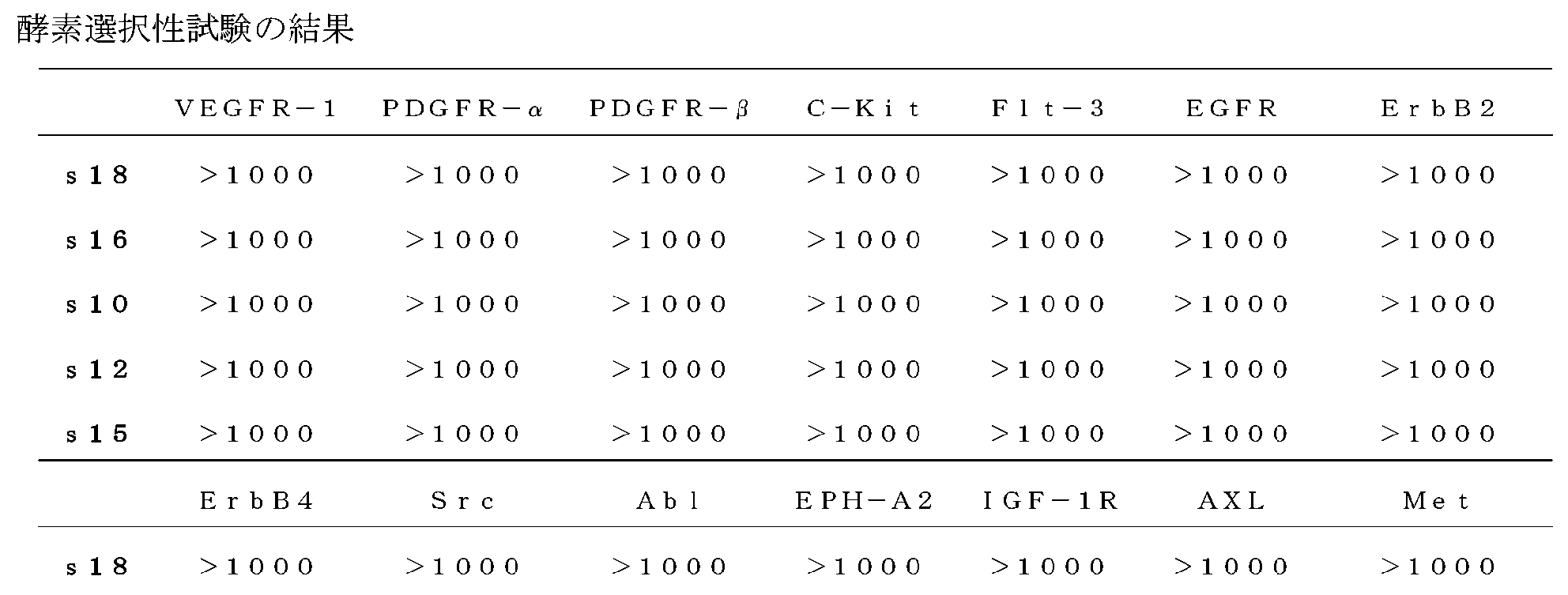
4-シクロプロピル-3-(2-((1-シクロプロピル-1H-ピラゾール-4-イル)アミノ)キナゾリン-7-イル)-N-(1-(3-(トリフルオロメチル)フェニル)エチル)ベンズアミド(S18)
4-シクロプロピル-3-(2-((1-シクロプロピル-1H-ピラゾール-4-イル)アミノ)キナゾリン-7-イル)-N-(1-(3-(トリフルオロメチル)フェニル)シクロプロピル)ベンズアミド(S19)
3-(2-シアノプロパン-2-イル)-N-(1-(3-(2-((1-シクロプロピル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)-4-メチルフェニル)エチル)ベンズアミド(S20)
3-(2-シアノプロパン-2-イル)-N-(1-(4-メチル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)フェニル)エチル)ベンズアミド(S21)
N-(1-(3-(2-((4-(ジメチルアミノ)フェニル)アミノ)キナゾリン-6-イル)-4-メチルフェニル)エチル)-3-(トリフルオロメチル)ベンズアミド(S25)
1-(1-(4-メチル-3-(2-((1-メチル-1H-ピラゾール-4-イル)アミノ)キナゾリン-6-イル)フェニル)エチル)-3-(3-(トリフルオロメチル)フェニル)ウレア(S27)
実験で使用したキナーゼは、当研究室で昆虫バキュロウイルス発現系を利用して発現・精製したプロテインキナーゼドメインの組換えタンパク質であり、ポリグルタミン酸-チロシンペプチドセグメント[Poly(Glu、Tyr)4:1]及びバナジン酸ナトリウムはSigma社から購入され、抗リン酸化モノクローナル抗体PY99はSanta Cruz社から購入され、ホースラディッシュペルオキシダーゼ標識ヤギ抗マウス二次抗体はCalbiochem社から購入され、ATP及びOPDはShanghai Sangon(上海生工)社から購入され、その他の試薬はすべてSinopharm(国薬集団化学試薬有限会社)から購入された。反応ELISAプレート(#2592)はCorning社から購入された。実験でプレート読み取りに使用される全波長マイクロプレートリーダーは、Molecular Device社の製品であり、モデル:SpectraMax 190であり、実験用水はSinopharm製の蒸留水であった。
化合物12000gを5分間遠心分離し、DMSOを添加して10-2Mのストック溶液を調製し、均一にボルテックスした後に、10分間超音波処理して、使用するまでに-40℃で保存した。試験中、DMSOを使用して化合物をストック溶液から試験濃度の100倍に希釈した(系内のDMSO濃度は1%であった)。
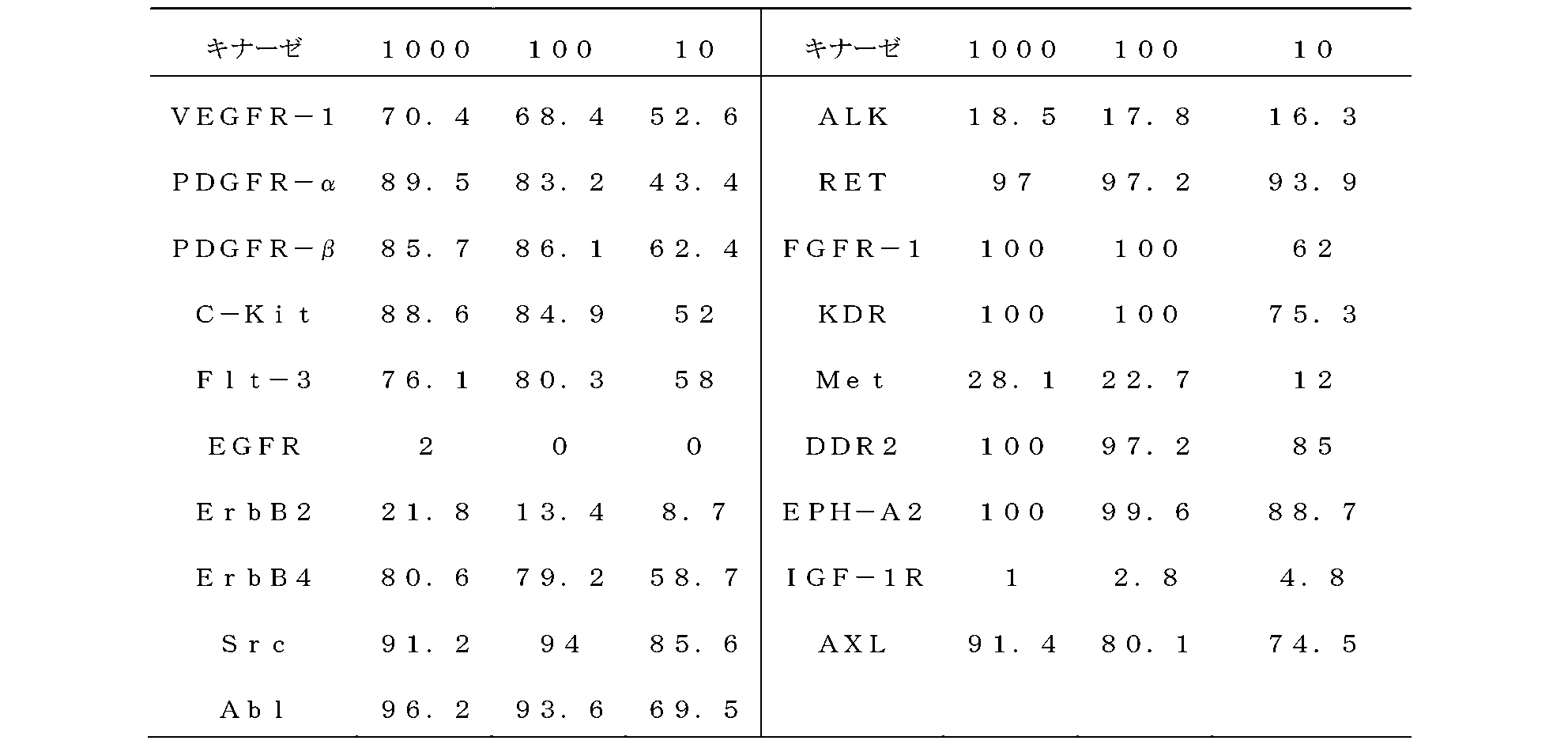
酵素が異なる以外に、他の試験方法及び条件はいずれも、効果実施例1におけるDDR2酵素活性試験方法と同じであった。
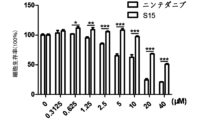
気管支上皮細胞株Beas-2B及び肺線維芽細胞株MRC-5に対する化合物S15の細胞毒性活性を試験することである。
図1は、肺線維芽細胞株MRC-5に対する陽性薬物ニンテダニブ(Nintedanib)及び化合物S15の細胞毒性活性の試験結果であり、図2は、気管支上皮細胞株Beas-2Bに対する陽性薬物ニンテダニブ及び化合物S15の細胞毒性活性の試験結果である。図1及び図2から分かるように、ニンテダニブは5μMの濃度で有意な細胞毒性を示したが、化合物S15は10μMでヒト気管支上皮細胞株Beas-2B及び肺線維芽細胞株MRC-5にほとんど毒性を示さなかった。上記の結果は、化合物S15の細胞毒性が陽性薬物ニンテダニブの細胞毒性よりはるかに低いことを示した。
本実験の目的は、ブレオマイシン(BLM)によって誘発される急性肺損傷及び炎症における化合物S15の治療可能性を調査することである。
モデル群(BLM):マウスに気管内注入を介してBLM(1.7U/kg)を一滴づつ注入した。
化合物S15群(S15):それぞれ30、60、及び90mg/kgの3つの投与群に分けられた。
陽性対照群(ニンテダニブ):ニンテダニブ投与群。
陰性対照群(対照):生理食塩水のみを使用した。
1.0等級(1点):正常な肺組織、
2.I等級(2点):軽度の肺胞炎であり、少量の炎症性細胞の浸潤があり、肺胞中隔はわずかに広がっている、
3.II等級(3点):中等度の肺胞炎であり、I等級よりも炎症細胞が多く、肺胞の形が乱れている、
4.III等級(4点):重度の肺胞炎であり、大量の炎症細胞が浸潤し、病変がびまん性になり、肺胞構造が完全に破壊されている。
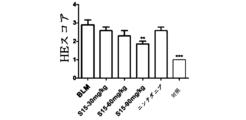
BLMで誘発された肺損傷のマウスモデルは、特発性肺線状疾患の研究で広く使用されている。BLM(2mg/kg)の経口投与後3日目に、化合物S15を30、60および90mg/kgの3つの投与量で12日間、1日1回(qd)経口投与した。ニンテダニブを、30mg/kgの単一の投与量で12日間、1日1回(qd)経口投与した。次に肺組織切片を作成し、H&E染色を使用してマウス肺切片の組織病理学的評価を行い、図3及び図4で示されるように、BLM誘導は重度の肺損傷を引き起こし、正常な肺胞構造が消失し、肺胞壁の肥厚が明らかであり、大量の炎症性細胞浸潤があり、限局性線状疾患病変が現れたが、化合物S15及びニンテダニブの投与群におけるBLM誘発性肺損傷は有意に改善された。
a.0.8mlのタンパク質標準の調製液をタンパク質標準(20mgのBSA)チューブに加え、十分溶解させて均一に混合し、25mg/mlのタンパク質標準液を調製した。調製後すぐに使用でき、-20℃で保存した。
b.適切な量の25mg/mlタンパク質標準を取り、それを0.5mg/mlの目標濃度に希釈させた。タンパク質サンプルと標準品は同じ溶液で希釈する必要があり、標準品は0.9%のNaCl又はPBSで希釈することもできることに注意されたい。希釈した後の0.5mg/mlのタンパク質標準は、-20℃で長期間保存できる。
サンプルの数に応じて、BCA試薬A:BCA試薬Bを50:1の容量比で適切な量のBCA作業溶液を調製し、十分に混合した。作業溶液を室温に置き、24時間以内で安定させた。
a.標準品を96ウェルプレートの標準品ウェルに0μl、1μl、2μl、4μl、8μl、12μl、16μl、20μlの8つの濃度で順次に加え、それに標準品を加えて希釈液を20μlに定容させ、標準品濃度がそれぞれ0mg/ml、0.025mg/ml、0.05mg/ml、0.1mg/ml、0.2mg/ml、0.3mg/ml、0.4mg/ml、0.5mg/mlに相当する。
b.適切な体積のサンプルを96ウェルプレートのサンプルウェルに加える。サンプルが20μl未満の場合は、標準品の希釈液を追加して20μlに定容させた。
c.各ウェルに200μlのBCA作業溶液を加え、37℃の環境下で20~30分間置いた。
d.540~595nmの波長範囲の間の吸光度を測定するか、又はマイクロプレートリーダーでA562を測定した。
e.使用したサンプルの体積と検量線に基づいて、サンプルのタンパク質濃度を算出した。
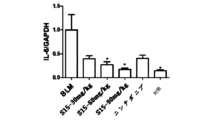
実験の各群の気管支肺胞洗浄液を分離し、図5及び図6で示されるように、BLM誘導は、BALFのマクロファージ、好中球を含む炎症細胞の総細胞数とタンパク質濃度を有意に増加できるが、S15は、炎症細胞の数と関連タンパク質の濃度を用量依存的に減らすことができる。
アルカリホスファターゼ(ALP)レベルおよび乳酸デヒドロゲナーゼ(LDH)レベル。関連する指標は、全自動血液指標分析装置および関連キット(アルカリホスファターゼアッセイキット及び乳酸デヒドロゲナーゼアッセイキット)を使用して測定された。
実験では、qRT-PCR技術を用いて肺組織における炎症性サイトカインのmRNAレベルを試験した。リアルタイム定量PCRによりTNF-α、IL-6、IL-1β、TGF-βなどのmRNAレベルを検出した。
約30mgの凍結保存した肺組織を秤量し、200μLのTrizol(Takara、9109#)を加えてホモジナイズして溶解し、RNA滅菌級ピペットチップによってウェル内で溶解した後の液体を収集し、対応する滅菌EPチューブに移した。400μLのクロロホルムを加え、30秒間激しく振とうし、4℃に置き、12000rpm遠心分離機で15分間遠心分離した。上層の水相層を新しいEPチューブに移し、等量のイソプロパノールを使用して水相中のRNAを沈殿させ、-20℃で1時間以上静置した。4℃、12000rpmで15分間遠心分離し、上清を廃棄した。75%のエタノールを加えてRNAペレットを洗浄し、4℃、12000rpmで15分間遠心分離し、上清を廃棄した。RNAペレットを室温で10~20分間放置して乾燥させた。25~200μLのRNaseフリー水を加えて溶解し、-80℃で保存した。
mRNAの逆転写はPrimeScriptTM RT Master Mix(Takara、RR036A)を使用して行い、体系は取扱説明書を参照した。簡単に説明すると、1μgのmRNAを20μLの体系に加え、均一に混合し、37℃の水浴で15分間一定温度に保存した後、85℃で5秒間酵素を失活させた。遠心分離後、再蒸留水で10倍に希釈した。
Q-PCR技術には、2x SYBR Green qPCR Master Mix(B21202、Biomake社)を使用し、反応系は取扱説明書を参照して調製した(10μLの2x SYBGreen、8.8μLのcDNAテンプレート、1.2μLの5μMプライマーMix)。反応条件は、95℃で5分間の予変性、95℃で30秒間の変性反応、60℃で30秒間のアニーリング、72℃で30秒間の伸長であり、反応サイクル数は40Cyclesであった。関連するプライマーは下記の表6に示される通りである。
以上の実験結果から、化合物S15はBLNによる肺損傷と炎症反応を効果的に軽減できると判断でき、その同等の用量群は、ニンテダニブと同等又はそれ以上の治療効果を示し、一方、高用量群は、許容できる場合に、より良い治療効果を示した。
1.0等級(1点):正常な肺組織であり、繊維状コラーゲン線維がないか、ほとんどない、
2.I等級(2点):コラーゲン繊維がわずかに増加し、細い束の形をする、
3.II等級(3点):コラーゲン線維が中等度に増加し、帯状に融合し、肺胞構造が乱れている、
4.III(等級4点):コラーゲン線維が有意に増加し、広帯状又はシート状をしており、肺胞が崩壊して融合し、構造が乱れている。
BLM(2mg/kg)の経口投与後3日目に、化合物S15を30、60及び90mg/kgの3つの投与群で12日間、1日1回(qd)経口投与した。ニンテダニブを、30mg/kgの単一の投与群で12日間、1日1回(qd)経口投与した。その後、図12及び図13で示されるように、肺組織切片を作製し、MASSON染色及びα-SMAの免疫組織化学的染色を行い、マウス肺切片に対して組織病理学的評価を行った。結果は、BLMがマウスの肺組織の肺胞中隔に大量のコラーゲン蓄積をもたらすことができ、コラーゲン染色が有意であり、肺胞構造がほぼ完全に消失し、肺間質の線維芽細胞が増加し、肺硬変を形成したことを示した。化合物S15は、BLMによって誘発された肺の損傷と炎症を有意に軽減でき、肺線維症も軽減することができた。α-平滑筋アクチン(α-SMA)陽性を発現する筋線維芽細胞は、コラーゲンの重要な供給源であるため、α-SMA筋線維芽細胞の特異的マーカーである。α-SMAの免疫組織化学的実験により、ブレオマイシンが重度の肺線維症を誘発できることも確認できる。化合物S15はコラーゲンとα-SMAの発現を用量依存的に低下させることができ、投与群(化合物S15群及びニンテダニブ群)のマウスの肺組織における炎症細胞浸潤は前者より軽く、線維芽細胞は有意に減少した。
ヒドロキシプロリン検出キットを使用してヒドロキシプロリンの変化を測定し、ステップは下記の通りである。
BALFにおける活性TGF-β1の発現レベルは、TGF-β1のELISA検出キット(Shanghai Wuhao Bio-Tech Co., Ltd)を使用して検出された。その手順は次の通りである。
実験では、qRT-PCR技術を使用して、肺組織における線維症関連マーカーのmRNAレベルを試験した。
実験方法は、効果実施例3の細胞毒活性試験実験と同じであった。
実験方法はウエスタンブロット実験と同じであった。
本群の実験は、BLMで誘発された急性肺損傷及び炎症における化合物S11-A/S11-Bの治療可能性を調査することを目的とする。
モデル群(Vehicle):マウスに気管を介してBLM(1.7U/kg)を注入した。
化合物S15群(S15):30、60、90mg/kgの3つの用量群に分けられた。
陽性対照群(ニンテダニブ):ニンテダニブ投与群。
陰性対照群(WT):生理食塩水のみ。
BLM(1.7U/kg)の経口投与後3日目に、化合物S11-Aを30mg/kgの3つの用量群で12日間、1日1回(qd)経口投与した。ニンテダニブを、30mg/kgの単一の用量群で12日間、1日1回(qd)経口投与した。次に、肺組織切片を調製し、H&E染色を使用してマウス肺切片の組織病理学的評価を行ったところ(図24及び図25)、ブレオマイシンは重度の肺損傷を誘発し、正常な肺胞構造が乱れ、肺胞壁の肥厚が有意であり、多数の炎症細胞が浸潤し、限局性線維性病変が現れたことを示した、経口S11-A及びニンテダニブ投与群では、BLM誘発性肺損傷が有意に改善された。
実験方法は、効果実施例5のヒドロキシプロリンレベルの評価方法と同じであった。
ヒドロキシプロリンはコラーゲンの主成分であり、アミノ酸全体の約13%を占めし、その他は少量のヒドロキシプロリン(約1%)を含むエラスチンを除いて、全部ヒドロキシプロリンを含まない。従って、ヒドロキシプロリンは、コラーゲン組織代謝の重要な指標及び線維症の重要なマーカーとして使用できる。図27から分かるように、BLM対照群と比較して、化合物S11-A/S11-Bはヒドロキシプロリンのレベルを有意に低下させることができる。
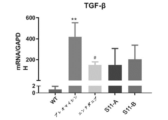
実験では、qRT-PCR技術を使用して、肺組織における線維症関連マーカーのmRNAレベルを測定した。
S11-A(30mg/kg)は、TGF-β1、Collagen1-α1及びα-SMAの発現を約50%減少させることができる(図28~図31)。従って、S11-Aの投与は、BLM誘発性肺線維症の進行を遅らせるか、さらには改善することができ、線維症に対するその治療効果は、ニンテダニブと同等であるか、それよりも優れている。
Claims (28)
- 下記の構造を有する式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。
R3は未置換若しくはR3-1に置換されたC6-10アリール、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリール、又は、未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルであり、
R3-1及びR3-2は独立して、ヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、C1-6アルコキシ、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-3は独立して1つ又は複数のハロゲンに置換されたC1-6アルキルであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R2はメチル、エチル、イソプロピル、又は、シクロプロピルであり、
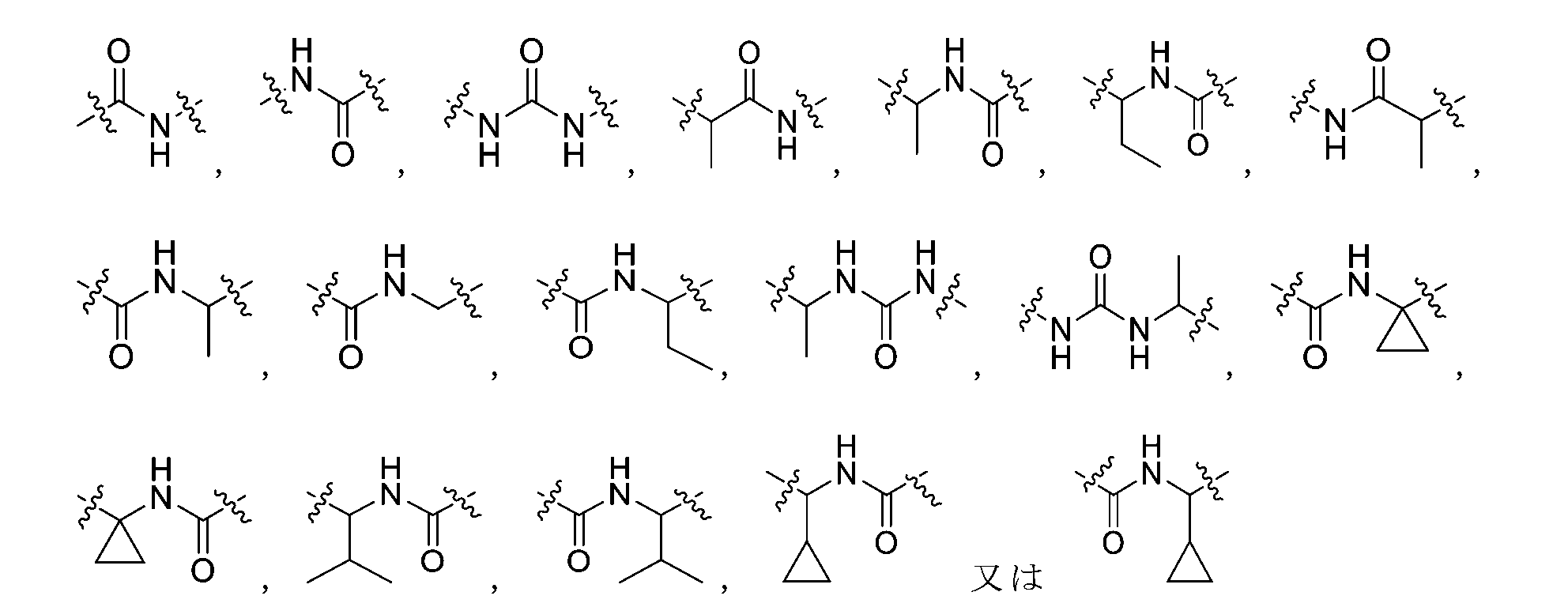
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、-CO-NH-CR4-7R4-8-、
R2がメチル又はエチルである場合、R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、-CO-NH-CR4-7R4-8-、
R2がイソプロピル又はシクロプロピルである場合、R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
Lの左端は
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
R1-1及びR1-2は独立して、未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又はNR1-1-4R1-1-5であり、
R1-1-1~R1-1-5は独立してヒドロキシ、又は、C1-6アルキルである。) - Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、C1-6アルコキシ、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立して、シアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R2はメチル、エチル、イソプロピル又はシクロプロピルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、-CO-NH-CR4-7R4-8-、
R2がメチル又はエチルである場合、R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、-CO-NH-CR4-7R4-8-、
R2がイソプロピル又はシクロプロピルである場合、R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
Lの左端は
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又はNR1-1-4R1-1-5であり、
R1-1-1~R1-1-5は独立してヒドロキシ、又は、C1-6アルキルである、ことを特徴とする請求項1に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3が未置換若しくはR3-1に置換されたC6-10アリールである場合、前記R3-1の数は1つ又は複数であり、複数個のR3-1が存在する場合、前記R3-1は同一、又は、異なり、
或いは、R3が未置換若しくはR3-1に置換されたC6-10アリールである場合、前記C6-10アリールはフェニルであり、
或いは、R3が未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記R3-2の数は1つ又は複数であり、複数個のR3-2が存在する場合、前記R3-2は同一、又は、異なり、
或いは、R3が未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記ヘテロアリールは「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~6員の」ヘテロアリールであり、
或いは、R3-1が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記R3-1-1の数は1つ又は複数であり、複数個のR3-1-1が存在する場合、前記R3-1-1は同一、又は、異なり、
或いは、R3-1が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R3-1が未置換若しくはR3-1-4に置換されたC6-10アリールである場合、前記R3-1-4の数は1つ又は複数であり、複数個のR3-1-4が存在する場合、前記R3-1-4は同一、又は、異なり、
或いは、R3-1が未置換若しくはR3-1-4に置換されたC6-10アリールである場合、前記C6-10アリールはフェニルであり、
或いは、R3-2が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記R3-1-1の数は1つ又は複数であり、複数個のR3-1-1が存在する場合、前記R3-1-1は同一、又は、異なり、
或いは、R3-2が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R3-2が未置換若しくはR3-1-4に置換されたC6-10アリールである場合、前記R3-1-4の数は1つ又は複数であり、複数個のR3-1-4が存在する場合、前記R3-1-4は同一、又は、異なり、
或いは、R3-2が未置換若しくはR3-1-4に置換されたC6-10アリールである場合、前記C6-10アリールはフェニルであり、
或いは、R3-1-1がハロゲンである場合、前記ハロゲンはフッ素、塩素、臭素又はヨウ素であり、
或いは、R3-1-4がハロゲンである場合、前記ハロゲンはフッ素、塩素、臭素又はヨウ素であり、
或いは、R2がメチル又はエチルである場合、Lは、
或いは、R2がイソプロピル又はシクロプロピルである場合、Lは、
或いは、R1が未置換若しくはR1-1に置換されたC6-10アリールである場合、前記R1-1の数は1つ又は複数であり、複数個のR1-1が存在する場合、前記R1-1は同一、又は、異なり、
或いは、R1が未置換若しくはR1-1に置換されたC6-10アリールである場合、前記C6-10アリールはフェニルであり、
或いは、R1が未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記R1-2の数は1つ又は複数であり、複数個のR1-2が存在する場合、前記R1-2は同一、又は、異なり、
或いは、R1が未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記ヘテロアリールは「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~6員の」ヘテロアリールであり、
或いは、R1-1が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記R1-1-1の数は1つ又は複数であり、複数個のR1-1-1が存在する場合、前記R1-1-1は同一、又は、異なり、
或いは、R1-1が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R1-1がC1-6アルコキシである場合、前記C1-6アルコキシはC1-4アルコキシであり、
或いは、R1-1が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記R1-1-2の数は1つ又は複数であり、複数個のR1-1-2が存在する場合、前記R1-1-2は同一、又は、異なり、
或いは、R1-1が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記C3-10シクロアルキルはC3-6シクロアルキルであり、
或いは、R1-2が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記R1-1-1の数は1つ又は複数であり、複数個のR1-1-1が存在する場合、前記R1-1-1は同一、又は、異なり、
或いは、R1-2が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R1-2がC1-6アルコキシである場合、前記C1-6アルコキシはC1-4アルコキシであり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記R1-1-2の数は1つ又は複数であり、複数個のR1-1-2が存在する場合、前記R1-1-2は同一、又は、異なり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記C3-10シクロアルキルはC3-6シクロアルキルであり、
或いは、R1-1-2がC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R1-1-4がC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R1-1-5がC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R4-1~R4-6が独立してC1-4アルキルである場合、前記C1-4アルキルはメチル、エチル、プロピル、イソプロピル、n-ブチル、イソブチル、sec-ブチル又はtert-ブチルであり、
或いは、R4-7及びR4-8がそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する場合、前記C3-6シクロアルキルはシクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである、ことを特徴とする請求項1又は2に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3が未置換若しくはR3-1に置換されたC6-10アリールである場合、前記R3-1の数は1個、2個、3個又は4個であり、
或いは、R3が未置換若しくはR3-1に置換されたC6-10アリールである場合、前記R3-1に置換されたC6-10アリールは、
或いは、R3が未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記R3-2の数は1個、2個又は3個であり、
或いは、R3が未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記ヘテロアリールはピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、イソキサゾリル、チアゾリル、イソチアゾリル、1,2,3-トリアゾリル、1,2,4-トリアゾリル、フラザニル、1,2,3-オキサジアゾリル、1,2,4-オキサジアゾリル、1,2,5-オキサジアゾリル、1,3,4-オキサジアゾリル、チアジアゾリル、ジチアゾリル、テトラゾリル、ピリジル、ピラニル、チオピラニル、ジアジニル、ピラジニル、ピリミジニル、ピリダジニル、オキサジニル、チアジニル、ジオキシニル、ジチイニル(dithiinyl)、1,2,3-トリアジニル、1,2,4-トリアジニル、1,3,5-トリアジニル又はテトラジニルであり、
或いは、R3が未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記R3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールは、
或いは、R3-1が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記R3-1-1の数は1個、2個又は3個であり、
或いは、R3-1が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、エチル、プロピル、イソプロピル、n-ブチル、イソブチル、sec-ブチル又はtert-ブチルであり、
或いは、R3-1が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記R3-1-1に置換されたC1-6アルキルは-CF3、又は、
或いは、R3-1が未置換若しくはR3-1-4に置換されたC6-10アリールである場合、前記R3-1-4の数は1個、2個、3個又は4個であり、
或いは、R3-2が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記R3-1-1の数は1個、2個又は3個であり、
或いは、R3-2が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、エチル、プロピル、イソプロピル、n-ブチル、イソブチル、sec-ブチル又はtert-ブチルであり、
或いは、R3-2が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記R3-1-1に置換されたC1-6アルキルは-CF3、又は、
或いは、R3-2が未置換若しくはR3-1-4に置換されたC6-10アリールである場合、前記R3-1-4の数は1個、2個、3個又は4個であり、
或いは、R3-1-1がハロゲンである場合、前記ハロゲンはフッ素であり、
或いは、R3-1-4がハロゲンである場合、前記ハロゲンはフッ素であり、
或いは、R1が未置換若しくはR1-1に置換されたC6-10アリールである場合、前記R1-1の数は1個、2個、3個又は4個であり、
或いは、R1が未置換若しくはR1-1に置換されたC6-10アリールである場合、前記R1-1に置換されたC6-10アリールは
或いは、R1が未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記R1-2の数は1個、2個又は3個であり、
或いは、R1が未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記ヘテロアリールはピロリル、フラニル、チエニル、イミダゾリル、ピラゾリル、オキサゾリル、イソキサゾリル、チアゾリル、イソチアゾリル、1,2,3-トリアゾリル、1,2,4-トリアゾリル、フラザニル、1,2,3-オキサジアゾリル、1,2,4-オキサジアゾリル、1,2,5-オキサジアゾリル、1,3,4-オキサジアゾリル、チアジアゾリル、ジチアゾリル、テトラゾリル、ピリジル、ピラニル、チオピラニル、ジアジニル、ピラジニル、ピリミジニル、ピリダジニル、オキサジニル、チアジニル、ジオキシニル、ジチイニル(dithiinyl)、1,2,3-トリアジニル、1,2,4-トリアジニル、1,3,5-トリアジニル又はテトラジニルであり、
或いは、R1が未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記R1-2に置換されたヘテロアリールは
或いは、R1-1が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記R1-1-1の数は1個、2個又は3個であり、
或いは、R1-1が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、エチル、プロピル、イソプロピル、n-ブチル、イソブチル、sec-ブチル又はtert-ブチルであり、
或いは、R1-1が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記R1-1-1に置換されたC1-6アルキルは
或いは、R1-1がC1-6アルコキシである場合、前記C1-6アルコキシはメトキシ、エトキシ、プロポキシ、イソプロポキシ、n-ブトキシ、イソブトキシ、sec-ブトキシ又はtert-ブトキシであり、
或いは、R1-1が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記R1-1-2の数は1個、2個又は3個であり、
或いは、R1-1が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記C3-10シクロアルキルはシクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルであり、
或いは、R1-1が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記R1-1-2に置換されたC3-10シクロアルキルは
或いは、R1-1が-NR1-1-4R1-1-5である場合、前記-NR1-1-4R1-1-5は-N(Me)2であり、
或いは、R1-2が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記R1-1-1の数は1個、2個又は3個であり、
或いは、R1-2が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、エチル、プロピル、イソプロピル、n-ブチル、イソブチル、sec-ブチル又はtert-ブチルであり、
或いは、R1-2が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記R1-1-1に置換されたC1-6アルキルは
或いは、R1-2がC1-6アルコキシである場合、前記C1-6アルコキシはメトキシ、エトキシ、プロポキシ、イソプロポキシ、n-ブトキシ、イソブトキシ、sec-ブトキシ又はtert-ブトキシであり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記R1-1-2の数は1個、2個又は3個であり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記C3-10シクロアルキルはシクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルであり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記R1-1-2に置換されたC3-10シクロアルキルは
或いは、R1-2が-NR1-1-4R1-1-5である場合、前記-NR1-1-4R1-1-5は-N(Me)2であり、
或いは、R1-1-4がC1-6アルキルである場合、前記C1-6アルキルはメチルであり、
或いは、R1-1-5がC1-6アルキルである場合、前記C1-6アルキルはメチルであり、
或いは、R4-1~R4-6が独立してC1-4アルキルである場合、前記C1-4アルキルはメチル又はエチルであり、
或いは、R4-7及びR4-8がそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成する場合、前記C3-6シクロアルキルはシクロプロピルである、ことを特徴とする請求項1又は2に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3が未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記ヘテロアリールはピラゾリルであり、
或いは、R3-1が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、イソプロピル、又は、tert-ブチルであり、
或いは、R3-2が未置換若しくはR3-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、イソプロピル、又は、tert-ブチルであり、
或いは、R1が未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールである場合、前記ヘテロアリールはピラゾリルであり、
或いは、R1-1が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、エチル、又は、イソプロピルであり、
或いは、R1-1がC1-6アルコキシである場合、前記C1-6アルコキシはメトキシであり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記C3-10シクロアルキルはシクロプロピル、又は、シクロペンチルであり、
或いは、R1-2が未置換若しくはR1-1-1に置換されたC1-6アルキルである場合、前記C1-6アルキルはメチル、エチル、又は、イソプロピルであり、
或いは、R1-2がC1-6アルコキシである場合、前記C1-6アルコキシはメトキシであり、
或いは、R1-2が未置換若しくはR1-1-2に置換されたC3-10シクロアルキルである場合、前記C3-10シクロアルキルはシクロプロピル、又は、シクロペンチルである、ことを特徴とする請求項4に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3が未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルである場合、前記R3-3の数は1つ又は複数であり、複数個のR3-3が存在する場合、前記R3-3は同一、又は、異なり、
或いは、R3が未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルである場合、前記C6-10アリールはフェニルであり、
或いは、R3が未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルである場合、前記C3-8シクロアルキルはシクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルであり、
或いは、R3-3が1つ又は複数のハロゲンに置換されたC1-6アルキルである場合、前記ハロゲンの数は1、2又は3個であり、
或いは、R3-3が1つ又は複数のハロゲンに置換されたC1-6アルキルである場合、前記ハロゲンはフッ素、塩素、臭素又はヨウ素であり、
或いは、R3-3が1つ又は複数のハロゲンに置換されたC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルであり、
或いは、R3-1-1が未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記R3-1-1-1の数は1つ又は複数であり、複数個のR3-1-1-1が存在する場合、前記R3-1-1-1は同一、又は、異なり、前記R3-1-1-1の数は1個、2個、3個又は4個であり、
或いは、R3-1-1が未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記ヘテロシクロアルキルは「ヘテロ原子がNであり、ヘテロ原子の数が1個又は2個である5~6員の」ヘテロシクロアルキルであり、
或いは、R3-1-1-1がC1-4アルキルである場合、前記C1-4アルキルは、メチル、エチル、プロピル、イソプロピル、n-ブチル、イソブチル、sec-ブチル又はtert-ブチルであり、
或いは、R1-2が未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記R1-1-3の数は1つ又は複数であり、複数個のR1-1-3が存在する場合、前記R1-1-3は同一、又は、異なり、
或いは、R1-2が未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルは「ヘテロ原子がNであり、ヘテロ原子の数が1個又は2個である5~6員の」ヘテロシクロアルキルであり、
或いは、R1-1-3がC1-6アルキルである場合、前記C1-6アルキルはC1-4アルキルである、ことを特徴とする請求項1又は2に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3が未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルである場合、前記R3-3の数は1個、2個、3個又は4個であり、
或いは、R3が未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルである場合、前記C3-8シクロアルキルはシクロペンチルであり、
或いは、R3-3が1つ又は複数のハロゲンに置換されたC1-6アルキルである場合、前記ハロゲンはフッ素であり、
或いは、R3-3が1つ又は複数のハロゲンに置換されたC1-6アルキルである場合、前記C1-6アルキルはメチルであり、
或いは、R3-1-1が未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記ヘテロシクロアルキルはピペラジニルであり、
或いは、R3-1-1-1がC1-4アルキルである場合、前記C1-4アルキルはエチルであり、
或いは、R1-2が未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記R1-1-3の数は1個、2個又は3個であり、
或いは、R1-2が未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルである場合、前記「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルはピペリジニルであり、
或いは、R1-1-3がC1-6アルキルである場合、前記C1-6アルキルはメチルである、ことを特徴とする請求項6に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
或いは、R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたフェニルであり、
或いは、R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
或いは、R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
或いは、R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
或いは、R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
或いは、R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-である、ことを特徴とする請求項1又は2に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたフェニルであり、
或いは、R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
或いは、R2がメチル又はエチルである場合、Lは-CHR4-2-NH-CO-であり、
或いは、R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-2-NH-CO-である、ことを特徴とする請求項8に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
或いは、R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
或いは、前記式Iで表される化合物がキラルC原子を含む場合、前記C原子はS配置又はR配置であり、
或いは、Lが-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-又は-NH-CO-NH-CHR4-6-である場合、前記-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-又は-NH-CO-NH-CHR4-6-は
- 前記式Iで表される化合物は下記のスキームのいずれかであって、
スキーム1:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム2:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム3:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-2-NH-CO-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-2-NH-CO-であり、
R4-2は水素、又は、C1-4アルキルであり、
スキーム4:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム5:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立してヒドロキシ、未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-1に置換されたC6-10アリール、又は、未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-1及びR1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、C1-6アルコキシ、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してヒドロキシ、又は、C1-6アルキルであり、
R2はイソプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム6:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらが連結する炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム7:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2はイソプロピル又はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム8:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R4-1~R4-6は独立して水素、又は、C1-4アルキルである、ことを特徴とする請求項1又は2に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - 前記式Iで表される化合物は下記のスキームのいずれかであって、
スキーム9:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリール、又は、未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-3は1つ又は複数のハロゲンに置換されたC1-6アルキルであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらが連結する炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム10:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリール、又は、未置換若しくはR3-3に置換されたC6-10アリール縮合C3-8シクロアルキルであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-3は1つ又は複数のハロゲンに置換されたC1-6アルキルであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2はイソプロピル又はシクロプロピルであり、
Lは-CO-NH-、-NH-CO-、-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、-NH-CO-NH-CHR4-6-、又は、-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム11:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ、ハロゲン、又は、未置換若しくはR3-1-1-1に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキルであり、
R3-1-1-1はC1-4アルキルであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-2に置換されたC3-10シクロアルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、NR1-1-4R1-1-5であり、
R1-1-1、R1-1-2、R1-1-3、R1-1-4及びR1-1-5は独立してC1-6アルキルであり、
R2がメチル又はエチルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-、-CHR4-5-NH-CO-NH-、又は、-NH-CO-NH-CHR4-6-であり、
R4-1~R4-6は独立して水素、又は、C1-4アルキルであり、
スキーム12:
Xは水素であり、
R3は未置換若しくはR3-1に置換されたC6-10アリール、又は、未置換若しくはR3-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~4個である5~10員の」ヘテロアリールであり、
R3-1及びR3-2は独立して未置換若しくはR3-1-1に置換されたC1-6アルキル、又は、未置換若しくはR3-1-4に置換されたC6-10アリールであり、
R3-1-1及びR3-1-4は独立してシアノ又はハロゲンであり、
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
R1-2は独立して未置換若しくはR1-1-1に置換されたC1-6アルキル、未置換若しくはR1-1-3に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である3~10員の」ヘテロシクロアルキル、又は、未置換若しくはR1-1-2に置換されたC3-10シクロアルキルであり、
R1-1-1、R1-1-2、及び、R1-1-3は独立してC1-6アルキルであり、
R2がメチルである場合、Lは-NH-CO-NH-、-CHR4-1-CO-NH-、-CHR4-2-NH-CO-、-NH-CO-CHR4-3-、-CO-NH-CHR4-4-又は-CHR4-5-NH-CO-NH-であり、
R2がイソプロピル又はシクロプロピルである場合、Lは-CO-NH-、-NH-CO-CHR4-3-、-CHR4-5-NH-CO-NH-又は-CO-NH-CR4-7R4-8-であり、
R4-1~R4-8は独立して水素、又は、C1-4アルキルであり、或いは、R4-7及びR4-8はそれらの間の炭素原子と一緒になってC3-6シクロアルキルを形成し、
スキーム13:
R1は未置換若しくはR1-2に置換された「ヘテロ原子がN、O及びSから選択された1つ又は複数であり、ヘテロ原子の数が1~3個である5~10員の」ヘテロアリールであり、
スキーム14:
R2はシクロプロピルであり、
スキーム15:
R2はイソプロピルである、ことを特徴とする請求項1又は2に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体。 - 請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体、及び医薬補助剤を含む医薬組成物。
- DDR阻害剤の調製における請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体、或いは請求項16に記載の医薬組成物の使用。
- 医薬は線維症、関節炎、アテローム性動脈硬化症又は腫瘍の治療に使用される、
医薬の調製における請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体、或いは請求項16に記載の医薬組成物の使用。 - 前記医薬は線維症、腫瘍、又は、関節炎の治療に使用される請求項18に記載の使用。
- 前記線維症は肺線維症である、請求項18又は19に記載の使用。
- DDR関連疾患の治療に使用される医薬の調製における請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体、或いは請求項16に記載の医薬組成物の使用。
- 前記DDR関連疾患は線維症、関節炎、アテローム性動脈硬化症又は腫瘍である請求項21に記載の使用。
- 前記DDR関連疾患は線維症、腫瘍、又は、関節炎である請求項22に記載の使用。
- 前記線維症は肺線維症である、請求項22又は23に記載の使用。
- 請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体、及びPD-1/PD-L1阻害剤を含む医薬組成物。
- 請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体と、PD-1/PD-L1阻害剤と、医薬補助剤とを含む医薬組成物。
- 腫瘍を治療するための医薬の調製における請求項25に記載の医薬組成物、或いは請求項26に記載の医薬組成物の使用。
- 前記式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体とPD-1/PD-L1阻害剤とを併用することを特徴とする、腫瘍を治療するための医薬の調製における請求項1~14のいずれか一項に記載の式Iで表される化合物、その薬学的に許容される塩、その互変異性体、又は、その立体異性体の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201910654591.7 | 2019-07-19 | ||
| CN201910654591 | 2019-07-19 | ||
| CN202010667271.8A CN112239459B (zh) | 2019-07-19 | 2020-07-13 | 稠环嘧啶氨基化合物、其制备方法、药物组合物及应用 |
| CN202010667271.8 | 2020-07-13 | ||
| PCT/CN2020/102653 WO2021013084A1 (zh) | 2019-07-19 | 2020-07-17 | 稠环嘧啶氨基化合物、其制备方法、药物组合物及应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022536549A JP2022536549A (ja) | 2022-08-17 |
| JP7300552B2 true JP7300552B2 (ja) | 2023-06-29 |
Family
ID=74170504
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022503815A Active JP7300552B2 (ja) | 2019-07-19 | 2020-07-17 | 縮合環ピリミジンアミノ化合物、その調製方法、医薬組成物及び使用 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11655239B2 (ja) |
| EP (1) | EP4001267A4 (ja) |
| JP (1) | JP7300552B2 (ja) |
| CN (1) | CN112239459B (ja) |
| CA (1) | CA3147852C (ja) |
| TW (1) | TWI869422B (ja) |
| WO (1) | WO2021013084A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115916759B (zh) * | 2020-06-19 | 2025-07-15 | 泰州红云制药有限公司 | 取代喹唑啉类化合物、其制备方法、药物组合及应用 |
| GB202111740D0 (en) * | 2021-08-16 | 2021-09-29 | Redx Pharma Plc | Fibrosis |
| CN119101036A (zh) * | 2023-06-08 | 2024-12-10 | 广州六顺生物科技有限公司 | 喹喔啉类化合物及其应用 |
| WO2025092989A1 (zh) * | 2023-11-03 | 2025-05-08 | 泰州红云制药有限公司 | 取代喹唑啉类化合物、其制备方法、药物组合及应用 |
| CN120774919A (zh) * | 2024-04-02 | 2025-10-14 | 中国科学院上海药物研究所 | 吡唑并[3,4-d]哒嗪酮类化合物、其制备方法、药物组合物及其应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006039718A2 (en) | 2004-10-01 | 2006-04-13 | Amgen Inc | Aryl nitrogen-containing bicyclic compounds and their use as kinase inhibitors |
| WO2016051186A1 (en) | 2014-10-01 | 2016-04-07 | Respivert Limited | N-phenyl-3-quinazolin-6-yl-benzamide derivatives as p38 kinase inhibitors |
| CN109305944A (zh) | 2017-07-28 | 2019-02-05 | 深圳睿熙生物科技有限公司 | 布鲁顿酪氨酸激酶的抑制剂 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7906522B2 (en) * | 2005-04-28 | 2011-03-15 | Kyowa Hakko Kirin Co., Ltd | 2-aminoquinazoline derivatives |
| CA2748319A1 (en) * | 2008-12-29 | 2010-07-08 | Fovea Pharmaceuticals | Substituted quinazoline compounds of general formula (i) and uses thereof for treating disorders relating to tyrosine kinase dysregulation |
| WO2017198202A1 (zh) * | 2016-05-19 | 2017-11-23 | 上海诚妙医药科技有限公司 | 尼达尼布的新晶型及其制备方法及其用途 |
| WO2018183559A1 (en) * | 2017-03-28 | 2018-10-04 | The General Hospital Corporation | Combination therapy against chemoresistance in leukemia |
-
2020
- 2020-07-13 CN CN202010667271.8A patent/CN112239459B/zh active Active
- 2020-07-17 WO PCT/CN2020/102653 patent/WO2021013084A1/zh not_active Ceased
- 2020-07-17 CA CA3147852A patent/CA3147852C/en active Active
- 2020-07-17 JP JP2022503815A patent/JP7300552B2/ja active Active
- 2020-07-17 EP EP20844824.1A patent/EP4001267A4/en active Pending
- 2020-07-17 TW TW109124324A patent/TWI869422B/zh active
- 2020-07-17 US US17/628,246 patent/US11655239B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006039718A2 (en) | 2004-10-01 | 2006-04-13 | Amgen Inc | Aryl nitrogen-containing bicyclic compounds and their use as kinase inhibitors |
| WO2016051186A1 (en) | 2014-10-01 | 2016-04-07 | Respivert Limited | N-phenyl-3-quinazolin-6-yl-benzamide derivatives as p38 kinase inhibitors |
| CN109305944A (zh) | 2017-07-28 | 2019-02-05 | 深圳睿熙生物科技有限公司 | 布鲁顿酪氨酸激酶的抑制剂 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220274962A1 (en) | 2022-09-01 |
| EP4001267A1 (en) | 2022-05-25 |
| TWI869422B (zh) | 2025-01-11 |
| US11655239B2 (en) | 2023-05-23 |
| CN112239459A (zh) | 2021-01-19 |
| JP2022536549A (ja) | 2022-08-17 |
| TW202116740A (zh) | 2021-05-01 |
| CA3147852A1 (en) | 2021-01-28 |
| CA3147852C (en) | 2023-02-14 |
| CN112239459B (zh) | 2021-11-26 |
| WO2021013084A1 (zh) | 2021-01-28 |
| EP4001267A4 (en) | 2023-07-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7300552B2 (ja) | 縮合環ピリミジンアミノ化合物、その調製方法、医薬組成物及び使用 | |
| JP6782255B2 (ja) | ヒストンデアセチラーゼ阻害薬及び組成物並びにそれらの使用の方法 | |
| TWI705815B (zh) | 用於治療補體相關疾病之組合物及治療方法 | |
| JP7057343B2 (ja) | 小児癌の処置方法 | |
| JP7539545B2 (ja) | 複素環化合物及びその使用 | |
| KR20170085590A (ko) | 신규 치환된 인다졸, 그의 제조 방법, 상기 신규 치환된 인다졸을 함유하는 제약 제제, 및 약물을 제조하기 위한 상기 신규 치환된 인다졸의 용도 | |
| HUE025553T2 (en) | CFTR modulators | |
| TR201818390T4 (tr) | Yeni̇ anti̇-i̇nflamatuvar ajanlar | |
| CN101827593A (zh) | 用于治疗(特别是)囊性纤维化的异噻唑并吡啶酮 | |
| WO2025011568A1 (zh) | 用作shp2抑制剂的杂环化合物、包含其的药物组合物及其制备方法和用途 | |
| BR112018075736B1 (pt) | Composto de amida alfa e beta insaturado derivado de benzotriazol usado como inibidor de tgf-betar1 | |
| JP2025530234A (ja) | Pi3k阻害剤としてのイソキノロン | |
| TR201815685T4 (tr) | Kanser tedavisi için akt ve mek inhibe edici bileşiklerin kombinasyonları. | |
| JP7695232B2 (ja) | ヘテロアリール血漿カリクレインインヒビター | |
| WO2020153414A1 (ja) | 複素環化合物及びその用途 | |
| CN117836270A (zh) | Usp30抑制剂及其用途 | |
| JP2025519540A (ja) | Pi3k阻害剤としてのベンゾピリミジン-4(3h)-オン | |
| JP2013166788A (ja) | Ppar調節剤の塩および代謝障害の治療方法 | |
| CN109415356B (zh) | 4-(5-(4,7-二甲基苯并呋喃-2-基)-1,2,4-噁二唑-3-基)苯甲酸的结晶形式及其制备方法 | |
| EP4079724A1 (en) | Fused ring compound and application thereof | |
| CN109476638A (zh) | 吡唑衍生物、其组合物及治疗用途 | |
| TW202412778A (zh) | 一種脯氨醯羥化酶抑制劑及其用途 | |
| WO2007124355A2 (en) | Vascular endothelial receptor specific inhibitors | |
| TWI905781B (zh) | 脯胺醯羥化酶抑制劑及其用途 | |
| CN110650955B (zh) | 用于治疗癫痫、神经变性病症和其他cns病症的化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220413 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220414 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20220414 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220705 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220930 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20221122 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230315 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20230315 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20230316 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20230406 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20230411 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230613 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230619 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7300552 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |