発明の詳細な説明
収容及び患者への投与のために圧縮可能な胃内滞留システムを圧縮してカプセル封入するためのシステム及び方法について説明する。圧縮可能な胃内滞留システムは、カプセルから解放されると展開して広がるようになっている。幾何学的形状、圧縮の必要性、及び圧縮可能な滞留システムの弾力性により、胃内滞留システムをカプセル封入するのが特に難しくなることがある。圧縮可能な胃内滞留システムを手動で圧縮しカプセル封入する方法は、遅くて非効率的である。説明するシステム及び方法は、圧縮可能な胃内滞留システムを効率的に圧縮しカプセル封入することを可能にする。実施形態によっては、このシステム及び方法は、自動化されたカプセル封入システムの一部であってもよい。実施形態によっては、このシステム及び方法を使用して、従来のカプセル封入技術を改良し、圧縮可能な胃内滞留システムを取り扱い且つカプセル封入することを可能にできる。
1つ以上のセグメントを連結する連結部材を含む胃内滞留システムのカプセル封入は、以下の工程を含む方法によって実施することができる。
A.非圧縮形態で、圧縮可能な胃内滞留システムを受け取る工程。実施形態によっては、圧縮可能な胃内滞留システムは、振動式すり鉢状送り装置又はピックアンドプレースコンベヤーで受け取られることがある。
B.圧縮可能な胃内滞留システムを圧縮位置に方向付ける工程。
C.圧縮可能な胃内滞留システムを圧縮形態に圧縮する工程。
D.圧縮形態にある圧縮可能な胃内滞留システムを容器の開口部に挿入する工程。実施形態によっては、圧縮可能な胃内滞留システムを、容器に挿入する前に、バンド又はキャップなどの保持要素によって圧縮形態に固定して、早期に展開された場合に圧縮可能な胃内システムが展開するのを防止することがある。
実施形態によっては、圧縮可能な胃内滞留システムを受け取り方向付けすることは、振動式すり鉢状送り装置によって実施されることがある。例えば、胃内滞留システムをすり鉢構造に注ぐことによって、振動式すり鉢状送り装置の大きなすり鉢構造に、大量の圧縮可能な滞留システムを挿入することができる。すり鉢構造で受け取られると、圧縮可能な胃内滞留システムはごちゃ混ぜになり互いに絡み合うことがある。胃内滞留システムの塊に振動を加えることにより、個々の胃内滞留システムは塊から解放され、振動式すり鉢状送り装置の外壁に近づくことができる。振動式すり鉢状送り装置の外壁は、上方に向かうらせん状の行路を含むことがある。上方に向かうらせん状の行路の形状は、胃内滞留システムを行路を上方に進ませ、これと同時に、更なる処理のために胃内滞留システムを好ましい向きに方向付けするように、設計されていることがある。振動式すり鉢状送り装置によって方向付けされた又は部分的に方向付けされた胃内滞留システムの出力は、更なる処理工程に向けて運ばれることがある。実施形態によっては、振動式すり鉢状送り装置の出力は、平坦な表面に置かれることがある。実施形態によっては、この平坦な表面は、胃内滞留システムを新たな場所に移動させるためのコンベヤーベルトなどの移動式表面であることもある。実施形態によっては、振動式すり鉢状送り装置のこの出力は、部分的にのみ方向付けされていると考えられることがある。例えば、振動式すり鉢状送り装置は、コンベヤーベルト上に平坦に中心合わせして胃内滞留システムを提供することができるが、圧縮システムの実施形態によっては、胃内滞留システムを圧縮するために、特定の回転方向を更に必要とすることがある。
実施形態によっては、胃内滞留システムの更なる方向付け及び位置決めのために、ピックアンドプレースシステムを使用することがある。ピックアンドプレースシステムは、胃内滞留システムの把持部分と係合するようになっていることがある。ピックアンドプレースシステムの器具の先端が、胃内滞留システムの把持部分と係合するようになっていることがある。実施形態によっては、把持部分に把持ハンドルが含まれていることがあり、ピックアンドプレースシステムは、その把持ハンドルによって胃内滞留システムを持ち上げるようになっていることがある。実施形態によっては、胃内滞留システムの把持部分の表面形状は、真空カップの形状と一致するようになっていることがあり、その結果、十分な吸引力が把持部分に印加されて、ピックアンドプレースシステムが胃内滞留システムを持ち上げて圧縮器具内に配置することが可能になる。例によっては、胃内滞留システムの把持部分に、可撓性アパーチャが設けられることがある。このアパーチャ内に挿入されて広がるようになっている拡張ヘッドが、摩擦によってこの可撓性アパーチャを把持することができ、ピックアンドプレースシステムが胃内滞留システムを持ち上げて圧縮器具内に配置できるようにする。実施形態によっては、ピックアンドプレースシステムは、胃内滞留システムを持ち上げて圧縮器具内に配置するために把持表面の外縁部を掴むことができる、空気圧駆動式の把持アームを含むことがある。ピックアンドプレースシステムは、胃内滞留システムの把持部分と適切に係合するために、胃内滞留システムの有無、位置、及び向きを認識するための光学センサを含むことがある。例えば、ピックアンドプレースシステムは、胃内滞留システムの回転方向に関わらず、ハンドル内の開口部の向きを認識して、把持ツールをハンドルと係合するように適切に位置決めすることができる。
実施形態によっては、胃内滞留システムを受け取り、整列、方向付けするために、振動式すり鉢状送り装置及びピックアンドプレースツールを組み合わせて使用することがある。例えば、振動式すり鉢状送り装置を、主に、絡み合った胃内滞留システムを塊から分離し、分離された個々のユニットをピックアンドプレースシステムに供給するために使用することができ、次いでピックアンドプレースシステムが、胃内滞留システムの方向付けと圧縮器具への配置を行うことができる。
本開示では、圧縮システム及び器具の複数の異なる実施形態を開示している。一般に、図示した圧縮システムは、カプセルなどの容器の内部に納めることができる圧縮形態に胃内滞留システムを折り畳むようになっている。(例えば、以下の図2~図3で説明するように)単一の連結部材で相互に接続された細長い部材を有する胃内滞留システムの場合、細長い部材(アームと呼ばれることもある)の各々に力をかけて、それぞれのアームの遠位端を互いにより近づけることがある。実施形態によっては、折り畳みは、中心の連結部材の付近で胃内滞留システムをアパーチャの中に押し込むことによって、達成されることがある。実施形態によっては、先細管を使用して、この先細管が胃内滞留システムの容器として最終的に機能するカプセルの開口部寸法よりもわずかにアパーチャが小さくなるまで狭くなるにつれて、アームを徐々に折り畳むことができる。実施形態によっては、ピストンによって連結部材に力が加えられるのと同時に、機械的に可変のアパーチャが胃内滞留システムのアームに圧力を徐々に加えることがある。例によっては、胃内滞留システムの連結部材の中央に力がかかっているときに、ピストンが胃内滞留システムのアームが完全に折り畳まれるのを妨げることがあるので、力は2段階でかけられることがある。例によっては、一旦、連結部材にかけられる力によってアームをこれ以上折り畳むことができなくなると、第2のより大きなピストンを使用して、胃内滞留システムの遠位端に力をかけて、折り畳み及び圧縮プロセスを終えることがある。実施形態によっては、アームを2群に近くに集めて、次いで蝶番機構を使用してこの2群を互いに近づけて最終的な圧縮形態を達成することがある。実施形態によっては、回転可能な蝶番が胃内滞留システムの各アームと個別に係合し、これらのアームを同時に互いに近づけて圧縮形態にすることがある。実施形態によっては、胃内滞留システムのアームを相互接続する可撓性ランナーシステムが把持され、胃内滞留システムのアームに圧縮力をかけるために使用されることがある。
一般的に、胃内滞留システムが圧縮形態にされた後で、その圧縮された胃内滞留システムを直ちに容器に挿入することが好ましい。実施形態によっては、ピストンを使用して圧縮された胃内滞留システムをカプセルに押し込みながら、なおも圧縮力をかけて、胃内滞留システムが非圧縮形態に開くのを防ぐことがある。実施形態によっては、圧縮された又は部分的に圧縮された胃内滞留システムを、格納容器又はカートリッジに装填することがある。実施形態によっては、連続的なカプセル封入の合間に圧縮工程のために一時停止する必要なく、圧縮された滞留システムのスタックに力をかけて、圧縮された滞留システムをカプセルに連続的に放出することにより、カートリッジの中身をカプセルに素早く装填することがある。
実施形態によっては、カプセル封入の前に、胃内滞留システムのアームをまとめて固定するバンド又はキャップによって、胃内滞留システムを圧縮形態に固定することがある。実施形態によっては、胃内滞留システムのアームの遠位端から保持バンドをすべらせてはめ、圧縮形態の周縁部の周りで胃内滞留システムのアームを固定することがある。実施形態によっては、保持キャップがアームの遠位端と直接的に係合して、胃内滞留システムを圧縮形態に固定することがある。保持バンド又は保持キャップは、ゼラチン又はヒドロキシプロピルメチルセルロースなどの、当技術分野で周知の材料から作製されることがある。実施形態によっては、保持バンド又はキャップは、胃内環境では溶解するが口腔又は食道環境では溶解しない材料から作製されることがあり、これにより、胃に届く前にシステムがあまりに早く解放されるのを防止する。更に、そのキャップ又はバンドは、挿入過程中に、胃内滞留システムとカプセルの内壁との間に隙間を生成することができ、これにより、圧縮された胃内滞留システムの外面の被膜表面の摩擦を低減することができる。
実施形態によっては、圧縮可能な胃内滞留システムは、治療薬を含むことができる被膜、又は胃内滞留システムの展開を制御若しくは胃内滞留システム内に収容される治療薬の放出速度を制御するのに使用できる被膜を有することがある。従って、カプセル封入過程の様々な工程で、複数の工程が行われることがある。例えば、胃内滞留システムと接触する表面は、摩擦を最小限に抑えるために、生体適合性のフッ素系重合体などの低摩擦剤で被覆されることがある。更に、システム及び装置は、必要に応じて被膜を省略することもあるカプセル封入過程のために特に意図された位置で胃内滞留システムと物理的に接触するように設計されることがある。更に、受け取り、方向付け、整列、圧縮、固定、及びパッケージ化するシステムの表面は、胃内滞留システムとその被膜に損傷を与えないようにするために、バリや鋭利な縁の無い、滑らかに粉砕された且つ/又はよく研磨された材料(例えば、よく研磨されたステンレス鋼)で構成されることがある。
図、特に本開示の図4~図14と関連付けて本開示のカプセル封入システム及び方法を更に考察する前に、胃内滞留システムの構造、機能、及び目的に関する更なる情報について、以下に開示する。本明細書のカプセル封入システムは、圧縮可能な胃内滞留システムの物理的特性に適応するように設計されている。更に、カプセル封入過程が、胃内滞留システムの適切な機能及び患者への治療薬の送達を妨げないように、配慮しなくてはならない。従って、胃内滞留システムの幾つかの実施形態の動作の詳細及び物理的な詳細を以下に開示する。明示的に開示する実施形態は、限定するものではなく、本明細書で説明するカプセル封入方法及びシステムは、胃内滞留システムの他の物理的形態のカプセル封入にも適合できることは、言うまでもない。
胃内滞留システムの一般原理
胃内滞留システムは、嚥下又は他の方法での投与(例えば、栄養管又は胃管)のいずれかによって、患者の胃に投与されるように設計されることがある。一旦、胃内滞留システムがしかるべき胃の中に置かれると、このシステムは所望の滞留期間(3日間、7日間、2週間、等)の間胃の中に留まることができ、従ってこのことは、胃と小腸を分離する幽門弁を通過するのを阻止することを必然的に伴う。胃内滞留システムは、最小限の突発放出で、滞留期間に渡って治療薬を放出する。胃の中に滞留している間、このシステムは食物又は他の胃の内容物の通常の通過を妨げない。このシステムは、所望の滞留期間の終わりに胃を通過して、患者から容易に排出される。システムが胃から小腸に通過するのが早すぎても、システムが腸閉塞を引き起こすことはなく、やはり、患者から容易に排出される。
投与
胃内滞留システムは、患者が飲み込むことができる、又は飲み込むことができない患者については他の方法で(例えば、胃瘻管、栄養管、胃管、又は胃への他の投与経路を介して)胃に投与することができる、カプセル又は他の容器に収容される。従って、胃内滞留システムは、飲み込むか又は他の方法で投与するのに十分な小さな形状に圧縮するか又は押し縮めることができ、カプセルなどの容器の中に配置されることが好ましい。従って、このシステムは、(折り畳み、圧縮、又はシステムのサイズを縮小させる他の方法により)容器内で圧縮された形態を有するようになっている。これらの胃内滞留システムのカプセル封入に関連した本開示の例について、本開示の様々な実施形態と関連付けて、以下で更に詳細に考察する。
そのような圧縮性の又は圧縮可能なシステムを、図1、図2、及び図2Aに示す。図1に示す胃内滞留システムの環状構造体は、二重らせんにねじることができ、これにより、カプセルの中に置くことができる概ね円筒形の形状に構造が圧縮される。図2及び図2Aに示す胃内滞留システムの星形構造体は、中央部分で折り畳んでカプセルの中に置くことができる。このシステムは、カプセルを飲み込むか、又は胃管によって患者に投与される。
胃の中でのシステムの展開
一旦、カプセル又は他の容器が患者の胃に到達すると、カプセルは溶解し、圧縮された胃内滞留システムを解放する。解放されると、システムは、環状又は星形などの元の形状に戻る。圧縮されていないすなわち非圧縮システムの寸法は、システムが胃の中に留まるべき期間の間、システムの幽門括約筋通過を防ぐのに適した寸法である。実施形態によっては、圧縮された胃内滞留システムは、例えば、カプセルが破損した場合に胃内滞留システムの不測の事態による早すぎる展開を防ぐことができる可溶性保持バンド又はキャップによって、更に固定されることがある。
胃の中にある間、胃内滞留システムは、消化、並びに胃又は胃腸管の他の正常な機能と適合する。胃内滞留システムは、糜粥(部分的に消化された食物)、又は胃を出て幽門括約筋を通って十二指腸に至る他の胃の内容物の通過を妨害も邪魔もしない。
胃内に滞留中のシステムからの治療薬の溶出
胃内滞留システムは、複数のキャリア重合体部材を含む。キャリア重合体部材は、キャリア重合体、分散剤、及び治療薬(又はその塩)を含む。複数のキャリア重合体部材は、1つ以上の連結ポリマー部材によって互いに連結される。薬剤は、システムの所望の滞留期間に、キャリア重合体部材から患者の胃液に溶出する。治療薬の放出は、キャリア重合体部材の適切な処方によって制御され、これには、キャリア重合体部材の処方で分散剤を使用すること、及び薬剤をキャリア重合体及び分散剤に混合する前に治療薬を所望のサイズの粒子にまで粉砕することを含む。更に、胃内滞留システムの外面には被膜が施されることがある。被膜には、更なる治療薬、又は治療薬の放出若しくは胃内滞留システムの滞留期間に影響を与えられる薬剤を含めることができる。本開示の上記及び下記で考察するように、胃内滞留システムのカプセル封入に注意を払い、胃内滞留システムによる治療薬の溶出を変える可能性のある損傷を避けなくてはならない。
胃からのシステムの通過
胃内滞留システムは、適切な時点、即ち、一旦システムの有効な治療薬送達寿命に達したとき、又はシステムの有効な治療薬送達寿命のうちの妥当な割合になった時点で、胃の中から外へ通過する。これは、連結ポリマー部材及びシステムの寸法を適切に選択することで成し遂げられる。完全な状態の非圧縮形態では、胃内滞留システムは幽門括約筋を通過しないように設計されている。連結ポリマー部材は、胃の中での滞留期間中に徐々に崩壊するように選択される。連結ポリマー部材が崩壊によって十分に弱くなると、胃内滞留システムは小さな断片に分解され、幽門括約筋を通過できるようになる。その後、システムは腸を通過し、患者から排出される。
安全要素
望ましい動作モードでは、胃内滞留システムは胃の中に滞留している間は完全な状態の非圧縮形態をとり、所望の滞留期間後に分解されるまでは幽門を通過しない。胃内滞留システムが完全な状態で腸に入ると、腸閉塞をもたらす可能性がある。従って、胃内滞留システムは、腸閉塞の可能性を回避するように、48時間以内、好ましくは24時間以内、より好ましくは12時間以内、更により好ましくは1~2時間以内に、連結ポリマーを溶解させて腸内環境で素早く結合を解くように設計される。これは、連結ポリマーとして腸溶性の重合体を使用することで容易に成し遂げられる。腸溶性重合体は、胃の中で生じる酸性のpH値に対しては比較的耐性があるが、十二指腸でみられるより高いpH値では急速に溶解する。安全要素として腸溶性の連結ポリマーを使用することにより、完全な状態の胃内滞留システムが不都合に小腸に通過するのが防止される。腸溶性の連結ポリマーを使用することで意図された滞留期間の前に胃内滞留システムを除去する方法も提供される。万一システムを除去することが必要な場合、患者は、重炭酸ナトリウム溶液などの弱アルカリ性の溶液を飲むか、又は、水酸化マグネシウム水和物(マグネシアのミルク)又は炭酸カルシウムなどの制酸剤を服用することができ、これにより、胃の中のpH値が上がり、腸溶性連結ポリマーの迅速な崩壊が起こる。その後、胃内滞留システムは分解され、患者から排出される。
定義
「キャリア重合体」は、本発明で使用するために、医薬品などの治療薬と混合するのに適した重合体である。
「親水性治療薬」、「親水性薬剤」、又は「親水性医薬品」は、容易に水に溶ける薬剤である。親水性薬剤は、1mg/ml以上の水への溶解度を有する薬剤として定義される。或いは、親水性薬剤は、1-オクタノール/水系で0.5未満のlog P(対数分配係数P、但しP=(1-オクタノール中の濃度)/(H2O中の濃度))を有する薬剤として定義することもできる。溶解度又はlog Pが測定されるときのpHは1.6であり、胃の中の環境に近い。
「疎水性治療薬」、「疎水性薬剤」、又は「疎水性医薬品」は、容易に水に溶けない薬剤である。疎水性薬剤は、1mg/ml未満の水への溶解度を有する薬剤として定義される。或いは、疎水性薬剤は、1-オクタノール/水系で1を超えるlog P(対数分配係数)を有する薬剤として定義することもできる。或いは、疎水性治療薬は、水よりもエタノール中でより高い溶解度を有する薬剤として定義することができる。或いは、疎水性治療薬は、100%模擬胃液よりも、40%エタノール/60%模擬胃液でより高い溶解度を有する薬剤として定義することができる。
「分散剤」は、治療薬の粒子サイズを最小にし、キャリア重合体マトリックス内で治療薬粒子を分散させるのを助ける物質として定義される。即ち、分散剤は、システムの製造中に粒子の集合又は凝集を最小にするか又は完全に防止するのに役立つ。従って、分散剤は、抗集合活性及び抗凝集活性を有し、キャリア重合体マトリックス内で治療薬の粒子が均等に分布するのを維持するのに役立つ。
「賦形剤」とは、それ自体は治療薬ではなく、治療薬の製剤の際に添加される物質である。賦形剤としては、結合剤、被覆剤、希釈剤、崩壊剤、乳化剤、調味料、流動促進剤、潤滑剤、及び防腐剤が挙げられるが、これらに限定はされない。特定の部類の分散剤は、より一般的な部類の賦形剤に含まれる。
「弾性重合体」又は「エラストマー」(「伸長性重合体」とも呼ばれる)とは、力を加えるとある期間の間元の形状から変形することができ、その後、加えられた力が取り除かれると実質的に元の形状に戻る重合体である。
「連結ポリマー」とは、例えば、第1のキャリア重合体部材を第2のキャリア重合体部材に結合させるなど、他の重合体と互いに結合するのに適した重合体である。
「実質的に一定の血漿レベル」とは、胃内滞留システムが胃の中に滞留する期間に渡って測定される平均血漿レベルの±25%以内に留まる血漿レベルを指す。
「生体適合性の」とは、材料又はシステムを説明するのに使用される場合、その材料又はシステムが、人間などの有機体と接触したときに、有害反応を引き起こさないか、最小限の許容できる有害反応しか引き起こさないことを示す。胃内滞留システムの状況では、生体適合性は、胃腸管の環境で評価される。
本明細書で使用する場合、単数形の「a」、「an」、及び「the」は、そうではないことが示されていない限り、又は文脈がそうではないことを明確に規定しない限り、複数についても述べているものとする。
「患者」、「個体」、又は「対象」とは、哺乳動物、好ましくは人間、又は犬若しくは猫などの家畜を指す。好ましい実施形態では、患者、個体、又は対象は人間である。
本明細書で使用する場合、粒子の「直径」とは、粒子の最長の寸法を指す。
本明細書で開示するシステム及び方法を用いて疾患又は障害を「治療する」とは、疾患若しくは障害又は疾患若しくは障害の1つ以上の症状のいずれかを軽減又は解消するために、或いは、疾患若しくは障害又は疾患若しくは障害の1つ以上の症状の進行を遅らせるために、或いは、疾患若しくは障害又は疾患若しくは障害の1つ以上の症状の重症度を軽減するために、追加の治療薬の有無に関わらず、本明細書で開示するシステムの1つ以上をそれを必要としている患者に投与することとして、定義される。本明細書で開示するシステム及び方法を用いて疾患又は障害を「抑制する」とは、疾患又は障害の臨床症状を抑制するために、或いは、疾患又は障害の有害な症状の発現を抑制するために、追加の治療薬の有無に関わらず、本明細書で開示するシステムの1つ以上をそれを必要としている患者に投与することとして、定義される。治療と抑制との違いは、治療は患者に疾患又は障害の有害な症状が発現した後で行われるものであり、一方、抑制は患者に疾患又は障害の有害な症状が発現する前に行われるものである。抑制は、部分的であることも、実質的に総合的であることも、又は総合的であることもある。一部の疾患又は障害は遺伝するので、遺伝子スクリーニングを使用して疾患又は障害の危険性がある患者を特定することがある。その後、本発明のシステム及び方法を使用して、有害な症状の発現を抑制するために、疾患又は障害の臨床症状を発症する危険性のある無症状の患者を治療することがある。
本明細書で開示するシステムの「治療用途」とは、上記で定義したように疾患又は障害の治療に、本明細書で開示するシステムの1つ以上を使用することと定義される。治療薬の「治療上効果的な量」とは、患者に投与された場合に、疾患若しくは障害、又は疾患若しくは障害の1つ以上の症状を軽減又は解消するのに、或いは、疾患若しくは障害、又は疾患若しくは障害の1つ以上の症状の進行を遅らせるのに、或いは、疾患若しくは障害、又は疾患若しくは障害の1つ以上の症状の重篤度を軽減するのに十分な治療薬の量である。治療上効果的な量は、単回投与として患者に投与するか、複数回投与として分割して投与することができる。
本明細書で開示するシステムの「予防的な使用」とは、上記で定義したように疾患又は障害を抑制するために、本明細書で開示するシステムのうちの1つ以上を使用することと定義される。治療薬の「予防上効果的な量」とは、患者に投与された場合に、疾患又は障害の臨床症状を抑制するのに、或いは、疾患又は障害の有害な症状の発現を抑制するのに十分な治療薬の量である。予防上効果的な量は、単回投与として患者に投与するか、複数回投与として分割して投与することができる。
「約(about)」又は「およそ(approximately)」という用語を使用して本明細書で数値を表現する場合、指定された値に加えて、指定された値に妥当に近い値の両方が含まれるものとする。例えば、「約50℃」又は「およそ50℃」という記載は、50℃自体に加えて50℃に近い値の開示の両方を含む。従って、「約X」又は「およそX」という語句は、値X自体の記載を含む。例えば「およそ50℃~60℃」又は「約50℃~60℃」などのように範囲が示される場合、当然のことだが、指定された両端の値が含まれ、各端点又は両方の端点に近い値は、各端点又は両端点に含まれる。即ち、「およそ50℃~60℃(又は約50℃~60℃)は、「50℃~60℃」と「およそ50℃~およそ60℃」(又は「約50℃~60℃」)の両方の記載と等価である。
特に断りの無い限り、組成物中の成分のパーセントは、重量パーセント、又は重量/重量パーセントで表わされる。組成物において相対重量パーセントという場合、組成物中の全ての成分を合算した総重量パーセントが合計100になることを想定している。1つ以上の成分の相対重量パーセントは、組成物中のそれらの成分の重量パーセントが合計で100になるように上方又は下方に調節することができることは当然であり、これは、どの特定の成分の重量パーセントも、その成分に対して指定された範囲の限界を超えないことが前提である。
本明細書で説明する幾つかの実施形態は、それらの実施形態の様々な要素に関して、「含む(comprising)」又は「含む(comprises)」として列挙される。代替的な実施形態では、それらの要素は、それらの要素に対して適用される「~から本質的になる(consisting essentially of)」又は「~から本質的になる(consists essentially of)」という移行句を用いて列挙されることがある。更なる代替的な実施形態では、それらの要素は、それらの要素に対して適用される「~からなる(consisting of)」又は「~からなる(consists of)」という移行句を用いて列挙されることがある。従って、例えば、構成物又は方法がA及びBを含むものとして本明細書で開示される場合、「A及びBから本質的になる」その構成物又は方法の代替的な実施形態、及び「A及びBからなる」その構成物又は方法の代替的な実施形態も、本明細書で開示されたとみなされる。同様に、様々な要素に関して「~から本質的になる」又は「~からなる」ものとして列挙された実施形態は、それらの要素に「含む」を当てはめたものとしても列挙することができる。最後に、様々な要素に関して「~から本質的になる」ものとして列挙された実施形態は、それらの要素に「~からなる」を当てはめたものとして列挙することもでき、また、様々な要素に関して「~からなる」ものとして列挙された実施形態は、それらの要素に「~から本質的になる」を当てはめたものとして列挙することもできる。
構成物又はシステムが、列挙された要素「から本質的になる」ものとして説明された場合、その構成物又はシステムは、明確に列挙された要素を含み、且つ、処理される状態(状態を処理する構成物の場合)、又は記載したシステムの特性(システムを含む構成物の場合)に実質的に影響を及ぼさない他の要素を含んでもよい。しかしながら、構成物又はシステムは、(システムを扱う構成物の場合)明確に列挙された要素以外の処理される状態に実質的に影響を及ぼす他の要素は含まないか、(システムを含む構成物の場合)システムの特性に実質的に影響を及ぼす他の要素は含まない。即ち、構成物又はシステムが、処理される状態又はシステムの特性に実質的に影響を及ぼす可能性がある、列挙された要素以外の余分な要素を含む場合、その構成物又はシステムは、処理される状態又はシステムの特性に実質的に影響を及ぼすのに十分な程の濃度又は量のそれらの余分な要素を含まない。ある方法が列挙された工程「から本質的になる」ものとして説明される場合、その方法は列挙された工程を含み、且つその方法によって処理される状態又はその方法によって製造されるシステムの特性に実質的に影響を及ぼさない他の工程を含んでもよいが、この方法は、明確に列挙された工程以外の、処理される状態又は製造されるシステムに実質的に影響を及ぼす他の工程は含まない。
本開示は、幾つかの実施形態を提供する。任意の実施形態からの任意の特徴は、可能であるなら、任意の他の実施形態からの任意の特徴と組み合わせることができることが企図されている。このように、開示する特徴を混合した構成は、本発明の範囲内である。
システムの幾何形状
胃内滞留システムについては、様々な幾何学的構成をとることができる。そのような構成の1つを図1に示しており、この構成は非圧縮形態では環状を採用している。胃内滞留システム100は、キャリア重合体部材102、及び連結ポリマーを含む結合部104から構成される。このシステムは、圧縮された形態でカプセル中に詰め込むために、連結ポリマー継手の位置で折り畳むか、らせん状にねじることができる。一旦カプセルが胃の中で溶解すると、システム100は、非圧縮形態の円形に広がり、幽門括約筋の通過を妨げる。この実施形態では、連結ポリマーはエラストマーとしても機能する。キャリア重合体部材102及び結合部104は、必ずしも原寸に比例していない。「アーム」102及び結合部104の寸法(長さ又は直径など)は、図に示したものとは異なることがある。
星形の別の構成を図2に示す。胃内滞留システム200は、放射状に突き出た細長い部材、即ち「アーム」付きの中央エラストマー206を囲んで構築される。そのようなアームの1つが、図では208とラベル付けされている。アームは、外側のキャリア重合体部材202、内側のキャリア重合体部材203、及び連結ポリマーを含む結合部204によって形成される。部材202、204、及び203は共に、この「星型」構造の「アーム」を構成する。エラストマー206はシステムを折り畳んでカプセル内に詰め込むことができる。これらの部材も必ずしも原寸比例しているとは限らない。
図2Aは、3本のアームを持つシステムの別の実施形態を示す。図2又は図2Aの星型構成の場合、アームは、接続エラストマー206の周囲に実質的に均等に離れていることが分かる。従って、N本のアームを有する星型装置の場合、これらのアームは(360/N)度離れていることになる。例えば、図2Aの装置の3本のアームは、約120度離れている。図1及び図2についても、各部材は必ずしも原寸比例しているとは限らない。
図3は図2又は図2Aのシステムの折り畳まれた状態を示しているが、このシステムはカプセル(図示せず)内に詰め込むために折り畳まれている。このシステムは、外側のキャリア重合体部材302、内側のキャリア重合体部材303、連結ポリマーを含む結合部304を備えるアーム308、並びにエラストマー306を有しており、エラストマーは、図2又は図2Aでの構成から変形されている。明確にするために、図3では、外側のキャリア重合体部材302、結合部304、及び内側のキャリア重合体部材303によって形成される「アーム」のうちの2本のみ示されている。図2及び図2Aのシステムに示すように、更なるアームが存在することがある。保持カプセルが胃の中で溶解すると、システム300は図2又は図2Aに示す星形の構成に広がり、システムの滞留期間中に幽門括約筋を通過するのを妨げる。キャリア重合体部材、結合部、及びエラストマーは、必ずしも原寸比例していない。キャリア重合体部材、結合部、及びエラストマーの寸法(長さ又は直径など)は、図に示したものとは異なることがある。
以下で更に詳細に考察するように、カプセル封入システムは、上記の様々な幾何形状、並びに以下で説明する更なる実施形態、並びに本明細書には明記しない圧縮可能な胃内滞留システムに適した幾何形状を含む圧縮可能な胃内滞留システムを提供するために使用することができる、様々なシステム幾何形状に対応するように設計することができる。
システムの寸法
このシステムは、患者がシステムを飲み込むことができる(又は、栄養管若しくは胃瘻管などの代替手段によってシステムを胃の中に導入できる)寸法を有する圧縮状態をとらなければならない。通常、このシステムは、カプセルなどの容器によって圧縮状態に保たれる。実施形態によっては、システムは、更に可溶性の保持バンド又は保持キャップによって圧縮状態に保たれることがある。胃の中に入ると、システムは容器から解放されて、システムが幽門括約筋を通過するのを防ぐ寸法を有する非圧縮状態、即ち広がった構造をとり、従って、システムは胃の中に保持される。
従って、このシステムは薬剤分野で一般に使用されるタイプの標準寸法のカプセルの内部に入らなければならない。米国で使用される標準的なカプセルの寸法を、以下の表1に示す(”Draft Guidance for Industry on Size, Shape, and Other Physical Attributes of Generic Tablets and Capsules”、URL:”https://www.regulations.gov/document?D=FDA-2013-N-1434-0002”を参照)。これらはカプセルの外のり寸法であり、寸法はカプセル製造会社によっても僅かに異なるので、システムは、表1の表示外径よりも約0.5~1mm小さくかつ表示長さよりも約1~2mm短い構成がとれなければならない。
カプセルは、ゼラチン又はヒドロキシプロピルメチルセルロースなどの、当技術分野で周知の材料から作製される。一実施形態では、カプセルは、胃内環境では溶解するが口腔又は食道環境では溶解しない材料から作製され、これにより、胃に届く前にシステムが早く解放されるのを防止する。
一実施形態では、システムは、例えば図3に示すような態様でカプセルに納めるために、圧縮状態に折り畳まれるか又は圧縮される。一旦カプセルが胃の中で溶解すると、システムは、例えば図2又は図2Aに示すような態様の胃内での滞留に適した構成をとる。好ましいカプセルのサイズは、00及び00el(00elサイズのカプセルは、およそ000カプセルの長さを有し、およそ00カプセルの幅を有する)であり、これにより、折り畳まれたシステムの長さ及び直径に制約が課される。
一旦容器から解放されると、システムは、胃内滞留システムの幽門括約筋の通過を防ぐのに適した寸法を有する非圧縮状態をとる。一実施形態では、システムは少なくとも2つの垂直な寸法を有し、それぞれは長さが少なくとも2cmである。即ち、胃内滞留システムは、少なくとも2つの垂直な方向に少なくとも約2cmの長さの測定値を持つ。別の実施形態では、平面に伸びたときの非圧縮状態にあるシステムの外周は2つの垂直な寸法を有し、それぞれは長さが少なくとも2cmである。この2つの垂直な寸法は、約2cm~約7cm、約2cm~約6cm、約2cm~約5cm、約2cm~約4cm、約2cm~約3cm、約3cm~約7cm、約3cm~約6cm、約3cm~約5cm、約3cm~約4cm、約4cm~約7cm、約4cm~約6cm、約4cm~約5cm、又は約4cm~約4cmの長さを別々に有することがある。これらの寸法は、胃内滞留システムが幽門括約筋を通過するのを防ぐ。
以下の説明でのカプセル封入のために使用するカプセルについての記述は、上述のカプセル寸法及び範囲のうちのいずれかを含むことがある。
N本のアーム(Nは3以上)を有する星形の重合体の場合、アームの寸法は、システムが少なくとも2つの垂直な寸法を有し、そのそれぞれが上記の長さであるようにすることができる。例えば、図2Aのシステムは、図2Bに示すように、三角形を外接させることができ、この三角形は、底辺B及び高さHの長さによって表現され、B及びHは垂直であり、これらは上記の通りの長さの2つの垂直な寸法を含む。これらの2つの垂直寸法は、胃内滞留システムの保持を容易にするために、上記のように選択される。
システムは最終的に、所望の滞留期間の終わりに胃の中で分解するように設計される。一旦連結ポリマーが壊れると、システムの残りの部材は、システムが幽門括約筋、小腸、及び大腸を通過できる寸法のものになる。最後に、システムは排便によって、又は小腸及び大腸でシステムが最終的に完全に溶解することで、身体から排出される。
システムの重合体組成
キャリア重合体、連結ポリマー、及びエラストマーの個々の重合体の選択は、システムの多くの特性に影響を及ぼし、例えば、治療薬の溶出速度(キャリア重合体及び他の要因に依存する)、システムの滞留期間(任意の重合体、主に連結ポリマーの崩壊に依存する)、システムが腸に通過した場合のシステムの結合解除時間(本明細書で考察するように、主に連結ポリマーの腸内での崩壊速度に依存する)、並びに圧縮形態でのシステムの保管可能期間(主にエラストマーの特性に依存する)などがそうである。システムは胃腸管に投与されるので、全てのシステム部材が胃腸環境に対して生体適合性であることが必要である。
キャリア重合体部材からの治療薬の溶出速度は、多数の要因によって影響を受ける。それらの要因には、キャリア重合体の組成及び特性(キャリア重合体自体は、数種類の重合体成分及び非重合体成分の混合物であればよい)、親水性/疎水性、荷電状態、pKa、及び水素結合能などの治療薬の特性、並びに胃内環境の特性が含まれる。胃の水性環境では、治療薬、特に親水性の薬剤の突発放出を回避すること(突発放出とは、胃の中でシステムが初めに展開されたときに、活性の薬剤成分が大量に初期送達されることを指す)、及び、数日間から数週間の期間に渡り薬剤の持続的な放出を維持することは、難題である。実施形態によっては、治療薬の突発放出の回避を助けるために、胃内滞留システムの外面に被膜を塗布することもある。従って、以下のカプセル封入システム及び方法は、胃内滞留システム及びその被膜の損傷(例えば、摩擦による)を最小限に抑えるように適合されることがある。
胃の中でのシステムの滞留期間は、連結ポリマーを選択することで調節される。システムは、腸溶性の連結ポリマーを使用しているにも関わらず、最終的には胃の中で分解する、というのも、胃の機械的作用及びpHの変動により、最終的に腸溶性の連結ポリマーが弱まるからである。胃の中で時間に依存して崩壊する連結ポリマーを使用して、システムが分解するまでの時間を調節し、従って滞留期間を調節することができる。一旦システムが分解すると、システムは腸に通過し、その後排出される。
システムで使用されるエラストマーは、このシステムの保管可能期間にとって最も重要である。システムが加圧されると、エラストマーには機械的応力がかかる。次いで、この応力は重合体のクリープを引き起こすことがあり、このクリープは、長期間に渡ると、システムがカプセル又は他の容器から解放されたときに非圧縮構成に戻れなくすることがあり、これにより、その後、システムが胃を早く通過してしまうことになる。重合体のクリープは温度に依存することもあるので、エラストマー及び他の重合体部材を選択する際には、システムの予期される保管条件も考慮する必要がある。
システム部材及び重合体は、胃内環境で全く膨潤しないか、膨潤するとしても最小限でなければならない。部材は、胃内環境での滞留期間中に、約20%以下、約10%以下、又は好ましくは約5%以下しか膨潤してはならない。
キャリア重合体部材のキャリア重合体
キャリア重合体部材は、胃内環境で胃内滞留システムから溶出されるべき治療薬を含有する。治療薬は、キャリア重合体に混合されて、キャリア重合体混合物を形成する。この混合物は、図1、図2、及び図3に示したシステムの棒などのように、システムのキャリア重合体部材として使用するための所望の形状に形成されることがある。本発明で使用するのに適した例示的なキャリア重合体としては、親水性セルロース誘導体(ヒドロキシプロピルメチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシメチルセルロース、ヒドロキシエチルセルロース、カルボキシメチルセルロース、カルボキシメチルセルロースナトリウムなど)、酢酸フタル酸セルロース、ポリビニルピロリドン、エチレン/ビニルアルコール共重合体、ポリビニルアルコール、カルボキシビニル重合体(カルボマー)、Carbopol(登録商標)酸性カルボキシ重合体、ポリカルボフィル、ポリエチレンオキシド(Polyox WSR)、多糖類及びそれらの誘導体、ポリアルキレンオキシド、ポリエチレングリコール、キトサン、アルギン酸塩、ペクチン、アカシア、トラガカント、グアーガム、イナゴマメゴム、酢酸ビニルピロリドンビニル共重合体、デキストラン、天然ガム、カンテン、アガロース、アルギン酸ナトリウム、カラギーナン、フコイダン、ファーセレラン、ラミナラン、イバラノリ属の海藻、キリンサイ属(eucheuma)の海藻、アラビアゴム、ガティガム、カラヤゴム、アラビノガラクタン、アミロペクチン、ゼラチン、ジェラン、ヒアルロン酸、プルラン、スクレログルカン、キサンタン、キシログルカン、マレイン酸無水物共重合体、エチレン無水マレイン酸共重合体、ポリメタクリル酸ヒドロキシエチル、メタクリル酸アンモニウム共重合体(Eudragit RL又はEudragit RSなど)、ポリ(アクリル酸エチル-メタクリル酸メチル)(Eudragit NE)、Eudragit E(メタクリル酸ジメチルアミノエチル及び中性メチルアクリル酸エステルに基づく陽イオン性共重合体)、ポリアクリル酸、ポリメタクリル酸、ポリカプロラクトンなどのポリラクトン、ポリ[ビス-(p-カルボキシフェノキシ)-プロパン無水物]などの重合無水物、ポリテレフタル酸無水物、ポリリシンなどのポリペプチド、ポリグルタミン酸、DETOSUとヘキサンジオール、デカンジオール、シクロヘキサンジメタノール、エチレングリコール、ポリエチレングリコール、及びポリオルトエステル(米国特許第4,304,767号明細書に記載され開示され参照により本明細書に組み込まれる)などのジオールとの共重合体、澱粉、特にアルファ化澱粉、及び澱粉ベースの重合体、カルボマー、マルトデキストリン、アミロマルトデキストリン、デキストラン、ポリ(2-エチル-2-オキサゾリン)、ポリエチレンイミン、ポリウレタン、ポリ乳酸、ポリグリコール酸、ポリ(乳酸-co-グリコール酸)(PLGA)、ポリヒドロキシアルカノエート、ポリヒドロキシブチラート、並びにそれらの共重合体、混合物、ブレンド、及び組み合わせ、が挙げられるが、これらに限定はされない。ポリカプロラクトン(PCL)は、好ましいキャリア重合体である。
他の賦形剤をキャリア重合体に添加して、治療薬の放出を調節することができる。そのような賦形剤は、約1%~15%、好ましくは約5%~10%、より好ましくは約5%又は約10%の量を添加することができる。そのような賦形剤の例としては、Poloxamer 407(Kolliphor P407、Sigma Cat # 62035として入手可能)、Pluronic P407、Eudragit EPO(Evonikから入手可能)、ヒプロメロース(Sigma、Cat # H3785から入手可能)、Kolliphor RH40(Sigma、Cat # 07076から入手可能)、ポリビニルカプロラクタム、ポリ酢酸ビニル、ポリエチレングリコール、及びSoluplus(BASFから入手可能。ポリビニルカプロラクタム、ポリ酢酸ビニル、及びポリエチレングリコールの共重合体)が挙げられる。
キャリア重合体部材の製造方法
治療薬を重合体マトリックスに混合するための混合温度は、通常、約80℃~約120℃の範囲であるが、この範囲の外側の温度で最もよく混合される重合体については、より高い又はより低い温度を使用することがある。遊離結晶の治療薬を使用する場合、混合温度は、薬剤粒子又は結晶が溶けないように、約80℃~約100℃が好ましい。
ホットメルト押し出し成形を使用して、キャリア重合体部材を調製することができる。1軸式、又は好ましくは2軸式装置を使用することができる。上述のように、重合体に混合された薬剤粒子が溶けない温度で溶けるキャリア重合体を使用すべきである、というのも、治療薬の粒子が溶けると、粒子の寸法分布特性が劇的に変わるからである。
溶解及び流し込み成形を使用して、キャリア重合体部材を調製することもできる。キャリア重合体及び治療薬、及び任意の他の所望の成分を一緒に混合する。(やはり、治療薬の粒子が溶けない温度で)キャリア重合体を溶かし、薬剤粒子が溶解物の中で均等に分散されるように溶解物を混合し、型に流し込み、冷却させる。
溶媒流し込み成形を使用して、キャリア重合体部材を調製することもできる。重合体を溶媒に溶かし、治療薬の粒子を添加する。粒子の寸法特性を変えないように、薬剤粒子を溶かさない溶媒を使用する必要がある。その後、溶媒-キャリア重合体粒子の混合物を混合して粒子を均等に分散させ、型に流し込み、溶媒を蒸発させる。
連結ポリマー
連結ポリマーは、1つ以上のキャリア重合体部材を1つ以上のキャリア重合体部材に連結するために、又は1つ以上のキャリア重合体部材を1つ以上のエラストマー部材に連結するために、又は1つ以上のエラストマー部材を1つ以上のエラストマー部材に連結するために使用される。連結ポリマーとして使用するには、腸溶性ポリマーが好ましい。腸溶性ポリマーは、胃の中で生じる状態などの酸性の状態下では比較的に不溶性であるが、小腸で生じる弱酸性から塩基性の状態の下では可溶である。約pH5以上で溶ける腸溶性ポリマーを連結ポリマーとして使用することができる、というのも、小腸の初めの部分である十二指腸のpHは約5.4~6.1の範囲であるからである。胃内滞留システムが完全な状態で幽門弁を通過した場合、腸溶性の連結ポリマーが溶解し、連結ポリマーによって連結されていた部材が分解され、滞留システムが小腸及び大腸を通過できるようになる。治療中に何らかの理由で胃内滞留システムを速やかに除去する必要が生じた場合、胃内滞留システムの速やかな結合解除を誘発するために、患者は弱塩基性水溶液(重炭酸塩溶液など)を飲むことができる。
例示的な連結ポリマーとしては、酢酸フタル酸セルロース、酢酸コハク酸セルロース、フタル酸メチルセルロース、フタル酸エチルヒドロキシセルロース、ポリ酢酸フタル酸ビニル、ポリ酢酸ブチル酸ビニル、酢酸ビニル-マレイン酸無水物共重合体、スチレン-マレイン酸モノエステル共重合体、メタクリル酸メタクリル酸メチル共重合体、アクリル酸メチル-メタクリル酸共重合体、メタクリラート-メタクリル酸-アクリル酸オクチル共重合体、並びにそれらの共重合体、混合物、ブレンド、及び組み合わせ、が挙げられるが、これらに限定はされない。本発明で用いることができる腸溶性ポリマーのうちの幾つかを、それらの溶解pHと共に表2に列挙する。(New York:Marcel Dekker社、2002年の、Drugs and the Pharmaceutical Sciences Volume 126、(Michael J. Rathbone、Jonathan Hadgraft、Michael S. Roberts編集)、第18章Modified-Release Drug Delivery Technology、Mukherji, Gour及びClive G. Wilson著の”Enteric Coating for Colonic Delivery”を参照。)約5又は約5.5以下のpHで溶解する腸溶性ポリマーを使用するのが好ましい。ポリ(メタクリル酸-co-アクリル酸エチル)(EUDRAGIT L 100-55という商品名で販売されている。EUDRAGITは、ドイツ、ダルムシュタット、Evonik Rohm GmbHの登録商標である)が好ましい腸溶性ポリマーである。酢酸フタル酸セルロース、酢酸コハク酸セルロース、及びフタル酸ヒドロキシプロピルメチルセルロースも、適切な腸溶性ポリマーである。
一実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約4を超えるpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約5を超えるpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約6を超えるpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約7を超えるpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約7.5を超えるpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約4~約5の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約4~約6の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約4~約7の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約4~約7.5の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約5~約6の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約5~約7の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約5~約7.5の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約6~約7の間のpHで溶解する。別の実施形態では、胃内滞留システムで使用される腸溶性ポリマーは約6~約7.5の間のpHで溶解する。
連結ポリマーとして使用するのに好ましい更なるポリマーは胃内環境で時間に依存して崩壊するポリマーである。トリアセチンは模擬胃液中で時間に依存して7日間で崩壊し、一方Plastoid Bは模擬胃液中で7日間の期間に渡りその強度を保持する。従って、Plastoid Bとトリアセチンを混合することで、時間に依存して崩壊するポリマーを容易に調製することができる。Plastoid B-トリアセチン混合物の崩壊時間は、混合物中で使用されるPlastoid Bの量を増やすことで延長することができ、一方、混合物中で使用されるPlastoid Bの量を減らすことで崩壊時間を短縮することができる。
実施形態によっては、キャリア重合体部材は、腸溶性ポリマーによって接合されるセグメントから構成される細長い部材(本明細書では実施形態によっては「アーム」とも呼ばれる)である。実施形態によっては、キャリア重合体部材は、腸溶性ポリマーによってシステムのエラストマー部材と接合される。これらの実施形態のいずれにおいても、腸溶性ポリマーがセグメント間の接合、及び細長い部材とエラストマー部材との接合の両方に使用される場合、セグメント間の接合に使用される腸溶性ポリマーは、細長い部材をエラストマー部材に接合するのに使用される腸溶性ポリマーと同じ腸溶性ポリマーであることがあり、或いは、セグメント間の接合に使用される腸溶性ポリマーは、細長い部材をエラストマー部材に接合するのに使用される腸溶性ポリマーとは異なる腸溶性ポリマーであればよい。セグメント間の接合に使用される腸溶性ポリマーは全て同じ腸溶性ポリマーであることがあり、又は全て異なる腸溶性ポリマーであることがあり、又はセグメント間の接合における幾つかの腸溶性ポリマーは同じであり、セグメント間の接合における幾つかの腸溶性ポリマーは異なることがある。即ち、各セグメント間の接合に使用される腸溶性ポリマー、及び細長い部材をエラストマー部材に接合するのに使用される腸溶性ポリマーは、独立して選択することができる。
可撓性連結ポリマー
可撓性連結ポリマー、即ち、エラストマーの連結ポリマー又はエラストマーは、胃内滞留システムの星形構造における中央のポリマーとして使用するのが好ましい。実施例10Bで調製されるエラストマーなどの架橋ポリカプロラクトンは、好ましい可撓性を有する連結ポリマーである。
エラストマー
エラストマー(弾性ポリマー又は伸長性ポリマーとも呼ばれる)は、胃内滞留システムを、例えば折り畳んだり加圧したりすることにより、圧縮されたシステムを含む容器又はカプセルを飲み込んで胃に投与するのに適した形態に圧縮することができる。胃の中でカプセルが溶解すると、胃内滞留システムは、システムの所望の滞留期間の間、患者の幽門括約筋を通過しない形状に広がる。従って、エラストマーは、妥当な保管可能期間の間、カプセル内に圧縮構成で保管することができ、且つカプセルから解放されると、元の形状又はほぼ元の形状に広がることができなければならない。好ましい実施形態では、エラストマーは、表2に列挙されたものなどの腸溶性ポリマーである。別の好ましい実施形態では、システムで使用される連結ポリマーも、エラストマーである。図1は、例えばカプセルに詰め込むために、連結ポリマーによって形成された継手の位置で円形リングを折り畳むという点で、連結ポリマーがエラストマーでもあるシステムの例を示している。
好ましい一実施形態では、連結ポリマーとエラストマーの両方が腸溶性ポリマーであり、これにより、システムが腸に入った場合、又は患者がシステムの通過を誘発するために弱塩基性溶液を飲んだ場合に、システムがより完全にキャリア重合体断片に分解するようになる。
使用することができるエラストマーの例としては、ウレタン-架橋ポリカプロラクトン(実施例10、B項を参照)、ポリ(アクリロイル6-アミノカプロン酸)(PA6ACA)、ポリ(メタクリル酸-co-アクリル酸エチル)(EUDRAGIT L 100-55)、及びポリ(アクリロイル6-アミノカプロン酸)(PA6ACA)とポリ(メタクリル酸-co-アクリル酸エチル)(EUDRAGIT L 100-55)との混合物、が挙げられる(実施例11を参照)。
滞留期間
胃内滞留システムの滞留期間は、システムを胃に投与してからシステムが胃を出てゆくまでの時間として定義される。一実施形態では、胃内滞留システムの滞留期間は約24時間、又は長くても約24時間である。一実施形態では、胃内滞留システムの滞留期間は約48時間、又は長くても約48時間である。一実施形態では、胃内滞留システムの滞留期間は約72時間、又は長くても約72時間である。一実施形態では、胃内滞留システムの滞留期間は約96時間、又は長くても約96時間である。一実施形態では、胃内滞留システムの滞留期間は約5日間、又は長くても約5日間である。一実施形態では、胃内滞留システムの滞留期間は約6日間、又は長くても約6日間である。一実施形態では、胃内滞留システムの滞留期間は約7日間、又は長くても約7日間である。一実施形態では、胃内滞留システムの滞留期間は約10日間、又は長くても約10日間である。一実施形態では、胃内滞留システムの滞留期間は約14日間、又は長くても約14日間である。一実施形態では、胃内滞留システムの滞留期間は約3週間、又は長くても約3週間である。一実施形態では、胃内滞留システムの滞留期間は約4週間、又は長くても約4週間である。一実施形態では、胃内滞留システムの滞留期間は約1ヶ月間、又は長くても約1ヶ月間である。
一実施形態では、胃内滞留システムの滞留期間は約24時間~約7日間の間である。一実施形態では、胃内滞留システムの滞留期間は約48時間~約7日間の間である。一実施形態では、胃内滞留システムの滞留期間は約72時間~約7日間の間である。一実施形態では、胃内滞留システムの滞留期間は約96時間~約7日間の間である。一実施形態では、胃内滞留システムの滞留期間は約5日間~約7日間の間である。一実施形態では、胃内滞留システムの滞留期間は約6日間~約7日間の間である。
一実施形態では、胃内滞留システムの滞留期間は約24時間~約10日間の間である。一実施形態では、胃内滞留システムの滞留期間は約48時間~約10日間の間である。一実施形態では、胃内滞留システムの滞留期間は約72時間~約10日間の間である。一実施形態では、胃内滞留システムの滞留期間は約96時間~約10日間の間である。一実施形態では、胃内滞留システムの滞留期間は約5日間~約10日間の間である。一実施形態では、胃内滞留システムの滞留期間は約6日間~約10日間の間である。一実施形態では、胃内滞留システムの滞留期間は約7日間~約10日間の間である。
一実施形態では、胃内滞留システムの滞留期間は約24時間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約48時間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約72時間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約96時間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約5日間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約6日間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約7日間~約14日間の間である。一実施形態では、胃内滞留システムの滞留期間は約10日間~約14日間の間である。
一実施形態では、胃内滞留システムの滞留期間は約24時間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約48時間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約72時間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約96時間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約5日間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約6日間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約7日間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約10日間~約3週間の間である。一実施形態では、胃内滞留システムの滞留期間は約14日間~約3週間の間である。
一実施形態では、胃内滞留システムの滞留期間は約24時間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約48時間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約72時間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約96時間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約5日間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約6日間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約7日間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約10日間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約14日間~約4週間の間である。一実施形態では、胃内滞留システムの滞留期間は約3週間~約4週間の間である。
一実施形態では、胃内滞留システムの滞留期間は約24時間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約48時間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約72時間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約96時間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約5日間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約6日間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約7日間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約10日間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約14日間~約1ヶ月間の間である。一実施形態では、胃内滞留システムの滞留期間は約3週間~約1ヶ月間の間である。
胃内滞留システムは、システムが胃の中に留まっている滞留時間又は滞留期間の少なくとも一部の間に、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約25%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約50%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約60%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約70%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約75%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約80%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約85%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約90%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約95%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約98%の間、治療上効果的な量の治療薬を放出する。一実施形態では、システムは、滞留期間の少なくとも約99%の間、治療上効果的な量の治療薬を放出する。
胃内滞留システムを用いる治療方法
胃内滞留システムを用いて、長期間に渡る治療薬の投与を必要とする症状を治療することができる。数ヶ月間、数年間、又は無期限を費やすことがある長期間に渡り治療薬を投与する場合、1週間に1回、2週間に1回、又は1ヶ月に1回、胃内滞留システムを投与することで、患者の服薬遵守及び利便性に大きな利点をもたらすことができる。
一旦胃内滞留システムが患者に投与されると、システムは胃内保持期間に渡って治療薬を持続的に放出する。胃内での保持期間が過ぎた後、システムは崩壊し胃から出てゆく。従って、胃内保持期間が1週間のシステムの場合、患者は毎週新しいシステムを飲み込む(又は他の手段を介して胃に投与する)ことになる。従って、一実施形態では、所望の総治療期間T-total(T-totalは、日単位での所望の治療期間)に渡って、複数日間Dの胃内滞留期間(D日は、日単位での胃内滞留期間)を有する本発明の胃内滞留システムを用いてシステム内の治療薬により患者を治療する方法は、この所望の総治療期間に渡り、経口投与又は他の手段によって、D日毎に新たな胃内滞留システムを患者の胃に導入することを含む。患者に投与される胃内滞留システムの数は、(T-total)を(D日)で割ったものになる。例えば、1年間(T-total=365日)の間患者の治療が望まれており、システムの胃内滞留期間が7日間(D日=7日)である場合、7日毎に1回新たなシステムを投与することになるので、およそ52個の胃内滞留システムを365日間に渡って患者に投与することになる。
キット及び製造品
本明細書では、本発明の胃内滞留システムを用いて患者を治療するためのキットも提供される。このキットは、例えば、所望の総治療期間に渡って患者に定期的に投与するのに十分な数の胃内滞留システムを含むことがある。日単位での総治療期間が(T-total)であり、胃内滞留システムの滞留期間が(D日)である場合、このキットは、D日毎の投与のために、((T-total)割る(D日))(整数に丸められる)に等しい数の胃内滞留システムを含む。このキットは、例えば、複数の容器に入った複数の胃内滞留システム(容器はカプセルであってもよい)を含むことがあり、任意選択的に、投与計画、治療期間、或いは、胃内滞留システム及び/又は胃内滞留システムに含まれる治療薬の使用に関係した他の情報についての、印刷した又はコンピュータ可読の説明書を含むこともある。例えば、患者に定められた総治療期間が1年間であり、胃内滞留システムの滞留期間が1週間である場合、このキットは52個のカプセルを含むことがあり、各カプセルが1つの胃内滞留システムを含んでおり、毎週同じ日に1回(例えば、土曜日毎に)1個のカプセルを飲み込むように指示がある。
所望の総治療期間に渡り患者に定期的に投与するのに十分な数の胃内滞留システムを含み、任意選択的に投与計画、治療期間、或いは、胃内滞留システム及び/又は胃内滞留システムに含まれる治療薬の使用に関係した他の情報についての説明書を含む製造品も、本発明に含まれる。製造品は、ディスペンサー、トレイ、又は所定の間隔で患者に胃内滞留システムを投与するのを助ける他の包装などの、適切なパッケージングにより供給することができる。
例示的なシステムの製造/組立
胃内滞留システムの星型構造の実施形態は、キャリア重合体部材を細長い部材形状をした「アーム」として調製することで組み立てることができ、このアームは、中央のエラストマーに接合される。アームが円筒形に調製されると、アームは平坦な近位端(円筒形の一方の基部、第1の基部)、遠位端(円筒形の他方の基部、第2の基部)、及びそれらの端部の間の円筒形の体積を囲む湾曲した外面から構成される。アームは、三角柱、直方体、又は他の形状に調製することもできる。
胃内滞留システムの中央のエラストマーは、図2Cに示す胃内滞留システム250の一実施形態の要素252のように、「星」形に調製することができる。図2Cでは、中央エラストマー252は星形をしている。星の枝部は、キャリア重合体セグメント254に接合される。セグメント254は、腸溶性連結器257を介してキャリア重合体セグメント256に接合される。セグメント256は、腸溶性連結器259を介してキャリア重合体セグメント258に接合される。254-257-256-259-258の組み立て品は、システム250の1本のアームを形成する。次いで、図2Cで254-257-256-259-258として示されるキャリア重合体部材のセグメントから構成される細長い部材(アーム)は、融解接合、接着剤、溶媒溶接、又は他の方法により、星の各枝の端部に接合することができる。
実施例10は、キャリア重合体部材「アーム」(A項)及び中央エラストマー(B項)の調製について記載している。
本発明の胃内滞留システムの製造は、以下の工程を含む方法によって実施することができる。
A.可撓性連結ポリマー部材を形成する工程。実施形態によっては、可撓性連結ポリマー部材は、少なくとも3つの複数の枝部を持つ星形をしている。
B.少なくとも3つの複数のキャリア重合体部材を形成する工程。キャリア重合体部材は、近位端及び遠位端を備える細長い部材である。
なお、形成する工程A及び形成する工程Bは、任意の順序で、又は同時に実施することができる。
C. 細長い部材を可撓性連結ポリマー部材に接合する工程。細長い部材を接合すると、外部抑制力がない場合には、結果として得られる組み立て品は、非圧縮形態の胃内滞留システムである。細長い部材は、非圧縮形態で胃内滞留システムが少なくとも2つの垂直寸法を有し、各寸法が少なくとも2cmである、即ち、胃内滞留システムが少なくとも2つの垂直方向に少なくとも約2cmの長さの測定値を持つように、或いは、平面に伸びて非圧縮形態にある胃内滞留システムの外周が2つの垂直寸法を有し、それぞれが長さが少なくとも2cmであるように、可撓性連結ポリマー部材に接合される。(垂直寸法の長さについて更に可能な値が、システム寸法を説明している章で提供されている。)
患者に投与するために胃内滞留システムをカプセル又は他の容器に入れるために、以下を含む更なる工程を実施することができる。
D.胃内滞留システムを圧縮し、経口投与又は胃管若しくは栄養管を経由して投与するのに適したカプセルなどの容器にシステムを挿入する工程。
上述のように、且つ以下で更に詳細に説明するように、本開示の主な焦点は、胃内滞留システムのカプセル封入のためのシステム及び方法に関する。
可撓性連結ポリマーを形成する工程Aは、射出成形、重力成形、圧縮成形、押し出し成形、又は3次元印刷などによる、成形ポリマーを調製するのに適した任意の方法によって実施することができる。可撓性連結ポリマーは、環状、円環状、球状、扁平楕円体(偏平回転楕円体、楕円体、若しくは偏球とも呼ばれる)状、又は立方体若しくは直方体などの少なくとも1つの回転対称軸を有する任意の他の形状に形成することができる。なお、可撓性連結ポリマーの形状は、細長い部材であるキャリア重合体部材を接合することができる枝部、突起部、又は凸状部を有することがある。また、可撓性連結ポリマーの形状は、細長い部材であるキャリア重合体部材を接合することができるへこみ、凹状部、くぼみ、又は有底穴を有することがある。
同様に、細長い部材形状をした少なくとも3つの複数のキャリア重合体部材を形成する工程Bは、キャリア重合体混合物を使用した射出成形、重力成形、圧縮成形、押し出し成形、又は3次元印刷などの、成形ポリマーを作製するのに適した任意の方法によって、実施することができる。形成の前に、本明細書で説明するように治療薬は粉砕され、その後、本明細書で説明するように適切なキャリア重合体、分散剤、及び他の成分と混合される。細長い部材は、中実直方体、中実三角柱、又は中実円筒の形状に形成されることがある。中実円筒形が好ましい。更に、本明細書に記すように、細長い部材は、連結ポリマーで結合された、好ましくは腸溶性ポリマーで結合された、2つ、3つ、またはそれ以上のセグメントから形成することができる。細長い部材は、突き合わせ継手を使用してセグメントを互いに結合することで(即ち、1つのセグメントの端部を別のセグメント端部に接着により、例えば両方のセグメントの端部の間に挟んだ接着性の腸溶性ポリマーフィルムにより、結合することができる)、又はセグメントを一緒に融解させることで形成することができ、或いは、カラー継手を使用してセグメントを互いに結合することで形成することができる(即ち、腸溶性ポリマーフィルムを2つのセグメントの端部の周りに巻いて、それらを互いに結合することができる)。
キャリア重合体部材の細長い部材を可撓性連結ポリマー部材に接合する工程Cは、融解接合、接着剤、溶媒溶接、又はポリマーの接合に適した任意の他の方法などの様々な方法により実施することができる。可撓性連結ポリマーが枝部を有する場合、キャリア重合体部材の細長い部材を可撓性連結ポリマー部材に接合するのにカラー継手を使用することができる。キャリア重合体部材の細長い部材と可撓性連結ポリマー部材との接合部は、腸溶性ポリマーを使用して形成することができる。一旦キャリア重合体部材を可撓性連結ポリマー部材に接合すると、外部抑制力が無い場合には、胃内滞留システムは非圧縮形態になる。
胃内滞留システムを圧縮し、そのシステムを容器に挿入する工程Dは、手動で又は機械的に、胃内滞留システムを圧縮形態に圧縮、折り畳み、又は加圧し、そのシステムを適切な大きさのカプセル又は他の容器に挿入することで実施することができる。胃内滞留システムを圧縮し容器にカプセル封入する技術については、以下でより詳細に考察する。
システムの圧縮及びカプセル封入
以下は、圧縮可能な胃内滞留システムを圧縮してカプセル封入するシステム及び方法の実施形態の詳細である。実施形態によっては、圧縮可能な胃内滞留システムは、1つ以上のセグメントを連結する連結部材を含むことがある。
実施形態によっては、この方法は、以下の工程のうちの1つ以上を含むことがある。
A.非圧縮形態で、圧縮可能な胃内滞留システムを受け取る工程。実施形態によっては、圧縮可能な胃内滞留システムは、例えば、振動式すり鉢状送り装置又はピックアンドプレースコンベヤーで受け取られることがある。
B.圧縮可能な胃内滞留システムを圧縮位置に方向付ける工程。
C.圧縮可能な胃内滞留システムを圧縮形態に圧縮する工程。
D.圧縮形態にある圧縮可能な胃内滞留システムを容器の開口部に挿入する工程。実施形態によっては、圧縮可能な胃内滞留システムを、容器に挿入する前に、バンド又はキャップなどの保持要素によって圧縮形態に固定して、カプセルにかかる圧力を最小限に抑えるか、且つ/又は、カプセルが損傷したり早期に展開されたりした場合に圧縮可能な胃内システムが展開するのを防止することがある。
図4A~図4Dは、整列器具(図示せず)に向けて胃内滞留システム402を整列させ送達するための例示的な振動式すり鉢状送り装置400を示す。図4Aでは、胃内滞留システム402の堆積物の塊403が、個々の胃内滞留システムが異なる方向に向いている状態で、振動式すり鉢状送り装置400に堆積されることがある。実施形態によっては、星形の胃内滞留システム402の広がったアームが互いに絡まり合うことがある。この状況では、圧縮及びカプセル封入のための位置に置くために、個々の胃内滞留システムをつかむ及び/又はつまむのが困難なことがある。当然ながら、星形以外の他の形態の胃内滞留システムも同様に絡み合うことがあり、結果的に同じ困難をもたらすことがある。実施形態によっては、振動式すり鉢状送り装置400の振動により、胃内滞留システムが位置を移動し、互いに分離するようになる。図4Bは、少数の個々の胃内滞留システム405、406、407、及び408が、振動式すり鉢状送り装置の中心付近の堆積物の塊から分離し、それらの胃内滞留システムが振動によって推し進められるにつれて、送り装置のらせん状の行路404に沿って上昇し始める様子を示す。図示されるように、胃内滞留システムは、胃内滞留システム407と比較した胃内滞留システム405及び406の向きなどのように、異なる向きで上昇することがある。胃内滞留システムがすり鉢状送り装置の振動によって移動する際の胃内滞留システムの運動の例示的な方向を、410で示す矢印で示す。
図4Cは、胃内滞留システムが振動式すり鉢状送り装置のらせん状行路を更に上昇している様子を示す。実施形態によっては、らせん状行路の形状及び材料特性は、下流の機器に送達するのに好ましい向きに胃内滞留システムを向けるように設計されることがある。胃内滞留システムは、前に図4Bに示した矢印410で示す方向とほぼ同じ運動の方向に続くことがある。胃内滞留システム402は、図4Cでは上行性らせん行路のうちの一階層を占有しているのが示されているが、当然ながら、振動式すり鉢状送り装置400の底部にある塊403からの胃内滞留システムは、塊から分離して、図4Bに示すようにらせんのより低階層に沿って上方へ移動し続けており、図示した胃内滞留システムは、上行性らせん行路のより高階層へ上昇し続ける。図4Dは、胃内滞留システムが上行性らせん行路の頂部に達し、配向フィルタ412に達する様子を示しており、この配向器具は、所望の向きではない胃内滞留システム(例えば、414)が上行性らせん行路の終端部を通過するのを防止する機械的構造であってもよい。実施形態によっては、正しくない向きで配向フィルタ412に到達する胃内滞留システムは、振動式すり鉢状送り装置400の底部にある塊403に戻るように外されることがある。実施形態によっては、配向器具を使用して、この器具に到達した所望の向きになっていない胃内滞留システムを、塊に戻すように外すのではなく、再整列させることもある。このようにして外された胃内滞留システムは、振動式すり鉢状送り装置の底部にある堆積物の塊に戻されることがあり、特定の胃内滞留システムが優先的な向きでフィルタに到達するまで、この過程が始めから繰り返されることがある。
図4A~図4Dは、例えば上記の図2A~図2Cに示したような、星形構造の胃内滞留システムのための振動式すり鉢状送り装置の実施形態を示している。しかしながら、本開示の範囲から逸脱することなく、他の形状の胃内滞留システム(例えば、図1に示したような環状構造)を使用することもできることは、言うまでもない。更に、6本のアームを備えた星形構造を示したが、当然ながらこの振動式すり鉢状送り装置は、システムが図2Bに関して上述したような少なくとも2つの垂直寸法を持てるような、N本のアーム(Nは3以上)を備えた星形構造でも使用することができる。
図5A~図5Dは、胃内滞留システムを、圧縮器具によって圧縮形態に圧縮するための位置に配置するためのピックアンドプレースシステム500の実施形態を示す。図5Aは、胃内滞留システムの一部と係合するようになっている治工具先端504を含むロボットアーム502を示す。一実施形態では、治工具先端は、胃内滞留システム506の把持部分の表面形状と嵌合するようになっている表面形状を有する真空カップであってもよい。実施形態によっては、胃内滞留システム506の把持部分は、凹状の表面、凸状の表面、又は滑らかで平坦な表面であればよい。対応する真空治工具先端は、治工具先端と胃内滞留システムの把持部分との間の吸引力を最大にするように、それぞれ凸状、凹状、又は滑らかで平坦であればよい。実施形態によっては、治工具先端504は、空気圧駆動式の把持アームであってもよい。実施形態によっては、治工具先端は、胃内滞留システムの把持部分を突き刺す針であってもよい。
実施形態によっては、胃内滞留システムの把持部分は、胃内滞留システムの把持部分508上に形成された突起であってもよい。実施形態によっては、この突起はハンドルのような形状をしていることがあり、空気圧駆動式の把持アームの把持部分がこのハンドルと係合することができる。実施形態によっては、空気圧駆動式の把持アームは、胃内滞留システムの把持部分508の外面と直接的に係合することがある。実施形態によっては、ロボットアーム502は、光学式認識技術を利用して、胃内滞留システムの有無及び向きを認識することがある。胃内滞留システム506は、表面510上に配置されることがある。実施形態によっては、表面510は、胃内滞留システムを拾い上げて圧縮のための位置に配置するロボットアームの近傍に胃内滞留を運ぶためのコンベヤーベルトであってもよい。実施形態によっては、表面510は、比較的に平坦な任意の表面であってもよい。
図5Bは、ロボットアーム502が胃内滞留システム506との接触位置に配置されて、胃内滞留システムの把持部分と係合する様子を示す。図5Cは、ロボットアーム502が胃内滞留システム506を表面510から離すように持ち上げている様子を示し、図5Dは、胃内滞留システムを圧縮し、容器にカプセル封入するために胃内滞留システムを準備するための器具512上に胃内滞留システムを配置している様子を示す。
図6A~図6Dは、胃内滞留システムを、圧縮器具によって圧縮形態に圧縮するための位置に配置するためのピックアンドプレースシステム600の更なる実施形態を示す。図6Aは、可撓性連結部材604から延びる6本の拡張アームを有し、この連結部材の中央を貫通するアパーチャ606を有する、星形の胃内滞留システム602の上面図を示す。実施形態によっては、連結部材開口部の幾何形状は、円環状であってもよい。連結部材は、上述のようなエラストマーなどの可撓性材料から作製されることがある。(例えば、図5A~図5Dに関して上述したような)ロボットアームの治工具先端608は、胃内滞留システム602の連結部材604のアパーチャ内に嵌合できる拡大可能な六角形のヘッドであればよい。図6Bは、拡大可能な六角形ヘッドの器具先端608が、ヘッドが拡大する前に、連結部材604のアパーチャ606内に配置されている様子を示す。
図6Cは、連結部材604のアパーチャ606内でヘッドが拡大された後の、拡大可能な六角形ヘッドの治工具先端608を示す。可撓性連結部材604は、拡大可能な六角形ヘッドの治工具先端608によって加えられる外向きの力によって僅かに変形し、従って、摩擦によって胃内滞留システムを把持することができる。図6Dは、胃内滞留システムを拡大可能な六角形ヘッドの器具先端608によって把持したときに、圧縮及び容器へのカプセル封入のための器具612上に配置する様子を示す。なお、図6A~図6Dで説明した実施形態は、上述したようなロボットアームに取り付けられる治工具先端の更なる変形例を提供するものである。
図7A~図7Cは、胃内滞留システム702を圧縮し、その胃内滞留システムを錠剤カプセルなどの容器に挿入するための第1の例示的な圧縮システム700を示す。実施形態によっては、先細管が、上述した器具512及び612に対応することがある。実施形態によっては、胃内滞留システムのアームが管の表面上に面一に置かれるように寸法決めされた先細管704の上部に、胃内滞留システムを配置することがある。実施形態によっては、管の開口部の直径は、アーム706の遠位端が先細管704の開口部の縁に載るように寸法決めされることがある。実施形態によっては、一次ピストン708が、胃内滞留システム702の連結部材710に力を加えるようになっていることがある。胃内滞留システムの連結部材710に対して一次ピストンによって加えられる力により、アーム706を折り畳むことができる。初期の力が、胃内滞留システム702のアームの遠位端706に加えられ、従って、胃内滞留システムの最小の曲げ力に打ち勝つための最大のてこの作用がもたらされることがある。
本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムの曲げ力は、(図7Aに示すように)アームが曲げ力によって曲げられていない時の位置では、少なくとも約0.1ニュートンである。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、曲げ力がかけられていない時に占める位置から約5度よりも大きくアームが曲げられた時に、少なくとも約0.2ニュートンの曲げ力を有する。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、曲げ力がかけられていない時に占める位置から約5度よりも大きくアームが曲げられた時に、少なくとも約0.4ニュートンの曲げ力を有する。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、曲げ力がかけられていない時に占める位置から約10度よりも大きくアームが曲げられた時に、少なくとも約0.2ニュートンの曲げ力を有する。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、曲げ力がかけられていない時に占める位置から約10度よりも大きくアームが曲げられた時に、少なくとも約0.6ニュートンの曲げ力を有する。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、(例えば、図7Cに示すように)曲げ力がかけられていない時に占める位置から約45度よりも大きくアームが曲げられた時に、少なくとも約0.2ニュートンの曲げ力を有する。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、曲げ力がかけられていない時に占める位置から約45度よりも大きくアームが曲げられた時に、少なくとも約1.5ニュートンの曲げ力を有する。実施形態によっては、胃内滞留システムは最大で約6.5ニュートンの曲げ力を有する。実施形態によっては、胃内滞留システムは最大で約4.0ニュートンの曲げ力を有する。実施形態によっては、胃内滞留システムは最大で約2.0ニュートンの曲げ力を有する。
図7Bは、胃内滞留システム702が一次ピストン708の力がかかることで部分的に折り畳まれたすなわち圧縮されたことを示す。一次ピストン708によって胃内滞留システム702に力がかけられと、先細管704の壁がアーム706をピストンに向けて内側に徐々に押し込みし、胃内滞留システムが先細管の中に押し込まれるにつれて、次第にアームを互いに近づけることができる。実施形態によっては、胃内滞留システム702と接触する先細管704の表面を研磨して、胃内滞留システムを損傷する危険性のある粗さ及び鋭利な縁を減らすことができる。実施形態によっては、胃内滞留システム702と接触する管の表面は、生体適合性のフッ素系重合体などの低摩擦被膜で被覆されてもよい。更に、胃内滞留システムと先細管との間の摩擦を低減することで、胃内滞留システムの外面に塗布された被膜又は医薬品を保護することができる。図7Bは、先細管704のある地点を過ぎた後で、且つ一次ピストン708の太さに応じて、ピストンがアーム706の間に閉じ込められて、ピストンが胃内滞留システムを圧縮形態に更に折り畳むのを妨げることがあることを、更に示している。この問題に対する1つの解決策は、ピストンを細くして、胃内滞留システムが十分に閉じて容器に押し込込まれるようにすることである。しかしながら、ピストンが細過ぎると、一次ピストン708によって胃内滞留システム702の連結部材710にかけられた力により、胃内滞留システムの構造に穴が開くかさもなければ損傷を受ける可能性がある。
実施形態によっては、ピストンの最小接触表面積は、約15平方ミリメートルであることが好ましい。実施形態によっては、ピストンの最小接触表面積は、約28平方ミリメートルであることが好ましい。実施形態によっては、ピストンの最小接触表面積は、約35平方ミリメートルであることが好ましい。実施形態によっては、大き過ぎる一次ピストン708は、図7Cで以下に説明するように、更なる処理工程で終わるべき折り畳み及び圧縮過程で、胃内滞留システムの十分な折り畳みを妨げることがある。一次ピストン708の接触表面積は、やはり制限要因となり得る、というのも、アームが、胃内滞留システムの連結部材710に接合された端部で互いに最接近することになるからである。従って、一次ピストンの最大接触表面積は、約20平方ミリメートルであることが好ましい。実施形態によっては、一次ピストンの最大接触表面積は、約33平方ミリメートルであることが好ましい。実施形態によっては、一次ピストンの最大接触表面積は、約40平方ミリメートルであることが好ましい。実施形態によっては、一次ピストンの最大接触表面積は、約80平方ミリメートルであることが好ましい。
図7Cは、第2段階中の例示的な圧縮システムの第2段階を示す。実施形態によっては、一次ピストン708が後退する一方でより大きい接触面積の二次ピストン712が胃内滞留システム702のアーム706の遠位端と係合して、胃内滞留システムが圧縮状態に完全に折り畳まれるまで、先細管704の中を胃内滞留システムを押し込み続けることがある。実施形態によっては、完全に圧縮された状態だと、胃内滞留システムの隣接するアーム706が互いに接触した状態となる。実施形態によっては、完全に圧縮された状態だと、アームが最も近くの隣接するアームからの最小の隙間を持つことになる。先細管704の底部の開口部は、圧縮された胃内滞留システムを受け取る容器(図示せず)の開口部よりも、わずかに大きくてもよい。実施形態によっては、容器は半カプセルであってもよい。胃内滞留システム702を半カプセルに完全に挿入した後で、カプセル内への胃内滞留システムの完全な封入を完了することができる。図8A~図8Bに関して以下で考察するように、先細管704を使用して、カプセル又は半カプセル以外の容器に挿入するように胃内滞留システム702を圧縮することもできる。
実施形態によっては、先細管704の上部開口部の直径は、少なくとも約30ミリメートルであってもよい。実施形態によっては、先細管704の上部開口部の直径は、少なくとも約40ミリメートルであってもよい。実施形態によっては、先細管704の上部開口部の直径は、少なくとも約45ミリメートルであってもよい。
実施形態によっては、先細管704の上部開口部の直径は、長くても約35ミリメートルであってもよい。実施形態によっては、先細管704の上部開口部の直径は、長くても約45ミリメートルであってもよい。実施形態によっては、先細管704の上部開口部の直径は、長くても約50ミリメートルであってもよい。
実施形態によっては、先細管704の底部の開口部の直径は、少なくとも約8.2ミリメートルであってもよい。実施形態によっては、先細管704の底部の開口部の直径は、少なくとも約9.8ミリメートルであってもよい。
実施形態によっては、先細管の逓減角度は少なくとも約5度であってもよい。実施形態によっては、先細管の逓減角度は少なくとも約15度であってもよい。実施形態によっては、先細管の逓減角度は少なくとも約30度であってもよい。実施形態によっては、先細管の逓減角度は少なくとも約45度であってもよい。実施形態によっては、先細管の逓減角度は最大で約15度であってもよい。実施形態によっては、先細管の逓減角度は最大で約30度であってもよい。実施形態によっては、先細管の逓減角度は最大で約45度であってもよい。実施形態によっては、先細管の逓減角度は最大で約60度であってもよい。
実施形態によっては、2つのアームの間又は胃内滞留システムの2つの折り畳み部分の間には隙間がある。実施形態によっては、この隙間は、保管中に胃内滞留システムの表面の損傷を防ぐのに役立つことがある。この隙間は、互いに接触する胃内滞留システムの表面の接着を防ぐこともある。実施形態によっては、圧縮状態にある胃内滞留システムの隣接するアーム間の好ましい最小の隙間は、約0.01ミリメートルであることが好ましい。実施形態によっては、圧縮状態にある胃内滞留システムの隣接するアーム間の好ましい最小の隙間は、約0.05ミリメートルであることが好ましい。実施形態によっては、圧縮状態にある胃内滞留システムの隣接するアーム間の好ましい最小の隙間は、約0.1ミリメートルであることが好ましい。実施形態によっては、この好ましい最小の隙間は、約0.2ミリメートルであることが好ましい。なお、アーム706間に設けられる隙間が大きすぎると、カプセルの寸法を大きくする必要があり、あるいは胃内滞留システムの寸法を小さくする必要がある。従って、実施形態によっては、胃内滞留システムの隣接するアーム間の好ましい最大の隙間は、約0.07ミリメートルである。実施形態によっては、胃内滞留システムの隣接するアーム間の好ましい最大の隙間は、約0.15ミリメートルである。実施形態によっては、胃内滞留システムの隣接するアーム間の好ましい最大の隙間は、約0.25ミリメートルである。
図8A~図8Bは、複数の圧縮された胃内滞留システムを同時に保持できるカートリッジ806に、複数の胃内滞留システム802を連続的に挿入するようになっている、例示的な圧縮システム800を示す。圧縮システム804は先細管として示されているが、当然ながら、本開示の範囲から逸脱することなく、本開示全体を通して開示されるような胃内滞留システム802を圧縮できる任意の適切な圧縮システムを使用することができる。上述のように、1つ以上のピストン808を使用して胃内滞留システム802を圧縮形態に押し込み、アパーチャを通過させることができる。実施形態によっては、圧縮された胃内滞留システム802をカプセルに挿入するのではなく、複数の胃内滞留システムを保持するようになっているカートリッジ806に胃内滞留システムを入れることがある。胃内滞留システムが圧縮システム800のアパーチャを通過するとき、胃内滞留システムがカートリッジに完全に挿入されるまで、ピストンがカートリッジ806の内容物に対して胃内滞留システムを押すことがある。この過程は、所望の数の胃内滞留システム802がカートリッジに挿入されるまで繰り返されることがある。実施形態によっては、充填されたカートリッジ806は、容器に挿入するための別個のシステムまで直ちに移動されることがある。実施形態によっては、充填されたカートリッジ806は、容器への挿入が望まれるまで、貯蔵庫に移動されることがある。
図8Bは、本開示の例による例示的な挿入システム850を示す。図示のように、圧縮された胃内滞留システム802を含むカートリッジ806を、容器(例えば、半カプセル)とピストン810との間に配置することがある。実施形態によっては、ピストン810が、カートリッジ806の一方の端部で胃内滞留システムに力をかけることがあり、カートリッジの反対側の端部から異なる胃内滞留システムが出てきて容器812に挿入されることがある。なお、図8Bではカートリッジ806と容器812との間に大きな空間があるように示されているが、胃内滞留システムが圧縮位置から開いてしまう危険性がないように、カートリッジ806と容器812との間の間隔を最小限に抑えることが望ましい。この挿入システムは、カートリッジの中身が尽きるまで、各胃内滞留システム802に別々の容器を供給しながら、カートリッジ806の中でピストン810を押し続けることができる。その後、ピストン810がカートリッジ806から取り除かれ、別の装填済カートリッジを用済みのカートリッジと入れ替えることで、この過程が素早く繰り返される。カートリッジ806内の胃内滞留システム802を個別に圧縮する必要がないので、滞留システムをカプセルに挿入する過程は非常に素早く実施することができる。実施形態によっては、カートリッジから個々の容器に胃内滞留システムを連続的に挿入する合間の最大時間は、約15秒未満であることが好ましい。実施形態によっては、カートリッジから個々の容器に胃内滞留システムを連続的に挿入する合間の最大時間は、約5秒未満であることが好ましい。実施形態によっては、カートリッジから個々の容器に胃内滞留システムを連続的に挿入する合間の最大時間は、約0.5秒未満であることが好ましい。実施形態によっては、カートリッジから個々の容器に胃内滞留システムを連続的に挿入する合間の最大時間は、約0.02秒未満であることが好ましい。
図9A~図9Cは、胃内滞留システム902を圧縮し、その胃内滞留システムを容器に挿入するための第2の例示的な圧縮システム900を示す。例示的な圧縮システム900では、胃内滞留システムを機械式アパーチャ904の上部に配置することができる。例によっては、機械式アパーチャ904は、上述の器具512及び612に対応することがある。実施形態によっては、機械式アパーチャ904の穴910の初期寸法は、アーム906の遠位端が機械式アパーチャの穴の縁に接触するように、選択されることがある。実施形態によっては、ピストン908が、胃内滞留システム902の連結部材912に力を加えるようになっていることがある。胃内滞留システムの連結部材912に対して一次ピストンによって加えられる力により、アーム906を折り畳むことができる。初期の力が、胃内滞留システム902のアームの遠位端906に加えられ、従って、胃内滞留システムの最小の曲げ力に打ち勝つための最大のてこの作用が生み出されることがある。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは少なくとも約0.1ニュートンの曲げ力を有する。本明細書で説明する胃内滞留システムの実施形態によっては、胃内滞留システムは、図7A~図7Dに関して上述したような異なる曲げ角度に関連した最小値、最大値、及び範囲内の曲げ力を有する。
図9Bは、胃内滞留システム902が、一次ピストン908により力をかけられた後で部分的に折り畳まれたすなわち圧縮された後の圧縮システム900を示す。一次ピストン908によって胃内滞留システム902に力がかかると、機械式アパーチャ904の穴910の寸法が徐々に小さくなり、アーム906をピストンに向けて内側に押し、胃内滞留システムが押し込まれ且つ穴の寸法が小さくなるにつれて、次第にアームを互いに近づけることができる。実施形態によっては、上述の圧縮システム700及び800と比べると、胃内滞留システム902と接触する機械式アパーチャの表面積は胃内滞留システムの表面のはるかに小さな部分と作用することがある。特に、一旦ピストンによって初期の力がかけられると、閉じていく機械式アパーチャ904は胃内滞留システムを更に圧縮するための力の主な源となることができる。実施形態によっては、機械式アパーチャは、胃内滞留システムのアームの切り欠き又は溝と嵌合するようになっていてもよい。このようにして、胃内滞留システムが圧縮されている間の滑りを防ぐことができ、上述のような被膜を含む胃内滞留システムの外面の摩擦損傷を防ぐことができる。実施形態によっては、ピストン908は、アーム906の初期位置とアームが部分的に圧縮された位置との間に少なくとも約75度の角度が形成されるまでの間だけ、力をかけ続けることがある。摩擦を受ける胃内滞留システムの表面の面積を減らすことで、胃内滞留システムの外面に塗布された被膜を保護することができる。図9Bは、機械式アパーチャ904の穴910のある閉じ量を過ぎた後で、且つ一次ピストン908の太さに応じて、ピストンがアーム906の間に閉じ込められて、ピストンが胃内滞留システムを圧縮形態に更に折り畳むのを妨げることがあることを、更に示している。この問題に対する1つの解決策は、ピストンを細くして、胃内滞留システが十分に閉じて容器に押し込まれるようにすることである。しかしながら、ピストンが細すぎると、一次ピストン908によって胃内滞留システム902の連結部材910にかけられた力により、胃内滞留システムの構造に穴が開くかさもなければ損傷を受ける可能性がある。
実施形態によっては、ピストンの最小接触表面積は、約15平方ミリメートルであることが好ましい。実施形態によっては、ピストンの最小接触表面積は、約28平方ミリメートルであることが好ましい。実施形態によっては、ピストンの最小接触表面積は、約35平方ミリメートルであることが好ましい。実施形態によっては、一次ピストン908が大きすぎると、図7Cで上記で説明したように、更なる処理工程で終わるべき折り畳み及び圧縮過程で、胃内滞留システムの十分な折り畳みを妨げることがある。一次ピストン908の接触表面積は、やはり制限要因となり得る、というのも、アームが胃内滞留システムの連結部材912に接合された端部で互いに最接近することになるからである。従って、一次ピストンの最大接触表面積は、約20平方ミリメートルであることが好ましい。実施形態によっては、一次ピストンの最大接触表面積は、約33平方ミリメートルであることが好ましい。実施形態によっては、一次ピストンの最大接触表面積は、約40平方ミリメートルであることが好ましい。実施形態によっては、一次ピストンの最大接触表面積は、約80平方ミリメートルであることが好ましい。
図9Cは、第2段階中の例示的な圧縮システムの第2段階を示す。実施形態によっては、一次ピストン908が後退する一方でより大きい接触面積の二次ピストン912が胃内滞留システム902のアーム906の遠位端と係合して、胃内滞留システムが圧縮状態に完全に折り畳まれるまで、先細管904の中を胃内滞留システムを押し込み続けることがある。実施形態によっては、完全圧縮状態だと、胃内滞留システムの隣接するアーム906が互いに接触した状態となる。実施形態によっては、完全圧縮状態だと、アームが最も近くの隣接するアームからの最小の隙間を持つことになる。先細管904の底部の開口部は、圧縮された胃内滞留システムを受け取る容器(図示せず)の開口部よりも、わずかに大きいことがある。実施形態によっては、容器は半カプセルであってもよい。胃内滞留システム902を半カプセルに完全に挿入した後で、カプセル内への胃内滞留システムの完全な封入を完了することができる。図8A~図8Bに関して上記で考察したように、機械式アパーチャ904を使用して、カプセル又は半カプセル以外の容器に挿入するように胃内滞留システム902を圧縮することもできる。
実施形態によっては、圧縮状態にある胃内滞留システムの隣接するアーム間の好ましい最小の隙間は、約0.01ミリメートルであることが好ましい。実施形態によっては、圧縮状態にある胃内滞留システムの隣接するアーム間の好ましい最小の隙間は、約0.05ミリメートルであることが好ましい。実施形態によっては、圧縮状態にある胃内滞留システムの隣接するアーム間の好ましい最小の隙間は、約0.1ミリメートルであることが好ましい。実施形態によっては、この好ましい最小の隙間は、約0.2ミリメートルであることが好ましい。なお、アーム906間に設けられる隙間が大きすぎると、胃内滞留システムによって送達できる治療薬の量を、与えられた利用可能な容器の体積に対して最大にできない可能性がある。従って、実施形態によっては、胃内滞留システムの隣接するアーム間の好ましい最大の隙間は、約0.07ミリメートルである。実施形態によっては、胃内滞留システムの隣接するアーム間の好ましい最大の隙間は、約0.15ミリメートルである。実施形態によっては、胃内滞留システムの隣接するアーム間の好ましい最大の隙間は、約0.25ミリメートルである。
図10A~図10Dは、本開示の例による、第3の例示的な圧縮システム1000を示す。図10Aは、連結部材1003から延びる4本のアームを有し、初期位置で二重回転板上に配置された胃内滞留システム1002を示す。実施形態によっては、二重回転板は、外側回転板1004及び内側回転板1006を含むことがある。実施形態によっては、外側取付ブロック1008及び内側取付ブロック1010をそれぞれの回転板上に配置して、非圧縮形態の胃内滞留システム1002のアームと係合させることがある。上記の図5A~図5D及び図6A~図6Dで説明した実施形態のようなピックアンドプレースシステムによって、胃内滞留システムを図10Aに示す位置及び向きに直接配置することができ、二重回転板は、それぞれ器具512及び612に対応することがある。実施形態によっては、外側回転板1004は可撓性蝶番部分1012を含むことがあり、この可撓性蝶番部分1012は、外側回転板を蝶番に沿って半分に折り畳むことができる。図10Bは、最終位置にある二重回転板を示しており、外側回転板1004の時計回りの回転及び内側回転板1006の反時計回りの回転によって、胃内滞留システム1002のアームの上部の対1007及びアームの底部の対1009が、それぞれ互いに近くなっている。実施形態によっては、アームのこれらの対が互いに押し付けられ、場合によっては融着するのを防ぐために、停止部1014を含めることがある。実施形態によっては、この停止部は、個々のアームを互いに押し付けることによって、胃内滞留システム1002の表面の被膜がこすられるのを防ぐこともある。図10Cは、胃内滞留システムが二重回転板の上部に載った状態であり、蝶番1012が胃内滞留システム1002の連結部材1003と整列して示されている、圧縮システム1000の側面図を示す。二重回転板によって胃内滞留システム1002のアームがまとめられているので、圧縮システムは、蝶番1012に沿って折り畳んで図10Dに示す折り畳んだ構成にすることができる。この折り畳みは、上部のアーム1007と底部のアーム1009をまとめて、胃内滞留システム1002を完全に圧縮された形態にすることができる。一旦胃内滞留システム1002が圧縮された形態にされると、胃内滞留システムを、折り畳まれた二重回転ブロックから(例えば、ピストンによって)容器に押し出すことができる。図10A~図10Dの例は、4本のアームを有する胃内滞留システムを用いて示したが、本開示の範囲から逸脱することなく、3本以上のアームを有する胃内滞留システムのアームをまとめて胃内滞留システムを圧縮する類似のシステムを使用できることは、言うまでもない。
図11A~図11Dは、本開示の例による、第4の例示的な圧縮システム1100を示す。圧縮システム1102は、圧縮され容器に挿入されることになる胃内滞留システム(図示せず)のアームの位置及び数に対応した数の回転可能蝶番1102を含むことがある。図示した図では、6本のアームを備えた胃内滞留システムに対応した6個の回転可能蝶番1102が示されている。上記の図5A~図5D及び図6A~図6Dで説明した実施形態のようなピックアンドプレースシステムによって、胃内滞留システムを、アームが回転可能蝶番1102と整列した状態の位置及び向きに直接的に配置することができる。各回転可能蝶番1102の先端には、回転可能蝶番1102上の真空カップにおいて吸引力を生み出すための真空ライン接続部1104があってもよい。真空カップは、回転可能蝶番1102が回転したときに、胃内滞留システムのアームを回転可能蝶番にしっかりと固定して引っ張ることができる。図11Bは、回転可能蝶番1102が部分的に回転した位置にある様子を示しており、これは、上記の図7B及び図9Bに示したような部分的に圧縮された胃内滞留システムに対応することがある。回転可能蝶番は、押上器具1110によって押し上げられることがあり、この押上器具1110は、胃内滞留システムの各アームが同じ割合で近づけるように、6個全ての回転可能蝶番1102を同時に且つ均等に押し上げる。図11Cは、上記の図7C及び図9Cに示すような完全に圧縮された胃内滞留システムに対応する位置にある回転可能蝶番1102を示す。図11Cでは、押上器具1110が圧縮システム1100の基礎プラットフォームから押し上げられている様子がより明確に分かる。更に図示するように、ピストン1106が、圧縮された胃内滞留システムの最終位置の真上に位置することがある。実施形態によっては、ピストンは、手動で又はロボットアームにより制御できるレバー1008によって操作することができる。実施形態によっては、レバー1008を必要とすることなく、ピストン自体が上下するように制御されることがある。図11Dは、下げられた位置にあるピストン1006及びレバー1008を示す。ピストン1006が下げられると、胃内滞留システムは、台板1112の開口部を通って圧縮システムから押し出されることがある。実施形態によっては、ピストン1006を動かすと、真空カップの吸引を中止し、胃内滞留システムが圧縮システムから押し出される際に胃内滞留システムに損傷を与えないようにすることがある。実施形態によっては、台板1112は脚1114によって持ち上げられて、圧縮システム1100の構造の下を容器が通過し、胃内滞留システムを受け取るための空間を規定することができる。
図12A~図12Dは、胃内滞留システムの伸長部分1206を相互接続できる可撓性ランナー1204を使用して胃内滞留システム1202を圧縮するための例示的な圧縮システム1200を示す。実施形態によっては、胃内滞留システム1202の形成中に、図12Aに示すように、可撓性ランナーシステムが胃内滞留システム1202の隣接するアーム1206を相互接続することがある。実施形態によっては、可撓性ランナーシステム1204は、胃内滞留システムの形成と同時の射出成形プロセスによって形成することができる。図12Bは、アーム間で可撓性ランナー408を掴むのに使用できるアンカーシステム1208を示す。アンカーシステムに矢印1210の方向の上向きの力をかけることができ、これにより、引き続いて、ランナーシステム1204がアーム1206を引っ張ることができる。図12Cは、アンカーシステム1208によって上向きの力がかけられた結果として、胃内滞留システム1202が部分的に折り畳まれたすなわち圧縮された様子を示す。実施形態によっては、胃内滞留システム1202が図12Dに示すように完全に圧縮されるまで、上向きの力をかけ続けることができる。実施形態によっては、可撓性ランナー1204はアーム1206の内部に配置されることがある(従って、図面では見えない)。実施形態によっては、可撓性ランナーを取り外すことができる。以下の図13A~図13B及び図14に関して以下で更に詳細に考察するように、容器に挿入する前に、胃内滞留システム1202に保持具を追加して、構造体を圧縮された形態に維持することがある。実施形態によっては、アンカーシステム1208を上記のような二次圧縮システムと併用して、胃内滞留システム1202を部分的に折り畳むことができ、この折り畳みは、容器への胃内滞留システムの挿入と共に完了することができる。例えば、図12Cに示す部分的に圧縮された胃内滞留システム1202を、部分的に穴が閉じた状態の図9A~図9Dの機械式アパーチャに配置して、第1のピストンによる初期の押し込み機能を置き換えることができる。例えば、一旦図12Cの部分的に圧縮された胃内滞留システム1202が上記の機械式アパーチャ904に配置されると、アパーチャを閉じることで、胃内滞留システムの圧縮を完了することができる。
図13A及び図13Bは、胃内滞留システムを圧縮形態に維持するための保持バンド1304を示す。図13Aは、保持バンド1304を、圧縮形態の胃内滞留システム1302の一方の端部上に配置できることを示す。保持バンド1304は、胃内滞留システム1402の端部上をスライドさせて、胃内滞留システムのアーム1306の遠位端の付近に配置し、胃内滞留システムが早期に展開された場合に胃内滞留システムが予定外に早く広がるのを防ぐことができる。例によっては、保持バンドは、ゼラチン又はヒドロキシプロピルメチルセルロースなどの、当技術分野で周知の材料から作製されることがある。一実施形態では、保持バンド1304は、胃内環境では溶解するが口腔又は食道環境では溶解しない材料から作製され、これにより、胃に届く前にシステムが早く解放されるのを防止する。図13Bは、そのバンドがはめられた後の胃内滞留システム1302のカプセル容器を示す。実施形態によっては、バンドの厚みにより、カプセルの内面と胃内滞留システムとの間に間隔が規定されることがある。実施形態によっては、カプセルの内面と胃内滞留システムとの間の間隔は、保持バンド1304の厚さによって決まることがある。実施形態によっては、保持バンド1304の好ましい最小の厚さは、少なくとも約0.01ミリメートルであってもよい。実施形態によっては、保持バンド1304の好ましい最小の厚さは、少なくとも約0.05ミリメートルであってもよい。実施形態によっては、保持バンド1304の好ましい最小の厚さは、少なくとも約0.1ミリメートルであってもよい。実施形態によっては、保持バンド1304の好ましい最小の厚さは、少なくとも約0.2ミリメートルであってもよい。或いは、保持バンド1304が厚すぎると、容器内に著しく無駄な空間がもたらされることがある。実施形態によっては、保持バンド1304の好ましい最大の厚さは約0.1ミリメートルであってもよい。実施形態によっては、保持バンド1304の好ましい最大の厚さは約0.2ミリメートルであってもよい。実施形態によっては、保持バンド1304の好ましい最大の厚さは約0.5ミリメートルであってもよい。
図14は、胃内滞留システム1402を圧縮形態に維持するための保持キャップ1404を示す。上記の保持バンドの概念と同様に、保持キャップ1404を使用して胃内滞留システム1402を圧縮形態に維持することができる。図14は、保持キャップ1404の複数の図、すなわち、底面図1406、側面図1408、及び上面図1410を提供する。保持キャップ1406の底面図1406は、胃内滞留システム1402のアームの断面と同じ全体形状を有するようになっている小さなくぼみ1407を示す。くぼみ1407の形状と胃内滞留システム1402のアームの断面の形状を一致させることで、保持キャップは胃内滞留システムの圧縮形態にあるアームと係合して、アームを所定の位置に保持することができる。保持キャップ1404は、胃内滞留システム1402の小さな表面積と係合するようになっており、胃内滞留システムのアームと係合するくぼみ1407があるので、キャップはアームの遠位端を越えた位置にスライドする必要はない。従って、保持キャップ1404と胃内滞留システム1402の被膜との干渉を最小限に抑えながら、依然として、胃内滞留システムが早期に展開された場合に胃内滞留システムが予定外に早く広がるのを防止することができる。実施例によっては、保持キャップ1404を、ゼラチン又はヒドロキシプロピルメチルセルロースなどの、当技術分野で周知の材料で作製することができる。一実施形態では、保持キャップ1404は、胃内環境では溶解するが口腔又は食道環境では溶解しない材料で作製され、これにより、胃に届く前にシステムが早く解放されるのを防止する。上記の図13Bの説明のように、保持キャップ1404によって固定された胃内滞留システム1402を、容器カプセルに挿入することができる。実施形態によっては、保持バンドの外側の縁1409の厚みにより、カプセルの内面と胃内滞留システムとの間に間隔が規定されることがある。実施形態によっては、カプセルの内面と胃内滞留システムとの間の間隔は、保持キャップ縁部1409の厚さによって決まることがある。実施形態によっては、保持キャップ縁部1409の好ましい最小の厚さは約0.01ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最小の厚さは約0.05ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最小の厚さは約0.1ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最小の厚さは約0.2ミリメートルであってもよい。実施形態によっては、保持キャップ1409の好ましい最小の厚さは約0.5ミリメートルであってもよい。或いは、保持キャップ縁部1409が厚すぎると、容器内に著しく無駄な空間がもたらされることがある。実施形態によっては、保持キャップ縁部1409の好ましい最大の厚さは0.1ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最大の厚さは0.2ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最大の厚さは0.5ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最大の厚さは0.2ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最大の厚さは1ミリメートルであってもよい。実施形態によっては、保持キャップ縁部1409の好ましい最大の厚さは1.25ミリメートルであってもよい。
図15A~図19Dは、胃内滞留システムの送達の更なる機械的安定性及び安全性を追加するために、本開示全体を通じて説明する胃内滞留システムを機械的に拘束する技法を示す。
図15A~図15Dは、胃内滞留システムの最終的な容器よりも小さなカプセルのキャップ1504(本明細書では、半カプセルとも呼ばれる)を使用して胃内滞留システム1502を機械的に固定するための技法を示す。図15Aは、胃内滞留システムの伸長部分をキャップで実際に固定する前の、胃内滞留システムの伸長部分をキャップ1504が固定できる様子を示しており、図15Bは、胃内滞留システムの伸長部分の端部がキャップ1504で固定された様子を示す。図15Cは、キャップ1504を備えた胃内滞留システム1502を、キャップ1504よりも大きな寸法の容器1506に挿入できる様子を示す。図15Dは、カプセル本体1506への挿入後にキャップ1504がわずかに突き出ている様子を示す。実施形態によっては、本開示の範囲から逸脱することなく、胃内滞留システム1502の長さは、カプセル本体1506の開口部を越えてキャップ1504が突き出ないような長さであってもよい。更に、実施形態によっては、本開示の範囲から逸脱することなく、キャップ1504によって固定される胃内滞留システム1502の端部は、胃内滞留システムの固定されていない側の端部をカプセル本体の開口部の方に向けて、カプセル本体1506に挿入することでもよい。最後に、図15Dは、カプセル本体1506の寸法に対応したキャップ1508を使用して、胃内滞留システム1502を包含する閉じた容器を形成できることを示す。この構成では、キャップ1504は、カプセル本体1506及びキャップ1508で形成されるより大きな容器の内部で、胃内滞留システム1502の機械的安全性を提供し続けることができる。実施形態によっては、キャップの厚みにより、カプセルの内面と胃内滞留システムとの間に間隔が規定されることがある。実施形態によっては、カプセルの内面と胃内滞留システムとの間の間隔は、キャップ1504の厚さによって決まることがある。実施形態によっては、キャップ1504の好ましい最小の厚さは、約0.01ミリメートルであってもよい。実施形態によっては、キャップ1504の好ましい最小の厚さは、約0.05ミリメートルであってもよい。実施形態によっては、キャップ1504の好ましい最小の厚さは、約0.1ミリメートルであってもよい。実施形態によっては、キャップ1504の好ましい最小の厚さは、約0.2ミリメートルであってもよい。或いは、キャップ1504が厚すぎると、容器内に著しく無駄な空間が生じることがある。実施形態によっては、キャップ1504の好ましい最大の厚さは0.1ミリメートルであってもよい。実施形態によっては、キャップ1504の好ましい最大の厚さは0.2ミリメートルであってもよい。実施形態によっては、キャップ1504の好ましい最大の厚さは0.5ミリメートルであってもよい。
図16A~図16Dは、胃内滞留形状に適合する小さな直径のカプセル鞘1604を使用して胃内滞留システム1602を機械的に固定するための技法を示す。図16Aは、胃内滞留システムの伸長部分をキャップで実際に固定する前の、胃内滞留システムの伸長部分を鞘1604が固定できる様子を示しており、図16Bは、胃内滞留システムの端部が鞘1604で固定された様子を示す。図16Cは、カプセル鞘1604を備えた胃内滞留システム1602を、鞘1604よりも大きな寸法のカプセル本体1606に挿入できる様子を示す。実施形態によっては、鞘1604によって固定された胃内滞留システム1602の端部を、図示するようにカプセル本体1606の開口部に向けることができる。実施形態によっては、本開示の範囲から逸脱することなく、鞘1604によって固定された胃内滞留システム1602の端部を、カプセル本体1606の開口部に最初に挿入することでもよい。図16Dは、カプセル本体1606への挿入後に胃内滞留システム1602がわずかに突き出ている様子を示す。実施形態によっては、本開示の範囲から逸脱することなく、胃内滞留システム1602は、カプセル本体1606の開口部を越えて胃内滞留システムが突き出ないような長さであってもよい。最後に、図16Dは、カプセル本体1606の寸法に対応したキャップ1608を使用して、胃内滞留システム1602を包含する閉じた容器を形成できることを示す。この構成では、鞘1604は、カプセル本体1606及びキャップ1608で形成されるより大きな容器の内部で、胃内滞留システム1602の機械的安全性を提供し続けることができる。実施形態によっては、鞘1604の厚みにより、カプセルの内面と胃内滞留システムとの間に間隔が規定されることがある。実施形態によっては、カプセルの内面と胃内滞留システムとの間の間隔は、鞘1604の厚さによって決まることがある。実施形態によっては、鞘1604の好ましい最小の厚さは、約0.01ミリメートルであってもよい。実施形態によっては、鞘1604の好ましい最小の厚さは、約0.05ミリメートルであってもよい。実施形態によっては、鞘1604の好ましい最小の厚さは、約0.1ミリメートルであってもよい。実施形態によっては、鞘1604の好ましい最小の厚さは、約0.2ミリメートルであってもよい。或いは、鞘1604が厚すぎると、容器内に著しく無駄な空間がもたらされることがある。実施形態によっては、鞘1604の好ましい最大の厚さは0.1ミリメートルであってもよい。実施形態によっては、鞘1604の好ましい最大の厚さは0.2ミリメートルであってもよい。実施形態によっては、鞘1604の好ましい最大の厚さは0.5ミリメートルであってもよい。
図13A~図16Dに関して上に述べたように、カプセル封入に加えて、本開示の例による鞘、バンド、又はキャップを使用して、利用者の胃に届く前に利用者の食道で胃内滞留システムが予定外に早く解放されるのを防止するのを助けることができる。利用者の食道での胃内滞留システムの早期の解放を防止する態様の1つには、折り畳まれた胃内滞留システムが折り畳まれていない構成に戻ろうとして外側に押すことにより加えられる力に対抗する、鞘、バンド、又はキャップによりもたらされる機械的支持がある。利用者の食道での胃内滞留システムの早期の解放を防止する別の態様には、鞘、バンド、又はリングは、一旦胃内環境に到達すると、なおも胃内滞留システムが展開するようにしなくてはならず、従って、胃内滞留システムが折り畳まれたすなわち圧縮された形態で胃から出る前に溶解しなくてはならない、ということがある。上述のように、(例えば、上記の図16A~図16Dに関して説明したような)鞘、(例えば、上記の図13A~図13Bに関して説明したような)バンド、又は(例えば、上記の図14及び図15A~図15Dに関して説明したような)キャップの厚さは、所望の機械的特性及び/又は溶解特性を達成するために変えることができる。キャップ、バンド、又は鞘の他の物理的寸法、例えば、キャップ、バンド、又は鞘の長さなども、所望の機械的特性及び/又は溶解特性を達成するために変えることができる。更に、異なる材料から構成された鞘、バンド、又はキャップを使用して、所望の機械的特性及び溶解特性を達成することができる。
胃内滞留システムの早期の解放を防ぐのを助ける態様の1つは、胃内滞留システムが鞘、バンド、又はキャップに対してかける機械的な力に耐えることである。胃内滞留システムを折り畳まれた配置に維持できるようにするためには、鞘、バンド、又はキャップは、胃内滞留システムを折り畳まれた配置にするのに使われた曲げ力以上(例えば、約50%、又は約100%上回る)の、折り畳まれた胃内滞留システムからの周方向応力(例えば、フープ応力又はシリンダー応力)に耐えることができなくてはならない。折り畳まれた胃内滞留システムによってかけられる周方向応力の量に耐えられるようにすることで、鞘、バンド、又はキャップは、利用者の食道における胃内滞留システムの早期の解放を防ぐのを助けることができる。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約0.1ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約0.15ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約0.2ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約0.3ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約0.4ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約0.6ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約1.5ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約2.25ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約3ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約2ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約3ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約4ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約6.5ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約10ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約20ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約40ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、最大で約100ニュートンの折り畳まれた胃内滞留システムからの周方向応力に耐えられることが好ましい。
鞘、バンド、又はキャップは、胃内環境に到達する前に利用者の食道での胃内滞留システムの解放を防ぐのを助けることができるが、一方で鞘、キャップ、バンド、又は保持鞘は、胃内滞留システムが胃内環境に到達して展開される総計時間に影響を及ぼすこともある。同時に、鞘、バンド、又はキャップは、胃内滞留システムが胃内環境に到達すると胃内滞留システムを解放できるようになっていなければならず、また、胃内滞留システムが胃から出ていってしまうほどの長い間、胃内滞留システムを圧縮形態に保持しないほうがよい。従って、鞘、バンド、又はキャップは、利用者の食道での胃内滞留システムの解放を防ぎながら、胃内滞留システムが一旦胃内環境に到達すると解放されて展開するように設計すればよい。実施形態によっては、キャップ、バンド、鞘、又は保持キャップは、胃内環境で特定の時間内に胃内滞留システムを展開できるように設計されることがある。胃内滞留システムの展開時間は、外側のカプセルとキャップ、バンド、鞘、又は保持キャップとを組み合わせた合算展開時間の観点から設計することができる。実施形態によっては、キャップ、バンド、鞘、又は保持キャップが(例えば、バンド、キャップ、又は鞘が酸性の胃内環境によって溶解された結果として)胃内滞留システムを展開できるように設計される時間は、(例えば、外側のカプセルが胃内環境で完全に溶解された後の)外側のカプセルが存在しない状態で、キャップ、バンド、鞘、又は保持キャップによってのみ胃内滞留システムが保持されているときに、胃内滞留システムが胃内環境で折り畳まれた配置から展開するのにかかる時間とすることがある。
実施形態によっては、鞘、バンド、又はキャップは、胃内滞留システムが胃内環境に到達する前は展開されないが、一旦胃内環境に到達すると比較的素早く解放されるように、設計されることがある。実施形態によっては、鞘、バンド、又はキャップは、長くても約5秒以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約10秒以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約30秒以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約1分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約2分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約4分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約8分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、長くても約12分以内に胃内環境で胃内滞留システムを展開できることが好ましい。
実施形態によっては、胃内滞留システムが胃内環境に入る前に解放されないことを更に確実にするために、鞘、バンド、又はキャップは、胃内環境に到達した直後に解放されないように設計されることがある。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約5秒後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約10秒後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約30秒後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約1分後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約2分後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約4分後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、鞘、バンド、又はキャップは、少なくとも約8分後に胃内環境で胃内滞留システムを展開できることが好ましい。
実施形態によっては、胃内環境での胃内滞留システムの展開に関して前段落で説明した時間は、鞘、バンド、又はキャップ単独での胃内滞留システムの保持に基づいていることがある。そのような実施形態では、鞘、バンド、又はキャップによって保持される胃内滞留システムを封入している外側のカプセルにより、胃内環境での胃内滞留システムの総展開時間に更なる時間が加算される。実施形態によっては、展開時間は、胃内環境で外側のカプセル(例えば、本明細書で説明したような容器)と鞘、バンド、又はキャップの両方が溶ける時間を考慮して設計されることがある。
実施形態によっては、鞘、バンド、又はキャップは、胃内滞留システムが胃内環境に到達する前は展開されないが、一旦胃内環境に到達すると比較的に素早く解放されるように、設計されることがある。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約5秒以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約10秒以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約30秒以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約1分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約2分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約4分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約8分以内に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、長くても約12分以内に胃内環境で胃内滞留システムを展開できることが好ましい。
実施形態によっては、胃内滞留システムが胃内環境に入る前に解放されないことを更に確実にするために、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、胃内環境に到達した直後に解放されないように設計されることがある。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約5秒後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約10秒後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約30秒後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約1分後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約2分後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約4分後に胃内環境で胃内滞留システムを展開できることが好ましい。実施形態によっては、外側のカプセルと鞘、バンド、又はキャップとの組み合わせは、少なくとも約8分後に胃内環境で胃内滞留システムを展開できることが好ましい。
図17A~図17Dは、胃内滞留システムをカプセル本体に挿入する前に、カプセル本体1702に充填された非水性ゲル1704を使用して、胃内滞留システム1708を機械的に固定するための技法を示す。図17Aは、胃内滞留システムをカプセル本体に挿入する前に、非水性ゲル1704をカプセル本体1702に適量ずつ供給するディスペンサー1706を示す。非水性ゲル1704は、カプセル材料1702を妨害又は溶解させないように選択されることがある。更に、非水性ゲル1704は、胃内環境では制御された速度で溶解して、適時に胃内滞留システムを非圧縮形態に展開できるように選択することができる。図17Bは、胃内滞留システム1708が圧縮形態でカプセル本体1702に挿入される様子を示す。図17Cは、カプセル本体1702に挿入した後の胃内滞留システム1708を示しており、胃内滞留システムの伸長部分を、カプセル本体の底部にある非水性ゲル1704の小さなたまりに挿入することができる。その後、非水性ゲル1704は凝固し、胃内滞留システム1708の伸長部分を一緒に固定して胃内滞留システムを圧縮形態に機械的に拘束するための非永続的な接着剤として作用することができる。図17Dは、キャップ1710がカプセル本体1702に取り付けられて、胃内滞留システムの完成した容器を形成している様子を示す。
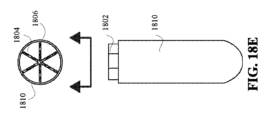
図18A~図18Eは、胃内滞留システムをカプセル本体1810に挿入する前に、胃内滞留システムの伸長部分1804に塗布された非水性ゲル1806を使用して、胃内滞留システム1802を機械的に固定するための技法を示す。図18Aは、本開示の例による胃内滞留システムの2つの図を示す。胃内滞留システム1802の第1の図は圧縮された胃内滞留システムの側面図を示しており、伸長部分は互いに近接してまとめられている。胃内滞留システム1802の第2の図は、第1の図に示した向きを基準にして上から見たときの、伸長部分1804の遠位端を示す。図示するように、圧縮形態にある伸長部分1804の間には隙間があってもよい。実施形態によっては、この隙間の好ましい最小の間隔は、約0.01ミリメートルであってもよい。実施形態によっては、隙間の好ましい最小の間隔は、約0.05ミリメートルであってもよい。実施形態によっては、隙間の好ましい最小の間隔は、約0.1ミリメートルであってもよい。実施形態によっては、隙間の好ましい最大の間隔は、約0.5ミリメートルであってもよい。実施形態によっては、隙間の好ましい最大の間隔は、約0.25ミリメートルであってもよい。図18Bは、非水性ゲルが胃内滞留システム1802の伸長部分1804の間の空間に浸透できるように、ディスペンサー1808によって非水性ゲル1806を伸長部分1804の遠位端上に適量ずつ供給する様子を示す。図18Cは、適用後に伸長部分1804の間の隙間に浸透した非水性ゲル1806を示す。図18Dは、胃内滞留システムがカプセル本体1810に挿入される様子を示す。図18Eは、カプセル本体1810に挿入された胃内滞留システム1802の側面図及び上面図を示す。上面図から分かるように、伸長部分1804の遠位端の間の隙間は、胃内滞留システムの伸長部分を機械的に固定するための非水性ゲル1806で満たすことができる。その後、カプセル本体1810にキャップを取り付けて、完成した容器(図示せず)を形成することができる。
図19A~図19Dは、胃内滞留システムをカプセル本体1910に挿入した後に、胃内滞留システムの伸長部分1904に塗布された非水性ゲル1908を使用して、胃内滞留システム1902を機械的に固定するための技法を示す。この技法は、図18A~図18Eで示したプロセスとほぼ同様であるが、図19A~図19Bに示すように、胃内滞留システム1902をカプセル本体1904に挿入する工程が、非水性ゲルを塗布する前に行われるという点が異なる。図19Cは、カプセル本体1904に挿入した後に胃内滞留システム1902の伸長部分の遠位端に非水性ゲルを塗布する様子を示す。図19Dは、最終結果が図18Eに示したのとほぼ同じ最終結果になる様子を示しており、カプセル本体1904の内部に包含された胃内滞留システムの伸長部分の間の隙間を非水性ゲル1908が占めている。その後、カプセル本体1904にキャップを取り付けて、完成した容器(図示せず)を形成することができる。
水性環境における星形の胃内滞留システムの展開時間に対するキャップ、バンド、又は鞘の効果を決定するための実験による試験では、本開示の例によるカプセル封入済の星形の胃内滞留システムの展開時間を、pH3.0のリン酸緩衝生理食塩水溶液中で測定した。この緩衝液は、水に1.36グラムの無水リン酸2水素カリウム、及び8.41グラムの塩化ナトリウムを溶かし、塩酸でpH3.0に調節し、1リットルに調製した。この実験では3つの構成が試験され、各構成では3つの試料が試験された。これら3つの構成のそれぞれでは、胃内滞留システムをcapsugel社のVCaps Plus HPMC 00EL外側カプセルの中に封入した。3つの構成は、以下の通りである。1)Capsugel社のVCaps Plus 0ELカプセルからのサイズ0ELのキャップを、00ELカプセルの本体に挿入する前に星形の胃内滞留システムの折り畳まれた脚にかぶせて配置し、星形の胃内滞留システムのキャップをかぶせた端部を00ELカプセルの開口部に最初に挿入し、その後、00ELキャップで蓋をして完成した容器を形成した。2)Capsugel社のVCaps Plus 0ELカプセルからのキャップの底部の1/3の部分を切断することで形成した鞘を00ELカプセルの本体に挿入する前に星形の胃内滞留システムの折り畳まれた脚の上に配置し、その後、00ELのキャップで蓋をして完成した容器を形成した。3)キャップをかぶせられていない折り畳まれた星形の胃内滞留システムを00ELカプセルの本体に挿入し、その後、00ELのキャップで蓋をして完成した容器を形成した。これら3つの構成のうちの1つでカプセル封入された星形の胃内滞留システムを包含するサイズ00ELのカプセルを、35mLのpH3.0の溶液を含む450mLのガラス広口瓶に入れた。ガラス広口瓶は、直径80ミリメートル、高さ94ミリメートルであり、PTFEで内側を覆われた蓋を持っている。剤形を瓶の中に入れ、瓶を密封し、逆さまにし、毎分30サイクルに設定された実験用の揺動装置に直ちに配置した。カプセルがpH3溶液に入れられたときに計時を開始した。瓶を目視で観察し、剤形が展開したときにタイマーを停めた。以下の3つの実施例は、上述の3つの構成それぞれについての3つの試行の結果を説明する。
実施例1:キャップ保持要素を備えたカプセル封入済胃内滞留システム
第1の構成での00EL外側カプセルの中身は、(例えば、上記の図15A~図15Dでキャップ1504によって示されるように)星形の胃内滞留システムの折り畳まれて収められている脚の端部に(例えば、上記の図15A~図15Dのキャップ1504などの)Capsugel社のVCaps Plus 0ELキャップからのキャップをかぶせた、星形の胃内滞留システムであった。第1の構成では、キャップをかぶせた星形を、まずキャップをかぶせた端部の方から外側の00ELカプセルの中に挿入した後で、00ELのキャップを使用して00ELカプセルを閉じ、完成した容器を形成した。以下の表3は、3回の試行での展開時間を列挙しており、計時を、00ELカプセルがpH3溶液の中に入れられた時に開始し、星形の胃内滞留システムの脚が展開された時に終了した。
これらの3回の試行について、00ELカプセルと追加の0ELキャップを組み合わせた星形の胃内滞留システムの展開にかかる平均時間は、7.4分であった。
実施例2:鞘保持要素を備えたカプセル封入済胃内滞留システム
第2の構成での00EL外側カプセルの中身は、(例えば、上記の図13Aの保持バンド1304及び図16A~図16Dの鞘1604によって示されるように)胃内滞留システムの折り畳まれて収められている脚を取り囲み、星形の胃内滞留システムの脚の遠位端付近に配置された鞘を備えた星形の胃内滞留システムであった。第2の構成では、鞘によって囲まれた星形の遠位端を00EL外側カプセルに挿入した後で、00ELカプセルキャップを取り付けて完成した容器を形成した。第2の構成では、第1の構成でキャップとして使用されたのと同じ種類のサイズ0ELキャップ(高さ約11ミリメートル)の底部の1/4~1/3の部分(高さ約3ミリメートル)を切断することで鞘を作製した。以下の表4は、3回の試行での展開時間を列挙しており、計時を、00ELカプセルがpH3溶液の中に入れられた時に開始し、星形の胃内滞留システムの脚が展開された時に終了した。
第2の構成の場合、00ELカプセルと0ELキャップの底部1/3の部分から形成された更なる0EL鞘の組み合わせによる星形の胃内滞留システムの展開にかかる平均時間は、5.9分であった。
実施例3:更なる保持要素のないカプセル封入済胃内滞留システム
第3の構成での00EL外側カプセルの中身は、(例えば、図8Bに示すような)00EL外側カプセルに直接挿入された、キャップの無い/鞘の無い胃内滞留システムであった。以下の表5は、第3の構成での3回の実験結果を示す。
表5の例では、鞘又はキャップの無い第3の構成では、胃内滞留システムの展開にかかる平均時間は2.6分であった。2.6分という平均展開時間は、キャップ及び鞘をそれぞれ利用した第1及び第2の構成の両方の平均時間よりも短い。更に、鞘を用いた第2の構成では、胃内滞留システムの伸長部分に完全なキャップをかぶせた第1の構成と比べて、胃内滞留システムの展開にかかる平均時間が5.6分とより短かった。
本発明は、以下の非限定的な例によって更に説明される。
本開示の幾つかの例は、1つ以上のセグメントを連結する連結部材を含んだ圧縮可能な胃内滞留システムをカプセル封入する方法に関し、この方法は、非圧縮形態にある圧縮可能な胃内滞留システムを受け取る工程と、圧縮可能な胃内滞留システムを圧縮位置に向ける工程と、圧縮可能な胃内滞留システムを圧縮形態に圧縮する工程と、圧縮形態にある圧縮可能な胃内滞留システムを容器の開口部に挿入する工程と、を含む。上に開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、1つ以上のセグメントを有する圧縮可能な胃内滞留システムは、複数の細長部材を含み、各細長部材は連結部材に取り付けられた近位端を有し、また各細長部材は連結部材に取り付けられず、近位端よりも連結部材からより遠い放射状の距離に位置する遠位端を有する。
上に開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮可能な胃内滞留システムを圧縮形態に圧縮する工程は、各細長部材の遠位端間の距離を短くする工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮可能な胃内滞留システムを圧縮形態に圧縮する工程は、各細長部材の遠位端を一つにまとめる工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮形態な胃内滞留システムは、圧縮可能な胃内滞留システムに外部の力が加えられていない場合に圧縮可能な胃内滞留システムを非圧縮形態にする弾力性を有する。
上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮可能な胃内滞留システムを向ける工程は、真空カップで連結部材の部分を固定する工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、連結部材の少なくとも一部の形状は、真空カップと嵌合するようになっている。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮可能な胃内滞留システムを向ける工程は、圧縮可能な胃内滞留システムを空気圧駆動式の締め付け具で固定する工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、各細長部材の遠位端間の距離を短くする工程は、連結部材に力をかけ、連結部材及び複数の細長部材がアパーチャを通過するようにする工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、アパーチャは容器の開口部の半径よりも小さな半径を有する。
上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、アパーチャは先細の囲いの端部に位置し、この先細の囲いによってかけられる力により、圧縮可能な胃内滞留システムの伸長部材を圧縮形態に圧縮する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮形態にある圧縮可能な胃内滞留システムを容器に挿入する工程は、容器をアパーチャと位置合わせし、圧縮可能な胃内滞留システムがアパーチャから押し出されたときに胃内滞留システムを受け取る工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、連結部材に力をかける工程により、圧縮可能な胃内滞留システムを部分的に容器に挿入するようにし、またこの方法は更に、圧縮可能な胃内滞留システムの全体がアパーチャを通過するまで、圧縮可能な胃内滞留システムの細長部材の遠位端に第2の力をかける工程を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、第1の物体によって力がかけられ、第1の物体よりも大きな第2の物体によって第2の力がかけられる。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、各細長部材の遠位端間の距離を短くする工程は、複数の細長部材のうちの第1群に属する細長部材の遠位端間の距離を短くする工程と、複数の細長部材のうちの第2群に属する細長部材の遠位端間の距離を短くする工程と、その後、第1群に属する細長部材の遠位端と第2群に属する細長部材の遠位端との距離を短くする工程と、を含む。
上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、アパーチャを通過した後で、圧縮可能な胃内滞留システムの一部が容器の開口部の外に延びる。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、この方法は、圧縮形態な胃内滞留システムが圧縮形態から非圧縮形態に広がるのに抗うようになっている保持具を圧縮可能な胃内滞留システムに取り付ける工程を更に含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持具は、圧縮可能な胃内滞留システムの各細長部材の遠位端と結合する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、この方法は、容器にキャップを施して、圧縮可能な胃内滞留システムを包含する密封された収容体を生成する工程を更に含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持具の外半径は、保持具と密封構造との間に隙間が形成されるように、密封構造の内半径よりも小さくなっている。
上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持具の外半径と密封構造の内半径との間の隙間は、約0.01ミリメートル、約0.05ミリメートル、約0.075ミリメートル、又は約0.1ミリメートルの最小寸法を有する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持具の外半径と密封構造の内半径との間の隙間は、約0.15ミリメートル、約0.2ミリメートル、又は約0.25ミリメートルの最大寸法を有する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持具は、圧縮形態にある圧縮可能な胃内滞留システムの細長部材間の間隔を維持するようになっている。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮形態にある圧縮可能な胃内滞留システムの細長部材間の間隔は、約0.01ミリメートル、0.05ミリメートル、約0.75ミリメートル、又は約0.1ミリメートルの最小寸法を有する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮形態にある圧縮可能な胃内滞留システムの細長部材間の間隔は、約0.15ミリメートル、約0.125ミリメートル、約0.1ミリメートル、又は約0.05ミリメートルの最大寸法を有する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、連結部材はエラストマーである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、容器は半カプセルである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、密封構造はカプセルである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮可能な胃内滞留システムを圧縮形態に維持する力は、少なくとも0.2ニュートンである。
本開示の幾つかの例は、1つ以上のセグメントを連結する連結部材を含む圧縮可能な胃内滞留システムをカプセル封入するシステムに関し、このシステムは、圧縮システム、及び圧縮された胃内滞留システムをカプセル封入するようになっているカプセル封入装置を含み、圧縮システムは、カプセル封入装置に機械的に連結され、複数の圧縮可能な胃内滞留システムを繰り返し圧縮してカプセル封入するようになっている。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮システムは、複数の胃内滞留システムをカプセル封入装置に向けて運ぶようになっている振動式すり鉢状送り装置を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、振動式すり鉢状送り装置は、胃内滞留システムを、カプセル封入装置によって受け取られるようになっている垂直な向きに向ける。
上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮システムは把持アームを含み、この把持アームは、圧縮可能な胃内滞留システムと係合し、胃内滞留システムを圧縮及びカプセル封入のための位置に向けるようになっている。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮システムは把持アームを含み、この把持アームは、圧縮可能な胃内滞留システムと係合し、胃内滞留システムを圧縮及びカプセル封入のための位置に向けるようになっている。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、把持アームは、第1の遠位端に真空カップを有するロボットアームを含み、この真空カップは、圧縮可能な胃内滞留システムの一部を把持するようになっている。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、把持アームは、胃内滞留システムの可撓性開口部の内部で拡大することで把持するようになっている拡大可能ヘッドを含む。
上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮システムは複数の回転蝶番を含み、各蝶番は胃内滞留システムの細長部材と係合する真空カップを含み、またこの圧縮システムは、これらの蝶番を同時に回転させ、それによって各細長部材を胃内滞留システムの圧縮形態に折り畳む、折り畳み機構を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、細長部材と係合する各真空カップは、蝶番が回転している間、それぞれの細長部材を圧縮システムに固定する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、カプセル封入装置は、圧縮形態にある圧縮可能な胃内滞留システムを容器の開口部に押し込むようになっているピストンを含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、容器は半カプセルである。
本開示の幾つかの例は、圧縮形態と非圧縮形態を持ち1つ以上のセグメントを連結する連結部材を含む圧縮可能な胃内滞留システムに関し、この圧縮可能な胃内滞留システムは、圧縮可能な胃内滞留システムに外部の力がかけられていないときに、圧縮可能な胃内滞留システムを非圧縮形態にする弾力性を有する。圧縮可能な胃内滞留システムは、第1の部分で把持されるようになっている。圧縮可能な胃内滞留システムは、圧縮形態に折り畳まれるようになっている。圧縮されたデバイスの圧縮形態は、容器の開口部に挿入されるようになっている。圧縮可能な胃内滞留システムは、圧縮可能な胃内滞留システムの遠位端に結合された保持具によって圧縮形態に更に固定される。
本開示の幾つかの例は、1つ以上のセグメントを連結する連結部材を含む複数の圧縮可能な胃内滞留システムをカプセル封入する方法に関し、この方法は、圧縮形態にある複数の胃内滞留システムを包含するカートリッジを受け取る工程と、容器内の複数の胃内滞留システムのうちの1つに継続的に力をかけて、圧縮形態にある複数の圧縮可能な胃内滞留システムをそれぞれの容器の開口部に順次挿入する工程と、を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、複数の胃内滞留システムの容器への順次挿入における連続的な挿入の合間の時間は15秒未満である。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、複数の胃内滞留システムの容器への順次挿入における連続的な挿入の合間の時間は5秒未満である。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、複数の胃内滞留システムの容器への順次挿入における連続的な挿入の合間の時間は0.5秒未満である。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、複数の胃内滞留システムの容器への順次挿入における連続的な挿入の合間の時間は0.1秒である。
本開示の幾つかの例は、圧縮形態と非圧縮形態を持つ圧縮可能な胃内滞留システムをカプセル封入するシステムに関し、このシステムは、圧縮形態にある圧縮可能な胃内滞留システムと、圧縮された胃内滞留システムからの外向きの機械的な力に抗うようになっている保持要素と、内部に圧縮された胃内滞留システム及び保持要素を包含する密封された収容体を含む容器と、を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、少なくとも約0.1ニュートン、少なくとも約0.15ニュートン、少なくとも約0.2ニュートン、少なくとも約0.3ニュートン、少なくとも約0.4ニュートン、少なくとも約0.6ニュートン、少なくとも約1.5ニュートン、少なくとも約2.25ニュートン、又は少なくとも約3ニュートンの周方向応力に耐えることができる。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、最大で約2ニュートン、最大で約3ニュートン、最大で約4ニュートン、最大で約6.5ニュートン、最大で約10ニュートン、最大で約20ニュートン、最大で約40ニュートン、最大で約60ニュートン、又は最大で約100ニュートンの周方向応力に耐えることができる。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、最大で約5秒以内、最大で約10秒以内、最大で約30秒以内、最大で約1分以内、最大で約2分以内、最大で約4分以内、最大で約8分以内、又は最大で約12分以内に、胃内環境で圧縮可能な滞留システムを圧縮形態から解放する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、少なくとも約5秒後、少なくとも約10秒後、少なくとも約30秒後、少なくとも約1分後、少なくとも約2分後、少なくとも約4分後、又は少なくとも約8分後に、胃内環境で圧縮可能な滞留システムを圧縮形態から解放する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素の厚さは、少なくとも約0.05ミリメートル、少なくとも約0.1ミリメートル、又は少なくとも約0.2ミリメートルである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素の厚さは、最大で約0.1ミリメートル、最大で約0.2ミリメートル、又は最大で約0.5ミリメートルである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮された胃内滞留システムは星形のものが折り畳まれた状態である。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素はキャップ、バンド、又は鞘である。
本開示の幾つかの例は、胃内滞留システムの予定外の早期の解放を防止する方法に関し、この方法は、圧縮形態にある胃内滞留システムを受け取る工程と、胃内滞留システムに保持要素を取り付ける工程と、を含み、この保持要素は、圧縮された胃内滞留システムからの外向きの機械的な力に抗うようになっており、またこの方法は、容器の密封収容体の内部に保持要素によって固定された胃内滞留システムを封入する工程と、を含む。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、少なくとも約0.1ニュートン、少なくとも約0.15ニュートン、少なくとも約0.2ニュートン、少なくとも約0.3ニュートン、少なくとも約0.4ニュートン、少なくとも約0.6ニュートン、少なくとも約1.5ニュートン、少なくとも約2.25ニュートン、又は少なくとも約3ニュートンの周方向応力に耐えることができる。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、最大で約2ニュートン、最大で約3ニュートン、最大で約4ニュートン、最大で約6.5ニュートン、最大で約10ニュートン、最大で約20ニュートン、最大で約40ニュートン、最大で約60ニュートン、又は最大で約100ニュートンの周方向応力に耐えることができる。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、長くても約5秒以内、長くても約10秒以内、長くても約30秒以内、長くても約1分以内、長くても約2分以内、長くても約4分以内、長くても約8分以内、又は長くても約12分以内に、胃内環境で圧縮可能な滞留システムを圧縮形態から解放する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素は、少なくとも約5秒後、少なくとも約10秒後、少なくとも約30秒後、少なくとも約1分後、少なくとも約2分後、少なくとも約4分後、又は少なくとも約8分後に、胃内環境で圧縮可能な滞留システムを圧縮形態から解放する。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素の厚さは、少なくとも約0.05ミリメートル、少なくとも約0.1ミリメートル、又は少なくとも約0.2ミリメートルである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素の厚さは、最大で約0.1ミリメートル、最大で約0.2ミリメートル、又は最大で約0.5ミリメートルである。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、圧縮された胃内滞留システムは星形のものが折り畳まれた状態である。上記で開示した例のうちの1つ以上に加えてあるいはその代わりに、例によっては、保持要素はキャップ、バンド、又は鞘である。
特定の引用によって本明細書で参照する全ての刊行物、特許、特許出願、及び公開された特許出願の開示内容は、その全体が参照により本明細書に組み込まれる。URL(Uniform Resource Locator)の先頭において「World-Wide-Web」を使用したウェブサイトの参照は、「World-Wide-Web」を「www」で置き換えることによってアクセスすることができる。
前述の発明は、明確に理解するために、図示又は例示として幾分か詳細に説明したが、特定の変更及び修正が行われる可能性があることは、当業者には明らかである。従って、明細書の記載及び実施例は、本発明の範囲を制限するものと解釈されるべきではない。