JP6903635B2 - 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 - Google Patents
抗増殖活性を有するピペリジノベンゾジアゼピン化合物 Download PDFInfo
- Publication number
- JP6903635B2 JP6903635B2 JP2018509597A JP2018509597A JP6903635B2 JP 6903635 B2 JP6903635 B2 JP 6903635B2 JP 2018509597 A JP2018509597 A JP 2018509597A JP 2018509597 A JP2018509597 A JP 2018509597A JP 6903635 B2 JP6903635 B2 JP 6903635B2
- Authority
- JP
- Japan
- Prior art keywords
- methyl
- pyrrole
- oxy
- cancer
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC*(*)C(NC)=N Chemical compound CC*(*)C(NC)=N 0.000 description 16
- DWKUKQRKVCMOLP-UHFFFAOYSA-N C1CC=NCC1 Chemical compound C1CC=NCC1 DWKUKQRKVCMOLP-UHFFFAOYSA-N 0.000 description 1
- WHLYHOCLTMUORC-UHFFFAOYSA-N CCOC(CCCCCOc(cc(c(C(N1C(CO)CCCC1)=O)c1)N)c1OC)=O Chemical compound CCOC(CCCCCOc(cc(c(C(N1C(CO)CCCC1)=O)c1)N)c1OC)=O WHLYHOCLTMUORC-UHFFFAOYSA-N 0.000 description 1
- RXDFNKIRDUHGDU-UHFFFAOYSA-N COC(CCCOc(cc(c(C(O)=O)c1)N=O)c1OC)=O Chemical compound COC(CCCOc(cc(c(C(O)=O)c1)N=O)c1OC)=O RXDFNKIRDUHGDU-UHFFFAOYSA-N 0.000 description 1
- NPUTUVDECBQMOJ-UHFFFAOYSA-N C[n]1c(C(OC)=O)cc(-c(cc2)ccc2N)c1 Chemical compound C[n]1c(C(OC)=O)cc(-c(cc2)ccc2N)c1 NPUTUVDECBQMOJ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/08—Tripeptides
- C07K5/0802—Tripeptides with the first amino acid being neutral
- C07K5/0804—Tripeptides with the first amino acid being neutral and aliphatic
- C07K5/0808—Tripeptides with the first amino acid being neutral and aliphatic the side chain containing 2 to 4 carbon atoms, e.g. Val, Ile, Leu
Description
式中、
点線は、C1とC2、C2とC3、及びC3とC4の1つ又は2つ以上の間に二重結合が存在していてもよいことを示し;
R1は、R7、=CH2、=CH−(CH2)m−CH3、=O、(CH2)m−OR7、(CH2)m−CO2R7、(CH2)m−NR7R8、O−(CH2)n−NR7R8、NH−C(O)−R7、O−(CH2)n−NH−C(O)−R7、O−(CH2)n−C(O)−NH−R7、(CH2)m−SO2R7、O−SO2R7、(CH2)m−C(O)R7、及び(CH2)m−C(O)NR7R8から選択され;
R2は、R9、=CH2、=CH−(CH2)r−CH3、=O、(CH2)r−OR9、(CH2)r−CO2R9、(CH2)r−NR9R10、O−(CH2)s−NR9R10、NH−C(O)−R9、O−(CH2)s−NH−C(O)−R9、O−(CH2)s−C(O)−NH−R9、(CH2)r−SO2R9、O−SO2R9、(CH2)r−COR9、及び(CH2)r−C(O)NR9R10から選択され;
R3は、H、C1−12アルキル、及びCH2Phから選択され;
R4は、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、C(=O)−NH−R24、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよい、フェニル及びC5−9ヘテロアリール基から選択され;ただし、置換されていてもよいC5−9ヘテロアリールは、インドリルではないことを条件とし;
R19は、H及び(CH2)t−NR20R21から選択され;
Y1は、N又はCHであり;
Y2は、N又はCHであり;Y1及びY2の少なくとも一方は、CHであり;
pは、0又は1であり;
j、m、r、及びtは独立して、0〜6の整数から選択され;
k、n、及びsは独立して、1〜6の整数から選択され;
X1は、O、S、NR13、CR13R14、CR13R14O、C(=O)、C(=O)NR13、NR13C(=O)、O−C(O)、及びC(O)−Oから選択され;
Lは、アミノ酸、2〜6個のアミノ酸を有するペプチド鎖、1つ又は2つ以上の炭素−炭素二重結合又は三重結合を含有し得る1〜12個の炭素原子を含有するアルキレン鎖、パラホルムアルデヒド鎖−(OCH2)1−12−、及びポリエチレングリコール鎖−(OCH2CH2)1−6−から選択され、これらの鎖は、O、S、及び/若しくはNH基、並びに/又はC3−9ヘテロアリーレン、並びに/又はフェニレンの1つ又は2つ以上により中断されていてもよく;
X2は、O、S、NR15、CR15R16、CR15R16O、C(=O)、C(=O)NR15、NR15C(=O)、O−C(O)、及びC(O)−Oから選択されるか、又は存在せず;
qは、0、1、2、3、4、5、及び6から選択され;
Aは:
各A1基について、Y3及びY4の1つは独立して、N−R17、S、及びOから選択され;Y3及びY4の他方は、CHであり;Y5は独立して、CH、N、S、及びCOHから選択され;
各A2基について、Y6及びY7の1つは独立して、N及びCHから選択され;Y6及びY7の他方は、CHであり;
R7及びR9は独立して、H、C1−12アルキル、C5−9ヘテロアリール、C6−15ヘテロアリールアルキル、フェニル、及びC7−12アラルキル基から選択され;ヘテロアリール、ヘテロアリールアルキル、フェニル、及びアラルキル基は、C1−6アルキル、OH、及びOC1−6アルキルから選択される最大3個の任意の置換基で置換されていてもよく;
R24は、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよい、フェニルであり;
R8、R10、R11、R12、R13、R14、R15、R16、R17、R20、及びR21は独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6は一緒になって二重結合を形成するか;
(ii)R5はHであり、かつR6はOHであるか;又は
(iii)R5はHであり、かつR6はOC1−6アルキルであるか
のいずれかであり;
ただし、pが0であり、かつAがA1である場合:
(a)少なくとも1つのA1基について、Y3及びY4の1つは、S及びOから選択されるか;若しくは
(b)少なくとも1つのA1基について、Y5は、Sであるか;又は
(c)R4は、ピロリル、イミダゾリル、置換されていてもよいピロリル、若しくは置換されていてもよいイミダゾリルではないこと
を条件とする。
式中、
点線は、C1とC2、C2とC3、及びC3とC4の1つ又は2つ以上の間に二重結合が存在していてもよいことを示し;
R1は、R7、=CH2、=CH−(CH2)m−CH3、=O、(CH2)m−OR7、(CH2)m−CO2R7、(CH2)m−NR7R8、O−(CH2)n−NR7R8、NH−C(O)−R7、O−(CH2)n−NH−C(O)−R7、O−(CH2)n−C(O)−NH−R7、(CH2)m−SO2R7、O−SO2R7、(CH2)m−C(O)R7、及び(CH2)m−C(O)NR7R8から選択され;
R2は、R9、=CH2、=CH−(CH2)r−CH3、=O、(CH2)r−OR9、(CH2)r−CO2R9、(CH2)r−NR9R10、O−(CH2)s−NR9R10、NH−C(O)−R9、O−(CH2)s−NH−C(O)−R9、O−(CH2)s−C(O)−NH−R9、(CH2)r−SO2R9、O−SO2R9、(CH2)r−COR9、及び(CH2)r−C(O)NR9R10から選択され;
R3は、H、C1−12アルキル、及びCH2Phから選択され;
R4は、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、C(=O)−NH−C6H4−(CH2)j−R18、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよい、フェニル及びC5−9ヘテロアリール基から選択され;ただし、置換されていてもよいC5−9ヘテロアリールは、インドリルではないことを条件とし;
R19は、H及び(CH2)t−NR20R21から選択され;
Y1は、N又はCHであり;
Y2は、N又はCHであり;Y1及びY2の少なくとも一方は、CHであり;
pは、0又は1であり;
j、m、r、及びtは独立して、0〜6の整数から選択され;
k、n、及びsは独立して、1〜6の整数から選択され;
X1は、O、S、NR13、CR13R14、CR13R14O、C(=O)、C(=O)NR13、NR13C(=O)、O−C(O)、及びC(O)−Oから選択され;
Lは、アミノ酸、2〜6個のアミノ酸を有するペプチド鎖、1つ又は2つ以上の炭素−炭素二重結合又は三重結合を含有し得る1〜12個の炭素原子を含有するアルキレン鎖、パラホルムアルデヒド鎖−(OCH2)1−12−、ポリエチレングリコール鎖−(OCH2CH2)1−6−から選択され、これらの鎖は、O、S、及び/若しくはNH基、並びに/又はC3−9ヘテロアリーレン、並びに/又はフェニレンの1つ又は2つ以上により中断されていてもよく;
X2は、O、S、NR15、CR15R16、CR15R16O、C(=O)、C(=O)NR15、NR15C(=O)、O−C(O)、及びC(O)−Oから選択されるか、又は存在せず;
qは、0、1、2、3、4、5、及び6から選択され;
Aは:
各A1基について、Y3及びY4の1つは独立して、N−R17、S、及びOから選択され;Y3及びY4の他方は、CHであり;Y5は独立して、CH、N、S、及びCOHから選択され;
各A2基について、Y6及びY7の1つは独立して、N及びCHから選択され;Y6及びY7の他方は、CHであり;
R7及びR9は独立して、H、C1−12アルキル、C5−9ヘテロアリール、C6−15ヘテロアリールアルキル、フェニル、及びC7−12アラルキル基から選択され;ヘテロアリール、ヘテロアリールアルキル、フェニル、及びアラルキル基は、C1−6アルキル、OH、及びOC1−6アルキルから選択される最大3個の任意の置換基で置換されていてもよく;
R18は、CO2R11及びNR11R12から選択され;
R8、R10、R11、R12、R13、R14、R15、R16、R17、R20、及びR21は独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6は一緒になって二重結合を形成するか;
(ii)R5はHであり、かつR6はOHであるか;又は
(iii)R5はHであり、かつR6はOC1−6アルキルであるか
のいずれかであり;
ただし、pが0であり、かつAがA1である場合:
(a)少なくとも1つのA1基について、Y3及びY4の1つは、S及びOから選択されるか;若しくは
(b)少なくとも1つのA1基について、Y5は、Sであるか;又は
(c)R4は、ピロリル、イミダゾリル、置換されていてもよいピロリル、若しくは置換されていてもよいイミダゾリルではないこと
を条件とする。
以下の略語は、本明細書全体を通して使用される:Ac アセチル;Alloc アリルオキシカルボニル;BAIB ビス(アセトキシ)ヨードベンゼン/(ジアセトキシヨード)ベンゼン;Boc tert−ブトキシカルボニル;BPD ベンゾピリドジアゼシン;CBz ベンジルオキシカルボニル;DBU 1,8−ジアザビシクロ[5.4.0]ウンデカ−7−エン;DHP ジヒドロピラン;DMAP 4−ジメチルアミノピリジン;DMF ジメチルホルムアミド;DMSO ジメチルスルホキシド;EDCl 1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド;Et エチル;Et2O ジエチルエーテル;EtOAc 酢酸エチル;EtOH エタノール;HATU (1−[ビス(ジメチルアミノ)メチレン]−1H−1,2,3−トリアゾロ[4,5−b]ピリジニウム3−オキシドヘキサフルオロホスフェート);HMDST ヘキサメチルジシラチアン;iBu イソ−ブチル;KOtBu カリウムt−ブトキシド;L−セレクトリドリチウム トリ−sec−ブチル(ヒドリド)ホウ酸塩;Me メチル;MeOH メタノール;PBD ピロロ[2,1−c][1,4]ベンゾ−ジアゼピン;PDD ピリジノベンゾジアゼピン;PIFA フェニルヨウ素(III)ビス[トリフルオロ酢酸塩];Ph フェニル;p−TSA/PTSA p−トルエンスルホン酸;Pyr ピリジン;TBAF テトラブチルアンモニウムフルオリド;TBS−Cl/TBDMSCl tert−ブチルジメチルシリルクロリド;TEA トリエチルアミン;TEMPO (2,2,6,6−テトラメチル−ピペリジン−1−イル)オキシル;TFA トリフルオロ酢酸;THF テトラヒドロフラン;THP テトラヒドロピラニル;Troc 2,2,2−トリクロロエチルカーボネート;及びTs(トシレート) p−トルエンスルホン酸。
N1:ピロール、ピリジン;
O1:フラン;
S1:チオフェン;
N1O1:オキサゾール、イソキサゾール、イソキサジン;
N2O1:オキサジアゾール(例えば1−オキサ−2,3−ジアゾリル、1−オキサ−2,4−ジアゾリル、1−オキサ−2,5−ジアゾリル、1−オキサ−3,4−ジアゾリル);
N3O1:オキサトリアゾール;
N1S1:チアゾール、イソチアゾール;
N2:イミダゾール、ピラゾール、ピリダジン、ピリミジン、ピラジン;
N3:トリアゾール、トリアジン;及び
N4:テトラゾール
に由来するものが挙げられるが、これらに限定されない。
O1:ベンゾフラン、イソベンゾフラン;
N1:インドール、イソインドール、インドリジン、イソインドリン;
S1:ベンゾチオフラン;
N1O1:ベンゾキサゾール、ベンズイソキサゾール;
N1S1:ベンゾチアゾール;
N2:ベンズイミダゾール、インダゾール;
O2:ベンゾジオキソール;
N2O1:ベンゾフラザン;
N2S1:ベンゾチアジアゾール;
N3:ベンゾトリアゾール;及び
N4:プリン(例えばアデニン、グアニン)、プテリジン
に由来するものが挙げられるが、これらに限定されない。
窒素保護基は本分野で周知である。好ましい窒素保護基は、一般式:
ヒドロキシル保護基は、本分野で周知であり、多くの好適な基は、Wuts, P.G.M. and Greene, T.W., Protective Groups in Organic Synthesis, 4th Edition, Wiley-lnterscience, 2007の16〜366頁、及びP. Kocienski, Protective Groups, 3rd Edition (2005)で説明されており、当該文献は、参照により本明細書に組み込む。
R1は、R7、=CH2、=CH−(CH2)m−CH3、=O、(CH2)m−OR7、(CH2)m−CO2R7、(CH2)m−NR7R8、O−(CH2)n−NR7R8、NH−C(O)−R7、O−(CH2)n−NH−C(O)−R7、O−(CH2)n−C(O)−NH−R7、(CH2)m−SO2R7、O−SO2R7、(CH2)m−C(O)R7、及び(CH2)m−C(O)NR7R8から選択される。R1が=CH2、=CH−(CH2)m−CH3、及び=Oから選択される選択肢について、それが結合するC環の炭素は、分子の原子価必要条件を満たすために、任意の二重結合を有することはできない。例えば、R1が=CH2であり、C環の縮合炭素に隣接するC環のC1位に位置し、かつR2がHである場合、得られる式(I)の化合物は:
R2は、R9、(CH2)r−OR9、(CH2)r−CO2R9、(CH2)r−NR9R10、O−(CH2)s−NR9R10、NH−C(O)−R9、O−(CH2)s−NH−C(O)−R9、O−(CH2)s−C(O)−NH−R9、(CH2)r−SO2R9、O−SO2R9、(CH2)r−COR9、及び(CH2)r−C(O)NR9R10から選択される。
好適には、R3は、H、C1−6アルキル、及びCH2Phから選択される。
R4は、最大3個の任意の置換基で置換されていてもよい、フェニル及びC5−9ヘテロアリール基から選択される。それゆえ、R4について選択されるフェニル基又はC5−9ヘテロアリール基のいずれも、最大3個の任意の置換基で置換されていてもよい。
式中、Z1は、NH、N−CH3、S、及びOから選択され;
Z2は、CH及びNから選択され;
Z3は、S及びOから選択され;
Z4は、CH及びNから選択され;
R22は、(CH2)jCO2R11、(CH2)jNR11R12、及びC(=O)−NH−C6H4−(CH2)j−R18から選択され;
R18は、CO2R11及びNR11R12から選択され;
jは、0〜6の整数から選択され;
R11及びR12は独立して、H及びC1−6アルキルから選択され;
R23は、H及びC1−6アルキルから選択される。
式中、Z1は、NH、N−CH3、S、及びOから選択され;
Z2は、CH及びNから選択され;
Z3は、S及びOから選択され;
Z4は、CH及びNから選択され;
R11は、H及びC1−6アルキルから選択され;
R23は、H及びC1−6アルキルから選択される。
(iii)について好適には、R5はHであり、かつR6はO−CH3及びO−CH2CH3から選択されるOC1−6アルキルである。
好適には、R7は、H、C1−12アルキル、C5−9ヘテロアリール、C6−15ヘテロアリールアルキル、フェニル、ベンジル、及びフェネチルから選択され;ヘテロアリール、ヘテロアリールアルキル、フェニル、及びアラルキル基は、C1−6アルキル、OH、及びOC1−6アルキルから選択される最大3個の基で置換されていてもよい。
好適には、R9は、H、C1−12アルキル、C5−9ヘテロアリール、C6−15ヘテロアリールアルキル、フェニル、ベンジル、及びフェネチルから選択され;ヘテロアリール、ヘテロアリールアルキル、フェニル、及びアラルキル基は、C1−6アルキル、OH、及びOC1−6アルキルから選択される最大3個の基で置換されていてもよい。
好適には、R8、R10、R11、R12、R13、R14、R15、R16、R17、R20、及びR21の各々は独立して、H、メチル、エチル、n−プロピル、i−プロピル、n−ブチル、s−ブチル、i−ブチル、及びt−ブチルから選択される。
好適には、R18は、CO2H、CO2CH3、CO2CH2CH3、NH(CH3)、及びNH2から選択される。
好適には、R19は、H、(CH2)t−N(CH2CH3)2、(CH2)t−N(CH3)2、(CH2)t−NH(CH2CH3)、(CH2)t−NH(CH3)、及び(CH2)t−NH2から選択される。
好適には、R24は、OH、メチル、エチル、プロピル、OCH3、OCH2CH3、CO2H、CO2CH3、CO2CH2CH3、O−(CH2)k−NH2、O−(CH2)k−NH(CH3)、(CH2)j−NH2、(CH2)j−NH(CH3)、C(=O)−NH−(CH2)k−NH2、C(=O)−NH−(CH2)k−NH(CH3)、C(=O)−NH−(CH2)k−C(=NH)NH(CH3)、及びC(=O)−NH−(CH2)k−C(=NH)NH2から選択される最大3個の任意の置換基で置換されていてもよい、フェニルである。
jの各場合は独立して、0〜6の整数から選択され、それゆえ、各jは独立して、0、1、2、3、4、5、及び6から選択される。
kの各場合は独立して、1〜6の整数から選択され、それゆえ、各kは独立して、1、2、3、4、5、及び6から選択される。
mは、0〜6の整数から選択され、それゆえ、mは、0、1、2、3、4、5、及び6から選択される。
nは、1〜6の整数から選択され、それゆえ、nは、1、2、3、4、5、及び6から選択される。
rは、0〜6の整数から選択され、それゆえ、rは、0、1、2、3、4、5、及び6から選択される。
sは、1〜6の整数から選択され、それゆえ、sは、1、2、3、4、5、及び6から選択される。
tは、0〜6の整数から選択され、それゆえ、tは、0、1、2、3、4、5、及び6から選択される。
Y1は、N又はCHである;好適には、Y1は、CHである。
Y2は、N又はCHである;好適には、Y2は、CHである。
好適には、X1は、O、S、NH、CH2、CH2O、C(=O)、C(=O)NR13、NR13C(=O)、O−C(O)、及びC(O)−Oから選択される。
好適には、X2は、O、S、NH、CH2、CH2O、C(=O)、C(=O)NR15、NR15C(=O)、O−C(O)、及びC(O)−Oから選択されるか、又は存在しない。
Lは、結合基である。好適には、ペプチド鎖、アルキレン鎖、パラホルムアルデヒド鎖、又はポリエチレングリコール鎖のいずれも、1個若しくは2個以上のヘテロ原子(例えばN、O、及びS)及び/又は1個若しくは2個以上のC5−9ヘテロアリーレン基(例えばピロリレン、ピラゾリレン、ピラゾリレン、1,2,3−トリアゾリレン、ピリジニレン)及び/又は1個若しくは2個以上のフェニレン基により中断されている。より好適には、鎖は、1〜3個のヘテロ原子及び/又は1〜3個のC5−9ヘテロアリーレン基及び/又は1〜3個のフェニレン基により中断されていてもよい。
一実施形態では、Aは、A1:
式中、各A1基について、Y3及びY4の1つは独立して、N−R17、S、及びOから選択され;Y3及びY4の他方は、CHであり;Y5は独立して、CH、N、S、及びCOHから選択される。
式中、Y5は、CH及びNから選択される。
式中、各A2基について、Y6及びY7の1つは独立して、N及びCHから選択され;Y6及びY7の他方は、CHである。
好適には、qは、0、1、2、及び3から選択される。
好適には、式(I)の6員芳香環は、パラ置換され:
本発明は、式(I)の化合物:
式中、点線は、C1とC2、C2とC3、及びC3とC4の1つ又は2つ以上の間に二重結合が存在していてもよいことを示す。
式(I)の化合物についての選択肢は、pが0であり、かつAがA1である場合:(a)少なくとも1つのA1基について、Y3及びY4の1つはS及びOから選択されるか;又は(b)少なくとも1つのA1基について、Y5はSであるか;又は(c)R4は置換されていてもよいピロリル又はイミダゾリルではないという条件を含有する。
式(I)の化合物:
式中、qは、0、1、2、3、4、5、又は6から選択され;
pは、0又は1であり;
Lは、1〜12個の炭素原子を含有するアルキレン鎖であり;
Y1は、N又はCHであり;
Y2は、N又はCHであり;Y1及びY2の少なくとも一方は、CHであり;
Y5は、CH及びNから選択され;
Z1は、O、S、NH、及びN−CH3から選択され;
Z2は、CH及びNから選択され;
Z3は、S及びOから選択され;
Z4は、CH及びNから選択され;
R22は、(CH2)jCO2H、(CH2)jCO2C1−6アルキル、(CH2)jNR11R12、及びC(=O)−NH−C6H4−(CH2)j−R18から選択され;
R18は、CO2R11及びNR11R12から選択され;
R19は、H及び(CH2)t−NR20R21から選択され;
j及びtは独立して、0〜6の整数から選択され;
R11、R12、及びR23は独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6は一緒になって二重結合を形成するか;
(ii)R5はHであり、かつR6はOHであるか;又は
(iii)R5はHであり、かつR6はOC1−6アルキルであるか
のいずれかであり;
ただし、化合物が(XVI)であり、かつpが0である場合、Z1は、O及びSから選択されることを条件とする。
式中、qは、0、1、2、3、4、5、又は6から選択され;
pは、0又は1であり;
Lは、1〜12個の炭素原子を含有するアルキレン鎖であり;
Y1は、N又はCHであり;
Y2は、N又はCHであり;Y1及びY2の少なくとも一方は、CHであり;
Y5は、CH及びNから選択され;
Z1は、O、S、NH、及びN−CH3から選択され;
Z2は、CH及びNから選択され;
Z3は、S及びOから選択され;
Z4は、CH及びNから選択され;
R19は、H及び(CH2)t−NR20R21から選択され;
tは、0〜6の整数から選択され;
R11、R20、R21、及びR23は独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6は一緒になって二重結合を形成するか;
(ii)R5はHであり、かつR6はOHであるか;又は
(iii)R5はHであり、かつR6はOC1−6アルキルであるか
のいずれかであり;
ただし、化合物が(XX)であり、かつpが0である場合、Z1は、O及びSから選択されることを条件とする。
(a)メチル(S)−5−(4−(4−((2−メトキシ−12−オキソ−6a,7,8,9,10,12−ヘキサヒドロベンゾ[e]ピリド−[1,2−a][1,4]ジアゼピン−3−イル)オキシ)ブタンアミド)−1−メチル−1H−ピロール−2−カルボキサミド)ベンゾ−[b]チオフェン−2−カルボキシレート(13)
(m)(S)−N−(2−アミノエチル)−4−(4−(4−(4−((2−メトキシ−12−オキソ−6a,7,8,9,10,12−ヘキサヒドロベンゾ[e]ピリド[1,2−a][1,4]ジアゼピン−3−イル)オキシ)ブタンアミド)−1−メチル−1H−ピロール−2−カルボキサミド)フェニル)−1−メチル−1H−ピロール−2−カルボキサミド(68)
点線は、C1とC2、C2とC3、及びC3とC4の1つ又は2つ以上の間に二重結合が存在していてもよいことを示し;
R1は、R7、=CH2、=CH−(CH2)m−CH3、=O、(CH2)m−OR7、(CH2)m−CO2R7、(CH2)m−NR7R8、O−(CH2)n−NR7R8、NH−C(O)−R7、O−(CH2)n−NH−C(O)−R7、O−(CH2)n−C(O)−NH−R7、(CH2)m−SO2R7、O−SO2R7、(CH2)m−C(O)R7、及び(CH2)m−C(O)NR7R8から選択され;
R2は、R9、=CH2、=CH−(CH2)r−CH3、=O、(CH2)r−OR9、(CH2)r−CO2R9、(CH2)r−NR9R10、O−(CH2)s−NR9R10、NH−C(O)−R9、O−(CH2)s−NH−C(O)−R9、O−(CH2)s−C(O)−NH−R9、(CH2)r−SO2R9、O−SO2R9、(CH2)r−COR9、及び(CH2)r−C(O)NR9R10から選択され;
R3は、H、C1−12アルキル、及びCH2Phから選択され;
R4は、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、C(=O)−NH−C6H4−(CH2)j−R18、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよい、フェニル及びC5−9ヘテロアリール基から選択され;
R19は、H及び(CH2)t−NR20R21から選択され;
Y1は、N又はCHであり;Y2は、N又はCHであり;Y1及びY2の少なくとも一方は、CHであり;
pは、0又は1であり;j、m、r、及びtは独立して、0〜6の整数から選択され;
k、n、及びsは独立して、1〜6の整数から選択され;
X1は、O、S、NR13、CR13R14、CR13R14O、C(=O)、C(=O)NR13、NR13C(=O)、O−C(O)、及びC(O)−Oから選択され;
Lは、アミノ酸、2〜6個のアミノ酸を有するペプチド鎖、1つ又は2つ以上の炭素−炭素二重結合又は三重結合を含有し得る1〜12個の炭素原子を含有するアルキレン鎖、パラホルムアルデヒド鎖−(OCH2)1−12−、ポリエチレングリコール鎖−(OCH2CH2)1−6−から選択され、これらの鎖は、O、S、及び/若しくはNH基、並びに/又はC3−9ヘテロアリーレン、並びに/又はフェニレンの1つ又は2つ以上により中断されていてもよく;
X2は、O、S、NR15、CR15R16、CR15R16O、C(=O)、C(=O)NR15、NR15C(=O)、O−C(O)、及びC(O)−Oから選択されるか、又は存在せず;
qは、0、1、2、3、4、5、及び6から選択され;
Aは:
各A1基について、Y3及びY4の1つは独立して、N−R17、S、及びOから選択され;Y3及びY4の他方は、CHであり;Y5は独立して、CH、N、S、及びCOHから選択され;
各A2基について、Y6及びY7の1つは独立して、N及びCHから選択され;Y6及びY7の他方は、CHであり;
R7及びR9は独立して、H、C1−12アルキル、C5−9ヘテロアリール、C6−15ヘテロアリールアルキル、フェニル、及びC7−12アラルキル基から選択され;ヘテロアリール、ヘテロアリールアルキル、フェニル、及びアラルキル基は、C1−6アルキル、OH、及びOC1−6アルキルから選択される最大3個の任意の置換基で置換されていてもよく;
R18は、CO2R11及びNR11R12から選択され;
R8、R10、R11、R12、R13、R14、R15、R16、R17、R20、及びR21は独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6は一緒になって二重結合を形成するか;又は(ii)R5はHであり、かつR6はOHであるか;又は(iii)R5はHであり、かつR6はOC1−6アルキルであるか
である。
本発明は、増殖性疾患の治療において用途を見出す。
抗体療法は、がん、免疫学的障害及び血管新生性障害を有する患者の標的化治療のために確立されている(Carter, P. (2006) Nature Reviews Immunology 6:343-357)。抗体−薬物コンジュゲート(ADC,antibody-drug conjugate)、すなわち、イムノコンジュゲートの、細胞毒性剤又は細胞分裂阻害剤、すなわち、がんの治療において腫瘍細胞を殺傷又は阻害するための薬物の局所的送達のための使用は、薬物部分の腫瘍への送達及び腫瘍内での細胞内蓄積を目的とする一方、これらのコンジュゲートされていない薬剤の全身性投与は正常細胞への許容できない毒性レベルをもたらし得る(Xie et al (2006) Expert. Opin. Biol. Ther. 6(3):281 -291、Kovtun ef a/ (2006) Cancer Res. 66(6):3214-3121、Law et al (2006) CancerRes. 66(4):2328-2337、Wu et al (2005) Nature Biotech. 23(9): 1 137-1 145、Lambert J. (2005) Current Opin. in Pharmacol. 5:543-549、Hamann P. (2005) Expert Opin. Ther. Patents 15(9): 1087-1 103、Payne, G. (2003) Cancer Cell 3:207-212、Trail ef a/ (2003) Cancer Immunol. Immunother. 52:328-337、Syrigos and Epenetos (1999) Anticancer Research 19:605-614)。
「抗体」という用語は具体的には、所望の生物学的活性、例えば標的細胞又は組織上の所望の抗原に結合する能力を示す限り、モノクローナル抗体、ポリクローナル抗体、二量体、多量体、多重特異性抗体(例えば二重特異性抗体)、インタクトな抗体、及び抗体断片を包含する。抗体は、マウス、ヒト、ヒト化、キメラであるか、又は他の種由来であってもよい。抗体は、特定の抗原を認識し、これに結合することができる免疫系により発生されるタンパク質である(Janeway, C, Travers, P., Walport, M., Shlomchik (2001) Immuno Biology, 5th Ed., Garland Publishing, New York)。標的抗原は一般的に、抗体上のCDRにより認識される、エピトープとも呼ばれる多くの結合部位を有する。異なるエピトープに特異的に結合する各抗体は、異なる構造を有する。したがって、1つの抗原は、1つ超の対応する抗体を有し得る。抗体は、全長イムノグロブリン分子、又は全長イムノグロブリン分子の免疫学的に活性な部分、すなわち、所望の標的の抗原若しくはその部分に免疫特異的に結合する抗原結合部位を含有する分子を含み、かかる標的として、がん細胞又は自己免疫疾患と関連付けられる自己免疫抗体を生成する細胞が挙げられるが、これらに限定されない。イムノグロブリンは、イムノグロブリン分子のいかなる種類(例えばIgG、IgE、IgM、IgD、及びIgA)、クラス(例えばIgG1、IgG2、IgG3、IgG4、IgA1、及びIgA2)若しくはサブクラス、又はアロタイプ(例えばヒトG1m1、G1m2、G1m3、非G1m1[G1m1以外のいずれかのアロタイプであるもの]、G1m17、G2m23、G3m21、G3m28、G3m11、G3m5、G3m13、G3m14、G3m10、G3m15、G3m16、G3m6、G3m24、G3m26、G3m27、A2m1、A2m2、Km1、Km2、及びKm3)のものであってもよい。イムノグロブリンは、ヒト、マウス、又はウサギ起源を含む、いかなる種に由来してもよい。
式Iの化合物は、単独で、又は1つの若しくは別のものとの、若しくは式Iの化合物とは異なる1つ若しくは2つ以上の薬理学的に活性な化合物との組合せで、投与することができる。
別に指定しない限り、これらの置換基の周知のイオン性形態、塩形態、溶媒和物形態、及び保護形態が、上記に含まれる。また、例えば、カルボン酸(−COOH)についての言及は、そのアニオン性(カルボキシレート)形態(−COO−)、その塩、又は溶媒和物、及び従来型保護形態を含む。同様に、アミノ基についての言及は、アミノ基のプロトン化形態(−N+HR1R2)、塩、又は溶媒和物、例えば、塩酸塩、及びアミノ基の従来型保護形態を含む。また、同様に、ヒドロキシル基についての言及は、そのアニオン性形態(−O−)、その塩、又は溶媒和物、及び従来型保護形態を含む。
ある特定の化合物は、1つ又は2つ以上の特定の形状的、光学的、鏡像異性、ジアステレオ異性、エピマーの、アトロピックの、立体異性、互変異性、コンフォメーションの、又はアノマーの形態で存在してもよく、本明細書で後に集合的に「異性体」(又は「異性形」)と呼ばれる、シス及びトランス体;E及びZ体;c、t、及びr体;エンド及びエキソ体;R、S、及びメソ体;D及びL体;d及びl体;(+)及び(−)体;ケト、エノール、及びエノレート形;シン及びアンチ体;向斜及び背斜体;アルファ及びベータ体;アキシャル及びエクアトリアル体;舟形、いす形、ねじれ形、エンベロープ形、及び半いす形;並びにこれらの組合せを含むが、これらに限定されない。
式(I)の化合物は、以下に説明する技術を使用して調製することができる。スキーム及び実施例の一部は、有機化学の分野の当業者に公知の、酸化、還元等を含む通常の反応、分離技術(抽出、蒸発、沈殿、クロマトグラフィー、濾過、研和、結晶化等)、及び分析手順の詳細を省略している場合がある。かかる反応及び技術の詳細は、Richard Larock, Comprehensive Organic Transformations, A Guide to Functional Group Preparations, 2nd Ed (2010)、及びMichael B. Smith and othersにより編集された多数巻のシリーズCompendium of Organic Synthetic Methods (1974 et seq.)を含む、いくつかの専門書で見ることができる。出発物質及び試薬は、市販の供給源から得てもよく、又は文献の方法を使用して調製してもよい。反応スキームの一部は、化学的変換から生じる少量の生成物(例えば、エステルの加水分解からのアルコール、二酸の脱炭酸からのCO2等)を省略している場合がある。加えて、一部の場合、反応中間体は、単離又は精製を行わずに(すなわちその場で)、続くステップで使用することができる。
概説
合成構築ブロック及び試薬をMaybridge Chemicals社(UK)、Fluorochem社(USA)、ChemShuttle社(USA)及びSigma-Aldrich社(UK)から購入した。溶媒をSigma-Aldrich社(UK)及びFisher Scientific社(UK)から購入した。無水反応を、窒素の不活性雰囲気下で、予め炉乾燥したガラス製品中で行った。無水溶媒をさらに乾燥させずに購入したまま使用した。薄層クロマトグラフィー(TLC,Thin Layer Chromatography)をシリカゲルアルミニウムプレート(Merck 60、F254)上で実施し、カラムクロマトグラフィーを、シリカゲル(Merck 9385、230〜400メッシュASTM、40〜63μM)(薄層クロマトグラフィー:UV(254nm)及び染色剤としての過マンガン酸カリウムのアルカリ水溶液によってモニタリングしながら)を手動で使用するか、又はGrace Reveleris(登録商標)X2自動フラッシュクロマトグラフィーシステムを使用して行った。NMRスペクトルは全て、Bruker社のDPX400分光計を使用して室温で得られ、化学シフトは、溶媒に対してppmで表され、カップリング定数はHzで表される。液体クロマトグラフィー質量分析(LCMS,Liquid Chromatography Mass Spectroscopy)による分析は全て、水(A)及びアセトニトリル(B)を含む移動相を用いてWaters社のAlliance 2695で実施した。ギ酸(0.1%)をアセトニトリルに添加して、分析を通して酸性条件を確保した。ファンクションタイプ:ダイオードアレイ(535回走査)。カラムタイプ:Monolithic C18 50×4.60mm。Waters社の2996 PDAを備えるWaters社の2695 HPLCに接続したWaters社のMicromass ZQ機器を使用して質量分析データを収集した。使用したWaters社のMicromass ZQパラメーターは次の通りであった:キャピラリー(kV)、3.38;コーン(V)、35;抽出装置(V)、3.0;ソース温度(℃)、100;脱溶媒温度(℃)、200;コーン流量(L/時)、50;脱溶媒流量(L/時)、250。マイクロ波反応をAnton Paar社のMonowave 300マイクロ波合成反応器で行った。他に述べられていなければ、収率は(TLC又はNMRにより均質な)単離した物質に関し、名称はIUPAC命名法に従って指定される。LCMSの勾配条件を以下に記載する。
1H NMR(400MHz,CDCl3)δ9.84(s,1H)、7.46〜7.37(m,2H)、6.98(d,J=8.2Hz,1H)、4.16(t,J=6.3Hz,2H)、3.91(s,3H)、3.69(s,3H)、2.56(t,J=7.2Hz,2H)、2.20(五重線,J=6.7Hz,2H);13C NMR(100MHz,CDCl3)δ190.9、173.4、153.8、149.9、130.1、126.8、111.6、109.2、67.8、56.0、51.7、30.3、24.2;MS m/z(EIMS)=271.9(M+Na)+;LCMS(方法A):tR=6.48分。
1H NMR(400MHz,CDCl3)δ10.42(s,1H)、7.60(s,1H)、7.39(s,1H)、4.21(t,J=6.3Hz,2H)、3.98(s,3H)、3.70(s,3H)、2.61〜2.53(m,2H)、2.22(五重線,J=6.6Hz,2H);13C NMR(100MHz,CDCl3)δ187.8、173.2、153.5、151.7、143.8、125.5、109.9、108.1、68.6、56.6、51.8、30.2、24.1;MS m/z(EIMS)=296.1(M−H)−;LCMS(方法A):tR=6.97分。
1H NMR(400MHz,MeOD)δ7.47(s,1H)、7.25(s,1H)、4.13(t,J=6.2Hz,2H)、3.94(s,3H)、3.68(s,3H)、2.54(t,J=7.2Hz,2H)、2.17〜2.06(m,2H);13C NMR(100MHz,MeOD)δ175.3、168.6、153.8、151.3、143.1、122.8、112.4、109.2、69.6、57.0、52.2、31.2、25.5;MS m/z(EIMS)=311.9(M−H)−;LCMS(方法A):tR=6.22分。
1H NMR(400MHz,CDCl3)δ7.68〜7.64(m,1H)、6.77〜6.70(m,1H)、4.16〜4.07(m,3H)、3.93〜3.89(m,3H)、3.83(s,1H)、3.67(s,3H)、3.15(d,J=1.4Hz,1H)、3.11(s,1H)、2.78(s,1H)、2.56〜2.50(m,3H)、2.21〜2.12(m,4H)、1.74〜1.55(m,4H);13C NMR(100MHz,CDCl3)δ173.3、168.1、154.6、148.2、137.4、127.6、111.4、108.3、68.3、60.6、56.7、53.5、51.7、43.3、38.0、34.9、30.3、24.1、19.7;MS m/z(EIMS)=411.0(M+H)+;LCMS(方法A):tR=6.28分。
1H NMR(400MHz,CDCl3)δ6.69(s,1H)、6.27〜6.18(m,1H)、4.03〜3.94(m,3H)、3.94〜3.82(m,3H)、3.81〜3.76(m,1H)、3.74(s,3H)、3.73〜3.68(m,1H)、3.67〜3.65(m,3H)、3.56(d,J=4.8Hz,1H)、3.03(s,1H)、2.51(t,J=7.2Hz,2H)、2.11(五重線,J=6.7Hz,2H)、1.68〜1.59(m,4H)、1.55〜1.40(m,2H);13C NMR(100MHz,CDCl3)δ173.6、171.2、150.3、141.8、141.1、113.2、112.3、102.4、67.5、60.8、60.4、56.8、51.6、30.4、25.8、24.3、21.0、19.9、14.2;MS m/z(EIMS)=381.0(M+H)+;LCMS(方法A):tR=5.52分。
1H NMR(400MHz,CDCl3)δ8.30(br s,1H)、7.63(br s,1H)、6.76(br s,1H)、5.92(ddt,J=17.2,10.6,5.4,5.4Hz,1H)、5.37〜5.28(m,1H)、5.20(dq,J=10.4,1.3Hz,1H)、4.65〜4.56(m,2H)、4.06(t,J=6.2Hz,2H)、3.94〜3.82(m,1H)、3.79(s,3H)、3.66(s,3H)、3.62〜3.54(m,1H)、3.40(br s,1H)、3.10〜2.88(m,1H)、2.52(t,J=7.4Hz,2H)、2.22〜2.04(m,3H)、1.64(br s,4H)、1.56〜1.31(m,2H);13C NMR(100MHz,CDCl3)δ173.5、170.6、153.9、149.7、144.8、132.6、130.1、117.6、116.9、110.8、107.1、106.0、67.7、65.6、60.7、56.3、53.5、51.6、43.1、30.5、25.7、24.4、19.7;MS m/z(EIMS)=465.1(M+H)+;LCMS(方法A):tR=6.47分。
MS m/z(EIMS)=462.9(M+H)+;LCMS(方法A):tR=6.30分。
MS m/z(EIMS)=546.7(M+H)+;LCMS(方法A):tR=7.70分。
MS m/z(EIMS)=532.9(M+H)+;LCMS(方法A):tR=6.98分。
MS m/z(EIMS)=430.2(M+H)+;LCMS(方法A):tR=7.90分。
MS m/z(EIMS)=329.9(M+H)+;LCMS(方法A):tR=5.52分。
MS m/z(EIMS)=844.0(M+H)+;LCMS(方法A):tR=8.10分。
1H NMR(CDCl3,400MHz)δ8.35(s,1H)、8.28(s,1H)、8.02(s,1H)、7.94(s,1H)、7.90(d,J=5.7Hz,1H)、7.75(d,J=8.8Hz,1H)、7.58(dd,J=8.7,2.1Hz,1H)、7.42〜7.41(m,1H)、7.13(d,J=1.6Hz,1H)、6.78(s,1H)、6.56(d,J=1.6Hz,1H)、4.25〜4.18(m,1H)、4.08(t,J=6.0Hz,2H)、3.93(s,3H)、3.88(s,3H)、3.83(s,3H)、3.79〜3.75(m,1H)、3.23〜3.16(m,1H)、2.52〜2.47(m,2H)、2.21(d,J=6.4Hz,1H)、2.18(d,J=2.1Hz,1H)、1.96(br s,2H)、1.86〜1.81(m,2H)、1.77〜1.66(m,2H);13C NMR(100MHz,CDCl3)δ170.0、167.6、163.4、163.2、160.0、150.7、148.0、140.0、139.2、137.6、135.8、134.2、130.6、123.0、122.9、121.5、121.0、120.1、116.2、111.7、110.3、104.3、68.1、56.1、53.5、52.5、49.7、40.0、36.8、33.0、24.9、24.5、22.9、18.3;MS m/z(EIMS)=658.0(M+H)+;LCMS(方法A):tR=6.92分。
MS m/z(EIMS)=683.7(M+H)+;LCMS(方法A):tR=7.35分。
MS m/z(EIMS)=656.2(M+H)+;LCMS(方法A):tR=6.53分。
MS m/z(EIMS)=844.9(M+H)+;LCMS(方法A):tR=8.22分。
1H NMR(CDCl3,400MHz)δ9.07(s,1H)、8.36(d,J=2.0Hz,1H)、8.13(s,1H)、8.03(s,1H)、7.90(d,J=5.7Hz,1H)、7.82(d,J=8.7Hz,1H)、7.56(dd,J=8.7,2.1Hz,1H)、7.49〜7.43(m,2H)、6.81(s,1H)、4.26〜4.17(m,2H)、4.10〜4.06(m,3H)、3.98〜3.93(m,6H)、3.93〜3.85(m,1H)、3.74(td,J=5.8,4.0Hz,1H)、3.27〜3.16(m,1H)、2.68〜2.60(m,2H)、2.29(五重線,J=6.4Hz,2H)、2.10〜2.02(m,1H)、1.97〜1.89(m,1H)、1.83〜1.77(m,2H)、1.76(s,2H);13C NMR(100MHz,CDCl3)δ169.7、167.5、163.3、163.2、160.3、156.7、150.4、148.0、140.0、139.3、135.8、135.0、130.6、123.2、120.1、115.4、114.9、110.3、98.0、67.8、65.2、56.1、52.6、49.6、39.8、35.9、32.9、31.0、29.3、24.7、24.6、22.9、18.4;MS m/z(EIMS)=659.1(M+H)+;LCMS(方法A):tR=7.00分。
MS m/z(EIMS)=230.9(M+H)+;LCMS(方法A):tR=5.17分。
MS m/z(EIMS)=868.1(M+H)+;LCMS(方法A):tR=8.22分。
1H NMR(CDCl3,400MHz)δ8.95(s,1H)、8.27(s,1H)、7.89(d,J=5.7Hz,1H)、7.59(d,J=8.6Hz,2H)、7.47〜7.41(m,4H)、7.19(d,J=2.0Hz,1H)、7.05(d,J=1.9Hz,1H)、6.79(s,1H)、4.25〜4.18(m,1H)、4.17〜4.12(m,1H)、4.12〜4.06(m,1H)、4.04(s,3H)、3.95(s,3H)、3.93(s,3H)、3.84(s,3H)、3.76〜3.71(m,1H)、3.26〜3.16(m,1H)、2.65〜2.57(m,2H)、2.26(t,J=6.4Hz,2H)、2.09〜2.01(m,2H)、1.96〜1.89(m,1H)、1.85〜1.77(m,2H)、1.67(dd,J=10.9,5.5Hz,1H);13C NMR(100MHz,CDCl3)δ169.7、167.5、163.3、161.7、156.5、150.4、148.0、140.0、135.8、135.6、133.7、130.6、126.1、125.5、123.1、122.8、120.0、114.6、111.6、110.2、67.8、56.1、51.2、49.6、39.8、37.0、35.8、32.8、31.0、29.7、24.7、24.5、22.9、18.4;MS m/z(EIMS)=682.1(M+H)+;LCMS(方法A):tR=7.03分。
MS m/z(EIMS)=668.8(M+H)+;LCMS(方法A):tR=7.42分。
MS m/z(EIMS)=677.0(M+Na)+;LCMS(方法A):tR=6.92分。
MS m/z(EIMS)=867.0(M+H)+;LCMS(方法A):tR=8.10分。
1H NMR(CDCl3,400MHz)δ8.09(s,1H)、8.04〜8.01(m,1H)、7.90(d,J=5.8Hz,1H)、7.58(s,1H)、7.56(s,1H)、7.44〜7.40(m,3H)、7.18(d,J=2.0Hz,1H)、7.12(d,J=1.8Hz,1H)、7.04(d,J=2.0Hz,1H)、6.78(s,1H)、6.50(d,J=1.9Hz,1H)、4.26〜4.18(m,1H)、4.07(t,J=6.0Hz,2H)、3.94(s,3H)、3.87(s,3H)、3.84(d,J=2.9Hz,6H)、3.76(td,J=5.7,3.9Hz,1H)、3.25〜3.15(m,1H)、2.49(t,J=7.0Hz,2H)、2.24〜2.18(m,2H)、2.10〜2.03(m,1H)、2.01〜1.93(m,2H)、1.86〜1.80(m,2H)、1.73〜1.66(m,1H);13C NMR(100MHz,CDCl3)δ169.9、167.6、163.5、161.7、159.7、150.7、147.9、139.9、136.4、130.2、126.1、125.4、123.3、123.0、120.6、119.8、114.6、111.7 110.2、103.9、68.1、56.1、53.8、51.2、49.7、39.9、37.0、36.7、33.0、31.0、29.3、24.9、24.5、22.9、18.4;MS m/z(EIMS)=681.0(M+H)+;LCMS(方法A):tR=6.98分。
MS (ES+):m/z=666(M+H)+;LCMS(方法A):tR=7.88分。
MS (ES+):m/z=652(M+H)+;LCMS(方法A):tR=7.13分。
MS (ES+):m/z=864(M+H)+;LCMS(方法A):tR=8.10分。
1H NMR(CDCl3,400MHz)δ8.14(br s,1H)、8.06(br s,1H)、7.91(d,J=5.7Hz,1H)、7.81(d,J=8.7Hz,2H)、7.65(d,J=8.6Hz,2H)、7.60(d,J=8.4Hz,2H)、7.46〜7.50(m,2H)、7.41(s,1H)、7.21(d,J=2.1Hz,1H)、7.08(d,J=1.9Hz,1H)、6.78〜6.82(m,1H)、4.24(d,J=14.0Hz,1H)、4.11〜4.18(m,2H)、3.95〜3.98(m,3H)、3.83〜3.86(m,6H)、3.74〜3.79(m,2H)、3.18〜3.30(m,2H)、2.60〜2.66(m,2H)、2.28(t,J=6.3Hz,2H)、1.97(d,J=6.3Hz,2H)、1.82〜1.88(m,2H);13C NMR(100MHz,CDCl3)δ215.5、171.1、167.5、165.0、163.4、161.7、150.3、147.8、141.3、140.0、136.2、130.8、128.1、125.6、123.5、123.1、121.5、120.6、119.3、114.7、111.7、110.2、67.9、56.1、51.2、49.7、39.8、37.0、34.3、30.9、25.6、24.5、23.0、18.4;MS(ES+):m/z=678(M+H)+;LCMS(方法A):tR=7.05分。
MS (ES+):m/z=841(M+H)+;LCMS(方法A):tR=8.15分。
1H NMR(CDCl3,400MHz)δ8.48(br s,1H)、8.39(d,J=1.9Hz,1H)、8.31(s,1H)、7.97(s,1H)、7.91(d,J=5.8Hz,1H)、7.77〜7.84(m,3H)、7.65(dd,J=8.8,2.0Hz,1H)、7.57(d,J=8.6Hz,2H)、7.38(s,1H)、6.79(s,1H)、4.24(dt,J=13.7,4.1Hz,1H)、4.09〜4.17(m,2H)、3.95(s,3H)、3.79〜3.82(m,3H)、3.74〜3.79(m,1H)、3.49(d,J=3.9Hz,1H)、3.29〜3.41(m,1H)、3.17〜3.28(m,1H)、2.58〜2.64(m,2H)、2.26(五重線,J=6.2Hz,2H)、2.05〜2.13(m,1H)、1.92〜2.01(m,1H)、1.83〜1.87(m,1H)、1.07〜1.19(m,1H);13C NMR(CDCl3,100MHz)δ171.2、167.5、165.5、163.4、163.2、150.4、147.8、141.5、140.0、139.3、138.0、135.1、134.4、130.6、128.2、123.0、121.4、120.9、119.2、116.4、111.7、110.1、67.9、56.0、52.6、49.7、39.8、34.2、30.9、24.7、24.5、22.9、18.3;MS(ES+):m/z=655(M+H)+;LCMS(方法A):tR=7.00分。
1H NMR(CDCl3,400MHz)δ9.16(s,1H)、8.01〜8.07(m,2H)、7.69〜7.75(m,2H)、7.21(br s,1H)、6.84(s,1H)、4.07(s,3H)、3.92(s,3H)、1.53(s,9H);MS(ES−):m/z=373(M−H)−;LCMS(方法A):tR=7.68分。
1H NMR(MeOD,400MHz)δ7.89〜7.95(m,2H)、7.72〜7.78(m,2H)、7.31(s,1H)、4.01(s,3H)、3.80(s,3H);13C NMR(MeOD,100MHz)δ168.0、143.6、132.5、131.6、126.9、123.3、120.6、92.6、68.1、52.3、36.7;MS(ES+):m/z=275(M+H)+;LCMS(方法A):tR=5.43分。
MS (ES+):m/z=789(M+H)+;LCMS(方法A):tR=7.87分。
1H NMR(CDCl3,400MHz)δ9.13(s,1H)、8.24(s,1H)、8.03(d,J=8.7Hz,2H)、7.90(d,J=5.7Hz,1H)、7.65〜7.75(m,2H)、7.43〜7.50(m,2H)、6.77〜6.83(m,1H)、4.12〜4.23(m,2H)、4.07(s,3H)、3.93(s,3H)、3.91(s,3H)、3.18〜3.27(m,1H)、2.80(s,3H)、2.56〜2.68(m,3H)、2.23〜2.31(m,2H)、1.85(d,J=10.1Hz,4H);13C NMR(CDCl3,100MHz)δ169.3、167.1、166.2、162.9、156.2、150.1、147.6、147.4、141.4、139.6、135.6、132.8、130.5、130.3、125.2、121.1、118.2、114.8、111.2、109.9、94.1、67.4、63.5、55.7、53.4、51.6、49.2、39.4、38.2、35.5、32.5、31.6、30.9、28.9、24.9、24.3、24.1、22.5、19.9、18.0;MS(ES+):m/z=603(M+H)+;LCMS(方法A):tR=6.57分。
1H NMR(CDCl3,400MHz)δ7.99〜8.07(m,2H)、7.69(s,1H)、7.61〜7.67(m,2H)、6.88(s,1H)、6.69(br s,1H)、6.25(br s,1H)、3.93(s,3H)、3.91(s,3H)、1.52(s,9H);13C NMR(CDCl3,100MHz)δ166.6、159.4、153.4、142.3、130.9、125.5、123.1、122.5、119.2、118.7、140.1、80.5、52.0、36.8、28.4;MS(ES+):m/z=374(M+H)+;LCMS(方法A):tR=7.52分。
1H NMR(MeOD,400MHz)δ7.99(d,J=8.7Hz,2H)、7.80(d,J=8.7Hz,2H)、7.13(d,J=1.9Hz,1H)、7.09(d,J=1.9Hz,1H)、3.96(s,3H)、3.89(s,3H);13C NMR(MeOD,100MHz)δ168.2、161.2、144.5、131.5、126.9、126.4、123.7、120.8、114.2、109.0、52.5、37.5;MS(ES+):m/z=274(M+H)+;LCMS(方法A):tR=4.98分。
MS (ES+):m/z=788(M+H)+;LCMS(方法A):tR=7.77分
1H NMR(CDCl3,400MHz)δ8.41(s,1H)、8.00(s,2H)、7.98(s,1H)、7.90(d,J=5.8Hz,1H)、7.72〜7.74(m,1H)、7.70〜7.72(m,1H)、7.41(s,1H)、7.14(d,J=1.8Hz,1H)、6.79(s,1H)、6.57(d,J=1.8Hz,1H)、4.22(d,J=14.1Hz,1H)、4.09(t,J=6.0Hz,2H)、3.89(s,3H)、3.88(s,3H)、3.83(s,3H)、3.74〜3.79(m,2H)、3.21(d,J=3.3Hz,1H)、2.47〜2.52(m,2H)、2.17〜2.23(m,2H)、1.93(br s,3H)、1.79〜1.85(m,2H);13C NMR(CDCl3,100MHz)δ170.0、167.6、166.8、163.6、159.8、150.7、147.9、142.9、139.9、130.7、124.9、122.8、121.6、121.5、120.8、119.1、111.8、110.4、104.6、68.1、56.1、52.0、49.7、39.9、36.9、33.0、31.0、25.0、24.5、22.9、18.3;MS(ES+):m/z=602(M+H)+;LCMS(方法A):tR=6.52分。
MS (ES+):m/z=853(M+H)+;LCMS(方法B):tR=3.83分
MS (ES+):m/z=944(M+H)+;LCMS(方法B):tR=3.45分。
1H NMR(DMSO−d6,400MHz)δ9.88〜9.96(m,1H)、9.81(s,2H)、9.50(s,1H)、8.32(br s,2H)、8.00(d,J=5.7Hz,1H)、7.67〜7.73(m,2H)、7.48(d,J=8.6Hz,2H)、7.39(d,J=1.8Hz,1H)、7.31〜7.35(m,2H)、7.30(d,J=1.6Hz,1H)、7.27(s,1H)、7.22(d,J=1.5Hz,1H)、6.96(d,J=1.6Hz,1H)、6.80(s,1H)、6.51〜6.55(m,2H)、4.09〜4.17(m,1H)、3.99〜4.05(m,1H)、3.90〜3.97(m,1H)、3.88(s,3H)、3.83(s,3H)、3.82(s,3H)、3.68〜3.72(m,1H)、3.05〜3.16(m,2H)、2.44(t,J=7.3Hz,2H)、2.02〜2.07(m,2H)、1.81〜1.91(m,1H)、1.68〜1.78(m,2H)、1.56(d,J=4.9Hz,2H);13C NMR(DMSO−d6,100MHz)δ168.8、166.3、164.7、159.5、159.2、150.2、147.1、144.7、139.8、137.0、129.6、128.2、126.1、124.6、124.3、122.0、121.8、120.4、120.2、118.8、113.7、111.3、109.6、104.7、67.7、67.2、55.6、51.1、49.2、38.5、36.2、36.1、35.4、31.8、30.2、24.7、23.7、22.5、17.7;MS(ES+):m/z=757(M+H)+;LCMS(方法A):tR=5.80分。
MS (ES+):m/z=430(M+H)+;LCMS(方法B):tR=4.07分。
MS (ES+):m/z=364(M+H)+;LCMS(方法B):tR=2.78分。
MS (ES+):m/z=844(M+H)+;LCMS(方法B):tR4.23分。
MS (ES+):m/z=831(M+H)+;LCMS(方法B):tR=3.82分。
MS (ES+):m/z=921(M+H)+;LCMS(方法B):tR=3.48分。
1H NMR(DMSO−d6,400MHz)δ10.13(s,1H)、9.98〜10.03(m,1H)、9.95(s,1H)、8.35 8.42(m,1H)、8.19(s,1H)、8.01(d,J=5.7Hz,1H)、7.95(d,J=8.9Hz,1H)、7.33〜7.40(m,2H)、7.23〜7.28(m,2H)、7.02(s,1H)、6.81(s,1H)、6.57(d,J=8.7Hz,2H)、5.00(br.s.,2H)、4.10〜4.14(m,1H)、3.86(s,3H)、3.83(s,3H)、3.65〜3.74(m,2H)、3.15〜3.19(m,1H)、3.06〜3.14(m,1H)、2.45(t,J=7.5Hz,3H)、2.11〜2.13(m,1H)、2.00〜2.08(m,4H)1.74(dd,J=9.0,5.3Hz,3H);MS(ES+):m/z=734(M+H)+;LCMS(方法A):tR=5.63分。
1H NMR(400MHz,CDCl3)δ9.84(s,1H)、7.42〜7.44(dd,J=8.2,1.9Hz,1H)、7.40(d,J=1.9Hz,1H)、6.96(d,J=8.1Hz,1H)、4.08〜4.15(m,4H)、3.92(s,3H)、2.34(t,J=7.5Hz,2H)、1.87〜1.94(m,2H)、1.68〜1.75(m,2H)、1.49〜1.56(m,2H)、1.25(t,J=7.2Hz,3H);MS(ES+):m/z=317(M+Na)+;LCMS(方法B):tR=3.82分。
1H NMR(400MHz,CDCl3)δ10.43(s,1H)7.58(s,1H)、7.40(s,1H)、4.10〜4.16(m,4H)、4.00(s,3H)、2.35(t,J=7.4Hz,2H)、1.84〜1.96(m,2H)、1.69〜1.76(m,2H)、1.50〜1.58(m,2H)、1.25(t,J=7.2Hz,3H);MS(ES+):m/z=340(M+H)+;LCMS(方法B):tR=4.02分。
1H NMR(400MHz,CDCl3)δ7.34(s,1H)、7.14(s,1H)、3.96〜4.03(m,4H)、3.84(s,3H)、2.24(t,J=7.4Hz,2H)、1.70〜1.77(m,2H)、1.55〜1.62(m,2H)、1.39〜1.45(m,2H)、1.13(t,J=7.1Hz,3H);MS(ES+):m/z=354(M−H)+;LCMS(方法B):tR=3.63分。
1H NMR(400MHz,CDCl3)δ7.60〜7.63(m,1H)、6.75〜6.77(m,1H)、4.02〜4.13(m,4H)、3.93(s,3H)、3.70〜3.78(m,1H)、3.39〜3.68(m,1H)、3.11〜3.18(m,3H)、2.32(t,J=7.6Hz,2H)、1.83〜1.91(m,2H)、1.39〜1.72(m,11H)、1.26(t,J=7.1Hz,3H);MS(ES+):m/z=453(M+H)+;LCMS(方法B):tR=3.63分。
1H NMR(400MHz,CDCl3)δ6.69(s,1H)、6.32(s,1H)、4.13(m,4H)、3.98(t,J=6.5Hz,2H)、3.79(s,3H)、3.67〜3.57(m,1H)、3.19〜3.22(m,4H)、2.87(s,2H)、2.32〜2.36(m,2H)、1.82〜1.89(m,2H)、1.65〜1.73(m,6H)、1.47〜1.55(m,3H)、1.27(t,J=7.1Hz,3H);MS(ES+):m/z=423(M+H)+;LCMS(方法B):tR=3.23分。
1H NMR(400MHz,CDCl3)δ8.23(br s,1H)、7.70(br s,1H)、6.78(s,1H)、5.90〜6.00(m,1H)、5.33〜5.38(m,1H)、5.24(dd,J=10.4,1.3Hz,1H)、4.63(m,2H)、4.12(q,J=7.1Hz,2H)4.05(t,J=6.6Hz,2H)、3.83(s,3H)、3.64〜3.72(m,1H)、3.02〜3.12(m,1H)、2.33(t,J=7.6Hz,2H)、1.84〜1.91(m,2H)、1.67〜1.74(m,10H)、1.66〜1.54(m,4H)、1.26(t,J=7.1Hz,3H);MS(ES+):m/z=507(M+H)+;LCMS(方法B):tR=3.70分。
1H NMR(400MHz,CDCl3)δ7.70〜7.72(m,1H)、7.09〜7.13(m,1H)、5.80〜5.98(m,1H)、5.25〜5.38(m,1H)、5.14〜5.19(m,2H)、4.63〜4.72(m,2H)、4.35〜4.50(m,1H)、4.13(q,J=7.1Hz,2H)、4.03〜4.08(m,1H)、3.96〜4.01(m,2H)、3.91(s,3H)、3.81〜3.83(m,1H)、3.45〜3.53(m,1H)、3.03〜3.10(m,1H)、2.33(t,J=7.6Hz,2H)、1.83〜1.90(m,2H)、1.62〜1.74(m,10H)、1.48〜1.53(m,2H);MS(ES+):m/z=505(M+H)+;LCMS(方法B):tR=3.57分。
1H NMR(400MHz,CDCl3)δ7.16(m,1H)、6.50(s,1H)、6.10(m,1H)、5.76〜5.81(m,1H)、5.03〜5.14(m,2H)、4.57〜4.69(m,2H)、4.37〜4.49(m,1H)、4.26〜4.34(m,1H)、4.12(q,J=7.1Hz,2H)、3.94〜4.01(m,3H)、3.90(s,3H)、3.62〜3.68(m,1H)、3.46〜3.68(m,2H)、3.03〜3.12(m,1H)、2.33(t,J=7.4Hz,2H)、1.66〜1.89(m,11H)、1.47〜1.57(m,6H)、1.25(t,J=7.1Hz,3H);MS(ES+):m/z=589(M+H)+;LCMS(方法B):tR=4.32分。
1H NMR(400MHz,CDCl3)δ7.18(s,1H)、6.19(s,1H)、5.99〜6.19(m,1H)、5.71〜5.81(m,1H)、5.02〜5.12(m,2H)、4.51〜4.67(m,1H)、4.36〜4.48(m,1H)、4.23〜4.31(m,1H)、3.88〜4.00(m,7H)、3.46〜3.66(m,2H)、3.02〜3.12(m,1H)、2.36(t,J=7.4Hz,2H)、1.79〜1.81(m,2H)、1.65〜1.75(m,10H)、1.49〜1.55(m,7H);MS(ES+):m/z=561(M+H)+;LCMS(方法B):tR=3.78分。
MS (ES+):m/z=453(M+H)+;LCMS(方法B):tR=4.07分。
MS (ES+):m/z=353(M+H)+;LCMS(方法B):tR=2.88分。
MS (ES+):m/z=896(M+H)+;LCMS(方法B):tR=4.25分。
MS (ES+):m/z=882(M+H)+;LCMS(方法B):tR=3.92分。
MS (ES+):m/z=972(M+H)+;LCMS(方法B):tR=3.55分。
1H NMR(DMSO−d6,400MHz)δ9.81〜9.85(m,1H)、9.58(s,1H)、9.51(s,2H)、8.00(d,J=5.7Hz,1H)、7.69〜7.72(m,2H)、7.47〜7.49(m,2H)、7.38〜7.43(m,1H)、7.30〜7.35(m,2H)、7.18〜7.24(m,1H)、7.11〜7.13(m,1H)、7.07(s,1H)、6.94〜6.98(m,1H)、6.80(br s,1H)、6.63〜6.72(m,2H)、6.52〜6.54(m,1H)、3.95〜4.14(m,3H)、3.89(s,3H)、3.83(s,3H)、3.70(s,3H)、3.65〜3.69(m,1H)、3.17(d,J=5.2Hz,2H)、2.28(t,J=6.5Hz,2H)、1.72〜1.78(m,4H)、1.62〜1.68(m,4H)、1.42〜1.48(m,3H)13C NMR(DMSO−d6,100MHz)δ169.5,166.3、164.6、159.5、159.2、150.3、147.1、144.8、139.8、137.0、129.6、128.2、126.6、124.6、124.3、122.7、122.1、121.8、121.7、120.5、120.4、118.7、113.7、111.3、109.6、109.3、104.7、68.1、55.6、36.3、36.1、35.5、28.3、25.2、25.1、23.7、22.5、17.7;MS(ES+):m/z=785(M+H)+;LCMS(方法A):tR=3.08分。
MS (ES+):m/z=697(M+H)+;LCMS(方法B):tR=3.98分。
MS (ES+):m/z=683(M+H)+;LCMS(方法B):tR=3.68分。
MS (ES+):m/z=773(M+H)+;LCMS(方法B):tR=3.27分。
1H NMR(DMSO−d6,400MHz)δ9.78(s,1H)、9.48(s,1H)、8.00(d,J=5.7Hz,1H)、7.32(d,J=8.8Hz,2H)、7.25(s,1H)、7.17(d,J=1.8Hz,1H)、6.82(d,J=1.9Hz,1H)、6.79(s,1H)、6.56(d,J=8.6Hz,2H)、4.13(dd,J=5.7,3.4Hz,5H)、3.80(s,3H)、3.79(s,3H)、3.17(s,1H)、3.07〜3.11(m,1H)、2.26(t,J=7.2Hz,3H)、1.75(dd,J=13.8,7.0Hz,6H)、1.60〜1.65(m,5H);MS(ES+):m/z=587(M+H)+;LCMS(方法B):tR=2.72分、MS(ES+):m/z=587(M+H)+;LCMS(方法A):tR=5.23分。
MS (ES+):m/z=896(M+H)+;LCMS(方法B):tR=3.12分。
1H NMR(DMSO−d6,400MHz)δ10.01(s,1H)、9.84(s,1H)、9.21(br s,2H)、8.41(s,1H)、8.01(d,J=5.7Hz,1H)、7.70(d,J=8.8Hz,2H)、7.44(d,J=8.7Hz,2H)、7.38(d,J=1.8Hz,1H)、7.31(d,J=1.9Hz,1H)、7.27(s,1H)、7.22(d,J=1.8Hz,1H)、6.98(d,J=1.8Hz,1H)、6.80(s,1H)、4.09〜4.19(m,2H)、3.99〜4.05(m,2H)、3.87(s,3H)、3.82(m,6H)、3.65〜3.72(m,2H)、3.45〜3.50(m,2H)、3.16(d,J=5.3Hz,3H)、2.96(t,J=5.8Hz,2H)、2.45(t,J=7.4Hz,2H)、2.00〜2.09(m,4H);(DMSO−d6,100MHz)δ203.1、168.8、166.3、164.7、161.6、159.6、150.2、147.1、139.8、137.0、129.5、125.9、124.2、122.0、120.6、120.4、111.2、109.8、109.3、98.8、95.4、85.9、78.8、71.0、67.7、55.6、49.2、48.5、36.3、31.8、30.2、24.7、22.5、17.7;MS(ES+):m/z=709(M+H)+;LCMS(方法B):tR=2.80分、MS(ES+):m/z=709(M+H)+;LCMS(方法A):tR=5.38分。
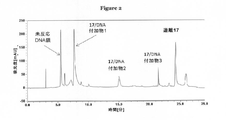
C8で連結したPDDモノマーと二重鎖転写因子コンセンサス配列との相互作用を、X-bridge MS C18 2.5μM OSTカラム(2.3×50mm)並びに移動相として、0.5mL/分の流量で40%のアセトニトリル/水及び100mMのTEAB(テトラエチルアンモニウムブロミド(TEAB,Tetraethylammonium bromide))/水の勾配並びに254nmにおけるUV検出を利用するHPLCアッセイを用いて研究した。1mMのストック溶液を形成するために、1Mの酢酸アンモニウムに溶解されたそれぞれの一本鎖オリゴヌクレオチドに関して、4:1のモル比のリガンド:オリゴヌクレオチドを使用した。オリゴヌクレオチドを、最初に、その1mM溶液を70℃まで10分間加熱し、続いて、8時間かけて徐々に冷却し、−20℃で終夜保存することによってアニーリングした。次いで、25μMのオリゴヌクレオチドの使用液を、アニーリングしたストック溶液を100mMの酢酸アンモニウムで希釈することによって調製した。リガンドをDMSOに溶解し、10mMのストック溶液を形成し、これを−20℃で4カ月以内の間保存した。100μMの薬物の使用液を、ストック溶液を100mMの酢酸アンモニウムで希釈することによって調製した。リガンドの使用液を室温でオリゴヌクレオチドの使用液に添加し、混合物を室温で異なる時間間隔でインキュベートした。
FRETアッセイに使用されるオリゴヌクレオチド配列は、Eurogentec社、Southampton、UKから購入した:TAMRA(6−カルボキシテトラメチルローダミン)及びFAM(6−カルボキシフルオレセイン)は、それぞれ、アクセプターとドナーフルオロフォアである。20μMのストック溶液から、400nMのFRET緩衝液中の溶液(50mMのカリウム、50mMのカコジル酸、pH7.4として最適化)を使用前に調製した。試料を90℃まで10分間加熱し、続いて、室温まで冷却し、この温度で5時間保存することにより、オリゴヌクレオチドをアニーリングした。FRET緩衝液を使用して、最初の5mMのDMSOストック溶液からの希釈を実施した。アニーリングしたDNA(50μL)及び試料溶液(50μL)を96ウェルプレート(MJ Research社、Waltham、MA)の各ウェルに添加し、DNA Engine Opticon(MJ Research社)で処理した。蛍光読み取りは、各読み取り前に30秒間温度を一定に維持して、30〜100℃の範囲にわたって0.5℃の間隔で行った。450〜495nmの入射照射を使用して、515〜545nmで検出した。生データをプログラムOrigin(バージョン7.0、OringinLab社)にインポートし、10点移動平均を使用してグラフを平滑化し、次いで、標準化した。融解温度の決定はスクリプトを使用して平滑化した融解曲線の一次微分の最大における値に基づいて行った。各試料の融解温度とブランクの融解温度の間の差(ΔTm)を比較目的で使用した。
細胞培養
アメリカ合衆国培養細胞系統保存機関(the American Type Culture Collection)からMDA MB231(トリプルネガティブヒト乳がん)を得た。細胞株を、加湿した5%CO2雰囲気下、37℃で、75cm2フラスコ(TPP社、Switzerland)中の単層培養で維持した。MDA MB231細胞株を、高グルコースDMEM(4.5g\l;Invitrogen社)、ウシ胎仔血清(10%、Biosera UK社)、非必須アミノ酸(1×;Invitrogen社)、L−グルタミン(2mM;Invitrogen社)及びペニシリン−ストレプトマイシン(1%v/v、Invitrogen社)中で維持した。ウシ胎仔血清(10%v/v、Invitrogen社)、L−グルタミン(2mM;Invitrogen社)、非必須アミノ酸(1×;Invitrogen社)及びペニシリン−ストレプトマイシン(1%v/v、Invitrogen社)を補充したダルベッコ改変イーグル培地(DMEM,Dulbecco’s Modified Eagles Media;Invitrogen社)でHeLa細胞株を維持した。継代するために、細胞をPBS(GIBCO 14040、Invitrogen社、UK)で洗浄し、トリプシン(GIBCO 25300、Invitrogen社、UK)でインキュベートし、新鮮な培地に再度播種した。播種のために、PBSで洗浄し、トリプシン処理し、8℃において8000rpmで5分間遠心分離し、新鮮な培地に再懸濁した細胞の非接着懸濁液において、顕微鏡検査(Nikon社、USA)によるNeubauer血球計算器(Assistant社、Germany)を使用して細胞をカウントした。
37℃で、5%CO2加湿雰囲気下、適当な培地を使用して、標準細胞培養条件で、細胞を増殖させた。細胞数を105細胞/mlに調整し、細胞株により1ウェル当たり5,000〜20,000個の細胞を添加した。細胞を24時間インキュベートし、三連で、適当な阻害剤濃度の1μlをウェルに添加した。各化合物に72時間連続して曝露した後、3−(4,5−ジメチルチアゾール−2−イル)−2,5−ジフェニルテトラゾリウムブロミド(MTT)(Lancaster Synthesis社、UK)比色アッセイを使用して、細胞毒性を決定した[34]。λ=570nmの分光光度法により吸光度を定量した(Envision Plate Reader、PerkinElmer社、USA)。GraphPad Prism(登録商標)ソフトウェアを使用する用量応答分析により、IC50値を計算した。
1. Antonow, D., and Thurston, D. E. (2011) Chem Rev 111, 2815-2864.
2. Cipolla, L., Araujo, A. C., Airoldi, C., and Bini, D. (2009) Anticancer Agents Med Chem 9, 1-31.
3. Gerratana, B. (2012) Med Res Rev 32, 254-293.
4. Hartley, J. A. (2011) Expert Opin Investig Drugs 20, 733-744.
5. Kamal, A., Reddy, K. L., Devaiah, V., Shankaraiah, N., and Reddy, D. R. (2006) Mini Rev Med Chem 6, 53-69.
6. Hurley, L. H., Reck, T., Thurston, D. E., Langley, D. R., Holden, K. G., Hertzberg, R. P., Hoover, J. R., Gallagher, G., Jr., Faucette, L. F., Mong, S. M., (1988) Chem Res Toxicol 1, 258-268.
7. Wells, G., Martin, C. R., Howard, P. W., Sands, Z. A., Laughton, C. A., Tiberghien, A., Woo, C. K., Masterson, L. A., Stephenson, M. J., Hartley, J. A., Jenkins, T. C., Shnyder, S. D., Loadman, P. M., Waring, M. J., and Thurston, D. E. (2006) J Med Chem 49, 5442-5461.
8. Brucoli, F., Hawkins, R. M., James, C. H., Jackson, P. J., Wells, G., Jenkins, T. C., Ellis, T., Kotecha, M., Hochhauser, D., Hartley, J. A., Howard, P. W., and Thurston, D. E. (2013) J Med Chem 56, 6339-6351.
9. Kotecha, M., Kluza, J., Wells, G., O'Hare, C. C., Forni, C., Mantovani, R., Howard, P. W., Morris, P., Thurston, D. E., Hartley, J. A., and Hochhauser, D. (2008) Mol Cancer Ther 7, 1319-1328.
10. Puvvada, M. S., Hartley, J. A., Jenkins, T. C., and Thurston, D. E. (1993) Nucleic Acids Res 21, 3671-3675.
11. Clingen, P. H., De Silva, I. U., McHugh, P. J., Ghadessy, F. J., Tilby, M. J., Thurston, D. E., and Hartley, J. A. (2005) Nucleic Acids Res 33, 3283-3291.
12. Puvvada, M. S., Forrow, S. A., Hartley, J. A., Stephenson, P., Gibson, I., Jenkins, T. C., and Thurston, D. E. (1997) Biochemistry 36, 2478-2484.
13. Barkley, M. D., Cheatham, S., Thurston, D. E., and Hurley, L. H. (1986) Biochemistry 25, 3021-3031.
14. Seifert, J., Pezeshki, S., Kamal, A., and Weisz, K. (2012) Organic & Biomolecular Chemistry 10, 6850-6860.
15. Smellie, M., Bose, D. S., Thompson, A. S., Jenkins, T. C., Hartley, J. A., and Thurston, D. E. (2003) Biochemistry 42, 8232-8239.
16. Kopka, M. L., Goodsell, D. S., Baikalov, I., Grzeskowiak, K., Cascio, D., and Dickerson, R. E. (1994) Biochemistry 33, 13593-13610.
17. Kizu, R., Draves, P. H., and Hurley, L. H. (1993) Biochemistry 32, 8712-8722.
18. Leimgruber, W., Stefanovic, V., Schenker, F., Karr, A., and Berger, J. (1965) J Am Chem Soc 87, 5791-5793.
19. Arima, K., Kosaka, M., Tamura, G., Imanaka, H., and Sakai, H. (1972) J Antibiot (Tokyo) 25, 437-444.
20. Sato, S., Iwata, F., Yamada, S., Kawahara, H., and Katayama, M. (2011) Bioorg Med Chem Lett 21, 7099-7101.
21. Thurston D.E. and Bose D.S., Chem Rev (1994); 94:433-465.
22. Damayanthi, Y., et al.; Journal of Organic Chemistry (1999), 64, 290-292;
23. Kumar, et al., Heterocyclic Communications (2002) 8, 19-26.
24. Kumar, R, Lown, J. W.; Oncology Research, (2003) 13, 221-233.
25. Baraldi, P. G. et al., Journal of Medicinal Chemistry (1999) 42, 5131-5141.
26. Wells, G., et al., Proc. Am. Assoc. Canc. Res. (2003) 44, 452.
27. Thurston, D. E.; Howard, P. W. WO 2004/043963.
28. Bose, D. S., Thompson, A. S., Ching, J. S., Hartley, J. A., Berardini, M.D., Jenkins, T. C., Neidele, S., Hurley, L. H., and Thurston, D. E. (1992) J. Am. Chem. Soc. 114, 4939.
29. Wu, J., Clingen, P. H., Spanswick, V. J., Mellinas-Gomez, M., Meyer, T., Puzanov, I., Jodrell, D., Hochhauser, D., and Hartley, J. A. (2013) Clin Cancer Res 19, 721-730.
30. Jenkins, T. C., Hurley, L. H., Neidle, S., and Thurston, D. E. (1994) J Med Chem 37, 4529-4537.
31. Hochhauser, D., Meyer, T., Spanswick, V. J., Wu, J., Clingen, P. H., Loadman, P., Cobb, M., Gumbrell, L., Begent, R. H.,Hartley, J. A., Jodrell, D., (2009) Clin Cancer Res 15, 2140-2147.
Claims (17)
- 式(I)の化合物:
式中、
点線は、C1とC2、C2とC3、及びC3とC4の1つ又は2つ以上の間に二重結合が存在していてもよいことを示し;
R1は、R7、=CH2、=CH−(CH2)m−CH3、=O、(CH2)m−OR7、(CH2)m−CO2R7、(CH2)m−NR7R8、O−(CH2)n−NR7R8、NH−C(O)−R7、O−(CH2)n−NH−C(O)−R7、O−(CH2)n−C(O)−NH−R7、(CH2)m−SO2R7、O−SO2R7、(CH2)m−C(O)R7、及び(CH2)m−C(O)NR7R8から選択され;
R2は、R9、CH2、=CH−(CH2)m−CH3、=O、(CH2)r−OR9、(CH2)r−CO2R9、(CH2)r−NR9R10、O−(CH2)s−NR9R10、NH−C(O)−R9、O−(CH2)s−NH−C(O)−R9、O−(CH2)s−C(O)−NH−R9、(CH2)r−SO2R9、O−SO2R9、(CH2)r−COR9、及び(CH2)r−C(O)NR9R10から選択され;
R3は、H、C1−12アルキル、及びCH2Phから選択され;
R4は、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、C(=O)−NH−R24、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよい、フェニル及びC5−9ヘテロアリール基から選択され;ただし、置換されていてもよい前記C5−9ヘテロアリールは、インドリルではないことを条件とし;
R19は、H及び(CH2)t−NR20R21から選択され;
Y1は、N又はCHであり;
Y2は、N又はCHであり;Y1及びY2の少なくとも一方は、CHであり;
pは、0又は1であり;
j、m、r、及びtは独立して、0〜6の整数から選択され;
k、n、及びsは独立して、1〜6の整数から選択され;
X1は、O、S、NR13、CR13R14、CR13R14O、C(=O)、C(=O)NR13、NR13C(=O)、O−C(O)、及びC(O)−Oから選択され;
Lは、アミノ酸、2〜6個のアミノ酸を有するペプチド鎖、1つ又は2つ以上の炭素−炭素二重結合又は三重結合を含有し得る1〜12個の炭素原子を含有するアルキレン鎖、パラホルムアルデヒド鎖−(OCH2)1−12−、及びポリエチレングリコール鎖−(OCH2CH2)1−6−から選択され、これらの鎖は、O、S、及び/若しくはNH基、並びに/又はC5−9ヘテロアリーレン、並びに/又はフェニレンの1つ又は2つ以上により中断されていてもよく;
X2は、O、S、NR15、CR15R16、CR15R16O、C(=O)、C(=O)NR15、NR15C(=O)、O−C(O)、及びC(O)−Oから選択されるか、又は存在せず;
qは、1であり;
Aは:
各A1基について、Y3及びY4の一方は独立して、N−R17、S、及びOから選択され;Y3及びY4の他方は、CHであり;Y5は独立して、CH、N、S、及びCOHから選択され;
各A2基について、Y6及びY7の一方は独立して、N及びCHから選択され;Y6及びY7の他方は、CHであり;
R7及びR9は独立して、H、C1−12アルキル、C5−9ヘテロアリール、C6−15ヘテロアリールアルキル、フェニル、及びC7−12アラルキル基から選択され;前記ヘテロアリール、ヘテロアリールアルキル、フェニル、及びアラルキル基は、C1−6アルキル、OH、及びOC1−6アルキルから選択される最大3個の任意の置換基で置換されていてもよく;
R24は、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよいフェニルであり;
R8、R10、R11、R12、R13、R14、R15、R16、R17、R20、及びR21は独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6は一緒になって二重結合を形成するか;
(ii)R5はHであり、かつR6はOHであるか;又は
(iii)R5はHであり、かつR6はOC1−6アルキルであるか
のいずれかであり;
ただし、pが0であり、かつAがA1である場合:
(a)少なくとも1つのA1基について、Y3及びY4の1つは、S及びOから選択されるか;若しくは
(b)少なくとも1つのA1基について、Y5は、Sであるか;又は
(c)R4は、ピロリル、イミダゾリル、置換されていてもよいピロリル、若しくは置換されていてもよいイミダゾリルではないこと
を条件とする、前記式(I)の化合物又はその塩若しくは溶媒和物。 - R24が、−C6H4−(CH2)j−R18であり、R18が、CO2R11及びNR11R12から選択される、請求項1に記載の式(I)の化合物又はその塩若しくは溶媒和物。
- R1が、R7、O−(CH2)n−NH−C(O)−R7、及びO−(CH2)n−C(O)−NH−R7から選択される、請求項1又は2に記載の式(I)の化合物又はその塩若しくは溶媒和物。
- R2が、Hである、請求項1〜3のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物。
- R3が、メチル及びエチルから選択される、請求項1〜4のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物。
- R4が、OH、C1−6アルキル、OC1−6アルキル、(CH2)j−CO2R11、O−(CH2)k−NR11R12、(CH2)j−NR11R12、C(=O)−NH−(CH2)k−NR11R12、C(=O)−NH−C6H4−(CH2)j−R18、及びC(=O)−NH−(CH2)k−C(=NH)NR11R12から選択される最大3個の任意の置換基で置換されていてもよい、フェニル、ピロリル、N−メチルピロリル、フラニル、チオフェニル、イミダゾリル、N−メチルイミダゾリル、オキサゾリル、チアゾリル、ピリジル、ベンゾフラニル、ベンゾチオフェニル、ベンズイミダゾリル、N−メチルベンゾイミダゾリル、ベンゾオキサゾリル、及びベンゾチアゾリルから選択される、請求項1〜5のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物。
- R5及びR6が、一緒になって二重結合を形成する、請求項1〜7のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物。
- 化合物が、以下の構造:
式中、qが、1であり;
pが、0又は1であり;
Lが、1〜12個の炭素原子を含有するアルキレン鎖であり;
Y1が、N又はCHであり;
Y2が、N又はCHであり;Y1及びY2の少なくとも一方が、CHであり;
Y5が、CH及びNから選択され;
Z1が、O、S、NH、及びN−CH3から選択され;
Z2が、CH及びNから選択され;
Z3が、S及びOから選択され;
Z4が、CH及びNから選択され;
R22が、(CH2)jCO2H、(CH2)jCO2C1−6アルキル、(CH2)jNR11R12、及びC(=O)−NH−C6H4−(CH2)j−R18から選択され;
R18が、CO2R11及びNR11R12から選択され;
R19が、H及び(CH2)t−NR20R21から選択され;
j及びtが独立して、0〜6の整数から選択され;
R11、R12、及びR23が独立して、H及びC1−6アルキルから選択され;
(i)R5及びR6が一緒になって二重結合を形成するか;
(ii)R5がHであり、かつR6がOHであるか;又は
(iii)R5がHであり、かつR6がOC1−6アルキルであるか
のいずれかであり;
ただし、前記化合物が(XVI)であり、かつpが0である場合、Z1が、O及びSから選択されることを条件とする、請求項1〜9のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物。 - (a)メチル(S)−5−(4−(4−((2−メトキシ−12−オキソ−6a,7,8,9,10,12−ヘキサヒドロベンゾ[e]ピリド−[1,2−a][1,4]ジアゼピン−3−イル)オキシ)ブタンアミド)−1−メチル−1H−ピロール−2−カルボキサミド)ベンゾ−[b]チオフェン−2−カルボキシレート(13)
(m)(S)−N−(2−アミノエチル)−4−(4−(4−(4−((2−メトキシ−12−オキソ−6a,7,8,9,10,12−ヘキサヒドロ−ベンゾ[e]ピリド[1,2−a][1,4]ジアゼピン−3−イル)オキシ)ブタンアミド)−1−メチル−1H−ピロール−2−カルボキサミド)フェニル)−1−メチル−1H−ピロール−2−カルボキサミド(68)
- 請求項1〜11のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物を含む、医薬。
- 請求項1〜11のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物を含む、増殖性疾患の治療剤。
- 増殖性疾患が、膀胱がん、骨がん、腸がん、脳がん、乳がん、子宮頸がん、結腸がん、頭頸部がん、白血病、肝臓がん、肺がん、リンパ腫、黒色腫、食道がん、口腔がん、卵巣がん、膵臓がん、前立腺がん、直腸がん、腎がん、網膜芽細胞腫、肉腫、皮膚がん、胃がん、精巣がん、甲状腺がん、及び子宮がんから選択される、請求項13に記載の治療剤。
- 請求項1〜11のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物と、薬学的に許容される賦形剤、担体、又は希釈剤とを含む医薬組成物。
- 増殖性疾患の治療のための医薬の製造における、請求項1〜11のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物の使用。
- 標的化コンジュゲートを提供するために、標的化剤に直接的又は間接的に結合した、請求項1〜11のいずれかに記載の式(I)の化合物又はその塩若しくは溶媒和物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021103836A JP2021152063A (ja) | 2015-08-21 | 2021-06-23 | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1514928.9 | 2015-08-21 | ||
| GBGB1514928.9A GB201514928D0 (en) | 2015-08-21 | 2015-08-21 | PDD compounds |
| PCT/GB2016/052565 WO2017032983A1 (en) | 2015-08-21 | 2016-08-19 | Piperidinobenzodiazepine compounds with anti proliferative activity |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021103836A Division JP2021152063A (ja) | 2015-08-21 | 2021-06-23 | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018525405A JP2018525405A (ja) | 2018-09-06 |
| JP2018525405A5 JP2018525405A5 (ja) | 2019-09-26 |
| JP6903635B2 true JP6903635B2 (ja) | 2021-07-14 |
Family
ID=54292043
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018509597A Active JP6903635B2 (ja) | 2015-08-21 | 2016-08-19 | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
| JP2021103836A Ceased JP2021152063A (ja) | 2015-08-21 | 2021-06-23 | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021103836A Ceased JP2021152063A (ja) | 2015-08-21 | 2021-06-23 | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US10975072B2 (ja) |
| EP (2) | EP4086251A1 (ja) |
| JP (2) | JP6903635B2 (ja) |
| KR (1) | KR20180043314A (ja) |
| CN (2) | CN108602803A (ja) |
| AU (1) | AU2016313228B2 (ja) |
| CA (1) | CA2996406A1 (ja) |
| DK (1) | DK3337795T3 (ja) |
| EA (1) | EA201890539A1 (ja) |
| GB (1) | GB201514928D0 (ja) |
| IL (1) | IL257650B (ja) |
| MX (1) | MX2018002242A (ja) |
| WO (1) | WO2017032983A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021152063A (ja) * | 2015-08-21 | 2021-09-30 | フェムトジェニックス リミテッドFemtogenix Limited | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201510010D0 (en) | 2015-06-09 | 2015-07-22 | King S College London | PDD and BPD compounds |
| US20180339985A1 (en) * | 2015-08-21 | 2018-11-29 | Femtogenix Limited | Pdd compounds |
| TW201808936A (zh) | 2016-05-18 | 2018-03-16 | 美商梅爾莎納醫療公司 | 吡咯并苯并二氮呯類及其共軛物 |
| US10526294B2 (en) | 2016-06-24 | 2020-01-07 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepines and conjugates thereof |
| WO2019104289A1 (en) | 2017-11-27 | 2019-05-31 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepine antibody conjugates |
| GB201814281D0 (en) * | 2018-09-03 | 2018-10-17 | Femtogenix Ltd | Cytotoxic agents |
| GB2597532A (en) | 2020-07-28 | 2022-02-02 | Femtogenix Ltd | Cytotoxic compounds |
Family Cites Families (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5841878A (ja) * | 1981-09-07 | 1983-03-11 | Fujisawa Pharmaceut Co Ltd | ベンゾジアゼピン誘導体、その製法およびそれを有効成分として含有する抗がん剤 |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US5366972A (en) | 1989-04-20 | 1994-11-22 | Boehringer Ingelheim Pharmaceuticals, Inc. | 5,11-dihydro-6H-dipyrido(3,2-B:2',3'-E)(1,4)diazepines and their use in the prevention or treatment of HIV infection |
| US5418229A (en) | 1990-01-06 | 1995-05-23 | Alker; David | Muscarinic receptor antagonists |
| WO1993013777A1 (en) | 1992-01-21 | 1993-07-22 | Merck & Co., Inc. | Method of using m1-selective antimuscarinic pyridobenzodiazepinones in axial myopia therapy |
| EP1120416A1 (en) | 1993-04-05 | 2001-08-01 | Pharmaceutical Discovery Corporation | Pyrido[2.3-b][1,4]benzodiazepinones as M2 receptor ligand for the treatment of neurological disorders |
| WO1996038422A1 (fr) | 1995-05-31 | 1996-12-05 | Yamanouchi Pharmaceutical Co., Ltd. | Derives condenses de benzodiazepinone et composition pharmaceutique les ayant pour base |
| US5650409A (en) | 1995-06-02 | 1997-07-22 | Cortex Pharmaceuticals, Inc. | Benzoyl piperidines/pyrrolidines for enhancing synaptic response |
| ES2275313T3 (es) | 1997-08-22 | 2007-06-01 | Kaken Pharmaceutical Co., Ltd. | Derivados de amida como promotores de la liberacion de la hormona del crecimiento. |
| EP1193270B1 (en) | 1998-08-27 | 2003-05-14 | Spirogen Limited | Pyrrolobenzodiazepines |
| US6608193B2 (en) | 2001-12-21 | 2003-08-19 | The Procter & Gamble Company | Methods for synthesis of amino-tetrahydroisoquinoline ring compounds |
| US7384934B2 (en) | 2002-08-05 | 2008-06-10 | Eli Lilly And Company | Piperazine substituted aryl benzodiazepines |
| GB0226593D0 (en) | 2002-11-14 | 2002-12-24 | Consultants Ltd | Compounds |
| US7456169B2 (en) | 2003-02-27 | 2008-11-25 | Abbott Laboratories Inc. | Heterocyclic kinase inhibitors |
| AU2003223107A1 (en) | 2003-03-31 | 2004-10-25 | Council Of Scentific And Industrial Research | Pyrene-linked pyrrolo (2,1-c) (1,4) benzodiazepine derivatives useful as anticancer agents |
| GB0308335D0 (en) | 2003-04-10 | 2003-05-14 | Novartis Ag | Organic compounds |
| GB0404578D0 (en) | 2004-03-01 | 2004-04-07 | Spirogen Ltd | Pyrrolobenzodiazepines |
| ES2604197T3 (es) | 2004-06-01 | 2017-03-03 | University Of Virginia Patent Foundation | Inhibidores dobles de molécula pequeña de cáncer y angiogénesis |
| WO2006008118A1 (en) | 2004-07-16 | 2006-01-26 | Proteosys Ag | Muscarinic antagonists with parp and sir modulating activity as cytoprotective agents |
| NZ580115A (en) | 2004-09-23 | 2010-10-29 | Genentech Inc | Cysteine engineered antibody light chains and conjugates |
| IT1362675B (it) | 2005-03-15 | 2009-06-25 | Menarini Internat Operations Luxembourg Sa | N-idrossiammidi -sostituiti con gruppi triciclici come inibitori dell'istone deacelitasi,loro preparazione ed impiego in formulazioni farmaceutiche |
| DE602006006199D1 (de) | 2005-10-05 | 2009-05-20 | Spirogen Ltd | 4-ä4-(5-oxo-2,3,5,11a-tetrahydro-5h-pyrrolo ä2, 1-cüä1,4übenzodiazepin-8-yloxy)-butyrylaminoü-1h-pyrrol-2-carbonsäurealkylesterderivate und verwandte verbindung zur behandlung einer proliferativen erkrankung |
| WO2008007661A1 (fr) | 2006-07-11 | 2008-01-17 | Takeda Pharmaceutical Company Limited | Composé hétérocyclique tricycique et son utilisation |
| CA2660799C (en) * | 2006-08-14 | 2013-03-19 | Council Of Scientific & Industrial Research | Pyrrolo[2,1-c][1,4]benzodiazepine hybrids and a process for the preparation thereof |
| EP2144628B1 (en) | 2007-05-08 | 2012-10-17 | Genentech, Inc. | Cysteine engineered anti-muc16 antibodies and antibody drug conjugates |
| MX2010003718A (es) | 2007-10-19 | 2010-04-21 | Genentech Inc | Anticuerpos anti-tenb2 producidos por ingenieria de cisteina y conjugados de farmaco y anticuerpo. |
| JP2009263283A (ja) | 2008-04-25 | 2009-11-12 | Toray Ind Inc | C型肝炎ウイルス阻害剤 |
| BRPI0914927B8 (pt) | 2008-06-17 | 2021-05-25 | Astrazeneca Ab | composto, composição farmacêutica e uso de um composto |
| GB0819095D0 (en) | 2008-10-17 | 2008-11-26 | Spirogen Ltd | Pyrrolobenzodiazepines |
| US20110263574A1 (en) | 2009-01-13 | 2011-10-27 | Proteosys Ag | Pirenzepine as otoprotective agent |
| IL271761B (en) | 2009-02-05 | 2022-09-01 | Immunogen Inc | (12as)-8-methoxy-9-benzyloxy-11,12,12a,13-tetrahydro-6h-indolo[2,1-c][1,4]benzodiazepine-6-one, 4-benzyloxy-5-methoxy -2-nitrobenzoic acid and a process for their preparation |
| ES2568262T3 (es) | 2009-04-23 | 2016-04-28 | Abbvie Inc. | Moduladores de receptores de 5-HT y sus métodos de uso |
| DE102009033392A1 (de) | 2009-07-16 | 2011-01-20 | Merck Patent Gmbh | Heterocyclische Verbindungen als Autotaxin-Inhibitoren II |
| CU20090172A6 (es) | 2009-10-09 | 2011-10-05 | Facultad De Quimica Universidad De La Habana | Sistemas tricíclicos y tetracíclicos con actividad sobre el sistema nervioso central y vascular |
| WO2011117882A1 (en) | 2010-03-22 | 2011-09-29 | Council Of Scientific & Industrial Research | Pyrrolo[2,l-c][l,4]benzodiazepine-benzothiazole or benzoxazole conjugates linked through piperazine moiety and process for the preparation thereof |
| EP2632469A2 (en) | 2010-10-25 | 2013-09-04 | Merck Sharp & Dohme Corp. | Tricyclic mglur5 receptor modulators |
| RU2748733C2 (ru) | 2011-02-15 | 2021-05-31 | Иммуноджен, Инк. | Цитотоксические производные бензодиазепина |
| US9006233B2 (en) | 2011-04-28 | 2015-04-14 | Uwm Research Foundation, Inc. | Gabaergic receptor subtype selective ligands and their uses |
| MX369715B (es) | 2012-04-30 | 2019-11-20 | Ucl Business Plc | Pirrolobenzodiacepinas. |
| CN115124573A (zh) * | 2013-09-02 | 2022-09-30 | 杭州多禧生物科技有限公司 | 应用于细胞结合分子-药物共轭体的新型细胞毒性分子 |
| AU2014362238A1 (en) | 2013-12-13 | 2016-06-09 | Genentech, Inc. | Anti-CD33 antibodies and immunoconjugates |
| GB201407816D0 (en) | 2014-05-02 | 2014-06-18 | King S College London | Pyrrolobenzodiazepine Compounds |
| DK3191135T3 (da) | 2014-09-12 | 2020-10-12 | Genentech Inc | Anti-HER2-antistoffer og immunokonjugater |
| TW201632520A (zh) | 2014-11-25 | 2016-09-16 | 拜耳製藥股份有限公司 | 經取代之吡啶並苯並二氮呯酮衍生物及其用途 |
| EP3226689B1 (en) | 2014-12-05 | 2020-01-15 | Merck Sharp & Dohme Corp. | Novel tricyclic compounds as inhibitors of mutant idh enzymes |
| WO2016089797A1 (en) | 2014-12-05 | 2016-06-09 | Merck Sharp & Dohme Corp. | Novel tricyclic compounds as inhibitors of mutant idh enzymes |
| MX2017009144A (es) | 2015-01-14 | 2017-11-22 | Bristol Myers Squibb Co | Dimeros de benzodiazepina unidos con puentes de heteroarileno, conjugados de estos, y sus metodos de preparacion y uso. |
| US9504694B2 (en) | 2015-03-19 | 2016-11-29 | Cellerant Therapeutics, Inc. | Isoquinolidinobenzodiazepines |
| GB201510010D0 (en) * | 2015-06-09 | 2015-07-22 | King S College London | PDD and BPD compounds |
| GB201514928D0 (en) * | 2015-08-21 | 2015-10-07 | King S College London | PDD compounds |
| US10399972B2 (en) | 2015-10-29 | 2019-09-03 | Merck Sharp & Dohme Corp. | Tricyclic compounds as inhibitors of mutant IDH enzymes |
| TW201808936A (zh) | 2016-05-18 | 2018-03-16 | 美商梅爾莎納醫療公司 | 吡咯并苯并二氮呯類及其共軛物 |
| US10526294B2 (en) | 2016-06-24 | 2020-01-07 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepines and conjugates thereof |
| WO2018053552A2 (en) | 2016-09-19 | 2018-03-22 | Cellerant Therapeutics, Inc. | Isoquinolidinobenzodiazepines |
| WO2018075842A1 (en) | 2016-10-20 | 2018-04-26 | Bristol-Myers Squibb Company | Condensed benzodiazepine derivatives and conjugates made therefrom |
-
2015
- 2015-08-21 GB GBGB1514928.9A patent/GB201514928D0/en not_active Ceased
-
2016
- 2016-08-19 MX MX2018002242A patent/MX2018002242A/es unknown
- 2016-08-19 EP EP22178645.2A patent/EP4086251A1/en active Pending
- 2016-08-19 CA CA2996406A patent/CA2996406A1/en active Pending
- 2016-08-19 CN CN201680060201.8A patent/CN108602803A/zh active Pending
- 2016-08-19 KR KR1020187007849A patent/KR20180043314A/ko not_active Application Discontinuation
- 2016-08-19 DK DK16756759.3T patent/DK3337795T3/da active
- 2016-08-19 EA EA201890539A patent/EA201890539A1/ru unknown
- 2016-08-19 WO PCT/GB2016/052565 patent/WO2017032983A1/en active Application Filing
- 2016-08-19 JP JP2018509597A patent/JP6903635B2/ja active Active
- 2016-08-19 CN CN202210543524.XA patent/CN114907345A/zh active Pending
- 2016-08-19 AU AU2016313228A patent/AU2016313228B2/en active Active
- 2016-08-19 EP EP16756759.3A patent/EP3337795B1/en active Active
-
2018
- 2018-02-21 IL IL257650A patent/IL257650B/en unknown
- 2018-02-21 US US15/901,714 patent/US10975072B2/en active Active
-
2021
- 2021-06-23 JP JP2021103836A patent/JP2021152063A/ja not_active Ceased
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021152063A (ja) * | 2015-08-21 | 2021-09-30 | フェムトジェニックス リミテッドFemtogenix Limited | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20180043314A (ko) | 2018-04-27 |
| EP3337795A1 (en) | 2018-06-27 |
| MX2018002242A (es) | 2018-05-02 |
| CN114907345A (zh) | 2022-08-16 |
| DK3337795T3 (da) | 2022-07-25 |
| US20180291021A1 (en) | 2018-10-11 |
| AU2016313228B2 (en) | 2020-12-24 |
| WO2017032983A1 (en) | 2017-03-02 |
| EA201890539A1 (ru) | 2018-09-28 |
| CA2996406A1 (en) | 2017-03-02 |
| GB201514928D0 (en) | 2015-10-07 |
| EP4086251A1 (en) | 2022-11-09 |
| US10975072B2 (en) | 2021-04-13 |
| JP2021152063A (ja) | 2021-09-30 |
| EP3337795B1 (en) | 2022-06-22 |
| JP2018525405A (ja) | 2018-09-06 |
| CN108602803A (zh) | 2018-09-28 |
| AU2016313228A1 (en) | 2018-04-12 |
| IL257650A (en) | 2018-04-30 |
| IL257650B (en) | 2022-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6903635B2 (ja) | 抗増殖活性を有するピペリジノベンゾジアゼピン化合物 | |
| US10399970B2 (en) | Pyrridinobenzodiazepine and benzopyrridodiazecine compounds | |
| JP5116686B2 (ja) | Cc−1065類似体の調製方法及び調製用化合物 | |
| TW201930292A (zh) | 作為變構shp2抑制劑的吡啶、吡嗪和三嗪化合物 | |
| US9999625B2 (en) | Pyrrolobenzodiazepine compounds | |
| US11912700B2 (en) | Anti-proliferative agents comprising substituted benzo[e]pyrido[1,2-a][1,4]diazepines | |
| CN112638380A (zh) | 小脑蛋白(crbn)配体 | |
| TWI669300B (zh) | 嘧啶類衍生物、其製備方法、其藥物組合物以及其在醫藥上的用途 | |
| TWI712605B (zh) | 含有cti藥效基團之雙功能性細胞毒性劑 | |
| JP2019521975A (ja) | 抗egfr抗体薬物コンジュゲート | |
| WO2019189732A1 (ja) | 光学活性な架橋型環状2級アミン誘導体 | |
| US10550125B2 (en) | Prodrugs of imidazotriazine compounds as CK2 inhibitors | |
| JP2022529583A (ja) | 異常細胞増殖を阻害するまたは増殖性疾患を治療するための細胞毒性ビス-ベンゾジアゼピン誘導体及び細胞結合剤とのその複合体 | |
| EA040562B1 (ru) | Соединения пиперидинобензодиазепина, обладающие антипролиферативной активностью | |
| JP2019510054A (ja) | シクロフィリンの阻害のための化合物及びその使用 | |
| GB2567126A (en) | PBC compounds | |
| TW202328162A (zh) | 新穎的澳瑞他汀(auristatin)類似物及其免疫綴合物 | |
| TW202334176A (zh) | 新穎的澳瑞他汀(auristatin)類似物及其免疫綴合物 | |
| CN117255790A (zh) | 一类化学偶联连接子及其用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190815 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190815 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200630 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200831 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201119 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210225 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210524 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210623 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6903635 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |