JP6889824B2 - 生体適合性材料、コーティング組成物、コーティング膜及び物品 - Google Patents
生体適合性材料、コーティング組成物、コーティング膜及び物品 Download PDFInfo
- Publication number
- JP6889824B2 JP6889824B2 JP2017525289A JP2017525289A JP6889824B2 JP 6889824 B2 JP6889824 B2 JP 6889824B2 JP 2017525289 A JP2017525289 A JP 2017525289A JP 2017525289 A JP2017525289 A JP 2017525289A JP 6889824 B2 JP6889824 B2 JP 6889824B2
- Authority
- JP
- Japan
- Prior art keywords
- biocompatible material
- cells
- article
- coating
- vinyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L29/00—Materials for catheters, medical tubing, cannulae, or endoscopes or for coating catheters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L33/00—Antithrombogenic treatment of surgical articles, e.g. sutures, catheters, prostheses, or of articles for the manipulation or conditioning of blood; Materials for such treatment
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F214/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen
- C08F214/18—Monomers containing fluorine
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F226/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen
- C08F226/06—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen by a heterocyclic ring containing nitrogen
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M1/00—Apparatus for enzymology or microbiology
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M3/00—Tissue, human, animal or plant cell, or virus culture apparatus
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Microbiology (AREA)
- Surgery (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Sustainable Development (AREA)
- Polymers & Plastics (AREA)
- Dermatology (AREA)
- Vascular Medicine (AREA)
- Hematology (AREA)
- Virology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Heart & Thoracic Surgery (AREA)
- Cell Biology (AREA)
- Materials For Medical Uses (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Paints Or Removers (AREA)
- Application Of Or Painting With Fluid Materials (AREA)
- Laminated Bodies (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Medical Preparation Storing Or Oral Administration Devices (AREA)
Description
本発明のコーティング方法は、物品に生体適合性を与えるコーティング膜を形成することができる。
上記耐熱性は、次の方法により評価する。熱重量分析装置を用いて、上記フルオロポリマーを空気雰囲気下、10℃/minで600℃まで昇温する。一定重量部と重量減少部からそれぞれ接線を引き、交点を熱分解温度とする。
上記耐薬品性は、次の方法による重量減少率で評価する。上記重量減少率は、次の計算式により算出する値である。
重量減少率=100―(次亜塩素酸ナトリウム(NaClO)水溶液に浸漬した後のフルオロポリマーの重量)/(NaClO水溶液に浸漬させる前のフルオロポリマーの重量)×100
NaClO水溶液に浸漬した後の重量は、フルオロポリマー(サンプル)を、5000ppmのNaClOを含む水溶液(pH13となる様に水酸化ナトリウムを添加して調製する)に、20℃で168時間浸漬させた後、フルオロポリマーを回収し、60℃で15時間乾燥して得られるフルオロポリマーの重量である。
なお、サンプルは13質量%のフルオロポリマーを含むポリマー溶液から、直径約58mmのシャーレ上にキャスト成膜したフィルムを使用する。
上記重合性ビニル基としては、ビニル基、アリル基、ビニルエーテル基、ビニルエステル基、アクリル基等が挙げられる。
元素分析により測定した。
テトラフルオロエチレンとN−ビニルピロリドンの共重合体(1)の調製
気密検査済みの耐圧性反応容器内を十分に窒素置換した後、脱酸素処理したアセトン(752g)及びN−ビニルピロリドン(27.2g)を添加した。続いてテトラフルオロエチレン(100g)を加圧添加し、攪拌しながら混合物の内温を60℃となる様に調整した上で、t−ブチルパーオキシピバレート1.7gを加えて反応を開始した。反応開始から35分後、残存するテトラフルオロエチレンを除去し、精製、乾燥することで目的の共重合体(1)を15g得た。得られた共重合体(1)は、重量平均分子量6.4×104、分子量分布1.9、50モル%のテトラフルオロエチレン単位及び50モル%のN−ビニルピロリドン単位を含む共重合体であることが分かった。テトラフルオロエチレン単位/N−ビニルピロリドン単位のモル比は1であり、フッ素含有率は36質量%であった。
テトラフルオロエチレンとN−ビニルピロリドンの共重合体(2)の調製
気密検査済みの耐圧性反応容器内を十分に窒素置換した後、脱酸素処理したメチルイソブチルケトン(90.3g)及びN−ビニルピロリドン(9.80g)を添加した。続いてテトラフルオロエチレンを加圧添加し、スターラーで攪拌しながら混合物の内温を60℃となる様に調整した上で、アゾビスイソブチロニトリル(0.197g)を加えて反応を開始した。反応開始から1時間後、残存するテトラフルオロエチレンを除去し、ヒドロキノン(0.132g)を添加した。次いで反応混合物を精製、乾燥させ目的の共重合体(2)を3.3g得た。得られた共重合体(2)は、重量平均分子量6.5×104、分子量分布2.0、34モル%のテトラフルオロエチレン単位及び66モル%のN−ビニルピロリドン単位を含む共重合体であった。テトラフルオロエチレン単位/N−ビニルピロリドン単位のモル比は0.52であり、フッ素含有率は24質量%であった。
共重合体(1)の0.1質量%メタノール溶液を室温でPETコーティング済みQCMチップ(円盤状:直径1.4cm)の片側反応面へスピンコートした。具体的には、上記溶液30μLをPETコーティング済みQCMチップ上に滴下し、60秒間、2000rpm回転させた。その後、室温にて3時間、ロータリー真空ポンプにて減圧乾燥し、コーティング膜(QCMチップ)を得た。得られたコーティング膜をQCM−Dに組み込み、以下の方法でコーティング膜上のタンパク質吸着試験(ウシ血清アルブミン)を評価した。実験の結果を表2〜4に示す。
上記の方法でPETコーティング済みQCMチップに重ねて共重合体(1)をコーティングしたQCMチップをQCM−Dに装着させ、23.4℃環境下のリン酸緩衝生理食塩水(PBS)中で安定化を行った。
実施例1と同様にQCM−Dを用いて、表2〜4に記載したように、共重合体(1)または(2)について、ウシ血清アルブミン(BSA)またはウシ血漿フィブリノーゲン(BPF)およびグロブリン(IgG)の吸着を評価した。実験の結果を表2〜4に示す。
ポリエチレンテレフタレート(PET)の1.0質量%溶液(トリフルオロ酢酸、ジクロロメタンと1,1,2,2−テトラクロロエタンの混合溶剤(混合比1/4/45)に溶解させたもの)を室温でQCMチップ(円盤状:直径1.4cm)の片側反応面へスピンコートした。具体的には、上記溶液30μLをQCMチップ上に滴下し、60秒間、2000rpm回転させた。その後、50℃にて3時間以上、ロータリー真空ポンプにて減圧乾燥し、コーティング膜を得た。
得られたコーティング膜について実施例1〜6と同様にタンパク質の吸着試験を実施した。実験の結果を表2〜4に示す。
共重合体(1)の0.1質量%メタノール溶液を室温でPETフィルム(1cm×1cm)上へスピンコートした。具体的には、上記溶液30μLをPETフィルム上に滴下し200rpmで10秒間回転した。その後、室温にて、ロータリー真空ポンプにて減圧乾燥し、コーティング膜を得た。さらにこのコーティングされたPETフィルムを0.5cm×0.5cmにカットしコーティング膜(PETフィルムの表面に形成されたコーティング膜)を得た。得られたコーティング膜について、以下の方法で抗血栓性(30分間)を評価した。結果を表5に示す。
得られたコーティング膜を直径3.3cmの秤量瓶の底に少量のシリコン接着剤で固定した。これを純水で3回洗浄後、リン酸塩緩衝生理食塩液(PBS)に12時間浸漬した。PBSを除いた後、PBSで3倍希釈した0.1%クエン酸ナトリウムを含む多血小板血漿(PRP、血小板数:2×105個/μL)を上記秤量瓶に2.0mL加え、37℃で30分間静置した。PRPを除き、PBSでコーティング膜を3回洗浄した。2%グルタルアルデヒドを含むPBSを加え4℃で2時間静置し、コーティング膜表面に粘着した血小板を固定化した。サンプルをPBSで3回、純水で1回洗浄し、1晩減圧乾燥を行った。得られたサンプルを金スパッタ装置で金コートし、走査型電子顕微鏡を用いてコーティング膜表面を倍率400倍で5視野任意に観察し、粘着した血小板数をカウントした。粘着した血小板の活性化が抑制され血小板形態が球状の場合(−)、わずかに偽足化または偏平化の場合(±)、明らかな偽足化または偏平化の場合(+)、明らかな偽足化または偏平化があり血小板同士の凝集が認められた場合(++)とした。
実施例7と同様の方法で共重合体(2)のコーティング膜を得た。得られたコーティング膜について実施例7と同様の方法で抗血栓性(30分間)を評価した。結果を表5に示す。
実施例7で用いたものと同様のPETフィルム(コーティング無)について実施例7と同様の方法で抗血栓性(30分間)を評価した。結果を表5に示す。
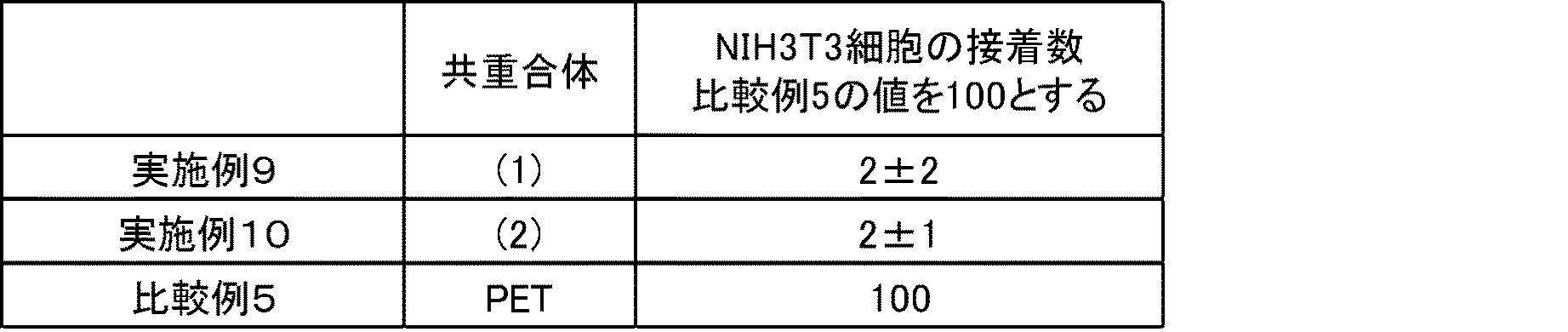
共重合体(1)の0.1質量%メタノール溶液を室温でPETフィルム(1.0cm×1.0cm)上へスピンコートした。具体的には、上記溶液30μLをPETフィルム上に滴下し、60秒間、2000rpm回転させた。その後、室温にて3時間、ロータリー真空ポンプにて減圧乾燥し、コーティング膜を得た。得られたコーティング膜について、以下の方法で細胞の接着試験を評価した。結果を表6に示す。
PETフィルム(1.0cm×1.0cm)上に共重合体(1)をスピンコートしたコーティング膜を24穴の細胞培養プレートの底に少量のシリコン接着剤で固定した。超純水で3回洗浄した後に37℃環境下のPBS中で12時間浸漬させた。
実施例9と同様の方法で共重合体(2)のコーティング膜を得た。得られたコーティング膜について実施例9と同様の方法で細胞接着試験を実施した。結果を表6に示す。
実施例9で用いたものと同様のPETフィルム(コーティング無)について、実施例9と同様の方法で細胞接着試験を実施した。結果を表6に示す。
共重合体(1)の0.1質量%メタノール溶液を室温でPETフィルム(1cm×1cm)上へスピンコートした。具体的には、上記溶液30μLをPETフィルム上に滴下し2000rpmで60秒間回転した。その後、室温にて、ロータリー真空ポンプにて減圧乾燥し、コーティング膜(PETフィルムの表面に形成されたコーティング膜)を得た。
得られたコーティング膜を24穴細胞培養ディッシュの底に少量のシリコン接着剤で固定した。これを純水で3回洗浄後、リン酸塩緩衝生理食塩液(PBS)に12時間浸漬した。PBSを除いた後、対数増殖期にある大腸菌(E.coli ATCC(R) 25922TM)を含む10質量% Muller−Hinton II (MH)培地でOD600=0.003に調製した分散液を上記細胞培養ディッシュに2.0mL加え、37℃で20時間静置培養した。上清を96穴の細胞培養ディッシュに100μLずつ加え、OD590を測定し大腸菌分散液の濃度を求めた。大腸菌が接着したコーティング膜は、24穴細胞培養ディッシュから取り出し、PBSで3回洗浄した後に新しい24穴細胞培養ディッシュに移した。接着した大腸菌の定量はBacTiter−GloTM Microbial Cell Viability Assayを用いて行った。10% BacTiter−GloTM Reagent水溶液500μLを大腸菌が接着したコーティング膜に添加し、5分間室温で静置した。その後、添加した水溶液を化学発光用96穴マイクロプレートに100μLずつ加え、プレートリーダーを用いて化学発光強度を測定した。
得られたコーティング膜を24穴細胞培養ディッシュの底に少量のシリコン接着剤で固定した。これを純水で3回洗浄後、リン酸塩緩衝生理食塩液(PBS)に12時間浸漬した。PBSを除いた後、対数増殖期にある大腸菌(E.coli ATCC(R) 25922TM)を含む10質量% Muller−Hinton II (MH)培地でOD600=0.003に調製した分散液を上記細胞培養ディッシュに2.0mL加え、37℃で20時間静置培養した。上清を除き、PBSでコーティング膜を3回洗浄した。2%グルタルアルデヒドを含むPBSを加え4℃で2時間静置し、コーティング膜表面に接着した大腸菌を固定化した。サンプルをPBSで3回、純水で1回洗浄し、1晩減圧乾燥を行った。得られたサンプルを金スパッタ装置で金コートし、走査型電子顕微鏡を用いてコーティング膜表面を倍率400倍及び2500倍で3視野任意に観察し、大腸菌の接着性、コロニー形成を評価した。大腸菌のコロニー形成が全く確認できないものを−、大腸菌数が400cells未満の小さなコロニーが分散して存在するもの±、大腸菌数が400cells以上の大きなコロニーが存在するものを+、大腸菌数が400cells以上の大きなコロニーが存在し、かつ広範囲にコロニー形成が広がっているものを++と表7に記す。
実施例11と同様の方法で共重合体(2)のコーティング膜を得た。得られたコーティング膜について実施例11と同様の方法で大腸菌の接着性および接着大腸菌のコロニー形成を評価した。結果を表7に示す。
実施例11で用いたものと同様のPETフィルム(コーティング無)について、実施例11と同様の方法で大腸菌の接着性および接着大腸菌のコロニー形成を評価した。結果を表7に示す。
テトラフルオロエチレンとN−ビニルピロリドンの共重合体(3)の調製
気密検査済みの耐圧性反応容器内を十分に窒素置換した後、脱酸素処理したアセトン(890g)及びN−ビニルピロリドン(NVP)(60.1g)を添加した。続いてテトラフルオロエチレン(TFE)(74g)を加圧添加し、攪拌しながら混合物の内温を60℃となる様に調整した上で、t−ブチルパーオキシピバレート(2.6g)を加えて反応を開始した。反応圧の低下に応じて、TFEとNVPを追加仕込みをおこない、圧が一定になるようにした。追加仕込みしたTFEは合計91g、NVPは200gであった。反応開始から218分後、残存するTFEを除去し、反応を完了させた。次いで反応混合物を精製、乾燥させ、目的の共重合体(3)を1284g得た。得られた共重合体(3)は、重量平均分子量4.3×104、分子量分布1.9、35モル%のTFE単位及び65モル%のNVP単位を含む共重合体であることが分かった。
テトラフルオロエチレンとN−ビニルピロリドンの共重合体(4)の調製
製造例3と同じ条件で重合をおこなった。ただし、追加仕込みしたTFEは合計88g、NVPは188gであった。反応開始から214分後、残存するTFEを除去し、反応を完了させた。次いで反応混合物を精製、乾燥させ、目的の共重合体(4)を1273g得た。得られた共重合体(4)は、重量平均分子量4.5×104、分子量分布1.9、37モル%のTFE単位及び63モル%のNVP単位を含む共重合体であることが分かった。
ヘキサフルオロプロピレンとN−ビニルピロリドンの共重合体(5)の調製
気密検査済みの耐圧性反応容器内を十分に窒素置換した後、脱酸素処理したアセトン(890g)及びN−ビニルピロリドン(NVP)(135g)を添加した。続いてヘキサフルオロプロピレン(HFP)(147g)を加圧添加し、撹拌しながら混合物の内温を60℃となる様に調整した上で、t−ブチルパーオキシピバレート(2.2g)を加えて反応を開始した。反応開始から164分後、残存するヘキサフルオロプロピレンを除去し、反応を完了させた。次いで反応混合物を精製、乾燥させ、目的の共重合体(5)を1157g得た。得られた共重合体(5)は、重量平均分子量1.1×104、分子量分布1.7、29モル%のHFP単位及び71モル%のNVP単位を含む共重合体であることが分かった。
トリフルオロクロロエチレンとN−ビニルピロリドンの共重合体(6)の調製
気密検査済みの耐圧性反応容器内を十分に窒素置換した後、脱酸素処理したアセトン(751g)及びN−ビニルピロリドン(26.0g)を添加した。続いてトリフルオロクロロエチレン(116g)を加圧添加し、攪拌しながら混合物の内温を60℃となる様に調整した上で、t−ブチルパーオキシピバレート(1.8g)を加えて反応を開始した。反応開始から120分後、残存するトリフルオロクロロエチレンを除去し、ヒドロキノン(1.1g)を添加した。次いで反応混合物を精製、乾燥させ、目的の共重合体(6)を3g得た。得られた共重合体(6)は、重量平均分子量4.7×104、分子量分布4.3、64モル%のトリフルオロクロロエチレン単位及び36モル%のN−ビニルピロリドン単位を含む共重合体であることが分かった。
BSA吸着量評価実験
製造例3〜6でえられた共重合体に関し、タンパク質吸着試験(ウシ血清アルブミン)をおこなった。
テトラフルオロエチレンとN−ビニルピロリドンの共重合体(7)の調製
気密検査済みの耐圧性反応容器内を十分に窒素置換した後、脱酸素処理したアセトン(890g)及びN−ビニルピロリドン(NVP)(36.0g)を添加した。続いてテトラフルオロエチレン(TFE)(131g)を加圧添加し、攪拌しながら混合物の内温を60℃となる様に調整した上で、t−ブチルパーオキシピバレート(2.6g)を加えて反応を開始した。反応圧の低下に応じて、TFEとNVPを追加仕込みをおこない、圧が一定になるようにした。追加仕込みしたTFEは合計90g、NVPは100gであった。反応開始から5時間後、残存するTFEを除去し、反応を完了させた。次いで反応混合物を精製、乾燥させ、目的の共重合体(7)を229g得た。得られた共重合体(7)は、重量平均分子量5.0×104、分子量分布2.0、46モル%のTFE単位及び54モル%のNVP単位を含む共重合体であることが分かった。
実施例1と同様にQCM−Dを用いて、表9に記載したように、共重合体(5)、(3)、又は(7)について、ウシ血漿フィブリノーゲン(BPF)の吸着を評価した。実験の結果を表9に示す。結果は比較例2の値を100として表9に示す。
実施例1と同様にQCM−Dを用いて、表10に記載したように、共重合体(5)、(3)、又は(7)について、グロブリン(IgG)の吸着を評価した。実験の結果を表10に示す。結果は比較例3の値を100として表10に示す。
Claims (11)
- フルオロポリマーからなる生体適合性材料であって、
前記フルオロポリマーは、フルオロオレフィンとアミド結合を有する重合性ビニル化合物との共重合体であり、フルオロオレフィン単位が65〜5モル%であり、アミド結合を有する重合性ビニル化合物単位が35〜95モル%であり、ゲル浸透クロマトグラフィーにより求める重量平均分子量が15000〜500000であり、ランダムポリマーであり、
前記フルオロオレフィンは、テトラフルオロエチレン、フッ化ビニリデン及びヘキサフルオロプロピレンからなる群より選択される少なくとも1種であり、
前記アミド結合を有する重合性ビニル化合物は、N−ビニル−β−プロピオラクタム、N−ビニル−2−ピロリドン、N−ビニル−γ−バレロラクタム、N−ビニル−2−ピペリドン、及び、N−ビニル−ヘプトラクタムからなる群より選択される少なくとも1種であることを特徴とする生体適合性材料。 - フルオロオレフィンは、テトラフルオロエチレン及びヘキサフルオロプロピレンからなる群より選択される少なくとも1種である請求項1記載の生体適合性材料。
- 請求項1又は2記載の生体適合性材料及び有機溶剤からなることを特徴とするコーティング組成物。
- 請求項1又は2記載の生体適合性材料からなることを特徴とする物品。
- 請求項1又は2記載の生体適合性材料を成形して得られることを特徴とする物品。
- 請求項1又は2記載の生体適合性材料、又は、請求項3記載のコーティング組成物を塗布して得られることを特徴とするコーティング膜。
- 請求項1又は2記載の生体適合性材料、又は、請求項3記載のコーティング組成物を塗布して得られるコーティング膜を備えることを特徴とする物品。
- 医療用具又は医療用容器である請求項4、5又は7記載の物品。
- 請求項4、5、7又は8記載の物品であって、抗血栓用、バイオ医薬用、抗菌用、細胞培養用、又は、抗タンパク吸着用に使用することを特徴とする物品。
- 請求項4、5、7、8又は9記載の物品であって、フィルム、シート、チューブ、バッグ、シャーレ、ディッシュ、ウェル、又は、バイアル瓶であることを特徴とする物品。
- 請求項1又は2記載の生体適合性材料、又は、請求項3記載のコーティング組成物を塗布する工程を含むことを特徴とするコーティング方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015121356 | 2015-06-16 | ||
| JP2015121356 | 2015-06-16 | ||
| PCT/JP2016/067907 WO2016204217A1 (ja) | 2015-06-16 | 2016-06-16 | 生体適合性材料、コーティング組成物、コーティング膜及び物品 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021016373A Division JP7123346B2 (ja) | 2015-06-16 | 2021-02-04 | 生体適合性材料、コーティング組成物、コーティング膜及び物品 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2016204217A1 JPWO2016204217A1 (ja) | 2018-04-05 |
| JP6889824B2 true JP6889824B2 (ja) | 2021-06-18 |
Family
ID=57545345
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017525289A Active JP6889824B2 (ja) | 2015-06-16 | 2016-06-16 | 生体適合性材料、コーティング組成物、コーティング膜及び物品 |
| JP2021016373A Active JP7123346B2 (ja) | 2015-06-16 | 2021-02-04 | 生体適合性材料、コーティング組成物、コーティング膜及び物品 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021016373A Active JP7123346B2 (ja) | 2015-06-16 | 2021-02-04 | 生体適合性材料、コーティング組成物、コーティング膜及び物品 |
Country Status (2)
| Country | Link |
|---|---|
| JP (2) | JP6889824B2 (ja) |
| WO (1) | WO2016204217A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7148998B2 (ja) * | 2018-04-09 | 2022-10-06 | 株式会社サイフューズ | 管状細胞構造体培養維持装置および管状細胞構造体維持補助具 |
| US20210198453A1 (en) * | 2018-09-14 | 2021-07-01 | Daikin Industries, Ltd. | Composition and multilayer body |
| DE102019102597A1 (de) * | 2019-02-01 | 2020-08-06 | DC Diagnostics Concept UG (haftungsbeschränkt) | Behältnis zur Verwahrung einer Körperflüssigkeit |
| CN112280103B (zh) * | 2020-10-29 | 2022-03-15 | 巢湖学院 | 一种抗菌包装膜及制备方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5100689A (en) * | 1987-04-10 | 1992-03-31 | University Of Florida | Surface modified surgical instruments, devices, implants, contact lenses and the like |
| US5443455A (en) * | 1993-07-27 | 1995-08-22 | Target Therapeutics, Inc. | Guidewire and method of pretreating metal surfaces for subsequent polymer coating |
| US7244443B2 (en) * | 2004-08-31 | 2007-07-17 | Advanced Cardiovascular Systems, Inc. | Polymers of fluorinated monomers and hydrophilic monomers |
| US8668919B2 (en) | 2009-03-03 | 2014-03-11 | Abbott Cardiovascular Systems Inc. | Polymer for creating hemocompatible surface |
-
2016
- 2016-06-16 JP JP2017525289A patent/JP6889824B2/ja active Active
- 2016-06-16 WO PCT/JP2016/067907 patent/WO2016204217A1/ja not_active Ceased
-
2021
- 2021-02-04 JP JP2021016373A patent/JP7123346B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP7123346B2 (ja) | 2022-08-23 |
| JPWO2016204217A1 (ja) | 2018-04-05 |
| WO2016204217A1 (ja) | 2016-12-22 |
| JP2021091908A (ja) | 2021-06-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7123346B2 (ja) | 生体適合性材料、コーティング組成物、コーティング膜及び物品 | |
| US11441120B2 (en) | Cell culture substrate | |
| US10669445B2 (en) | Ion complex material having function of inhibiting adhesion of biological substance and method for manufacturing the same | |
| US9701939B2 (en) | Thermoresponsive cell culture supports | |
| JP6810386B2 (ja) | 低タンパク質吸着性材料、低タンパク質吸着性物品、低細胞付着性材料および低細胞付着性物品 | |
| Gottenbos et al. | Initial adhesion and surface growth of Pseudomonas aeruginosa on negatively and positively charged poly (methacrylates) | |
| US12534637B2 (en) | Coating film having thinly-spreading and irregularity-conforming properties, and structural base having such film | |
| WO2015115568A1 (ja) | 温度応答性基材、その製造方法及びその評価方法 | |
| EP3719113A1 (en) | Cell culture container capable of long-term culture, and method for manufacturing same | |
| JP6214583B2 (ja) | 高分子基材、その用途及びその製造方法 | |
| KR20100049532A (ko) | 세포 배양 기재 | |
| JP6447787B2 (ja) | 細胞培養基材 | |
| Salehi-Nik et al. | Surface modification of silicone tubes by functional carboxyl and amine, but not peroxide groups followed by collagen immobilization improves endothelial cell stability and functionality | |
| JP2016026520A (ja) | タンパク質付着防止用化合物、塗布液および医療用デバイス | |
| US12291701B2 (en) | Cell culture container having minute volume | |
| JP2018123275A (ja) | 細胞接着防止剤 | |
| US20240287322A1 (en) | Composition for forming coating film, coating film, and cell culture vessel | |
| US20240336891A1 (en) | Base material for cell culture in serum-free medium | |
| US20250011602A1 (en) | Adhesion suppressing material of biological substances | |
| US11246966B2 (en) | Copolymer-comprising antimicrobial, cell culture, antithrombotic, or biopharmaceutical article | |
| US20220135806A1 (en) | Method for producing polymer compatible with biomaterials | |
| TW201602260A (zh) | 具有活體物質的附著抑制能之離子複合材料 | |
| Bittrich et al. | Control of Protein Adsorption and Cell Adhesion by Mixed Polymer Brushes Made by the “Grafting-To” Approach | |
| Serbetci et al. | Proteins and cells on polyurethane surfaces | |
| US20230392037A1 (en) | Biological substance low adhesion material comprising copolymer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7426 Effective date: 20171226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20171226 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190426 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200331 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200601 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200716 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20201104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210204 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210204 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210216 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210224 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210420 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210428 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6889824 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |