JP6852182B2 - プシコースの効率的な製造方法 - Google Patents
プシコースの効率的な製造方法 Download PDFInfo
- Publication number
- JP6852182B2 JP6852182B2 JP2019550531A JP2019550531A JP6852182B2 JP 6852182 B2 JP6852182 B2 JP 6852182B2 JP 2019550531 A JP2019550531 A JP 2019550531A JP 2019550531 A JP2019550531 A JP 2019550531A JP 6852182 B2 JP6852182 B2 JP 6852182B2
- Authority
- JP
- Japan
- Prior art keywords
- fructose
- psicose
- raffinate
- weight
- production
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H3/00—Compounds containing only hydrogen atoms and saccharide radicals having only carbon, hydrogen, and oxygen atoms
- C07H3/02—Monosaccharides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/10—Selective adsorption, e.g. chromatography characterised by constructional or operational features
- B01D15/18—Selective adsorption, e.g. chromatography characterised by constructional or operational features relating to flow patterns
- B01D15/1814—Recycling of the fraction to be distributed
- B01D15/1821—Simulated moving beds
- B01D15/185—Simulated moving beds characterised by the components to be separated
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
- B01D15/361—Ion-exchange
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H1/00—Processes for the preparation of sugar derivatives
- C07H1/06—Separation; Purification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/02—Monosaccharides
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Analytical Chemistry (AREA)
- Molecular Biology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Sustainable Development (AREA)
- General Chemical & Material Sciences (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Treatment Of Liquids With Adsorbents In General (AREA)
Description
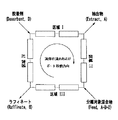
活性基が付着された陽イオン交換樹脂充填カラムを含み、原料投入口、およびプシコース分画と果糖ラフィネートを排出する排出口を備えた擬似移動層(simulated moving bed、SMB)クロマトグラフィー分離器、並びに
前記分離器から排出された果糖ラフィネートの提供を受けて果糖を分離する果糖分離装置を含むプシコース製造装置に関する。
プシコース転換工程は、プシコース転換反応を行って果糖含有原料からプシコースを転換する工程であって、工程の生産物として果糖から転換されたプシコースを含有する反応液を得る。
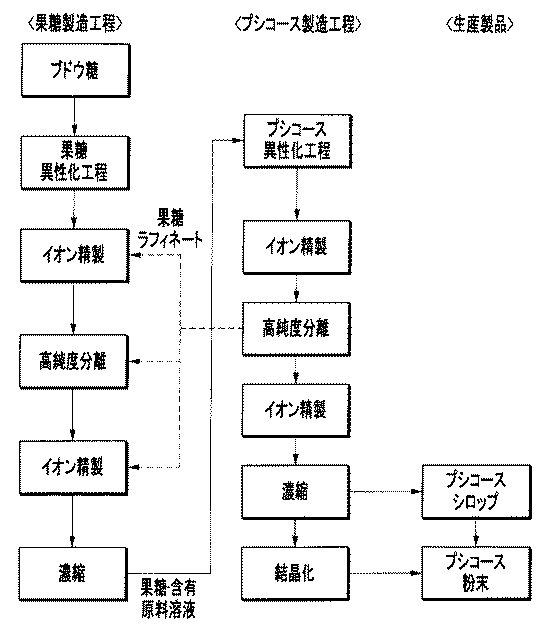
本発明によるプシコースの製造工程は、前記プシコース転換反応物をイオン精製および擬似移動層(SMB)クロマトグラフィー分離工程に付すプシコース転換反応物の分離工程を含むことができる。具体的な一例では、前記プシコース転換反応物にSMBクロマトグラフィー分離を行って、転換反応物よりプシコース含量の高いプシコース分画と果糖ラフィネートに分離し、分離したプシコース分画をプシコース濃縮工程または結晶化工程に投入して、果糖ラフィネートを果糖製造工程に投入して再循環させる。
本発明によるプシコース製造の高純度クロマトグラフィー分離工程で得られた果糖ラフィネートを果糖製造の分離工程に投入して果糖含有原料を製造し、製造された果糖含有原料をプシコース製造工程の原料として投入してプシコースを製造する。
本発明による果糖製造工程で得られる最終生産物は、プシコース転換反応のための反応原料としてプシコース製造工程に投入する。
本発明のプシコース製造工程において、SMBクロマトグラフィーを用いた高純度分離工程で得られたプシコース分画は、プシコース濃縮工程を経て液状シロップとして製品化するか、プシコース結晶化工程を経てプシコース結晶として製品化することができる。
韓国公開特許第2014−0054997に記載の製造方法と実質的に同一の生物学的方法により、果糖基質からプシコースシロップを製造した。
上記製造例1で得られた2種類のプシコースシロップについて、有色およびイオン成分などの不純物を除去するために、陽イオン交換樹脂、陰イオン交換樹脂、および陽イオンと陰イオン交換樹脂の混合樹脂で充填した常温のカラムに、1時間当りイオン交換樹脂2倍体積の速度で通液させて脱塩させた。
上記製造例2で得られた果糖含量88重量%の果糖含有原料溶液を用いてプシコース含量95重量%の固形分10トンを生産するために、流量3.8m3/hrでプシコース転換工程と分離工程を行った。プシコース転換工程を経て得られた反応物のプシコース含量は20〜23重量%であり、イオン精製の後、45〜50重量%の濃度で分離工程を通過させた。Ca+タイプ分離(SMB)樹脂を用いて分離時に生成するラフィネートは、1時間当り3m3ずつ生成した。
本実験は、果糖ラフィネートの再循環の有無による糖組成および収率の差を確認するために行った。
上記実施例1と同じ方法で、果糖含量95重量%のシロップを用いたプシコース含量95重量%の固形分10トンを生産するために、流量3.8m3/hrでプシコース異性化工程と分離工程を行った。プシコース転換工程を経て得られた反応生産物のプシコース含量は21〜25重量%であり、イオン精製の後、45〜50重量%の濃度で分離工程を通過させた。Ca+タイプ分離樹脂を用いて分離時に生成するラフィネート(果糖分画)は、1時間当り3m3ずつ生成した。
果糖ラフィネートの再循環の有無による糖組成および収率の差を確認するために、上記実施例2と実質的に同じ方法で実験を行った。但し、上記実施例2において果糖含量88重量%原料の代わりに、果糖含量95重量%の原料を用いてプシコース転換反応を行った。
プシコース製造過程で得られた果糖ラフィネートと類似の組成でプシコース転換率を評価した。即ち、果糖純度95重量%シロップを50重量%に希釈してCa2+イオンを0.005〜0.01mMで添加した後、1.0mMのMnをさらに添加してプシコース転換工程を確認し、その結果を表5に示した。
Claims (18)
- プシコース転換反応物を擬似移動層(simulated moving bed、SMB)クロマトグラフィーで分離してプシコース分画と果糖ラフィネートを得て、
得られた果糖ラフィネートを果糖異性化反応を用いる果糖製造の分離工程に投入して果糖含有原料を製造し、
得られた果糖含有原料を用いてプシコース転換反応を行う工程を含み、
前記擬似移動層クロマトグラフィー分離工程で得られた果糖ラフィネートは、糖類合計100重量%を基準にして、85〜99重量%の果糖および2.0重量%以下のプシコースを含み、
前記果糖製造の分離工程は、イオン精製工程および擬似移動層クロマトグラフィーを用いた分離工程を含み、
前記プシコース転換反応に投入される果糖含有原料の果糖含量は、全糖類含量100重量%を基準にして85重量%以上であり、
前記果糖含有原料の電気伝導度が0〜15μs/cmであるプシコースの製造方法。 - 前記プシコース転換反応物は、果糖原料を用いた生物学的プシコース転換工程で得られるものである請求項1に記載の製造方法。
- 前記果糖製造の分離工程は、果糖異性化反応物をイオン精製する第1次イオン精製、擬似移動層クロマトグラフィーを用いた分離工程、第2次イオン精製工程、および濃縮工程を含み、前記果糖ラフィネートは前記第1次イオン精製、擬似移動層クロマトグラフィーを用いた高純度分離、および第2次イオン精製よりなる群から選択された1種以上の工程に投入される請求項1に記載の製造方法。
- 前記イオン精製工程は、イオン交換樹脂クロマトグラフィーを用いて行う請求項3に記載の製造方法。
- 前記果糖含有原料は、カルシウムイオン濃度が0.05mM以下の範囲である請求項1に記載の製造方法。
- 前記擬似移動層クロマトグラフィー分離工程で得られる果糖ラフィネートは、電気伝導度が20〜200μs/cmである請求項1に記載の製造方法。
- 前記果糖製造の分離工程で得られる果糖液と前記果糖ラフィネートは、果糖液と果糖ラフィネートをそれぞれ50ブリックスに調整した場合、果糖液と果糖ラフィネートの全100重量%を基準にして、果糖液65〜95重量%と果糖ラフィネート5〜35重量%である請求項1に記載の製造方法。
- 前記擬似移動層クロマトグラフィー分離工程は、カルシウム活性基が付着された陽イオン交換樹脂充填カラムクロマトグラフで行われる請求項1に記載の製造方法。
- 前記プシコース転換反応は、プシコース転換率が15%〜70%である生物学的触媒を使用する請求項1に記載の製造方法。
- 前記擬似移動層クロマトグラフィー分離工程で得られる果糖ラフィネートを、熱交換器を通じて冷却する工程をさらに含む請求項1に記載の製造方法。
- 前記製造方法は、連続式で行われる請求項1に記載の製造方法。
- 前記プシコース分画を濃縮し、前記濃縮物からプシコースを結晶化してプシコース結晶と結晶化母液を得る工程をさらに含む請求項1に記載の方法。
- 果糖含有原料からプシコースへの転換反応を行うプシコース転換反応器、
活性基が付着された陽イオン交換樹脂充填カラムを含み、原料投入口、およびプシコース分画と果糖ラフィネートを排出する排出口を備えた擬似移動層(simulated moving bed、SMB)クロマトグラフィー分離器、
果糖異性化反応を用いる果糖製造装置、及び、
前記果糖製造装置と前記プシコース転換反応器とを連結する連結部を含み、
前記果糖製造装置は、果糖異性化反応を行う果糖異性化反応器、イオン交換樹脂が充填されたカラムを備えたイオン精製器、活性基が付着された陽イオン交換樹脂充填カラム、及び、原料投入口と果糖分画およびラフィネートを排出する排出口とを備えた擬似移動層(simulated moving bed、SMB)クロマトグラフィー分離器を含み、
前記擬似移動層クロマトグラフィー分離器から排出された果糖ラフィネートは、連結部を通じて前記果糖製造装置に投入されて果糖含量原料として製造され、前記プシコース製造装置のプシコース転換反応器に投入され、
前記擬似移動層クロマトグラフィー分離器から排出された果糖ラフィネートは、果糖ラフィネートの糖類合計100重量%を基準にして、85〜99重量%の果糖および2.0重量%以下のプシコースを含み、
前記プシコース転換反応器に投入される果糖含有原料は、果糖含量が85重量%以上であり、電気伝導度が0〜15μs/cmである、プシコース製造装置。 - 前記プシコース転換反応器は、生物学的方法で果糖含有原料からプシコースへの転換反応を行う請求項13に記載のプシコース製造装置。
- 前記クロマトグラフィー分離器から排出された果糖ラフィネートの冷却のための熱交換器をさらに含む請求項13に記載のプシコース製造装置。
- プシコース転換反応器に投入する前に、前記果糖含有原料を貯蔵する貯蔵槽をさらに含む請求項13に記載のプシコース製造装置。
- 前記プシコース製造装置は、前記分離器から排出された果糖ラフィネートの提供により果糖を分離する果糖分離装置をさらに含み、
前記果糖分離装置は、前記分離器から排出された果糖分画を濃縮する濃縮器、および、前記濃縮器から排出された果糖含有原料をプシコース製造装置に提供するための果糖製造装置とプシコース製造装置を連結する連結部を含む請求項13に記載のプシコース製造装置。 - 前記イオン交換樹脂が充填されたカラムを備えたイオン精製器が、クロマトグラフィー分離器と濃縮器の間に連結された請求項13に記載のプシコース製造装置。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2016-0167048 | 2016-12-08 | ||
| KR1020160167048A KR102004941B1 (ko) | 2016-12-08 | 2016-12-08 | 효율적인 사이코스의 제조 방법 |
| PCT/KR2017/013542 WO2018105934A2 (ko) | 2016-12-08 | 2017-11-24 | 사이코스의 효율적인 제조 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020500557A JP2020500557A (ja) | 2020-01-16 |
| JP6852182B2 true JP6852182B2 (ja) | 2021-03-31 |
Family
ID=62491280
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019550531A Active JP6852182B2 (ja) | 2016-12-08 | 2017-11-24 | プシコースの効率的な製造方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11358980B2 (ja) |
| EP (1) | EP3553070B1 (ja) |
| JP (1) | JP6852182B2 (ja) |
| KR (1) | KR102004941B1 (ja) |
| CN (1) | CN110062762B (ja) |
| TW (1) | TWI659108B (ja) |
| WO (1) | WO2018105934A2 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102065155B1 (ko) * | 2016-12-08 | 2020-02-11 | 주식회사 삼양사 | 사이코스의 제조방법 |
| EP3561080B1 (fr) * | 2018-04-23 | 2023-08-02 | Novasep Process Solutions | Procede de fabrication de fructose a partir de glucose |
| CN108866247A (zh) * | 2018-09-18 | 2018-11-23 | 上海立足生物科技有限公司 | 连续大规模分离制备d-阿洛酮糖的方法和设备 |
| CN109022521B (zh) * | 2018-09-18 | 2023-05-05 | 上海立足生物科技有限公司 | 一种由淀粉制备d-阿洛酮糖的方法 |
| CN109022520B (zh) * | 2018-09-18 | 2023-05-05 | 上海立足生物科技有限公司 | 一种阿洛酮糖的生产工艺 |
| KR102590473B1 (ko) * | 2019-10-31 | 2023-10-17 | 주식회사 삼양사 | 개선된 알룰로스의 제조 방법 |
| US20220380400A1 (en) * | 2019-10-31 | 2022-12-01 | Samyang Corporation | Improved method for manufacturing allulose |
| KR102389709B1 (ko) * | 2019-11-29 | 2022-04-22 | 씨제이제일제당 주식회사 | 알룰로스 제조용 조성물 및 이를 이용한 알룰로스의 제조 방법 |
| CN113080357B (zh) * | 2021-05-17 | 2023-09-15 | 江苏赛威分离科技有限公司 | 一种低热量复配甜味剂及其生产工艺 |
| CN114032263A (zh) * | 2021-07-21 | 2022-02-11 | 山东福洋生物科技股份有限公司 | 一种生物发酵法生产高纯度阿洛酮糖晶体的方法 |
| CN114671919B (zh) * | 2022-03-25 | 2023-05-12 | 山东兆光色谱分离技术有限公司 | 一种基于色谱分离生产结晶阿洛酮糖的方法 |
| CN116716365A (zh) * | 2023-05-22 | 2023-09-08 | 山东奥博生物科技有限公司 | 基于中空纤维和模拟移动床的连续化生产d-阿洛酮糖的方法及系统 |
| KR20250094878A (ko) * | 2023-12-19 | 2025-06-26 | 대상 주식회사 | 이온교환을 이용한 알룰로스 함유 용액의 정제방법 |
| WO2025153524A1 (en) | 2024-01-16 | 2025-07-24 | Savanna Ingredients Gmbh | Process for the synthesis and purification of allulose |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2985589A (en) | 1957-05-22 | 1961-05-23 | Universal Oil Prod Co | Continuous sorption process employing fixed bed of sorbent and moving inlets and outlets |
| JPS4627841Y1 (ja) | 1967-08-03 | 1971-09-27 | ||
| JP4627841B2 (ja) * | 2000-06-08 | 2011-02-09 | 国立大学法人 香川大学 | プシコースの分離方法 |
| KR100967093B1 (ko) * | 2008-04-01 | 2010-07-01 | 주식회사 신동방씨피 | 고순도 무수결정과당의 제조방법 |
| KR101189640B1 (ko) * | 2010-03-26 | 2012-10-12 | 씨제이제일제당 (주) | D-사이코스 결정을 제조하는 방법 |
| CN102946961B (zh) | 2010-03-30 | 2015-11-25 | 杜邦营养生物科学有限公司 | 分离方法 |
| US8802843B2 (en) * | 2012-05-22 | 2014-08-12 | Orochem Technologies, Inc. | Tagatose production using simulated moving bed separation |
| KR101539096B1 (ko) | 2012-08-10 | 2015-07-24 | 주식회사 삼양제넥스 | 사이코스 에피머화 효소 및 이를 이용한 사이코스로 전환용 조성물 |
| KR20140054997A (ko) | 2012-10-30 | 2014-05-09 | 현대모비스 주식회사 | 차량용 수납박스의 잠금장치 |
| KR20140080282A (ko) | 2012-12-20 | 2014-06-30 | 주식회사 삼양제넥스 | D-사이코스 3-에피머화 효소를 이용한 과당으로부터 사이코스의 제조방법 |
| US20140275518A1 (en) * | 2013-03-14 | 2014-09-18 | Orochem Technologies, Inc. | L-glucose production from l-glusose/l-mannose mixtures using simulated moving bed separation |
| KR101318422B1 (ko) | 2013-04-09 | 2013-10-15 | 주식회사 삼양제넥스 | D-사이코스 에피머화 효소, 및 이를 이용하는 사이코스 생산방법 |
| MX374397B (es) | 2013-06-05 | 2025-03-06 | Cj Cheiljedang Corp | Metodo de produccion para tagatosa. |
| KR101749527B1 (ko) | 2014-10-20 | 2017-06-21 | 씨제이제일제당(주) | D-사이코스 결정을 제조하는 방법 |
| KR20160062349A (ko) * | 2014-11-25 | 2016-06-02 | 씨제이제일제당 (주) | 고순도 d-사이코스를 제조하는 방법 |
| KR102087396B1 (ko) * | 2015-11-16 | 2020-03-10 | 주식회사 삼양사 | 과당-함유 기질로부터 사이코스를 생산하는 방법 |
| KR102065155B1 (ko) * | 2016-12-08 | 2020-02-11 | 주식회사 삼양사 | 사이코스의 제조방법 |
| KR102072695B1 (ko) * | 2016-12-08 | 2020-03-02 | 주식회사 삼양사 | 재순환을 이용한 사이코스의 제조방법 및 장치 |
-
2016
- 2016-12-08 KR KR1020160167048A patent/KR102004941B1/ko active Active
-
2017
- 2017-11-24 CN CN201780075573.2A patent/CN110062762B/zh active Active
- 2017-11-24 EP EP17877905.4A patent/EP3553070B1/en active Active
- 2017-11-24 US US16/463,977 patent/US11358980B2/en active Active
- 2017-11-24 JP JP2019550531A patent/JP6852182B2/ja active Active
- 2017-11-24 WO PCT/KR2017/013542 patent/WO2018105934A2/ko not_active Ceased
- 2017-11-29 TW TW106141516A patent/TWI659108B/zh active
Also Published As
| Publication number | Publication date |
|---|---|
| US20200377540A1 (en) | 2020-12-03 |
| EP3553070A2 (en) | 2019-10-16 |
| CN110062762A (zh) | 2019-07-26 |
| WO2018105934A3 (ko) | 2018-08-02 |
| TWI659108B (zh) | 2019-05-11 |
| TW201827606A (zh) | 2018-08-01 |
| CN110062762B (zh) | 2022-10-04 |
| WO2018105934A2 (ko) | 2018-06-14 |
| KR20180065782A (ko) | 2018-06-18 |
| KR102004941B1 (ko) | 2019-07-29 |
| US11358980B2 (en) | 2022-06-14 |
| JP2020500557A (ja) | 2020-01-16 |
| EP3553070C0 (en) | 2024-09-11 |
| EP3553070A4 (en) | 2020-07-29 |
| EP3553070B1 (en) | 2024-09-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6852182B2 (ja) | プシコースの効率的な製造方法 | |
| JP7148656B2 (ja) | 再循環を用いたプシコースの製造方法 | |
| JP6977054B2 (ja) | プシコースの製造方法 | |
| KR102857629B1 (ko) | 개선된 알룰로스의 제조 방법 | |
| CA3156624C (en) | Improved method for manufacturing allulose | |
| KR102590473B1 (ko) | 개선된 알룰로스의 제조 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190605 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200616 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200910 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210224 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210310 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6852182 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |