JP6810331B2 - 生体活性多孔性骨移植インプラント - Google Patents
生体活性多孔性骨移植インプラント Download PDFInfo
- Publication number
- JP6810331B2 JP6810331B2 JP2019005634A JP2019005634A JP6810331B2 JP 6810331 B2 JP6810331 B2 JP 6810331B2 JP 2019005634 A JP2019005634 A JP 2019005634A JP 2019005634 A JP2019005634 A JP 2019005634A JP 6810331 B2 JP6810331 B2 JP 6810331B2
- Authority
- JP
- Japan
- Prior art keywords
- bioactive glass
- implant
- fiber
- implants
- bone
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000007943 implant Substances 0.000 title claims description 266
- 210000000988 bone and bone Anatomy 0.000 title claims description 150
- 230000000975 bioactive effect Effects 0.000 title description 28
- 239000000835 fiber Substances 0.000 claims description 230
- 239000000463 material Substances 0.000 claims description 171
- 239000005313 bioactive glass Substances 0.000 claims description 142
- 239000008187 granular material Substances 0.000 claims description 95
- 239000011148 porous material Substances 0.000 claims description 75
- 238000010521 absorption reaction Methods 0.000 claims description 36
- 239000012876 carrier material Substances 0.000 claims description 23
- 239000002202 Polyethylene glycol Substances 0.000 claims description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 8
- 229920001223 polyethylene glycol Polymers 0.000 claims description 8
- 239000002131 composite material Substances 0.000 claims description 7
- 239000011573 trace mineral Substances 0.000 claims description 6
- 235000013619 trace mineral Nutrition 0.000 claims description 6
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 claims description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims description 4
- 239000000377 silicon dioxide Substances 0.000 claims description 4
- 229920001577 copolymer Polymers 0.000 claims description 3
- 229920002134 Carboxymethyl cellulose Polymers 0.000 claims description 2
- 229910019142 PO4 Inorganic materials 0.000 claims description 2
- 235000011187 glycerol Nutrition 0.000 claims description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 claims description 2
- 239000010452 phosphate Substances 0.000 claims description 2
- 150000003904 phospholipids Chemical class 0.000 claims description 2
- 229920001606 poly(lactic acid-co-glycolic acid) Polymers 0.000 claims description 2
- 239000004626 polylactic acid Substances 0.000 claims description 2
- 239000004005 microsphere Substances 0.000 claims 2
- 239000011159 matrix material Substances 0.000 description 58
- 238000000576 coating method Methods 0.000 description 43
- 239000011248 coating agent Substances 0.000 description 42
- 230000035876 healing Effects 0.000 description 39
- 210000004027 cell Anatomy 0.000 description 30
- 239000011521 glass Substances 0.000 description 24
- 235000015097 nutrients Nutrition 0.000 description 23
- 238000009826 distribution Methods 0.000 description 22
- 239000000203 mixture Substances 0.000 description 22
- 238000000034 method Methods 0.000 description 20
- 239000012530 fluid Substances 0.000 description 19
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 19
- 230000004663 cell proliferation Effects 0.000 description 18
- 230000008901 benefit Effects 0.000 description 17
- 239000001506 calcium phosphate Substances 0.000 description 17
- 239000002241 glass-ceramic Substances 0.000 description 13
- 239000007787 solid Substances 0.000 description 13
- 102000008186 Collagen Human genes 0.000 description 12
- 108010035532 Collagen Proteins 0.000 description 12
- 229920001436 collagen Polymers 0.000 description 12
- 239000012634 fragment Substances 0.000 description 12
- 229910000389 calcium phosphate Inorganic materials 0.000 description 11
- 235000011010 calcium phosphates Nutrition 0.000 description 11
- 230000000694 effects Effects 0.000 description 11
- 239000006260 foam Substances 0.000 description 11
- 230000001976 improved effect Effects 0.000 description 11
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 10
- 239000002657 fibrous material Substances 0.000 description 10
- 210000001519 tissue Anatomy 0.000 description 10
- 230000033115 angiogenesis Effects 0.000 description 9
- 210000001185 bone marrow Anatomy 0.000 description 9
- 230000021164 cell adhesion Effects 0.000 description 9
- 230000007547 defect Effects 0.000 description 9
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 9
- 239000010410 layer Substances 0.000 description 9
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 9
- 238000001878 scanning electron micrograph Methods 0.000 description 9
- 238000005524 ceramic coating Methods 0.000 description 8
- 238000007634 remodeling Methods 0.000 description 8
- 229920002994 synthetic fiber Polymers 0.000 description 8
- 230000008467 tissue growth Effects 0.000 description 8
- 208000027418 Wounds and injury Diseases 0.000 description 7
- 230000000845 anti-microbial effect Effects 0.000 description 7
- 239000011575 calcium Substances 0.000 description 7
- 239000003102 growth factor Substances 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 6
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 6
- 229910052791 calcium Inorganic materials 0.000 description 6
- 230000012292 cell migration Effects 0.000 description 6
- 230000006378 damage Effects 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 239000003814 drug Substances 0.000 description 6
- 239000006112 glass ceramic composition Substances 0.000 description 6
- 230000033001 locomotion Effects 0.000 description 6
- 229910052751 metal Inorganic materials 0.000 description 6
- 239000002184 metal Substances 0.000 description 6
- 230000011164 ossification Effects 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 238000002054 transplantation Methods 0.000 description 6
- 229940078499 tricalcium phosphate Drugs 0.000 description 6
- 229910000391 tricalcium phosphate Inorganic materials 0.000 description 6
- 235000019731 tricalcium phosphate Nutrition 0.000 description 6
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 5
- 239000000654 additive Substances 0.000 description 5
- 235000011132 calcium sulphate Nutrition 0.000 description 5
- 230000024245 cell differentiation Effects 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- -1 etc.) Substances 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 238000011065 in-situ storage Methods 0.000 description 5
- 229910052500 inorganic mineral Inorganic materials 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 150000002739 metals Chemical class 0.000 description 5
- 238000013508 migration Methods 0.000 description 5
- 235000010755 mineral Nutrition 0.000 description 5
- 239000011707 mineral Substances 0.000 description 5
- 210000004623 platelet-rich plasma Anatomy 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 229910052725 zinc Inorganic materials 0.000 description 5
- 239000011701 zinc Substances 0.000 description 5
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 239000007795 chemical reaction product Substances 0.000 description 4
- 229910052802 copper Inorganic materials 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- 239000010419 fine particle Substances 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- 239000002105 nanoparticle Substances 0.000 description 4
- 230000008439 repair process Effects 0.000 description 4
- 229910052712 strontium Inorganic materials 0.000 description 4
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 description 4
- 230000032258 transport Effects 0.000 description 4
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 3
- 102000009123 Fibrin Human genes 0.000 description 3
- 108010073385 Fibrin Proteins 0.000 description 3
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 229910004298 SiO 2 Inorganic materials 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- 230000004071 biological effect Effects 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000001124 body fluid Anatomy 0.000 description 3
- 239000010839 body fluid Substances 0.000 description 3
- 230000008468 bone growth Effects 0.000 description 3
- 229910000019 calcium carbonate Inorganic materials 0.000 description 3
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 3
- 239000000920 calcium hydroxide Substances 0.000 description 3
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 3
- 229910010293 ceramic material Inorganic materials 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 230000006835 compression Effects 0.000 description 3
- 238000007906 compression Methods 0.000 description 3
- 239000012141 concentrate Substances 0.000 description 3
- 229950003499 fibrin Drugs 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- 229920002674 hyaluronan Polymers 0.000 description 3
- 229960003160 hyaluronic acid Drugs 0.000 description 3
- 238000002513 implantation Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 208000014674 injury Diseases 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 229910052749 magnesium Inorganic materials 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 230000035800 maturation Effects 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 230000010534 mechanism of action Effects 0.000 description 3
- 230000003204 osmotic effect Effects 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 238000007493 shaping process Methods 0.000 description 3
- 229910052709 silver Inorganic materials 0.000 description 3
- 239000004332 silver Substances 0.000 description 3
- 238000005245 sintering Methods 0.000 description 3
- 210000000130 stem cell Anatomy 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 230000017423 tissue regeneration Effects 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 2
- 102000007350 Bone Morphogenetic Proteins Human genes 0.000 description 2
- 108010007726 Bone Morphogenetic Proteins Proteins 0.000 description 2
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 2
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 2
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 2
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 2
- 239000004599 antimicrobial Substances 0.000 description 2
- 239000003443 antiviral agent Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 239000003124 biologic agent Substances 0.000 description 2
- 239000013060 biological fluid Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 230000014461 bone development Effects 0.000 description 2
- 229940112869 bone morphogenetic protein Drugs 0.000 description 2
- 230000010072 bone remodeling Effects 0.000 description 2
- 239000001175 calcium sulphate Substances 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 239000004568 cement Substances 0.000 description 2
- 239000000919 ceramic Substances 0.000 description 2
- 210000002808 connective tissue Anatomy 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 239000004503 fine granule Substances 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 230000001788 irregular Effects 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 230000002503 metabolic effect Effects 0.000 description 2
- 230000003278 mimic effect Effects 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 238000000465 moulding Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 210000000963 osteoblast Anatomy 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 230000035790 physiological processes and functions Effects 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 238000009987 spinning Methods 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 230000008961 swelling Effects 0.000 description 2
- GBNXLQPMFAUCOI-UHFFFAOYSA-H tetracalcium;oxygen(2-);diphosphate Chemical compound [O-2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O GBNXLQPMFAUCOI-UHFFFAOYSA-H 0.000 description 2
- 230000009772 tissue formation Effects 0.000 description 2
- 229940088594 vitamin Drugs 0.000 description 2
- 239000011782 vitamin Substances 0.000 description 2
- 235000013343 vitamin Nutrition 0.000 description 2
- 229930003231 vitamin Natural products 0.000 description 2
- 239000002699 waste material Substances 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102000011782 Keratins Human genes 0.000 description 1
- 108010076876 Keratins Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- 210000003484 anatomy Anatomy 0.000 description 1
- 230000002491 angiogenic effect Effects 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012237 artificial material Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 238000006065 biodegradation reaction Methods 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 239000002639 bone cement Substances 0.000 description 1
- 230000037180 bone health Effects 0.000 description 1
- 210000002805 bone matrix Anatomy 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- 235000010216 calcium carbonate Nutrition 0.000 description 1
- 235000011116 calcium hydroxide Nutrition 0.000 description 1
- 239000004068 calcium phosphate ceramic Substances 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000004709 cell invasion Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000005482 chemotactic factor Substances 0.000 description 1
- 239000007931 coated granule Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000007120 differential activation Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000001523 electrospinning Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 239000011152 fibreglass Substances 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 210000002997 osteoclast Anatomy 0.000 description 1
- 210000005009 osteogenic cell Anatomy 0.000 description 1
- 238000006213 oxygenation reaction Methods 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000011241 protective layer Substances 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000002278 reconstructive surgery Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- 239000010948 rhodium Substances 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 210000004872 soft tissue Anatomy 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 230000007838 tissue remodeling Effects 0.000 description 1
- 239000002407 tissue scaffold Substances 0.000 description 1
- 230000003827 upregulation Effects 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/56—Porous materials, e.g. foams or sponges
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
- A61L27/10—Ceramics or glasses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
- A61L27/12—Phosphorus-containing materials, e.g. apatite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/28—Materials for coating prostheses
- A61L27/30—Inorganic materials
- A61L27/306—Other specific inorganic materials not covered by A61L27/303 - A61L27/32
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/28—Materials for coating prostheses
- A61L27/30—Inorganic materials
- A61L27/32—Phosphorus-containing materials, e.g. apatite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/40—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
- A61L27/42—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having an inorganic matrix
- A61L27/425—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having an inorganic matrix of phosphorus containing material, e.g. apatite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/40—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
- A61L27/42—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having an inorganic matrix
- A61L27/427—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having an inorganic matrix of other specific inorganic materials not covered by A61L27/422 or A61L27/425
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/40—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
- A61L27/44—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix
- A61L27/446—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix with other specific inorganic fillers other than those covered by A61L27/443 or A61L27/46
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/40—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material
- A61L27/44—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix
- A61L27/48—Composite materials, i.e. containing one material dispersed in a matrix of the same or different material having a macromolecular matrix with macromolecular fillers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/58—Materials at least partially resorbable by the body
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/02—Polyalkylene oxides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/02—Materials or treatment for tissue regeneration for reconstruction of bones; weight-bearing implants
Description
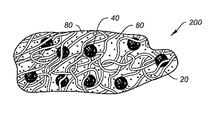
本開示は、骨移植インプラントが長期間に渡って細胞増殖および新組織の成長を支持することができるように相乗的に作用する構造的および機能的特徴の組合せを有するように設計された骨移植材料およびこれらの材料から形成されたインプラントを提供する。前記インプラントは、適切な血管新生、最適化された細胞の接着、移動、増殖、および分化を可能にするために必要な多孔性および孔径分布を提供する。インプラントは生体適合性合成材料から形成され、治癒過程全体を通して継続する細胞増殖を支持するのに必要な機械的完全性を提供する。さらに、前記材料は取り扱いが改善されるように処方され、解剖学的部位にカスタマイズされたインプラントを製造するためにインプラントの外寸および形状を容易に造形および/またはカスタマイズすることが可能になる。
Claims (9)
- 繊維クラスターの形態の生体活性ガラス材料を含む第1成分、担体材料を含む第2成分、および生体活性ガラス微細球を含む第3成分を有する適合性のパテ
を含む複合骨移植インプラントであって、
前記繊維クラスターが、生体活性ガラスシェルに部分的にまたは完全に被覆された、生体活性ガラス繊維および細粒を含み、
生体活性ガラス繊維、細粒、及びシェルのそれぞれがその他の成分とは異なる吸収能力を有する前記インプラント。 - シェルが部分的にまたは完全に焼結されている、請求項1に記載のインプラント。
- 繊維クラスターが多孔性である、請求項1に記載のインプラント。
- 繊維クラスターが、約100ナノメートルから約1ミリメートルまでの範囲の孔径を特徴とする細孔を含む、請求項3に記載のインプラント。
- 生体活性ガラス材料が、ゾルゲル由来生体活性ガラス、メルト由来生体活性ガラス、シリカ系生体活性ガラス、シリカを含まない生体活性ガラス、結晶化生体活性ガラス、および微量元素を含有する生体活性ガラスからなる群より選択される、請求項1に記載のインプラント。
- 生体活性ガラス材料が、ホウ酸塩系生体活性ガラスおよびリン酸塩系生体活性ガラスからなる群より選択されるシリカを含まない生体活性ガラスを含む、請求項1に記載のインプラント。
- 担体材料が、リン脂質、カルボキシメチルセルロース(CMC)、グリセリン、ポリエチレングリコール(PEG)、ポリ乳酸(PLA)、または乳酸-グリコール酸共重合体(PLGA)を含む、請求項1に記載のインプラント。
- 生体活性ガラス繊維および細粒が、生体活性ガラスシェルに完全に被覆される、請求項1に記載のインプラント。
- 生体活性ガラス微細球が、生体体活性ガラス繊維、細粒及びシェルとは異なる吸収能力を有する、請求項1に記載のインプラント。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13/830,629 US8883195B2 (en) | 2013-03-14 | 2013-03-14 | Bioactive porous bone graft implants |
| US13/830,629 | 2013-03-14 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016502289A Division JP6470253B2 (ja) | 2013-03-14 | 2014-03-14 | 生体活性多孔性骨移植インプラント |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019088825A JP2019088825A (ja) | 2019-06-13 |
| JP6810331B2 true JP6810331B2 (ja) | 2021-01-06 |
Family
ID=51528031
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016502289A Active JP6470253B2 (ja) | 2013-03-14 | 2014-03-14 | 生体活性多孔性骨移植インプラント |
| JP2019005634A Active JP6810331B2 (ja) | 2013-03-14 | 2019-01-17 | 生体活性多孔性骨移植インプラント |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016502289A Active JP6470253B2 (ja) | 2013-03-14 | 2014-03-14 | 生体活性多孔性骨移植インプラント |
Country Status (7)
| Country | Link |
|---|---|
| US (4) | US8883195B2 (ja) |
| EP (2) | EP2968659B1 (ja) |
| JP (2) | JP6470253B2 (ja) |
| CN (2) | CN105246519A (ja) |
| AU (1) | AU2014240175B2 (ja) |
| ES (1) | ES2909417T3 (ja) |
| WO (1) | WO2014152102A2 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010060090A1 (en) * | 2008-11-24 | 2010-05-27 | Georgia Tech Research Corporation | Systems and methods to affect anatomical structures |
| US9045362B2 (en) * | 2013-03-15 | 2015-06-02 | Mosci Corp. | Bioactive glass scaffolds, and method of making |
| US11225430B2 (en) * | 2012-03-26 | 2022-01-18 | Steven Jung | Bioactive glass scaffolds, and method of making |
| US9623153B2 (en) | 2014-09-23 | 2017-04-18 | Warsaw Orthopedic, Inc. | Bone graft materials and methods of use |
| EP3217925A4 (en) * | 2014-11-14 | 2018-08-08 | Warsaw Orthopedic, Inc. | Bone graft materials, devices and methods of use |
| US10238507B2 (en) | 2015-01-12 | 2019-03-26 | Surgentec, Llc | Bone graft delivery system and method for using same |
| US10064273B2 (en) | 2015-10-20 | 2018-08-28 | MR Label Company | Antimicrobial copper sheet overlays and related methods for making and using |
| CN107362388B (zh) * | 2017-07-11 | 2020-04-03 | 同济大学 | 一种生物玻璃纤维-改性聚酯复合敷料及其制备方法 |
| TWI675136B (zh) * | 2017-10-24 | 2019-10-21 | 路可 呂 | 導光與組織整合之生物纖維構件 |
| US11116647B2 (en) | 2018-04-13 | 2021-09-14 | Surgentec, Llc | Bone graft delivery system and method for using same |
| US10687828B2 (en) | 2018-04-13 | 2020-06-23 | Surgentec, Llc | Bone graft delivery system and method for using same |
| US11090412B2 (en) | 2018-12-21 | 2021-08-17 | Zavation Medical Products Llc | Bone repair composition and kit |
| JP2023507564A (ja) * | 2019-12-20 | 2023-02-24 | テファ, インコーポレイテッド | 骨欠損部再建用の再吸収性インプラント |
| TWI764332B (zh) * | 2020-10-22 | 2022-05-11 | 擎睿生醫有限公司 | 植骨組合物 |
Family Cites Families (63)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA1264674A (en) | 1984-10-17 | 1990-01-23 | Paul Ducheyne | Porous flexible metal fiber material for surgical implantation |
| US5030233A (en) | 1984-10-17 | 1991-07-09 | Paul Ducheyne | Porous flexible metal fiber material for surgical implantation |
| US4861733A (en) | 1987-02-13 | 1989-08-29 | Interpore International | Calcium phosphate bone substitute materials |
| JPH06116114A (ja) | 1992-10-09 | 1994-04-26 | Nikon Corp | 骨充填材 |
| US5626861A (en) | 1994-04-01 | 1997-05-06 | Massachusetts Institute Of Technology | Polymeric-hydroxyapatite bone composite |
| FI101129B (sv) | 1995-01-13 | 1998-04-30 | Vivoxid Oy | Nya bioaktiva glas och deras användning |
| US6149688A (en) * | 1995-06-07 | 2000-11-21 | Surgical Dynamics, Inc. | Artificial bone graft implant |
| US5776193A (en) | 1995-10-16 | 1998-07-07 | Orquest, Inc. | Bone grafting matrix |
| US6902584B2 (en) | 1995-10-16 | 2005-06-07 | Depuy Spine, Inc. | Bone grafting matrix |
| US6051247A (en) * | 1996-05-30 | 2000-04-18 | University Of Florida Research Foundation, Inc. | Moldable bioactive compositions |
| US5977204A (en) * | 1997-04-11 | 1999-11-02 | Osteobiologics, Inc. | Biodegradable implant material comprising bioactive ceramic |
| US5874101A (en) * | 1997-04-14 | 1999-02-23 | Usbiomaterials Corp. | Bioactive-gel compositions and methods |
| WO1998053768A1 (en) | 1997-05-30 | 1998-12-03 | Osteobiologics, Inc. | Fiber-reinforced, porous, biodegradable implant device |
| US6139585A (en) | 1998-03-11 | 2000-10-31 | Depuy Orthopaedics, Inc. | Bioactive ceramic coating and method |
| US6398814B1 (en) | 1998-09-14 | 2002-06-04 | Bionx Implants Oy | Bioabsorbable two-dimensional multi-layer composite device and a method of manufacturing same |
| CA2377402C (en) | 1999-06-14 | 2011-01-18 | Imperial College Innovations | Silver-containing, sol-gel derived bioglass compositions |
| JP2003521973A (ja) * | 1999-11-30 | 2003-07-22 | ビオンクス インプランツ オサケユイチア | 生体吸収性骨促進性固定プレート |
| JP2004501719A (ja) | 2000-07-03 | 2004-01-22 | オステオテック インコーポレーテッド | 骨から誘導された骨形成性インプラント |
| US7005135B2 (en) * | 2001-01-30 | 2006-02-28 | Ethicon Inc. | Glass scaffolds with controlled resorption rates and methods for making same |
| FI117963B (fi) | 2001-04-26 | 2007-05-15 | Eija Marjut Pirhonen | Luuta korvaavat materiaalit |
| US20040009598A1 (en) | 2001-07-11 | 2004-01-15 | Hench Larry L | Use of bioactive glass compositions to stimulate osteoblast production |
| US6955716B2 (en) | 2002-03-01 | 2005-10-18 | American Dental Association Foundation | Self-hardening calcium phosphate materials with high resistance to fracture, controlled strength histories and tailored macropore formation rates |
| EP1344538A1 (en) | 2002-03-14 | 2003-09-17 | Degradable Solutions AG | Porous biodegradable implant material and method for its fabrication |
| FI120333B (fi) | 2003-08-20 | 2009-09-30 | Bioretec Oy | Huokoinen lääketieteellinen väline ja menetelmä sen valmistamiseksi |
| US20050090905A1 (en) | 2003-10-23 | 2005-04-28 | Hawkins Michael E. | Porous implant with a dried, lubricious when wet, in vivo absorbable coating |
| CA2557231C (en) | 2004-03-05 | 2013-12-31 | The Trustees Of Columbia University In The City Of New York | Multi-phased, biodegradable and osteointegrative composite scaffold for biological fixation of musculoskeletal soft tissue to bone |
| US8163030B2 (en) | 2004-05-06 | 2012-04-24 | Degradable Solutions Ag | Biocompatible bone implant compositions and methods for repairing a bone defect |
| FR2873683B1 (fr) | 2004-07-27 | 2007-06-15 | Inst Nat Sciences Appliq | Bioverre poreux et procede de preparation |
| US20060121609A1 (en) | 2004-09-21 | 2006-06-08 | Yannas Ioannis V | Gradient scaffolding and methods of producing the same |
| US8535357B2 (en) | 2004-12-09 | 2013-09-17 | Biomet Sports Medicine, Llc | Continuous phase compositions for ACL repair |
| US7621963B2 (en) | 2005-04-13 | 2009-11-24 | Ebi, Llc | Composite bone graft material |
| FI20055194A (fi) * | 2005-04-27 | 2006-10-28 | Bioretec Oy | Bioabsorboituva ja bioaktiivinen komposiittimateriaali ja menetelmä komposiitin valmistamiseksi |
| WO2006118554A1 (en) | 2005-05-02 | 2006-11-09 | Shanghai Institute Of Ceramics | A degradable, macroporous bioactive glass scaffold as well as its preparation and manufacturing methods |
| FI20055304L (fi) | 2005-06-13 | 2007-02-20 | Bioretec Oy | Bioabsorboituva implantti, jolla on muuttuva ominaisuus |
| US8690957B2 (en) | 2005-12-21 | 2014-04-08 | Warsaw Orthopedic, Inc. | Bone graft composition, method and implant |
| US20070240601A1 (en) | 2006-04-14 | 2007-10-18 | Ming Cherng Chou | Biodegradable BB Pellet |
| GB0612028D0 (en) | 2006-06-16 | 2006-07-26 | Imp Innovations Ltd | Bioactive glass |
| AU2007265379B9 (en) | 2006-06-29 | 2014-05-29 | Orthovita, Inc. | Bioactive bone graft substitute |
| ES2338694T3 (es) | 2006-09-20 | 2010-05-11 | Inion Oy | Composiciones de vidrio bioactivo. |
| NL1032851C2 (nl) * | 2006-11-10 | 2008-05-14 | Fondel Finance B V | Kit en werkwijze voor het fixeren van een prothese of deel daarvan en/of het vullen van benige defecten. |
| US8753391B2 (en) | 2007-02-12 | 2014-06-17 | The Trustees Of Columbia University In The City Of New York | Fully synthetic implantable multi-phased scaffold |
| ITTO20070373A1 (it) | 2007-05-29 | 2008-11-30 | Torino Politecnico | Coppa acetabolare ceramica monoblocco per protesi d'anca. |
| FR2918658B1 (fr) * | 2007-07-09 | 2010-12-03 | Centre Nat Rech Scient | Verres bioactifs dopes en strontium. |
| US20100136086A1 (en) | 2008-05-12 | 2010-06-03 | Day Thomas E | Dynamic bioactive nanofiber scaffolding |
| KR100932949B1 (ko) | 2008-07-14 | 2009-12-21 | 한국기계연구원 | 계층적 기공구조를 포함하는 다공성 세라믹 볼 및 이의제조방법 |
| US8353966B2 (en) * | 2009-01-15 | 2013-01-15 | The Curators Of The University Of Missouri | Scaffold for bone and tissue repair in mammals |
| WO2011001028A1 (en) | 2009-06-29 | 2011-01-06 | Bonalive Biomaterials Oy | A bioactive glass for use in conditions relating to bone infections |
| WO2011005933A2 (en) | 2009-07-10 | 2011-01-13 | Bio2 Technologies, Inc. | Devices and methods for tissue engineering |
| US20110206828A1 (en) | 2009-07-10 | 2011-08-25 | Bio2 Technologies, Inc. | Devices and Methods for Tissue Engineering |
| US8337875B2 (en) * | 2009-07-16 | 2012-12-25 | The Curators Of The University Of Missouri | Controlling vessel growth and directionality in mammals and implantable material |
| US20110081396A1 (en) | 2009-09-09 | 2011-04-07 | The Ohio State University Research Foundation | Glass ceramic scaffolds with complex topography |
| WO2011044182A2 (en) | 2009-10-07 | 2011-04-14 | Bio2 Technologies, Inc. | Devices and methods for tissue engineering |
| EP2493425B1 (en) | 2009-10-29 | 2016-10-05 | Prosidyan, Inc. | Dynamic bioactive bone graft material and methods for handling |
| CA2779103A1 (en) | 2009-10-29 | 2011-05-05 | Prosidyan, Inc. | Bone graft material |
| CN102596271B (zh) * | 2009-10-29 | 2017-09-08 | 普罗斯蒂安公司 | 具有设计的孔隙率的动态生物活性骨移植物材料 |
| EP2322134B1 (en) | 2009-11-12 | 2012-09-12 | BonAlive Biomaterials Oy | Implantable paste and its use |
| AU2011223652B2 (en) * | 2010-03-03 | 2015-01-29 | Novabone Products, Llc | Devices and methods for the regeneration of bony defects |
| US8734831B2 (en) | 2010-04-16 | 2014-05-27 | Snu R&Db Foundation | Method for manufacturing a porous ceramic scaffold having an organic/inorganic hybrid coating layer containing a bioactive factor |
| CA2797976A1 (en) | 2010-05-06 | 2012-02-23 | Bio2 Technologies, Inc. | Devices and methods for tissue engineering |
| US20120265167A1 (en) | 2010-12-21 | 2012-10-18 | Simonson Rush E | Biocompatible material for orthopedic uses |
| EP2522373A1 (en) | 2011-05-11 | 2012-11-14 | Dentsply IH AB | Biocompatible component |
| RU2665361C2 (ru) | 2011-10-24 | 2018-08-29 | СИНЕРДЖИ БАЙОМЕДИКАЛ ЭлЭлСи | Композиции и их применение в регенерации костей |
| US8449904B1 (en) | 2012-03-26 | 2013-05-28 | Mosci, Corp. | Bioactive glass scaffolds, and method of making |
-
2013
- 2013-03-14 US US13/830,629 patent/US8883195B2/en active Active
-
2014
- 2014-03-14 WO PCT/US2014/026951 patent/WO2014152102A2/en active Application Filing
- 2014-03-14 ES ES14768023T patent/ES2909417T3/es active Active
- 2014-03-14 AU AU2014240175A patent/AU2014240175B2/en active Active
- 2014-03-14 JP JP2016502289A patent/JP6470253B2/ja active Active
- 2014-03-14 CN CN201480015431.3A patent/CN105246519A/zh active Pending
- 2014-03-14 CN CN202010572327.1A patent/CN112023117A/zh active Pending
- 2014-03-14 EP EP14768023.5A patent/EP2968659B1/en active Active
- 2014-03-14 EP EP21218365.1A patent/EP4032559A1/en active Pending
- 2014-11-07 US US14/536,228 patent/US10335516B2/en active Active
-
2019
- 2019-01-17 JP JP2019005634A patent/JP6810331B2/ja active Active
- 2019-07-01 US US16/458,858 patent/US11129925B2/en active Active
-
2021
- 2021-09-27 US US17/485,766 patent/US20220080085A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20220080085A1 (en) | 2022-03-17 |
| EP2968659B1 (en) | 2022-01-05 |
| US20150064229A1 (en) | 2015-03-05 |
| JP6470253B2 (ja) | 2019-02-13 |
| JP2019088825A (ja) | 2019-06-13 |
| WO2014152102A3 (en) | 2015-02-12 |
| US11129925B2 (en) | 2021-09-28 |
| US20140271785A1 (en) | 2014-09-18 |
| EP4032559A1 (en) | 2022-07-27 |
| CN105246519A (zh) | 2016-01-13 |
| CN112023117A (zh) | 2020-12-04 |
| US8883195B2 (en) | 2014-11-11 |
| AU2014240175A1 (en) | 2015-08-13 |
| ES2909417T3 (es) | 2022-05-06 |
| WO2014152102A2 (en) | 2014-09-25 |
| US20200000970A1 (en) | 2020-01-02 |
| AU2014240175B2 (en) | 2017-09-28 |
| EP2968659A2 (en) | 2016-01-20 |
| US10335516B2 (en) | 2019-07-02 |
| EP2968659A4 (en) | 2016-09-14 |
| JP2016515028A (ja) | 2016-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6810331B2 (ja) | 生体活性多孔性骨移植インプラント | |
| US10478528B2 (en) | Bone graft implants containing allograft | |
| JP6416866B2 (ja) | 生体活性多孔性複合骨移植インプラント | |
| US10500312B2 (en) | Bioactive porous bone graft compositions with collagen | |
| US20190099515A1 (en) | Implantable fusion devices comprising bioactive glass | |
| JP5792736B2 (ja) | 人工的に作り出した多孔性を有する動的な生体活性骨移植材料 | |
| KR20120101021A (ko) | 골 이식재 | |
| US20220143271A1 (en) | Reinforced biocompatible scaffold |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190207 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190207 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191218 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200317 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200512 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200731 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20201020 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20201119 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201119 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20201119 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6810331 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |