JP6768697B2 - 頚動脈血流の逆流を確立する方法およびシステム - Google Patents
頚動脈血流の逆流を確立する方法およびシステム Download PDFInfo
- Publication number
- JP6768697B2 JP6768697B2 JP2017552957A JP2017552957A JP6768697B2 JP 6768697 B2 JP6768697 B2 JP 6768697B2 JP 2017552957 A JP2017552957 A JP 2017552957A JP 2017552957 A JP2017552957 A JP 2017552957A JP 6768697 B2 JP6768697 B2 JP 6768697B2
- Authority
- JP
- Japan
- Prior art keywords
- blood flow
- sheath
- access device
- carotid artery
- shunt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- NJQVYYMYVMYHQA-HPFDTCNMSA-N CCC(CC1)[C@@H](C)C1(C1)C2C1C2C Chemical compound CCC(CC1)[C@@H](C)C1(C1)C2C1C2C NJQVYYMYVMYHQA-HPFDTCNMSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3613—Reperfusion, e.g. of the coronary vessels, e.g. retroperfusion
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3653—Interfaces between patient blood circulation and extra-corporal blood circuit
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3653—Interfaces between patient blood circulation and extra-corporal blood circuit
- A61M1/3656—Monitoring patency or flow at connection sites; Detecting disconnections
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M1/00—Suction or pumping devices for medical purposes; Devices for carrying-off, for treatment of, or for carrying-over, body-liquids; Drainage systems
- A61M1/36—Other treatment of blood in a by-pass of the natural circulatory system, e.g. temperature adaptation, irradiation ; Extra-corporeal blood circuits
- A61M1/3621—Extra-corporeal blood circuits
- A61M1/3653—Interfaces between patient blood circulation and extra-corporal blood circuit
- A61M1/3659—Cannulae pertaining to extracorporeal circulation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/10—Balloon catheters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M39/00—Tubes, tube connectors, tube couplings, valves, access sites or the like, specially adapted for medical use
- A61M39/02—Access sites
- A61M39/06—Haemostasis valves, i.e. gaskets sealing around a needle, catheter or the like, closing on removal thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/33—Controlling, regulating or measuring
- A61M2205/3331—Pressure; Flow
- A61M2205/3334—Measuring or controlling the flow rate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2205/00—General characteristics of the apparatus
- A61M2205/75—General characteristics of the apparatus with filters
- A61M2205/7545—General characteristics of the apparatus with filters for solid matter, e.g. microaggregates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M39/00—Tubes, tube connectors, tube couplings, valves, access sites or the like, specially adapted for medical use
- A61M39/22—Valves or arrangement of valves
- A61M39/223—Multiway valves
Description
本出願は、同時係属の米国仮特許出願第62/145,809号(発明の名称「頚動脈血流の逆流を確立する方法およびシステム(METHODS AND SYSTEMS FOR ESTABLISHING RETROGRADE CAROTID ARTERIAL BLOOD FLOW)」、2015年4月10日に出願)の優先権を主張する。上述の出願日の優先権を主張し、この仮特許出願はその全体を参照して本明細書に組み入れる。
本願の開示は、概して、医療方法および医療機器に関する。特に、本願の開示は、頚動脈ステント留置術および他の手技の間に、頚動脈血管にアクセスし、血流の逆流を確立するための方法およびシステムに関する。
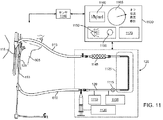
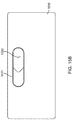
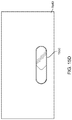
図1Aは、逆流システム100の第1の実施態様を示しており、このシステムは、脳血管(特に内頚動脈)への塞栓の放出を制限または防止するために、頚動脈分岐部の領域内における血液循環の逆流を確立し容易にするのに適している。システム100は、頚動脈と相互に作用して、頚動脈から、例えば内頚静脈(または、別の大静脈や、代わりの実施態様における外部レセプタクルなどの別のリターンサイト)などの静脈リターンサイトに逆流を提供する。逆流システム100は、動脈アクセスデバイス110と、静脈リターンデバイス115と、動脈アクセスデバイス110から静脈リターンデバイス115までの逆流通路を提供するシャント120と、を含んでいる。血流制御アセンブリ125はシャント120と相互に作用する。以下により詳細に記述するように、血流制御アセンブリ125は、総頚動脈から内頚静脈までの逆流を調節しおよび/またはモニターするのに適している。血流制御アセンブリ125は、シャント120、内部の血流パスおよび外部の血流パスのいずれか一方あるいは両方を介して血流パスと相互に作用する。より詳細に下に記述されるように、動脈アクセスデバイス110は少なくとも部分的に、総頚動脈CCAに挿入され、静脈リターンデバイス115は少なくとも部分的に、内頚静脈IJVなどの静脈リターンサイトに挿入される。動脈アクセスデバイス110および静脈リターンデバイス115は、結合位置127a、127bにおいて、シャント120と結合される。総頚動脈を通る血流が遮断される場合、内頚動脈と静脈系との間の自然な圧力勾配によって、血液は、脳血管から内頚動脈とシャント120とを通って静脈系まで、逆方向RG(図2A)に流れる。血流制御アセンブリ125は、逆流する血流を調整し、増大させ(augment)、支援し(assist)、モニターし、および/または別の方法で調節する。
脳の側副血行路(Collateral Brain Circulation)
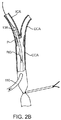
ウィリス輪CWは、脳の主たる動脈吻合の主要部であり、脳に供給する全ての主な動脈、すなわち2本の内頚動脈(ICA)と椎骨脳底動脈系(vertebral basilar system)とが接続する。血液は、ウィリス輪から、前大脳動脈、中大脳動脈および後大脳動脈によって脳まで運ばれる。動脈間のこの連絡は、脳を通る側副血行路(collateral circulation)を形成することができる。代わりのルートを通る血流を形成することができるので、脳に血液を提供する血管の1つ以上が遮断状態(blockage)の場合には、安全機構を提供する。動脈系のどこかが遮断状態にあったとしても(例えば、本願明細書に記述されるようにICAが結紮されたときでも)、脳は、ほとんどの場合、適切な血液供給を受け続けることができる。ウィリス輪を通る血流は、血液の枯渇した側(deprived side)に血液を再分配する多数の経路によって、適切な脳血流を保証する。
図5は、患者の頚部中の関連する血管の拡大図を示す。総頚動脈CCAは、分岐部Bで、内頚動脈ICAおよび外頚動脈ECAに分岐する。分岐部は、ほぼ第4頚椎のレベルに位置する。図5は分岐部Bに生成されたプラークPを示す。
先に述べたように、逆流システム100は、動脈アクセスデバイス110と、静脈リターンデバイス115と、動脈アクセスデバイス110から静脈リターンデバイス115への逆流のための通路を提供するシャント120と、を含んでいる。システムはまた、血流制御アセンブリ125を含んでおり、それはシャント120と相互に作用して、シャント120を介して逆流する血流を調節および/またはモニターする。逆流システム100の構成要素の典型的な実施態様を、ここに記述する。
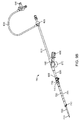
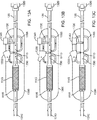
図6Aは、動脈アクセスデバイス110の典型的な実施態様を示しており、遠位シース605、近位伸張部610、血流ライン615、アダプターまたはYコネクター620、および止血バルブ625を含む。動脈アクセスデバイスはまた、先細の先端650を持つ拡張器645およびイントロデューサーガイドワイヤー611を含む。拡張器およびイントロデューサーガイドワイヤーを備える動脈アクセスデバイスは、血管へのアクセスを増加するために共に用いられる。動脈アクセスデバイスの特徴は、経頚部アクセスに最適化できることである。例えば、アクセスデバイスの構成要素の配置を、鋭角の挿入によって血管の潜在的な損傷を制限し、非外傷性および安全なシースの挿入を可能にし、ならびに血管内に挿入するシース、シース拡張器、およびイントロデューサーガイドワイヤーの長さを制限するように、最適化できる。
次に図10を参照すると、静脈リターンデバイス115は、遠位シース910および血流ライン915を含むことができ、システムの使用中、シャント120に接続されてシャント120の脚部を形成する。遠位シース910は、切開または穿刺を通して静脈リターン場所(頚静脈または大腿静脈など)に導入するのに適している。遠位シース910および血流ライン915は永久に取り付けることができ、または、図10Aに示すように、従来のルアーフィッティング(luer fitting)を用いて取り付けることができる。任意で、図10Bに示すように、シース910はYコネクター1005によって血流ライン915に結合することができる。Yコネクター1005は、止血バルブ1010を含んでもよい。静脈リターンデバイスはまた、内頚静脈または他の静脈への静脈リターンデバイスの導入を容易にする、静脈シース拡張器(venous sheath dilator)1015およびイントロデューサーガイドワイヤー611を含む。動脈アクセス拡張器645と同様に、静脈拡張器1015はガイドワイヤーの中央の管腔を含んでおり、それにより、静脈シースと拡張器との組合せをガイドワイヤー611上に設置できる。任意で、静脈シース910は、近位端または遠位端に栓1025を備える洗い流しライン1020を含むことができる。
シャント120は、動脈アクセスカテーテル110と静脈リターンカテーテル115との間の流体の連絡を提供し、それらの間で逆流する血流の経路を提供する単一チューブまたは複数の接続チューブから形成することができる。図1Aに示すように、シャント120は、その一端で、(コネクター127aを介して)動脈アクセスデバイス110の血流ライン615に接続し、他端で、(コネクター127bを介して)静脈リターンカテーテル115の血流ライン915に接続する。
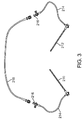
ある。上述のように、シャントの長さは調節できる。ある実施態様において、シャントと動脈および/または静脈アクセスデバイスとの間のコネクターは血流抵抗を最小化するように構成される。ある実施態様において、図1A〜1Dに示すように、動脈アクセスシース110、逆流シャント120および静脈リターンシース115を組み合わせ、低い血流抵抗の動静脈AVシャントを作り出す。上述のように、これら全てのデバイスの接続および血流ラインを最適化し、血流の抵抗を最小化または低減する。ある実施態様において、AVシャントは、動脈シース110内にデバイスがなく、AVシャントが血液の粘度および60mmHgの水圧の静圧を伴う流体源と接続している場合、最大で300mL/分までの血流を可能にする血流抵抗を有する。実際のシャントの抵抗は、(図11に示すような)チェックバルブ(check valve)1115またはフィルター1145の存在の有無、またはシャントの長さに依存して変動してもよく、150乃至300mL/分の血流が可能となり得る。
血流制御アセンブリ125は、逆流シャント120と相互に作用して、総頚動脈から、例えば大腿静脈、内頚静脈などの静脈リターンサイトへの、または外部レセプタクル130への逆流速度を調節および/またはモニターする。これに関して、ユーザーは、血流制御アセンブリ125により、現存のシステムより高い最大血流速度を達成することができ、また、逆流する血流速度を選択的に調節、設定、または調整することができる。以下により完全に記載するように、様々な機構を利用して、逆流速度を調節することができる。以下に記載するように、ユーザーは、血流制御アセンブリ125により、様々な処置法に適した様式で逆流する血流を構成することができる。
コントローラ1130は、逆流の状態に関して、ユーザーに視覚的および/または音声的な信号を提供する1以上のインジケータ(表示部)を含むことができる。音声表示は、ユーザーに対して血流コントローラ1130の視覚的チェックを要求せずに、血流状態をユーザーに気づかせるのに有利である。インジケータは、スピーカー1150および/またはライト1155、またはユーザーに逆流の状態を伝えるためのあらゆる他の手段を含むことができる。コントローラ1130は、システムの1以上のセンサと通じて、インジケータの作動を制御できる。または、インジケータの作動を、血流制御アクチュエーター1165の1つを動かすユーザーと直接結び付けてもよい。インジケータは、スピーカーまたはライトである必要はない。インジケータは、視覚的に逆流の状態を示す単なるボタンまたはスイッチにすることができる。例えば、ある状態(例えば、押されたまたは下がった状態)のボタンは、逆流が速い状態にあることを視覚的に表示してもよい。または、特定のラベルを付けた血流状態を指すスイッチまたはダイヤルが、逆流がラベルを付けた状態にあることを、視覚的に表示してもよい。
コントローラ1130は、ユーザーが押し(press)、切り替え(switch)、操作し(manipulate)、または動かす(actuate)ことのできる1以上のアクチュエーターを含んで、逆流する血流速度を調節し、および/または血流速度をモニターすることができる。例えば、コントローラ1130は、コントローラが逆流の態様を選択的に変更するためにユーザーが動かすことのできる血流制御アクチュエーター1165(例えば、1以上のボタン、ノブ、ダイヤル、スイッチなど)を含むことができる。例えば、図示された実施態様では、血流制御アクチュエーター1165は様々な別個の位置に回転できるノブであり、それぞれはシステム100に特定の逆流状態を達成させるコントローラ1130に対応する。それらの状態は、例えば、(a)オフ(OFF)状態、(b)低流(LO-FLOW)状態、(c)高流(HI-FLOW)状態、および(d)吸引(ASPIRATE)状態を含んでいる。前述の状態は単なる例示であり、異なる状態または状態の組合せも利用できると認識されるべきである。コントローラ1130は、センサ、バルブ、可変抵抗成分および/またはポンプを含むシステムの1以上の構成要素と相互に作用することにより、様々な逆流状態を達成する。コントローラ1130はまた、ユーザーがコントローラ1130を積極的に動かす必要のないように、逆流速度を調節しおよび/または血流速度をモニターする電気回路およびソフトウェアを含むこともできると認識されるべきである。
上述のように、血流制御アセンブリ125は、1以上のセンサを含む、または1以上のセンサと相互に作用することができ、それは、システム100と連絡しており、および/または患者の組織と連絡している。センサの各々は、物理的な刺激(例えば、熱、光、音、圧力、磁気、運動などを含む)に応答するのに適していてもよく、また、計測もしくは表示用、またはコントローラ1130の操作用に得られた信号を伝えるのに適してもよい。ある実施態様では、血流センサ1135はシャント120と相互に作用して、シャント120を通る血流の状況(例えば、血流の流速または容積流量など)を検知する。血流センサ1135は、血流の容積流量または流速の値を直接表示するディスプレイに、直接連結することができる。または、血流センサ1135は、表示用の容積流量または流速のデータをコントローラ1130に入力することができる。
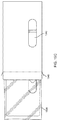
逆流システム100の典型的な実施態様において、逆流システムの全ての構成要素は、動脈シース、動脈シース拡張器、静脈シース、静脈シース拡張器、血流シャント/血流コントローラーおよび1以上のシースガイドワイヤーを含む、単一で無菌のパッケージに共に包装される。一つの構成において、構成要素を段ボールまたはポリマーのカードなどの平らなカード上に乗せ、これは構成要素を受け取り、閉じるようにサイズおよび形が決められる、1以上の開口部または切り抜きを持つ。別の構成において、カードを、パッケージの外形を縮小するよう、本のように、またはあらゆる二つ折り(clamshell)の様式で開閉するように構成する。この実施態様において、カードは、閉じた形態の時に製品の少なくとも一部分が見えるような切り抜きを有してもよい。図15Aは、開いた形態のブックカード(book card)1510上に乗るキットを示す。図15Bは、閉じた形態のブックカードを備えるキットを示す。切り抜き1520は、カードが閉じた形態にあるときでさえ、血流コントローラーハウジング1300など、パッケージデバイスの少なくとも1つの一部分の視覚化を可能にする。図15Cは、無菌の袋1530および棚状のカートン(shelf carton)1540を含む、追加のパッケージの構成要素に挿入されるキットおよびブックカードを示す。この実施態様において、棚状のカートン1540もまた、図15Dに示すように、ブックカード内の切り抜き1520と1列に並び、閉じた棚状のカートンの外側から製品の少なくとも一部分の視覚化を可能にする、切り抜き1550を含む。汚れまたは損傷から無菌の袋を保護するために、ナイロンまたは他の透明なフィルム材料を棚状のカートンの窓に貼ってもよい。
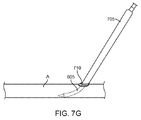
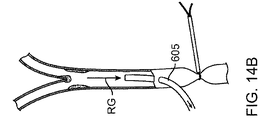
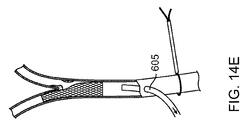
図14A〜14Eを参照すると、本願で開示された方法の異なる段階における頚動脈分岐部を通る血流が記載されている。最初は、図14Aに示すように、動脈アクセスデバイス110の遠位シース605が総頚動脈CCAに導入される。上述のように、総頚動脈CCAへの侵入は、経頚部アプローチまたは経大腿部アプローチを介してなされてもよく、直接の外科的な切開または経皮的アクセスのいずれかでもよい。動脈アクセスデバイス110のシース605が総頚動脈CCAに導入された後、図14Aに示すように、血流は順行性の方向AGで継続し、血流は、総頚動脈から内頚動脈ICAおよび外頚動脈ECAの両方に入るだろう。
Claims (11)
- 経頚部アクセスデバイスであって:
内部管腔を規定するシース本体を有する動脈アクセスシースであって、総頚動脈内に導入され、前記頸動脈から血流を受け取るように、前記シース本体のサイズおよび形が決められる、動脈アクセスシース;
前記シース本体の近位端に取り付ける細長いチューブであって、コネクターが前記チューブを前記シース本体と接続する、細長いチューブ;
前記細長いチューブの近位端にあるアダプターであって、前記アダプターは血流シャントラインと取り外し可能に接続するのに適合しているハブを有し、前記アダプターは前記経頚部アクセスデバイスの内部管腔に近接して配置されるバルブをさらに有し、前記バルブは前記経頚部アクセスデバイスの前記内部管腔から前記ハブに向かう流量を制御する、アダプター;
前記アダプターの近位端に接続する近位伸長部であって、細長い本体から形成された、近位伸長部;
前記近位伸長部が止血バルブを前記アダプターから離して配置するように、前記近位伸長部の近位端にある止血バルブ;および
前記近位伸長部の近位端に接続し、洗い流すための流体の通路を前記シース本体内に提供する、洗い流しラインを含む、経頚部アクセスデバイス。 - 前記細長いチューブを前記アダプターに接続する前記コネクター上に位置する小穴をさらに含む、請求項1記載の経頚部アクセスデバイス。
- 前記バルブが、前記経頚部アクセスデバイスの前記内部管腔からの血流を可能にする開状態と、前記経頚部アクセスデバイスの前記内部管腔からの血流を遮断する閉状態と、の間を移行する、請求項1記載の経頚部アクセスデバイス。
- 前記シース本体の一部を覆い、かつ前記シース本体の一部を露出するように、前記シース本体上に配置できるシースストッパーをさらに含み、前記シースストッパーは、前記頚動脈内への前記シース本体の挿入を前記シース本体の露出された遠位部分に制限し、フランジは前記シースストッパーの遠位端に配置される、請求項1記載の経頚部アクセスデバイス。
- 前記フランジが可膨張性または機械的に拡張可能である、請求項4記載の経頚部アクセスデバイス。
- 経頚部アクセスデバイスであって:
内部管腔を規定するシース本体を有する動脈アクセスシースであって、総頚動脈内に導入され、前記頸動脈から血流を受け取るように、前記シース本体のサイズおよび形が決められる、動脈アクセスシース;
前記シース本体の近位端にあるアダプターであって、前記アダプターは血流シャントラインと取り外し可能に接続するのに適合しているハブを有し、前記アダプターは前記経頚部アクセスデバイスの内部管腔に近接して配置されるバルブをさらに有し、前記バルブは前記経頚部アクセスデバイスの前記内部管腔から前記ハブに向かう流量を制御する、アダプター;
前記アダプターの近位端に接続する近位伸長部であって、細長い本体から形成された、近位伸長部;
前記近位伸長部が止血バルブを前記アダプターから離して配置するように、前記近位伸長部の近位端にある止血バルブ;および
前記近位伸長部の近位端に接続し、洗い流すための流体の通路を前記シース本体内に提供する、洗い流しラインを含む、経頚部アクセスデバイス。 - 前記シース本体を前記アダプターに接続するコネクター上に位置する小穴をさらに含む、請求項6記載の経頚部アクセスデバイス。
- 前記バルブが、前記経頚部アクセスデバイスの前記内部管腔からの血流を可能にする開状態と、前記経頚部アクセスデバイスの前記内部管腔からの血流を遮断する閉状態と、の間を移行する、請求項6記載の経頚部アクセスデバイス。
- 前記シース本体の一部を覆い、かつ前記シース本体の一部を露出するように、前記シース本体上に配置できるシースストッパーをさらに含み、前記シースストッパーは、前記頚動脈内への前記シース本体の挿入を前記シース本体の露出された遠位部分に制限し、フランジは前記シースストッパーの遠位端に配置される、請求項6記載の経頚部アクセスデバイス。
- 前記アダプターの前記ハブと取り外し可能に接続する血流シャントラインをさらに含み、前記血流シャントライン上に単一のハウジングをさらに含み、前記ハウジングは:
前記血流シャントを通して血流の低流状態と高流状態との間を動かすことのできる血流制御要素;
前記血流シャントを通る血流を可能にする開状態と、前記血流シャントを通る血流を遮断する閉状態と、の間を移行できるバルブ;
流体フィルター;および
一方向チェックバルブを含む、請求項1または6に記載の経頚部アクセスデバイス。 - 前記血流シャントラインが前記アクセスデバイスからリターンサイトに流量を切り替える、請求項10記載のデバイス。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562145809P | 2015-04-10 | 2015-04-10 | |
| US62/145,809 | 2015-04-10 | ||
| PCT/US2016/026483 WO2016164606A1 (en) | 2015-04-10 | 2016-04-07 | Methods and systems for establishing retrograde carotid arterial blood flow |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020158552A Division JP7053747B2 (ja) | 2015-04-10 | 2020-09-23 | 頚動脈血流の逆流を確立する方法およびシステム |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018510729A JP2018510729A (ja) | 2018-04-19 |
| JP2018510729A5 JP2018510729A5 (ja) | 2019-05-09 |
| JP6768697B2 true JP6768697B2 (ja) | 2020-10-14 |
Family
ID=57073360
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017552957A Active JP6768697B2 (ja) | 2015-04-10 | 2016-04-07 | 頚動脈血流の逆流を確立する方法およびシステム |
| JP2020158552A Active JP7053747B2 (ja) | 2015-04-10 | 2020-09-23 | 頚動脈血流の逆流を確立する方法およびシステム |
| JP2022058009A Active JP7375088B2 (ja) | 2015-04-10 | 2022-03-31 | 頚動脈血流の逆流を確立する方法およびシステム |
| JP2023182915A Pending JP2024001255A (ja) | 2015-04-10 | 2023-10-25 | 頚動脈血流の逆流を確立する方法およびシステム |
Family Applications After (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020158552A Active JP7053747B2 (ja) | 2015-04-10 | 2020-09-23 | 頚動脈血流の逆流を確立する方法およびシステム |
| JP2022058009A Active JP7375088B2 (ja) | 2015-04-10 | 2022-03-31 | 頚動脈血流の逆流を確立する方法およびシステム |
| JP2023182915A Pending JP2024001255A (ja) | 2015-04-10 | 2023-10-25 | 頚動脈血流の逆流を確立する方法およびシステム |
Country Status (8)
| Country | Link |
|---|---|
| US (4) | US10238853B2 (ja) |
| EP (2) | EP3280354B1 (ja) |
| JP (4) | JP6768697B2 (ja) |
| CN (2) | CN107072769B (ja) |
| AU (3) | AU2016246756B2 (ja) |
| CA (1) | CA2981853C (ja) |
| ES (1) | ES2759930T3 (ja) |
| WO (1) | WO2016164606A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022084915A (ja) * | 2015-04-10 | 2022-06-07 | シルク・ロード・メディカル・インコーポレイテッド | 頚動脈血流の逆流を確立する方法およびシステム |
Families Citing this family (102)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10233085B4 (de) | 2002-07-19 | 2014-02-20 | Dendron Gmbh | Stent mit Führungsdraht |
| US20070225749A1 (en) | 2006-02-03 | 2007-09-27 | Martin Brian B | Methods and devices for restoring blood flow within blocked vasculature |
| US8430837B2 (en) | 2007-02-05 | 2013-04-30 | Boston Scientific Scimed, Inc. | Thrombectomy apparatus and method |
| US10076346B2 (en) | 2007-04-17 | 2018-09-18 | Covidien Lp | Complex wire formed devices |
| US11202646B2 (en) | 2007-04-17 | 2021-12-21 | Covidien Lp | Articulating retrieval devices |
| EP2497520B1 (en) | 2007-07-18 | 2022-04-13 | Silk Road Medical, Inc. | Systems for establishing retrograde carotid arterial blood flow |
| US8858490B2 (en) | 2007-07-18 | 2014-10-14 | Silk Road Medical, Inc. | Systems and methods for treating a carotid artery |
| US11337714B2 (en) | 2007-10-17 | 2022-05-24 | Covidien Lp | Restoring blood flow and clot removal during acute ischemic stroke |
| US10123803B2 (en) | 2007-10-17 | 2018-11-13 | Covidien Lp | Methods of managing neurovascular obstructions |
| EP2231037B1 (en) | 2007-12-26 | 2015-08-12 | Lazarus Effect, Inc. | Retrieval systems |
| BRPI0908500A8 (pt) | 2008-02-22 | 2018-10-23 | Micro Therapeutics Inc | métodos de formação de imagens da restauração do fluxo de sangue em vaso sangüíneo ocludido com trombo, da dissolução parcial ou substancial e do desalojamento de trombo, equipamento auto-expansível de remoção de trombo e massa removível, integrada, de trombo-equipamento |
| US9510854B2 (en) | 2008-10-13 | 2016-12-06 | Boston Scientific Scimed, Inc. | Thrombectomy catheter with control box having pressure/vacuum valve for synchronous aspiration and fluid irrigation |
| WO2012009675A2 (en) | 2010-07-15 | 2012-01-19 | Lazarus Effect, Inc. | Retrieval systems and methods for use thereof |
| WO2012162437A1 (en) | 2011-05-23 | 2012-11-29 | Lazarus Effect, Inc. | Retrieval systems and methods for use thereof |
| US9072624B2 (en) | 2012-02-23 | 2015-07-07 | Covidien Lp | Luminal stenting |
| US10159479B2 (en) | 2012-08-09 | 2018-12-25 | Silk Road Medical, Inc. | Suture delivery device |
| US9314248B2 (en) | 2012-11-06 | 2016-04-19 | Covidien Lp | Multi-pivot thrombectomy device |
| US10076399B2 (en) | 2013-09-13 | 2018-09-18 | Covidien Lp | Endovascular device engagement |
| US9592139B2 (en) | 2013-10-04 | 2017-03-14 | Covidien Lp | Stents twisted prior to deployment and untwisted during deployment |
| CN105722474B (zh) | 2013-11-13 | 2018-09-21 | 柯惠有限合伙公司 | 以原电池方式辅助医疗装置与血栓的附着 |
| US9265512B2 (en) | 2013-12-23 | 2016-02-23 | Silk Road Medical, Inc. | Transcarotid neurovascular catheter |
| US9241699B1 (en) | 2014-09-04 | 2016-01-26 | Silk Road Medical, Inc. | Methods and devices for transcarotid access |
| US10182801B2 (en) | 2014-05-16 | 2019-01-22 | Silk Road Medical, Inc. | Vessel access and closure assist system and method |
| US9883877B2 (en) | 2014-05-19 | 2018-02-06 | Walk Vascular, Llc | Systems and methods for removal of blood and thrombotic material |
| US11027104B2 (en) | 2014-09-04 | 2021-06-08 | Silk Road Medical, Inc. | Methods and devices for transcarotid access |
| ES2770321T3 (es) | 2015-02-04 | 2020-07-01 | Route 92 Medical Inc | Sistema de trombectomía por aspiración rápida |
| US10426497B2 (en) | 2015-07-24 | 2019-10-01 | Route 92 Medical, Inc. | Anchoring delivery system and methods |
| US11065019B1 (en) | 2015-02-04 | 2021-07-20 | Route 92 Medical, Inc. | Aspiration catheter systems and methods of use |
| WO2016130647A1 (en) | 2015-02-11 | 2016-08-18 | Lazarus Effect, Inc. | Expandable tip medical devices and methods |
| US10925709B2 (en) | 2015-04-30 | 2021-02-23 | Silk Road Medical, Inc. | Systems and methods for transcatheter aortic valve treatment |
| US10159779B2 (en) * | 2015-05-04 | 2018-12-25 | Antionette Olivarez | Vital sleeve |
| WO2016197036A1 (en) | 2015-06-03 | 2016-12-08 | Brian Martin | Flexible intravascular treatment devices and associated systems and methods of use |
| DE102015009190A1 (de) * | 2015-07-16 | 2017-01-19 | B. Braun Avitum Ag | Dialysekanüle |
| US10561440B2 (en) | 2015-09-03 | 2020-02-18 | Vesatek, Llc | Systems and methods for manipulating medical devices |
| US10688282B2 (en) | 2015-09-25 | 2020-06-23 | Covidien Lp | Medical device delivery system |
| US10537344B2 (en) | 2015-10-23 | 2020-01-21 | Covidien Lp | Rotatable connection between an intervention member and a manipulation member of an endovascular device |
| US10874410B2 (en) | 2015-11-04 | 2020-12-29 | Covidien Lp | Clot removal by adhesion |
| US10052185B2 (en) | 2016-02-12 | 2018-08-21 | Covidien Lp | Vascular device marker attachment |
| US10265089B2 (en) | 2016-02-12 | 2019-04-23 | Covidien Lp | Vascular device visibility |
| CN113350659A (zh) | 2016-02-24 | 2021-09-07 | 禾木(中国)生物工程有限公司 | 柔性增强的神经血管导管 |
| US10492805B2 (en) | 2016-04-06 | 2019-12-03 | Walk Vascular, Llc | Systems and methods for thrombolysis and delivery of an agent |
| WO2017199670A1 (ja) * | 2016-05-18 | 2017-11-23 | テルモ株式会社 | 血液検査システムおよび血液検査システムの制御方法 |
| CN110381855B (zh) | 2017-01-06 | 2023-07-04 | 因赛普特有限责任公司 | 用于动脉瘤治疗装置的抗血栓涂层 |
| WO2018132387A1 (en) | 2017-01-10 | 2018-07-19 | Route 92 Medical, Inc. | Aspiration catheter systems and methods of use |
| CN110520076B (zh) | 2017-02-21 | 2022-06-03 | 丝路医疗公司 | 血管植入物 |
| US11298145B2 (en) | 2017-05-12 | 2022-04-12 | Covidien Lp | Retrieval of material from vessel lumens |
| US10722257B2 (en) | 2017-05-12 | 2020-07-28 | Covidien Lp | Retrieval of material from vessel lumens |
| US11191555B2 (en) | 2017-05-12 | 2021-12-07 | Covidien Lp | Retrieval of material from vessel lumens |
| US11129630B2 (en) | 2017-05-12 | 2021-09-28 | Covidien Lp | Retrieval of material from vessel lumens |
| US10709464B2 (en) | 2017-05-12 | 2020-07-14 | Covidien Lp | Retrieval of material from vessel lumens |
| CN110612057B (zh) | 2017-06-07 | 2022-05-31 | 柯惠有限合伙公司 | 用于检测中风的系统和方法 |
| US10945746B2 (en) | 2017-06-12 | 2021-03-16 | Covidien Lp | Tools for sheathing treatment devices and associated systems and methods |
| US10478322B2 (en) | 2017-06-19 | 2019-11-19 | Covidien Lp | Retractor device for transforming a retrieval device from a deployed position to a delivery position |
| US10575864B2 (en) | 2017-06-22 | 2020-03-03 | Covidien Lp | Securing element for resheathing an intravascular device and associated systems and methods |
| CN114711851A (zh) | 2017-07-05 | 2022-07-08 | 丝路医疗公司 | 用于经颈动脉进入的方法和装置 |
| US10342686B2 (en) | 2017-08-10 | 2019-07-09 | Covidien Lp | Thin film mesh hybrid for treating vascular defects |
| US11141259B2 (en) | 2017-11-02 | 2021-10-12 | Silk Road Medical, Inc. | Fenestrated sheath for embolic protection during transcarotid carotid artery revascularization |
| US10835398B2 (en) | 2017-11-03 | 2020-11-17 | Covidien Lp | Meshes and devices for treating vascular defects |
| US11058444B2 (en) | 2017-12-11 | 2021-07-13 | Covidien Lp | Electrically enhanced retrieval of material from vessel lumens |
| US10709463B2 (en) | 2017-12-11 | 2020-07-14 | Covidien Lp | Electrically enhanced retrieval of material from vessel lumens |
| AU2019262972A1 (en) | 2018-05-01 | 2020-10-15 | Incept, Llc | Devices and methods for removing obstructive material from an intravascular site |
| US11395665B2 (en) | 2018-05-01 | 2022-07-26 | Incept, Llc | Devices and methods for removing obstructive material, from an intravascular site |
| AU2019269606A1 (en) | 2018-05-17 | 2020-12-03 | Route 92 Medical, Inc. | Aspiration catheter systems and methods of use |
| US20190388107A1 (en) | 2018-06-22 | 2019-12-26 | Covidien Lp | Electrically enhanced retrieval of material from vessel lumens |
| US11471582B2 (en) | 2018-07-06 | 2022-10-18 | Incept, Llc | Vacuum transfer tool for extendable catheter |
| WO2020010310A1 (en) | 2018-07-06 | 2020-01-09 | Imperative Care, Inc. | Sealed neurovascular extendable catheter |
| US11678905B2 (en) | 2018-07-19 | 2023-06-20 | Walk Vascular, Llc | Systems and methods for removal of blood and thrombotic material |
| WO2020023541A1 (en) | 2018-07-24 | 2020-01-30 | Penumbra, Inc. | Apparatus and methods for controlled clot aspiration |
| US11612430B2 (en) | 2019-03-19 | 2023-03-28 | Covidien Lp | Electrically enhanced retrieval of material from vessel lumens |
| US11766539B2 (en) | 2019-03-29 | 2023-09-26 | Incept, Llc | Enhanced flexibility neurovascular catheter |
| WO2020236931A1 (en) * | 2019-05-20 | 2020-11-26 | Neovasc Tiara Inc. | Introducer with hemostasis mechanism |
| CN110251158A (zh) * | 2019-05-28 | 2019-09-20 | 北京悦琦创通科技有限公司 | 一种经颅多普勒系统及经颅多普勒数据处理方法 |
| US11523838B2 (en) | 2019-06-12 | 2022-12-13 | Covidien Lp | Retrieval of material from corporeal lumens |
| US11191558B2 (en) | 2019-06-12 | 2021-12-07 | Covidien Lp | Retrieval of material from corporeal lumens |
| JP2022542148A (ja) * | 2019-07-25 | 2022-09-29 | エムジー ストローク アナリティクス インコーポレイテッド | 脳動脈からの吸引力を向上させるカテーテルシステム |
| US10835258B1 (en) | 2019-08-21 | 2020-11-17 | Lakshmikumar Pillai | Systems and methods for retrograde perfusion and clearance of emboli |
| WO2021076642A1 (en) | 2019-10-15 | 2021-04-22 | Imperative Care, Inc. | Systems and methods for multivariate stroke detection |
| US20220401111A1 (en) * | 2019-10-31 | 2022-12-22 | Silk Road Medical, Inc. | Systems and methods for neurovascular interventions |
| US11395668B2 (en) | 2019-12-12 | 2022-07-26 | Covidien Lp | Electrically enhanced retrieval of material from vessel lumens |
| US11974752B2 (en) | 2019-12-12 | 2024-05-07 | Covidien Lp | Electrically enhanced retrieval of material from vessel lumens |
| US20210315598A1 (en) | 2019-12-18 | 2021-10-14 | Imperative Care, Inc. | Methods of placing large bore aspiration catheters |
| US11633272B2 (en) | 2019-12-18 | 2023-04-25 | Imperative Care, Inc. | Manually rotatable thrombus engagement tool |
| WO2021127004A1 (en) | 2019-12-18 | 2021-06-24 | Imperative Care, Inc. | Methods and systems for treating venous thromboembolic disease |
| WO2021158965A1 (en) | 2020-02-07 | 2021-08-12 | 2Mg, Inc. | Devices and methods for removal of material in a vasculature |
| EP4117762A4 (en) | 2020-03-10 | 2024-05-08 | Imperative Care Inc | NEUROVASCULAR CATHETER WITH INCREASED FLEXIBILITY |
| US11622695B1 (en) | 2020-04-23 | 2023-04-11 | Shifamed Holdings, Llc | Intracardiac sensors with switchable configurations and associated systems and methods |
| CN111568624B (zh) * | 2020-06-01 | 2021-11-26 | 河南省中医院(河南中医药大学第二附属医院) | 鼻腔支架鼻中隔固定器 |
| EP4196205A1 (en) * | 2020-08-11 | 2023-06-21 | Silk Road Medical, Inc. | Balloon catheter for transcarotid procedures |
| US11207497B1 (en) | 2020-08-11 | 2021-12-28 | Imperative Care, Inc. | Catheter with enhanced tensile strength |
| CN116367795A (zh) | 2020-08-25 | 2023-06-30 | 施菲姆德控股有限责任公司 | 可调节的心房间分流器及相关联的系统和方法 |
| CN116322463A (zh) * | 2020-09-28 | 2023-06-23 | 项目莫里股份有限公司 | 用于组合成像和治疗递送或其它用途的逆行和独立可铰接的嵌套导管系统 |
| DE112021000009T5 (de) * | 2020-10-29 | 2022-07-14 | Beijing Wemed Medical Equipment Co., Ltd. | Kraftrückkoppelungsvorrichtung und -verfahren für einen Führungsdraht des Roboters für interventionelle Chirurgie |
| WO2022103973A1 (en) | 2020-11-12 | 2022-05-19 | Shifamed Holdings, Llc | Adjustable implantable devices and associated methods |
| WO2022133302A1 (en) * | 2020-12-18 | 2022-06-23 | Silk Road Medical, Inc. | Vascular conduit to facilitate temporary direct access of a vessel |
| WO2022153259A1 (en) | 2021-01-17 | 2022-07-21 | Inspiremd Ltd. | Shunts with blood-flow indicators |
| EP4313255A1 (en) * | 2021-03-25 | 2024-02-07 | Inspire M.D Ltd | Device for shunting blood between the arterial and venous systems |
| EP4329643A1 (en) | 2021-04-27 | 2024-03-06 | Contego Medical, Inc. | Thrombus aspiration system and methods for controlling blood loss |
| US11963713B2 (en) | 2021-06-02 | 2024-04-23 | Covidien Lp | Medical treatment system |
| US11944374B2 (en) | 2021-08-30 | 2024-04-02 | Covidien Lp | Electrical signals for retrieval of material from vessel lumens |
| WO2023220766A1 (en) * | 2022-05-16 | 2023-11-23 | Three Peaks Medical Pty Ltd | Dilator positioning assembly |
| WO2024064153A1 (en) * | 2022-09-21 | 2024-03-28 | Silk Road Medical, Inc. | Sheaths configured for vascular access |
| WO2024067688A1 (zh) * | 2022-09-29 | 2024-04-04 | 深圳市先健纬康科技有限公司 | 一种体外循环系统 |
Family Cites Families (86)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4301803A (en) | 1978-10-06 | 1981-11-24 | Kuraray Co., Ltd. | Balloon catheter |
| JPS59161808U (ja) | 1983-02-10 | 1984-10-30 | 株式会社日本メディカル・サプライ | 大動脈カニユ−ラ |
| US4865581A (en) | 1987-05-29 | 1989-09-12 | Retroperfusion Systems, Inc. | Retroperfusion control apparatus, system and method |
| AU6376190A (en) | 1989-10-25 | 1991-05-02 | C.R. Bard Inc. | Occluding catheter and methods for treating cerebral arteries |
| US5769830A (en) | 1991-06-28 | 1998-06-23 | Cook Incorporated | Soft tip guiding catheter |
| US5584803A (en) | 1991-07-16 | 1996-12-17 | Heartport, Inc. | System for cardiac procedures |
| JPH07265412A (ja) | 1994-03-31 | 1995-10-17 | Terumo Corp | 血液補助循環装置 |
| JPH0871161A (ja) | 1994-09-12 | 1996-03-19 | Terumo Corp | イントロデューサー |
| US5727594A (en) | 1995-02-09 | 1998-03-17 | Choksi; Pradip | Low actuation pressure unidirectional flow valve |
| CA2218105A1 (en) | 1995-03-30 | 1996-10-03 | Heartport, Inc. | Endovascular cardiac venting catheter and method |
| US6673040B1 (en) | 1996-04-16 | 2004-01-06 | Cardeon Corporation | System and methods for catheter procedures with circulatory support in high risk patients |
| JPH1052490A (ja) | 1996-05-02 | 1998-02-24 | Hagiwara Denki Kk | シャント形成部位における血流状態のモニター装置 |
| US20010049517A1 (en) | 1997-03-06 | 2001-12-06 | Gholam-Reza Zadno-Azizi | Method for containing and removing occlusions in the carotid arteries |
| JPH1033666A (ja) | 1996-07-19 | 1998-02-10 | Buaayu:Kk | バイパスチューブ |
| US5876367A (en) | 1996-12-05 | 1999-03-02 | Embol-X, Inc. | Cerebral protection during carotid endarterectomy and downstream vascular protection during other surgeries |
| US6152912A (en) | 1997-06-10 | 2000-11-28 | Target Therapeutics, Inc. | Optimized high performance spiral-wound vascular catheter |
| US6889082B2 (en) | 1997-10-09 | 2005-05-03 | Orqis Medical Corporation | Implantable heart assist system and method of applying same |
| US5935108A (en) | 1997-11-14 | 1999-08-10 | Reflow, Inc. | Recanalization apparatus and devices for use therein and method |
| US20050131453A1 (en) | 1998-03-13 | 2005-06-16 | Parodi Juan C. | Apparatus and methods for reducing embolization during treatment of carotid artery disease |
| US6206868B1 (en) | 1998-03-13 | 2001-03-27 | Arteria Medical Science, Inc. | Protective device and method against embolization during treatment of carotid artery disease |
| US6540712B1 (en) * | 1998-03-13 | 2003-04-01 | Arteria Medical Science, Inc. | Methods and low profile apparatus for reducing embolization during treatment of carotid artery disease |
| AR017498A1 (es) | 1998-03-13 | 2001-09-12 | Arteria Medical Science Llc | Dispositivo para proteccion contra embolizaciones, en angioplastia de carotida |
| US6423032B2 (en) | 1998-03-13 | 2002-07-23 | Arteria Medical Science, Inc. | Apparatus and methods for reducing embolization during treatment of carotid artery disease |
| US6908474B2 (en) | 1998-05-13 | 2005-06-21 | Gore Enterprise Holdings, Inc. | Apparatus and methods for reducing embolization during treatment of carotid artery disease |
| US6645222B1 (en) | 1998-05-13 | 2003-11-11 | Arteria Medical Science, Inc. | Puncture resistant branch artery occlusion device and methods of use |
| US6936060B2 (en) | 1998-05-13 | 2005-08-30 | Arteria Medical Sciences, Inc. | Apparatus and methods for removing emboli during a surgical procedure |
| DE69940078D1 (de) * | 1998-07-13 | 2009-01-22 | Jms Co Ltd | Medizinische Schlauchverbindungsvorrichtung |
| US6210365B1 (en) | 1998-08-14 | 2001-04-03 | Cardiovention, Inc. | Perfusion catheter system having sutureless arteriotomy seal and methods of use |
| IT1304770B1 (it) | 1998-12-03 | 2001-03-29 | Gioacchino Coppi | Sistema endovascolare per il trattamento delle stenosi carotidee ecatetere per tale sistema. |
| US6161547A (en) | 1999-01-15 | 2000-12-19 | Coaxia, Inc. | Medical device for flow augmentation in patients with occlusive cerebrovascular disease and methods of use |
| US6682505B2 (en) | 1999-03-12 | 2004-01-27 | Arteria Medical Science, Inc. | Catheter for removing emboli from saphenous vein grafts and native coronary arteries |
| US6383172B1 (en) | 1999-04-02 | 2002-05-07 | Coaxia, Inc. | Retrograde venous perfusion with isolation of cerebral circulation |
| EP1194074A4 (en) | 1999-05-19 | 2002-09-11 | Innerdyne Medical Inc | SYSTEM AND METHOD TO ENABLE VASCULAR ACCESS |
| AU781760B2 (en) | 1999-06-14 | 2005-06-09 | W.L. Gore & Associates, Inc. | Methods and low profile apparatus for reducing embolization during treatment of carotid artery disease |
| CA2366813A1 (en) | 2000-01-26 | 2001-08-02 | Heartport, Inc. | Vascular incisor and method |
| US20030191474A1 (en) * | 2000-02-16 | 2003-10-09 | Cragg Andrew H. | Apparatus for performing a discectomy through a trans-sacral axial bore within the vertebrae of the spine |
| US6485502B2 (en) | 2000-03-10 | 2002-11-26 | T. Anthony Don Michael | Vascular embolism prevention device employing filters |
| US6527746B1 (en) | 2000-08-03 | 2003-03-04 | Ev3, Inc. | Back-loading catheter |
| US6582448B1 (en) | 2000-12-21 | 2003-06-24 | Advanced Cardiovascular Systems, Inc. | Vessel occlusion device for embolic protection system |
| US6595980B1 (en) | 2001-02-23 | 2003-07-22 | Coaxia, Inc. | Devices and methods for preventing distal embolization using flow reversal by occlusion of the brachiocephalic artery |
| US7604612B2 (en) | 2001-05-01 | 2009-10-20 | St. Jude Medical, Cardiology Division, Inc. | Emboli protection devices and related methods of use |
| ATE384488T1 (de) | 2001-11-09 | 2008-02-15 | Rubicon Medical Inc | Stent-ablagevorrichtung mit embolieschutz |
| US20030212304A1 (en) | 2002-03-16 | 2003-11-13 | Lattouf Omar M. | Systems and method for practicing counter-cardiac retrograde perfusion |
| US6790043B2 (en) | 2002-03-28 | 2004-09-14 | Board Of Trustees Of The University Of Arkansas | Method and apparatus for surgical training |
| US7033336B2 (en) | 2002-03-29 | 2006-04-25 | Gore Enterprise Holdings, Inc. | Proximal catheter assembly having a relief valve |
| US6855136B2 (en) | 2002-04-03 | 2005-02-15 | Gore Enterprise Holdings, Inc. | Infusion catheter having an atraumatic tip |
| US7223253B2 (en) | 2002-07-29 | 2007-05-29 | Gore Enterprise Holdings, Inc. | Blood aspiration system and methods of use |
| US7776008B2 (en) | 2003-08-08 | 2010-08-17 | Playtex Products, Inc. | Manual breast pump |
| CN100534392C (zh) * | 2003-11-21 | 2009-09-02 | 戴维·W·常 | 用于治疗颈动脉的器械 |
| EP1696806B1 (en) | 2003-11-21 | 2012-08-29 | Silk Road Medical, Inc. | Apparatus for treating a carotid artery |
| US7879011B2 (en) | 2004-11-18 | 2011-02-01 | Silk Road Medical, Inc. | Endoluminal delivery of anesthesia |
| US7833259B2 (en) | 2005-07-25 | 2010-11-16 | Cook Incorporated | Fenestrated endoluminal stent system |
| WO2007033963A1 (en) * | 2005-09-19 | 2007-03-29 | Minvasys | Apparatus and methods for protected angioplasty and stenting at a carotid bifurcation |
| CA2634754A1 (en) * | 2005-12-29 | 2007-07-12 | Nmt Medical, Inc. | Syringe activated-valve for flushing a catheter and methods thereof |
| JP2007301326A (ja) | 2006-05-09 | 2007-11-22 | Akio Ichihara | 深部血管穿刺具 |
| US8460335B2 (en) | 2006-09-11 | 2013-06-11 | Embrella Cardiovascular, Inc. | Method of deflecting emboli from the cerebral circulation |
| EP2497520B1 (en) | 2007-07-18 | 2022-04-13 | Silk Road Medical, Inc. | Systems for establishing retrograde carotid arterial blood flow |
| US20100228269A1 (en) * | 2009-02-27 | 2010-09-09 | Garrison Michi E | Vessel closure clip device |
| US8545432B2 (en) | 2009-06-03 | 2013-10-01 | Silk Road Medical, Inc. | System and methods for controlling retrograde carotid arterial blood flow |
| US8858490B2 (en) * | 2007-07-18 | 2014-10-14 | Silk Road Medical, Inc. | Systems and methods for treating a carotid artery |
| US8343029B2 (en) * | 2007-10-24 | 2013-01-01 | Circulite, Inc. | Transseptal cannula, tip, delivery system, and method |
| US9308348B2 (en) * | 2007-11-21 | 2016-04-12 | Actuated Medical, Inc. | Devices and methods for clearing occlusions and for providing irrigation in in-situ artificial and natural lumens |
| ES2821762T3 (es) * | 2008-02-05 | 2021-04-27 | Silk Road Medical Inc | Sistema de catéter de intervención |
| WO2009099764A1 (en) | 2008-02-05 | 2009-08-13 | Silk Road Medical, Inc. | Interventional sheath with retention features |
| US8574245B2 (en) | 2008-08-13 | 2013-11-05 | Silk Road Medical, Inc. | Suture delivery device |
| JP2012500049A (ja) | 2008-08-13 | 2012-01-05 | シルク・ロード・メディカル・インコーポレイテッド | 縫合糸送達デバイス |
| EP2379129B1 (en) | 2008-12-23 | 2017-09-13 | Silk Road Medical, Inc. | Methods and systems for treatment of acute ischemic stroke |
| US20100204684A1 (en) | 2009-01-13 | 2010-08-12 | Garrison Michi E | Methods and systems for performing neurointerventional procedures |
| US8545552B2 (en) | 2010-02-26 | 2013-10-01 | Silk Road Medical, Inc. | Systems and methods for transcatheter aortic valve treatment |
| WO2012021406A2 (en) | 2010-08-12 | 2012-02-16 | Silk Road Medical, Inc. | Systems and methods for treating a carotid artery |
| JP2014521462A (ja) * | 2011-08-05 | 2014-08-28 | シルク・ロード・メディカル・インコーポレイテッド | 急性虚血性脳卒中を治療するための方法及びシステム |
| US10159479B2 (en) | 2012-08-09 | 2018-12-25 | Silk Road Medical, Inc. | Suture delivery device |
| US10272269B2 (en) | 2012-11-13 | 2019-04-30 | Silk Road Medical, Inc. | Devices and methods for endoluminal delivery of either fluid or energy for denervation |
| WO2014160887A2 (en) * | 2013-03-28 | 2014-10-02 | Silk Road Medical, Inc. | Methods and systems for establishing retrograde carotid arterial blood flow |
| WO2014160613A1 (en) | 2013-03-29 | 2014-10-02 | Silk Road Medical, Inc, | Systems and methods for aspirating from a body lumen |
| US20150080942A1 (en) | 2013-09-13 | 2015-03-19 | Silk Road Medical, Inc. | System and Method for Assisted Manual Compression of Blood Vessel |
| US9265512B2 (en) | 2013-12-23 | 2016-02-23 | Silk Road Medical, Inc. | Transcarotid neurovascular catheter |
| US9241699B1 (en) | 2014-09-04 | 2016-01-26 | Silk Road Medical, Inc. | Methods and devices for transcarotid access |
| US10182801B2 (en) | 2014-05-16 | 2019-01-22 | Silk Road Medical, Inc. | Vessel access and closure assist system and method |
| US11027104B2 (en) | 2014-09-04 | 2021-06-08 | Silk Road Medical, Inc. | Methods and devices for transcarotid access |
| CA2977072A1 (en) | 2015-02-24 | 2016-09-01 | Silk Road Medical, Inc. | Suture delivery device |
| WO2016164606A1 (en) * | 2015-04-10 | 2016-10-13 | Silk Road Medical, Inc. | Methods and systems for establishing retrograde carotid arterial blood flow |
| US10925709B2 (en) | 2015-04-30 | 2021-02-23 | Silk Road Medical, Inc. | Systems and methods for transcatheter aortic valve treatment |
| CN104998334A (zh) | 2015-05-27 | 2015-10-28 | 黄志辉 | 一种动脉鞘管和动脉鞘管的使用方法 |
| CN110520076B (zh) | 2017-02-21 | 2022-06-03 | 丝路医疗公司 | 血管植入物 |
| US11141259B2 (en) | 2017-11-02 | 2021-10-12 | Silk Road Medical, Inc. | Fenestrated sheath for embolic protection during transcarotid carotid artery revascularization |
-
2016
- 2016-04-07 WO PCT/US2016/026483 patent/WO2016164606A1/en unknown
- 2016-04-07 JP JP2017552957A patent/JP6768697B2/ja active Active
- 2016-04-07 CN CN201680002661.5A patent/CN107072769B/zh active Active
- 2016-04-07 AU AU2016246756A patent/AU2016246756B2/en active Active
- 2016-04-07 EP EP16777294.6A patent/EP3280354B1/en active Active
- 2016-04-07 CA CA2981853A patent/CA2981853C/en active Active
- 2016-04-07 EP EP19189904.6A patent/EP3622981A1/en active Pending
- 2016-04-07 US US15/093,406 patent/US10238853B2/en active Active
- 2016-04-07 CN CN202011116482.9A patent/CN112220980B/zh active Active
- 2016-04-07 ES ES16777294T patent/ES2759930T3/es active Active
-
2019
- 2019-03-12 US US16/299,524 patent/US11433226B2/en active Active
-
2020
- 2020-06-17 AU AU2020204046A patent/AU2020204046B2/en active Active
- 2020-09-23 JP JP2020158552A patent/JP7053747B2/ja active Active
-
2021
- 2021-04-22 US US17/237,911 patent/US20210236790A1/en active Pending
- 2021-06-11 US US17/345,544 patent/US20210299425A1/en active Pending
-
2022
- 2022-02-14 AU AU2022200974A patent/AU2022200974B2/en active Active
- 2022-03-31 JP JP2022058009A patent/JP7375088B2/ja active Active
-
2023
- 2023-10-25 JP JP2023182915A patent/JP2024001255A/ja active Pending
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022084915A (ja) * | 2015-04-10 | 2022-06-07 | シルク・ロード・メディカル・インコーポレイテッド | 頚動脈血流の逆流を確立する方法およびシステム |
| JP7375088B2 (ja) | 2015-04-10 | 2023-11-07 | シルク・ロード・メディカル・インコーポレイテッド | 頚動脈血流の逆流を確立する方法およびシステム |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2018510729A (ja) | 2018-04-19 |
| CA2981853A1 (en) | 2016-10-13 |
| JP2021007761A (ja) | 2021-01-28 |
| AU2020204046B2 (en) | 2021-12-02 |
| EP3280354A4 (en) | 2018-12-05 |
| JP2022084915A (ja) | 2022-06-07 |
| CN107072769B (zh) | 2020-11-06 |
| US20210236790A1 (en) | 2021-08-05 |
| US20160296690A1 (en) | 2016-10-13 |
| US20210299425A1 (en) | 2021-09-30 |
| CN107072769A (zh) | 2017-08-18 |
| US11433226B2 (en) | 2022-09-06 |
| US10238853B2 (en) | 2019-03-26 |
| CN112220980A (zh) | 2021-01-15 |
| ES2759930T3 (es) | 2020-05-12 |
| JP7053747B2 (ja) | 2022-04-12 |
| AU2022200974B2 (en) | 2024-03-14 |
| AU2016246756A1 (en) | 2017-10-26 |
| WO2016164606A1 (en) | 2016-10-13 |
| JP7375088B2 (ja) | 2023-11-07 |
| EP3280354B1 (en) | 2019-09-04 |
| CN112220980B (zh) | 2023-12-08 |
| AU2022200974A1 (en) | 2022-03-03 |
| CA2981853C (en) | 2023-09-26 |
| AU2016246756B2 (en) | 2020-03-19 |
| US20190366070A1 (en) | 2019-12-05 |
| AU2020204046A1 (en) | 2020-07-09 |
| EP3280354A1 (en) | 2018-02-14 |
| EP3622981A1 (en) | 2020-03-18 |
| JP2024001255A (ja) | 2024-01-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7053747B2 (ja) | 頚動脈血流の逆流を確立する方法およびシステム | |
| JP5693661B2 (ja) | 頚動脈血流の逆流を確立する方法およびシステム | |
| US11864988B2 (en) | Fenestrated sheath for embolic protection during transcarotid carotid artery revascularization | |
| US20140296769A1 (en) | Methods and Systems for Establishing Retrograde Carotid Arterial Blood Flow | |
| JP2011510796A (ja) | 介入カテーテルシステム及び方法 | |
| US20200397472A1 (en) | Transcarotid vascular access sheath | |
| US20220047267A1 (en) | Balloon catheter for transcarotid procedures | |
| US20210145453A1 (en) | Embolic protection in connection with transcarotid carotid artery revascularization | |
| US20230165696A1 (en) | Stents having bridge length pattern variations |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190327 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190327 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200129 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200212 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200511 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200825 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200923 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6768697 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |