JP6622691B2 - 体外受精技術で使用される方法および品質管理として使用される分子系マウス胚アッセイ - Google Patents
体外受精技術で使用される方法および品質管理として使用される分子系マウス胚アッセイ Download PDFInfo
- Publication number
- JP6622691B2 JP6622691B2 JP2016503087A JP2016503087A JP6622691B2 JP 6622691 B2 JP6622691 B2 JP 6622691B2 JP 2016503087 A JP2016503087 A JP 2016503087A JP 2016503087 A JP2016503087 A JP 2016503087A JP 6622691 B2 JP6622691 B2 JP 6622691B2
- Authority
- JP
- Japan
- Prior art keywords
- embryo
- embryos
- expression
- fluorescence
- stage
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 210000001161 mammalian embryo Anatomy 0.000 title claims description 203
- 238000000034 method Methods 0.000 title claims description 100
- 238000000338 in vitro Methods 0.000 title claims description 29
- 238000003556 assay Methods 0.000 title description 56
- 238000003908 quality control method Methods 0.000 title description 22
- 230000004720 fertilization Effects 0.000 title description 19
- 210000002257 embryonic structure Anatomy 0.000 claims description 168
- 230000014509 gene expression Effects 0.000 claims description 82
- 210000002459 blastocyst Anatomy 0.000 claims description 76
- 108700008625 Reporter Genes Proteins 0.000 claims description 58
- 230000009261 transgenic effect Effects 0.000 claims description 54
- 210000004027 cell Anatomy 0.000 claims description 45
- 239000003550 marker Substances 0.000 claims description 35
- 230000035899 viability Effects 0.000 claims description 35
- 230000001105 regulatory effect Effects 0.000 claims description 32
- 108700019146 Transgenes Proteins 0.000 claims description 29
- 101710126211 POU domain, class 5, transcription factor 1 Proteins 0.000 claims description 27
- 102000034287 fluorescent proteins Human genes 0.000 claims description 18
- 108091006047 fluorescent proteins Proteins 0.000 claims description 18
- 239000005090 green fluorescent protein Substances 0.000 claims description 18
- 238000011156 evaluation Methods 0.000 claims description 17
- 239000003153 chemical reaction reagent Substances 0.000 claims description 16
- 108010043121 Green Fluorescent Proteins Proteins 0.000 claims description 15
- 102000004144 Green Fluorescent Proteins Human genes 0.000 claims description 15
- 108091005957 yellow fluorescent proteins Proteins 0.000 claims description 14
- 230000000694 effects Effects 0.000 claims description 12
- 230000008569 process Effects 0.000 claims description 12
- 108010083123 CDX2 Transcription Factor Proteins 0.000 claims description 11
- 102000006277 CDX2 Transcription Factor Human genes 0.000 claims description 11
- 230000007045 gastrulation Effects 0.000 claims description 11
- 241000124008 Mammalia Species 0.000 claims description 10
- 238000012258 culturing Methods 0.000 claims description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 10
- 108010054624 red fluorescent protein Proteins 0.000 claims description 9
- 108010082025 cyan fluorescent protein Proteins 0.000 claims description 8
- 210000000287 oocyte Anatomy 0.000 claims description 8
- 101100247004 Rattus norvegicus Qsox1 gene Proteins 0.000 claims description 7
- 239000000654 additive Substances 0.000 claims description 7
- 238000005138 cryopreservation Methods 0.000 claims description 6
- 238000011282 treatment Methods 0.000 claims description 6
- 108090000790 Enzymes Proteins 0.000 claims description 5
- 102000004190 Enzymes Human genes 0.000 claims description 5
- 101000928179 Homo sapiens Agouti-related protein Proteins 0.000 claims description 5
- 239000001963 growth medium Substances 0.000 claims description 5
- 102000055839 human AGRP Human genes 0.000 claims description 5
- 210000000472 morula Anatomy 0.000 claims description 5
- 238000003860 storage Methods 0.000 claims description 5
- 238000010257 thawing Methods 0.000 claims description 5
- 241000283073 Equus caballus Species 0.000 claims description 4
- 241001494479 Pecora Species 0.000 claims description 4
- 238000000746 purification Methods 0.000 claims description 4
- 241000894007 species Species 0.000 claims description 4
- 239000006163 transport media Substances 0.000 claims description 3
- 238000004017 vitrification Methods 0.000 claims description 3
- 238000010792 warming Methods 0.000 claims description 3
- 238000012360 testing method Methods 0.000 description 80
- 230000013020 embryo development Effects 0.000 description 60
- 108090000623 proteins and genes Proteins 0.000 description 41
- 239000002609 medium Substances 0.000 description 38
- 230000012010 growth Effects 0.000 description 35
- 241000699666 Mus <mouse, genus> Species 0.000 description 33
- 238000011161 development Methods 0.000 description 33
- 230000018109 developmental process Effects 0.000 description 33
- 239000003921 oil Substances 0.000 description 27
- 102100035423 POU domain, class 5, transcription factor 1 Human genes 0.000 description 26
- 230000029803 blastocyst development Effects 0.000 description 15
- 230000000877 morphologic effect Effects 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 14
- 239000000463 material Substances 0.000 description 12
- 241001465754 Metazoa Species 0.000 description 11
- 230000001779 embryotoxic effect Effects 0.000 description 11
- 102000004169 proteins and genes Human genes 0.000 description 11
- 238000010186 staining Methods 0.000 description 11
- 238000011830 transgenic mouse model Methods 0.000 description 10
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 9
- 238000000386 microscopy Methods 0.000 description 9
- 230000001850 reproductive effect Effects 0.000 description 9
- 230000035945 sensitivity Effects 0.000 description 8
- 238000011144 upstream manufacturing Methods 0.000 description 8
- 239000012636 effector Substances 0.000 description 7
- 231100000238 embryotoxicity Toxicity 0.000 description 7
- 241000699670 Mus sp. Species 0.000 description 6
- -1 Nanog Proteins 0.000 description 6
- 230000004069 differentiation Effects 0.000 description 6
- 230000000670 limiting effect Effects 0.000 description 6
- 238000012546 transfer Methods 0.000 description 6
- 230000000007 visual effect Effects 0.000 description 6
- 101000575041 Homo sapiens Male-enhanced antigen 1 Proteins 0.000 description 5
- 102100025532 Male-enhanced antigen 1 Human genes 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 238000000799 fluorescence microscopy Methods 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 230000036961 partial effect Effects 0.000 description 5
- 241000283690 Bos taurus Species 0.000 description 4
- 108010062540 Chorionic Gonadotropin Proteins 0.000 description 4
- 102000011022 Chorionic Gonadotropin Human genes 0.000 description 4
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 4
- 102000008100 Human Serum Albumin Human genes 0.000 description 4
- 108091006905 Human Serum Albumin Proteins 0.000 description 4
- 102000006830 Luminescent Proteins Human genes 0.000 description 4
- 108010047357 Luminescent Proteins Proteins 0.000 description 4
- 241000699660 Mus musculus Species 0.000 description 4
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 4
- 230000033228 biological regulation Effects 0.000 description 4
- 238000004113 cell culture Methods 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 235000013601 eggs Nutrition 0.000 description 4
- 231100000351 embryotoxic Toxicity 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 238000010195 expression analysis Methods 0.000 description 4
- 229940084986 human chorionic gonadotropin Drugs 0.000 description 4
- 230000008774 maternal effect Effects 0.000 description 4
- 210000001778 pluripotent stem cell Anatomy 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 238000002054 transplantation Methods 0.000 description 4
- 230000002159 abnormal effect Effects 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000003623 enhancer Substances 0.000 description 3
- 238000002073 fluorescence micrograph Methods 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 208000021267 infertility disease Diseases 0.000 description 3
- 238000004020 luminiscence type Methods 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 230000035479 physiological effects, processes and functions Effects 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 238000004451 qualitative analysis Methods 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 231100000419 toxicity Toxicity 0.000 description 3
- 230000001988 toxicity Effects 0.000 description 3
- 102000000905 Cadherin Human genes 0.000 description 2
- 108050007957 Cadherin Proteins 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- 238000000116 DAPI staining Methods 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 101000851376 Homo sapiens Tumor necrosis factor receptor superfamily member 8 Proteins 0.000 description 2
- 101000666896 Homo sapiens V-type immunoglobulin domain-containing suppressor of T-cell activation Proteins 0.000 description 2
- 102100025751 Mothers against decapentaplegic homolog 2 Human genes 0.000 description 2
- 101710143123 Mothers against decapentaplegic homolog 2 Proteins 0.000 description 2
- 102100022670 Nuclear receptor subfamily 6 group A member 1 Human genes 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 101710150336 Protein Rex Proteins 0.000 description 2
- 241000282898 Sus scrofa Species 0.000 description 2
- 108700009124 Transcription Initiation Site Proteins 0.000 description 2
- 102100036857 Tumor necrosis factor receptor superfamily member 8 Human genes 0.000 description 2
- 102100038282 V-type immunoglobulin domain-containing suppressor of T-cell activation Human genes 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 210000000805 cytoplasm Anatomy 0.000 description 2
- 210000001671 embryonic stem cell Anatomy 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 239000012595 freezing medium Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000009931 harmful effect Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 231100000683 possible toxicity Toxicity 0.000 description 2
- 230000035935 pregnancy Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 229910052594 sapphire Inorganic materials 0.000 description 2
- 239000010980 sapphire Substances 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000003104 tissue culture media Substances 0.000 description 2
- 230000002103 transcriptional effect Effects 0.000 description 2
- YMHOBZXQZVXHBM-UHFFFAOYSA-N 2,5-dimethoxy-4-bromophenethylamine Chemical compound COC1=CC(CCN)=C(OC)C=C1Br YMHOBZXQZVXHBM-UHFFFAOYSA-N 0.000 description 1
- 108010006533 ATP-Binding Cassette Transporters Proteins 0.000 description 1
- 102000005416 ATP-Binding Cassette Transporters Human genes 0.000 description 1
- 102100034134 Activin receptor type-1B Human genes 0.000 description 1
- 101710173011 Activin receptor type-1B Proteins 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 102100025683 Alkaline phosphatase, tissue-nonspecific isozyme Human genes 0.000 description 1
- 102100035248 Alpha-(1,3)-fucosyltransferase 4 Human genes 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 101710149863 C-C chemokine receptor type 4 Proteins 0.000 description 1
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 description 1
- 102100032976 CCR4-NOT transcription complex subunit 6 Human genes 0.000 description 1
- 101100257372 Caenorhabditis elegans sox-3 gene Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 108091005944 Cerulean Proteins 0.000 description 1
- 102000009410 Chemokine receptor Human genes 0.000 description 1
- 108050000299 Chemokine receptor Proteins 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 241000579895 Chlorostilbon Species 0.000 description 1
- 102100031196 Choriogonadotropin subunit beta 3 Human genes 0.000 description 1
- 108091005960 Citrine Proteins 0.000 description 1
- 102000010970 Connexin Human genes 0.000 description 1
- 108050001175 Connexin Proteins 0.000 description 1
- 108010069241 Connexin 43 Proteins 0.000 description 1
- 102000001045 Connexin 43 Human genes 0.000 description 1
- 102100024810 DNA (cytosine-5)-methyltransferase 3B Human genes 0.000 description 1
- 101710123222 DNA (cytosine-5)-methyltransferase 3B Proteins 0.000 description 1
- 101150063564 DPPA3 gene Proteins 0.000 description 1
- 101150006195 Dppa4 gene Proteins 0.000 description 1
- 102100031960 E3 ubiquitin-protein ligase TRIM71 Human genes 0.000 description 1
- 108091005947 EBFP2 Proteins 0.000 description 1
- 108091005942 ECFP Proteins 0.000 description 1
- 102000002322 Egg Proteins Human genes 0.000 description 1
- 108010000912 Egg Proteins Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 108010066805 F-Box Proteins Proteins 0.000 description 1
- 102000018700 F-Box Proteins Human genes 0.000 description 1
- 108090000381 Fibroblast growth factor 4 Proteins 0.000 description 1
- 102100028072 Fibroblast growth factor 4 Human genes 0.000 description 1
- 108090000380 Fibroblast growth factor 5 Proteins 0.000 description 1
- 102100028073 Fibroblast growth factor 5 Human genes 0.000 description 1
- 102000004315 Forkhead Transcription Factors Human genes 0.000 description 1
- 108090000852 Forkhead Transcription Factors Proteins 0.000 description 1
- 102100039290 Gap junction gamma-1 protein Human genes 0.000 description 1
- 108010086677 Gonadotropins Proteins 0.000 description 1
- 102000006771 Gonadotropins Human genes 0.000 description 1
- 108010090293 Growth Differentiation Factor 3 Proteins 0.000 description 1
- 102100035364 Growth/differentiation factor 3 Human genes 0.000 description 1
- 108010020382 Hepatocyte Nuclear Factor 1-alpha Proteins 0.000 description 1
- 102100022057 Hepatocyte nuclear factor 1-alpha Human genes 0.000 description 1
- 102100027849 Homeobox protein GBX-2 Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000574445 Homo sapiens Alkaline phosphatase, tissue-nonspecific isozyme Proteins 0.000 description 1
- 101001022185 Homo sapiens Alpha-(1,3)-fucosyltransferase 4 Proteins 0.000 description 1
- 101000922348 Homo sapiens C-X-C chemokine receptor type 4 Proteins 0.000 description 1
- 101000776619 Homo sapiens Choriogonadotropin subunit beta 3 Proteins 0.000 description 1
- 101000881866 Homo sapiens Developmental pluripotency-associated protein 3 Proteins 0.000 description 1
- 101001064500 Homo sapiens E3 ubiquitin-protein ligase TRIM71 Proteins 0.000 description 1
- 101001038874 Homo sapiens Glycoprotein hormones alpha chain Proteins 0.000 description 1
- 101000859754 Homo sapiens Homeobox protein GBX-2 Proteins 0.000 description 1
- 101000994365 Homo sapiens Integrin alpha-6 Proteins 0.000 description 1
- 101000935043 Homo sapiens Integrin beta-1 Proteins 0.000 description 1
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 1
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 1
- 101001109682 Homo sapiens Nuclear receptor subfamily 6 group A member 1 Proteins 0.000 description 1
- 101000584499 Homo sapiens Polycomb protein SUZ12 Proteins 0.000 description 1
- 101000666775 Homo sapiens T-box transcription factor TBX3 Proteins 0.000 description 1
- 101000596543 Homo sapiens THAP domain-containing protein 11 Proteins 0.000 description 1
- 101000835745 Homo sapiens Teratocarcinoma-derived growth factor 1 Proteins 0.000 description 1
- 101000596852 Homo sapiens Testis-expressed protein 19 Proteins 0.000 description 1
- 101000800116 Homo sapiens Thy-1 membrane glycoprotein Proteins 0.000 description 1
- 101000976622 Homo sapiens Zinc finger protein 42 homolog Proteins 0.000 description 1
- 102100032816 Integrin alpha-6 Human genes 0.000 description 1
- 108010041100 Integrin alpha6 Proteins 0.000 description 1
- 102000000426 Integrin alpha6 Human genes 0.000 description 1
- 102100025304 Integrin beta-1 Human genes 0.000 description 1
- 108010022222 Integrin beta1 Proteins 0.000 description 1
- 102000012355 Integrin beta1 Human genes 0.000 description 1
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 1
- 108700021430 Kruppel-Like Factor 4 Proteins 0.000 description 1
- 108091026898 Leader sequence (mRNA) Proteins 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 102000013013 Member 2 Subfamily G ATP Binding Cassette Transporter Human genes 0.000 description 1
- 108010090306 Member 2 Subfamily G ATP Binding Cassette Transporter Proteins 0.000 description 1
- 101100224389 Mus musculus Dppa5a gene Proteins 0.000 description 1
- 101100288960 Mus musculus Lefty1 gene Proteins 0.000 description 1
- 101100310657 Mus musculus Sox1 gene Proteins 0.000 description 1
- 101100310650 Mus musculus Sox18 gene Proteins 0.000 description 1
- 101100257376 Mus musculus Sox3 gene Proteins 0.000 description 1
- 102100038895 Myc proto-oncogene protein Human genes 0.000 description 1
- 101710135898 Myc proto-oncogene protein Proteins 0.000 description 1
- 101150012532 NANOG gene Proteins 0.000 description 1
- 101710093927 Nuclear receptor subfamily 6 group A member 1 Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 102100030702 Polycomb protein SUZ12 Human genes 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 108010017324 STAT3 Transcription Factor Proteins 0.000 description 1
- 102100030054 Secreted frizzled-related protein 2 Human genes 0.000 description 1
- 108050007987 Secreted frizzled-related protein 2 Proteins 0.000 description 1
- 102100024040 Signal transducer and activator of transcription 3 Human genes 0.000 description 1
- 101150001847 Sox15 gene Proteins 0.000 description 1
- 241000862969 Stella Species 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 206010042573 Superovulation Diseases 0.000 description 1
- 102000052935 T-box transcription factor Human genes 0.000 description 1
- 108700035811 T-box transcription factor Proteins 0.000 description 1
- 108010014480 T-box transcription factor 5 Proteins 0.000 description 1
- 102100038409 T-box transcription factor TBX3 Human genes 0.000 description 1
- 102100024755 T-box transcription factor TBX5 Human genes 0.000 description 1
- 102100035063 THAP domain-containing protein 11 Human genes 0.000 description 1
- 101150052863 THY1 gene Proteins 0.000 description 1
- 102100026404 Teratocarcinoma-derived growth factor 1 Human genes 0.000 description 1
- 102100035110 Testis-expressed protein 19 Human genes 0.000 description 1
- 108091036066 Three prime untranslated region Proteins 0.000 description 1
- 102100033523 Thy-1 membrane glycoprotein Human genes 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 101710150448 Transcriptional regulator Myc Proteins 0.000 description 1
- 102100039362 Transducin-like enhancer protein 1 Human genes 0.000 description 1
- 101710101305 Transducin-like enhancer protein 1 Proteins 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- 241000219793 Trifolium Species 0.000 description 1
- 241000545067 Venus Species 0.000 description 1
- 101001029301 Xenopus tropicalis Forkhead box protein D3 Proteins 0.000 description 1
- 102100023550 Zinc finger protein 42 homolog Human genes 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000004952 blastocoel Anatomy 0.000 description 1
- 230000035584 blastogenesis Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000007248 cellular mechanism Effects 0.000 description 1
- 239000011035 citrine Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000004624 confocal microscopy Methods 0.000 description 1
- 108010015426 connexin 45 Proteins 0.000 description 1
- 238000007596 consolidation process Methods 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000008143 early embryonic development Effects 0.000 description 1
- 210000003981 ectoderm Anatomy 0.000 description 1
- 230000002282 effect on embryo Effects 0.000 description 1
- 210000002308 embryonic cell Anatomy 0.000 description 1
- 230000008011 embryonic death Effects 0.000 description 1
- 239000010976 emerald Substances 0.000 description 1
- 229910052876 emerald Inorganic materials 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 230000035558 fertility Effects 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 238000012921 fluorescence analysis Methods 0.000 description 1
- 108010021843 fluorescent protein 583 Proteins 0.000 description 1
- IJJVMEJXYNJXOJ-UHFFFAOYSA-N fluquinconazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1N1C(=O)C2=CC(F)=CC=C2N=C1N1C=NC=N1 IJJVMEJXYNJXOJ-UHFFFAOYSA-N 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 230000006545 glycolytic metabolism Effects 0.000 description 1
- 239000002622 gonadotropin Substances 0.000 description 1
- 239000003966 growth inhibitor Substances 0.000 description 1
- 239000007952 growth promoter Substances 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000009097 homeostatic mechanism Effects 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 208000000509 infertility Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000011344 liquid material Substances 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 108091005949 mKalama1 Proteins 0.000 description 1
- 108091005958 mTurquoise2 Proteins 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000012533 medium component Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 238000007431 microscopic evaluation Methods 0.000 description 1
- 230000006705 mitochondrial oxidative phosphorylation Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000007479 molecular analysis Methods 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000012758 nuclear staining Methods 0.000 description 1
- 150000007523 nucleic acids Chemical group 0.000 description 1
- 230000030648 nucleus localization Effects 0.000 description 1
- 230000000050 nutritive effect Effects 0.000 description 1
- 238000002515 oligonucleotide synthesis Methods 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 210000003101 oviduct Anatomy 0.000 description 1
- 210000004681 ovum Anatomy 0.000 description 1
- 210000002826 placenta Anatomy 0.000 description 1
- 102000004401 podocalyxin Human genes 0.000 description 1
- 108090000917 podocalyxin Proteins 0.000 description 1
- 210000004508 polar body Anatomy 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- 239000012254 powdered material Substances 0.000 description 1
- 230000002250 progressing effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 108020001580 protein domains Proteins 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 230000023895 stem cell maintenance Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 102000035160 transmembrane proteins Human genes 0.000 description 1
- 108091005703 transmembrane proteins Proteins 0.000 description 1
- 210000000143 trophectoderm cell Anatomy 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 239000013598 vector Substances 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New breeds of animals
- A01K67/027—New breeds of vertebrates
- A01K67/0275—Genetically modified vertebrates, e.g. transgenic
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/02—Animal zootechnically ameliorated
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; CARE OF BIRDS, FISHES, INSECTS; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0393—Animal model comprising a reporter system for screening tests
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Zoology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Environmental Sciences (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Biodiversity & Conservation Biology (AREA)
- Animal Husbandry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Analytical Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
本出願は、2013年3月14日に出願された「体外受精技術と共に使用される方法および品質管理として使用される分子系マウス胚アッセイ(A METHOD AND QUALITY CONTROL MOLECULAR BASED MOUSE EMBRYO ASSAY FOR USE WITH IN VITRO FERTILIZATION TECHNOLOGY)」という発明の名称の米国仮出願第61/783,557号の優先権を主張するものであり、その開示内容全体が参照により本明細書に組み込まれる。
プラスチックやガラス製品ならびに、手袋、プレート、培地、化学薬品および油などの他の消耗品の使用と同様に、配偶子および胚の培養は、生殖研究室の不可欠な部分である。IVFの場合、全ての消耗品および材料の品質管理は、胚培養にとって最適な環境を維持し、こうして、正常な胚の生理およびその後の妊娠率を保証するために重要である。従って、いくつかの実施形態は、IVF消耗品および材料の胚に対する影響または効果(例えば、潜在的毒性)を評価する方法に関する。
「トランスジェニック(遺伝子導入)」という用語は、宿主ゲノムに組み込まれたか、宿主細胞内で複製することができ、かつ1種以上の細胞産物の発現を引き起こすことができるDNAのセグメントを意味するかそれに関する。例示的な導入遺伝子は、対応する非形質転換細胞または動物に対して新規な表現型を有する宿主細胞またはそこから発生した動物を提供することができる。「トランスジェニック動物」は、その細胞の少なくとも一部において染色体外因子として存在するかその生殖細胞系DNAに安定に組み込まれた非内因性核酸配列を有する非ヒト動物、通常は哺乳類を意味する。
胚の成長、発生および/または品質に基づいて、臨床的ARTで使用される特定の製品の適合性を評価する。胚発生の定性的スコア化は、例えば、発光、強度もしくは蛍光または色などのあらゆる他の視覚的指標を評価するマーカーの定性的/定量的発現の評価に基づくことができる。いくつかの実施形態では、発現分析と共に胚の形態の評価も実施および利用することができる。
ART製品に関連する胚の影響または毒性を評価するための標準MEAアッセイよりも高レベルの感度を有する方法およびアッセイキットについても同様に本明細書に記載されている。本方法は、少なくとも多能性マーカーに作動可能に連結されたレポーター遺伝子の調節領域を有するトランスジェニック胚を含むアッセイを提供する工程を含むことができる。また、正常な胚発生を促進するかそれを生じさせることが知られている対照製品を提供することができる。対照製品は、ARTにおける試験製品の意図される使用と同じまたは同様の使用を有することができる。
ARTで使用される培地または材料の毒性および生殖不能性などのいくつかの因子は、胚の発生に影響を与える可能性がある。以下の実施例は、最適な培養条件および最適以下の培養条件下での胚の生存度を評価するためのアッセイについて記載する。多能性調節因子が蛍光顕微鏡を用いて可視化された胚を示す。発生のうち1細胞期または2細胞期からの胚発生を評価するために使用される多能性マーカーとしては、例えば、正常な胚発生を保証する役割を担うSOX2、Oct−4、Nanogならびにそれらの上流メディエーターおよび下流エフェクターが挙げられる。
図1は、初期段階のマウスの胚における多能性調節因子Oct−4の発現を示す蛍光顕微鏡写真である。最適な条件(対照)および最適以下の条件(試験)下で2細胞期の胚を生体外で培養した。約48時間後に、この胚をOct−4に特異的な抗体(赤色)で染色し、蛍光顕微鏡により評価した(Oct−4はOct−3/4ともいう)。図1からはっきり分かるように、最適な成長条件下でインキュベートした左側の胚は、均一な染色により十分に発色されている。対照的に、右側の胚盤胞は、最適以下の成長条件下でインキュベートしたものである。右側の胚の右側の細胞には、Oct−4染色の欠如が観察され、これは、最適以下の成長条件により、胚発生の初期段階であっても胚発生の遅れおよびOct−4発現の減少が生じることを実証している。
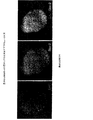
図2Aおよび図2Bは、胚盤胞期でのOct−4の発現を示す。これらの胚を生体外で96時間培養した後、DAPI(青色の核染色、左の画像)および抗Oct−4抗体(赤色、中央の画像)で染色し、蛍光顕微鏡により観察した。各図の右の画像は、DAPI画像とOct−4画像とを1つにまとめた画像を表わし、染色の重なりは紫色で示されている。図2Aには、均一なOct−4染色により実証されるように、最適な成長条件下で正常な胚発生が観察される。対照的に、図2Bの胚は、最適以下の成長条件下でインキュベートしたものである。図2Bに矢印で示されているように、これらの胚には壁のような栄養外胚葉細胞上にOct−4染色の欠如が観察される。最適以下の培養条件は、本特許請求されている技術を使用することなく形態評価の従来のMEA標準QCプロトコルを用いた場合、胚盤胞が正常であるように見え、かつ正常な速度で発生しているように見えるため、最適以下であることが明らかになったり特定可能になったりすることはない。しかし、図2Bにおいて成長の遅さが観察されることで、胚盤胞の発生は、図2Aに観察される胚発生および胚盤胞分化よりも定性的に均一性も最適さも低いことは明らかである。
図3A、図3Bおよび図3Cは、最適な条件または最適以下の条件下で成長させた胚におけるSox2の発現パターンを示す。図3A〜図3Cは、対照のマウスの胚の蛍光顕微鏡写真である。胚を生体外で胚盤胞期までインキュベートし、固定し、DAPI(青色)および抗Sox2抗体(緑色)で染色し、顕微鏡で観察した。図3Aの左側の画像は、96時間の培養後の胚のDAPI染色を示す。図3Aの中央の画像は、Sox2生存度マーカーの染色パターンを示し、右側の画像はそれらを1つにまとめた画像である。胚に観察される染色パターンは均一であり、最適な条件下での正常で健康な胚盤胞発生を証明している。均一な染色ならびに胚盤胞の明瞭な分化に留意されたい。
図4は、本技術の優れた評価または品質管理能力特徴をさらに実証している。図4は、対照のマウスの胚の蛍光顕微鏡写真を表わす。胚を生体外で胚盤胞期までインキュベートし、染色し、顕微鏡で観察した。図4の左側の画像は、96時間の培養後に、固定し、かつDAPI(青色)で染色し、顕微鏡で観察して成長を評価した胚を示す。胚において観察される染色パターンは均一であり、最適な条件下で正常で健康な胚盤胞発生を証明している。図4の中央の画像は、緑色蛍光で染色したCDX−2転写因子を有する胚を示す。図4の右側の画像は、CDX−2染色とDAPI染色とを1つにまとめた画像である。栄養外胚葉には均一な染色が認められるが、内細胞塊には認められないことに留意されたい。矢印は、染色されていない内細胞塊を示す。
多能性マーカーに連結されたレポーター遺伝子を含むトランスジェニックマウスを使用して、最適な条件および最適以下の条件下で、分子系マウス胚アッセイ(mMEA)を行った。POUタンパク質ドメイン、クラス5、転写因子1(Pou5f1、別名:Oct−4)プロモーターおよび遠位エンハンサーの制御下で高感度緑色蛍光タンパク質(EGFP)を発現するトランスジェニック雄マウス(B6、CBA−Tg(Pou5f1−EGFP)2Mnn/J、ジャクソン研究所)を使用した。
1細胞期の胚を、最適な条件および最適以下の条件下で20μLの培地ドロップ当たり3〜4個の胚群で培養した。48時間の培養後に、胚の形態を確認し、発生段階を決定し、GFPの蛍光強度の関数としてOct−4の発現レベルを評価するために、光顕微鏡(立体鏡)およびUV顕微鏡(UV光を備えた倒立顕微鏡)の両方を用いて胚発生を評価した。両方の方法により同じ胚を評価した。光学顕微鏡により決定される胚発生(図5A)は、8細胞期および8細胞期を超える胚の両方を示し、蛍光強度(図5B)により、低強度(光なし〜弱い光、0〜1)または高強度(中〜強い光、2〜3)として特徴づけた。図5Bに示すように、正常な形態を有する8細胞期の胚は、8細胞期の胚の低強度(矢印)により実証されるような低いOct−4の発現を有することがある。
1細胞期の胚を回収し、最適な条件または最適以下の条件下で20μLの培地ドロップ当たり3〜4個の胚群で培養した。48時間後に、2つの評価器により胚の各群の盲検評価を行った。すなわち1つの評価器により、光学顕微鏡(立体鏡)により胚群の形態を決定し、第2の評価器により、胚群の蛍光強度を決定した。96時間後に胚の各群について別の評価を行って、胚盤胞発生を決定した。
実施例3:異なる品質の油の存在下で胚盤胞発生を評価するために使用される分子系マウス胚アッセイ
CDX2−GFPを含むトランスジェニックマウスの胚を使用して、異なる品質の油:(1)良質な油、(2)5%の悪質な油、(3)7.5%の悪質な油、(4)10%の悪質な油および(5)15%の悪質な油の存在下で分子系マウス胚アッセイ(mMEA)を行った。上に列挙した油の品質のそれぞれについて18個の胚を試験した。これらの胚を48時間および96時間後に立体顕微鏡を用いて評価して形態学的に胚盤胞発生を評価し、かつ48時間および96時間後に蛍光顕微鏡を用いてGFPの発現を評価した。従来のMEAプロトコルを用いて、96時間後に80%以上のあらゆる胚のスコア化(拡大した胚盤胞および孵化胚盤胞)がパスすれば、試験したパラメータを利用可能であるとみなす。以下に示すように、形態学的分析のみでは、分子的発現方法ほど高感度でなく、7.5%の悪質な油について1回の偽陽性が生じた。
図8Aは、48時間後の形態評価での胚の早期の卵割発生、具体的には8細胞期未満(青色)の胚の割合および8細胞期以上(赤色)の胚の割合を示す。48時間後に同じ胚のCdx−2発現/蛍光強度も評価した。蛍光について0〜3の相対的かつ主観的な尺度(0は「蛍光なし」を意味し、1は「低い蛍光」を意味し、2は「中間の蛍光」を意味し、かつ3は「高い蛍光」を意味する)で胚を評定した。0〜1(「蛍光なし」または「低い蛍光」、青色)、2〜3(「中間の蛍光」または「高い蛍光」、赤色)として評定された発生中の胚の割合は、図8Bに示されている。
図8Cおよび図8Dは、96時間後に光学顕微鏡(図8C)および蛍光顕微鏡(図8D)により決定された胚盤胞発生(青色:初期の胚盤胞、赤色:胚盤胞、緑色:拡大した胚盤胞、紫色:孵化胚盤胞)を示す。図8Cに示すように、「良質な油」、「5%の悪質な油」および「7.5%の悪質な油」の全てが、MEAまたは形態学的分析を用いて許容されるものとみなされる80%の閾値を満たしている。10%および15%の悪質な油は、80%の閾値に届かなかった。特に96時間後の蛍光強度に関する胚盤胞の評価では、最適な条件と最適以下の条件との間で発生差が区別されない。図8Eは、48時間後に各蛍光強度を示す胚の数として示されるそれらの蛍光状態による各種処理条件下での胚の分布を示す。蛍光について0〜3(0は「蛍光なし」を意味し、1は「低い蛍光」を意味し、2は「中間の蛍光」を意味し、かつ3は「高い蛍光」を意味する)の相対的かつ主観的な尺度で胚を評定した。
以下の表1および表2は、形態評価のみを用いる場合に、7.5%の悪質な油*で偽陽性が生じたことを示している。対照的に、分子系MEAにより、48時間もの早期において最適以下の発生が特定されている。表2のデータにより示されているように、形態のみを用いた場合、7.5%の悪質な油により、80%超のカットオフ値を記録しているが、Cdx−2の発生発現は、それらの胚が7.5%の悪質な油により悪影響を受けていることを実証した。これは、視覚的形態学的分析のみの場合と比較すると、本明細書に記載されている分子系MEAにより提供されるいくつかの実施形態により感度が上昇することを示している。
a.最適以下の培地成分の決定
多能性マーカーに連結されたレポーター遺伝子を含むトランスジェニックマウスの胚を、異なる品質のヒト血清アルブミン(HSA)を含む20μLの培地ドロップでインキュベートした。これらの胚を鉱油で覆い、古典的な細胞培養条件(空気中に5%のCO2を含む湿気のある雰囲気)下、37℃でインキュベートした。48時間および96時間の培養後に、胚を形態およびGFPの発現について評価した。
Claims (26)
- 生殖補助医療(ART)のために使用される製品を評価するための方法であって、
少なくとも1種の胚の生存度マーカーの調節領域に作動可能に連結された少なくとも1種のレポーター遺伝子および/または少なくとも1種の胚の生存度マーカーの調節領域に作動可能に連結された少なくとも1種の導入遺伝子を含む、非ヒト動物由来のトランスジェニック胚を用意する工程と、
前記製品と直接物理的に接触した状態で前記胚を指定された持続期間にわたって生体外で培養する工程と、
前記胚の少なくとも1つの発生段階の間に、前記少なくとも1種のレポーター遺伝子および/または前記導入遺伝子の発現を評価する工程と、
前記評価に基づき、ARTでのその意図される使用と同様の方法で使用される前記製品の許容性または不十分性を決定する工程と、
を含む方法。 - 前記胚の少なくとも1つの発生段階の間に、前記胚の形態を評価する工程をさらに含む、請求項1に記載の方法。
- 前記トランスジェニック胚は、1細胞期または2細胞期の胚である、請求項1に記載の方法。
- 前記トランスジェニック胚は、哺乳類由来である、請求項1に記載の方法。
- 前記哺乳類は、マウス、ブタ、ウマ、ウシ、ヒツジまたは非ヒト霊長類である、請求項4に記載の方法。
- 前記少なくとも1種のレポーター遺伝子は、蛍光タンパク質をコードする、請求項1に記載の方法。
- 前記評価する工程は、前記蛍光タンパク質の蛍光強度を決定する工程を含む、請求項6に記載の方法。
- 前記評価する工程は、
(i)前記胚の少なくとも1つの画像を取得する工程と、
(ii)前記画像に基づき前記レポーター遺伝子の発現レベルを決定する工程と、
を含む、請求項1に記載の方法。 - 工程(ii)をコンピュータにより行う、請求項8に記載の方法。
- (iii)前記発現レベルを閾値レベルおよび/または対照レベルと比較する工程
をさらに含む、請求項8に記載の方法。 - 工程(iii)をコンピュータにより行う、請求項10に記載の方法。
- 前記評価する工程は、前記発現レベルを閾値レベルおよび/または対照レベルと比較する工程を含む、請求項1に記載の方法。
- 前記評価する工程は、前記発現レベルを相対的に比較する工程を含む、請求項1に記載の方法。
- 前記評価する工程は、対照条件下で培養したトランスジェニック胚における前記少なくとも1種のレポーター遺伝子の発現を比較する工程をさらに含む、請求項1に記載の方法。
- 前記少なくとも1つの発生段階は、1細胞期、2細胞期、4細胞期、8細胞期、桑実胚期、胚盤胞期および/または原腸形成期である、請求項1に記載の方法。
- 前記製品は、前記少なくとも1種のレポーター遺伝子の発現が、前記製品の使用により前記胚が影響を受けないことを示すのに十分である場合に許容される、請求項1に記載の方法。
- 前記製品は、針、カテーテル、マイクロツール、実験器具、注射器、組織培養皿、組織培養プレート、ピペットチップ、皿、プレート、水、水精製システム、培地、培地添加物、および配偶子、胚もしくは組織培養培地と物理的に接触する他の容器、装置または試薬からなる群から選択される、請求項1に記載の方法。
- 前記生存度マーカーは、Oct−4、Cdx2、Sox2およびNanogからなる群から選択される、請求項1に記載の方法。
- 前記蛍光タンパク質は、緑色蛍光タンパク質、赤色蛍光タンパク質、黄色蛍光タンパク質またはシアン蛍光タンパク質である、請求項6に記載の方法。
- 生殖補助医療(ART)のために使用される製品を評価するための方法であって、
少なくとも1種の胚の生存度マーカーの調節領域に作動可能に連結された少なくとも1種のレポーター遺伝子を含む、非ヒト動物由来のトランスジェニック胚を用意する工程と、
培養プロセスにおいてARTで使用することが提案されている製品を用いる工程と、
前記胚を指定された持続期間にわたって前記培養プロセスに従って生体外で培養する工程と、
指定された持続期間の少なくとも一部の間に前記培養した胚における前記少なくとも1種のレポーター遺伝子の発現を評価する工程と、
前記少なくとも1種のレポーター遺伝子の発現に基づいて、前記製品を用いることによる前記胚に対する影響を評価する工程と、
前記評価に基づき、前記製品の許容性または不十分性を決定する工程と、
を含む方法。 - 前記製品を、ARTでのその意図される使用と同様の方法で使用する、請求項20に記載の方法。
- 前記胚は、1細胞期または2細胞期の胚である、請求項20に記載の方法。
- 前記製品は、配偶子および胚培養培地、配偶子および胚操作/処理培地、輸送培地、卵母細胞を裸化するための酵素、精子を分離するための勾配試薬、凍結/ガラス化培地、解凍/加温培地、培地添加物、ピペットおよび胚操作装置、ヒトのARTプロセスで使用される実験器具ならびにARTに関わるあらゆる溶液、試薬または装置からなる群から選択される、請求項20に記載の方法。
- ヒトのARTプロセスで使用される実験器具が、遠心管、凍結保存装置、冷凍貯蔵装置、針、カテーテル、マイクロツール、注射器、組織培養皿、組織培養プレート、ピペットチップ、皿、プレート、水、水精製システム、ならびに配偶子と物理的に接触する他の容器、装置または試薬からなる群より選択される、請求項23に記載の方法。
- 前記発現を評価する工程は、ARTでの使用が提案されている前記製品を用いて培養した1つ以上の胚の発現を、前記提案されている製品を用いずに培養した1つ以上の胚の発現と比較する工程を含む、請求項20に記載の方法。
- 前記提案されている製品を用いずに培養した前記1つ以上の胚を、対照製品を用いて培養する、請求項25に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361783557P | 2013-03-14 | 2013-03-14 | |
| US61/783,557 | 2013-03-14 | ||
| PCT/US2014/029410 WO2014153173A1 (en) | 2013-03-14 | 2014-03-14 | A method and quality control molecular based mouse embryo assay for use with in vitro fertilization technology |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016521118A JP2016521118A (ja) | 2016-07-21 |
| JP6622691B2 true JP6622691B2 (ja) | 2019-12-18 |
Family
ID=51581438
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016503087A Active JP6622691B2 (ja) | 2013-03-14 | 2014-03-14 | 体外受精技術で使用される方法および品質管理として使用される分子系マウス胚アッセイ |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20140302493A1 (ja) |
| EP (1) | EP2971059B1 (ja) |
| JP (1) | JP6622691B2 (ja) |
| CN (2) | CN110079605A (ja) |
| AU (1) | AU2014236260B2 (ja) |
| BR (1) | BR112015022446B1 (ja) |
| CA (1) | CA2915540C (ja) |
| WO (1) | WO2014153173A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10667499B2 (en) | 2013-03-14 | 2020-06-02 | FUJIFILM Irvine Scientific, Inc. | Method and quality control molecular based mouse embryo assay for use with in vitro fertilization technology |
| CN107058455B (zh) * | 2016-08-10 | 2021-09-17 | 黑龙江省农业科学院畜牧研究所 | 猪2细胞胚胎体积的测量方法 |
| WO2018044789A1 (en) * | 2016-08-29 | 2018-03-08 | Progena, Inc. | Autologous somatic stem cell therapy, method of controllable preparation of therapeutic composition and procedure of adaptive treatment of ivf patient |
| WO2020031185A2 (en) * | 2018-08-06 | 2020-02-13 | Carmel Diagnostics Ltd. | Cellular tissue analysis method and device |
| CN108986901B (zh) * | 2018-09-14 | 2022-11-29 | 钟影 | Ivf质量控制方法、终端设备及系统 |
| CN110850070B (zh) * | 2019-11-22 | 2021-06-01 | 北京大学 | 一种基于荧光标记转基因动物模型评价化学物质生殖发育毒性的方法 |
| CN113355386B (zh) * | 2021-06-02 | 2022-05-17 | 福建省妇幼保健院 | 一种应用三原核受精卵检测体外受精环境质量的方法 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2430653A1 (en) * | 2000-11-27 | 2002-08-08 | Yissum Research Development Company Of The Hebrew University In Jerusalem | Transfection of human embryonic stem cells |
| US9086403B2 (en) * | 2004-06-03 | 2015-07-21 | The Johns Hopkins University | Methods of screening for cell proliferation or neoplastic disorders |
| WO2006040763A2 (en) * | 2004-10-12 | 2006-04-20 | Technion Research & Development Foundation Ltd. | Isolated primate embryonic cells and methods of generating and using same |
| PL2535403T3 (pl) * | 2005-12-08 | 2019-10-31 | Univ Louisville Res Found Inc | Bardzo małe komórki macierzyste typu embrionalnego (VSEL) oraz sposoby ich izolowania i zastosowania |
| US20070254309A1 (en) * | 2006-04-20 | 2007-11-01 | Northern Sydney And Central Coast Area Health Service | Methods for Assessing Embryo Viability |
| CN101603025B (zh) * | 2008-06-13 | 2011-05-04 | 北京瑞途之星科技有限公司 | 胚胎干细胞样多能性细胞及其制备方法 |
| CN102333861A (zh) * | 2008-09-30 | 2012-01-25 | 路易斯维尔大学研究基金会有限公司 | 用于分离非常小的胚胎样(vsel)干细胞的方法 |
| CN104293646A (zh) * | 2009-08-22 | 2015-01-21 | 里兰斯坦福初级大学理事会 | 成像并评估胚胎、卵母细胞和干细胞 |
| CN102382796B (zh) * | 2010-08-31 | 2014-08-27 | 中国科学院上海生命科学研究院 | 调控胚胎干细胞及早期胚胎的胚层分化的方法和试剂 |
-
2014
- 2014-03-14 CA CA2915540A patent/CA2915540C/en active Active
- 2014-03-14 JP JP2016503087A patent/JP6622691B2/ja active Active
- 2014-03-14 CN CN201910056408.3A patent/CN110079605A/zh active Pending
- 2014-03-14 AU AU2014236260A patent/AU2014236260B2/en active Active
- 2014-03-14 BR BR112015022446-6A patent/BR112015022446B1/pt active IP Right Grant
- 2014-03-14 EP EP14769405.3A patent/EP2971059B1/en active Active
- 2014-03-14 CN CN201480024414.6A patent/CN105431543B/zh active Active
- 2014-03-14 US US14/214,298 patent/US20140302493A1/en not_active Abandoned
- 2014-03-14 WO PCT/US2014/029410 patent/WO2014153173A1/en active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| CN105431543A (zh) | 2016-03-23 |
| CN110079605A (zh) | 2019-08-02 |
| JP2016521118A (ja) | 2016-07-21 |
| EP2971059A1 (en) | 2016-01-20 |
| AU2014236260A1 (en) | 2015-10-22 |
| AU2014236260B2 (en) | 2020-01-16 |
| BR112015022446A2 (ja) | 2017-08-22 |
| BR112015022446B1 (pt) | 2022-05-17 |
| US20140302493A1 (en) | 2014-10-09 |
| CN105431543B (zh) | 2019-02-19 |
| WO2014153173A1 (en) | 2014-09-25 |
| EP2971059B1 (en) | 2019-09-25 |
| CA2915540C (en) | 2021-08-31 |
| CA2915540A1 (en) | 2014-09-25 |
| EP2971059A4 (en) | 2016-10-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6622691B2 (ja) | 体外受精技術で使用される方法および品質管理として使用される分子系マウス胚アッセイ | |
| Posfai et al. | Evaluating totipotency using criteria of increasing stringency | |
| Wakayama et al. | Equivalency of nuclear transfer‐derived embryonic stem cells to those derived from fertilized mouse blastocysts | |
| Hendriks et al. | Artificial gametes: a systematic review of biological progress towards clinical application | |
| Hu et al. | Induction of mouse totipotent stem cells by a defined chemical cocktail | |
| US10667499B2 (en) | Method and quality control molecular based mouse embryo assay for use with in vitro fertilization technology | |
| Zhu et al. | Human embryo polarization requires PLC signaling to mediate trophectoderm specification | |
| Gomes Fernandes et al. | Characterization of migratory primordial germ cells in the aorta-gonad-mesonephros of a 4.5-week-old human embryo: a toolbox to evaluate in vitro early gametogenesis | |
| Jyotsana et al. | Use of peripheral blood for production of buffalo (Bubalus bubalis) embryos by handmade cloning | |
| Wuensch et al. | Quantitative monitoring of pluripotency gene activation after somatic cloning in cattle | |
| Schatten et al. | Cytoskeletal architecture of human oocytes with a focus on centrosomes and their significant role in fertilization | |
| Brooks et al. | Assessing equine embryo developmental competency by time-lapse image analysis | |
| Zhao et al. | Maternal Ezh1/2 deficiency in oocyte delays H3K27me2/3 restoration and impairs epiblast development responsible for embryonic sub-lethality in mouse | |
| Ren et al. | Single-cell transcriptomics reveals male germ cells and Sertoli cells developmental patterns in dairy goats | |
| Durcova‐Hills et al. | Reprogramming primordial germ cells (PGC) to embryonic germ (EG) cells | |
| Gilbert et al. | Genetic mouse embryo assay: improving performance and quality testing for assisted reproductive technology (ART) with a functional bioassay | |
| Frost et al. | Two alternative methods for the retrieval of somatic cell populations from the mouse ovary | |
| JP5030039B2 (ja) | 幹細胞の分化能の評価方法 | |
| JP2010200676A (ja) | 多能性幹細胞の選別方法 | |
| WO2015171250A1 (en) | A method and quality control molecular based mouse embryo assay for use with in vitro fertilization technology | |
| WO2010073760A1 (ja) | 幹細胞の分化能の評価方法 | |
| Noli | Comparative analyses of twin blastocysts | |
| WO2024061369A1 (en) | Composition and methods of aging-related agent screening and target analysis | |
| Dumdie | Molecular Determinants of Oocyte and Embryo Developmental Competence | |
| EP4358707A1 (en) | Method and use of a transgenic mouse line |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20160414 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160510 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170302 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20180131 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180306 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180605 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180705 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20181120 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190219 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190709 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191008 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20191029 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20191122 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6622691 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |