JP6276175B2 - 潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン - Google Patents
潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン Download PDFInfo
- Publication number
- JP6276175B2 JP6276175B2 JP2014506794A JP2014506794A JP6276175B2 JP 6276175 B2 JP6276175 B2 JP 6276175B2 JP 2014506794 A JP2014506794 A JP 2014506794A JP 2014506794 A JP2014506794 A JP 2014506794A JP 6276175 B2 JP6276175 B2 JP 6276175B2
- Authority
- JP
- Japan
- Prior art keywords
- dose
- period
- patient
- day
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000000694 effects Effects 0.000 title claims description 144
- 230000002411 adverse Effects 0.000 title claims description 139
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 201
- 238000000034 method Methods 0.000 claims description 163
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 116
- 238000011282 treatment Methods 0.000 claims description 90
- 210000005259 peripheral blood Anatomy 0.000 claims description 67
- 239000011886 peripheral blood Substances 0.000 claims description 67
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 claims description 66
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 claims description 66
- 230000000926 neurological effect Effects 0.000 claims description 64
- 241000282414 Homo sapiens Species 0.000 claims description 58
- 230000004044 response Effects 0.000 claims description 43
- 229960003008 blinatumomab Drugs 0.000 claims description 35
- 239000008194 pharmaceutical composition Substances 0.000 claims description 32
- 230000003211 malignant effect Effects 0.000 claims description 31
- 210000004027 cell Anatomy 0.000 claims description 28
- 210000004698 lymphocyte Anatomy 0.000 claims description 27
- 206010025323 Lymphomas Diseases 0.000 claims description 26
- 238000006243 chemical reaction Methods 0.000 claims description 25
- 208000032839 leukemia Diseases 0.000 claims description 22
- 208000024891 symptom Diseases 0.000 claims description 20
- 230000001404 mediated effect Effects 0.000 claims description 17
- 206010010904 Convulsion Diseases 0.000 claims description 13
- 230000005856 abnormality Effects 0.000 claims description 10
- 206010003591 Ataxia Diseases 0.000 claims description 9
- 201000007201 aphasia Diseases 0.000 claims description 8
- 230000002490 cerebral effect Effects 0.000 claims description 8
- 230000036461 convulsion Effects 0.000 claims description 8
- 206010044565 Tremor Diseases 0.000 claims description 7
- 206010033799 Paralysis Diseases 0.000 claims description 5
- 230000000737 periodic effect Effects 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 3
- 208000027765 speech disease Diseases 0.000 claims description 2
- 210000003169 central nervous system Anatomy 0.000 description 58
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 44
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 33
- 230000027455 binding Effects 0.000 description 29
- 206010028980 Neoplasm Diseases 0.000 description 23
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 22
- 239000003814 drug Substances 0.000 description 20
- 238000001802 infusion Methods 0.000 description 19
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 17
- 239000000523 sample Substances 0.000 description 17
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 16
- 239000000427 antigen Substances 0.000 description 16
- 108091007433 antigens Proteins 0.000 description 16
- 102000036639 antigens Human genes 0.000 description 16
- 201000011510 cancer Diseases 0.000 description 16
- 125000003275 alpha amino acid group Chemical group 0.000 description 15
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 14
- 230000002354 daily effect Effects 0.000 description 14
- 229940079593 drug Drugs 0.000 description 14
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 13
- 230000001225 therapeutic effect Effects 0.000 description 13
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 12
- 238000001990 intravenous administration Methods 0.000 description 12
- 229920001184 polypeptide Polymers 0.000 description 12
- 102000004196 processed proteins & peptides Human genes 0.000 description 12
- 108090000765 processed proteins & peptides Proteins 0.000 description 12
- 230000008569 process Effects 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 8
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 7
- 230000008499 blood brain barrier function Effects 0.000 description 7
- 210000001218 blood-brain barrier Anatomy 0.000 description 7
- 208000004209 confusion Diseases 0.000 description 7
- 230000000875 corresponding effect Effects 0.000 description 7
- 201000010099 disease Diseases 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 206010013395 disorientation Diseases 0.000 description 7
- 230000000977 initiatory effect Effects 0.000 description 7
- 238000002560 therapeutic procedure Methods 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- 206010019233 Headaches Diseases 0.000 description 6
- 238000002512 chemotherapy Methods 0.000 description 6
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 6
- 231100000869 headache Toxicity 0.000 description 6
- 239000002773 nucleotide Substances 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 210000004881 tumor cell Anatomy 0.000 description 6
- 208000011776 Aggressive B-cell non-Hodgkin lymphoma Diseases 0.000 description 5
- 238000013459 approach Methods 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 239000013610 patient sample Substances 0.000 description 5
- 210000002966 serum Anatomy 0.000 description 5
- 238000011269 treatment regimen Methods 0.000 description 5
- 206010003062 Apraxia Diseases 0.000 description 4
- 208000028564 B-cell non-Hodgkin lymphoma Diseases 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 102000004127 Cytokines Human genes 0.000 description 4
- 108060003951 Immunoglobulin Proteins 0.000 description 4
- 108091028043 Nucleic acid sequence Proteins 0.000 description 4
- 206010037660 Pyrexia Diseases 0.000 description 4
- 230000009831 antigen interaction Effects 0.000 description 4
- 230000009286 beneficial effect Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 230000001472 cytotoxic effect Effects 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 239000012530 fluid Substances 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- 102000018358 immunoglobulin Human genes 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 208000011977 language disease Diseases 0.000 description 4
- 150000007523 nucleic acids Chemical group 0.000 description 4
- 230000001575 pathological effect Effects 0.000 description 4
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 230000002441 reversible effect Effects 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- RTQWWZBSTRGEAV-PKHIMPSTSA-N 2-[[(2s)-2-[bis(carboxymethyl)amino]-3-[4-(methylcarbamoylamino)phenyl]propyl]-[2-[bis(carboxymethyl)amino]propyl]amino]acetic acid Chemical compound CNC(=O)NC1=CC=C(C[C@@H](CN(CC(C)N(CC(O)=O)CC(O)=O)CC(O)=O)N(CC(O)=O)CC(O)=O)C=C1 RTQWWZBSTRGEAV-PKHIMPSTSA-N 0.000 description 3
- 208000004736 B-Cell Leukemia Diseases 0.000 description 3
- 101100383038 Homo sapiens CD19 gene Proteins 0.000 description 3
- 108091008874 T cell receptors Proteins 0.000 description 3
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 239000012472 biological sample Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000001185 bone marrow Anatomy 0.000 description 3
- 238000002591 computed tomography Methods 0.000 description 3
- 206010052015 cytokine release syndrome Diseases 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 230000006735 deficit Effects 0.000 description 3
- 239000012634 fragment Substances 0.000 description 3
- 229960001001 ibritumomab tiuxetan Drugs 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 230000036210 malignancy Effects 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- 210000002381 plasma Anatomy 0.000 description 3
- 230000001052 transient effect Effects 0.000 description 3
- HKZAAJSTFUZYTO-LURJTMIESA-N (2s)-2-[[2-[[2-[[2-[(2-aminoacetyl)amino]acetyl]amino]acetyl]amino]acetyl]amino]-3-hydroxypropanoic acid Chemical compound NCC(=O)NCC(=O)NCC(=O)NCC(=O)N[C@@H](CO)C(O)=O HKZAAJSTFUZYTO-LURJTMIESA-N 0.000 description 2
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 2
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 2
- 208000003950 B-cell lymphoma Diseases 0.000 description 2
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 2
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 2
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 2
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 2
- 206010028813 Nausea Diseases 0.000 description 2
- 206010060860 Neurological symptom Diseases 0.000 description 2
- 206010047700 Vomiting Diseases 0.000 description 2
- 230000006978 adaptation Effects 0.000 description 2
- 238000009175 antibody therapy Methods 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- 238000001574 biopsy Methods 0.000 description 2
- 210000001124 body fluid Anatomy 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 231100000433 cytotoxic Toxicity 0.000 description 2
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 2
- 229940127089 cytotoxic agent Drugs 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 231100000517 death Toxicity 0.000 description 2
- 230000001627 detrimental effect Effects 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 238000012063 dual-affinity re-targeting Methods 0.000 description 2
- 239000012636 effector Substances 0.000 description 2
- 230000003203 everyday effect Effects 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 206010016256 fatigue Diseases 0.000 description 2
- 201000003444 follicular lymphoma Diseases 0.000 description 2
- 230000001900 immune effect Effects 0.000 description 2
- 238000003364 immunohistochemistry Methods 0.000 description 2
- 238000002595 magnetic resonance imaging Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 229960000485 methotrexate Drugs 0.000 description 2
- 230000000116 mitigating effect Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 210000001616 monocyte Anatomy 0.000 description 2
- 230000008693 nausea Effects 0.000 description 2
- 238000011275 oncology therapy Methods 0.000 description 2
- 229960005489 paracetamol Drugs 0.000 description 2
- 238000009521 phase II clinical trial Methods 0.000 description 2
- 230000000750 progressive effect Effects 0.000 description 2
- 125000006850 spacer group Chemical group 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 150000003431 steroids Chemical class 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000011287 therapeutic dose Methods 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- -1 vials Substances 0.000 description 2
- 230000008673 vomiting Effects 0.000 description 2
- SZNGISRDKLUUNN-YLXLXVFQSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s,3s)-2-amino-3-methylpentanoyl]amino]-3-methylbutanoyl]amino]propanoyl]amino]pentanedioic acid Chemical compound CC[C@H](C)[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N[C@H](C(O)=O)CCC(O)=O SZNGISRDKLUUNN-YLXLXVFQSA-N 0.000 description 1
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- SVUOLADPCWQTTE-UHFFFAOYSA-N 1h-1,2-benzodiazepine Chemical compound N1N=CC=CC2=CC=CC=C12 SVUOLADPCWQTTE-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- TVEXGJYMHHTVKP-UHFFFAOYSA-N 6-oxabicyclo[3.2.1]oct-3-en-7-one Chemical compound C1C2C(=O)OC1C=CC2 TVEXGJYMHHTVKP-UHFFFAOYSA-N 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 208000000044 Amnesia Diseases 0.000 description 1
- 102000009075 Angiopoietin-2 Human genes 0.000 description 1
- 108010048036 Angiopoietin-2 Proteins 0.000 description 1
- 108020005098 Anticodon Proteins 0.000 description 1
- 208000019901 Anxiety disease Diseases 0.000 description 1
- 208000006740 Aseptic Meningitis Diseases 0.000 description 1
- 241000937413 Axia Species 0.000 description 1
- 208000025321 B-lymphoblastic leukemia/lymphoma Diseases 0.000 description 1
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 1
- 208000008035 Back Pain Diseases 0.000 description 1
- 206010048962 Brain oedema Diseases 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- 241001631457 Cannula Species 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 206010010301 Confusion and disorientation Diseases 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- WDJUZGPOPHTGOT-OAXVISGBSA-N Digitoxin Natural products O([C@H]1[C@@H](C)O[C@@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@@](C)([C@H](C6=CC(=O)OC6)CC5)CC4)CC3)CC2)C[C@H]1O)[C@H]1O[C@@H](C)[C@H](O[C@H]2O[C@@H](C)[C@@H](O)[C@@H](O)C2)[C@@H](O)C1 WDJUZGPOPHTGOT-OAXVISGBSA-N 0.000 description 1
- 201000008370 Discitis Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 1
- 101000582320 Homo sapiens Neurogenic differentiation factor 6 Proteins 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- 108090001007 Interleukin-8 Proteins 0.000 description 1
- 206010060738 Intervertebral discitis Diseases 0.000 description 1
- 206010027201 Meningitis aseptic Diseases 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 206010051696 Metastases to meninges Diseases 0.000 description 1
- 102100030589 Neurogenic differentiation factor 6 Human genes 0.000 description 1
- 206010067482 No adverse event Diseases 0.000 description 1
- 101710160107 Outer membrane protein A Proteins 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 241000219061 Rheum Species 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 1
- 208000001871 Tachycardia Diseases 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 108020004566 Transfer RNA Proteins 0.000 description 1
- 206010046543 Urinary incontinence Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 206010000269 abscess Diseases 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 208000014619 adult acute lymphoblastic leukemia Diseases 0.000 description 1
- 201000011184 adult acute lymphocytic leukemia Diseases 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000036506 anxiety Effects 0.000 description 1
- 230000006793 arrhythmia Effects 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 230000001174 ascending effect Effects 0.000 description 1
- 229960002707 bendamustine Drugs 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229940049706 benzodiazepine Drugs 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 230000006931 brain damage Effects 0.000 description 1
- 231100000874 brain damage Toxicity 0.000 description 1
- 208000006752 brain edema Diseases 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 230000006041 cell recruitment Effects 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000002577 cryoprotective agent Substances 0.000 description 1
- 231100000409 cytocidal Toxicity 0.000 description 1
- 230000000445 cytocidal effect Effects 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000002498 deadly effect Effects 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000000779 depleting effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 1
- WDJUZGPOPHTGOT-XUDUSOBPSA-N digitoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)CC5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O WDJUZGPOPHTGOT-XUDUSOBPSA-N 0.000 description 1
- 229960000648 digitoxin Drugs 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 208000002173 dizziness Diseases 0.000 description 1
- 210000001951 dura mater Anatomy 0.000 description 1
- 206010013932 dyslexia Diseases 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 238000001839 endoscopy Methods 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 238000011221 initial treatment Methods 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000004904 long-term response Effects 0.000 description 1
- 231100000863 loss of memory Toxicity 0.000 description 1
- 231100000897 loss of orientation Toxicity 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 201000011649 lymphoblastic lymphoma Diseases 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 230000006996 mental state Effects 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 210000004457 myocytus nodalis Anatomy 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- 230000002314 neuroinflammatory effect Effects 0.000 description 1
- 230000035482 neurologic reaction Effects 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 235000003715 nutritional status Nutrition 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 108091033319 polynucleotide Proteins 0.000 description 1
- 102000040430 polynucleotide Human genes 0.000 description 1
- 239000002157 polynucleotide Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 208000017426 precursor B-cell acute lymphoblastic leukemia Diseases 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 238000002864 sequence alignment Methods 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008174 sterile solution Substances 0.000 description 1
- 238000005728 strengthening Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 230000006794 tachycardia Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 206010043554 thrombocytopenia Diseases 0.000 description 1
- 239000000439 tumor marker Substances 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 230000036642 wellbeing Effects 0.000 description 1
- 208000015897 writing disease Diseases 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5094—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for blood cell populations
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
- G01N33/5047—Cells of the immune system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
- A61K2039/507—Comprising a combination of two or more separate antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
Description
抗体は多くの疾患(特に癌)の治療で有効な手段であるが、それらの投与は必ずしも副作用を伴わないわけではない。有害作用は患者の健康状態に可逆的又は不可逆的変化を引き起こし得る。有害作用は有害であり所望されないものであり得るので、それらを回避することが希求される。しかしながら、医薬が有害作用を引き起こし得ることは公知であるが、医薬が甚だしく有益な治療効果を有するか又は救命すら可能であるので、その処方及び投与は避けがたく又は許容されている。
臨床試験では、有害作用(AE)と重篤な有害作用(SAE)との間には大まかな区別が存在し得る。具体的には、有害作用は、有害事象共通用語規準(Common Terminology Criteria for Adverse Events(CTCAE))にしたがって5段階に分類できる。グレード1は軽度のAE、グレード2は中等度AE、グレード3は重篤なAE、グレード4は生命にかかわるか又は身体傷害性AEに関し、一方、グレード5はAE関連死を意味する。
サイトカイン放出及び神経学的反応が、T細胞レセプターに結合モノクローナル抗体だけでなく、T細胞レセプターのCD3部分と結合するCD19xCD3二特異性単鎖抗体(ブリナツモマブ(MT103)と称される)でも観察されている。
ブリナツモマブ(MT103)は、リンパ腫向性の組換え二特異性単鎖CD19xCD3抗体であり、前記はほぼすべてのB細胞及びB腫瘍細胞の表面のCD19と結合し、さらに同時にT細胞を動員し、それによってT細胞の標的B細胞又はB腫瘍細胞殺滅を引き起こす。ブリナツモマブは、単一ポリペプチド鎖として集合させた以下の4つの免疫グロブリン可変ドメインから成る。2つの可変ドメインは、CD19(大半のB細胞及びB腫瘍細胞上で発現される細胞表面抗原)のための結合部位を形成する。他の2つの可変ドメインは、T細胞上のCD3複合体のための結合部位を形成する。ブリナツモマブは、腫瘍細胞に対抗する、身体の細胞傷害性(又は細胞破壊性)T細胞を指向するように設計され、癌療法の新しい治療アプローチである。現在ブリナツモマブは臨床試験中である。
これら望ましくない副作用のより良好な管理を試みるために、CD19xCD3二特異性単鎖抗体の投与態様を、ボーラス輸液から前記抗体のより長時間の持続的な静脈内投与に切り替えた。Bargouらの論文(Science 321(2008):974-7)に示されているように、非ホジキンリンパ腫患者に4週間にわたって持続的に投与された0.005mg/m2/日の低い用量によって、リンパ腫の標的細胞が血中から排除された。部分的及び完全な腫瘍退縮が0.015mg/m2/dの用量レベルで最初に観察され、0.06mg/m2/日の用量レベルで処置された7人全ての患者が腫瘍の退縮を示した(前掲書(Bargou et al.))。CD19xCD3二特異性単鎖抗体はまた、骨髄及び肝臓から腫瘍細胞の除去をもたらした。しかしながら、この試験(なお進行中)は、CD19xCD3二特異性単鎖抗体フォーマットの血液細胞由来癌の治療における治療的潜在能力の概念を臨床的に証明したが、前述の臨床試験の行程中に神経学的反応が認められた。したがって、ブリナツモマブは、非ホジキンリンパ腫(NHL)。急性リンパ芽球性白血病(ALL)、慢性リンパ球性白血病(CLL)及び/又はマントル細胞リンパ腫の治療に非常に有望な候補医薬であるので、その必要がある患者のCD19xCD3二特異性単鎖抗体による治療で望ましくない有害作用を減らすか又は完全に回避することが希求される。
T細胞集団のより緩徐な活性化を可能にする薬学的手段及び方法(WO2007/068354参照)が、CD19xCD3二特異性単鎖抗体処置患者で顕著な有害副作用の回避に既に有益であったが、神経学的反応は、特に5から10マイクログラム/m2/日(すなわち24時間)を超える用量の抗体が投与される事例では残念ながらこれらの手段によっては予防できなかった。
これらの実施態様は、本明細書でその特徴が明らかにされて記載され、特許請求の範囲に反映される。
本開示に引用される全ての刊行物及び特許は参照によりその全体が本明細書に含まれる。参照により含まれる資料が本明細書と矛盾するか又は一致しない範囲に対しては、本明細書がそのような資料に優先するであろう。特段の指示がなければ、一連の要素に先行する“少なくとも”という用語は、当該一連の要素の全てに言及していると理解されるべきである。当業者は、単なる日常的な実験を用いることによって本明細書に記載した本発明の具体的な実施態様と等価の多くの態様を認識し又は確認し得よう。そのような等価物は本発明に包含されるべきものである。
以下の本明細書及び特許請求の範囲を通して、文脈が特段に必要としないならば、“comprise”という語及びその変形(例えば“comprises”及び“comprising”)は、記載の整数若しくは工程又は整数若しくは工程群を含むことを意味するが、他の任意の整数若しくは工程又は整数若しくは工程群を排除しない。
いくつかの文書類が本明細書の本文を通して引用される。本明細書に引用された前記文書類の各々(全ての特許、特許出願、学術刊行物、製造業者の仕様書、指示書などを含む)が、(上記又は下記を問わず)参照により本明細書にその全体が含まれる。本明細書のそのような引用のいずれも、本発明が先行発明の理由からそのような引用に先行する資格を与えられないことを容認するものと解されるべきではない。
具体的には、本発明者らは、CD19xCD3二特異性抗体を投与された患者は、約1.5以下のB:T細胞比又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する場合CNS事象に遭遇することを観察した。したがって、白血病及びリンパ腫で発生する悪性のCD19陽性リンパ球の治療において、本発明は初めて、低B:T細胞比又は低総B細胞数を、神経学的反応を含む有害作用発生の潜在的な高リスク因子として確立させた(実施例2、3及び4を参照されたい)。
特に、本出願の発明者らは、低B:T細胞比又は末梢血の低総B細胞数を示す非ホジキンリンパ腫(NHL)患者及び急性リンパ芽球性白血病(ALL)患者は、早期神経学的反応発達のリスクが高まることを観察した。この神経学的反応は主にCD19xCD3二特異性抗体による治療の初日に発生する。特に、神経学的反応の大半は治療開始後約12から120時間後に発生した。これらの神経学的反応は一過性で完全に可逆性であり、治療停止後3から72時間以内に後遺症を伴うことなく消散した。本発明者らは、CD19xCD3二特異性抗体を用いた多様な臨床試験でこれらの予期せぬ観察を得た。
NHL臨床試験(上記で引用したBargou et al.を参照されたい)では、総計39人の患者が2008年8月まで処置された。この時点で、CD19xCD3二特異性抗体治療の永久的中断に至った神経学的反応を示す全ての患者が、低B:T細胞比(すなわち約1.5より低いB:T細胞比閾値)を有していることが見出された。特に、低B:T細胞比を示す10人の患者で5神経学的反応が観察され(5/10)、一方、高B:T細胞比(すなわち1.5より高いB:T細胞比)を有する患者はいずれも、CD19xCD3二特異性抗体処置の永久的中断に至ることになる神経学的反応を示さなかった(0/29)。
その後、当該概略理論の予測的分析を実施するため及びリスクが上昇した患者のために特に軽減工程を見出すために、低B:T細胞比及び/又は低総B細胞数(すなわち早期神経学的反応のリスク上昇)を示す患者の特異的コホートを確立した。
別のフェーズII臨床試験では、患者の体表面積1m2当たり15μg/日のCD19xCD3二特異性抗体が、少なくとも4週間持続輸液によって成人ALL患者に投与された。B:T細胞比が1:5未満の高リスクグループの11人のALL患者のうちの1人が神経学的反応を示し、治療の中断に至った。対照的に、B:T細胞比が1.5より高い低リスクグループの6人の患者のいずれも神経学的反応を示さなかった。
さらにまた、39人のNHL患者の遡及的分析で、末梢血における1:5以下から1:10のベースラインB細胞対T細胞(B:T)比は、その後の神経学的AEの発生の唯一の予測因子と認定された。この予測値は続いて8人のさらに別の患者で予測的に確認された(実施例1参照)。
これらのデータは、CD19xCD3二特異性抗体で治療される患者の白血病及びリンパ腫(例えばNHL、MCL、CLL及びALL)で生じる悪性CD19陽性リンパ球の治療時の有害作用(神経学的反応を含む)発生の潜在的高リスク因子として、低B:T細胞比(すなわち約1.5以下のB:T細胞比)を確立させた(実施例1及び4参照)。
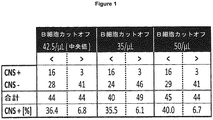
より具体的には、評価可能な全ての患者を、それら患者の個々の末梢血における最初のB細胞数の中央値(中央値42.5/マイクロリットル)によって分析したとき、この中央値より低い44人のうち16人の患者がCNS事象を有し(36.4%)、一方、この中央値を超える44人のうち3人の患者がCNS事象を有し(6.8%)、特記すれば中央値を示す1人の患者はCNS事象を示さなかった。
特記すれば、高総B細胞数を示すグループでCNS事象を示した3人の患者はいずれも、彼らを他の大半の患者から区別する細目を有していた。例えば、2人の患者は、開始用量としてMTDを超えていると決定された90μg/m2/日の最高用量を投与されていたし、第三の患者はブリナツモマブの小休止と再開の後でのみ治療を中断した(これは新規な治療サイクルとは考えられず、したがって再開前のB細胞数ではなく最初のB細胞数が用いられた)。再開前の総B細胞数が用いられていたならば、この患者はまた35/μL未満のB細胞数の患者グループに分類されていたであろう。
同様に、有害作用リスクを評価するために約50/マイクロリットル(50/μL)のB細胞数をカットオフと考えることは、カットオフとして中央値を用いる場合とほぼ同一である。すなわち、低B細胞数(<50/μL)を示す45人の患者のうち16人がCNS事象を示し(40.0%)、一方、高B細胞数(>50/μL)を示す44人の患者のうち3人がCNS事象を示した(6.7%).この情報の要旨については図1を参照されたい。
同様に、ブリナツモマブ治療の開始前の中央値の総B細胞数は、永久的中断に至るCNS事象を示さない全患者について113.25/μLで、そのようなCNS事象を示す全患者については1.12/μLであった。
したがって、CD19xCD3二特異性抗体で処置されたとき、有害作用を惹起するリスクがあり得る患者の認定を可能にする方法を提供することが本発明の目的であった。本方法は、薬剤コンプライアンスを改善するであろう。なぜならば、有害作用を惹起するリスクがある患者の認定は、CD19xCD3二特異性抗体の投薬レジメンの調節を可能にするからである。実際、本発明者らは、約1.5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数は、CD19xCD3二特異性抗体治療で有害作用を惹起する潜在的なリスク因子であり得るという本発明者らの発見を活用し、したがってこれらの有害作用を予防及び/又は改善するために投薬レジメンを開発した。
“リスクを評価(分析)する”ということは、本発明の第一の特徴の方法が、患者が有害作用に遭遇する高い又は低い蓋然性又は確率を有するか否かに関して評価又は分析しようとすることを意味する。したがって、一般的に知られているように、リスクは患者が有害作用に遭遇する又は遭遇しないということを必ずしも意味しない。
本発明では、患者が約1:5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有するとき、前記患者は高い潜在的有害作用リスク(有害作用の開始リスクもまた含む)を有し、一方、約1:5より高いB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞を超える総B細胞数を有する患者は前記リスクをもたないか、又は少なくとも低い潜在的有害作用リスク(有害作用の開始リスクもまた含む)を有する。
したがって、本発明の第一の特徴の方法の関係で用いられるとき“〜の指標である”という用語は、B:T細胞比が約1:5以下である場合及び/又は総B細胞数が末梢血1マイクロリットル当たり約50B細胞未満である場合、患者は高い潜在的有害作用リスクを有すること、又はB:T細胞比が約1:5より高い場合及び/又は総B細胞数が末梢血1マイクロリットル当たり約50B細胞より高い場合、患者は低い潜在的有害作用リスクを有することを意味する。
“有害作用”は、CD19xCD3二特異性抗体による患者の治療で投薬により生じる有害で望ましくない作用である。有害作用(adverse effect)はまた“副作用(side effect)”とも呼ぶことができる。いくつかの有害作用は、中断治療を開始するとき又は強めるときにのみ発生する。本発明者らは、CD19xCD3二特異性抗体による患者の処置で認められる有害作用は、処置の開始後12から120時間後に発生し可逆性であることを認めた。
しかしながら本明細書に記載したように、本発明者らは、B:T細胞比及び/又は総B細胞数は、患者が潜在的有害副作用リスクを示すか否かの指標であることを見出した。具体的には、約1:5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数は、患者が潜在的副作用リスクを示すことの指標であり、一方、約1:5より高いB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞を超える総B細胞数は、患者が前記リスクをもたないか又は潜在的副作用リスクが低いことの指標である。
前述のように、本発明の第一の特徴の方法は有害作用リスクの評価(分析)のためであり、前記はリスクの蓋然性又は確率の評価/分析を含む。したがって、有害作用の関係で用いられるとき“潜在的”という用語は、患者が約1:5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有したとしても、前記患者が必ずしも有害作用に遭遇する必要はないことを意味する。
本発明にしたがえば、有害作用は、好ましくは神経学的反応を特徴とする(前記反応はまた本明細書では時に“CNS反応”又は“CNS事象”と称され、そのためにこれら用語は等しく用いられ得る)。前記神経学的反応は、好ましくは錯乱、運動失調、見当識障害、発語異常、失語症、言語障害、小脳症状、振せん、失行症、痙攣、大発作痙攣、麻痺及び平衡異常から成る群から選択される1つ以上の反応である。
グレード1:軽度の有害作用
グレード2:中等度の有害作用
グレード3:重篤な有害作用
グレード4:生命に危険が及ぶ又は身体損傷をもたらす有害作用
グレード5:患者の死亡
本発明の第一の特徴の方法の関係で用いられるとき、“〜によって媒介される”は、患者が遭遇する可能性がある又は可能性がない有害作用がCD19xCD3二特異性抗体の投与によって引き起こされることを意味する。換言すれば、CD19xCD3抗体は、患者で潜在的有害作用を引き起こし得る原因因子である。
投与はボーラス投与又は持続投与の形態であり、持続投与が好ましい。
本発明にしたがえば、“サンプル”とは、人間の患者から入手される、ポリヌクレオチド又はポリペプチド又は前記の部分を含む任意の生物学的サンプルを意図する。生物学的サンプルには、体液(例えば血液、血清、血漿、尿、唾液、髄液及び脊髄液)及び悪性CD19陽性リンパ球が見出される組織源が含まれる。患者から組織生検及び体液を入手する方法は当業界では周知である。一般的には、末梢血単核球(PBMC)、特にB細胞及びT細胞を含む生物学的サンプルが供給源として好ましい。末梢血単核球(PBMC)、特にB細胞及びT細胞を含むサンプルは、好ましくは人間の患者の末梢血から採取される。
他の好ましいサンプルは、全血、血清、血漿又は髄液であり、血漿又は血清がもっとも好ましい。しかしながら、人間の患者の末梢血由来サンプルが特に好ましい。
本発明にしたがって処置された患者集団のB:T細胞比は、好ましくは約1.5以下(約1:6、1:7、1:8、1:9、1:10、1:11、1:12、1:13、1:14、1:15、1:20、1:100、1:200、1:400、1:500、1:1000、1:2000、1:3000、1:4000、1:5000又は前記より低いB:T細胞比を含む)であり、約1:8、1:9、1:10、1:50、1:100、1:500、1:1000未満は前記患者の潜在的有害作用リスクの指標である。
“B:T細胞比を決定する”とは以下の工程を含む:
(a)患者のサンプルで、好ましくは患者の末梢血サンプルで総B細胞数を決定する工程;
(b)患者のサンプルで、好ましくは患者の末梢血サンプルで総T細胞数を決定する工程;
(c)工程(a)のB細胞数と工程(b)のT細胞数との比を決定してB:T細胞比を得る工程。
特記すれば、低B:T細胞比は高T:B細胞比と見ることができ、逆もまた真なりである。したがって、低B:T細胞比として本明細書で提供される比は逆にする必要があろう。
対照的に、約1:5より高いB:T細胞比(約1:4、1:3、1:2、1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、10:1又はそれより高いB:T細胞比を含む)を示す患者は、CD19xCD3二特異性抗体の投与に際して潜在的有害作用を示すリスクが低い。したがって、これらの患者は、T細胞と比較してより多数のB細胞及びCNS事象のリスク患者と比較してより多数のB細胞を有する。
患者の総B細胞数は、好ましくは末梢血1マイクロリットル当たり約50B細胞以上であり、好ましくは末梢血1マイクロリットル当たり約51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115又はそれより多い総B細胞数を含む。
一般的には、CD19xCD3二特異性抗体で処置したときの患者の有害作用リスクが低い指標として、総B細胞の好ましい最低数は、好ましくは50より多い総B細胞、より好ましくは40、41、又は42より多い総B細胞、さらに好ましくは末梢血1マイクロリットル当たり35より多い総B細胞であるべきである。
一般的には、CD19xCD3二特異性抗体で処置したときの患者の有害作用リスクが高い指標として、患者の総B細胞は、好ましくは末梢血1マイクロリットル当たり50未満の総B細胞、より好ましくは末梢血1マイクロリットル当たり42、41又は40未満の総B細胞、さらに好ましくは末梢血1マイクロリットル当たり35未満の総B細胞である。
したがって、本発明はまた、CD19xCD3二特異性抗体を人間の患者に投与することによって媒介される前記患者の潜在的有害作用リスクを評価(分析)する方法を意図し、前記方法は、前記患者のサンプルで前記患者のB細胞対T細胞の比を決定する工程を含み、ここで約1.5より高い比又は末梢血1マイクロリットル当たり約50B細胞より多い総B細胞数は、前記患者の潜在的有害作用リスクが低いことの指標である。
しかしながら、治療中にモニターしたとき、本明細書に記載のB細胞数に応じてこれらの低リスク患者が高リスク患者に分類される場合には、高リスク患者のために本明細書に記載した治療レジメンに付す必要があるかもしれない。
(a)前記患者由来のサンプルでB細胞対T細胞の比及び/又は総B細胞を決定する工程;
(b)当該決定工程の結果に基づき潜在的有害作用リスクを有する人間の患者を認定する工程;及び
(c)潜在的有害作用リスクを有すると認定された人間の患者に特定の投薬スケジュールにしたがってCD19xCD3二特異性抗体を投与し、前記人間の患者で潜在的な有害作用の可能性を軽減する工程を含む。
本発明の方法はさらに、前記抗体の投与中にB細胞対T細胞の比及び/又は総B細胞数を周期的に決定する工程を含む。さらにまた、本方法ではB細胞対T細胞の比及び/又は総B細胞数の周期的な決定の結果に基づいて特定の投薬スケジュールを調節して、当該治療中の潜在的有害作用リスクを軽減することができる。
本発明の関係では、“CD19xCD3二特異性抗体の投与”又は“CD19xCD3二特異性抗体を投与する”又は前記の任意の文法形は、CD19xCD3二特異性抗体が医薬組成物(場合によって医薬的に許容できる担体を含む)の形態であることを意味する。したがって、CD19xCD3二特異性抗体を含む医薬組成物は人間の患者に投与されることは理解されるべきである。
“投与する”という用語はその全ての文法形において、CD19xCD3二特異性抗体を(医薬組成物の形態で)単独治療薬剤として又は別の治療薬剤との組合せとして投与することを意味する。したがって、本発明の医薬組成物を、共助療法的アプローチで、すなわち他の医薬又は薬剤(例えば悪性CD19陽性リンパ球を患者で治療するための他の医薬及び/又は本発明の方法の関係で有益であり得る任意の他の治療薬剤)との同時投与で利用することが意図される。
例えば、本発明の方法が、B系列急性リンパ芽球性白血病又は攻撃性NHLの治療のために実施される場合、標的B細胞をCNSから除去するために有利には硬膜下腔内化学療法を併用することができる。例えば、硬膜下腔内化学療法は、本明細書に記載の方法にしたがってCD19xCD3二特異性単鎖抗体を投与する前に実施することができる。
CD19xCD3二特異性抗体(例えば医薬組成物の形態として)の投与はボーラス注射でも、又は、間断なく若しくは本明細書で時々用いられるように持続的であってもよいが、間断なく又は持続的に投与されるのが好ましい。間断のない投与は、本質的に中断がない投与を指す。“本質的に中断されない”には、通例流れ又は空間的拡張が途切れない間断のない投与が含まれる。
いくつかの実施態様では、前記第一の用量は治療的に活性を示さない。すなわち前記は治療用量以下である。厳密に固執するわけではないが、本発明の目的のためには5μg/m2/日以下の用量は治療用量以下であると考える。
本発明の好ましい実施態様では、第二の用量は治療的に活性を示す。“治療的に有効な量”又は“治療的に活性を示す”とは、投与の目的である治療効果を生じるCD19xCD3二特異性抗体の用量を意味する。
“悪性”とは、進行性に悪化する疾患(特にリンパ腫又は白血病及び本明細書に記載する疾患)をもたらすリンパ球を指す。前記用語は、癌(ここではリンパ腫及び白血病及び本明細書に記載の疾患)の表現としてもっともよく知られている。悪性CD19陽性リンパ球(特にB細胞)はその個々の増殖が無限であり、隣接組織に侵襲する能力を有し、遠位組織に拡散する能力(転移)を有し得る。本明細書で用いるとき、悪性は癌性と同義である。
しかしながら、“正常な”(非悪性)リンパ球(特にB細胞)もまたCD19を発現するので、CD19xCD3二特異性抗体はまたこれらの正常リンパ球(特にB細胞)と結合し、細胞傷害性T細胞の補充に際して(二特異性CD19xCD3抗体の第二の特異性のために)、これら正常なB細胞を枯渇させると予想できる。しかも、これら正常B細胞集団はCD19xCD3二特異性抗体の非存在下で復元されることが予想される。Leandroとその共同研究者らは、抗CD20抗体によるB細胞の枯渇の後で、B細胞は慢性関節リウマチ患者で復元されることを観察した(Arthritis Rheum. 2006 Feb:54(2):613-20)。CD20はCD19と同様ほぼ全てのB細胞で発現されるので、二特異性CD19xCD3抗体による枯渇に際してB細胞もまた復元されると予想できる。
白血病は、好ましくはB系列急性リンパ芽球性白血病(ALL)である。
有害作用は、好ましくは神経学的反応、好ましくは錯乱、運動失調、見当識障害、発語異常、失語症、言語障害、小脳症状、振せん、失行症、痙攣、大発作痙攣、麻痺及び平衡異常から成る群から選択される1つ以上の反応である(実施例2及び3もまた参照されたい)。
1.医薬の存在
CD19xCD3二特異性抗体は、例えばB細胞リンパ腫又は白血病細胞に存在する悪性CD19陽性リンパ球に対するT細胞の細胞傷害性もまた標的とする。このことを考えれば、有害作用の原因となるのは患者の体内のCD19xCD3二特異性の存在であることは妥当な推定であり得る。さらにまた、副作用は、CD19xCD3二特異性抗体が生物学的に活性を示す身体部分でのみ観察される。
したがって、CD19xCD3二特異性抗体による治療時の神経学的反応は、患者の脳脊髄液(CSF;髄液)中の前記抗体の存在に依存すると考えられる。このことは、T細胞と同様にCD19xCD3二特異性抗体は、低B:T細胞比を示すNHL患者のCSFでのみ見出されるという事実によって支持され得る。本明細書で説明するように、この患者集団は抗体治療時に神経学的反応の発生リスクが高い。この発見は、高リスクNHL及びALL患者では、CD19xCD3二特異性抗体は血管とCNS(脳を含む)を分ける血管周囲間隙に進入できることを示唆しているかもしれない。その場所でCD19xCD3二特異性抗体は続いて局所のB細胞(良性又は悪性)を標的とするT細胞と結合し、前記は局所のサイトカインの放出をもたらし、順次神経学的反応を引き起こし得る。
さらにまた、神経学的反応はCD19xCD3二特異性抗体の用量に左右されるように思われる。例えば、神経学的反応は、体表面1m2当たり5μgのCD19xCD3二特異性抗体の持続的投与時には観察されなかったが、体表面1m2当たり15μg以上のCD19xCD3二特異性抗体の持続的投与時には観察された。この理由のために、本明細書に記載するように、5μg/日/m2未満の用量は治療用量以下であるように思われる。薬剤の用量の影響は添付の実施例に示すデータから明らかである。この観察は、低B:T細胞比及び/又は低総B細胞数を有する高リスク患者で神経学的反応の用量依存性を暗示しているかもしれない。
上記に示したように、CD19xCD3二特異性抗体治療時の神経学的反応は、i)標的細胞(すなわちCD19抗原保持B細胞)及びii)エフェクター細胞(すなわちCD3抗原を保持する細胞傷害活性を示すT細胞)のPVS/CNSにおける存在に依存すると考えられる。
前記の観点から、PVS/CNSから例えば標的B細胞を枯渇させることによって神経学的反応が回避されるはずであるという仮説は興味深い。実際のところ、これは、B系列急性リンパ芽球性白血病(ALL)患者が現在CD19xCD3二特異性抗体で処置されている前述のフェーズII試験でまさに観察された事柄である。
上記を勘案すれば、治療有効性を損なうことなく上記に示した要因のいずれか1つを欠落させることは瑣末な作業ではない。なぜならば、例えばNHLのPVS/CNSでB細胞の存在を除くことは容易に行い得ることではないからである。さらにまた、他の手段(高用量のステロイドの前投与又は同時投与を含む)は、高リスク患者の神経学的反応を予防できなかった。
しかしながら、本発明の方法/投薬レジメンを適用することによって、患者が約1.5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する場合、そのような有害作用リスクが高まった患者について有害作用を改善及び/又は予防することが可能である。本発明は、CD19xCD3二特異性抗体による治療に影響を与える可能性がある上述の要因とは別個に投薬レジメン(方法)を提供することを想定する。
前記の好ましい特徴では、好ましくは、患者は下記に記載するように前記抗体の第三の用量を第三の期間投与される。したがって、三ステージ方法(投薬レジメン)の関係で本明細書に記載する実施態様及び特徴を前記の好ましい特徴で適用できる。
本発明の方法のある特徴では、前記第二の期間は前記第一の期間を超える。“超える”という用語は、第二の期間が第一の期間よりも少なくとも1日長いことを意味する。
ある実施態様では、二特異性抗体の投薬量を計算することができる。例えば、CNS事象に対してリスクを有する患者集団でCD19xCD3二特異性抗体の適切な用量を決定する際にB:T細胞比及び/又は総B細胞数の重要性を示すデータに基づいて、当該患者集団のための適切な投薬量の決定で医師を補助する計算式を用いることができる。この式は、CD19xCD3二特異性抗体(ブリナツモマブ)の用量とB及びT細胞数との関係を基にしている。例えば、
c(定常係数)=CD19xCD3二特異性抗体の用量xT細胞数/B細胞数
であり、それは、
CD19xCD3二特異性抗体の用量=cxB細胞数/T細胞数
を意味する。また別には、個々の患者のB:T細胞比又は総B細胞数に基づいて個別化用量を利用することが可能で、この場合、二特異性抗体の用量は、B:T細胞比又は総B細胞数のどちらかを定常係数と掛けることによって計算される。
本発明の別の特徴では、前記第一の期間は少なくとも3日の長さが想定され、したがってさらに長期間、例えば8、9、10、11、12、13又は14日は除外されない。“より長期間”は、それによって最小単位として丸一日に限定されず、すなわち半日又は丸々数時間もまた意図し得る。しかしながら好ましくは、最小時間単位は丸一日である。したがって、前記第一の期間は3日を超える。より好ましくは、前記第一の期間は3日から10日の間で、7日が特に好ましい。
本明細書で用いられるように、“XからY”と規定される時間間隔は、“XからYの間”と規定される時間間隔と一致する。両方の時間間隔は特に上限及び下限もまた含む。このことは、例えば“3から10日”又は“3から10日の間”という時間間隔は1、2、3、4、5、6、7及び/又は8日間の期間を含むことを意味する。
しかしながら、この改善を達成するために、約1.5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する人間の患者を、第一の用量のCD19xCD3二特異性抗体を第一の期間投与することによって前記抗体に“順応させる”ことが必要である(ここで前記第一の用量は連続する(第二の)用量より低い)。投与はボーラス注射又は持続投与であり得るが、連続投与が好ましい。
第一の期間と同様に、第二の期間も、当該患者の例えば年齢、性別、体重などの観点から多様であり得る。
したがって、本発明の別の特徴では、前記第二の期間は少なくとも18日の長さであり、したがってさらに長期間、例えば19、20、25、30、35、40、45、49、50、55、60、65、70、75、80、81、82、83、84、85、86、87、88又は90日は除外されない。“より長期間”は、それによって最小単位として丸一日に限定されず、すなわち半日又は丸々数時間もまた意図し得る。しかしながら好ましくは、最小時間単位は丸一日である。したがって、前記第二の期間は18日を超える。より好ましくは、前記第二の期間は18日から81日の間で、21日又は49日が特に好ましい。
本発明の方法/投薬レジメンのより好ましい実施態様では、前記第一の期間は3日から10日の間で、さらに前記第二の期間は18から81日の間である。
さらに好ましい実施態様では、前記第一の期間は7日で、さらに前記第二の期間は21日又は49日である。
最小残留症状(MRD)は、患者が緩解(疾患に関し無症状又は無徴候)にあるとき治療中又は治療後に患者で残留する少数の白血病/リンパ腫細胞に与えられる名称である。10年前までは、癌の判定/検出のために用いられた試験のいずれもMRDの検出には十分に鋭敏ではなかった。しかしながら今日では、非常に鋭敏な分子生物学的試験(DNA、RNA又はタンパク質を基にする)が利用可能で、これらは組織サンプル中の微量レベルの癌細胞(時には百万の正常細胞中に1個の癌細胞ほどの微量)を測定することができる。
癌(特に白血病)治療では、MRD検査は以下のいくつかの重要な役割を有する:治療が癌を根絶したか否か又は微量が残存しているか否かの決定、種々の治療の有効性の比較、患者の緩解状態及び白血病又は癌の再発のモニター、並びに要求にもっとも適合する治療の選択(治療の個別化)。
したがって、本発明の方法/投薬レジメンのさらに別の特徴では、前記第一の用量は1から15μg/m2/日の間、すなわち1、2、3、4、5、6、7、8、9、10、11、12、13、14、15μg/m2/日である。5又は15μg/m2/日の用量が特に好ましい。
“m2”は、患者の体表面(BSA)の平方メートルを示す。“正常な”平均BSAは、一般的に成人については約1.73m2、新生児については約0.25m2、2歳の小児については約0.5m2、9歳の小児については約1.07m2、10歳の小児については約1.14m2、12‐13歳の小児については約1.33m2、男性については約1.9m2及び女性については約1.6m2であるとされる。
しかしながら、BSAはまた以下の式の1つによってより正確に計算できる(これらの式の各々はBSAを計算するときに利用できる):
−Mostellerの式(Mosteller, N Engl J Med, 1987 Oct 22, 317(17):1098)
BSA(m2)=([身長(cm)x体重(kg)]/3600)1/2、又はインチ及びポンドで
BSA(m2)=([身長(インチ)x体重(ポンド)]/3131)1/2、
−DuBoisの式(DuBois, Arch Int Med, 1916, 17:863-871):
BSA(m2)=0.007184x身長(cm)0.725x体重(kg)0.425
−Haycockの式(Haycock, The Journal of Pediatrics, 1978, 93(1):62-66)
BSA(m2)=0.024265x身長(cm)0.3964x体重(kg)0.5378
−Gehanの式(Gehan, Cancer Chemother Rep, 1970, 54:225-35)
BSA(m2)=0.0235x身長(cm)0.42246x体重(kg)0.51456
−Boydの式(Boyd, University of Minnesota Press, 1935)
BSA(m2)=0.0003207x身長(cm)0.3x体重(g)(0.7285-(0.0188xlog10(g))
例えば1μg/m2/日の用量は、1m2の体表面につき1μgのCD19xCD3二特異性抗体が1日を通して均等に又は持続的に投与されることを意味する。“1日を通して持続的に”とは、中断することなく永続的に進行させ得る輸液を指す。
本明細書で用いられるように、“XからYの間”と規定される用量間隔は、“XからY”と規定される用量間隔と一致する。両方の用量間隔は特に上限及び下限もまた含む。このことは、例えば“15から60の間”又は“15から60”という用量間隔は、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59及び/又は60μg/m2/日を含むことを意味する。
本明細書で与えられる範囲は5ずつの増加量によって示されることは理解されねばならない。しかしながら、これらの範囲はまた、より小さな増加量、例えば1ずつの増加によって示されるもの(10から30は例えば30まで10、11、12、13などを含む)又はさらに小さな増加量、例えば小数点の後の値を包含する。
(i)5μg/m2の二特異性抗体を1日、続いて残りの期間(2日目及びその後毎日)に毎日の用量として15μg/m2を投与;及び/又は
(ii)15μg/m2の二特異性抗体を1日、続いて残りの期間(2日目及びその後毎日)に毎日の用量として45μg/m2を投与;及び/又は
(iii)5μg/m2の二特異性抗体を1日、続いて15μg/m2の投与を1日、続いて残りの期間(2日目及びその後毎日)に毎日の用量として45μg/m2を投与;及び/又は
(iv)10−80μg/m2未満の二特異性抗体を1日、続いて10−80μg/m2の用量の投与(2日目及びその後毎日);及び/又は
(v)10−80μg/m2未満の二特異性抗体を1日、続いて10−80μg/m2未満の用量の投与を1日、続いて10−80μg/m2未満の用量の投与(3日目及びその後毎日)。
さらにまた一日当たりきっかりの用量を用いることができる。
前記第三の用量の投与は静脈内投与である。前記はボーラス注射の形態で又は持続的に投与されるが、持続的投与が好ましい。
本発明の方法のある特徴では、前記第三の期間は前記第一及び第二の期間を超える。“超える”という用語は、第三の期間が第一及び第二の期間より少なくとも1日長いことを意味する。
第一及び第二の期間の存続期間と同様に、第三の期間の存続期間は当該患者の例えば年齢、性別、体重などの観点から多様であり得る。
本発明の三ステージ投薬レジメンの特徴では、前記第一の期間は少なくとも3日の長さであり、したがってさらに長期間、例えば8、9、10、11、12、13又は14日は除外されない。“より長期間”は、それによって最小単位として丸一日に限定されず、すなわち半日又は丸々数時間もまた意図し得る。しかしながら好ましくは、最小時間単位は丸一日である。したがって、前記第一の期間は3日を超える。より好ましくは、前記第一の期間は3日から10日の間で、7日が特に好ましい。
本明細書で用いられるように、“XからY”と規定される時間間隔は、“XからYの間”と規定される時間間隔と一致する。両方の時間間隔は特に上限及び下限もまた含む。このことは、例えば“3から10日”又は“3から10日の間”という時間間隔は1、2、3、4、5、6、7及び/又は8日間の期間を含むことを意味する。
本明細書で用いられるように、“XからY”と規定される時間間隔は、“XからYの間”と規定される時間間隔と一致する。両方の時間間隔は特に上限及び下限もまた含む。このことは、例えば“3から10日”又は“3から10日の間”という時間間隔は1、2、3、4、5、6、7及び/又は8日間の期間を含むことを意味する。
本発明の三ステージ投薬レジメンの特徴では、前記第三の期間は少なくとも8日の長さであり、したがってさらに長期間、例えば8、9、10、11、12、13、 14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、32、34、36、38、40、42、44、46、48、50、52、54、56、58、60、61、62、63、64、65、66、67、68、69、70及び/又は71日は除外されない。“より長期間”は、それによって最小単位として丸一日に限定されず、すなわち半日又は丸々数時間もまた意図し得る。しかしながら好ましくは、最小時間単位は丸一日である。
本明細書で用いられるように、“XからY”と規定される時間間隔は、“XからYの間”と規定される時間間隔と一致する。両方の時間間隔は特に上限及び下限もまた含む。このことは、例えば“18から78日”又は“18から78日の間”という時間間隔は、1、2、3、4、5、6、7、8、9、10、11、12、13、 14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、32、34、36、38、40、42、44、46、48、50、52、54、56、58、60、61、62、63、64、65、66、67、68、69、70及び/又は71日間の期間を含むことを意味する。
本発明の三ステージ方法/投薬レジメンのより好ましい実施態様では、前記第一の期間は3日から10日間の間で、前記第二の期間は3日から10日の間で、さらに前記第三の期間は8日から78日の間である。
さらに好ましい実施態様では、前記第一の期間は7日で、前記第二の期間は7日で、さらに前記第三の期間は14又は42日である。
本発明の三ステージ方法/投薬レジメンの実施態様では、前記第三の用量は前記第一及び第二の用量を超える。前記第二及び第三の用量は、好ましくは治療的に活性を示す。特記すれば、前記第二の用量は前記第一の用量を超える。
本発明の三ステージ方法/投薬レジメンのさらに別の特徴では、前記第二の用量は1から15μg/m2/日の間、好ましくは5から15μg/m2/日の間、すなわち1、2、3、4、5、6、7、8、9、10、11、12、13、 14、15μg/m2/日である。特に好ましくは15μg/m2/日の用量である。
本明細書で用いられるように、“XからYの間”と規定される用量間隔は、“XからY”と規定される用量間隔と一致する。両方の用量間隔は特に上限及び下限もまた含む。このことは、例えば“1から15の間”又は“1から15”という用量間隔は、1、2、3、4、5、6、7、8、9、10、11、12、13、 14、15μg/m2/日の用量を含むことを意味する。
本発明の三ステージ方法/投薬レジメンのさらに別の特徴では、前記第三の用量は15から60μg/m2/日の間、より好ましくは20から60μg/m2/日の間、すなわち15、20、25、30、35、40、45、50、55及び60μg/m2/日である。特に好ましくは60μg/m2/日の用量である。また別には、前記第三の用量は15から90μg/m2/日の間、より好ましくは60から90μg/m2/日の間、すなわち15、20、25、30、35、40、45、50、55、60、70、80及び90μg/m2/日である。
特に好ましくは、前記第一の用量は5μg/m2/日で、前記第二の用量は15μg/m2/日で、さらに前記第三の用量は60μg/m2/日である。また別には前記第三の用量は90μg/m2/日でもよい。
本明細書で用いられるように、“XからYの間”と規定される用量間隔は、“XからY”と規定される用量間隔と一致する。両方の用量間隔は特に上限及び下限もまた含む。このことは、例えば“15から60の間”又は“15から60”という用量間隔は、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59及び/又は60μg/m2/日の用量を含むことを意味する。同様に、このことは、例えば“15から90の間”又は“15から90”という用量間隔は、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89又は90μg/m2/日の用量を含むことを意味する。
また本発明は人間の患者で悪性CD19陽性リンパ球を治療する方法に関し、前記方法は、(a)前記抗体の第一の用量を第一の期間投与する工程、(b)前記抗体の第二の用量を第二の期間投与する工程、及び連続的に(c)前記工程の第三の用量を第三の期間投与する工程を含む。
さらにまた、本発明は、CD19xCD3二特異性抗体を人間の患者に投与することによって媒介される有害作用を軽減及び/又は予防する方法に関し、前記方法は(a)前記抗体の第一の用量を第一の期間投与する工程、(b)前記抗体の第二の用量を第二の期間投与する工程、及び連続的に(c)前記工程の第三の用量を第三の期間投与する工程を含む。
好ましくは、当該第一、第二及び第三の期間は本明細書の他の場所に記載されているとおりである。
用量に関しては、本明細書の別の場所に記載したように、第二の用量は第一の用量を超え、さらに第三の用量は第二の用量を超えることが好ましい。より好ましくは、第一の用量は5μg/m2/日で第二の用量は15μg/m2/日で第三の用量は60μg/m2/日である。また別には第三の用量はまた90又は120μg/m2/日でもよい。これらの用量と等価の1日当たりのきっかりの用量を以前に考察した係数を用いて決定することができる。例えば5μg/m2/日の用量は9.5μg/日に変換し9又は10μg/日に四捨五入する。15μg/m2の用量は、四捨五入に応じて112μg/m2、114μg/m2又は116μg/m2に変換される。
本明細書に用いられているように、“CD19xCD3二特異性抗体”(CD19xCD3二特異性単鎖抗体を含む)は、2つの結合ドメインを含む少なくとも1つのポリペプチド鎖を有する結合物質(“バインダー”)を指し、例えばDual-Affinity Re-Targeting(DART)抗体、ジアボディ、ドメイン抗体(dAb)又はナノボディである。特に好ましいCD19xCD3二特異性抗体は単一ポリペプチド鎖を含み、前記は2つの結合ドメインを有する。そのような単鎖抗体は本発明の方法/投薬レジメンの関係で好ましい。各結合ドメインは、抗体重鎖由来の少なくとも1つの可変領域(“VH又はH領域”)(第一の結合ドメインのVH領域はCD3エプシロン分子と特異的に結合する)を含み、さらに第二の結合ドメインのVH領域はCD19と特異的に結合する。2つの結合ドメインは場合によって短いポリペプチドスペーサーで互いに連結される。ポリペプチドスペーサーの非限定的な例はGly-Gly-Gly-Gly-Ser(G-G-G-G-S)及び前記の繰り返しである。各結合ドメインはさらにまた抗体軽鎖由来の1つの可変領域(“VL又はL領域”)を含むことができ、第一及び第二の結合ドメインの各々のVH領域及びVL領域はポリペプチドリンカー(例えばEP623679B1に開示され特許請求されたタイプのもの)で互いに連結されるが、ただしいずれの事例でも、前記リンカーは、第一の結合ドメインのVH領域及びVL領域と第二の結合ドメインのVH領域及びVL領域が互いに対を形成して、その結果それらが対応する第一及び第二の結合ドメインと特異的に結合するのを可能にするために十分に長い。そのようなCD19xCD3二特異性単鎖抗体はWO99/54440及びWO2004/106381に極めて詳細に記載されている。
“抗体”という用語の定義にはまた、キメラ抗体、単鎖抗体及びヒト化抗体のような具体化物とともに抗体フラグメント(例えばとりわけFabフラグメント)が含まれる。抗体フラグメント又は誘導体はさらにまたF(ab’)2、Fv、scFvフラグメント又は一ドメイン抗体、一可変ドメイン抗体若しくは免疫グロブリン一可変ドメインを含む。後者は、単に1つの可変ドメインのみを含み(VH又はVLであり得る)、他のV領域又はドメインに依存することなく抗原又はエピトープと特異的に結合する(例えば上記に引用した文献(Harlow and Lane(1988)及び(1999))を参照されたい)。そのような免疫グロブリン一可変ドメインは、単離された抗体一可変ドメインポリペプチドだけでなく抗体一可変ドメインポリペプチド配列の1つ以上のモノマーを含むより大きなポリペプチドもまた包含する。
VH(CD19)-VL(CD19)-VH(CD3)-VL(CD3)、
VL(CD19)-VH(CD19)-VL(CD3)-VH(CD3)、
VH(CD19)-VL(CD19)-VL(CD3)-VH(CD3)、
VL(CD3)-VH(CD3)-VH(CD19)-VL(CD19)、
VH(CD3)-VL(CD3)-VH(CD19)-VL(CD19)、
VL(CD3)-VH(CD3)-VL(CD19)-VH(CD19)、又は
VH(CD3)-VL(CD3)-VL(CD19)-VH(CD19)。
(a)配列番号:11(RYTMH)、より好ましくは配列番号:11(GYTFTRYTMH)でCD3 CDR-H1として、配列番号:12(YINPSRGYTNYNQKFKD)でCD3 CDR-H2として、及び配列番号:13(YYDDHYCLDY)でCD3 CDR-H3として示される重鎖の抗CD3 CDR;及び/又は
(b)配列番号:14(RASSSVSYMN)でCD3 CDR-L1として、配列番号:15(DTSKVAS)でCD3 CDR-L2として、及び配列番号:16(QQWSSNPLT)でCD3 CDR-L3として示される軽鎖の抗CD3 CDR;及び/又は
(c)配列番号:17(SYWMN)、より好ましくは配列番号:17(GYAFSSYWMN)でCD19 CDR-H1として、配列番号:18(QIWPGDGDTNYNGKFKG)でCD19 CDR-H2として、及び配列番号:19(RETTTVGRYYYAMDY)でCD19 CDR-H3として示される重鎖の抗CD19 CDR;及び/又は
(d)配列番号:20(KASQSVDYDGDSYLN)でCD19 CDR-L1として、配列番号:21(DASNLVS)でCD19 CDR-L2として、及び配列番号:22(QQSTEDPWT)でCD19 CDR-L3として示される軽鎖の抗CD19 CDR。
本明細書で用いられるCDRは、Kabatの番号付けシステムにしたがう。Kabatの番号付けシステムは、一定の態様で抗体の残基の番号付けのための広く受け入れられているスタンダードである(Kabat et al., Sequences of Proteins of Immunological Interest, 1991)。
(a)配列番号:3に示されるCD19可変重鎖(ヌクレオチド配列は配列番号:4に示される);及び/又は
(b)配列番号:5に示されるCD19可変軽鎖(ヌクレオチド配列は配列番号:6に示される);及び/又は
(c)配列番号:7に示されるCD3可変重鎖(ヌクレオチド配列は配列番号:8に示される);及び/又は
(d)配列番号:9に示されるCD3可変軽鎖(ヌクレオチド配列は配列番号:10に示される)。
より好ましくは、本発明の方法で利用されるCD19xCD3二特異性抗体は、CD19可変重鎖及び軽鎖及び/又はCD3可変重鎖及び軽鎖を含む。さらに好ましくは、本発明の方法で利用されるCD19xCD3二特異性抗体は、CD19可変重鎖及び軽鎖をCD3可変重鎖及び軽鎖に加えて含む。
別の選択肢では、前記二特異性単鎖抗体は以下から成る群から選択されるアミノ酸配列を含むこともまた好ましい:
(a)配列番号:1に示されるアミノ酸配列;
(b)配列番号:2に示される核酸配列によってコードされるアミノ酸配列;
(c)(b)の核酸配列と少なくとも70%、80%、90%、95%又は99%の同一性を有する核酸配列によってコードされるアミノ酸配列、ここで前記アミノ酸配列はCD3及びCD19と特異的に結合できる;及び
(d)(b)のヌクレオチド配列に対する遺伝暗号の結果として縮退を示す核酸配列によってコードされるアミノ酸配列、ここで前記アミノ酸配列はCD3及びCD19と特異的に結合できる。
さらにまた、WO99/54440に記載のCD19xCD3二特異性抗体MT103が、WO2004/106381及びWO2008/119565に記載されているCD19xCD3二特異性抗体同様に特に好ましい。
(i)人間の患者にCD19xCD3二特異性抗体を投与する;又は
(ii)人間の患者で悪性CD19陽性リンパ球を治療する;及び/又は
(iii)人間の患者にCD19xCD3二特異性抗体を投与することによって媒介される有害作用を改善又は予防する(ここで前記抗体は、先行する開示のいずれか1つで規定された投薬レジメンにしたがって投与されるべきである)。
(i)人間の患者へのCD19xCD3二特異性抗体の投与;又は
(ii)人間の患者での悪性CD19陽性リンパ球の治療;及び/又は
(iii)人間の患者にCD19xCD3二特異性抗体を投与することによって媒介される有害作用の改善又は予防(ここで前記抗体は、先行する開示のいずれか1つで規定された投薬レジメンにしたがって投与されるべきである)。
本発明の医薬組成物は場合によって医薬用担体を含むことができる。適切な医薬用担体の例は当業界では周知であり、リン酸緩衝食塩水溶液、無菌的溶液などが含まれる。静脈内ベヒクルには、水分及び栄養補充液、電解質補充液(例えばリンゲルデキストロースをベースにしたもの)などが含まれる。保存料及び他の添加剤(例えば抗菌剤、抗酸化剤、キレート剤、不活性ガスなど)もまた存在し得る。さらにまた、本発明の医薬組成物は、さらに別の薬剤、例えば本明細書の別の場所で説明した化学療法剤を含むことができる。
別の実施態様では、本発明は、本明細書に記載した第一の用量及び第二の用量を、三ステージ投薬レジメン/方法の関係で記載した第三の用量に加えて含む(医薬)キット又は医薬パッケージに関する。
別の特徴では、当該(医薬)キット又は医薬パッケージは、三ステージ投薬レジメン/方法の関係で本明細書に記載した3つの用量の全て、すなわち第一、第二及び第三の用量を含む。
また別には、意図される第一の用量及び/又は第二の用量及び/又は第三の用量は、対応する数の1日分用量に分離されずに、全体として又は部分として1つの単一容器(例えば輸液バッグ)に収められることもまた意図される。前記単一容器は、第一の期間及び/又は第二の期間のために要求される用量を、部分として(例えば1から3日間のため)又は全体として(すなわち第一又は第二の期間のため)含む。このことは、1つの単一容器は、例えば“第一の用量”のための7日分の1日用量(前記は第一の期間中に用いられるべきものである)、並びに同様に第二及び第三の用量ためのものを含むことを意味する。
さらにまた、本発明は、前述の医薬パッケージ又はキット及び本発明の方法にしたがって前記を連続的に使用するための指示書に関する。前記医薬パッケージ又はキットはさらに、人間の患者のリンパ腫又は白血病に存在する悪性CD19陽性リンパ球の治療、又はCD19xCD3二特異性抗体を患者に投与することによって媒介される有害作用の改善又は予防に当該内容物を用いることができることを指示するラベル又はインプリントを含む。
本発明の医薬パッケージ又はキットはさらに化学療法剤を含むこともまた想定される。
さらに別の特徴では、本発明は医薬パッケージ又はキットを提供し、ここで前記第一及び/又は第二の用量は、先行する開示のいずれか1つの方法にしたがった投薬レジメンの投与のために適切である(調製される)ように用意される。
CD19特異的BiTE抗体ブリナツモマブで処置される非ホジキンリンパ腫患者のサブセットにおける可逆性神経学的有害作用事象のための予想因子の認定
ブリナツモマブは、二特異性T細胞動員物質(bispecific T cell engager)(BiTE(商標))クラスのCD19/CD3-二特異性抗体構築物で、再発型非ホジキンリンパ腫(NHL)及びB-前駆細胞急性リンパ球性白血病(ALL)を示す患者で単一薬剤として高率で長期の応答を示す。ブリナツモマブは、治療初日に神経学的有害作用事象(AE)(例えば錯乱、言語障害又は小脳症状)を発する患者のサブセットを例外として、好ましい安全性プロフィールを有する。これまでのところ、全ての関連する神経学的AE(48人の患者のうち11人)は一過性であり、完全に元に戻り、輸液の停止後3から72時間以内に後遺症なく消散した。いずれの事例でも頭部の磁性共鳴画像化に際して病理学的所見は認められなかった。治療の中断にもかかわらず、神経学的AEを示した4人の患者で対象のリンパ腫の緩解が得られた。輸液停止後数時間以内に採取した脳脊髄液(CSF)の分析によって、症状を示した患者の大半で検出可能レベルのブリナツモマブが示され、一方、神経学的症状を示さなかった1人の患者で輸液中のCSFにブリナツモマブは検出できなかった。さらにまた、CSF中のアルブミン及びTリンパ球のレベル増加は、可能な基礎的事象として血液脳関門(BBB)の妨害を支持している。内皮ストレスレベル及びBBB完全性マーカーが神経学的AEに対してそれぞれ相関性を示すか否かを解明するために、患者の血清サンプルのアンギオポエチン-2及びS100βについての分析が進行中である。39人のNHL患者の遡及的分析では、1:10以下の末梢血のベースラインB細胞対T細胞比が、神経学的AEのその後の発生の唯一の予想因子と認定された。この予想値を続いて8人のさらに別の患者で見込みとして確認した。結論すれば、ブリナツモマブ治療の開始後に神経学的AEを生じるリスクを有する患者を見込みとして認定するための単純な手段が確認された。治療の中断を避けるために、これらの高リスク患者で緩和手段を現在試験中である。
CD19xCD3二特異性抗体で処置した患者における観察(1)の概要
−早期CNS事象の共通の特色
・最初の症状はMT103輸液の開始後12−48時間後に出現する:興奮、言語障害、時に振せん、運動失調
・輸液停止に至るより重篤な症状は24−72時間後に出現する:錯乱、見当識障害、運動失調、失語症、痙攣
・MT103輸液の停止後、CNS症状の完全な消散は1−3日以内に認められる;一般的には後遺症は無し
・大半のCNS事象はポリクローナルT細胞の初期活性化及び再分布期に分類される
−ゆっくりと発生するCNS事象の特色
・小脳症状に偏る
・処置の間の種々の時点、しばしば処置の開始時点又は増加工程で発生する
・振せん、軽度な言語障害、軽度な筆記障害;数日間持続し得る
−他のCNS事象
・他のCNS事象との関係が証明されていない追加の観察症状:頭痛、発熱、吐き気
−CNS事象のMT103用量応答関係
・CNS事象の用量応答関係は明白である;カットオフは5から15μg/m2/日の間の用量レベルである。
CD19xCD3二特異性抗体で処置した患者における観察(2)の概要
−CNS事象は予想可能であるように思われる
・CNS事象と低B:T細胞比(又は低B細胞数)との相関性
・CNS事象の発生の明白なカットオフとして認定された1:10未満のB:T比
・他の生化学的又は臨床的パラメーターはCNS事象と相関しないように思われる
−CNS事象を有し病理学的所見の認められない患者の頭部MRI、CSF分析はBBBの開放及び神経炎症事象を提唱する
・検出可能レベルのMT103及び症状を示す患者の大半で見出されるタンパク質及び血清アルブミンレベルの増加は、血液脳関門(BBB)の一次的破壊を提唱する
・CNS事象が存在しない1人の患者ではMT103が見出されない
・CSF分析はまた症状を示す幾人かの患者で単球及びTリンパ球数の増加を示し、それは神経炎症プロセスの指標である
・CNS事象はBBBの漸進的開放を反映しているか(興奮>錯乱>失語症、運動失調>痙攣)?
−CNS事象の発生率は症状及び/又は腫瘍負荷と相関し得る
・15μg/m2/日で、3/8のNHL患者(37%)及び11人のALL高リスク患者のうち1人のみ(9%)がCNS事象を生じた
・B-ALL患者は硬膜下腔内化学療法(及び静脈内高用量メトトレキセート)を日常的に受け、おそらくCNSの腫瘍細胞負荷が低下する(“不顕性新生物性髄膜炎(occult meningeosis neoplastica)”)
CD19xCD3二特異性抗体で処置した患者のCNS事象の概要
臨床試験においてCD19xCD3二特異性抗体で処置した患者のCNS事象の用量依存性
15μg/m2/日を7日間さらに60μg/m2/日を21日間投与され高い潜在的有害作用リスクを有する1人の患者は有害作用(神経学的反応)を示さなかった
患者108-003
・女、66歳
・FLグレード2、IVB(FD:09/2006)
・関連病歴:貧血、血小板減少症(前処置 2xゼバリン及びFLによる骨髄浸潤)、gGT及びAP上昇、ベンゾジアゼピン濫用、ステータスはアフター2、脊椎椎間板炎及び膿瘍によるアウリウス(aureaus)敗血症
・以前のリンパ腫処置:
−6xR-CHOP 14, 8xR 09/2006−02/2007
−R mono 05/07
−1. ゼバリン11/07
−2. ゼバリン01/08
・最初のB:T細胞比(1:10.5)にしたがい高リスク(コホート15/60)
・2009年1月5日に治療開始(15μg/m2/24時)
・発熱、2日間頭痛(経口パラセタモール及びノバルジンにより容易に管理)
・1月12日に60μg/m2/24時に用量増加
・再び発熱、頭痛(経口パラセタモール及びノバルジンにより容易に管理)
・神経学的事象無し
・“段階的”用量に良好な耐性
・骨髄機能の改善が考えられる
5μg/m2/日を7日間さらに60μg/m2/日を21日間投与され高い潜在的有害作用リスクを有する1人の患者は軽度の有害作用(神経学的反応)を示した
・MCL、男、42歳
・B:T 1:2
・2009年1月19日に5μg/m2/日で治療開始
・1日目:発熱及び冷感、頭痛、更なる問題無し
・ステップ:1月26日、6時間後発熱、強い頭痛
・27.01.09:疲労感、吐き気、嘔吐(内視鏡検査にて病理学的所見無し)、心拍170/分で完全不整脈→カリウム及びジギトキシンの代替後1日以内に緩解
・頭部CTスキャン及びCSF実施、CTは病理学的所見無し
・CSF:タンパク質わずかに上昇55mg/mL、細胞:23ゼーレン(Zellen)/μL、主に単球及びいくつかの活性化リンパ球
・27.01.09午後:軽度の振せん、失行症、“精神的状態の低下(slow mental state)”、夕方:軽度の言語障害(小脳症状?)、進行する軽度の症状のためにデキサメタゾン投与を決定、次の2日間にわたって軽度の改善29.01.09
・ゆっくりとした症状の改善、完全な緩解は31.03.09
・更なる処置コース:ギター演奏における困難が再発
・4週間処置後:-37%
・8週間処置後:PR/Cru
本発明の治療レジメンを受けた高い潜在的有害作用リスクを有する患者
患者108-005
・男、71歳、FL IIIB
・B:T細胞比:57:1363(低い、1:23.9)
・最初の診断:1997年
・多数の先行治療:12x リツキシマブ(単独)、6x リツキシマブ-ベンダムスチン、6x R-CHOP、自己SCT
・ブリナツモマブ開始日:2009年8月17日
・治療期間:8週間
・耐性良好(SAE無し)
・神経学的有害作用無し
・8週後CTスキャン:-65%=リンパ腫の部分的緩解
本発明の治療レジメンを受けた高い潜在的有害作用リスクを有するさらに別の患者
患者109-031
・男、60歳、濾胞性リンパ腫 IVAE
・B:T細胞比:0:429(低い)
・最初の診断:05/09
・以前の治療:プレフェースw、ビンクリスチン/デコルチン、6x R-CHOP
・ブリナツモマブ治療開始:30.11.09
・治療期間:8週間
・耐性良好(各ステップで一過性症状、ステロイドで対応可能)
・神経学的有害作用無し
・リンパ種は8週間後に-56%(リンパ種の部分的緩解)
本発明のまた別の態様は、以下のとおりであってもよい。
〔1〕以下の工程を含む、CD19xCD3二特異性抗体の投与による処置の結果として潜在的有害作用リスクを有すると認定された人間の患者を、潜在的有害作用を改善及び/又は予防することによって治療する方法:
(a)前記患者由来のサンプルでB細胞対T細胞の比及び/又は総B細胞を決定する工程;
(b)当該決定工程の結果に基づき潜在的有害作用リスクを有する人間の患者を認定する工程;及び
(c)潜在的有害作用リスクを有すると認定された人間の患者に特定の投薬スケジュールにしたがってCD19xCD3二特異性抗体を投与し、前記人間の患者で潜在的な有害作用の可能性を軽減する工程。
〔2〕前記患者の末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数が前記患者の潜在的有害作用リスクの指標である、前記〔1〕に記載の方法。
〔3〕前記患者の末梢血サンプルで約1:5以下のB細胞対T細胞の比が前記患者の潜在的有害作用リスクの指標である、前記〔1〕に記載の方法。
〔4〕前記患者のための特定の投薬スケジュールが以下の工程を含む、前記〔1〕から〔3〕のいずれか1項に記載の方法:
(c1)CD19xCD3二特異性抗体の第一の用量を第一の期間投与する工程;及び連続的に
(c2)前記抗体の第二の用量を第一の期間又は第二の期間投与する工程;及び場合によって連続的に
(c3)前記抗体の第三の用量を第一若しくは第二の期間又は第三の期間投与する工程;
ここで前記第二の用量は前記第一の用量を超え、さらに前記第三の用量は前記第二の用量を超える。
〔5〕前記抗体の投与中にB細胞対T細胞の比及び/又は総B細胞数を周期的に決定する工程をさらに含む、前記〔4〕に記載の方法。
〔6〕前記特定の投薬スケジュールをB細胞対T細胞の比及び/又は総B細胞数の周期的な決定の結果に基づいて調節して、当該治療中の潜在的有害作用リスクを軽減してもよい、前記〔5〕に記載の方法。
〔7〕前記抗体が二特異性単鎖抗体である、前記〔1〕から〔6〕のいずれか1項に記載の方法。
〔8〕前記抗体がMT103である、前記〔7〕に記載の方法。
〔9〕前記人間の患者が、悪性CD19陽性リンパ腫又は白血病細胞を含むか、又は含むと考えられる、前記〔1〕から〔8〕のいずれか1項に記載の方法。
〔10〕工程(c1)、(c2)及び/又は(c3)の投与ルートが静脈内である、前記〔1〕から〔9〕のいずれか1項に記載の方法。
〔11〕前記有害作用が神経学的反応を特徴とする、前記〔1〕から〔10〕のいずれか1項に記載の方法。
〔12〕神経学的反応が、錯乱、運動失調、見当識障害、発語異常、失語症、言語障害、小脳症状、振せん、失行症、痙攣、大発作痙攣、麻痺及び平衡異常から成る群から選択される1つ以上の反応である、前記〔11〕に記載の方法。
〔13〕前記第二の期間が前記第一の期間を超える、前記〔4〕から〔12〕のいずれか1項に記載の方法。
〔14〕前記第三の期間が前記第一の期間及び/又は前記第二の期間を超える、前記〔4〕から〔12〕のいずれか1項に記載の方法。
〔15〕前記第一の期間が3日を超える、前記〔4〕から〔14〕のいずれか1項に記載の方法。
〔16〕前記第一の期間が3日から10日の間で、7日が好ましい、前記〔4〕から〔15〕のいずれか1項に記載の方法。
〔17〕前記第二の期間が18日を超える、前記〔4〕から〔16〕のいずれか1項に記載の方法。
〔18〕前記第二の期間が18日から81日の間で、21又は49日が好ましい、前記〔4〕から〔17〕のいずれか1項に記載の方法。
〔19〕前記第一の期間が3日から10日の間で、さらに前記第二の期間が18日から81日の間である、前記〔4〕から〔18〕のいずれか1項に記載の方法。
〔20〕前記第一の期間が7日で、さらに前記第二の期間が21又は49日である、前記〔19〕に記載の方法。
〔21〕前記第一の用量が1から15μg/m 2 /日の間で、5又は15μg/m 2 /日が好ましい、前記〔4〕から〔20〕のいずれか1項に記載の方法。
〔22〕前記第二の用量が15から60μg/m 2 /日の間で、60μg/m 2 /日が好ましい、前記〔4〕から〔21〕のいずれか1項に記載の方法。
〔23〕前記第二の用量が治療的に活性を示す、前記〔4〕から〔22〕のいずれか1項に記載の方法。
〔24〕前記抗体の第三の用量を、第一及び第二の期間の第一及び第二の用量の後の第三の期間に投与する工程をさらに含む、前記〔4〕から〔23〕のいずれか1項に記載の方法。
〔25〕前記第三の期間が前記第一及び第二の期間を超え、さらに前記第二の用量が前記第一の用量を超える、前記〔24〕に記載の方法。
〔26〕前記第一の期間が3日を超える、前記〔24〕又は〔25〕に記載の方法。
〔27〕前記第一の期間が3日から10日の間で、7日が好ましい、前記〔24〕から〔26〕のいずれか1項に記載の方法。
〔28〕前記第二の期間が3日を超える、前記〔24〕から〔27〕のいずれか1項に記載の方法。
〔29〕前記第二の期間が3日から10日の間で、7日が好ましい、前記〔24〕から〔28〕のいずれか1項に記載の方法。
〔30〕前記第三の期間が8日を超える、前記〔24〕から〔29〕のいずれか1項に記載の方法。
〔31〕前記第三の期間が8日から78日の間で、14又は42日が好ましい、前記〔24〕から〔30〕のいずれか1項に記載の方法。
〔32〕前記第一の期間が3日から10日の間で、さらに前記第二の期間が3日から10日の間で、さらに前記第三の期間が8日から78日の間である、前記〔24〕から〔31〕のいずれか1項に記載の方法。
〔33〕前記第一の期間が7日で、前記第二の期間が7日で、さらに前記第三の期間が14又は42日である、前記〔32〕に記載の方法。
〔34〕前記第三の用量が前記第一及び第二の用量を超える、前記〔24〕から〔33〕のいずれか1項に記載の方法。
〔35〕前記第一の用量が1から15μg/m 2 /日の間で、5μg/m 2 /日が好ましい、又は前記第一の用量が2から29μg/日の間で、9若しくは10μg/日が好ましい、前記〔24〕から〔34〕のいずれか1項に記載の方法。
〔36〕前記第二の用量が1から15μg/m 2 /日の間で、15μg/m 2 /日が好ましい、又は前記第二の用量が2から29μg/日の間で、28若しくは29μg/日が好ましい、前記〔24〕から〔35〕のいずれか1項に記載の方法。
〔37〕前記第三の用量が15から60μg/m 2 /日の間で、60μg/m 2 /日が好ましい、又は前記第三の用量が28から116μg/日の間で、112μg/日が好ましい、前記〔24〕から〔36〕のいずれか1項に記載の方法。
〔38〕第三の用量の投与ルートが静脈内である、前記〔24〕から〔37〕のいずれか1項に記載の方法。
〔39〕前記第二の用量及び第三の用量が治療的に活性を示す、前記〔24〕から〔38〕のいずれか1項に記載の方法。
〔40〕前記人間の患者が悪性CD19陽性リンパ腫又は白血病と診断される、前記〔1〕から〔39〕のいずれか1項に記載の方法。
〔41〕前記リンパ種が、不活性又は攻撃性B細胞非ホジキンリンパ腫(B NHL)、マントル細胞リンパ腫(MCL)又は慢性リンパ球性白血病(CLL)を含む、前記〔40〕に記載の方法。
〔42〕前記白血病がB系列急性リンパ芽球性白血病(ALL)を含む、前記〔41〕に記載の方法。
〔43〕以下の工程を含む、CD19xCD3二特異性抗体の投与による処置の結果として潜在的有害作用リスクを示す人間の患者を認定する方法:
(a)前記患者由来のサンプルでB細胞対T細胞の比及び/又は総B細胞を決定する工程;及び
(b)当該決定工程の結果に基づき潜在的有害作用リスクを示す人間の患者を認定する工程。
〔44〕前記患者の末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数が前記患者の潜在的有害作用リスクの指標である、前記〔43〕に記載の方法。
〔45〕前記患者の末梢血サンプルで約1:5以下のB細胞対T細胞比であるB細胞対T細胞の比が前記患者の潜在的有害作用リスクの指標である、前記〔43〕に記載の方法。
〔46〕約1:5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する人間の患者で、悪性CD19陽性リンパ球を治療する方法において使用するためのCD19xCD3二特異性抗体であって、前記方法が、
(a)前記患者にCD19xCD3二特異性抗体の第一の用量を第一の期間投与する工程、及び連続的に
(b)前記患者に前記抗体の第二の用量を第二の期間投与する工程、及び場合によって連続的に
(c)前記患者に前記抗体の第三の用量を第一若しくは第二の期間又は第三の期間投与する工程を含み、
前記第二の用量が前記第一の用量を超え、さらに前記第三の用量が前記第二の用量を超える、前記CD19xCD3二特異性抗体。
〔47〕約1:5以下のB:T細胞比及び/又は末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する人間の患者にCD19xCD3二特異性抗体を投与することによって媒介される有害作用を改善及び/又は予防する方法において使用するためのCD19xCD3二特異性抗体であって、前記方法が、
(a)前記患者に前記抗体の第一の用量を第一の期間投与する工程、及び連続的に
(b)前記患者に前記抗体の第二の用量を第二の期間投与する工程、及び場合によって連続的に
(c)前記患者に前記抗体の第三の用量を第一若しくは第二の期間又は第三の期間投与する工程を含み、
前記第二の用量が前記第一の用量を超え、さらに前記第三の用量が前記第二の用量を超える、前記CD19xCD3二特異性抗体。
〔48〕前記抗体の投与中にB細胞対T細胞の比及び/又は総B細胞数を周期的に決定する工程をさらに含む、前記〔46〕又は〔47〕に記載の二特異性抗体。
〔49〕二特異性抗体の投与をB細胞対T細胞の比及び/又は総B細胞数の周期的な決定の結果に基づいて調節して、当該治療中の潜在的有害作用リスクを軽減してもよい、前記〔48〕に記載の方法。
〔50〕前記抗体が二特異性単鎖抗体である、前記〔46〕から〔49〕のいずれか1項に記載の二特異性抗体。
〔51〕前記抗体がMT103である、前記〔50〕に記載の二特異性抗体。
〔52〕前記人間の患者が、悪性CD19陽性リンパ腫又は白血病細胞を含むか、又は含むと考えられる、前記〔46〕から〔51〕のいずれか1項に記載の二特異性抗体。
〔53〕工程(a)、(b)及び/又は(c)の投与ルートが静脈内である、前記〔46〕から〔52〕のいずれか1項に記載の二特異性抗体。
〔54〕前記有害作用が神経学的反応を特徴とする、前記〔46〕から〔53〕のいずれか1項に記載の二特異性抗体。
〔55〕神経学的反応が、錯乱、運動失調、見当識障害、発語異常、失語症、言語障害、小脳症状、振せん、失行症、痙攣、大発作痙攣、麻痺及び平衡異常から成る群から選択される1つ以上の反応である、前記〔54〕に記載の二特異性抗体。
〔56〕前記第二の期間が前記第一の期間を超える、前記〔46〕から〔55〕のいずれか1項に記載の二特異性抗体。
〔57〕前記第三の期間が前記第一の期間及び/又は前記第二の期間を超える、前記〔46〕から〔56〕のいずれか1項に記載の二特異性抗体。
〔58〕前記第一の期間が3日を超える、前記〔46〕から〔57〕のいずれか1項に記載の二特異性抗体。
〔59〕前記第一の期間が3日から10日の間で、7日が好ましい、前記〔46〕から〔58〕のいずれか1項に記載の二特異性抗体。
〔60〕前記第二の期間が18日を超える、前記〔46〕から〔59〕のいずれか1項に記載の二特異性抗体。
〔61〕前記第二の期間が18日から81日の間で、21又は49日が好ましい、前記〔46〕から〔60〕のいずれか1項に記載の二特異性抗体。
〔62〕前記第一の期間が3日から10日の間で、さらに前記第二の期間が18日から81日の間である、前記〔46〕から〔61〕のいずれか1項に記載の二特異性抗体。
〔63〕前記第一の期間が7日で、さらに前記第二の期間が21又は49日である、前記〔46〕から〔62〕のいずれか1項に記載の二特異性抗体。
〔64〕前記第一の用量が1から15μg/m 2 /日の間で、5若しくは15μg/m 2 /日が好ましい、又は前記第一の用量が2から29μg/日の間で、9、10、28若しくは29μg/日が好ましい、前記〔46〕から〔63〕のいずれか1項に記載の二特異性抗体。
〔65〕前記第二の用量が15から60μg/m 2 /日の間で、60μg/m 2 /日が好ましい、又は前記第二の用量が28から116μg/日の間で、112μg/日が好ましい、前記〔46〕から〔64〕のいずれか1項に記載の二特異性抗体。
〔66〕前記第二の用量が治療的に活性を示す、前記〔46〕から〔65〕のいずれか1項に記載の二特異性抗体。
〔67〕前記抗体の第三の用量を、第一及び第二の期間の第一の用量及び第二の用量の後の第三の期間に投与する工程をさらに含む、前記〔46〕から〔66〕のいずれか1項に記載の二特異性抗体。
〔68〕前記第三の期間が前記第一及び第二の期間を超え、さらに前記第二の用量が前記第一の用量を超える、前記〔67〕に記載の二特異性抗体。
〔69〕前記第一の期間が3日を超える、前記〔67〕又は〔68〕に記載の二特異性抗体。
〔70〕前記第一の期間が3日から10日の間で、7日が好ましい、前記〔67〕から〔69〕のいずれか1項に記載の二特異性抗体。
〔71〕前記第二の期間が3日を超える、前記〔67〕から〔70〕のいずれか1項に記載の二特異性抗体。
〔72〕前記第二の期間が3日から10日の間で、7日が好ましい、前記〔67〕から〔71〕のいずれか1項に記載の二特異性抗体。
〔73〕前記第三の期間が8日を超える、前記〔67〕から〔72〕のいずれか1項に記載の二特異性抗体。
〔74〕前記第三の期間が8日から78日の間で、14又は42日が好ましい、前記〔67〕から〔73〕のいずれか1項に記載の二特異性抗体。
〔75〕前記第一の期間が3日から10日の間で、さらに前記第二の期間が3日から10日の間で、さらに前記第三の期間が8日から78日の間である、前記〔67〕から〔74〕のいずれか1項に記載の二特異性抗体。
〔76〕前記第一の期間が7日で、前記第二の期間が7日で、さらに前記第三の期間が14又は42日である、前記〔75〕に記載の二特異性抗体。
〔77〕前記第三の用量が前記第一及び第二の用量を超える、前記〔67〕から〔76〕のいずれか1項に記載の二特異性抗体。
〔78〕前記第一の用量が1から15μg/m 2 /日の間で、5μg/m 2 /日が好ましい、又は前記第一の用量が2から29μg/日の間で、9若しくは10μg/日が好ましい、前記〔67〕から〔77〕のいずれか1項に記載の二特異性抗体。
〔79〕前記第二の用量が1から15μg/m 2 /日の間で、15μg/m 2 /日が好ましい、又は前記第二の用量が2から29μg/日の間で、28若しくは29μg/日が好ましい、前記〔67〕から〔78〕のいずれか1項に記載の二特異性抗体。
〔80〕前記第三の用量が15から60μg/m 2 /日の間で、60μg/m 2 /日が好ましい、又は前記第三の用量が28から116μg/日の間で、112μg/日が好ましい、前記〔67〕から〔79〕のいずれか1項に記載の二特異性抗体。
〔81〕第三の用量の投与ルートが静脈内である、前記〔67〕から〔80〕のいずれか1項に記載の二特異性抗体。
〔82〕前記第二の用量及び第三の用量が治療的に活性を示す、前記〔67〕から〔81〕のいずれか1項に記載の二特異性抗体。
〔83〕前記人間の患者が悪性CD19陽性リンパ腫又は白血病と診断される、前記〔46〕から〔82〕のいずれか1項に記載の二特異性抗体。
〔84〕前記リンパ種が、不活性又は攻撃性B細胞非ホジキンリンパ腫(B NHL)、マントル細胞リンパ腫(MCL)又は慢性リンパ球性白血病(CLL)を含む、前記〔83〕に記載の二特異性抗体。
〔85〕前記白血病がB系列急性リンパ芽球性白血病(ALL)を含む、前記〔84〕に記載の二特異性抗体。
〔86〕前記態様のいずれか1項に規定の方法で使用される医薬組成物の調製のためのCD19xCD3二特異性抗体の使用。
〔87〕前記態様のいずれか1項に規定の第一の用量及び第二の用量を含む医薬パッケージ又はキット。
〔88〕前記態様のいずれか1項に規定の第三の用量をさらに含む、前記〔87〕に記載の医薬パッケージ又はキット。
〔89〕第一及び/又は第二の用量を患者に投与するための手段をさらに含む、前記〔87〕又は〔88〕に記載の医薬パッケージ又はキット。
Claims (16)
- CD19xCD3二特異性抗体の投与による処置の結果として潜在的有害作用リスクを有すると認定された人間の患者を、潜在的有害作用を改善及び/又は予防することによって治療するための医薬組成物であって、
前記患者が、
(a)前記患者由来のサンプルで総B細胞を決定する工程、
(b)当該決定工程の結果に基づき潜在的有害作用リスクを有する人間の患者を認定する工程を含む方法によって認定され、
前記方法が、CD19xCD3二特異性抗体の投与前に行われ、
前記医薬組成物が、潜在的有害作用リスクを有すると認定された人間の患者に特定の投薬スケジュールにしたがって投与して、前記人間の患者で潜在的な有害作用の可能性を軽減するCD19xCD3二特異性抗体を含み、
前記患者の末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数が前記患者の潜在的有害作用リスクの指標であり、
前記患者のための特定の投薬スケジュールが以下の工程:
(c1)CD19xCD3二特異性抗体の第一の用量を第一の期間投与する工程、及び連続的に
(c2)前記抗体の第二の用量を第一の期間又は第二の期間投与する工程;及び任意に連続的に
(c3)前記抗体の第三の用量を、前記第一若しくは第二の期間又は第三の期間、前記患者へ投与する工程;を含み、
ここで
前記第二の用量は前記第一の用量を超え、かつ、前記第三の用量が前記第二の用量を超え、
前記第一の期間が少なくとも3日であり、
前記第二の期間が前記第一の期間を超え、
前記第三の期間が前記第一の期間及び/又は前記第二の期間を超え、
前記第一の用量が1から15μg/m 2 /日の間であり、又は、前記第一の用量が2から29μg/日の間である
ことを特徴とする、医薬組成物。 - 末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する人間の患者で、悪性CD19陽性リンパ球を治療するためのCD19xCD3二特異性抗体を含む医薬組成物であって、前記医薬組成物が、
(a)前記患者に第一の期間に投与する第一の用量のCD19xCD3二特異性抗体、
(b)前記第一の期間に続いて前記患者に第二の期間に投与する第二の用量の前記抗体、及び、任意に
(c)前記第一若しくは第二の期間又は第三の期間に前記患者へ投与する第三の用量の前記抗体
を含み、
前記第二の用量が前記第一の用量を超え、かつ、前記第三の用量が前記第二の用量を超え、
前記第一の期間が少なくとも3日であり、
前記第二の期間が前記第一の期間を超え、
前記第三の期間が前記第一の期間及び/又は前記第二の期間を超え、
前記第一の用量が1から15μg/m 2 /日の間であり、又は、前記第一の用量が2から29μg/日の間であり、
前記総B細胞数がCD19xCD3二特異性抗体の投与前に決定されることを特徴とする、医薬組成物。 - 末梢血1マイクロリットル当たり約50B細胞未満の総B細胞数を有する人間の患者にCD19xCD3二特異性抗体を投与することによって媒介される有害作用を改善及び/又は予防するためのCD19xCD3二特異性抗体を含む医薬組成物であって、前記医薬組成物が、
(a)前記患者に第一の期間に投与する第一の用量の前記抗体、
(b)前記第一の期間に続いて前記患者に第二の期間に投与する第二の用量の前記抗体、
及び、任意に
(c)前記第一若しくは第二の期間又は第三の期間に前記患者へ投与する第三の用量の前記抗体
を含み、
前記第二の用量が前記第一の用量を超え、かつ、前記第三の用量が前記第二の用量を超え、
前記第一の期間が少なくとも3日であり、
前記第二の期間が前記第一の期間を超え、
前記第三の期間が前記第一の期間及び/又は前記第二の期間を超え、
前記第一の用量が1から15μg/m 2 /日の間であり、又は、前記第一の用量が2から29μg/日の間であり、
前記総B細胞数がCD19xCD3二特異性抗体の投与前に決定されることを特徴とする、医薬組成物。 - 前記治療又は改善及び/又は予防が、前記抗体の投与中にB細胞対T細胞の比及び/又は総B細胞数を周期的に決定することを含む、請求項1〜3のいずれか1項に記載の医薬組成物。
- 前記特定の投薬スケジュールをB細胞対T細胞の比及び/又は総B細胞数の周期的な決定の結果に基づいて調節して、当該治療中の潜在的有害作用リスクを軽減してもよい、請求項4に記載の医薬組成物。
- 前記抗体が二特異性単鎖抗体である、請求項1から5のいずれか1項に記載の医薬組成物。
- 前記抗体がMT103である、請求項6に記載の医薬組成物。
- 前記人間の患者が、悪性CD19陽性リンパ腫又は白血病細胞を含むか、又は含むと考えられる、請求項1から7のいずれか1項に記載の医薬組成物。
- 前記有害作用が神経学的反応を特徴とする、請求項1から8のいずれか1項に記載の医薬組成物。
- 神経学的反応が、錯乱、運動失調、見当識障害、発語異常、失語症、言語障害、小脳症状、振せん、失行症、痙攣、大発作痙攣、麻痺及び平衡異常から成る群から選択される1つ以上の反応である、請求項9に記載の医薬組成物。
- 前記第一の期間が7日で、さらに前記第二の期間が21又は49日である、請求項1〜10のいずれか1項に記載の医薬組成物。
- 第一及び第二の期間の第一及び第二の用量の後の第三の期間に投与する第三の用量の前記抗体を含む、請求項4から11のいずれか1項に記載の医薬組成物。
- 前記第三の期間が前記第一及び第二の期間を超え、さらに前記第二の用量が前記第一の用量を超える、請求項12に記載の医薬組成物。
- 前記第三の期間が8日から78日の間である、請求項12又は13に記載の医薬組成物。
- 前記第二の用量が、1から15μg/m2/日の間、又は、2から29μg/日の間である、請求項12から14のいずれか1項に記載の医薬組成物。
- 前記第三の用量が、15から60μg/m2/日の間、又は、28から116μg/日の間である、請求項12から15のいずれか1項に記載の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161479961P | 2011-04-28 | 2011-04-28 | |
| US61/479,961 | 2011-04-28 | ||
| PCT/EP2012/001857 WO2012146394A1 (en) | 2011-04-28 | 2012-04-30 | Dosage regimen for administering a cd19xcd3 bispecific antibody to patients at risk for potential adverse effects |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017194928A Division JP6539709B2 (ja) | 2011-04-28 | 2017-10-05 | 潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2014513088A JP2014513088A (ja) | 2014-05-29 |
| JP2014513088A5 JP2014513088A5 (ja) | 2015-06-25 |
| JP6276175B2 true JP6276175B2 (ja) | 2018-02-07 |
Family
ID=46178514
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014506794A Active JP6276175B2 (ja) | 2011-04-28 | 2012-04-30 | 潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン |
| JP2017194928A Active JP6539709B2 (ja) | 2011-04-28 | 2017-10-05 | 潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017194928A Active JP6539709B2 (ja) | 2011-04-28 | 2017-10-05 | 潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US10191034B2 (ja) |
| EP (2) | EP3753572A1 (ja) |
| JP (2) | JP6276175B2 (ja) |
| KR (2) | KR102147533B1 (ja) |
| CN (2) | CN103648529A (ja) |
| AU (2) | AU2012247762B2 (ja) |
| CA (1) | CA2832360C (ja) |
| ES (1) | ES2806142T3 (ja) |
| MX (1) | MX354371B (ja) |
| WO (1) | WO2012146394A1 (ja) |
Families Citing this family (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HUE025759T2 (en) * | 2009-10-27 | 2016-04-28 | Amgen Res (Munich) Gmbh | Dosage system for administering CD19xCD3 bispecific antibody |
| CN103648529A (zh) * | 2011-04-28 | 2014-03-19 | 安进研发(慕尼黑)股份有限公司 | 用于给处于潜在不良反应的风险的患者施用CD19xCD3双特异性抗体的给药方案 |
| US10851178B2 (en) | 2011-10-10 | 2020-12-01 | Xencor, Inc. | Heterodimeric human IgG1 polypeptides with isoelectric point modifications |
| AU2013347184B2 (en) * | 2012-11-13 | 2018-06-14 | Astellas Pharma Inc. | Agents for treatment of claudin expressing cancer diseases |
| US10131710B2 (en) | 2013-01-14 | 2018-11-20 | Xencor, Inc. | Optimized antibody variable regions |
| US9701759B2 (en) | 2013-01-14 | 2017-07-11 | Xencor, Inc. | Heterodimeric proteins |
| US9605084B2 (en) | 2013-03-15 | 2017-03-28 | Xencor, Inc. | Heterodimeric proteins |
| AU2014205086B2 (en) * | 2013-01-14 | 2019-04-18 | Xencor, Inc. | Novel heterodimeric proteins |
| US11053316B2 (en) | 2013-01-14 | 2021-07-06 | Xencor, Inc. | Optimized antibody variable regions |
| US10487155B2 (en) | 2013-01-14 | 2019-11-26 | Xencor, Inc. | Heterodimeric proteins |
| JO3529B1 (ar) | 2013-02-08 | 2020-07-05 | Amgen Res Munich Gmbh | مضاد التصاق خلايا الدم البيض من أجل التخفيف من الاثار السلبية الممكنة الناتجة عن مجالات ارتباط cd3- المحدد |
| CA2906927C (en) | 2013-03-15 | 2021-07-13 | Xencor, Inc. | Modulation of t cells with bispecific antibodies and fc fusions |
| CN105377889B (zh) * | 2013-03-15 | 2020-07-17 | Xencor股份有限公司 | 异二聚体蛋白 |
| US10106624B2 (en) | 2013-03-15 | 2018-10-23 | Xencor, Inc. | Heterodimeric proteins |
| US10858417B2 (en) | 2013-03-15 | 2020-12-08 | Xencor, Inc. | Heterodimeric proteins |
| US9822186B2 (en) | 2014-03-28 | 2017-11-21 | Xencor, Inc. | Bispecific antibodies that bind to CD38 and CD3 |
| WO2015181683A1 (en) | 2014-05-30 | 2015-12-03 | Amgen Research (Munich) Gmbh | Risk-stratification of b-precursor acute lymphoblastic leukemia patients |
| US10259887B2 (en) | 2014-11-26 | 2019-04-16 | Xencor, Inc. | Heterodimeric antibodies that bind CD3 and tumor antigens |
| MA55043A (fr) | 2014-11-26 | 2021-12-29 | Xencor Inc | Anticorps hétérodimériques se liant à l'antigène cd3 et l'antigène cd20 |
| EP3237449A2 (en) | 2014-12-22 | 2017-11-01 | Xencor, Inc. | Trispecific antibodies |
| WO2016141387A1 (en) | 2015-03-05 | 2016-09-09 | Xencor, Inc. | Modulation of t cells with bispecific antibodies and fc fusions |
| CA2991799A1 (en) | 2015-07-15 | 2017-01-19 | Zymeworks Inc. | Drug-conjugated bi-specific antigen-binding constructs |
| MA44909A (fr) | 2015-09-15 | 2018-07-25 | Acerta Pharma Bv | Association thérapeutique d'un inhibiteur du cd19 et d'un inhibiteur de la btk |
| EP3387013B1 (en) | 2015-12-07 | 2022-06-08 | Xencor, Inc. | Heterodimeric antibodies that bind cd3 and psma |
| JP2019517499A (ja) * | 2016-06-02 | 2019-06-24 | イムノコア リミテッド | gp100特異的TCR−抗CD3 scFv融合タンパク質の投薬レジメン |
| KR102523402B1 (ko) | 2016-06-14 | 2023-04-19 | 젠코어 인코포레이티드 | 이중특이적 체크포인트 억제제 항체 |
| JP7021127B2 (ja) | 2016-06-28 | 2022-02-16 | ゼンコア インコーポレイテッド | ソマトスタチン受容体2に結合するヘテロ二量体抗体 |
| US10793632B2 (en) | 2016-08-30 | 2020-10-06 | Xencor, Inc. | Bispecific immunomodulatory antibodies that bind costimulatory and checkpoint receptors |
| SG11201903302UA (en) | 2016-10-14 | 2019-05-30 | Xencor Inc | Bispecific heterodimeric fusion proteins containing il-15/il-15ralpha fc-fusion proteins and pd-1 antibody fragments |
| WO2019006472A1 (en) | 2017-06-30 | 2019-01-03 | Xencor, Inc. | TARGETED HETETRODIMERIC FUSION PROTEINS CONTAINING IL-15 / IL-15RA AND ANTIGEN-BINDING DOMAINS |
| US10981992B2 (en) | 2017-11-08 | 2021-04-20 | Xencor, Inc. | Bispecific immunomodulatory antibodies that bind costimulatory and checkpoint receptors |
| CA3082383A1 (en) | 2017-11-08 | 2019-05-16 | Xencor, Inc. | Bispecific and monospecific antibodies using novel anti-pd-1 sequences |
| JP2021506291A (ja) | 2017-12-19 | 2021-02-22 | ゼンコア インコーポレイテッド | 改変されたil−2 fc融合タンパク質 |
| CA3096052A1 (en) | 2018-04-04 | 2019-10-10 | Xencor, Inc. | Heterodimeric antibodies that bind fibroblast activation protein |
| CN112437777A (zh) | 2018-04-18 | 2021-03-02 | Xencor股份有限公司 | 包含IL-15/IL-15RA Fc融合蛋白和TIM-3抗原结合结构域的靶向TIM-3的异源二聚体融合蛋白 |
| US11524991B2 (en) | 2018-04-18 | 2022-12-13 | Xencor, Inc. | PD-1 targeted heterodimeric fusion proteins containing IL-15/IL-15Ra Fc-fusion proteins and PD-1 antigen binding domains and uses thereof |
| CN113195523A (zh) | 2018-10-03 | 2021-07-30 | Xencor股份有限公司 | IL-12异源二聚体Fc融合蛋白 |
| TW202028244A (zh) * | 2018-10-09 | 2020-08-01 | 美商建南德克公司 | 用於確定突觸形成之方法及系統 |
| CN114173875A (zh) | 2019-03-01 | 2022-03-11 | Xencor股份有限公司 | 结合enpp3和cd3的异二聚抗体 |
| US20220204620A1 (en) * | 2019-04-30 | 2022-06-30 | Amgen Research (Munich) Gmbh | Means and methods for treating burkitt lymphoma or leukemia |
| KR20230031981A (ko) | 2019-05-14 | 2023-03-07 | 프로벤션 바이오, 인코포레이티드 | 제1형 당뇨병을 예방하기 위한 방법 및 조성물 |
| US11919956B2 (en) | 2020-05-14 | 2024-03-05 | Xencor, Inc. | Heterodimeric antibodies that bind prostate specific membrane antigen (PSMA) and CD3 |
| IL300666A (en) | 2020-08-19 | 2023-04-01 | Xencor Inc | ANTI–CD28 COMPOSITIONS |
| EP4240491A1 (en) | 2020-11-06 | 2023-09-13 | Novartis AG | Cd19 binding molecules and uses thereof |
| MX2023005234A (es) | 2020-11-06 | 2023-05-18 | Novartis Ag | Terapia de combinacion de agente anti-cd19 y agente de direccionamiento a celulas b para el tratamiento de neoplasias malignas de celulas b. |
| EP4305067A1 (en) | 2021-03-09 | 2024-01-17 | Xencor, Inc. | Heterodimeric antibodies that bind cd3 and cldn6 |
| WO2022192586A1 (en) | 2021-03-10 | 2022-09-15 | Xencor, Inc. | Heterodimeric antibodies that bind cd3 and gpc3 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE120761T1 (de) | 1987-05-21 | 1995-04-15 | Creative Biomolecules Inc | Multifunktionelle proteine mit vorbestimmter zielsetzung. |
| TR200003087T2 (tr) * | 1998-04-21 | 2001-02-21 | Micromet Ag | Yeni CD19 X CD3 Spesifik polipeptidler ve kullanımları |
| RU2005141512A (ru) | 2003-05-31 | 2007-07-20 | Микромет Аг (De) | Фармацевтические композиции, включающие биспецифические анти-cd3, анти-cd19 конструкции антител для лечения расстройств, связанных с b-клетками |
| DK1976886T3 (en) | 2005-12-16 | 2015-03-02 | Amgen Res Munich Gmbh | Means and methods for the treatment of tumor diseases |
| BRPI0809594A2 (pt) * | 2007-04-03 | 2019-08-27 | Micromet Ag | polipeptídeo, seqüência de ácido nucléico, vetor, hospedeiro, processo para a produção de um polipeptídeo, composição farmacêutica, uso de um polipeptídeo, método para prevenção, tratamento ou melhora de uma doença, em um indivíduo com necessidade do mesmo, kit, método para a identificação de um polipeptídeo(s) |
| PL2520590T3 (pl) | 2007-04-03 | 2019-02-28 | Amgen Research (Munich) Gmbh | Domena wiążąca wykazująca krzyżową swoistość gatunkową |
| CN107184977A (zh) * | 2008-11-07 | 2017-09-22 | 安进研发(慕尼黑)股份有限公司 | 急性淋巴细胞白血病的治疗方法 |
| HUE025759T2 (en) * | 2009-10-27 | 2016-04-28 | Amgen Res (Munich) Gmbh | Dosage system for administering CD19xCD3 bispecific antibody |
| ES2842937T3 (es) * | 2010-11-10 | 2021-07-15 | Amgen Res Munich Gmbh | Prevención de efectos adversos provocados por dominios de unión específicos de CD3 |
| CN103648529A (zh) * | 2011-04-28 | 2014-03-19 | 安进研发(慕尼黑)股份有限公司 | 用于给处于潜在不良反应的风险的患者施用CD19xCD3双特异性抗体的给药方案 |
| US9486475B2 (en) * | 2013-02-08 | 2016-11-08 | Amgen Research (Munich) Gmbh | PPS for the prevention of potential adverse effects caused by CD3 specific binding domains |
| JO3529B1 (ar) * | 2013-02-08 | 2020-07-05 | Amgen Res Munich Gmbh | مضاد التصاق خلايا الدم البيض من أجل التخفيف من الاثار السلبية الممكنة الناتجة عن مجالات ارتباط cd3- المحدد |
-
2012
- 2012-04-30 CN CN201280020887.XA patent/CN103648529A/zh active Pending
- 2012-04-30 EP EP20178760.3A patent/EP3753572A1/en active Pending
- 2012-04-30 EP EP12724289.9A patent/EP2701741B1/en active Active
- 2012-04-30 CN CN201710597419.3A patent/CN107303387A/zh active Pending
- 2012-04-30 AU AU2012247762A patent/AU2012247762B2/en active Active
- 2012-04-30 WO PCT/EP2012/001857 patent/WO2012146394A1/en active Application Filing
- 2012-04-30 ES ES12724289T patent/ES2806142T3/es active Active
- 2012-04-30 US US14/113,755 patent/US10191034B2/en active Active
- 2012-04-30 KR KR1020137031150A patent/KR102147533B1/ko active IP Right Grant
- 2012-04-30 MX MX2013012448A patent/MX354371B/es active IP Right Grant
- 2012-04-30 KR KR1020207023808A patent/KR102345943B1/ko active IP Right Grant
- 2012-04-30 CA CA2832360A patent/CA2832360C/en active Active
- 2012-04-30 JP JP2014506794A patent/JP6276175B2/ja active Active
-
2017
- 2017-08-21 AU AU2017218919A patent/AU2017218919A1/en not_active Abandoned
- 2017-10-05 JP JP2017194928A patent/JP6539709B2/ja active Active
-
2018
- 2018-12-12 US US16/217,366 patent/US11579142B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CA2832360C (en) | 2022-05-03 |
| EP2701741A1 (en) | 2014-03-05 |
| MX354371B (es) | 2018-02-28 |
| WO2012146394A1 (en) | 2012-11-01 |
| CN107303387A (zh) | 2017-10-31 |
| US20140199307A1 (en) | 2014-07-17 |
| AU2012247762A1 (en) | 2013-10-17 |
| AU2012247762B2 (en) | 2017-07-06 |
| JP2018046824A (ja) | 2018-03-29 |
| JP6539709B2 (ja) | 2019-07-03 |
| KR20140043350A (ko) | 2014-04-09 |
| US20190293635A1 (en) | 2019-09-26 |
| EP3753572A1 (en) | 2020-12-23 |
| ES2806142T3 (es) | 2021-02-16 |
| KR102345943B1 (ko) | 2021-12-31 |
| JP2014513088A (ja) | 2014-05-29 |
| KR20200104415A (ko) | 2020-09-03 |
| CN103648529A (zh) | 2014-03-19 |
| US10191034B2 (en) | 2019-01-29 |
| MX2013012448A (es) | 2014-02-27 |
| CA2832360A1 (en) | 2012-11-01 |
| AU2017218919A1 (en) | 2017-09-07 |
| EP2701741B1 (en) | 2020-06-10 |
| KR102147533B1 (ko) | 2020-08-25 |
| US11579142B2 (en) | 2023-02-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6276175B2 (ja) | 潜在的有害作用リスクのある患者にCD19xCD3二特異性抗体を投与するための投薬レジメン | |
| AU2010311559B2 (en) | Dosage regimen for administering a CD19xCD3 bispecific antibody | |
| BR122019016866B1 (pt) | Método para avaliar (analisar) o risco dos efeitos adversos potenciaispara um paciente humano mediados pela administração de um anticorpobiespecífico de cd19xcd3 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150430 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150430 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160224 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160523 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160824 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20161102 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170202 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170331 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170502 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20170605 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171005 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20171204 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20180104 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20180111 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6276175 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |