JP6092261B2 - 抗ウイルス化合物 - Google Patents
抗ウイルス化合物 Download PDFInfo
- Publication number
- JP6092261B2 JP6092261B2 JP2014558092A JP2014558092A JP6092261B2 JP 6092261 B2 JP6092261 B2 JP 6092261B2 JP 2014558092 A JP2014558092 A JP 2014558092A JP 2014558092 A JP2014558092 A JP 2014558092A JP 6092261 B2 JP6092261 B2 JP 6092261B2
- Authority
- JP
- Japan
- Prior art keywords
- carboxylic acid
- hydroxy
- pyrrolidine
- amino
- naphthalene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 Oc(c(cccc1)c1cc1)c1C(*[C@@](C1)CN(CC2CCCCC2)[C@@]1c1ncc(-c2ccccc2)[o]1)=O Chemical compound Oc(c(cccc1)c1cc1)c1C(*[C@@](C1)CN(CC2CCCCC2)[C@@]1c1ncc(-c2ccccc2)[o]1)=O 0.000 description 6
- ACNBSHOSYNFEJQ-OLZOCXBDSA-N COC([C@H](C1)N(CC2CCCCC2)CC[C@H]1N)=O Chemical compound COC([C@H](C1)N(CC2CCCCC2)CC[C@H]1N)=O ACNBSHOSYNFEJQ-OLZOCXBDSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N OC(C(F)(F)F)=O Chemical compound OC(C(F)(F)F)=O DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- LBRXHOPVDMLJCW-RZSVFLSASA-N C/C(/N)=C(\C=C/C=C)/Br Chemical compound C/C(/N)=C(\C=C/C=C)/Br LBRXHOPVDMLJCW-RZSVFLSASA-N 0.000 description 1
- XUCMXXAZYCWLEN-BTFOHMIHSA-N C/C=C(/COC(N(C[C@@H](C1)OS(c2ccc(C)cc2)(=O)=O)C1c1nc(cccc2)c2[o]1)=O)\C=C/C=C Chemical compound C/C=C(/COC(N(C[C@@H](C1)OS(c2ccc(C)cc2)(=O)=O)C1c1nc(cccc2)c2[o]1)=O)\C=C/C=C XUCMXXAZYCWLEN-BTFOHMIHSA-N 0.000 description 1
- HAHPRFKJPFJPKI-JTQLQIEISA-N CC(C)(C)CCN(CC(C1)=[N+]=N)[C@@H]1C(OC)=O Chemical compound CC(C)(C)CCN(CC(C1)=[N+]=N)[C@@H]1C(OC)=O HAHPRFKJPFJPKI-JTQLQIEISA-N 0.000 description 1
- RNMVWSAJMIKMDY-IUCAKERBSA-N CC(C)(C)OC(N(CC[C@@H](C1)O)[C@@H]1C(OC)=O)=O Chemical compound CC(C)(C)OC(N(CC[C@@H](C1)O)[C@@H]1C(OC)=O)=O RNMVWSAJMIKMDY-IUCAKERBSA-N 0.000 description 1
- JNIVAMILFKQRQC-HOCLYGCPSA-N CC(C)(C)OC(N(CC[C@@H](C1)OS(c2ccc(C)cc2)(=O)=O)[C@@H]1C(OC)=O)=O Chemical compound CC(C)(C)OC(N(CC[C@@H](C1)OS(c2ccc(C)cc2)(=O)=O)[C@@H]1C(OC)=O)=O JNIVAMILFKQRQC-HOCLYGCPSA-N 0.000 description 1
- SDIKSYQJURNZIL-BDAKNGLRSA-N CC(C)(C)OC(N(CC[C@H](C1)N=[N+]=N)[C@@H]1C(OC)=O)=O Chemical compound CC(C)(C)OC(N(CC[C@H](C1)N=[N+]=N)[C@@H]1C(OC)=O)=O SDIKSYQJURNZIL-BDAKNGLRSA-N 0.000 description 1
- HAOXYRATYSKLSG-OAHLLOKOSA-N CC(C)(C)O[C@H](C1)CN(C(OCc2ccccc2)=O)C1=C Chemical compound CC(C)(C)O[C@H](C1)CN(C(OCc2ccccc2)=O)C1=C HAOXYRATYSKLSG-OAHLLOKOSA-N 0.000 description 1
- VTRGJDSQUBURDB-DUSLRRAJSA-N CC(C)(C)O[C@H](CC1c2nc(cccc3)c3[o]2)CN1C(OCc1ccccc1)=O Chemical compound CC(C)(C)O[C@H](CC1c2nc(cccc3)c3[o]2)CN1C(OCc1ccccc1)=O VTRGJDSQUBURDB-DUSLRRAJSA-N 0.000 description 1
- JCIGYNJCCWXVIH-CVEARBPZSA-N CC(C)(C)O[C@H](C[C@H]1c2ncc[o]2)CN1C(OCc1ccccc1)=O Chemical compound CC(C)(C)O[C@H](C[C@H]1c2ncc[o]2)CN1C(OCc1ccccc1)=O JCIGYNJCCWXVIH-CVEARBPZSA-N 0.000 description 1
- LDCHQLFDKUTDSP-MDWODPDHSA-N CC1(C=CC=CC1)c1cnc([C@H](C2)N(CC3CCCCC3)C[C@H]2NC(c(ccc2c3cccc2)c3O)=O)[o]1 Chemical compound CC1(C=CC=CC1)c1cnc([C@H](C2)N(CC3CCCCC3)C[C@H]2NC(c(ccc2c3cccc2)c3O)=O)[o]1 LDCHQLFDKUTDSP-MDWODPDHSA-N 0.000 description 1
- KBWOQDZAOSEOGF-ZDUSSCGKSA-N COC([C@H](C1)N(CC2CCCCC2)CCC1=[N+]=N)=O Chemical compound COC([C@H](C1)N(CC2CCCCC2)CCC1=[N+]=N)=O KBWOQDZAOSEOGF-ZDUSSCGKSA-N 0.000 description 1
- SHYCNVQYHJEFJJ-NQIIRXRSSA-N COC([C@H](C1)N(CC2CCCCC2)C[C@@H]1NC(c(ccc1c2cccc1)c2O)=O)=O Chemical compound COC([C@H](C1)N(CC2CCCCC2)C[C@@H]1NC(c(ccc1c2cccc1)c2O)=O)=O SHYCNVQYHJEFJJ-NQIIRXRSSA-N 0.000 description 1
- FPBGGHWZOPEXMR-RYUDHWBXSA-N COC([C@H](C1)N(CC2CCCCC2)C[C@H]1N=[N+]=[N-])=O Chemical compound COC([C@H](C1)N(CC2CCCCC2)C[C@H]1N=[N+]=[N-])=O FPBGGHWZOPEXMR-RYUDHWBXSA-N 0.000 description 1
- WCIFBCVKXZIWBR-JEAXJGTLSA-N COC([C@H](C1)NCC[C@H]1N=[N+]=[N-])O Chemical compound COC([C@H](C1)NCC[C@H]1N=[N+]=[N-])O WCIFBCVKXZIWBR-JEAXJGTLSA-N 0.000 description 1
- ZRZSUEGVAWYGBP-WABBHOIFSA-N C[N+](=N)=N[C@@H](C1)CN[C@@H]1C(O)OC Chemical compound C[N+](=N)=N[C@@H](C1)CN[C@@H]1C(O)OC ZRZSUEGVAWYGBP-WABBHOIFSA-N 0.000 description 1
- SHHGSZVXJWSCTB-KBPBESRZSA-N Cc1cnc([C@H](C[C@@H](C2)N)N2C(OCc2ccccc2)=O)[o]1 Chemical compound Cc1cnc([C@H](C[C@@H](C2)N)N2C(OCc2ccccc2)=O)[o]1 SHHGSZVXJWSCTB-KBPBESRZSA-N 0.000 description 1
- BLLOKDDEKMHUKM-KGLIPLIRSA-N Cc1cnc([C@H](C[C@H](C2)O)N2C(OCc2ccccc2)=O)[o]1 Chemical compound Cc1cnc([C@H](C[C@H](C2)O)N2C(OCc2ccccc2)=O)[o]1 BLLOKDDEKMHUKM-KGLIPLIRSA-N 0.000 description 1
- OHWIHFWQMRBQMV-UHFFFAOYSA-N O=CNc(cccc1)c1Br Chemical compound O=CNc(cccc1)c1Br OHWIHFWQMRBQMV-UHFFFAOYSA-N 0.000 description 1
- QDFOWWUSLOCTAO-REWPJTCUSA-N Oc(c(cccc1)c1cc1)c1C(N[C@@H](C1)CN(CC2CCCCC2)[C@@H]1C(N1CCC1)=O)=O Chemical compound Oc(c(cccc1)c1cc1)c1C(N[C@@H](C1)CN(CC2CCCCC2)[C@@H]1C(N1CCC1)=O)=O QDFOWWUSLOCTAO-REWPJTCUSA-N 0.000 description 1
- YUJOKPWXAVUIOK-WFASDCNBSA-N Oc(c(cccc1)c1cc1)c1C(N[C@@H](C1)CN[C@@H]1c1ncc[o]1)=O Chemical compound Oc(c(cccc1)c1cc1)c1C(N[C@@H](C1)CN[C@@H]1c1ncc[o]1)=O YUJOKPWXAVUIOK-WFASDCNBSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/04—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D207/10—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D207/16—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/60—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Virology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Veterinary Medicine (AREA)
- Molecular Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Hydrogenated Pyridines (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pyrrole Compounds (AREA)
Description
nは、1または2であり;
Qは、1個以上のQ’で置換されたフェニルまたはナフタレンであり;
Q’は、ヒドロキシル、低級アルキル、またはハロであり;
R1は、低級アルキル、シクロアルキル、フェニル、またはヘテロシクロアルキルであり;
R2は、−C(=O)OR2’、−C(=O)R2’、−C(=O)ON(R2’)2、任意に1個以上のR2’で置換されていてもよい単環式または二環式ヘテロアリールであり;
R2’はそれぞれ、独立してH、低級アルキルまたはヘテロシクロアルキルであり;
R3は、Hまたは低級アルキルであり;
Xは、CH2またはC(=O)である]
またはその医薬的に許容できる塩を提供する。
本出願は、式の化合物および医薬的に許容できる賦形剤を含む医薬組成物を提供する。
本明細書中で用いる句“a”または“an”の物は、1以上のその物を表わす;たとえば、a compoundは、one or more compounds(1種類以上の化合物)またはat least one compound(少なくとも1種類の化合物)を表わす。したがって、“a” (または“an”)、“one or more(1以上)”、および“at least one(少なくとも1)”は本明細書中で互換性をもって使用できる。
本明細書中で用いる用語“任意の(optional)”または“任意に(optionally)”は、それに続いて記載する事象または状況が出現してもよいが、その必要はないこと、およびその記載はその事象または状況が出現する場合とそれが出現しない場合とを含むことを意味する。たとえば、“任意に置換されていてもよい”は、その任意に置換されていてもよい部分が水素原子または置換基を含むことができることを意味する。
本明細書中で用いる用語“アルキル”は、1〜10個の炭素原子を含む非分枝鎖または分枝鎖、飽和、一価の炭化水素残基を表わす。用語“低級アルキル”は、1〜6個の炭素原子を含む直鎖または分枝鎖の炭化水素残基を表わす。本明細書中で用いる“C1−10アルキル”は、1〜10個の炭素から構成されるアルキルを表わす。アルキル基の例には低級アルキルが含まれるが、これらに限定されず、メチル、エチル、プロピル、i−プロピル、n−ブチル、i−ブチル、t−ブチルまたはペンチル、イソペンチル、ネオペンチル、ヘキシル、ヘプチル、およびオクチルが含まれる。
用語“ハロアルコキシ”または“ハロ−低級アルコキシ”または“低級ハロアルコキシ”は、低級アルコキシ基において1個以上の炭素原子が1個以上のハロゲン原子で置換されたものを表わす。
本明細書中で用いる用語“ヘテロアリール”または“ヘテロ芳香族”は、少なくとも1つの芳香環または部分不飽和環をもつ、環当たり4〜8個の原子を含む環原子5〜12個の単環式または二環式ラジカルであって、1個以上のN、OまたはSヘテロ原子を含み、残りの環原子が炭素であるものを意味する;ヘテロアリールラジカルの結合点は芳香環または部分不飽和環上にあると理解される。当業者に周知のように、ヘテロアリール環はそれらの全炭素カウンターパートより低い芳香族性をもつ。したがって、本発明の目的にとって、ヘテロアリール基はある程度の芳香族性をもつだけでよい。ヘテロアリール部分の例には5〜6個の環原子および1〜3個のヘテロ原子をもつ単環式芳香族複素環が含まれ、これには下記のものが含まれるが、これらに限定されない:ピリジニル、ピリミジニル、ピラジニル、オキサジニル、ピロリル、ピラゾリル、イミダゾリル、オキサゾリル、4,5−ジヒドロ−オキサゾリル、5,6−ジヒドロ−4H−[1,3]オキサゾリル、イソオキサゾール、チアゾール、イソチアゾール、トリアゾリン、チアジアゾールおよびオキサジアキソリン(oxadiaxoline);これらは任意に、下記のものから選択される1個以上、好ましくは1または2個の置換基で置換されていてもよい:ヒドロキシ、シアノ、アルキル、アルコキシ、チオ、低級ハロアルコキシ、アルキルチオ、ハロ、低級ハロアルキル、アルキルスルフィニル、アルキルスルホニル、ハロゲン、アミノ、アルキルアミノ、ジアルキルアミノ、アミノアルキル、アルキルアミノアルキル、およびジアルキルアミノアルキル、ニトロ、アルコキシカルボニルおよびカルバモイル、アルキルカルバモイル、ジアルキルカルバモイル、アリールカルバモイル、アルキルカルボニルアミノおよびアリールカルボニルアミノ。二環式部分の例には下記のものが含まれるが、これらに限定されない:キノリニル、イソキノリニル、ベンゾフリル、ベンゾチオフェニル、ベンゾオキサゾール、ベンゾイソオキサゾール、ベンゾチアゾール、ナフチリジニル、5,6,7,8−テトラヒドロ−[1,6]ナフチリジニル、およびベンゾイソチアゾール。二環式部分は任意にいずれの環において置換されていてもよいが、結合点はヘテロ原子を含む環上にある。
本出願は、式Iの化合物
nは、1または2であり;
Qは、1個以上のQ’で置換されたフェニルまたはナフタレンであり;
Q’は、ヒドロキシル、低級アルキル、またはハロであり;
R1は、低級アルキル、シクロアルキル、フェニル、またはヘテロシクロアルキルであり;
R2は、−C(=O)OR2’、−C(=O)R2’、−C(=O)ON(R2’)2、任意に1個以上のR2’で置換されていてもよい単環式または二環式ヘテロアリールであり;
R2’はそれぞれ、独立してH、低級アルキルまたはヘテロシクロアルキルであり;
R3は、Hまたは低級アルキルであり;
Xは、CH2またはC(=O)である]
またはその医薬的に許容できる塩を提供する。
本出願は、R3がHである、式Iの化合物を提供する。
本出願は、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、XがCH2であり、R3がHである、式Iの化合物を提供する。
本出願は、XがCH2であり、かつnが1である、式Iの化合物を提供する。
本出願は、R2が−C(=O)N(R2’)2である、式Iの化合物を提供する。
本出願は、R2が−C(=O)N(R2’)2であり、かつR3がHである、式Iの化合物を提供する。
本出願は、R2が−C(=O)N(R2’)2であり、XがCH2であり、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、R2が−C(=O)OR2’である、式Iの化合物を提供する。
本出願は、R2が−C(=O)OR2’であり、かつR2’が低級アルキルである、式Iの化合物を提供する。
本出願は、R2’が低級アルキルであり、XがCH2であり、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、R1が低級アルキルまたはシクロアルキルである、式Iの化合物を提供する。
本出願は、R1が低級アルキルまたはシクロアルキルであり、R2が−C(=O)OR2’であり、R2’が低級アルキルであり、XがCH2であり、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、R3がHである、式Iの化合物を提供する。
本出願は、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、XがCH2であり、かつR3がHである、式Iの化合物を提供する。
本出願は、XがCH2であり、かつnが1である、式Iの化合物を提供する。
本出願は、R2が−C(=O)N(R2’)2である、式Iの化合物を提供する。
本出願は、R2が−C(=O)N(R2’)2であり、かつR3がHである、式Iの化合物を提供する。
本出願は、R2が−C(=O)N(R2’)2であり、XがCH2であり、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、R2が−C(=O)OR2’である、式Iの化合物を提供する。
本出願は、R2が−C(=O)OR2’であり、かつR2’が低級アルキルである、式Iの化合物を提供する。
本出願は、R2’が低級アルキルであり、XがCH2であり、R3がHであり、かつnが1である、式Iの化合物を提供する。
本出願は、R1が低級アルキルまたはシクロアルキルである、式Iの化合物を提供する。
本出願は、R1が低級アルキルまたはシクロアルキルであり、R2が−C(=O)OR2’であり、R2’が低級アルキルであり、XがCH2であり、R3がHであり、かつnが1である、式Iの化合物を提供する。
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 tert−ブチルエステル;
(2S,4S)−1−(3,3−ジメチル−ブチル)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−5−ベンゾオキサゾール−2−イル−1−シクロヘキシルメチル−ピロリジン−3−イル)−アミド;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 メチルエステル;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−メチル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−フェニル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−1−シクロヘキシルメチル−5−オキサゾール−2−イル−ピロリジン−3−イル)−アミド;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロペンチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 ベンジルアミド;
(2S,4S)−1−シクロヘキサンカルボニル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 イソプロピルアミド;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 プロピルアミド;
(2S,4S)−1−シクロブチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルアミド;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルアミド;
(2R,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−1−イソブチル−ピロリジン−2−カルボン酸 エチルエステル;
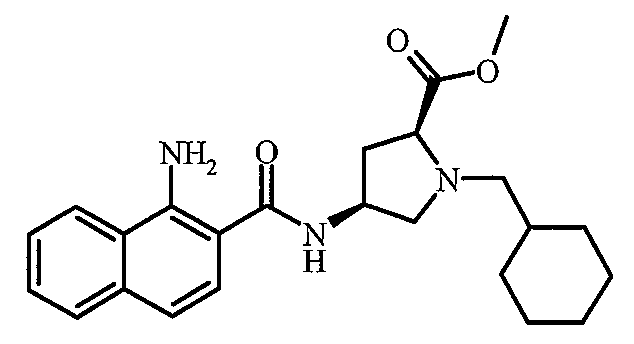
(2S,4S)−4−[(1−アミノ−ナフタレン−2−カルボニル)−アミノ]−1−シクロヘキシルメチル−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(8−ヒドロキシ−キノリン−7−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(ピロリジン−1−カルボニル)−ピロリジン−3−イル]−アミド;
(2S,4R)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;および
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−5−(アゼチジン−1−カルボニル)−1−シクロヘキシルメチル−ピロリジン−3−イル]−アミド。
本出願は、さらに、免疫系調節薬もしくはHCVの複製を阻害する抗ウイルス薬またはその組合わせを投与することを含む、上記方法を提供する。
本出願は、抗ウイルス薬がHCVプロテアーゼ阻害薬、HCVポリメラーゼ阻害薬、HCVヘリカーゼ阻害薬、HCVプライマーゼ阻害薬、HCV融合阻害薬、およびその組合わせからなる群から選択される、上記方法を提供する。
本出願は、式Iの化合物および医薬的に許容できる賦形剤を含む組成物を提供する。
本出願は、本明細書に記載する化合物、組成物、または方法を提供する。
化合物
本発明により包含される、本発明の範囲に含まれる代表的化合物の例を下記の表に提示する。これらの例およびそれに続く製造法は、当業者が本発明をより明瞭に理解し、実施することができるように提供される。それらは本発明の限定とみなすべきではなく、本発明の説明および代表例にすぎない。
一般的スキーム
合成−一般的反応スキーム
幾つかの経路で投与するための本発明化合物の医薬組成物をこの例に記載するように調製した。
本発明の化合物を多様な経口投与剤形およびキャリヤー中に配合することができる。経口投与は、錠剤、コーティング錠、糖衣丸、硬および軟ゼラチンカプセル剤、液剤、乳剤、シロップ剤、または懸濁液剤の形態で行なうことができる。本発明の化合物は、他の投与経路のうちでは特に、連続(静脈内点滴) 局所 非経口、筋肉内、静脈内、皮下、経皮(これは透過促進剤を含有することができる)、口腔、鼻腔、吸入および坐剤投与を含めた他の投与経路で投与した場合に有効である。好ましい投与様式は、一般に、好都合な各日投与計画を用いる経口様式であり、これは疾患の程度および有効成分に対する患者の応答に従って調整できる。
適応症
本発明の化合物およびそれらの異性体形態ならびにその医薬的に許容できる塩類は、HCV感染症を治療および予防するのに有用である。
本出願は、式Iの化合物を投与することを含む、細胞においてHCVの複製を阻害するための方法を提供する。
本発明の化合物およびそれらの異性体形態ならびにその医薬的に許容できる塩類は、単独で、またはHCVライフサイクルに関与するウイルスもしくは細胞のエレメントもしくは機能をターゲティングする他の化合物と併用した際に、HCV感染症を治療および予防するのに有用である。本発明に有用なクラスの化合物には、限定ではなく、すべてのクラスのHCV抗ウイルス薬が含まれる。
本出願は、さらに、免疫系調節薬もしくはHCVの複製を阻害する抗ウイルス薬またはその組合わせを投与することを含む、上記方法を提供する。
本出願は、抗ウイルス薬がHCVプロテアーゼ阻害薬、HCVポリメラーゼ阻害薬、HCVヘリカーゼ阻害薬、HCVプライマーゼ阻害薬、HCV融合阻害薬、およびその組合わせからなる群から選択される、上記方法を提供する。
一般的に用いられる略号には下記のものが含まれる:アセチル(Ac)、アゾ−ビス−イソブチロニトリル(AIBN)、大気(Atm)、9−ボラビシクロ[3.3.1]ノナン(9−BBNまたはBBN)、2,2’−ビス(ジフェニルホスフィノ)−1,1’−ビナフチル(BINAP)、tert−ブトキシカルボニル(Boc)、ピロ炭酸ジ−tert−ブチルまたはbocアンヒドリド(BOC2O)、ベンジル(Bn)、ブチル(Bu)、ケミカルアブストラクツ登録番号(CASRN)、ベンジルオキシカルボニル(CBZまたはZ)、カルボニルジイミダゾール(CDI)、1,4−ジアザビシクロ[2.2.2]オクタン(DABCO)、三フッ化ジエチルアミノ硫黄(DAST)、ジベンジリデンアセトン(dba)、1,5−ジアザビシクロ[4.3.0]ノナ−5−エン(DBN)、1,8−ジアザビシクロ[5.4.0]ウンデカ−7−エン(DBU)、N,N’−ジシクロヘキシルカルボジイミド(DCC)、1,2−ジクロロエタン(DCE)、ジクロロメタン(DCM)、2,3−ジクロロ−5,6−ジシアノ−1,4−ベンゾキノン(DDQ)、アゾジカルボン酸ジエチル(DEAD)、アゾジカルボン酸 ジ−イソ−プロピル(DIAD)、水素化ジ−イソ−ブチルアルミニウム(DIBALまたはDIBAL−H)、ジ−イソ−プロピルエチルアミン(DIPEA)、N,N−ジメチルアセトアミド(DMA)、4−N,N−ジメチルアミノピリジン(DMAP)、N,N−ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)、1,1’−ビス−(ジフェニルホスフィノ)エタン(dppe)、1,1’−ビス−(ジフェニルホスフィノ)フェロセン(dppf)、1−(3−ジメチルアミノプロピル)−3−エチルカルボジイミド塩酸塩(EDCI)、2−エトキシ−1−エトキシカルボニル−1,2−ジヒドロキノリン(EEDQ)、エチル(Et)、酢酸エチル(EtOAc)、エタノール(EtOH)、2−エトキシ−2H−キノリン−1−カルボン酸 エチルエステル(EEDQ)、ジエチルエーテル(Et2O)、エチルイソプロピルエーテル(EtOiPr)、O−(7−アザベンゾトリアゾール−1−イル)−N、N,N’N’−テトラメチルウロニウムヘキサフルオロホスフェート酢酸(HATU)、酢酸(HOAc)、1−N−ヒドロキシベンゾトリアゾール(HOBt)、高速液体クロマトグラフィー(HPLC)、イソ−プロパノール(IPA)、イソプロピルマグネシウムクロリド(iPrMgCl)、ヘキサメチルジシラザン(HMDS)、液体クロマトグラフィー質量分析(LCMS)、リチウムヘキサメチルジシラザン(LiHMDS)、メタ−クロロペルオキシ安息香酸(m−CPBA)、メタノール(MeOH)、融点(mp)、MeSO2−(メシルまたはMs)、メチル(Me)、アセトニトリル(MeCN)、m−クロロ過安息香酸(MCPBA)、質量スペクトル(ms)、メチル t−ブチルエーテル(MTBE)、メチルテトラヒドロフラン(MeTHF)、N−ブロモスクシンイミド(NBS)、n−ブチルリチウム(nBuLi)、N−カルボキシアンヒドリド(NCA)、N−クロロスクシンイミド(NCS)、N−メチルモルホリン(NMM)、N−メチルピロリドン(NMP)、クロロクロム酸ピリジニウム(PCC)、ジクロロ−((ビス−ジフェニルホスフィノ)フェロセニル)パラジウム(II)(Pd(dppf)Cl2)、酢酸パラジウム(II)(Pd(OAc)2)、トリス(ジベンジリデンアセトン)二パラジウム(0)(Pd2(dba)3)、二クロム酸ピリジニウム(PDC)、フェニル(Ph)、プロピル(Pr)、イソ−プロピル(i−Pr)、ポンド/平方インチ(psi)、ピリジン(pyr)、1,2,3,4,5−ペンタフェニル−1’−(ジ−tert−ブチルホスフィノ)フェロセン(Q−Phos)、室温(周囲温度、rtまたはRT)、sec−ブチルリチウム(sBuLi)、tert−ブチルジメチルシリルまたはt−BuMe2Si(TBDMS)、フッ化テトラ−n−ブチルアンモニウム(TBAF)、トリエチルアミン(TEAまたはEt3N)、2,2,6,6−テトラメチルピペリジン 1−オキシル(TEMPO)、トリフレートまたはCF3SO2−(Tf)、トリフルオロ酢酸(TFA)、1,1’−ビス−2,2,6,6−テトラメチルヘプタン−2,6−ジオン(TMHD)、O−ベンゾトリアゾール−1−イル−N,N,N’,N’−テトラメチルウロニウムテトラフルオロボレート(TBTU)、薄層クロマトグラフィー(TLC)、テトラヒドロフラン(THF)、トリメチルシリルまたはMe3Si(TMS)、p−トルエンスルホン酸1水和物(TsOHまたはpTsOH)、4−Me−C6H4SO2−またはトシル(Ts)、およびN−ウレタン−N−カルボキシアンヒドリド(UNCA)。接頭辞ノルマル(n)、イソ(i−)、第二級(sec−)、第三級(tert−)およびneoを含む一般的な名称は、アルキル部分と共に用いられる場合、それらの慣用される意味をもつ。(J. Rigaudy and D. P. Klesney, Nomenclature in Organic Chemistry, IUPAC 1979 Pergamon Press, Oxford.)。
本発明の化合物は、以下の具体例のセクションに記載される具体的な合成反応に示す多様な方法により製造できる。
(2S,4S)−4−アミノ−1−シクロヘキシルメチル−ピロリジン−2−カルボン酸 メチルエステルの製造
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル
(2S,4S)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル
(2S,4S)−1−(3,3−ジメチル−ブチル)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル
(2S,4S)−1−シクロペンチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル
(2S,4S)−1−シクロブチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル
(2S,4S)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−1−イソブチル−ピロリジン−2−カルボン酸 エチルエステル
(2S,4S)−1−シクロヘキサンカルボニル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 tert−ブチルエステル
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルアミド
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−5−(アゼチジン−1−カルボニル)−1−シクロヘキシルメチル−ピロリジン−3−イル]−アミド
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 プロピルアミド
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 イソプロピルアミド
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 ベンジルアミド
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(ピロリジン−1−カルボニル)−ピロリジン−3−イル]−アミド
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸アミド
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 メチルエステル
(2R,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 メチルエステル
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 メチルエステル
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 エチルエステル
(2S,4S)−4−[(1−アミノ−ナフタレン−2−カルボニル)−アミノ]−1−シクロヘキシルメチル−ピロリジン−2−カルボン酸 メチルエステル
(2S,4S)−1−シクロヘキシルメチル−4−[(8−ヒドロキシ−キノリン−7−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 メチルエステル
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルエステル
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルアミド
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−1−シクロヘキシルメチル−5−オキサゾール−2−イル−ピロリジン−3−イル)−アミド
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−メチル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−フェニル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−5−ベンゾオキサゾール−2−イル−1−シクロヘキシルメチル−ピロリジン−3−イル)−アミド
レプリコンルシフェラーゼレポーターアッセイを用いる、化合物のHCV GT1b阻害レプリコン活性の測定
2209−23細胞系はRocheにおいて、先に記載されたようにヘパトーマ細胞系Huh−7をGT−1b Con1サブゲノム バイシストロニックレプリコン(bicistronic replicon)で安定トランスフェクションすることにより開発された。サブゲノムレプリコン細胞系を、R. Bartenschlager (J Virol. 2003 Mar; 77 (5):3007-19)から得られたキュアした(cured)Huh7細胞において樹立した。GT−1a H77サブゲノムレプリコンベクターpRLuc H77 1b 75 S/Iは、GT−1b Con1サブゲノムレプリコンの非構造領域を、GT−1b Con1株に由来するNS3タンパク質の最初の75アミノ酸以外において、H77株のひとつで置き換えることにより作製された(J Virol. 2001 77:5352-59)。GT−1a pRLuc H77 1b 75 S/Iサブゲノムレプリコン細胞系を、R. Bartenschlager. (J Virol. 2003 Mar; 77 (5):3007-19)から得られたキュアしたHuh7細胞において樹立した。
細胞生存性試験のために、2209−23細胞をウェル当たり5000個の細胞密度で透明平底96ウェルプレート(Becton Dickinson,カタログ# 35 3075)にプレーティングした。WST−1細胞増殖アッセイ(Roche Diagnostic,カタログ# 11644807001)を用いて細胞生存性を測定した。アッセイプレートをレプリコンアッセイの場合と同じ方式で設定した。製造業者の指示に従って、化合物インキュベーションの3日後に10μlのWST−1試薬を各ウェルに37℃および5% CO2で2時間添加した。450nm(基準フィルター650nm)における吸収の読みを、MRX Revelationマイクロタイタープレートリーダー(Lab System)により測定した。CC50値は化合物が存在しない非処理対照と比較して細胞生存性を50%低下させるのに要した化合物濃度と定義され、化合物用量応答データの非線形フィッティングにより決定された。代表的なアッセイデータを下記の表IIにみることができる。
本明細書は以下の発明の開示を包含する:
[1]式Iの化合物
Aは、CHまたはNであり;
nは、1または2であり;
R 1 は、低級アルキル、シクロアルキル、フェニル、またはヘテロシクロアルキルであり;
R 2 は、−C(=O)OR 2 ’、−C(=O)N(R 2 ’) 2 、任意に1個以上のR 2 ’で置換されていてもよい単環式または二環式ヘテロアリールであり;
R 2 ’はそれぞれ、独立してH、低級アルキルまたはヘテロシクロアルキルであり;
R 3 は、Hまたは低級アルキルであり;
R 4 は、ヒドロキシルまたはアミノであり;
Xは、CH 2 またはC(=O)である]
またはその医薬的に許容できる塩。
[2]R 3 がHであり、かつXがCH 2 である、[2]に記載の化合物。
[3]nが2である、[2]に記載の化合物。
[4]nが1である、[2]に記載の化合物。
[5]R 2 が−C(=O)N(R 2 ’) 2 である、[4]に記載の化合物。
[6]R 2 が、任意に1個以上のR 2 ’で置換されていてもよい単環式または二環式ヘテロアリールである、[4]に記載の化合物。
[7]R 2 が−C(=O)OR 2 ’である、[4]に記載の化合物。
[8]R 2 ’が低級アルキルである、[7]に記載の化合物。
[9]R 1 が低級アルキルまたはシクロアルキルである、[8]に記載の化合物。
[10]R 1 がシクロヘキシルである、[9]に記載の化合物。
[11]下記の群から選択される化合物:
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 tert−ブチルエステル;
(2S,4S)−1−(3,3−ジメチル−ブチル)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−5−ベンゾオキサゾール−2−イル−1−シクロヘキシルメチル−ピロリジン−3−イル)−アミド;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 メチルエステル;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−メチル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−フェニル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−1−シクロヘキシルメチル−5−オキサゾール−2−イル−ピロリジン−3−イル)−アミド;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロペンチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 ベンジルアミド;
(2S,4S)−1−シクロヘキサンカルボニル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 イソプロピルアミド;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 プロピルアミド;
(2S,4S)−1−シクロブチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルアミド;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルアミド;
(2R,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−1−イソブチル−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−4−[(1−アミノ−ナフタレン−2−カルボニル)−アミノ]−1−シクロヘキシルメチル−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(8−ヒドロキシ−キノリン−7−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(ピロリジン−1−カルボニル)−ピロリジン−3−イル]−アミド;
(2S,4R)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;および
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−5−(アゼチジン−1−カルボニル)−1−シクロヘキシルメチル−ピロリジン−3−イル]−アミド。
[12]療法有効物質として使用するための、[1]〜[11]のいずれかに記載の化合物。
[13]C型肝炎ウイルス(HCV)感染症の治療または予防のための、[1]〜[11]のいずれかに記載の化合物の使用。
[14]C型肝炎ウイルス(HCV)感染症の治療または予防のための医薬を調製するための、[1]〜[11]のいずれかに記載の化合物の使用。
[15]C型肝炎ウイルス(HCV)感染症の治療または予防のための、[1]〜[11]のいずれかに記載の化合物。
[16]その必要がある患者に療法有効量の[1]〜[11]のいずれかに記載の化合物を投与することを含む、C型肝炎ウイルス(HCV)感染症を処置するための方法。
[17][1]〜[11]のいずれかに記載の化合物および医薬的に許容できる賦形剤を含む医薬組成物。
[18]以上に記載した発明。
Claims (17)
- R3がHであり、かつXがCH2である、請求項1に記載の化合物。
- nが2である、請求項2に記載の化合物。
- nが1である、請求項2に記載の化合物。
- R2が−C(=O)N(R2’)2である、請求項4に記載の化合物。
- R2が、任意に1個以上のR2’で置換されていてもよい単環式または二環式ヘテロアリールである、請求項4に記載の化合物。
- R2が−C(=O)OR2’である、請求項4に記載の化合物。
- R2’が低級アルキルである、請求項7に記載の化合物。
- R1が低級アルキルまたはシクロアルキルである、請求項8に記載の化合物。
- R1がシクロヘキシルである、請求項9に記載の化合物。
- 下記の群から選択される化合物:
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 tert−ブチルエステル;
(2S,4S)−1−(3,3−ジメチル−ブチル)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−5−ベンゾオキサゾール−2−イル−1−シクロヘキシルメチル−ピロリジン−3−イル)−アミド;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 メチルエステル;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−メチル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(5−フェニル−オキサゾール−2−イル)−ピロリジン−3−イル]−アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 ((3S,5S)−1−シクロヘキシルメチル−5−オキサゾール−2−イル−ピロリジン−3−イル)−アミド;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロペンチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 ベンジルアミド;
(2S,4S)−1−シクロヘキサンカルボニル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 イソプロピルアミド;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 プロピルアミド;
(2S,4S)−1−シクロブチルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルアミド;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピペリジン−2−カルボン酸 エチルアミド;
(2R,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−2−メチル−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−1−イソブチル−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−4−[(1−アミノ−ナフタレン−2−カルボニル)−アミノ]−1−シクロヘキシルメチル−ピロリジン−2−カルボン酸 メチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(8−ヒドロキシ−キノリン−7−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4S)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸アミド;
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−1−シクロヘキシルメチル−5−(ピロリジン−1−カルボニル)−ピロリジン−3−イル]−アミド;
(2S,4R)−1−ベンジル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 エチルエステル;
(2S,4R)−1−シクロヘキシルメチル−4−[(1−ヒドロキシ−ナフタレン−2−カルボニル)−アミノ]−ピロリジン−2−カルボン酸 メチルエステル;および
1−ヒドロキシ−ナフタレン−2−カルボン酸 [(3S,5S)−5−(アゼチジン−1−カルボニル)−1−シクロヘキシルメチル−ピロリジン−3−イル]−アミド。 - 療法有効物質として使用するための、請求項1〜11のいずれか1項に記載の化合物。
- 請求項1〜11のいずれか1項に記載の化合物を含む、C型肝炎ウイルス(HCV)感染症の治療または予防のための医薬組成物。
- C型肝炎ウイルス(HCV)感染症の治療または予防のための医薬を調製するための、請求項1〜11のいずれか1項に記載の化合物の使用。
- C型肝炎ウイルス(HCV)感染症の治療または予防のための、請求項1〜11のいずれか1項に記載の化合物。
- 請求項1〜11のいずれか1項に記載の化合物を含む、C型肝炎ウイルス(HCV)感染症を治療するための医薬組成物。
- 請求項1〜11のいずれか1項に記載の化合物および医薬的に許容できる賦形剤を含む医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261602687P | 2012-02-24 | 2012-02-24 | |
| US61/602,687 | 2012-02-24 | ||
| PCT/EP2013/053409 WO2013124335A1 (en) | 2012-02-24 | 2013-02-21 | Antiviral compounds |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015508088A JP2015508088A (ja) | 2015-03-16 |
| JP6092261B2 true JP6092261B2 (ja) | 2017-03-08 |
Family
ID=47740975
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014558092A Expired - Fee Related JP6092261B2 (ja) | 2012-02-24 | 2013-02-21 | 抗ウイルス化合物 |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US9090559B2 (ja) |
| EP (1) | EP2817291A1 (ja) |
| JP (1) | JP6092261B2 (ja) |
| KR (1) | KR20140130449A (ja) |
| CN (1) | CN104185624B (ja) |
| BR (1) | BR112014015582A8 (ja) |
| CA (1) | CA2857262A1 (ja) |
| MX (1) | MX2014009799A (ja) |
| RU (1) | RU2014137052A (ja) |
| WO (1) | WO2013124335A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112014015582A8 (pt) * | 2012-02-24 | 2017-07-04 | Hoffmann La Roche | compostos antivirais |
| CN109641874A (zh) | 2016-05-10 | 2019-04-16 | C4医药公司 | 用于靶蛋白降解的c3-碳连接的戊二酰亚胺降解决定子体 |
| EP3454862B1 (en) | 2016-05-10 | 2024-09-11 | C4 Therapeutics, Inc. | Spirocyclic degronimers for target protein degradation |
| WO2017197055A1 (en) | 2016-05-10 | 2017-11-16 | C4 Therapeutics, Inc. | Heterocyclic degronimers for target protein degradation |
| WO2017197051A1 (en) | 2016-05-10 | 2017-11-16 | C4 Therapeutics, Inc. | Amine-linked c3-glutarimide degronimers for target protein degradation |
| EP3641762B1 (en) | 2017-06-20 | 2026-02-18 | C4 Therapeutics, Inc. | N/o-linked degrons and degronimers for protein degradation |
| EP4494698A3 (en) | 2017-08-04 | 2025-04-23 | Takeda Pharmaceutical Company Limited | Inhibitors of plasma kallikrein and uses thereof |
| US11837363B2 (en) | 2020-11-04 | 2023-12-05 | Hill-Rom Services, Inc. | Remote management of patient environment |
Family Cites Families (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4213765A (en) | 1979-01-02 | 1980-07-22 | Union Carbide Corporation | Oxidative coal desulfurization using lime to regenerate alkali metal hydroxide from reaction product |
| US5807876A (en) | 1996-04-23 | 1998-09-15 | Vertex Pharmaceuticals Incorporated | Inhibitors of IMPDH enzyme |
| US6054472A (en) | 1996-04-23 | 2000-04-25 | Vertex Pharmaceuticals, Incorporated | Inhibitors of IMPDH enzyme |
| AU723730B2 (en) | 1996-04-23 | 2000-09-07 | Vertex Pharmaceuticals Incorporated | Urea derivatives as inhibitors of IMPDH enzyme |
| BR9712544B1 (pt) | 1996-10-18 | 2013-10-22 | Inibidores de proteases de serina, composição farmacêutica compreendendo os mesmos e seus usos | |
| GB9623908D0 (en) | 1996-11-18 | 1997-01-08 | Hoffmann La Roche | Amino acid derivatives |
| EP0966465B1 (en) | 1997-03-14 | 2003-07-09 | Vertex Pharmaceuticals Incorporated | Inhibitors of impdh enzyme |
| US6010848A (en) | 1997-07-02 | 2000-01-04 | Smithkline Beecham Corporation | Screening methods using an atpase protein from hepatitis C virus |
| PT1012180E (pt) | 1997-08-11 | 2005-04-29 | Boehringer Ingelheim Ca Ltd | Analogos de peptidos inibidores da hepatite c |
| JP2003525200A (ja) | 1998-07-27 | 2003-08-26 | イスティトゥト ディ リチェルケ ディ ビオロジア モレコラーレ ピー.アンジェレッティ ソチエタ ペル アツィオニ | ポリメラーゼ阻害剤としてのジケト酸誘導体 |
| US6323180B1 (en) * | 1998-08-10 | 2001-11-27 | Boehringer Ingelheim (Canada) Ltd | Hepatitis C inhibitor tri-peptides |
| CN1325309A (zh) | 1998-08-21 | 2001-12-05 | 维洛药品公司 | 用于治疗或预防病毒感染和相关疾病的化合物、组合物和方法 |
| EP1109580A4 (en) | 1998-09-04 | 2004-05-26 | Viropharma Inc | METHOD FOR TREATING OR PREVENTING VIRAL INFECTIONS AND RELATED DISEASES |
| KR20010079907A (ko) | 1998-09-25 | 2001-08-22 | 비로파마 인코포레이티드 | 바이러스 감염 및 관련 질병의 치료 및 예방 방법 |
| AU769383B2 (en) | 1999-03-19 | 2004-01-22 | Vertex Pharmaceuticals Incorporated | Inhibitors of IMPDH enzyme |
| EP1225899A2 (en) | 1999-11-04 | 2002-07-31 | Virochem Pharma Inc. | Method for the treatment or prevention of flaviviridae viral infection using nucleoside analogues |
| AU2001261377A1 (en) | 2000-05-10 | 2001-11-20 | Smith Kline Beecham Corporation | Novel anti-infectives |
| US6448281B1 (en) | 2000-07-06 | 2002-09-10 | Boehringer Ingelheim (Canada) Ltd. | Viral polymerase inhibitors |
| SV2003000617A (es) | 2000-08-31 | 2003-01-13 | Lilly Co Eli | Inhibidores de la proteasa peptidomimetica ref. x-14912m |
| CZ20033368A3 (en) | 2001-06-11 | 2004-04-14 | Shire Biochem Inc. | Thiophene derivatives as antiviral agents for flavivirus infection |
| WO2002100846A1 (en) | 2001-06-11 | 2002-12-19 | Shire Biochem Inc. | Compounds and methods for the treatment or prevention of flavivirus infections |
| AR035543A1 (es) | 2001-06-26 | 2004-06-16 | Japan Tobacco Inc | Agente terapeutico para la hepatitis c que comprende un compuesto de anillo condensado, compuesto de anillo condensado, composicion farmaceutica que lo comprende, compuestos de benzimidazol, tiazol y bifenilo utiles como intermediarios para producir dichos compuestos, uso del compuesto de anillo con |
| CA2448737C (en) | 2001-07-20 | 2010-06-01 | Boehringer Ingelheim (Canada) Ltd. | Viral polymerase inhibitors |
| EP2335700A1 (en) | 2001-07-25 | 2011-06-22 | Boehringer Ingelheim (Canada) Ltd. | Hepatitis C virus polymerase inhibitors with a heterobicylic structure |
| DE60221875T2 (de) | 2001-11-02 | 2007-12-20 | Glaxo Group Ltd., Greenford | 4-(6-gliedrige)-heteroaryl-acyl-pyrrolidinderivate als hcv-inhibitoren |
| EP1440068A1 (en) | 2001-11-02 | 2004-07-28 | Glaxo Group Limited | Acyl dihydro pyrrole derivatives as hcv inhibitors |
| EP1440070A1 (en) | 2001-11-02 | 2004-07-28 | Glaxo Group Limited | 4-(5-membered)-heteroaryl acyl pyrrolidine derivatives as hcv inhibitors |
| WO2004113353A1 (en) | 2003-06-19 | 2004-12-29 | Amedis Pharmaceuticals Ltd. | Silicon-comprising aminothiazole derivatives as cdk inhibitors |
| DE602005017582D1 (en) | 2004-01-30 | 2009-12-24 | Medivir Ab | Hcv ns-3 serine protease inhibitoren |
| US20070167426A1 (en) | 2004-06-02 | 2007-07-19 | Schering Corporation | Compounds for the treatment of inflammatory disorders and microbial diseases |
| US7601686B2 (en) * | 2005-07-11 | 2009-10-13 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| GB0526614D0 (en) | 2005-12-30 | 2006-02-08 | Novartis Ag | Organic compounds |
| US20090062537A1 (en) | 2006-03-03 | 2009-03-05 | Kwangho Lee | N-Formyl Hydrozyamine Compounds |
| US8329159B2 (en) | 2006-08-11 | 2012-12-11 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| DE102006048924A1 (de) | 2006-10-17 | 2008-04-24 | Bayer Healthcare Ag | Acylaminopyrazole |
| JP2010529069A (ja) | 2007-06-07 | 2010-08-26 | エフ.ホフマン−ラ ロシュ アーゲー | Nk3アンタゴニストとしてのプロリンアミド誘導体 |
| WO2010009196A1 (en) | 2008-07-15 | 2010-01-21 | Temple University Of The Commonwealth System Of Higher Education | Synthesis of bis-peptides oligomers comprising at least one n-substituted diketopiperazine as structural moiety |
| US20110195929A1 (en) * | 2008-08-05 | 2011-08-11 | Summit Corporation Plc | Compounds for the treatment of flaviviral infections |
| EP2475254A4 (en) * | 2009-09-11 | 2013-05-22 | Enanta Pharm Inc | HEPATITIS C-VIRUS HEMMER |
| WO2011049988A2 (en) * | 2009-10-20 | 2011-04-28 | Eiger Biopharmaceuticals, Inc. | Indazoles to treat flaviviridae virus infection |
| EP2345643A1 (en) * | 2009-12-29 | 2011-07-20 | Polichem S.A. | New tertiary 8-hydroxyquinoline-7-carboxamide derivatives and uses thereof |
| BR112014015582A8 (pt) * | 2012-02-24 | 2017-07-04 | Hoffmann La Roche | compostos antivirais |
-
2013
- 2013-02-21 BR BR112014015582A patent/BR112014015582A8/pt not_active IP Right Cessation
- 2013-02-21 US US14/376,336 patent/US9090559B2/en not_active Expired - Fee Related
- 2013-02-21 MX MX2014009799A patent/MX2014009799A/es unknown
- 2013-02-21 KR KR1020147023576A patent/KR20140130449A/ko not_active Withdrawn
- 2013-02-21 CA CA2857262A patent/CA2857262A1/en not_active Abandoned
- 2013-02-21 WO PCT/EP2013/053409 patent/WO2013124335A1/en not_active Ceased
- 2013-02-21 EP EP13705187.6A patent/EP2817291A1/en not_active Withdrawn
- 2013-02-21 CN CN201380010537.XA patent/CN104185624B/zh not_active Expired - Fee Related
- 2013-02-21 JP JP2014558092A patent/JP6092261B2/ja not_active Expired - Fee Related
- 2013-02-21 RU RU2014137052A patent/RU2014137052A/ru not_active Application Discontinuation
-
2015
- 2015-06-09 US US14/734,176 patent/US9403805B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| US9403805B2 (en) | 2016-08-02 |
| BR112014015582A2 (pt) | 2017-06-13 |
| HK1204618A1 (en) | 2015-11-27 |
| RU2014137052A (ru) | 2016-04-10 |
| KR20140130449A (ko) | 2014-11-10 |
| BR112014015582A8 (pt) | 2017-07-04 |
| EP2817291A1 (en) | 2014-12-31 |
| US20150005283A1 (en) | 2015-01-01 |
| CA2857262A1 (en) | 2013-08-29 |
| US9090559B2 (en) | 2015-07-28 |
| CN104185624B (zh) | 2016-10-12 |
| MX2014009799A (es) | 2014-09-08 |
| JP2015508088A (ja) | 2015-03-16 |
| CN104185624A (zh) | 2014-12-03 |
| US20150274711A1 (en) | 2015-10-01 |
| WO2013124335A1 (en) | 2013-08-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6092261B2 (ja) | 抗ウイルス化合物 | |
| JP5808496B2 (ja) | 抗ウイルス化合物 | |
| JP5923181B2 (ja) | Hcvns5aの阻害剤 | |
| JP6018715B2 (ja) | 抗ウイルス化合物 | |
| US20120328565A1 (en) | Antiviral compounds | |
| JP2016510050A (ja) | 抗ウイルス性化合物 | |
| JP6122514B2 (ja) | 抗ウイルス化合物 | |
| HK1204618B (en) | Antiviral compounds | |
| HK1200847B (en) | Inhibitors of hcv ns5a |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160219 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160907 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20160908 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161129 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170110 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170208 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6092261 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |