JP6049637B2 - 放射線不透過性塞栓粒子 - Google Patents
放射線不透過性塞栓粒子 Download PDFInfo
- Publication number
- JP6049637B2 JP6049637B2 JP2013550965A JP2013550965A JP6049637B2 JP 6049637 B2 JP6049637 B2 JP 6049637B2 JP 2013550965 A JP2013550965 A JP 2013550965A JP 2013550965 A JP2013550965 A JP 2013550965A JP 6049637 B2 JP6049637 B2 JP 6049637B2
- Authority
- JP
- Japan
- Prior art keywords
- mole fraction
- particulate material
- material according
- composition
- present
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000002245 particle Substances 0.000 title description 68
- 230000003073 embolic effect Effects 0.000 title description 36
- 239000011236 particulate material Substances 0.000 claims description 92
- 239000000203 mixture Substances 0.000 claims description 61
- 239000008187 granular material Substances 0.000 claims description 32
- 229910021193 La 2 O 3 Inorganic materials 0.000 claims description 30
- 229910010413 TiO 2 Inorganic materials 0.000 claims description 29
- 229910004298 SiO 2 Inorganic materials 0.000 claims description 24
- 230000010102 embolization Effects 0.000 claims description 19
- 230000001225 therapeutic effect Effects 0.000 claims description 17
- 229920000642 polymer Polymers 0.000 claims description 16
- 239000000126 substance Substances 0.000 claims description 13
- 206010053648 Vascular occlusion Diseases 0.000 claims description 10
- 208000021331 vascular occlusion disease Diseases 0.000 claims description 10
- 206010046798 Uterine leiomyoma Diseases 0.000 claims description 8
- 208000009443 Vascular Malformations Diseases 0.000 claims description 7
- 239000011248 coating agent Substances 0.000 claims description 7
- 238000000576 coating method Methods 0.000 claims description 7
- 201000010260 leiomyoma Diseases 0.000 claims description 7
- 210000000056 organ Anatomy 0.000 claims description 7
- 230000004962 physiological condition Effects 0.000 claims description 7
- 208000032843 Hemorrhage Diseases 0.000 claims description 6
- 229910019142 PO4 Inorganic materials 0.000 claims description 6
- 229910000323 aluminium silicate Inorganic materials 0.000 claims description 6
- 208000034158 bleeding Diseases 0.000 claims description 6
- 230000000740 bleeding effect Effects 0.000 claims description 6
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 claims description 6
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 claims description 6
- 239000010452 phosphate Substances 0.000 claims description 6
- 238000002271 resection Methods 0.000 claims description 6
- 229920001983 poloxamer Polymers 0.000 claims description 5
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 claims description 4
- 230000010109 chemoembolization Effects 0.000 claims description 4
- 229920001577 copolymer Polymers 0.000 claims description 4
- 229960000502 poloxamer Drugs 0.000 claims description 4
- 201000007954 uterine fibroid Diseases 0.000 claims description 4
- 239000004615 ingredient Substances 0.000 claims description 3
- 239000011159 matrix material Substances 0.000 claims description 3
- 208000010579 uterine corpus leiomyoma Diseases 0.000 claims description 3
- 239000000306 component Substances 0.000 description 47
- CPLXHLVBOLITMK-UHFFFAOYSA-N Magnesium oxide Chemical compound [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 43
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 38
- 239000011521 glass Substances 0.000 description 34
- 239000000463 material Substances 0.000 description 32
- 150000002500 ions Chemical class 0.000 description 28
- 239000011734 sodium Substances 0.000 description 28
- 230000000694 effects Effects 0.000 description 23
- 239000000395 magnesium oxide Substances 0.000 description 22
- 239000000284 extract Substances 0.000 description 20
- 239000010936 titanium Substances 0.000 description 19
- 239000011787 zinc oxide Substances 0.000 description 19
- 239000002609 medium Substances 0.000 description 18
- 210000004027 cell Anatomy 0.000 description 17
- 230000003833 cell viability Effects 0.000 description 17
- 238000012360 testing method Methods 0.000 description 17
- 210000001519 tissue Anatomy 0.000 description 17
- 239000011575 calcium Substances 0.000 description 16
- 238000011534 incubation Methods 0.000 description 16
- 239000000523 sample Substances 0.000 description 16
- 238000004400 29Si cross polarisation magic angle spinning Methods 0.000 description 14
- 239000000243 solution Substances 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- 102000003855 L-lactate dehydrogenase Human genes 0.000 description 11
- 108700023483 L-lactate dehydrogenases Proteins 0.000 description 11
- 238000005481 NMR spectroscopy Methods 0.000 description 11
- 239000011859 microparticle Substances 0.000 description 11
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 10
- 239000011777 magnesium Substances 0.000 description 10
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 10
- 101000720655 Homo sapiens Oxysterol-binding protein-related protein 11 Proteins 0.000 description 9
- 102100025875 Oxysterol-binding protein-related protein 11 Human genes 0.000 description 9
- 238000006243 chemical reaction Methods 0.000 description 9
- 239000003795 chemical substances by application Substances 0.000 description 9
- 238000000113 differential scanning calorimetry Methods 0.000 description 9
- 238000002474 experimental method Methods 0.000 description 9
- 230000003993 interaction Effects 0.000 description 9
- 239000000758 substrate Substances 0.000 description 9
- 238000002441 X-ray diffraction Methods 0.000 description 8
- 238000000540 analysis of variance Methods 0.000 description 8
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 8
- 238000011156 evaluation Methods 0.000 description 8
- 238000005259 measurement Methods 0.000 description 8
- 239000001301 oxygen Substances 0.000 description 8
- 229910052760 oxygen Inorganic materials 0.000 description 8
- 239000000843 powder Substances 0.000 description 8
- 101100462341 Homo sapiens OSBPL2 gene Proteins 0.000 description 7
- 101000992392 Homo sapiens Oxysterol-binding protein-related protein 6 Proteins 0.000 description 7
- 101150054848 Osbpl9 gene Proteins 0.000 description 7
- 102100025925 Oxysterol-binding protein-related protein 2 Human genes 0.000 description 7
- 102100032149 Oxysterol-binding protein-related protein 6 Human genes 0.000 description 7
- 102100032162 Oxysterol-binding protein-related protein 9 Human genes 0.000 description 7
- 101100518421 Schizosaccharomyces pombe (strain 972 / ATCC 24843) orc2 gene Proteins 0.000 description 7
- 101100261632 Zea mays TSB2 gene Proteins 0.000 description 7
- 230000015556 catabolic process Effects 0.000 description 7
- 239000000919 ceramic Substances 0.000 description 7
- 238000002983 circular dichroism Methods 0.000 description 7
- 239000002872 contrast media Substances 0.000 description 7
- 239000013078 crystal Substances 0.000 description 7
- 238000006731 degradation reaction Methods 0.000 description 7
- 238000013461 design Methods 0.000 description 7
- 238000010790 dilution Methods 0.000 description 7
- 239000012895 dilution Substances 0.000 description 7
- 238000001727 in vivo Methods 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 238000002843 lactate dehydrogenase assay Methods 0.000 description 7
- 238000001228 spectrum Methods 0.000 description 7
- 239000011701 zinc Substances 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 6
- 238000007792 addition Methods 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 229910002091 carbon monoxide Inorganic materials 0.000 description 6
- 238000004113 cell culture Methods 0.000 description 6
- 210000002950 fibroblast Anatomy 0.000 description 6
- 210000004623 platelet-rich plasma Anatomy 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 241000894007 species Species 0.000 description 6
- 230000000007 visual effect Effects 0.000 description 6
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 5
- 102000008946 Fibrinogen Human genes 0.000 description 5
- 108010049003 Fibrinogen Proteins 0.000 description 5
- 101000854060 Homo sapiens Oxygen-regulated protein 1 Proteins 0.000 description 5
- 101000720693 Homo sapiens Oxysterol-binding protein-related protein 1 Proteins 0.000 description 5
- 231100000416 LDH assay Toxicity 0.000 description 5
- 206010028980 Neoplasm Diseases 0.000 description 5
- 241000283973 Oryctolagus cuniculus Species 0.000 description 5
- 102100025924 Oxysterol-binding protein-related protein 1 Human genes 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 239000012298 atmosphere Substances 0.000 description 5
- 239000007857 degradation product Substances 0.000 description 5
- 229940012952 fibrinogen Drugs 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 229910052697 platinum Inorganic materials 0.000 description 5
- 239000013641 positive control Substances 0.000 description 5
- 230000004044 response Effects 0.000 description 5
- 239000000377 silicon dioxide Substances 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 238000005004 MAS NMR spectroscopy Methods 0.000 description 4
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 210000004204 blood vessel Anatomy 0.000 description 4
- 238000011088 calibration curve Methods 0.000 description 4
- 201000011510 cancer Diseases 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 231100000135 cytotoxicity Toxicity 0.000 description 4
- 230000003013 cytotoxicity Effects 0.000 description 4
- 238000004090 dissolution Methods 0.000 description 4
- 238000002149 energy-dispersive X-ray emission spectroscopy Methods 0.000 description 4
- 230000007794 irritation Effects 0.000 description 4
- 229920001606 poly(lactic acid-co-glycolic acid) Polymers 0.000 description 4
- 229910052710 silicon Inorganic materials 0.000 description 4
- 239000010703 silicon Substances 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- 238000004611 spectroscopical analysis Methods 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- 208000012671 Gastrointestinal haemorrhages Diseases 0.000 description 3
- 101000992396 Homo sapiens Oxysterol-binding protein-related protein 3 Proteins 0.000 description 3
- 101000992390 Homo sapiens Oxysterol-binding protein-related protein 7 Proteins 0.000 description 3
- 238000000134 MTT assay Methods 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- 102100032154 Oxysterol-binding protein-related protein 3 Human genes 0.000 description 3
- 102100032150 Oxysterol-binding protein-related protein 7 Human genes 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 208000027418 Wounds and injury Diseases 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 229940039231 contrast media Drugs 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 238000013401 experimental design Methods 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 208000030304 gastrointestinal bleeding Diseases 0.000 description 3
- 230000009477 glass transition Effects 0.000 description 3
- 239000002241 glass-ceramic Substances 0.000 description 3
- 230000005484 gravity Effects 0.000 description 3
- 208000014674 injury Diseases 0.000 description 3
- 229910052746 lanthanum Inorganic materials 0.000 description 3
- FZLIPJUXYLNCLC-UHFFFAOYSA-N lanthanum atom Chemical compound [La] FZLIPJUXYLNCLC-UHFFFAOYSA-N 0.000 description 3
- 229910052749 magnesium Inorganic materials 0.000 description 3
- 230000002503 metabolic effect Effects 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 238000000034 method Methods 0.000 description 3
- 230000000877 morphologic effect Effects 0.000 description 3
- 239000013642 negative control Substances 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 229920001992 poloxamer 407 Polymers 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 238000011002 quantification Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000002885 thrombogenetic effect Effects 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 231100000002 MTT assay Toxicity 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 208000001647 Renal Insufficiency Diseases 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 206010053476 Traumatic haemorrhage Diseases 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 230000001464 adherent effect Effects 0.000 description 2
- 230000025164 anoikis Effects 0.000 description 2
- 229920000249 biocompatible polymer Polymers 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 238000013043 cell viability test Methods 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- 238000001142 circular dichroism spectrum Methods 0.000 description 2
- 230000035602 clotting Effects 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 238000013400 design of experiment Methods 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- -1 for example Inorganic materials 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000009616 inductively coupled plasma Methods 0.000 description 2
- 238000002354 inductively-coupled plasma atomic emission spectroscopy Methods 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 208000017169 kidney disease Diseases 0.000 description 2
- 201000006370 kidney failure Diseases 0.000 description 2
- MRELNEQAGSRDBK-UHFFFAOYSA-N lanthanum(3+);oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[La+3].[La+3] MRELNEQAGSRDBK-UHFFFAOYSA-N 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 229910001425 magnesium ion Inorganic materials 0.000 description 2
- 238000013178 mathematical model Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 238000011587 new zealand white rabbit Methods 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 2
- 230000035515 penetration Effects 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 238000002601 radiography Methods 0.000 description 2
- 230000000250 revascularization Effects 0.000 description 2
- 238000013207 serial dilution Methods 0.000 description 2
- 239000008159 sesame oil Substances 0.000 description 2
- 235000011803 sesame oil Nutrition 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 238000005063 solubilization Methods 0.000 description 2
- 230000007928 solubilization Effects 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 239000012086 standard solution Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 230000036962 time dependent Effects 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 210000004291 uterus Anatomy 0.000 description 2
- 230000006496 vascular abnormality Effects 0.000 description 2
- UOGZWWISWPADQM-SDVXZCCESA-N (1r,2r,3r,4s,6s)-2,3,6-trichloro-4,7-bis(dichloromethyl)-7-methylbicyclo[2.2.1]heptane Chemical compound Cl[C@H]1C[C@@]2(C(Cl)Cl)[C@@H](Cl)[C@H](Cl)[C@@H]1C2(C(Cl)Cl)C UOGZWWISWPADQM-SDVXZCCESA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- TVZRAEYQIKYCPH-UHFFFAOYSA-N 3-(trimethylsilyl)propane-1-sulfonic acid Chemical compound C[Si](C)(C)CCCS(O)(=O)=O TVZRAEYQIKYCPH-UHFFFAOYSA-N 0.000 description 1
- 208000009304 Acute Kidney Injury Diseases 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 1
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 1
- 210000003771 C cell Anatomy 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 235000008733 Citrus aurantifolia Nutrition 0.000 description 1
- 206010053567 Coagulopathies Diseases 0.000 description 1
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 241000976924 Inca Species 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 229920002274 Nalgene Polymers 0.000 description 1
- 206010067482 No adverse event Diseases 0.000 description 1
- 101150015512 OSBPL10 gene Proteins 0.000 description 1
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical compound [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 1
- 102100031469 Oxysterol-binding protein-related protein 10 Human genes 0.000 description 1
- 102000013566 Plasminogen Human genes 0.000 description 1
- 108010051456 Plasminogen Proteins 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 208000033626 Renal failure acute Diseases 0.000 description 1
- 101001121313 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Oxysterol-binding protein homolog 1 Proteins 0.000 description 1
- 101001121316 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Oxysterol-binding protein homolog 2 Proteins 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 235000011941 Tilia x europaea Nutrition 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 238000010162 Tukey test Methods 0.000 description 1
- 206010054094 Tumour necrosis Diseases 0.000 description 1
- 208000024248 Vascular System injury Diseases 0.000 description 1
- 208000012339 Vascular injury Diseases 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 201000011040 acute kidney failure Diseases 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 229910000287 alkaline earth metal oxide Inorganic materials 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 238000013096 assay test Methods 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 238000003705 background correction Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000002457 bidirectional effect Effects 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 239000003114 blood coagulation factor Substances 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 208000002458 carcinoid tumor Diseases 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 239000004568 cement Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 239000000701 coagulant Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000002591 computed tomography Methods 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000008358 core component Substances 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 239000011350 dental composite resin Substances 0.000 description 1
- 210000003298 dental enamel Anatomy 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 238000004945 emulsification Methods 0.000 description 1
- 238000011067 equilibration Methods 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000000445 field-emission scanning electron microscopy Methods 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 239000008098 formaldehyde solution Substances 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 239000000156 glass melt Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 239000001307 helium Substances 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 1
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 1
- BDAGIHXWWSANSR-NJFSPNSNSA-N hydroxyformaldehyde Chemical compound O[14CH]=O BDAGIHXWWSANSR-NJFSPNSNSA-N 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 230000016507 interphase Effects 0.000 description 1
- 238000002697 interventional radiology Methods 0.000 description 1
- 238000002075 inversion recovery Methods 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 238000002350 laparotomy Methods 0.000 description 1
- 239000004571 lime Substances 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 239000007769 metal material Substances 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- VMGAPWLDMVPYIA-HIDZBRGKSA-N n'-amino-n-iminomethanimidamide Chemical compound N\N=C\N=N VMGAPWLDMVPYIA-HIDZBRGKSA-N 0.000 description 1
- 230000001338 necrotic effect Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 210000002381 plasma Anatomy 0.000 description 1
- 239000011505 plaster Substances 0.000 description 1
- 229920000307 polymer substrate Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 210000003240 portal vein Anatomy 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 239000012925 reference material Substances 0.000 description 1
- BOLDJAUMGUJJKM-LSDHHAIUSA-N renifolin D Natural products CC(=C)[C@@H]1Cc2c(O)c(O)ccc2[C@H]1CC(=O)c3ccc(O)cc3O BOLDJAUMGUJJKM-LSDHHAIUSA-N 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000004626 scanning electron microscopy Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000012064 sodium phosphate buffer Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000000371 solid-state nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- 229910000018 strontium carbonate Inorganic materials 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 238000000870 ultraviolet spectroscopy Methods 0.000 description 1
- 210000000685 uterine artery Anatomy 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- JLYXXMFPNIAWKQ-UHFFFAOYSA-N γ Benzene hexachloride Chemical compound ClC1C(Cl)C(Cl)C(Cl)C(Cl)C1Cl JLYXXMFPNIAWKQ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
- A61K33/244—Lanthanides; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/06—Aluminium, calcium or magnesium; Compounds thereof, e.g. clay
- A61K33/08—Oxides; Hydroxides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/04—X-ray contrast preparations
- A61K49/0409—Physical forms of mixtures of two different X-ray contrast-enhancing agents, containing at least one X-ray contrast-enhancing agent which is not a halogenated organic compound
- A61K49/0414—Particles, beads, capsules or spheres
- A61K49/0419—Microparticles, microbeads, microcapsules, microspheres, i.e. having a size or diameter higher or equal to 1 micrometer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/143—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P41/00—Drugs used in surgical methods, e.g. surgery adjuvants for preventing adhesion or for vitreum substitution
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Inorganic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Radiology & Medical Imaging (AREA)
- Diabetes (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Surgery (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Materials For Medical Uses (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Glass Compositions (AREA)
Description
本出願は、2012年1月28日提出の米国特許仮出願第61/437,566号の恩典を主張し、これはあらゆる目的のためにその全体が参照により本明細書に組み入れられる。
本発明は、放射線不透過性であり、塞栓術実施に適した、粒状材料に関する。
ポリマー粒子は、子宮平滑筋腫などの血管過多腫瘍および血管奇形などの血管異常(それらに限定されるわけではない)の処置における血管の選択的閉塞のために、インターベンショナルラジオロジーの放射線科医によってしばしば用いられる。しかし、現行の最先端技術を用いた粒子は、そのような製品の市場への浸透を制限する多くの欠点に悩まされている。欠点には、粒子が放射線不透過性でないことが含まれる。したがって、医師は粒子の設置を放射線撮影によってモニターすることができない。その結果、非標的塞栓形成および貫通塞栓形成による逆流などの、塞栓術の合併症が検出不可能となる。この問題に対する現行のアプローチには、放射線撮影によって認識できる造影剤を含む媒質中に粒子を分散させることが含まれる。しかし、これは造影剤自体の問題を引き起こす。造影剤によって誘発される腎症は、造影剤に曝露された患者の約7パーセントで起こる。造影剤によって誘発される腎症は、腎不全を引き起こしうる急性腎損傷によって特徴付けられる。造影剤への曝露は、院内腎不全の三番目に多い原因である。加えて、現在用いられている粒子の分解は制御することができない。非分解性であるか、または異なる程度の分解性を有する粒子を選択することができれば、塞栓術の対象となる様々な損傷のためのより多くの処置選択肢が可能となる。経時的に分解する粒子の使用によって、処置した損傷がなくなった後に、閉塞した血管の血管再生が可能となり、正常組織への血流の回復が起こり得る。これは、胃腸出血の処置などの場合に望ましいであろう。他の場合には、非分解性粒子の使用により、根元的血管の血管再生が防止される。これは、血管奇形などの血管損傷において望ましいであろう。
TiO2、La2O3、Na2OおよびMgOまたはSrOの1つまたは複数を含む粒状材料を提供する。1つの態様において、粒状材料は:0.4〜0.7モル分率のSiO2;0.04〜0.7モル分率のTiO2;0.04〜0.5モル分率のLa2O3;0.03〜0.3モル分率のMgO;および0.03〜0.3モル分率のNa2Oを含む。1つの態様において、MgOは0.05〜0.2モル分率で存在する。粒状材料は任意にSrOを含んでいてもよい。SrOが含まれる場合、MgOおよびSrOは合わせて0.05〜0.3モル分率で存在しうる。または、MgOおよびSrOは合わせて0.05〜0.2モル分率で存在する。La2O3は0.04〜0.4モル分率または0.04〜0.3モル分率で存在しうる。TiO2は0.04〜0.3モル分率または0.04〜0.2モル分率で存在しうる。SiO2は0.4〜0.6モル分率または0.4〜0.5モル分率で存在しうる。Na2Oは0.03〜0.2モル分率または0.03-0.15モル分率で存在する。
[本発明1001]
SiO 2 、TiO 2 、La 2 O 3 、Na 2 OおよびMgOの1つまたは複数を含む粒状材料。
[本発明1002]
下記の1つまたは複数を含む、本発明1001の粒状材料:
0.4〜0.7モル分率のSiO 2 ;
0.04〜0.7モル分率のTiO 2 ;
0.04〜0.5モル分率のLa 2 O 3 ;
0.03〜0.3モル分率のMgO;および
0.03〜0.3モル分率のNa 2 O。
[本発明1003]
下記を含む、本発明1001の粒状材料:
0.4〜0.7モル分率のSiO 2 ;
0.04〜0.7モル分率のTiO 2 ;
0.04〜0.5モル分率のLa 2 O 3 ;
0.03〜0.3モル分率のMgO;および
0.03〜0.3モル分率のNa 2 O。
[本発明1004]
MgOが0.03〜0.2モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1005]
SrOをさらに含む、本発明1001の粒状材料。
[本発明1006]
MgOおよびSrOが合わせて0.03〜0.3モル分率で存在する、本発明1005の粒状材料。
[本発明1007]
MgOおよびSrOが合わせて0.05〜0.2モル分率で存在する、本発明1006の粒状材料。
[本発明1008]
La 2 O 3 が0.04〜0.4モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1009]
La 2 O 3 が0.04〜0.3モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1010]
TiO 2 が0.04〜0.3モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1011]
TiO 2 が0.04〜0.2モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1012]
SiO 2 が0.4〜0.6モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1013]
SiO 2 が0.5〜0.6モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1014]
Na 2 Oが0.03〜0.2モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1015]
Na 2 Oが0.03〜0.15モル分率で存在する、前記本発明のいずれかの粒状材料。
[本発明1016]
放射線不透過性である、前記本発明のいずれかの粒状材料。
[本発明1017]
生体適合性である、前記本発明のいずれかの粒状材料。
[本発明1018]
インビボで分解性である、前記本発明のいずれかの粒状材料。
[本発明1019]
実質的に6ヶ月よりも長期で分解する、本発明1018の粒状材料。
[本発明1020]
治療成分をさらに含む、前記本発明のいずれかの粒状材料。
[本発明1021]
前記治療成分が生理的条件下で放出される、本発明1020の粒状材料。
[本発明1022]
Q 1 〜Q 3 のQ-スペシエーション(Q-speciation)を有する、前記本発明のいずれかの粒状材料。
[本発明1023]
Q 1 のQ-スペシエーションを有する、本発明1022の粒状材料。
[本発明1024]
45〜1180μmの平均直径を有する、前記本発明のいずれかの粒状材料。
[本発明1025]
200および1000μmの平均直径を有する、本発明1024の粒状材料。
[本発明1026]
300〜500μmの平均直径を有する、本発明1025の粒状材料。
[本発明1027]
500〜710μmの平均直径を有する、本発明1025の粒状材料。
[本発明1028]
ポリマーコーティングをさらに含む、前記本発明のいずれかの粒状材料。
[本発明1029]
前記ポリマーコーティングが乳酸-グリコール酸コポリマーを含む、本発明1028の粒状材料。
[本発明1030]
前記ポリマーコーティングがポロキサマーを含む、本発明1028の粒状材料。
[本発明1031]
前記ポリマーコーティングがPluronic F-127を含む、本発明1030の粒状材料。
[本発明1032]
治療成分をさらに含む、本発明1028の粒状材料。
[本発明1033]
前記治療成分が生理的条件下で放出される、本発明1032の粒状材料。
[本発明1034]
0.1モル分率以下のアルミノケイ酸塩、リン酸塩またはその組み合わせを含む、前記本発明のいずれかの粒状材料。
[本発明1035]
血管閉塞において用いるための、前記本発明のいずれかの粒状材料。
[本発明1036]
血管奇形の処置のための、本発明1035の粒状材料。
[本発明1037]
臓器切除のための、本発明1035の粒状材料。
[本発明1038]
化学塞栓術のための、本発明1035の粒状材料。
[本発明1039]
出血の処置のための、本発明1035の粒状材料。
[本発明1040]
子宮筋腫塞栓術のための血管閉塞において用いるための、本発明1001〜1024または1026〜1034のいずれかの粒状材料。
粒状材料の粒子は中核および任意の圧縮可能な外殻/基材を含む。中核はSiO2、La2O3、Na2O、MgOおよびSrOの1つまたは複数を含む。任意の圧縮可能な外殻/基材は生体適合性ポリマーを含む。さらに提供される粒状材料は、SiO2、La2O3、TiO2、ZnO、MgO、Na2O、SrO、およびCaOの1つまたは複数を含む中核を有する。いくつかの態様において、粒状材料は、リン酸塩およびアルミノケイ酸塩を実質的に含まない。いくつかの態様において、粒状材料は、0.1モル分率以下のアルミノケイ酸塩、リン酸塩またはその組み合わせを含む。驚くことに、粒状材料は生体適合性であるが、リン酸塩またはアルミノケイ酸塩を必要としない。
1つの態様において、粒状材料は、ガラスセラミックの特性を有する。そのような態様において、成分が網目を構成し、これはアモルファスまたは結晶であり得る。成分にはSiO2、La2O3、TiO2、ZnO、MgO、Na2O、SrO、およびCaOが含まれる。様々な中核成分の量(ならびに成分の互いの比)を改変することで、材料の特徴をその所期の使用に対して調整することが可能となる。
La2O3は0.04〜0.5のモル分率で存在する。もう1つの態様において、La2O3は0.04〜0.4モル分率で存在する。もう1つの態様において、La2O3は0.04〜0.3モル分率で存在する。La2O3は粒状材料に放射線不透過性を提供する。ランタンは、歯科適用においてガラスセラミックおよび歯科用複合材料中の放射線不透過剤として何十年も用いられてきた。La2O3は現行の最先端技術を用いた塞栓剤よりもすぐれた放射線不透過性を提供する。材料が分解するにつれてのLa3+の放出は、治療上の利益を提供するというさらなる利益を有する可能性がある。例えば、La3+は特定の癌のアノイキスを促進し、したがって粒状材料の所期の使用がそれらの癌のアノイキスを開始するためである場合には有益である。それらの使用のために、ランタンの量をその目的のために調整する。
治療特性を有するさらなる成分を、粒状材料に加えることができる。1つの態様において、そのような治療成分は、粒子へのインビボ表面改変に関連して放出する。次いで、これらの成分は体内で粒子から放出される。網目改変成分の構成を用いて、治療成分の放出を制御する。そのような成分の例には、治療的イオンおよび化学療法剤が含まれる。治療的イオンには、例えば、Ca2+が含まれ、これは凝固を助ける。1つの態様において、カルシウムは粒子中にCaOの形で提供される。
1つの態様において、粒状材料はセラミックである。セラミックは、加熱およびその後の冷却によって調製される、無機、非金属材料である。セラミックは通常は、例えば、アルミニウムと酸素、カルシウムと酸素ならびにケイ素と窒素などの金属と非金属元素との間で形成される。セラミックは結晶性、部分的結晶性またはアモルファス構造を有し得、ガラスとも呼ばれるセラミックガラスを含む。他のセラミックには、エナメル、ガラスセラミック(セラミック結晶を含むガラス)、および無機セメント型材料(セメント、プラスターおよび石灰)が含まれる。1つの態様において、粒状材料はガラスである。ガラスは非結晶性、すなわちアモルファス構造を有する任意の固体で、加熱によりガラス転移を示す。
図1は、1つの態様による粒子を示す。粒子は、前述の中核101と同様、生体適合性ポリマーの圧縮可能な外殻/基材103も含む。そのような態様を図1に示す。前に述べたとおり、中核をポリマー基材に懸濁することもできる。可能なポリマーには、乳酸-グリコール酸コポリマー(「PLGA」)およびポロキサマーが含まれる。1つの態様において、外殻/基材には、BASFから入手可能なPluronic F127が含まれる。この外殻/基材は、治療的利益のための薬物溶出を可能にする。例には、悪性腫瘍の化学塞栓術が含まれる。具体例には、肝臓の肝細胞癌が含まれる。溶出されうるさらなる薬物には、例えば、血管閉塞の程度を増強する血栓形成剤が含まれる。外殻/基材の圧縮可能性は、粒状材料の臨床的配備において有用である。
粒状材料の個々の粒子は平均直径45から1180μmの間である。または、粒子は平均直径200から1000μmの間である。粒子の様々な用途は粒子の異なるサイズを必要とする。したがって、1つの態様において、粒子は、悪性腫瘍塞栓術において必要とされうる、深部腫瘍壊死のために有用な、100〜300μmの平均直径を有する。もう1つの態様において、粒子は、300〜500μmの平均直径を有し、胃腸または外傷性出血を処置するために用いられる。300〜500μmの粒子は、子宮筋腫塞栓術およびほとんどの他の臓器または腫瘍塞栓術のための粒子の初期サイズとしても用いることができる。もう1つの別の態様において、粒子は500〜710μmの平均直径を有する。500〜710μmの粒子は、子宮筋腫の塞栓術でも用いられる。子宮筋腫の塞栓術のために、どのサイズ範囲、すなわち300〜500μmまたは500〜710μmを用いるかは、粒子の他の特徴に依存する。さらにもう1つの別の態様において、粒子は710〜1000μmの平均直径を有し、胃腸出血または外傷性出血などの出血部位に対し、「頭部圧」を低下させるための近位塞栓術のために有用である。
本発明の粒状材料を、血管閉塞のために用いてもよい。1つの態様において、門脈塞栓術、化学塞栓術および任意の原因による出血を含む、子宮筋腫、血管奇形および他の血管異常または損傷、臓器切除の処置において、血管閉塞を用いる。
ガラス粒状材料の合成
一般に、分析等級試薬の適切な量を適宜秤量し、プラスチック容器内で振盪することにより十分に混合する(30分間)。各バッチの粉末を白金るつぼ中、適切な温度(最初は1520℃で1時間)で加熱する。次いで、ガラス溶融物を水中で急冷する。得られたガラスフリットを乾燥器内で乾燥し(120℃、1日)、粉砕し、ふるいにかけて、その後の分析用のガラス粉末を回収する。表1および2は粒状材料のための組成の例を示す。表2は本明細書の最後に添付。
粒子組成物(モル分率)(0.52〜0.57)SiO2-0.035CaO-(0.00〜0.29)-ZnO-0.035MgO-(0.00〜0.188)La2O3-0.035SrO-(0.00〜0.05)TiO2-0.035Na2Oをこの実験のために合成した。分析等級試薬:二酸化ケイ素、炭酸カルシウム、酸化亜鉛、酸化マグネシウム、酸化ランタン(III)、炭酸ストロンチウム、二酸化チタンおよび炭酸ナトリウム(Sigma Aldrich、カナダ)を秤量し、プラスチック容器(Nalgene(商標)、Sigma Aldrich、カナダ)中で1時間均質に混合した。各バッチの粉末を白金るつぼ(50mL)中に入れ、次いでBench-Top High Temperature Muffle Furnace(EQ-KSL、MTI Corporation. USA)を用いて加熱(1480℃、1時間)し、水中で急冷した。得られたフリットを乾燥器内で乾燥し(120℃、1日)、めのう遊星ミル(Pulverisette 7;Laval Labs Inc.、カナダ)中で粉砕し、様々な孔径を通してふるいにかけて、以下のサイズ範囲の粉末微粒子を生成した:<45μm;45〜212μm;212〜300μm;355〜500μm;>500μm。この実験で生成したすべてのバッチの粒子を、この後さらなる評価のために乾燥デシケーター中で保存した。
示差走査熱量測定(DSC)
一般に、DSCを用いて各ガラスのガラス転移温度(Tg)の開始を、示差走査熱量計(DSC)を用いて判定する。258.15℃(最大725℃まで)の温度間隔を、空気中で、対応させた白金るつぼ中のアルミナ(または他の適切な参照)と共に用いる。用いたDSCの耐用性はおよそ2%である。
実施例1で作成した粒子のDSC分析を実施して、ガラス転移温度(Tg)の値を得た。試料(約80mg)を窒素雰囲気下、白金るつぼ中で、空の参照るつぼと一緒に加熱した。標準参照材料は所与の温度範囲のためにすでに事前選択している。Tgを示差走査熱量計(DSC:TA Instruments-DQ200)で、25℃から725℃の間を、258.15℃の温度間隔で測定した。8つの粒子(ORP1〜3、ORP5〜7、ORP9およびORP11)のDSCトレースを図2に示す。表4は、Tg低下線形混合多項式モデルの要約したANOVA表である。L-Pseudo成分コーディングに関して作成した回帰モデルに基づき、各材料組成物のTg挙動の観察値と計算値との間の比較を表にして表5に示す。L-Pseudo成分に関する最終数学的モデルを以下のとおり式1で示す:
Tg(℃)=+634.82ZnO+833.28La2O3+677.19SiO2+699.01TiO2 式1。
一般に、XRDを用いてガラスのアモルファス特性を確認する。各ガラスの粉末試料を圧迫してディスク(Φ32mm×3mm)を形成する。回折パターンを、X線回折装置を用い、40KVおよび35mAの単色化CuKα(λ=1.54060A)照射により収集する。走査角範囲(2θ)を10°から70°まで、ステップサイズ0.033423°およびステップ時間59.69秒で実施する。
粒子のX線回折(XRD)測定を、X線発生装置(40kV;35mA)に接続し、Cu標的X線管を備えた、彎曲位置敏感検出器によるINEL CPS-120回折計を用いて実施した。試料を、選択した微量粒子(45〜212μm)を中空角形スチールウェーハ中に圧迫することにより調製した。入射ビーム経路における単色計は、試料をCu Kα1,α2に衝突させる波長を制限する。X線ビームは試料上に約6°で入射し、彎曲位置敏感検出器は走査角範囲10°<2θ<110°のすべての散乱したX線を収集する。XRDスペクトルの収集時間は1800秒である。粉末試料を、測定および移動操作を逐次プログラムすることを可能にする、INELのx-yトランスレーションステージ上に設置した。
二次標準シェッフェ多項式の係数を推定するために3,4、定義ドメイン(デザインスペース)内の異なる組成変種(デザインポイント)を表す13の実験による二次ユーザー定義計画を、Design-Expert 8.0.4ソフトウェア(Stat-Ease, Inc.)を用いて作成した。これらのデザインポイントは、各組成物の制約された範囲に基づいて決定し:6つの実験は頂点先端に設定し;さらなる6つはアキシャルチェックブレンドを調べ、1つは定義デザインスペース内の全体の重心であった。これらの点は、ドメインの興味が持たれる点はそのトップ、サイドの真ん中、フェースの真ん中、およびその重心である、シェッフェの提案と明らかに一致する(表1参照)。混合計画法により、等式を得る。この式はYを、4つの組成因子(ZnO、La2O3、SiO2およびTiO2、それぞれX1、X2、X3およびX4と示す)と連結する。
YA=β1X1+β2X2+β3X3+β4X4+e 式3
式中、X1〜X4は組成因子であり、β1〜4係数は個々の組成因子X1〜4の効果である。eは残差と呼び、この値は選択した各ガラスの計算値と実験値との間の差である。保持するガラスの数が式中の係数の数と同じである場合、これは0となる。選択したガラスの数が係数の数よりも多い場合、残差は各実験で異なる値を有する。
Y=β1X1+β2X2+β3X3+β4X4+β12X1X2+β13X1X3+β14X1X4+β23X2X3+β24X2X4+β123X1X2X3+β124X1X2X4+β134X1X3X4+β234X2X3X4+e 式4
式中、X1〜X4は組成因子であり、β1〜4係数は個々の組成因子X1〜4の効果であり;β12〜24は組成因子間の二方向相互作用の効果を表す回帰の係数であり;β123〜234は組成因子間の三方向相互作用の効果を表す回帰の係数であり、eは残差である。
zi=(xi−Li)/(1−ΣL) 式5
式中、xiは元の成分比率を表し、Liはi番目の成分の下限(限界)を表し、Lはデザインにおけるすべての成分のすべての下限(限界)の合計を表し、1は混合物合計を表す。
実施例5
真の密度を、本明細書において合成したすべての粒子についてと、市販の対照材料:Contour(商標)(PVA微粒子)についても、ヘリウム比重びん(AccuPyc 1340、Micromeritics)を用いて測定した。結果は5つの測定記録の平均の代表である。図4Aおよび4Bは得られた等高線プロットで、実成分コーディングにおける4つの様々なTi添加(0.017、0.033、0.042および0.05モル)での実験的粒子密度(g/cc)に対する組成-相互作用効果を示す。(A)はTi:0.017モル分率であり;(B)はTi:0.033モル分率であり;(C)はTi:0.042モル分率であり;かつ(D)はTi:0.050モル分率である。
N2吸収/脱着を、Brunauer-Emmett-Teller(BET)法を用いて調べ、調製したガラス粉末の比表面積(SSA)および多孔度を求める。ガラス試料(約0.15g±0.05g)を窒素雰囲気下、77.35Kに、平衡間隔10秒で置く。
実施例7
走査電子顕微鏡(SEM)観察のために、粉末試料(粒径範囲:355〜500μm)を直径10mm×高さ3mmのAlスタブに固定し、約27nmの白金で金スパッターコーター(SC7640、Fisons Instruments)を用いてコーティングした。続いて、形態学的および化学的分析のために、試料を、Oxford Incaエネルギー分散性x線分光法(EDS)装置を備えたHitachi S-4700 FEG-SEMのチャンバーに移した。下方二次電子(SE)検出器で、加速電圧5.0kVおよび作動距離11〜12mmを用いた。
一般に、ガラスの29Si MAS-NMRスペクトルを、ケイ素に対する1.5μsの高電力パルス(P1)取得を用い、回転周波数5kHzで記録する。29Si MAS-NMR試料を、リサイクル/遅延時間(recycle/delay time)を約2秒に設定して回転させる。29Si NMR化学シフトをppmで報告し、周囲のプローブ温度で、2,2-ジメチル-2シラペンタン-5-スルホン酸ナトリウム(DSS)または他の適切な参照品に対して外部参照した29Siにより記録する。固体状態のNMRについて、MASを用いて記録したシフトは試料の等方性バルク磁化率とは無関係である。理想的材料では、データの化学シフトの推定誤差は約0.1ppmで;この値を超える小さい変動が観察されることもある。
29Siマジック角回転(MAS)NMR試験を、9.4T磁石のBruker Avance NMR分光計(79.51MHz 29Si ラーモア回転数)で、回転子直径7mmのプローブヘッドを用いて実施した。標品(<45μm)を5.00kHzで回転させた。rf磁場強度28kHzで、80°のパルス長を用い、シングルパルス励起で200スキャンを蓄積した。待ち時間を、インバージョンリカバリシーケンスにより求めたスピン格子緩和時間の3倍となるよう選択した。スピン格子緩和時間は15秒から26秒の範囲である。化学シフトスケールを、-91.34ppmの二次化学シフト標準としてカオリンに対して外部参照した。ピーク最大点およびピーク幅上の誤差バーは±1ppmである。
それぞれpH7.4±0.1およびpH3.0±0.2のトリス-HCl緩衝液およびクエン酸緩衝溶液を調製して、正常および極度の生理的条件(ISO10993-14による)を模擬する。いずれの緩衝溶液もガラスからの分解生成物の定量のために用いる。各粒状材料100mgを、振盪水浴中で37℃に維持したポリプロピレンチューブ中、各溶液(n=3)10mlに浸漬し、2Hzで撹拌する。標品を様々な期間−例えば、1、3、7、または30日間保存する。各期間の後、標品を取り出し、等級5のWhatmanろ紙を通してろ過し、ろ液をイオン含有量分析のために保持する。がラスからの分解生成物を同定し、誘導結合プラズマ−質量分析計を用いて定量する。各抽出物の分析を三つ組で実施する(n=3(条件ごとの抽出物)、各抽出物に対して3回の分析を実施)。
塞栓剤からのイオン放出特性を、インキュベーション時間(X)に対するイオン放出濃度(Y)に関して記載する。インキュベーション時間は相間関数の入力ではないため、時間依存性関数を非線形回帰多項、ガウス、正弦波および指数モデルに、Prism 5.0ソフトウェア(GraphPad software Inc.)を用いてあてはめた。各塞栓剤に関する4つの要素の最適モデルは1フェーズ減衰結合モデルである:
Y=Y0+(プラトー−Y0)*(1−exp(-K*X)) 式7
式中:
「Y」および「X」はそれぞれイオン放出濃度(ppm)およびインキュベーション時間(時間)であり;
「Y0」は初期イオン放出時のイオン放出濃度(ppm)であり;ここでY値はX0=1における値であり;
「プラトー」は無限時間におけるイオン放出濃度(ppm)であり、ここでY値はX=120時間における値であり;
「K」は「tau」インキュベーション時間の逆数で表した速度定数であり、単位は日の逆数であり;
「tau」はイオン放出が推定「ymax」(ppm)の63%に達するのに必要な時間を意味し;
「t1/2」は最終「ymax」値の50%に達するための半減期(時間)を意味し、「t1/2=tau *LN(2)」:
「ts」はY0とプラトーとの間の差を意味し;
「R2」は、Prism 5.0(GraphPad Inc.)ソフトウェアで求めた、指数非線形回帰の最適からの点の距離の二乗の合計である。R2の値は0.0から1.0の間の有理数であり、最適線はR2=1.0のものである。
樹立マウス線維芽細胞株L929(American Type Culture Collection CCL 1線維芽細胞、NCTCクローン929)を、10%ウシ胎仔血清および1%(2mM)L-グルタミンを補足したM199培地中で培養する。細胞を、5%CO2インキュベーター内、37℃の、T-75フラスコ中で成長させる。細胞がコンフルエンシーに達すれば、これらを0.25%トリプシンを用いて化学的に取り出し、遠心分離し、新鮮培地に再懸濁して、さらなる接種のための新しい単細胞懸濁液を作成する。
3T3細胞を24穴プレート(Sarstedt、アイルランド)中1×104/mlの密度で播種する。M199培地を陰性対照として用い、培地プラス細胞を陽性対照として用いる。次いで、プレートを37℃の細胞培養インキュベーター(5%CO2/95%空気雰囲気)内で24時間インキュベートする。24時間後、滅菌組織培養水100μlを対照ウェルに加える。関連する実験抽出物(粒子を含む)100μlを試験のために適切なウェルに加える。次いで、プレートを37℃の細胞培養インキュベーター(5%CO2/95%空気雰囲気)内で24時間インキュベートする。24時間のインキュベーション後、各ウェルを培地量の10%に等しい量(100μl)のMTT(Sigma Aldrich、アイルランド)に曝露する。プレートをインキュベーターに3時間戻す。インキュベーション後、MTT可溶化溶液を各ウェルに元の培地量と等しい量(1ml)で加える。結晶の溶解を増強するために、各ウェルをピペットを用いて滴定し、その後、各ウェルの吸光度を570nmの波長で分光測光法により測定する。細胞陽性対照ウェルは100%の代謝活性を有すると仮定し、実験抽出物に曝露した細胞の代謝活性パーセンテージをこれに対して計算した。
分解試験のための粒子抽出物の調製
粒子およびContour(商標)(市販の対照)(Lot No.:13473927および13599201)0.1gを、2Hzで回転振動させた振盪水浴(Stuart Sb40、Techne Inc.、USA)中、37℃で、滅菌組織培養水(Sigma-Aldrich、カナダ)10ml6に12、24、48、96および120時間浸漬した。それぞれの保存期間の後、試料を滅菌0.20μmフィルター(Sarstedt、カナダ)を用いてろ過し、ろ液をインビトロ評価まで7℃で保存した。
このプロトコルのために、すべての粒子をインキュベーション前に121°/25barで、20分間の高圧滅菌(AMSCO Medallist)によって滅菌した。Contour(商標)の事前滅菌バッチ(Lot No.:13473927および13599201)を対照として用いた。続いて、等量(0.1g)の各滅菌ガラス(ORP1-3、ORP5-7、ORP9、ORP11)およびContour(商標)を10mLの滅菌組織培養水(Sigma-Aldrich、カナダ)に24時間浸漬し、37℃のインキュベーター内部に設置したローラー(約2Hzで回転)上に置いた。各保存期間の後、試料を滅菌0.20μmフィルター(Sarstedt、カナダ)を用いてろ過し、ろ液をインビトロ評価まで7℃で保存した。
15〜20継代の不死化ラット線維芽細胞(NIH-3T3;American Type Tissue Collection、Manassas、VA)を、実験のために用いた。細胞を75-cm2組織培養フラスコ内の5%ウシ胎仔血清(FCS;56℃で60分間熱不活化)を補足したダルベッコ改変イーグル培地(DMEM)中で成長させた。細胞を剥離するために2mLの0.25%トリプシン-EDTAを用いて、70%コンフルエンスで1週間に2回細胞を継代し、8mLのDMEMに再懸濁した。フラスコを37℃、10%CO2の加湿雰囲気下で維持した。細胞代謝の変化を避けるために、日常的細分化の間、または細胞培養実験のために、抗生物質は用いなかった。実験で用いるための線維芽細胞を70%コンフルエンスで回収し、トリプシン-EDTAを用いて剥離し、1×104細胞/mLの濃度で懸濁し、コールターカウンターを用いて検証した。
NIH-3T3細胞(200μL)を96-非組織培養処理ポリスチレンプレート(CoStar、Corning、カナダ)中、1×104細胞/mLの密度で播種した。DMEM+5%FCS培地プラス滅菌組織培養水だけを陰性対照として用い、培地プラス細胞プラス滅菌組織培養水を陽性対照として用いた。すべての試料で連続希釈を行い(25、50、75および100%)、三つ組で行った。したがって、4プレート(各希釈度に対応)を37℃の細胞培養インキュベーター(10%CO2/95%空気雰囲気)内で24時間インキュベートした。24時間後、5、10および15μLの滅菌組織培養水を、それぞれのプレート(75、50および25%希釈に対応)の各ウェルに加えた。次いで、試験のために、20μLの関連する実験抽出物を適切なウェルに加えた。プレートを37℃の細胞培養インキュベーター(10%CO2/95%空気雰囲気)内で再度24時間インキュベートした7。MTT試薬(M2128、Sigma Aldrich Canada)の5mg/mL溶液をリン酸緩衝化食塩水中で調製し、ボルテックス処理し、滅菌ろ過(0.20μm)した。プレートを24時間インキュベートした後、各ウェルを培地量の10%に等しい量の調製したMTTに曝露した。次いで、各希釈セットの4プレートをインキュベーターに3時間戻した。インキュベーション後、MTT可溶化溶液(カタログコード:M8910)を各ウェルに元の培地量と等しい量で加えた。各ウェルを回転テーブル上で緩やかに撹拌して、ホルマザン結晶の溶解を増強した。その後、各ウェルの吸光度を、多検出マイクロプレート読み取り器(Synergy HT、BIO-TEK)上、570nmの波長で分光測光法により測定した。細胞陽性対照ウェルは100%の細胞生存度に対応する100%の代謝活性を有すると仮定し、実験抽出物に曝露した細胞の細胞生存度パーセンテージをこれに対して計算した。
乳酸脱水素酵素(LDH)検定を、比色乳酸脱水素酵素(LDH)検定(TOX-7(製品コード:050M6079)、Sigma Aldrich、カナダ)により、供給会社からの説明に従って測定した。培地中のLDHの量は存在する溶解/死滅細胞の数に比例し;したがって、この検定を用いて細胞死を推定することができる。この検定は、培地中に放出された細胞質LDHの量の関数としての膜の完全性を測定する。簡単に言うと、等量のLDH検定基質(カタログ番号:L2402)、補助因子(カタログ番号:L2527)および色素溶液(カタログ番号:L2277)を混合することにより、検定混合物を調製した。すべての培養物(70μL)に対し、4×96-非組織培養処理ポリスチレンプレート(CoStar、Corning、カナダ)中、検定混合物を培地に2対1の割合で加えた。各プレートはそれぞれ25、50、75および100%の培地希釈度に対応する。室温、暗所(各プレートをAlフォイルで覆った)で、ローラー上で緩やかに回転させてインキュベートした後、呈色反応を1N HClで停止した。MTT検定と同様、DMEM+5%FCS培地プラス滅菌組織培養水だけを陰性対照として用い、培地プラス細胞プラス滅菌組織培養水を陽性対照として用いた。吸光度を、多検出マイクロプレート読み取り器(Synergy HT、BIO-TEK)を用い、650nmで背景補正を行って、490nmで測定した。
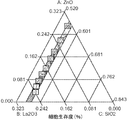
各実験を三つ組で実施し、Prism 5.0ソフトウェア(GraphPad software, Inc.)を用いて解析した。結果を三つ組の測定の平均±標準偏差で表す。群間の比較のために、一元配置分散分析(ANOVA)と、続いてチューキーの事後検定を行った。有意性のレベルをp<0.05に設定した。図18Aは、25、50および100%連続希釈度での、24時間塞栓微粒子抽出物のORP1〜3、ORP5〜7、ORP9およびORP11ならびにContour(商標)存在下での、細胞生存度を示す。結果は平均±SDを表す(有意な統計学的差(p<0.05)は試験した抽物のいずれの間でも観察されなかった)。図18Bは、25、50、75および100%連続希釈度での、24時間塞栓微粒子抽出物のORP1〜3、ORP5〜7、ORP9およびORP11ならびにContour(商標)存在下での、細胞毒性を示す。結果は平均±SDを表す(有意な統計学的差(p<0.05)は試験した抽出物のいずれの間でも観察されなかった)。図19は、実成分コーディングにおける4つの様々なTi添加(0.017(図19A)、0.033(図19B)、0.042(図19C)および0.05モル(図19D))における実験的塞栓材料細胞生存度(%)に対する組成-相互作用効果を示す等高線プロットを示す。
OccluRad対PVA(Contour)の放射線不透過性を、各製品を充填したGammex Tissue Characterizationファントムインサートのコンピューター断層撮影スキャンを用いて評価した。図20は、食塩水/造影剤の様々な希釈度でのORP対PVAの放射線不透過性の比較である。結果を材料のハウンスフィールド単位(HU)値で示す。
子宮動脈内の埋め込み後の局所効果を予備的に試験するために、動物ユニット(ニュージーランドホワイトウサギ)を用いた。材料(ORP5)を関連する血管系に、25G蝶型カニューレを用い、食塩水の懸濁液(8mg/mL)で送達した。動物8匹を用いた;4匹はORP5で処置し、4匹はContourで処置した。動物を21日後にイソフルランおよびKCl(後者はIVにより2mg/kgで投与)を用いて安楽死させた。開腹術を行い、両方の卵巣を含む子宮を摘出した。左右の子宮角を切除し、10%ホルムアルデヒド溶液中に固定し、組織学的評価のために適宜切断した。組織学的試料を子宮角に沿って4〜6の異なるレベル(サイズに応じて)で採取し;その後、日常的なヘマトキシリンおよびエオシン染色を行った。
この試験は、ISO 10993-10に従って行った。試験品(粒子ORP5の抽出物)の刺激を生じる可能性を、試験品の皮下注射後に評価した。3匹のニュージーランドホワイトウサギをこの試験で用いた。各ウサギに0.2mLの試験品または媒体を皮内注射した。極性媒体は生理食塩水で、非極性媒体はゴマ油であった。各動物の処置計画を図22に示す。表24は、実験のドレーズ等級付けシステムを示す。
遠紫外線(UV)円偏光二色性(CD)スペクトルを、温度制御能力を備えたJasco J-810分光偏光計(Easton、MD)を用いて記録した。NaOHおよびH2SO4を用いてpH7.4±0.05に調節した25mMリン酸ナトリウム緩衝液中のヒト血漿由来フィブリノゲン(F4883、無プラスミノゲン、58%タンパク質、96%凝固性タンパク質含有;Sigma Aldrich、ON)の6.4mg/mL溶液を、塞栓抽出物の溶液(各抽出物についてn=3で実施例9で調製した、イオン分解生成物含有) で0.2mg/mLに希釈した。フィブリノゲン保存溶液の濃度を、280nmのUV分光法で、製造者のモル吸光係数を用いて定量した。すべてのスペクトルを0.5mmパス長石英キュベット(Hellma、Mullheim、ドイツ)中、37℃(NESLAB RTE-111浴、Thermo Scientific、Newington、NHで制御)で3回繰り返して収集した(260〜190nm、1nmステップ、50nm/分)。各イオン分解溶液の三つ組のスペクトルを平均し、リン酸緩衝液(25mM;pH7.4±0.05)によるブランクを差し引き、平均残差楕円率([θ])に変換した。試料間の相対的フィブリノゲン立体配座を、約208および222nmでα-らせん帯に対応する最小限で[θ]を比較することによりモニターした。図24は、時間に対するイオン溶解生成物の関数として、遠紫外線円偏光二色性(CD)分光法によりモニターしたFg配座における変化を示す。図24Aは、ORP5の経時的なCDスペクトルの例である。図24BおよびCは、各イオン溶解生成物のFg CDスペクトルの約208および222nmで最小限での強度(3回繰り返しの平均、ブランク減算;平均偏差を示す)である。すべてのデータは平均残差楕円率[θ]で報告する。示す凡例は3つの図すべてに適用される。
全血および血小板の使用に関するすべてのプロトコルは、Capital Health Research Ethics Boardによって承認された。血液(31.5mL)を、Victoria General HospitalのLaboratory Blood Collection施設で、健康な無アスピリンヒト志願者から、クエン酸デキストロース(ACD)抗凝結剤を含む7つの4.5mLガラスBD Vacutainerチューブ(カタログ番号364606、Becton-Dickinson、Franklin Lakes、NJ)中に静脈穿刺により採取した。血液の最初のチューブ(4.5mL)は凝固因子を多く含むため、これを廃棄し、次いで残りの27mLを回収したことに留意することが重要である。血小板を多く含む血漿(PRP)を、Eppendorf 5702遠心機を用いてACD-凝固阻止血液を遠心分離(1500rpm、8分、25℃)することにより生成した。滅菌プラスチックパスツールピペットを用いて、PRPの個々の遠沈管への注意深い移動を完了した。
Claims (34)
- 以下を含む、血管閉塞において用いるための粒状材料:
0.4〜0.57モル分率のSiO2;
0〜0.05モル分率のTiO2;
0.04〜0.188モル分率のLa2O3;
0.068〜0.29モル分率のZnO;ならびに
Na2O、MgO、SrO、およびCaO、
ここでNa2O、MgO、SrO、およびCaOは合わせて0.14モル分率で存在する。 - MgOが0.035モル分率で存在する、請求項1記載の粒状材料。
- SrOが0.035モル分率で存在する、請求項1または2記載の粒状材料。
- Na2Oが0.035モル分率で存在する、請求項1、2、または3記載の粒状材料。
- CaOが0.035モル分率で存在する、請求項1〜4のいずれか一項記載の粒状材料。
- Na2O、MgO、SrO、およびCaOがそれぞれ0.035モル分率で存在する、請求項1記載の粒状材料。
- La2O3が0.04〜0.068モル分率で存在する、請求項1〜6のいずれか一項記載の粒状材料。
- TiO2が0.017〜0.05モル分率で存在する、請求項1〜7のいずれか一項記載の粒状材料。
- 以下から成る、請求項1記載の粒状材料:
0.562モル分率のSiO2;
0.042モル分率のTiO2;
0.068モル分率のLa2O3;
0.035モル分率のMgO;
0.035モル分率のNa2O;
0.188モル分率のZnO;
0.035モル分率のCaO;および
0.035モル分率のSrO。 - 0.1モル分率以下のアルミノケイ酸塩、リン酸塩またはその組み合わせを含む、請求項1記載の粒状材料。
- 治療成分をさらに含む、請求項1〜10のいずれか一項記載の粒状材料。
- 前記治療成分が生理的条件下で放出される、請求項11記載の粒状材料。
- Q1〜Q3のQ−スペシエーション(Q-speciation)を有する、請求項1〜12のいずれか一項記載の粒状材料。
- Q2〜Q3のQ−スペシエーションを有する、請求項13記載の粒状材料。
- 45〜1180μmの平均直径を有する、請求項1〜14のいずれか一項記載の粒状材料。
- 200〜1000μmの平均直径を有する、請求項15記載の粒状材料。
- 300〜500μmの平均直径を有する、請求項15記載の粒状材料。
- 500〜710μmの平均直径を有する、請求項15記載の粒状材料。
- 請求項1〜18のいずれか一項記載の粒状材料;および
該粒状材料をコーティングするポリマー、またはその中に該粒状材料を懸濁するポリマーマトリックス
を含む、組成物。 - 前記ポリマーが乳酸−グリコール酸コポリマーを含む、請求項19記載の組成物。
- 前記ポリマーがポロキサマーを含む、請求項19記載の組成物。
- 治療成分をさらに含む、請求項19〜21のいずれか一項記載の組成物。
- 前記治療成分が生理的条件下で放出される、請求項22記載の組成物。
- 血管奇形の処置のための、請求項1〜18のいずれか一項記載の粒状材料。
- 臓器切除のための、請求項1〜18のいずれか一項記載の粒状材料。
- 化学塞栓術のための、請求項1〜18のいずれか一項記載の粒状材料。
- 出血の処置のための、請求項1〜18のいずれか一項記載の粒状材料。
- 子宮筋腫塞栓術のための、請求項1〜18のいずれか一項記載の粒状材料。
- 血管閉塞において用いるための、請求項19〜23のいずれか一項記載の組成物。
- 血管奇形の処置のための、請求項29記載の組成物。
- 臓器切除のための、請求項29記載の組成物。
- 化学塞栓術のための、請求項29記載の組成物。
- 出血の処置のための、請求項29記載の組成物。
- 子宮筋腫塞栓術のための血管閉塞において用いるための、請求項19〜23のいずれか一項記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161437566P | 2011-01-28 | 2011-01-28 | |
| US61/437,566 | 2011-01-28 | ||
| PCT/IB2012/000341 WO2012101524A2 (en) | 2011-01-28 | 2012-01-27 | Radiopaque embolic particles |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2014508701A JP2014508701A (ja) | 2014-04-10 |
| JP6049637B2 true JP6049637B2 (ja) | 2016-12-21 |
Family
ID=46581213
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013550965A Active JP6049637B2 (ja) | 2011-01-28 | 2012-01-27 | 放射線不透過性塞栓粒子 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US9757480B2 (ja) |
| EP (1) | EP2667879B1 (ja) |
| JP (1) | JP6049637B2 (ja) |
| CN (1) | CN103458903B (ja) |
| AU (1) | AU2012210256B2 (ja) |
| BR (1) | BR112013019218A2 (ja) |
| CA (1) | CA2825512C (ja) |
| EA (1) | EA201370170A1 (ja) |
| SG (2) | SG10201600678WA (ja) |
| WO (1) | WO2012101524A2 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014145509A1 (en) * | 2013-03-15 | 2014-09-18 | The Regents Of The University Of California | Enteric ct contrast material based on low-z atoms |
| CA2968129C (en) * | 2014-11-26 | 2023-11-07 | Abk Biomedical Inc. | Radioembolic particles |
| GB201506381D0 (en) * | 2015-04-15 | 2015-05-27 | Isis Innovation | Embolization particle |
| US10053693B2 (en) * | 2016-01-19 | 2018-08-21 | Mubin I. Syed | Method for controlling obesity using minimally invasive means |
| JP6925014B2 (ja) | 2017-02-15 | 2021-08-25 | ドリームメディカルパートナーズ株式会社 | 塞栓材の製造方法 |
| US11433598B2 (en) * | 2018-01-08 | 2022-09-06 | The University Of Toledo | Bioactive glass/polymer composite filament, and methods of making |
| JP2022533812A (ja) * | 2019-05-31 | 2022-07-26 | エービーケー バイオメディカル インコーポレイテッド | 放射線不透過性ガラス材料 |
| CN114159462B (zh) * | 2021-11-06 | 2023-02-03 | 中国人民解放军海军军医大学 | SiO2在制备抗辐射药物或治疗电离辐射损伤药物中的用途 |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ511762A (en) * | 1993-07-19 | 2003-09-26 | Univ British Columbia | Anti-angiogenic compositions and methods of use |
| DE4428839C2 (de) | 1994-08-01 | 1997-01-23 | Ivoclar Ag | Alkali-Zink-Silicat-Glaskeramiken und -Gläser und Verfahren zur Herstellung der Glaskeramiken |
| CN1044595C (zh) * | 1994-11-17 | 1999-08-11 | 山东省硅酸盐研究设计院 | 无铅无镉陶瓷釉上颜料及其制备方法 |
| FI101129B (sv) | 1995-01-13 | 1998-04-30 | Vivoxid Oy | Nya bioaktiva glas och deras användning |
| US5702361A (en) | 1996-01-31 | 1997-12-30 | Micro Therapeutics, Inc. | Method for embolizing blood vessels |
| EP0953548B1 (en) | 1997-07-30 | 2006-05-03 | Hoya Corporation | Method of producing glass substrate for information recording medium |
| US6423343B1 (en) * | 1998-01-23 | 2002-07-23 | Usbiomaterials Corporation | Bioactive glass treatment of inflammation in skin conditions |
| US6482427B2 (en) | 1999-04-23 | 2002-11-19 | Unicare Biomedical, Inc. | Compositions and methods for repair of osseous defects and accelerated wound healing |
| AU2001234928A1 (en) | 2000-02-10 | 2001-08-20 | Hae Young Lee | Illuminating cap for a valve stem |
| BRPI0300644B8 (pt) * | 2003-02-20 | 2022-04-26 | Fundacao Univ Federal De Sao Carlos | Processo de preparação de biosilicatos particulados, bioativos e reabsorvíveis, composições para preparar ditos biosilicatos e biosilicatos particulados bioativos e reabsorvíveis. |
| US7569626B2 (en) | 2003-06-05 | 2009-08-04 | Dfine, Inc. | Polymer composites for biomedical applications and methods of making |
| ATE369829T1 (de) * | 2003-12-22 | 2007-09-15 | 3M Espe Ag | Glasfüllmaterial und verfahren zur herstellung |
| DE102004011218B4 (de) | 2004-03-04 | 2006-01-19 | Schott Ag | Röntgenopakes Glas, Verfahren zu seiner Herstellung und seine Verwendung |
| JP2005350325A (ja) | 2004-06-14 | 2005-12-22 | Ohara Inc | Yb含有ガラス |
| FR2892819B1 (fr) * | 2005-10-28 | 2008-02-01 | Centre Nat Rech Scient | Nanoparticules a luminescence persistance pour leur utilisation en tant qu'agent de diagnostic destine a l'imagerie optique in vivo |
| FR2908891B1 (fr) * | 2005-10-28 | 2017-04-21 | Centre Nat De La Rech Scient - Cnrs | Nanoparticules a luminescence persistante de type aluminate pour leur utilisation en tant qu'agent de diagnostic destine a l'imagerie optique in vivo |
| CN101484396B (zh) | 2006-07-11 | 2012-07-25 | 日本电气硝子株式会社 | 密封用玻璃组合物和密封材料 |
| US20100021550A1 (en) | 2007-01-12 | 2010-01-28 | Yanfang Li | Radiopaque biodegradable vascular embolic microspheres |
| KR20110081849A (ko) | 2008-10-17 | 2011-07-14 | 아사히 화이바 구라스 가부시키가이샤 | 저융점 유리, 그것을 사용한 수지 조성물, 수지 성형품 |
-
2012
- 2012-01-27 SG SG10201600678WA patent/SG10201600678WA/en unknown
- 2012-01-27 BR BR112013019218A patent/BR112013019218A2/pt not_active IP Right Cessation
- 2012-01-27 EA EA201370170A patent/EA201370170A1/ru unknown
- 2012-01-27 SG SG2013057294A patent/SG192181A1/en unknown
- 2012-01-27 US US13/980,316 patent/US9757480B2/en active Active
- 2012-01-27 JP JP2013550965A patent/JP6049637B2/ja active Active
- 2012-01-27 WO PCT/IB2012/000341 patent/WO2012101524A2/en active Application Filing
- 2012-01-27 EP EP12738789.2A patent/EP2667879B1/en active Active
- 2012-01-27 CA CA2825512A patent/CA2825512C/en active Active
- 2012-01-27 AU AU2012210256A patent/AU2012210256B2/en not_active Ceased
- 2012-01-27 CN CN201280015284.0A patent/CN103458903B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US9757480B2 (en) | 2017-09-12 |
| US20130295020A1 (en) | 2013-11-07 |
| CN103458903A (zh) | 2013-12-18 |
| CN103458903B (zh) | 2017-07-04 |
| EA201370170A1 (ru) | 2014-01-30 |
| EP2667879A4 (en) | 2016-07-06 |
| CA2825512C (en) | 2017-11-14 |
| JP2014508701A (ja) | 2014-04-10 |
| AU2012210256A1 (en) | 2013-08-22 |
| WO2012101524A2 (en) | 2012-08-02 |
| CA2825512A1 (en) | 2012-08-02 |
| WO2012101524A3 (en) | 2013-03-14 |
| SG192181A1 (en) | 2013-08-30 |
| EP2667879B1 (en) | 2020-05-20 |
| NZ613872A (en) | 2016-01-29 |
| BR112013019218A2 (pt) | 2016-10-11 |
| AU2012210256B2 (en) | 2017-03-02 |
| SG10201600678WA (en) | 2016-03-30 |
| EP2667879A2 (en) | 2013-12-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6049637B2 (ja) | 放射線不透過性塞栓粒子 | |
| Rusu et al. | Size-controlled hydroxyapatite nanoparticles as self-organized organic–inorganic composite materials | |
| Laranjeira et al. | Different hydroxyapatite magnetic nanoparticles for medical imaging: Its effects on hemostatic, hemolytic activity and cellular cytotoxicity | |
| Kermanian et al. | One-pot hydrothermal synthesis of a magnetic hydroxyapatite nanocomposite for MR imaging and pH-Sensitive drug delivery applications | |
| Zhou et al. | Amorphous calcium phosphate nanospheres/polylactide composite coated tantalum scaffold: facile preparation, fast biomineralization and subchondral bone defect repair application | |
| Kesse et al. | Elaboration of superparamagnetic and bioactive multicore–shell nanoparticles (Γ-Fe2O3@ SiO2-CaO): A promising material for bone cancer treatment | |
| US20240024535A1 (en) | Orthopedic implant having a crystalline calcium phosphate coating and methods for making the same | |
| Obadia et al. | Effect of sodium doping in β-tricalcium phosphate on its structure and properties | |
| Momeni et al. | Developing an in situ forming polyphosphate coacervate as a new liquid embolic agent: from experimental design to pilot animal study | |
| Kolmas et al. | Effect of carbonate substitution on physicochemical and biological properties of silver containing hydroxyapatites | |
| KR20140132345A (ko) | 골 시멘트 조성물 | |
| CN102380126B (zh) | 一种新型的纳米银骨水泥 | |
| Alkhraisat et al. | Effect of silica gel on the cohesion, properties and biological performance of brushite cement | |
| Nayak et al. | Physiochemical and bactericidal activity evaluation: Silver‐augmented 3D‐printed scaffolds—An in vitro study | |
| Song et al. | Synthesis of Ce/Gd@ HA/PLGA scaffolds contributing to bone repair and MRI enhancement | |
| US11890392B2 (en) | Absorbable bone wax and preparation method thereof | |
| KR101381108B1 (ko) | 말뼈를 이용한 나노 세라믹 골시멘트 및 이의 제조 방법 | |
| de Souza Niero et al. | Composite beads of alginate and biological hydroxyapatite from poultry and mariculture for hard tissue repair | |
| NZ613872B2 (en) | Radiopaque embolic particles | |
| CN108057031A (zh) | 预防手术后异位骨化的缓释吲哚美辛纳米颗粒及其注射剂 | |
| Kolekar et al. | Hemolytic and biological assessment of lithium substituted hydroxyapatite nanoparticles for L929 and Hela cervical cancer cells | |
| Chen et al. | An implantable composite scaffold for amplified chemodynamic therapy and tissue regeneration | |
| Domínguez et al. | Effect of the structural and morphological properties of surfactant-assisted hydroxyapatite on dermal irritation and antibacterial activity | |
| JP5183157B2 (ja) | 新規な塞栓形成組成物 | |
| US20140314867A1 (en) | Vitamin k2 microspheres |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150121 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150424 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20160106 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20160106 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160215 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160506 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160712 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160915 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161018 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20161114 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20161122 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6049637 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |