JP5873003B2 - IgGデコイ受容体融合タンパク質の血液脳関門送達のための組成物および方法 - Google Patents
IgGデコイ受容体融合タンパク質の血液脳関門送達のための組成物および方法 Download PDFInfo
- Publication number
- JP5873003B2 JP5873003B2 JP2012500979A JP2012500979A JP5873003B2 JP 5873003 B2 JP5873003 B2 JP 5873003B2 JP 2012500979 A JP2012500979 A JP 2012500979A JP 2012500979 A JP2012500979 A JP 2012500979A JP 5873003 B2 JP5873003 B2 JP 5873003B2
- Authority
- JP
- Japan
- Prior art keywords
- receptor
- tnf
- extracellular domain
- bbb
- immunoglobulin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108700015048 receptor decoy activity proteins Proteins 0.000 title claims description 114
- 238000000034 method Methods 0.000 title claims description 60
- 210000001218 blood-brain barrier Anatomy 0.000 title description 134
- 230000008499 blood brain barrier function Effects 0.000 title description 133
- 108020001507 fusion proteins Proteins 0.000 title description 133
- 102000037865 fusion proteins Human genes 0.000 title description 126
- 239000000203 mixture Substances 0.000 title description 56
- 102000005962 receptors Human genes 0.000 claims description 290
- 108020003175 receptors Proteins 0.000 claims description 290
- 230000004927 fusion Effects 0.000 claims description 124
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 claims description 118
- 102000003298 tumor necrosis factor receptor Human genes 0.000 claims description 118
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 102
- 150000007523 nucleic acids Chemical class 0.000 claims description 77
- 108060003951 Immunoglobulin Proteins 0.000 claims description 72
- 102000018358 immunoglobulin Human genes 0.000 claims description 72
- 210000004027 cell Anatomy 0.000 claims description 71
- 150000001413 amino acids Chemical group 0.000 claims description 67
- 108090000623 proteins and genes Proteins 0.000 claims description 64
- 102000039446 nucleic acids Human genes 0.000 claims description 63
- 108020004707 nucleic acids Proteins 0.000 claims description 63
- 230000027455 binding Effects 0.000 claims description 59
- 230000001588 bifunctional effect Effects 0.000 claims description 46
- 102000004169 proteins and genes Human genes 0.000 claims description 41
- 101000852815 Homo sapiens Insulin receptor Proteins 0.000 claims description 38
- 102000047882 human INSR Human genes 0.000 claims description 38
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 36
- 239000013598 vector Substances 0.000 claims description 35
- 208000015114 central nervous system disease Diseases 0.000 claims description 27
- 102000003746 Insulin Receptor Human genes 0.000 claims description 25
- 108010001127 Insulin Receptor Proteins 0.000 claims description 25
- 101710097160 Tumor necrosis factor ligand superfamily member 10 Proteins 0.000 claims description 25
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 claims description 21
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 claims description 21
- 102000013275 Somatomedins Human genes 0.000 claims description 21
- 239000003446 ligand Substances 0.000 claims description 20
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 claims description 19
- 108010065825 Immunoglobulin Light Chains Proteins 0.000 claims description 19
- 238000011282 treatment Methods 0.000 claims description 19
- 102000013463 Immunoglobulin Light Chains Human genes 0.000 claims description 18
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 17
- 108010038501 Interleukin-6 Receptors Proteins 0.000 claims description 16
- 230000006907 apoptotic process Effects 0.000 claims description 16
- 239000000411 inducer Substances 0.000 claims description 16
- 102000010781 Interleukin-6 Receptors Human genes 0.000 claims description 15
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 claims description 14
- 102000050554 Eph Family Receptors Human genes 0.000 claims description 14
- 108091008815 Eph receptors Proteins 0.000 claims description 14
- 102000011965 Lipoprotein Receptors Human genes 0.000 claims description 14
- 108010061306 Lipoprotein Receptors Proteins 0.000 claims description 14
- 102000007238 Transferrin Receptors Human genes 0.000 claims description 14
- 108010033576 Transferrin Receptors Proteins 0.000 claims description 14
- 230000000295 complement effect Effects 0.000 claims description 14
- 108091008605 VEGF receptors Proteins 0.000 claims description 13
- 102000009484 Vascular Endothelial Growth Factor Receptors Human genes 0.000 claims description 13
- 201000006417 multiple sclerosis Diseases 0.000 claims description 13
- 229940124676 vascular endothelial growth factor receptor Drugs 0.000 claims description 13
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 12
- 239000013604 expression vector Substances 0.000 claims description 12
- 238000004519 manufacturing process Methods 0.000 claims description 12
- 108010019813 leptin receptors Proteins 0.000 claims description 11
- 102000005861 leptin receptors Human genes 0.000 claims description 11
- 208000030886 Traumatic Brain injury Diseases 0.000 claims description 9
- 201000006474 Brain Ischemia Diseases 0.000 claims description 8
- 206010008120 Cerebral ischaemia Diseases 0.000 claims description 8
- 230000001154 acute effect Effects 0.000 claims description 8
- 206010008118 cerebral infarction Diseases 0.000 claims description 8
- 239000008194 pharmaceutical composition Substances 0.000 claims description 8
- 208000020431 spinal cord injury Diseases 0.000 claims description 8
- 230000009529 traumatic brain injury Effects 0.000 claims description 8
- 230000001684 chronic effect Effects 0.000 claims description 7
- 210000003527 eukaryotic cell Anatomy 0.000 claims description 6
- 230000001640 apoptogenic effect Effects 0.000 claims description 5
- 102000003675 cytokine receptors Human genes 0.000 claims description 5
- 108010057085 cytokine receptors Proteins 0.000 claims description 5
- 230000001939 inductive effect Effects 0.000 claims description 5
- 208000024827 Alzheimer disease Diseases 0.000 claims description 4
- 102000014461 Ataxins Human genes 0.000 claims description 3
- 108010078286 Ataxins Proteins 0.000 claims description 3
- 208000022526 Canavan disease Diseases 0.000 claims description 3
- 206010008025 Cerebellar ataxia Diseases 0.000 claims description 3
- 208000024412 Friedreich ataxia Diseases 0.000 claims description 3
- 201000011240 Frontotemporal dementia Diseases 0.000 claims description 3
- 208000023105 Huntington disease Diseases 0.000 claims description 3
- 208000018737 Parkinson disease Diseases 0.000 claims description 3
- 208000000609 Pick Disease of the Brain Diseases 0.000 claims description 3
- 201000007737 Retinal degeneration Diseases 0.000 claims description 3
- 208000006289 Rett Syndrome Diseases 0.000 claims description 3
- 208000009415 Spinocerebellar Ataxias Diseases 0.000 claims description 3
- 208000026911 Tuberous sclerosis complex Diseases 0.000 claims description 3
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 claims description 3
- 201000004562 autosomal dominant cerebellar ataxia Diseases 0.000 claims description 3
- 230000000626 neurodegenerative effect Effects 0.000 claims description 3
- 208000001749 optic atrophy Diseases 0.000 claims description 3
- 230000004258 retinal degeneration Effects 0.000 claims description 3
- 208000009174 transverse myelitis Diseases 0.000 claims description 3
- 208000009999 tuberous sclerosis Diseases 0.000 claims description 3
- 208000026072 Motor neurone disease Diseases 0.000 claims description 2
- 210000004962 mammalian cell Anatomy 0.000 claims description 2
- 208000005264 motor neuron disease Diseases 0.000 claims description 2
- 102100040247 Tumor necrosis factor Human genes 0.000 claims 17
- 102000046283 TNF-Related Apoptosis-Inducing Ligand Human genes 0.000 claims 4
- 102000009465 Growth Factor Receptors Human genes 0.000 claims 2
- 108010009202 Growth Factor Receptors Proteins 0.000 claims 2
- 210000003989 endothelium vascular Anatomy 0.000 claims 2
- 230000000392 somatic effect Effects 0.000 claims 1
- 241000282414 Homo sapiens Species 0.000 description 89
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 86
- 125000003275 alpha amino acid group Chemical group 0.000 description 72
- 235000001014 amino acid Nutrition 0.000 description 70
- 210000004556 brain Anatomy 0.000 description 68
- 229940024606 amino acid Drugs 0.000 description 55
- 108091006020 Fc-tagged proteins Proteins 0.000 description 52
- 229940027941 immunoglobulin g Drugs 0.000 description 41
- 235000018102 proteins Nutrition 0.000 description 40
- 239000000047 product Substances 0.000 description 32
- 210000000056 organ Anatomy 0.000 description 31
- 230000032258 transport Effects 0.000 description 27
- 239000000427 antigen Substances 0.000 description 26
- 108091007433 antigens Proteins 0.000 description 26
- 102000036639 antigens Human genes 0.000 description 26
- 102100024598 Tumor necrosis factor ligand superfamily member 10 Human genes 0.000 description 21
- -1 AA Amino Acid Chemical class 0.000 description 20
- 206010063836 Atrioventricular septal defect Diseases 0.000 description 19
- 108090000765 processed proteins & peptides Proteins 0.000 description 19
- 238000006467 substitution reaction Methods 0.000 description 19
- 210000003169 central nervous system Anatomy 0.000 description 18
- 239000003814 drug Substances 0.000 description 18
- 241000699666 Mus <mouse, genus> Species 0.000 description 16
- 108010076504 Protein Sorting Signals Proteins 0.000 description 16
- 239000003795 chemical substances by application Substances 0.000 description 16
- 239000002299 complementary DNA Substances 0.000 description 16
- 230000001225 therapeutic effect Effects 0.000 description 16
- 101000611183 Homo sapiens Tumor necrosis factor Proteins 0.000 description 14
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 14
- 239000012634 fragment Substances 0.000 description 14
- 230000014509 gene expression Effects 0.000 description 14
- 239000000243 solution Substances 0.000 description 14
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 13
- 210000004369 blood Anatomy 0.000 description 13
- 239000008280 blood Substances 0.000 description 13
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 102000057041 human TNF Human genes 0.000 description 13
- 125000005647 linker group Chemical group 0.000 description 13
- 239000002773 nucleotide Substances 0.000 description 13
- 125000003729 nucleotide group Chemical group 0.000 description 13
- 238000002741 site-directed mutagenesis Methods 0.000 description 13
- 108010006025 bovine growth hormone Proteins 0.000 description 12
- 238000001990 intravenous administration Methods 0.000 description 12
- 239000013612 plasmid Substances 0.000 description 12
- 238000003752 polymerase chain reaction Methods 0.000 description 12
- 241000701022 Cytomegalovirus Species 0.000 description 11
- 238000002965 ELISA Methods 0.000 description 11
- 108010022394 Threonine synthase Proteins 0.000 description 11
- 230000002093 peripheral effect Effects 0.000 description 11
- 239000012679 serum free medium Substances 0.000 description 11
- 108020004414 DNA Proteins 0.000 description 10
- 108700026244 Open Reading Frames Proteins 0.000 description 10
- 108010000449 TNF-Related Apoptosis-Inducing Ligand Receptors Proteins 0.000 description 10
- 102000002259 TNF-Related Apoptosis-Inducing Ligand Receptors Human genes 0.000 description 10
- 102000004419 dihydrofolate reductase Human genes 0.000 description 10
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 10
- 229940046166 oligodeoxynucleotide Drugs 0.000 description 10
- 239000002953 phosphate buffered saline Substances 0.000 description 10
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 10
- 108010091135 Immunoglobulin Fc Fragments Proteins 0.000 description 9
- 102000018071 Immunoglobulin Fc Fragments Human genes 0.000 description 9
- 102000015696 Interleukins Human genes 0.000 description 9
- 108010063738 Interleukins Proteins 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 230000008901 benefit Effects 0.000 description 9
- 230000002490 cerebral effect Effects 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- 230000013595 glycosylation Effects 0.000 description 9
- 238000006206 glycosylation reaction Methods 0.000 description 9
- 238000002347 injection Methods 0.000 description 9
- 239000007924 injection Substances 0.000 description 9
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 9
- 229920001184 polypeptide Polymers 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- 102000004196 processed proteins & peptides Human genes 0.000 description 9
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 8
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 8
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 8
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 8
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 8
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 8
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 8
- 125000000539 amino acid group Chemical group 0.000 description 8
- 150000001875 compounds Chemical class 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 229940079593 drug Drugs 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 229960000485 methotrexate Drugs 0.000 description 8
- 230000002441 reversible effect Effects 0.000 description 8
- 239000011780 sodium chloride Substances 0.000 description 8
- 229940124597 therapeutic agent Drugs 0.000 description 8
- 208000030507 AIDS Diseases 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 7
- 241000283707 Capra Species 0.000 description 7
- 102000004127 Cytokines Human genes 0.000 description 7
- 108090000695 Cytokines Proteins 0.000 description 7
- 101000801232 Homo sapiens Tumor necrosis factor receptor superfamily member 1B Proteins 0.000 description 7
- 241000282560 Macaca mulatta Species 0.000 description 7
- 239000002253 acid Substances 0.000 description 7
- 239000004480 active ingredient Substances 0.000 description 7
- 230000003321 amplification Effects 0.000 description 7
- 239000003937 drug carrier Substances 0.000 description 7
- 239000013613 expression plasmid Substances 0.000 description 7
- 238000009396 hybridization Methods 0.000 description 7
- 229940072221 immunoglobulins Drugs 0.000 description 7
- 238000003780 insertion Methods 0.000 description 7
- 230000037431 insertion Effects 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 230000001404 mediated effect Effects 0.000 description 7
- 238000003199 nucleic acid amplification method Methods 0.000 description 7
- 239000000546 pharmaceutical excipient Substances 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 241000282412 Homo Species 0.000 description 6
- 241000288906 Primates Species 0.000 description 6
- 208000006011 Stroke Diseases 0.000 description 6
- 239000002775 capsule Substances 0.000 description 6
- 238000007918 intramuscular administration Methods 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 230000035515 penetration Effects 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 239000000829 suppository Substances 0.000 description 6
- 238000001890 transfection Methods 0.000 description 6
- 108020004705 Codon Proteins 0.000 description 5
- 241000699802 Cricetulus griseus Species 0.000 description 5
- 206010012289 Dementia Diseases 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 5
- 101100046559 Mus musculus Tnfrsf12a gene Proteins 0.000 description 5
- 239000004365 Protease Substances 0.000 description 5
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 5
- 238000013459 approach Methods 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 229940098773 bovine serum albumin Drugs 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 230000008878 coupling Effects 0.000 description 5
- 238000010168 coupling process Methods 0.000 description 5
- 238000005859 coupling reaction Methods 0.000 description 5
- UQLDLKMNUJERMK-UHFFFAOYSA-L di(octadecanoyloxy)lead Chemical compound [Pb+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O UQLDLKMNUJERMK-UHFFFAOYSA-L 0.000 description 5
- 239000000539 dimer Substances 0.000 description 5
- 208000035475 disorder Diseases 0.000 description 5
- 238000009826 distribution Methods 0.000 description 5
- 238000010353 genetic engineering Methods 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 238000012417 linear regression Methods 0.000 description 5
- 230000014759 maintenance of location Effects 0.000 description 5
- 239000011159 matrix material Substances 0.000 description 5
- 239000011347 resin Substances 0.000 description 5
- 229920005989 resin Polymers 0.000 description 5
- 239000000523 sample Substances 0.000 description 5
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 5
- 238000007920 subcutaneous administration Methods 0.000 description 5
- 239000006228 supernatant Substances 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 238000007910 systemic administration Methods 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 4
- 208000003174 Brain Neoplasms Diseases 0.000 description 4
- 208000014644 Brain disease Diseases 0.000 description 4
- 108010092160 Dactinomycin Proteins 0.000 description 4
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 4
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 4
- 108090001061 Insulin Proteins 0.000 description 4
- 102000004877 Insulin Human genes 0.000 description 4
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 4
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 4
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 4
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 4
- 229920001213 Polysorbate 20 Polymers 0.000 description 4
- XQJCEKXQUJQNNK-ZLUOBGJFSA-N Ser-Ser-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O XQJCEKXQUJQNNK-ZLUOBGJFSA-N 0.000 description 4
- 238000002835 absorbance Methods 0.000 description 4
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 208000029028 brain injury Diseases 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 238000010367 cloning Methods 0.000 description 4
- 125000000151 cysteine group Chemical class N[C@@H](CS)C(=O)* 0.000 description 4
- 229960000640 dactinomycin Drugs 0.000 description 4
- 239000006274 endogenous ligand Substances 0.000 description 4
- 229960000556 fingolimod Drugs 0.000 description 4
- KKGQTZUTZRNORY-UHFFFAOYSA-N fingolimod Chemical compound CCCCCCCCC1=CC=C(CCC(N)(CO)CO)C=C1 KKGQTZUTZRNORY-UHFFFAOYSA-N 0.000 description 4
- ZXQYGBMAQZUVMI-GCMPRSNUSA-N gamma-cyhalothrin Chemical compound CC1(C)[C@@H](\C=C(/Cl)C(F)(F)F)[C@H]1C(=O)O[C@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 ZXQYGBMAQZUVMI-GCMPRSNUSA-N 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 4
- 230000001965 increasing effect Effects 0.000 description 4
- 229940125396 insulin Drugs 0.000 description 4
- 238000007912 intraperitoneal administration Methods 0.000 description 4
- 150000002605 large molecules Chemical class 0.000 description 4
- 229920002521 macromolecule Polymers 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 239000003550 marker Substances 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 4
- 210000001672 ovary Anatomy 0.000 description 4
- 239000008188 pellet Substances 0.000 description 4
- 238000010647 peptide synthesis reaction Methods 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 4
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 4
- 238000001556 precipitation Methods 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- 230000002792 vascular Effects 0.000 description 4
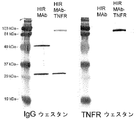
- 238000001262 western blot Methods 0.000 description 4
- 210000004885 white matter Anatomy 0.000 description 4
- SYTBZMRGLBWNTM-SNVBAGLBSA-N (R)-flurbiprofen Chemical compound FC1=CC([C@H](C(O)=O)C)=CC=C1C1=CC=CC=C1 SYTBZMRGLBWNTM-SNVBAGLBSA-N 0.000 description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- 239000004475 Arginine Substances 0.000 description 3
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 3
- 108010078791 Carrier Proteins Proteins 0.000 description 3
- 206010008089 Cerebral artery occlusion Diseases 0.000 description 3
- 238000011537 Coomassie blue staining Methods 0.000 description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- 238000001712 DNA sequencing Methods 0.000 description 3
- 208000016192 Demyelinating disease Diseases 0.000 description 3
- QMMFVYPAHWMCMS-UHFFFAOYSA-N Dimethyl sulfide Chemical compound CSC QMMFVYPAHWMCMS-UHFFFAOYSA-N 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 102000004889 Interleukin-6 Human genes 0.000 description 3
- 108090001005 Interleukin-6 Proteins 0.000 description 3
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 3
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 3
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 3
- 239000004472 Lysine Substances 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 108091005804 Peptidases Proteins 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 101710187830 Tumor necrosis factor receptor superfamily member 1B Proteins 0.000 description 3
- 102100033733 Tumor necrosis factor receptor superfamily member 1B Human genes 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 3
- 235000009697 arginine Nutrition 0.000 description 3
- 235000009582 asparagine Nutrition 0.000 description 3
- 229960001230 asparagine Drugs 0.000 description 3
- 235000003704 aspartic acid Nutrition 0.000 description 3
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 210000004899 c-terminal region Anatomy 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 3
- 235000018417 cysteine Nutrition 0.000 description 3
- 231100000135 cytotoxicity Toxicity 0.000 description 3
- 230000003013 cytotoxicity Effects 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 210000005153 frontal cortex Anatomy 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 235000013922 glutamic acid Nutrition 0.000 description 3
- 239000004220 glutamic acid Substances 0.000 description 3
- 210000004884 grey matter Anatomy 0.000 description 3
- 210000002216 heart Anatomy 0.000 description 3
- 238000010348 incorporation Methods 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 208000027866 inflammatory disease Diseases 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 238000010253 intravenous injection Methods 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 210000004185 liver Anatomy 0.000 description 3
- 210000004072 lung Anatomy 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 229930182817 methionine Natural products 0.000 description 3
- 201000007309 middle cerebral artery infarction Diseases 0.000 description 3
- 210000004498 neuroglial cell Anatomy 0.000 description 3
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 3
- 239000010452 phosphate Substances 0.000 description 3
- 239000006187 pill Substances 0.000 description 3
- 230000008488 polyadenylation Effects 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 229960004197 prasugrel Drugs 0.000 description 3
- DTGLZDAWLRGWQN-UHFFFAOYSA-N prasugrel Chemical compound C1CC=2SC(OC(=O)C)=CC=2CN1C(C=1C(=CC=CC=1)F)C(=O)C1CC1 DTGLZDAWLRGWQN-UHFFFAOYSA-N 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 230000000069 prophylactic effect Effects 0.000 description 3
- 125000006239 protecting group Chemical group 0.000 description 3
- 238000010839 reverse transcription Methods 0.000 description 3
- 230000009919 sequestration Effects 0.000 description 3
- 239000007790 solid phase Substances 0.000 description 3
- 238000010532 solid phase synthesis reaction Methods 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 2
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 2
- XZKIHKMTEMTJQX-UHFFFAOYSA-N 4-Nitrophenyl Phosphate Chemical compound OP(O)(=O)OC1=CC=C([N+]([O-])=O)C=C1 XZKIHKMTEMTJQX-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 2
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 2
- 206010012305 Demyelination Diseases 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 2
- 108010072051 Glatiramer Acetate Proteins 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- 241000725303 Human immunodeficiency virus Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 206010020751 Hypersensitivity Diseases 0.000 description 2
- 102000009490 IgG Receptors Human genes 0.000 description 2
- 108010073807 IgG Receptors Proteins 0.000 description 2
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 2
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 108010025815 Kanamycin Kinase Proteins 0.000 description 2
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 2
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 2
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 2
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 2
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 2
- 101150027568 LC gene Proteins 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 2
- 241000699660 Mus musculus Species 0.000 description 2
- 108090000526 Papain Proteins 0.000 description 2
- 102000057297 Pepsin A Human genes 0.000 description 2
- 108090000284 Pepsin A Proteins 0.000 description 2
- 108091093037 Peptide nucleic acid Proteins 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 208000024571 Pick disease Diseases 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 239000012980 RPMI-1640 medium Substances 0.000 description 2
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 2
- 229920005654 Sephadex Polymers 0.000 description 2
- 239000012507 Sephadex™ Substances 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 2
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 description 2
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 description 2
- 108700019146 Transgenes Proteins 0.000 description 2
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 2
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 208000026935 allergic disease Diseases 0.000 description 2
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 230000000844 anti-bacterial effect Effects 0.000 description 2
- 229940121375 antifungal agent Drugs 0.000 description 2
- 239000003429 antifungal agent Substances 0.000 description 2
- 239000000739 antihistaminic agent Substances 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 210000004204 blood vessel Anatomy 0.000 description 2
- 210000004781 brain capillary Anatomy 0.000 description 2
- 230000006931 brain damage Effects 0.000 description 2
- 231100000874 brain damage Toxicity 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 239000007958 cherry flavor Substances 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 229960002436 cladribine Drugs 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000012761 co-transfection Methods 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 238000002648 combination therapy Methods 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 229960004397 cyclophosphamide Drugs 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 229960002806 daclizumab Drugs 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000004925 denaturation Methods 0.000 description 2
- 230000036425 denaturation Effects 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- BGRWYRAHAFMIBJ-UHFFFAOYSA-N diisopropylcarbodiimide Natural products CC(C)NC(=O)NC(C)C BGRWYRAHAFMIBJ-UHFFFAOYSA-N 0.000 description 2
- 239000002612 dispersion medium Substances 0.000 description 2
- 238000001211 electron capture detection Methods 0.000 description 2
- 230000003511 endothelial effect Effects 0.000 description 2
- PROQIPRRNZUXQM-ZXXIGWHRSA-N estriol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H]([C@H](O)C4)O)[C@@H]4[C@@H]3CCC2=C1 PROQIPRRNZUXQM-ZXXIGWHRSA-N 0.000 description 2
- 210000003191 femoral vein Anatomy 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- ASUTZQLVASHGKV-JDFRZJQESA-N galanthamine Chemical compound O1C(=C23)C(OC)=CC=C2CN(C)CC[C@]23[C@@H]1C[C@@H](O)C=C2 ASUTZQLVASHGKV-JDFRZJQESA-N 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 235000004554 glutamine Nutrition 0.000 description 2
- 229920000669 heparin Polymers 0.000 description 2
- 210000004408 hybridoma Anatomy 0.000 description 2
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical compound O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 2
- 230000001900 immune effect Effects 0.000 description 2
- 230000036039 immunity Effects 0.000 description 2
- 230000002757 inflammatory effect Effects 0.000 description 2
- 239000007972 injectable composition Substances 0.000 description 2
- 238000001361 intraarterial administration Methods 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 2
- 229960000310 isoleucine Drugs 0.000 description 2
- 239000007951 isotonicity adjuster Substances 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- 229960005027 natalizumab Drugs 0.000 description 2
- 230000004770 neurodegeneration Effects 0.000 description 2
- 208000015122 neurodegenerative disease Diseases 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 239000008203 oral pharmaceutical composition Substances 0.000 description 2
- 229940055729 papain Drugs 0.000 description 2
- 235000019834 papain Nutrition 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 229940111202 pepsin Drugs 0.000 description 2
- 210000005259 peripheral blood Anatomy 0.000 description 2
- 239000011886 peripheral blood Substances 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 229940068968 polysorbate 80 Drugs 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000000770 proinflammatory effect Effects 0.000 description 2
- 235000019419 proteases Nutrition 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 238000000163 radioactive labelling Methods 0.000 description 2
- 238000002708 random mutagenesis Methods 0.000 description 2
- 238000010188 recombinant method Methods 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 238000000611 regression analysis Methods 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 229960004641 rituximab Drugs 0.000 description 2
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 210000002027 skeletal muscle Anatomy 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 239000000600 sorbitol Substances 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 208000011580 syndromic disease Diseases 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 2
- 230000009424 thromboembolic effect Effects 0.000 description 2
- 238000011830 transgenic mouse model Methods 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- 239000004474 valine Substances 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 229960005080 warfarin Drugs 0.000 description 2
- PJVWKTKQMONHTI-UHFFFAOYSA-N warfarin Chemical compound OC=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=CC=C1 PJVWKTKQMONHTI-UHFFFAOYSA-N 0.000 description 2
- WMBWREPUVVBILR-WIYYLYMNSA-N (-)-Epigallocatechin-3-o-gallate Chemical compound O([C@@H]1CC2=C(O)C=C(C=C2O[C@@H]1C=1C=C(O)C(O)=C(O)C=1)O)C(=O)C1=CC(O)=C(O)C(O)=C1 WMBWREPUVVBILR-WIYYLYMNSA-N 0.000 description 1
- PROQIPRRNZUXQM-UHFFFAOYSA-N (16alpha,17betaOH)-Estra-1,3,5(10)-triene-3,16,17-triol Natural products OC1=CC=C2C3CCC(C)(C(C(O)C4)O)C4C3CCC2=C1 PROQIPRRNZUXQM-UHFFFAOYSA-N 0.000 description 1
- KYRUKRFVOACELK-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(4-hydroxyphenyl)propanoate Chemical compound C1=CC(O)=CC=C1CCC(=O)ON1C(=O)CCC1=O KYRUKRFVOACELK-UHFFFAOYSA-N 0.000 description 1
- FDKWRPBBCBCIGA-REOHCLBHSA-N (2r)-2-azaniumyl-3-$l^{1}-selanylpropanoate Chemical compound [Se]C[C@H](N)C(O)=O FDKWRPBBCBCIGA-REOHCLBHSA-N 0.000 description 1
- LJCBAPRMNYSDOP-LVCYMWGESA-N (2s)-3-(7-carbamimidoylnaphthalen-2-yl)-2-[4-[(3s)-1-ethanimidoylpyrrolidin-3-yl]oxyphenyl]propanoic acid;hydron;chloride;pentahydrate Chemical compound O.O.O.O.O.Cl.C1N(C(=N)C)CC[C@@H]1OC1=CC=C([C@H](CC=2C=C3C=C(C=CC3=CC=2)C(N)=N)C(O)=O)C=C1 LJCBAPRMNYSDOP-LVCYMWGESA-N 0.000 description 1
- SSNHGLKFJISNTR-DYSNNVSPSA-N (6ar,10ar)-6,6,9-trimethyl-3-pentyl-6a,7,8,10a-tetrahydrobenzo[c]chromen-1-ol;2-[(1r,6r)-3-methyl-6-prop-1-en-2-ylcyclohex-2-en-1-yl]-5-pentylbenzene-1,3-diol Chemical compound OC1=CC(CCCCC)=CC(O)=C1[C@H]1[C@H](C(C)=C)CCC(C)=C1.C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@@H]21 SSNHGLKFJISNTR-DYSNNVSPSA-N 0.000 description 1
- HMLGSIZOMSVISS-ONJSNURVSA-N (7r)-7-[[(2z)-2-(2-amino-1,3-thiazol-4-yl)-2-(2,2-dimethylpropanoyloxymethoxyimino)acetyl]amino]-3-ethenyl-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid Chemical compound N([C@@H]1C(N2C(=C(C=C)CSC21)C(O)=O)=O)C(=O)\C(=N/OCOC(=O)C(C)(C)C)C1=CSC(N)=N1 HMLGSIZOMSVISS-ONJSNURVSA-N 0.000 description 1
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- VGONTNSXDCQUGY-RRKCRQDMSA-N 2'-deoxyinosine Chemical group C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC2=O)=C2N=C1 VGONTNSXDCQUGY-RRKCRQDMSA-N 0.000 description 1
- NEMPBEUBSBVJOO-UHFFFAOYSA-M 2-[3-(4-iodophenyl)-5-phenyltetrazol-2-ium-2-yl]-4,5-dimethyl-1,3-thiazole;bromide Chemical compound [Br-].S1C(C)=C(C)N=C1[N+]1=NC(C=2C=CC=CC=2)=NN1C1=CC=C(I)C=C1 NEMPBEUBSBVJOO-UHFFFAOYSA-M 0.000 description 1
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 1
- HYCKBFLTZGORKA-HNPMAXIBSA-N 3,7-dihydropurin-6-one;1-[(2r,4s,5r)-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound O=C1NC=NC2=C1NC=N2.O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 HYCKBFLTZGORKA-HNPMAXIBSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- NUKYPUAOHBNCPY-UHFFFAOYSA-N 4-aminopyridine Chemical compound NC1=CC=NC=C1 NUKYPUAOHBNCPY-UHFFFAOYSA-N 0.000 description 1
- 206010065040 AIDS dementia complex Diseases 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- PQSUYGKTWSAVDQ-ZVIOFETBSA-N Aldosterone Chemical compound C([C@@]1([C@@H](C(=O)CO)CC[C@H]1[C@@H]1CC2)C=O)[C@H](O)[C@@H]1[C@]1(C)C2=CC(=O)CC1 PQSUYGKTWSAVDQ-ZVIOFETBSA-N 0.000 description 1
- PQSUYGKTWSAVDQ-UHFFFAOYSA-N Aldosterone Natural products C1CC2C3CCC(C(=O)CO)C3(C=O)CC(O)C2C2(C)C1=CC(=O)CC2 PQSUYGKTWSAVDQ-UHFFFAOYSA-N 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 108010058207 Anistreplase Proteins 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- XHVAWZZCDCWGBK-WYRLRVFGSA-M Aurothioglucose Chemical compound OC[C@H]1O[C@H](S[Au])[C@H](O)[C@@H](O)[C@@H]1O XHVAWZZCDCWGBK-WYRLRVFGSA-M 0.000 description 1
- 208000032116 Autoimmune Experimental Encephalomyelitis Diseases 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 239000005552 B01AC04 - Clopidogrel Substances 0.000 description 1
- 239000005528 B01AC05 - Ticlopidine Substances 0.000 description 1
- 239000005465 B01AC22 - Prasugrel Substances 0.000 description 1
- 108010027740 BHT 3009 Proteins 0.000 description 1
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- RZZPDXZPRHQOCG-OJAKKHQRSA-O CDP-choline(1+) Chemical compound O[C@@H]1[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OCC[N+](C)(C)C)O[C@H]1N1C(=O)N=C(N)C=C1 RZZPDXZPRHQOCG-OJAKKHQRSA-O 0.000 description 1
- 101150071146 COX2 gene Proteins 0.000 description 1
- 101100114534 Caenorhabditis elegans ctc-2 gene Proteins 0.000 description 1
- 101100283604 Caenorhabditis elegans pigk-1 gene Proteins 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 208000018652 Closed Head injury Diseases 0.000 description 1
- ITRJWOMZKQRYTA-RFZYENFJSA-N Cortisone acetate Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)COC(=O)C)(O)[C@@]1(C)CC2=O ITRJWOMZKQRYTA-RFZYENFJSA-N 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 229930105110 Cyclosporin A Natural products 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- FDKWRPBBCBCIGA-UWTATZPHSA-N D-Selenocysteine Natural products [Se]C[C@@H](N)C(O)=O FDKWRPBBCBCIGA-UWTATZPHSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- 101150074155 DHFR gene Proteins 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- VPGRYOFKCNULNK-ACXQXYJUSA-N Deoxycorticosterone acetate Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)COC(=O)C)[C@@]1(C)CC2 VPGRYOFKCNULNK-ACXQXYJUSA-N 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 101100099879 Equus caballus TNF gene Proteins 0.000 description 1
- 108010008165 Etanercept Proteins 0.000 description 1
- 229940123583 Factor Xa inhibitor Drugs 0.000 description 1
- 102000009109 Fc receptors Human genes 0.000 description 1
- 108010087819 Fc receptors Proteins 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-N Fluorane Chemical compound F KRHYYFGTRYWZRS-UHFFFAOYSA-N 0.000 description 1
- WMBWREPUVVBILR-UHFFFAOYSA-N GCG Natural products C=1C(O)=C(O)C(O)=CC=1C1OC2=CC(O)=CC(O)=C2CC1OC(=O)C1=CC(O)=C(O)C(O)=C1 WMBWREPUVVBILR-UHFFFAOYSA-N 0.000 description 1
- 102000006395 Globulins Human genes 0.000 description 1
- 108010044091 Globulins Proteins 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 1
- 206010019196 Head injury Diseases 0.000 description 1
- 241000700721 Hepatitis B virus Species 0.000 description 1
- 101000599951 Homo sapiens Insulin-like growth factor I Proteins 0.000 description 1
- 101001076292 Homo sapiens Insulin-like growth factor II Proteins 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 1
- ZJVFLBOZORBYFE-UHFFFAOYSA-N Ibudilast Chemical compound C1=CC=CC2=C(C(=O)C(C)C)C(C(C)C)=NN21 ZJVFLBOZORBYFE-UHFFFAOYSA-N 0.000 description 1
- 102000009786 Immunoglobulin Constant Regions Human genes 0.000 description 1
- 108010009817 Immunoglobulin Constant Regions Proteins 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102100037852 Insulin-like growth factor I Human genes 0.000 description 1
- 102100025947 Insulin-like growth factor II Human genes 0.000 description 1
- 108010005716 Interferon beta-1a Proteins 0.000 description 1
- 108010005714 Interferon beta-1b Proteins 0.000 description 1
- 108090000467 Interferon-beta Proteins 0.000 description 1
- 102000003996 Interferon-beta Human genes 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 102000051628 Interleukin-1 receptor antagonist Human genes 0.000 description 1
- 108700021006 Interleukin-1 receptor antagonist Proteins 0.000 description 1
- 102000000588 Interleukin-2 Human genes 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 1
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical compound OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 1
- QEFRNWWLZKMPFJ-ZXPFJRLXSA-N L-methionine (R)-S-oxide Chemical compound C[S@@](=O)CC[C@H]([NH3+])C([O-])=O QEFRNWWLZKMPFJ-ZXPFJRLXSA-N 0.000 description 1
- QEFRNWWLZKMPFJ-UHFFFAOYSA-N L-methionine sulphoxide Natural products CS(=O)CCC(N)C(O)=O QEFRNWWLZKMPFJ-UHFFFAOYSA-N 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 102000016267 Leptin Human genes 0.000 description 1
- 108010092277 Leptin Proteins 0.000 description 1
- 239000012097 Lipofectamine 2000 Substances 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 102000004083 Lymphotoxin-alpha Human genes 0.000 description 1
- 108090000542 Lymphotoxin-alpha Proteins 0.000 description 1
- 102000003959 Lymphotoxin-beta Human genes 0.000 description 1
- 108090000362 Lymphotoxin-beta Proteins 0.000 description 1
- 108010016230 MBP-8298 Proteins 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 244000246386 Mentha pulegium Species 0.000 description 1
- 235000016257 Mentha pulegium Nutrition 0.000 description 1
- 235000004357 Mentha x piperita Nutrition 0.000 description 1
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 1
- 241000238367 Mya arenaria Species 0.000 description 1
- 230000004988 N-glycosylation Effects 0.000 description 1
- 108091007491 NSP3 Papain-like protease domains Proteins 0.000 description 1
- 241001045988 Neogene Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 1
- BLZLODDEPXSDCY-UHFFFAOYSA-N OC(=O)CC(O)=O.OC(=O)C1=CC=CC=C1 Chemical compound OC(=O)CC(O)=O.OC(=O)C1=CC=CC=C1 BLZLODDEPXSDCY-UHFFFAOYSA-N 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 101150000187 PTGS2 gene Proteins 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 108020002230 Pancreatic Ribonuclease Proteins 0.000 description 1
- 102000005891 Pancreatic ribonuclease Human genes 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- QNVSXXGDAPORNA-UHFFFAOYSA-N Resveratrol Natural products OC1=CC=CC(C=CC=2C=C(O)C(O)=CC=2)=C1 QNVSXXGDAPORNA-UHFFFAOYSA-N 0.000 description 1
- 206010039101 Rhinorrhoea Diseases 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- XSVMFMHYUFZWBK-NSHDSACASA-N Rivastigmine Chemical compound CCN(C)C(=O)OC1=CC=CC([C@H](C)N(C)C)=C1 XSVMFMHYUFZWBK-NSHDSACASA-N 0.000 description 1
- XZKQVQKUZMAADP-IMJSIDKUSA-N Ser-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H](CO)C(O)=O XZKQVQKUZMAADP-IMJSIDKUSA-N 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 108010023197 Streptokinase Proteins 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 101150033527 TNF gene Proteins 0.000 description 1
- 108010014401 TWEAK Receptor Proteins 0.000 description 1
- 102000016946 TWEAK Receptor Human genes 0.000 description 1
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 1
- CBPNZQVSJQDFBE-FUXHJELOSA-N Temsirolimus Chemical compound C1C[C@@H](OC(=O)C(C)(CO)CO)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 CBPNZQVSJQDFBE-FUXHJELOSA-N 0.000 description 1
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-N Thiophosphoric acid Chemical class OP(O)(S)=O RYYWUUFWQRZTIU-UHFFFAOYSA-N 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- LUKBXSAWLPMMSZ-OWOJBTEDSA-N Trans-resveratrol Chemical compound C1=CC(O)=CC=C1\C=C\C1=CC(O)=CC(O)=C1 LUKBXSAWLPMMSZ-OWOJBTEDSA-N 0.000 description 1
- 102000004338 Transferrin Human genes 0.000 description 1
- 108090000901 Transferrin Proteins 0.000 description 1
- 206010054094 Tumour necrosis Diseases 0.000 description 1
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 description 1
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 108010046516 Wheat Germ Agglutinins Proteins 0.000 description 1
- JOOSFXXMIOXKAZ-UHFFFAOYSA-H [Au+3].[Au+3].[O-]C(=O)CC(S)C([O-])=O.[O-]C(=O)CC(S)C([O-])=O.[O-]C(=O)CC(S)C([O-])=O Chemical compound [Au+3].[Au+3].[O-]C(=O)CC(S)C([O-])=O.[O-]C(=O)CC(S)C([O-])=O.[O-]C(=O)CC(S)C([O-])=O JOOSFXXMIOXKAZ-UHFFFAOYSA-H 0.000 description 1
- 229960003697 abatacept Drugs 0.000 description 1
- 239000003070 absorption delaying agent Substances 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- FHEAIOHRHQGZPC-KIWGSFCNSA-N acetic acid;(2s)-2-amino-3-(4-hydroxyphenyl)propanoic acid;(2s)-2-aminopentanedioic acid;(2s)-2-aminopropanoic acid;(2s)-2,6-diaminohexanoic acid Chemical compound CC(O)=O.C[C@H](N)C(O)=O.NCCCC[C@H](N)C(O)=O.OC(=O)[C@@H](N)CCC(O)=O.OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 FHEAIOHRHQGZPC-KIWGSFCNSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229960002964 adalimumab Drugs 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 238000000246 agarose gel electrophoresis Methods 0.000 description 1
- 229960002478 aldosterone Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 150000001370 alpha-amino acid derivatives Chemical class 0.000 description 1
- 235000008206 alpha-amino acids Nutrition 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 229960003318 alteplase Drugs 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 229960004238 anakinra Drugs 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 239000002870 angiogenesis inducing agent Substances 0.000 description 1
- 229960000983 anistreplase Drugs 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 230000001772 anti-angiogenic effect Effects 0.000 description 1
- 230000001078 anti-cholinergic effect Effects 0.000 description 1
- 230000001387 anti-histamine Effects 0.000 description 1
- 230000002590 anti-leukotriene effect Effects 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 230000000692 anti-sense effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 238000003491 array Methods 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- 229960002170 azathioprine Drugs 0.000 description 1
- LMEKQMALGUDUQG-UHFFFAOYSA-N azathioprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC=NC2=C1NC=N2 LMEKQMALGUDUQG-UHFFFAOYSA-N 0.000 description 1
- 229940092705 beclomethasone Drugs 0.000 description 1
- NBMKJKDGKREAPL-DVTGEIKXSA-N beclomethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O NBMKJKDGKREAPL-DVTGEIKXSA-N 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- 229940125388 beta agonist Drugs 0.000 description 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 1
- 229960002537 betamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 1
- AFYNADDZULBEJA-UHFFFAOYSA-N bicinchoninic acid Chemical compound C1=CC=CC2=NC(C=3C=C(C4=CC=CC=C4N=3)C(=O)O)=CC(C(O)=O)=C21 AFYNADDZULBEJA-UHFFFAOYSA-N 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 238000006664 bond formation reaction Methods 0.000 description 1
- 210000005013 brain tissue Anatomy 0.000 description 1
- 239000006189 buccal tablet Substances 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- 229910001622 calcium bromide Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- WGEFECGEFUFIQW-UHFFFAOYSA-L calcium dibromide Chemical compound [Ca+2].[Br-].[Br-] WGEFECGEFUFIQW-UHFFFAOYSA-L 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- JGIATAMCQXIDNZ-UHFFFAOYSA-N calcium sulfide Chemical compound [Ca]=S JGIATAMCQXIDNZ-UHFFFAOYSA-N 0.000 description 1
- 229940112129 campath Drugs 0.000 description 1
- 229960000590 celecoxib Drugs 0.000 description 1
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000012412 chemical coupling Methods 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 230000006726 chronic neurodegeneration Effects 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- 229960003009 clopidogrel Drugs 0.000 description 1
- GKTWGGQPFAXNFI-HNNXBMFYSA-N clopidogrel Chemical compound C1([C@H](N2CC=3C=CSC=3CC2)C(=O)OC)=CC=CC=C1Cl GKTWGGQPFAXNFI-HNNXBMFYSA-N 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- 230000024203 complement activation Effects 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 239000003636 conditioned culture medium Substances 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 229940038717 copaxone Drugs 0.000 description 1
- 229960003290 cortisone acetate Drugs 0.000 description 1
- 229940111134 coxibs Drugs 0.000 description 1
- 239000003255 cyclooxygenase 2 inhibitor Substances 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 239000002619 cytotoxin Substances 0.000 description 1
- 229960003850 dabigatran Drugs 0.000 description 1
- YBSJFWOBGCMAKL-UHFFFAOYSA-N dabigatran Chemical compound N=1C2=CC(C(=O)N(CCC(O)=O)C=3N=CC=CC=3)=CC=C2N(C)C=1CNC1=CC=C(C(N)=N)C=C1 YBSJFWOBGCMAKL-UHFFFAOYSA-N 0.000 description 1
- 229960000288 dabigatran etexilate Drugs 0.000 description 1
- KSGXQBZTULBEEQ-UHFFFAOYSA-N dabigatran etexilate Chemical compound C1=CC(C(N)=NC(=O)OCCCCCC)=CC=C1NCC1=NC2=CC(C(=O)N(CCC(=O)OCC)C=3N=CC=CC=3)=CC=C2N1C KSGXQBZTULBEEQ-UHFFFAOYSA-N 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 239000005549 deoxyribonucleoside Substances 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 229960004486 desoxycorticosterone acetate Drugs 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000000378 dietary effect Effects 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- UGMCXQCYOVCMTB-UHFFFAOYSA-K dihydroxy(stearato)aluminium Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[Al](O)O UGMCXQCYOVCMTB-UHFFFAOYSA-K 0.000 description 1
- RCTCWZRPYFBGLQ-WMCRPSJMSA-N dirucotide Chemical compound C([C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 RCTCWZRPYFBGLQ-WMCRPSJMSA-N 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 231100000276 dose-dependent cytotoxicity Toxicity 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 210000001671 embryonic stem cell Anatomy 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 239000002702 enteric coating Substances 0.000 description 1
- 238000009505 enteric coating Methods 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- 229960001348 estriol Drugs 0.000 description 1
- 229960000403 etanercept Drugs 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 208000012997 experimental autoimmune encephalomyelitis Diseases 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 239000003527 fibrinolytic agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229940014144 folate Drugs 0.000 description 1
- OVBPIULPVIDEAO-LBPRGKRZSA-N folic acid Chemical compound C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-LBPRGKRZSA-N 0.000 description 1
- 235000019152 folic acid Nutrition 0.000 description 1
- 239000011724 folic acid Substances 0.000 description 1
- KANJSNBRCNMZMV-ABRZTLGGSA-N fondaparinux Chemical compound O[C@@H]1[C@@H](NS(O)(=O)=O)[C@@H](OC)O[C@H](COS(O)(=O)=O)[C@H]1O[C@H]1[C@H](OS(O)(=O)=O)[C@@H](O)[C@H](O[C@@H]2[C@@H]([C@@H](OS(O)(=O)=O)[C@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O[C@@H]4[C@@H]([C@@H](O)[C@H](O)[C@@H](COS(O)(=O)=O)O4)NS(O)(=O)=O)[C@H](O3)C(O)=O)O)[C@@H](COS(O)(=O)=O)O2)NS(O)(=O)=O)[C@H](C(O)=O)O1 KANJSNBRCNMZMV-ABRZTLGGSA-N 0.000 description 1
- 229960001318 fondaparinux Drugs 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 229960003980 galantamine Drugs 0.000 description 1
- ASUTZQLVASHGKV-UHFFFAOYSA-N galanthamine hydrochloride Natural products O1C(=C23)C(OC)=CC=C2CN(C)CCC23C1CC(O)C=C2 ASUTZQLVASHGKV-UHFFFAOYSA-N 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 229960003776 glatiramer acetate Drugs 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 235000001050 hortel pimenta Nutrition 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 229940098197 human immunoglobulin g Drugs 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 229940099472 immunoglobulin a Drugs 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000003701 inert diluent Substances 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 230000003960 inflammatory cascade Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 229960000598 infliximab Drugs 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000012966 insertion method Methods 0.000 description 1
- 230000008776 intercellular pathway Effects 0.000 description 1
- 229960004461 interferon beta-1a Drugs 0.000 description 1
- 229960003161 interferon beta-1b Drugs 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 229960001388 interferon-beta Drugs 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 230000026045 iodination Effects 0.000 description 1
- 238000006192 iodination reaction Methods 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- 229960003299 ketamine Drugs 0.000 description 1
- 229960004577 laquinimod Drugs 0.000 description 1
- GKWPCEFFIHSJOE-UHFFFAOYSA-N laquinimod Chemical compound OC=1C2=C(Cl)C=CC=C2N(C)C(=O)C=1C(=O)N(CC)C1=CC=CC=C1 GKWPCEFFIHSJOE-UHFFFAOYSA-N 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 229960000681 leflunomide Drugs 0.000 description 1
- VHOGYURTWQBHIL-UHFFFAOYSA-N leflunomide Chemical compound O1N=CC(C(=O)NC=2C=CC(=CC=2)C(F)(F)F)=C1C VHOGYURTWQBHIL-UHFFFAOYSA-N 0.000 description 1
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 description 1
- 229940039781 leptin Drugs 0.000 description 1
- XMGQYMWWDOXHJM-UHFFFAOYSA-N limonene Chemical compound CC(=C)C1CCC(C)=CC1 XMGQYMWWDOXHJM-UHFFFAOYSA-N 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 150000002690 malonic acid derivatives Chemical class 0.000 description 1
- 238000013411 master cell bank Methods 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- BUGYDGFZZOZRHP-UHFFFAOYSA-N memantine Chemical compound C1C(C2)CC3(C)CC1(C)CC2(N)C3 BUGYDGFZZOZRHP-UHFFFAOYSA-N 0.000 description 1
- 229960004640 memantine Drugs 0.000 description 1
- 230000008384 membrane barrier Effects 0.000 description 1
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 1
- 229960001428 mercaptopurine Drugs 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- LSDPWZHWYPCBBB-UHFFFAOYSA-O methylsulfide anion Chemical compound [SH2+]C LSDPWZHWYPCBBB-UHFFFAOYSA-O 0.000 description 1
- HPNSFSBZBAHARI-UHFFFAOYSA-N micophenolic acid Natural products OC1=C(CC=C(C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-UHFFFAOYSA-N 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- DYKFCLLONBREIL-KVUCHLLUSA-N minocycline Chemical compound C([C@H]1C2)C3=C(N(C)C)C=CC(O)=C3C(=O)C1=C(O)[C@@]1(O)[C@@H]2[C@H](N(C)C)C(O)=C(C(N)=O)C1=O DYKFCLLONBREIL-KVUCHLLUSA-N 0.000 description 1
- 229960004023 minocycline Drugs 0.000 description 1
- 210000003470 mitochondria Anatomy 0.000 description 1
- 229960001156 mitoxantrone Drugs 0.000 description 1
- 108091005601 modified peptides Proteins 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 210000002161 motor neuron Anatomy 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 229940014456 mycophenolate Drugs 0.000 description 1
- HPNSFSBZBAHARI-RUDMXATFSA-N mycophenolic acid Chemical compound OC1=C(C\C=C(/C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-RUDMXATFSA-N 0.000 description 1
- VMGAPWLDMVPYIA-HIDZBRGKSA-N n'-amino-n-iminomethanimidamide Chemical compound N\N=C\N=N VMGAPWLDMVPYIA-HIDZBRGKSA-N 0.000 description 1
- VYNKVNDKAOGAAQ-RUZDIDTESA-N n-[(1r)-2-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]-2-oxo-1-phenylethyl]-1h-indole-6-carboxamide Chemical compound C1CN(C)CCC1N1CCN(C(=O)[C@H](NC(=O)C=2C=C3NC=CC3=CC=2)C=2C=CC=CC=2)CC1 VYNKVNDKAOGAAQ-RUZDIDTESA-N 0.000 description 1
- 229960003086 naltrexone Drugs 0.000 description 1
- DQCKKXVULJGBQN-XFWGSAIBSA-N naltrexone Chemical compound N1([C@@H]2CC3=CC=C(C=4O[C@@H]5[C@](C3=4)([C@]2(CCC5=O)O)CC1)O)CC1CC1 DQCKKXVULJGBQN-XFWGSAIBSA-N 0.000 description 1
- 208000010753 nasal discharge Diseases 0.000 description 1
- 229940037525 nasal preparations Drugs 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 101150091879 neo gene Proteins 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 208000004296 neuralgia Diseases 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 208000021722 neuropathic pain Diseases 0.000 description 1
- 230000007171 neuropathology Effects 0.000 description 1
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 1
- 238000001821 nucleic acid purification Methods 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 239000007968 orange flavor Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- PFGVNLZDWRZPJW-OPAMFIHVSA-N otamixaban Chemical compound C([C@@H](C(=O)OC)[C@@H](C)NC(=O)C=1C=CC(=CC=1)C=1C=C[N+]([O-])=CC=1)C1=CC=CC(C(N)=N)=C1 PFGVNLZDWRZPJW-OPAMFIHVSA-N 0.000 description 1
- 229950009478 otamixaban Drugs 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 230000036407 pain Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 239000008196 pharmacological composition Substances 0.000 description 1
- 229960003742 phenol Drugs 0.000 description 1
- 150000008298 phosphoramidates Chemical class 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 102000054765 polymorphisms of proteins Human genes 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 238000011045 prefiltration Methods 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 230000004952 protein activity Effects 0.000 description 1
- 108020001580 protein domains Proteins 0.000 description 1
- 230000004853 protein function Effects 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 108010045647 puromycin N-acetyltransferase Proteins 0.000 description 1
- 239000002510 pyrogen Substances 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 229960000160 recombinant therapeutic protein Drugs 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- BOLDJAUMGUJJKM-LSDHHAIUSA-N renifolin D Natural products CC(=C)[C@@H]1Cc2c(O)c(O)ccc2[C@H]1CC(=O)c3ccc(O)cc3O BOLDJAUMGUJJKM-LSDHHAIUSA-N 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 235000021283 resveratrol Nutrition 0.000 description 1
- 229940016667 resveratrol Drugs 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 239000002342 ribonucleoside Substances 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- KGFYHTZWPPHNLQ-AWEZNQCLSA-N rivaroxaban Chemical compound S1C(Cl)=CC=C1C(=O)NC[C@@H]1OC(=O)N(C=2C=CC(=CC=2)N2C(COCC2)=O)C1 KGFYHTZWPPHNLQ-AWEZNQCLSA-N 0.000 description 1
- 229960001148 rivaroxaban Drugs 0.000 description 1
- 229960004136 rivastigmine Drugs 0.000 description 1
- 229960000371 rofecoxib Drugs 0.000 description 1
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 238000010845 search algorithm Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 235000016491 selenocysteine Nutrition 0.000 description 1
- ZKZBPNGNEQAJSX-UHFFFAOYSA-N selenocysteine Natural products [SeH]CC(N)C(O)=O ZKZBPNGNEQAJSX-UHFFFAOYSA-N 0.000 description 1
- 229940055619 selenocysteine Drugs 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 238000001542 size-exclusion chromatography Methods 0.000 description 1
- 210000003625 skull Anatomy 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000005063 solubilization Methods 0.000 description 1
- 230000007928 solubilization Effects 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000003153 stable transfection Methods 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 230000005477 standard model Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229960005202 streptokinase Drugs 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- NCEXYHBECQHGNR-QZQOTICOSA-N sulfasalazine Chemical compound C1=C(O)C(C(=O)O)=CC(\N=N\C=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-QZQOTICOSA-N 0.000 description 1
- 229960001940 sulfasalazine Drugs 0.000 description 1
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 229960001685 tacrine Drugs 0.000 description 1
- YLJREFDVOIBQDA-UHFFFAOYSA-N tacrine Chemical compound C1=CC=C2C(N)=C(CCCC3)C3=NC2=C1 YLJREFDVOIBQDA-UHFFFAOYSA-N 0.000 description 1
- 229960001967 tacrolimus Drugs 0.000 description 1
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 1
- 229960000235 temsirolimus Drugs 0.000 description 1
- QFJCIRLUMZQUOT-UHFFFAOYSA-N temsirolimus Natural products C1CC(O)C(OC)CC1CC(C)C1OC(=O)C2CCCCN2C(=O)C(=O)C(O)(O2)C(C)CCC2CC(OC)C(C)=CC=CC=CC(C)CC(C)C(=O)C(OC)C(O)C(C)=CC(C)C(=O)C1 QFJCIRLUMZQUOT-UHFFFAOYSA-N 0.000 description 1
- 229960000278 theophylline Drugs 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 229960000103 thrombolytic agent Drugs 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 229960005001 ticlopidine Drugs 0.000 description 1
- PHWBOXQYWZNQIN-UHFFFAOYSA-N ticlopidine Chemical compound ClC1=CC=CC=C1CN1CC(C=CS2)=C2CC1 PHWBOXQYWZNQIN-UHFFFAOYSA-N 0.000 description 1
- 210000001578 tight junction Anatomy 0.000 description 1
- 229960005062 tinzaparin Drugs 0.000 description 1
- 229960000187 tissue plasminogen activator Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 230000005030 transcription termination Effects 0.000 description 1
- 230000031998 transcytosis Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 239000012581 transferrin Substances 0.000 description 1
- 230000010474 transient expression Effects 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 230000001650 transport into the brain Effects 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- 229960005294 triamcinolone Drugs 0.000 description 1
- GFNANZIMVAIWHM-OBYCQNJPSA-N triamcinolone Chemical compound O=C1C=C[C@]2(C)[C@@]3(F)[C@@H](O)C[C@](C)([C@@]([C@H](O)C4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 GFNANZIMVAIWHM-OBYCQNJPSA-N 0.000 description 1
- 238000009966 trimming Methods 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- 235000011178 triphosphate Nutrition 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 1
- 229940079023 tysabri Drugs 0.000 description 1
- 238000012036 ultra high throughput screening Methods 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 150000003673 urethanes Chemical class 0.000 description 1
- 210000003708 urethra Anatomy 0.000 description 1
- 229960005356 urokinase Drugs 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 229960002004 valdecoxib Drugs 0.000 description 1
- LNPDTQAFDNKSHK-UHFFFAOYSA-N valdecoxib Chemical compound CC=1ON=C(C=2C=CC=CC=2)C=1C1=CC=C(S(N)(=O)=O)C=C1 LNPDTQAFDNKSHK-UHFFFAOYSA-N 0.000 description 1
- 108700026220 vif Genes Proteins 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 235000012431 wafers Nutrition 0.000 description 1
- 239000009637 wintergreen oil Substances 0.000 description 1
- ZXIBCJHYVWYIKI-PZJWPPBQSA-N ximelagatran Chemical compound C1([C@@H](NCC(=O)OCC)C(=O)N2[C@@H](CC2)C(=O)NCC=2C=CC(=CC=2)C(\N)=N\O)CCCCC1 ZXIBCJHYVWYIKI-PZJWPPBQSA-N 0.000 description 1
- 229960001522 ximelagatran Drugs 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2869—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against hormone receptors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/6425—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the peptide or protein in the drug conjugate being a receptor, e.g. CD4, a cell surface antigen, i.e. not a peptide ligand targeting the antigen, or a cell surface determinant, i.e. a part of the surface of a cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6865—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from skin, nerves or brain cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70578—NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/32—Fusion polypeptide fusions with soluble part of a cell surface receptor, "decoy receptors"
Description
本願は、2009年3月18日出願の米国仮出願第61/161,320号(出典明示により全体として本明細書の一部とする)の利益を請求する。
腫瘍壊死因子受容体(TNFR)などの標的受容体の可溶性細胞外ドメイン(ECD)は、ヒトの疾患において治療作用を有する。受容体ECDは、内因性リガンド、例えば、腫瘍壊死因子(TNF)−αを封鎖し、それにより、内因性リガンドの内因性標的受容体へのアクセスを遮断する外因性デコイ(decoy)受容体として作用する。デコイ受容体は、脳疾患の強力な新規治療となる可能性があった。しかしながら、デコイ受容体は、他の巨大分子薬物のように、血液脳関門(BBB)を横断しない。かくして、今日までに、組み換えデコイ受容体の全身投与によって脳障害患者を治療することはできなかった。
本明細書には、BBBを横断してIgG−受容体ECD(デコイ受容体)融合タンパク質を対象のCNSへ送達するための組成物および関連する方法が記載される。特に、該方法は、受容体ECDおよびBBBの表面に発現される受容体の細胞外ドメインに結合する抗体を含む二官能性デコイ受容体融合抗体の治療上有効量を全身投与することによって、デコイ受容体のCNSへの送達を可能にする。
(ii)受容体細胞外ドメインに融合した免疫グロブリン軽鎖、および免疫グロブリン重鎖の両方
をコードする単一タンデム発現ベクターを真核細胞中に安定に組み込むことを含む、二官能性デコイ受容体融合抗体を製造する方法であって、該コードされた免疫グロブリン重鎖および免疫グロブリン軽鎖がBBB上に発現された受容体に対する抗体由来であるところの方法が提供される。いくつかの具体例において、該BBB上に発現された受容体は、インスリン受容体、トランスフェリン受容体、インスリン様成長因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体である。いくつかの具体例において、該コードされた受容体細胞外ドメインは、TNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン受容体由来である。いくつかの具体例において、該TNF−α受容体由来の受容体細胞外ドメインは、免疫グロブリン重鎖または免疫グロブリン軽鎖のカルボキシル末端に共有結合される。いくつかの具体例において、該TNF−α受容体由来のコードされた受容体細胞外ドメインは、免疫グロブリン重鎖のカルボキシル末端に共有結合される。
本明細書に挙げられた全ての出版物、特許、および特許出願は、出典明示により、あたかも個々の出版物、特許または特許出願が詳細かつ個々に出典明示により本明細書の一部とされることが示されたかの如く、同程度まで本明細書の一部とされる。
本発明の新規な特徴は、特に、添付の特許請求の範囲で示される。本発明の特徴および利益のより良い理解は、発明の本質を利用する実例となる具体例を示す下記の詳細な説明、および添付の図面を参照して得られるであろう。
I.序文
II.いくつかの定義
III.血液脳関門
IV.BBBを横断する輸送のためのデコイ受容体融合抗体
V.組成物
VI.核酸、ベクター、細胞および製造
VII.方法
VIII.実施例
IX.配列
AA アミノ酸
BBB 血液脳関門
BCA ビシンコニン酸
BGH ウシ成長ホルモン
CDR 相補性決定領域
CHO チャイニーズハムスター卵巣
CMV サイトメガロウイルス
DC 希釈クローニング
DHFR ジヒドロ葉酸還元酵素
ECD 細胞外ドメイン
ED50 50%飽和をもたらす有効用量
FR フレームワーク領域
FS フランキング領域
FWD 順方向
HC 重鎖
HIR ヒトインスリン受容体
HIRMAb HIRに対するMAb
HIRMAb HC HIRMAbの重鎖
HIRMAb LC HIRMAbの軽鎖
HIRMAb−TNFR HIRMAbおよびTNFR ECDの融合タンパク質(ここに、TNFRがHCカルボキシル末端に融合する)
HT ヒポキサンチン−チミジン
IgG 免疫グロブリンG
IGF インスリン様成長因子
LC 軽鎖
MAb モノクローナル抗体
MAH マウス抗−ヒトIgG
MTX メトトレキサート
MW 分子量
N アスパラギン
nt ヌクレオチド
ODN オリゴデオキシヌクレオチド
orf オープンリーディングフレーム
pA ポリ−アデニル化
PAGE ポリアクリルアミドゲル電気泳動
PBS リン酸緩衝化セーライン
PBST PBSおよびTween−20
PCR ポリメラーゼ連鎖反応
pI 等電点
R 受容体
REV 逆方向
RNase A リボヌクレアーゼA
RT 逆転写
RT 室温
SDM 部位特異的変異誘発
SDS ドデシル硫酸ナトリウム
SEC サイズ排除クロマトグラフィー
Ser セリン
SFM 無血清培地
TH トロイの木馬
TNF 腫瘍壊死因子
TNFR TNF受容体
TV タンデムベクター
UTV ユニバーサルTV
VH 重鎖の可変領域
VL 軽鎖の可変領域
遺伝子操作されたデコイ受容体は、特に受容体ECDがヒト免疫グロブリンG、例えばIgG1のFcフラグメントのアミノ末端に融合される場合、強力な新規治療剤である。Fcフラグメントは、2つの定常領域鎖からなる二量体タンパク質である。ほとんどの受容体は膜内で二量体を形成するので、受容体ECDのFcフラグメントへの融合により、受容体タンパク質の天然二量体コンフィギュレーションが可能となる。デコイ受容体のよく記載される一例は、TNFαデコイ受容体−Fc融合タンパク質である。TNFαデコイ受容体−Fc融合タンパク質は、プロ炎症性サイトカイン、TNFαを封鎖し、それにより、その内因性リガンドによる内因性TNFRの活性化を阻害する能力のために、末梢性炎症疾患の強力な生物学的治療剤である。しかしながら、TNFR:Fc融合タンパク質は、CNS疾患のために処方することはできない。
「抗体」なる語は、天然または部分合成もしくは全合成免疫グロブリンをいう。該用語は、また、抗原結合ドメインである結合ドメインまたは抗原結合ドメインに相同性の結合ドメインを有するいずれかのポリペプチドまたはタンパク質を包含する。CDR移植(grafted)抗体もまた、該用語によって意図される。
BBBは、脳および脊髄の毛細管を形成する内皮細胞を一緒に固める密着な結合によって形成される(Pardridge, 2008, Bioconj Chem, 19: 1327−1338)。ヒトの脳において、400マイルの脳毛細管が存在する。BBBをイン・ビボで形成する脳毛細管内皮原形質膜を横断する電気抵抗は、いずれの生物膜と同様に高い。血液と器官との間の遊離溶質交換のための通常の細胞間隙および細胞間経路は、CNSには存在しない。結果的に、血液中の薬物は、2つのメカニズム、すなわち、(i)小型分子の高い脂溶性のための自由拡散、および(ii)内因性BBBトランスポーターを介する輸送のうちの1つだけを介して脳にアクセスすることができる。デコイ受容体組成物のためのBBB薬物送達問題の解決に対する1のアプローチは、BBB内のある特定の内因性輸送システムにアクセスできるように、デコイ受容体を再操作することである。本明細書に記載の方法は、本明細書に記載のデコイ受容体融合抗体組成物の全身投与後、機能的デコイ受容体が末梢血からCNS中へBBBを横断できるようにする。本明細書中に記載の方法は、BBB上の表面に発現された発現受容体(例えば、ヒトインスリン受容体)を利用して、所望の二官能性受容体ECD−BBB受容体融合抗体を末梢血からCNS中へ輸送する。
一の態様において、本発明は、重鎖免疫グロブリンまたは軽鎖免疫グロブリンのアミノ酸配列に共有結合した受容体ECD(例えば、ヒトTNF−α受容体ECD)のアミノ酸配列を含有する二官能性デコイ受容体融合抗体を利用する組成物および方法を提供する。かかる二官能性デコイ受容体融合抗体は、BBB上に発現された受容体および該受容体ECDのリガンドに結合することができる。該組成物および方法は、BBBを横断して末梢血からCNS中へデコイ受容体を輸送するのに有用である。
顕著なことには、本明細書に記載の二官能性デコイ受容体融合抗体は、高い割合で、それらの分離した構成タンパク質の活性、すなわち、BBB受容体AbのBBB受容体、例えば、ヒトインスリン受容体ECDに対する結合、およびデコイ受容体ECD(例えば、TNF−α受容体)の同族(cognate)リガンドに対する結合を保持する。
デコイ受容体−BBB受容体Ab融合抗体のBBBを横断する輸送は、標準的な方法によってBBB受容体Abを単独でBBBを横断して輸送する場合と比較してもよい。例えば、動物モデル、例えば、非ヒト霊長類のような哺乳動物によるデコイ受容体−BBB受容体Ab融合抗体の薬物動力学および脳への取り込みを用いてもよい。同様に、デコイ受容体リガンド結合を決定するための標準的なモデル(例えば、ELISA)を用いて、デコイ受容体ECD単独の機能およびデコイ受容体−BBB受容体Ab融合抗体の一部としての機能を比較してもよい。例えば、TNFαのHIRMAb−TNF−デコイ受容体融合タンパク質に対する結合 対 TNF受容体(TNFR)−II:ヒトIgG1 Fc融合タンパク質(TNFR:Fcと称する)に対する結合を明らかにする実施例4を参照のこと。BBB受容体に関する結合アフィニティーをまた、デコイ受容体−BBB受容体Ab融合抗体 対 BBB受容体Ab単独に関して比較することができる。例えば、実施例4を参照のこと。
本発明は、また、核酸、ベクター、細胞、および製造方法を提供する。いくつかの具体例において、本発明は、本明細書に記載のポリペプチドをコードする核酸、例えば、(i)重鎖免疫グロブリンおよび該重鎖免疫グロブリンとフレーム内の受容体細胞外ドメインをコードする第1の配列、(ii)軽鎖免疫グロブリンおよび該軽鎖免疫グロブリンとフレーム内の受容体細胞外ドメインをコードする第2の配列、または(iii)(i)または(ii)の相補性配列を含む核酸を提供する。該上記の核酸によってコードされる重鎖および軽鎖免疫グロブリンは、BBB受容体、例えば、ヒトインスリン受容体、トランスフェリン受容体、インスリン様成長因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体に対する抗体由来である。いくつかの場合、該コードされる受容体ECDは、TNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン受容体由来である。いくつかの場合、該コードされる受容体のアミノ酸配列は、外来受容体の一つ由来のECDのアミノ酸配列に対し、少なくとも約80%、85%、90%、95%、または少なくとも約80%〜約100%のうちの他のパーセント同一である。いくつかの場合、該核酸は、ヒト、マウス、ラット、またはブタTNF−α受容体の細胞外ドメインに対し、少なくとも約80%、85%、90%、95%、または少なくとも約80%〜約100%のうちの他のパーセント同一のアミノ酸配列を含むECDをコードする。いくつかの具体例において、第1の配列は、配列番号4または7に相当するアミノ酸配列に対し、少なくとも約80%、85%、90%、95%、または少なくとも約80%〜約100%のうちの他のパーセント同一のアミノ酸配列をコードする。他の具体例において、第2の配列は、配列番号6に相当するアミノ酸配列に対し、少なくとも約80%、85%、90%、95%、または少なくとも約80%〜約100%のうちの他のパーセント同一のアミノ酸配列をコードする。
本明細書に記載のデコイ受容体−BBB受容体Ab融合抗体のいずれかを全身投与することによって、デコイ受容体をBBBを横断して送達するための方法が本明細書中に記載される。いくつかの具体例において、受容体細胞外ドメインのアミノ酸配列に共有結合した重鎖免疫グロブリンまたは軽鎖免疫グロブリンのアミノ酸配列を含む二官能性デコイ受容体融合抗体であって、BBB上に発現された受容体および該受容体細胞外ドメインのリガンドに結合する該融合抗体を含む医薬組成物を対象に全身投与することによって、CNS疾患を治療するために、本明細書に記載の組成物を投与する。いくつかの場合、治療されるべきCNS疾患は、急性CNS疾患、例えば、局所脳虚血、全脳虚血、外傷性脳損傷、または脊髄損傷である。いくつかの場合、治療されるべきCNS疾患は、慢性CNS疾患である。いくつかの具体例において、慢性CNS疾患は、神経変性CNS疾患、例えば、アルツハイマー病、パーキンソン病、筋萎縮性側索硬化症、ハンチントン病、多発性硬化症、横断性脊髄炎、運動ニューロン疾患、ピック病、結節硬化症、カナバン病、レット症候群、脊髄小脳失調症、フリードライヒ失調症、視神経萎縮、または網膜変性である。
インスリン様成長お因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体に対する抗体を含有し、該デコイ受容体は、TNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン受容体由来のECDを含有する。いくつかの具体例において、投与されるべき該デコイ受容体−BBB受容体Ab融合抗体は、TNF−α受容体−ヒトインスリン受容体Ab融合抗体である。
対象が自己免疫、炎症疾患、または神経系に影響を及ぼすアレルギー疾患(例えば、Allanら(2003), Philos Trans R Soc Lond B Biol Sci, 358(1438):1669−1677参照)に罹患しているか、または罹患する危険性がある場合、本明細書に記載のデコイ受容体−BBB受容体Ab融合抗体(例えば、TNF−α受容体ECD−BBB受容体Ab融合抗体)をいずれかの組合せにおいて1以上の下記の治療剤、すなわち、免疫抑制剤(例えば、タクロリマス(tacrolimus)、シクロスポリン(cyclosporin)、ラパマイシン(rapamicin)、メトトレキサート(methotrexate)、シクロホスファミド(cyclophosphamide)、アザチオプリン(azathioprine)、メルカプトウリン(mercaptopurine)、マイコフェノラート(mycophenolate)、またはFTY720)、グルココルチコイド(例えば、プレドニソン、コルチゾンアセテート、プレドニソロン、メチルプレドニソロン、デクサメタゾン、ベータメタゾン、トリアムシノロン(triamcinolone)、ベクロメタゾン、フルドロコルチゾンアセテート、デオキシコルチコステロンアセテート、アルドステロン)、非スイテロイド性抗炎症薬(例えば、サリチル酸塩、アリールアルカン酸、2−アリールプロピオン酸、N−アリールアントラニル酸、オキシカム、コキシブ(coxibs)、またはスルホンアニリド)、Cox−2−特異的阻害剤(例えば、バルデコキシブ(valdecoxib)、セレコキシブ(celecoxib)、またはロフェコキシブ(rofecoxib))、レフルノミド(leflunomide)、金チオグルコース、金チオマレート、オーロフィン(aurofin)、スルファザラジン(sulfasalazine)、ヒドロキシクロロキニン、ミノサイクリン、TNF−α結合タンパク質(例えば、インフリキシマブ(infliximab)、エタネルセプト(etanercept)、またはアダリムマブ(adalimumab))、アバタセプト(abatacept)、アナキンラ(anakinra)、インターフェロン−β、インターフェロン−γ、インターロイキン−2、アレルギーワクチン、抗ヒスタミン、抗ロイコトリエン、ベータ−アゴニスト、テオフィリン、または抗コリン作用剤と一緒に使用することができる。
対象が多発性硬化症に罹患しているか、または罹患する危険性がある場合、本明細書に記載のデコイ受容体−BBB受容体Ab融合抗体(例えば、インターロイキン(IL)−6デコイ受容体ECD−BBB受容体Ab融合抗体)をいずれかの組合せにおいて1以上の下記の例示的多発性硬化症治療剤、すなわち、インターフェロンβ−1a、インターフェロンβ−1b、グラチラマーアセテート(CopaxoneR(登録商標))、ミトキサントロン(NovantroneR)、低用量ナルトレキソン、ナタリズマブ(Natalizumab)(TysabriR)、SativexR、エイムスプロ(Aimspro)(ヤギ血清)、トリメスタ(Trimesta)(経口エストリオール)、ラキニモド(Laquinimod)、FTY720(フィンゴリモド(Fingolimod))、MBP8298、NeuroVaxR、TovaxinR、レビムン(Revimmune)、CHR−1103、BHT−3009、BG−12、クラドリビン(Cladribine)、ダクリズマブ(daclizumab)(Zenapax)リツキシマブ(Rituximab)(Rituxan)、シクロホスファミド、キャンパス(Campath)、ファムプリジン(Fampridine)−SR、MN−166、テムシロリマス(Temsirolimus)、またはRPI−78Mと一緒に使用することができる。
対象が認知症に罹患しているか、または罹患する危険性がある場合、本明細書に記載のデコイ受容体−BBB受容体Ab融合抗体(例えば、TNF関連アポトーシス誘導性リガンド受容体(TRAIL−R)ECD−BBB受容体Ab融合抗体)をいずれかの組合せにおいて認知症を治療するための1以上の薬剤または方法と一緒に使用することができる。認知症を治療するための治療剤/治療の例は、限定するものではないが、FlurizanTM(登録商標)(MPC−7869,r フルルビプロフェン(r flurbiprofen))、メマンチン(memantine)、ガラタミン(galantamine)、リバスチグミン(rivastigmine)、ドネジピル(donezipil)、タクリン(tacrine)、Aβ1−42免疫療法、レスベラトロール(resveratrol)、(−)−エピガロカテキン−3−ガラート、スタチン、ビタミンC、またはビタミンEを包含する。
対象が血栓塞栓性障害(例えば、卒中)に罹患しているか、または罹患する危険性がある場合、1以上の他の抗血栓塞栓剤とのいずれかの組合せにおいて、本明細書に記載のデコイ受容体−BBB受容体Ab融合抗体(例えば、アポトーシスのTNF様弱インデューサー(TWEAK)受容体デコイECD−BBB受容体Ab融合抗体)を用いて該対象を治療することができる。抗血栓塞栓剤の例は、限定するものではないが、血栓溶解剤(例えば、アルテプラーゼ、アニストレプラーゼ、ストレプトキナーゼ、ウロキナーゼ、または組織プラスミノーゲンアクチベーター)、ヘパリン、チンザパリン(tinzaparin)、ワーファリン(warfarin)、ダビガトラン(dabigatran)(例えば、ダビガトランエテキレート(dabigatran etexilate))、因子Xa阻害剤(例えば、フォンダパリヌクス(fondaparinux)、ドラパリヌクス(draparinux)、リバロキサバン(rivaroxaban)、DX−9065a、オタミキサバン(otamixaban)、LY517717、またはYM150)、チクロピジン(ticlopidine)、クロピドグレル(clopidogrel)、CS−747(プラスグレル(prasugrel),LY640315)、キシメラガトラン(ximelagatran)、またはBIBR 1048を包含する。
NP 001057のアミノ酸23−257に対応するヒトTNFR−II細胞外ドメイン(ECD)を、表2に記載のオリゴデオキシヌクレオチド(ODNs)を用いるポリメラーゼ連鎖反応(PCR)によってクローン化し、ヒトU87グリア細胞から単離したポリA+RNAの逆転写からcDNAを得た。該TNFR cDNAを、25ng ポリA+RNA−由来のcDNA、0.2μM 順方向および逆方向ODNプライマー(表Iの各々、配列番号1および配列番号2)、0.2mM デオキシヌクレオシドトリホスフェート、および50μl Pfuバッファー中の2.5U PfuUltra DNAポリメラーゼを用いるPCRによってクローン化した。Mastercycler温度サイクラー中、95℃で2分間の開始変性工程、次いで、95℃で30秒間の変性を30サイクル、55℃で30秒間のアニーリング工程、および72℃で1分間の増幅工程を用いて増幅を行い、次いで、72℃で10分間、最終インキュベーションを行った。PCR産物を0.8%アガロースゲル電気泳動中で分析し、ヒトTNFR cDNAに対応する〜0.6kbの予想される主要単一バンドを生じた(図2A)。TNFR ECDのアミノ酸配列は、クローン化したTFR ECD cDNAのヌクレオチド配列から推定し、Leu23−Asp257を含んでいた(NP 001057)。
重鎖(HC)およびTNFR ECDの融合タンパク質を発現する発現プラスミドをpCD−HIRMAb−TNFRと称する。ヒトTNFR−II ECD(NP 001057)のアミノ酸Leu23−Asp257に対応する成熟ヒトTNFR cDNAを該pCD−HIRMAb−HC発現プラスミド(図2B)のHpaI部位に挿入することによって該プラスミドを操作して、pCD−HIRMAb−TNFRを製造した(図2B)。該pCD−HIRMAb−HCプラスミドは、キメラHIRMAbのHCをコードし、該プラスミドおよび軽鎖(LC)発現プラスミドpHIRMAb−LCを用いるCOS細胞のデュアルトランスフェクションにより、キメラHIRMAbの一過性発現を可能にする。TNFR順方向(FWD)PCRプライマー(表I)は、「CA」ヌクレオチドを導入して、オープンリーディングフレームを維持し、かつ、HIRMAb HCのCH3領域のカルボキシル末端とそのシグナルペプチドを差し引いたTNFR ECDのアミノ末端との間に、Ser−Ser−Serリンカーを導入する。該TNFRモノマーの各HCのカルボキシル末端への融合は、図1に示される。該設計は、該TNFRを、TNFR ECDの好ましいコンフォメーションである二量体コンフィギュレーションに立体的に限定し、受容体ダイマーとして結晶化する(Chanら(2000), Immunity, 13:419−422)。該TNFR逆方向(REV)PCRプライマー(表I)は、TNFR ECDタンパク質の末端のアスパラギン酸の直後に、終止コドン「TGA」を導入する。該操作されたpCD−HIRMAb−TNFR発現ベクターは、DNA配列決定によって確認された。
COS細胞は、μg DNA:uL リポフェクタミンの比率1:2.5でリポフェクタミン2000を用いて、pCD−HIRMAb−LCおよびpCD−HIRMAb−TNFR(ここに、pCD−HIRMAb−LCは、HIRMAb−TNFR融合タンパク質中に組み込まれた同じ軽鎖であるキメラHIRMAbの軽鎖をコードする発現プラスミドである)でデュアルトランスフェクトした。トランスフェクション後、該細胞を無血清培地中で培養した。COS細胞を最初、ヒトIgG特異的ELISAで発現をスクリーニングするために、6ウェルクラスター皿に播種した。次いで、10xT500フラスコ中、トランスフェクトしたCOS細胞の培養のために、該トランスフェクションをスケールアップした。馴化した無血清培地を3日目および7日目に収集した。該融合タンパク質をタンパク質Aアフィニティークロマトグラフィーによって精製した。
本発明の作業において、デコイ受容体のアミノ末端は、IgG鎖のカルボキシル末端に融合される。予想外にも、該コンフィギュレーションは、二官能性デコイ受容体−BBB受容体Ab融合抗体を生じた。
ヒトWEHI−13VAR細胞(CRL−2148)をAmerican Type Culture Collection(Manassas,VA)から得、TNFα細胞毒性のバイオアッセイとして用いた(Espevik and Nissen−Meyer, (1986), J. Immunol. Methods, 95:99−105)。該細胞を24ウェルクラスター皿に、10%胎仔ウシ血清(FBS)を含有するRPMI−1640培地中300,000細胞/ウェルで播種した。一晩培養後、該培地の半分を吸引除去し、200μlの新鮮なRPMI−1640培地、50μl/ウェルの10μg/mLのアクチノマイシンD(最終濃度=1.0μg/mL)、および最終濃度が1〜100pg/mLのヒト組み換えTNFαで置き換えた。いくつかのウェルにおいて、TNFαをウェルに加える前の30分間、TNFαを組み換えTNFR:Fc、またはHIRMAb−TNFR融合タンパク質に複合体化させた。該TNFR:FcまたはHIRMAb−TNFR融合タンパク質の最終濃度は、1.4nMであった。加湿インキュべーター中、37℃で一晩(20時間)インキュベーション後、該培地にチアゾイルブルーテトラゾリウムブロミド(MTT)を最終濃度0.5mg/mLまで補足した。37℃で3時間インキュベーション後、可溶化溶液(48%イソプロパノール、2% 1N HCl)の添加によって、該反応を停止した。570nmおよび650nmでの吸光度を測定し、A570−A650差をコンピューターで計算した。MTTは、健康細胞中のミトコンドリアによって、ホルマザン結晶に酸化され、該反応は、細胞の生存に反比例する。アクチノマイシンDの不在下で、該TNFαは、1−100pg/mL濃度にて、細胞に対して毒性ではなかった。しかしながら、アクチノマイシンDの存在下で、TNFαのこれらの濃度は、ED50値 5−10pg/mLヒトTNFαを伴う用量依存性細胞毒を生じた(図8)。しかしながら、該TNFαの細胞毒効果は、1.4nM濃度のTNFR:Fc融合タンパク質またはHIRMAb−TNFR融合タンパク質と共に該サイトカインを共インキュベーションすることによって遮断された(図8)。これは、該TNFRデコイ受容体がHIRMAbのカルボキシル末端への融合にかかわらず、生物学的に活性であることを示す。
ヒトU87グリア細胞からクローン化された該デコイ受容体の235AA TNFR配列(AA465〜699,配列番号4)内に、174および210位置に多形が存在する。該HIRMAb−TNFR重鎖(配列番号4)の638位置のアルギニン(Arg)は、235AA TNFR ECDのArg−174に対応する。メチオニン(Met)が該ヒトTNFR配列(GenBank AAA36755)の174位置に見出されるので、該Arg−174は天然のR174M多形である。R638M部位特異的変異誘発(SDM)を周知の方法によって実施でき、配列番号7に示されるように、Arg−638をMet−638に変換する。該HIRMAb−TNFR重鎖(配列番号4)の674位置のリジン(Lys)は、235AA TNFR ECDのLys−210に対応する。該ヒトTNFR配列(GenBank AAA36755)のグルタミン酸(Glu)が210位置に見出されるので、該Lys−210は天然のK210E多形である。K674E部位特異的変異誘発(SDM)を周知の方法によって実施でき、配列番号7に示されるように、Lys−674をGlu−674に変換する。pCD−HIRMAb−TNFR発現ベクターのTNFR−R638M多形(配列番号7)での操作は、周知の部位特異的変異誘発法を用いて、ヒトTNFR−R638M FWD(表3、配列番号8)およびヒトTNFR−R638M REV(表3、配列番号9)ODNプライマーを用いるSDMによって実施される。同様に、pCD−HIRMAb−TNFR発現ベクターのTNFR−K674E多形での操作は、ヒトTNFR−K674E FWD(表3、配列番号10)およびヒトTNFR−K674E REV(表3、配列番号11)ODNプライマーを用いるSDMによって実施される。
HIRMAb−TNFR融合タンパク質は、図1に示されるように、2つの重鎖(HC)および2つの軽鎖(LC)からなる。したがって、宿主細胞は、HC遺伝子およびLC遺伝子の両方で永続的にトランスフェクトされなければならない。さらに、宿主細胞は、トランス遺伝子挿入部位の周囲の増幅を有する細胞系統の単離を可能にする遺伝子で永続的にトランスフェクトされなければならない。これは、ジヒドロ葉酸還元酵素(DHFR)をコードしている遺伝子で宿主細胞をトランスフェクション後の、メトトレキサート(MTX)での細胞系統の選択を用いて達成される。したがって、最終的には製造のためのマスター・セル・バンク(Master Cell Bank)をもたらす単一細胞における3つの遺伝子全ての高産生を得る必要がある。3つの遺伝子全ての高い発現を保証するために、タンデムベクター(TV)と呼ばれる一片のDNAを図9に概説されるように操作した。pTV−HIRMAb−TNFRと称するHIRMAb−TNFR融合タンパク質のためのTVの遺伝子操作は、pTV−HIRMAbのHpaI部位へのTNFR ECD cDNAの挿入によって完了した。該TNFR ECD cDNAは、カスタムODNsおよびpCD−HIRMAb−TNFR(図2B)を鋳型として用いるPCRによって生成された。pTV−HIRMAbは、HIRMAb HCオープンリーディングフレームの3’末端に独特のHpaI制限酵部位を有するキメラHIRMAbをコードするタンデムベクターである。pTV−HIRMAbは、HIRMAb LCおよびHC遺伝子のタンデム発現カセットを含有し、各カセットは、イントロンを有するCMVプロモーターによって駆動し、各カセットは、ウシ成長ホルモン(BGH)ポリアデニル化(pA)配列によって終了する。pTV−HIRMAbは、また、ネズミジヒドロ葉酸還元酵素(DHFR)のための第3の発現カセットを含有し、それは、SV40プロモーターによって駆動し、B型肝炎ウイルス(HBV)pA配列によって終了する。HIRMAb−TNFR HC発現カセットは、イントロンを有するCMVプロモーター、9ntの全Kozak部位(GCCGCCACC)、2,100ntのHIRMAb HC−TNFR融合タンパク質オープンリーディングフレーム、およびBGH pA配列からなる。図9に示されるタンデムベクターによってコードされる699 AA HIRMAb−TNFR HCタンパク質は、配列番号4におけるものと同一であり、19アミノ酸IgGシグナルペプチド(AA1〜19、配列番号4)、442アミノ酸HIRMAb HC(AA20〜461、配列番号4)、3アミノ酸リンカー(Ser−Ser−Ser)、およびそのシグナルペプチドを差し引いた235アミノ酸ヒトTNFR−II ECD(AA465〜699、配列番号4)からなる。該重鎖融合タンパク質の予測分子量は、グリコシル化を差し引いて、73,900Daであり、予測等電点(pI)は8.45である。該融合タンパク質のTNFR ECD部分の推定アミノ酸配列は、22個のシステイン残基を含み、2個のN−結合コンセンサスグリコシル化部位をTNFR ECD内のAsn−149およびAsn−171に含んだ(配列番号4)。図9に記載のタンデムベクターによって産生されるHIRMAb−TNFR融合タンパク質は、2つの融合重鎖(AA20−699、配列番号4)および2つの軽鎖(LC)からなる。LC発現カセットは、イントロンを有するCMVプロモーター、9ntの全Kozak部位(GCCGCCACC)、705ntのHIRMAb LC融合タンパク質オープンリーディングフレーム、およびBGH pA配列を含む。図9に示されるタンデムベクターによってコードされる214AA HIRMAb−LCタンパク質は、配列番号6におけるものと同一であり、20アミノ酸IgGシグナルペプチド(AA1〜20、配列番号6)、および214アミノ酸HIRMAb LC(AA21〜234、配列番号6)からなる。
無血清培地(SFM)適応性DG44チャイニーズハムスター卵巣(CHO)細胞を、エレクトロポレーターを用いて、PvuIで線形化後の5μgのpTV−HIRMAb−TNFRでエレクトロポレーションした。5 x 106細胞を200μLのリン酸緩衝化セーライン(PBS)および0.2cmキュベット中、方形波および160ボルトを用いて、該DNAでエレクトロポレーションした。細胞をCHO無血清培地(SFM)中に懸濁し、4x96ウェルプレート中で培養した。安定なトランスフェクタントの選択は、エレクトロポレーションの2日後、0.54mg/ml G418を用いて開始した。トランスフェクトタントのコロニーが明らかになったとき、すなわち、21目に、ヒトIgG ELISAのために、上清のアリコートを採取した。陽性コロニーを単離し、さらなる特徴付のために個々に培養した。DG44細胞は、内因性DHFRを欠き、内因性葉酸合成に関して、栄養分、ヒポキサンチンおよびチミジン(HT)に依存する。該TVを有するトランスフェクト細胞は、外因性DHFRを発現する。トランスフェクト細胞系統は、さらに、HT−欠損培地中に置くことによって選択された。トランス遺伝子挿入部位周囲の増幅を有する系統は、細胞を、20nM MTXで開始する増加濃度のMTXに付すことによって選択された。80−160nM MTXにて細胞系統の安定化後、1ウェルあたり1細胞の限界希釈クローニング(DC)によって、高生産性クローンを単離し、DCの各ラウンドにて全部で4000個のウェルに播種し、高容量マイクロプレートディスペンサーおよびマイクロプレートウォッシャーを用いるヒトIgG ELISAを用いて、培地IgGを測定した。クローン化した細胞を、軌道振盪機上の125mLのプラスチック角瓶中、1−2百万細胞/mLの生存細胞密度にて増殖させ、IgG ELISAによる測定の場合、無血清培地中約10mg/LのヒトIgGレベルを生産した。
HIRMAbは、旧世界霊長類のインスリン受容体と交差反応するが、低級種のインスリン受容体を認識しないので、HIRMAb−TNFR融合タンパク質の脳浸透を成体アカゲザル(Rhesus monkey)において測定した。さらに、ヒトIgG1 Fc領域に融合した市販のTNFRデコイ受容体(TNFR:Fcと称する)をR&D Systemsから購入した。該TNFR:Fc融合タンパク質は、デコイ受容体融合タンパク質に関する当該分野の状況を示す。該TNFR:Fcは、いずれのBBB受容体に対しても特異性を示さず、BBBに浸透しないと予測される。しかしながら、該TNFR:Fc融合タンパク質のBBB輸送は、測定されたことがない。さらに、IgG分子がBBBを横断するという文献における証拠があり[Zlokovicら、A saturable mechanism for transport of immunoglobulin G across the blood−brain barrier of the guinea pig(モルモットの血液脳関門を横断する免疫グロブリンGの輸送のための飽和可能なメカニズム)、Exp. Neurol, 107, 263−270, 1990]、TNFR:Fc融合タンパク質は、ヒトIgG1の定常領域の大部分を含有するので、該タンパク質もまた、BBBを横断することを推測できた。脳への取り込み研究について、CHO−由来HIRMAb−TNFR融合タンパク質は、該TNFR:Fc融合タンパク質の非酸化的放射性ヨウ素化と平行して、トリチウム化された。該[3H]−HIRMAb−TNFRおよび[125I]−TNFR:Fc融合タンパク質を共に、アカゲザルに注射した。結果は、TNFR:Fc融合タンパク質はBBBを横断せず、BBB分子のトロイの木馬に融合後、TNFRの脳浸透における顕著な増加があることを実証する。また、霊長類の非脳器官における該融合タンパク質の取り込みを測定し、それは、該デコイ受容体のHIRMAbへの融合が該医薬のCNSに対する選択的標的化をもたらすことを示す。
器官PS積=[(%ID/g)/AUC]*1000
HIRMAb−TNFR融合タンパク質は、[3H]で放射能標識され、TNFR:Fc融合タンパク質は、[125I]で放射能標識され、これらのタンパク質を成体アカゲザルの静脈内に共注射した。血漿放射能のクリアランスを図12Aに示し、TCAにより沈澱性であった血漿放射能を図12Bに示す。PKパラメーターの概算のために、血漿クリアランスプロフィール(図12A)を双指数関数(Methods)にフィットさせ、それを各融合タンパク質につき、表4に示す。脳および末梢器官による該融合タンパク質の取り込みは、% I.D./100グラム組織として測定され、これらの値を表5に示す。該融合タンパク質の分布の脳体積(VD)は、毛細管除去(capillary depletion)法で測定され、ホモジネートについてのVD値、血管ペレット、および血管後上清を表6に示す。
該キメラHIRMAb HCの相補性決定領域(CDRs)およびフレームワーク領域(FR)を包含する該融合タンパク質のHCのドメイン構造を図10に示す。定常領域もまた、図10に示し、ヒトIgG1に由来する。CH1、ヒンジ、CH2、およびCH3ドメインを含むC領域のアミノ酸配列を図10に示す。キメラHIRMAb LCのCDRsおよびFRsを包含するLCのドメイン構造は、図11に示す。定常領域は、ヒトカッパLCに由来し、ヒトカッパ定常領域を含むアミノ酸配列を図11に示す。
腫瘍壊死因子(TNF)−αは、脳の急性および慢性障害において病原的役割を果たすプロ炎症性サイトカインである。TNF−αおよびTNFRのどちらも、脳虚血においてアップレギュレートされる(Lambertsenら(2007) Neurosci., 144:934−949)。TNFR細胞外ドメイン(ECD)の経頭蓋投与は、中大脳動脈閉塞(MCAO)モデルにおいて、梗塞のサイズを減少させる(Nawashiroら(1997), Brain Res., 778:265−271)。TNFR ECDは、血液脳関門(BBB)を横断しない大型分子なので、該可溶性デコイ受容体は、脳に直接注射しなければならない。脊髄損傷(SCI)において、ヒトIgG1 FcフラグメントおよびヒトTNFRタイプIIのECDの融合タンパク質のクモ膜下投与は、SCIに関連ずるニューロパシー疼痛を減少させる(Marchandら(2008), Eur. J. Pain, 1−12)。同様に、外傷性脳損傷(TBI)モデルにおけるTNFR−II:Fc融合タンパク質の経頭蓋投与は、治療的である(Knoblachら(1999), J. Neuroimmunol., 95:115−125)。しかしながら、TNFR:Fc融合タンパク質はBBBを横断しないので、TBIにおけるTNFR:Fc融合タンパク質の静脈内投与は、治療的ではない(Knoblachら(1999), J. Neuroimmunol., 95:115−125)。虚血または脳もしくは脊髄損傷などの急性脳障害のほかに、BBB輸送可能TNFR:Fc融合タンパク質の使用はまた、慢性神経変性においても治療的でありうる(Tweedieら(2007), Curr. Alzheimer Res., 4:375−378)。
デコイ血管内皮成長因子(VEGF)受容体(VEGF):Fc融合タンパク質は、操作し、発現させることができる(Holashら(2002), Proc. Natl. Acad. Sci. USA, 99:11393−11398)。VEGF:Fc融合タンパク質は、新規な血管成長のための成長因子である内因性VEGFを隔離すると予想される。かかる医薬は、脳癌を包含する癌における抗血管形成因子としての特定の使用を有しうる。しかしながら、VEGF:Fc融合タンパク質は、BBBを横断することが予測されない大型分子薬物である(Pardridge, (2008), Bioconj. Chem., (19:1327−1338)。IgG融合タンパク質、例えば、TNFRに関して図1に示されるような融合タンパク質として、VEGFRデコイ受容体を再操作することが必要である。VEGFのかかる形態は、内因性インスリン受容体上の輸送を介してヒトBBBに浸透するであろう。いったんBBBを横断すれば、次いで、MAb−VEGR融合タンパク質は、BBBの後ろに、脳内にVEGFを隔離し、脳癌における新規な血管成長を減少させるであろう。
アポトーシスの腫瘍壊死因子様弱インデューサー(TWEAK)は、TNF遺伝子ファミリーのメンバーである。TWEAK受容体は、Fn14と呼ばれる膜タンパク質である。可溶性Fn14デコイ受容体は、Fn14のECDがヒトIgG1 Fcフラグメントのアミノ末端に融合したFc融合タンパク質として操作されている。TWEAK:Fc融合タンパク質は、中大脳動脈閉塞モデルにおいて卒中のサイズを減少させ、TWEAK:Fc融合タンパク質は、該大型分子医薬はBBBを包含しないので、経頭蓋注射によって脳に投与されなければならない(Yepesら(2005), Am. J. Pathol., 166:511−520; Zhangら(2007), J. Cereb. Blood Flow Metab., 27:534−544)。しかしながら、ヒトにおける急性卒中治療を施すために、頭部に穴を開けることは実際的ではない。したがって、Fn14 ECDがBBB浸透性IgGのカルボキシル末端に融合した図1に示されるようなIgG−Fn14融合タンパク質として、Fn14デコイ受容体を再操作することが必要である。かかるタンパク質は、静脈内注射によって非侵襲性で与えることができ、次いで、BBBを横断して虚血脳中への受容体を介して輸送される。
リンホトキシンα(LTα)は、また、TNFαとしても知られ、リンホトキシンβ(Ltβ)と共に膜において、ヘテロ−三量体複合体を形成することができる。Ltβ複合体は、Ltβ受容体(LtβR)を活性化させて、細胞内シグナル変換現象および炎症カスケードを開始する。LtβR ECDは、デコイ受容体として作用し、内因性Ltβを隔離する場合があり、それは、脳疾患において治療的であることができる。LtβR:Fc融合タンパク質は、実験的脱髄において治療的であり(Plantら、2007)、ヒト脱髄、例えば、多発性硬化症において治療的でありうる。しかしながら、LtβR:Fc融合タンパク質は、ヒトBBBを横断することが予測されない。LtβRデコイ受容体は、図1に示されるようなMAb−LtβR融合タンパク質として再操作されることができる。かかる融合タンパク質は、BBBを横断し、BBBの後ろに、脳内で内因性Ltβを隔離するであろう。
TNF関連アポトーシス誘導性リガンド(TRAIL)は、炎症性サイトカインであり、TRAIL受容体(TRAIL−R)への結合を介して作用する。TRAILは、ヒト免疫不全ウイルス(HIV)−1による脳におけるニューロンの感染後、後天性免疫不全症候群(AIDS)の認知症において病原的役割を果たす(Ryanら(2004), J. Neuroimmunol., 148:127−139)。AIDSまたはニューロAIDSの神経学的発現の治療に対する新規なアプローチは、可溶性TRAIL−Rデコイ受容体での、脳におけるTRAILの隔離でありうる。しかしながら、TRAIL−RのECDまたはそのFc融合タンパク質は、BBBを横断する輸送を欠くため、脳に浸透しないであろう。該問題は、TRAIL−Rデコイ受容体を図1に示されるようなMAb−TRAIL−R融合タンパク質として再操作することによって、解決することができた。MAb−TRAIL−R融合タンパク質は、BBBを横断する受容体介在性輸送を経験し、脳に侵入し、そこで、該融合タンパク質は、TRAILを脳内に隔離するであろう。
インターロイキン(IL)−6のような炎症性サイトカインは、脱髄疾患、例えば、実験的自己免疫脳脊髄炎(EAE)、または多発性硬化症において役割を果たしうる。IL−6受容体(IL−6R)は、可溶性IL−6Rデコイ受容体タンパク質の投与後、脳内で内因性IL−6の作用を抑制することができた。IL−6RのECDがヒトIgG1 Fcフラグメントのアミノ末端に融合したIL−6R:Fc融合タンパク質の投与は、EAEにおいて治療的である(Linkerら(2008), J. Neuroimmunol., 205:64−72)。しかしながら、多発性硬化症におけるIL−6R:Fc融合タンパク質の脳中への浸透は、イン・ビボでのBBBを介する輸送を欠くので、制限されうる。対照的に、図1に示されるようなMAb−IL−6R融合タンパク質は、受容体−媒介性輸送を介してBBBに浸透し、それにより、BBBの後ろに、脳においてIL−6を隔離することができた。
Claims (50)
- 標的受容体細胞外ドメインのアミノ末端に共有結合した重鎖免疫グロブリンまたは軽鎖免疫グロブリンのアミノ酸配列を含む二官能性デコイ受容体融合抗体であって、BBB上に発現された受容体および標的受容体細胞外ドメインのリガンドに結合する融合抗体。
- 該BBB上に発現された受容体がインスリン受容体、トランスフェリン受容体、インスリン様成長因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体である、請求項1記載の二官能性デコイ受容体融合抗体。
- 該BBB上に発現された受容体がインスリン受容体である、請求項2記載の二官能性デコイ受容体融合抗体。
- 該インスリン受容体がヒトインスリン受容体である、請求項3記載の二官能性デコイ受容体融合抗体。
- 該二官能性デコイ受容体融合抗体が、該ヒトインスリン受容体との結合に関して、配列番号4および6または配列番号6および7のアミノ酸配列を含む二官能性デコイ受容体融合抗体と競合する、請求項4記載の二官能性デコイ受容体融合抗体。
- 該標的受容体細胞外ドメインがサイトカイン受容体由来である、請求項1記載の二官能性デコイ受容体融合抗体。
- 該標的受容体細胞外ドメインがTNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン(ephrin)受容体由来である、請求項1記載の二官能性デコイ受容体融合抗体。
- 該標的受容体細胞外ドメインがTNF−α受容体細胞外ドメインを含む、請求項7記載の二官能性デコイ受容体融合抗体。
- 該TNF−α受容体細胞外ドメインが、配列番号4のアミノ酸465〜699のTNF−α受容体細胞外ドメインに対して少なくとも95%同一のアミノ酸配列を含む、請求項8記載の二官能性デコイ受容体融合抗体。
- TNF−α受容体細胞外ドメインが、重鎖免疫グロブリンまたは軽鎖免疫グロブリンのカルボキシル末端に融合している、請求項8記載の二官能性デコイ受容体融合抗体。
- TNF−α受容体細胞外ドメインが重鎖免疫グロブリンのカルボキシル末端に融合している、請求項8記載の二官能性デコイ受容体融合抗体。
- (i)重鎖免疫グロブリンおよび該重鎖免疫グロブリンとフレーム内の標的受容体細胞外ドメインをコードする第1の配列、
(ii)軽鎖免疫グロブリンおよび該軽鎖免疫グロブリンとフレーム内の標的受容体細胞外ドメインをコードする第2の配列、または
(iii)(i)または(ii)の相補性配列
を含む核酸であって、該重鎖および軽鎖免疫グロブリンがBBB受容体に対する抗体に由来し、該免疫グロブリンが該標的受容体細胞外ドメインのアミノ末端に共有結合している、核酸。 - 該コードされた標的受容体細胞外ドメインがTNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン受容体由来である、請求項12記載の核酸。
- 該コードされた標的受容体細胞外ドメインがTNF−α受容体由来である、請求項13記載の核酸。
- 該TNF−α受容体由来のコードされた標的細胞外ドメインが、重鎖免疫グロブリンまたは軽鎖免疫グロブリンのカルボキシル末端に融合している、請求項14記載の核酸。
- 該TNF−α受容体由来のコードされた標的細胞外ドメインが、重鎖免疫グロブリンのカルボキシル末端に融合している、請求項14記載の核酸。
- 該TNF−α受容体由来のコードされた標的細胞外ドメインが、配列番号4のアミノ酸465〜699のTNF−α受容体細胞外ドメインに対して少なくとも95%同一のアミノ酸配列を含む、請求項14記載の核酸。
- 該BBB受容体に対する抗体が、ヒトインスリン受容体、トランスフェリン受容体、インスリン様成長因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体に対する抗体である、請求項12記載の核酸。
- (i)またはその相補体を含む、請求項12記載の核酸。
- さらに、免疫グロブリン軽鎖をコードする核酸配列またはその相補配列を含み、ここに、該コードされた免疫グロブリン軽鎖がBBB受容体に対する抗体由来である、請求項19記載の核酸。
- (ii)またはその相補体を含む、請求項12記載の核酸。
- さらに、免疫グロブリン重鎖をコードする核酸配列またはその相補配列を含み、ここに、該コードされた免疫グロブリン重鎖がBBB受容体に対する抗体由来である、請求項21記載の核酸。
- 該第1の配列が配列番号4または7に対応するアミノ酸配列に対して少なくとも95%同一のアミノ酸配列をコードし、または該第2の配列が配列番号6に対応するアミノ酸配列に対して少なくとも95%同一のアミノ酸配列をコードする、請求項12記載の核酸。
- 高ストリンジェンシー条件下で、配列番号3または5のアミノ酸配列をコードする核酸にハイブリダイズする、請求項12記載の核酸。
- 請求項12記載の核酸を含む、核酸ベクター。
- (i)を含み、さらに、BBB受容体に対する抗体由来の軽鎖免疫グロブリンをコードする核酸配列を含むか、または
(ii)を含み、さらに、BBB受容体に対する抗体由来の重鎖免疫グロブリンをコードする核酸を含む、請求項25記載の核酸ベクター。 - 請求項25記載の核酸ベクターを含む細胞。
- 請求項26記載の核酸ベクターを含む細胞。
- 哺乳動物細胞である、請求項27記載の細胞。
- CNS疾患の治療のための医薬組成物の製造のための、標的受容体細胞外ドメインのアミノ末端に共有結合した重鎖免疫グロブリンまたは軽鎖免疫グロブリンのアミノ酸配列を含む二官能性デコイ受容体融合抗体の使用であって、該融合抗体がBBB上に発現された受容体および標的受容体細胞外ドメインのリガンドに結合するところの、使用。
- 該BBB上に発現された受容体がインスリン受容体、トランスフェリン受容体、インスリン様成長因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体である、請求項30記載の使用。
- 該BBB上に発現された受容体がインスリン受容体である、請求項31記載の使用。
- 該標的受容体細胞外ドメインがTNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン受容体由来である、請求項30記載の使用。
- 該標的受容体細胞外ドメインがTNF−α受容体由来である、請求項33記載の使用。
- 該CNS疾患が急性CNS疾患である、請求項30記載の使用。
- 該急性CNS疾患が全脳虚血、局所脳虚血、外傷性脳損傷、または脊髄損傷である、請求項35記載の使用。
- 該CNS疾患が慢性CNS疾患である、請求項30記載の使用。
- 該慢性CNS疾患が神経変性CNS疾患である、請求項37記載の使用。
- 該神経変性CNS疾患がアルツハイマー病、パーキンソン病、筋萎縮性側索硬化症、ハンチントン病、多発性硬化症、横断性脊髄炎、運動ニューロン疾患、ピック病、結節硬化症、カナバン病、レット症候群、脊髄小脳失調症、フリードライヒ失調症、視神経萎縮、または網膜変性である、請求項38記載の使用。
- 該TNF−α受容体由来の標的細胞外ドメインが、重鎖免疫グロブリンまたは軽鎖免疫グロブリンのカルボキシル末端に共有結合している、請求項34記載の使用。
- 該TNF−α受容体由来の標的細胞外ドメインが重鎖免疫グロブリンのカルボキシル末端に共有結合している、請求項34記載の使用。
- (i)標的受容体細胞外ドメインに融合した免疫グロブリン重鎖、および免疫グロブリン軽鎖の両方、または
(ii)標的受容体細胞外ドメインに融合した免疫グロブリン軽鎖、および免疫グロブリン重鎖の両方
をコードする単一タンデム発現ベクターを真核細胞中に安定に組み込むことを含む、二官能性デコイ受容体融合抗体を製造する方法であって、該コードされた免疫グロブリン重鎖および免疫グロブリン軽鎖がBBB上に発現された受容体に対する抗体由来であり、該免疫グロブリンが標的受容体細胞外ドメインのアミノ末端に共有結合しているところの、方法。 - 該単一タンデム発現ベクターが(i)をコードする、請求項42記載の方法。
- 該単一タンデム発現ベクターが(ii)をコードする、請求項42記載の方法。
- 該BBB上に発現された受容体がインスリン受容体、トランスフェリン受容体、インスリン様成長因子(IGF)受容体、レプチン受容体、またはリポタンパク質受容体である、請求項42記載の方法。
- 該BBB上に発現された標的受容体がインスリン受容体である、請求項45記載の方法。
- 該コードされた標的受容体細胞外ドメインがTNF−α受容体、TNF関連アポトーシス誘導性リガンド(TRAIL)受容体、アポトーシスのTNF様弱インデューサー(TWEAK)受容体、IL−6受容体、血管内皮成長因子受容体、またはエフリン受容体由来である、請求項42記載の方法。
- 該標的受容体細胞外ドメインがTNF−α受容体由来である、請求項47記載の方法。
- 該TNF−α受容体由来の標的受容体細胞外ドメインが免疫グロブリン重鎖または免疫グロブリン軽鎖のカルボキシル末端に融合している、請求項48載の方法。
- 該TNF−α受容体由来の標的受容体細胞外ドメインが免疫グロブリン重鎖のカルボキシル末端に融合している、請求項48記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16132009P | 2009-03-18 | 2009-03-18 | |
| US61/161,320 | 2009-03-18 | ||
| PCT/US2010/027882 WO2010108048A2 (en) | 2009-03-18 | 2010-03-18 | Compositions and methods for blood-brain barrier delivery of igg-decoy receptor fusion proteins |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012521194A JP2012521194A (ja) | 2012-09-13 |
| JP2012521194A5 JP2012521194A5 (ja) | 2013-05-02 |
| JP5873003B2 true JP5873003B2 (ja) | 2016-03-01 |
Family
ID=42740242
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012500979A Active JP5873003B2 (ja) | 2009-03-18 | 2010-03-18 | IgGデコイ受容体融合タンパク質の血液脳関門送達のための組成物および方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US9533055B2 (ja) |
| EP (1) | EP2408474B1 (ja) |
| JP (1) | JP5873003B2 (ja) |
| CA (1) | CA2748889A1 (ja) |
| WO (1) | WO2010108048A2 (ja) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8741260B2 (en) * | 2005-10-07 | 2014-06-03 | Armagen Technologies, Inc. | Fusion proteins for delivery of GDNF to the CNS |
| WO2008022349A2 (en) * | 2006-08-18 | 2008-02-21 | Armagen Technologies, Inc. | Agents for blood-brain barrier delivery |
| CA2694762A1 (en) * | 2007-07-27 | 2009-02-05 | Armagen Technologies, Inc. | Methods and compositions for increasing alpha-l-iduronidase activity in the cns |
| US9533055B2 (en) | 2009-03-18 | 2017-01-03 | Armagen Technologies, Inc. | Compositions and methods for blood-brain barrier delivery of IgG-decoy receptor fusion proteins |
| US8834874B2 (en) | 2009-10-09 | 2014-09-16 | Armagen Technologies, Inc. | Methods and compositions for increasing iduronate 2-sulfatase activity in the CNS |
| LT2646470T (lt) | 2010-11-30 | 2017-06-12 | F. Hoffmann-La Roche Ag | Mažo giminingumo antitransferino receptorių antikūnai ir jų panaudojimas pernešti gydomąjį vienos grandinės antikūną (scfv) per hematoencefalinį barjerą |
| CA2857647C (en) | 2011-12-02 | 2022-04-19 | Armagen Technologies, Inc. | Methods and compositions for increasing arylsulfatase a activity in the cns |
| US10774132B2 (en) | 2012-01-09 | 2020-09-15 | The Scripps Research Instittue | Ultralong complementarity determining regions and uses thereof |
| EP2908837B1 (en) * | 2012-10-19 | 2019-02-13 | Vect-Horus | Compositions for drug delivery |
| US9644021B2 (en) | 2013-01-11 | 2017-05-09 | The California Institute For Biomedical Research | Bovine fusion antibodies |
| AU2014251388B2 (en) | 2013-04-12 | 2017-03-30 | Evox Therapeutics Limited | Therapeutic delivery vesicles |
| US20150093399A1 (en) | 2013-08-28 | 2015-04-02 | Bioasis Technologies, Inc. | Cns-targeted conjugates having modified fc regions and methods of use thereof |
| SG11201606577YA (en) | 2014-02-10 | 2016-09-29 | Merck Patent Gmbh | TARGETED TGFβ INHIBITION |
| US10538589B2 (en) | 2015-01-14 | 2020-01-21 | Armagen Inc. | Methods and compositions for increasing N-acetylglucosaminidase (NAGLU) activity in the CNS using a fusion antibody comprising an anti-human insulin receptor antibody and NAGLU |
| US9553885B2 (en) * | 2015-06-08 | 2017-01-24 | Illusive Networks Ltd. | System and method for creation, deployment and management of augmented attacker map |
| EP3563863B1 (en) | 2016-12-28 | 2023-07-12 | JCR Pharmaceuticals Co., Ltd. | Lyophilized preparation |
| CA3128035A1 (en) | 2020-08-13 | 2022-02-13 | Bioasis Technologies, Inc. | Combination therapies for delivery across the blood brain barrier |
| EP4359430A2 (en) * | 2021-06-23 | 2024-05-01 | Lycia Therapeutics, Inc. | Bifunctional compounds containing igf-2 polypeptides |
| WO2024080843A1 (ko) * | 2022-10-14 | 2024-04-18 | 주식회사 아임뉴런 | 뇌혈관장벽 투과성 융합 단백질 및 이의 용도 |
Family Cites Families (95)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5618920A (en) | 1985-11-01 | 1997-04-08 | Xoma Corporation | Modular assembly of antibody genes, antibodies prepared thereby and use |
| US4902505A (en) | 1986-07-30 | 1990-02-20 | Alkermes | Chimeric peptides for neuropeptide delivery through the blood-brain barrier |
| US4801575A (en) | 1986-07-30 | 1989-01-31 | The Regents Of The University Of California | Chimeric peptides for neuropeptide delivery through the blood-brain barrier |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5229500A (en) | 1989-08-30 | 1993-07-20 | Regeneron Pharmaceuticals, Inc. | Brain derived neurotrophic factor |
| US5180820A (en) | 1989-08-30 | 1993-01-19 | Barde Yves Alain | Brain-derived neurotrophic factor |
| NZ235148A (en) * | 1989-09-05 | 1991-12-23 | Immunex Corp | Tumour necrosis factor receptor protein and dna sequences |
| US6541610B1 (en) * | 1989-09-05 | 2003-04-01 | Immunex Corporation | Fusion proteins comprising tumor necrosis factor receptor |
| US6329508B1 (en) | 1989-09-07 | 2001-12-11 | Alkermes, Inc. | Transferrin receptor reactive chimeric antibodies |
| US5672683A (en) | 1989-09-07 | 1997-09-30 | Alkermes, Inc. | Transferrin neuropharmaceutical agent fusion protein |
| US5182107A (en) | 1989-09-07 | 1993-01-26 | Alkermes, Inc. | Transferrin receptor specific antibody-neuropharmaceutical or diagnostic agent conjugates |
| US5977307A (en) | 1989-09-07 | 1999-11-02 | Alkermes, Inc. | Transferrin receptor specific ligand-neuropharmaceutical agent fusion proteins |
| US5527527A (en) | 1989-09-07 | 1996-06-18 | Alkermes, Inc. | Transferrin receptor specific antibody-neuropharmaceutical agent conjugates |
| US5154924A (en) | 1989-09-07 | 1992-10-13 | Alkermes, Inc. | Transferrin receptor specific antibody-neuropharmaceutical agent conjugates |
| EP1132471A3 (de) * | 1989-09-12 | 2001-11-28 | F. Hoffmann-La Roche Ag | TNF-bindende Proteine |
| US5527288A (en) | 1990-12-13 | 1996-06-18 | Elan Medical Technologies Limited | Intradermal drug delivery device and method for intradermal delivery of drugs |
| TW279133B (ja) | 1990-12-13 | 1996-06-21 | Elan Med Tech | |
| US6060069A (en) | 1991-05-20 | 2000-05-09 | Dura Pharmaceuticals, Inc. | Pulmonary delivery of pharmaceuticals |
| US6287792B1 (en) | 1991-06-17 | 2001-09-11 | The Regents Of The University Of California | Drug delivery of antisense oligonucleotides and peptides to tissues in vivo and to cells using avidin-biotin technology |
| DE69230545T2 (de) | 1991-08-21 | 2000-07-06 | Novartis Ag | Antikörperderivate |
| CA2119463C (en) | 1991-09-20 | 2003-09-16 | Leu-Fen H. Lin | Glial cell line-derived neutrophic factor |
| JPH06228199A (ja) | 1992-11-27 | 1994-08-16 | Takeda Chem Ind Ltd | 血液脳関門通過可能なペプチド結合体 |
| CA2115900A1 (en) | 1993-02-22 | 1994-08-23 | Gerald W. Becker | Pharmaceutical screens and antibodies |
| US5997501A (en) | 1993-11-18 | 1999-12-07 | Elan Corporation, Plc | Intradermal drug delivery device |
| PT706799E (pt) | 1994-09-16 | 2002-05-31 | Merck Patent Gmbh | Imunoconjugados ii |
| US5656284A (en) | 1995-04-24 | 1997-08-12 | Balkin; Michael S. | Oral transmucosal delivery tablet and method of making it |
| AU6163196A (en) | 1995-06-07 | 1996-12-30 | Smithkline Beecham Corporation | Method for obtaining receptor agonist antibodies |
| ATE254450T1 (de) | 1995-09-19 | 2003-12-15 | Fujisawa Pharmaceutical Co | Aerosolzusammensetzungen |
| US6015662A (en) | 1996-01-23 | 2000-01-18 | Abbott Laboratories | Reagents for use as calibrators and controls |
| US5837231A (en) | 1996-06-27 | 1998-11-17 | Regents Of The University Of Minnesota | GM-CSF administration for the treatment and prevention of recurrence of brain tumors |
| US8173127B2 (en) | 1997-04-09 | 2012-05-08 | Intellect Neurosciences, Inc. | Specific antibodies to amyloid beta peptide, pharmaceutical compositions and methods of use thereof |
| WO1999000150A2 (en) | 1997-06-27 | 1999-01-07 | Regents Of The University Of California | Drug targeting of a peptide radiopharmaceutical through the primate blood-brain barrier in vivo with a monoclonal antibody to the human insulin receptor |
| WO1999000951A1 (en) | 1997-06-30 | 1999-01-07 | Motorola Inc. | Circuit and packet switched network interconnection |
| US6482923B1 (en) | 1997-09-17 | 2002-11-19 | Human Genome Sciences, Inc. | Interleukin 17-like receptor protein |
| US6165783A (en) | 1997-10-24 | 2000-12-26 | Neuro Spheres Holdings Ltd. | Erythropoietin-mediated neurogenesis |
| US6016800A (en) | 1997-10-24 | 2000-01-25 | Century; Theodore J. | Intrapulmonary aerosolizer |
| US6743427B1 (en) | 1997-12-02 | 2004-06-01 | Neuralab Limited | Prevention and treatment of amyloidogenic disease |
| AU757230B2 (en) | 1997-12-11 | 2003-02-06 | Alza Corporation | Device for enhancing transdermal agent flux |
| AU760854B2 (en) | 1998-06-22 | 2003-05-22 | Immunomedics Inc. | Use of bi-specific antibodies for pre-targeting diagnosis and therapy |
| US6348210B1 (en) | 1998-11-13 | 2002-02-19 | Alza Corporation | Methods for transdermal drug administration |
| US6375975B1 (en) | 1998-12-21 | 2002-04-23 | Generex Pharmaceuticals Incorporated | Pharmaceutical compositions for buccal and pulmonary application |
| IL143596A0 (en) * | 1998-12-22 | 2002-04-21 | Genentech Inc | Vascular endothelial cell growth factor antagonists and uses thereof |
| US6284262B1 (en) | 1999-01-26 | 2001-09-04 | Virgil A. Place | Compact dosage unit for buccal administration of a pharmacologically active agent |
| US7214658B2 (en) * | 2004-07-06 | 2007-05-08 | Tact Ip, Llc | Method of delivering a TNF antagonist to the brain of a human by perispinal administration without direct intrathecal injection |
| BR0009247A (pt) | 1999-03-05 | 2001-11-20 | Epigenesis Pharmaceuticals Inc | Método para validar/invalidar alvo(s) e vias |
| US7410941B1 (en) | 1999-04-13 | 2008-08-12 | The Kenneth S. Warren Institute, Inc. | Methods for treatment of neurodegenerative conditions by peripherally administered erythropoietin |
| WO2000077178A1 (en) | 1999-06-16 | 2000-12-21 | Boston Biomedical Research Institute | IMMUNOLOGICAL CONTROL OF β-AMYLOID LEVELS IN VIVO |
| CZ299516B6 (cs) | 1999-07-02 | 2008-08-20 | F. Hoffmann-La Roche Ag | Konjugát erythropoetinového glykoproteinu, zpusobjeho výroby a použití a farmaceutická kompozice sjeho obsahem |
| JP3589912B2 (ja) | 1999-09-03 | 2004-11-17 | 泰久 福井 | ホスファチジルイノシトール−3,4−二リン酸を認識するモノクローナル抗体 |
| US20020052311A1 (en) | 1999-09-03 | 2002-05-02 | Beka Solomon | Methods and compostions for the treatment and/or diagnosis of neurological diseases and disorders |
| US6585971B1 (en) | 1999-11-12 | 2003-07-01 | Harbor-Ucla Research And Education Institute | Recombinant α-L-iduronidase, methods for producing and purifying the same and methods for treating disease caused by deficiencies thereof |
| ES2433011T3 (es) | 1999-12-20 | 2013-12-05 | Immunex Corporation | Receptor TWEAK |
| US6248262B1 (en) | 2000-02-03 | 2001-06-19 | General Electric Company | Carbon-reinforced thermoplastic resin composition and articles made from same |
| CA2401645A1 (en) | 2000-02-29 | 2001-09-07 | Lexicon Genetics Incorporated | Novel human transporter proteins and polynucleotides encoding the same |
| US6372250B1 (en) | 2000-04-25 | 2002-04-16 | The Regents Of The University Of California | Non-invasive gene targeting to the brain |
| US6696274B2 (en) | 2000-05-03 | 2004-02-24 | Supratek Pharma, Inc. | Ligand for enhancing oral and CNS delivery of biological agents |
| US7078376B1 (en) | 2000-08-11 | 2006-07-18 | Baxter Healthcare S.A. | Therapeutic methods for treating subjects with a recombinant erythropoietin having high activity and reduced side effects |
| US20030165853A1 (en) | 2000-12-04 | 2003-09-04 | The Regents Of The University Of California Office Of Technology Transfer | Antisense imaging of gene expression of the brain in vivo |
| PT1471871E (pt) | 2001-02-02 | 2007-06-05 | Ortho Mcneil Pharm Inc | Tratamento de disfunção neurológica compreendendo sulfamatos de frutopiranose e eritropoietina |
| US20040072291A1 (en) | 2001-02-06 | 2004-04-15 | Carr Francis J. | Modified human brain-derived neutrophic factor (bdnf) with reduced immunogenicity |
| AU2002322720B2 (en) | 2001-07-25 | 2008-11-13 | Raptor Pharmaceutical Inc. | Compositions and methods for modulating blood-brain barrier transport |
| AU2002329775C1 (en) | 2001-08-17 | 2011-04-07 | Eli Lilly And Company | Assay method for alzheimer's disease |
| US7125843B2 (en) | 2001-10-19 | 2006-10-24 | Neose Technologies, Inc. | Glycoconjugates including more than one peptide |
| US7053202B2 (en) | 2001-10-19 | 2006-05-30 | Millennium Pharmaceuticals, Inc. | Immunoglobulin DNA cassette molecules, monobody constructs, methods of production, and methods of use therefor |
| DK1517921T3 (da) | 2002-06-28 | 2006-10-09 | Domantis Ltd | Immunglobulin-enkeltvariable antigen-bindende domæner og dobbeltspecifikke konstruktioner deraf |
| US20050142141A1 (en) | 2002-11-27 | 2005-06-30 | Pardridge William M. | Delivery of enzymes to the brain |
| US7388079B2 (en) | 2002-11-27 | 2008-06-17 | The Regents Of The University Of California | Delivery of pharmaceutical agents via the human insulin receptor |
| US20040102369A1 (en) | 2002-11-27 | 2004-05-27 | The Regents Of The University Of California | Transport of basic fibroblast growth factor across the blood brain barrier |
| ATE534730T1 (de) | 2003-02-11 | 2011-12-15 | Shire Human Genetic Therapies | Diagnose und behandlung von multiplen sulfatase- erkrankungen und anderen mit hilfe eines formylglycin bildenden enzyms |
| AU2003286870A1 (en) | 2003-06-05 | 2005-01-04 | Salk Institute For Biological Studies | Targeting polypeptides to the central nervous system |
| US7294704B2 (en) | 2003-08-15 | 2007-11-13 | Diadexus, Inc. | Pro108 antibody compositions and methods of use and use of Pro108 to assess cancer risk |
| EP1548031A1 (en) | 2003-12-22 | 2005-06-29 | Dubai Genetics FZ-LLC | Nature-identical erythropoietin |
| US8536315B2 (en) | 2004-01-30 | 2013-09-17 | Shire Pharmaceuticals Ireland Limited | Production and purification of recombinant arylsulftase |
| US7939490B2 (en) * | 2004-12-13 | 2011-05-10 | University Of Maryland, Baltimore | TWEAK as a therapeutic target for treating central nervous system diseases associated with cerebral edema and cell death |
| CA2589860A1 (en) | 2005-01-24 | 2006-08-03 | Amgen Inc. | Humanized anti-amyloid antibody |
| EP1917030A4 (en) | 2005-08-03 | 2011-03-09 | Immunogen Inc | IMMUNKONJUGATFORMULIERUNGEN |
| CA2619725C (en) | 2005-08-18 | 2016-06-07 | Ramot At Tel Aviv University Ltd. | Single chain antibodies against beta-amyloid peptide |
| US8741260B2 (en) | 2005-10-07 | 2014-06-03 | Armagen Technologies, Inc. | Fusion proteins for delivery of GDNF to the CNS |
| US8053569B2 (en) * | 2005-10-07 | 2011-11-08 | Armagen Technologies, Inc. | Nucleic acids encoding and methods of producing fusion proteins |
| US8124095B2 (en) | 2005-10-07 | 2012-02-28 | Armagen Technologies, Inc. | Fusion proteins for delivery of erythropoietin to the CNS |
| WO2008022349A2 (en) * | 2006-08-18 | 2008-02-21 | Armagen Technologies, Inc. | Agents for blood-brain barrier delivery |
| EP2120998B1 (en) | 2006-11-28 | 2013-08-07 | HanAll Biopharma Co., Ltd. | Modified erythropoietin polypeptides and uses thereof for treatment |
| US20100172919A1 (en) | 2007-06-15 | 2010-07-08 | Jan Grimm | Noveltreatment for neurological disorders |
| CA2694762A1 (en) | 2007-07-27 | 2009-02-05 | Armagen Technologies, Inc. | Methods and compositions for increasing alpha-l-iduronidase activity in the cns |
| WO2009070597A2 (en) | 2007-11-26 | 2009-06-04 | Armagen Technologies, Inc. | Fusion proteins for delivery of gdnf to the cns |
| BRPI0913991A2 (pt) * | 2008-07-02 | 2015-11-17 | Emergent Product Dev Seattle | imunoterápicos da il6 |
| US20100077498A1 (en) | 2008-09-11 | 2010-03-25 | Pardridge William M | Compositions and methods for blood-brain barrier delivery in the mouse |
| US20100098693A1 (en) | 2008-10-07 | 2010-04-22 | Pardridge William M | Compositions and methods for blood-brain barrier delivery of organophosphatases |
| US9533055B2 (en) | 2009-03-18 | 2017-01-03 | Armagen Technologies, Inc. | Compositions and methods for blood-brain barrier delivery of IgG-decoy receptor fusion proteins |
| US8859515B2 (en) | 2009-06-24 | 2014-10-14 | Curna, Inc. | Treatment of tumor necrosis factor receptor 2 (TNFR2) related diseases by inhibition of natural antisense transcript to TNFR2 |
| US8834874B2 (en) | 2009-10-09 | 2014-09-16 | Armagen Technologies, Inc. | Methods and compositions for increasing iduronate 2-sulfatase activity in the CNS |
| US9320711B2 (en) | 2010-06-25 | 2016-04-26 | Shire Human Genetic Therapies, Inc. | Methods and compositions for CNS delivery of heparan N-sulfatase |
| CA2857647C (en) | 2011-12-02 | 2022-04-19 | Armagen Technologies, Inc. | Methods and compositions for increasing arylsulfatase a activity in the cns |
| WO2015012944A1 (en) | 2013-07-22 | 2015-01-29 | Armagen Technologies, Inc | Methods and compositions for increasing enzyme activity in the cns |
-
2010
- 2010-03-18 US US13/141,682 patent/US9533055B2/en active Active
- 2010-03-18 EP EP10754139.3A patent/EP2408474B1/en active Active
- 2010-03-18 JP JP2012500979A patent/JP5873003B2/ja active Active
- 2010-03-18 CA CA2748889A patent/CA2748889A1/en not_active Abandoned
- 2010-03-18 WO PCT/US2010/027882 patent/WO2010108048A2/en active Application Filing
-
2016
- 2016-11-21 US US15/357,894 patent/US20170066832A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| EP2408474A4 (en) | 2013-01-23 |
| US20170066832A1 (en) | 2017-03-09 |
| US20120269807A1 (en) | 2012-10-25 |
| JP2012521194A (ja) | 2012-09-13 |
| EP2408474A2 (en) | 2012-01-25 |
| WO2010108048A3 (en) | 2010-11-11 |
| EP2408474B1 (en) | 2019-06-26 |
| WO2010108048A2 (en) | 2010-09-23 |
| CA2748889A1 (en) | 2010-09-23 |
| US9533055B2 (en) | 2017-01-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5873003B2 (ja) | IgGデコイ受容体融合タンパク質の血液脳関門送達のための組成物および方法 | |
| US20200254113A1 (en) | Fusion proteins for delivery of gdnf to the cns | |
| JP6283711B2 (ja) | 血液脳関門輸送用融合タンパク質 | |
| JP5959795B2 (ja) | 血液脳関門送達のための物質 | |
| EP2440578B1 (en) | Use of an anti-tau ps422 antibody for the treatment of brain diseases | |
| JP2021008488A (ja) | Cnsにおけるイズロン酸 2−スルファターゼ活性を増加させるための方法および組成物 | |
| EP2523683B1 (en) | Fusion proteins for delivery of erythropoietin to the cns | |
| NZ719092A (en) | Tumor necrosis factor-like ligand 1a specific antibodies and compositions and uses thereof | |
| CA3184105A1 (en) | Methods and compositions for increasing alpha-l-iduronidase activity in the cns | |
| EP4063385A1 (en) | Gipr antibody and fusion protein between same and glp-1, and pharmaceutical composition and application thereof | |
| US11780916B2 (en) | GIPR antibody and GLP-1 fusion protein thereof, and pharmaceutical composition and application thereof | |
| US11542336B2 (en) | GCGR antibody and GLP-1 fusion protein thereof, pharmaceutical composition thereof and application thereof | |
| EP3808847A1 (en) | Apj antibody, fusion protein thereof with elabela, and pharmaceutical compositions and use thereof | |
| KR101804988B1 (ko) | 신규 항-tfpi 항체 및 이를 포함하는 조성물 | |
| KR20220062084A (ko) | 면역 복합체 매개된 콩팥 장애의 치료를 위한 재조합 IgG Fc 다량체 | |
| CN117715932A (zh) | 一种cdc平台抗体 | |
| KR20240022546A (ko) | 항il-36r 항체 및 그의 사용 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130313 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130313 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20140120 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140805 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141104 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20141111 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141204 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20141211 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141225 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150204 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150602 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150901 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20151001 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20151030 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151201 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20151222 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160114 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5873003 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |