JP5749652B2 - 血清学的マーカーを用いた炎症性腸疾患(ibd)の予測方法 - Google Patents
血清学的マーカーを用いた炎症性腸疾患(ibd)の予測方法 Download PDFInfo
- Publication number
- JP5749652B2 JP5749652B2 JP2011535773A JP2011535773A JP5749652B2 JP 5749652 B2 JP5749652 B2 JP 5749652B2 JP 2011535773 A JP2011535773 A JP 2011535773A JP 2011535773 A JP2011535773 A JP 2011535773A JP 5749652 B2 JP5749652 B2 JP 5749652B2
- Authority
- JP
- Japan
- Prior art keywords
- ibd
- sample
- antibody
- markers
- level
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 208000022559 Inflammatory bowel disease Diseases 0.000 title claims description 306
- 238000000034 method Methods 0.000 title claims description 142
- 230000000405 serological effect Effects 0.000 title description 26
- 206010009900 Colitis ulcerative Diseases 0.000 claims description 85
- 201000006704 Ulcerative Colitis Diseases 0.000 claims description 85
- 238000012896 Statistical algorithm Methods 0.000 claims description 57
- 230000001965 increasing effect Effects 0.000 claims description 30
- 208000011231 Crohn disease Diseases 0.000 claims description 25
- 238000007637 random forest analysis Methods 0.000 claims description 20
- 230000002496 gastric effect Effects 0.000 claims description 3
- XGWFJBFNAQHLEF-UHFFFAOYSA-N 9-anthroic acid Chemical compound C1=CC=C2C(C(=O)O)=C(C=CC=C3)C3=CC2=C1 XGWFJBFNAQHLEF-UHFFFAOYSA-N 0.000 claims 2
- 241001408449 Asca Species 0.000 claims 1
- 239000000523 sample Substances 0.000 description 215
- 239000003550 marker Substances 0.000 description 111
- 238000004458 analytical method Methods 0.000 description 59
- 238000002965 ELISA Methods 0.000 description 51
- 239000003814 drug Substances 0.000 description 49
- 239000000427 antigen Substances 0.000 description 47
- 102000036639 antigens Human genes 0.000 description 47
- 108091007433 antigens Proteins 0.000 description 47
- 239000012634 fragment Substances 0.000 description 43
- 229940079593 drug Drugs 0.000 description 42
- 238000013528 artificial neural network Methods 0.000 description 41
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 40
- 238000012360 testing method Methods 0.000 description 39
- 201000010099 disease Diseases 0.000 description 38
- 108090000765 processed proteins & peptides Proteins 0.000 description 37
- 102000004169 proteins and genes Human genes 0.000 description 36
- 102000004196 processed proteins & peptides Human genes 0.000 description 35
- 108090000623 proteins and genes Proteins 0.000 description 35
- 235000018102 proteins Nutrition 0.000 description 34
- 229920001184 polypeptide Polymers 0.000 description 33
- 238000003018 immunoassay Methods 0.000 description 32
- 210000000440 neutrophil Anatomy 0.000 description 32
- 210000002966 serum Anatomy 0.000 description 31
- 239000002953 phosphate buffered saline Substances 0.000 description 28
- 238000004422 calculation algorithm Methods 0.000 description 25
- 238000009826 distribution Methods 0.000 description 25
- 108010040721 Flagellin Proteins 0.000 description 24
- 150000001413 amino acids Chemical group 0.000 description 24
- 238000003745 diagnosis Methods 0.000 description 24
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 24
- 238000012545 processing Methods 0.000 description 23
- 238000003556 assay Methods 0.000 description 22
- 239000000243 solution Substances 0.000 description 21
- 208000024891 symptom Diseases 0.000 description 21
- 108700028353 OmpC Proteins 0.000 description 20
- 210000004027 cell Anatomy 0.000 description 20
- 238000012549 training Methods 0.000 description 19
- 239000002552 dosage form Substances 0.000 description 18
- 230000035945 sensitivity Effects 0.000 description 18
- 108010018054 CBir1 flagellin Proteins 0.000 description 17
- 239000013610 patient sample Substances 0.000 description 17
- 230000008569 process Effects 0.000 description 17
- 108010074051 C-Reactive Protein Proteins 0.000 description 15
- 102100032752 C-reactive protein Human genes 0.000 description 15
- 229920000057 Mannan Polymers 0.000 description 15
- 238000001514 detection method Methods 0.000 description 15
- 238000005259 measurement Methods 0.000 description 15
- 102000016911 Deoxyribonucleases Human genes 0.000 description 14
- 108010053770 Deoxyribonucleases Proteins 0.000 description 14
- 238000010790 dilution Methods 0.000 description 14
- 239000012895 dilution Substances 0.000 description 14
- 230000009257 reactivity Effects 0.000 description 14
- 230000004054 inflammatory process Effects 0.000 description 13
- 206010061218 Inflammation Diseases 0.000 description 12
- 102000010445 Lactoferrin Human genes 0.000 description 12
- 108010063045 Lactoferrin Proteins 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 210000004369 blood Anatomy 0.000 description 12
- 239000008280 blood Substances 0.000 description 12
- 230000000670 limiting effect Effects 0.000 description 12
- 239000002585 base Substances 0.000 description 11
- 238000011161 development Methods 0.000 description 11
- 230000000694 effects Effects 0.000 description 11
- 230000014509 gene expression Effects 0.000 description 11
- CSSYQJWUGATIHM-IKGCZBKSSA-N l-phenylalanyl-l-lysyl-l-cysteinyl-l-arginyl-l-arginyl-l-tryptophyl-l-glutaminyl-l-tryptophyl-l-arginyl-l-methionyl-l-lysyl-l-lysyl-l-leucylglycyl-l-alanyl-l-prolyl-l-seryl-l-isoleucyl-l-threonyl-l-cysteinyl-l-valyl-l-arginyl-l-arginyl-l-alanyl-l-phenylal Chemical compound C([C@H](N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)C1=CC=CC=C1 CSSYQJWUGATIHM-IKGCZBKSSA-N 0.000 description 11
- 229940078795 lactoferrin Drugs 0.000 description 11
- 235000021242 lactoferrin Nutrition 0.000 description 11
- 239000002609 medium Substances 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 235000002639 sodium chloride Nutrition 0.000 description 11
- 241000283707 Capra Species 0.000 description 10
- 241000282414 Homo sapiens Species 0.000 description 10
- 102100029441 Nucleotide-binding oligomerization domain-containing protein 2 Human genes 0.000 description 10
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 10
- 230000001086 cytosolic effect Effects 0.000 description 10
- 238000010166 immunofluorescence Methods 0.000 description 10
- 238000002991 immunohistochemical analysis Methods 0.000 description 10
- 208000002551 irritable bowel syndrome Diseases 0.000 description 10
- 210000002381 plasma Anatomy 0.000 description 10
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 9
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 9
- 108010069316 Leukocyte L1 Antigen Complex Proteins 0.000 description 9
- 102000001109 Leukocyte L1 Antigen Complex Human genes 0.000 description 9
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 9
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 9
- 230000027455 binding Effects 0.000 description 9
- 239000000872 buffer Substances 0.000 description 9
- 239000003795 chemical substances by application Substances 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 239000008188 pellet Substances 0.000 description 9
- 230000001225 therapeutic effect Effects 0.000 description 9
- 210000001519 tissue Anatomy 0.000 description 9
- 238000010200 validation analysis Methods 0.000 description 9
- 102000005720 Glutathione transferase Human genes 0.000 description 8
- 108010070675 Glutathione transferase Proteins 0.000 description 8
- 235000001014 amino acid Nutrition 0.000 description 8
- 230000000844 anti-bacterial effect Effects 0.000 description 8
- 238000013459 approach Methods 0.000 description 8
- 206010009887 colitis Diseases 0.000 description 8
- 238000002405 diagnostic procedure Methods 0.000 description 8
- 208000027138 indeterminate colitis Diseases 0.000 description 8
- 238000012544 monitoring process Methods 0.000 description 8
- 150000007523 nucleic acids Chemical class 0.000 description 8
- 239000007787 solid Substances 0.000 description 8
- 238000010186 staining Methods 0.000 description 8
- 239000006228 supernatant Substances 0.000 description 8
- 210000002700 urine Anatomy 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 7
- 108090000790 Enzymes Proteins 0.000 description 7
- 230000000845 anti-microbial effect Effects 0.000 description 7
- 230000001580 bacterial effect Effects 0.000 description 7
- 238000001574 biopsy Methods 0.000 description 7
- 238000005119 centrifugation Methods 0.000 description 7
- 210000001072 colon Anatomy 0.000 description 7
- 230000001419 dependent effect Effects 0.000 description 7
- 229940088598 enzyme Drugs 0.000 description 7
- -1 etc.) Chemical compound 0.000 description 7
- 238000009396 hybridization Methods 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- 210000005253 yeast cell Anatomy 0.000 description 7
- 208000004998 Abdominal Pain Diseases 0.000 description 6
- 206010012735 Diarrhoea Diseases 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 206010018691 Granuloma Diseases 0.000 description 6
- 101001125026 Homo sapiens Nucleotide-binding oligomerization domain-containing protein 2 Proteins 0.000 description 6
- 108060003951 Immunoglobulin Proteins 0.000 description 6
- 101150083031 Nod2 gene Proteins 0.000 description 6
- 229920001213 Polysorbate 20 Polymers 0.000 description 6
- 230000003044 adaptive effect Effects 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 102000018358 immunoglobulin Human genes 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 239000012528 membrane Substances 0.000 description 6
- 210000004379 membrane Anatomy 0.000 description 6
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 6
- 108020004999 messenger RNA Proteins 0.000 description 6
- 230000007170 pathology Effects 0.000 description 6
- 239000000546 pharmaceutical excipient Substances 0.000 description 6
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 6
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 6
- 238000004445 quantitative analysis Methods 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- 238000012706 support-vector machine Methods 0.000 description 6
- 229940124597 therapeutic agent Drugs 0.000 description 6
- 102000001554 Hemoglobins Human genes 0.000 description 5
- 108010054147 Hemoglobins Proteins 0.000 description 5
- 108700002045 Nod2 Signaling Adaptor Proteins 0.000 description 5
- 230000000356 anti-lactoferrin effect Effects 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 230000000968 intestinal effect Effects 0.000 description 5
- 238000012986 modification Methods 0.000 description 5
- 230000004048 modification Effects 0.000 description 5
- 238000003752 polymerase chain reaction Methods 0.000 description 5
- 238000004393 prognosis Methods 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000000306 recurrent effect Effects 0.000 description 5
- 238000012163 sequencing technique Methods 0.000 description 5
- 210000000813 small intestine Anatomy 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 239000007790 solid phase Substances 0.000 description 5
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 4
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 4
- 206010061818 Disease progression Diseases 0.000 description 4
- 238000008157 ELISA kit Methods 0.000 description 4
- 208000018522 Gastrointestinal disease Diseases 0.000 description 4
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 4
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 4
- 102000016387 Pancreatic elastase Human genes 0.000 description 4
- 108010067372 Pancreatic elastase Proteins 0.000 description 4
- 108010013381 Porins Proteins 0.000 description 4
- 102000017033 Porins Human genes 0.000 description 4
- 229920002472 Starch Polymers 0.000 description 4
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 4
- 229930006000 Sucrose Natural products 0.000 description 4
- 239000007983 Tris buffer Substances 0.000 description 4
- 208000025865 Ulcer Diseases 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 229960002685 biotin Drugs 0.000 description 4
- 239000011616 biotin Substances 0.000 description 4
- 229940098773 bovine serum albumin Drugs 0.000 description 4
- 239000003593 chromogenic compound Substances 0.000 description 4
- 230000005750 disease progression Effects 0.000 description 4
- 238000001962 electrophoresis Methods 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 239000000284 extract Substances 0.000 description 4
- 239000007850 fluorescent dye Substances 0.000 description 4
- 230000004927 fusion Effects 0.000 description 4
- 230000002068 genetic effect Effects 0.000 description 4
- 238000010801 machine learning Methods 0.000 description 4
- LUEWUZLMQUOBSB-GFVSVBBRSA-N mannan Chemical class O[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@H]3[C@H](O[C@@H](O)[C@@H](O)[C@H]3O)CO)[C@@H](O)[C@H]2O)CO)[C@H](O)[C@H]1O LUEWUZLMQUOBSB-GFVSVBBRSA-N 0.000 description 4
- 238000002493 microarray Methods 0.000 description 4
- 108020004707 nucleic acids Proteins 0.000 description 4
- 102000039446 nucleic acids Human genes 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 238000002823 phage display Methods 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000003127 radioimmunoassay Methods 0.000 description 4
- 210000000664 rectum Anatomy 0.000 description 4
- 210000003296 saliva Anatomy 0.000 description 4
- 239000008107 starch Substances 0.000 description 4
- 235000019698 starch Nutrition 0.000 description 4
- 239000005720 sucrose Substances 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- XZKIHKMTEMTJQX-UHFFFAOYSA-N 4-Nitrophenyl Phosphate Chemical compound OP(O)(=O)OC1=CC=C([N+]([O-])=O)C=C1 XZKIHKMTEMTJQX-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 3
- 241000894006 Bacteria Species 0.000 description 3
- 238000012286 ELISA Assay Methods 0.000 description 3
- 241000588724 Escherichia coli Species 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 3
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- 238000012897 Levenberg–Marquardt algorithm Methods 0.000 description 3
- 206010037660 Pyrexia Diseases 0.000 description 3
- 229920002125 Sokalan® Polymers 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 230000003321 amplification Effects 0.000 description 3
- 230000002391 anti-complement effect Effects 0.000 description 3
- 108010008730 anticomplement Proteins 0.000 description 3
- LMEKQMALGUDUQG-UHFFFAOYSA-N azathioprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC=NC2=C1NC=N2 LMEKQMALGUDUQG-UHFFFAOYSA-N 0.000 description 3
- 229960002170 azathioprine Drugs 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000002902 bimodal effect Effects 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 210000001124 body fluid Anatomy 0.000 description 3
- 239000010839 body fluid Substances 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 235000010980 cellulose Nutrition 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 239000003246 corticosteroid Substances 0.000 description 3
- 229960001334 corticosteroids Drugs 0.000 description 3
- 230000009089 cytolysis Effects 0.000 description 3
- 238000003066 decision tree Methods 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 108010003342 flaB flagellin Proteins 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 229940014259 gelatin Drugs 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 229940099472 immunoglobulin a Drugs 0.000 description 3
- 229940027941 immunoglobulin g Drugs 0.000 description 3
- 230000002055 immunohistochemical effect Effects 0.000 description 3
- 229960000598 infliximab Drugs 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 201000002313 intestinal cancer Diseases 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 239000010410 layer Substances 0.000 description 3
- 239000002502 liposome Substances 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 238000004949 mass spectrometry Methods 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 3
- 229960001428 mercaptopurine Drugs 0.000 description 3
- KBOPZPXVLCULAV-UHFFFAOYSA-N mesalamine Chemical compound NC1=CC=C(O)C(C(O)=O)=C1 KBOPZPXVLCULAV-UHFFFAOYSA-N 0.000 description 3
- 229960004963 mesalazine Drugs 0.000 description 3
- 229960000485 methotrexate Drugs 0.000 description 3
- 239000011859 microparticle Substances 0.000 description 3
- 210000004877 mucosa Anatomy 0.000 description 3
- 238000003199 nucleic acid amplification method Methods 0.000 description 3
- 229920001542 oligosaccharide Polymers 0.000 description 3
- 150000002482 oligosaccharides Chemical class 0.000 description 3
- 238000010647 peptide synthesis reaction Methods 0.000 description 3
- 239000013641 positive control Substances 0.000 description 3
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 3
- 229960004618 prednisone Drugs 0.000 description 3
- 238000003259 recombinant expression Methods 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 230000000717 retained effect Effects 0.000 description 3
- 238000009589 serological test Methods 0.000 description 3
- NCEXYHBECQHGNR-QZQOTICOSA-N sulfasalazine Chemical compound C1=C(O)C(C(=O)O)=CC(\N=N\C=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-QZQOTICOSA-N 0.000 description 3
- 229960001940 sulfasalazine Drugs 0.000 description 3
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 3
- 239000000829 suppository Substances 0.000 description 3
- 238000001356 surgical procedure Methods 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- 230000009466 transformation Effects 0.000 description 3
- 230000036269 ulceration Effects 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- 208000016261 weight loss Diseases 0.000 description 3
- 238000001262 western blot Methods 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- JVTIXNMXDLQEJE-UHFFFAOYSA-N 2-decanoyloxypropyl decanoate 2-octanoyloxypropyl octanoate Chemical compound C(CCCCCCC)(=O)OCC(C)OC(CCCCCCC)=O.C(=O)(CCCCCCCCC)OCC(C)OC(=O)CCCCCCCCC JVTIXNMXDLQEJE-UHFFFAOYSA-N 0.000 description 2
- KUWPCJHYPSUOFW-YBXAARCKSA-N 2-nitrophenyl beta-D-galactoside Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1OC1=CC=CC=C1[N+]([O-])=O KUWPCJHYPSUOFW-YBXAARCKSA-N 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 2
- 229920000936 Agarose Polymers 0.000 description 2
- 108700028369 Alleles Proteins 0.000 description 2
- 208000019901 Anxiety disease Diseases 0.000 description 2
- 208000002109 Argyria Diseases 0.000 description 2
- 102100026189 Beta-galactosidase Human genes 0.000 description 2
- 241000222122 Candida albicans Species 0.000 description 2
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 2
- 206010009944 Colon cancer Diseases 0.000 description 2
- 206010010904 Convulsion Diseases 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 241000792859 Enema Species 0.000 description 2
- 206010015943 Eye inflammation Diseases 0.000 description 2
- 206010016717 Fistula Diseases 0.000 description 2
- 101710151190 Flagellin A Proteins 0.000 description 2
- 208000012671 Gastrointestinal haemorrhages Diseases 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 239000012981 Hank's balanced salt solution Substances 0.000 description 2
- 108010033040 Histones Proteins 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 208000005016 Intestinal Neoplasms Diseases 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- 206010030113 Oedema Diseases 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 108010001441 Phosphopeptides Proteins 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 206010038063 Rectal haemorrhage Diseases 0.000 description 2
- 241000582914 Saccharomyces uvarum Species 0.000 description 2
- 238000012300 Sequence Analysis Methods 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- 108010008038 Synthetic Vaccines Proteins 0.000 description 2
- 210000001744 T-lymphocyte Anatomy 0.000 description 2
- 108091023040 Transcription factor Proteins 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- 101000638142 Treponema pallidum (strain Nichols) Membrane lipoprotein TmpC Proteins 0.000 description 2
- 241000364021 Tulsa Species 0.000 description 2
- 108010046334 Urease Proteins 0.000 description 2
- 206010000269 abscess Diseases 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 230000002776 aggregation Effects 0.000 description 2
- 238000004220 aggregation Methods 0.000 description 2
- 229940113720 aminosalicylate Drugs 0.000 description 2
- 208000007502 anemia Diseases 0.000 description 2
- 230000036506 anxiety Effects 0.000 description 2
- 206010003246 arthritis Diseases 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 230000006399 behavior Effects 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 108010005774 beta-Galactosidase Proteins 0.000 description 2
- 239000003618 borate buffered saline Substances 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 229940095731 candida albicans Drugs 0.000 description 2
- 238000005251 capillar electrophoresis Methods 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 210000004534 cecum Anatomy 0.000 description 2
- 208000019902 chronic diarrheal disease Diseases 0.000 description 2
- 239000007979 citrate buffer Substances 0.000 description 2
- 238000003759 clinical diagnosis Methods 0.000 description 2
- 238000004891 communication Methods 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000036461 convulsion Effects 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 238000007405 data analysis Methods 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 239000008121 dextrose Substances 0.000 description 2
- 230000029087 digestion Effects 0.000 description 2
- VIYFPAMJCJLZKD-UHFFFAOYSA-L disodium;(4-nitrophenyl) phosphate Chemical compound [Na+].[Na+].[O-][N+](=O)C1=CC=C(OP([O-])([O-])=O)C=C1 VIYFPAMJCJLZKD-UHFFFAOYSA-L 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 238000006073 displacement reaction Methods 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 239000007920 enema Substances 0.000 description 2
- 210000003238 esophagus Anatomy 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 238000000855 fermentation Methods 0.000 description 2
- 230000004151 fermentation Effects 0.000 description 2
- 230000003890 fistula Effects 0.000 description 2
- 210000003495 flagella Anatomy 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 208000030304 gastrointestinal bleeding Diseases 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 235000014304 histidine Nutrition 0.000 description 2
- 210000003405 ileum Anatomy 0.000 description 2
- 229940124541 immunological agent Drugs 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 210000004969 inflammatory cell Anatomy 0.000 description 2
- 230000002757 inflammatory effect Effects 0.000 description 2
- 210000004347 intestinal mucosa Anatomy 0.000 description 2
- 210000000936 intestine Anatomy 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- XMBWDFGMSWQBCA-YPZZEJLDSA-N iodane Chemical compound [125IH] XMBWDFGMSWQBCA-YPZZEJLDSA-N 0.000 description 2
- 229940044173 iodine-125 Drugs 0.000 description 2
- 230000003902 lesion Effects 0.000 description 2
- 239000008297 liquid dosage form Substances 0.000 description 2
- 208000019423 liver disease Diseases 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 230000000813 microbial effect Effects 0.000 description 2
- 238000000386 microscopy Methods 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 210000003097 mucus Anatomy 0.000 description 2
- 238000007899 nucleic acid hybridization Methods 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 238000012302 perinuclear staining Methods 0.000 description 2
- 229940124531 pharmaceutical excipient Drugs 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 238000013139 quantization Methods 0.000 description 2
- 230000002787 reinforcement Effects 0.000 description 2
- 238000007894 restriction fragment length polymorphism technique Methods 0.000 description 2
- 238000003757 reverse transcription PCR Methods 0.000 description 2
- 102200157268 rs55882956 Human genes 0.000 description 2
- 238000003118 sandwich ELISA Methods 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 238000007423 screening assay Methods 0.000 description 2
- 238000011896 sensitive detection Methods 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 238000012421 spiking Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 210000002784 stomach Anatomy 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- 230000000007 visual effect Effects 0.000 description 2
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 1
- UCTWMZQNUQWSLP-VIFPVBQESA-N (R)-adrenaline Chemical compound CNC[C@H](O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-VIFPVBQESA-N 0.000 description 1
- 229930182837 (R)-adrenaline Natural products 0.000 description 1
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical group C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- AUVALWUPUHHNQV-UHFFFAOYSA-N 2-hydroxy-3-propylbenzoic acid Chemical class CCCC1=CC=CC(C(O)=O)=C1O AUVALWUPUHHNQV-UHFFFAOYSA-N 0.000 description 1
- HDBQZGJWHMCXIL-UHFFFAOYSA-N 3,7-dihydropurine-2-thione Chemical compound SC1=NC=C2NC=NC2=N1 HDBQZGJWHMCXIL-UHFFFAOYSA-N 0.000 description 1
- XMTQQYYKAHVGBJ-UHFFFAOYSA-N 3-(3,4-DICHLOROPHENYL)-1,1-DIMETHYLUREA Chemical compound CN(C)C(=O)NC1=CC=C(Cl)C(Cl)=C1 XMTQQYYKAHVGBJ-UHFFFAOYSA-N 0.000 description 1
- CKRJGDYKYQUNIM-UHFFFAOYSA-N 3-fluoro-2,2-dimethylpropanoic acid Chemical compound FCC(C)(C)C(O)=O CKRJGDYKYQUNIM-UHFFFAOYSA-N 0.000 description 1
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- YRNWIFYIFSBPAU-UHFFFAOYSA-N 4-[4-(dimethylamino)phenyl]-n,n-dimethylaniline Chemical compound C1=CC(N(C)C)=CC=C1C1=CC=C(N(C)C)C=C1 YRNWIFYIFSBPAU-UHFFFAOYSA-N 0.000 description 1
- RBCCQATUVPNPGQ-UHFFFAOYSA-N 4-hexadecylaniline Chemical compound CCCCCCCCCCCCCCCCC1=CC=C(N)C=C1 RBCCQATUVPNPGQ-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 241000893512 Aquifex aeolicus Species 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 241000606125 Bacteroides Species 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 241000605900 Butyrivibrio fibrisolvens Species 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 108010045403 Calcium-Binding Proteins Proteins 0.000 description 1
- 241000222120 Candida <Saccharomycetales> Species 0.000 description 1
- 241000282465 Canis Species 0.000 description 1
- 241000193469 Clostridium pasteurianum Species 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 238000011537 Coomassie blue staining Methods 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- 150000008574 D-amino acids Chemical class 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- KHMVXSQLPUNRCF-UHFFFAOYSA-N DL-Adalin Natural products C1CCC2CC(=O)CC1(CCCCC)N2 KHMVXSQLPUNRCF-UHFFFAOYSA-N 0.000 description 1
- 238000000018 DNA microarray Methods 0.000 description 1
- 238000001712 DNA sequencing Methods 0.000 description 1
- 102000007260 Deoxyribonuclease I Human genes 0.000 description 1
- 108010008532 Deoxyribonuclease I Proteins 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 241000282324 Felis Species 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 201000003741 Gastrointestinal carcinoma Diseases 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 241000147041 Guaiacum officinale Species 0.000 description 1
- 241001503513 Helicobacter bilis Species 0.000 description 1
- 241000590006 Helicobacter mustelae Species 0.000 description 1
- 241000590002 Helicobacter pylori Species 0.000 description 1
- 108091027305 Heteroduplex Proteins 0.000 description 1
- 102000006947 Histones Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000798114 Homo sapiens Lactotransferrin Proteins 0.000 description 1
- 108010048209 Human Immunodeficiency Virus Proteins Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010022971 Iron Deficiencies Diseases 0.000 description 1
- 208000000913 Kidney Calculi Diseases 0.000 description 1
- 239000006391 Luria-Bertani Medium Substances 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 102000016943 Muramidase Human genes 0.000 description 1
- 108010014251 Muramidase Proteins 0.000 description 1
- 208000007101 Muscle Cramp Diseases 0.000 description 1
- 241000187479 Mycobacterium tuberculosis Species 0.000 description 1
- 101100454133 Mycobacterium tuberculosis (strain ATCC 25618 / H37Rv) kstR2 gene Proteins 0.000 description 1
- 208000031888 Mycoses Diseases 0.000 description 1
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 206010029148 Nephrolithiasis Diseases 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 108091005461 Nucleic proteins Chemical group 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 108010079246 OMPA outer membrane proteins Proteins 0.000 description 1
- 241001165050 Ocala Species 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 108700006385 OmpF Proteins 0.000 description 1
- 101710203379 Outer membrane porin C Proteins 0.000 description 1
- 101710160101 Outer membrane protein C Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 208000008469 Peptic Ulcer Diseases 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241000235070 Saccharomyces Species 0.000 description 1
- 206010040943 Skin Ulcer Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 208000033809 Suppuration Diseases 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 102000004357 Transferases Human genes 0.000 description 1
- 108090000992 Transferases Proteins 0.000 description 1
- LUEWUZLMQUOBSB-UHFFFAOYSA-N UNPD55895 Natural products OC1C(O)C(O)C(CO)OC1OC1C(CO)OC(OC2C(OC(OC3C(OC(O)C(O)C3O)CO)C(O)C2O)CO)C(O)C1O LUEWUZLMQUOBSB-UHFFFAOYSA-N 0.000 description 1
- 206010046851 Uveitis Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 238000000246 agarose gel electrophoresis Methods 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- AIWXJLPLVDPBHE-UHFFFAOYSA-N amino 2-hydroxybenzoate Chemical class NOC(=O)C1=CC=CC=C1O AIWXJLPLVDPBHE-UHFFFAOYSA-N 0.000 description 1
- 206010002022 amyloidosis Diseases 0.000 description 1
- 230000001188 anti-phage Effects 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- LUEWUZLMQUOBSB-MHJOMNRISA-N beta-D-Manp-(1->4)-beta-D-Manp-(1->4)-beta-D-Manp-(1->4)-D-Manp Chemical compound O[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3[C@H](OC(O)[C@@H](O)[C@H]3O)CO)[C@@H](O)[C@H]2O)CO)[C@@H](O)[C@H]1O LUEWUZLMQUOBSB-MHJOMNRISA-N 0.000 description 1
- 210000000941 bile Anatomy 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000003150 biochemical marker Substances 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000012888 bovine serum Substances 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 229960001714 calcium phosphate Drugs 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- 229960003340 calcium silicate Drugs 0.000 description 1
- 235000012241 calcium silicate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 229940075510 carbopol 981 Drugs 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 108091092356 cellular DNA Proteins 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 238000009388 chemical precipitation Methods 0.000 description 1
- 239000012504 chromatography matrix Substances 0.000 description 1
- 239000013611 chromosomal DNA Substances 0.000 description 1
- 208000037976 chronic inflammation Diseases 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 238000002052 colonoscopy Methods 0.000 description 1
- 238000004737 colorimetric analysis Methods 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000005094 computer simulation Methods 0.000 description 1
- 239000012059 conventional drug carrier Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 150000001879 copper Chemical class 0.000 description 1
- 150000004699 copper complex Chemical class 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000003935 denaturing gradient gel electrophoresis Methods 0.000 description 1
- 238000000326 densiometry Methods 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- 238000012774 diagnostic algorithm Methods 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000009266 disease activity Effects 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 210000004921 distal colon Anatomy 0.000 description 1
- 230000000857 drug effect Effects 0.000 description 1
- 210000001198 duodenum Anatomy 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 238000001839 endoscopy Methods 0.000 description 1
- 229940095399 enema Drugs 0.000 description 1
- 229940079360 enema for constipation Drugs 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 229960005139 epinephrine Drugs 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 230000005713 exacerbation Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 230000002550 fecal effect Effects 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 238000004401 flow injection analysis Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 238000002875 fluorescence polarization Methods 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 210000002175 goblet cell Anatomy 0.000 description 1
- 229940091561 guaiac Drugs 0.000 description 1
- 150000003278 haem Chemical class 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229940037467 helicobacter pylori Drugs 0.000 description 1
- 208000035861 hematochezia Diseases 0.000 description 1
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 150000002411 histidines Chemical class 0.000 description 1
- 102000050459 human LTF Human genes 0.000 description 1
- 229940098197 human immunoglobulin g Drugs 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 210000003767 ileocecal valve Anatomy 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 238000010820 immunofluorescence microscopy Methods 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000010365 information processing Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 208000003243 intestinal obstruction Diseases 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007914 intraventricular administration Methods 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- 208000018937 joint inflammation Diseases 0.000 description 1
- 210000002429 large intestine Anatomy 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 238000007477 logistic regression Methods 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 239000008176 lyophilized powder Substances 0.000 description 1
- 125000003588 lysine group Chemical class [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 239000004325 lysozyme Substances 0.000 description 1
- 229960000274 lysozyme Drugs 0.000 description 1
- 235000010335 lysozyme Nutrition 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 125000000311 mannosyl group Chemical group C1([C@@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000013178 mathematical model Methods 0.000 description 1
- 238000000816 matrix-assisted laser desorption--ionisation Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000000329 molecular dynamics simulation Methods 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 210000000214 mouth Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 238000003062 neural network model Methods 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 230000036963 noncompetitive effect Effects 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 238000013021 overheating Methods 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 239000000123 paper Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 208000011906 peptic ulcer disease Diseases 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 238000003322 phosphorimaging Methods 0.000 description 1
- INAAIJLSXJJHOZ-UHFFFAOYSA-N pibenzimol Chemical compound C1CN(C)CCN1C1=CC=C(N=C(N2)C=3C=C4NC(=NC4=CC=3)C=3C=CC(O)=CC=3)C2=C1 INAAIJLSXJJHOZ-UHFFFAOYSA-N 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 102000054765 polymorphisms of proteins Human genes 0.000 description 1
- WCWKKSOQLQEJTE-UHFFFAOYSA-N praseodymium(3+) Chemical compound [Pr+3] WCWKKSOQLQEJTE-UHFFFAOYSA-N 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000012342 propidium iodide staining Methods 0.000 description 1
- 235000004252 protein component Nutrition 0.000 description 1
- 238000004451 qualitative analysis Methods 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 238000012419 revalidation Methods 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 238000007480 sanger sequencing Methods 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- HOZOZZFCZRXYEK-HNHWXVNLSA-M scopolamine butylbromide Chemical compound [Br-].C1([C@@H](CO)C(=O)OC2C[C@@H]3[N+]([C@H](C2)[C@@H]2[C@H]3O2)(C)CCCC)=CC=CC=C1 HOZOZZFCZRXYEK-HNHWXVNLSA-M 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 210000004739 secretory vesicle Anatomy 0.000 description 1
- 238000012882 sequential analysis Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 231100000019 skin ulcer Toxicity 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000012128 staining reagent Substances 0.000 description 1
- 239000012058 sterile packaged powder Substances 0.000 description 1
- 238000013530 stochastic neural network Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000013517 stratification Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 210000004876 tela submucosa Anatomy 0.000 description 1
- MPLHNVLQVRSVEE-UHFFFAOYSA-N texas red Chemical compound [O-]S(=O)(=O)C1=CC(S(Cl)(=O)=O)=CC=C1C(C1=CC=2CCCN3CCCC(C=23)=C1O1)=C2C1=C(CCC1)C3=[N+]1CCCC3=C2 MPLHNVLQVRSVEE-UHFFFAOYSA-N 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- 230000007306 turnover Effects 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 238000005199 ultracentrifugation Methods 0.000 description 1
- 239000005526 vasoconstrictor agent Substances 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
- 108010088577 zinc-binding protein Proteins 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/564—Immunoassay; Biospecific binding assay; Materials therefor for pre-existing immune complex or autoimmune disease, i.e. systemic lupus erythematosus, rheumatoid arthritis, multiple sclerosis, rheumatoid factors or complement components C1-C9
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/06—Gastro-intestinal diseases
- G01N2800/065—Bowel diseases, e.g. Crohn, ulcerative colitis, IBS
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Hematology (AREA)
- Engineering & Computer Science (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Rehabilitation Therapy (AREA)
- Biotechnology (AREA)
- Rheumatology (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Peptides Or Proteins (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
世界的に発生し、そして数百万の人々を苦しめている炎症性腸疾患(IBD)は、病因不明の3つの胃腸疾患:クローン病(CD)、潰瘍性大腸炎(UC)、及び分類不能大腸炎(indeterminate colitis)(IC)を表現するのに用いられる総称である。IBDは、過敏性腸症候群(IBS)と共に、米国人全体の半数が一生の間には罹る疾患であり、その費用はIBDでは26億ドル以上及びIBSでは80億ドル以上である。このような高額な医療費の一次決定因子は、消化器疾患を診断することの困難性にある。IBD及びIBSの費用は、これらの疾患を患う人達が米国の国内平均より年に少なくとも8日も多くの日数労働を休んでいる関係から、生産性の損失によっていっそう嵩んでいる。
(a)小児個体から前記試料を得ること;
(b)前記試料を転換して(transforming)1種又は2種以上のマーカーの存在又はレベルを測定すること、ここでマーカーは抗フラジェリン抗体を含むものとし;そして
(c)前記抗フラジェリン抗体を含む1種又は2種以上のマーカーの存在又はレベルに基づき統計的アルゴリズムを用いて前記試料をIBD試料又は非IBD試料と分類すること
を含む前記分類方法を提供する。
(a)小児個体から前記試料を得ること;
(b)前記試料を転換して1種又は2種以上のマーカーの存在又はレベルを測定すること、ここでマーカーは抗フラジェリン抗体を含むものとし;そして
(c)前記抗フラジェリン抗体を含む1種又は2種以上のマーカーの存在又はレベルに基づき統計的アルゴリズムを用いて前記試料をIBD試料又は非IBD試料と分類すること
を含む前記診断方法を提供する。
本明細書中で用いる下記の用語は、他に断らない限り、その用語が本来有していると考えられる意味を持つ。
患者、例えば、炎症性腸疾患(IBD)に罹っている小児患者を診断することは、IBDと他の疾患又は障害との間の症状の類似性のゆえに困難であるということができる。本発明は、一定の診断マーカーとりわけ抗フラジェリン抗体(例えば、抗CBir−1抗体)の存在及びレベルを検出することによって、小児個体由来の生物学的試料をIBD(例えば、CD又はUC)試料と分類することの的確性(accuracy)を実質的に改善することができるという意外な発見に一部基づいている。「抗フラジェリン抗体」という用語は本明細書中で用いる場合、例えば、参考までに本明細書に引用するPCT特許公報第WO03/053220号及び米国特許第7,361,733号に記載のように細菌鞭毛(bacterial flagella)のタンパク質成分に対する抗体を含む。「フラジェリン」という用語は、抗フラジェリン抗体と免疫反応性である細菌鞭毛タンパク質を含む。微生物のフラジェリンは、中空の円筒内にそれら自体を配列してフィラメントを形成する細胞鞭毛に見出されるタンパク質である。
(a)小児個体から前記試料を得ること;
(b)前記試料を転換して1種又は2種以上のマーカーの存在又はレベルを測定すること、ここでマーカーは抗フラジェリン抗体を含むものとし;そして
(c)前記抗フラジェリン抗体を含む1種又は2種以上のマーカーの存在又はレベルに基づき統計的アルゴリズムを用いて前記試料をIBD試料又は非IBD試料と分類すること
を含む前記分類方法を提供する。
(a)小児個体から前記試料を得ること;
(b)前記試料を転換して1種又は2種以上のマーカーの存在又はレベルを測定すること、ここでマーカーは抗フラジェリン抗体を含むものとし;そして
(c)前記抗フラジェリン抗体を含む1種又は2種以上のマーカーの存在又はレベルに基づき統計的アルゴリズムを用いて前記試料をIBD試料又は非IBD試料と分類すること
を含む前記診断方法を提供する。
(a)小児個体由来の試料中の抗フラジェリン抗体(例えば、抗CBir−1抗体)及び場合により抗好中球抗体、抗サッカロミセス・セレビシエ抗体、抗菌抗体及びそれらの組み合わせからなる群から選択される少なくとも1種の追加のマーカーの存在又はレベルを測定すること;及び
(b)前記抗フラジェリン抗体及び場合により少なくとも1種の追加のマーカーの存在又はレベルに基づき統計的アルゴリズムを用いて前記小児個体におけるIBDの存在又は重症度を決定すること
を含む方法を提供する。
(a)前記小児個体由来の試料中の抗フラジェリン抗体(例えば、抗CBir−1抗体)及び場合により抗好中球抗体、抗サッカロミセス・セレビシエ抗体、抗菌抗体、及びそれらの組み合わせからなる群から選択される少なくとも1種の追加のマーカーの存在又はレベルを測定すること;及び
(b)抗フラジェリン抗体及び場合により少なくとも1種の追加のマーカーの存在又はレベルに基づき統計的アルゴリズムを用いて小児個体におけるIBDの存在又は重症度を決定すること
を含む方法を提供する。
(a)抗フラジェリン抗体及び場合により抗好中球抗体、抗サッカロミセス・セレビシエ抗体、抗菌抗体、及びそれらの組み合わせからなる群から選択される少なくとも1種の追加のマーカーの試料中の存在又はレベルを示すデータ集合を生成するように構成されたデータ取得モジュール;
(b)前記データ集合に統計処理を適用することによって前記データ集合を処理して、抗フラジェリン抗体及び場合により少なくとも1種の追加のマーカーの存在又はレベルに基づいて試料をIBD試料又は非IBD試料と分類する統計的に導かれた決定を生成するように構成されたデータ処理モジュール;及び
(c)前記統計的に導かれた決定を表示するように構成された表示モジュール
を含む前記システムを提供する。
(a)抗フラジェリン抗体及び場合により抗好中球抗体、抗サッカロミセス・セレビシエ抗体、抗菌抗体、及びそれらの組み合わせからなる群から選択される少なくとも1種の追加のマーカーの試料中の存在又はレベルを示すデータ集合を生成するように構成されたデータ取得モジュール;
(b)前記データ集合に統計処理を適用することによって前記データ集合を処理して、抗フラジェリン抗体及び場合により少なくとも1種の追加のマーカーの存在又はレベルに基づいて試料をCD試料、UC試料、又は非IBD試料と分類する統計的に導かれた決定を生成するように構成されたデータ処理モジュール;及び
(c)前記統計的に導出された決定を表示するように構成された表示モジュール
を含む前記システムを提供する。
クローン病(CD)は、消化管のあらゆる部分を含むことがある慢性炎症の疾患である。一般に、小腸の遠位部、すなわち、回腸、及び盲腸が冒される。他の場合に、疾患は小腸、結腸、又は肛門直腸の部位に限定される。CDは、十二指腸及び胃に影響を及ぼすことがあり、そしてよりまれには食道及び口腔に影響を及ぼすことがある。
種々の炎症性腸疾患(IBD)マーカー、例えば、生化学的マーカー、血清学的マーカー、遺伝学的マーカー、又は他の臨床上若しくは超音波検査上の特徴は、例えば小児個体由来の試料をIBD試料と分類することによる、IBDの決定のために本発明の統計的アルゴリズムに用いるのに適している。本明細書中に記載のIBDマーカーは、例えば小児個体由来の試料をCD試料又はUC試料と分類することによって、IBDの臨床的サブタイプ間を識別するために本発明の統計的アルゴリズムに用いるのにも適している。本発明に用いるのに適当なマーカーの例として、限定的でなく、抗フラジェリン抗体(例えば、抗CBir−1抗体)、抗好中球抗体(例えば、ANCA、pANCA、cANCA、NSNA、SAPPA等)、抗サッカロミセス・セレビシエ抗体(例えば、ASCA−IgA、ASCA−IgG、ASCA−IgM等)、抗菌抗体(例えば、抗OmpC抗体、他の抗フラジェリン抗体、抗I2抗体等)、ラクトフェリン、抗ラクトフェリン抗体、エラスターゼ、C反応性タンパク質(CRP)、カルプロテクチン、ヘモグロビン、NOD2/CARD15、及びそれらの組み合わせを挙げることができる。本発明の統計的アルゴリズムに用いるのに適当なさらなるマーカーがあることは当業者に公知であろう。
当該技術分野で公知の任意の種類の分析、方法、及びキットを用いて、試料中の1種又は2種以上のマーカーの存在又はレベルを測定して当該試料がIBD又はその臨床的サブタイプと関連しているか否かを分類することができる。
或る観点において、本発明は、試料をIBD試料又は非IBD試料と分類する統計的アルゴリズム又は統計処理を用いて試料がIBDと関連しているか否かを分類する方法、システム、及びコードを提供する。他の観点において、本発明は、試料をCD試料、UC試料、又は非IBD試料と分類する統計的アルゴリズム又は統計処理を用いて試料がIBDの臨床的サブタイプと関連しているか否かを分類する(すなわち、CDとUCとの間を識別する)方法、システム、及びコードを提供する。好ましくは、複数の統計的アルゴリズム又は統計処理は、独立して、1つ又は2つ以上の学習統計的分類子システムを含む。本明細書中に記載のように、学習統計的分類子システムの組み合わせは、有利には、試料がIBD又はその臨床的サブタイプと関連しているか否かを分類するための改善された感度、特異度、陰性的中率、陽性的中率、及び/又は総体的的確性を提供する。
図1は、本発明の1つの態様による疾患分類システム(DCS)(100)を表す。図1に示すように、DCSは、プロセッサ(115)及びメモリモジュール(110)を備えた、DCSインテリジェンスモジュール(105)、例えば、コンピュータを含む。インテリジェンスモジュールは、1つ又は2つ以上の直接接続(direct connection)(例えば、USB、Firewire、又は他のインターフェース)及び1つ又は2つ以上のネットワーク接続(例えば、モデム又は他のネットワークインターフェース機器を含む)を通じて情報を送信及び受信するための通信モジュール(図示せず)も含む。メモリモジュールは、内部メモリ装置及び1つ又は2つ以上の外部メモリ装置を含んでいることができる。インテリジェンスモジュールは、ディスプレイモジュール(125)、例えば、モニター又はプリンターも含んでいる。1つの観点において、インテリジェンスモジュールは、データ、例えば、直接接続を介して又はネットワーク(140)を通じて、データ収集モジュール、例えば、試験システム(150)からの患者試験結果、を受け取る。例えば、試験システムは、1つ又は2つ以上の患者試料(155)についてマルチアナライト(multianalyte)試験を行いそしてその試験結果をインテリジェンスモジュールに自動的に提供するように構成することができる。データは、ユーザーによる直接入力を介してインテリジェンスモジュールに提供することもでき、又はポータブル媒体、例えば、コンパクトディスク(CD)又はデジタル多用途ディスク(DVD)からダウンロードすることができる。試験システムは、インテリジェンスモジュールに直結させて、インテリジェンスモジュールと統合させることができ、又はネットワークを通じてインテリジェンスモジュールとリモート結合させることができる。インテリジェンスモジュールは、周知であるようなネットワークを通じて1つ又は2つ以上のクライアントシステム(130)へ及びそこからデータ通信することもできる。例えば、要求中の医師又はヘルスケア提供者は、クライアントシステム(130)を用いて、研究室又は病院に置かれている(resident)ことができるインテリジェンスモジュールからレポートを取得及び閲覧することができる。
小児個体由来の試料がIBD(例えば、CD又はUC)試料と分類された後は、本発明の方法、システム、及びコードはさらにその小児個体にIBD又はIBDサブタイプと関連した1種又は2種以上の症状を治療するのに有効な薬剤の治療的有効量を投与することを含んでいることができる。治療のために、IBD薬は、単独で投与することができ、又は1種若しくは2種以上の追加のIBD薬及び/又はIBD薬と関連した副作用を軽減する1種若しくは2種以上の薬剤と組み合わせて同時投与することができる。
以下の実施例は、限定的な意図でなく、特許請求の範囲に記載の発明を説明するために提供するものである。
この実施例は、ELISA分析を用いた試料中のANCAレベルの分析を説明する。
本実施例は、例えば、米国特許第5,750,355号及び第5,830,675号に記載のように蛍光免疫測定法を用いて試料中のpANCAの有無を分析することを説明する。とりわけ、pANCAの存在は、DNaseを用いた好中球の処理後の陽性値の欠如(例えば、検出可能な抗体マーカー及び/又は対照と比較した場合の特異的な細胞の染色パターンの欠如)について測定することによって検出される。
1.充分な容積の1Xハンクス平衡塩類溶液(HBSS)中に好中球を再懸濁させて細胞約2.5×106個/mLを達成する。
2.Cytospin3遠心分離機(Shandon社;Pittsburgh,PA)を500rpmで5分間用いて、再懸濁させた好中球0.01mLを各スライドに付与する。
3.試料を覆うのに充分な容積の100%エタノール中でスライドを10分間インキュベートすることによりスライドに好中球を固定化する。空気乾燥させる。スライドは−20℃で保存することができる。
1.トリス−HCl(pH7.9)40mM、塩化ナトリウム10mM、塩化マグネシウム6mM、及び塩化カルシウム10mMを含む緩衝液1mL当たりにPromega RQ1(商標)DNase(Promega;Madison,WI)3単位を混合することによりDNase溶液を調製する。
2.リン酸緩衝生理食塩水(pH7.0〜7.4)約100mLを用いて、前記プロトコールを用いて調製したスライドを5分間リンスする。各スライド当たりDNase溶液0.05mL中で37℃において約30分間、固相化された好中球をインキュベートする。リン酸緩衝生理食塩水100〜250mLを用いて室温においてスライドを3回洗浄する。本明細書中に記載のように実施したDNase反応は、核又は細胞の好中球の形態に有意な変化を起こすことなく細胞のDNAの実質的に完全な消化を生じさせる。
1.DNaseで処理したスライド及び処理していないスライドに、リン酸緩衝生理食塩水中の1:20希釈のヒト血清0.05mLを添加する。ブランクとしてクリーンなスライドにリン酸緩衝生理食塩水0.05mLを添加する。容積損失を最小にするのに充分な湿度において室温で約0.5〜1.0時間インキュベートする。
2.リン酸緩衝生理食塩水100〜250mLを含む容器に浸漬することによって血清を洗い流す。
3.リン酸緩衝生理食塩水中に5分間スライドを浸漬する。軽く吸い取って乾かす。
4.希釈度1:1000の抗体:リン酸緩衝生理食塩水の、ヤギF(ab’)2抗ヒトIgG(μ)−FITC(Tago Immunologicals;Burlingame,CA)0.05mLを各スライドに添加する。容積損失を最小にするのに充分な湿度において室温で30分間インキュベートする。
5.リン酸緩衝生理食塩水100〜250mLを用いて抗体を洗い流す。リン酸緩衝生理食塩水100〜250mL中に5分間スライドを浸漬し、次いで空気乾燥させる。
6.蛍光顕微鏡により40Xで蛍光パターンを読む。
7.望ましい場合には、リン酸緩衝生理食塩水を用いて室温で充分にスライドをリンスし、そして室温で10秒間染色することによりヨウ化プロピジウム染色試薬によってDNAを染色することができる。リン酸緩衝生理食塩水100〜250mLを用いて室温においてスライドを3回洗浄し、そしてカバーガラスを乗せる。
本実施例は、酵母細胞ウェル(well)マンナンの調製及びELISA分析を用いた試料中のASCAレベルの分析を説明する。
本実施例は、OmpCタンパク質の調製及びELISAアッセイ分析を用いた試料中の抗OmpC抗体レベルの分析を説明する。
本実施例は、組換えI2タンパク質の調製及びELISA分析又は組織学的分析を用いた試料中の抗I2抗体レベルの分析を説明する。
本実施例は、血清学的マーカーのパネルを用いて試料がIBD又はその臨床的サブタイプと関連しているか否かを分類する学習統計的分類子システムを組み合わせることから導かれる診断的アルゴリズムを説明する。
血清学的試験は、医師が炎症性腸疾患(IBD)の診断を行い及び疾患をクローン病(CD)又は潰瘍性大腸炎(UC)と分類するのを補助することができる。IBDに対する血清学的試験として、例えば、ASCA(IgA及びIgG)、抗OmpC、抗CBir1及びpANCAの分析を挙げることができる。本実施例に記載のIBD血清学的マーカー解析に対する1つのアルゴリズム的アプローチは、統計的分類子からなる高性能なコンピュータを用いた解析とそれに続くニューラルネットワークである。本実施例において、分析結果はカットオフ値との比較をせずに、むしろアルゴリズムによって疾患及び非疾患のパターンを検出する。本実施例では、863例の健常及び胃腸の対照、633例のCD、及び556例のUCからなる既知の診断を有する2,052例の血清試料のコホートを用いる。
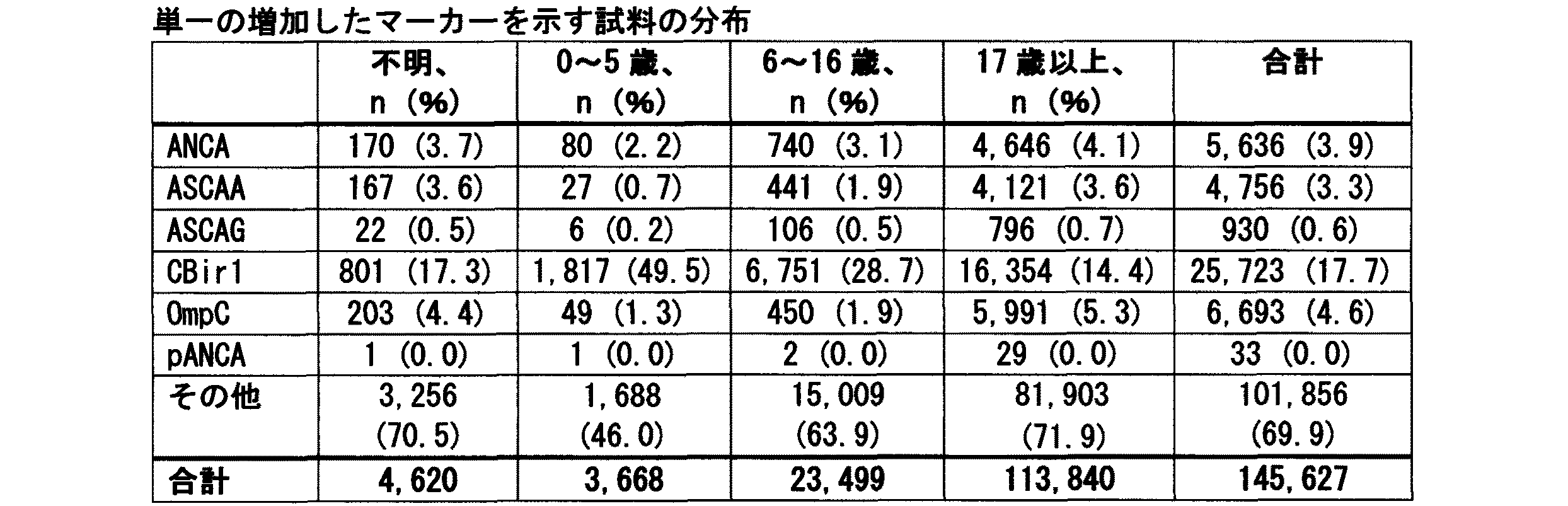
本実施例において、145,627例の同定されていない試験結果のデータベースを臨床的洞察のためにマイニングした。13の正規化されたテーブルを含むリレーショナル臨床データベース(PrOS)のクエリーを行ない、そしてオープンソースソフトウェアパッケージRを用いて連続的な密度プロットを形成した。年齢分布は二峰性であった。分離したピークが年齢15〜20歳について観察され、そして次に、より広いプラトーが年齢20〜55歳について見られた。臨床データベースにおける個々のマーカー値の分布は、訓練/検証コホート(N=2,052)に用いられた分布より正規分布していた。大部分のマーカー分布は臨床データベースでより低かったが、これは多くの試料が健常者又は非IBD患者に由来するためと考えることができる。顕著な例外は抗CBir1であり、訓練/検証の場合より臨床的データベースにおいて高い分布を示した。臨床データベースにおける性別分布は患者の年齢と共に変化した。分布は成人で女性に偏っており(63%/37%)、年齢6〜16歳の年長児童で等しく(51%/49%)、そして幼児で男性に偏っていた(44%/56%)。小児の場合(年齢0〜5歳)の診断基準には有意な差があった。小児患者の高レベルの抗CBir1は、小児のクローン病を予測するアルゴリズムによって用いられる重要な要素である。ASCA IgA及びASCA IgGのような他のマーカーの高いレベルは、クローン病罹患と診断された小児においては一般に観察されなかった。これらの年齢に基づく差異がアルゴリズムにより明確に「表現」されなかった20%の小児ケースについて、本アルゴリズムがその訓練データの多様性に基づいて前記の差異を自動的に発見して利用したことは注目すべきことである。この臨床データの解析は、臨床的生成(clinical production)データとIBD診断試験を開発するのに最初に用いられた訓練/検証データとの間の類似性及び関係を明らかにするのに有益な手段である。
表2〜6は年齢及び性別分布を示す。実際に、年齢分布は二峰性であった(図5)。分離したピークが年齢15〜20歳について観察され、そして次に、より広いプラトーが年齢20〜55歳について見られた。性別分布は患者の年齢と共に変化した。分布は成人で女性に偏っており、年長児童で等しく、そして幼児で男性に偏っていた。全ての年齢群にわたって有病率はUC予測に対しCD予測の方がより高く、最大の差が年齢0〜5歳群において観察された。
図6は、臨床的予測に対する開発コホート及びマーカーの分布を示す。概して、データは、マーカー分布が訓練/検証の場合より生成臨床データベースの場合の方が低かったことを示す。例外は抗CBir1であり、臨床データベースの場合の方が高かった。個々のマーカー値の分布は対数正規分布(対数変換後に正規分布)であり、訓練/検証コホートに用いられたデータより臨床データの方が正規分布していた。
図7は、診断予測により階層化されたマーカーのチャートを示す。4つの横列1)全て;2)非IBD;3)CD及び4)UCが設けられている。5つの縦列は、マーカー1)ANCA;2)OmpC;3)ASCAA;4)ASCAG及び5)CBir1を示す。診断予測を行なうのに用いられるマーカーは年齢により変化する。例えば、CD診断(第3横列)において、抗CBir1(第5縦列)は小児において増加する(点線対実線)。
図8は、年齢により階層化されたマーカーのチャートを示す。4つの横列1)全て;2)0〜5歳;3)6〜16歳及び4)17歳以上が設けられている。5つの縦列は、マーカー1)ANCA;2)OmpC;3)ASCAA;4)ASCAG及び5)CBir1を示す。成人の場合に、CD診断予測はASCAA及び抗CBir1の両方のレベル増加と関連している(実線矢印)。小児の場合には、CD診断予測は抗CBir1のレベル増加と関連しているがASCAAとは関連していない(破線)。
実質的な(n=145,627)臨床データベースを用いてPROMETHEUS IBD Serology 7の遡及的(retrospective)分析を行い、以下の結論に至った。
Prometheus IBD Serology 7試験を開発し、そして全体の大きさが2,052例の患者試料であるコホートを用いて検証した。この解析において、幅広いさまざまな一般的な臨床胃腸病学サイトからの追加の1,574例の試料を加えることにより開発コホートを拡大した。この拡大した開発コホートを用いて、スマートアルゴリズム法(すなわち、拡大したコホートを用いた再訓練及び再検証)を再適用し、以下の知見を得た。
IBDの診断における血清学的マーカーの役割は、科学文献に十分に報告されてきた。一定の血清学的マーカーの経時的な挙動及び診断予測一致性のレベルへのそれらのマーカーの影響をより良く理解するために、マーカー濃度及び診断予測の臨床データベースをクエリーを行なった。
Claims (14)
- 小児被験者由来の試料が炎症性腸疾患(IBD)と関連しているか否かを分類する方法であって、
(a)前記試料を転換して2種以上のマーカーの存在又はレベルを測定すること、ここでマーカーは抗フラジェリン抗体及びASCA−IgAを含むものとし;そして
(b)前記抗フラジェリン抗体及び前記ASCA−IgAを含む2種以上のマーカーの存在又はレベルに基づき前記試料からパターンを形成すること;そして
(c)統計的アルゴリズムを用いて前記試料をIBD試料又は非IBD試料と分類することを含み、
前記統計的アルゴリズムが前記2種以上のマーカーのパターンをIBDパターン又は非IBDパターンとして認識し、前記IBDパターンがクローン病(CD)パターン及び潰瘍性大腸炎(UC)パターンを含み、前記非IBDパターンが健常パターン及び胃腸の対象パターンを含み、
前記IBD試料がクローン病試料であり、前記クローン病試料中の前記ASCA−IgAのレベルが、非IBD試料と比較して増加しない、前記分類方法。 - 前記抗フラジェリン抗体が抗CBir−1抗体である、請求項1に記載の方法。
- 前記抗CBir−1抗体のレベルが非IBD試料と比べIBD試料で増加する、請求項2に記載の方法。
- 2種以上のマーカーがANCA、pANCA、ASCA−IgG、抗OmpC抗体、及びそれらの組み合わせからなる群から選択される1又は複数のマーカーを更に含む、請求項1に記載の方法。
- 2種以上のマーカーがASCA−IgGを更に含む、請求項1に記載の方法。
- 非IBD試料と比較して、IBD試料中の前記ASCA−IgGのレベルが同じである、請求項5に記載の方法。
- 小児被験者由来の試料が炎症性腸疾患(IBD)と関連しているか否かを診断するためのデータ取得方法であって、
(a)前記試料を転換して2種以上のマーカーの存在又はレベルを測定すること、ここでマーカーは抗フラジェリン抗体及びASCA−IgAを含むものとし;そして
(b)前記抗フラジェリン抗体及び前記ASCA−IgAを含む2種以上のマーカーの存在又はレベルに基づき前記試料からパターンを形成すること;そして
(c)統計的アルゴリズムを用いて前記試料をIBD試料又は非IBD試料と分類することを含み、
前記統計的アルゴリズムが前記2種以上のマーカーのパターンをIBDパターン又は非IBDパターンとして認識し、前記IBDパターンがクローン病(CD)パターン及び潰瘍性大腸炎(UC)パターンを含み、前記非IBDパターンが健常パターン及び胃腸の対象パターンを含み、
前記IBD試料がクローン病試料であり、前記クローン病試料中の前記ASCA−IgAのレベルが、非IBD試料と比較して増加しない、前記データ取得方法。 - 前記抗フラジェリン抗体が抗CBir−1抗体である、請求項7に記載の方法。
- 前記抗CBir−1抗体のレベルが非IBD試料と比べIBD試料で増加する、請求項8に記載の方法。
- 2種以上のマーカーがANCA、pANCA、ASCA−IgG、抗OmpC抗体、及びそれらの組み合わせからなる群から選択される1又は複数のマーカーを更に含む、請求項7に記載の方法。
- 2種以上のマーカーがASCA−IgGを更に含む、請求項7に記載の方法。
- 非IBD試料と比較して、IBD試料中の前記ASCA−IgGのレベルが同じである、請求項11に記載の方法。
- 前記統計的アルゴリズムが単一の学習統計的分類子システム、又は少なくとも2種以上の学習統計的分類子システムの組み合わせである、請求項1又は7に記載の方法。
- 前記少なくとも2種以上の学習統計的分類子システムがランダムフォレストである、請求項13に記載の方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11353708P | 2008-11-11 | 2008-11-11 | |
| US61/113,537 | 2008-11-11 | ||
| US11834608P | 2008-11-26 | 2008-11-26 | |
| US61/118,346 | 2008-11-26 | ||
| PCT/US2009/063924 WO2010056682A2 (en) | 2008-11-11 | 2009-11-10 | Methods for prediction of inflammatory bowel disease (ibd) using serologic markers |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012508383A JP2012508383A (ja) | 2012-04-05 |
| JP5749652B2 true JP5749652B2 (ja) | 2015-07-15 |
Family
ID=42170662
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011535773A Expired - Fee Related JP5749652B2 (ja) | 2008-11-11 | 2009-11-10 | 血清学的マーカーを用いた炎症性腸疾患(ibd)の予測方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20100129838A1 (ja) |
| EP (1) | EP2359137A4 (ja) |
| JP (1) | JP5749652B2 (ja) |
| AU (1) | AU2009314259B2 (ja) |
| CA (1) | CA2794757A1 (ja) |
| WO (1) | WO2010056682A2 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010062960A2 (en) | 2008-11-26 | 2010-06-03 | Cedars-Sinai Medical Center | METHODS OF DETERMINING RESPONSIVENESS TO ANTI-TNFα THERAPY IN INFLAMMATORY BOWEL DISEASE |
| EP2960342A1 (en) * | 2009-04-14 | 2015-12-30 | Nestec S.A. | Inflammatory bowel disease prognostics |
| JP5631635B2 (ja) * | 2010-06-03 | 2014-11-26 | オリンパスメディカルシステムズ株式会社 | 医療業務支援装置 |
| CA2830362A1 (en) * | 2011-03-25 | 2012-10-04 | Dermot P. Mcgovern | Methods of diagnosing and treating intestinal granulomas and low bone density in inflammatory bowel disease |
| WO2015067913A1 (en) | 2013-11-07 | 2015-05-14 | Diagnodus Limited | Biomarkers |
| EP2769321B1 (en) * | 2011-10-21 | 2016-06-01 | Nestec S.A. | Methods for improving inflammatory bowel disease diagnosis |
| EP2978440B1 (en) | 2013-03-27 | 2019-10-02 | Cedars-Sinai Medical Center | Treating fibrosis by inhibiting tl1a and diagnosing fibrosis by detecting il31ra |
| US10316083B2 (en) | 2013-07-19 | 2019-06-11 | Cedars-Sinai Medical Center | Signature of TL1A (TNFSF15) signaling pathway |
| CA2932571A1 (en) | 2013-12-03 | 2015-06-11 | Nestec S.A. | Methods for predicting post-operative recurrence of crohn's disease |
| CN105849769A (zh) | 2013-12-24 | 2016-08-10 | 索尼公司 | 检查服务器、通信终端、检查系统、以及检查方法 |
| JP2015207111A (ja) | 2014-04-18 | 2015-11-19 | ソニー株式会社 | 検査サーバ、検査方法および検査システム |
| CN118773299A (zh) | 2016-03-17 | 2024-10-15 | 西达-赛奈医疗中心 | 通过rnaset2诊断炎性肠病的方法 |
| CN116973572A (zh) * | 2023-06-02 | 2023-10-31 | 东南大学附属中大医院 | 基于血、粪便铁蛋白检测评估肠屏障损伤严重程度的方法 |
Family Cites Families (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4277250A (en) | 1979-12-10 | 1981-07-07 | Baylor College Of Medicine | Methods for detecting and quantifying occult blood |
| JPH0684970B2 (ja) | 1987-03-31 | 1994-10-26 | 株式会社京都医科学研究所 | 糞便中の潜血検出方法 |
| US5081040A (en) | 1987-06-29 | 1992-01-14 | Helena Laboratories Corporation | Composition and kit for testing for occult blood in human and animal excretions, fluids, or tissue matrixes |
| JPH0736013B2 (ja) | 1991-04-27 | 1995-04-19 | 一男 田畑 | 潜血検出用試薬 |
| US5885527A (en) | 1992-05-21 | 1999-03-23 | Biosite Diagnostics, Inc. | Diagnostic devices and apparatus for the controlled movement of reagents without membrances |
| EP0615129B1 (en) | 1993-03-10 | 2000-05-31 | Cedars-Sinai Medical Center | Methods for selectively detecting perinuclear anti-neutrophil cytoplasmic antibody of ulcerative colitis or primary sclerosing cholangitis |
| US5830675A (en) | 1993-03-10 | 1998-11-03 | Cedars-Sinai Medical Center | Methods for selectively detecting perinuclear anti-neutrophil cytoplasmic antibody of ulcerative colitis, primary sclerosing cholangitis, or type 1 autoimmune hepatitis |
| US6074835A (en) | 1996-04-12 | 2000-06-13 | Regents Of The Univ. Of California | Diagnosis, prevention and treatment of ulcerative colitis, and clinical subtypes thereof, using histone H1 |
| US5916748A (en) * | 1996-04-12 | 1999-06-29 | Cedars-Sinai Medical Center | Method of diagnosing a clinical subtype of crohn's disease with features of ulcerative colitis |
| US5932429A (en) * | 1996-04-12 | 1999-08-03 | Cedars-Sinai Medical Center | Methods of diagnosing clinical subtypes of crohn's disease |
| US6033864A (en) * | 1996-04-12 | 2000-03-07 | The Regents Of The University Of California | Diagnosis, prevention and treatment of ulcerative colitis, and clinical subtypes thereof, using microbial UC pANCA antigens |
| US6218129B1 (en) * | 1998-05-15 | 2001-04-17 | Prometheus Laboratories, Inc. | Inflammatory bowel disease first step assay system |
| US6406862B1 (en) | 1998-10-06 | 2002-06-18 | The United States Of America As Represented By The Secretary Of The Army | Dip-stick assay for C-reactive protein |
| US6309643B1 (en) | 1999-04-30 | 2001-10-30 | The Regents Of The University Of California | IBD-associated microbial antigens and methods of using same |
| FR2802536B1 (fr) | 1999-11-23 | 2003-06-13 | Chru Lille | Oligomannosides de synthese, leur preparation et leur utilisation a la detection d'anticorps et a la prevention d'infections |
| FR2806739B1 (fr) | 2000-03-27 | 2005-02-18 | Fond Jean Dausset Ceph | Genes impliques dans les maladies inflammatoires de l'intestin et leur utilisation |
| US6838250B2 (en) | 2000-03-31 | 2005-01-04 | Ortho-Clinical Diagnostics, Inc. | Immunoassay for C-reactive protein |
| US7138237B1 (en) | 2000-05-19 | 2006-11-21 | Cedars-Sinai Medical Center | Diagnosis, prevention and treatment of Crohn's disease using the OmpC antigen |
| US20050164929A1 (en) * | 2000-11-06 | 2005-07-28 | Lupine Logic, Inc. | Methods of preventing and treating inflammatory bowel disease |
| DE60138829D1 (de) | 2000-11-14 | 2009-07-09 | Techlab Inc | Verfahren zur unterscheidung des reizkolons von der entzündlichen darmerkrankung (inflammatory bowel disease, ibd) und zur überwachung von patienten mit ibd unter verwendung von endogenem gesamt-lactoferrin als marker |
| DK2224012T3 (da) * | 2001-12-17 | 2013-05-13 | Corixa Corp | Sammensætninger og fremgangsmåder til terapi og diagnose af inflammatoriske tarmsygdomme |
| US20030204507A1 (en) * | 2002-04-25 | 2003-10-30 | Li Jonathan Qiang | Classification of rare events with high reliability |
| WO2004037073A2 (en) | 2002-10-25 | 2004-05-06 | Techlab, Inc. | Inflammatory bowel disease and irritable bowel syndrome ibd-first chek diagnostic panel |
| US7662569B2 (en) * | 2003-04-11 | 2010-02-16 | Cedars-Sinai Medical Center | Methods of assessing Crohn's disease patient phenotype by I2 serologic response |
| US20040242972A1 (en) * | 2003-05-28 | 2004-12-02 | General Electric Company | Method, system and computer product for prognosis of a medical disorder |
| US20050060295A1 (en) * | 2003-09-12 | 2005-03-17 | Sensory Networks, Inc. | Statistical classification of high-speed network data through content inspection |
| EP1687447A4 (en) | 2003-11-03 | 2008-04-02 | Univ Duke | METHODS FOR IDENTIFYING INDIVIDUALS WITH PERIOPERATIVE RISK OF BLEEDING, RENAL DYSFUNCTION OR ICTUS |
| US7592150B2 (en) * | 2003-12-03 | 2009-09-22 | Glycominds, Ltd | Method for diagnosing diseases based on levels of anti-glycan antibodies |
| CA2560826C (en) * | 2004-03-23 | 2014-05-13 | Lifeline Nutraceuticals Corporation | Antioxidant-promoting herbal extract compositions for alleviating oxidative stress in a mammal |
| US20060154276A1 (en) * | 2004-05-13 | 2006-07-13 | Prometheus Laboratories Inc. | Methods of diagnosing inflammatory bowel disease |
| US20060019410A1 (en) | 2004-07-21 | 2006-01-26 | Qualyst, Inc. | Apparatus, kits and methods for evaluating binding interactions, for detecting and quantifying binding molecules, and for sample preparation |
| JP4577083B2 (ja) * | 2005-04-28 | 2010-11-10 | 味の素株式会社 | クローン病の診断方法 |
| US7873479B2 (en) * | 2005-12-01 | 2011-01-18 | Prometheus Laboratories Inc. | Methods of diagnosing inflammatory bowel disease |
| US20080085524A1 (en) * | 2006-08-15 | 2008-04-10 | Prometheus Laboratories Inc. | Methods for diagnosing irritable bowel syndrome |
| US20100015156A1 (en) * | 2007-03-06 | 2010-01-21 | Cedars-Sinai Medical Center | Diagnosis of inflammatory bowel disease in children |
-
2009
- 2009-11-10 JP JP2011535773A patent/JP5749652B2/ja not_active Expired - Fee Related
- 2009-11-10 CA CA2794757A patent/CA2794757A1/en not_active Abandoned
- 2009-11-10 US US12/615,983 patent/US20100129838A1/en not_active Abandoned
- 2009-11-10 EP EP09826631A patent/EP2359137A4/en not_active Withdrawn
- 2009-11-10 WO PCT/US2009/063924 patent/WO2010056682A2/en active Application Filing
- 2009-11-10 AU AU2009314259A patent/AU2009314259B2/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| EP2359137A2 (en) | 2011-08-24 |
| US20100129838A1 (en) | 2010-05-27 |
| EP2359137A4 (en) | 2012-05-30 |
| AU2009314259B2 (en) | 2015-06-11 |
| AU2009314259A1 (en) | 2011-07-07 |
| CA2794757A1 (en) | 2010-05-20 |
| WO2010056682A2 (en) | 2010-05-20 |
| JP2012508383A (ja) | 2012-04-05 |
| WO2010056682A3 (en) | 2010-07-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5749652B2 (ja) | 血清学的マーカーを用いた炎症性腸疾患(ibd)の予測方法 | |
| JP5634023B2 (ja) | 試料が炎症性腸疾患と関連しているか分類する方法 | |
| US7873479B2 (en) | Methods of diagnosing inflammatory bowel disease | |
| EP2769321B1 (en) | Methods for improving inflammatory bowel disease diagnosis | |
| US7759079B2 (en) | Methods of diagnosing inflammatory bowel disease | |
| CA2758531C (en) | Inflammatory bowel disease prognostics | |
| US20120171672A1 (en) | Inflammatory bowel disease prognostics | |
| JP2013511988A (ja) | 過敏性腸症候群診断用の新規なゲノムバイオマーカー | |
| EP2710383B1 (en) | Performance of a biomarker panel for irritable bowel syndrome | |
| US7943328B1 (en) | Method and system for assisting in diagnosing irritable bowel syndrome | |
| WO2017079653A2 (en) | Methods of detecting inflammatory markers and treating inflammatory conditions in companion animals | |
| US8445215B1 (en) | Assays and methods for the detection of Crohn's disease |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20120829 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121030 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130510 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130514 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130813 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130903 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20131203 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20131210 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20131225 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140108 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140304 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140603 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20141031 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141118 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141119 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150428 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150514 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5749652 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |