JP5491069B2 - 有機原材料からフッ化水素を分離するための方法 - Google Patents
有機原材料からフッ化水素を分離するための方法 Download PDFInfo
- Publication number
- JP5491069B2 JP5491069B2 JP2009118184A JP2009118184A JP5491069B2 JP 5491069 B2 JP5491069 B2 JP 5491069B2 JP 2009118184 A JP2009118184 A JP 2009118184A JP 2009118184 A JP2009118184 A JP 2009118184A JP 5491069 B2 JP5491069 B2 JP 5491069B2
- Authority
- JP
- Japan
- Prior art keywords
- chloro
- hydrogen fluoride
- tetrafluoropropane
- stream
- trifluoropropene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/38—Separation; Purification; Stabilisation; Use of additives
- C07C17/383—Separation; Purification; Stabilisation; Use of additives by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/07—Preparation of halogenated hydrocarbons by addition of hydrogen halides
- C07C17/087—Preparation of halogenated hydrocarbons by addition of hydrogen halides to unsaturated halogenated hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/25—Preparation of halogenated hydrocarbons by splitting-off hydrogen halides from halogenated hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C19/00—Acyclic saturated compounds containing halogen atoms
- C07C19/08—Acyclic saturated compounds containing halogen atoms containing fluorine
- C07C19/10—Acyclic saturated compounds containing halogen atoms containing fluorine and chlorine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C21/00—Acyclic unsaturated compounds containing halogen atoms
- C07C21/02—Acyclic unsaturated compounds containing halogen atoms containing carbon-to-carbon double bonds
- C07C21/18—Acyclic unsaturated compounds containing halogen atoms containing carbon-to-carbon double bonds containing fluorine
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
[0002]この発明は、共沸様混合物である構成物を分離するための方法に関する。より特定的には、この発明は、フッ化水素および少なくとも一種のハイドロフルオロカーボンを含む共沸様混合物からフッ化水素を分離するための方法に関する。
[0006]上記のように、HCFO−1233xfの過剰のHFとの反応は、HCFC−244bb、未反応のHF、および未反応のHCFO−1233xfを含む反応生成物を生成する。本発明者は、HFの存在がHCFC−244bbを脱塩化水素化してHFO−1234yfを形成する反応方法にとって有害であることを見出した。それ故に、HFO−1234yfの合成における出発原料として有用であるためには、HCFC−244bb原材料は好ましくは実質的にHFを含まない。
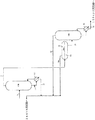
(a)フッ化水素、2−クロロ−1,1,1,2−テトラフルオロプロパン、および2−クロロ−3,3,3−トリフルオロプロペンを含む未加工の有機原材料を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第一の蒸留流と、フッ化水素が豊富な第一の底部流とを生成すること;
(b)前記第一の蒸留流を冷却して、2−クロロ−1,1,1,2−テトラフルオロプロパンおよび2−クロロ−3,3,3−トリフルオロプロペンが豊富な有機層と、フッ化水素が豊富な酸性層とを含む中間組成物を生成すること;および任意工程であるが好ましい工程として、
(c)前記有機層を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第二の蒸留流と、実質的にフッ化水素を含まない精製された有機原材料を含む第二の底部流とを生成すること;
を含む、有機原材料を精製するための方法を提供する。
(a)2−クロロ−3,3,3−トリフルオロプロペンを含む第一の供給流を、フッ化水素を含む第二の供給流、および任意に、フッ化水素を含む一つまたはそれより多くの再利用流とともに反応させて、2−クロロ−1,1,1,2−テトラフルオロプロパン、フッ化水素、および2−クロロ−3,3,3−トリフルオロプロペンを含む粗生成物流を生成すること;
(b)前記粗生成物流を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第一の蒸留流と、フッ化水素が豊富な第一の底部流とを生成すること;
(c)前記第一の蒸留流を冷却して、2−クロロ−1,1,1,2−テトラフルオロプロパンおよび2−クロロ−3,3,3−トリフルオロプロペンが豊富な有機層と、フッ化水素が豊富な酸性層とを含む中間組成物を生成すること;および任意工程であるが好ましい工程として、
(d)前記有機層を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第二の蒸留流と、2−クロロ−1,1,1,2−テトラフルオロプロパンが豊富で実質的にフッ化水素を含まない有機組成物を含む第二の底部流とを生成すること;
を含む、2−クロロ−1,1,1,2−テトラフルオロプロパンを準備するための方法を提供する。
(a)2−クロロ−3,3,3−トリフルオロプロペンを、フッ化水素とともに反応させて、2−クロロ−1,1,1,2−テトラフルオロプロパン、フッ化水素、および2−クロロ−3,3,3−トリフルオロプロペンを含む粗生成物流を生成すること;
(b)前記粗生成物流を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第一の蒸留流と、フッ化水素が豊富な第一の底部流とを生成すること;
(c)前記蒸留流を冷却して、2−クロロ−1,1,1,2−テトラフルオロプロパンおよび2−クロロ−3,3,3−トリフルオロプロペンが豊富な有機層と、フッ化水素が豊富な酸性層とを含む第一の中間組成物を生成すること;
(d)前記有機層を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第二の蒸留流と、2−クロロ−1,1,1,2−テトラフルオロプロパンが豊富で実質的にフッ化水素を含まない第二の中間組成物を含む第二の底部流とを生成すること;および
(e)前記第二の中間組成物中の2−クロロ−1,1,1,2−テトラフルオロプロパンの少なくとも一部を脱塩化水素化して、2,3,3,3−テトラフルオロプロペンを含む最終生成物を生成すること;
を含む、2,3,3,3−テトラフルオロプロペンを生成するための方法を提供する。
[0024]この実施例は本発明に従った第一の蒸留操作の効果を説明する。
[0025]およそ100lbs(5×104g)の、1233xf+HF→244bbの気相反応からの反応器流出物を蒸留カラムに充填した。蒸留カラムは10ガロン(4×10−2m3)のリボイラー、2インチ(5cm)ID×8フィート(2×102cm)のプロパックカラム、およびシェルアンドチューブ型コンデンサからなっていた。カラムは約30の理論段数を有していた。蒸留カラムは温度伝送器、圧力伝送器、および差圧伝送器を備えていた。原料の組成は約70重量%のHFおよび約30重量%の有機物(主にHCFO−1233xfおよびHCFC−244bbの混合物)であった。約100psig(7×105Pa)の圧力で蒸留を実行して、有機物を回収した。約20〜30重量%のHFを含む、総計で38lbs(1.7×104g)の蒸留物を収集した。残分は、GC分析によれば平均で55%のHCFO−1233xfおよび45%のHCFC−244bbを有した。リボイラーの底部をシリンダー分離器に排出し、主にHFを62lbs(2.8×104g)回収した。
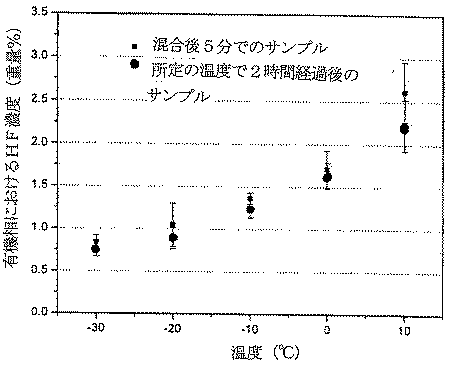
[0027]この実施例は本発明に従った液−液相分離操作の分離効果を説明する。
[0028]相分離器への供給はHF、HCFO−1233xf、およびHCFC−244bbの混合物である。有機層とHF層の分離を約+10℃〜約−30℃の範囲の温度において試した。+10℃で、最も高い濃度のHF(2.23±0.30重量%)が有機層中に検出され、−30℃で、最も低い濃度のHF(0.76±0.09重量%)が有機層中に検出された。HF層中のHF濃度は約90±5重量%だった。有機層およびHF層のGC分析は、有機層とHF層の間で有機物組成に違いが無いことを示した。
[0034]この実施例は本発明に従った第二の蒸留操作の分離効果を説明する。
[0035]蒸留カラムへの供給は、HF、1233xf、および244bbの混合物であった。およそ37.4ポンド(1.7×104g)の、44.4重量パーセントのHCFC−244bbおよび55.6重量パーセントのHCFO−1233xfからなる有機物の混合物による残分とともに3重量パーセントのHFを含有する原料を蒸留カラムに充填した。該混合物は不均一であった。蒸留カラムは10ガロン(4×10−2m3)のリボイラー、2インチ(5cm)ID×8フィート(2×102cm)のプロパックカラム、およびシェルアンドチューブ型コンデンサからなっていた。カラムは約30の理論段数を有していた。蒸留カラムは温度伝送器、圧力伝送器、および差圧伝送器を備えていた。約23−25psig(1.6×105〜1.7×105Pa)の圧力で蒸留を実施した。蒸留物をサンプリングし、HF濃度を決定するために滴定し、GCによって規則的な間隔で分析した。
[0038]この実施例もまた、本発明に従った第二の蒸留操作の分離効率を説明する。
[0041]この実施例は、本発明の実施形態に従った三工程の総合HF回収方法についての計算された原料バランスを示す。
[0043]計算のための基準および仮定は以下の通りである:100lbs(5×104g)の反応器留出物(すなわち、第一の蒸留カラムへの供給の組成物(HF回収第一工程への供給物)は65lbs(2.9×104g)のHF、35lbs(1.0×104g)の有機物(すなわち、1233xf/244bbの混合物));反応器に供給するHF対有機物のモル比は20対1である;HF回収方法の第二工程(相分離)の後の、有機層中におけるHFの重量%は2%である;HF回収方法の第二工程(相分離)の後の、HF層中における有機物の重量%は15%である。HF回収方法の三工程全てについて原料バランスを表3に示す。
Claims (3)
- (a)フッ化水素、2−クロロ−1,1,1,2−テトラフルオロプロパン、および2−クロロ−3,3,3−トリフルオロプロペンを含む未加工の有機原材料を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第一の蒸留流と、フッ化水素が豊富な第一の底部流とを生成すること;および
(b)前記第一の蒸留流を−30℃〜+10℃の温度に冷却して、2−クロロ−1,1,1,2−テトラフルオロプロパンおよび2−クロロ−3,3,3−トリフルオロプロペンが豊富な有機層と、フッ化水素が豊富な酸性層とを含む中間組成物を生成すること;
を含む、有機原材料を精製するための方法。 - (a)2−クロロ−3,3,3−トリフルオロプロペンを含む第一の供給流を、フッ化水素を含む第二の供給流、および任意に、フッ化水素を含む一つまたはそれより多くの再利用流とともに反応させて、2−クロロ−1,1,1,2−テトラフルオロプロパン、フッ化水素、および2−クロロ−3,3,3−トリフルオロプロペンを含む粗生成物流を生成すること;
(b)前記粗生成物流を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第一の蒸留流と、フッ化水素が豊富な第一の底部流とを生成すること;
(c)前記第一の蒸留流を−30℃〜+10℃の温度に冷却して、2−クロロ−1,1,1,2−テトラフルオロプロパンおよび2−クロロ−3,3,3−トリフルオロプロペンが豊富な有機層と、フッ化水素が豊富な酸性層とを含む中間組成物を生成すること;および
(d)前記有機層を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第二の蒸留流と、2−クロロ−1,1,1,2−テトラフルオロプロパンが豊富で実質的にフッ化水素を含まない有機組成物を含む第二の底部流とを生成すること;
を含む、2−クロロ−1,1,1,2−テトラフルオロプロパンを生成するための方法。 - (a)2−クロロ−3,3,3−トリフルオロプロペンを、フッ化水素とともに反応させて、2−クロロ−1,1,1,2−テトラフルオロプロパン、フッ化水素、および2−クロロ−3,3,3−トリフルオロプロペンを含む粗生成物流を生成すること;
(b)前記粗生成物流を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第一の蒸留流と、フッ化水素が豊富な第一の底部流とを生成すること;
(c)前記蒸留流を−30℃〜+10℃の温度に冷却して、2−クロロ−1,1,1,2−テトラフルオロプロパンおよび2−クロロ−3,3,3−トリフルオロプロペンが豊富な有機層と、フッ化水素が豊富な酸性層とを含む第一の中間組成物を生成すること;
(d)前記有機層を蒸留して、2−クロロ−1,1,1,2−テトラフルオロプロパン、2−クロロ−3,3,3−トリフルオロプロペン、およびフッ化水素の共沸様組成物を含む第二の蒸留流と、2−クロロ−1,1,1,2−テトラフルオロプロパンが豊富で実質的にフッ化水素を含まない第二の中間組成物を含む第二の底部流とを生成すること;および
(e)前記第二の中間組成物中の2−クロロ−1,1,1,2−テトラフルオロプロパンの少なくとも一部を脱塩化水素化して、2,3,3,3−テトラフルオロプロペンを含む最終生成物を生成すること;
を含む、2,3,3,3−テトラフルオロプロペンを生成するための方法。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US5351808P | 2008-05-15 | 2008-05-15 | |
| US61/053,518 | 2008-05-15 | ||
| US12/464,666 | 2009-05-12 | ||
| US12/464,666 US8168837B2 (en) | 2008-05-15 | 2009-05-12 | Process for separating hydrogen fluoride from organic feedstocks |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009298781A JP2009298781A (ja) | 2009-12-24 |
| JP5491069B2 true JP5491069B2 (ja) | 2014-05-14 |
Family
ID=40940406
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009118184A Active JP5491069B2 (ja) | 2008-05-15 | 2009-05-15 | 有機原材料からフッ化水素を分離するための方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US8168837B2 (ja) |
| EP (1) | EP2119692B1 (ja) |
| JP (1) | JP5491069B2 (ja) |
| KR (1) | KR101629908B1 (ja) |
| CN (1) | CN101684060B (ja) |
| ES (1) | ES2428904T3 (ja) |
| MX (1) | MX2009005158A (ja) |
Families Citing this family (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9493384B2 (en) | 2007-07-06 | 2016-11-15 | Honeywell International Inc. | Process for producing 2,3,3,3-tetrafluoropropene |
| US8845921B2 (en) * | 2008-04-09 | 2014-09-30 | Honeywell International Inc. | Separation of close boiling compounds by addition of a third compound |
| US8975454B2 (en) | 2008-07-31 | 2015-03-10 | Honeywell International Inc. | Process for producing 2,3,3,3-tetrafluoropropene |
| US8252965B2 (en) * | 2008-08-22 | 2012-08-28 | Honeywell International Inc. | Method for separating halocarbons |
| US8008243B2 (en) | 2008-10-31 | 2011-08-30 | Honeywell International Inc. | Azeotrope-like compositions of 1,1,2,3-tetrachloropropene and hydrogen fluoride |
| US9061958B2 (en) | 2009-03-24 | 2015-06-23 | Arkema Inc. | Separation of R-1233 from hydrogen fluoride |
| KR101684333B1 (ko) | 2009-03-24 | 2016-12-08 | 알케마 인코포레이티드 | 불화수소로부터 r1233의 분리 |
| EP2499110B1 (en) * | 2009-11-10 | 2020-02-26 | Daikin Industries, Ltd. | Method for purifying 2,3,3,3-tetrafluoropropene |
| AU2010341533B2 (en) * | 2009-12-22 | 2015-04-23 | The Chemours Company Fc, Llc. | Compositions comprising 2,3,3,3-tetrafluoropropene, 1,1,2,3-tetrachloropropene, 2-chloro-3,3,3-trifluoropropene, or 2-chloro-1,1,1,2-tetrafluoropropane |
| US8927791B2 (en) * | 2010-04-29 | 2015-01-06 | Honeywell International Inc. | Method for producing tetrafluoropropenes |
| US8378158B2 (en) * | 2010-12-03 | 2013-02-19 | Honeywell International Inc. | Azeotrope-like compositions of (Z)-1-chloro-3,3,3-trifluoropropene and hydrogen fluoride |
| US9000240B2 (en) | 2011-05-19 | 2015-04-07 | Honeywell International Inc. | Integrated process for the production of 1-chloro-3,3,3-trifluoropropene |
| FR2977584B1 (fr) * | 2011-07-08 | 2014-12-05 | Arkema France | Procede de separation et recuperation du 2,3,3,3-tetrafluoropropene et de l'acide fluorhydrique |
| EP2755937B1 (en) * | 2011-09-15 | 2019-10-30 | Daikin Industries, Ltd. | Method for purifying chlorinated hydrocarbon |
| KR20140071456A (ko) * | 2011-09-30 | 2014-06-11 | 허니웰 인터내셔날 인코포레이티드 | 2,3,3,3-테트라플루오로프로펜의 제조 방법 |
| IN2014DN03381A (ja) * | 2011-11-04 | 2015-06-26 | Haiyou Wang | |
| CN104125939B (zh) * | 2012-01-09 | 2016-06-29 | 纳幕尔杜邦公司 | 反应器钝化方法 |
| EP2812298A4 (en) * | 2012-02-10 | 2015-09-16 | Haiyou Wang | IMPROVED PROCESS FOR PRODUCING 2,3,3,3-TETRAFLUOROPROPENE |
| EP2819978A4 (en) * | 2012-02-29 | 2015-11-04 | Honeywell Int Inc | PROCESS FOR PRODUCTION OF 2,3,3,3-TETRAFLUOROPROPENE |
| US9018428B2 (en) | 2012-09-06 | 2015-04-28 | Honeywell International Inc. | Reactor and agitator useful in a process for making 1-chloro-3,3,3-trifluoropropene |
| CN102974114B (zh) * | 2012-12-18 | 2014-10-29 | 上海试四化学品有限公司 | 一种二氯乙烷蒸馏装置以及蒸馏工艺 |
| US9334206B2 (en) * | 2013-03-15 | 2016-05-10 | Honeywell International Inc. | Integrated process to produce 2,3,3,3-tetrafluoropropene |
| FR3003565B1 (fr) | 2013-03-20 | 2018-06-29 | Arkema France | Composition comprenant hf et 2,3,3,3-tetrafluoropropene |
| WO2015006258A1 (en) * | 2013-07-12 | 2015-01-15 | Arkema Inc. | Method of separating organofluorine compounds using membrane |
| CN103613481B (zh) * | 2013-11-01 | 2015-08-12 | 西安近代化学研究所 | 氟化氢和2-氯-1,1,1-三氟丙烯混合物的分离方法 |
| WO2016187507A1 (en) | 2015-05-21 | 2016-11-24 | The Chemours Company Fc, Llc | HYDROFLUORINATION OF 1233xf TO 244bb BY SbF5 |
| JP6052340B2 (ja) * | 2015-05-29 | 2016-12-27 | ダイキン工業株式会社 | 含フッ素化合物含有組成物の製造方法 |
| CN108251895A (zh) * | 2016-12-29 | 2018-07-06 | 江苏鲁汶仪器有限公司 | 一种氟化氢气相腐蚀设备及方法 |
| US10351494B1 (en) * | 2018-01-08 | 2019-07-16 | Honeywell International Inc. | Systems and methods for reducing the formation of impurities during 244bb dehydrochlorination to 1234yf |
| US11555001B2 (en) | 2018-06-06 | 2023-01-17 | Honeywell International Inc. | Method for dehydrochlorination of HCFC-244bb to manufacture HFO-1234yf |
| FR3100461B1 (fr) * | 2019-09-06 | 2021-09-03 | Arkema France | Procédé de purification d’hydrofluorocarbures |
| CN113735063B (zh) * | 2021-09-26 | 2023-04-18 | 金宏气体股份有限公司 | 一种9n电子级hf的提纯装置及提纯工艺 |
| US20230234901A1 (en) * | 2022-01-26 | 2023-07-27 | Honeywell International Inc. | Preparation of an improved composition from 1-chloro-3,3,3-trifluoropropene (hfo-1233zd) high boiling residue by-product |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5918481A (en) * | 1997-11-20 | 1999-07-06 | Alliedsignal Inc. | Process for separating hydrogen fluoride from fluorocarbons |
| JP4387671B2 (ja) * | 2001-01-25 | 2009-12-16 | ハネウェル・インターナショナル・インコーポレーテッド | フルオロカーボンの製造方法 |
| US8084653B2 (en) * | 2004-04-29 | 2011-12-27 | Honeywell International, Inc. | Method for producing fluorinated organic compounds |
| US20090182179A1 (en) | 2008-01-15 | 2009-07-16 | Honeywell International Inc. | Hydrofluorination of 2-chloro-3,3,3-trifluoropropene to 2-chloro-1,1,1,2-tetrafluoropropane with catalysts of sbcl3, sbcl5, sbf5, ticl4, sncl4, cr2o3 and fluorinated cr2o3 |
| US7897823B2 (en) * | 2004-10-29 | 2011-03-01 | E. I. Du Pont De Nemours And Company | Process for production of azeotrope compositions comprising hydrofluoroolefin and hydrogen fluoride and uses of said azeotrope compositions in separation processes |
| US20080030615A1 (en) * | 2005-06-29 | 2008-02-07 | Maximino Vasquez | Techniques to switch between video display modes |
| US7476771B2 (en) * | 2005-11-01 | 2009-01-13 | E.I. Du Pont De Nemours + Company | Azeotrope compositions comprising 2,3,3,3-tetrafluoropropene and hydrogen fluoride and uses thereof |
| PT3336073T (pt) * | 2006-01-03 | 2022-12-21 | Honeywell Int Inc | Método para produzir compostos orgânicos fluorados |
| PL2433921T3 (pl) * | 2006-08-24 | 2014-06-30 | Du Pont | Sposoby oddzielania fluoroolefin od fluorowodoru poprzez destylację azeotropową |
| PL2170785T3 (pl) * | 2007-06-27 | 2018-12-31 | Arkema Inc. | Sposób wytwarzania fluorowodoroolefin |
| PL2634231T3 (pl) * | 2008-05-07 | 2022-08-16 | The Chemours Company Fc, Llc | Kompozycje |
-
2009
- 2009-05-12 US US12/464,666 patent/US8168837B2/en active Active
- 2009-05-13 ES ES09160188T patent/ES2428904T3/es active Active
- 2009-05-13 EP EP09160188.0A patent/EP2119692B1/en active Active
- 2009-05-14 CN CN200910149754.2A patent/CN101684060B/zh active Active
- 2009-05-14 MX MX2009005158A patent/MX2009005158A/es active IP Right Grant
- 2009-05-15 KR KR1020090042786A patent/KR101629908B1/ko active Active
- 2009-05-15 JP JP2009118184A patent/JP5491069B2/ja active Active
-
2012
- 2012-03-19 US US13/423,726 patent/US8519201B2/en active Active
-
2013
- 2013-08-02 US US13/957,560 patent/US8716538B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| KR101629908B1 (ko) | 2016-06-13 |
| US20120190901A1 (en) | 2012-07-26 |
| US8519201B2 (en) | 2013-08-27 |
| CN101684060B (zh) | 2014-04-02 |
| MX2009005158A (es) | 2009-12-18 |
| KR20090119743A (ko) | 2009-11-19 |
| ES2428904T3 (es) | 2013-11-12 |
| CN101684060A (zh) | 2010-03-31 |
| US8168837B2 (en) | 2012-05-01 |
| EP2119692B1 (en) | 2013-07-24 |
| US8716538B2 (en) | 2014-05-06 |
| US20130338408A1 (en) | 2013-12-19 |
| EP2119692A1 (en) | 2009-11-18 |
| US20090287027A1 (en) | 2009-11-19 |
| JP2009298781A (ja) | 2009-12-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5491069B2 (ja) | 有機原材料からフッ化水素を分離するための方法 | |
| JP5788380B2 (ja) | フッ化水素からのr−1233の分離 | |
| JP5826819B2 (ja) | 第3の化合物を加えることによる沸点の近い化合物の分離 | |
| US9045386B2 (en) | Integrated process and methods of producing (E)-1-chloro-3,3,3-trifluoropropene | |
| JP6220352B2 (ja) | HCFC−1233zdの生産方法 | |
| US9334206B2 (en) | Integrated process to produce 2,3,3,3-tetrafluoropropene | |
| JP2013538809A (ja) | トランス−1−クロロ−3,3,3−トリフルオロプロペンを製造するための連続低温プロセス | |
| JP2020063304A (ja) | フッ化水素からのr−1233の分離 | |
| JP5338240B2 (ja) | フッ化水素の分離方法 | |
| US20180056210A1 (en) | SEPARATION OF (Z)-1-CHLORO-3,3,3-TRIFLUOROPROPENE (HCFO-1233zd(Z)) AND 1-CHLORO-1,3,3,3-TETRAFLUOROPROPANE (HCFC-244fa) BY ADDING A THIRD COMPONENT |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120508 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130719 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130729 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131029 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140129 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140227 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5491069 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |