JP5334382B2 - 電気化学セル及びこれを用いた燃料電池 - Google Patents
電気化学セル及びこれを用いた燃料電池 Download PDFInfo
- Publication number
- JP5334382B2 JP5334382B2 JP2007169028A JP2007169028A JP5334382B2 JP 5334382 B2 JP5334382 B2 JP 5334382B2 JP 2007169028 A JP2007169028 A JP 2007169028A JP 2007169028 A JP2007169028 A JP 2007169028A JP 5334382 B2 JP5334382 B2 JP 5334382B2
- Authority
- JP
- Japan
- Prior art keywords
- electrochemical cell
- formula
- represented
- cation
- alkyl group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/14—Cells with non-aqueous electrolyte
- H01M6/18—Cells with non-aqueous electrolyte with solid electrolyte
- H01M6/181—Cells with non-aqueous electrolyte with solid electrolyte with polymeric electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M8/1016—Fuel cells with solid electrolytes characterised by the electrolyte material
- H01M8/1018—Polymeric electrolyte materials
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0082—Organic polymers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Sustainable Energy (AREA)
- Sustainable Development (AREA)
- Life Sciences & Earth Sciences (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Dispersion Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Inorganic Chemistry (AREA)
- Fuel Cell (AREA)
- Secondary Cells (AREA)
- Hybrid Cells (AREA)
Description
燃料電池は、発電効率が高く環境負荷抑制に優れており、これらの問題の解決に貢献が期待されている次世代型エネルギー供給デバイスである。
また、燃料電池は、電解質の種類により分類されるが、中でも固体高分子形燃料電池は、小型で且つ高出力を得ることができる。このため、小規模の定置型用、移動体用、携帯端末用のエネルギー供給源としての適用について研究・開発が進められている。
例えば、固体高分子電解質として、スルホン化ポリエーテルエーテルケトン、スルホン化ポリエーテルスルホン、スルホン化ポリエーテルエーテルスルホン、スルホン化ポリスルフィド、ポリベンズイミダゾールといった種々の芳香族系炭化水素系固体高分子電解質が検討されている(例えば特許文献1〜6参照)。
中本博文,松岡秀幸,渡邉正義,「アルキルアミンとオキソ酸からなるプロトン性イオン液体の特性」,電気化学会第73回大会 講演要旨集,2006年,p147
R 1 R 2 R 3 HX + …(1)
(式(1)中のXはN、Pのいずれか、R 1 、R 2 及びR 3 はそれぞれC1〜C18のいずれかのアルキル基(但しR 1 =R 2 =R 3 の構造は除く)を示す)
R 1 R 2 HS + …(2)
(式(2)中のR 1 、R 2 はそれぞれC1〜C18のいずれかのアルキル基(但しR 1 =R 2 の構造は除く)を示す)
R 5 R 6 H 2 X + …(4)
(式(4)中のXはN、Pのいずれか、R 5 及びR 6 はそれぞれC1〜C18のいずれかのアルキル基(但しR 5 =R 6 の構造は除く)を示す)
R 5 H 2 S + …(5)
(式(5)中のR 5 はC1〜C18のいずれかのアルキル基を示す)
R 8 H 3 X + …(7)
(式(7)中のXはN、Pのいずれか、R 8 はC1〜C18のいずれかのアルキル基を示す)
R 4 YO m (OH) n−1 O − …(3)
(式(3)中のYはS、C、N、Pのいずれか、R 4 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 7 YO m (OH) n−1 O − …(6)
(式(6)中のYはS、C、N、Pのいずれか、R 7 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 9 YO m (OH) n−1 O − …(8)
(式(8)中のYはS、C、N、Pのいずれか、R 9 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 11 YO m (OH) n−1 O − …(10)
(式(10)中のYはS、C、N、Pのいずれか、R 11 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)のいずれかで表されるアニオン又はこれらの任意の組合せに係るアニオンとを含み、相互に異なる少なくとも2種類のイオン伝導体を含有する電解質を用いた電気化学セルであって、上記少なくとも2種類のイオン伝導体のうち、一種が酸素還元活性が最も高いイオン伝導体であり、他種がそのイオン伝導体よりも水素酸化活性が高い異種のイオン伝導体である、ことを特徴とする。
上記イオン伝導体は、次式(13)
(CH 3 )(C 2 H 5 ) 2 HN + …(13)
で表されるカチオンと、次式(3)
R 4 YO m (OH) n−1 O − …(3)
(式中のYはS、C、N、Pのいずれか、R 4 はCH 3 、CH 2 F、CHF 2 、CF 3 のいずれかであるアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
で表されるアニオンとを含んで成ることを特徴とする。
上記イオン伝導体は、次式(19)
R 11 YO m (OH) n−1 O − …(10)
(式中のYはS、C、N、Pのいずれか、R 11 はCH 3 、CH 2 F、CHF 2 、CF 3 のいずれかであるアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
で表されるアニオンとを含んで成ることを特徴とする。
R 1 R 2 R 3 HX + …(1)
(式(1)中のXはN、Pのいずれか、R 1 、R 2 及びR 3 はそれぞれC1〜C18のいずれかのアルキル基(但しR 1 =R 2 =R 3 の構造は除く)を示す)
R 1 R 2 HS + …(2)
(式(2)中のR 1 、R 2 はそれぞれC1〜C18のいずれかのアルキル基(但しR 1 =R 2 の構造は除く)を示す)
R 5 R 6 H 2 X + …(4)
(式(4)中のXはN、Pのいずれか、R 5 及びR 6 はそれぞれC1〜C18のいずれかのアルキル基(但しR 5 =R 6 の構造は除く)を示す)
R 5 H 2 S + …(5)
(式(5)中のR 5 はC1〜C18のいずれかのアルキル基を示す)
R 8 H 3 X + …(7)
(式(7)中のXはN、Pのいずれか、R 8 はC1〜C18のいずれかのアルキル基を示す)
R 4 YO m (OH) n−1 O − …(3)
(式(3)中のYはS、C、N、Pのいずれか、R 4 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 7 YO m (OH) n−1 O − …(6)
(式(6)中のYはS、C、N、Pのいずれか、R 7 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 9 YO m (OH) n−1 O − …(8)
(式(8)中のYはS、C、N、Pのいずれか、R 9 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 11 YO m (OH) n−1 O − …(10)
(式(10)中のYはS、C、N、Pのいずれか、R 11 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)のいずれかで表されるアニオン又はこれらの任意の組合せに係るアニオンとを含み、相互に異なる少なくとも2種類のイオン伝導体を含有する電解質を用いた電気化学セルであって、上記少なくとも2種類のイオン伝導体のうち、一種が酸素還元活性が最も高いイオン伝導体であり、他種がそのイオン伝導体よりも水素酸化活性が高い異種のイオン伝導体である。
(CH 3 )(C 2 H 5 ) 2 HN + …(13)
で表されるカチオンと、次式(3)
R 4 YO m (OH) n−1 O − …(3)
(式中のYはS、C、N、Pのいずれか、R 4 はCH 3 、CH 2 F、CHF 2 、CF 3 のいずれかであるアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
で表されるアニオンとを含んで成る。
R 11 YO m (OH) n−1 O − …(10)
(式中のYはS、C、N、Pのいずれか、R 11 はCH 3 、CH 2 F、CHF 2 、CF 3 のいずれかであるアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
で表されるアニオンとを含んで成る。
具体的には、これらカチオンのアルキル基がC1〜C6であることで、電極に用いる白金等へのプロトンの供給が容易になり、酸素還元活性がより向上しうる。また、アルキル基がC1〜C6であることで高イオン密度となり高いプロトン伝導性が得られる。
特に、アニオンのフルオロアルキル基がCF3であるときに、極めて優れた酸素還元活性を発現することができる。
(CH3)(C2H5)R12HX+ …(11)
(式中のXはN又はP、R12はH又はC1〜C6のいずれかのアルキル基を示す)
で表されるカチオンを用いることが好ましい。
(CH3)(C2H5)2HX+ …(12)
(式中のXはN又はPを示す)
で表されるカチオンを用いることができる。特に、次式(13)
(CH3)(C2H5)2HN+ …(13)
で表されるカチオンを用いることがより好ましい。
(C2H5)H3X+ …(14)
(式中のXはN、Pのいずれかを示す)
(C2H5)H2S+ …(15)
で表されるカチオンを用いることが好ましい。具体的には、次式(16)
(C2H5)H3N+ …(16)
で表されるカチオンを用いることがより好ましい。
代表的には、上記電解質材料(イオン伝導体)を適用した電解質膜を、燃料電池セルやそのシステムに使用することができる。これにより、中温域(120℃程度)の運転を可能とし、ラジエーター負荷を従来のPEM型燃料電池に対して低下させ、ラジエターサイズを低減しうる。その結果、システム容積の低減、システム重量の軽量化が可能となる。
なお、上述のイオン伝導体を含有する電解質においては高プロトン伝導率を有し、他の高分子型電解質に比べて水の存在に依存することなく高いプロトン伝導性を発現する。またその構成成分が水不溶性であるため、この電解質を使用する燃料電池においてはそのカソードで生成する水に対して電解質の構成成分が溶出することがない。
このため、燃料電池のカソードにおいて生成する水により溶解されない電解質を提供することができ、また燃料電池の寿命を大幅に延長できるという効果を奏するものである。
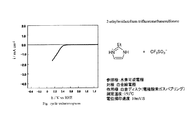
(1)diethylmethylammonium trifluoromethanesulfonateの合成
Ar雰囲気のグローブボックス中でジエチルメチルアミンとトリフルオロメタンスルホン酸を等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したジエチルメチルアミンとトリフルオロメタンスルホン酸を混合し、攪拌することで目的のイオン伝導体を得た。
参照極として水素可逆電極、対極には白金線電極、作用極には白金ディスク電極を使用し、作用極に酸素ガスをバブリングした状態でサイクリックボルタンメトリーの測定を行った。測定は3極式のセルを用いて測定温度150℃、電位掃印速度10mV/Sの条件で行った。
サイクリックボルタンメトリー測定結果を図1に示す。
(2)の酸素還元反応の評価を行ったセルと同様のセルを用い、作用極に酸素、対極には水素をそれぞれバブリングした状態で燃料電池発電を行った。
測定は150℃、電位掃印速度10mV/Sの条件で行った。
燃料電池発電試験の結果を図9に示す。
(2)の酸素還元反応の評価を行ったセルと同様のセルを用い、作用極に酸素、対極には水素をそれぞれバブリングした状態で開回路起電力の測定を行った。
測定は150℃の条件で行った。
開放起電力の測定の結果を図10に示す。
(1)ethylpiperidinium trifluoromethanesulfonateの合成
Ar雰囲気のグローブボックス中でエチルピペリジニウムとトリフルオロメタンスルホン酸を等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したエチルピペリジニウムとトリフルオロメタンスルホン酸を混合し、攪拌することで目的のイオン伝導体を得た。
酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図2に示す。
(1)dimethylethylammonium trifluoromethanesulfonateの合成
Ar雰囲気のグローブボックス中でジメチルエチルアミンとトリフルオロメタンスルホン酸を等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したジメチルエチルアミンとトリフルオロメタンスルホン酸を混合し、攪拌することで目的のイオン伝導体を得た。
酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図3に示す。
(1)diethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateの合成
diethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateそれぞれの合成は実施例1および実施例3と同様の方法で行った。
diethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateそれぞれの酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図11に示す。
diethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateそれぞれの水素酸化反応の評価は、参照極として水素可逆電極、対極には白金線電極、作用極には白金ディスク電極を使用し、作用極に水素ガスをバブリングした状態でサイクリックボルタンメトリーの測定を行った。測定は3極式のセルを用いて測定温度150℃、電位掃印速度10mV/Sの条件で行った。
サイクリックボルタンメトリー測定結果を図12に示す。
diethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateそれぞれの酸素還元反応および水素酸化反応の比較から(図11および図12)、酸素還元反応に高い活性を有するdiethylmethylammonium trifluoromethanesulfonateと、水素酸化反応に高い活性を有するdimethylethylammonium trifluoromethanesulfonateを共存させることで2種類のイオン伝導体からなる電解質を作製した。具体的には、Ar雰囲気のグローブボックス中でdiethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateがモル比で9:1となるよう秤量した後、混合し、攪拌することで目的のイオン伝導体を得た。
(5)酸素還元反応、水素酸化反応の評価
(4)で作製したdiethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateからなるイオン伝導体の酸素還元反応は実施例1と同様の方法で行った。また水素酸化反応は(3)と同様の方法で行った。(2)および(3)で測定したdiethylmethylammonium trifluoromethanesulfonate、dimethylethylammonium trifluoromethanesulfonateそれぞれの酸素還元反応と水素酸化反応のサイクリックボルタンメトリー測定結果と、(4)で作製したdiethylmethylammonium trifluoromethanesulfonateとdimethylethylammonium trifluoromethanesulfonateからなるイオン伝導体の酸素還元反応と水素酸化反応のサイクリックボルタンメトリー測定結果から算出した、同電流密度でのセル電圧(イオン伝導体によるIRロスを差し引いたときのセル電圧)の評価結果を図13に示す。
(1)diethylmethylammonium bis(trifluoro−methanesulfonyl)imideの合成
Ar雰囲気のグローブボックス中でジエチルメチルアミンとトリフルオロメタンスルホニルイミドを等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したジエチルメチルアミンとトリフルオロメタンスルホニルイミドを混合し、攪拌することで目的のイオン伝導体を得た。
酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図4に示す。
(1)diethylmethylammonium hydrogensulfonateの合成
Ar雰囲気のグローブボックス中でジエチルメチルアミンと硫酸を等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したジエチルメチルアミンと硫酸を混合し、攪拌することで目的のイオン伝導体を得た。
酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図5に示す。
(1)2−ethylimidazolium trifluoromethanesulfonateの合成
2−エチルイミダゾールを蒸留水に溶解し、そこに冷却しながら2−エチルイミダゾールと等モル量のトリフルオロメタンスルホン酸を滴下し攪拌した。この反応生成物を100℃で予備乾燥した後、120℃で真空乾燥し2−エチルイミダゾリウムトリフレートを得た。
酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図6に示す。
(1)Buthylimidazolium bis(trifluoro−methanesulfonyl)imideの合成
Ar雰囲気のグローブボックス中でブチルイミダゾールとトリフルオロメタンスルホニルイミドを等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したブチルイミダゾールとトリフルオロメタンスルホニルイミドを混合し、攪拌することで目的のイオン伝導体を得た。
燃料電池発電試験は実施例1と同様の方法で行った。燃料電池発電試験の結果を図9に示す。
(1)燃料電池発電試験
イオン伝導体として無水リン酸を使用した以外は、実施例1と同様の方法で燃料電池発電試験を行った。燃料電池発電試験の結果を図9に示す。
(1)燃料電池発電試験
イオン伝導体として1M硫酸を使用し、測定温度を30℃とした以外は、実施例1と同様の方法で燃料電池発電試験を行った。燃料電池発電試験の結果を図9に示す。
(1)Triethylammonium trifluoromethanesulfonateの合成
Ar雰囲気のグローブボックス中でトリエチルアミンとトリフルオロメタンスルホン酸を等モル量となるよう秤量した。秤量後、液体窒素で冷却しながら、秤量したトリエチルアミンとトリフルオロメタンスルホン酸を混合し、攪拌することで目的のイオン伝導体を得た。
酸素還元反応の評価は実施例1と同様の方法で行った。
サイクリックボルタンメトリー測定結果を図7に示す。また、実施例1、比較例1及び比較例7のサイクリックボルタンメトリー測定結果を図8に示す。
また、実施例1と比較例4〜6の燃料電池発電試験の結果から、本発明の好適形態である電気化学セルは、比較例4〜6に比べ、高い酸素還元活性を有しているため優れた発電特性を示す。さらに、比較例5の無水リン酸は、商用化されているリン酸型燃料電池で使用されるイオン伝導体であるが、本発明の好適形態である電気化学セルは、比較例5に比べ優れた発電特性を示すことから、目的としている高温・無加湿条件下で優れた燃料電池発電特性をしめす燃料電池用電気化学セルとして有用である。
また、実施例1の開放起電力の測定結果から、本発明の好適である電気化学セルは、測定時間内での開放起電力の低下が見られないことから高い化学的な耐久性を有している。
さらに、実施例4から酸素還元活性の高いイオン伝導体にそのイオン伝導体よりも高い水素酸化活性を有するイオン伝導体を加えることで、酸素還元活性および水素酸化活性の両方に高い活性を示めし、セル電圧が向上することから、目的としている高温・無加湿条件下で優れた燃料電池発電特性をしめす燃料電池用電気化学セルとして有用である。
Claims (18)
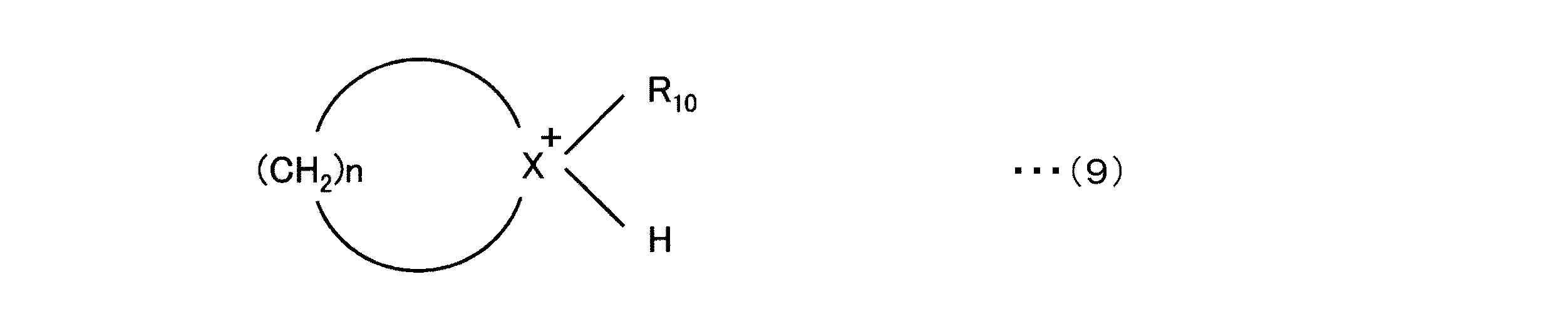
- 下記式(1)、(2)、(4)、(5)、(7)及び(9)
R 1 R 2 R 3 HX + …(1)
(式(1)中のXはN、Pのいずれか、R 1 、R 2 及びR 3 はそれぞれC1〜C18のいずれかのアルキル基(但しR 1 =R 2 =R 3 の構造は除く)を示す)
R 1 R 2 HS + …(2)
(式(2)中のR 1 、R 2 はそれぞれC1〜C18のいずれかのアルキル基(但しR 1 =R 2 の構造は除く)を示す)
R 5 R 6 H 2 X + …(4)
(式(4)中のXはN、Pのいずれか、R 5 及びR 6 はそれぞれC1〜C18のいずれかのアルキル基(但しR 5 =R 6 の構造は除く)を示す)
R 5 H 2 S + …(5)
(式(5)中のR 5 はC1〜C18のいずれかのアルキル基を示す)
R 8 H 3 X + …(7)
(式(7)中のXはN、Pのいずれか、R 8 はC1〜C18のいずれかのアルキル基を示す)
R 4 YO m (OH) n−1 O − …(3)
(式(3)中のYはS、C、N、Pのいずれか、R 4 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 7 YO m (OH) n−1 O − …(6)
(式(6)中のYはS、C、N、Pのいずれか、R 7 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 9 YO m (OH) n−1 O − …(8)
(式(8)中のYはS、C、N、Pのいずれか、R 9 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
R 11 YO m (OH) n−1 O − …(10)
(式(10)中のYはS、C、N、Pのいずれか、R 11 はアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)のいずれかで表されるアニオン又はこれらの任意の組合せに係るアニオンとを含み、相互に異なる少なくとも2種類のイオン伝導体を含有する電解質を用いた電気化学セルであって、
上記少なくとも2種類のイオン伝導体のうち、一種が酸素還元活性が最も高いイオン伝導体であり、他種がそのイオン伝導体よりも水素酸化活性が高い異種のイオン伝導体である、ことを特徴とする電気化学セル。 - 上記式(1)、(2)、(4)、(5)、(7)及び(9)のいずれかで表されるカチオン又はこれらの任意の組合せに係るカチオンと上記式(3)、(6)、(8)及び(10)のいずれかで表されるアニオン又はこれらの任意の組合せに係るアニオンとを含み、相互に異なる2種類のイオン伝導体を含有する電解質を用いた電気化学セルであって、
上記2種類のイオン伝導体のうち、一種が酸素還元活性が相対的に高いイオン伝導体であり、他種がそのイオン伝導体よりも水素酸化活性が相対的に高い異種のイオン伝導体であり、
上記酸素還元活性が相対的に高いイオン伝導体の含有量が50mol%以上である、ことを特徴とする請求項1に記載の電気化学セル。 - 上記カチオンのアルキル基(R 1 、R 2 、R 3 、R 5 、R 6 、R 8 、R 10 )がC1〜C6のいずれかであることを特徴とする請求項1又は2に記載の電気化学セル。
- 上記脂肪族複素環式化合物の環を形成する炭素数が6以下であることを特徴とする請求項1〜3のいずれか1つの項に記載の電気化学セル。
- 上記アニオンのアルキル基又はフルオロアルキル基(R 4 、R 7 、R 9 、R 11 )が、CH 3 、CH 2 F、CHF 2 、CF 3 のいずれかであることを特徴とする請求項1〜4のいずれか1つの項に記載の電気化学セル。
- 上記カチオンは、次式(11)
(CH 3 )(C 2 H 5 )R 12 HX + …(11)
(式中のXはN又はP、R 12 はH又はC1〜C6のいずれかのアルキル基を示す)
で表されることを特徴とする請求項1〜5のいずれか1つの項に記載の電気化学セル。 - 上記式(11)のR 12 がH、CH 3 、C 2 H 5 のいずれかであることを特徴とする請求項6に記載の電気化学セル。
- 上記カチオンは、次式(12)
(CH 3 )(C 2 H 5 ) 2 HX + …(12)
(式中のXはN又はPを示す)
で表されることを特徴とする請求項7に記載の電気化学セル。 - 上記カチオンは、次式(13)
(CH 3 )(C 2 H 5 ) 2 HN + …(13)
で表されることを特徴とする請求項8に記載の電気化学セル。 - 上記カチオンは、次式(14)または(15)
(C 2 H 5 )H 3 X + …(14)
(式中のXはN、Pのいずれかを示す)
(C 2 H 5 )H 2 S + …(15)
で表されることを特徴とする請求項1〜9のいずれか1つの項に記載の電気化学セル。 - 上記カチオンは、次式(16)
(C 2 H 5 )H 3 N + …(16)
で表されることを特徴とする請求項10に記載の電気化学セル。 - 請求項1〜13のいずれか1つの項に記載の電気化学セルを適用して成ることを特徴とする燃料電池。
- イオン伝導体を含有する電解質を用いた電気化学セルであって、
上記イオン伝導体は、次式(13)
(CH 3 )(C 2 H 5 ) 2 HN + …(13)
で表されるカチオンと、次式(3)
R 4 YO m (OH) n−1 O − …(3)
(式中のYはS、C、N、Pのいずれか、R 4 はCH 3 、CH 2 F、CHF 2 、CF 3 のいずれかであるアルキル基又はフルオロアルキル基、m及びnはそれぞれ1又は2を示す)
で表されるアニオンとを含んで成ることを特徴とする電気化学セル。 - 上記アニオンが、CF 3 SO 3 − であることを特徴とする請求項15に記載の電気化学セル。
- 上記アニオンが、CF 3 SO 3 − であることを特徴とする請求項17に記載の電気化学セル。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007169028A JP5334382B2 (ja) | 2006-10-27 | 2007-06-27 | 電気化学セル及びこれを用いた燃料電池 |
| EP07020844A EP1916733B1 (en) | 2006-10-27 | 2007-10-24 | Electrochemical cell and fuel cell using the same |
| US11/976,609 US8071253B2 (en) | 2006-10-27 | 2007-10-25 | Electrochemical cell using an ionic conductor |
| US13/283,403 US8535849B2 (en) | 2006-10-27 | 2011-10-27 | Electrochemical cell and fuel cell using an ionic conductor |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006291956 | 2006-10-27 | ||
| JP2006291956 | 2006-10-27 | ||
| JP2007169028A JP5334382B2 (ja) | 2006-10-27 | 2007-06-27 | 電気化学セル及びこれを用いた燃料電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008135365A JP2008135365A (ja) | 2008-06-12 |
| JP5334382B2 true JP5334382B2 (ja) | 2013-11-06 |
Family
ID=39027070
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007169028A Expired - Fee Related JP5334382B2 (ja) | 2006-10-27 | 2007-06-27 | 電気化学セル及びこれを用いた燃料電池 |
Country Status (3)
| Country | Link |
|---|---|
| US (2) | US8071253B2 (ja) |
| EP (1) | EP1916733B1 (ja) |
| JP (1) | JP5334382B2 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2723283A1 (en) * | 2008-05-15 | 2009-11-19 | Basf Se | Proton-conducting membrane and use thereof |
| WO2012174463A1 (en) * | 2011-06-17 | 2012-12-20 | E. I. Du Pont De Nemours And Company | Improved composite polymer electrolyte membrane |
| JP2017178790A (ja) * | 2016-03-28 | 2017-10-05 | Tdk株式会社 | スルホニウム塩、電解液およびリチウムイオン二次電池 |
| CN113761654B (zh) * | 2021-08-18 | 2023-09-19 | 上海卫星工程研究所 | 火星环绕器地火转移过程太阳翼自主偏置控制方法及系统 |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4839249A (en) | 1988-07-25 | 1989-06-13 | Eveready Battery Company, Inc. | Low temperature molten composition comprised of ternary alkyl sulfonium salts |
| EP0574791B1 (de) | 1992-06-13 | 1999-12-22 | Aventis Research & Technologies GmbH & Co. KG | Polymerelektrolyt-Membran und Verfahren zu ihrer Herstellung |
| DK0840760T3 (da) * | 1995-07-27 | 2000-04-17 | Aventis Res & Tech Gmbh & Co | Polymerelektrolytter og fremgangsmåde til deres fremstilling |
| US5599639A (en) | 1995-08-31 | 1997-02-04 | Hoechst Celanese Corporation | Acid-modified polybenzimidazole fuel cell elements |
| JPH09245818A (ja) | 1996-02-29 | 1997-09-19 | Aisin Aw Co Ltd | 燃料電池用電解質膜及びその製造方法 |
| JP3970390B2 (ja) | 1997-08-22 | 2007-09-05 | 旭化成株式会社 | 固体高分子燃料電池用膜−電極接合体 |
| JP4051736B2 (ja) | 1997-10-16 | 2008-02-27 | 住友化学株式会社 | 高分子電解質、高分子電解質膜、及び燃料電池 |
| AUPQ237199A0 (en) | 1999-08-23 | 1999-09-16 | Rtm Research And Development Pty. Ltd. | Fast lithiumion conducting doped plastic crystals |
| JP4036279B2 (ja) * | 2001-10-09 | 2008-01-23 | よこはまティーエルオー株式会社 | プロトン伝導体及びこれを用いた燃料電池 |
| JP2003257476A (ja) * | 2002-02-27 | 2003-09-12 | Fuji Photo Film Co Ltd | 電解質組成物および非水電解質二次電池 |
| ATE407434T1 (de) | 2002-06-19 | 2008-09-15 | Ube Industries | Polyelektrolytmembran und herstellungsverfahren dafür |
| US20040038127A1 (en) | 2002-08-20 | 2004-02-26 | Schlaikjer Carl Roger | Small cation/delocalizing anion as an ambient temperature molten salt in electrochemical power sources |
| WO2004114445A1 (en) * | 2003-05-01 | 2004-12-29 | Arizona Board Of Regents A Body Corporate Acting On Behalf Of Arizona State University | Ionic liquids and ionic liquid acids with high temperature stability for fuel cell and other high temperature applications, method of making and cell employing same |
| US20050106440A1 (en) | 2003-11-19 | 2005-05-19 | Honda Motor Co., Ltd. | Proton conductor and method for producing the same |
| JP2005174911A (ja) * | 2003-11-19 | 2005-06-30 | Honda Motor Co Ltd | プロトン伝導体及びその製造方法 |
| CN100468856C (zh) * | 2003-12-29 | 2009-03-11 | 国际壳牌研究有限公司 | 在高温下使用的电化学元件 |
| US20050287441A1 (en) | 2004-06-23 | 2005-12-29 | Stefano Passerini | Lithium polymer electrolyte batteries and methods of making |
| JP2006190618A (ja) | 2005-01-07 | 2006-07-20 | Tosoh Corp | イオン性液体組成物及びそれを含む電気化学デバイス |
| JP2008004533A (ja) * | 2006-05-22 | 2008-01-10 | Nissan Motor Co Ltd | イオン伝導体 |
-
2007
- 2007-06-27 JP JP2007169028A patent/JP5334382B2/ja not_active Expired - Fee Related
- 2007-10-24 EP EP07020844A patent/EP1916733B1/en not_active Not-in-force
- 2007-10-25 US US11/976,609 patent/US8071253B2/en not_active Expired - Fee Related
-
2011
- 2011-10-27 US US13/283,403 patent/US8535849B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| US20080131751A1 (en) | 2008-06-05 |
| US20120040272A1 (en) | 2012-02-16 |
| EP1916733A1 (en) | 2008-04-30 |
| EP1916733B1 (en) | 2011-12-14 |
| US8535849B2 (en) | 2013-09-17 |
| JP2008135365A (ja) | 2008-06-12 |
| US8071253B2 (en) | 2011-12-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ryu et al. | Effect of type and stoichiometry of fuels on performance of polybenzimidazole-based proton exchange membrane fuel cells operating at the temperature range of 120–160 C | |
| Boaventura et al. | Activation procedures characterization of MEA based on phosphoric acid doped PBI membranes | |
| Yang et al. | Approaches and technical challenges to high temperature operation of proton exchange membrane fuel cells | |
| Li et al. | The CO poisoning effect in PEMFCs operational at temperatures up to 200 C | |
| CN100544087C (zh) | 固体高分子型燃料电池用电解质膜及其制造方法以及固体高分子型燃料电池用膜电极接合体 | |
| JP4036279B2 (ja) | プロトン伝導体及びこれを用いた燃料電池 | |
| KR101496403B1 (ko) | 캐소드 촉매층, 막 전극 접합체, 고분자 전해질형 연료전지 및 그 제조방법 | |
| Cho et al. | Effect of catalyst layer ionomer content on performance of intermediate temperature proton exchange membrane fuel cells (IT-PEMFCs) under reduced humidity conditions | |
| Yandrasits et al. | New directions in perfluoroalkyl sulfonic acid–based proton-exchange membranes | |
| Thanganathan et al. | Nanocomposite hybrid membranes containing polyvinyl alcohol or poly (tetramethylene oxide) for fuel cell applications | |
| Fishel et al. | Electrochemical Hydrogen Pumping 24 | |
| JP5334382B2 (ja) | 電気化学セル及びこれを用いた燃料電池 | |
| Yoshimi et al. | Temperature and humidity dependence of the electrode polarization in intermediate-temperature fuel cells employing CsH2PO4/SiP2O7-based composite electrolytes | |
| Shen et al. | Intermediate-temperature, non-humidified proton exchange membrane fuel cell with a highly proton-conducting Fe0. 4Ta0. 5P2O7 electrolyte | |
| Okanishi et al. | Effect of PEFC operating conditions on the durability of sulfonated poly (arylene ether sulfone ketone) multiblock membranes | |
| US11482720B2 (en) | Membrane-electrode assembly with improved durability and proton conductivity and method for manufacturing the same | |
| JP2015529383A (ja) | 向上した性能を有する活性層の形成 | |
| Cho et al. | Aniline as a Cationic and Aromatic Contaminant in PEMFCs | |
| JP5062722B2 (ja) | 無水・高温下に作動可能なプロトン導電性燃料電池用膜、及びその製造方法 | |
| CA2646994C (en) | Electrocatalyst for electrochemical cell, method for producing the electrocatalyst, electrochemical cell, single cell of fuel cell, and fuel cell | |
| Ramani et al. | The chalkboard: The polymer electrolyte fuel cell | |
| Okanishi et al. | Durability of an aromatic block copolymer membrane in practical PEFC operation | |
| Matsui et al. | Development of novel proton conductors consisting of solid acid/pyrophosphate composite for intermediate-temperature fuel cells | |
| JP2008103262A (ja) | イオン伝導体及びこれを用いた電解質並びにエネルギーデバイス | |
| Itoh et al. | Proton-conducting electrolyte membranes based on hyperbranched polymer with a sulfonic acid group for high-temperature fuel cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100622 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100622 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20121226 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130308 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130717 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130730 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |